ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к антисмысловому олигомеру, который вызывает пропуск экзона 51 в человеческом гене дистрофина, и к фармацевтической композиции, содержащей этот олигомер.
Предшествующий уровень техники
[0002] Мышечная дистрофия Дюшенна (МДД) представляет собой наиболее распространенную форму наследственной прогрессирующей мышечной дистрофии, поражающей одного из приблизительно 3500 новорожденных мальчиков. Хотя двигательные функции редко отличаются от здоровых людей в младенчестве и детстве, мышечная слабость наблюдается у детей в возрасте приблизительно от 4 до 5 лет. Впоследствии мышечная слабость прогрессирует до потери способности передвигаться приблизительно к 12 годам и к смерти в результате сердечной или дыхательной недостаточности в возрасте 20-30 лет. МДД является тяжелым нарушением. В настоящее время не существует доступной эффективной терапии МДД, и существует острая необходимость в разработке нового терапевтического агента.
[0003] Как известно, МДД вызвана мутацией в гене дистрофина. Ген дистрофина располагается на X-хромосоме и является огромным по размеру геном, состоящим из 2,2 миллиона пар нуклеотидов ДНК. ДНК транскрибируется с образованием предшественников мРНК, интроны удаляются посредством сплайсинга с образованием мРНК длиной 11058 оснований, в которой 79 экзонов соединены вместе. Эта мРНК транслируется с образованием белка дистрофина длиной 3685 аминокислотных остатков. Белок дистрофин связан с поддержанием стабильности мембраны в мышечных клетках и необходим для уменьшения хрупкости мышечных клеток. Ген дистрофина у пациентов с МДД содержит мутацию и, следовательно, белок дистрофин, функционирующий в мышечных клетках, редко экспрессируется. Поэтому структура мышечных клеток не может поддерживаться в организме пациентов с МДД, что приводит к входу большого количества ионов кальция в мышечные клетки. Вследствие этого развивается похожий на воспалительный ответ, способствующий развитию фиброза, что затрудняет регенерацию мышечных клеток.
[0004] Мышечная дистрофия Беккера (МДБ) также вызывается мутацией в гене дистрофина. Симптомы включают мышечную слабость, сопровождающуюся атрофией мышц, но прогрессия мышечной слабости, как правило, умеренная или слабая по сравнению с МДД. Во многих случаях начало заболевания приходится на взрослый возраст. Различия в клинических симптомах между МДД и МДБ, как полагают, основаны на том, нарушает или нет мутация открытую рамку считывания для аминокислот при трансляции мРНК для дистрофина с образованием белка дистрофина (Непатентный документ 1). В частности, при МДД наличие мутации вызывает сдвиг рамки считывания для аминокислот таким образом, что прекращается экспрессия функционального белка дистрофина, в то время как при МДБ функционирующий, хотя и неполноценный, белок дистрофин образуется, поскольку рамка считывания для аминокислот сохраняется, в то время как часть экзонов отсутствует в результате мутации.
[0005] Пропуск экзонов, как ожидают, будет служить способом лечения МДД. Такой способ включает модификацию сплайсинга с целью восстановления рамки считывания для аминокислот в мРНК дистрофина и индукции экспрессии белка дистрофина, обладающего частично восстановленной функцией (Непатентный документ 2). Часть аминокислотной последовательности, являющейся мишенью для пропуска экзона, будет утрачена. По этой причине белок дистрофин, экспрессирующийся при такой обработке, становится короче нормального белка, но поскольку рамка считывания для аминокислот сохраняется, функция стабилизации мышечных клеток частично восстанавливается. Следовательно, ожидается что пропуск экзона приведет к тому, что МДД будет иметь симптомы, похожие на симптомы МДБ, которая является более умеренным заболеванием. Подход, основанный на пропуске экзонов, прошел испытания на животных с применением мышей или собак и в настоящее время изучается в рамках клинических исследований на людях с МДД.
[0006] Пропуск экзонов можно индуцировать посредством связывания антисмысловых нуклеиновых кислот либо, мишенью которых являются либо 5'-, либо 3'-сайты сплайсинга, либо как 5'-, так и 3'-сайты сплайсинга, либо сайты внутри экзона. Экзон включится в мРНК только при узнавании обоих сайтов сплайсинга комплексом сплайсосомы. Таким образом, пропуск экзона можно индуцировать, действуя на сайты сплайсинга с помощью антисмысловых нуклеиновых кислот. Более того, связывание белка SR с экзонным энхансером сплайсинга (ESE, exonic splicing enhancer) считается необходимым для узнавания экзона механизмом сплайсинга. Соответственно, пропуск экзона можно индуцировать, действуя на ESE.
[0007] Поскольку мутации в гене дистрофина могут различаться у разных пациентов с МДД, антисмысловые нуклеиновые кислоты следует конструировать на основании сайта или типа соответствующей генетической мутации. Ранее антисмысловые нуклеиновые кислоты, индуцирующие пропуск всех 79 экзонов, были получены Steve Wilton, et al., из Университета Западной Австралии (University of Western Australia) (Непатентный документ 3), а антисмысловые нуклеиновые кислоты, индуцирующие пропуск 39 экзонов, были получены Annemieke Aartsma-Rus, et al., из Нидерландов (Непатентный документ 4).
[0008] Считается, что приблизительно 13% всех пациентов с МДД можно лечить посредством пропуска экзона 51 (здесь и далее называемого «экзоном 51»). В последние годы многие организации сообщали об исследованиях, где экзон 51 в гене дистрофина был мишенью для пропуска экзона (Патентные документы 1-6, Непатентные документы 5-6). Однако техника пропуска экзона 51 с высокой эффективностью еще на была изобретена.
Документы, относящиеся к предшествующему уровню техники
Патентный документ
[0009] Патентный документ 1: Международная публикация WO 2004/048570
Патентный документ 2: Международная публикация WO 2002/024906
Патентный документ 3: Международная публикация WO 2010/048586
Патентный документ 4: Международная публикация WO 2010/050801
Патентный документ 5: US 2010/0168212
[0010] Непатентный документ 1: Monaco A. P. et al., Genomics 1988; 2: p. 90-95
Непатентный документ 2: Matsuo M., Brain Dev 1996; 18: p. 167-172
Непатентный документ 3: Wilton S. D., e t al., Molecular Therapy 2007: 15: p. 1288-96
Непатентный документ 4: Annemieke Aartsma-Rus et al., (2002) Neuromuscular Disorders 12: S71-S77
Непатентный документ 5: Aoki Y., et al., Molecular therapy 2010: 18: p.1995-2005
Непатентный документ 6: Nakano S., et al., Pediatr Int. 2011: 53: 524-429
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Задачи изобретения
[0011] В свете описанных обстоятельств существует потребность в получении антисмысловых олигомеров, индуцирующих пропуск экзона 51 в гене дистрофина с высокой эффективностью, и в лекарственных средствах для лечения мышечной дистрофии, содержащих эти олигомеры.
Средства решения задачи
[0012] По результатам подробных исследований технического содержания упомянутых выше документов и структуры гена дистрофина авторы настоящего изобретения обнаружили, что пропуск экзона 51 можно индуцировать с высокой эффективностью посредством введения антисмыслового олигомера, имеющего нуклеотидные последовательности, представленные SEQ ID NO:1 и 2. На основании этого открытия авторы настоящего изобретения создали настоящее изобретение.
[0013] Таким образом, настоящее изобретение заключается в следующем.
[1] Антисмысловой олигомер, выбранный из группы, состоящей из приведенных ниже пунктов с (a) по (d):
(a) антисмысловой олигомер, содержащий нуклеотидную последовательность SEQ ID NO: 1 или 2;
(b) антисмысловой олигомер, состоящий из нуклеотидной последовательности, содержащей делецию, замену, вставку и/или добавление 1-5 нуклеотидов в нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека;
(c) антисмысловой олигомер, имеющий нуклеотидную последовательность, по меньшей мере на 80% идентичную нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека; и
(d) антисмысловой олигомер, который гибридизуется в строгих условиях с олигонуклеотидом, состоящим из нуклеотидной последовательности, комплементарной нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
[2] Антисмысловой олигомер, выбранный из группы, состоящей из приведенных ниже пунктов с (e) по (h):
(e) антисмысловой олигомер, состоящий из нуклеотидной последовательности SEQ ID NO: 1 или 2;
(f) антисмысловой олигомер, состоящий из нуклеотидной последовательности, содержащей делецию, замену, вставку и/или добавление 1-3 нуклеотидов в нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека;
(g) антисмысловой олигомер, состоящий из нуклеотидной последовательности, по меньшей мере на 80% идентичную нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека; и
(h) антисмысловой олигомер, который гибридизуется в строгих условиях с олигонуклеотидом, состоящим из нуклеотидной последовательности, комплементарной нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
[3] Антисмысловой олигомер, выбранный из группы, состоящей из приведенных ниже пунктов (i) и (j):
(i) антисмысловой олигомер, состоящий из нуклеотидной последовательности SEQ ID NO: 1 или 2; и
(j) антисмысловой олигомер, имеющий нуклеотидную последовательность, по меньшей мере на 90% идентичную нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
[4] Антисмысловой олигомер по любому из приведенных выше п.п.1-3, который является олигонуклеотидом.
[5] Антисмысловой олигомер по приведенному выше п.4, где остаток сахара и/или область соединения через фосфатную группу по меньшей мере одного нуклеотида, входящего в состав олигонуклеотида, модифицированы.
[6] Антисмысловой олигомер по приведенным выше п.4 или 5, где остаток сахара по меньшей мере одного нуклеотида, входящего в состав олигонуклеотида, является рибозой, в которой 2'-OH-группа заменена любой группой, выбранной из группы, состоящей из OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br и I (где R является алкилом или арилом и R' является алкиленом).
[7] Антисмысловой олигомер по любому из приведенных выше п.п.4-6, где область соединения через фосфатную группу по меньшей мере одного нуклеотида, входящего в состав олигонуклеотида, является любой областью, выбираемой из группы, состоящей из тиофосфатной связи, дитиофосфатной связи, алкилфосфонатной связи, фосфорамидатной связи и боранофосфатной связи.
[8] Антисмысловой олигомер по любому из приведенных выше п.п.1-3, который является морфолино-олигомером.
[9] Антисмысловой олигомер по приведенному выше п.8, где морфолиновое кольцо, область соединения через фосфатную группу, 3'-конец и/или 5'-конец по меньшей мере одного морфолино, входящего в состав олигомера, модифицированы.
[10] Антисмысловой олигомер по приведенным выше п.9 или 10, где область соединения через фосфатную группу по меньшей мере одного морфолино, входящего в состав морфолино-олигомера, является любой областью, выбранной из фосфодиамидатной связи, тиофосфатной связи, дитиофосфатной связи, алкилфосфонатной связи, фосфорамидатной связи и боранофосфатной связи.
[11] Антисмысловой олигомер по приведенному выше п.10, который является фосфодиамидатным морфолино-олигомером.
[12] Антисмысловой олигомер по любому из приведенных выше п.п.9-11, в котором 5'-конец имеет любую их приведенных ниже химических формул (1)-(3):
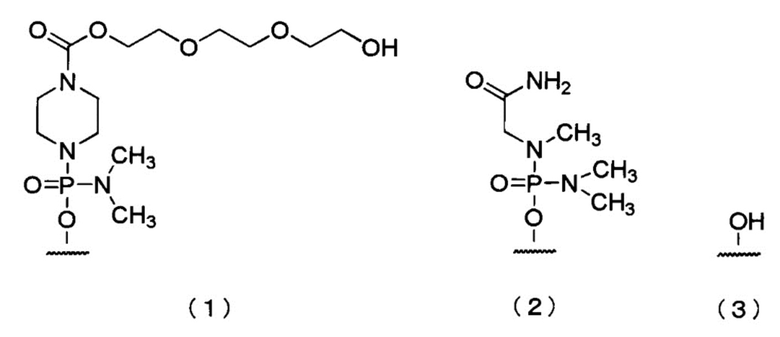
[13] Фармацевтическая композиция для лечения мышечной дистрофии, содержащая в качестве активного ингредиента антисмысловой олигомер по любому из приведенных выше п.п.1-12 или его фармацевтически приемлемую соль или гидрат.
[14] Фармацевтическая композиция по приведенному выше п.13, содержащая фармацевтически приемлемый носитель.
[15] Способ лечения мышечной дистрофии, включающий введение пациенту с мышечной дистрофией антисмыслового олигомера по любому из приведенных выше п.п.1-12 или фармацевтической композиции по приведенным выше п.13 или 14.
[16] Способ лечения по приведенному выше п.15, где пациентом с мышечной дистрофией является пациент с делециями нуклеотидов внутри экзонов 29-50, 50, 45-50, 48-50, 49-50, 52, 52-63, 13-50, 19-50, 43-50 или 47-50.
[17] Способ лечения по приведенным выше п. 15 или 16, где пациентом является человек.
[18] Применение антисмыслового олигомера по любому из приведенных выше п.п.1-12 для получения фармацевтической композиции для лечения мышечной дистрофии.
[19] Антисмысловой олигомер по любому из приведенных выше п.п. 1-12 для применения в лечении мышечной дистрофии.
[20] Антисмысловой олигомер по приведенному выше п.19, где пациентом с мышечной дистрофией в указанном лечении является пациент с делециями нуклеотидов внутри экзонов 29-50, 50, 45-50, 48-50, 49-50, 52, 52-63, 13-50, 19-50, 43-50 или 47-50.
[21] Антисмысловой олигомер по приведенному выше п.19 или 20, где пациентом является человек.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
[0014] Антисмысловой олигомер настоящего изобретения может индуцировать пропуск экзона 51 в гене дистрофина человека с высокой эффективностью. Также симптомы мышечной дистрофии Дюшенна можно эффективно облегчить посредством введения фармацевтической композиции настоящего изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0015] Фиг. 1 показывает эффективность пропуска экзона 51 в гене дистрофина человека в линии клеток рабдомиосаркомы человека (клетки RD).
Вариант осуществления настоящего изобретения
[0016] Здесь и далее приведено подробное описание настоящего изобретения. Варианты осуществления настоящего изобретения, описанные ниже, приведены в качестве примера, лишь для описания настоящего изобретения, но не для ограничения настоящего изобретения следующими вариантами осуществления настоящего изобретения. Настоящее изобретение можно осуществить различными способами, не отступая от сути настоящего изобретения.
[0017] 1. Антисмысловой олигомер
Настоящее изобретение представляет антисмысловой олигомер (здесь и далее называемый антисмысловым олигомером настоящего изобретения), который вызывает пропуск экзона 51 в гене дистрофина человека с высокой эффективностью.
[0018] [Экзон 51 в гене дистрофина человека]
В настоящем изобретении термин «ген» предназначен для обозначения геномного гена, а также включает кДНК, предшественник мРНК и мРНК. Предпочтительно, чтобы ген был предшественником мРНК, т.е. пре-мРНК.
В геноме человека ген дистрофина человека располагается в локусе Xp21.2. Ген дистрофина человека имеет размер, равный 2,2 миллиона пар нуклеотидов и является самым большим геном среди известных генов человека. Однако кодирующие области гена дистрофина человека, рассредоточенные в виде 79 экзонов на всем протяжении гена дистрофина человека, составляют лишь 14 т.п.о. (Roberts, RG. et al., Genomics, 16: 536-538 (1993)). Пре-мРНК, которая является транскриптом гена дистрофина человека, подвергается сплайсингу с образованием зрелой мРНК размером 14 т.о. Нуклеотидная последовательность гена дистрофина человека дикого типа известна (№ доступа в GenBank - NM_004006).
Нуклеотидная последовательность экзона 51 в гене дистрофина человека дикого типа представлена SEQ ID NO: 3.
[0019] [Антисмысловой олигомер]
Антисмысловой олигомер настоящего изобретения создан для индукции пропуска экзона 51 в гене дистрофина человека, с модифицированием тем самым белка, кодируемого геном дистрофина типа МДД, в белок дистрофина типа МДБ. Соответственно, экзон 51 в гене дистрофина, который является мишенью пропуска экзона с помощью антисмыслового олигомера, включает как дикий тип, так и мутантные типы.
[0020] Антисмысловой олигомер настоящего изобретения является именно антисмысловым олигомером, выбираемым из группы, состоящей из приведенных ниже п. с (a) по (d).
(a) антисмысловой олигомер, содержащий нуклеотидную последовательность SEQ ID NO: 1 или 2;
(b) антисмысловой олигомер, состоящий из нуклеотидной последовательности, содержащей делецию, замену, вставку и/или добавление 1-5 нуклеотидов в нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека;
(c) антисмысловой олигомер, имеющий нуклеотидную последовательность, по меньшей мере на 80% идентичную нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека; и
(d) антисмысловой олигомер, который гибридизуется в строгих условиях с олигонуклеотидом, состоящим из нуклеотидной последовательности, комплементарной нуклеотидной последовательности SEQ ID NO: 1 или 2, и обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
[0021] В частности, антисмысловые олигомеры по п. с (b) по (d) являются мутантами антисмыслового олигомера по п. (a) и соответствуют мутациям в гене дистрофина у пациентов, напр., полиморфизму.
В другом варианте осуществления настоящего изобретения антисмысловой олигомер настоящего изобретения является именно антисмысловым олигомером, выбираемым из группы, состоящей из приведенных ниже п. с (k) по (n).
(k) антисмысловой олигомер, содержащий нуклеотидную последовательность, представленную любой из SEQ ID NOs: 6-33;
(l) антисмысловой олигомер, состоящий из нуклеотидной последовательности, содержащей делецию, замену, вставку и/или добавление 1-5 нуклеотидов в нуклеотидной последовательности, представленной любой из SEQ ID NOs: 6-33, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека;
(m) антисмысловой олигомер, имеющий нуклеотидную последовательность, по меньшей мере на 80% идентичную нуклеотидной последовательности любой из SEQ ID NOs: 6-33, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека; и
(n) антисмысловой олигомер, который гибридизуется в строгих условиях с олигонуклеотидом, состоящим из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, представленной любой из SEQ ID NOs: 6-33, и обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
В частности, антисмысловые олигомеры по п. с (l) по (n) являются мутантами антисмыслового олигомера по п. (k) и соответствуют мутациям в гене дистрофину у пациентов, напр., полиморфизму.
Также антисмысловой олигомер настоящего изобретения является антисмысловым олигомером, выбираемым из группы, состоящей из приведенных ниже п. с (o) по (r).
(o) антисмысловой олигомер, состоящий из нуклеотидной последовательности, представленной любой из SEQ ID NOs: 6-33;
(p) антисмысловой олигомер, состоящий из нуклеотидной последовательности, содержащей делецию, замену, вставку и/или добавление 1-3 нуклеотидов в нуклеотидной последовательности, представленной любой из SEQ ID NOs: 6-33, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека;
(q) антисмысловой олигомер, имеющий нуклеотидную последовательность, по меньшей мере на 80% идентичную нуклеотидной последовательности любой из SEQ ID NOs: 6-33, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека; и
(r) антисмысловой олигомер, который гибридизуется в строгих условиях с олигонуклеотидом, состоящим из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, представленной любой из SEQ ID NOs: 6-33, и обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
Более того, антисмысловой олигомер настоящего изобретения является антисмысловым олигомером, выбираемым из группы, состоящей из приведенных ниже п. (i) и (j):
(i) антисмысловой олигомер, состоящий из нуклеотидной последовательности, любой из SEQ ID NOs: 6-33; или
(j) антисмысловой олигомер, состоящий из нуклеотидной последовательности, по меньшей мере на 90% идентичной нуклеотидной последовательности любой из SEQ ID NOs: 6-33, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
[0022] Как применяют в настоящей заявке, термин «антисмысловой олигомер, который гибридизуется в строгих условиях», относится, например, к антисмысловому олигомеру, получаемому при гибридизации колоний, гибридизации бляшек, гибридизации по Саузерну и т.п., используя в качестве зонда весь олигонуклеотид, состоящий из нуклеотидной последовательности, комплементарной нуклеотидной последовательности, например, SEQ ID NO: 1, или его часть. Способ гибридизации, который можно использовать, включает способы, описанные, например, в "Sambrook & Russell, Molecular Cloning: A Laboratory Manual Vol. 3, Cold Spring Harbor, Laboratory Press 2001," "Ausubel, Current Protocols in Molecular Biology, John Wiley & Sons 1987-1997," и пр.
[0023] Как применяют в настоящей заявке, ʺстрогие условия» могут быть любыми из условий «малой строгости», условий «средней строгости» и чрезмерно строгих условий. Условиями «малой строгости» являются, например, 5×SSC, 5×раствор Денхардта, 0,5% додецилсульфат натрия, 50% формамид при 32°С. Условиями «средней строгости» являются, например, 5×SSC, 5×раствор Денхардта, 0,5% додецилсульфат натрия, 50% формамид при 42°С или 5×SSC, 1% додецилсульфат натрия, 50 мМ Трис-HCl (pH 7,5), 50% формамид при 42°С. Чрезмерно строгими условиями являются, например, (1) 5×SSC, 5×раствор Денхардта, 0,5% додецилсульфат натрия, 50% формамид при 50°С, (2) 0,2×SSC, 0,1% додецилсульфат натрия при 60°С, (3) 0,2×SSC, 0,1% додецилсульфат натрия при 62°С, (4) 0,2×SSC, 0,1% додецилсульфат натрия при 65°С или (5) 0,1×SSC, 0,1% додецилсульфат натрия при 65°С, но не ограничиваются ими. В этих условиях ожидается, что антисмысловые олигомеры с большей гомологией будут с успехом получены при более высоких температурах, хотя в строгость гибридизации вовлечены разнообразные факторы, включающие температуру, концентрацию зонда, длину зонда, ионную силу, время, концентрацию соли и другие, и специалисты в данной области техники могут приблизительно подобрать эти факторы для достижения схожей строгости.
[0024] При применении для гибридизации имеющихся в продаже наборов можно использовать, например, Alkphos Direct Labeling and Detection System (GE Healthcare). В этом случае в соответствии с приложенным протоколом после культивирования с меченым зондом в течение ночи мембрану отмывают основным буфером для отмывки, содержащим 0,1% (вес/объем) додецилсульфата натрия при 55°С, выявляя тем самым гибридизованный антисмысловой олигомер. Альтернативно, в случае создания зонда на основе всей нуклеотидной последовательности, комплементарной нуклеотидной последовательности SEQ ID NO: 3, или ее части гибридизацию можно выявить с помощью набора DIG Nucleic Acid Detection Kit (Roche Diagnostics), когда зонд метят дигоксигенином (DIG), используя имеющийся в продаже реагент (например, PCR Labeling Mix (Roche Diagnostics), и т.п.).
[0025] Помимо антисмысловых олигомеров, описанных выше, другие антисмысловые олигомеры, которые могут гибридизоваться, включают антисмысловые олигомеры, идентичные на 90% или более, 91% или более, 92% или более, 93% или более, 94% или более, 95% или более, 96% или более, 97% или более, 98% или более, 99% или более, 99,1% или более, 99,2% или более, 99,3% или более, 99,4% или более, 99,5% или более, 99,6% или более, 99,7% или более, 99,8% или более, или 99,9% или более нуклеотидной последовательности SEQ ID NO: 1 или 2, в соответствии с расчетом с использованием программ для поиска гомологии, таких как FASTA и BLAST, с применением параметров, заданных по умолчанию.
[0026] Идентичность нуклеотидных последовательностей можно определить, используя FASTA (Science 227 (4693): 1435-1441, (1985)) или алгоритм BLAST (Basic Local Alignment Search Tool средство поиска основного локального совмещения) Karlin и Altschul (Proc. Natl. Acad. Sci. USA 872264-2268, 1990; Proc. Natl. Acad. Sci. USA 90: 5873, 1993). Были разработаны программы, названные blastn, blastx, tblastn и tblastx, на основе алгоритма BLAST (Altschul SF et al., J. Mol. Biol. 215: 403, 1990). В случае установления нуклеотидной последовательности, используя blastn, параметрами являются, например, оценка=100 и длина слова=12. В случае использования программ BLAST и Gapped BLAST (BLAST с использованием пропусков) применяют параметры, заданные по умолчанию для каждой программы.
[0027] Термин «вызывает пропуск экзона 51 в гене дистрофина человека», предназначен для обозначения того, что в результате связывания антисмыслового олигомера настоящего изобретения с сайтом, соответствующим экзону 51 транскрипта (например, пре-мРНК) гена дистрофина человека, например, связывания в результате сплайсинга нуклеотидной последовательности, соответствующей 5'-концу экзона 53 с 3'-концом экзона 50, у пациентов с МДД с делецией экзона 52, когда транскрипт подвергается сплайсингу, образуется зрелая мРНК, в которой нет сдвига рамки считывания.
[0028] В настоящей заявке описанное выше «связывание», как предполагается, означает, что при смешивании антисмыслового олигомера настоящего изобретения с транскриптом с гена дистрофина человека, оба гибридизуются в физиологических условиях с образованием двухцепочечной нуклеиновой кислоты. Термин «в физиологических условиях» относится к условиям, заданным для воспроизводства in vivo окружения по показателю рН, состава солей и температуры. Условиями являются, например, 25-40°С, предпочтительно 37°С, рН 5-8, предпочтительно рН 7,4, и 150 мМ концентрация хлорида натрия.
[0029] Вызывается или нет пропуск экзона 51 в гене дистрофина человека, можно подтвердить посредством введения антисмыслового олигомера настоящего изобретения в клетку, экспрессирующую дистрофин (например, в клетки рабдомиосаркомы человека), амплификации района, окружающего экзон 51 мРНК с гена дистрофина человека, на основе общей РНК из клетки, экспрессирующей дистрофин, с помощью ОТ-ПЦР и выполнения «вложенной» ПЦР или анализа последовательности на амплифицированном с помощью ПЦР продукте.
Эффективность пропуска можно определить следующим образом. мРНК гена дистрофина человека выделяют из исследуемых клеток; в мРНК измеряют уровень «А» полинуклеотидной полосы в случае, когда экзон 51 пропущен, и уровень «В» полинуклеотидной полосы в случае, когда экзон 51 не пропущен. Используя эти величины измерений «А» и «В», рассчитывают эффективность согласно следующему уравнению:
Эффективность пропуска (%)=A/(A+B)×100
[0030] Предпочтительно, чтобы антисмысловой олигомер настоящего изобретения вызывал пропуск экзона 51 с эффективностью равной 10% или более, 20% или более, 30% или более, 40% или более, 50% или более, 60% или более, 70% или более, 80% или более и 90% или более.
Расчет эффективности пропуска можно посмотреть в Международной публикации заявки WO2012/029986.
[0031] Антисмысловой олигомер настоящего изобретения включает, например, олигонуклеотид, морфолино-олигомер или пептидную нуклеиновую кислоту (ПНК), имеющий длину от 16 до 35 нуклеотидов. Предпочтительно, чтобы длина составляла от 19 до 32, от 20 до 31, от 21 до 30 нуклеотидов, и предпочтительными являются морфолино-олигомеры.
[0032] Описанный выше олигонуклеотид (здесь и далее называемый олигонуклеотидом настоящего изобретения) представляет собой антисмысловой олигомер настоящего изобретения, состоящий из нуклеотидов в качестве составных единиц. Такие нуклеотиды могут быть любыми из рибонуклеотидов, дезоксирибонуклеотидов и модифицированных нуклеотидов.
[0033] Модифицированный нуклеотид относится к нуклеотиду, имеющему полностью и частично модифицированные нуклеиновые основания, остатки сахаров и/или области соединения через фосфатную группу, который является рибонуклеотидом или дезоксирибонуклеотидом.
[0034] В настоящем изобретении нуклеиновые основания включают, например, аденин, гуанин, гипоксантин, цитозин, тимин, урацил и их модифицированные основания. Примеры таких модифицированных оснований включают, но не ограничиваются псевдоурацилом, 3-метилурацилом, дигидроурацилом, 5-алкилцитозинами (например, 5-метилцитозином), 5-алкилурацилами (например, 5-этилурацилом), 5-галогенурацилами (5-бромурацилом), 6-азапиримидином, 6-алкилпиримидинами (6-метилурацилом), 2-тиоурацилом, 4-тиоурацилом, 4-ацетилцитозином, 5-(карбоксигидроксиметил)урацилом, 5'-карбоксиметиламинометил-2-тиоурацилом, 5-карбоксиметиламинометилурацилом, 1-метиладенином, 1-метилгипоксантином, 2,2-диметилгуанином, 3-метилцитозином, 2-метиладенином, 2-метилгуанином, N6-метиладенином, 7-метилгуанином, 5-метоксиаминометил-2-тиоурацилом, 5-метиламинометилурацилом, 5-метилкарбонилметилурацилом, 5-метилоксиурацилом, 5-метил-2-тиоурацилом, 2-метилтио-N6-изопентениладенином, урацил-5-оксиуксусной кислотой, 2-тиоцитозином, пурином, 2,6-диаминопурином, 2-аминопурином, изогуанином, индолом, имидазолом, ксантином и т.д.
[0035] Модификация остатка сахара может включать, например, модификации в 2'-положении рибозы и модификации других положений сахара. Модификация в 2'-положении рибозы включает замену 2'-ОН рибозы на OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br и I, где R представляет собой алкил или арил, а R' представляет собой алкилен.
Модификация в других положениях сахара включает, например, замену О в 4'-положении рибозы или дезоксирибозы на S, образование мостика между 2'- и 4'-положениями сахара, например, LNA (locked nucleic acid, закрытой нуклеиновой кислоты) или ENA (2'-O,4'-C-ethylene-bridged nucleic acids, нуклеиновых кислот с 2'-О,4'-С-этиленовым мостиком), но без ограничения ими.
[0036] Модификация области соединения через фосфатную группу включает, например, модификацию с заменой фосфодиэфирной связи на тиофосфатную связь, дитиофосфатную связь, алкилфосфонатную связь, фосфорамидатную связь или боранофосфатную связь (Enya et al., Bioorganic & Medicinal Chemistry, 2008, 18, 9154-9160) (см., например, отечественные повторные публикации в Японии РСТ-заявок с № 2006/129594 и 2006/038608).
[0037] В настоящем изобретении предпочтительно, чтобы алкилом был неразветвленный или разветвленный алкил, содержащий от 1 до 6 атомов углерода. Конкретные примеры включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, неопентил, трет-пентил, н-гексил и изогексил. Алкил может необязательно быть замещенным. Примерами таких заместителей являются галоген, алкокси, циано и нитро. Алкил может быть замещен 1-3 заместителями.
В настоящем изобретении предпочтительно, чтобы циклоалкилом был циклоалкил, содержащий 5-12 атомов углерода. Конкретные примеры включают циклопентил, циклогексил, циклогептил, циклооктил, циклодецил и циклододецил.
В настоящем изобретении галоген включает фтор, хлор, бром и йод.
Алкокси представляет собой неразветвленный или разветвленный алкокси, содержащий 1-6 атомов углерода, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси, н-пентилокси, изопентилокси, н-гексилокси, изогексилокси и т.д. Среди прочего, алкокси, содержащий 1-3 атомов углерода, является предпочтительным.
[0038] В настоящем изобретении предпочтительно, чтобы арилом был арил, содержащий 6-10 атомов углерода. Конкретные примеры включают фенил, α-нафтил и β-нафтил. Среди прочих, предпочтительным является фенил. Арил может быть, при желании, замещенным. Примерами таких заместителей являются алкил, галоген, алкокси, циано и нитро. Арил может быть замещен одним-тремя такими заместителями.
В настоящем изобретении предпочтительно, чтобы алкиленом был неразветвленный или разветвленный алкилен, содержащий от 1 до 6 атомов углерода. Конкретные примеры включают метилен, этилен, триметилен, тетраметилен, пентаметилен, гексаметилен, 2-(этил)триметилен и 1-(метил)тетраметилен.
В настоящем изобретении ацил включает неразветвленный или разветвленный алканоил или ароил. Примеры алканоила включают формил, ацетил, 2-метилацетил, 2,2-диметилацетил, пропионил, бутирил, изобутирил, пентаноил, 2,2-диметилпропионил, гексаноил и т.д. Примеры ароила включают бензоил, толуоил и нафтоил. Ароил может быть при желании замещенным в замещаемых положениях и может быть замещен алкилом(ами).
[0039] Предпочтительно, чтобы олигонуклеотидом настоящего изобретения был антисмысловой олигомер настоящего изобретения, содержащий составную единицу, представляемую общей формулой ниже, где группа -ОН в положении 2' рибозы замещена метокси, а областью соединения через фосфатную группу является тиофосфатная связь:
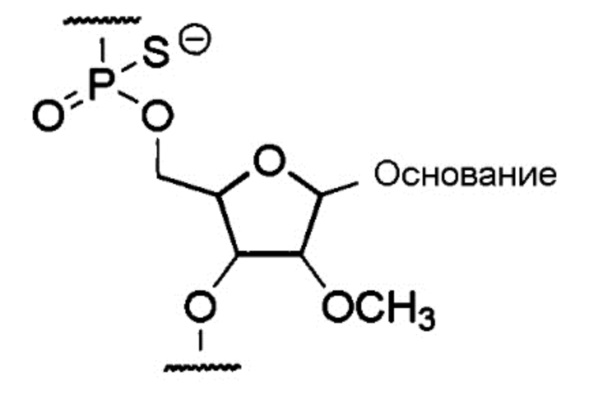
где основание представляет собой нуклеиновое основание.
[0040] Олигонуклеотид настоящего изобретения можно без труда синтезировать, используя различные автоматизированные синтезаторы (например, AKTA oligopilot plus 10/100 (GE Healthcare)). В альтернативном случае синтез можно также поручить сторонней организации (например, Promega Inc., Takara Co. или Japan Bio Service Co.) и т.д.
[0041] Морфолино-олигомером настоящего изобретения является антисмысловой олигомер настоящего изобретения, содержащий составную единицу, представленную общей формулой ниже:
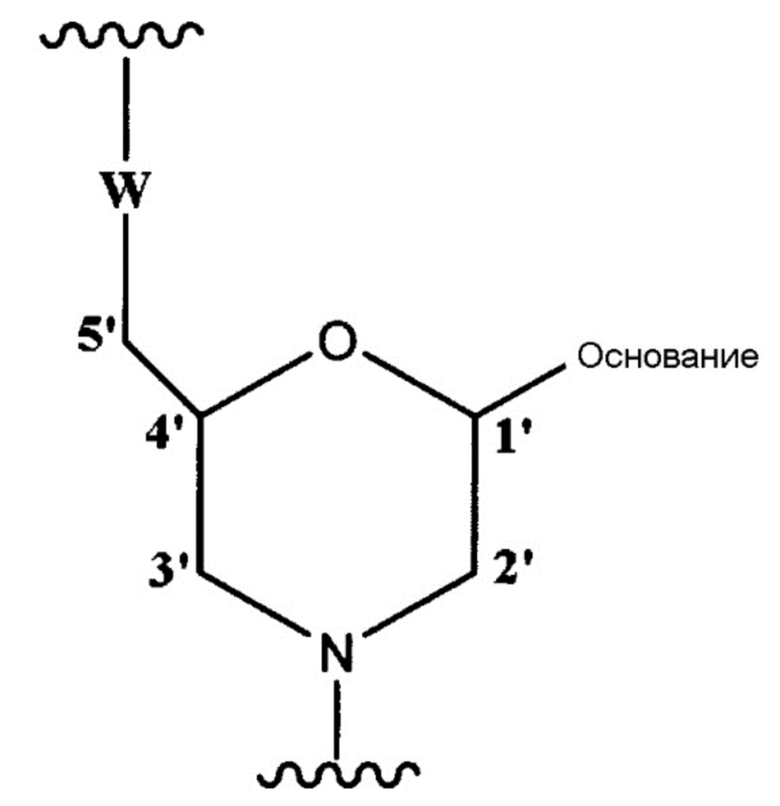
где основание имеет то же определенное выше значение, и
W представляет собой группу, представленную любой из следующих групп:
[0042]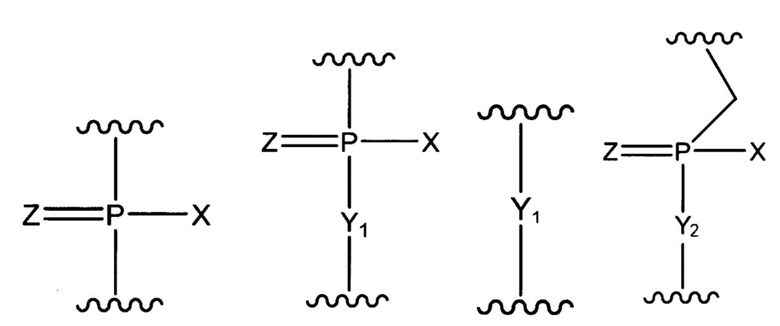
где X представляет собой -CH2R1, -O-CH2R1, -S-CH2R1, -NR2R3 или F;
R1 представляет собой Н или алкил;
R2 и R3, которые могут быть одинаковыми или различными, представляют собой каждый Н, алкил, циклоалкил или арил;
Y1 представляет собой O, S, CH2 или NR1;
Y2 представляет собой O, S или NR1;
Z представляет собой O или S.
[0043] Предпочтительно, чтобы морфолино-олигомером был олигомер, содержащий составную единицу, представленную общей формулой ниже, (морфолино-фосфородиамидатный олигомер (здесь далее называемый РМО, phosphorodiamidate morpholino oligomer)).
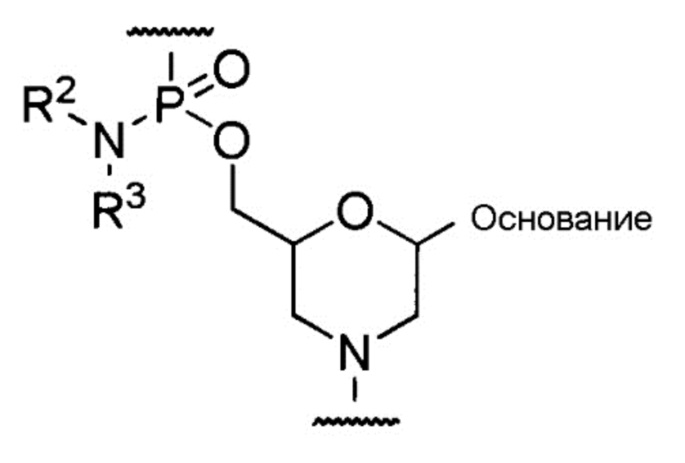
где основание, R2 и R3 имеют то же определенное выше значение.
Морфолино олигомер настоящего изобретения содержит полностью или частично модифицированные нуклеиновые основания, группы морфолинового кольца, области соединения через фосфатную группу, 3'-конец и/или 5'-конец, составляющие морфолино-олигомер.
[0044] Модификация области соединения через фосфатную группу включает, например, модификацию с заменой фосфородиамидатной связью, тиофосфатной связью, дитиофосфатной связью, алкилфосфонатной связью, фосфорамидатной связью и боранофосфатной связью (Enya et al., Bioorganic & Medicinal Chemistry, 2008, 18, 9154-9160) (см., например, отечественные повторные публикации в Японии РСТ-заявок с № 2006/129594 и 2006/038608).
Морфолино олигомер можно получить в соответствии, например, с WO 1991/009033 или WO 2009/064471. В частности, РМО можно получить с помощью процедуры, описанной в WO 2009/064471, или получить с помощью представленного ниже процесса.
[0045] [Способ получения PMO]
Вариантом РМО является, например, соединение, представляемое общей формулой (I) ниже, (здесь и далее РМО (I)).
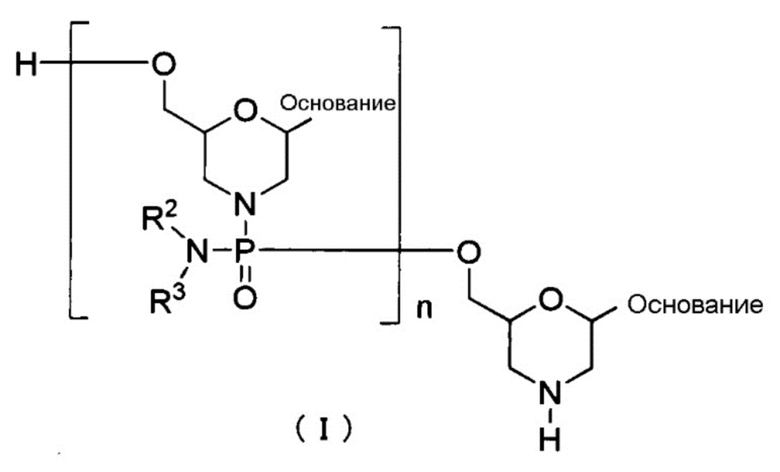
где основание, R2 и R3 имеют то же определенное выше значение; и,
n является заданным целым числом от 1 до 99, предпочтительно, заданным целым числом от 24 до 34, от 27 до 31 или от 28 до 30, предпочтительно, 29.
[0046] РМО (I) можно получить в соответствии с известным способом, например можно получить посредством выполнения следующих стадий процедур.
Соединения и реагенты, используемые в стадиях ниже, специально не ограничены при условии, что их обычно используют для получения РМО.
Также все следующие стадии можно выполнить с использованием жидкофазного способа или твердофазного способа (используя руководства и имеющиеся в продаже автоматизированные устройства для твердофазного синтеза). При получении РМО твердофазным способом желательно использовать автоматизированный синтезатор ввиду простых технических требований и точного синтеза.
[0047] (1) Стадия A:
Соединение, представленное общей формулой (II) ниже (здесь и далее называемого Соединением (II)) реагирует с кислотой с образованием соединения, представленного общей формулой (III) ниже (здесь и далее называемого Соединением (III)):
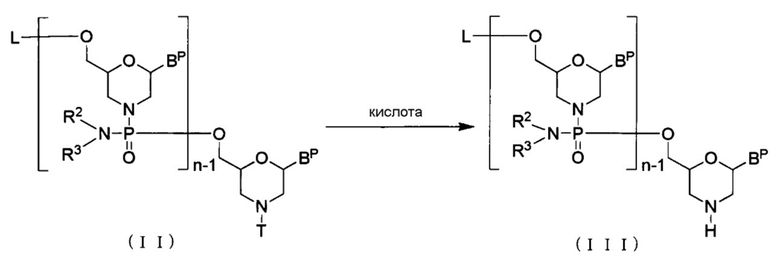
где n, R2 и R3 имеют то же определенное выше значение;
каждое BP независимо представляет собой нуклеиновое основание, которое при желании может быть защищено;
Т представляет собой тритил, монометокситритил или диметокситритил; и
L представляет собой водород, ацил или группу, представленную общей формулой (IV) ниже, (здесь и далее называемую группой (IV).
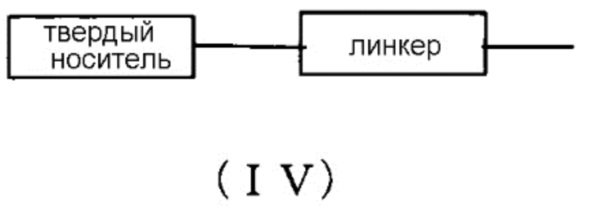
[0048] В случае BP «нуклеиновое основание» включает то же нуклеиновое основание, что в случае «основания» при условии, что аминогруппу или гидроксильную группу в нуклеиновом основании, представленном BP, можно защитить.
Такая защитная группа для аминогруппы специально не ограничивается при условии, что она используется в качестве защитной группы для нуклеиновых кислот. Конкретные примеры включают бензоил, 4-метоксибензоил, ацетил, пропионил, бутирил, изобутирил, фенилацетил, феноксиацетил, 4-трет-бутилфеноксиацетил, 4-изопропилфеноксиацетил и (диметиламино)метилен. Конкретные примеры защитной группы для гидроксильной группы включают 2-цианоэтил, 4-нитрофенетил, фенилсульфонилэтил, метилсульфонилэтил и триметилсилилэтил, и фенил, который может быть замещен 1-5 электроноакцепторными группами в оптимальных замещаемых положениях, дифенилкарбамоил, диметилкарбамоил, диэтилкарбамоил, метилфенилкарбамоил, 1-пиролидинилкарбамоил, морфолинокарбамоил, 4-(трет-бутилкарбокси)бензил, 4-[(диметиламино)карбокси]бензил и 4-(фенилкарбокси)бензил (см., например, WO 2009/064471).
[0049] «Твердый носитель» специально не ограничивается при условии, что это носитель, применяемый для твердофазной реакции синтеза нуклеиновых кислот. Желательно, чтобы твердый носитель обладал следующими свойствами: например, (i) был труднорастворимым в реагентах, которые можно использовать для синтеза морфолино-производных нуклеиновых кислот, (например, в дихлорметане, ацетонитриле, тетразоле, N-метилимидазоле, пиридине, уксусном ангидриде, лутидине, трифторуксусной кислоте); (ii) был химически устойчивым к реагентам, используемым для синтеза морфолино-производных нуклеиновых кислот; (iii) его можно было химически модифицировать; (iv) его можно было нагрузить желаемыми морфолино-производными нуклеиновых кислот; (v) он обладал прочностью, достаточной, чтобы выдерживать высокое давление на протяжении всех обработок; и (vi) он характеризовался постоянным диапазоном диаметра частиц и их распределением. В частности, он включает поддающийся разбуханию полистирол (например, аминометилполистирольную смолу, поперечно сшитую 1% дивинилбензолом (200-400 меш) (2,4-3,0 ммоль/г) (производства Tokyo Chemical Industry), аминометилированную полистирольную смолу ·HCl [1% дивинилбензола, 100-200 меш] (производства Peptide Institute, Inc.)), не поддающийся разбуханию полистирол (например, основной носитель (производства GE Healthcare), присоединенный к цепи ПЭГ полистирол (например, NH2-ПЭГ-смолу (производства Watanabe Chemical Co), смолу TentaGel), стекло с контролируемым размером пор (стекло с контролируемым размером пор; CPG) (производства, например, CPG), оксалильное стекло с контролируемым размером пор (см., например, Alul et al., Nucleic Acid Research, Vol. 19, 1527 (1991)), носитель TentaGel-аминополиэтиленгликоль-дериватизированный носитель (например, Wright et al., см., Tetrahedron Letters, Vol. 34, 3373 (1993) и сополимер Poros-полистирол/дивинилбензол.
«Линкер», который можно применять, является известным линкером, обычно используемым для соединения нуклеиновых кислот или морфолино-производных нуклеиновых кислот. Примеры включают 3-аминопропил, сукцинил, 2,2'-диэтанолсульфонил и длинноцепочечный алкиламино (LCAA, long-chain alkyl amino).
[0050] Эту стадию можно выполнить, проводя реакцию между Соединением (II) и кислотой.
[0051] «Кислота», которую можно использовать на этой стадии, включает, например, трифторуксусную кислоту, дихлоруксусную кислоту и трихлоруксусную кислоту. Соответственно, используемая кислота находится в диапазоне, например, от 0,1 моль-эквивалента до 1000 моль-эквивалентов, если исходить из 1 моль Соединения (II), предпочтительно, в диапазоне от 1 моль-эквивалента до 100 моль-эквивалентов, если исходить из 1 моль Соединения (II)
В сочетании с описанной выше кислотой можно использовать органический амин. Органический амин специально не ограничивается и включает, например, триэтиламин. Соответственно, количество используемого органического амина находится в диапазоне, например, от 0,01 моль-эквивалентов до 10 моль-эквивалентов и, предпочтительно, в диапазоне от 0,1 моль-эквивалентов до 2 моль-эквивалентов, если исходить из 1 моль кислоты.
В случае использования на этой стадии соли или смеси кислоты и органического амина соль или смесь включает, например, соль или смесь трифторуксусной кислоты и триэтиламина, а конкретнее, смесь 1 эквивалента триэтиламина и 2 эквивалентов трифторуксусной кислоты.
Кислота, которую можно применять на этой стадии, можно также применять в форме, разведенной в соответствующем растворителе, в концентрации, составляющей от 0,1% до 30%. Растворитель специально не ограничивается, когда речь идет об инертном по отношению к реакции растворителе, и включает, например, дихлорметан, ацетонитрил, спирт (этанол, изопропанол, трифторэтанол и т.д.), воду или их смесь.
[0052] Предпочтительно, чтобы температура описанной выше реакции находилась в диапазоне, например, от 10°С до 50°С, предпочтительнее, в диапазоне от 20°С до 40°С и, наиболее предпочтительно, в диапазоне от 25°С до 35°.
Время реакции может варьировать в зависимости от вида используемой кислоты и температуры реакции и находится, соответственно, в диапазоне, как правило, от 0,1 минуты до 24 часов, предпочтительно, в диапазоне от 1 минуты до 5 часов.
[0053] После завершения этой стадии можно добавить основание, при необходимости, для нейтрализации кислоты, оставшейся в системе. «Основание» специально не ограничивается и включает, например, диизопропиламин. Основание можно также применять в форме, разведенной в соответствующем растворителе, в концентрации, составляющей от 0,1% (объем/объем) до 30% (объем/объем).
Растворитель, применяемый на этой стадии, специально не ограничивается, когда речь идет об инертном по отношению к реакции растворителе, и включает дихлорметан, ацетонитрил, спирт (этанол, изопропанол, трифторэтанол и т.д.), воду или их смесь. Предпочтительно, чтобы температура описанной выше реакции находилась в диапазоне, например, от 10°С до 50°С, предпочтительнее, в диапазоне от 20°С до 40°С и, наиболее предпочтительно, в диапазоне от 25°С до 35°С.
Время реакции может варьировать в зависимости от вида используемой кислоты и температуры реакции и находится, соответственно, в диапазоне, как правило, от 0,1 минуты до 24 часов, предпочтительно, в диапазоне от 1 минуты до 5 часов.
[0054] В случае Соединения (II) соединение общей формулы (IIa) ниже (в дальнейшем Соединение (IIa)), где n равно 1, а L представляет собой группу (IV), можно получить с помощью следующей процедуры.
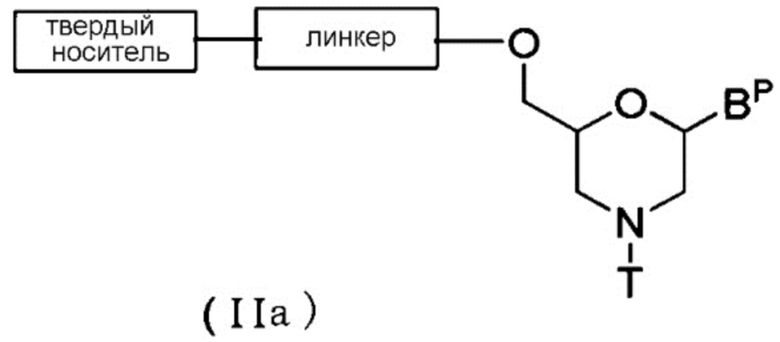
где BP, T, линкер и твердый носитель имеют то же определенное выше значение.
[0055] Стадия 1:
Соединение, представленное общей формулой (V) ниже, реагирует с ацилирующим агентом с образованием соединения, представленного общей формулой (VI) ниже (здесь и далее называемого Соединением (VI)).
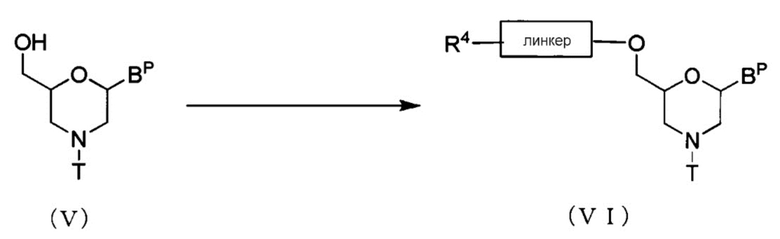
где BP, T и линкер имеют то же определенное выше значение; и,
R4 представляет собой гидрокси- галогеновую, карбоксильную или аминогруппу.
[0056] Эту стадию можно выполнить с помощью известных процедур для введения линкеров, используя Соединение (V) в качестве исходного вещества.
В частности, соединение, представленное общей формулой (VIa) ниже, можно получить посредством выполнения способа, известного как этерификация, используя Соединение (V) и янтарный ангидрид.
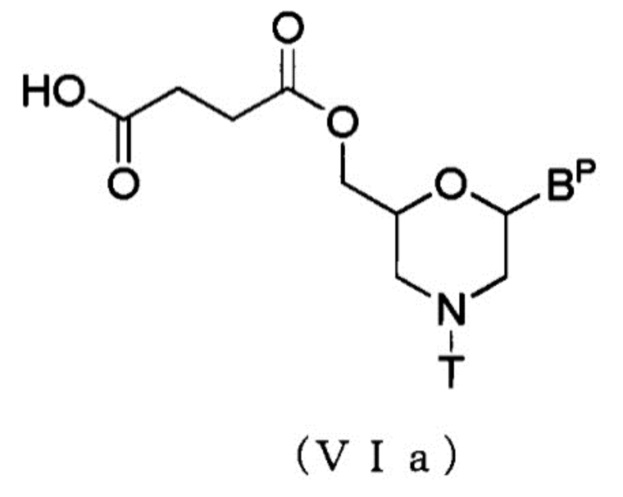
где BP и T имеют то же определенное выше значение.
[0057] Стадия 2:
Соединение (VI) реагирует с твердым носителем с помощью конденсирующего агента с образованием Соединения (IIa).
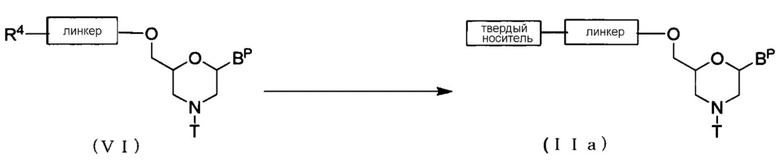
где BP, R4, T, линкер и твердый носитель имеют то же определенное выше значение.
Эту стадию можно выполнить, используя Соединение (VI) и твердый носитель, в соответствии с процессом, известным как реакция конденсации.
В случае Соединения (II) соединение, представленное общей формулой (IIa2) ниже, где n равно 2-99 (предпочтительно, n является заданным целым числом от 25 до 35, от 28 до 32 или от 29 до 31, предпочтительно 30), а L является группой, представленной общей формулой (IV), можно получить, используя Соединение (IIa) в качестве исходного материала и повторяя стадию А и стадию В способа получения РМО, описанного здесь, нужное число раз.
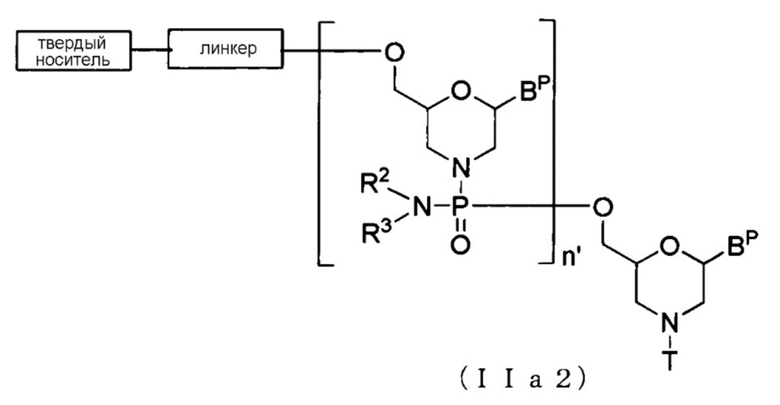
где BP, R2, R3, T, линкер и твердый носитель имеют то же определенное выше значение; и,
n' составляет от 1 до 98 (в конкретном варианте осуществления настоящего изобретения, n' составляет от 1 до 34, от 1 до 33, от 1 до 32, от 1 до 31, от 1 до 30, от 1 до 29, от 1 до 28, от 1 до 27, от 1 до 26, от 1 до 25, от 1 до 24).
[0058] (2) Стадия B
Соединение (III) реагирует с морфолино-мономерным соединением в присутствии основания с образованием соединения, представленного общей формулой (VII) ниже (здесь и далее называемого Соединением (VII)):
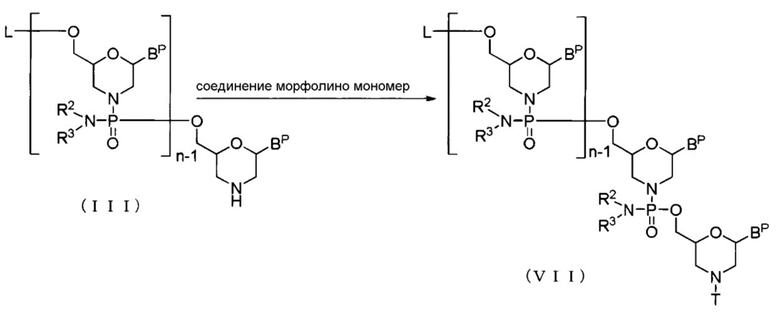
где BP, L, n, R2, R3 и T имеют то же определенное выше значение.
[0059] Эту стадию можно выполнить, проведя реакцию Соединения(III) с морфолино-мономерным соединением в присутствии основания.
[0060] Морфолино-мономерное соединение включает, например, соединения, представленные общей формулой (VIII) ниже:
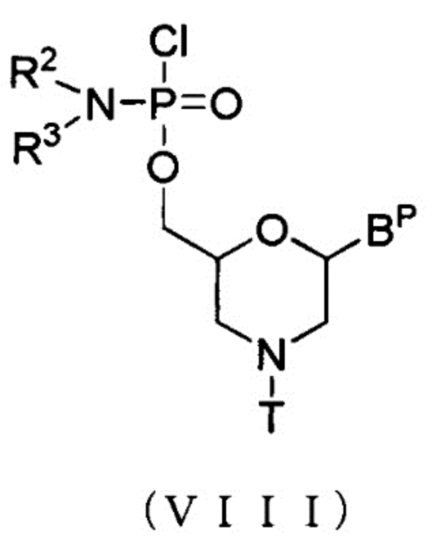
где BP, R2, R3 и T имеют то же определенное выше значение.
Основание», которое можно применять на этой стадии, включает, например, диизопропиламин, триэтиламин и N-этилморфолин. Применяемое количество основания находится, соответственно, в диапазоне от 1 моль-эквивалента до 1000 моль-эквивалентов, если исходить из 1 моль Соединения (III), предпочтительно, от 10 моль-эквивалентов до 100 моль-эквивалентов, если исходить из 1 моль соединения (III).
Морфолино-мономерное соединение и основание, которые можно применять на этой стадии, можно также использовать в форме, разведенной в соответствующем растворителе, в концентрации, составляющей от 0,1% до 30%. Растворитель специально не ограничивается, когда речь идет об инертном по отношению к реакции растворителе, и включает, например, N,N-диметилимидазолидон, N-метилпиперидон, диметилформамид, дихлорметан, ацетонитрил, тетрагидрофуран или их смесь.
[0061] Предпочтительно, чтобы температура реакции находилась в диапазоне, например, от 0°С до 100°С, предпочтительнее, в диапазоне от 10°С до 50°С.
Время реакции может варьировать в зависимости от вида используемого основания и температуры реакции и находится, соответственно, в диапазоне, как правило, от 1 минуты до 48 часов, предпочтительно, в диапазоне от 30 минут до 24 часов.
[0062] Кроме того, после завершения этой стадии можно добавить ацилирующий агент, в случае необходимости. «Ацилирующий агент» включает, например, уксусный ангидрид, ацетилхлорид и феноксиуксусный ангидрид. Ацилирующий агент может также использоваться в виде разведения соответствующим растворителем в концентрации, составляющей от 0,1% до 30%. Растворитель специально не ограничивается, когда речь идет об инертном по отношению к реакции растворителе, и включает, например, дихлорметан, ацетонитрил, тетрагидрофуран, спирт(ы) (этанол, изопропанол, трифторэтанол и т.д.), воду или их смесь.
При необходимости, основание, такое как пиридин, лутидин, коллидин, триэтиламин, диизопропилэтиламин, N-этилморфолин и т.д., можно также применять в комбинации с ацилирующим агентом. Количество ацилирующего агента находится, соответственно, в диапазоне от 0,1 моль-эквивалентов до 10000 моль-эквивалентов и, предпочтительно, в диапазоне от 1 моль-эквивалента до 1000 моль-эквивалентов. Количество основания находится, соответственно, в диапазоне, например, от 0,1 моль-эквивалентов до 100 моль-эквивалентов и, предпочтительно, в диапазоне от 1 моль-эквивалента до 10 моль-эквивалентов, если исходить из 1 моль ацилирующего агента.
Предпочтительно, чтобы температура этой реакции находилась в диапазоне от 10°С до 50°С, предпочтительнее, в диапазоне от 10°С до 50°С, еще более предпочтительно, в диапазоне от 20°С до 40°С и, наиболее предпочтительно, в диапазоне от 25°С до 35°С. Время реакции может варьировать в зависимости от вида используемого ацилирующего агента и температуры реакции и находится, соответственно, в диапазоне, как правило, от 0,1 минуты до 24 часов, предпочтительно, в диапазоне от 1 минуты до 5 часов.
[0063] (3) Стадия C:
В Соединении (VII), полученном на Стадии B, защитную группу удаляют, применяя агент для снятия защиты, с образованием соединения, представленного общей формулой (IX).
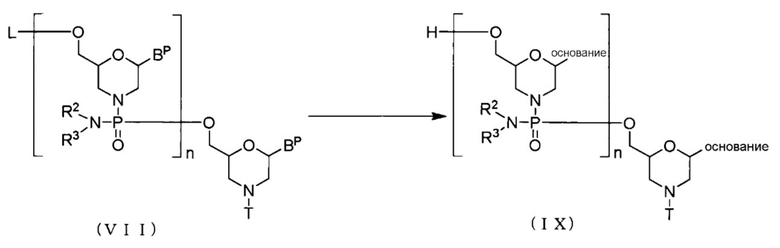
где основание, BP, L, n, R2, R3 и T имеют то же определенное выше значение.
[0064] Эту стадию можно выполнить, проведя реакцию Соединения(VII) с агентом для снятия защиты.
[0065] «Агент для снятия защиты» включает, например, концентрированный водный раствор аммиака и метиламин. «Агент для снятия защиты», применяемый на этой стадии, можно также применять в форме, разведенной, например, водой, метанолом, этанолом, изопропиловым спиртом, ацетонитрилом, тетрагидрофураном, диметилформамидом, N,N-диметилимидазолидоном, N-метилпиперидоном или смесью этих растворителей. Среди прочих предпочтительным является этанол. Применяемое количество агента для снятия защиты находится, соответственно, в диапазоне, например, от 1 моль-эквивалента до 100000 моль-эквивалентов и, предпочтительно, в диапазоне от 10 моль-эквивалентов до 1000 моль-эквивалентов, если исходить из 1 моль соединения (VII).
[0066] Предпочтительно, чтобы температура реакции находилась в диапазоне от 15°С до 75°С, предпочтительнее, в диапазоне от 40°С до 70°С, еще более предпочтительно, в диапазоне от 50°С до 60°С. Время реакции снятия защиты может варьировать в зависимости от вида используемого Соединения (VII), температуры реакции и т.п., и находится, соответственно, в диапазоне, как правило, от 10 минут до 30 часов, предпочтительно, в диапазоне от 30 минут до 24 часов и, еще более предпочтительно, в диапазоне от 5 часов до 20 часов.
[0067] (4) Стадия D:
PMO (I) получают, проводя реакцию Соединения (IX), образованного на стадии С, с кислотой:
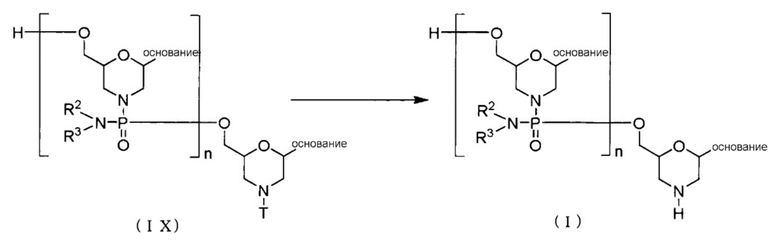
где основание, n, R2, R3 и T имеют то же определенное выше значение.
[0068] Эту стадию можно выполнить, добавив кислоту к Соединению(IX).
[0069] «Кислота», которую можно применять на этой стадии, включает, например, трихлоруксусную кислоту, дихлоруксусную кислоту, уксусную кислоту, фосфорную кислоту, соляную кислоту и т.д. Применяемая кислота используется надлежащим образом, чтобы обеспечивать рН раствора в диапазоне от 0,1 до 4,0 и, предпочтительнее, в диапазоне от 1,0 до 3,0. Растворитель специально не ограничивается, когда речь идет об инертном по отношению к реакции растворителе, и включает, например, ацетонитрил, воду или смесь этих растворителей.
[0070] Соответствующая температура реакции находится в диапазоне от 10°С до 50°С, предпочтительно, в диапазоне от 20°С до 40°С, еще более предпочтительно, в диапазоне от 25°С до 35°С. Время реакции снятия защиты может варьировать в зависимости от вида используемого Соединения (IX), температуры реакции и т.п, и находится, соответственно, в диапазоне от 0,1 минуты до 5 часов, предпочтительно, в диапазоне от 1 минуты до 1 часа и, еще более предпочтительно, в диапазоне от 1 минуты до 30 минут.
[0071] РМО (I) можно получить, проводя с реакционной смесью, полученной на этой стадии, разделение и очистку обычными средствами, таким как экстракция, концентрирование, нейтрализация, фильтрация, разделение центрифугированием, перекристаллизация, хроматография на колонке С8-С18 с обращенной фазой, катионообменная хроматография на колонке, анионообменная хроматография на колонке, гель-фильтрация на колонке, жидкостная хроматография высокого разрешения, диализ, ультрафильтрация и т.д., по отдельности или в сочетании. Таким образом, можно выделить и очистить желаемый РМО (I) (см., например, WO 1991/09033).
При очистке РМО (I) с использованием хроматографии с обращенной фазой в качестве растворителя для элюирования можно применять, например, смесь растворов 20 мМ триэтиламина/ацетатного буфера и ацетонитрила.
При очистке РМО (I) с использованием ионообменной хроматографии в качестве растворителя для элюирования можно применять, например, смесь растворов 1 М солевого раствора и 10 мМ водного раствора гидроксида натрия.
[0072] Пептидная нуклеиновая кислота является олигомером настоящего изобретения, имеющим в качестве составной единицы группу, представленную следующей общей формулой:
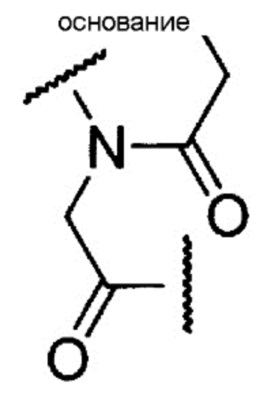
где основание имеет то же определенное выше значение.
[0073] Пептидо-нуклеиновые кислоты можно получить, в соответствии со следующей литературой.
1) P. E. Nielsen, M. Egholm, R. H. Berg, O. Buchardt, Science, 254, 1497 (1991)
2) M. Egholm, O. Buchardt, P. E. Nielsen, R. H. Berg, Jacs., 114, 1895 (1992)
3) K. L. Dueholm, M. Egholm, C. Behrens, L. Christensen, H. F. Hansen, T. Vulpius, K. H. Petersen, R. H. Berg, P. E. Nielsen, O. Buchardt, J. Org. Chem., 59, 5767 (1994)
4) L. Christensen, R. Fitzpatrick, B. Gildea, K. H. Petersen, H. F. Hansen, T. Koch, M. Egholm, O. Buchardt, P. E. Nielsen, J. Coull, R. H. Berg, J. Pept. Sci., 1, 175 (1995)
5) T. Koch, H. F. Hansen, P. Andersen, T. Larsen, H. G. Batz, K. Otteson, H. Orum, J. Pept. Res., 49, 80 (1997)
[0074] В олигомере настоящего изобретения 5'-конец может быть любой из химических структур (1)-(3) ниже и, предпочтительно, является (3)-ОН.
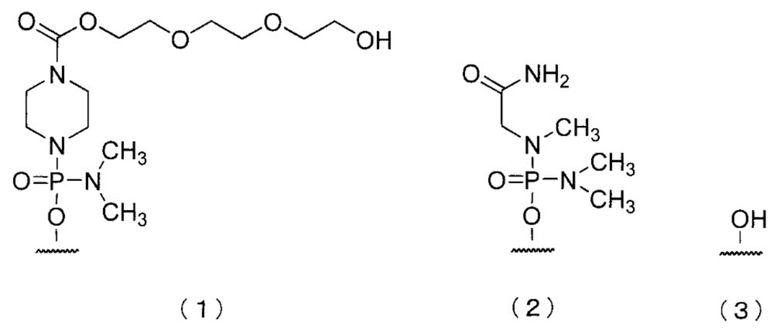
Здесь и далее группы, представленные (1), (2) и (3) выше, называют «группой (1)», «группой (2)» и «группой (3)» соответственно.
[0075] 2. Фармацевтическая композиция
Олигомер настоящего изобретения вызывает пропуск экзона 51 с более высокой эффективностью, чем антисмысловые олигомеры известного уровня техники. Поэтому ожидается, что степень мышечной дистрофии можно уменьшить с высокой эффективностью посредством введения фармацевтической композиции, включающей олигомер настоящего изобретения, пациентам с МДД с мутацией, при которой восстанавливается рамка считывания при пропуске экзона 51, например, пациентам с делецией экзона 29-50, пациентам с делецией экзона 50, пациентам с делецией экзона 45-50, пациентам с делецией экзона 48-50, пациентам с делецией экзона 49-50, пациентам с делецией экзона 52, пациентам с делецией экзона 52-63, пациентам с делецией экзона 13-50, пациентам с делецией экзона 19-50, пациентам с делецией экзона 43-50 или пациентам с делецией экзона 47-50. Например, при применении фармацевтической композиции, содержащей олигомер настоящего изобретения, даже в меньшей дозе, чем доза олигомеров известного уровня техники, можно достичь тех же терапевтических эффектов. Соответственно, можно уменьшить побочные эффекты, и это является экономным.
В другом варианте осуществления настоящее изобретение представляет фармацевтическую композицию для лечения мышечной дистрофии, включающую в качестве активного ингредиента олигомер настоящего изобретения, его фармацевтически приемлемую соль или гидрат, (здесь и далее называемую композицией настоящего изобретения).
Также настоящее изобретение представляет способ лечения мышечной дистрофии, включающий введение пациенту с МДД олигомера настоящего изобретения.
В указанном способе лечения олигомер настоящего изобретения можно вводить в виде фармацевтической композиции для лечения мышечной дистрофии.
Более того, настоящее изобретение представляет применение олигомера настоящего изобретения для получения фармацевтической композиции для лечения мышечной дистрофии и олигомера настоящего изобретения, применимого для лечения мышечной дистрофии.
[0076] Примерами фармацевтически приемлемой соли олигомера настоящего изобретения, содержащейся в композиции настоящего изобретения, являются соли щелочных металлов, такие как соли натрия, калия и лития; соли щелочноземельных металлов, такие как соли кальция и магния; соли металлов, такие как соли алюминия, железа, цинка, меди, никеля, кобальта и т.д., аммонийные соли, соли органических аминов, такие как соли трет-октиламина, дибензиламина, морфолина, глюкозамина, алкилового эфира фенилглицина, этилендиамина, N-метилглюкамина, гуанидина, диэтиламина, триэтиламина, дициклогексиламина, N,N'-дибензилэтилендиамина, хлорпрокаина, прокаина, диэтаноламина, N-бензилфенэтиламина, пиперазина, тетраметиламмония, трис(гидроксиметил)аминометана, соли гидрогалогенидов, такие как соли гидрофторатов, гидрохлоридов, гидробромидов и гидроиодидов, соли неорганических кислот, такие как нитраты, перхлораты, сульфаты, фосфаты и т.д., (низший алкан)сульфонаты, такие как метансульфонаты, трифторметансульфонаты и этансульфонаты, арилсульфонаты, такие как бензолсульфонаты и пара-толуолсульфонаты, соли органических кислот, такие как ацетаты, малаты, фумараты, сукцинаты, цитраты, тартраты, оксалаты, малеаты и т.д., и соли аминокислот, такие как соли глицина, лизина, аргинина, орнитина, глютаминовой кислоты и аспарагиновой кислоты. Эти соли можно получить известными способами. В альтернативном случае олигомер настоящего изобретения, содержащийся в композиции настоящего изобретения, может быть в форме его гидрата.
[0077] Способ введения композиции настоящего изобретения специально не ограничивается при условии, что он является фармацевтически приемлемым путем для введения, и может быть выбран в зависимости от способа лечения. Ввиду легкости доставки в мышечные ткани предпочтительными являются внутривенное введение, внутриартериальное введение, внутримышечное введение, подкожное введение, пероральное введение, введение в ткани, чрескожное введение и т.д. Также лекарственные формы, подходящие для композиции настоящего изобретения, специально не ограничиваются и включают, например, различные инъекции, пероральные агенты, капли, ингаляции, мази, лосьоны и т.д.
[0078] При введении олигомера настоящего изобретения пациентам с мышечной дистрофией предпочтительно, чтобы композиция настоящего изобретения содержала носитель, способствующий доставке олигомера в мышечные ткани. Такой носитель специально не ограничивается, когда речь идет о фармацевтически приемлемом носителе, и примеры включают катионные носители, такие как катионные липосомы, катионные полимеры и т.д., или носители с использованием оболочки вируса. Катионными носителями являются, например, липосомы, состоящие из 2-О-(2-диэтиламиноэтил)карабамоил-1,3-О-диолеоилглицерина и фосфолипидов в качестве основных составляющих (в дальнейшем называемые «липосомами А»), Oligofectamine (зарегистрированный товарный знак) (производства Invitrogen Corp.), Lipofectin (зарегистрированный товарный знак) (производства Invitrogen Corp.), Lipofectamine (зарегистрированный товарный знак) (производства Invitrogen Corp.), Lipofectamine 2000 (зарегистрированный товарный знак) (производства Invitrogen Corp.), DMRIE-C (зарегистрированный товарный знак) (производства Invitrogen Corp.), GeneSilencer (зарегистрированный товарный знак) (производства Gene Therapy Systems), TransMessenger (зарегистрированный товарный знак) (производства QIAGEN, Inc.), TransIT TKO (зарегистрированный товарный знак) (производства Mirus) и Nucleofector II (Lonza). Среди прочих предпочтительными являются липосомы А. Примерами катионных полимеров являются JetSI (зарегистрированный товарный знак) (производства Qbiogene, Inc.) и Jet-PEI (зарегистрированный товарный знак) (полиэтиленимин, производства Qbiogene, Inc.). Примером носителей с использованием оболочки вируса является GenomeOne (зарегистрированный товарный знак) (липосома HVJ-E, производства Ishihara Sangyo). В альтернативном случае могут также использоваться медицинские изделия, описанные в патенте Японии с № 2924179, и катионные носители, описанные в отечественных повторных публикациях в Японии РСТ-заявок с № 2006/129594 и 2008/096690.
Более подробную информацию см. в патенте США № 4235871, в патенте США № 4,737,323, WO96/14057, ʺNew RRC, Liposomes: A practical approach, IRL Press, Oxford (1990) pages 33-104ʺ и т.п.
[0079] Концентрация олигомера настоящего изобретения, содержащегося в композиции настоящего изобретения, может варьировать в зависимости от вида носителя и т.д. и находится, соответственно, в диапазоне от 0,1 нМ до 100 мкМ, предпочтительно, в диапазоне от 100 нМ до 10 мкМ. Весовое соотношение олигомера настоящего изобретения, содержащегося в композиции настоящего изобретения, и носителя (носитель/антисмысловой олигомер настоящего изобретения) может варьировать в зависимости от свойств олигомера, типа носителя и т.д. и находится, соответственно, в диапазоне от 0,1 до 100, предпочтительно, в диапазоне от 0,1 до 10.
[0080] Помимо олигомера настоящего изобретения и носителя, описанного выше, фармацевтически приемлемые добавки могут при желании входить в состав композиции настоящего изобретения. Примерами таких добавок являются вспомогательные средства для эмульгирования (например, жирные кислоты, содержащие 6-22 атомов углерода, и их фармацевтически приемлемые соли, альбумин и декстран), стабилизаторы (например, холестерин и фосфатидная кислота), агенты для придания изотоничности (например, хлорид натрия, глюкоза, мальтоза, лактоза, сахароза, трегалоза) и агенты для контролирования рН (например, соляная кислота, серная кислота, фосфорная кислота, уксусная кислота, гидроксид натрия, гидроксид калия и триэтаноламин). Можно применять одну или несколько таких добавок. Содержание добавки в композиции настоящего изобретения составляет 90% по весу или менее, предпочтительно, 70% по весу или менее и, более предпочтительно, 50% по весу или менее.
[0081] Композицию настоящего изобретения можно получить посредством добавления олигомера настоящего изобретения к дисперсии носителя и надлежащего перемешивания смеси. Добавки можно добавлять на соответствующей стадии или до, или после добавления олигомера настоящего изобретения. Содержащий воду растворитель, который можно применять при добавлении олигомера настоящего изобретения, специально не ограничивается, когда речь идет о фармацевтически приемлемом растворителе, и примерами являются вода для инъекции или дистиллированная вода для инъекции, раствор электролитов, такой как физиологический солевой раствор и т.д., и раствор сахара, такой как раствор глюкозы, раствор мальтозы и т.д. Специалист в данной области техники может соответствующим образом подобрать условия для рН и температуры в таком случае.
[0082] Композицию настоящего изобретения можно приготовить, например, в виде жидкой формы и ее лиофилизированного препарата. Лиофилизированный препарат можно приготовить с помощью лиофилизации композиции настоящего изобретения в жидкой форме обычным способом. Лиофилизацию можно провести, например, посредством надлежащей стерилизации композиции настоящего изобретения, находящейся в жидкой форме, распределения аликвот по контейнерам-флаконам, выполнения предварительного замораживания в течение 2 часов в условиях приблизительно от -40°С до -20°С, первичного высушивания при 0-10°С при пониженном давлении, а затем вторичного высушивания при приблизительно 15-25°С при пониженном давлении. Как правило, лиофилизированный препарат композиции настоящего изобретения можно получить с помощью замещения содержимого флакона азотом и закупоривания.
[0083] Как правило, лиофилизированный препарат композиции настоящего изобретения можно применять после восстановления посредством добавления произвольного подходящего раствора (жидкости для восстановления) и перерастворения препарата. Такая жидкость для перерастворения включает воду для инъекции, физиологический солевой раствор и другие жидкости для инфузии. Объем жидкости для восстановления может варьировать в зависимости от намеченного применения и т.д. и специально не ограничивается, и подходящий объем превышает в 0,5-2 раза объем до лиофилизации или составляет не более 500 мл.
[0084] Желательно контролировать вводимую дозу композиции настоящего изобретения, принимая во внимание следующие факторы: тип и лекарственную форму содержащегося олигомера настоящего изобретения, состояние пациентов, в том числе возраст, вес тела и т.д., путь введения, характеристики и степень заболевания. Суточная доза, рассчитанная как количество антисмыслового олигомера настоящего изобретения, как правило, находится в интервале от 0,1 мг до 10 г/человека и, предпочтительно, от 1 мг до 1 г/человека. Этот интервал числовых значений может иногда меняться в зависимости от типа целевого заболевания, пути введения и молекулы-мишени. Следовательно, в каком-то случае может быть достаточной доза ниже этого интервала, и наоборот, иногда может потребоваться доза выше этого интервала. Композицию можно вводить от одного до нескольких раз в день или с интервалами от одного дня до нескольких дней.
[0085] В другом варианте применения композиции настоящего изобретения представлена фармацевтическая композиция, содержащая вектор, способный экспрессировать олигонуклеотид настоящего изобретения, и описанный выше носитель. Таким экспрессионным вектором может быть вектор, способный экспрессировать множество олигонуклеотидов настоящего изобретения. Композицию можно составлять в форме с фармацевтически приемлемыми добавками, как в случае композиции настоящего изобретения, содержащей олигомер настоящего изобретения. Концентрация экспрессионного вектора, содержащегося в композиции, может варьировать в зависимости от типа носителя и т.д. и находится, соответственно, в диапазоне от 0,1 нМ до 100 мкМ, предпочтительно, в диапазоне от 100 нМ до 10 мкМ. Весовое соотношение экспрессионного вектора, содержащегося в композиции, и носителя (носитель/экспрессионный вектор) может варьировать в зависимости от свойств экспрессионного вектора, типа носителя и т.д. и находится, соответственно, в диапазоне от 0,1 до 100, предпочтительно, в диапазоне от 0,1 до 10. Содержание носителя, входящего в состав композиции, является таким же, как и в случае композиции настоящего изобретения, содержащей олигомер настоящего изобретения, а способ получения фармацевтической композиции, включающей вектор, является таким же, как и в случае композиции настоящего изобретения.
[0086] Здесь и далее будет приведено более подробное описание настоящего изобретения со ссылкой на ПРИМЕРЫ и ТЕСТОВЫЕ ПРИМЕРЫ ниже, но они не предназначены для ограничения настоящего изобретения.
ПРИМЕРЫ
[0087] [СПРАВОЧНЫЙ ПРИМЕР 1]
4-{[(2S, 6R)-6-(4-бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксомасляная кислота, нагруженная на аминополистирольную смолу
Стадия 1: Получение 4-{[(2S,6R)-6-(4- бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксомасляной кислоты
В атмосфере аргона 3,44 г N-{1-[(2R,6S)-6-(гидроксиметил)-4-тритилморфолин-2-ил]-2-оксо-1,2-дигидропиримидин-4-ил}бензамида и 1,1 г 4-диметиламинопиридина (4-DMAP) суспендировали в 50 мл дихлорметана, и к суспензии добавляли 0,90 г янтарного ангидрида с последующим перемешиванием при комнатной температуре в течение 3 часов. К реакционной смеси добавляли 10 мл метанола и концентрировали смесь при пониженном давлении. Остаток экстрагировали, используя этилацетат и 0,5 М водный раствор дигидрофосфата калия. Образованный в результате органический слой промывали последовательно 0,5 М водным раствором дигидрофосфата калия, водой и соляным раствором в указанном порядке. Образованный в результате органический слой сушили над сульфатом натрия и концентрировали при пониженном давлении с образованием 4,0 г продукта.
[0088] Стадия 2; Получение 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксомасляной кислоты, нагруженной на аминополистирольную смолу
После растворения 4,0 г 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1(2Н)-ил)-4-тритилморфолин-2-ил]метокси}-4-оксомасляной кислоты в 200 мл пиридина (обезвоженного) к раствору добавляли 0,73 г 4-DMAP и 11,5 г 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорида. Затем к смеси добавляли 25,0 г аминополистирольной смолы Primer support 200 amino (производства GE Healthcare Japan Co., Ltd., 17-5214-97), и 8,5 мл триэтиламина с последующим встряхиванием при комнатной температуре в течение 4 дней. После завершения реакции смолу отделяли с помощью фильтрации. Полученную в результате смолу последовательно промывали пиридином, метанолом и дихлорметаном в указанном порядке и сушили при пониженном давлении. К образованной в результате смоле добавляли 200 мл тетрагидрофурана (обезвоженного), 15 мл уксусного ангидрида и 15 мл 2,6-лутидина и смесь встряхивали при комнатной температуре в течение 2 часов. Смолу отделяли с помощью фильтрации, последовательно промывали пиридином, метанолом и дихлорметаном в указанном порядке и сушили при пониженном давлении с образованием 26,7 г продукта.
Величину привеса продукта определяли на основании молярного количества тритила на г смолы посредством измерения поглощения ультрафиолетовых лучей при 409 нм, используя известный способ. Величина привеса смолы составляла 192,2 мкмоль/г.
Условия измерения УФ
Прибор: U-2910 (Hitachi, Ltd.)
Растворитель: метансульфоновая кислота
Длина волны: 265 нм
Значение ε: 45000
[0089] В соответствии с описаниями в ПРИМЕРАХ 1, 2 ниже и в СПРАВОЧНОМ ПРИМЕРЕ 1 ниже были синтезированы РМО, представленные РМО с № 1-3 в ТАБЛИЦЕ 1. Синтезированный РМО растворяли в воде для инъекции (производства Otsuka Pharmaceutical Factory, Inc.).
[0090]
SEQ ID NO; 588 в патентном документе 3,
5'-конец: группа (3)
[0091] [ПРИМЕР 1]
PMO № 1
0,2 г (26 мкмоль) 4-{[(2S,6R)-6-(4-бензамидо-2-оксопиримидин-1-ил)-4-тритилморфолин-2-ил]метокси}-4-оксомасляной кислоты, нагруженной на аминополистирольную смолу (Справочный пример 1), наносили на колонку с фильтром. Затем начинали синтетический цикл, показанный ниже, используя прибор для синтеза нуклеиновых кислот (AKTA Oligopilot 10 plus). Заданное морфолино-мономерное соединение добавляли на каждом цикле соединения с образованием нуклеотидной последовательности заявленного соединения (см. Таблицу 2 ниже).
[0092]
[0093] Применяемым раствором для снятия защиты был раствор дихлорметана, содержащий 3% (вес/объем) трифторуксусной кислоты. Применяемым раствором для нейтрализации и промывки был раствор, полученный в результате растворения N,N-диизопропилэтиламина до конечной концентрации 10% (объем/объем) и тетрагидрофурана до 5% (объем/объем) в дихлорметане, содержащем 35% (объем/объем) ацетонитрила. Применяемым раствором А для соединения был раствор, полученный в результате растворения морфолино-мономерного соединения в тетрагидрофуране до концентрации 0,10 М. Применяемым раствором В для соединения был раствор, полученный в результате растворения N,N-диизопропилэтиламина до концентрации 20% (объем/объем) и тетрагидрофурана до концентрации 10% (объем/объем) в ацетонитриле. Применяемым раствором для кэпирования был раствор, полученный в результате растворения 20% (объем/объем) уксусного ангидрида и 30% (объем/объем) 2,6-лутидина в ацетонитриле.
[0094] Аминополистирольную смолу, нагруженную синтезированным выше РМО, извлекали из реакционного сосуда и сушили при комнатной температуре в течение по крайней мере 2 часов при пониженном давлении. Высушенный РМО, нагруженный на аминополистирольную смолу, загружали в реакционный сосуд и к нему добавляли 5 мл смеси 28% водного раствора аммиака-этанола (1/4). Смесь перемешивали при 55°С в течение 15 часов. Аминополистирольную смолу отделяли с помощью фильтрации и промывали 1 мл смеси воды-этанола (1/4). Образованный в результате фильтрат концентрировали при пониженном давлении. Образованный в результате остаток растворяли в 10 мл смеси растворителей, состоящей из 20 мМ буфера уксусная кислота - триэтиламин (буфера ТЕАА) и 10- мл ацетонитрила, (4/1) и фильтровали через мембранный фильтр. Полученный фильтрат очищали с помощью ВЭЖХ с обращенной фазой. Применяли условия, показанные в Таблице 3 ниже.
[0095]
[0096] Исследовали каждую фракцию, целевой продукт восстанавливали и концентрировали при пониженном давлении. К концентрированному остатку добавляли 0,5 мл 2М водного раствора фосфорной кислоты и перемешивали смесь в течение 15 минут. Более того, добавляли 2 мл 2М водного раствора гидроксида натрия для подщелачивания смеси, а затем фильтровали через мембранный фильтр (0,45 мкм).
Образованный в результате водный раствор, содержащий целевой продукт, очищали с помощью колонки с анионообменной смолой. Применяли условия, показанные в Таблице 4 ниже.
[0097]
[0098] Каждую фракцию исследовали (с помощью ВЭЖХ) и целевой продукт получали в виде водного раствора. К образованному в результате водному раствору добавляли 0,1 М фосфатного буфера (рН 6,0) для нейтрализации. Затем смесь обессоливали с помощью обращенно-фазовой ВЭЖХ в условиях, описанных в Таблице 5 ниже.
[0099]
[0100] Целевой продукт восстанавливали и проводили концентрирование при пониженном давлении. Образованный в результате остаток растворяли в воде. Полученный водный раствор лиофилизировали с образованием целевого соединения в виде белого, похожего на хлопок твердого вещества.
ESI-TOF-MS (время-пролетная масс-спектрометрия с ионизацией электрораспылением)
Рассчитанное значение: 10021,46
Установленное значение: 10021,91
[0101] [ПРИМЕР 2]
PMO № 2
Целевое соединение получали в соответствии с процедурой, описанной в ПРИМЕРЕ 1.
ESI-TOF-MS Рассчитанное значение: 9916,71
Установленное значение: 9916,43
[0102] [СРАВНИТЕЛЬНЫЙ ПРИМЕР 1]
PMO № 3
Целевое соединение получали в соответствии с процедурой, описанной в ПРИМЕРЕ 1.
ESI-TOF-MS Рассчитанное значение: 9949,46
Установленное значение: 9949.41
[0103] [ТЕСТОВЫЙ ПРИМЕР 1]
Исследование in vitro
Эксперименты проводили, применяя антисмысловые олигомеры PMO № 1 и 2 настоящего изобретения и антисмысловой олигомер PMO № 3. Последовательности разных антисмысловых олигомеров приведены в Таблице 6 ниже.
[0104]
[0105] С помощью набора для нуклеофекции клеточных линий Amaxa Cell Line Nucleofector Kit L на Nucleofector II (Lonza) 0,3, 1, 3, 10 мкМ олигомеров PMO № 1 и 2 настоящего изобретения и антисмыслового олигомера PMO № 3 трансфицировали 3,5×105 клеток RD (клеточная линия рабдомиосаркомы человека). Применяли программу Program T-030.
После трансфекции клетки культивировали в течение трех дней в 2 мл минимальной питательной среды Игла (EMEM, Eagle's minimal essential medium) (производства Sigma, здесь и далее та же самая), содержащей 10% фетальной бычьей сыворотки (FCS, fetal calf serum) (производства Invitrogen) при 37°C и 5% CO2. Клетки промывали фосфатно-солевым буфером (производства Nissui, здесь и далее тот же самый) и добавляли к клеткам 500 мкл ISOGEN II (производства Nippon Gene). После инкубации клеток при комнатной температуре в течение нескольких минут для проведения лизиса клеток лизат собирали в пробирку Eppendorf. Общую РНК экстрагировали в соответствии с протоколом, приложенным к ISOGEN. Концентрацию экстрагированной общей РНК определяли с помощью NanoDrop ND-1000 (производства LMS).
Проводили одностадийную ОТ-ПЦР с 400 нг экстрагированной общей РНК с помощью набора для ОТ-ПЦР Qiagen One Step RT-PCR Kit (производства Qiagen). Реакционный раствор готовили в соответствии с протоколом, приложенным к набору. PTC-100 (производства MJ Research) применяли в качестве термоциклера. Применяли следующую программу ОТ-ПЦР.
50°C, 30 мин: реакция обратной транскрипции
95°C, 15 мин: тепловая денатурация
[94°C, 30 секунд; 60°C, 30 секунд; 72°C, 60 секунд]×35 циклов: ПЦР-амплификация
72°C, 10 мин: конечная элонгация
[0106] Нуклеотидные последовательности прямого праймера и обратного праймера, применяемых для ОТ-ПЦР, приведены ниже.
Прямой праймер: 5'- CTGAGTGGAAGGCGGTAAAC-3' (SEQ ID NO: 5)
Обратный праймер: 5'- GAAGTTTCAGGGCCAAGTCA-3' (SEQ ID NO: 6)
[0107] Продукт реакции, 1 мкл описанной выше ОТ-ПЦР, анализировали с помощью Bioanalyzer (производства Agilent Technologies, Inc.). Измеряли уровень «А» полинуклеотидной полосы в случае, когда экзон 51 пропущен, и уровень «В» полинуклеотидной полосы в случае, когда экзон 51 не пропущен. На основании этих измерений значений «A» и «B» определяли эффективность пропуска по следующему уравнению:
Эффективность пропуска (%)=A/(A+B)×100
[0108] Результаты экспериментов
Результаты показаны на Фиг.1. этот эксперимент показал, что антисмысловые олигомеры настоящего изобретения могут вызывать пропуск экзона 51 с более высокой эффективностью, чем антисмысловой олигомер PMO № 3.
[Пример 3]
PMO № 4-6
Целевое соединение получали в соответствии с процедурой, описанной в ПРИМЕРЕ 1. Последовательности различных антисмысловых олигомеров приведены ниже.
[ПРИМЕР 4]
2'-O-метокси-тиофосфаты, представленные SEQ ID NOS: 9-33
Различные антисмысловые целевые олигомеры были получены в Japan Bio Service Co. Последовательности различных антисмысловых олигомеров приведены в Таблице 8.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
[0109] Результаты экспериментов, приведенные в ТЕСТОВЫХ ПРИМЕРАХ, показывают, что олигомеры настоящего изобретения вызывали пропуск экзона 51 с высокой эффективностью в клетках RD. Таким образом, олигомеры настоящего изобретения являются особенно полезными для лечения МДД.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NIPPON SHINYAKU CO., LTD.
NATIONAL CENTER OF NEUROLOGY AND PSYCHIATRY
<120> АНТИСМЫСЛОВАЯ НУКЛЕИНОВАЯ КИСЛОТА
<130> G1311WO
<150> JPA2014-48897
<151> 2014-03-12
<160> 34
<170> PatentIn версия 3.5
<210> 1
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 1
cggtaagttc tgtcctcaag gaagatggca 30
<210> 2
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 2
ctcatacctt ctgcttcaag gaagatggca 30
<210> 3
<211> 233
<212> ДНК
<213> Homo sapiens
<400> 3
ctcctactca gactgttact ctggtgacac aacctgtggt tactaaggaa actgccatct 60
ccaaactaga aatgccatct tccttgatgt tggaggtacc tgctctggca gatttcaacc 120
gggcttggac agaacttacc gactggcttt ctctgcttga tcaagttata aaatcacaga 180
gggtgatggt gggtgacctt gaggatatca acgagatgat catcaagcag aag 233
<210> 4
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 4
ctccaacatc aaggaagatg gcatttctag 30
<210> 5
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 5
ctgagtggaa ggcggtaaac 20
<210> 6
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 6
gaagtttcag ggccaagtca 20
<210> 7
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 7
aacatcaagg aagatggcat t 21
<210> 8
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 8
tccaacatca aggaagatgg c 21
<210> 9
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 9
acctccaaca tcaaggaaga t 21
<210> 10
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 10
gaguaacagu cugaguagga g 21
<210> 11
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 11
ugugucacca gaguaacagu c 21
<210> 12
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 12
aaccacaggu ugugucacca g 21
<210> 13
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 13
uuuccuuagu aaccacaggu u 21
<210> 14
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 14
gagauggcag uuuccuuagu a 21
<210> 15
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 15
uucuaguuug gagauggcag u 21
<210> 16
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 16
aagauggcau uucuaguuug g 21
<210> 17
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 17
aacaucaagg aagauggcau u 21
<210> 18
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 18
agguaccucc aacaucaagg a 21
<210> 19
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 19
cugccagagc agguaccucc a 21
<210> 20
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 20
cgguugaaau cugccagagc a 21
<210> 21
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 21
uguccaagcc cgguugaaau c 21
<210> 22
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 22
cgguaaguuc uguccaagcc c 21
<210> 23
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 23
gaaagccagu cgguaaguuc u 21
<210> 24
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 24
aucaagcaga gaaagccagu c 21
<210> 25
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 25
uuauaacuug aucaagcaga g 21
<210> 26
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 26
cucugugauu uuauaacuug a 21
<210> 27
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 27
caccaucacc cucugugauu u 21
<210> 28
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 28
caaggucacc caccaucacc c 21
<210> 29
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 29
uugauauccu caaggucacc c 21
<210> 30
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 30
gaucaucucg uugauauccu c 21
<210> 31
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 31
ucugcuugau gaucaucucg u 21
<210> 32
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 32
ggcauuucua guuuggagau g 21
<210> 33
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 33
caaggaagau ggcauuucua g 21
<210> 34
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетическая нуклеиновая кислота
<400> 34
ccuccaacau caaggaagau g 21
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2825834C2 |
| АНТИСМЫСЛОВАЯ НУКЛЕИНОВАЯ КИСЛОТА | 2016 |
|
RU2724554C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2012 |
|
RU2651468C1 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2702424C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2015 |
|
RU2695430C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИСМЫСЛОВОЙ ОЛИГОНУКЛЕОТИД, И ЕЕ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ МЫШЕЧНОЙ ДИСТРОФИИ ДЮШЕННА | 2019 |
|
RU2799442C2 |
| ИНГИБИТОР СИГНАЛА МИОСТАТИНА | 2019 |
|
RU2820270C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2011 |
|
RU2567664C2 |
| АНТИСМЫСЛОВЫЕ НУКЛЕИНОВЫЕ КИСЛОТЫ | 2012 |
|
RU2619184C2 |
| МОДУЛЯТОРЫ И МОДУЛЯЦИЯ РНК РЕЦЕПТОРА КОНЕЧНЫХ ПРОДУКТОВ ГЛУБОКОГО ГЛИКИРОВАНИЯ | 2020 |
|
RU2820247C2 |
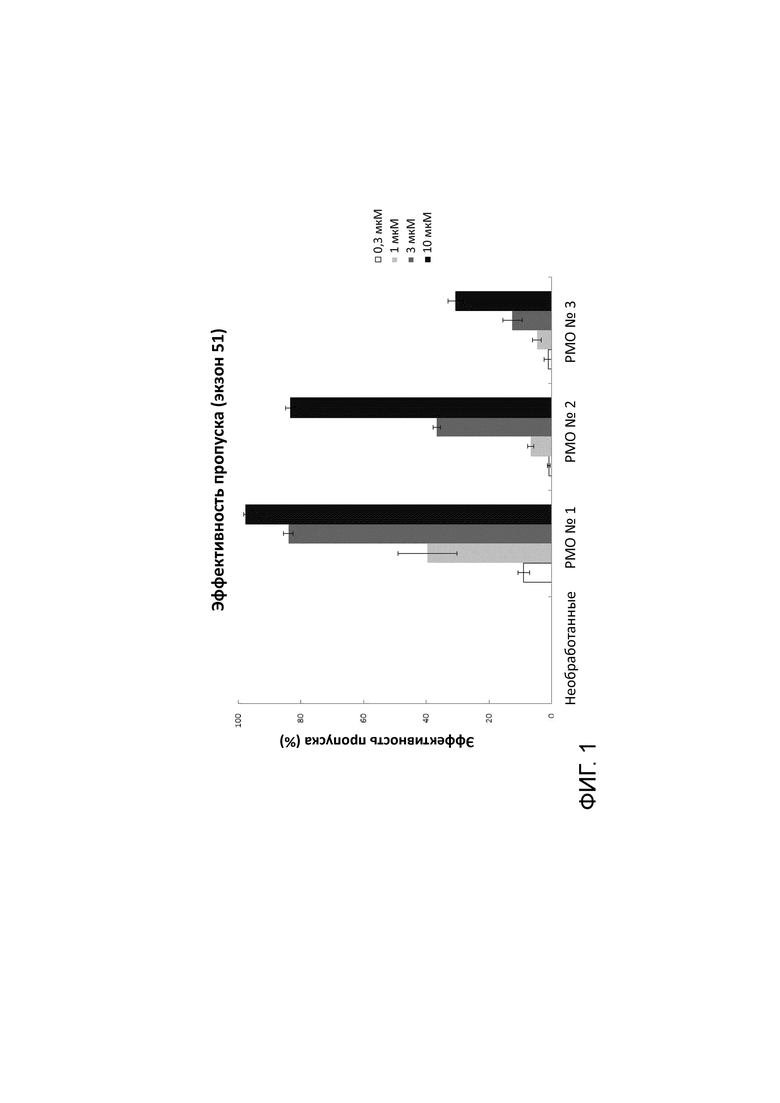
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая антисмысловой олигомер для лечения мышечной дистрофии, и фармацевтическая композиция, содержащая вышеуказанный антисмысловой олигомер, для лечения пациента с мышечной дистрофией. В одном из вариантов реализации антисмысловой олигомер обладает длиной от 21 до 30 нуклеотидов и включает 15 нуклеотидов из нуклеотидной последовательности SEQ ID NO: 1, а также обладает активностью, вызывающей пропуск экзона 51 в гене дистрофина человека. Изобретение расширяет арсенал средств для лечения мышечной дистрофии. 2 н. и 10 з.п. ф-лы, 1 ил., 8 табл., 7 пр.
1. Антисмысловой олигомер для лечения мышечной дистрофии, обладающий длиной от 21 до 30 нуклеотидов, включающий 15 нуклеотидов из нуклеотидной последовательности SEQ ID NO: 1, и обладающий активностью, вызывающей пропуск экзона 51 в гене дистрофина человека.
2. Антисмысловой олигомер для лечения мышечной дистрофии по п. 1, который представляет собой олигонуклоетид.
3. Антисмысловой олигомер для лечения мышечной дистрофии по п. 2, в котором модифицирован остаток сахара и/или область соединения через фосфатную группу по меньшей мере одного нуклеотида, входящего в состав олигонуклеотида.
4. Антисмысловой олигомер для лечения мышечной дистрофии по п. 2, в котором остаток сахара по меньшей мере одного нуклеотида, составляющего олигонуклеотид, представляет собой рибозу, в которой 2'-ОН-группа заменена любой группой, выбранной из группы, состоящей из OR, R, R'OR, SH, SR, NH2, NHR, NR2, N3, CN, F, Cl, Br и I (где R представляет собой неразветвленный или разветвленный алкил, имеющий от 1 до 6 атомов углерода, или арил, имеющий от 6 до 10 атомов углерода, и R' представляет собой неразветвленный или разветвленный алкилен, имеющий от 1 до 6 атомов углерода).
5. Антисмысловой олигомер для лечения мышечной дистрофии по п. 2, в котором область соединения через фосфатную группу по меньшей мере одного нуклеотида, входящего в состав олигонуклеотида представляет собой любую область, выбранную из группы, состоящей из тиофосфатной связи, дитиофосфатной связи, алкилфосфонатной связи, фосфорамидатной связи и боранофосфатной связи.
6. Антисмысловой олигомер для лечения мышечной дистрофии по п. 1, который представляет собой морфолино-олигомер.
7. Антисмысловой олигомер для лечения мышечной дистрофии по п. 6, который представляет собой фосфодиамидатный морфолино-олигомер.
8. Антисмысловой олигомер для лечения мышечной дистрофии по п. 6, в котором 5'-конец имеет любую из приведенных ниже химических формул (1)-(3):
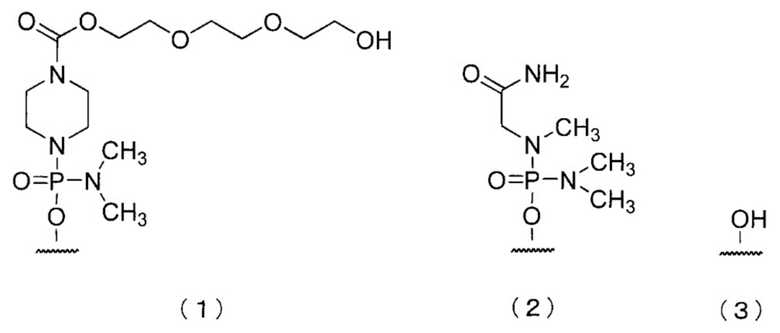 .
.
9. Фармацевтическая композиция для лечения пациента с мышечной дистрофией, содержащая в качестве активного ингредиента антисмысловой олигомер по п. 1, в суточной дозе в виде количества антисмыслового олигомера в интервале от 0,1 мг/человека до 10 г/человека.
10. Фармацевтическая композиция по п. 9, содержащая фармацевтически приемлемый носитель.
11. Фармацевтическая композиция по п. 9, где пациентом с мышечной дистрофией является пациент с делециями нуклеотидов внутри экзонов 29-50, 50, 45-50, 48-50, 49-50, 52, 52-63, 13-50, 19-50, 43-50 или 47-50.
12. Фармацевтическая композиция по п. 11, в которой пациентом является человек.
| RU 2013114396 А, 10.10.2014 | |||
| WO 2010048586 A1, 29.04.2010 | |||
| МОЛЕКУЛЫ ХИМИЧЕСКИ МОДИФИЦИРОВАННОЙ КОРОТКОЙ ИНТЕРФЕРИРУЮЩЕЙ НУКЛЕИНОВОЙ КИСЛОТЫ, КОТОРЫЕ ОПОСРЕДУЮТ ИНТЕРФЕРЕНЦИЮ РНК | 2006 |
|
RU2418068C2 |
Авторы
Даты
2020-08-24—Публикация
2015-03-11—Подача