Заявляемая группа изобретений относится к биотехнологии и касается способа конструирования на основе бактерий рода Rhodococcus штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью, а также рекомбинантного штамма Rhodococcus rhodochrous продуцента фермента нитрилазы, катализирующей прямой гидролиз нитрилов карбоновых кислот в соответствующие кислоты, а также биокаталитического способа синтеза органических кислот, в частности, акриловой кислоты в форме акрилата аммония (далее - акрилат) с использованием клеток этого штамма в качестве биокатализатора.
Развитие технологии производства полимеров в последние годы привело к разработке новых видов полимеров, в состав которых входят акриловая кислота и ее производные. В настоящее время наиболее распространенным способом получения акриловой кислоты является окисление пропилена. Альтернативными способами являются способы получения водных растворов акрилата с помощью микроорганизмов. Один вариант предусматривает получение акрилата путем ферментации Сахаров (US 2016017382), а другой - биокаталитическое получение из акрилонитрила (RU 2323977). Преимуществами таких способов являются мягкие условия процесса - водная среда, комнатная температура, нормальное давление. Недостатками ферментационного способа являются низкая концентрация получаемых растворов акрилата и высокая их загрязненность продуктами жизнедеятельности микроорганизмов. Преимущества биокаталитического способа заключаются в высокой концентрации и чистоте получаемого продукта.
Известно биокаталитическое получение акрилата аммония с помощью как штамма бактерий рода Rhodococcus (ЕР 0444640, RU 2188864), так и штамма бактерий рода Alcaligenes (RU 2323977), обладающих нитрилазной ферментной активностью. В этих изобретениях отсутствует описание операционной стабильности штаммов-биокатализаторов, и не указаны способы ее улучшения. Под операционной стабильностью подразумевают устойчивость биокатализатора к необратимой инактивации ферментной активности в ходе подачи акрилонитрила в реакционную смесь для получения акрилата. Операционная стабильность является существенным фактором, влияющим на эффективность, и, как следствие, экономическую обоснованность процесса биокаталитического получения акрилата. Эта стабильность зависит как от природы используемого фермента, так и от свойств штамма, продуцирующего этот фермент.
В указанных выше изобретениях используют различные нитрилазы, что может влиять на операционную стабильность биокатализаторов, содержащих такие нитрилазы. Поэтому в качестве ближайшего аналога заявляемого способа будем рассматривать способ с использованием штамма Alcaligenes denitrificans С-32 VKM B-2243D (RU 2323977), продуцирующего ту же нитрилазу, что и в заявляемом способе. В то же время в качестве ближайшего аналога заявляемого штамма будем рассматривать штамм Alcaligenes denitrificans ВКПМ В-9582 (RU 2337954), являющийся производным от штамма Alcaligenes denitrificans С-32 VKM B-2243D и отличающийся от него повышенной нитрилазной активностью.
Задачей заявляемой группы изобретений является расширение арсенала штаммов-биокатализаторов с нитрилазной активностью.
Задача решена путем:
- разработки способа конструирования на основе бактерий рода Rhodococcus штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью, путем интеграции в геном штамма-реципиента бактерий рода Rhodococcus двух копий гена нитрилазы NitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D;
- конструирования рекомбинантного штамма бактерий Rhodococcus rhodochrous ВКПМ АС-2111, обладающего нитрилазной активностью;
- разработки способа синтеза акриловой кислоты в форме акрилата аммония из акрилонитрила с использованием в качестве биокатализатора штамма бактерий Rhodococcus rhodochrous ВКПМ АС-2111.
Заявляемый штамм получен путем интеграции в геном штамма Rhodococcus rhodochrous ВКМ Ас-1515Д (RU 2053300) двух копий гена нитрилазы NitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D; он является штаммом-биокатализатором, обладающим нитрилазной активностью и повышенной операционной стабильностью при использовании в заявляемом способе синтеза акриловой кислоты.
Заявляемый штамм депонирован во Всероссийской коллекции промышленных микроорганизмов (ВКПМ) и имеет регистрационный номер Rhodococcus rhodochrous ВКПМ АС-2111.
Штамм Rhodococcus rhodochrous ВКПМ АС-2111, в хромосому которого интегрированы гены нитрилазы из Alcaligenes denitrificans С-32 VKM B-2243D, приобретает нитрилазную активность и способность служить биокатализатором при синтезе органических кислот из соответствующих нитрилов. При добавлении водных растворов нитрилов к суспензии клеток Rhodococcus rhodochrous ВКПМ АС-2111 (используемого в качестве биокатализатора) происходит синтез органических кислот в виде аммонийных солей, в частности, акриловой кислоты.
Характеристика заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111
Морфологические свойства. Клетки штамма неподвижны Грам+. Спор не образуют, некислотоустойчивы. В возрасте 18-20 ч клетки образуют длинные (до 20 мкм) слабо ветвящиеся нити, которые через 48-72 ч распадаются на палочковидные и кокковидные элементы. В старых культурах наблюдают плеоморфные клетки в виде колб, груш, булав. Деление клеток происходит по раскалывающемуся и сгибающемуся типам.
Физиологические свойства. Облигатный аэроб. Редуцирует нитраты. Тест с метиловым красным, реакция Фогес-Проскауэра (Егоров Н.С. (ред.) и др. Руководство к практическим занятиям по микробиологии. М: 1983) отрицательные. Образует сероводород. Штамм оксидазоотрицательный, каталазо- и фосфатазаположительный. Крахмал и целлюлозу не гидролизует, твин 60 и 80 гидролизует. Аденин не утилизирует. Клетки не выдерживают нагревания в снятом молоке при 72°С в течение 15 мин. Штамм растет при рН 6-9, температуре 5-45°С. Кислоту образует из следующих Сахаров и спиртов: глюкозы, фруктозы, мальтозы, сахарозы, сорбита, манита и глицерина. Газообразования ни на одном сахаре не обнаружено. В качестве единственного источника азота использует соединения аммония, нитраты и мочевину. В качестве единственного источника углерода использует мальтозу, манит, сорбит, глюкозу, глицерин, лактат, пируват, бензоат, n- и m-гидроксибензоат, тирозин; не использует рамнозу, галактозу, инозит, а-кетоглутарат. В клеточной стенке заявляемого штамма содержатся мезо-диаминопимелиновая кислота, арабиноза и галактоза, что характерно для коринеподобных бактерий с IV типом клеточной стенки. Клетки также содержат липид A(LCN), характерный для родококков.
Заявляемый штамм обладает высоким уровнем стабильной нитрилазной активности в неселективных условиях, т.е. в отсутствии в среде антибиотиков. Уровень утраты гена нитрилазы после роста в неселективных условиях для штамма Rhodococcus rhodochrous ВКПМ АС-2111 составляет менее 0.1%.
Получение биокатализатора в общем виде и оценка его нитрилазной активности
Для получения клеток штамма-биокатализатора Rhodococcus rhodochrous, содержащего два гена нитрилазы, штамм выращивают при 25-30% в течение 48-72 часов на синтетических средах, содержащих в качестве источника углерода сахара или спирты или карбоновые кислоты в концентрациях 0.1-4%, а в качестве источника азота соединения аммония, нитраты или мочевину в концентрациях 0.4-2%. Полученные клетки отделяют от культуральной жидкости центрифугированием при 5-16 тыс.об/мин, ресуспендируют в 10 мМ фосфатном буфере рН 7,0-8,0 до концентрации 20-40 г по сухой массе/л и хранят в таком виде при 4°С или отделяют клетки центрифугированием при 4-16 тыс. об/мин., полученный осадок клеток хранят в виде пасты при минус 18°С.
Ферментативную активность клеток определяют с использованием в качестве субстрата нитрила акриловой кислоты, по следующей методике: 1 мл клеточной суспензии смешивают с акрилонитрилом (до конечной концентрации 20,0 г/л) в герметичных пластиковых пробирках, помещают пробирки в водяную баню с температурой 20°С и термостатируют их необходимое количество времени. Трансформацию проводят при постоянном перемешивании. Реакцию останавливают внесением в реакционную смесь 6 Н HCl в объеме 0,05 мл. Бактериальные клетки отделяют центрифугированием. Концентрацию акриловой кислоты в надосадочной жидкости рассчитывают по количеству образовавшегося аммония, который определяют спектрофотометрическим методом с помощью реагента Несслера. За единицу удельной нитрилазной активности принимают количество фермента, катализирующего образование 1 мкмоль акрилата аммония в минуту.
Способ синтеза акрилата аммония в общем виде
Синтез акрилата аммония осуществляют путем непрерывной подачи 100% акрилонитрила в реакционную смесь, содержащую водную суспензию бикатализатора (от 1 до 10 г клеток по сухой массе на 1 л реакционной смеси) в термостатируемом сосуде (при температуре от 20 до 40°С, предпочтительнее от 30 до 36°С), с постоянным перемешиванием (от 100 до 400 об\мин). Значение рН варьирует от 6 до 12, предпочтительнее от 7 до 9.
Содержание конечного продукта - акрилата аммония определяют с помощью высокоэффективной жидкостной хроматографии. Заявляемый способ позволяет получать растворы, содержащие до 450 г/л акрилата аммония.
Изобретение проиллюстрировано следующими примерами.
Пример 1. Конструирование плазмиды pRY1-nit1 для интеграции одной копии гена нитрилазы из штамма Alcaligenes denitrificans С-32 VKM 2243D в хромосому штамма Rhodococcus rhodochrous ВКМ Ас-1515Д.
Плазмида состоит из генной кассеты, вставленной в вектор pRY1 (Рябченко и др. Клонирование гена амидазы Rhodococcus rhodochrous М8 и его экспрессия в Escherichia coli. Генетика, 2006, т. 42, N 8, стр. 1075-1082). Генная кассета состоит из гена нитрилазы Alcaligenes denitrificans С-32 (обозначенного nit) с последовательностью SEQ ID 01, фланкированного фрагментами ДНК, обозначенными H1 (последовательность SEQ ID 02) и Н2 (последовательность SEQ ID 03). Ген нитрилазы и фрагменты H1 и Н2 наработаны и объединены в генную кассету H1-nit-H2 с помощью полимеразной цепной реакции. Генная кассета H1-nit-H2 вставлена в плазмиду pRY1 путем лигирования по сайтам рестриктаз BamHI и EcoRI. В результате получают плазмиду pRY1-nit1.
Пример 2. Конструирование плазмиды pRY1-nit2 для интеграции второй копии гена нитрилазы штамма Alcaligenes denitrificans С-32 VKM 2243D в хромосому штамма Rhodococcus rhodochrous ВКМ Ас-1515Д.
Плазмида состоит из генной кассеты, вставленной в вектор pRY1. Генная кассета состоит из гена нитрилазы Alcaligenes denitrificans С-32 (обозначенного nit) с последовательностью SEQ ID 01, фрагмента ДНК, обозначенного H1 (последовательность SEQ ID 02), и фрагмента ДНК, обозначенного Н3 (последовательность SEQ ID 04). Ген нитрилазы, фрагменты H1 и Н3 наработаны и объединены в генную кассету Н3-H1-nit с помощью полимеразной цепной реакции. Генная кассета Н3-H1-nit вставлена в плазмиду pRY1 путем лигирования по сайтам рестриктаз BamHI и EcoRI. В результате получают плазмиду pRY1-nit2.
Пример 3. Конструирование заявляемого штамма обладающего нитрилазной активностью на основе штамма Rhodococcus rhodochrous ВКМ Ас-1515Д
Для конструирования заявляемого штамма полученную плазмиду pRY1-nit1 вводят в штамм Е. coli S17-1 (R. Simon et al. 1983. A Broad Host Range Mobilization System for In Vivo Genetic Engineering: Transposon Mutagenesis in Gram Negative Bacteria. Nature Biotechnology. 1983 volume 1, pages 784-791), путем химической трансформации по методу (Маниатис и др. Методы генетической инженерии. Молекулярное клонирование. М.: Мир, 1984. - 479 с.), и отбора клонов на среде, содержащей ампициллин. Затем проводят конъюгационные скрещивания клонов E. coli S17-1, содержащих плазмиду pRY1-nit1, со штаммом Rhodococcus rhodochrous ВКМ Ас-1515Д по известной методике (Voeykova et al. Transfer of plasmid pTO1 from Escherichia coli to various representatives of the order Actinomycetales by intergeneric conjugation. FEMS Microbiol Lett. 1998 May 1; 162(1):47-52). Сначала отбирают клоны R. rhodochrous, устойчивые к антибиотику тиостептону, а на следующем этапе проводят рассевают эти культуры до отдельных колоний на среде LB (состав как описано в Рябченко и др. Клонирование гена амидазы Rhodococcus rhodochrous М8 и его экспрессия в Escherichia coli. Генетика, 2006, т. 42, N 8, стр. 1075-1082), и отбирают клоны, чувствительные к тиострептону. Среди этих клонов отбирают те, которые обладают нитрилазной активностью. Они содержат в хромосоме одну копию гена нитрилазы.
На следующем этапе плазмиду pRY1-nit2 вводят в штамм E. coli S17-1 путем химической трансформации и отбора клонов на среде, содержащей ампициллин. Затем проводят конъюгационные скрещивания клонов E. coli S17-1, содержащих плазмиду pRY1-nit2, со штаммом R. rhodochrous, содержащим одну копию гена нитрилазы в хромосоме. После отбора клонов, устойчивых к антибиотику тиострептону, получают заявляемый штамм Rhodococcus rhodochrous ВКПМ АС-2111, содержащий две копии гена нитрилазы в хромосоме.
Подобное верно также и для Rhodococcus rhodochrous М8 и Rhodococcus aetherivorans АС2063 (VKM AC-2610D).
Пример 4. Конструирование штамма с нитрилазной активностью на основе штамма Rhodococcus rhodochrous М8 ВКПМ АС-926
Все операции проводят аналогично примеру 3, за исключением того, что вместо штамма Rhodococcus rhodochrous ВКМ Ас-1515Д используют штамм Rhodococcus rhodochrous М8 ВКПМ АС-926. В результате получают штамм Rhodococcus rhodochrous М8 2nit, содержащий две копии гена NitC1 в хромосоме.
Пример 5. Конструирование штамма с нитрилазной активностью на основе штамма Rhodococcus aetherivorans АС2063 VKM AC-2610D
Все операции проводят аналогично примеру 3 за исключением того, что вместо штамма Rhodococcus rhodochrous ВКМ Ас-1515Д используют штамм Rhodococcus aetherivorans АС2063 VKM AC-2610D. В результате получают штамм Rhodococcus aetherivorans АС2063 2nit, содержащий две копии гена NitC1 в хромосоме.
Пример 6. Получение биокатализатора на основе биомассы штамма Rhodococcus rhodochrous ВКПМ АС-2111
Клетки штамма Rhodococcus rhodochrous ВКПМ АС-2111 засевают на скошенную агаризованную среду LB и культивируют 2 суток при 30±1°С.
Клетки, полученные таким образом, смывают физиологическим раствором и засевают в жидкую питательную среду следующего состава: мас. %: KH2PO4 - 0,1; Na2HPO4×12Н2О - 0,25; глюкоза - 2,0; мочевина - 1,2; MgSO4×7H2O - 0.1; CoSO4×6H2O - 0.004; FeSO4×7H2O - 0,001; ЭДТА - 0,002; дрожжевой экстракт - 0.5; вода - остальное, рН 7.2±0.2. Культивируют в колбах Эрленмейера объемом 300 мл, заполненных на 1/6 часть, в течение 48 часов с непрерывным перемешиванием (180 об/мин) при температуре 30±1°С. Полученную культуральную жидкость используют для засева лабораторного ферментера из расчета 0,1 V/V.
Для культивирования штамма в лабораторном ферментере используют среду следующего состава, мас. %: KH2PO4 - 0,1; Na2HPO4×12Н2О - 0,25; глюкоза - 2,5; мочевина - 1,8; MgSO4×7H2O - 0.1; CoSO4×6H2O - 0.006; FeSO4×7H2O - 0,004; ЭДТА - 0,008; дрожжевой экстракт - 0.05; CH3COONa - 1.0; вода - остальное, рН 7.2±0.2.
Культивирование проводят при температуре 30±1°С. Подачу воздуха осуществляют из расчета 1,5 V/V, скорость вращения мешалки изменяют, обеспечивая уровень аэрации не менее 50% насыщения кислорода.
По истечении 24±0,3 часов роста культуры в ферментер начинают подачу 50% уксусной кислоты, служащей источником углерода, поддерживая значение рН 7,5±0,5.
Через 72 часа культивирования проводят измерение удельной нитрилазной активности (по методике, указанной выше), которая составляет 6,5 ед/мг с.в. клеток. Клетки биокатализатора отделяют от питательной среды центрифугированием и хранят в виде клеточной пасты при температуре -18°С.
Пример 7. Получение биокатализатора на основе биомассы штамма Rhodococcus rhodochrous M8 2nit
Все операции проводят также, как в примере 6, за исключением того, что вместо заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 используют штамм Rhodococcus rhodochrous М8 2nit, полученный, как в примере 4. В результате получают клетки биокатализатора, обладающие нитрилазной активностью 6,4 ед/мг с.в. клеток. Клетки биокатализатора отделяют от питательной среды центрифугированием, и хранят в виде клеточной пасты при температуре -18°С.
Пример 8. Получение биокатализатора на основе биомассы штамма Rhodococcus aetherivorans АС2063 2nit
Все операции проводят также, как в примере 6, за исключением того, что вместо заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 используют штамм Rhodococcus aetherivorans АС2063 2nit, полученный, как в примере 5. В результате получают клетки биокатализатора, обладающие нитрилазной активностью 6,4 ед/мг с.в. клеток. Клетки биокатализатора отделяют от питательной среды центрифугированием и хранят в виде клеточной пасты при температуре -18°С.
Пример 9. Оценка операционной стабильности биокатализатора на основе клеток заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 в сравнении с клетками штамма - ближайшего аналога при получении акриловой кислоты в форме акрилата аммония из акрилонитрила
Клетки заявляемого штамма получают, как указано в примере 6, а клетки штамма ближайшего аналога Alcaligenes denitrificans ВКПМ В-9582, используемого в качестве контроля, получают, как описано в RU 2337954. Сравнение проводят путем использования в качестве биокатализатора при синтезе акрилата аммония из акрилонитрила в одинаковых условиях (при одинаковой скорости подачи акрилонитрила и при одинаковой концентрации единиц активности биокатализатора).
Реакцию проводят в 3-х стеклянных реакторах объемом 250 мл при 36°С с постоянным перемешиванием для каждого биокатализатора. Начальная масса реакционной смеси составляет 64 г. Подачу акрилонитрила осуществляют непрерывно, с такой скоростью, чтобы концентрация акрилонитрила в реакционной смеси не превышала 10 г/л. Концентрацию акрилонитрила и акрилата аммония контролируют каждые 30 минут.
При получении акрилата аммония с помощью биокатализатора на основе заявляемого штамма используют 54,96 мг клеток (по сухому веществу) с удельной нитрилазной активностью 5,9 ед/мг с.в. клеток. При получении акрилата аммония с помощью контрольного биокатализатора на основе штамма A. denitrificans ВКПМ В-9582 используют 48,4 мг клеток по сухому веществу с удельной нитрилазной активностью 6,7 ед/мг с.в. клеток. В обоих случаях количество единиц активности в реакционной смеси составляет 324 ед.
Параметры процессов синтеза акрилата аммония с обоими биокатализаторами представлены в таблице 1.
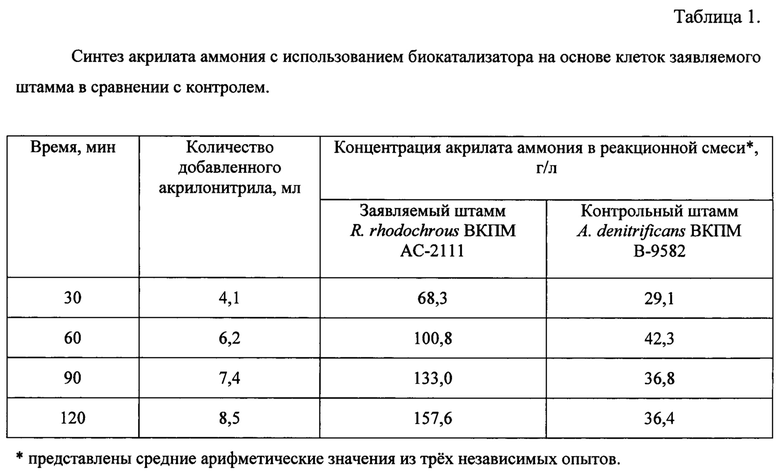
В результате в течение 2 часов процесса с использованием биокатализатора на основе клеток заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 происходит постоянное увеличение концентрации акрилата аммония, что приводит к накоплению до 157 г/л акрилата аммония. При использовании биокатализатора на основе клеток штамма-ближайшего аналога A. denitrificans ВКПМ В-9582 увеличение концентрации акрилата аммония прекращается после первого часа процесса, и в результате получают 36 г/л акрилата аммония. Быстрая остановка синтеза акрилата аммония связана с быстрой инактивацией активности в клетках контрольного биокатализатора. Это связано с тем, что биокатализатор на основе заявляемого штамма обладает повышенной операционной стабильностью и не инактивируется в ходе процесса синтеза.
Подобное верно также и для штаммов, содержащих две копии гена нитрилазы NitC1: Rhodococcus rhodochrous М8 2nit и Rhodococcus aetherivorans АС2063 2nit.
Пример 10. Получение раствора акрилата аммония с концентрацией 300 г/л из акрилонитрила с использованием биокатализатора на основе клеток штамма Rhodococcus rhodochrous ВКПМ АС-2111
Клетки заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 используют в качестве биокатализатора для получения раствора акрилата аммония с концентрацией 300 г/л из акрилонитрила.
Реакцию проводят в стеклянном реакторе объемом 250 мл при 33°С с постоянным перемешиванием. Начальная масса реакционной смеси равна 49 г. Подачу акрилонитрила осуществляют плавно с понижающейся скоростью за 5 часов таким образом, чтобы его остаточная концентрация была не более 10 г/л. Концентрацию акрилонитрила и акрилата аммония контролируют каждые 30 минут.
При получении акрилата аммония с помощью биокатализатора на основе заявляемого штамма используют 86,1 мг клеток по сухому веществу с удельной нитрилазной активностью 6,5 ед/мг с.в. клеток, клеточная нагрузка по сухому веществу от исходной реакционной массы составляла 0,18%, количество единиц активности в реакционной смеси составляло 560 единиц. Режим подачи акрилонитрила, остаточное содержание акрилонитрила и накопление акриловой кислоты в форме акрилата аммония в ходе реакции представлены в таблице 2.
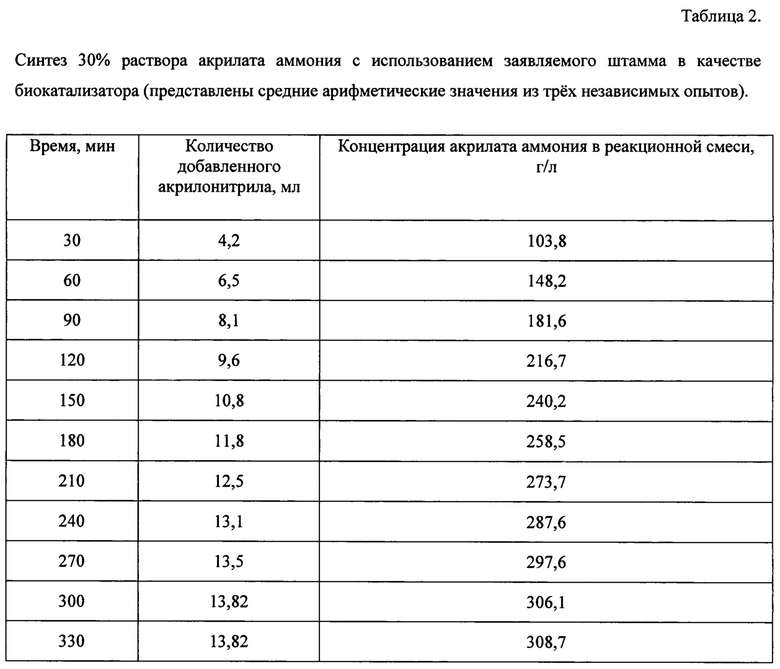
В результате за 5,5 часов получают реакционную смесь, содержащую 308,67 г/л акрилата аммония. Остаточная концентрация акрилонитрила составляет менее 0,1 г/л.
Пример 11. Получение раствора акрилата аммония с концентрацией 450 г/л из акрилонитрила с использованием биокатализатора на основе клеток штамма Rhodococcus rhodochrous ВКПМ АС-2111
Клетки заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 используют в качестве биокатализатора для получения раствора акрилата аммония с концентрацией 450 г/л по соли из акрилонитрила.
Реакцию проводят в стеклянном реакторе объемом 250 мл при 32°С с постоянным перемешиванием. Начальная масса реакционной смеси равна 38,1 г. Подачу акрилонитрила осуществляют плавно с понижающейся скоростью за 6,5 часов таким образом, чтобы его остаточная концентрация составляла не более 8 г/л. Концентрацию акрилонитрила и акрилата аммония контролировали каждые 30 минут.
При получении акрилата аммония с помощью биокатализатора на основе заявляемого штаммма используют 266,8 мг клеток по сухому веществу с удельной нитрилазной активностью 6,1 ед/мг с.в. клеток, клеточная нагрузка по сухому веществу от исходной реакционной массы составляет 0,7%, количество единиц активности в реакционной смеси составляет 1630 ед. Режим подачи акрилонитрила, остаточное содержание акрилонитрила и накопление акрилата аммония в ходе реакции представлены в таблице 3.
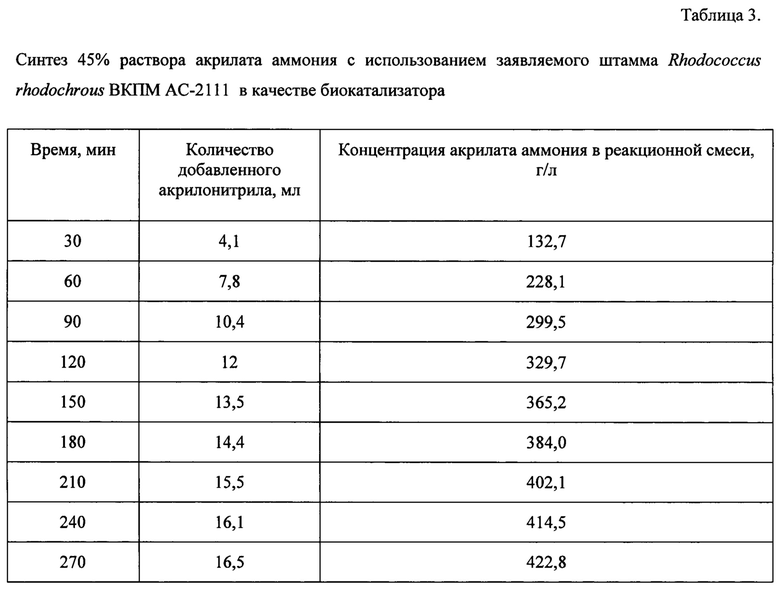
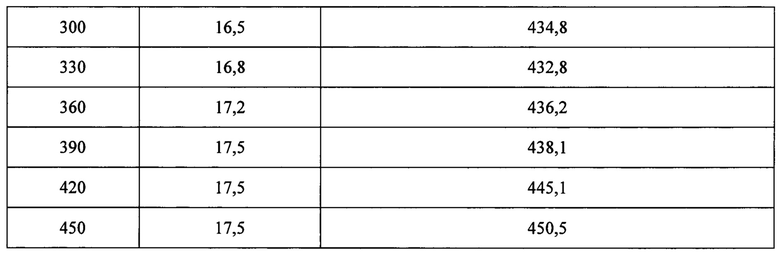
Через 7,5 часов инкубации в реакционной смеси получают концентрацию акрилата аммония 450,54 г/л. Остаточное содержание акрилонитрила составляет менее 0,01 г/л.
Таким образом,
- разработан способ конструирования штамма-биокатализатора на основе бактерий рода Rhodococcus, обладающего нитрилазной активностью;
- показано, что при трансформации акрилонитрила фермент нитрилаза более стабилен в клетках бактерий рода Rhodococcus, чем в клетках бактерий рода Alcaligenes;
- сконструирован штамм Rhodococcus rhodochrous ВКПМ АС-2111, обладающий нитрилазной активностью и повышенной операционной стабильностью при синтезе из акрилонитрила акриловой кислоты в форме акрилата аммония;
- разработан способ получения акрилата аммония с использованием в качестве биокатализатора заявляемого штамма Rhodococcus rhodochrous ВКПМ АС-2111 (до 450 г/л акрилата).
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение «Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов» Национального исследовательского центра «Курчатовский институт» (НИЦ «Курчатовский институт» - ГосНИИгенетика)
Акционерное общество “Биоамид” (АО “Биоамид”)
<120> Способ конструирования на основе бактерий рода Rhodococcus штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью, рекомбинантный штамм бактерий Rhodococcus rhodochrous, полученный таким способом, способ синтеза акриловой кислоты с использованием этого штамма в качестве биокатализатора
<160> 4
<210> 1
<211> 1117
<212> DNA
<213> Alcaligenes denitrificans С-32 VKM B-2243D
<400> 1
сс 2
atg gtt tcg tat aac agc aag ttc ctc gcg gca acc gtt cag gca 47
Met Val Ser Tyr Asn Ser Lys Phe Leu Ala Ala Thr Val Gln Ala
1 5 10 15
gag ccg gta tgg ctc gac gca gac gca acg atc gac aag tcg atc 92
Glu Pro Val Trp Leu Asp Ala Asp Ala Thr Ile Asp Lys Ser Ile
20 25 30
ggc atc atc gaa gaa gct gcc caa aag ggc gcg agt ctg atc gct 137
Gly Ile Ile Glu Glu Ala Ala Gln Lys Gly Ala Ser Leu Ile Ala
35 40 45
ttc ccg gaa gta ttc att ccg ggc ttc ccc tat tgg gcg tgg ctc 182
Phe Pro Glu Val Phe Ile Pro Gly Phe Pro Tyr Trp Ala Trp Leu
50 55 60
ggc gac gtg aag tac agc cta agc ttt act tca cgc tat cac gag 227
Gly Asp Val Lys Tyr Ser Leu Ser Phe Thr Ser Arg Tyr His Glu
65 70 75
aat tcg ttg gag cta ggt gac gac cgt atg cgt cgc ctc cag ctg 272
Asn Ser Leu Glu Leu Gly Asp Asp Arg Met Arg Arg Leu Gln Leu
80 85 90
gcc gcg cgc cgc aac aaa atc gca ctc gtc atg ggc tat tcg gag 317
Ala Ala Arg Arg Asn Lys Ile Ala Leu Val Met Gly Tyr Ser Glu
95 100 105
cgg gaa gcc gga tcg cgc tat atg agc cag gtg ttc atc gac gag 362
Arg Glu Ala Gly Ser Arg Tyr Met Ser Gln Val Phe Ile Asp Glu
110 115 120
cgt ggc gag atc gtt gcc aat cgg cgc aag ctg aag ccc aca cac 407
Arg Gly Glu Ile Val Ala Asn Arg Arg Lys Leu Lys Pro Thr His
125 130 135
gtt gag cgt acg atc tac ggc gaa ggc aac gga acc gat ttc ctc 452
Val Glu Arg Thr Ile Tyr Gly Glu Gly Asn Gly Thr Asp Phe Leu
140 145 150
acg cac gac ttc gcg ttc gga cgc gtc ggt gga ttg aac tgc tgg 497
Thr His Asp Phe Ala Phe Gly Arg Val Gly Gly Leu Asn Cys Trp
155 160 165
gaa cat ttc caa ccg ctc agc aag ttc atg atg tac agc ctc ggt 542
Glu His Phe Gln Pro Leu Ser Lys Phe Met Met Tyr Ser Leu Gly
170 175 180
gag cag gtc cac gtt gca tcg tgg ccg gcg atg ttc gct ctt cag 587
Glu Gln Val His Val Ala Ser Trp Pro Ala Met Phe Ala Leu Gln
185 190 195
ccg gat gtt ttc caa ctg agc atc gaa gcc aac gcg acg gtc acc 632
Pro Asp Val Phe Gln Leu Ser Ile Glu Ala Asn Ala Thr Val Thr
200 205 210
cgc tcg tac gca atc gaa ggc caa acc ttt gtg ctt tgc tcg acg 677
Arg Ser Tyr Ala Ile Glu Gly Gln Thr Phe Val Leu Cys Ser Thr
215 220 225
cag gtg atc gga cct agc gcg atc gaa acg ttc tgc ctc aac gac 722
Gln Val Ile Gly Pro Ser Ala Ile Glu Thr Phe Cys Leu Asn Asp
230 235 240
gaa cag cgc gca ctg ttg ccg caa gga tgt ggc tgg gcg cgc att 767
Glu Gln Arg Ala Leu Leu Pro Gln Gly Cys Gly Trp Ala Arg Ile
245 250 255
tac ggc ccg gat gga agc gag ctt gcg aag cct ct ggcg gaa gat 812
Tyr Gly Pro Asp Gly Ser Glu Leu Ala Lys Pro Leu Ala Glu Asp
260 265 270
gct gag ggg atc ttg tac gca gag atc gat ctg gag cag att ctg 857
Ala Glu Gly Ile Leu Tyr Ala Glu Ile Asp Leu Glu Gln Ile Leu
275 280 285
ctg gcg aag gct gga gcc gat ccg gtc ggg cac tat tcg cgg cct 902
Leu Ala Lys Ala Gly Ala Asp Pro Val Gly His Tyr Ser Arg Pro
290 295 300
gac gtg ctg tcg gtc cag ttc gac ccg cgc aat cat acg cca gtt 947
Asp Val Leu Ser Val Gln Phe Asp Pro Arg Asn His Thr Pro Val
305 310 315
cat cgc atc ggc att gac ggt cgc ttg gat gtg aat acc cgc agt 992
His Arg Ile Gly Ile Asp Gly Arg Leu Asp Val Asn Thr Arg Ser
320 325 330
cgc gtg gag aat ttc cga ctg cga caa gcg gct gag cag gag cgt 1037
Arg Val Glu Asn Phe Arg Leu Arg Gln Ala Ala Glu Gln Glu Arg
335 340 345
cag gca tcc aag cgg ctc gga acg aaa ctc ttt gaa caa tcc ctt 1082
Gln Ala Ser Lys Arg Leu Gly Thr Lys Leu Phe Glu Gln Ser Leu
350 355 360
ctg gct gaa gaa ccg gtc cca gca aag tag agc tc 1117
Leu Ala Glu Glu Pro Val Pro Ala Lys ***
365
<210> 2
<211> 522
<212> DNA
<213> Rhodococcus rhodochrous ВКМ Ас-1515Д
<400> 2
ggatccccgg agtcttcatc ctgttttggg atgcgcagga ttaacacatc tacacattga 60
catccgttcc gatgtgaagt aaaaattgtc acgtagggcg gcaggcgaag tctgcagctc 120
gaacatcgaa gggtgggagc cgagagatcg gagacgcaga cacccggagg gaacctagcc 180
tcccggaccg atgcgtgtcc tggcaacgcc tcaagattca gcgcaagcga ttcaatcttg 240
ttacttccag aaccgaatca cgtccccgta gtgtgcgggg agagcgcccg aacgcaggga 300
tggtatccat gcgccccttc tcttttcgaa cgagaaccgg ccgctacagc cgacccggag 360
acactgtgac gccgttcaac gattgttgtg ctgtgaagga ttcactcaag ccaactgata 420
tcgccattcc gttgccggaa catttgacac cttctcccta cgagtagaag ccagctggac 480
ccctctttga gcccagctcc gatgaaagga atgaggccat gg 522
<210> 3
<211> 539
<212> DNA
<213> Rhodococcus rhodochrous ВКМ Ас-1515Д
<400> 3
gactcgatga tcggtgtcag taatgcgctc acaccccagg aagtgatcgt atgagtgaag 60
acacactcac tgatcggctc ccggcgactg ggaccgccgc accgccccgc gacaatggcg 120
agcttgtatt caccgagcct tgggaagcaa cggcattcgg ggtcgccatc gcgctttcgg 180
atcagaagtc gtacgaatgg gagttcttcc gacagcgtct cattcactcc atcgctgagg 240
ccaacggttg cgaggcatac tacgagagct ggacaaaggc gctcgaggcc agcgtggtcg 300
actcggggct gatcagcgaa gatgagatcc gcgagcgcat ggaatcgatg gccatcatcg 360
actgacatcc cctgcgtttc catccagcag cagtgcgggc gtaccccgac ggggctgagc 420
cgacggggta cgcccgcact tcatcaatga cgttctgagg cacacagcgc agagtcgagc 480
tgagtgcctc agaacgtcat gacggtggtt cctaattcgg ctcggtgggt actgaattc 539
<210> 4
<211> 440
<212> DNA
<213> Rhodococcus rhodochrous ВКМ Ас-1515Д
<400> 4
ggtacctcgc tgtaccggcg gcctcacccg aacccggccg ccgcgcaacg catcggctgg 60
ccggtccgcg gacgtggctg cgcacacgag gccggcagcc gactccgtgt gctgccccgt 120
tctcaccgac ggtcccgtcc gccggtcgat cccgaggggg cactgcgctg tcgtgtcggc 180
ggctcgaggt gcgtcgtgat cacggcgtcg tcttcctgtc acggcccaca tcgccctgca 240
cacgcagggt cgcggaacgc aatcgaccct gcgatccggg gacgtgtgga ccttcggtgt 300
tgtcgtccgg cccaaatact acttcacata gtatttatgt cgagcaatgg gtcggcggca 360
catccatcac ggcgtacgtc ccgggcctcc agcgtcgatg tccgcgcagc acgcaggaac 420
aggcacgggg atcctctaga 440
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ БАКТЕРИЙ ALCALIGENES DENITRIFICANS - ПРОДУЦЕНТ НИТРИЛАЗЫ | 2007 |
|
RU2337954C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКРИЛОВЫХ МОНОМЕРОВ И ШТАММ БАКТЕРИЙ RHODOCOCCUS RHODOCHROUS ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2006 |
|
RU2304165C1 |
| ШТАММ БАКТЕРИЙ ALCALIGENES DENITRIFICANS-ПРОДУЦЕНТ НИТРИЛАЗЫ | 2001 |
|
RU2177034C1 |
| ПОВЫШЕНИЕ РЕАКЦИОННОЙ СПОСОБНОСТИ НИТРИЛГИДРАТАЗЫ С ПОМОЩЬЮ АЛЬДЕГИДА | 2022 |
|
RU2827406C2 |
| БИОТЕХНОЛОГИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ АКРИЛАТА АММОНИЯ | 2006 |
|
RU2323977C2 |
| СРЕДСТВА И СПОСОБЫ ПОЛУЧЕНИЯ АМИДНЫХ СОЕДИНЕНИЙ С МЕНЬШИМ КОЛИЧЕСТВОМ АКРИЛОВОЙ КИСЛОТЫ | 2015 |
|
RU2730624C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА ПОЛИАКРИЛАМИДА С УВЕЛИЧЕННОЙ ВЯЗКОСТЬЮ | 2017 |
|
RU2751919C2 |
| ШТАММ БАКТЕРИЙ ALCALIGENES SPECIES - ПРОДУЦЕНТ НИТРИЛАЗЫ | 1995 |
|
RU2081169C1 |
| Способ получения секретируемой полностью функциональной фосфолипазы А2 в дрожжах Saccharomyces cerevisiae, белок-предшественник для осуществления этого способа (варианты) | 2019 |
|
RU2728240C1 |
| Генетическая конструкция, кодирующая предшественник белка YB-1 человека, штамм Escherichia coli - продуцент предшественника белка YB-1 человека, способ микробиологического синтеза этого предшественника | 2019 |
|
RU2728237C1 |
Группа изобретений относится к конструированию штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью. Предложен способ конструирования на основе бактерий рода Rhodococcus штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью, путем интеграции в геном штамма-реципиента бактерий рода Rhodococcus двух копий последовательности SEQ ID 01, представляющей собой ген нитрилазы nitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D. Также предложен рекомбинантный штамм бактерий Rhodococcus rhodochrous ВКПМ АС-2111, представляющий собой биокатализатор, обладающий нитрилазной активностью. Указанный штамм получен путем интеграции двух копий гена нитрилазы nitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D в штамм-реципиент Rhodococcus rhodochrous ВКМ Ас-1515Д. Указанный штамм-биокатализатор используют в способе синтеза акриловой кислоты в форме акрилата аммония. 3 н.п. ф-лы, 3 табл., 11 пр.
1. Способ конструирования на основе бактерий рода Rhodococcus штамма-биокатализатора, обладающего нитрилазной активностью и повышенной операционной стабильностью, путем интеграции в геном штамма-реципиента бактерий рода Rhodococcus двух копий последовательности SEQ ID 01, представляющей собой ген нитрилазы nitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D.
2. Рекомбинантный штамм бактерий Rhodococcus rhodochrous ВКПМ АС-2111 - биокатализатор, обладающий нитрилазной активностью и полученный способом по п. 1 путем интеграции двух копий гена нитрилазы nitC1 из штамма Alcaligenes denitrificans С-32 VKM B-2243D в штамм-реципиент Rhodococcus rhodochrous ВКМ Ас-1515Д.
3. Способ синтеза акриловой кислоты в форме акрилата аммония путем подачи акрилонитрила в водную суспензию штамма-биокатализатора и инкубирования с перемешиванием, отличающийся тем, что в качестве штамма-биокатализатора используют рекомбинантный штамм по п. 2.
| БИОТЕХНОЛОГИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ АКРИЛАТА АММОНИЯ | 2006 |
|
RU2323977C2 |
| ШТАММ БАКТЕРИЙ ALCALIGENES DENITRIFICANS - ПРОДУЦЕНТ НИТРИЛАЗЫ | 2007 |
|
RU2337954C1 |
| WO 2005054456 A1, 16.06.2005 | |||
| НОВИКОВ А.Д | |||
| И ДР | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Биотехнология, 2016, T | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Железобетонный фасонный камень для кладки стен | 1920 |
|
SU45A1 |
Авторы
Даты
2020-09-01—Публикация
2018-12-13—Подача