Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно к новым составам для лечения и/или профилактики ожирения, содержащим N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и их оптические изомеры и фармацевтически приемлемые соли, фармацевтической композиции на основе упомянутых составов, лекарственному средству на основе упомянутых составов или упомянутой фармацевтической композиции и готовой лекарственной форме на основе упомянутых составов, упомянутой фармацевтической композиции или упомянутого лекарственного средства.
На сегодняшний день одним из самых актуальных и распространенных хронических заболеваний в мире является ожирение. Резкое увеличение количества людей, страдающих ожирением, связано с рядом причин, к которым относятся снижение доли физического труда, а также физических нагрузок в целом (вплоть до пешей ходьбы), изменение рациона питания на более богатый жирами и углеводами, популярность высококалорийных напитков и фаст-фуда, увеличение уровня стрессов и нервных расстройств, компьютеризация досуга [1].
По данным Всемирной Организации Здравоохранения (ВОЗ) за 2016 год более 1,9 млрд. человек старше 18 лет и более 340 млн. детей и подростков (из которых порядка 41 млн. приходится на детей до 5 лет) в мире имеют ожирение или избыточную массу тела (по индексу Кетле выше 25 кг/м2), причем тяжесть течения и наличие тяжелой сопутствующей патологии наблюдается у большинства (89%) больных. По количеству людей, имеющих ожирение или избыточную массу тела, а также скорости распространения, ожирение считается эпидемией неинфекционного характера. При сохраняющемся темпе распространения ожирения, по прогнозам экспертов ВОЗ к 2025 году эти цифры удвоятся. Наиболее частой сопутствующей патологией является сахарный диабет 2 типа, артериальная гипертензия, атеросклероз сосудов нижних конечностей, ишемическая болезнь сердца, нарушение репродуктивной и сексуальной функции, некоторые формы онкопатологии. Ожирение приводит к сокращению продолжительности и ухудшению качества жизни. Эпидемиологические исследования свидетельствуют о том, что ожирение приводит к сокращению продолжительности жизни на 8-10 лет, способствует развитию сопутствующих заболеваний и приводит к таким психологическим последствиям, как низкая самооценка, депрессия, тревога, снижение психологической адаптации и другие [2, 3, 4].
Основным регулятором пищевого поведения человека является центральная нервная система, в первую очередь, гипоталамус, выполняющий функцию высшего вегетативного центра, регулирующего обмен веществ, терморегуляцию, деятельность кровеносных сосудов и внутренних органов, пищевое, половое поведение, психические функции. Гипоталамус получает сигналы от различных органов и систем организма, объединяет и действует на организм через различные нисходящие пути с целью сохранения энергетического равновесия. В случае регуляции пищевого поведения и обмена веществ такими сигналами могут служить гормоны пищеварительного тракта, такие как грелин, пептид YY, холецистокинин, а также инсулин и гормоны жировой ткани, прежде всего лептин и адипонектин. Сбои в регуляторной функции гипоталамуса могут повлечь за собой развитие ожирения, однако чаще всего они обусловлены именно некорректными сигналами, получаемыми и обрабатываемыми гипоталамусом. Так, развитие ожирения часто связано с гормоном жировой ткани лептином, который вырабатывается в ответ на прием пищи. Лептин стимулирует POMC-нейроны гипоталамуса, вызывая тем самым чувство насыщения и снижение количества потребляемой пищи и тормозит работу AgRP/NPY-нейронов гипоталамуса, возбуждение которых вызывает чувство голода. Голодание приводит к снижению уровня лептина в сыворотке, а также к активации гипоталамо-гипофизарно-надпочечниковой оси, ингибированию гормона роста, функции щитовидной железы и репродуктивной функции, что может привести к развитию ожирения. Мутации в гене лептина или мутации лептиновых рецепторов (связанное с лептином генетическое ожирение), или избыток лептина (приводящий к развитию лептинорезистентности рецепторов гипоталамуса) также вызывают развитие морбидного ожирения, сопровождающегося множеством нейроэндокринных отклонений [18-22].
Таким образом, ожирение или избыточная масса тела могут быть обусловлены рядом причин, притом чаще всего имеет место их совокупность. Так, по Международной Классификации Болезней (МКБ-10), ожирение относится к классу болезней эндокринной системы, расстройства питания и нарушения обмена веществ, в который входят следующие группы: болезни щитовидной железы (синдром врожденной йодной недостаточности, в том числе эндемические состояния, связанные с дефицитом йода, и состояния, являющиеся следствием неадекватной секреции тиреоидных гормонов у развивающегося плода, а так же связанные с природными зобогенными факторами; болезни щитовидной железы, связанные с йодной недостаточностью, и сходные состояния, такие как приобретенный гипотиреоз вследствие недостатка йода; субклинический гипотиреоз вследствие йодной недостаточности; другие формы гипотиреоза; другие формы нетоксического зоба; тиреотоксикоз (гипертиреоз); тиреоидит; другие болезни щитовидной железы), сахарный диабет (сахарный диабет I типа, в том числе лабильный, с началом в молодом возрасте, с наклонностью к кетозу; сахарный диабет II типа, в том числе диабет с началом во взрослом возрасте, с началом в зрелом возрасте, без склонности к кетозу, стабильный, а также инсулиннезависимый сахарный диабет молодых; сахарный диабет (как I, так и II типа), связанный с недостаточностью питания; другие уточненные формы сахарного диабета; сахарный диабет неуточненный), другие нарушения регуляции глюкозы и внутренней секреции поджелудочной железы, нарушения других эндокринных желез (гипопаратиреоз; гиперпаратиреоз и другие нарушения паращитовидной (околощитовидной) железы; гиперфункция гипофиза; гипофункция и другие нарушения гипофиза; синдром Иценко-Кушинга; адреногенитальные расстройства; гиперальдостеронизм; другие нарушения надпочечников; дисфункция яичников; дисфункция яичек; нарушения полового созревания, не классифицированные в других рубриках; полигландулярная дисфункция; болезни вилочковой железы; другие эндокринные нарушения, в том числе при других болезнях); недостаточность питания; другие виды недостаточности питания; ожирение и другие виды избыточности питания (локализованное отложение жира; ожирение, обусловленное избыточным поступлением энергетических ресурсов; ожирение, вызванное приемом лекарственных препаратов; крайняя степень ожирения, сопровождаемая альвеолярной гиповентиляцией; другие формы ожирения, в том числе болезненное ожирение, а также ожирение неуточненное; и другие виды избыточности питания, такие как гипервитаминоз А, гиперкаротинемия, синдром мегадоз витамина В6, гипервитаминоз D и другие; а также последствия избыточности питания); нарушения обмена веществ (нарушения обмена ароматических аминокислот; нарушения обмена аминокислот с разветвленной цепью и обмена жирных кислот; другие нарушения обмена аминокислот; непереносимость лактозы; другие нарушения обмена углеводов; нарушения обмена сфинголипидов и другие болезни накопления липидов; нарушения обмена глюкозаминогликанов; нарушения обмена гликопротеинов; нарушения обмена липопротеидов и другие липидемии; нарушения обмена пуринов и пиримидинов; нарушения обмена порфирина и билирубина, в том числе дефекты каталазы и пероксидазы; нарушения минерального обмена; кистозный фиброз; амилоидоз; уменьшение объема жидкости, в том числе обезвоживание, уменьшение объема плазмы или внеклеточной жидкости, гиповолемия; другие нарушения водно-солевого обмена или кислотно-щелочного равновесия; другие нарушения обмена веществ, в том числе вызванные приемом лекарственных препаратов, и, в том числе, аденолипоматоз Лонуа-Бансода, триметиламинурия; эндокринные и метаболические нарушения, возникшие после медицинских процедур; расстройства питания и нарушения обмена веществ при других болезнях). Кроме того, ожирение может являться одним из следствий различных психических расстройств и расстройств поведения (5 класс по МКБ-10), в том числе хромосомных патологий, которые относятся к категории умственной отсталости (в частности синдром Берьесона-Форсмана-Леманна, синдром Альстрема, синдром Протея (синдром Коэна), Х-сцепленный синдром задержки умственного развития типа Борка (синдром МЕНМО), синдром Прадера-Вилли (в том числе связанный с делецией 6q16), синдром Сотоса, сидром Уивера (синдром Уивера-Смитта), синдром Шерешевского-Тёрнера, синдром Уилсона-Тернера (Wilson-Turner syndrome, WTS), синдром Х-сцепленной умственной отсталости 6 (MRXS6), с гинекомастией и ожирением), синдром Беквита-Видемана). С точки зрения генетики можно выделить следующие формы ожирения: моногенное ожирение, генетические синдромы, ассоциированные с ожирением, и простое ожирение, характеризующееся полигенным наследованием. С точки зрения этиопатогенетической классификации ожирение подразделяют на экзогенно-конституциональное ожирение (первичное, алиментарно-конституциональное), гиноидного и андроидного типа; и симптоматическое (вторичное) ожирение, которое в свою очередь подразделяют на симптоматическое ожирение с установленным генетическим дефектом (в том числе в составе известных генетических синдромов с полиорганным поражением), церебральное симптоматическое ожирение, эндокринное симптоматическое ожирение, и ятрогенное симптоматическое ожирение (обусловленное приемом ряда лекарственных препаратов) [18-22].
Имеющиеся научные данные свидетельствуют о том, что целью лечения ожирения является умеренное снижение массы тела с обязательным уменьшением риска развития сопутствующих заболеваний, стабилизации достигнутой массы тела, улучшением качества и продолжительности жизни. Согласно рекомендациям ВОЗ, основу комплексной программы контроля массы тела составляют немедикаментозные методы терапии: рациональное гипокалорийное питание, повышение физической активности, изменение образа жизни. В медицине широко применяются способы лечения больных ожирением с применением аппаратной физиотерапии, методов бальнеотерапии [5, 6]. Весьма распространено хирургическое лечение ожирения, такое как применение внутрижелудочного баллона, регулируемое бандажирование желудка (РБЖ), продольная резекция желудка (ПРЖ) или рукавная, вертикальная, СЛИВ-резекция, операция гастрошунтирования (ГШ), билиопанкреатическое шунтирование (БПШ). Однако хирургическое лечение часто имеет ряд серьезных побочных эффектов, таких как тяжесть в желудке, тупые боли в эпигастрии, тошнота и рвота, перфорация желудка или непроходимость кишечника, язвообразование, гастро-интестинальные кровотечения, демпинг-синдром, метаболические осложнения, связанные с недостаточным поступлением белка, минералов и витаминов, холелитиаз, а также развитие рефлюкс-эзофагита, кровотечение из ворот селезенки или линии шва, прорезывание скрепочного шва, которые могут привести к серьезным последствиям для здоровья, требующим хирургического вмешательства, несостоятельность анастомозов, и, кроме того, возможен летальный исход (например, при билиопанкреатическом шунтировании процент летального исхода может составлять порядка 8%) [7]. Таким образом, несмотря на разработанные многочисленные виды хирургических операций при ожирении, практически все операции имеют существенные недостатки и побочные эффекты различной степени тяжести, имеется также ряд индивидуальных противопоказаний для подобных операций. Основной причиной обращения людей, страдающих ожирением, к хирургическим методам лечения является то, что большинство (вплоть до 95%) пациентов не могут достичь и потом удержать клинически значимого снижения массы тела, а при выраженном ожирении эффективность консервативной терапии не превышает 5-10%. Наиболее распространенными причинами, которые не позволяют людям достичь значимого снижения массы тела, являются неправильный, самостоятельный выбор диеты, которая не предоставляет организму необходимого количества питательных веществ, что приводит к сложностям в ее соблюдении и наличие стрессовых ситуаций, в которых большая часть людей употребляет высококалорийные продукты и напитки, и может злоупотреблять алкоголем. Составлением рациона питания для лечения ожирения и избыточной массы тела нужно заниматься совместно со специалистами – эндокринологом, диетологом, физиотерапевтом и психологом, поскольку он должен быть полноценным, сбалансированным и содержать в себе все необходимые для организма компоненты (белки, углеводы, жиры, микроэлементы и витамины), а также необходимо учитывать индивидуальные особенности организма, в том числе гормональный дисбаланс. Консультация психолога проводится с целью создания у пациента правильного психологического настроя для изменения своего образа жизни (правильного питания, которое необходимо соблюдать на протяжении всей жизни пациента, и занятия физическими нагрузками, необходимыми для поддержания организма в здоровом состоянии). Для облегчения адаптации пациента к новому образу жизни возможно назначение ноотропных препаратов, что особенно актуально в том случае, если пациент подвергается многочисленным стрессовым ситуациям и злоупотребляет алкоголем. Также, в комплексе с диетой, для лечения ожирения и избыточной массы тела специалисты назначают биологически активные добавки и препараты, понижающие аппетит (анорексигенные препараты) [8, 9].
Таким образом, комплексное и эффективное лечение ожирения должно включать в себя правильное, сбалансированное питание, физические нагрузки, а на начальном этапе лечения и при необходимости (например, в том случае, если пациент снова начал неправильно питаться и набирать вес, или в случае злоупотребления алкоголем) – назначение анорексигенных и ноотропных препаратов, причем наиболее предпочтительным является совмещение ноотропной и анорексигенной активности в одном препарате.
Фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) давно и прочно зарекомендовал себя как эффективный препарат для лечения заболеваний ЦНС различного генеза, особенно связанных с интоксикацией, сопровождающихся ухудшением интеллектуально-мнестических функций, снижением двигательной активности; лечения невротических состояний, проявляющихся вялостью, повышенной истощаемостью, снижением психомоторной активности, нарушением внимания, ухудшением памяти; лечения нарушений процесса обучения; лечения психоорганических синдромов, проявляющихся интеллектуально-мнестическими нарушениями и апатико-абулическими явлениями, а также вялоапатических состояний при шизофрении; лечения судорожных состояний; лечения ожирения алиментарно-конституционального генеза; профилактики гипоксии, повышения устойчивости к стрессу; коррекции функционального состояния организма в экстремальных условиях профессиональной деятельности с целью предупреждения развития утомления и для повышения умственной и физической работоспособности; коррекции суточного биоритма, при инверсии цикла сон-бодрствование; для лечения хронического алкоголизма (с целью уменьшения явлений астении, депрессии, интеллектуально-мнестических нарушений, купирования «симптома отмены») [10].

N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам)
Фонтурацетам повышает устойчивость тканей мозга к гипоксии и токсическим воздействиям, обладает анксиолитической активностью [11]; оказывает положительное влияние на обменные процессы, стимулирует окислительно-восстановительные процессы, повышает энергетический потенциал организма за счет утилизации глюкозы [12]; повышает содержание норадреналина, дофамина и серотонина в мозге, не влияет на уровень содержания ГАМК, не связывается с GABAA и GABAB рецепторами, не оказывает заметного влияния на спонтанную биоэлектрическую активность мозга; проявляет умеренно выраженный стимулирующий эффект, проявляющийся в отношении двигательных реакций, повышении физической работоспособности, выраженном антагонизме каталептическому действию нейролептиков, а также ослаблении выраженности снотворного действия этанола и гексобарбитала; проявляет адаптогенное действие в повышении устойчивости организма к стрессу в условиях чрезмерных психических и физических нагрузок, при утомлении, гипокинезии и иммобилизации, при низких температурах; стимулирует выработку антител в ответ на введение антигена, что указывает на иммуностимулирующие свойства, но в то же время не способствует развитию гиперчувствительности немедленного типа и не изменяет аллергическую воспалительную реакцию кожи, вызванную введением чужеродного белка; не обладает тератогенными, мутагенными, канцерогенными и эмбриотоксичными свойствами; имеет низкую токсичность [10].
Ноотропный эффект препарата сочетается с анксиолитической активностью, он оказывает некоторый анальгезирующий эффект, повышая порог болевой чувствительности. На фоне приема препарата также отмечено улучшение зрения, которое проявляется в увеличении остроты, яркости и полей зрения [10].
При курсовом применении фонтурацетам оказывает выраженный анорексигенный эффект [10]. При этом, ноотропные эффекты фонтурацетама позволяют создать благоприятный психологический климат у пациента, облегчая адаптацию пациента к соблюдению здорового образа жизни, повышают устойчивость пациента к стрессам в условиях чрезмерных психических и физических нагрузок, при утомлении, гипокинезии и иммобилизации, что уменьшает вероятность рецидивов, выражающихся в употреблении высококалорийных и жирных продуктов и напитков, злоупотреблении алкоголем и возможной минимизации физических нагрузок. В связи с чем, специалисту в данной области очевидно, что фонтурацетам может использоваться в качестве дополнения к сбалансированной диете и физическим нагрузкам для длительного применения с целью коррекции массы тела для лечения ожирения или избыточной массы тела, обусловленных болезнями эндокринной системы, расстройством питания, нарушениями обмена веществ, психическими расстройствами и/или расстройствами поведения.
Известны аналоги фонтурацетама 2-(2-оксо-4-фенилпирролидин-1-ил)уксусная кислота и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат, которые являются активаторами когнитивных функций [13].
Известно также соединение 4-фенилпирролидон-2, являющееся структурно родственным фонтурацетаму, однако его биологическая активность не описана.
Авторы настоящего изобретения неожиданно обнаружили, что новые составы, включающие фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат, имеют лучшие свойства, чем субстанция-порошок фонтурацетама, используемый в фармацевтической промышленности в настоящее время, и выбранный авторами настоящего изобретения в качестве прототипа.

2-(2-оксо-4-фенилпирролидин-1-ил)уксусная кислота
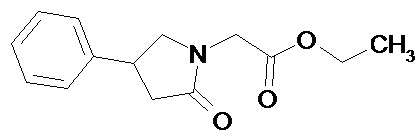
этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат
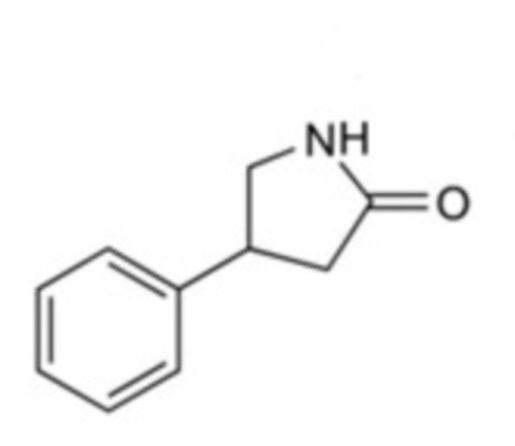
4-фенилпирролидон-2
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и других готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя новый состав N-карбамоил-метил-4-фенил-2-пирролидона и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, дезинтегранты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также иные фармацевтически приемлемые поверхностно-активные вещества, и смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как бензиловый спирт, уротропин, этилендиаминтетрауксусная кислота, бензойная кислота, хлорбутанол, сорбиновая кислота, парабены, алкилпиридиний, бензетоний и их фармацевтически приемлемые соли и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, таких как гидрофильные полимерные замедлители высвобождения, например, производные целлюлозы, полиэтиленоксид, желатин, поливиниловый спирт, поливинилпирролидон, альгинаты, карбомеры, гидрофобные замедлители высвобождения, такие как глицерилбегенат, моностеарат алюминия. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, буферные растворы, а также их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры (такие как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, микрокристаллическая целлюлоза, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Для регулирования pH могут быть использованы различные органические и неорганические кислоты, такие как яблочная, аскорбиновая, лимонная, уксусная, янтарная, винная, фумаровая, молочная, аспарагиновая, глутаровая, глутаминовая, сорбиновая кислоты. Примерами диспергирующих агентов и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, коллоидный диоксид кремния, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или получены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные [14]. Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты – лизин, орнитин и аргинин.
Задачей настоящего изобретения является разработка стабильного при хранении, негигроскопичного, хорошо растворимого, экономически целесообразного, промышленно реализуемого, препаративного состава фонтурацетама (N-карбамоил-метил-4-фенил-2-пирролидона) для лечения и/или профилактики ожирения или избыточной массы тела.
Стабильность в твердом состоянии и срок хранения активных компонентов являются очень важными факторами. Лекарственное соединение и композиции, включающие его, должны обладать способностью храниться в течение значительных периодов времени, не проявляя значимого изменения физико-химических свойств активного компонента (например, его химического состава, плотности, гигроскопичности и растворимости).
Таким образом, авторы изобретения неожиданно обнаружили, что присутствие 4-фенилпирролидона-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, или их оптических изомеров и фармацевтически приемлемых солей, в субстанции фонтурацетама улучшает некоторые свойства субстанции фонтурацетама, такие как стабильность, скорость растворения, снижает гигроскопичность. При этом наличие 4-фенилпирролидона-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, или их оптических изомеров и фармацевтически приемлемых солей в составе согласно настоящему изобретению не только не приводит к снижению активности фонтурацетама (прототипа), но и, напротив, может повысить фармацевтическую активность субстанции фонтурацетама. Новые составы, содержащие фонтурацетам, согласно настоящему изобретению не приводят к развитию гиперчувствительности немедленного типа и не изменяют аллергическую воспалительную реакцию кожи, вызванную введением чужеродного белка; не обладают тератогенными, мутагенными, канцерогенными и эмбриотоксичными свойствами; имеют низкую токсичность. В связи с чем, новые составы, содержащие фонтурацетам, согласно настоящему изобретению могут использоваться для лечения и/или профилактики ожирения, в качестве анорексигенного и ноотропного средства, для лечения и профилактики токсических и психологических эффектов, вызванных злоупотреблением алкоголя (с целью уменьшения явлений астении, интеллектуально-мнестических нарушений, купирования «синдрома отмены»).
Технические результаты настоящего изобретения:
- повышение стабильности (времени хранения) состава согласно настоящему изобретению по сравнению с прототипом;
- повышение скорости растворения состава по сравнению с прототипом;
- снижение гигроскопичности состава по сравнению с прототипом;
- расширение арсенала средств, обладающих анорексигенной активностью, для лечения и профилактики ожирения или избыточной массы тела;
- повышение активности заявленного состава по сравнению с прототипом.
Поставленная задача решается, а технический результат достигается созданием состава для лечения и/или профилактики ожирения, обладающего анорексигенной активностью, включающего N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и по меньшей мере одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирроли-дин-1-ил)ацетат и/или их оптические изомеры и/или их фармацевтически приемлемые соли, причем упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,25% до 20,00%, и/или 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве не более 20,00% мас и/или этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве не более 20,00% мас.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- дополнительное соединение представляет собой 4-фенилпирролидон-2 в количестве от 0,25 до 1,00% мас.;
- упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,30 до 0,60% мас.;
- упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,50 до 0,60% мас.;
- дополнительное соединение представляет собой 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,01 до 1,00% мас.;
- упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,50% мас.;
- упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,20% мас.;
- дополнительное соединение представляет собой этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,01 до 1,00% мас.;
- упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,50% мас.;
- упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,20% мас.
Поставленная задача также осуществляется, а технический результат достигается созданием фармацевтической композиции для лечения и/или профилактики ожирения, причем упомянутая композиция содержит в терапевтически эффективном количестве любой вышеупомянутый состав и по меньшей мере один фармацевтически приемлемый носитель.
Поставленная задача также осуществляется, а технический результат достигается созданием лекарственного средства для лечения и/или профилактики ожирения, в виде таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, причем упомянутое средство содержит в терапевтически эффективном количестве любой вышеупомянутый состав или вышеупомянутую фармацевтическую композицию.
Предметом настоящего изобретения является состав для лечения и/или профилактики ожирения или избыточной массы тела, включающий N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и по меньшей мере одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и/или их оптические изомеры и/или их фармацевтически приемлемые соли, причем упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,25% до 20,00%, и/или 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве не более 20,00% мас и/или этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве не более 20,00% мас.
Более предпочтительным является состав, характеризующийся тем, что дополнительное соединение представляет собой 4-фенилпирролидон-2 в количестве от 0,25 до 1,00% мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,30 до 0,60% мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,50 до 0,60 % мас.
Более предпочтительным является состав, характеризующийся тем, что дополнительное соединение представляет собой 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,01 до 1,00 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,50 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,20 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,01 до 1,00 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,50 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,20 % мас.
Более предпочтительным является состав, характеризующийся тем, что упомянутый состав содержит фонтурацетам в количестве более 96,00% мас.
Более предпочтительным является состав, характеризующийся тем, что ожирение или избыточная масса тела представляет собой первичное ожирение или избыточную массу тела.
Более предпочтительным является состав, характеризующийся тем, что ожирение или избыточная масса тела представляет собой ожирение или избыточную массу тела алиментарно-конституционального генеза.
Более предпочтительным является состав, характеризующийся тем, что предназначен для лечения ожирения или избыточной массы тела, обусловленных заболеваниями эндокринной системы, расстройством питания и/или нарушением обмена веществ.
Более предпочтительным является состав, характеризующийся тем, что предназначен для лечения ожирения или избыточной массы тела, обусловленных по меньшей мере одним заболеванием, выбранным из группы, состоящей из болезней щитовидной железы, сахарного диабета, нарушений регуляции глюкозы, нарушений внутренней секреции эндокринных желез, недостаточности питания, избыточности питания, нарушений обмена веществ, психических расстройств и расстройств поведения, ожирения или избыточной массы тела, вызванных приемом лекарственных препаратов.
Также предметом настоящего изобретения является фармацевтическая композиция для лечения и/или профилактики ожирения или избыточной массы тела, которая содержит терапевтически эффективное количество упомянутого состава, включающего фонтурацетам и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и их оптические изомеры и фармацевтически приемлемые соли, и по меньшей мере, один фармацевтически приемлемый носитель.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемыми эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с составом, включающим фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и их оптические изомеры и фармацевтически приемлемые соли, по настоящему изобретению может включать и другие активные субстанции, в том числе обладающие активностью, при условии, что они не вызывают нежелательных эффектов.
При необходимости использования фармацевтической композиции по настоящему изобретению в клинической практике она может смешиваться с традиционными фармацевтическими носителями.
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в частности, в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом настоящего изобретения также является лекарственное средство для лечения и/или профилактики ожирения или избыточной массы тела, в виде таблеток, капсул или раствора для инъекций, помещенных в фармацевтически приемлемую упаковку, содержащее в терапевтически эффективном количестве состав, включающий фонтурацетам и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и их оптические изомеры и фармацевтически приемлемые соли, или фармацевтическую композицию по настоящему изобретению.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка средства, содержащего новый состав N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10-500 мг, предпочтительно – 50-300 мг. Поэтому во время получения из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10-500 мг нового состава N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению, предпочтительно – 50-300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно – от одного до шести раз).
Предметом настоящего изобретения также является готовая лекарственная форма для лечения и/или профилактики ожирения или избыточной массы тела, в виде таблеток, капсул или раствора для инъекций, помещенных в фармацевтически приемлемую упаковку, содержащая в терапевтически эффективном количестве состав, включающий фонтурацетам и, по меньшей мере, одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат и их оптические изомеры и фармацевтически приемлемые соли, фармацевтическую композицию по настоящему изобретению или лекарственное средство по настоящему изобретению.
Предметом настоящего изобретения также является применение состава по настоящему изобретению для лечения и/или профилактики ожирения или избыточной массы тела.
Предметом настоящего изобретения также является применение фармацевтической композиции по настоящему изобретению, лекарственного средства по настоящему изобретению или готовой лекарственной формы по настоящему изобретению для лечения и/или профилактики ожирения или избыточной массы тела.
Предметом настоящего изобретения также является способ лечения и/или профилактики ожирения или избыточной массы тела, включающий прием пациентом, имеющим указанное ожирение или избыточную массу тела, фармацевтической композиции по настоящему изобретению, лекарственного средства по настоящему изобретению или готовой лекарственной формы по настоящему изобретению.
Представленные ниже примеры осуществления изобретений иллюстрируют, но не ограничивают заявленную группу изобретений.
Пример 1. Получение фонтурацетама (N-карбамоилметил-4-фенил-2-пирролидона).
Синтез целевого продукта осуществляли по методике [15], в которой использовали способность N-алкилированных эфиров 4-аминомасляной кислоты циклизоваться в N-алкилпирролидин-2-оны.
К раствору 7,50 г (27,6 ммоль) гидрохлорида н-бутилового эфира 4-амино-3-фенилмасляной кислоты и 5,61 г (30,3 ммоль) иодацетамида в 150 мл ДМФА добавляли 19,07 г (82,8 ммоль) K3PO4·H2O и 10 г молекулярных сит 4Å. Полученную суспензию перемешивали при комнатной температуре в течение 24 ч, фильтровали, фильтрат упаривали в вакууме досуха.
Для проведения циклизации полученный в остатке н-бутиловый эфир 4-карбамоилметиламино-3-фенилмасляной кислоты растворяли в 150 мл толуола, к раствору добавляли 2 г (8,68 ммоль) K3PO4·H2O и 0,05 г (0,15 ммоль) Bu4NBr. Суспензию кипятили в течение 2 ч. с обратным холодильником, охлаждали, фильтровали, фильтрат упаривали досуха, осадок промывали водой обессоленной, охлажденной до температуры от 0 до 5ºС. Далее влажный N-карбамоилметил-4-фенил-2-пирролидон сушили при температуре от 60 до 65ºС до потери в массе при высушивании не более 0,5%. Конечный продукт очищали от примесей колоночной хроматографией. Выход 3,55 г (63%). Т. пл. для рацемического продукта 129–130 °C.
Пример 2. Определение содержания 4-фенилпирролидона-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата в составе фонтурацетама.
Состав фонтурацетама исследовали на содержание 4-фенилпирролидона-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата методом ВЭЖХ с использованием стандартов.
Подвижная фаза (ПФ) А. 1,0 мл трифторуксусной кислоты помещали в мерную колбу вместимостью 1000 мл, прибавляли 500 мл воды для хроматографии и перемешивали, затем доводили объем раствора водой для хроматографии до метки и дегазировали любым удобным способом.
Срок годности раствора 1 мес.
Подвижная фаза (ПФ) В. Ацетонитрил для хроматографии.
Испытуемый раствор. Около 750 мг (точная навеска) порошка субстанции фонтурацетама помещали в мерную колбу вместимостью 250 мл, растворяли в 150 мл воды для хроматографии, помещали на ультразвуковую баню и выдерживали в течение 5 мин. Затем после охлаждения до комнатной температуры доводили объем раствора водой для хроматографии до метки и перемешивали. Полученный раствор фильтровали через мембранный фильтр с диаметром пор 0,45 мкм, отбрасывая первые 2 мл фильтрата.
Стандартный раствор (а). Около 25 мг (точная навеска) стандартного образца фонтурацетама помещали в мерную колбу вместимостью 25 мл и растворяли в 15 мл воды для хроматографии, доводили объем раствора этим же растворителем до метки и перемешивали.
Cтандартный раствор (b). 1,0 мл стандартного раствора (а) помещали в мерную колбу вместимостью 25 мл, доводили объем раствора водой для хроматографии до метки и перемешивали. Затем 1,0 мл полученного раствора помещали в мерную колбу вместимостью 20 мл, доводили объем раствора водой для хроматографии до метки и перемешивали.
Таблица 1. Хроматографические условия
Элюирование осуществляли в градиентном режиме в соответствии с таблицей 1.
Таблица 2. Условия элюирования
Хроматографировали стандартный раствор (b) не менее 5 раз. Время регистрации хроматограммы 8 мин. Все пики были хорошо различимы. Время удерживания пика фонтурацетама – около 4,0 мин. Время удерживания пика 4-фенилпирролидона-2 относительно пика фонтурацетама составляет около 1,9, пика 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты – около 1,6 и пика этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата – около 2,4.
Хроматографировали испытуемый раствор и стандартный раствор, получая не менее 3 хроматограмм. При этом не учитывали пики, площади которых составляли менее 30 % площади пика фонтурацетама на хроматограмме стандартного раствора (b).
Пример 3. Получение образцов фонтурацетама, содержащих дополнительные соединения.
Образцы состава фонтурацетама с содержанием 4-фенилпирролидона-2 0,25%, 0,3%, 0,5%, 0,6%, 1,0% и 20,0% мас. были получены из образца, полученного в примере 1, путем добавления к образцу расчетного количества 4-фенилпирролидона-2 и тщательного перемешивания полученного состава.
Образцы состава фонтурацетама с содержанием 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты 0,01%, 0,6%, 1,0% и 20,0% мас. были получены из образца, полученного в примере 1, путем добавления к образцу расчетного количества 2-(2-оксо-4-фенилпирролидин-1-ил) уксусной кислоты и тщательного перемешивания полученного состава.
Образцы состава фонтурацетама с содержанием этил-2-(2-оксо-4-фенилпирролидин-1-ил) ацетат 0,01%, 0,6%, 1,0% и 20,0% мас. были получены из образца, полученного в примере 1, путем добавления к образцу расчетного количества этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата и тщательного перемешивания полученного состава.
Пример 4. Определение кинетики растворения новых составов, включающих фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 4-фенилпирролидон-2, фонтурацетам и 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, и фонтурацетам и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат.
Кинетику растворения нового состава N-карбамоилметил-4-фенил-2-пирролидона, полученного в примере 3, оценивали по содержанию субстанции N-карбамоилметил-4-фенил-2-пирролидона и сравнивали с кинетикой растворения прототипа. Прибор для определения скорости растворения представлял собой трехгорлый сосуд емкостью 1 л. В один из тубусов вводили термометр, в другой – стеклянную трубку для взятия проб и их комплексирования, а в третий – основную деталь прибора – цилиндрическую корзинку высотой 3,6 см и диаметром 2,5 см, сделанную из нержавеющей стали в виде сетки с отверстиями диаметром 40 меш (около 0,351 мм). Корзинка была насажена на ось мотора.
В сосуд наливали растворяющую среду (1000 мл), в данном эксперименте представлявшую собой щелочной раствор панкреатина, что соответствует среде слюны человека и является важным для определения растворимости сублингвальных (ородисперсных) лекарственных форм. Исследуемый образец помещали в цилиндрическую корзинку, которую устанавливали на расстоянии 2 см от дна сосуда.
Температуру растворяющей среды во время опыта поддерживали постоянной (37±0,5°С). Скорость вращения корзинки в среде регулировали с точностью ±5%, она составляла 200 об/мин. Через установленные интервалы времени отбирали для анализа пробы по 1-2 мл для определения содержания растворенного вещества. Взятый объем растворителя тотчас же восполняли новым. Контроль растворения проводили по выбранному компоненту – N-карбамоилметил-4-фенил-2-пирролидону.
Для сравнительных образцов 1-4 использовали 200 мг нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 0,25%, 0,6 %, 1,0% и 20,0% мас. 4-фенилпирролидона-2, соответственно, а для сравнительного образца 5 – 200 мг прототипа.
Для сравнительных образцов 6-9 использовали 200 мг нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 0,01%, 0,6%, 1,0% и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, соответственно.
Для сравнительных образцов 10-13 использовали 200 мг нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 0,01%, 0,6%, 1,0% и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, соответственно.
Температуру растворяющей среды во время опыта поддерживали постоянной (37±0,5°С). Скорость вращения корзинки в среде регулировали с точностью ±5%, она составляла 200 об/мин. Через установленные интервалы времени отбирали для анализа пробы по 1-2 мл для определения содержания лекарственного вещества. Взятый объем растворителя тотчас же восполняли новым.
Полученные результаты в процентах растворенного действующего вещества от максимальной концентрации приведены в таблицах 3-5.
Таблица 3. Кинетика растворения N-карбамоилметил-4-фенил-2-пирролидона с 4-фенилпирролидоном-2
(прототип)
Таблица 4. Кинетика растворения N-карбамоилметил-4-фенил-2-пирролидона с 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислотой
(прототип)
Таблица 5. Кинетика растворения N-карбамоилметил-4-фенил-2-пирролидона этил-2-(2-оксо-4-фенилпирролидин-1-ил) ацетатом
(прототип)
Результаты свидетельствуют о том, что скорость растворения новых составов N-карбамоилметил-4-фенил-2-пирролидона выше, чем скорость растворения прототипа. В частности, время, в течение которого происходит 50 % растворение новых композиций N-карбамоилметил-4-фенил-2-пирролидона, статистически значительно меньше, чем для сравнительного образца прототипа, что может быть особенно полезным для получения таблеток в ородисперсной форме.
Пример 5. Исследование стабильности при хранения нового состава.
Стабильность новых составов N-карбамоилметил-4-фенил-2-пирролидона, полученных в примере 3, оценивали по содержанию субстанции и сравнивали со стабильностью прототипа методом ускоренного старения.
Все образцы хранили в стеклянных флаконах, укупоренных резиновыми пробками с алюминиевыми колпачками, в климатической камере в условия ускоренных испытаний. Содержание действующего вещества определяли методом ВЭЖХ с использованием стандартов.
Метод «ускоренного старения» заключается в выдерживании испытуемого лекарственного средства при температурах и влажности, превышающих температуру и влажность его хранения в процессе обращения. При повышенных температурах, как правило, ускоряются протекающие в лекарственных средствах физико-химические процессы, приводящие со временем к нежелательным изменениям качества. Таким образом, при повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается в сравнении со сроком годности при температуре хранения. Это позволяет значительно сократить время, необходимое для установления срока годности.
По результатам, полученным в процессе «ускоренного старения» лекарственного средства, можно решить также обратную задачу, т.е. установить температуру хранения, обеспечивающую какой-либо заданный срок годности.
Срок годности (С) при температуре хранения (tхр) связан с экспериментальным сроком годности (СЭ) при повышенной температуре экспериментального хранения (tэ) следующей зависимостью:
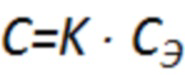 ,
,
где коэффициент соответствия 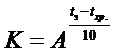
Температурный коэффициент скорости химической реакции (A) принят равным 2,5. Приведенная зависимость основана на правиле Вант-Гоффа о 2-4-кратном росте скоростей химических реакций при увеличении температуры на 10°С.
В соответствии с общей фармакопейной статьей ОФС.1.1.0009.15 значение коэффициента соответствия (K) в зависимости от выбранного температурного интервала ( ), равного 30℃, составляет 15,6. Срок экспериментального хранения при выбранном сроке годности 3 года составляет 71 сутки.
), равного 30℃, составляет 15,6. Срок экспериментального хранения при выбранном сроке годности 3 года составляет 71 сутки.
Статистическую обработку параметров и оформление результатов исследования проводили в соответствии с Правилами надлежащей клинической практики Евразийского экономического союза с помощью статистического пакета SPSS Statistics 19.0.
Показано, что новые составы N-карбамоилметил-4-фенил-2-пирролидона согласно изобретению, а именно: 0,25%, 0,6 %, 1,0% и 20,0% мас. 4-фенилпирролидона-2 (образцы 1-4, соответственно), 0,01%, 0,6%, 1,0% и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты (образцы 6-9, соответственно), и 0,01%, 0,6%, 1,0% и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата (образцы 10-13, соответственно), обладают статистически достоверно увеличенной стабильностью при хранении по сравнению с прототипом. Результаты представлены ниже в таблицах 6-8.
Установлено, что после 71 суток хранения в условиях метода ускоренного старения новые составы N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению обладают статистически достоверно увеличенной стабильностью. Субстанция прототипа остаётся стабильной в течение менее 10 суток, далее содержание N-карбамоилметил-4-фенил-2-пирролидона уменьшается более чем на 4 %. То есть новые составы N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению являются значительно более стабильным при хранении по сравнению с прототипом.
Таблица 6. Оценка стабильности состава с 4-фенилпирролидоном-2 методом ускоренного старения в сравнении с прототипом
Таблица 7. Оценка стабильности состава с 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислотой методом ускоренного старения в сравнении с прототипом
Таблица 8. Оценка стабильности состава с этил-2-(2-оксо-4-фенилпирролидин-1-ил) ацетатом методом ускоренного старения в сравнении с прототипом.
Пример 6. Определение гигроскопичности.
Пониженная гигроскопичность является большим преимуществом новых составов N-карбамоилметил-4-фенил-2-пирролидона при получении и хранении субстанции.
Гигроскопичность оценивали при хранении твердого соединения в камерах с постоянной относительной влажностью при комнатной температуре в течение 96 часов. Сравнение безводных новых составов N-карбамоилметил-4-фенил-2-пирролидона с содержанием 0,25%, 0,6 %, 1,0% и 20,0% мас. 4-фенилпирролидона-2 (образцы 1-4, соответственно), 0,01%, 0,6%, 1,0% и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты (образцы 6-9, соответственно), и 0,01%, 0,6%, 1,0% и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата (образцы 10-13, соответственно) и прототипа при комнатной температуре показало, что прототип является гигроскопичным и обнаруживает большое увеличение влажности, начиная с 60 % относительной влажности. Новые составы N-карбамоилметил-4-фенил-2-пирролидона не обнаруживали никакого существенного увеличения влажности за исключением хранения при относительной влажности выше 90 %. Результаты представлены ниже в таблицах 9-11.
Таблица 9. Оценка гигроскопичности при комнатной температуре (96 ч) состава с 4-фенилпирролидоном-2 в сравнении с прототипом
Таблица 10. Оценка гигроскопичности при комнатной температуре (96 ч) состава с 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислотой в сравнении с прототипом
Таблица 11. Оценка гигроскопичности при комнатной температуре (96 ч) состава с этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетатом в сравнении с прототипом
Пример 7. Исследование общетоксического действия новых составов, включающих фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 20,0% мас. 4-фенилпирролидона-2, фонтурацетам и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, и фонтурацетам и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата.
Цель исследования: определение переносимых, токсических и летальных доз и причин наступления гибели животных, оценка степени повреждающего действия препарата при его длительном введении на мелких лабораторных животных, выявление наиболее чувствительных органов и систем организма и исследование степени обратимости вызываемых повреждений
Изучение острой токсичности:
Материалы и методы:
Изучение острой токсичности заявленного состава, содержащего фонтурацетам и 20,00% мас. 4-фенилпирролидона-2, при однократном внутрижелудочном введении проведено на 20 белых нелинейных мышах-самцах весом 18-20 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Испытывали дозы препарата 180, 250, 320 и 390 мг (по фонтурацетаму)/кг массы тела. На протяжении 14 дней оценивали общее состояние животных. О токсичности препаратов судили по гибели животных и общей картине интоксикации. Статистический анализ выполняли с помощью программного обеспечения Statistica 6.0.
Параметры острой токсичности дали следующие результаты:
DL50 = 418 мг/кг, DL16 = 334 мг/кг, DL84= 581 мг/кг.
Таким образом, исследованный препарат по параметрам острой токсичности по классификации Hodge и Sterner (1943) может быть отнесен к умеренно токсичным соединениям.
Субхроническую токсичность препарата исследовали на 25 белых нелинейных крысах-самцах весом 168-229 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Животным опытных групп в течение 30 дней ежедневно один раз в день вводили исследуемый препарат внутрижелудочно в дозах 6 и 60 мг (по фонтурацетаму)/кг массы тела в виде взвеси в 2% крахмальном геле, что, соответственно, равно и в 10 раз превышает терапевтическую дозу для человека с учетом межвидового пересчета. После окончания эксперимента всех животных умерщвляли для проведения дальнейшего патоморфологического исследования внутренних органов и тканей.
Местно-раздражающее действие оценивали при макроскопическом и микроскопическом исследовании мест введения препаратов – желудочно-кишечного тракта.
Статистическое сравнение опытных и контрольных групп проводили по t-критерию Стьюдента.
Результаты.
В группах животных, получавших внутрижелудочно суспензии исследуемого препарата в дозе 60 мг/кг, наблюдалась тенденция к снижению скорости прироста массы тела. Изученный препарат в дозах 6 и 60 мг/кг не вызывал отклонений биохимических и гематологических показателей. Не наблюдалось изменение суточного диуреза для групп животных, получавших опытный препарат, по отношению к группе контрольных животных, получавших внутрижелудочно 2% крахмальный гель в аналогичном объеме.
Патоморфологическое и микроскопическое исследование внутренних органов свидетельствовало об отсутствии в испытанных дозах выраженных признаков токсического действия препарата на внутренние органы, однако указывало на возможное проявление его местнораздражающего действия на слизистую оболочку желудка после 30 дней внутрижелудочного введения в дозе, в 10 раз превышающей терапевтическую с учетом межвидового пересчета доз.
Аналогично исследовали составы, включающие фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, и фонтурацетам и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата.
В ходе исследования было установлено, что новые составы согласно настоящему изобретению, включающие фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 4-фенилпирролидон-2, фонтурацетам и 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, и фонтурацетам и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат, не проявляют мутагенных свойств в опытах на дрозофилах, не обладают аллергенностью, не обладают репродуктивной токсичностью.
Пример 8. Получение лекарственного средства в форме таблеток.
Смешивали 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг состава фонтурацетама согласно настоящему изобретению, содержащего 0,6 мас.% 4-фенилпирролидона-2, и спрессовывали в брусок. Полученный брусок измельчали в гранулы и просеивали через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетировали в подходящую форму таблетки весом 560 мг каждая.
Пример 9. Получение лекарственного средства в форме таблеток замедленного высвобождения.
В установку для грануляции и сушки технологией псевдоожижения загружали просеянные гидроксипропилметилцеллюлозу низкой вязкости и состав фонтурацетама согласно настоящему изобретению, содержащий 0,1 мас.% 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты и 0,1 мас.% этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата и запускали процесс гранулирования, используя в качестве увлажнителя воду. Процесс сушки продолжали до достижения показателя «потери в массе при высушивании» значения 2,0±0,5 %.
По окончании процесса гранулирования полученный сухой гранулят калибровали через металлическое сито с диаметром отверстий 0,8 мм.
В смеситель барабанного типа загружали просеянную микрокристаллическую целлюлозу, откалиброванный гранулят и просеянную лактозу. Перемешивали в течение 2-4 минут. Затем загружали просеянный тальк, кремния диоксид коллоидный, перемешивали в течение 2-3 минут, затем загружали просеянный магния стеарат, гидроксипропилметилцеллюлозу высокой вязкости, и перемешивали в течение 1-2 минут.
Таблеточную массу прессовали на ротационном прессе, используя пуансоны круглой формы (глубокая сфера) диаметром 8,0 ± 0,2 мм.
Пример 10. Получение лекарственного средства в форме капсул.
Тщательно смешивали состав фонтурацетама согласно настоящему изобретению, содержащий 20% мас.% этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, с порошком лактозы в соотношении 2 к 1. Полученную порошкообразную смесь упаковывали по 300 мг в желатиновые капсулы подходящего размера.
Пример 11. Получение лекарственного средства в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций.
Смешивали 500 мг состава фонтурацетама согласно настоящему изобретению, содержащего 0,5 мас.% 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты и 0,1 мас.% этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, с 300 мг хлорбутанола, 2 мл пропиленгликоля, 4 мл ПАВ Твин-80 и 100 мл инъекционной воды. Полученный раствор фильтровали и помещали по 1 мл в ампулы, которые запаивали.
Пример 12. Исследование анорексигенного действия новых составов, содержащих фонтурацетам согласно настоящему изобретению.
Анорексигенное действие новых составов для лечения и профилактики ожирения, включающих фонтурацетам с содержанием 0,25%, 0,6%, 1,0% и 20,0% мас. 4-фенилпирролидона-2 (образцы 1, 2, 3, 4, соответственно), 0,01%, 0,6%, 1,0% и 20,0% мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты (образцы 6, 7, 8, 9, соответственно), и 0,01%, 0,6%, 1,0% и 20,0% мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата (образцы 10, 11, 12, 13, соответственно) исследовали на модели ожирения алиментарно-конституционального генеза [16]. Образец 5 содержал прототип (содержащий фонтурацетам, но не содержащий аналогов и близкородственных фонтурацетаму соединений – 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты и этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата).
В исследовании использовали 175 самцов крыс линии Вистар, которые получали рацион, содержащий около 70% свиного и говяжьего сала, рыбу, мясо, углеводы ad libitum. Изменение массы тела регистрировали каждые 7-10 дней. Крыс содержали по пять особей в терморегулируемых боксах (с температурой в среднем 21°С) при 12-часовом цикле дня и ночи и с круглосуточным доступом к воде и пище. Откорм животных начинали в месячном возрасте, после того, как их масса тела превысила 50 г [17]. Через 3,5-4 месяца масса тела животных в экспериментальных группах и группе контроля превышала нормальную массу тела крыс, которых кормят лабораторным рационом, более чем на 25%. Именно такая форма ожирения наиболее часто встречается у населения промышленно-развитых стран и обусловлена неправильным питанием на фоне гиподинамии. У всех животных отмечалось снижение двигательной активности, особенно выраженное после приема пищи. Далее крыс делили на 35 групп (34 экспериментальные группы и группа контроля), в каждой группе по 5 животных: образцы 1, 2, 3, 4, 5, 6, 7, 9, 10, 11, 12, 13, получавшие по 100 мг/сутки соответствующего состава, содержащего фонтурацетам, в пересчете на человека, образцы 1, 2, 3, 4, 5, 6, 7, 9, 10, 11, 12, 13, получавшие по 200 мг/сутки соответствующего состава, содержащего фонтурацетам, в пересчете на человека, образцы 2, 5, 7, 11, получавшие по 50 мг/сутки соответствующего состава, содержащего фонтурацетам, в пересчете на человека, образцы 2, 5, 7, 11, получавшие по 250 мг/сутки соответствующего состава, содержащего фонтурацетам, в пересчете на человека, а также группа контроля, получавшая плацебо. Разделение крыс по группам проводили таким образом, чтобы масса тела крыс в пределах группы не отличалась более чем на 5%. Лечение ожирения у крыс осуществляли в течение 45 дней посредством ежедневного перорального введения при помощи зонда составов, содержащих фонтурацетам, в дозировке, соответствующей экспериментальной группе. Животным контрольной группы вводили перорально при помощи зонда плацебо. Крысы экспериментальных и контрольной групп продолжали получать вышеуказанный высококалорийный рацион. Для определения эффективности лечения ожирения животных продолжали взвешивать каждые 7 дней, оценивали их активность в тесте «открытое поле», измеряли количество потребляемого корма, а также проводили биохимические анализы крови. Из уровня техники известны показатели массы тела и биохимические показатели крови у крыс линии Вистар в норме и при ожирении алиментарно-конституционального генеза (таблицы 12-13) [17].
Таблица 12. Белковый состав сыворотки крови при алиментарно-конституциональном ожирении у крыс, М±m
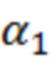
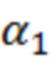 -глобулины
-глобулины
 -глобулины
-глобулины
Таблица 13. Показатели липидного обмена в сыворотке крови при алиментарно-конституциональном ожирении у крыс, М±m




Таким образом, из литературных данных, представленных в таблицах 12-13, были выявлены биохимические показатели крови, которые значимо отличаются у крыс линии Вистар в норме и при ожирении алиментарно-конституционального генеза, а именно количество альбуминов, α2 –глобулинов, β – глобулинов, γ – глобулинов, липопротеинов очень низкой плотности (ЛПОНП), липопротеинов высокой плотности (ЛПВП2). Анорексигенную активность составов, содержащих фонтурацетам, согласно настоящему изобретению оценивали посредством измерения вышеуказанных биохимических показателей в крови животных по сравнению с аналогичной активностью при лечении прототипом (Таблицы 14, 15, 16, 17).
Таблица 14. Биохимические показатели крови у крыс с алиментарно-конституциональным ожирением, получавшим лечение составами, содержащими фонтурацетам, согласно настоящему изобретению в дозировке 100 мг/сутки в пересчете на человека (по сравнению с прототипом).
Таблица 15. Биохимические показатели крови у крыс с алиментарно-конституциональным ожирением, получавшим лечение составами, содержащими фонтурацетам, согласно настоящему изобретению в дозировке 200 мг/сутки в пересчете на человека (по сравнению с прототипом).
Таблица 16. Биохимические показатели крови у крыс с алиментарно-конституциональным ожирением, получавшим лечение составами, содержащими фонтурацетам, согласно настоящему изобретению в дозировке 50 мг/сутки в пересчете на человека (по сравнению с прототипом).
Таблица 17. Биохимические показатели крови у крыс с алиментарно-конституциональным ожирением, получавшим лечение составами, содержащими фонтурацетам, согласно настоящему изобретению в дозировке 250 мг/сутки в пересчете на человека (по сравнению с прототипом).
В процессе лечения у крыс экспериментальных групп, получающих лечение составами, содержащими фонтурацетам, согласно настоящему изобретению наблюдалось статистически значимое снижение аппетита (которое отмечалось по снижению количества потребляемого корма, данные не приведены), и, соответственно, массы тела по сравнению с крысами контрольной группы (в группах, получавшей лечение новыми составами согласно настоящему изобретению в дозе 50 мг/сутки в пересчете на человека снижение массы тела составило порядка 17-20%, в группах, получавших лечение в дозировке 100 мг/сутки – порядка 23-27%, в группах, получавших 200 мг/сутки – порядка 29-33%, и в группах, получавших 250 мг/сутки – порядка 35-38%) и статистически значимое увеличение двигательной активности (в тесте «открытое поле», данные не приведены).
Представленные данные статистически значимо (p<0,05) свидетельствуют о том, что новые составы, содержащие фонтурацетам, согласно настоящему изобретению обладают анорексигенным эффектом, в связи с чем могут использоваться для лечения и/или профилактики ожирения или избыточной массы тела. Кроме того, новые составы согласно настоящему изобретению обладают более высокой анорексигенной активностью, которая обусловлена, по всей видимости, улучшением физико-химических свойств, новых составов по сравнению с прототипом (фонтурацетамом).
Изобретение может быть использовано в медицине, химии, фармакологии и химико-фармацевтической промышленности.
Список литературы
1. Каримов Т.К., Бермаганбетова С.К.: «Факторы вызывающие ожирение и их алиментарная коррекция» // Медицинский журнал Западного Казахстана, № 1-2 (38), 2013, С. 47-51.
2. Беляков Н.А., Мазуров В.И.: «Ожирение. Руководство для врачей» // Санкт-Петербург, 2003, 520 С.
3. Ожирение и избыточный вес. Сайт Всемирной Организации Здравоохранения. https://www.who.int/ru/news-room/fact-sheets/detail/obesity-and-overweight.
4. Бессенен Д.Г., Кушнер Р.: «Избыточный вес и ожирение. Профилактика, диагностика, лечение» // Москва, «Бином», 2004, 240 С.
5. Саакян Ж.М.: «Применение контрастных ванн, ультразвука и синусоидальных модулированных токов в комплексном лечении алиментарно-конституционального ожирения» // автореферат диссертации на соискание ученой степени кандидата медицинских наук, Москва., 2001, 22 С.
6. Пономаренко Г.Н.: «Физиотерапия: национальное руководство // М.: ГЭОТАР-Медиа, 2009, 854 С.
7. Колешко С.В., Дубровщик О.И., Мармыш Г.Г., Довнар И.С.: «Хирургические методы лечения ожирения: реалии и возможности на современном этапе» // Журнал Гродненского государственного медицинского университета, № 2, 2016, С. 5-9.
8. Роик О.В.: «Эффективность консервативного и оперативного методов лечения алиментарно-конституционального ожирения III-IV степени» // автореферат диссертации на соискание ученой степен кандидата медицинских наук, Москва, 1997, 27 С.
9. Лечение алиментарного ожирения, 21.11.2018 // http://dangetv.ru/lechenie-ozhireniya/lechenie-alimentarnogo-ozhireniya.
10. Статья «Фенотропил», Справочник лекарственных препаратов, Интернет-сайт «Регистр лекарственных средств России» Rlsnet.ru, https://www.rlsnet.ru/tn_index_id_27152.htm.
11. Патент РФ № 2050851, опубликованный 27.12.1995.
12. Патент РФ № 2183117, опубликованный 10.06.2002.
13. Патент US № 4144246, опубликованный 13.03.1979.
14. Berge S.M., Bighley L.D., Monkhouse D.C.: «Pharmaceutical Salts» // Journal of Pharmaceutical Sciences, V. 66, № 1, 1977, P. 1-19.
15. Ворона М., Вейнберг Г., Викайнис С., Кузнецов Е., Лебедев А., Пономарёв Ю., Чернобровый А., Звейниеце Л., Дамброва М.: «Новые методы синтеза 2-[(4-R)-2-оксо-4-фенилпирролидин-1-ил]ацетамида ((R)-фенотропила)» // Химия гетероциклических соединений, Т. 48, № 5, 2012, С. 775 – 778.
16. Boroumand-Naini M., Petersen S.A.: «Dietary-induced obesity in rats – effects of a high diets differing in caloricfic density» // The Journal of Physiology, V. 410, 1989, P. 55.
17. Курганова И.А.: «Показатели липидного и белкового обмена крови и состояние клеток печени при экспериментальном ожирении» // Диссертация на соискание ученой степени кандидата медицинских наук, Новосибирск, 2002, 126 С.
18. Михалева О.Г., Бардымова Т.П., Березина М.В.: «Моногенные формы ожирения» // Сибирский медицинский журнал (Иркутск), № 6, 2014, С. 5-11.
19. Романцова Т.И.: «Патогенетический подход к лечению ожирения и сахарного диабета 2 типа» // Ожирение и метаболизм, № 4, 2008, С. 2-10.
20. Романцова Т.И.: «Эпидемия ожирения: очевидные и вероятные причины» // Ожирение и метаболизм, № 1, 20011, С. 5-19.
21. Hebebrand J., Holm J.C., Woodward E., Baker J.L., Blaak E., Durrer Schutz D., Farpour-Lambert N.J., Frühbeck G., Halford J.G.C., Lissner L., Micic D., Mullerova D., Roman G., Schindler K., Toplak H., Visscher T.L.S., Yumuk V.: «A Proposal of the European Association for the Study of Obesity to Improve the ICD-11 Diagnostic Criteria for Obesity Based on the Three Dimensions Etiology, Degree of Adiposity and Health Risk» // Obesity Facts, V. 10, № 4, 2017, Р. 284-307.
22. Хамнуева Л.Ю., Андреева Л.С., Кошикова И.Н.: «Ожирение. Классификация, этиология, патогенез, клиника, диагностика, лечение», Учебное пособие // Иркутск, 2007, 33 С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Новые составы N-карбамоилметил-4-фенил-2-пирролидона | 2018 |
|
RU2699669C1 |
| Новый состав N-карбамоилметил-4-фенил-2-пирролидона | 2017 |
|
RU2696277C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФОНТУРАЦЕТАМА ИЗ ФЕНИБУТА | 2024 |
|
RU2827339C1 |
| ПРОИЗВОДНОЕ 4-ФЕНИЛПИРРОЛИДИНОНА-2, СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ С НООТРОПНОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ НАРУШЕНИЙ НЕРВНОЙ СИСТЕМЫ | 2015 |
|
RU2611623C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА | 2017 |
|
RU2663899C1 |
| Производные 4-фенилпирролидона, обладающие противосудорожной и ноотропной активностью, как средства лечения эпилепсии и пароксизмальных состояний | 2017 |
|
RU2748419C2 |
| Способ крупномасштабного синтеза калиевой соли 2-[2-(2-оксо-4-фенилпирролидин-1-ил)ацетамидо]этансульфокислоты | 2019 |
|
RU2711655C1 |
| Соединения, обладающие антиишемическими, антиангинальными, цитопротективными свойствами, способ их получения и их применение, способ лечения нейродегенеративного заболевания, способ лечения психического расстройства | 2019 |
|
RU2741910C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2524651C1 |
| ФАРМАЦЕВТИЧЕСКИЙ ВОДОРАСТВОРИМЫЙ СОСТАВ ИЗ ДЕЙСТВУЮЩЕГО НАЧАЛА В ВИДЕ N-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА И, ПО МЕНЬШЕЙ МЕРЕ, ОДНОГО ВСПОМОГАТЕЛЬНОГО НЕЙТРАЛЬНОГО ОРГАНИЧЕСКОГО НИЗКОМОЛЕКУЛЯРНОГО КОМПОНЕНТА И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2347565C1 |
Группа изобретений относится к области медицины и фармацевтики. Первый объект представляет собой применение состава, включающего N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и по меньшей мере одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат, их оптические изомеры и их фармацевтически приемлемые соли, для лечения и/или профилактики ожирения или избыточной массы тела. Второй объект - применение фармацевтической композиции, лекарственного средства или готовой лекарственной формы, содержащей(его) в терапевтически эффективном количестве состав. Технический результат заключается в повышении стабильности (времени хранения) состава, повышении скорости растворения, снижении гигроскопичности состава по сравнению с прототипом; расширении арсенала средств, обладающих анорексигенной активностью, для лечения и профилактики ожирения или избыточной массы тела; повышении активности заявленного состава по сравнению с прототипом. 2 н. и 14 з.п. ф-лы, 17 табл., 12 пр.
1. Применение состава, включающего N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и по меньшей мере одно дополнительное соединение, выбранное из группы, включающей 4-фенилпирролидон-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат, их оптические изомеры и их фармацевтически приемлемые соли, для лечения и/или профилактики ожирения или избыточной массы тела, причем упомянутый состав содержит от 0,25 до 1,00 % мас. 4-фенилпирролидона-2, его оптического изомера или его фармацевтически приемлемой соли и/или от 0,01 до 1,00 % мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, ее оптического изомера или ее фармацевтически приемлемой соли и/или от 0,01 до 1,00 % мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, его оптического изомера или его фармацевтически приемлемой соли.
2. Применение по п. 1, характеризующееся тем, что дополнительное соединение представляет собой 4-фенилпирролидон-2 в количестве от 0,25 до 1,00 % мас.
3. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,30 до 0,60 % мас.
4. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,50 до 0,60 % мас.
5. Применение по п. 1, характеризующееся тем, что дополнительное соединение представляет собой 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,01 до 1,00 % мас.
6. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,50 % мас.
7. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит 2-(2-оксо-4-фенилпирролидин-1-ил)уксусную кислоту в количестве от 0,10 до 0,20 % мас.
8. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,01 до 1,00 % мас.
9. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,50 % мас.
10. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетат в количестве от 0,10 до 0,20 % мас.
11. Применение по п. 1, характеризующееся тем, что упомянутый состав содержит фонтурацетам в количестве более 96,00 % мас.
12. Применение по п. 1, характеризующееся тем, что ожирение или избыточная масса тела представляет собой первичное ожирение или избыточную массу тела.
13. Применение по п. 1, характеризующееся тем, что ожирение или избыточная масса тела представляет собой ожирение или избыточную массу тела алиментарно-конституционального генеза.
14. Применение по любому из пп. 1-13, характеризующееся тем, что ожирение или избыточная масса тела обусловлены заболеваниями эндокринной системы, расстройством питания и/или нарушением обмена веществ.
15. Применение по любому из пп. 1-14, характеризующееся тем, что ожирение или избыточная масса тела обусловлены по меньшей мере одним заболеванием, выбранным из группы, состоящей из болезней щитовидной железы, сахарного диабета, нарушений регуляции глюкозы, нарушений внутренней секреции эндокринных желез, недостаточности питания, избыточности питания, нарушений обмена веществ, психических расстройств и расстройств поведения, ожирения или избыточной массы тела, вызванных приемом лекарственных препаратов.
16. Применение фармацевтической композиции, лекарственного средства или готовой лекарственной формы, содержащей(его) в терапевтически эффективном количестве состав, включающий N-карбамоилметил-4-фенил-2-пирролидон (фонтурацетам) и по меньшей мере одно дополнительное соединение, выбранное из фенилпирролидона-2, 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, их оптических изомеров и их фармацевтически приемлемых солей, причем упомянутый состав содержит от 0,25 до 1,00 % мас. 4-фенилпирролидона-2, его оптического изомера или его фармацевтически приемлемой соли и/или от 0,01 до 1,00 % мас. 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, ее оптического изомера или ее фармацевтически приемлемой соли и/или от 0,01 до 1,00 % мас. этил-2-(2-оксо-4-фенилпирролидин-1-ил)ацетата, его оптического изомера или его фармацевтически приемлемой соли, для лечения и/или профилактики ожирения или избыточной массы тела.
| Новые составы N-карбамоилметил-4-фенил-2-пирролидона | 2018 |
|
RU2699669C1 |
| ПРОИЗВОДНЫЕ 2-ОКСО-1-ПИРРОЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2001 |
|
RU2291860C2 |
| RU 2017129085 A, 15.02.2019 | |||
| WO 2015060702 A1, 30.04.2015 | |||
| ZVEJNIECE L | |||
| et al | |||
| S-phenylpiracetam, a selective DAT inhibitor, reduces body weight gain without influencing locomotor activity // Pharmacology Biochemistry and Behavior | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| - V | |||
| Счетная линейка для вычисления объемов земляных работ | 1919 |
|
SU160A1 |
| - P | |||
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
Авторы
Даты
2020-09-14—Публикация
2019-08-30—Подача