Изобретение относится к области медицины, фармакологии и химико-фармацевтической промышленности, а именно новому составу, содержащему N-карбамоилметил-4-фенил-2-пирролидон и 4-фенилпирролидон-2,, фармацевтической композиции на основе упомянутого состава и лекарственному средству на основе упомянутой фармацевтической композиции.
Ноотропы, они же нейрометаболические стимуляторы - лекарственные средства, предназначенные для оказания специфического воздействия на высшие психические функции мозга. Считается, что ноотропы способны стимулировать умственную деятельность, активизировать когнитивные функции, улучшать память и увеличивать способность к обучению. Предполагается, что ноотропы увеличивают устойчивость мозга к разнообразным вредным воздействиям, таким как чрезмерные нагрузки или гипоксия.
К ноотропным лекарственным средствам нового поколения относится препарат с МНН Фонтурацетам (N-карбамоил-метил-4-фенил-2-пирролидон), который зарегистрирован и разрешен к промышленному производству Минздравом России в 2003 г. В отличие от других ноотропов, он имеет наиболее широкий спектр фармакологической активности [Патент РФ №2539375, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ ТАБЛЕТКИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, 20.01.2015].
Фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) давно и прочно зарекомендовал себя как эффективный препарат для лечения заболеваний ЦНС различного генеза, особенно связанных с сосудистыми заболеваниями и нарушениями обменных процессов в мозге, интоксикацией (в частности, при посттравматических состояниях и явлениях хронической цереброваскулярной недостаточности), сопровождающихся ухудшением интеллектуально-мнестических функций, снижением двигательной активности; лечения невротических состояний, проявляющихся вялостью, повышенной истощаемостью, снижением психомоторной активности, нарушением внимания, ухудшением памяти; лечения нарушения процесса обучения; лечения депрессии легкой и средней степени тяжести; лечения психоорганических синдромов, проявляющихся интеллектуально-мнестическими нарушениями и апатико-абулическими явлениями, а также вялоапатических состояний при шизофрении; лечения судорожных состояний; лечения ожирения (алиментарно-конституционального генеза); профилактики гипоксии, повышения устойчивости к стрессу; коррекции функционального состояния организма в экстремальных условиях профессиональной деятельности с целью предупреждения развития утомления и для повышения умственной и физической работоспособности; коррекции суточного биоритма, при инверсии цикла сон-бодрствование; для лечения хронического алкоголизма (с целью уменьшения явлений астении, депрессии, интеллектуально-мнестических нарушений) [Статья «Фенотропил», Справочник лекарственных препаратов Rlsnet.ru, https://www.rlsnet.ru/tn_index_id_27152.htm].
Фонтурацетам обладает выраженным антиамнестическим действием, оказывает прямое активирующее влияние на интегративную деятельность головного мозга, способствует консолидации памяти, улучшает концентрацию внимания и умственную деятельность, облегчает процесс обучения, повышает скорость передачи информации между полушариями головного мозга и устойчивость тканей мозга к гипоксии и токсическим воздействиям, обладает противосудорожным действием и анксиолитической активностью, регулирует процессы активации и торможения ЦНС, улучшает настроение [Патент РФ №2050851, ВЕЩЕСТВО, ПРОЯВЛЯЮЩЕЕ НООТРОПНУЮ АКТИВНОСТЬ, 27.12.1995]; оказывает положительное влияние на обменные процессы и кровообращение мозга, стимулирует окислительно-восстановительные процессы, повышает энергетический потенциал организма за счет утилизации глюкозы, улучшает регионарный кровоток в ишемизированных участках мозга [Патент РФ №2183117, СРЕДСТВО ДЛЯ НОРМАЛИЗАЦИИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ, 10.06.2002]; повышает содержание норадреналина, дофамина и серотонина в мозге, не влияет на уровень содержания ГАМК, не связывается с ГАМКА и ГАМКВ рецепторами, не оказывает заметного влияния на спонтанную биоэлектрическую активность мозга; проявляет умеренно выраженный стимулирующий эффект, проявляющийся в отношении двигательных реакций, повышении физической работоспособности, выраженном антагонизме каталептическому действию нейролептиков, а также ослаблении выраженности снотворного действия этанола и гексобарбитала; проявляет адаптогенное действие в повышении устойчивости организма к стрессу в условиях чрезмерных психических и физических нагрузок, при утомлении, гипокинезии и иммобилизации, при низких температурах; стимулирует выработку антител в ответ на введение антигена, что указывает на иммуностимулирующие свойства, но в то же время не способствует развитию гиперчувствительности немедленного типа и не изменяет аллергическую воспалительную реакцию кожи, вызванную введением чужеродного белка; не обладает тератогенными, мутагенными, канцерогенными и эмбриотоксичными свойствами; имеет низкую токсичность.
Умеренный психостимулирующий эффект препарата сочетается с анксиолитической активностью, он улучшает настроение, оказывает некоторый анальгезирующий эффект, повышая порог болевой чувствительности. На фоне приема препарата отмечено улучшение зрения, которое проявляется в увеличении остроты, яркости и полей зрения [Статья «Фенотропил», Справочник лекарственных препаратов Rlsnet.ru, https://www.rlsnet.ru/tn_index_id_27152.htm].
Из уровня техники известна фармацевтическая композиция, обладающая ноотропной активностью, включающая в качестве действующего вещества N-карбамоил-метил-4-фенил-2-пирролидон [Патент РФ №2240783, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ НООТРОПНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, 27.11.2004].
Из уровня техники известна фармацевтическая композиция в форме таблетки, обладающая ноотропной и нейромодуляторной активностью, характеризующаяся тем, что включает в качестве субстанции активного начала N-карбамоилметил-4-фенил-2-пирролидон, обладающая антидепрессивной активностью [Патент РФ №2232578, ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ, 20.07.2004].
Из уровня техники известна фармацевтическая композиция, обладающая ноотропным действием, в виде раствора для инъекций, содержащая фенотропил и воду для инъекций, отличающаяся тем, что она дополнительно содержит 2-гидроксипропил-β-циклодекстрин [Патент РФ №2414898, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ, ОБЛАДАЮЩАЯ НООТРОПНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, 27.03.2011].
Из уровня техники известна фармацевтическая композиция в форме раствора для инъекций, обладающая ноотропной и нейромодуляторной активностью, характеризующаяся тем, что она включает в качестве активного начала N-карбамоилметил-4-фенил-2-пирролидон, в качестве вспомогательных веществ гидроксиэтилкрахмал 200/0.5 и воду для инъекций [Патент РФ №2524651, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, 27.07.2014].
Из уровня техники известна фармацевтическая композиция в форме таблетки, содержащая N-карбамоил-метил-4-фенил-2-пирролидон и вспомогательные компоненты, отличающаяся тем, что она содержит в качестве вспомогательных компонентов моногидрат лактозы, карбоксиметилцеллюлозу, поливинилпирролидон и соль стеариновой кислоты [Патент РФ №2560691, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ОСНОВЕ К-КАРБАМОИЛА-МЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА, 20.08.2015].
Из уровня техники также известен состав (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)ацетамида, обладающему модуляторной активностью с соразмерным влиянием, способ получения фармацевтической субстанции, отличающийся тем, что полученное сырье подвергают очистке, кристаллизации, стабилизации путем обработки состава деминерализованной водой и изотермической кристаллизации из пропанола с последующей сушкой, что обеспечивает увеличение эффективности, безопасности, стабильности и широты терапевтического применения [Патент РФ №2480214, СОСТАВ, ОБЛАДАЮЩИЙ МОДУЛЯТОРНОЙ АКТИВНОСТЬЮ С СОРАЗМЕРНЫМ ВЛИЯНИЕМ, ФАРМАЦЕВТИЧЕСКАЯ СУБСТАНЦИЯ (ВАРИАНТЫ), ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ, ФАРМАЦЕВТИЧЕСКАЯ И ПАРАФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКИХ СОСТАВОВ, 27.04.2013].
Широкий спектр фармакологической активности N-карбамоил-метил-4-фенил-2-пирролидона служит основанием для его клинического применения. Таким образом, N-карбамоил-метил-4-фенил-2-пирролидон является средством с уникальным спектром фармакологического действия, вытекающим из его активности.
Авторы настоящего изобретения неожиданно обнаружили, что новый состав, включающий фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 4-фенилпирролидон-2, имеет лучшие свойства, чем N-карбамоил-метил-4-фенил-2-пирролидон (он же 2-(4-Фенил-2-оксо-1-пирролидинил)ацетамид), используемый в фармацевтической промышленности в настоящее время, именуемый в дальнейшем «прототип».
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное начало» (лекарственная субстанция, лекарственное вещество) означает физиологически активное вещество синтетического или иного (биотехнологического, растительного, животного, микробного и прочего) происхождения, обладающее фармакологической активностью и являющееся активным началом фармацевтической композиции, используемой для производства и изготовления лекарственного препарата (средства).
«Лекарственное средство (препарат)» - вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя новый состав N-карбамоил-метил-4-фенил-2-пирролидона и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или приготовлены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, малеаты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные (Подробное описание свойств таких солей дано в Berge S.M., et al., "Pharmaceutical Salts" // J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты - лизин, орнитин и аргинин.
Задачей настоящего изобретения является разработка стабильного при хранении, негигроскопичного, хорошо растворимого, экономически целесообразного, промышленно реализуемого, препаративного состава фонтурацетама (N-карбамоил-метил-4-фенил-2-пирролидона).
Стабильность в твердом состоянии и срок хранения активных компонентов являются очень важными факторами. Лекарственное соединение и композиции, включающие его, должны обладать способностью храниться в течение значительных периодов времени, не проявляя значительного изменения физико-химических свойств активного компонента (например, его химического состава, плотности, гигроскопичности и растворимости).
Таким образом, авторы изобретения неожиданно обнаружили, что присутствие небольшого количества 4-фенилпирролидона-2 в субстанции фонтурацетама улучшает некоторые свойства субстанции фонтурацетама.
Технические результаты настоящего изобретения:
- повышение стабильности (времени хранения) состава по сравнению с фонтурацетамом,
- повышение скорости растворения состава по сравнению с фонтурацетамом,
- снижение гигроскопичности состава по сравнению с фонтурацетамом,
- расширение арсенала средств, обладающих ноотропной активностью.
Поставленная задача решается, а технический результат достигается получением нового состава, который включает фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 4-фенилпирролидон-2, отличающийся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве не более 1,00% мас.
Более предпочтительным является состав, включающий 4-фенилпирролидон-2 в количестве от 0,05 до 1,00% мас.
Еще более предпочтительным является состав, включающий 4-фенилпирро-лидон-2 в количестве 0,30-0,60% мас.
Еще более предпочтительным является состав, включающий 4-фенилпирролидон-2 в количестве 0,50-0,60% мас.
Также в предпочтительном варианте осуществления изобретения состав содержит фонтурацетам в количестве более 96,00% мас. и индивидуальные сопроводительные идентифицированные и не идентифицированные примеси в суммарном количестве менее 3,00% мас., более предпочтительно, менее 2% мас., еще более предпочтительно, менее 1% мас., еще более предпочтительно, менее 0,5% мас.
Еще одним объектом данного изобретения является новый фармацевтическая композиция, обладающая ноотропной активностью, которая содержит терапевтически эффективное количество упомянутого состава, включающего фонтурацетам и 4-фенилпирролидон-2, по меньшей мере, один фармацевтически приемлемый носитель.
Еще одним объектом данного изобретения является лекарственное средство, обладающее ноотропной активностью, в виде таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, содержащее упомянутую фармацевтическую композицию, которая содержит терапевтически эффективное количество упомянутого состава, включающего фонтурацетам и 4-фенилпирролидон-2, по меньшей мере, один фармацевтически приемлемый носитель.
Фармацевтические композиции могут включать фармацевтически приемлемые эксципиенты. Под фармацевтически приемлемым эксципиентами подразумеваются применяемые в сфере фармацевтики разбавители, вспомогательные агенты и/или носители. Фармацевтическая композиция наряду с составом, включающим фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 4-фенилпирролидон-2, по настоящему изобретению может включать и другие активные субстанции, в том числе обладающие активностью, при условии, что они не вызывают нежелательных эффектов.
При необходимости использования фармацевтической композиции по настоящему изобретению в клинической практике она может смешиваться с традиционными фармацевтическими носителями.
Носители, используемые в фармацевтических композициях по настоящему изобретению, представляют собой носители, которые применяются в сфере фармацевтики для получения распространенных форм, в частности, в пероральных формах используются связующие вещества, смазывающие агенты, дезинтеграторы, растворители, разбавители, стабилизаторы, суспендирующие агенты, корригенты вкуса; в формах для инъекций используются антисептические агенты, солюбилизаторы, стабилизаторы; в местных формах используются основы, разбавители, смазывающие агенты, антисептические агенты.
Предметом данного изобретения также является лекарственное средство, обладающее ноотропной активностью, в виде таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, содержащее в терапевтически эффективном количестве состав, включающий фонтурацетам и 4-фенилпирролидон-2 в количестве от 0,05 до 1,00% мас., или фармацевтическую композицию по настоящему изобретению.
Лекарственные средства могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка средства, содержащего новый состав N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению, у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов в организме, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 10-500 мг, предпочтительно - 50-300 мг. Поэтому во время приготовления из фармацевтической композиции лекарственного средства по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 10-500 мг нового состава N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению, предпочтительно - 50-300 мг. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно - от одного до шести раз).
Представленные ниже примеры осуществления изобретений иллюстрируют, но не ограничивают заявленную группу изобретений.
Примеры осуществления изобретений
Пример 1. Получение фонтурацетама
4-амино-3-фенилмасляной кислоты гидрохлорид загружают в реактор с изопропиловым спиртом, перемешивают 5-10 минут, загружают эквимолярное количество триэтиламина. Реакционную массу нагревают при перемешивании до температуры от 80 до 85°C и выдерживают при данной температуре и перемешивании от 20 до 30 минут. По окончании выдержки подвижную суспензию фильтруют, осадок промывают горячим изопропиловым спиртом, отжимают и сушат при температуре от 60 до 65°C до потери в массе при высушивании не более 0,5%.
Высушенную 4-амино-3-фенилмасляную кислоту сплавляют при температуре от 140 до 145°C при перемешивании. Перемешивание ведут до полного растворения. Далее раствор нагревают до температуры от 140 до 160°C и выдерживают от 30 до 35 минут, отключают нагрев, перемешивают до температуры в массе от 95 до 100°C.
В сплав загружают воду обессоленную, продолжают перемешивание до температуры не более 30°C.
Далее массу охлаждают в холодильной камере до температуры не более 5°C, фильтруют, полученный 4-фенил-2-пирролидинон промывают водой обессоленной и сушат при температуре от 35 до 40°C до постоянного веса.
В реакторе нагревают натрий металлический в растворе толуола и спирта изопропилового до температуры от 98 до 101°C, выдерживают при перемешивании от 1 до 1,5 часов, загружают 4-фенил-2-пирролидинон и перемешивают 1 час, массу охлаждают до температуры от 20 до 25°C, загружают катализатор (ТЭБАХ), перемешивают от 10 до 15 минут, затем загружают этилхлорацетат, не допуская повышения температуры более 26°C.
Полученную суспензию выдерживают при перемешивании 2 часа и передают на фильтрацию, осадок тщательно отжимают, промывают толуолом, раствор упаривают на роторном испарителе «до окончания погона».
Полученный N-этоксикарбонилметил-4-фенилпирролидон-2 загружают в предварительно охлажденный до температуры не выше -10°C водный раствор аммиака и перемешивают 24 часа.
Охлажденную до температуры не более -10°C подвижную суспензию фильтруют, осадок промывают водой обессоленной, охлажденной до температуры от 0 до 5°C. Влажный (RS)-2-(2-оксо-4-фенилпирролидин-1-ил)-ацетамида сушат при температуре от 60 до 65°C до потери в массе при высушивании не более 0,5%.
Пример 2. Определение содержания 4-фенилпирролидона-2 в составе фонтурацетама.
Полученный в Примере 1 состав исследовали на содержание 4-фенилпирролидона-2 методом ВЭЖХ с использованием стандартов.
Подвижная фаза (ПФ) А. 1,0 мл трифторуксусной кислоты помещают в мерную колбу вместимостью 1000 мл, прибавляют 500 мл воды для хроматографии и перемешивают, затем доводят объем раствора водой для хроматографии до метки и дегазируют любым удобным способом.
Срок годности раствора 1 мес.
Подвижная фаза (ПФ) В. Ацетонитрил для хроматографии.
Испытуемый раствор. Около 750 мг (точная навеска) порошка субстанции фенотропила помещают в мерную колбу вместимостью 250 мл, растворяют в 150 мл воды для хроматографии, помещают на ультразвуковую баню и выдерживают в течение 5 мин. Затем после охлаждения до комнатной температуры доводят объем раствора водой для хроматографии до метки и перемешивают. Полученный раствор фильтруют через мембранный фильтр с диаметром пор 0,45 мкм, отбрасывая первые 2 мл фильтрата.
Стандартный раствор (a). Около 25 мг (точная навеска) стандартного образца фонтурацетама помещают в мерную колбу вместимостью 25 мл и растворяют в 15 мл воды для хроматографии, доводят объем раствора этим же растворителем до метки и перемешивают.
Стандартный раствор (b). 1,0 мл стандартного раствора (a) помещают в мерную колбу вместимостью 25 мл, доводят объем раствора водой для хроматографии до метки и перемешивают. 1,0 мл полученного раствора помещают в мерную колбу вместимостью 20 мл, доводят объем раствора водой для хроматографии до метки и перемешивают.

Элюирование осуществляется в градиентном режиме в соответствии с таблицей 1.
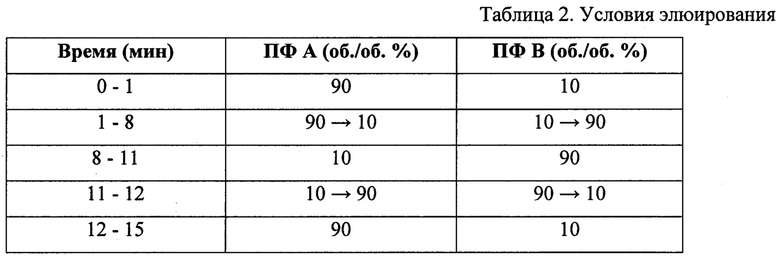
Хроматографируют стандартный раствор (b) не менее 5 раз. Время регистрации хроматограммы 8 мин. Время удерживания пика фонтурацетама - около 4,0 мин. Времена удерживания пика 4-фенилпирролидона-2 относительно пика фонтурацетама около 1,09.
Хроматографируют испытуемый раствор и стандартный раствор, получая не менее 3 хроматограмм. Не учитывают пики, площади которых составляет менее 30% площади пика фонтурацетама на хроматограмме стандартного раствора (b).
Пример 3. Получение образцов фонтурацетама, содержащих 0,05%, 0,3%, 0,6%, 1,0% мас. 4-фенилпирролидона-2.
Образцы состава фонтурацетама с содержанием 4-фенилпирролидона-2 0,05%, 0,3%, 0,5%, 0,6% и 1,0% мас. были получены из образца, полученного в примере 1, путем добавления к образцу расчетного количества 4-фенилпирролидона-2 и тщательного перемешивания полученного состава.
Пример 4. Определение кинетики растворения нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 4-фенилпирролидон-2.
Кинетику растворения нового состава N-карбамоилметил-4-фенил-2-пирролидона, полученного в примере 3, оценивают по содержанию субстанции N-карбамоилметил-4-фенил-2-пирролидона и сравнивают с кинетикой растворения прототипа. Прибор для определения скорости растворения представляет собой трехгорлый сосуд емкостью 1 л. В один из тубусов вводят термометр, в другой - стеклянную трубку для взятия проб и их комплексирования, а в третий - основную деталь прибора - цилиндрическую корзинку высотой 3,6 см и диаметром 2,5 см, сделанную из нержавеющей стали в виде сетки с отверстиями диаметром 40 меш (около 0,351 мм). Корзинка насажена на ось мотора.
В сосуд наливают растворяющую среду (1000 мл), в данном эксперименте щелочной раствор панкреатина, что соответствует среде слюны человека и является важным для определения растворимости сублингвальных (ородисперсных) лекарственных форм. Исследуемый образец помещают в цилиндрическую корзинку, которую устанавливают на расстоянии 2 см от дна сосуда.
Температуру растворяющей среды во время опыта поддерживают постоянной (37±0,5°C). Скорость вращения корзинки в среде регулируют с точностью ±5%, она составляет 200 об/мин. Через установленные интервалы времени отбирают для анализа пробы по 1-2 мл для определения содержания растворенного вещества. Взятый объем растворителя тотчас же восполняют новым. Контроль растворения проводят по выбранному компоненту - N-карбамоилметил-4-фенил-2-пирролидону.
Для сравнительных образцов 1-3 используют 200 мг нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 0,05%, 0,6% и 1,0% мас. 4-фенилпирролидона-2, соответственно, а для сравнительного образца 4-200 мг прототипа.
Температуру растворяющей среды во время опыта поддерживают постоянной (37±0,5°C). Скорость вращения корзинки в среде регулируют с точностью ±5%, она составляет 200 об/мин. Через установленные интервалы времени отбирают для анализа пробы по 1-2 мл для определения содержания лекарственного вещества. Взятый объем растворителя тотчас же восполняют новым.
Полученные результаты в процентах растворенного действующего вещества от максимальной концентрации приведены в таблице 3.
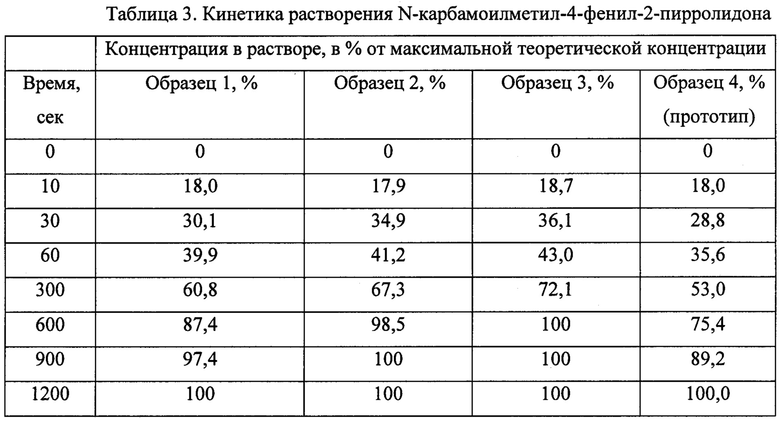
Результаты демонстрируют, что скорость растворения нового состава N-карбамоилметил-4-фенил-2-пирролидона выше, чем скорость растворения прототипа. В частности, время, в течение которого происходит 50% растворение новой композиции N-карбамоилметил-4-фенил-2-пирролидона, статистически значительно меньше, чем для сравнительного образца прототипа, что может быть особенно полезным для получения таблеток в ородисперсной форме.
Пример 5. Исследование стабильности при хранения нового состава
Стабильность нового состава N-карбамоилметил-4-фенил-2-пирролидона, полученного в примере 3, оценивают по содержанию субстанции (снижается за счет образования примеси 2-(2-оксо-4-фенилпирролидин-1-ил)уксусной кислоты, являющейся продуктом дезамидирования фонтурацетама), и сравнивают со стабильностью прототипа методом ускоренного старения.
Все образцы хранились в стеклянных флаконах, укупоренных резиновыми пробками с алюминиевыми колпачками, в климатической камере в условия ускоренных испытаний. Содержание действующего вещества определяют методом ВЭЖХ с использованием стандартов.
Метод «ускоренного старения» заключается в выдерживании испытуемого лекарственного средства при температурах и влажности, превышающих температуру и влажность его хранения в процессе обращения. При повышенных температурах, как правило, ускоряются протекающие в лекарственных средствах физико-химические процессы, приводящие со временем к нежелательным изменениям качества. Таким образом, при повышенной температуре промежуток времени, в течение которого контролируемые показатели качества лекарственного средства сохраняются в допустимых пределах (экспериментальный срок годности), искусственно сокращается в сравнении со сроком годности при температуре хранения. Это позволяет значительно сократить время, необходимое для установления срока годности.
По результатам, полученным в процессе «ускоренного старения» лекарственного средства, можно решить также обратную задачу, т.е. установить температуру хранения, обеспечивающую какой-либо заданный срок годности.
Срок годности (C) при температуре хранения (txp) связан с экспериментальным сроком годности (CЭ) при повышенной температуре экспериментального хранения (tэ) следующей зависимостью:
C=K⋅CЭ,
где коэффициент соответствия 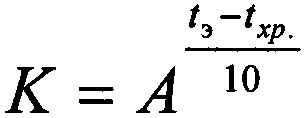 .
.
Температурный коэффициент скорости химической реакции (А) принят равным 2,5. Приведенная зависимость основана на правиле Вант-Гоффа о 2-4-кратном росте скоростей химических реакций при увеличении температуры на 10°C.
В соответствии с общей фармакопейной статьей ОФС.1.1.0009.15 значение коэффициента соответствия (K) в зависимости от выбранного температурного интервала (tэ-tхр), равного 30°C, составляет 15,6. Срок экспериментального хранения при выбранном сроке годности 3 года составляет 71 сутки.
Статистическую обработку параметров и оформление результатов исследования проводят в соответствии с Правилами надлежащей клинической практики Евразийского экономического союза с помощью статистического пакета SPSS Statistics 19.0.
Показано, что новый состав N-карбамоилметил-4-фенил-2-пирролидона согласно изобретению (содержит 0,05%, 0,60% и 1,00% мас. 4-фенилпирролидона-2, образцы 1-3, соответственно) обладает статистически достоверно увеличенной стабильностью при хранении по сравнению с прототипом.
Установлено, что после 71 суток хранения в условиях метода ускоренного старения новый состав N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению обладает статистически достоверно увеличенной стабильностью. Субстанция прототипа остается стабильной в течение менее 10 суток, далее содержание N-карбамоилметил-4-фенил-2-пирролидона уменьшается почти на 3%. То есть новый состав N-карбамоилметил-4-фенил-2-пирролидона по настоящему изобретению является значительно более стабильным при хранении по сравнению с прототипом.

Пример 6. Определение гигроскопичности.
Пониженная гигроскопичность является большим преимуществом нового состава N-карбамоилметил-4-фенил-2-пирролидона при получении и хранении субстанции.
Гигроскопичность оценивали при хранении твердого соединения в камерах с постоянной относительной влажностью при комнатной температуре в течение 96 часов. Сравнение безводных нового состава N-карбамоилметил-4-фенил-2-пирролидона с содержанием 0,05%, 0,6% и 1,0% мас. 4-фенилпирролидона-2 (образцы 1-3, соответственно) и прототипа при комнатной температуре показало, что прототип является гигроскопичным и обнаруживает большое увеличение влажности, начиная с 60% относительной влажности. Новый состав N-карбамоилметил-4-фенил-2-пирролидона не обнаруживает никакого существенного увеличения влажности за исключением хранения при относительной влажности выше 90%. Результаты представлены ниже в таблице 5.
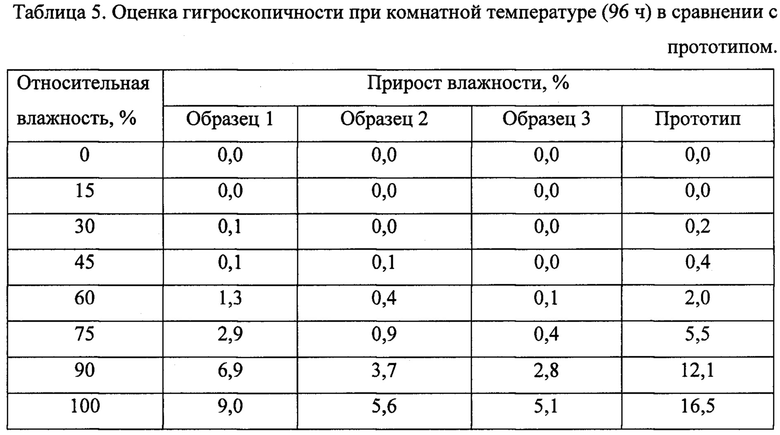
Пример 7. Исследование общетоксического действия нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 4-фенилпирролидон-2.
Цель исследования: определение переносимых, токсических и летальных доз и причин наступления гибели животных, оценка степени повреждающего действия препарата при его длительном введении на мелких лабораторных животных, выявление наиболее чувствительных органов и систем организма и исследование степени обратимости вызываемых повреждений
Изучение острой токсичности:
Материалы и методы:
Изучение острой токсичности заявленного состава, содержащего фонтурацетам и 1,00% мас. 4-фенилпирролидона-2, при однократном внутрижелудочном введении проведено на 20 белых нелинейных мышах-самцах весом 18-20 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Испытывали дозы препарата 180, 250, 320 и 390 мг (по фонтурацетаму)/кг массы тела. На протяжении 14 дней оценивали общее состояние животных. О токсичности препаратов судили по гибели животных и общей картине интоксикации. Статистический анализ выполнялся с помощью программного обеспечения Statistica 6.0.
Параметры острой токсичности дали следующие результаты:
DL50=418 мг/кг, DL16=334 мг/кг, DL84=581 мг/кг.
Таким образом, исследованный препарат по параметрам острой токсичности по классификации Hodge и Sterner (1943) может быть отнесен к умеренно токсичным соединениям.
Субхроническую токсичность препарата исследовали на 25 белых нелинейных крысах-самцах весом 168-229 г, содержащихся в стандартных условиях вивария со свободным доступом к воде и корму. Животным опытных групп в течение 30 дней ежедневно один раз в день вводили исследуемый препарат внутрижелудочно в дозах 6 и 60 мг (по фонтурацетаму)/кг массы тела в виде взвеси в 2% крахмальном геле, что соответственно, равно и в 10 раз превышает терапевтическую дозу для человека с учетом межвидового пересчета. После окончания эксперимента всех животных умерщвляли для проведения дальнейшего патоморфологического исследования внутренних органов и тканей.
Местно-раздражающее действие оценивали при макроскопическом и микроскопическом исследовании мест введения препаратов - желудочно-кишечного тракта.
Статистическое сравнение опытных и контрольных групп проводили по t-критерию Стьюдента.
Результаты.
В группах животных, получавших внутрижелудочно суспензии исследуемого препарата в дозе 60 мг/кг, наблюдалась тенденция к снижению скорости прироста массы тела, незначительное, но достоверное увеличение активности трансаминаз крови и снижение спонтанной двигательной активности животных. Изученный препарат в дозах 6 и 60 мг/кг не вызывал отклонений биохимических и гематологических показателей. Не наблюдалось изменения суточного диуреза для групп животных, получавших опытный препарат, по отношению к группе контрольных животных, получавших внутрижелудочно 2% крахмальный гель в аналогичном объеме.
Патоморфологическое и микроскопическое исследование внутренних органов свидетельствуют об отсутствии в испытанных дозах выраженных признаков токсического действия препарата на внутренние органы, однако указывают на возможное проявление его местнораздражающего действия на слизистую оболочку желудка после 30 дней внутрижелудочного введения в дозе, в 10 раз превышающей терапевтическую с учетом межвидового пересчета доз.
Заявленный новый состав, включающий фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 1,00% мас. 4-фенилпирролидона-2, не проявляет мутагенных свойств в опытах на дрозофилах, не обладает аллергенностью, не обладает репродуктивной токсичностью.
Пример 8. Получение лекарственного средства в форме таблеток. Смешивают 1600 мг крахмала, 1600 мг измельченной лактозы, 400 мг талька и 1000 мг состава фонтурацетама согласно настоящему изобретению и спрессовывают в брусок. Полученный брусок измельчают в гранулы и просеивают через сита, собирая гранулы размером 14-16 меш. Полученные гранулы таблетируют в подходящую форму таблетки весом 560 мг каждая.
Пример 9. Получение лекарственного средства в форме капсул. Тщательно смешивают состав фонтурацетама согласно настоящему изобретению с порошком лактозы в соотношении 2 к 1. Полученную порошкообразную смесь упаковывают по 300 мг в желатиновые капсулы подходящего размера.
Пример 10. Получение лекарственного средства в форме инъекционных композиций для внутримышечных, внутрибрюшинных или подкожных инъекций. Смешивают 500 мг состава фонтурацетама согласно настоящему изобретению с 300 мг хлорбутанола, 2 мл пропиленгликоля и 100 мл инъекционной воды. Полученный раствор фильтруют и помещают по 1 мл в ампулы, которые запаивают.
Пример 11. Исследование антиамнестической активности.
Антиамнестическую активность нового состава, включающего фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидона) и 1,00% мас. 4-фенилпирролидона-2, исследуют на модели условного рефлекса пассивного избегания (УРПИ) у самцов крыс линии Wistar массой 180-250 г. Для этого используют установку "Passive avoidence" фирмы "Lafauette instrument company" (США), состоящую из камеры с электродным полом, освещенной гильотинообразно закрывающимся отверстием с ярко освещенной платформой. Для выработки УРПИ крысу помещают на платформу хвостом к отверстию в камеру с электродным полом. В течение 180 с регистрируют латентное время первого захода животного в камеру. Через 3 мин после помещения животного в камеру в момент, когда животное находилось в ней, а не на платформе, отверстие закрывают и наносят через пол неустранимое электроболевое раздражение (8 электроимпульсов амплитудой 0,5 мА и длительностью 1 с каждый, интервал между импульсами 2 с). После этого животное извлекают из камеры. Сохранность УРПИ проверяют через 24 ч после его выработки, помещая крысу на платформу установки таким же образом, как и при обучении. В течение 180 с регистрируют латентное время первого захода в камеру. Если крыса не заходит в нее, латентное время считали равным 180 с.
В качестве амнестических факторов используют электросудорожный шок (ЭСШ 120 В, 300 мс), наносимый через корниальные электроды непосредственно после выработки УРПИ, или скополамин, вводимый подкожно в дозе 1 мг/кг за 60 мин до выработки УРПИ.
Новый состав фонтурацетама в дозе 25, 50 и 100 мг/кг, препарат сравнения пирацетам в дозе 100 и 300 мг/кг или 0,9%-ный раствор натрия хлорида вводят внутрибрюшинно за 45 мин до обучения.
Как следует из данных, приведенных в таблице 6, использование нового состава N-карбамоилметил-4-фенил-2-пирролидона снижает выраженность постконвульсионной ретроградной амнезии. Выраженность эффекта проявляет прямую зависимость от дозы. Пирацетам проявляет антиамнестический эффект в дозе не менее 300 мг/кг, превышающей минимальную выявленную антиамнестическую дозу нового состава N-карбамоилметил-4-фенил-2-пирролидона (25 мг/кг) в 12 раз. Помимо этого, новый состав N-карбамоилметил-4-фенил-2-пирролидона в дозах от 25 до 100 мг/кг снижает выраженность амнезии, вызванной скополамином. При этом в указанных минимальных дозах новый состав N-карбамоилметил-4-фенил-2-пирролидона увеличивает латентный период захода в "опасную" камеру в 4,5 раза по сравнению с латенцией захода в нее амнезированных ЭСШ крыс, которым был введен не препарат, а изотонический раствор натрия хлорида. Следовательно, антиамнестический эффект нового состава фонтурацетама выше, и он эффективен в меньших дозах, чем пирацетам.

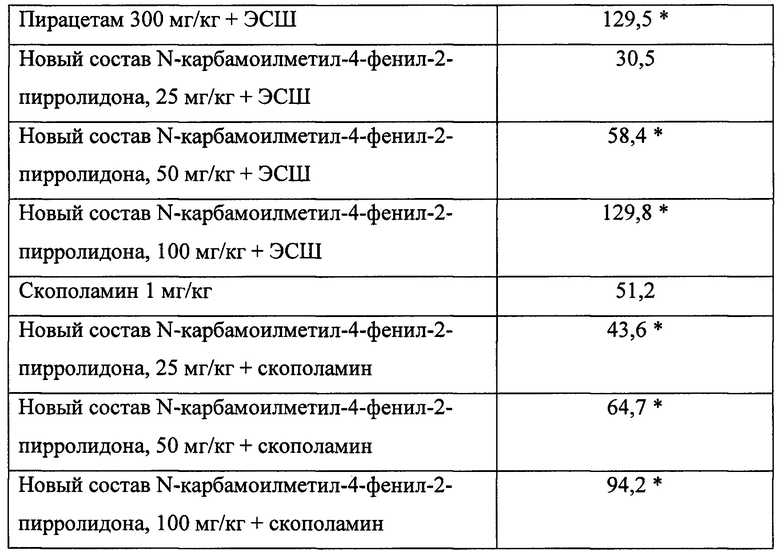
* - p<0,05 по сравнению с группой «Натрия хлорид + ЭСШ»
Изобретение может быть использовано в медицине, химии, фармакологии и химико-фармацевтической промышленности.
| название | год | авторы | номер документа |
|---|---|---|---|
| Новые составы N-карбамоилметил-4-фенил-2-пирролидона | 2018 |
|
RU2699669C1 |
| НОВЫЕ СОСТАВЫ N-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОЖИРЕНИЯ | 2019 |
|
RU2732245C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ РАСТВОРА ДЛЯ ИНЪЕКЦИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2524651C1 |
| ПРОИЗВОДНОЕ 4-ФЕНИЛПИРРОЛИДИНОНА-2, СОДЕРЖАЩАЯ ЕГО КОМПОЗИЦИЯ С НООТРОПНОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ НАРУШЕНИЙ НЕРВНОЙ СИСТЕМЫ | 2015 |
|
RU2611623C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ФОРМЕ ТАБЛЕТКИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2013 |
|
RU2539375C1 |
| СРЕДСТВО ДЛЯ НОРМАЛИЗАЦИИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ И СПОСОБ ЛЕЧЕНИЯ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ | 2000 |
|
RU2183117C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА | 2017 |
|
RU2663899C1 |
| СРЕДСТВО ДЛЯ ПОВЫШЕНИЯ УРОВНЯ НЕЙРОТРОФИЧЕСКОГО ФАКТОРА ГОЛОВНОГО МОЗГА (BDNF) В МОДЕЛИ ХРОНИЧЕСКОГО НЕПРЕДСКАЗУЕМОГО УМЕРЕННОГО СТРЕССА | 2023 |
|
RU2836915C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОНТУРАЦЕТАМА ИЗ ФЕНИБУТА | 2024 |
|
RU2827339C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ НООТРОПНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2003 |
|
RU2240783C1 |
Изобретение относится к медицине, в частности к составу, фармацевтической композиции и лекарственному средству, обладающему ноотропной активностью. Заявленный состав содержит N-карбамоилметил-4-фенил-2-пирролидон и 4-фенилпирролидон-2. Осуществление изобретения позволяет получить фармацевтическую композицию и лекарственное средство, обладающее повышенной стабильностью по сравнению с фонтурацетамом, повышенной скоростью растворения и сниженной гигроскопичностью. 3 н. и 2 з.п. ф-лы, 6 табл., 11 пр.
1. Состав, обладающий ноотропной активностью, включающий фонтурацетам (N-карбамоилметил-4-фенил-2-пирролидон) и 4-фенилпирролидон-2 в количестве от 0,3 до 1,00% мас.
2. Состав по п. 1, отличающийся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,30 до 0,60% мас.
3. Состав по п. 2, отличающийся тем, что упомянутый состав содержит 4-фенилпирролидон-2 в количестве от 0,50 до 0,60% мас.
4. Фармацевтическая композиция, обладающая ноотропной активностью, отличающаяся тем, что упомянутая композиция содержит в терапевтически эффективном количестве состав по любому из пп. 1-3 и, по меньшей мере, один фармацевтически приемлемый носитель.
5. Лекарственное средство, обладающее ноотропной активностью, в виде таблеток, капсул или инъекций, помещенных в фармацевтически приемлемую упаковку, отличающееся тем, что упомянутое средство содержит фармацевтическую композицию по п. 4.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| et al | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Прибор для вычерчивания участков параболы | 1923 |
|
SU776A1 |
| НОВАЯ ПРЕПАРАТИВНАЯ ФОРМА ВЕЩЕСТВА, ОБЛАДАЮЩЕГО НООТРОПНОЙ И НЕЙРОМОДУЛЯТОРНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2007 |
|
RU2327458C1 |
| СОСТАВ, ОБЛАДАЮЩИЙ МОДУЛЯТОРНОЙ АКТИВНОСТЬЮ С СОРАЗМЕРНЫМ ВЛИЯНИЕМ, ФАРМАЦЕВТИЧЕСКАЯ СУБСТАНЦИЯ (ВАРИАНТЫ), ПРИМЕНЕНИЕ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ, ФАРМАЦЕВТИЧЕСКАЯ И ПАРАФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКИХ СОСТАВОВ | 2011 |
|
RU2480214C1 |
Авторы
Даты
2019-08-01—Публикация
2017-08-15—Подача