Область изобретения
В целом настоящее изобретение относится к новым аспектам медицинской практики, способам лечения и фармацевтическим композициям. Более конкретно, настоящее изобретение относится к применению вальпроевой кислоты (VPA) и ее фармацевтически приемлемых солей для лечения или профилактики образования тромбов и улучшения или нормализации эндогенного сосудистого фибринолиза.
Уровень техники
Как представляется, перечень или обсуждение предыдущего опубликованного документа в этом описании не обязательно должны быть приняты в качестве подтверждения того, что настоящий документ является частью уровня техники или общеизвестной информацией.
Сердечно-сосудистые заболевания являются основной причиной заболеваемости и смертности в западном мире, а в последние десятилетия также стали проблемой, приобретающей актуальность в развивающихся странах. По оценкам, 80 миллионов взрослых американцев (каждый третий) имеют одно или более проявлений сердечно-сосудистых заболеваний (СС3), таких как гипертензия, ишемическая болезнь сердца, сердечная недостаточность или инсульт. Данные о смертности показывают, что СС3 являлись основной причиной смерти в 35% всех смертей в 2005 году в Соединенных Штатах, в большинстве своем связанные с инфарктом миокарда, инсультом или их осложнениями. Для подавляющего большинства пациентов с острыми сердечно-сосудистыми патологиями характерно предшествующее воздействие по меньшей мере одного из основных факторов риска, таких как курение, измененные уровни липидов в крови, гипертензия, диабет, абдоминальное ожирение и неспецифическое воспаление.
С патофизиологической точки зрения, основные проявления инфаркта миокарда и ишемического инсульта обусловлены внезапной блокадой питательного кровоснабжения из-за образования сгустка крови в просвете артериального сосуда. В большинстве случаев, образование тромба провоцируется разрывом легко повреждаемой атеросклеротической бляшки, в результате чего запускается каскад химических реакций с веществами, активирующими тромбоциты и систему плазменной коагуляции. Активированные тромбоциты образуют тромбоцитарную пробку, содержащую генерируемый коагуляцией фибрин, необходимый для формирования сгустка, который расширяется в просвете сосуда до возникновения обструкции или блокирования потока крови, что приводит к гипоксическому поражению тканей (так называемому инфаркту). Таким образом, тромботические сердечно-сосудистые поражения происходят в результате двух различных процессов: медленно прогрессирующего длительного атеросклероза сосудистой стенки, с одной стороны, и внезапного острого образования сгустка, который стремительно блокирует поток крови, с другой стороны. Не желая быть связанными с теорией, полагают, что настоящее изобретение исключительно относится к последнему процессу.
В последнее время в качестве важного фактора риска тромбообразования было признано воспаление. Сосудистое воспаление является характерной особенностью стенки сосуда, пораженной атеросклерозом, при этом воспалительная активностью является определяющим фактором подверженности атеросклеротической бляшки к разрыву и активации внутрисосудистого свертывания. Кроме того, аутоиммунные состояния с системным воспалением, такие как ревматоидный артрит, системная красная волчанка и различные формы васкулитов, существенно повышают риск развития инфаркта миокарда и инсульта.
Традиционные подходы к профилактике и лечению сердечно-сосудистых заболеваний направлены на: 1) замедление прогрессирования основного атеросклеротического процесса; 2) предотвращение свертывания крови в случае разрыва бляшки; или 3) непосредственное удаление тромботической массы, вызвавшей обструкции сосуда. Вкратце, антиатеросклеротическое лечение направлено на модулирование влияния общих факторов риска и включает рекомендации по питанию, снижение веса, физические упражнения, отказ от курения, лечение для нормализации уровня холестерина и кровяного давления и т.д.
Профилактика образования сгустка в основном основана на применении антитромбоцитарных препаратов, ингибирующих активацию и/или агрегацию тромбоцитов, но и необязательно включает прием пероральных антикоагулянтов, таких как варфарин, направленных на предотвращение тромбоэмболических осложнений. Апостериорное лечение острых атеротромбозных патологий требует либо непосредственного фармакологического лизиса тромба с помощью тромболитических средств, таких как рекомбинантный тканевой активатор плазминогена, либо чрезкожной механической дилатации сосуда с обструкцией.
Несмотря на то, что многоцелевая антиатеросклеротическая терапия и профилактика образования сгустка с помощью антиагрегантов снижают частоту инфаркта миокарда и ишемического инсульта, указанные патологии по-прежнему остаются одной из основных проблем здравоохранения. Эти данные показывают, что для пациентов с сердечнососудистыми факторами риска таких профилактических мер недостаточно для полного предотвращения возникновения атеротромбоза.
Аналогично, тромботические состояния в венозном русле, а также тромбоэмболические осложнения, такие как эмболия легочной артерии, по-прежнему являются причиной значительного уровня заболеваемости и смертности. Венозный тромбоз характеризуется различными клиническими проявлениями, при этом относительная значимость активации тромбоцитов по сравнению с плазменной коагуляцией несколько отличается, с преобладанием последней в развитии венозного тромбоза. Тем не менее, несмотря на эти различия, указанные основные механизмы, которые вызывают тромботические окклюзии сосудов аналогичны тем, которые наболюдаются в артериальном русле кровообращения. Кроме того, риск венозного тромбоза, хотя и не ассоциирован с атеросклерозом напрямую, связан с общими факторами риска сердечно-сосудистых заболеваний, такими как воспаление и метаболические нарушения.
В своей совокупности, существующая терапия и общее управление факторами риска предлагают недостаточную защиту от тромбообразования, как в артериальном, так и в венозном русле, и не могут вызвать обратное развитие тяжелых последствий таких нарушений. Это создает необходимость в разработке новых профилактических и терапевтических мишеней, особенно более эффективных подходов, которые могли бы предотвратить опасную ишемию тканей, и предпочтительно на ранней безсимптомной стадии заболевания.
Представляет интерес обнаруженный тот факт, что с другой стороны у здорового индивидуума существует естественная система "последней линии обороны", которая может быть активирована, если процесс свертывания крови, несмотря на профилактические меры, все-таки развивается в сосудистой сети. Вкратце, инициирование тромботического механизма как в артериальном, так и в венозном русле приводит к активации внутреннего клеточного слоя кровеносного сосуда (эндотелия), при этом клетка, незамедлительно реагируя, высвобождает большие количества вещества, растворяющего сгусток - тканевого активатора плазминогена (t-PA). Это повышает уровни просветного t-PA до уровней, наблюдаемых при медикаментозной тромболитической терапии (т.е. введения рекомбинантного t-PA), но эффективность этой эндогенной реакции в 100 раз выше, в связи с чрезвычайно быстрым началом действия.
Накопленные клинические, эпидемиологические и экспериментальные данные поддерживают предположение о том, что если эта тромбропротективная функция стенки кровеносных сосудов не нарушена, она обеспечивает мощную защиту от формирования тромбов, препятствующих потоку крови. К сожалению, однако, способность к незамедлительному высвобождению t-PA нарушается при некоторых патологических состояниях с повышенной склонностью к тромбообразованию. К таким состоянием относятся атеросклероз, гипертензия, абдоминальное ожирение, курение, малоподвижный образ жизни и неспецифическое воспаление. Это ухудшение, скорее всего, связано с уменьшением синтеза и, следовательно, снижением активности активатора фибринолиза в эндотелиальных клетках.
Кроме того, наши данные и результаты других исследователей продемонстрировали, что эффективность реакции эндогенного фибринолиза снижается у пациентов с повышенным риском атеротромботической патологии, такой как атеросклероз (Osterlund, В., et al. Acta Anaesthesiol Scand 52, 1375-1384 (2008), Newby, D.E., et al. Circulation 103, 1936-1941 (2001). Последние данные свидетельствуют о том, что воспаление может быть основным патогенетическим механизмом, лежащим в основе сниженной продукции t-PA при указанном состоянии. Мы продемонстрировали, что длительное воздействие на воспалительные цитокины: фактор некроза опухоли альфа (ФНО-альфа) и интерлейкин-1 бета (ИЛ-1b), обуславливает существенное подавление транскрипции t-PA (Ulfhammer, Е., et al. Journal of Thrombosis and Haemostasis 4, 1781-1789 (2006), Larsson, P., et al. Thromb Res 123, 342-351 (2008). Вызывает интерес тот известный факт, что атеросклеротические бляшки ассоциируются с местным, потенциально серьезным, воспалительным процессом в сосудистой стенке; при этом можно предположить, что эта воспалительная среда препятствует фибринолитическим реакциям в тех конкретных участках сосудистой системы, где это имеет решающее значение для поддержания высокой фибринолитической активности, тем самым увеличивая риск тромбообразования. Аналогичным образом, также кажется вероятным, что увеличение числа случаев тромботических осложнений у пациентов с системными воспалительными патологиями (например, аутоиммунными заболеваниями и метаболическим синдромом), также может быть связано с супрессивным действием циркулирующих провоспалительных цитокинов на синтез t-PA и/или повышенными уровнями ингибитора активатора плазминогена 1 (PAI-1).
Ввиду вышеизложенного, альтернативным четвертым подходом, направленным на снижение частоты клинических случаев тромботических патологий, должно быть восстановление потенциала фибринолитической системы "последней линии обороны" у пациентов с нарушением ее функции. Предприняты значительные усилия для обнаружения возможных способов повышения параметров исходного, а также стимулированного эндогенного фибринолиза у субъектов со сниженой фибринолитической активностью, ассоциированной с факторами риска. Однако предыдущие попытки, направленные на повышение синтеза t-PA, например, с помощью статинов и ретиноевой кислоты, оказались неудачными. Другие способы повышения фибринолиза путем блокирования естественных ингибиторов активности t-PA, таких как ингибитор активатора плазминогена-1 (PAI-1) и карбоксипептидаза U (CPU), также оказались безуспешными, главным образом, из-за их ограничений как возможных лекарственных препаратов, таких как неудовлетворительные фармакокинетические свойства препаратов-кандидатов.
Фибринолитическую активность t-P подавляется ингибитором активатора плазминогена 1 (PAI-1) посредством комплексообразования с молекулой t-PA. В силу своего антифибринолитического эффекта, PAI-1 уменьшает способность растворять сгустки крови, тем самым увеличивая риск клинических случаев тромботических патологий (Hrafnklsdottir et al, J Thromb Haemost 2004; 2:1960-8).
PAI-1 циркулирует в низких концентрациях в плазме (обычно около 5-10 нг/мл в утренних образцах), но в популяции концентрация PAI-1 в плазме демонстрирует отчетливое смещенное вправо распределение. Как правило, уровни циркулирующего PAI-1 повышаются с возрастом. Повышенные уровни PAI-1 предрасполагают к тромбообразованию. Индивидуально для каждого пациента, уровни выше 100 нг/мл расцениваются как существенный фактор риска развития сердечно-сосудистых заболеваний, даже в отсутствие других типичных факторов риска. Кроме того, повышенные уровни PAI-1 часто регистрируются у пациентов с нарушениями метаболизма, связанными с ожирением, такими как сахарный диабет 2 типа и метаболический синдром.
Уровни циркулирующего PAI-1 демонстрируют выраженные суточные изменения с пиковыми значениями около 06:00 часов и минимальными значениями около 16:00 часов, как показано на Фиг. 1 (см. также, например, Scheer and Shea, Blood 2014). Как и ожидалось, повышение уровня PAI-1 в утренние часы совпадает с временным пиком возникновения тромботических патологий, таких как инфаркт миокарда.
У пациентов с ожирением и/или метаболическим синдромом регистрируются более высокие уровни циркулирующего PAI-1 и повышенные суточные пики, как показано на Фиг. 1. У таких пациентов концентрации в плазме обычно находятся в пределах от 15 до 60 нг/мл в утренних образцах; при этом уровни не являются нормально распределенными и характеризуются ярко выраженной положительной асимметрией. Уровни PAI-1 в плазме от 100 до 500 мг/мл в утренних образцах нередко наблюдаются у пациентов с ожирением и метаболическим синдромом. Таким образом, пациенты с ожирением и/или метаболическим синдромом особенно подвержены риску возникновения тромботических патологий, обусловленных ингибирующим действием PAI-1 на активность t-PA.
Таким образом, представляет интерес профилактика сердечно-сосудистых заболеваний, путем снижения уровня PAI-1, а более конкретно - блокирование утреннего повышения концентрации указанного вещества в плазме. Такой подход позволил бы теоретически получить еще большую эффективность у пациентов с ожирением и/или метаболическим синдромом.
В настоящее время мы неожиданно обнаружили, что вальпроевая кислота (VPA) потенциально снижает уровни PAI-1 в плазме с соответствующим снижением активности PAI-1 до такой степени, что обеспечивает возможность повышения активности эндогенного t-PA. Следовательно, введение VPA в низких дозах таким образом, что уровни VPA или ее метаболитов в плазме совпадают с пиковыми уровнями PAI-1 в плазме, позволяет достичь полезного эффекта при лечении или профилактике патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов.
В WO 2012/120262 обсуждается применение вальпроевой кислоты с целью улучшения или нормализации процесса эндогенного фибринолиза, нарушенного в результате местного или системного воспаления. Тем не менее, в указанной публикации нет указаний на то, что VPA может ингибировать действие PAI-1 и, следовательно, нет предположений о введении VPA с целью противодействия (т.е. уменьшения) пиковым уровням PAI-1, таким образом, обеспечивая лечение (т.е. оптимизированное лечение) патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов.
В публикации US 2007/0232528 A1 описаны составы с контролируемым высвобождением, включающие вальпроевую кислоту для применения в лечении заболеваний, таких как рак. Эти публикации не предполагают введение VPA с Целью противодействия пиковым уровням PAI-1, для лечения патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов, и поэтому не предлагают составы, предназначенные для указанного применения.
Описание изобретения
Настоящее изобретение относится к процессу деградации или распада фибрина (также называемому фибринолизом), а более конкретно - к композициям и способам для лечения патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов (например, тромбообразованием).
В частности, настоящее изобретение относится к способам применения вальпроевой кислоты или ее фармацевтически приемлемых солей в лечении или профилактике патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов.
Настоящее изобретение также относится к фармацевтическим композициям, составленным таким образом, чтобы замедлить высвобождение вальпроевой кислоты или ее фармацевтически приемлемых солей, что в результате обеспечивает пригодность указанных композиций для применения в таких способах.
Терапевтические способы лечения
Как описано в настоящем документе, было обнаружено, что вальпроевая кислота или ее фармацевтически приемлемые соли способны ингибировать активность PAI-1 (например, путем снижения уровней РАМ), который сам по себе является ингибитором t-PA. Поэтому, вальпроевая кислота или ее фармацевтически приемлемые соли способны усиливать действие t-PA и, следовательно, пригодны для применения в лечении или профилактике патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов.
В частности, авторы настоящего изобретения неожиданно обнаружили, что у субъектов-людей, получавших VPA, снижались уровни циркулирующего РАI-1. У здоровых мужчин после лечения VPA уровни циркулирующего PAI-1 в плазме существенно снижались - более чем на 50%, а у пациентов с коронарным атеросклерозом - на около 45%, последствия чего дополнительно описаны в Примере 1 настоящего документа.
Тот факт, что лечение с применением VPA снижает уровни PAI-1 в плазме у пациентов-мужчин был неожиданным, учитывая, что данные in vitro, полученные в результате культивирования эндотелиальных клеток (одного из основных продуцентов плазменного PAI-1) не продемонстрировали снижение уровней мРНК PAI-1 после лечения VPA, наоборот, отмечали небольшое, но достоверное увеличение продукции PAI-1 на 30%. В этих исследованиях также не обнаружили каких-либо эффектов VPA на плазменные модели PAI-1 in vivo у свиней (Svennerholm et al., PLoS One. 2014 May 12;9(5):e97260. doi: 10.1371/journal.pone.0097260. eCollection 2014) или у мышей (неопубликованные данные).
В первом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В альтернативном первом аспекте настоящего изобретения предлагается применение вальпроевой кислоты или ее фармацевтически приемлемой соли для изготовления лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В дополнительном альтернативном первом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, имеющего для этого показания; причем способ включает введение по меньшей мере одной дозы терапевтически эффективного количества вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
Специалисту в данной области техники будет понятно, что ссылки в настоящем документе на варианты реализации конкретных аспектов настоящего изобретения будут включать ссылки на все другие варианты реализации этих аспектов настоящего изобретения. Таким образом, любой один или более вариантов реализации любого аспекта настоящего изобретения могут быть объединены с любым одним или более другими такими вариантами реализации изобретения для того, чтобы сформировать более конкретные варианты реализации изобретения без отступления от описания настоящего изобретения, представленного в данном документе.
В настоящем документе ссылки на патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, будут относиться, в частности, к патологическим состояниям, связанным с образованием тромбов.
В конкретном варианте реализации первого аспекта настоящего изобретения, максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В другом конкретном варианте реализации первого аспекта настоящего изобретения, максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В более конкретном варианте реализации первого аспекта настоящего изобретения, максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) и до достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
Во втором аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10 (например, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
В альтернативном втором аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для изготовления лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
В дополнительном альтернативном втором аспекте настоящего изобретения предлагается способ лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина у пациента, имеющего для этого показания, при этом указанное лечение включает введение по меньшей мере одной терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
Во избежание неоднозначности толкования, специалисту в данной области техники будет понятно, что ссылки на соединения по настоящему изобретению, как это предусмотрено в настоящем документе выше, будут применяться ко второму аспекту настоящего изобретения (и альтернативным аспектам и/или их конкретным вариантам реализации) таким же образом, как они применяются ко всем другим аспектам настоящего изобретения, описанным в данном документе (и альтернативным аспектам и/или конкретным вариантам их реализации).
В данном контексте термин "терапевтическое окно" следует понимать как относящийся к плазменным уровням соответствующего соединения или его соли и/или метаболита, при которых, как правило, будет достигаться соответствующий (то есть, проявляемый в обычных условиях) лечебный эффект этого соединения. Термин может относиться к диапазону уровней в плазме или к определенному уровню в плазме.
Используемую в данном описании ссылку на количество на миллилитр (/мл) следует понимать как обозначение количества на миллилитр плазмы (т.е. плазмы крови пациента). Используемую в данном описании ссылку на молярную концентрацию следует понимать, как относящуюся к концентрации в плазме (т.е. в плазме крови пациента).
В альтернативном втором аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента находится в диапазоне ниже от около 50 до около 170 мкг/мл (например, ниже около 50, около 70, около 90, около 110, около 130, около 150 или около 170 мкг/мл).
В дополнительном альтернативном втором аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента составляет по меньшей мере от около 70 до около 700 мкМ (например, по меньшей мере около 70, около 140, около 210, около 280, около 350, около 420, около 490, около 560, около 630 или около 700 мкМ).
В еще одном альтернативном втором аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента находится в диапазоне ниже от около 350 до около 1200 мкМ/мл (например, ниже около 350, около 490, около 630, около 770, около 910, около 1050 или около 1190 мкг/мл).
Во избежание неоднозначности толкования, специалисту в данной области техники будет понятно, что ссылки на определенные максимальные количества и концентрации в плазме во втором аспекте настоящего изобретения могут также потребовать, как минимум, терапевтически эффективного количества в указанном образце плазмы.
В частности, специалисту в данной области техники будет понятно, что ссылки на определенные максимальные (т.е. там, где значения указаны как "ниже") и минимальные (т.е. там, где значения указаны как "по меньшей мере") количества и/или концентрации в плазме могут быть объединены для формирования диапазонов (т.е. при этом количество в плазме находится в диапазоне от минимального значения до максимального значения).
Например, в одном варианте реализации второго аспекта настоящего изобретения пациент имеет концентрацию в плазме вальпроевой кислоты или ее соли и/или метаболита, составляющую от около 10 до 170 мкг/мл.
В других таких вариантах реализации изобретения пациент имеет концентрацию вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющую: от около 10 до около 70 мкг/мл (или от около 50 до около 90, от около 70 до около 110, от около 90 до около 130, от около 110 до около 150, от около 130 до около 170, или от около 150 до около 190 мкг/мл);
от около 10 до около 50 мкг/мл (или от около 10 и до около 100, от около 30 до около, от около 50 до около 170, или от около 70 до около 190 мкг/мл);
от около 30 до около 190 мкг/мл (например, от около 50 до около 170, от около 70 до около 150, от около 90 до около 130, от около 30 до около 110, от около 50 до около 130, или от около 70 до около 170 мкг/мл).
Специалисту в данной области техники будет понятно, что ссылки на определенные минимальные плазменные уровни в данном описании (например, согласно второму аспекту настоящего изобретения) будут включать ссылки на такие уровни в тот период времени, когда у пациента достигается стационарное состояние концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме. Кроме того, специалисту в данной области техники будет понятно, что ссылки на пациента с достигнутым стационарным состоянием концентрации могут относиться к уровням в плазме, достигнутым после лечения указанного пациента соединениями по настоящему изобретению (в их терапевтически эффективной дозе) в течение по меньшей мере от двух до пяти дней (например, по меньшей мере пять дней).
Специалисту в данной области техники также будет понятно, что ссылки на максимальные и минимальные уровни в плазме согласно второму аспекту настоящего изобретения (включая все варианты реализации изобретения и их альтернативные аспекты) могут также применяться к уровням в плазме, наблюдаемым для Cmax вальпроевой кислоты или ее соли и/или метаболита, как это указано в других аспектах настоящего изобретения (например, в первом аспекте настоящего изобретения).
В третьем аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту в течение периода времени от около 20:00 часов до около 06:00 часов.
В альтернативном третьем аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль в изготовлении лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту в течение периода времени от около 20:00 часов до около 06:00 часов.
В дополнительном альтернативном третьем аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, имеющего для этого показания, при этом способ включает введение пациенту терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение периода времени от около 20:00 часов до около 06:00 часов.
В конкретном варианте реализации третьего аспекта настоящего изобретения, лечение включает введение пациенту терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение периода времени от около 21:00 часов до около 05:00 часов (например, от около 22:00 часов до около 04:00 часов).
Специалисту в данной области техники будет понятно, что определения периодов времени с применением 24-часовой системы также могут относиться к определению периодов времени с применением 12-часовой системы (т.е. AM и РМ обознают периоды времени до и после 12:00, соответственно). Так, например, 20:00 также может быть указано как 8:00 РМ (8:00 вечера), а 6:00 также может быть указано как 06:00 AM (6:00 утра).
В конкретном варианте реализации третьего аспекта настоящего изобретения (в частности, когда для лечения применяют фармацевтическую композицию, состав которой не предусматривает замедленное высвобождение активного ингредиента), лечение включает введение пациенту терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение периода времени от около 02:00 часов до около 06:00 часов (например, от около 03:00 часов до около 05:00 часов, например, около 4:00 часов).
В другом конкретном варианте реализации третьего аспекта настоящего изобретения (в частности, когда для лечения применяют фармацевтическую композицию, состав которой предусматривает замедленное высвобождение активного ингредиента согласно описанному в восьмом аспекте настоящего изобретения), лечение включает введение пациенту терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение периода времени от около 20:00 часов до около 00:00 часов (например, от около 21:00 часов до около 23:00 часов, например, около 22:00 часов).
В альтернативных вариантах реализации третьего аспекта настоящего изобретения, лечение включает введение пациенту терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение периода времени, определенного на основе профиля высвобождения указанного состава для того, чтобы обеспечить концентрациию в плазме вальпроевой кислоты или ее соли и/или метаболита, как это требуется согласно первому и/или второму аспекту настоящего изобретения.
Как описано в настоящем документе, специалист в данной области техники сможет определить, каким образом вводить соединения по настоящему изобретению (например, в течение определенного периода времени), чтобы достичь параметров, описанных в настоящем документе (таких, как те, которые описаны в первом и втором аспектах изобретения).
Во избежание неоднозначности толкования, в конкретных вариантах реализации третьего аспекта настоящего изобретения доза означает однократную дозу, которая указывает, что доза является только дозой соединения, полученного пациентом в течение (например, соответствующего) 24-часового периода.
В четвертом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение пациенту фармацевтической композиции, содержащей дозу вальпроевой кислоты или ее фармацевтически приемлемой соли за один раз и в такой форме, чтобы по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождалась из композиции в течение периода времени от около 02:00 часов до около 06:00 часов.
В альтернативном четвертом аспекте настоящего изобретения предлагается применение вальпроевой кислоты или ее фармацевтически приемлемой соли в изготовлении лекарственного средства для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов; при этом указанное лечение включает введение пациенту фармацевтической композиции, содержащей дозу вальпроевой кислоты или ее фармацевтически приемлемой соли за один раз и в такой форме, чтобы по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождалась из композиции в течение периода времени от около 02:00 часов до около 06:00 часов.
В дополнительном альтернативном четвертом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, у пациента, имеющего для этого показания; при этом указанное лечение включает введение пациенту фармацевтической композиции, содержащей терапевтически эффективную дозу вальпроевой кислоты или ее фармацевтически приемлемой соли за один раз и в такой форме, чтобы по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождалась из композиции в течение периода времени от около 02:00 часов до около 06:00 часов.
В конкретном варианте реализации четвертого аспекта настоящего изобретения, лечение включает введение пациенту фармацевтической композиции, содержащей терапевтически эффективную дозу вальпроевой кислоты, или ее фармацевтически приемлемой соли за один раз и в такой форме, чтобы по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождалась из композиции в течение периода времени от около 03:00 часов до около 05:00 часов (например, от около 04:00 часов до около 05:00 часов, например, в около 05:00 часов).
В конкретном варианте реализации четвертого аспекта настоящего изобретения лечение включает введение фармацевтической композиции, как описано в восьмом аспекте настоящего изобретения в данном документе ниже (включая все варианты его реализации).
В пятом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, при этом указанное лечение включает:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме;
(ii) введение пациенту по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме.
В альтернативном пятом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль в изготовлении лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, при этом указанное лечение включает:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение пациенту по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме.
В еще одном альтернативном пятом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, имеющего для этого показания; при этом способ включает следующие этапы:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение пациенту по меньшей мере одной терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме.
Как описано в настоящем документе, концентрации PAI-1 в плазме можно контролировать с помощью методик, хорошо известных специалистам в данной области техники. Так, например, уровни PAI-1, как правило, измеряются в плазме. Кровь можно собирать шприцом из локтевой вены через одинаковые промежутки времени, например, каждый час, каждый второй час или каждый третий час в течение 24 часов. Образцы крови незамедлительно центрифугируют с целью отделения плазмы от сыворотки. После этого определяют уровень PAI-1 в плазме с использованием коммерчески доступных наборов ELISA, таких как Coaliza® PAI-1 (Chromogenix), TriniLIZE® PAI-1 (Trinity Biotech), Imubind® Plasma PAI-1 (American Diagnostica), Zymutest PAI-1 (Hyphen Biomed), Milliplex PAI-1 (MerckMillipore), набор Elisa для человека Novex PAI-1 (Life technology), набор ELISA для человека PAI1 (SERPINE1) (Abcam, ab108891).
В конкретном варианте реализации пятого аспекта настоящего изобретения, максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до (например, за три часа, например, за 2 часа или за 1 час или за 0,5 часа) и до достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В другом конкретном варианте реализации пятого аспекта настоящего изобретения, максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В более конкретном варианте реализации пятого аспекта настоящего изобретения максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) и до достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
Специалисту в данной области техники будет понятно, что временные характеристики и уровень Cmax VPA будут зависеть от вводимой дозы (и, в некоторой степени, от формы, в которой эту дозу вводят). Специалист в данной области сможет измерить концентрацию VPA или метаболита и/или ее соли в плазме, а также определить временные характеристики и уровень Cmax (и, при необходимости, корректировать дозу и форму VPA, соответственно). Конкретные дозы (т.е. терапевтические дозы) VPA, которые могут вводится, и уровни Cmax, которые могут быть получены, включают те, которые описаны в настоящем документе.
В шестом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, при этом указанное лечение включает:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
В альтернативном шестом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль в изготовлении лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, при этом указанное лечение включает:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
В еще одном альтернативном шестом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, имеющего для этого показания; при этом способ включает следующие этапы:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение по меньшей мере одной терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в тот период времени, когда у пациента отмечается максимальная концентрация PAI-1 в плазме (Cmax); при этом у пациента регистрируются концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющие по меньшей мере от около 10 до около 100 мкг/мл, например, по меньшей мере около 10, по меньшей мере около 20, около 30, приблизительно 40, около 50, около 60, около 70, около 80, около 90 или около 100 мкг/мл).
В альтернативном шестом аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента находится в диапазоне ниже от около 50 до около 170 мкг/мл (например, ниже около 50, около 70, около 90, около 110, около 130, около 150 или около 170 мкг/мл).
В дополнительном альтернативном шестом аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента составляет по меньшей мере от около 70 до около 700 мкМ (например, по меньшей мере около 70, около 140, около 210, около 280, около 350, около 420, около 490, около 560, около 630 или около 700 мкМ).
В еще одном альтернативном шестом аспекте настоящего изобретения концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме пациента находится в диапазоне ниже от около 350 до около 1200 мкМ/мл (например, ниже около 350, около 490, около 630, около 770, около 910, около 1050 или около 1190 мкг/мл).
Во избежание неоднозначности толкования, специалисту в данной области техники будет понятно, что ссылки в данном описании на уровни и концентрации "вальпроевой кислоты или ее соли и/или метаболита" (например, уровни в плазме и концентрации в плазме) относятся, в частности, к уровням и концентрациям вальпроевой кислоты (например, уровням в плазме и концентрациям в плазме).
Более того, специалисту в данной области техники будет понятно, что ссылки на определенные максимальные количества и концентрации в плазме в шестом аспекте настоящего изобретения могут также потребовать, как минимум, терапевтически эффективного количества в указанном образце плазмы. Более того, специалисту в данной области техники будет понятно, что ссылки на определенные максимальные (т.е. там, где значения указаны как "ниже") и минимальные (т.е. там, где значения указаны как "по меньшей мере") количества и/или концентрации в плазме могут быть объединены для формирования диапазонов (т.е., при этом количество в плазме находится в диапазоне от минимального значения до максимального значения).
Например, в одном варианте реализации второго аспекта настоящего изобретения пациент имеет концентрацию вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющую от около 10 до 170 мкг/мл. В других таких вариантах реализации изобретения пациент имеет концентрацию вальпроевой кислоты или ее соли и/или метаболита в плазме, составляющую:
от около 10 до около 70 мкг/мл (или от около 50 до около 90, от около 70 до около 110, от около 90 до около 130, от около 110 до около 150, от около 130 до около 170, или от около 150 до около 190 мкг/мл);
от около 10 до около 50 мкг/мл (например, от около 10 и до около 100, от около 30 до около, от около 50 до около 170, или от около 70 до около 190 мкг/мл);
от около 30 до около 190 мкг/мл (например, от около 50 до около 170, от около 70 до около 150, от около 90 до около 130, от около 30 до около 110, от около 50 до около 130, или от около 70 до около 170 мкг/мл).
В седьмом аспекте настоящего изобретения предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение пациенту одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение 24 часов, причем доза составляет от около 50 мг до около 1000 мг (например, от около 200 мг до около 600 мг).
В альтернативном седьмом аспекте настоящего изобретения предлагается применение вальпроевой кислотой или ее фармацевтически приемлемой соли в изготовлении лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение пациенту одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение 24 часов, причем доза составляет от около 50 мг до около 1000 мг (например, от около 200 мг до около 600 мг).
В дополнительном седьмом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, у пациента, имеющего для этого показания; при этом указанное лечение включает введение пациенту одной терапевтически эффективной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение 24 часов, причем доза составляет от около 50 мг до около 1000 мг (например, от около 200 мг до около 600 мг).
Если не указано или не очевидно из контекста иное (например, при рассмотрении характеристик конкретного состава), ссылки на дозу соединений по настоящему изобретению (например, дозу вальпроевой кислоты или ее фармацевтически приемлемой соли) будут относиться к дозе вальпроевой кислоты (т.е. дозе самой вальпроевой кислоты) или эффективной (т.е. эквивалентной) дозе вальпроевой кислоты при введении в форме, которая включает или состоит из одной или более ее соли.
В конкретном варианте реализации седьмого аспекта настоящего изобретения, доза составляет от около 200 мг до около 400 мг, например, около 400 или около 300 мг. В другом конкретном варианте реализации седьмого аспекта настоящего изобретения доза составляет от около 300 мг до около 500 мг, например, около 350 мг. В другом конкретном варианте реализации седьмого аспекта настоящего изобретения доза составляет от около 400 мг до около 600 мг, например, около 450 мг или около 550 мг. В другом конкретном варианте реализации седьмого аспекта настоящего изобретения доза составляет от около 400 мг до около 800 мг, например, около 575, около 650 или около 700 мг.
Опять же, во избежание неоднозначности толкования, все ссылки в данном описании на конкретные аспекты настоящего изобретения (например, согласно первому аспекту настоящего изобретения) будут включать ссылки на все альтернативные такие аспекты настоящего изобретения (например, альтернативные и дополнительные альтернативные первые аспекты настоящего изобретения).
Кроме того, специалисту в данной области техники будет понятно, что все варианты реализации, предпочтения, конкретные определения и т.п., упомянутые в настоящем документе, могут быть объединены с любым одним или более другими вариантами реализации, предпочтениями, конкретными определениями и т.п., также указанными в данном документе.
При использовании в данном описании ссылки на значение или количество (включая количество времени), термины "около", "примерно" и "приблизительно" следует понимать как относящиеся к значению, которое находится в пределах 10% от оцененного значения.
При использовании в данном описании ссылки на конкретный момент времени (включая начало или конец определенного периода времени), термины "около" и "примерно" следует понимать как относящиеся к значению, которое находится в пределах 30 минут (например, в пределах 20 минут, например, в течение 10 минут) указанного определенного времени. Кроме того, предполагается, что каждая ссылка на термины "примерно", "около" и "приблизительно" (например, в отношении времени и количеств) может быть исключена из текста всего документа.
В данном контексте термин "соединения по настоящему изобретению" будет относиться к вальпроевой кислоте и ее фармацевтически приемлемой соли. Специалисту в данной области техники будет понятно, что ссылки на вальпроевую кислоту и ее фармацевтически приемлемые соли (например, термин "вальпроевая кислота или ее фармацевтически приемлемая соль") могут включать ссылки на смеси различных фармацевтически приемлемых солей, а также ссылки на смеси вальпроевой кислоты (т.е. в несолевой форме) и ее фармацевтически приемлемых солей (включая смеси таких солей), все из которых могут быть отнесены к соединениям по настоящему изобретению.
Специалисту в данной области техники из настоящего описания будет понятно, что термин "предотвращение" конкретного патологического состояния может также означать "профилактику" указанного патологического состояния и наоборот. Таким образом, каждая ссылка в данном описании на "предотвращение" патологического состояния может быть заменена ссылкой на "профилактику" указанного патологического состояния.
Специалисту в данной области техники будет понятно, что термины "лечение" и "лечить" в настоящем описании имеют свое привычное значение в области медицины. В частности, эти термины могут относиться к достижению снижения тяжести одного или более клинических симптомов, связанных с соответствующим патологическим состоянием.
Специалисту в данной области техники также будет понятно, что термины "предотвращение" и "предотвращать" в настоящем описании имеют свое привычное значение в области медицины. В частности, эти термины могут относиться к достижению снижения вероятности развития соответствующего патологического состояния (у пациента) (например, снижения по меньшей мере на 10% по сравнению с исходным уровнем, такого как снижения по меньшей мере на 20% или, более конкретно, снижения по меньшей мере на 30%).
Специалисту в данной области техники также будет понятно, что ссылки на профилактику (или предотвращение) конкретного патологического состояния могут также включать ссылки на лечение другого патологического состояния. Например, лечение первичного патологического состояния может также рассматриваться как форма профилактики вторичного патологического состояния.
В конкретных вариантах реализации аспектов настоящего изобретения (с первого по седьмой, включая все альтернативные аспекты) предлагаются соединения для применения в (и/или применение в и/или способах) профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов (в частности, тромбообразованием).
В данном контексте термин "патологические состояния" следует понимать как относящийся к идентифицируемым заболеваниям или нарушениям.
Как описано в настоящем документе, патологические состояния, которые можно лечить или предупреждать в соответствии с настоящим изобретением, связанны с избыточным отложением фибрина и/или образованием тромбов. Указанные состояния включают, но не ограничиваются ими, атеросклероз, инфаркт миокарда, ишемический инсульт, тромбоз глубоких вен, тромбоз поверхностных вен, тромбофлебит, легочную эмболию, диссеминированное внутрисосудистое свертывание крови, патологию сосудов почек и перемежающуюся хромоту (например, атеросклероз, инфаркт миокарда, ишемический инсульт, тромбоз глубоких вен, легочная эмболия, диссеминированное внутрисосудистое свертывание крови, патология сосудов почек и перемежающаяся хромота).
Таким образом, в конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, выбрано из группы, состоящей из атеросклероза, инфаркта миокарда, ишемического инсульта, тромбоза глубоких вен, легочной эмболии, диссеминированного внутрисосудистого свертывания крови, патологии сосудов почек и перемежающейся хромоты.
Таким образом, в более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, выбрано из группы, состоящей из инфаркта миокарда, ишемического инсульта и легочной эмболии.
В других более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, выбрано из группы, состоящей из инфаркта миокарда и ишемического инсульта (например, инфаркта миокарда).
Специалисту в данной области техники будет понятно, что ссылки на ишемический инсульт включают ссылки на обширные ишемические нарушения (т.е. те, которые обусловлены длительным нарушением кровотока), микроинсульты и транзиторные ишемические атаки (ТИА).
Таким образом, в более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, представляет собой ишемический инсульт, такой как обширный ишемический инсульт, ишемический микроинсульт или ТИА.
В еще более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, представляет собой ишемический инсульт, такой как обширный ишемический инсульт и ишемический микроинсульт.
В частности, можно полагать, что соединения по настоящему изобретению, при введении согласно схем лечения, определенных выше (например, как указано с первого по седьмой аспект настоящего изобретения), могут быть особенно пригодны для профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов (например, ишемический инсульт и/или инфаркт миокарда). Таким образом, все ссылки на лечение и профилактику указанных патологических состояний в настоящем документе будут включать конкретные ссылки на профилактику указанных патологических состояний.
Таким образом, в еще более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, лечение и профилактика патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, будет означать профилактику ишемического инсульта, такого как обширный ишемический инсульт, ишемический микроинсульт или ТИА.
Как отмечалось выше, тромботические сердечно-сосудистые происходят в результате двух различных процессов: медленно прогрессирующего длительного атеросклероза сосудистой стенки, с одной стороны, и внезапного острого образования сгустка, который стремительно блокирует поток крови, с другой стороны. Конкретные патологические состояния, которые могут быть пролечены, являются теми, которые касаются последнего процесса.
В конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологические состояния, которые можно лечить или предупреждать в соответствии с настоящим изобретением, являются такими, которые полностью или по меньшей мере частично обусловлены увеличенным отложением фибрина и/или снижением фибринолитической активности в результате местного или системного воспаления. Указанные состояния включают, но не ограничиваются ими, инфаркт миокарда, стабильную стенокардию, нестабильную стенокардию, перемежающуюся хромоту, ишемический инсульт, транзиторную ишемическую атаку, тромбоз глубоких вен и легочную эмболию. При этих патологических состояниях могут регистрироваться повышенные уровни PAI-1 в плазме.
В конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние может быть выбрано из группы, состоящей из тромбоза глубоких вен и легочной эмболии.
В конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние представляет собой тромбоз глубоких вен.
В конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние может быть выбрано из группы, состоящей из тромбоза поверхностных вен и тромбофлебита.
В более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние представляет собой тромбоз поверхностных вен.
В более конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, патологическое состояние представляет собой тромбофлебит.
Кроме того, патологические состояния, которые можно лечить в соответствии с настоящим изобретением, являются теми, которые полностью или по меньшей мере частично обусловлены увеличенным отложением фибрина и/или снижением фибринолитической активности в результате местного или системного воспаления. Указанные патологические состояния включают, но не ограничиваются ими, атеросклероз, метаболический синдром, диабет, диссеминированное внутрисосудистое свертывание крови, ревматоидный артрит, гломерулонефрит, системную красную волчанку, васкулиты, аутоиммунные невропатии и гранулематозное заболевание, а также воспаления, ассоциированные с другими патологическими состояниями (такими как метаболический синдром, диабет, диссеминированное внутрисосудистое свертывание крови, ревматоидный артрит, гломерулонефрит, системная красная волчанка, васкулиты, аутоиммунные невропатии и гранулематозное заболевание, а также воспаление, ассоциированное с другими патологическими состояниями).
В дополнение к традиционной диагностике системного или местного воспаления, проводимой врачом и известной в данной области техники, местное или системное воспаление может быть диагностировано у пациентов с помощью одного или более биомаркеров, ассоциированных с воспалением. Указанные биомаркеры включают, но не ограничиваются ими, С-реактивный белок, ФНО-альфа, высокочувствительный С-реактивный белок (вч-СРБ), фибриноген, ИЛ-1 бета и ИЛ-6. Конкретные способы определения наличия у пациента системного или местного воспаления включают те, которые описаны ниже.
Кроме того, атеросклеротические бляшки, как известно, ассоциированы с очень локализованным воспалительным процессом. Следовательно, местное воспаление можно также опосредовано диагностировать при наличии атеросклеротических бляшек, обнаруженных при ультразвуковом исследовании сосудов или с помощью других методов визуализации.
Специалисту в данной области техники будет понятно, что существует несколько различных вариантов для определения недостаточного уровня фибринолиза у пациента (т.е. сниженной фибринолитической активности). Например, высокие уровни циркулирующих PAI-1, как правило, считаются признаком недостаточного фибринолиза и могут быть определены в плазме с использованием коммерчески доступных способов (включая, но не ограничиваясь ими, Coaliza® PAI-1 (Chromogenix), TriniLIZE® PAI-1 (Trinity Biotech), Imubind® Plasma PAI-1 (American Diagnostica), Zymutest PAI-1 (Hyphen Biomed), Milliplex PAI-1 (MerckMillipore), набор Elisa для человека Novex PAI-1 (Life technology), набор ELISA для человека РАI1 (SERPINE1) (Abeam, ab108891). Кроме того, низкие системные уровни свободного, активного t-PA также являются показателем общего недостаточного фибринолиза, и также могут быть измерены с помощью коммерческих способов (антиген и активность TriniLIZE® t-PA (Trinity Biotech), как и наличие генотипа низкой продукции (Т) полиморфизма t-PA -7351 С/Т. Функциональные анализы измерения времени лизиса сгустка также использовали для оценки общего фибринолиза (Thrombinoscope™(Synapse, BV, Маастрихт, Нидерланды), IL/ROTEM® (Term International GmbH, Мюнхен, Германия), TEG® (Haemoscope, Niles), CloFAL assay (Peikang Biotechnology Co. Ltd. Шанхай, Китай).
Специалисту в данной области техники будет понятно, что повышенное отложение фибрина и/или сниженная фибринолитическая активность из-за "местного или системного воспаления", как описано в настоящем документе, можно определять с применением одного или более биомаркеров, ассоциированных с воспалением, включая, но не ограничиваясь ими, С-реактивный белок, ФНО-альфа, высокочувствительный С-реактивный белок (вч-СРБ), фибриноген, ИЛ-1бета, и ИЛ-6 (например, при повышении концентрации одного или более из этих биомаркеров по сравнению с контрольным уровнем, известным в данной области техники). Коммерческие аналитические платформы, которые могут применяться для количественного определения этих биомаркеров включают, но не ограничиваются ими, Afinion™ (Medinor АВ, Швеция), СА-7000 (Siemens Healthcare Diagnostics Inc, Нью-Йорк, США), Система иммуноферментного анализа Immulite® 2000 (Siemens Healthcare Diagnostics Inc).
Конкретные биомаркеры, с помощью которых можно идентифицировать местное или системное воспаление, включают высокочувствительный С-реактивный белок (вч-СРБ) (на уровне или выше 2,0 мг/л сыворотки) и фибриноген (на уровне или выше 3 мг/л сыворотки) (Corrado Е., et al. An update on the role of markers of inflammation in atherosclerosis, Journal of atherosclerosis and Thrombosis, 2010; 17:1-11, Koenig W., Fibrin(ogen) in cardiovascular disease: an update, Thrombosis Haemostasis 2003; 89:601-9).
Если не указано иное, в данном описании термин "пациент" включает пациентов млекопитающих (например, непарнокопытных, крупный рогатый скот, свиней, овец, коз, приматов, мышей, крыс и домашних животных в целом, включая собак, кошек, морских свинок, хорьков и кроликов). В частности, термин "пациент" относится к человеку.
Специалисту в данной области техники из настоящего описания будет понятно, что ссылки на плазму будут относиться к плазме крови пациента.
Специалисту в данной области техники из настоящего описания будет понятно, что ссылки на максимальную концентрацию в плазме (или "Cmax") конкретных веществ будут относиться к максимальной концентрации этого вещества в плазме крови (т.е. в плазме крови пациента). В контексте введения этого агента, Cmax будет относиться к той концентрации, которая возникает непосредственно в результате такого введения (т.е. Cmax, возникающей в результате абсорбции этого агента).
В данном контексте, время, в течение которого возникает Cmax конкретного вещества, также может упоминаться как Тmax.
Специалисту в данной области техники будет понятно, что Cmax может возникнуть в определенный момент времени (т.е. конкретный пик концентрации в плазме) или в течение длительного периода (т.е. когда концентрация в плазме достигает плато); при этом оба из этих периодов могут относиться ко времени, в течение которого возникает Cmax (Tmax). В случаях, когда Cmax возникает в течение длительного периода, время, при котором возникает Cmax, также может быть принято в средней точке этого периода, хотя обычно подразумевается, что Cmax будет возникать в виде четко различимого пика в определенное время.
Как описано в настоящем документе, колебания концентрации PAI-1 в плазме пациента (в частности, человека) известны своим циркадным ритмом. Как правило, максимальная концентрация PAI-1 в плазме (Cmax), как ожидается, наблюдается в около 06:00 часов.
Таким образом, ссылки в настоящем документе на время, при котором возникает Cmax PAI-1, могут быть заменены на термин "около 06:00 часов".
Все абсолютные периоды времени (т.е. конкретные моменты и периоды времени, определяемые как находящиеся между конкретными моментами времени), указанные в настоящем документе, относятся к фактическому местному времени (т.е. времени на "часах"), по которому живет пациент. Кроме того, указанные периоды времени предполагают, что пациент адаптируется к местному времени (например, имеет достаточно времени, чтобы адаптироваться к изменениям в часовом поясе или так называемому времени, устанавливаемому для рационального использования светлой части суток).
Специалисту в данной области техники будет понятно, что время максимальной концентрации PAI-1 и соединений по настоящему изобретению (или их солей и/или метаболитов) в плазме можно определить с применением методик, которые хорошо известны специалистам в данной области техники, например, путем мониторинга концентрации PAI-1 и соединений по настоящему изобретению (или их солей и/или метаболитов) в течение соответствующего периода времени.
Как описано в настоящем документе, мониторинг уровней соединений по изобретению (или их солей и/или метаболитов) можно осуществлять с применением методик, которые хорошо известны специалистам в данной области техники. Например, уровни вальпроата в плазме определяются в клинической практике, например, с помощью технологии однородного иммуноферментного анализа, основанного на конкуренции антител между вальпроатом в образце и вальпроатом, меченым ферментом и добавленным в тест-систему (например, VALP2, Roche/Cobas, art nr 05108438190 (Roche Diagnostics Scandinavia AB). Когда вальпроат, меченный ферментом, связывается с антителом, фермент глюкозо-6-фосфат-дегидрогеназа (G6PDH) блокируется и не может усваивать субстрат фермента в тест-системе. С другой стороны, когда вальпроат, меченный ферментом, не связывается с антителом, субстрат доступен для фермента и может быть усвоен. Усвоение субстрата измеряется опосредовано, с учетом образования NADH из NAD (коферментная реакция). NADH поглощает УФ-свет селективно при 340 нм. Это означает, что при высоких концентрациях вальпроата в образце отмечается большое изменение оптической плотности при длине волны 340 нм; и наоборот, при низкой концентрации вальпроата может быть небольшое изменение оптической плотности при длине волны 340 нм. Потребление субстрата приводит к изменению цвета, которое измеряется фотохроматографически при длине волны 340 и 415 нм. Оптическая плотность прямо пропорциональна концентрации вальпроата в образце.
Специалист сможет идентифицировать соединения, присутствующие в плазме как метаболиты соединений по настоящему изобретению. Конкретные метаболиты соединений по настоящему изобретению, которые могут быть упомянуты, включают анион вальпроата (например, метаболиты, которые содержат фрагмент аниона валпроата).
Специалисту в данной области техники будет понятно, что ссылки на мониторинг концентрации PAI-1 в плазме (т.е концентрацию в плазме крови в организме пациента) могут относиться к мониторингу по меньшей мере в течение одного (например, одного) 24-часового периода (например, до начала лечения с применением соединения по настоящему изобретению). Такой мониторинг может быть непрерывным или может включать осуществление измерений через определенные промежутки времени в течение этого периода (что может означать, в частности, что в последнем случае время между первым и последним измерениями составляет менее 24 часов, например, около 20 часов).
Специалисту в данной области техники также будет понятно, что такой мониторинг может быть вместе с тем проведен в течение периода времени, который, как ожидается, включает Cmax PAI-1, по оценкам специалиста в данной области техники. Так, например, если Cmax of PAI-1 ожидается около 06:00 часов, такой мониторинг можно осуществлять от 04:00 часов до 08:00 часов (например, от 05:00 часов до 07:00 часов).
Выбор времени для введения и количество дозы соединений по настоящему изобретению также приведет к низкой концентрации вальпроевой кислоты или ее соли и/или метаболита в плазме в определенные периоды времени.
Таким образом, в конкретном варианте реализации от первого до седьмого аспекта настоящего изобретения, введение соединений по настоящему изобретению осуществляется таким образом, что концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме в течение периода времени от около 14:00 часов до около 18:00 часов (например, от около 15:00 часов до около 17:00, например, около 16:00 часов) составляет менее чем около 350 мкМ (например менее чем около 300 мкМ, например, менее чем около 250 мкМ или, более конкретно, менее чем 200 мкм, например, менее чем около 150 мкМ или менее чем около 100 мкМ).
В более конкретном варианте реализации от первого до седьмого аспекта настоящего изобретения, введение соединений по настоящему изобретению осуществляется таким образом, что концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме в течение периода времени от около 15:00 часов до около 17:00 часов (например, от около 15:30 часов до около 16:30) составляет менее чем около 300 мкМ (например, менее чем около 200 мкМ (например, менее чем около 150 мкМ или менее чем около 100 мкМ).
Кроме того, специалист в данной области техники сможет регулировать как время, так и дозы введения соединений по настоящему изобретению для того, чтобы соответствовать требованиям временных характеристик Cmax и/или достичь максимальной или минимальной концентрации в плазме в заданное время.
В данном контексте термины "терапевтически эффективное количество" и "терапевтически эффективная доза" относятся к количеству активного агента (т.е. соединений по настоящему изобретению), которое обуславливает требуемый фармакологический или терапевтический эффект у пациента, предпочтительно без чрезмерных нежелательных побочных эффектов. Следует понимать, что терапевтически эффективное количество может варьироваться от пациента к пациенту.
В частности, терапевтически эффективная доза соединения по настоящему изобретению, представляет собой количество, достаточное для лечения или профилактики соответствующего патологического состояния и его осложнений; в частности, при выборе указанного количества следует стремиться минимизировать побочные эффекты (например, нежелательные явления, вызванные действием терапевтического агента).
Основываясь на настоящем описании, специалист в данной области техники сможет корректировать вводимую дозу соединений по настоящему изобретению для достижения желаемого биологического эффекта с применением методов, известных специалистам в данной области техники.
Специалисту в данной области техники будет понятно, что дозу соединений по настоящему изобретению можно титровать таким образом, что доза будет обуславливать снижение уровня PAI-1 в плазме по меньшей мере на около 20% (например, по меньшей мере на около 30%).
В конкретных вариантах реализации настоящего изобретения (например, конкретные варианты реализации от первого до седьмого аспекта настоящего изобретения), доза соединений по настоящему изобретению является достаточной для достижения снижения уровня PAI-1 в плазме по меньшей мере на около 20% (например, по меньшей мере на около 30%), т.е. дозу титруют до достижения требуемого снижения уровней PAI-1 в плазме.
В более конкретных вариантах реализации настоящего изобретения (например, конкретные варианты реализации от первого до седьмого аспекта настоящего изобретения) доза является достаточной для достижения снижения уровней PAI-1 в плазме по меньшей мере на около 40% (например, по меньшей мере на около 50%, например, по меньшей мере на около 60%).
Аналогичные титрования дозы известны в данной области техники; при этом начальная доза, увеличение дозы, интервалы измерений PAI-1 (как правило, в утренних образцах), желаемое уменьшение уровней PAI-1 и шаг увеличения потенциальной дозы могут быть выбраны специалистом в данной области техники.
В некоторых вариантах реализации настоящего изобретения начальные дозы для таких титрований могут находиться в диапазоне, например, 50, 100, 150, 200, 250 или 300 мг, а увеличивать дозу можно на 20-100 мг каждые 7-28 дней после нового измерения РАМ. Например, в одном таком измерении начальная доза перед титрованием дозы составляет 50 мг, впоследствии дозу повышают с шагом 50 мг каждые 7 дней до снижения уровней циркулирующего PAI-1 на 20%. В другом таком измерении начальная доза перед титрованием дозы составляет 100 мг, впоследствии дозу повышают с шагом 100 мг каждые 14 дней до снижения уровней циркулирующего PAI-1 на 20%.
Не желая быть связанными любой теорией, полагают, что неожиданные эффекты, возникающие в результате введения соединений по настоящему изобретению, как описано в данном документе, могут быть получены путем введения доз соединений в таком количестве, при котором не ожидается значительный уровень нежелательных явлений.
Таким образом, в конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения для лечения может быть необходимо введение дозы вальпроевой кислоты или ее фармацевтический приемлемой соли (например, одной такой дозы в течение 24-часового периода), которую выбирают таким образом, чтобы минимизировать уровень нежелательных явлений в результате такого лечения (например, выбирают дозу достаточно низкого уровня, что позволяет избежать возникновения таких нежелательных явлений).
Такие количества могут варьироваться в зависимости от частоты и способа введения, пола, возраста, веса и общего состояния субъекта, подвергаемого лечению, природы и тяжести патологического состояния, подвергаемого лечению, или других видов лечения, применяемых для индивидуума, и могут быть определены с помощью обычных методик в этой области техники. Количество, которое является эффективным для конкретной терапевтической цели, будет зависеть от тяжести патологического состояния, а также от веса и общего состояния субъекта. Следует понимать, что определение соответствующей дозы может быть осуществлено с помощью рутинного экспериментирования путем конструирования матрицы значений и тестирования различных точек в матрице, что находится в пределах обычной квалификации специалиста в данной области техники.
Несмотря на обсуждение конкретных доз в настоящем документе, специалисту в данной области техники будет понятно, что количество и схемы лечения с применением VPA, или ее фармацевтически приемлемой соли, необходимые для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромба, как описано в настоящем документе, могут быть определены лечащим врачом с помощью рутинных методов.
В конкретных вариантах реализации от первого до седьмого аспекта настоящего изобретения, соединения по настоящему изобретению могут быть введены:
(i) в однократной дозе в течение 24-часового периода (т.е. в однократной суточной дозе); и/или
(ii) в общей дозе в течение 24-часового периода (т.е. общей суточной дозе) от около 50 мг до около 1000 мг (в частности, от около 200 мг до около 600 мг, например от около 300 мг до около 500 мг).
Более конкретно, однократная суточная доза, описанная выше (например, в пункте (i) непосредственно выше), может быть введена в период времени от около 20:00 до около 06:00 часов.
В более конкретном варианте реализации изобретения однократная суточная доза (например, описанная в пункте (i) выше) может быть введена в период времени от около 21:00 до около 05:00 часов (например, от около 22:00 до около 04:00 часов).
В еще более конкретных вариантах реализации (в частности, когда для лечения применяют фармацевтическую композицию, состав которой не предусматривает замедленное высвобождение активного ингредиента), однократная суточная доза (например, описанная в пункте (i) выше) может быть введена в течение периода времени от около 02:00 часов до около 06:00 часов (например, от около 03:00 часов до около 05:00 часов, например, около 4:00 часов).
В дополнительных конкретных вариантах реализации изобретения (в частности, когда для лечения применяют фармацевтическую композицию, состав которой предусматривает замедленное высвобождение активного ингредиента, такого как описанный в восьмом аспекте изобретения в настоящем документе), однократная суточная доза (например, описанная в пункте (i) выше) может быть введена в течение периода времени от около 20:00 часов до около 00:00 часов (например, от около 21:00 часов до около 23:00 часов, например, около 22:00 часов).
В альтернативных вариантах реализации изобретения (в частности, когда для лечения применяют фармацевтическую композицию, состав которой предусматривает замедленное высвобождение активного ингредиента, такого как описанный в восьмом аспекте изобретения в настоящем документе), однократная суточная доза (например, описанная в пункте (i) выше) может быть введена перед сном (т.е. непосредственно перед тем, когда пациент начинает делать попытки заснуть, что в альтернативном варианте может быть описано как "перед отходом ко сну", "перед тем, как лечь в постель" или тому подобное).
В конкретных вариантах реализации настоящего изобретения (например, конкретные варианты реализации от первого до седьмого аспекта настоящего изобретения), соединения по настоящему изобретению могут быть введены таким образом, что концентрация в плазме вальпроевой кислоты, или ее соли и/или метаболита в течение определенного периода (например, 24-часового периода) моделирует концентрацию PAI-1 в плазме в течение того же периода.
В данном контексте ссылки на уровень в плазме, который "моделирует" другой уровень, будут означать, что относительные уровни двух агентов в плазме характеризуются по существу сходными закономерностями изменений (например, полученные кривые концентраций двух агентов в плазме могут быть по существу совпадающими при наложении, хотя абсолютные уровни/концентрации этих двух агентов могут быть разными). Термин "моделирует" имеет свое обычное значение в данной области техники, т.е. означает "походить", "симулировать", "приближенно равняться", "следовать" или "воплощать", но не обязательно означает "повторять точно или совершенно определенно".
Специалисту в данной области техники будет понятно, что помимо вечерней дозы, можно вводить более низкую утреннюю дозу, которая будет абсорбироваться, когда уровень PAI-1 начнет возрастать в конце дня. Например, при одном таком лечении 10-500 мг (например, 50-300 мг, более конкретно 100 или 200 мг) вводят примерно через 10-14 часов (например, 12 часов) после вечерней дозы.
Таким образом, в конкретном варианте реализации настоящего изобретения вводят более низкую утреннюю дозу в дополнение к вечерней дозе, которая будет составлять от около 10 до около 500 мг (например, от около 50 до около 300 мг, более конкретно 100 или около 200 мг), вводимой в течение периода времени, который составляет от около 10 до около 14 часов (например, около 12 часов) после вечерней дозы. В конкретном варианте реализации настоящего изобретения утренняя доза составляет от около 20 до около 50% (например, около 20, около 30 или около 40%) вечерней дозы.
В более конкретном варианте реализации настоящего изобретения предлагается состав для введения один раз в сутки, который обеспечивает тот же эффект, что и утренняя и вечерняя дозы, описанные в варианте реализации непосредственно выше; при этом состав может быть представлен, например, в виде двухслойного состава с активным ядром, обуславливающим второй малый пик, совпадающий с повышением PAI-1, или в виде гранулами с другим покрытием и/или составом, составленным для такого профиля высвобождения.
Как описано в данном документе, было обнаружено, что вальпроевая кислота (VPA) потенциально снижает уровни PAI-1 в плазме до такой степени, что обеспечивает возможность повышения активности эндогенного t-PA. В частности, введение VPA таким образом, что ее уровни в плазме совпадают с пиковыми уровнями PAI-1 в плазме, позволяет лечить или предотвращать патологические состояния, связанные с избыточным отложением фибрина и/или образованием тромбов.
Таким образом, ссылки в данном документе (например, от первого до седьмого аспекта настоящего изобретения) на применение в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, могут также относиться к лечению или профилактике патологического состояния, при которых, как ожидается, будет польза от снижения активности PAI-1 (т.е. патологическое состояние можно лечить или предотвращать таким способом).
Во избежание неоднозначности толкования, указанные конкретные патологические состояния обозначают состояния, связанные с избыточным отложением фибрина и/или образование тромбов, как известно специалисту в данной области техники (в частности, как описано в настоящем документе); также могут обозначать патологические состояния, при которых, как ожидается, будет польза от снижения активности PAI-1 (т.е. патологическое состояние можно лечить или предотвращать таким способом), что можно расценивать как результат снижения уровней PAI-1 в плазме.
В частности, в дополнительном аспекте настоящего изобретения предлагается способ снижения уровней PAI-1 (т.е. уровней PAI-1 в плазме) у пациента, имеющего для этого показания; причем способ включает этап введения терапевтически эффективного количества вальпроевой кислоты, или ее фармацевтически приемлемой соли.
Аналогичным образом, конкретные способы лечения или профилактики патологических состояний, связанных с избыточным отложением фибрина и/или образованием тромбов, как указано в данном описании, также могут быть расценены как способы снижения уровней PAI-1 у пациента, имеющего для этого показания.
Например, в еще одном дополнительном альтернативном первом аспекте настоящего изобретения предлагается способ снижения уровней PAI-1 у пациента, имеющего для этого показания; причем способ включает введение по меньшей мере одной дозы терапевтически эффективного количества вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
В данном контексте ссылки на снижения уровня PAI-1 (и, аналогично, на снижение (или ингибирование) активности PAI-1, например, ссылки на ингибирование РАI-1) могут относиться к уровням PAI-1 в плазме во время лечения соединениями по данному изобретению, которые регистрируются (например, снижаются или поддерживаются) на более низких уровнях по сравнению с уровнями PAI-1 (например, по меньшей мере на 10% ниже, например, по меньшей мере на 20% ниже, например, по меньшей мере на 30% ниже, по меньшей мере на 40% ниже, по меньшей мере на 50% ниже или по меньшей мере на 60% ниже), наблюдаемыми до лечения соединениями по настоящему изобретению.
Соединения по настоящему изобретению
Так же, как указано в настоящем описании, термин "соединения по настоящему изобретению" будет относиться к вальпроевой кислоте и ее фармацевтически приемлемым солям, включая их смеси. Специалисту в данной области техники будет понятно, что вальпроевая кислота может также называться, в частности, 2-пропилпентановая кислота и VPA.
Соединения, представленные в настоящем описании, включают, где это уместно, все диастереомерные, энантиомерные и эпимерные формы. Для соединений, описанных в настоящем документе, которые существуют в виде таутомеров, все таутомеры включены в формулы, описанные в настоящем документе. Кроме того, соединения, описанные в настоящем документе, могут быть составлены в форме, и/или применяться в форме солей (например, фармацевтически приемлемых солей). Специалисту в данной области техники будет понятно, что ссылки в настоящем описании на соли соединений будут включать ссылки на фармацевтически приемлемые соли.
Соединения, описанные в настоящем документе, могут быть получены с использованием методов и процедур, известных специалистам в данной области техники. Примерные синтетические способы, используемые для синтеза соединений по настоящей заявке, включают, например, те, которые описаны в Nogrady (1985) Medicinal Chemistry А Biochemical Approach, Oxford University Press, New York, pages 388-392; Silverman (1992); Fieser and Fieser's Reagents for Organic Synthesis, Volumes 1-17 (John Wiley and Sons, 1991); Rodd's Chemistry of Carbon Compounds, Volumes 1-5 and Supplemental (Elsevier Science Publishers, 1989); Organic Reactions, Volumes 1-40 (John Wiley and Sons, 1991), March's Advanced Organic Chemistry, (John Wiley and Sons, 4th Edition) and Larock's Comprehensive Organic Transformations (VCH Publishers Inc., 1989).
VPA может быть коммерчески доступным, например, от компании Sigma-Aldrich (под номером продукта Р4543 по состоянию на 1 октября 2014 года). Фармацевтически приемлемые соли VPA (например, ее натриевой соли), также могут быть коммерчески доступны. Также будет понятно, что VPA или ее фармацевтически приемлемые соли могут быть синтезированы с применением методик, хорошо известных специалистам в данной области техники.
Как описано в настоящем документе, VPA может составляться и/или вводиться в форме фармацевтически приемлемой соли.
Специалисту в данной области техники будет понятно, что фармацевтически приемлемые соли (например, из VPA) могут включать, но не ограничиваются ими:
(a) соли, образующиеся при замещении кислотного протона ионами металлов, например, ионом щелочного металла (например, лития, натрия, калия), ионом щелочноземельного металла (например, магния или кальция) или ионом алюминия или образующиеся при замещении катионом аммония (NH4+);
(b) соли, образованные взаимодействием VPA с фармацевтически приемлемым органическим основанием, которое включает алкиламины, такие как этаноламин, диэтаноламин, триэтаноламин, трометамин, N-метилглюкамин, дициклогексиламин, трис(гидроксиметил)метиламин и соли с аминокислотами, такими как аргинин, лизин и т.п.;
(c) соли, образованные в результате реакции VPA с фармацевтически приемлемой кислотой, что обеспечивает образование кислотно-аддитивных солей. Фармацевтически приемлемые кислоты включают хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту, метафосфорную кислоту и т.п.; или органическую кислоту, такую как, например, уксусная кислота, пропионовая кислота, гексановая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, трифторуксусная кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил) бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, толуолсульфоновая кислота, 2- нафталинсульфоновая кислота, 4-метилбицикло[2.2.2]окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 4,4'-метиленбис-(3-гидрокси-2-ен-1-карбоновая кислота), 3-фенилпропионовая кислота, триметилуксусная кислота, третичная бутилуксусная кислота, лаурилсерная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и тому подобное.
Конкретные фармацевтически приемлемые соли VPA, которые могут быть упомянуты, включают те, которые упомянуты в пункте (а) выше. Более конкретные фармацевтически приемлемые соли VPA, которые могут быть упомянуты, включают те, в которых протон карбоновой кислоты замещен щелочно-земельным ионом (например, магнием или кальцием) или, более конкретно, ионом щелочного металла (например, литием, натрием или калием).
В конкретных вариантах реализации каждого аспекта изобретения VPA вводят и/или составляют (при необходимости) в форме ее натриевой соли (т.е. валпроата натрия). В более конкретных вариантах реализации изобретения VPA вводят и/или составляют (при необходимости) в форме смеси VPA (т.е. в несолевой форме) и ее натриевой соли (т.е. валпроата натрия), например, в равных пропорциях.
Например, в конкретных вариантах реализации настоящего изобретения (т.е. каждого аспекта настоящего изобретения), VPA можно вводить и/или составлять (при необходимости) в форме смеси ее натриевой соли (т.е. валпроата натрия) и вальпроевой кислоты. В данной области техники известны несколько таких смесей, например, вальпроат полунатрий, также известный как дивальпрокс натрия (молярное соотношение между вальпроевой кислотой и вальпроатом натрия 1:1), который доступен на рынке, например, как Депакот и Депакот ER (от компании AbbVie Inc.); и вальпроат натрия (соотношение между вальпроевой кислотой и вальпроатом натрия 1:2,3), который доступен на рынке, например, как Эпилекс Хроно.
Дополнительные фармацевтически приемлемые соли, которые могут быть упомянуты, включают описанные в работах Berge et al., J. Pharm. Sci. 1977, 66, 1-19; и "Handbook of Pharmaceutical Salts, Properties, and Use", Stah and Wermuth, Ed.; Wiley-VCH and VHCA, Zurich, 2002 (содержание которых включено в данный документ во всей их полноте).
Ссылки на "соли" соединений по настоящему изобретению следует понимать как относящиеся к солевым формам, которые могут образовываться путем обмена анионами или катионами с соединениями по настоящему изобретению, например, в плазме крови.
В частности, термин "соли" может также относиться к их фармацевтически приемлемым солям, таким как те, которые описаны в настоящем документе.
Как описано в настоящем документе, VPA можно также составлять и/или вводить в форме пролекарства или фармацевтически приемлемой соли указанного пролекарства.
В данном контексте термин "пролекарство" при использовании в отношении VPA следует понимать как относящееся к соединению, которое может преобразовываться в VPA in vivo (т.е. после введения).
Такие пролекарства могут быть идентифицированы специалистом в данной области техники и могут включать сложный эфир (например, метиловый или этиловый эфир) или амидные производные VPA. Конкретные пролекарства, которые могут быть упомянуты, включают 2-пропилпентанамид (также известный как вальпромид).
В случае, если соединения по настоящему изобретению вводят в виде пролекарства, специалист в данной области техники сможет корректировать вводимую дозу для достижения эквивалентной дозы VPA, в соответствии с установленными требованиями.
Коммерчески доступные продукты, содержащие вальпровую кислоту и/или валпроат натрия, или их пролекарства включают, но не ограничиваются ими:
Депакот (Abbvie Inc.), Абсенор (Orion Corporation) Конвулекс (Pfizer), Конвулекс CR, Депакен/Депакин/ Депалепт/Депракин (Abbvie Inc. /Sanofi Aventis), Депакин Хроно (Sanofi), Депакен-Р (Kyowa Hakko Kogyo), Селеница-Р (Kowa), Энкорат (Sun Pharmaceuticals India), Энкорат Хроно (Sun Pharmaceuticals), Эпивал (Abbott Laboratories), Эпилим (Sanofi), Эпилим Хроносферы гранулы с модифицированным высвобождением, Эпилим Хроно таблетки с контролируемым высвобождением, Эпилим Хроно таблетки с пролонгированным высвобождением, Ставзор (Noven Pharmaceuticals), Валкот (Abbott Laboratories), Валпакин (Sanofi Aventis), Депамид (Sanofi-Avetis), Дипексил-R (Bial), Элиаксим (Bial), таблетки вальпроата натрия Сандоз (Sanofi), Вальпро таблетки (Alphapharm), Вальпроат Уинтроп таблетки (Sanofi), Валпреаз (Sigma), Эпилим ЕС таблетки с модифицированным высвобождением (Sanofi-Aventis), Ориепт (Wockhardt), Эпилим Хроно (Sanofi) (соотношение валпроевой кислоты и вальпроата натрия 1:2,3), Эпилим ЕС 200 (Sanofi), Валпрол CR (Intas Pharmaceutical), Эписента с пролонгированным высвобождением (Beacon), капсулы вальпроевой кислоты, USP (Teva), Ставзор (Noven), Орфирил (Desitin Pharmaceuticals).
Коммерчески доступные продукты, содержащие вальпроевую кислоту и/или вальпроат натрия, или пролекарства также будут включать генерический вариант вышеуказанных составов, которые могут продаваться/быть доступными на рынке под другим названием.
Введение соединений
Специалисту в данной области техники будет понятно, что в настоящем документе также предлагается фармацевтическая композиция, содержащая вальпроевую кислоту или ее фармацевтически приемлемую соль, и необязательно содержащая одно или более фармацевтически приемлемых вспомогательных веществ для применения в лечении или профилактике патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов, как описано в аспектах настоящего изобретения (от первого до седьмого, включая все варианты их реализации).
Соединения по настоящему изобретению можно вводить субъекту удобным способом, например, с помощью перорального, внутривенного, внутримышечного, подкожного, внутрибрюшинного, интраназального, трансбуккального, чрескожного, внутрикожного путей, или в суппозиториях, как известно в данной области техники. В частности, соединения по настоящему изобретению можно вводить перорально; например, в виде фармацевтической композиции, пригодной для перорального введения (например, таблетки, капсулы, буккальные пленки, спрей или тому подобное).
В частности, фармацевтические композиции, пригодные для перорального введения, могут быть представлены в виде отдельных единиц, таких как капсулы или таблетки (например, таблетки), каждая из которых содержит заранее определенное количество активного ингредиента, и которая может включать пригодное вспомогательное вещество. Кроме того, перорально доступные составы могут быть в форме порошка или гранул, раствора или суспензии в водной или неводной жидкости, или жидкой эмульсии типа "масло-в-воде" или "вода-в-масле".
Композиции, предназначенные для перорального применения, могут быть получены согласно любому известному способу; причем такие композиции могут содержать один или более агентов, выбранных из группы, состоящей из подсластителей, ароматизаторов, красителей и консервантов, с тем чтобы обеспечить фармацевтически надлежащие и приятные на вкус препараты.
Например, таблетки могут содержать активный ингредиент(ы) в смеси с нетоксичными фармацевтически приемлемыми вспомогательными веществами, пригодными для изготовления таблеток. Такие вспомогательные вещества могут представлять собой, например, инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия; гранулирующие и дезинтегрирующие агенты, например, кукурузный крахмал или альгиновая кислота; связующие агенты, например, крахмал, желатин или гуммиарабик; и смазывающие агенты, например стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без покрытия или покрыты с помощью известных методов для замедления дезинтеграции и абсорбции в желудочно-кишечном тракте и тем самым для обеспечения пролонгированного действия в течение более длительного периода. Например, для задержки высвобождения может быть использовано вещество, такое как глицерилмоностеарат или глицерилдистеарат. Таблетки также могут быть покрыты с помощью методов, описанных в патентах США №4,356,108; 4,166,452; и 4,265,874, содержание которых включено в настоящее описание посредством ссылки, с целью получения осмотических терапевтических таблеток с контролируемым высвобождением.
Кроме того, составы для перорального применения могут быть представлены в виде твердых желатиновых капсул, в которых активный ингредиент смешан с инертным твердым разбавителем, например, карбонатом кальция, лактозой, фосфатом кальция или каолином, или в виде мягких желатиновых капсул, в которых активный ингредиент смешан с водной средой (такой как смешивающаяся с водой жидкость, например, полиэтиленгликоль) или масляной средой, например, арахисовым маслом, жидким парафином или оливковым маслом. Такие желатиновые капсулы могут быть составлены так, чтобы они содержали гранулы активного ингредиента, которые могут быть приготовлены (например, покрыты) таким образом, как описано в настоящем документе для таблеток.
Кроме того, составы для перорального применения могут быть представлены в форме таблеток, состоящих из прессованных микрочастиц (например, гранул), которые могут быть отдельно покрыты микрочастицами.
Таким образом, в вариантах реализации изобретения, в которых состав содержит микрочастицы (например, в капсуле или таблетке, такой как таблетка, состоящая из прессованных микрочастиц или капсул, содержащих гранулы), такие микрочастицы могут иметь различные покрытия (или составлены для замедленного высвобождения с использованием полимеров, как описано ниже), при этом такие покрытия/составы могут быть выбраны для регулирования высвобождения соединений по настоящему изобретению; например, для контроля абсорбции и визуализации профиля плазмы, имитирующего профиль PAI-1 в плазме. Применение таких покрытий/препаратов для контроля абсорбции/высвобождения лекарственного средства известно в данной области техники и может, например, основываться на различных полимерах, например, акриловой кислоты или целлюлозы, и описывается более подробно ниже.
Дозированные лекарственные формы, образованные множественными структурно обособленными единицами, в меньшей степени зависят от степени наполнения желудка и поэтому могут обуславливать меньшую вариабельность, например, абсорбционных профилей у разных пациентов.
Отдельные компоненты дозированных лекарственных форм, образованных множественными структурно обособленными единицами, могут быть приготовлены общеизвестными способами, включая гранулирование, окомковывание, экструзию, экструзию горячего расплава, таблетирование и/или нанесение покрытий. Примеры получения таблеток и/или капсул из покрытых оболочкой гранул/микротаблеток приведены, например, в WO 96/01621, WO 96/01624, Siddique, Khanam and Bigoniya, AAPS PharmSciTech 2010. Эти ссылки также предоставляют информацию о том, как различные материалы могут применяться для контроля высвобождения лекарственного средства из таблетки или капсулы (или из гранул в указанной таблетке или капсуле).
В частности, специалист в данной области техники будет знать, что вальпроевая кислота представляет собой жидкость, а вальпроат натрия гигроскопичен. Пригодные наполнители и способы получения этих типов ингредиентов известны в данной области техники и включают, например, покрытие компонентов подходящим полимером (например, сополимерами метакриловой кислоты разных типов) и/или нерастворимыми в воде материалами, такими как воски/жирные кислоты и т.д., для достижения пониженной гигроскопичности. Такие полимеры можно также применять для замедления высвобождения и/или абсорбции лекарственного средства согласно настоящему изобретению.
Для трансбуккального и сублингвального применения могут быть использованы кремы, мази, желе, растворы суспензий и тому подобное, содержащие соединения по настоящему изобретению.
Фармацевтические композиции также могут быть в форме суппозиториев для ректального введения соединений по настоящему изобретению. Указанные композиции могут быть получены путем смешивания соединения по настоящему изобретению с пригодным нераздражающим вспомагательным веществом, которое является твердым при обычной температуре, но жидким при ректальной температуре и, таким образом, будет расплавляться в прямой кишке с высвобождением лекарственного средства. Такие материалы включают, например, масло какао и полиэтиленгликоль.
Фармацевтические композиции, содержащие соединения по настоящему изобретению, также могут быть представлены в форме липосомных систем доставки, таких как небольшие однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы могут быть образованы из различных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Фармацевтические формы, пригодные для инъекционного применения, включают, но не ограничиваются ими, стерильные водные (водорастворимые) растворы или дисперсии и стерильные порошки для экстемпорального приготовления стерильных инъекционных растворов или дисперсий. Во всех случаях, лекарственная форма должна быть стерильной и должна быть жидкой до такой степени, чтобы ее можно было ввести с помощью шприца. Композиция должна быть стабильной при заданных условиях изготовления и хранения и должна быть защищена от загрязняющего воздействия микроорганизмов, таких как бактерии и грибы. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, стерильную воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.), их пригодные смеси и растительные масла. Надлежащая текучесть может поддерживаться, например, применением материалов покрытия, таких как лецитин, поддержанием необходимого размера частиц в случае дисперсий и применением поверхностно-активных веществ. Предупреждение воздействия микроорганизмов может быть достигнуто с помощью различных антибактериальных и противогрибковых агентов, таких как парабены, хлорбутанол, фенол, аскорбиновая кислота, тимеросал и т.п. Во многих случаях будет предпочтительным включать в композицию изотонические агенты, например, сахара или натрия хлорид. Пролонгированная абсорбция инъекционных композиций может быть обеспечена применением в композициях агентов, замедляющих абсорбцию, например, моностеарата алюминия и желатина.
Стерильные инъекционные растворы получают путем объединения активного материала в необходимом количестве в подходящем растворителе с различными другими ингредиентами, перечисленными выше, с последующей стерилизацией фильтрованием, в случае необходимости. Как правило, дисперсии получают путем включения различных стерилизованных активных ингредиентов в стерильную несущую среду, которая содержит основную дисперсионную среду и необходимые другие ингредиенты из перечисленных выше. В случае стерильных порошков для приготовления стерильных инъекционных растворов, предпочтительные способы приготовления представляют собой вакуумную сушку и сушку вымораживанием, в результате которых получают порошок активного ингредиента плюс любой дополнительный желательный ингредиент из раствора, предварительно стерилизованного фильтрованием.
Мы обнаружили, что соединения по настоящему изобретению можно с удобством вводить субъекту перорально, в частности, в виде таблетки или капсулы (например, таблетки). Более того, мы обнаружили, что конкретные схемы введения, рассматриваемые в настоящем изобретении, являются особенно пригодными для перорального введения в виде таблетки или капсулы, которая составляется таким образом, что высвобождение соединений по настоящему изобретению из указанной таблетки или капсулы после перорального введения замедляется.
В настоящем документе ссылки на составы, предусматривающие замедленное или контролируемое высвобождение, будут понятны специалистам в данной области техники. В этом отношении будет понятно, что термины "замедленный" и "контролируемый" могут использоваться взаимозаменяемо.
В восьмом аспекте настоящего изобретения предлагается фармацевтическая композиция, содержащая вальпровую кислоту или ее фармацевтически приемлемую соль; при этом композиция имеет форму таблетки или капсулы для перорального введения и составлена таким образом, что по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождается в течение периода времени от около четырех до около восьми часов после введения.
В настоящем документе ссылки на капсулы будут включать капсулы, наполненные активным ингредиентом в порошкообразной форме или в форме гранул и/или микрочастиц, причем гранулы и/или микрочастицы могут быть покрыты, как описано в настоящем документе, и капсула сама по себе может быть покрыта. Кроме того, гранулы могут быть приготовлены для конкретных профилей высвобождения с применением, например, различных замедляющих/контролируемых высвобождение полимеров (и/или нанесения покрытия на гранулы).
В настоящем документе ссылки на таблетку будут включать таблетки, полученные из прессованных гранул и/или микрочастиц, причем гранулы и/или микрочастицы могут быть покрыты, как описано в настоящем документе, и таблетка сама по себе может быть покрыта.
В настоящем документе (особенно в отношении восьмого аспекта изобретения, включая все его варианты реализации) термин "по существу все" будет относиться к количеству, которое составляет по меньшей мере 60% от общего присутствующего количества (т.е. общего количества, включенного в композицию). В частности, этот термин может относиться к количеству, которое составляет по меньшей мере 70% от общего количества, например, по меньшей мере 80% от общего количества. Конкретнее, этот термин может относиться к количеству, которое составляет по меньшей мере 90% от общего количества, например, по меньшей мере 95% (например, по меньшей мере 99%) от общего количества.
В конкретном варианте реализации восьмого аспекта изобретения ссылки по существу на всю вальпроевую кислоту или ее фармацевтически приемлемую соль, которые высвобождаются, могут относиться по существу ко всей одной дозе (т.е. по меньшей мере одной терапевтически эффективной дозе).
Специалисту в данной области техники будет понятно, что высвобождение активного ингредиента может быть отсрочено, если композиция вводится с приемом пищи или вскоре после приема пищи. Таким образом, ссылки на время, затрачиваемое на высвобождение активного ингредиента, могут относиться ко времени, затраченному на такое высвобождение, когда композицию вводят пациенту по меньшей мере через два часа после того, как этот пациент принимал пищу (что можно назвать введением натощак или тому подобное).
Также может быть оценена возможная польза от введения соединения по настоящему изобретению с пищей (например, для уменьшения побочных эффектов со стороны желудочно-кишечного тракта). Таким образом, в конкретном варианте реализации от первого до седьмого аспекта настоящего изобретения лечение включает введение вальпроевой кислоты или ее фармацевтически приемлемой соли с пищей (например, введение пациенту, который принимал пищу менее чем за два часа до введения или пациенту, который будет направлен на прием пищи в течение 30 минут после введения).
В данном контексте (особенно в отношении восьмого аспекта изобретения, включая все его варианты реализации) ссылки на активный ингредиент, который "высвобождается" (из фармацевтической композиции), будут относиться к активному ингредиенту, находящемуся в форме, которая доступна для абсорбции (т.е. системной абсорбции из желудочно-кишечного тракта при пероральном введении). Этот термин при использовании его в отношении таблеток и/или капсул для перорального введения будет указывать на то, что активный ингредиент не содержится в указанной таблетке или капсуле (которая может включать активный ингредиент, более не содержащийся в гранулах (например, покрытых гранулах) и/или микрочастицах, содержащихся в указанных таблетках или капсулах), но вместе с тем распределяется в желудочно-кишечном тракте.
В конкретном варианте реализации восьмого аспекта настоящего изобретения фармацевтическая композиция составлена таким образом, что по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождается в течение периода времени от около шести до около восьми часов после введения (например, от около шести до около семи часов после введения, или, например, от около семи до около восьми часов после введения, например, около семи часов после введения).
В более конкретных (и альтернативных) вариантах реализации восьмого аспекта настоящего изобретения фармацевтическая композиция составлена таким образом, что по существу вся вальпроевая кислота или ее фармацевтически приемлемая соль высвобождается в течение периода, который составляет:
(i) от около трех до около пяти часов после введения (от около четырех до около пяти часов после введения);
(ii) от около четырех до около шести часов после введения;
(iii) от около пяти до около семи часов после введения;
(iv) от около шести до около восьми часов после введения; или
(v) от около восьми до около десяти часов после введения.
В конкретном варианте реализации восьмого аспекта настоящего изобретения фармацевтическая композиция может дополнительно содержать один или более фармацевтически приемлемых вспомогательных веществ (например, фармацевтически приемлемый адъювант, разбавитель или носитель), таких как описанные в настоящем документе. В таких вариантах реализации соединения по настоящему изобретению могут быть представлены в смеси с указанным одним или более фармацевтически приемлемыми веществами.
Специалисту в данной области техники будет понятно, что фармацевтические составы (например, таблетки или капсулы), содержащие соединения по настоящему изобретению (такие как описанные в восьмом аспекте настоящего изобретения, включая его варианты реализации), будут содержать всю или часть терапевтически эффективной дозы соединений по настоящему изобретению.
Во избежание неоднозначности толкования, такая доза может быть представлена в одной единице композиции (например, в виде одной таблетки или капсулы) или может быть обеспечена комбинированным введением нескольких единиц состава, каждая из которых содержит соответствующую часть дозы (например, две таблетки, каждая из которых содержит половину требуемой дозы, или множество микрочастиц, каждая из которых содержит необходимую часть требуемой дозы).
В частности, указанные составы (например, таблетки для перорального введения) могут содержать одну терапевтически эффективную дозу. Таким образом, в конкретных вариантах реализации восьмого аспекта настоящего изобретения композиция включает дозу (например, общую суточную дозу) вальпроевой кислоты или ее фармацевтически приемлемую соль, как определено в любом одном или более аспектов изобретения (от первого до седьмого, включая все варианты их реализации).
В зависимости от требуемой дозы, фармацевтические составы, которые могут быть упомянуты, включают те, в которых активный ингредиент присутствует в количестве по меньшей мере 1% (или по меньшей мере 10%, по меньшей мере 30% или по меньшей мере 50%) по весу. То есть, отношение активного ингредиента к другим компонентам (например, фармацевтически приемлемого вспомогательного вещества) фармацевтической композиции составляет по меньшей мере 1:99 (или по меньшей мере 10:90, по меньшей мере 30:70 или по меньшей мере 50:50) по весу.
Таким образом, специалисту в данной области техники будет понятно, что в настоящем изобретении дополнительно предлагается способ получения фармацевтических составов, как описано в данном документе (например, описанный в восьмом аспекте изобретения, включая его варианты реализации), который включает составление соединений по настоящему изобретению с помощью способа, описанного в данном документе. В частности, такой процесс может включать следующие этапы:
(a) приведение соединений по настоящему изобретению в связь с одним или более фармацевтически приемлемыми вспомогательными веществами (например, для образования их смеси); а также
(b) составление в виде таблетки или капсулы (как описано в настоящем документе).
Специалисту в данной области техники будет понятно, что термин "приведение в связь" означает, что соответствующие компоненты являются пригодными для введения в комбинации друг с другом.
Как описано в данном документе, соединения по настоящему изобретению могут вводиться и/или составляться в форме, покрытой веществом или вводимым с ним, для замедления высвобождения активного ингредиента. В частности, препараты в форме таблетки могут быть покрыты таким веществом и/или составлены из полимеров, которые регулируют высвобождение. Кроме того, состав в форме капсулы может быть составлен таким образом, что капсула составлена из или содержит количество (т.е. эффективное количество) такого вещества.
Таким образом, фармацевтические композиции по восьмому аспекту изобретения могут упоминаться как композиции "с замедленным высвобождением" или композиции с "контролируемым высвобождением" или тому подобное.
В таких случаях специалисту в данной области техники будет понятно, что вещество для замедления высвобождения активного ингредиента будет выбираться и/или составлятьсятаким образом, чтобы замедлять высвобождение активного ингредиента в течение требуемого времени (например, в течение около шести часов).
Специалисту в данной области техники будут известны вещества, применяемые для замедления (т.е. задержки) высвобождения активных ингредиентов, особенно при введении в форме или пероральных композициях (таких как таблетки и капсулы). Такие вещества могут быть описаны, например, в Remington's Pharmaceutical Science и US Pharmacopeia (Фармакопея Соединенных Штатов - Национальный формуляр (USP-NF), Remington: The Science and Practice of Pharmacy, 19 Ed. (Easton, Pa.: Mack Publishing Company, 1995); Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa. 1975; Liberman, H. A. and Lachman, L, Eds., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980; and Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Ed. (Lippincott Williams Wilkins 1999), содержание которых включено в настоящее описание в полном объеме.
Например, вещества, применяемые для замедления высвобождения активных ингредиентов могут включать полимеры с замедленным высвобождением, такие как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза, хитозан, слизь алоэ, пектин, этилцеллюлоза, поливинилхлорид, полиэтилен и поливинилпирролидон (ПВП) (например, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, карбоксиметилцеллюлоза, хитозан, слизь алоэ, пектин, этилцеллюлоза, поливинилхлорид и полиэтилен). Кроме того, одним из способов получения покрытия с замедленным высвобождением является смешивание водорастворимого полимера, такого как НРМС, с водонерастворимым полимером, таким как этилцеллюлоза. Специалисту в данной области техники будет понятно, что различные применяемые вещества и различные их соотношения приведут к различным моделями высвобождения и смогут адаптировать состав соответствующим образом (то есть добиться желаемого профиля высвобождения).
Специалисту в данной области техники будет понятно, что когда композиции вводят и/или составляют в форме, покрытой или вводимой с веществом, для замедления высвобождения активного ингредиента, упомянутое вещество материал может состоять из более чем одной фармацевтически приемлемой субстанции (например, одного или более фармацевтически приемлемого покрытия). Например, когда композиции по восьмому аспекту настоящего изобретения вводят в форме таблетки, указанная таблетка может содержать одно или более фармацевтически приемлемых покрытий из вещества, замедляющего высвобождение активного ингредиента.
В таких случаях специалисту в данной области техники будет понятно, что замедление высвобождения активного ингредиента из композиции (например, таблетки) достигается в результате комбинированного эффекта этих покрытий. Например, когда таблетка покрыта так, чтобы замедлить высвобождение в течение в общей сложности шести часов после перорального введения, таблетка может содержать два слоя покрытия, при этом каждое покрытие замедляет высвобождение в течение трех часов (или одно покрытие замедляет высвобождение в течение двух часов и одно дополнительное покрытие замедляет высвобождение в течение четырех часов), то есть после удаления первого покрытия воздействию подвергается второе покрытие и так далее (другими словами, указанные покрытия подвергаются воздействию последовательно).
В конкретных вариантах реализации восьмого аспекта настоящего изобретения, когда композиции по восьмому аспекту настоящего изобретения содержат одно или более покрытий (например, находятся в виде таблетки с покрытием), одно или более из указанных покрытий могут представлять собой покрытие для предотвращения высвобождения активного ингредиента или предотвращения воздействия на дополнительные покрытия в желудке. В частности, одно или более (например, одно) из указанных покрытий могут быть энтеросолюбильным покрытием. Указанные энтеросолюбильные покрытия будут хорошо известны специалисту в данной области техники.
В некоторых вариантах реализации восьмого аспекта настоящего изобретения (в частности, относящихся к таблеткам, имеющим одно или более покрытий), сердцевинный компонент (например, сердцевинный компонент таблетки с покрытием) может содержать один или более компонентов, предназначенных для содействия дезинтеграции в водной среде.
Таким образом, в конкретном варианте реализации восьмого аспекта настоящего изобретения состав представлен в виде таблетки (или капсулы) для перорального введения, содержащей одну или более сердцевин с покрытием (например, одна сердцевина с покрытием или множество гранул или микрочастиц с покрытием, имеющих такую сердцевину), при этом указанная(ые) сердцевина(ы) содержит(ат) вальпровую кислоту или ее фармацевтически приемлемую соль, причем:
(i) указанное покрытие сформировано из вещества, выбранного и/или составленного таким образом, чтобы замедлять выделение активного ингредиента в течение требуемого времени (например, в течение около шести часов); а также
(ii) указанная сердцевина составлена таким образом, чтобы способствовать дезинтеграции в водной среде (например, содержащей один или более дезинтегрантов).
Такие дезинтегранты будут хорошо известны специалистам в данной области техники, включая агенты, предназначенные для набухания при контакте с водными средами.
Специалисту в данной области техники будет понятно, что существует несколько веществ, которые могут применяться для формирования энтеросолюбильного покрытия на таблетке/капсуле и/или гранулах/микротаблетах/пеллетах/дозированных лекарственных формах, образованных множественными структурно обособленными единицами/частицами. Эти вещества включают, но не ограничиваются, шеллак, воски, жирные кислоты, полимеры, пластмассы и растительные волокна.
Примеры таких полимеров включают, но не ограничиваются ими, фталат гипмеллозы (фталат гидроксипропилметилцеллюлозы, НРМСР), сукцинат ацетат гипмеллозы, тримеллитат ацетат целлюлозы, сополимеры акриловой кислоты/метакриловой кислоты (например, поли(метакриловая кислота-со-метилметакрилат), ацетатфталат целлюлозы (CAT), поли(винилацетатфталат, PVAP) и этилакрилат. Другие вещества для энтеросолюбильного покрытия включают декстрины, амилозный крахмала и производные крахмала, натрия альгинат, Зейн и Аква-Зейн R.
Коммерчески доступные системы для энтеросолюбильных покрытий и покрытий для длительного высвобождения включают варианты ОПАДРИ® (Colorcon), Титанкоат, Колликоат® (BASF), Эудрагит®, (например, Эудрагит® RL, Эудрагит® RS, Эудрагит® S, Эудрагит® L и Эудрагит® Е), Шефкоат ЕС and Шефкоат Ent.
Специалисту в данной области техники будет понятно, что различные вещества имеют различные свойства, например, можно использовать вещество с более щелочными характеристиками рН для контроля профиля абсорбции, например, замедляя высвобождение лекарственного средства в течение определенного времени. Также, для получения определенного профиля можно изменять толщину покрытия. Кроме того, в случае применения покрытых гранул, например, в капсуле или прессованной таблетке, с целью имитации профиля концентрации PAI-1 в плазме для соединений по настоящему изобретению могут применяться различные покрытия (и/или толщина покрытий). Более конкретно, комбинация из нескольких (например, 2-5) гранул/микрочастиц с различным покрытием можно применять для достижения желаемого эффекта с целью имитации профиля концентрации PAI-1 в плазме для соединений по настоящему изобретению.
Одним из способов продления замедления абсорбции энтеросолюбильного покрытия является смешивание полимера с энтеросолюбильным покрытием с меньшим количеством полимера с замедленным высвобождением; как описано, например, в работе Tirpude and Puranik, J Adv Pharm Technol Res 2011, авторы которой смешивали 10% акриловых полимеров с пролонгированным высвобождением (Eudragit NE30D) с 90% энтеросолюбильных акриловых полимеров (Eudragit L30D555). Таким образом, вещества, такие как полимеры с различными характеристиками растворения, могут комбинироваться в различных соотношениях для достижения желаемого профиля абсорбции согласно настоящему изобретению. Другие примеры способов получения различных профилей абсорбции с применением различных гидрофильных полимеров и способов приготовления матричных таблеток из гранул описаны в Roy, Brahma, Nandi and Parida, Int J Appl Basic Med Res. 2013.
Различные способы достижения регулируемого высвобождения с применением матричных таблеток и описание различных полимеров и матриц также приведены в http://www.pharmainfo.net/reviews/matrix-tablets-important-tool-oral-controlled-release-dosage-forms, что полностью включено в настоящую заявку посредством ссылки.
Для более подробной информации о энтеросолюбильных покрытиях см., например, Singh Deep Hussan et al., IOSR Jounal of Pharmacy (2012), и Handbook of Pharmaceutical Excipients Rowe, Raymond C; Sheskey, Paul J; Cook, Walter G; Fenton, Marian E., Seventh edition, содержание которых полностью включено в настоящую заявку посредством ссылки.
Для некоторых покрытий может потребоваться применение пластификатора(ов) для получения надлежащих результатов, при этом о таких агентах специалисту в данной области техники известно. Такие пластификаторы включают, например, цитратные эфиры, глицерин, пропиленгликоль, диэтилфталат, дибутилфталат, дибутилсебакат, трибутилцитрат, ацетилированные моноглицериды, триацетин и глицеринтриацетат.
Пигменты и/или эти пластификаторы могут быть добавлены, например, к полимерному раствору для улучшения технических характеристик, например, мембраны, или изменения параметров высвобождения.
Для предотвращения инактивации соединения по настоящему изобретению могут быть покрыты или вводиться с веществом. Например, активное вещество можно вводить в адъюванте, например, вводить совместно с ферментными ингибиторами или в липосомах. Адъюванты, рассматриваемые в настоящем документе, включают, но не ограничиваются ими, резорцины, неионные поверхностно-активные вещества, такие как полиоксиэтиленовый олеиловый эфир и n-гексадецилполиэтиленовый эфир. Ингибиторы ферментов включают; но не ограничиваются ими, ингибитор трипсина поджелудочной железы, диизопропилфторфосфат (DFP) и трасилол. Липосомы включают эмульсии Р40 типа вода-в-масле-в-воде, а также обычные липосомы. Дисперсии также могут быть получены в глицерине, жидких полиэтиленгликолях и их смесях и в маслах. При обычных условиях хранения и применения эти препараты содержат консервант для предотвращения роста микроорганизмов.
Как описано в настоящем документе, специалисту в данной области техники будет понятно, что при пероральном введении активное соединение может быть объединено с инертным разбавителем или пригодным к употреблению в пищу носителем или может быть заключено в желатиновую капсулу с твердой или мягкой оболочкой или может быть прессовано в таблетки, или может быть включено непосредственно в пищевой рацион. Для перорального терапевтического введения активное вещество можно совмещать со вспомогательными веществами и применять в форме таблеток для проглатывания, буккальных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, облаток и т.п. Кроме того, активное вещество может быть включено в препараты и композиции с замедленным высвобождением. Например, активное вещество может быть включено в таблетки/капсулы с энтеросолюбильной оболочкой и/или двухфазные составы для высвобождения, которые будут известны специалистам в данной области техники. Например, состав с двухфазным высвобождением может быть такого типа, как описано в публикации US 2007/0232528 A1 (содержание которой включено в настоящий документ в полном объеме), причем составы могут быть пригодными для введения в период от около 22:00 до 00:00 часов (например, около 23:00 часов).
В данном контексте термин "фармацевтически приемлемое вспомогательное вещество" будет включать фармацевтически приемлемые адъюванты, разбавители и носители, известные специалистам в данной области техники. Вспомогательные вещества могут включать любые и все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические и замедляющие абсорбцию агенты и тому подобное.
Таким образом, таблетки, пастилки, пилюли, капсулы и тому подобное могут также содержать следующие элементы: связующий агент, такой как трагакант, аравийская камедь, кукурузный крахмал или желатин; вспомогательные вещества, такие как дикальцийфосфат; дезинтегрирующий агент, такой как кукурузный крахмал, картофельный крахмал, альгиновая кислота и тому подобное; смазывающий агент, такой как стеарат магния; также может быть добавлен подсластитель, такой как сахароза, лактоза или сахарин, или ароматизатор, такой как перечная мята, гаультериевое масло или ароматизатор вишни. Когда стандартная лекарственная форма представляет собой капсулу, она может содержать, помимо веществ вышеуказанного типа, жидкий носитель. В составе покрытий могут содержаться различные другие вещества; при этом эти вещества могут модифицировать физические характеристики стандартной лекарственной формы иным образом. Например, таблетки, пилюли или капсулы могут быть покрыты шеллаком, сахаром или и тем и другим. Сироп или эликсир могут содержать активное соединение, сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консервантов, краситель и ароматизаторы, такие как вишневый или апельсиновый ароматизаторы. Разумеется, любой материал, применяемый при приготовлении любой стандартной лекарственной формы, должен быть фармацевтически чистым и по существу нетоксичным в применяемых количествах.
Применение таких вспомогательных веществ хорошо известно в данной области техники; см., например, в Remington's Pharmaceutical Science и US Pharmacopeia (Фармакопея Соединенных Штатов - Национальный формуляр (USP-NF), Remington: The Science and Practice of Pharmacy, 19 Ed. (Easton, Pa.: Mack Publishing Company, 1995); Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa. 1975; Liberman, H.A. and Lachman, L, Eds., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980; and Pharmaceutical Dosage Forms and Drug Delivery Systems, 7th Ed. (Lippincott Williams Wilkins 1999).
Как описано в настоящем документе, таблетки и/или капсулы, составленные для замедленного высвобождения соединений по настоящему изобретению из указанной таблетки после перорального введения (как описано в восьмом аспекте изобретения и его вариантах реализации), особенно пригодны для применения при лечении или профилактике патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов в соответствии с конкретными схемами введения, описанными в данном документе.
Таким образом, в девятом аспекте настоящего изобретения предлагается фармацевтическая композиция, как описано в восьмом аспекте настоящего изобретения (включая любой один или более вариантов его реализации) для применения в лечении или профилактике патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов, причем указанное лечение является таким, как описано в любом аспекте настоящего изобретения (от первого до седьмого, включая любой один или более вариантов их реализации).
В альтернативном девятом аспекте настоящего изобретения предлагается применение фармацевтической композиции, как описано в восьмом аспекте настоящего изобретения (включая любой один или более вариантов его реализации), в изготовлении лекарственного средства для применения в лечении или профилактике патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов, причем указанное лечение является таким, как описано в любом (с первого по седьмой) аспекте настоящего изобретения, (включая любой один или более вариантов их реализации).
В дополнительном альтернативном девятом аспекте настоящего изобретения предлагается способ лечения или профилактики патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов у пациента, имеющего для этого показания, как описано в любом (с первого по седьмой) аспекте настоящего изобретения, (включая любой один или более вариантов их реализации), при этом вальпроевую кислоту или ее фармацевтически приемлемую соль вводят в форме фармацевтической композиции, как описано в восьмом аспекте настоящего изобретения (включая любой один или более вариантов его реализации).
Как описано в настоящем документе, специалист в данной области техники сможет регулировать состав и способ введения соединений по настоящему изобретению для достижения желаемых параметров, таких как желаемое время и/или уровни концентрации в плазме конкретных агентов.
Например, специалисту в данной области техники известно, что различные составы соединений по настоящему изобретению являются коммерчески доступными и могут быть введены способом, пригодным для применения, в частности, в лечении, как описано в аспектах (с первого по седьмой) настоящего изобретения.
Таким образом, в конкретных вариантах реализации изобретения (например, конкретные варианты реализации от первого по седьмой и девятого аспектов изобретения) предлагается вальпроевая кислота или ее фармацевтически приемлемая соль для применения в лечении или профилактике патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов; при этом указанное лечение включает введение пациенту дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в форме (т.е. введение определенного состава) и в определенной дозе и времени, как указано в следующей таблице.
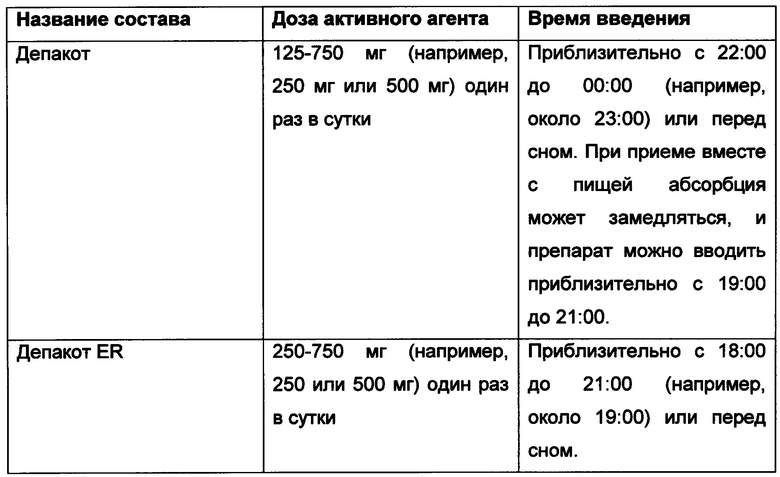
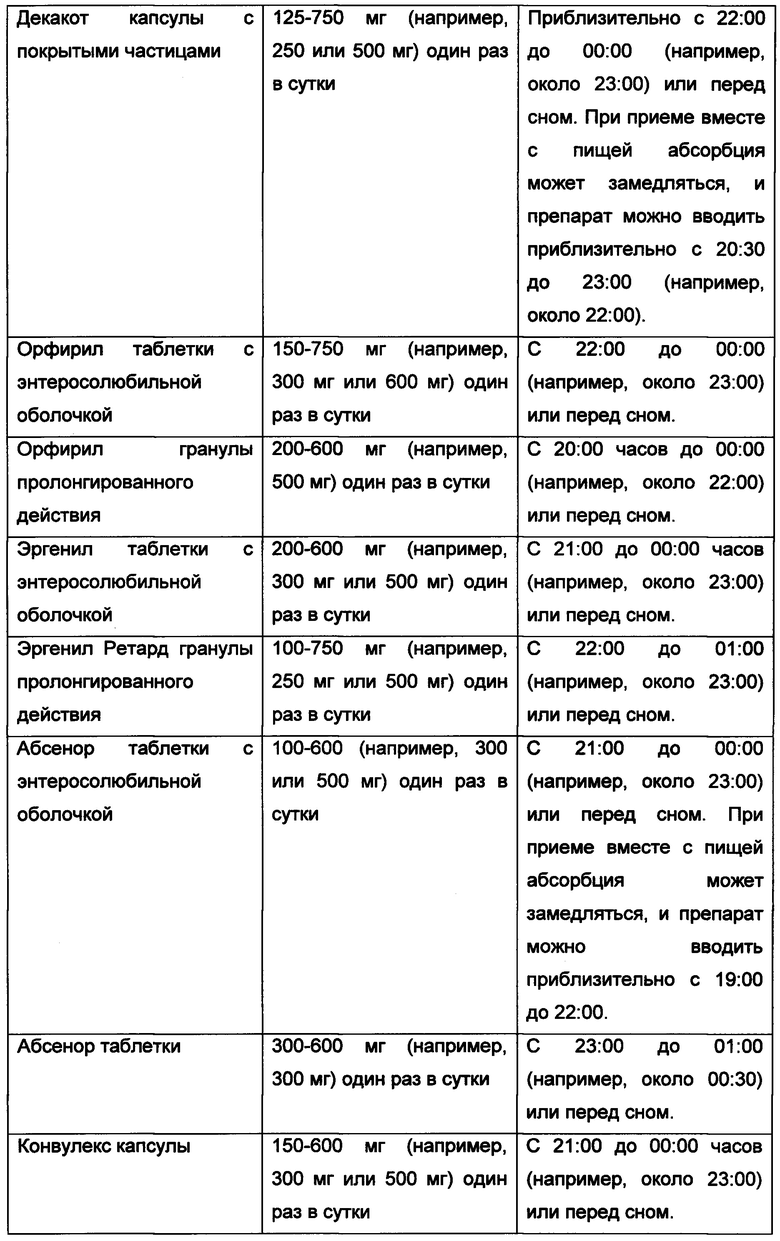
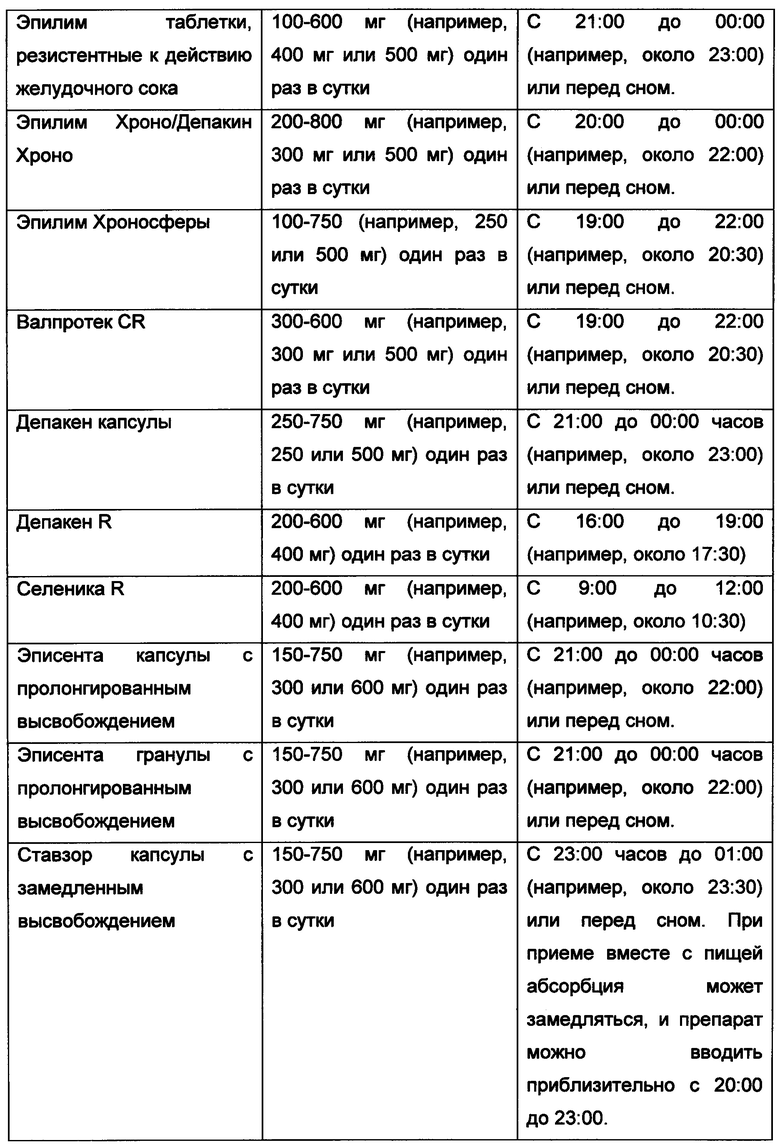

В данном контексте ссылки на название некоторых составов будут относиться к соответствующему составу, который продается/доступен на рынке соответствующей территории (например, в США, Великобритании или Швеции) по состоянию на 1 октября 2014 года.
Ссылки в приведенной выше таблице на конкретные составы с конкретным названием будут содержать ссылки на по существу идентичные составы, которые могут иметь другое название (например, идентичные составы, продаваемые и/или доступные на рынке с другим названием продукта).
Как описано в настоящем документе, специалисту в данной области техники будет понятно, что введение препарата пациенту с пищей или вскоре после приема пищи может замедлять высвобождение активного ингредиента, что позволяет соответствующим образом регулировать время введения. Если не указано иное, ссылки на введение конкретного состава в определенное время (например, в течение определенного периода времени) будут относиться к введению пациенту натощак.
Комбинированные способы лечения
Соединения по настоящему изобретению можно также вводить в комбинации (например, в комбинированном препарате) с другими терапевтическими агентами, которые пригодны для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов.
В частности, фармацевтические композиции, описанные в восьмом аспекте изобретения (включая его варианты реализации), могут включать соединения по настоящему изобретению вместе с одним или более фармацевтически приемлемыми вспомогательными веществами и одним или более другими терапевтическими агентами, которые могут быть пригодны для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов.
В конкретном варианте реализации от первого до седьмого аспекта изобретения вальпроевую кислоту или ее фармацевтически приемлемую соль вводят в комбинации с одним или более (например, одним) другими терапевтическими агентами, которые могут применяться для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов.
В конкретном варианте реализации восьмого аспекта изобретения фармацевтический состав дополнительно содержит один или более (например, один) других терапевтических агентов, которые пригодны для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов. В таких вариантах реализации изобретения, соединения по настоящему изобретению могут быть представлены в смеси с указанным одним или более другими терапевтическими агентами.
Таким образом, специалисту в данной области техники будет понятно, что в изобретении дополнительно предлагается способ получения фармацевтических составов, как описано в настоящем документе (таких, как описаны в восьмом аспекте изобретения, включая варианты его реализации), причем этот способ включает следующие этапы:
(a) приведение соединений по настоящему изобретению в связь с одним или более фармацевтически приемлемыми вспомогательными веществами (например, для образования их смеси); и/или одним или более (например, одним) другими терапевтическими агентами, которые могут быть пригодны для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов; а также
(b) составление в виде таблетки или капсулы (как описано в настоящем документе, например, с одним или более покрытиями).
Как упоминается в настоящем документе, другие терапевтические агенты, которые пригодны для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, включают: один или более антитромболитических агентов; и/или один или более антикоагулянтов; и/или один или более антиагрегантов; и/или один или более вазодилататоров, как известно специалистам в данной области техники.
В конкретных вариантах реализации, соединения по настоящему изобретению можно вводить и/или составлять в комбинации с:
- одним или более антитромбоцитарными агентами, включая но не ограничиваясь, аспирин, персантин, тикагрелор и клопидогрель;
- одним или более антикоагулянтами, такими как гепарин, низкомолекулярный гепарин (НМГ), варфарин, анизиндион, фениндон, бисидроксику марин, бивалирудин, эптифибатид; одним или более вазодилататорами, такими как нитрилы (например, амилнитрил, нитроглицерин, нитрил натрия, изосорбид динитрат), папаверин, никотиновая кислота и циклодельтат.
- одним или более агентов, предотвращающих сердечно-сосудистые патологии, но не ограничиваясь ими, статины, бета-блокаторы, ингибиторы ангиотензинпревращающего фермента, антагонисты рецепторов ангиотензина II или диуретики; и/или
- одним или более противовоспалительных средств, включая стероиды и НПВС (включая, но не ограничиваясь ими, аспирин, ибупрофен, напроксен и диклофенак);
- одним или более тромболитических агентов, выбранных, например, из рекомбинантного
t-PA, проурокиназы, урокиназы или стрептокиназы.
В более конкретных вариантах реализации, соединения по настоящему изобретению можно вводить и/или составлять в комбинации с аспирином (т.е. терапевтически эффективным количеством аспирина).
В еще более конкретных вариантах реализации, соединения по настоящему изобретению можно вводить и/или составлять в комбинации с клопидогрелем (т.е. терапевтически эффективным количеством клопидогреля) или тикагрелором (т.е. терапевтически эффективным количеством тикагрелора).
Во избежание неоднозначности толкования, специалисту в данной области техники будет понятно, что термин "введение в комбинации с" включает сопутствующее, последовательное и раздельное введение. В этом отношении, последовательное введение может относиться к введению в рамках одного и того же терапевтического вмешательства (например, в течение одного часа после введения соединения по настоящему изобретению).
Специалисту в данной области техники будет понятно, что ссылки на агент, который вводится в комбинации с другим агентом, могут также содержать набор компонентов, содержащий соответствующие агенты (т.е. как отдельные компоненты в одном наборе).
Специалисту в данной области техники также будет понятно, что ссылки на первый агент, вводимый в комбинации со вторым агентом, также будут относиться ко второму агенту, вводимому в комбинации с первым агентом и так далее.
Группы пациентов
Специалисту в данной области техники будет понятно, что ссылки в настоящем документе на "пациента" относятся к живым животным, которые могут подвергаться лечению или профилактике, описанным в настоящем документе. В частности, термин "пациент" будет относиться к млекопитающему. Конкретнее, термин "пациент" будет относиться к человеку (такому как взрослый человек).
Соединения по настоящему изобретению могут быть особенно пригодными в лечении или профилактике (в частности, профилактике) патологических состояний, связанных с избыточным осаждением фибрина и/или образованием тромбов (таких как описанные в настоящем документе) у пациентов с повышенным риском развития одного или более указанных патологических состояний.
В конкретном варианте реализации от первого до седьмого аспектов изобретения (включая все варианты их реализации), лечение или профилактика (например, профилактика, которая также может называться предупреждением) проводятся пациенту с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов (при этом специалист в данной области техники будет понимать это воздействие как направленное на уменьшение риска развития соответствующего состояния, как описано в настоящем документе).
Как описано в настоящем документе, несколько патологических состояний и факторов риска ассоциированых с повышенной восприимчивостью к тромботическим патологиям (т.е. образованию тромбов). К таким состоянием относятся атеросклероз, гипертензия, абдоминальное ожирение, курение, малоподвижный образ жизни и неспецифическое воспаление. Таким образом, в конкретных вариантах реализации от первого до седьмого аспектов изобретения (включая все варианты их реализации), лечение или профилактика (например, профилактика, которая также может называться предупреждением) проводятся пациенту, имеющего одно или более таких патологических состояний/факторов риска.
В более конкретных вариантах реализации изобретения пациент с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, является пациентом, который:
(i) страдает одним или более патологическими состояниями, связанными с повышенным риском образования тромбов, такими как метаболический синдром (например, диабет типа II), онкологические заболевания, сердечная недостаточность, почечная недостаточность и/или сепсис;
(ii) в анамнезе имел один или более случаев патологического состояния, связанного с повышенным риском образования тромбов, таких как один или более случаев инфаркта миокарда, ишемического инсульта и легочной эмболии (например, один или более случаев ишемического инсульта, такого как обширный ишемический инсульт, ишемический микроинсульт или ТИА); и/или
(iii) имеет один или более факторов образа жизни и/или окружающей среды, которые ставят пациента под упомянутый повышенный риск, такие как курение, ожирение и/или малоподвижность (например, лежачий больной, такой как пациент стационара или учреждения по уходу за престарелыми людьми).
Таким образом, в конкретных вариантах реализации изобретения ссылки на пациента с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, будут включать ссылки на пациента с ожирением, например пациента с индексом массы тела (ИМТ), который составляет больше 25 (например, больше 30 и больше 35).
В данном контексте ссылки на пациента с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, могут также включать пациентов (например, пациентов мужского пола), достигших 50-летнего возраста или старше (например, 60-летнего возраста или старше).
В конкретных вариантах реализации изобретения пациент с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, может также быть пациентом с повышенными уровнями PAI-1.
Например, как описано в настоящем документе, пациент с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, может также быть пациентом, у которого диагностировано местное или системное воспаление, например, ассоциированное с повышенными уровнями PAI-1.
Таким образом, в конкретных вариантах реализации изобретения пациент с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, может быть пациентом, имеющим уровни PAI-1 в утренней плазме выше около 20 нг/мл (например, выше около 40 нг/мл, например, выше около 60 нг/мл, например, выше около 80 нг/мл или, более конкретно, выше около 100 нг/мл).
Например, пациент с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, может быть пациентом, имеющим уровни PAI-1 в утренней плазме выше около 20 нг/мл (например, выше около 40 нг/мл, например, выше около 60 нг/мл, например, выше около 80 нг/мл или, более конкретно, выше около 100 нг/мл), и в анамнезе у которого зарегистрирован один или более случаев инфаркта миокарда, ишемического инсульта и легочной эмболии (например, один или более случаев ишемического инсульта, таких как обширный ишемический инсульт, ишемический микроинсульт или ТИА).
В некоторых вариантах реализации изобретения пациент не страдает от:
(i) патологии ЦНС или психического расстройства, такого как эпилепсия, мигрень и/или биполярное расстройство; и/или
(ii) синдрома фрагильной Х-хромосомы и/или семейного аденоматозного полипоза.
Таким образом, в конкретном варианте реализации от первого до седьмого аспекта изобретения (включая все варианты их реализации) лечение или профилактика (например, профилактика) проводится у пациента, который:
(a) имеет повышенный риск развития патологического состояния, с избыточным отложением фибрина и/или образованием тромбов (в частности, как определено в настоящем документе); а также
(b) не имеет патологии ЦНС или психического расстройства (как определено в настоящем документе, в частности эпилепсии и/или биполярного расстройства).
Фигуры
На Фигуре 1 схематически представлен циркадный ритм (т.е. изменения) уровней PAI-1 у взрослого человека в течение типового 24-часового периода. Нижняя кривая представляет собой изменение уровней PAI-1 у нормального (т.е. здорового) пациента. Верхняя кривая представляет собой изменение уровней PAI-1 у пациента, имеющего повышенные уровни PAI-1 (например, у пациентов с ожирением и/или метаболическим синдромом). Ось у представляет собой произвольные уровни в плазме и укорочена для иллюстрации положительно искаженного распределения в сторону высоких плазменных уровней при ожирении/метаболическом синдроме. Ось х представляет собой время на часах.
Примеры
Следующие примеры включены для дополнительной иллюстрации настоящего изобретения, хотя специалисту в данной области техники будет понятно, что изобретение никоим образом не ограничено конкретными аспектами, описанными в нем.
Пример 1. VPA и PAI-1
Эффекты VPA на PAI-1 были проанализированы в двух разных исследованиях обоснованности концепции с участием здоровых субъектов, а также у пациентов с выраженной атеросклеротической болезнью. Исследования имели рандомизированный перекрестный дизайн, а уровни PAI-1 анализировали до и после ингибирования HDAC с помощью вальпроевой кислоты. Уровни PAI-1 в плазме измеряли утром в первый день исследования, а также в конце периода лечения с помощью VPA (см. пример 2 для получения подробной информации об анализе РАI-1).
В первом исследовании 10 здоровых некурящих белых мужчин (со средним ИМТ около 26) в возрасте 50-70 лет были включены и лечились вальпроевой кислотой (Ergenyl Retard, Sanofi) по 500 мг два раза в сутки в течение 14 дней. Неожиданно мы обнаружили более чем 50% снижение (с 22,2 до 10,8 нг/мл, р<0,05) уровней циркулирующего PAI-1 в плазме в течение периода середины утра по сравнению с уровнями периода середины утра, регистрируемыми до лечения VPA.
Во втором исследовании принимали участие 16 некурящих белых мужчин в возрасте 50-80 лет с инфарктом миокарда в анамнезе. В дополнение к обычным назаначениям (бета-блокаторы, ингибиторы АПФ, статины, аспирин) пациенты принимали 500 мг вальпроевой кислоты (Ergenyl Retard, Sanofi) два раза в сутки в течение 28 дней. В этом исследовании мы обнаружили 45% снижение уровней циркулирующего PAI-1 в плазме (с 19,6 нг/мл до 11 нг/мл (р=0,01) в течение периода середины утра.
Пример 2. Промежуточное исследование конечных критериев оценки: Эффекты вальпроевой кислоты на уровень PAI-1 у человека in vivo
Промежуточное исследование конечных критериев оценки с обоснованностью концепции проводили среди пациентов с ТИА/микроинсультом; причем оценку проводили до и после лечения вальпроевой кислотой. Вальпроевую кислоту вводили в форме таблетки с энтеросолюбильной оболочкой с замедленной абсорбцией.
В исследовании участвовали 20 пациентов с ТИА/микроинсультом. Пациентов исследовали до и после перорального приема 400 мг вальпроевой кислоты один раз в сутки в 11 часов вечера в течение 2 недель. Уровни PAI-1 в плазме и концентрации вальпроевой кислоты в плазме ежедневно анализировали в течение периода исследования в следующие моменты времени: 03:00, 06:00, 10:00, 16:00 и 22:00. Уровни PAI-1 измеряли с помощью коммерчески доступного набора ELISA (Coaliza PAI-1, Chromogenix АВ), а концентрацию вальпроевой кислоты и ее метаболитов в плазме крови анализировали в соответствии с установившейся клинической практикой в лаборатории Университета Sahlgrenska, Гетеборг, Швеция.
Установлено, что пиковая концентрация вальпроевой кислоты в плазме определяется в период от 03:00 до 06:00 утра, а затем снижается до очень низких уровней при минимальных концентрациях РАI-1. пиковая концентрация вальпроевой кислоты в плазме совпадает с пиковым уровнем PAI-1 в плазмы в период от 03:00 до 06:00 утра. Концентрация вальпроевой кислоты и уровней PAI-1 в плазме следуют друг за другом с выраженным циркадным подъемом с пиком в ранние утренние часы. Уровни PAI-1 в плазме после лечения снижаются примерно на 30%.
Пример 3. Исследование клинических исходов у пациентов с высоким риском, получавших вальпроевую кислоту с целью профилактики рецидивов тромбоэмболических патологий
Исследование клинических исходов проводили среди пациентов высокого риска, которые в недавнем анамнезе перенесли обширное атеротромботическое сердечно-сосудистое поражение (инфаркт миокарда или ТИА/ишемический инсульт), с целью анализа профилактического эффекта введения вальпроевой кислоты на риск возникновения рецидивов. Ежегодный риск рецидива атеротромботической патологии у исследуемой популяции оценен примерно в 7%.
В параллельном исследовании пациентов рандомизировали для получения двойного заслепленного лечения с пероральным применением 400 мг вальпроевой кислотой (как в Примере 2) или плацебо один раз в сутки в 11 часов вечера, в дополнение к оптимальной традиционной терапии. Частоту событий контролировали с помощью статистики Каплана- Мейера. Первичным критерием оценки эффективности являлась комбинированная частота либо смертности, либо несмертельного инфаркта миокарда или ишемического инсульта. Исследование было событийно-управляемым в общей сложности 180 событиями.
Ожидается, что исследование докажет снижение указанного риска на около 30% в результате длительного приема вальпроевой кислоты в дополнение к обычной терапии, т.е. снижение ежегодной абсолютной частоты событий до около 5%. Таким образом, ожидается, что исследование подтвердит клиническую эффективность и возможность применения вальпроевой кислоты для вторичной профилактики сердечно-сосудистых заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ С ОТСРОЧЕННЫМ ВЫСВОБОЖДЕНИЕМ, СОДЕРЖАЩИЕ ВАЛЬПРОЕВУЮ КИСЛОТУ, И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2760304C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ТРОМБООБРАЗОВАНИЯ ИЛИ ЭМБОЛИИ | 2011 |
|
RU2611662C2 |
| СОСТАВ ДЛЯ ИНГИБИРОВАНИЯ ОБРАЗОВАНИЯ АГОНИСТОВ 5-HT2B И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2017 |
|
RU2746000C2 |
| АНТИТРОМБОТИЧЕСКИЕ СОЕДИНЕНИЯ | 2012 |
|
RU2604733C2 |
| ТРОМБОЛИТИЧЕСКИЕ СРЕДСТВА | 1995 |
|
RU2142799C1 |
| ЛЕЧЕНИЕ ГИПЕРКИНЕТИЧЕСКИХ ДВИГАТЕЛЬНЫХ РАССТРОЙСТВ | 2015 |
|
RU2753740C2 |
| ВВЕДЕНИЕ ДЕЙТЕРИРОВАННЫХ УСИЛИТЕЛЕЙ CFTR | 2016 |
|
RU2761344C2 |
| Твердые композиции на основе бетагистина для перорального применения с непульсирующим пролонгированным высвобождением | 2018 |
|
RU2774644C2 |
| СПОСОБЫ И КОМПОЗИЦИИ С ПРИМЕНЕНИЕМ ИММУНОМОДУЛИРУЮЩИХ СОЕДИНЕНИЙ ПРИ КОМБИНИРОВАННОМ ЛЕЧЕНИИ | 2007 |
|
RU2426542C2 |
| НОВЫЕ КОМПОЗИЦИИ И СПОСОБЫ | 2018 |
|
RU2767410C2 |
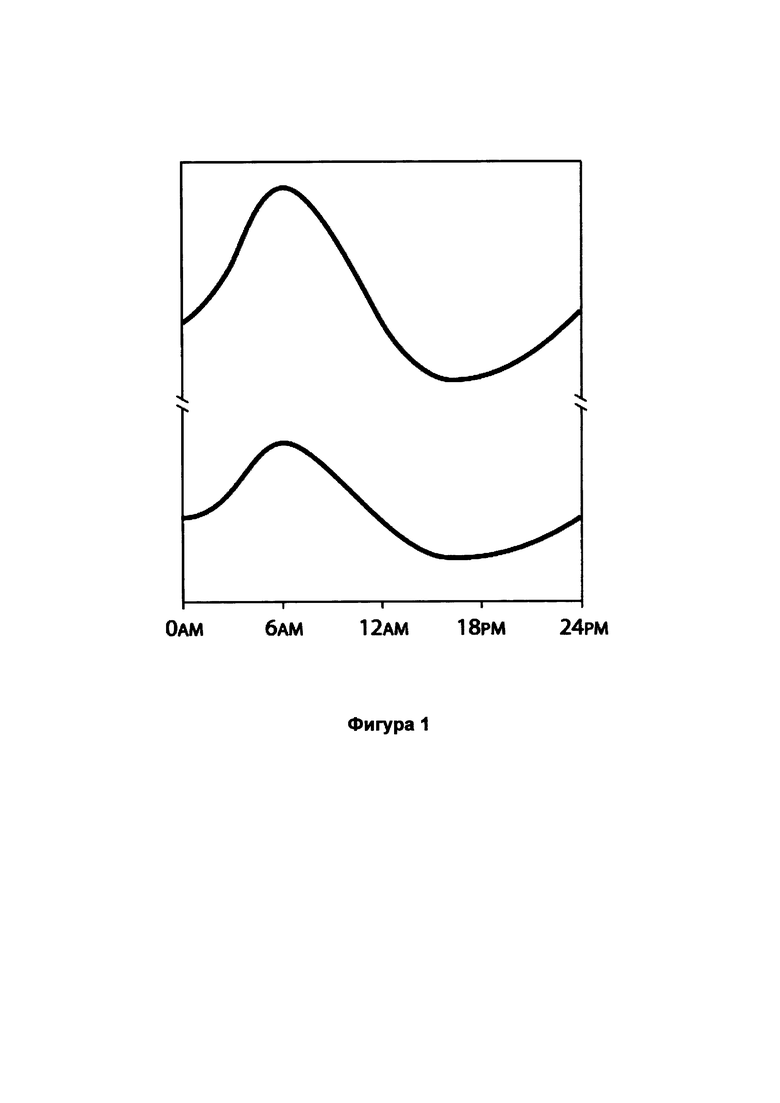
Изобретение относится к применению вальпроевой кислоты или ее фармацевтически приемлемой соли для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента. 3 н. и 14 з.п. ф-лы, 3 пр., 1 табл., 1 ил.
1. Применение вальпроевой кислоты или ее фармацевтически приемлемой соли для лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов, при этом указанное лечение включает введение по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли пациенту таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
2. Применение по п. 1, отличающееся тем, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) и до одного часа после достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
3. Применение по п. 1, отличающееся тем, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до (например, за два часа до) момента времени достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
4. Способ лечения или профилактики патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов у пациента, включающий стадии:
(i) мониторинг концентрации PAI-1 в плазме у пациента с целью определения момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме; а также
(ii) введение пациенту по меньшей мере одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли таким образом, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от четырех часов до и до одного часа после момента времени или периода времени, в течение которого достигается максимальная концентрация PAI-1 в плазме.
5. Способ по п. 4, отличающийся тем, что максимальная концентрация вальпроевой кислоты или ее соли и/или ее метаболита в плазме (Cmax) наблюдается у пациента в течение периода времени, который составляет от трех часов до момента времени достижения максимальной концентрации PAI-1 в плазме (Cmax) у пациента.
6. Применение по пп. 1-3 или способ по п. 4 или 5, отличающееся тем, что лечение включает введение пациенту одной дозы вальпроевой кислоты или ее фармацевтически приемлемой соли в течение 24 часов, причем доза составляет от 50 мг до 1000 мг.
7. Применение по пп. 1-3 или способ по любому из пп. 4-6, отличающееся тем, что введение вальпроевой кислоты или ее фармацевтически приемлемой соли осуществляется таким образом, что концентрация вальпроевой кислоты или ее соли и/или метаболита в плазме в течение периода времени от 14:00 часов до 18:00 часов составляет менее чем 350 мкМ.
8. Применение по пп. 1-3 или способ по любому из пп. 4-7, отличающееся тем, что вальпроевую кислоту или ее фармацевтически приемлемую соль вводят:
(i) в однократной дозе в течение 24-часового периода; и/или
(ii) в общей дозе в течение 24-часового периода от 50 мг до 1000 мг.
9. Применение по пп. 1-3 или способ по любому из пп. 4-8, отличающееся тем, что вальпроевую кислоту или ее фармацевтически приемлемую соль вводят:
(i) в однократной дозе в течение 24-часового периода; и/или
(ii) в дозе, достаточной для достижения снижения уровней PAI-1 в плазме по меньшей мере на 20%.
10. Применение по пп. 1-3 или способ по любому из пп. 4-9, отличающееся тем, что введение вальпроевой кислоты или ее фармацевтически приемлемой соли осуществляется таким образом, что концентрация в плазме вальпроевой кислоты, или ее соли и/или метаболита в течение 24-часового периода моделирует концентрацию PAI-1 в плазме в течение того же периода.
11. Применение по пп. 1-3 или способ по любому из пп. 4-10, отличающееся тем, что патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, выбрано из группы, состоящей из атеросклероза, инфаркта миокарда, ишемического инсульта, тромбоза глубоких вен, тромбоза поверхностных вен, тромбофлебита, легочной эмболии, диссеминированного внутрисосудистого свертывания крови, патологии сосудов почек и перемежающейся хромоты.
12. Применение по пп. 1-3 или способ по любому из пп. 4-11, отличающееся тем, что патологическое состояние, связанное с избыточным отложением фибрина и/или образованием тромбов, представляет собой:
(a) ишемический инсульт, такой как обширный ишемический инсульт и ишемический микроинсульт; и/или
(b) инфаркт миокарда.
13. Применение по пп. 1-3 или способ по любому из пп. 4-12, отличающееся тем, что лечение или профилактика осуществляется человеку.
14. Применение по пп. 1-3 или способ по любому из пп. 4-13, отличающееся тем, что лечение или профилактика осуществляется пациенту с повышенным риском развития патологического состояния, связанного с избыточным отложением фибрина и/или образованием тромбов.
15. Применение по пп. 1-3 или способ по любому из пп. 4-14, отличающееся тем, что лечение или профилактика включает введение вальпроевой кислоты или ее фармацевтически приемлемой соли в комбинации с аспирином, клопидогрелом и/или тикагрелором.
16. Применение фармацевтической композиции, содержащей вальпроевую кислоту или ее фармацевтически приемлемую соль, содержащей одно или более фармацевтически приемлемых вспомогательных веществ для лечения или профилактики патологического состояния, связанного с избыточным осаждением фибрина и/или образованием тромбов по любому из пп. 4-15.
17. Применение по п. 16, отличающееся тем, что указанная композиция дополнительно содержит аспирин, клопидогрел и/или тикагрелор.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства М., Новая волна 2012 с.39-40 статья Ацедипол | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| ЭНЦИКЛОПЕДИЯ ЛЕКАРСТВ М., РЛС 2001 с.266 статья Депакин хроно 500 | |||
| US 6713086 B2, 30.03.2004 | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| ANGLETON P | |||
| et al | |||
| Diuring variation of tissue-type plasminogen activator and its rapid inhibitor | |||
Авторы
Даты
2020-09-22—Публикация
2015-10-08—Подача