[001] Настоящая заявка испрашивает приоритет и определение даты подачи согласно параграфу 119 (е) раздела 35 Свода законов США на основании предварительной заявки на патент США 62/233,267, поданной 25 сентября 2015 года, содержание которой полностью включено в настоящее описание посредством ссылки.
[002] Конъюнктивит, в разговорной речи называемый «розовый глаз» ("pink eye"), представляет собой воспаление глаза, вызывающее отек и раздражение. Указанное заболевание поражает конъюнктиву, тонкую прозрачную мембрану, которая покрывает склеру глазного яблока и выстилает внутреннюю поверхность век. Конъюнктивит чаще всего вызван вирусом или бактериальной инфекцией, хотя также могут играть некоторую роль аллергия, химические раздражители и первичные патологии. Симптомы конъюнктивита включают, без ограничений, покраснение склеры и/или внутреннего века, зуд в области глаза (зуд в глазах), ощущение инородного тела (песок в глазах или поцарапанные глаза), жжение в глазах, помутнение зрения, повышенную чувствительность к свету или светобоязнь, опухшие внутренние веки, повышенную выработку слезной жидкости, водянистые выделения, слизисто-гнойные выделения, которые могут образовывать корочку на ресницах во время сна. Как вирусный, и так бактериальный конъюнктивит являются очень заразными.
[003] Бактериальный конъюнктивит, обычно вызываемый такими пирогенными бактериями, как стафилококк или стрептококк, можно лечить с применением антибиотиков в форме глазных капель, таблеток или мазей. Может потребоваться нанесение глазных капель или мазей на внутреннюю часть века три-четыре раза в день в течение пяти-семи дней. Прием таблеток может потребоваться в течение нескольких дней. Лечение помогает сократить продолжительность инфекции и ассоциированные с ней симптомы, которые обычно продолжаются от 2 до 21 дня. Лечение также будет уменьшать количество времени, в течение которого индивидуум, страдающий бактериальным конъюнктивитом, является заразным. В отличие от бактериальной инфекции, в настоящее время не существует эффективного лечения вирусного конъюнктивита.
[004] Хотя конъюнктивит обычно представляет собой заболевание, не нуждающееся в лечении, некоторые формы конъюнктивита являются серьезными и опасными для зрения, поскольку заболевание может вызвать рубцевание роговицы. Более тяжелые формы конъюнктивита включают бактериальный конъюнктивит, вызываемый гонореей и хламидией, а также вирусный конъюнктивит, вызываемый определенными штаммами аденовируса.
[005] Таким образом, существует потребность в разработке фармацевтических композиций и средств лечения конъюнктивита, в частности вирусного конъюнктивита.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[006] В аспектах настоящего изобретения предложен способ лечения индивидуума, имеющего вирусный конъюнктивит. Описанный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение ослабляет симптом, ассоциированный с вирусным конъюнктивитом, вследствие чего происходит лечение индивидуума. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для лечения вирусного конъюнктивита. Описанный в настоящем документе вирусный конъюнктивит включает эпидемический кератоконъюнктивит, фарингоконъюнктивальную лихорадку, неспецифический спорадический фолликулярный конъюнктивит или хронический папиллярный конъюнктивит. Вирусный конъюнктивит, описанный в настоящем документе, может быть вызван аденовирусом В человека, аденовирусом D человека или аденовирусом Е человека.
[007] В других аспектах настоящего изобретения предложены способы уменьшения или подавления уровня вируса, титра вируса, репликации вируса, синтеза белка и/или тРНК у индивидуума. Описанные способы включают введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение уменьшает или подавляет уровень вируса, титр вируса, репликацию вируса, синтез белка и/или тРНК. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей одну амфиназу для уменьшения или подавления уровня вируса, титра вируса, репликации вируса, синтеза белка и/или тРНК у индивидуума.
[008] В других аспектах настоящего изобретения предложен способ уменьшения или подавления уровня индуцирующей воспаление молекулы у индивидуума. Раскрытый способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение уменьшает или подавляет уровень индуцирующей воспаление молекулы. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одной амфиназу для уменьшения или подавления уровня индуцирующей воспаление молекулы. Индуцирующая воспаление молекула, описанная в настоящем документе, включает вещество Р, пептид, связанный с геном кальцитонина, глутамат или их комбинацию.
[009] В других аспектах настоящего изобретения предложен способ уменьшения или подавления уровня индуцирующего воспаление простагландина у индивидуума. Предложенный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение уменьшает или подавляет уровень индуцирующего воспаление простагландина. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для уменьшения или подавления уровня индуцирующего воспаление простагландина. Индуцирующий воспаление простагландин включает 15dPGJ2.
[010] В других аспектах настоящего изобретения предложен способ стимуляции или улучшения активности сигнального пути рецептора, активируемого пролифератором пероксисом (PPAR), у индивидуума. Предложенный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение стимулирует или увеличивает активность сигнального пути PPAR. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для стимуляции или увеличения активности сигнального пути PPAR. Активность сигнального пути PPAR включает активность сигнального пути PPAR-α, активность сигнального пути PPAR-γ и активность сигнального пути PPAR-δ (также известного как PPAR-β).
[011] В других аспектах настоящего изобретения предложен способ, который способствует установлению изменения фенотипа M1 в М2 у индивидуума. Описанный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение индуцирует апоптоз клеток M1-макрофагов, способствует дифференцировке клеток М2-макрофагов или и то, и другое, тем самым способствуя установлению изменения фенотипа Ml в М2. Также описывается применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для содействия установления изменения фенотипа M1 в М2.
[012] В других аспектах настоящего изобретения предложен способ модуляции уровня цитокина Th1 и/или уровня цитокина Th2 у индивидуума. Предложенный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение снижает уровни интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой Th1-клеткой, повышает уровень ИЛ-10, высвобождаемого Th2-клеткой или и то, и другое, что приводит к модуляции уровня цитокина Th1 и/или цитокина Th2. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для модуляции уровня цитокина Th1 и/или уровня цитокина Th2.
[013] В других аспектах настоящего изобретения предложен способ уменьшения или подавления активности сигнального пути NFκВ у индивидуума. Предложенный способ включает введение индивидууму, нуждающемуся в этом, фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы. Такое введение снижает или подавляет активность сигнального пути NFκВ. Также предложено применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для уменьшения или подавления активности сигнального пути NFκВ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[014] Вирусы представляют собой важные патогены, которые могут инфицировать животных, в том числе людей, и растения. Несмотря на их большое разнообразие, все вирусы являются облигатными внутриклеточными паразитами, а это означает, что каждый вирус зависит от клетки-хозяина и от ее клеточных процессов, чтобы завершить свой цикл репликации. В качестве первого шага к завершению своего цикла репликации вирусу необходимо проникнуть в клетку-хозяина. Это достигается посредством белков на поверхности вируса, взаимодействующих с белками на поверхности клетки-хозяина, что позволяет вирусу присоединиться к клеточной мембране или адсорбироваться на ней. Такая ассоциация вызывает нарушение целостности клеточной мембраны, что позволяет вирусу или его генетическому содержимому высвободиться в цитоплазму клетки-хозяина. Затем вирус задействует механизмы репликации инфицированной клетки-хозяина, чтобы создать копии своего генома и упаковать эти копии в только что синтезированные вирусные частицы. По завершении стадии репликации вируса потомство вируса высвобождается из инфицированной клетки-хозяина посредством отпочковывания или апоптоза для того, чтобы найти новые клетки-хозяева для инфицирования.
[015] Во время инфекции как вирусы в оболочке, так и вирусы без оболочки индуцируют несколько масштабных метаболических изменений на инфицированных клетках, включая перегруппировку фосфолипидов и ганглиозидов, богатых сиаловой кислотой, в плазматической мембране клетки-хозяина. Увеличение присутствия богатых сиаловой кислотой ганглиозидов и анионных фосфолипидов приводит к повышенной электроотрицательности плазматической мембраны. Например, в здоровых клетках липидный бислой клеточной мембраны организован таким образом, что анионные фосфолипиды располагаются на внутриклеточной стороне мембраны. Такая асимметрия анионных фосфолипидов активно поддерживается АТФ-зависимыми транспортными процессами, которые транслоцируют эти фосфолипиды с внеклеточной стороны во внутриклеточную сторону плазматической мембраны. Однако при вирусной инфекции этот процесс транслокации нарушается, что приводит к присутствию анионного фосфолипида на внеклеточной стороне плазматической мембраны. Кроме того, поскольку этот эффект и зависит от хозяина, и не зависит от вируса, присутствие анионных фосфолипидов на внеклеточной поверхности плазматической мембраны являлось бы общим признаком для любой клетки, инфицированной вирусом. Таким образом, в целом клетки, инфицированные вирусом, более отрицательно заряжены, чем гомологичные неинфицированные клетки.
[016] Не желая ограничиваться каким-либо одним механизмом, поскольку описанные в настоящем документе ранпирназа и/или амфиназа представляют собой ярковыраженные катионные молекулы, эти белки будут обладать  электростатическим сродством (аффиностью) к анионной, электроотрицательно заряженной поверхности инфицированных вирусом клеток и, следовательно, они будут более активно интернализоваться клетками, инфицированными вирусом. Клетки, не инфицированные вирусом, не смогут транспортировать ранпирназу и/или амфиназу, описанную в настоящем документе, в свою цитоплазму, поскольку на их плазматических мембранах отсутствуют анионные, электроотрицательно заряженные поверхности. Таким образом, описанная в настоящем документе ранпирназа и/или амфиназа особенно предпочтительно взаимодействует с клетками, инфицированными вирусом. Такая высокая избирательность в отношении инфицированных вирусом клеток позволила исследовать ранпирназу и/или амфиназу, описанную в настоящем документе, для разработки средства лечения заболеваний и расстройств, вызванных вирусом.
электростатическим сродством (аффиностью) к анионной, электроотрицательно заряженной поверхности инфицированных вирусом клеток и, следовательно, они будут более активно интернализоваться клетками, инфицированными вирусом. Клетки, не инфицированные вирусом, не смогут транспортировать ранпирназу и/или амфиназу, описанную в настоящем документе, в свою цитоплазму, поскольку на их плазматических мембранах отсутствуют анионные, электроотрицательно заряженные поверхности. Таким образом, описанная в настоящем документе ранпирназа и/или амфиназа особенно предпочтительно взаимодействует с клетками, инфицированными вирусом. Такая высокая избирательность в отношении инфицированных вирусом клеток позволила исследовать ранпирназу и/или амфиназу, описанную в настоящем документе, для разработки средства лечения заболеваний и расстройств, вызванных вирусом.
[017] В настоящем документе описаны ранпирназы и амфиназы, композиции, содержащие эти ферменты, и способ и применения лечения вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшения или подавления уровня вируса или титра вируса, уменьшения или подавления репликации вируса, уменьшения или подавления синтеза белка, уменьшения или подавления уровня тРНК, уменьшения или подавления уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействия установлению изменения фенотипа M1 в М2, модуляции цитокинов Th1 и Th2 и/или уменьшения или подавления сигнала NFκВ-пути с применением таких ранпирназ, амфиназ или композиций, содержащих такие ранпирназы и/или амфиназы. Ранпирназа и амфиназа, описанные в настоящем документе, являются высокоспецифичными для серотипов аденовируса и в высокой степени гидрофильными, что облегчает их способность проникать сквозь окулярные барьеры, чтобы потенциально улучшить поглощение лекарственного средства в ткани-мишени.
[018] Вирусный конъюнктивит обладает двумя основными проявлениями, которые необходимо минимизировать, а именно присутствие и репликация вируса и иммунный ответ хозяина, который приводит к клиническим симптомам. Для успешной терапии недостаточно действовать только в отношении одного из этих двух аспектов. Описанная в настоящем документе ранпирназа или амфиназа, по всей видимости, обладает как противовирусными, так и иммуномодулирующими механизмами действия.
[019] В аспектах настоящего изобретения предложена, в частности, ранпирназа. Ранпирназа - это рибонуклеаза амфибий, первоначально выделенная из ооцитов и/или ранних эмбрионов Rana pipiens (северной леопардной лягушки). Ранпирназа, которую первоначально называли белок Р-30 или Р-30, является членом суперсемейства белка рибонуклеазы панкреатического типа (РНКаза А). Ранпирназа, которая изначально экспрессируется в виде полипептида-предшественника, подвергается процессингу для удаления как участка пептида-предшественника, так и стартового метионина с получением основного фермента, богатого лизином, с молекулярной массой приблизительно 12 кДа. Пироглутамиловый остаток в N-концевой области является неотъемлемой частью активного сайта ранпирназы и значимым образом способствует каталитической и биологической активности ранпиразы, а также необычно высокой конформационной стабильности. Другой структурной особенностью ранпирназы является С-концевая дисульфидная связь (87-104), которая стабилизирует компактную структуру указанного белка. Это, в свою очередь, делает ранпирназу очень устойчивой к эндогенным протеазам. Другая особенность ранпирназы, которая делает ее устойчивой к эндогенным протеазам, - это низкая аффинность связывания внутри клетки по сравнению со специфичными ингибиторами РНКазы, что позволяет ранпирназе оставаться активной внутри клетки, в то время как большинство РНКаз млекопитающих ингибируются.
[020] Ранпиназа, в первую очередь, нацеливается на быстро реплицирующиеся и/или быстро растущие клетки посредством связывания с рецепторами клеточной поверхности и интернализации в цитоплазму через АР-2/клатрин-опосредованный эндоцитоз. Затем фермент переносится в эндоплазматический ретикулум, где он приводит к деградации РНК-субстрата с предпочтением к последовательностям урациловых и гуаниновых нуклеотидов. Например, картирование сайта расщепления с применением природных субстратов транспортных РНК (тРНК) in vitro выявило преимущественные сайты расщепления по UG-и GG-остаткам, а также расщепления по CG-сайтам. По всей видимости, ранпирназа преимущественно нацеливается на транспортную РНК как на субстрат, что приводит к отсутствию повреждений матричной РНК (мРНК) и рибосомальной РНК (рРНК) неповрежденной. Деградация тРНК при помощи ранпирназы приводит к ингибированию синтеза белка.
[021] Тем не менее, биологические эффекты ранпирназы не могут быть объяснены исключительно уменьшением синтеза белка, что свидетельствует о том, что ранпирназа нацеливается на дополнительные или альтернативные молекулы РНК. Один альтернативный механизм приписывали пути РНК-интерференции и деградации микроРНК и/или миРНК. Эти малые РНК, аналогичные тРНК, незащищены белками и ранпирназа также может вызывать их деградацию. Ранпирназа может также вызывать деградацию предшественников малых РНК и, таким образом, продуцировать миРНК и влиять на экспрессию гена. Недавние результаты выявили новые классы регуляторных РНК (30-40 нт), которые можно получить из небольших некодирующих РНК, в особенности из тРНК, что свидетельствует о том, что ранпирназа может продуцировать миРНК непосредственно из своего внутриклеточного субстрата - тРНК.
[022] Также было показано, что ранпирназа обладает иммуномодулирующими механизмами действия за счет интерференции с путем передачи сигнала ядерного фактора энхансера легкой цепи каппа активированных В клеток «каппа-би» (NFκВ). Небольшое исследование in vitro показало, что ранпирназа ингибирует транслокацию NFκВ в ядро. NFκВ, белковый комплекс, который контролирует транскрипцию ДНК, является ключевым основным регулятором воспаления в ответ на провоспалительную стимуляцию. NFκВ встречается почти во всех клетках животных и регулирует клеточные ответы на стимулы, такие как стрессовое воздействие, свободные радикалы, бактериальные и/или вирусные антигены. Кроме того, NFκB играет ключевую роль в регуляции иммунного ответа на инфекцию (κ-легкие цепи являются важными компонентами иммуноглобулинов). Путем ингибирования транслокации NFκВ в ядро, где это необходимо для усиления воспаления, воспалительный процесс будет ослабляться. Кроме того, фактор некроза опухоли-альфа (ФНО-α) и интерлейкин 1-b (ИЛ-1b) как активируют, так и активируются NFκВ посредством «петли» с положительной обратной связью, в которой гены, которые регулируются NFκВ, также вызывают активацию NFκВ. Провоспалительные цитокины (включая ФНО-α и ИЛ-1b) «привлекают» клетки, участвующие в воспалительных реакциях, к сайтам воспаления, ферменты, которые продуцируют медиаторы воспаления, иммунные рецепторы и молекулы адгезии, которые играют важную роль в первоначальном рекрутинге нейтрофилов и макрофагов к очагам воспаления. Таким образом, активация и транслокация NFκВ, следовательно, приводит к скоординированному увеличению экспрессии многих генов, продукты которых опосредуют воспалительные и иммунные ответы. Такой тип положительной регуляторной петли может усиливать и сохранять местные воспалительные ответы. Таким образом, тот результат, что ранпирназа блокировала провоспалительные эффекты, опосредованные активностью NFκВ, свидетельствует о том, что этот фермент может эффективно подавлять воспалительный ответ. Интересно отметить, что как у мышей, так и у людей с острой травмой (в случае мышей) или эпидемическим кератоконъюнктивитом (в случае пациента, у которого диагностировали аденовирусную инфекцию) NFκВ транслоцировался в ядро из цитоплазмы в эпителиальных клетках конъюнктивы. Это является очень важным наблюдением, поскольку лекарственное средство, такое как ранпирназа, которая обладает способностью блокировать такую транслокацию, способно «нокаутировать» воспалительный ответ на такие триггеры. При этом не было обнаружено непосредственных исследований, которые бы оценивали иммуномодулирующие действия ранпирназы in vivo.
[023] Несколько посвященных противовирусным свойствам ранпирназы исследований также помогают понять, как ранпирназа может влиять на образование вирусов. Было показано, что ранпирназа: 1) ингибирует репликацию ВИЧ-1 (в качестве примера) вплоть до 99,9% в анализе антигена р24 при конечных концентрациях, которые не являются цитотоксическими; 2) ингибирует образование синцития, которое часто возникает при активных вирусных инфекциях; 3) ингибирует раннюю трансактивацию вирусных промоторных последовательностей при помощи белка tatIII; и 4) приводит к деградации РНК вируса внутри клетки, а также различных видов клеточной тРНК, но не клеточной мРНК или рРНК. Эти данные свидетельствуют о том, что применяемая вне клетки ранпирназа способна проникать внутрь инфицированных клеток и ингибировать репликацию вируса по меньшей мере посредством двух возможных механизмов: 1) непосредственной деградации РНК вируса и 2) косвенным образом путем деградации тРНК. Поскольку РНКазы представляют собой ферменты, специализирующиеся на рибонуклеолитической деградации соответствующих субстратов РНК, представляется маловероятным, что штаммы вирусов будут развивать устойчивость к их каталитической активности.
[024] В одном варианте реализации описанная в настоящем документе ранпирназа содержит SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа обладает идентичностью аминокислотной последовательности, например, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: ID Nr. 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №:: 13, SEQ ID №: 14, SEQ ID NO: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа обладает идентичностью аминокислотной последовательности в диапазоне, например, от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 97%, от приблизительно 80% до приблизительно 97%, от приблизительно 85% до приблизительно 97%, от приблизительно 90% до приблизительно 97% или от приблизительно 95% до приблизительно 97% с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26.
[025] В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа содержит, например, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №. 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26 или не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа содержит, например, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26; или не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26.
[026] Описанная в настоящем документе ранпирназа может содержать N-концевую область, блокированную пироглутаминовой кислотой (<Glu). В одном аспекте блокировку N-концевой области пироглутаминовой кислотой получают путем автоциклизации глутамина (Gln). Описанная в настоящем документе ранпирназа также может содержать N-конец, блокированный пирролидонкарбоновой кислотой. В аспектах данного варианта реализации ранпирназа, содержащая SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26, содержит N-концевую область, блокированную пироглутаминовой кислотой или пирролидонкарбоновой кислотой.
[027] Аспекты настоящего изобретения включают, в частности, амфиназу. Амфиназа, которая представляет собой другой член надсемейства белка РНКазы А панкреатического типа, также была выделена из амфибий и является более основным вариантом ранпирназы. Амфиназа, которая изначально экспрессируется в виде полипептида-предшественника, подвергается процессингу для удаления как участка пептида-предшественника, так и стартового метионина с образованием активного фермента с молекулярной массой приблизительно 13 кДа. Подобно ранпирназе, амфиназа, в первую очередь, нацеливается на быстро реплицирующиеся и/или быстро растущие клетки путем деградации РНК и, как минимум, ингибирует синтез белка.
[028] В одном варианте реализации описанная в настоящем документе амфиназа содержит SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №; 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39. В аспектах этого варианте реализации описанная в настоящем документе амфиназа обладает идентичностью аминокислотной последовательности, например, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №; 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39. В еще других аспектах данного варианта реализации описанная в настоящем документе амфиназа обладает идентичностью аминокислотной последовательности в диапазоне, от, например, приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 97%, от приблизительно 80% до приблизительно 97%, от приблизительно 85% до приблизительно 97%, от приблизительно 90% до приблизительно 97% или от приблизительно 95% до приблизительно 97% с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39.
[029] В других аспектах данного варианта реализации описанная в настоящем документе амфиназа содержит, например, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39 или не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №; 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39. В еще других аспектах данного варианта реализации описанная в настоящем документе амфиназа содержит, например, по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №; 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39 или не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39.
[030] Другие ранпирназы и амфиназы, подходящие для композиций, способов и применений, описанных в настоящем документе, описаны, например, в патентах США №№5,559,122, 5,728,805, 6,239,257, 6,175,003, 6,423,515, 7,229,824, 7,443,535, 7,443,536, 7,474,542, 7,559,553, 7,556,555, 7,763,449, 7,559,551, 7,559,552, 7,556,554, 8,518,399, 8,663,964, 8,808,690, каждый из которых полностью включен посредством ссылки. Аналогичным образом, обычная заявка на патент США под названием «Methods of Treating Viral Infection, Particularly Rabies, Mers-Cov, Influenza, Ebola, Chinkungunya, Venezuelan Equine Encephalitis, Canine Parvovirus, Adenovirus. Respiratory Syncytial Virus, Rhinovirus, and Poxvirus in Mammalian Patients», поданная 24 марта 2015 года, также полностью включена посредством ссылки.
[031] В другом варианте реализации описанную в настоящем документе ранпирназу и/или амфиназу можно рекомбинантно модифицировать для добавления функциональных доменов без ингибирования эндогенной активности ранпирназы и/или амфиназы, описанной в настоящем документе. Например, к описанной в настоящем документе ранпирназе и/или амфиназе можно добавить фрагмент эозинофильного катионного белка для того, чтобы обеспечить или значительно улучшить бактерицидные свойства. Такие конструкции описаны в публикации Torrent et all «Bactericidal Activity Engineered on Human Pancreatic Ribonuclease and Onconase», Mol. Pharm. 6 (2): 531-542 (2009), которая полностью включена посредством ссылки. Если один терапевтический препарат позволяет лечить как бактериальный, так и вирусный конъюнктивит, при этом по-прежнему отвечая на обычный основной иммунный ответ на такое стрессовое воздействие, это может иметь большое значение.
[032] В настоящем изобретении описание предложены различные варианты полипептидов, где одну аминокислоту заменяют на другую, такие как, например, описанная в настоящем документе ранпирназа или описанная в настоящем документе амфиназа. Замену можно оценить при помощи множества факторов, таких как, например, физические свойства заменяемой аминокислоты (см. таблицу ниже) или того, как исходная аминокислота будет допускать замену (см. следующую таблицу ниже). Методы выбора того, какую аминокислоту можно заменить на другую аминокислоту в полипептиде, известны специалисту в данной области техники.


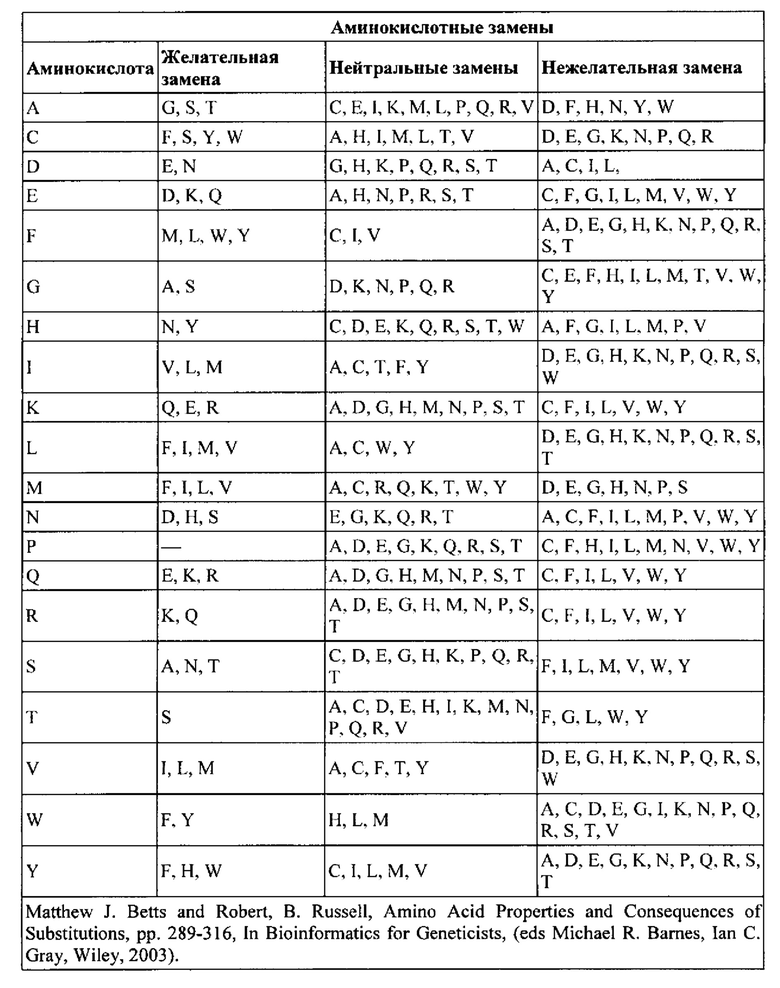
[033] В аспектах данного варианта реализации гидрофобную аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой гидрофобной аминокислотой. Примеры гидрофобных аминокислот включают, например, С, F, I, L, М, V и W. В другом аспекте данного варианта реализации алифатическую аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой алифатической аминокислотой. Примеры алифатических аминокислот включают, например, A, I, L, Р и V. В еще одном аспекте данного варианта реализации ароматическую аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой ароматической аминокислотой. Примеры ароматических аминокислот включают, например, F, Н, W и Y. В еще одном аспекте данного варианта реализации участвующую в стэкинг-взаимодействиях аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой участвующей в стэкинг-взаимодействиях аминокислотой. Примеры участвующих в стэкинг-взаимодействиях аминокислот включают, например, F, Н, W и Y. В еще одном аспекте данного варианта реализации полярную аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой полярной аминокислотой. Примеры полярных аминокислот включают, например, D, Е, K, N, Q и R. В еще другом аспекте данного варианта реализации менее полярная или индифферентная аминокислота в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой менее полярной или индифферентной аминокислотой. Примеры менее полярных или индифферентных аминокислот включают, например, А, Н, G, Р, S, Т и Y. В еще одном аспекте данного варианта реализации положительно заряженную аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заместить другой положительно заряженной аминокислотой. Примеры положительно заряженных аминокислот включают, например, K, R и Н. В еще одном аспекте данного варианта реализации отрицательно заряженную аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой отрицательно заряженной аминокислотой. Примеры отрицательно заряженных аминокислот включают, например, D и Е. В другом аспекте данного варианта реализации малую аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой малой аминокислотой. Примеры малых аминокислот включают, например, A, D, G, N, Р, S и Т. В еще одном аспекте данного варианта реализации С-бета-разветвленную аминокислоту в одном конкретном положении в ранпирназе и/или амфиназе, описанной в настоящем документе, можно заменить другой С-бета-разветвленной аминокислотой. Примеры С-бета-разветвленных аминокислот включают, например, I, Т и V.
[034] В одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает антивирусной активностью, способной уменьшать или подавлять уровень вируса или титр вируса. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает антивирусной активностью, способной уменьшать или подавлять уровень вируса или титр вируса, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по крайней мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по своей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной снижать или подавлять уровень вируса или титр вируса в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[035] В одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает антивирусной активностью, способной уменьшать или подавлять репликацию вируса. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает антивирусной активностью, способной уменьшать или подавлять репликацию вируса, например, по меньшей на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 50%, по меньшей мере на 35%, по меньшей мере на 35%, по меньшей мере на 35%, по меньшей мере на 50%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной уменьшать или подавлять репликацию вируса в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10 до 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[036] В варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной уменьшать или подавлять синтез белка по меньшей мере в одной клетке. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной уменьшать или подавлять синтез белка по меньшей мере в одной клетке, например, по меньшей на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной уменьшать или подавлять синтез белка по меньшей мере в одной клетке в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[037] В варианте реализации ранпирназа и/или амфиназа, описанная в настоящем документе, обладает противовирусной активностью, способной уменьшать или подавлять уровень тРНК по меньшей мере в одной клетке. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовирусной активностью, способной уменьшать или подавлять уровень тРНК по меньшей мере в одной клетке, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации ранпирназа и/или амфиназа, описанная в настоящем документе, обладает противовирусной активностью, способной уменьшать или подавлять уровень тРНК по меньшей мере в одной клетке в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[038] В одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни индуцирующей воспаление молекулы. В аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни вещества Р (SP), пептида, связанного с геном кальцитонина (CGRP), глутамата или их комбинации. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни SP, CGRP, глутамата или их комбинации, высвобождаемой из сенсорного нейрона, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 65%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни SP, CGRP, глутамата или их комбинации, высвобождаемой из сенсорного нейрона в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[039] Простагландины опосредуют местный воспалительный ответ и участвуют во всех воспалительных функциях посредством действия на рецепторы простагландинов и опосредуют воспалительную передачу сигнала, включая хемотаксис (макрофаги, нейтрофилы и эозинофилы), вазодилатацию и адгезию. Однако PG-опосредованный воспалительный ответ является самоограничивающимся (не требует лечения). Основным фактором этого самоограничения является простагландин, называемый 15dPGJ2, который является эндогенным агонистом сигнального пути рецептора гамма, активируемого пролифератором пероксисом (PPAR-γ). Сигнальный путь PPAR-γ) индуцирует апоптоз клеток M1-макрофагов, посредством чего уменьшаются уровни провоспалительных Th1-цитокинов и 2) способствует дифференцировке моноцитов в клетки М2-макрофаги. Клетки М2-макрофаги продуцируют и высвобождают Th2 противовоспалительные цитокины.
[040] В одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни индуцирующего воспаление простагландина. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни индуцирующего воспаление простагландина, высвобождаемого из сенсорного нейрона, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровни индуцирующего воспаление простагландина, высвобождаемого из сенсорного нейрона, в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80% от приблизительно 80% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[041] В другом варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью по существу аналогичной 15dPGJ2. В аспектах данного варианта реализации противовоспалительная активность описанной в настоящем документе ранпирназы и/или амфиназы составляет, например, по меньшей мере 5%, по меньшей мере 15%, по меньшей мере 25%, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%», по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90% или по меньшей мере 95% от активности, наблюдаемой для 15dPGJ2. В других аспектах данного варианта реализации противовоспалительная активность описанной в настоящем документе ранпирназы и/или амфиназы находится в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 25% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 80% до приблизительно 90%, от приблизительно 25% до приблизительно 80%, от приблизительно 50% до приблизительно 80%, от приблизительно 60% до приблизительно 80%, от приблизительно 70% до приблизительно 80%, от приблизительно 25% до приблизительно 70%, от приблизительно 50% до приблизительно 70%, от приблизительно 25% до приблизительно 60%, от приблизительно 50% до приблизительно 60% или от приблизительно 25% до приблизительно 50% активности, наблюдаемой для 15dPGJ2.
[042] Рецепторы, активируемые пролифераторами пероксисом (PPAR), представляют собой группу ядерных рецепторных белков, которые действуют как факторы транскрипции, регулирующие экспрессию генов. Известно, что все PPAR гетеродимеризуются с ретиноидным Х-рецептором (RXR) и связываются с определенными областями на ДНК генов-мишеней, называемыми отвечающими на гормон элементами пролифератора пероксисом (PPRE). PPAR играют важную роль в регуляции клеточной дифференцировки, развития и метаболизма (углеводы, липиды, белки), а также опухолегенеза у высших организмов. Указанное семейство включает три члена: PPAR-α, PPAR-γ и PPAR-δ (также известный как PPAR-β). PPAR-α экспрессируется в печени, почках, сердце, мышцах, жировой ткани, а также в других тканях. PPAR-δ экспрессируется во многих тканях, но выраженным образом в головном мозге, жировой ткани и коже. PPAR-γ содержит три альтернативно сплайсированные формы, каждая из которых обладает различным профилем экспрессии гена. PPAR-γ1 экспрессируется практически во всех тканях, включая сердце, мышцы, толстую кишку, почки, поджелудочную железу и селезенку. PPAR-γ2 главным образом экспрессируется в жировой ткани. PPAR-γ3 экспрессируется в макрофагах, толстой кишке и белой жировой ткани. Эндогенные лиганды для PPAR включают свободные жирные кислоты и эйкозаноиды. PPAR-γ активируется PGJ2 (простагландином), тогда как PPAR-α активируется лейкотриеном В4.
[043] В варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать или улучшать активность всех сигнальных путей PPAR. В других вариантах реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать или улучшать активность одного или двух сигнальных путей PPAR.
[044] В другом варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать или улучшать активность сигнального пути PPAR-α. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPAR-α, например, по меньшей мере на 5%, по меньшей мере на 15%, по меньшей мере на 25%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPAR-α в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 25% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 80% до приблизительно 90%, от приблизительно 25% до приблизительно 80%, от приблизительно 50% до приблизительно 80%, от приблизительно 60% до приблизительно 80%, от приблизительно 70% до приблизительно 80%, от приблизительно 25% до приблизительно 70%, от приблизительно 50% до приблизительно 70%, от приблизительно 25% до приблизительно 60%, от приблизительно 50% до приблизительно 60% или от приблизительно 25% до приблизительно 50%.
[045] В другом варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать или улучшать активность сигнального пути PPAR-δ. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPAR-δ, например, по меньшей мере на 5%, по меньшей мере на 15%, по меньшей мере на 25%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPAR-δ в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 25% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 80% до приблизительно 90%, от приблизительно 25% до приблизительно 80%, от приблизительно 50% до приблизительно 80%, от приблизительно 60% до приблизительно 80%, от приблизительно 70% до приблизительно 80%, от приблизительно 25% до приблизительно 70%, от приблизительно 50% до приблизительно 70%, от приблизительно 25% до приблизительно 60%, от приблизительно 50% до приблизительно 60% или от приблизительно 25% до приблизительно 50%.
[046] В другом варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать или улучшать активность сигнального пути PPAR-γ. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPAR-γ, например, по меньшей мере на 5%, по меньшей мере на 15%, по меньшей мере на 25%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа стимулирует или улучшает активность сигнального пути PPARγ в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 25% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, приблизительно 70% до приблизительно 90%, от приблизительно 80% до приблизительно 90%, от приблизительно 25% до приблизительно 80%, от приблизительно 50% до приблизительно 80%, от приблизительно 60% до приблизительно 80%, от приблизительно 70% до приблизительно 80%, от приблизительно 25% до приблизительно 70%, от приблизительно 50% до приблизительно 70%, от приблизительно 25% до приблизительно 60%, от приблизительно 50% до приблизительно 60% или от приблизительно 25% до приблизительно 50%.
[047] Макрофаги активируются и поляризуются в различимые фенотипы, экспрессирующие уникальные молекулы клеточной поверхности и секретирующие дискретные наборы цитокинов и хемокинов. Классический M1-фенотип поддерживает провоспалительные Th1-ответы, регулируемые цитокинами, такими как, например, интерлейкин-6 (ИЛ-6), ИЛ-12 и ИЛ-23, тогда как альтернативный М2-фенотип в целом поддерживает противовоспалительные процессы, регулируемые ИЛ-10. М2-клетки можно дополнительно классифицировать на подгруппы, М2а, M2b и М2с, в зависимости от типа стимуляции и последующей экспрессии поверхностных молекул и цитокинов.
[048] В еще одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной содействовать установлению изменения фенотипа M1 в М2. В аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной индуцировать апоптоз клеток М1-макрофагов. В другом аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной стимулировать дифференцировку клеток М2-макрофагов. В еще одном аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной индуцировать апоптоз клеток M1-макрофагов и стимулировать дифференцировку клеток М2-макрофагов.
[049] В еще одном варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной модулировать уровни Th1-цитокина и/или Th2-цитокина. В аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, например, по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%), от приблизительно 50% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[050] В другом аспекте данного варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной повышать уровень ИЛ-10, высвобождаемого из Th2-клетки. В другом аспекте данного варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной повышать уровень ИЛ-10, высвобождаемого из Th2-клетки, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще другом аспекте данного варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной повышать уровень ИЛ-10, высвобождаемого из Th2-клетки, в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[051] В другом аспекте данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, и повышать уровень ИЛ-10, высвобождаемого из Th2-клетки. В других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%, и способной повышать уровень ИЛ-10, высвобождаемого из Th2-клетки, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще другом аспекте данного варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%, и способной повышать уровень ИЛ-10, высвобождаемого из Th2-клетки, в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70%, или от приблизительно 50% до приблизительно 70%.
[052] В другом варианте реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать или подавлять активность сигнального пути NFκB. В аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать или подавлять активность сигнального пути NFκB, например, по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%. В еще других аспектах данного варианта реализации описанная в настоящем документе ранпирназа и/или амфиназа обладает противовоспалительной активностью, способной уменьшать или подавлять активность сигнального пути NFκВ в диапазоне, например, от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[053] Аспекты настоящего изобретения описывают, в частности, композицию. Описанную в настоящем документе композицию в целом вводят в качестве фармацевтически приемлемой композиции. В контексте настоящего изобретения термин «фармацевтически приемлемый» относится к любому молекулярному объекту или композиции, которая не вызывает побочной, аллергической или другой неблагоприятной или нежелательной реакции при введении индивидууму. В контексте настоящего изобретения термин «фармацевтически приемлемая композиция» является синонимом для «фармацевтической композиции» и означает терапевтически эффективную концентрацию активного ингредиента, такого как, например, любого одного из ранпирназы и/или амфиназы, описанной в настоящем документе. Фармацевтическая композиция, описанная в настоящем документе, является подходящей для медицинских и ветеринарных применений. Фармацевтическую композицию можно вводить индивидууму отдельно или в комбинации с другими дополнительными активными ингредиентами, агентами, лекарственными средствами или гормонами.
[054] Аспекты настоящего изобретения включают, в частности, фармацевтическую композицию. Фармацевтическая композиция, описанная в настоящем документе, содержит по меньшей мере одну ранпирназу, описанную в настоящем документе, и/или по меньшей мере одну амфиназу, описанную в настоящем документе. Фармацевтическая композиция, содержащая по меньшей мере одну описанную в настоящем документе ранпирназу и/или по меньшей мере одну описанную в настоящем документе амфиназу, при введении индивидууму стимулирует противовоспалительный ответ против по меньшей мере одного штамма вируса, вызывающего вирусный конъюнктивит.
[055] В другом аспекте данного варианта реализации фармацевтическая композиция представляет собой лекарственное средство для лечения описанного в настоящем документе вирусного конъюнктивита. В аспектах данного варианта реализации по меньшей мере одну описанную в настоящем документе ранпирназу и/или по меньшей мере одну описанную в настоящем документе амфиназу применяют для получения лекарственного средства для лечения вирусного конъюнктивита, описанного в настоящем документе. В аспектах данного варианта реализации ранпирназу и/или амфиназу, описанную в настоящем документе, применяют в количестве, достаточном для лечения вирусного конъюнктивита, описанного в настоящем документе, уменьшая по меньшей мере одно физиологическое состояние или симптом, ассоциированный с описанным в настоящем документе вирусным конъюнктивитом.
[056] В одном варианте реализации описанная в настоящем документе фармацевтическая композиция содержит одну ранпирназу и/или амфиназу, описанную в настоящем документе. В одном варианте реализации описанная в настоящем документе фармацевтическая композиция содержит ряд ранпирназ и/или амфиназ, описанных в настоящем документе. В аспектах данного варианта реализации описанная в настоящем документе фармацевтическая композиция содержит, например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 ранпирназ и/или амфиназ, описанных в настоящем документе. В других аспектах данного варианта реализации описанная в настоящем документе фармацевтическая композиция содержит, например, по меньшей мере 1, по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 11, по меньшей мере 12, по меньшей мере 13, по меньшей мере 14 или по меньшей мере 15 ранпирназ и/или амфиназ, описанных в настоящем документе. В еще других аспектах данного варианта реализации описанная в настоящем документе фармацевтическая композиция содержит, например, не более 1, не более 2, не более 3, не более 4, не более 5, не более 6, не более 7, не более 8, не более 9, не более 10, не более 11, не более 12, не более 13, не более 14 или не более 15 ранпирназ и/или амфиназ, описанных в настоящем документе. В еще других аспектах данного варианта реализации описанная в настоящем документе фармацевтическая композиция содержит, например, от 1 до 2, от 1 до 3, от 1 до 4, от 1 до 5, от 1 до 6, от 1 до 7, от 1 до 8, от 1 до 9, от 1 до 10, от 1 до 11, от 1 до 12, от 1 до 13, от 1 до 14, от 1 до 15, от 2 до 3, от 2 до 4, от 2 до 5, от 2 до 6, от 2 до 7, от 2 до 8, от 2 до 9, от 2 до 10, от 2 до 11, от 2 до 12, от 2 до 13, от 2 до 14, от 2 до 15, от 3 до 4, от 3 до 5, от 3 до 6, от 3 до 7, от 3 до 8, от 3 до 9, от 3 до 10, от 3 до 11, от 3 до 12, от 3 до 13, от 3 до 14, от 3 до 15, от 4 до 5, от 4 до 6, от 4 до 7, от 4 до 8, от 4 до 9, от 4 до 10, от 4 до 11, от 4 до 12, от 4 до 13, от 4 до 14, от 4 до 15, от 5 до 6, от 5 до 7, от 5 до 8, от 5 до 9, от 5 до 10, от 5 до 11, от 5 до 12, от 5 до 13, от 5 до 14, от 5 до 15, от 6 до 7, от 6 до 8, от 6 до 9, от 6 до 10, от 6 до 11, от 6 до 12, от 6 до 13, от 6 до 14, от 6 до 15, от 7 до 8, от 7 до 9, от 7 до 10, от 7 до 11, от 7 до 12, от 7 до 13, от 7 до 14, от 7 до 15, от 8 до 9, от 8 до 10, от 8 до 11, от 8 до 12, от 8 до 13, от 8 до 14, от 8 до 15, от 9 до 10, от 9 до 11, от 9 до 12, от 9 до 13, от 9 до 14, от 9 до 15, от 10 до 11, от 10 до 12, от 10 до 13, от 10 до 14, от 10 до 15, от 11 до 12, от 11 до 13, от 11 до 14, от 11 до 15, от 12 до 13, от 12 до 14, от 12 до 15, от 13 до 14, от 13 до 15 или 14-15 ранпирназ и/или амфиназ, описанных в настоящем документе.
[057] Количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, представляет собой количество, достаточное для получения соответствующего противовоспалительного ответа у индивидуума. Обычно это количество также не вызывает значительных нежелательных побочных эффектов. Такое количество будет варьироваться в зависимости от того, введение какой конкретно ранпирназы и/или амфиназы проводят. Оптимальное количество для конкретной фармацевтической композиции можно установить при помощи стандартных исследований, включающих наблюдение за титрами провоспалительных цитокинов, титрами противовоспалительных цитокинов, титрами простагландинов, за уменьшением по меньшей мере одного симптома, ассоциированного с вирусным конъюнктивитом, и за другими ответами у индивидуумов. Первоначальный курс приема фармацевтической композиции может включать 1, 2, 3 или 4 дозы фармацевтической композиции с заданными интервалами, оптимальными для обеспечения противовоспалительного ответа.
[058] В целом эффективное и безопасное количество ранпирназы и/или амфиназы, описанной в настоящем документе, содержащееся в фармацевтической композиции, варьирует от приблизительно 1 фг до 3000 мг. В аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, приблизительно 1 фг, приблизительно 2 фг, приблизительно 3 фг, приблизительно 4 фг, приблизительно 5 фг, приблизительно 6 фг, приблизительно 7 фг, приблизительно 8 фг, приблизительно 9 фг, приблизительно 10 фг, приблизительно 15 фг, приблизительно 20 фг, приблизительно 25 фг, приблизительно 30 фг, приблизительно 35 фг, приблизительно 40 фг, приблизительно 45 фг, приблизительно 50 фг, приблизительно 55 фг, приблизительно 60 фг, приблизительно 65 фг, приблизительно 70 фг, приблизительно 75 фг, приблизительно 80 фг, приблизительно 85 фг, приблизительно 90 фг, приблизительно 95 фг, приблизительно 100 фг, приблизительно 110 фг, приблизительно 120 фг, приблизительно 130 фг, приблизительно 140 фг, приблизительно 150 фг, приблизительно 160 фг, приблизительно 170 фг, приблизительно 180 фг, приблизительно 190 фг, приблизительно 200 фг, приблизительно 210 фг, приблизительно 220 фг, приблизительно 230 фг, приблизительно 240 фг, приблизительно 250 фг, приблизительно 260 фг, приблизительно 270 фг, приблизительно 280 фг, приблизительно 290 фг, приблизительно 300 фг, приблизительно 310 фг, приблизительно 320 фг, приблизительно 330 фг, приблизительно 340 фг, приблизительно 350 фг, приблизительно 360 фг, приблизительно 370 фг, приблизительно 380 фг, приблизительно 390 фг, приблизительно 400 фг, приблизительно 410 фг, приблизительно 420 фг, приблизительно 430 фг, приблизительно 440 фг, приблизительно 450 фг, приблизительно 460 фг, приблизительно 470 фг, приблизительно 480 фг, приблизительно 490 фг, приблизительно 500 фг, приблизительно 510 фг, приблизительно 520 фг, приблизительно 530 фг, приблизительно 540 фг, приблизительно 550 фг, приблизительно 560 фг, приблизительно 570 фг, приблизительно 580 фг, приблизительно 590 фг, приблизительно 600 фг, приблизительно 610 фг, приблизительно 620 фг, приблизительно 630 фг, приблизительно 640 фг, приблизительно 650 фг, приблизительно 660 фг, приблизительно 670 фг, приблизительно 680 фг, приблизительно 690 фг, приблизительно 700 фг, приблизительно 710 фг, приблизительно 720 фг, приблизительно 730 фг, приблизительно 740 фг, приблизительно 750 фг, приблизительно 760 фг, приблизительно 770 фг, приблизительно 780 фг, приблизительно 790 фг, приблизительно 800 фг, приблизительно 810 фг, приблизительно 820 фг, приблизительно 830 фг, приблизительно 840 фг, приблизительно 850 фг, приблизительно 860 фг, приблизительно 870 фг, приблизительно 880 фг, приблизительно 890 фг, приблизительно 900 фг, приблизительно 910 фг, приблизительно 920 фг, приблизительно 930 фг, приблизительно 940 фг, приблизительно 950 фг, приблизительно 960 фг, приблизительно 970 фг, приблизительно 980 фг, приблизительно 990 фг или приблизительно 1000 фг.
[059] В других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, по меньшей мере 1 фг, по меньшей мере 2 фг, по меньшей мере 3 фг, по меньшей мере 4 фг, по меньшей мере 5 фг, по меньшей мере 6 фг, по меньшей мере 7 фг, по меньшей мере 8 фг, по меньшей мере 9 фг, по меньшей мере 10 фг, по меньшей мере 15 фг, по меньшей мере 20 фг, по меньшей мере 25 фг, по меньшей мере 30 фг, по меньшей мере 35 фг, по меньшей мере 40 фг, по меньшей мере 45 фг, по меньшей мере 50 фг, по меньшей мере 55 фг, по меньшей мере 60 фг, по меньшей мере 65 фг, по меньшей мере 70 фг, по меньшей мере 75 фг, по меньшей мере 80 фг, по меньшей мере 85 фг, по меньшей мере 90 фг, по меньшей мере 95 фг, по меньшей мере 100 фг, по меньшей мере 110 фг, по меньшей мере 120 фг, по меньшей мере 130 фг, по меньшей мере 140 фг, по меньшей мере 150 фг, по меньшей мере 160 фг, по меньшей мере 170 фг, по меньшей мере 180 фг, по меньшей мере 190 фг, по меньшей мере 200 фг, по меньшей мере 210 фг, по меньшей мере 220 фг, по меньшей мере 230 фг, по меньшей мере 240 фг, по меньшей мере 250 фг, по меньшей мере 260 фг, по меньшей мере 270 фг, по меньшей мере 280 фг, по меньшей мере 290 фг, по меньшей мере 300 фг, по меньшей мере 310 фг, по меньшей мере 320 фг, по меньшей мере 330 фг, по меньшей мере 340 фг, по меньшей мере 350 фг, по меньшей мере 360 фг, по меньшей мере 370 фг, по меньшей мере 380 фг, по меньшей мере 390 фг, по меньшей мере 400 фг, по меньшей мере 410 фг, по меньшей мере 420 фг, по меньшей мере 430 фг, по меньшей мере 440 фг, по меньшей мере 450 фг, по меньшей 460 фг, по меньшей мере 470 фг, по меньшей мере 480 фг, по меньшей мере 490 фг, по меньшей мере 500 фг, по меньшей мере 510 фг, по меньшей мере 520 фг, по меньшей мере 530 фг, по меньшей мере 540 фг, по меньшей мере 550 фг, по меньшей мере 560 фг, по меньшей мере 570 фг, по меньшей мере 580 фг, по меньшей мере 590 фг, по меньшей мере 600 фг, по меньшей мере 610 фг, по меньшей мере 620 фг, по меньшей мере 630 фг, по меньшей мере 640 фг, по меньшей мере 650 фг, по меньшей мере 660 фг, по меньшей мере 670 фг, по меньшей мере 680 фг, по меньшей мере 690 фг, по меньшей мере 700 фг, по меньшей мере 710 фг, по меньшей мере 720 фг, по меньшей мере 730 фг, по меньшей мере 740 фг, по меньшей мере 750 фг, по меньшей мере 760 фг, по меньшей мере 770 фг, по меньшей мере 780 фг, по меньшей мере 790 фг, по меньшей мере 800 фг, по меньшей мере 810 фг, по меньшей мере 820 фг, по меньшей мере 830 фг, по меньшей мере 840 фг, по меньшей мере 850 фг, по меньшей мере 860 фг, по меньшей мере 870 фг, по меньшей мере 880 фг, по меньшей мере 890 фг, по меньшей мере 900 фг, по меньшей мере 910 фг, по меньшей мере 920 фг, по меньшей мере 930 фг, по меньшей мере 940 фг, по меньшей мере 950 фг, по меньшей мере 960 фг, по меньшей мере 970 фг, по меньшей мере 980 фг, по меньшей мере 990 фг или по меньшей мере 1000 фг.
[060] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, не более 1 фг, не более 2 фг, не более 3 фг, не более 4 фг, не более 5 фг, не более 6 фг, не более 7 фг, не более 8 фг, не более 9 фг, не более 10 фг, не более 15 фг, не более 20 фг, не более 25 фг, не более 30 фг, не более 35 фг, не более 40 фг, не более 45 фг, не более 50 фг, не более 55 фг, не более 60 фг, не более 65 фг, не более 70 фг, не более 75 фг, не более 80 фг, не более 85 фг, не более 90 фг, не более 95 фг, не более 100 фг, не более 110 фг, не более 120 фг, не более 130 фг, не более 140 фг, не более 150 фг, не более 160 фг, не более 170 фг, не более 180 фг, не более 190 фг, не более 200 фг, не более 210 фг, не более 220 фг, не более 230 фг, не более 240 фг, не более 250 фг, не более 260 фг, не более 270 фг, не более 280 фг, не более 290 фг, не более 300 фг, не более 310 фг, не более 320 фг, не более 330 фг, не более 340 фг, не более 350 фг, не более 360 фг, не более 370 фг, не более 380 фг, не более 390 фг, не более 400 фг, не более 410 фг, не более 420 фг, не более 430 фг, не более 440 фг, не более 450 фг, не более 460 фг, не более 470 фг, не более 480 фг, не более 490 фг, не более 500 фг, не более 510 фг, не более 520 фг, не более 530 фг, не более 540 фг, не более 550 фг, не более 560 фг, не более 570 фг, не более 580 фг, не более 590 фг, не более 600 фг, не более 610 фг, не более 620 фг, не более 630 фг, не более 640 фг, не более 650 фг, не более 660 фг, не более 670 фг, не более 680 фг, не более 690 фг, не более 700 фг, не более 710 фг, не более 720 фг, не более 730 фг, не более 740 фг, не более 750 фг, не более 760 фг, не более 770 фг, не более 780 фг, не более 790 фг, не более 800 фг, не более 810 фг, не более 820 фг, не более 830 фг, не более 840 фг, не более 850 фг, не более 860 фг, не более 870 фг, не более 880 фг, не более 890 фг, не более 900 фг, не более 910 фг, не более 920 фг, не более 930 фг, не более 940 фг, не более 950 фг, не более 960 фг, не более 970 фг, не более 980 фг, не более 990 фг или не более 1000 фг.
[061] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 1 фг до приблизительно 10 фг, от приблизительно 1 фг до приблизительно 20 фг, от приблизительно 1 фг до приблизительно 30 фг, от приблизительно 1 фг до приблизительно 40 фг, от приблизительно 1 фг до приблизительно 50 фг, от приблизительно 1 фг до приблизительно 60 фг, от приблизительно 1 фг до приблизительно 70 фг, от приблизительно 1 фг до приблизительно 80 фг, от приблизительно 1 фг до приблизительно 90 фг, от приблизительно 1 фг до приблизительно 100 фг, от приблизительно 1 фг до приблизительно 110 фг, от приблизительно 1 фг до приблизительно 120 фг, от приблизительно 1 фг до приблизительно 130 фг, от приблизительно 1 фг до приблизительно 140 фг, от приблизительно 1 фг до приблизительно 150 фг, от приблизительно 5 фг до приблизительно 10 фг, от приблизительно 5 фг до приблизительно 20 фг, от приблизительно 5 фг до приблизительно 30 фг, от приблизительно 5 фг до приблизительно 40 фг, от приблизительно 5 фг до приблизительно 50 фг, от приблизительно 5 фг до приблизительно 60 фг, от приблизительно 5 фг до приблизительно 70 фг, от приблизительно 5 фг до приблизительно 80 фг, от приблизительно 5 фг до приблизительно 90 фг, от приблизительно 5 фг до приблизительно 100 фг, от приблизительно 5 фг до приблизительно 110 фг, от приблизительно 5 фг до приблизительно 120 фг, от приблизительно 5 фг до приблизительно 130 фг, от приблизительно 5 фг до приблизительно 140 фг, от приблизительно 5 фг до приблизительно 150 фг, от приблизительно 10 фг до приблизительно 20 фг, от приблизительно 10 фг до приблизительно 30 фг, от приблизительно 10 фг до приблизительно 40 фг, от приблизительно 10 фг до приблизительно 50 фг, от приблизительно 10 фг до приблизительно 60 фг, от приблизительно 10 фг до приблизительно 70 фг, от приблизительно 10 фг до приблизительно 80 фг, от приблизительно 10 фг до приблизительно 90 фг, от приблизительно 10 фг до приблизительно 100 фг, от приблизительно 10 фг до приблизительно 110 фг, от приблизительно 10 фг до приблизительно 120 фг, от приблизительно 10 фг до приблизительно 130 фг, от приблизительно 10 фг до приблизительно 140 фг, от приблизительно 10 фг до приблизительно 150 фг, от приблизительно 10 фг до приблизительно 175 фг, от приблизительно 10 фг до приблизительно 200 фг, от приблизительно 10 фг до приблизительно 225 фг, от приблизительно 10 фг до приблизительно 250 фг, от приблизительно 25 фг до приблизительно 50 фг, от приблизительно 25 фг до приблизительно 75 фг, от приблизительно 25 фг до приблизительно 100 фг, от приблизительно 25 фг до приблизительно 125 фг, от приблизительно 25 фг до приблизительно 150 фг, от приблизительно 25 фг до приблизительно 175 фг, от приблизительно 25 фг до приблизительно 200 фг, от приблизительно 25 фг до приблизительно 225 фг, от приблизительно 25 фг до приблизительно 250 фг, от приблизительно 50 фг до приблизительно 75 фг, от приблизительно 50 фг до приблизительно 100 фг, от приблизительно 50 фг до приблизительно 125 фг, от приблизительно 50 фг до приблизительно 150 фг, от приблизительно 50 фг до приблизительно 175 фг, от приблизительно 50 фг до приблизительно 200 фг, от приблизительно 50 фг до приблизительно 225 фг, от приблизительно 50 фг до приблизительно 250 фг, от приблизительно 75 фг до приблизительно 100 фг, от приблизительно 75 фг до приблизительно 125 фг, от приблизительно 75 фг до приблизительно 150 фг, от приблизительно 75 фг до приблизительно 175 фг, от приблизительно 75 фг до приблизительно 200 фг, от приблизительно 75 фг до приблизительно 225 фг или от приблизительно 75 фг до приблизительно 250 фг.
[062] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 100 фг до приблизительно 125 фг, от приблизительно 100 фг до приблизительно 150 фг, от приблизительно 100 фг до приблизительно 175 фг, от приблизительно 100 фг до приблизительно 200 фг, от приблизительно 100 фг до приблизительно 225 фг, от приблизительно 100 фг до приблизительно 250 фг, от приблизительно 100 фг до приблизительно 275 фг, от приблизительно 100 фг до приблизительно 300 фг, от приблизительно 100 фг до приблизительно 325 фг, от приблизительно 100 фг до приблизительно 350 фг, от приблизительно 100 фг до приблизительно 375 фг, от приблизительно 100 фг до приблизительно 400 фг, от приблизительно 100 фг до приблизительно 425 фг, от приблизительно 100 фг до приблизительно 450 фг, от приблизительно 100 фг до приблизительно 475 фг, от приблизительно 100 фг до приблизительно 500 фг, от приблизительно 100 фг до приблизительно 525 фг, от приблизительно 100 фг до приблизительно 550 фг, от приблизительно 100 фг до приблизительно 575 фг, от приблизительно 100 фг до приблизительно 600 фг, от приблизительно 125 фг до приблизительно 150 фг, от приблизительно 125 фг до приблизительно 175 фг, от приблизительно 125 фг до приблизительно 200 фг, от приблизительно 125 фг до приблизительно 225 фг, от приблизительно 125 фг до приблизительно 250 фг, от приблизительно 125 фг до приблизительно 275 фг, от приблизительно 125 фг до приблизительно 300 фг, от приблизительно 125 фг до приблизительно 325 фг, от приблизительно 125 фг до приблизительно 350 фг, от приблизительно 125 фг до приблизительно 375 фг, от приблизительно 125 фг до приблизительно 400 фг, от приблизительно 125 фг до приблизительно 425 фг, от приблизительно 125 фг до приблизительно 450 фг, от приблизительно 125 фг до приблизительно 475 фг, от приблизительно 125 фг до приблизительно 500 фг, от приблизительно 125 фг до приблизительно 525 фг, от приблизительно 125 фг до приблизительно 550 фг, от приблизительно 125 фг до приблизительно 575 фг, от приблизительно 125 фг до приблизительно 600 фг, от приблизительно 150 фг до приблизительно 175 фг, от приблизительно 150 фг до приблизительно 200 фг, от приблизительно 150 фг до приблизительно 225 фг, от приблизительно 150 фг до приблизительно 250 фг, от приблизительно 150 фг до приблизительно 275 фг, от приблизительно 150 фг до приблизительно 300 фг, от приблизительно 150 фг до приблизительно 325 фг, от приблизительно 150 фг до приблизительно 350 фг, от приблизительно 150 фг до приблизительно 375 фг, от приблизительно 150 фг до приблизительно 400 фг, от приблизительно 150 фг до приблизительно 425 фг, от приблизительно 150 фг до приблизительно 450 фг, от приблизительно 150 фг до приблизительно 475 фг, от приблизительно 150 фг до приблизительно 500 фг, от приблизительно 150 фг до приблизительно 525 фг, от приблизительно 150 фг до приблизительно 550 фг, от приблизительно 150 фг до приблизительно 575 фг, от приблизительно 150 фг до приблизительно 600 фг, от приблизительно 200 фг до приблизительно 225 фг, от приблизительно 200 фг до приблизительно 250 фг, от приблизительно 200 фг до приблизительно 275 фг, от приблизительно 200 фг до приблизительно 300 фг, от приблизительно 200 фг до приблизительно 325 фг, от приблизительно 200 фг до приблизительно 350 фг, от приблизительно 200 фг до приблизительно 375 фг, от приблизительно 200 фг до приблизительно 400 фг, от приблизительно 200 фг до приблизительно 425 фг, от приблизительно 200 фг до приблизительно 450 фг, от приблизительно 200 фг до приблизительно 475 фг, от приблизительно 200 фг до приблизительно 500 фг, от приблизительно 200 фг до приблизительно 525 фг, от приблизительно 200 фг до приблизительно 550 фг, от приблизительно 200 фг до приблизительно 575 фг, от приблизительно 200 фг до приблизительно 600 фг, от приблизительно 200 фг до приблизительно 625 фг, от приблизительно 200 фг до приблизительно 650 фг, от приблизительно 200 фг до приблизительно 675 фг, от приблизительно 200 фг до приблизительно 700 фг, от приблизительно 200 фг до приблизительно 725 фг, от приблизительно 200 фг до приблизительно 750 фг, от приблизительно 200 фг до приблизительно 775 фг, от приблизительно 200 фг до приблизительно 800 фг, от приблизительно 200 фг до приблизительно 825 фг, от приблизительно 200 фг до приблизительно 850 фг, от приблизительно 200 фг до приблизительно 875 фг, от приблизительно 200 фг до приблизительно 900 фг, от приблизительно 200 фг до приблизительно 925 фг, от приблизительно 200 фг до приблизительно 950 фг, от приблизительно 200 фг до приблизительно 975 фг, от приблизительно 200 фг до приблизительно 1000 фг.
[063] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 250 фг до приблизительно 275 фг, от приблизительно 250 фг до приблизительно 300 фг, от приблизительно 250 фг до приблизительно 325 фг, от приблизительно 250 фг до приблизительно 350 фг, от приблизительно 250 фг до приблизительно 375 фг, от приблизительно 250 фг до приблизительно 400 фг, от приблизительно 250 фг до приблизительно 425 фг, от приблизительно 250 фг до приблизительно 450 фг, от приблизительно 250 фг до приблизительно 475 фг, от приблизительно 250 фг до приблизительно 500 фг, от приблизительно 250 фг до приблизительно 525 фг, от приблизительно 250 фг до приблизительно 550 фг, от приблизительно 250 фг до приблизительно 575 фг, от приблизительно 250 фг до приблизительно 600 фг, от приблизительно 250 фг до приблизительно 625 фг, от приблизительно 250 фг до приблизительно 650 фг, от приблизительно 250 фг до приблизительно 675 фг, от приблизительно 250 фг до приблизительно 700 фг, от приблизительно 250 фг до приблизительно 725 фг, от приблизительно 250 фг до приблизительно 750 фг, от приблизительно 250 фг до приблизительно 775 фг, от приблизительно 250 фг до приблизительно 800 фг, от приблизительно 250 фг до приблизительно 825 фг, от приблизительно 250 фг до приблизительно 850 фг, от приблизительно 250 фг до приблизительно 875 фг, от приблизительно 250 фг до приблизительно 900 фг, от приблизительно 250 фг до приблизительно 925 фг, от приблизительно 250 фг до приблизительно 950 фг, от приблизительно 250 фг до приблизительно 975 фг, от приблизительно 250 фг до приблизительно 1,000 фг, от приблизительно 300 фг до приблизительно 325 фг, от приблизительно 300 фг до приблизительно 350 фг, от приблизительно 300 фг до приблизительно 375 фг, от приблизительно 300 фг до приблизительно 400 фг, от приблизительно 300 фг до приблизительно 425 фг, от приблизительно 300 фг до приблизительно 450 фг, от приблизительно 300 фг до приблизительно 475 фг, от приблизительно 300 фг до приблизительно 500 фг, от приблизительно 300 фг до приблизительно 525 фг, от приблизительно 300 фг до приблизительно 550 фг, от приблизительно 300 фг до приблизительно 575 фг, от приблизительно 300 фг до приблизительно 600 фг, от приблизительно 300 фг до приблизительно 625 фг, от приблизительно 300 фг до приблизительно 650 фг, от приблизительно 300 фг до приблизительно 675 фг, от приблизительно 300 фг до приблизительно 700 фг, от приблизительно 300 фг до приблизительно 725 фг, от приблизительно 300 фг до приблизительно 750 фг, от приблизительно 300 фг до приблизительно 775 фг, от приблизительно 300 фг до приблизительно 800 фг, от приблизительно 300 фг до приблизительно 825 фг, от приблизительно 300 фг до приблизительно 850 фг, от приблизительно 300 фг до приблизительно 875 фг, от приблизительно 300 фг до приблизительно 900 фг, от приблизительно 300 фг до приблизительно 925 фг, от приблизительно 300 фг до приблизительно 950 фг, от приблизительно 300 фг до приблизительно 975 фг, от приблизительно 300 фг до приблизительно 1000 фг, от приблизительно 400 фг до приблизительно 425 фг, от приблизительно 400 фг до приблизительно 450 фг, от приблизительно 400 фг до приблизительно 475 фг, от приблизительно 400 фг до приблизительно 500 фг, от приблизительно 400 фг до приблизительно 525 фг, от приблизительно 400 фг до приблизительно 550 фг, от приблизительно 400 фг до приблизительно 575 фг, от приблизительно 400 фг до приблизительно 600 фг, от приблизительно 400 фг до приблизительно 625 фг, от приблизительно 400 фг до приблизительно 650 фг, от приблизительно 400 фг до приблизительно 675 фг, от приблизительно 400 фг до приблизительно 700 фг, от приблизительно 400 фг до приблизительно 725 фг, от приблизительно 400 фг до приблизительно 750 фг, от приблизительно 400 фг до приблизительно 775 фг, от приблизительно 400 фг до приблизительно 800 фг, от приблизительно 400 фг до приблизительно 825 фг, от приблизительно 400 фг до приблизительно 850 фг, от приблизительно 400 фг до приблизительно 875 фг, от приблизительно 400 фг до приблизительно 900 фг, от приблизительно 400 фг до приблизительно 925 фг, от приблизительно 400 фг до приблизительно 950 фг, от приблизительно 400 фг до приблизительно 975 фг или от приблизительно 400 фг до приблизительно 1000 фг.
[064] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 500 фг до приблизительно 525 фг, от приблизительно 500 фг до приблизительно 550 фг, от приблизительно 500 фг до приблизительно 575 фг, от приблизительно 500 фг до приблизительно 600 фг, от приблизительно 500 фг до приблизительно 625 фг, от приблизительно 500 фг до приблизительно 650 фг, от приблизительно 500 фг до приблизительно 675 фг, от приблизительно 500 фг до приблизительно 700 фг, от приблизительно 500 фг до приблизительно 725 фг, от приблизительно 500 фг до приблизительно 750 фг, от приблизительно 500 фг до приблизительно 775 фг, от приблизительно 500 фг до приблизительно 800 фг, от приблизительно 500 фг до приблизительно 825 фг, от приблизительно 500 фг до приблизительно 850 фг, от приблизительно 500 фг до приблизительно 875 фг, от приблизительно 500 фг до приблизительно 900 фг, от приблизительно 500 фг до приблизительно 925 фг, от приблизительно 500 фг до приблизительно 950 фг, от приблизительно 500 фг до приблизительно 975 фг, от приблизительно 500 фг до приблизительно 1000 фг, от приблизительно 600 фг до приблизительно 625 фг, от приблизительно 600 фг до приблизительно 650 фг, от приблизительно 600 фг до приблизительно 675 фг, от приблизительно 600 фг до приблизительно 700 фг, от приблизительно 600 фг до приблизительно 725 фг, от приблизительно 600 фг до приблизительно 750 фг, от приблизительно 600 фг до приблизительно 775 фг, от приблизительно 600 фг до приблизительно 800 фг, от приблизительно 600 фг до приблизительно 825 фг, от приблизительно 600 фг до приблизительно 850 фг, от приблизительно 600 фг до приблизительно 875 фг, от приблизительно 600 фг до приблизительно 900 фг, от приблизительно 600 фг до приблизительно 925 фг, от приблизительно 600 фг до приблизительно 950 фг, от приблизительно 600 фг до приблизительно 975 фг, от приблизительно 600 фг до приблизительно 1000 фг, от приблизительно 700 фг до приблизительно 725 фг, от приблизительно 700 фг до приблизительно 750 фг, от приблизительно 700 фг до приблизительно 775 фг, от приблизительно 700 фг до приблизительно 800 фг, от приблизительно 700 фг до приблизительно 825 фг, от приблизительно 700 фг до приблизительно 850 фг, от приблизительно 700 фг до приблизительно 875 фг, от приблизительно 700 фг до приблизительно 900 фг, от приблизительно 700 фг до приблизительно 925 фг, от приблизительно 700 фг до приблизительно 950 фг, от приблизительно 700 фг до приблизительно 975 фг, от приблизительно 700 фг до приблизительно 1000 фг, от приблизительно 800 фг до приблизительно 825 фг, от приблизительно 800 фг до приблизительно 850 фг, от приблизительно 800 фг до приблизительно 875 фг, от приблизительно 800 фг до приблизительно 900 фг, от приблизительно 800 фг до приблизительно 925 фг, от приблизительно 800 фг до приблизительно 950 фг, от приблизительно 800 фг до приблизительно 975 фг или от приблизительно 800 фг до приблизительно 1000 фг.
[065] В аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, приблизительно 1 нг, приблизительно 2 нг, приблизительно 3 нг, приблизительно 4 нг, приблизительно 5 нг, приблизительно 6 нг, приблизительно 7 нг, приблизительно 8 нг, приблизительно 9 нг, приблизительно 10 нг, приблизительно 15 нг, приблизительно 20 нг, приблизительно 25 нг, приблизительно 30 нг, приблизительно 35 нг, приблизительно 40 нг, приблизительно 45 нг, приблизительно 50 нг, приблизительно 55 нг, приблизительно 60 нг, приблизительно 65 нг, приблизительно 70 нг, приблизительно 75 нг, приблизительно 80 нг, приблизительно 85 нг, приблизительно 90 нг, приблизительно 95 нг, приблизительно 100 нг, приблизительно 110 нг, приблизительно 120 нг, приблизительно 130 нг, приблизительно 140 нг, приблизительно 150 нг, приблизительно 160 нг, приблизительно 170 нг, приблизительно 180 нг, приблизительно 190 нг, приблизительно 200 нг, приблизительно 210 нг, приблизительно 220 нг, приблизительно 230 нг, приблизительно 240 нг, приблизительно 250 нг, приблизительно 260 нг, приблизительно 270 нг, приблизительно 280 нг, приблизительно 290 нг, приблизительно 300 нг, приблизительно 310 нг, приблизительно 320 нг, приблизительно 330 нг, приблизительно 340 нг, приблизительно 350 нг, приблизительно 360 нг, приблизительно 370 нг, приблизительно 380 нг, приблизительно 390 нг, приблизительно 400 нг, приблизительно 410 нг, приблизительно 420 нг, приблизительно 430 нг, приблизительно 440 нг, приблизительно 450 нг, приблизительно 460 нг, приблизительно 470 нг, приблизительно 480 нг, приблизительно 490 нг, приблизительно 500 нг, приблизительно 510 нг, приблизительно 520 нг, приблизительно 530 нг, приблизительно 540 нг, приблизительно 550 нг, приблизительно 560 нг, приблизительно 570 нг, приблизительно 580 нг, приблизительно 590 нг, приблизительно 600 нг, приблизительно 610 нг, приблизительно 620 нг, приблизительно 630 нг, приблизительно 640 нг, приблизительно 650 нг, приблизительно 660 нг, приблизительно 670 нг, приблизительно 680 нг, приблизительно 690 нг, приблизительно 700 нг, приблизительно 710 нг, приблизительно 720 нг, приблизительно 730 нг, приблизительно 740 нг, приблизительно 750 нг, приблизительно 760 нг, приблизительно 770 нг, приблизительно 780 нг, приблизительно 790 нг, приблизительно 800 нг, приблизительно 810 нг, приблизительно 820 нг, приблизительно 830 нг, приблизительно 840 нг, приблизительно 850 нг, приблизительно 860 нг, приблизительно 870 нг, приблизительно 880 нг, приблизительно 890 нг, приблизительно 900 нг, приблизительно 910 нг, приблизительно 920 нг, приблизительно 930 нг, приблизительно 940 нг, приблизительно 950 нг, приблизительно 960 нг, приблизительно 970 нг, приблизительно 980 нг, приблизительно 990 нг или приблизительно 1000 нг.
[066] В других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, по меньшей мере 1 нг, по меньшей мере 2 нг, по меньшей мере 3 нг, по меньшей мере 4 нг, по меньшей мере 5 нг, по меньшей мере 6 нг, по меньшей мере 7 нг, по меньшей мере 8 нг, по меньшей мере 9 нг, по меньшей мере 10 нг, по меньшей мере 15 нг, по меньшей мере 20 нг, по меньшей мере 25 нг, по меньшей мере 30 нг, по меньшей мере 35 нг, по меньшей мере 40 нг, по меньшей мере 45 нг, по меньшей мере 50 нг, по меньшей мере 55 нг, по меньшей мере 60 нг, по меньшей мере 65 нг, по меньшей мере 70 нг, по меньшей мере 75 нг, по меньшей мере 80 нг, по меньшей мере 85 нг, по меньшей мере 90 нг, по меньшей мере 95 нг, по меньшей мере 100 нг, по меньшей мере 110 нг, по меньшей мере 120 нг, по меньшей мере 130 нг, по меньшей мере 140 нг, по меньшей мере 150 нг, по меньшей мере 160 нг, по меньшей мере 170 нг, по меньшей мере 180 нг, по меньшей мере 190 нг, по меньшей мере 200 нг, по меньшей мере 210 нг, по меньшей мере 220 нг, по меньшей мере 230 нг, по меньшей мере 240 нг, по меньшей мере 250 нг, по меньшей мере 260 нг, по меньшей мере 270 нг, по меньшей мере 280 нг, по меньшей мере 290 нг, по меньшей мере 300 нг, по меньшей мере 310 нг, по меньшей мере 320 нг, по меньшей мере 330 нг, по меньшей мере 340 нг, по меньшей мере 350 нг, по меньшей мере 360 нг, по меньшей мере 370 нг, по меньшей мере 380 нг, по меньшей мере 390 нг, по меньшей мере 400 нг, по меньшей мере 410 нг, по меньшей мере 420 нг, по меньшей мере 430 нг, по меньшей мере 440 нг, по меньшей мере 450 нг, по меньшей мере 460 нг, по меньшей мере 470 нг, по меньшей мере 480 нг, по меньшей мере 490 нг, по меньшей мере 500 нг, по меньшей мере 510 нг, по меньшей мере 520 нг, по меньшей мере 530 нг, по меньшей мере 540 нг, по меньшей мере 550 нг, по меньшей мере 560 нг, по меньшей мере 570 нг, по меньшей мере 580 нг, по меньшей мере 590 нг, по меньшей мере 600 нг, по меньшей мере 610 нг, по меньшей мере 620 нг, по меньшей мере 630 нг, по меньшей мере 640 нг, по меньшей мере 650 нг, по меньшей мере 660 нг, по меньшей мере 670 нг, по меньшей мере 680 нг, по меньшей мере 690 нг, по меньшей мере 700 нг, по меньшей мере 710 нг, по меньшей мере 720 нг, по меньшей мере 730 нг, по меньшей мере 740 нг, по меньшей мере 750 нг, по меньшей мере 760 нг, по меньшей мере 770 нг, по меньшей мере 780 нг, по меньшей мере 790 нг, по меньшей мере 800 нг, по меньшей мере 810 нг, по меньшей мере 820 нг, по меньшей мере 830 нг, по меньшей мере 840 нг, по меньшей мере 850 нг, по меньшей мере 860 нг, по меньшей мере 870 нг, по меньшей мере 880 нг, по меньшей мере 890 нг, по меньшей мере 900 нг, по меньшей мере 910 нг, по меньшей мере 920 нг, по меньшей мере 930 нг, по меньшей мере 940 нг, по меньшей мере 950 нг, по меньшей мере 960 нг, по меньшей мере 970 нг, по меньшей мере 980 нг, по меньшей мере 990 нг или по меньшей мере 1000 нг.
[067] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, не более 1 нг, не более 2 нг, не более 3 нг, не более 4 нг, не более 5 нг, не более 6 нг, не более 7 нг, не более 8 нг, не более 9 нг, не более 10 нг, не более 15 нг, не более 20 нг, не более 25 нг, не более 30 нг, не более 35 нг, не более 40 нг, не более 45 нг, не более 50 нг, не более 55 нг, не более 60 нг, не более 65 нг, не более 70 нг, не более 75 нг, не более 80 нг, не более 85 нг, не более 90 нг, не более 95 нг, не более 100 нг, не более 110 нг, не более 120 нг, не более 130 нг, не более 140 нг, не более 150 нг, не более 160 нг, не более 170 нг, не более 180 нг, не более 190 нг, не более 200 нг, не более 210 нг, не более 220 нг, не более 230 нг, не более 240 нг, не более 250 нг, не более 260 нг, не более 270 нг, не более 280 нг, не более 290 нг, не более 300 нг, не более 310 нг, не более 320 нг, не более 330 нг, не более 340 нг, не более 350 нг, не более 360 нг, не более 370 нг, не более 380 нг, не более 390 нг, не более 400 нг, не более 410 нг, не более 420 нг, не более 430 нг, не более 440 нг, не более 450 нг, не более 460 нг, не более 470 нг, не более 480 нг, не более 490 нг, не более 500 нг, не более 510 нг, не более 520 нг, не более 530 нг, не более 540 нг, не более 550 нг, не более 560 нг, не более 570 нг, не более 580 нг, не более 590 нг, не более 600 нг, не более 610 нг, не более 620 нг, не более 630 нг, не более 640 нг, не более 650 нг, не более 660 нг, не более 670 нг, не более 680 нг, не более 690 нг, не более 700 нг, не более 710 нг, не более 720 нг, не более 730 нг, не более 740 нг, не более 750 нг, не более 760 нг, не более 770 нг, не более 780 нг, не более 790 нг, не более 800 нг, не более 810 нг, не более 820 нг, не более 830 нг, не более 840 нг, не более 850 нг, не более 860 нг, не более 870 нг, не более 880 нг, не более 890 нг, не более 900 нг, не более 910 нг, не более 920 нг, не более 930 нг, не более 940 нг, не более 950 нг, не более 960 нг, не более 970 нг, не более 980 нг, не более 990 нг или не более 1000 нг.
[068] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 1 нг до приблизительно 10 нг, от приблизительно 1 нг до приблизительно 20 нг, от приблизительно 1 нг до приблизительно 30 нг, от приблизительно 1 нг до приблизительно 40 нг, от приблизительно 1 нг до приблизительно 50 нг, от приблизительно 1 нг до приблизительно 60 нг, от приблизительно 1 нг до приблизительно 70 нг, от приблизительно 1 нг до приблизительно 80 нг, от приблизительно 1 нг до приблизительно 90 нг, от приблизительно 1 нг до приблизительно 100 нг, от приблизительно 1 нг до приблизительно 110 нг, от приблизительно 1 нг до приблизительно 120 нг, от приблизительно 1 нг до приблизительно 130 нг, от приблизительно 1 нг до приблизительно 140 нг, от приблизительно 1 нг до приблизительно 150 нг, от приблизительно 5 нг до приблизительно 10 нг, от приблизительно 5 нг до приблизительно 20 нг, от приблизительно 5 нг до приблизительно 30 нг, от приблизительно 5 нг до приблизительно 40 нг, от приблизительно 5 нг до приблизительно 50 нг, от приблизительно 5 нг до приблизительно 60 нг, от приблизительно 5 нг до приблизительно 70 нг, от приблизительно 5 нг до приблизительно 80 нг, от приблизительно 5 нг до приблизительно 90 нг, от приблизительно 5 нг до приблизительно 100 нг, от приблизительно 5 нг до приблизительно 110 нг, от приблизительно 5 нг до приблизительно 120 нг, от приблизительно 5 нг до приблизительно 130 нг, от приблизительно 5 нг до приблизительно 140 нг, от приблизительно 5 нг до приблизительно 150 нг, от приблизительно 10 нг до приблизительно 20 нг, от приблизительно 10 нг до приблизительно 30 нг, от приблизительно 10 нг до приблизительно 40 нг, от приблизительно 10 нг до приблизительно 50 нг, от приблизительно 10 нг до приблизительно 60 нг, от приблизительно 10 нг до приблизительно 70 нг, от приблизительно 10 нг до приблизительно 80 нг, от приблизительно 10 нг до приблизительно 90 нг, от приблизительно 10 нг до приблизительно 100 нг, от приблизительно 10 нг до приблизительно 110 нг, от приблизительно 10 нг до приблизительно 120 нг, от приблизительно 10 нг до приблизительно 130 нг, от приблизительно 10 нг до приблизительно 140 нг, от приблизительно 10 нг до приблизительно 150 нг, от приблизительно 10 нг до приблизительно 175 нг, от приблизительно 10 нг до приблизительно 200 нг, от приблизительно 10 нг до приблизительно 225 нг, от приблизительно 10 нг до приблизительно 250 нг, от приблизительно 25 нг до приблизительно 50 нг, от приблизительно 25 нг до приблизительно 75 нг, от приблизительно 25 нг до приблизительно 100 нг, от приблизительно 25 нг до приблизительно 125 нг, от приблизительно 25 нг до приблизительно 150 нг, от приблизительно 25 нг до приблизительно 175 нг, от приблизительно 25 нг до приблизительно 200 нг, от приблизительно 25 нг до приблизительно 225 нг, от приблизительно 25 нг до приблизительно 250 нг, от приблизительно 50 нг до приблизительно 75 нг, от приблизительно 50 нг до приблизительно 100 нг, от приблизительно 50 нг до приблизительно 125 нг, от приблизительно 50 нг до приблизительно 150 нг, от приблизительно 50 нг до приблизительно 175 нг, от приблизительно 50 нг до приблизительно 200 нг, от приблизительно 50 нг до приблизительно 225 нг, от приблизительно 50 нг до приблизительно 250 нг, от приблизительно 75 нг до приблизительно 100 нг, от приблизительно 75 нг до приблизительно 125 нг, от приблизительно 75 нг до приблизительно 150 нг, от приблизительно 75 нг до приблизительно 175 нг, от приблизительно 75 нг до приблизительно 200 нг, от приблизительно 75 нг до приблизительно 225 нг или от приблизительно 75 нг до приблизительно 250 нг.
[069] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 100 нг до приблизительно 125 нг, от приблизительно 100 нг до приблизительно 150 нг, от приблизительно 100 нг до приблизительно 175 нг, от приблизительно 100 нг до приблизительно 200 нг, от приблизительно 100 нг до приблизительно 225 нг, от приблизительно 100 нг до приблизительно 250 нг, от приблизительно 100 нг до приблизительно 275 нг, от приблизительно 100 нг до приблизительно 300 нг, от приблизительно 100 нг до приблизительно 325 нг, от приблизительно 100 нг до приблизительно 350 нг, от приблизительно 100 нг до приблизительно 375 нг, от приблизительно 100 нг до приблизительно 400 нг, от приблизительно 100 нг до приблизительно 425 нг, от приблизительно 100 нг до приблизительно 450 нг, от приблизительно 100 нг до приблизительно 475 нг, от приблизительно 100 нг до приблизительно 500 нг, от приблизительно 100 нг до приблизительно 525 нг, от приблизительно 100 нг до приблизительно 550 нг, от приблизительно 100 нг до приблизительно 575 нг, от приблизительно 100 нг до приблизительно 600 нг, от приблизительно 125 нг до приблизительно 150 нг, от приблизительно 125 нг до приблизительно 175 нг, от приблизительно 125 нг до приблизительно 200 нг, от приблизительно 125 нг до приблизительно 225 нг, от приблизительно 125 нг до приблизительно 250 нг, от приблизительно 125 нг до приблизительно 275 нг, от приблизительно 125 нг до приблизительно 300 нг, от приблизительно 125 нг до приблизительно 325 нг, от приблизительно 125 нг до приблизительно 350 нг, от приблизительно 125 нг до приблизительно 375 нг, от приблизительно 125 нг до приблизительно 400 нг, от приблизительно 125 нг до приблизительно 425 нг, от приблизительно 125 нг до приблизительно 450 нг, от приблизительно 125 нг до приблизительно 475 нг, от приблизительно 125 нг до приблизительно 500 нг, от приблизительно 125 нг до приблизительно 525 нг, от приблизительно 125 нг до приблизительно 550 нг, от приблизительно 125 нг до приблизительно 575 нг, от приблизительно 125 нг до приблизительно 600 нг, от приблизительно 150 нг до приблизительно 175 нг, от приблизительно 150 нг до приблизительно 200 нг, от приблизительно 150 нг до приблизительно 225 нг, от приблизительно 150 нг до приблизительно 250 нг, от приблизительно 150 нг до приблизительно 275 нг, от приблизительно 150 нг до приблизительно 300 нг, от приблизительно 150 нг до приблизительно 325 нг, от приблизительно 150 нг до приблизительно 350 нг, от приблизительно 150 нг до приблизительно 375 нг, от приблизительно 150 нг до приблизительно 400 нг, от приблизительно 150 нг до приблизительно 425 нг, от приблизительно 150 нг до приблизительно 450 нг, от приблизительно 150 нг до приблизительно 475 нг, от приблизительно 150 нг до приблизительно 500 нг, от приблизительно 150 нг до приблизительно 525 нг, от приблизительно 150 нг до приблизительно 550 нг, от приблизительно 150 нг до приблизительно 575 нг, от приблизительно 150 нг до приблизительно 600 нг, от приблизительно 200 нг до приблизительно 225 нг, от приблизительно 200 нг до приблизительно 250 нг, от приблизительно 200 нг до приблизительно 275 нг, от приблизительно 200 нг до приблизительно 300 нг, от приблизительно 200 нг до приблизительно 325 нг, от приблизительно 200 нг до приблизительно 350 нг, от приблизительно 200 нг до приблизительно 375 нг, от приблизительно 200 нг до приблизительно 400 нг, от приблизительно 200 нг до приблизительно 425 нг, от приблизительно 200 нг до приблизительно 450 нг, от приблизительно 200 нг до приблизительно 475 нг, от приблизительно 200 нг до приблизительно 500 нг, от приблизительно 200 нг до приблизительно 525 нг, от приблизительно 200 нг до приблизительно 550 нг, от приблизительно 200 нг до приблизительно 575 нг, от приблизительно 200 нг до приблизительно 600 нг, от приблизительно 200 нг до приблизительно 625 нг, от приблизительно 200 нг до приблизительно 650 нг, от приблизительно 200 нг до приблизительно 675 нг, от приблизительно 200 нг до приблизительно 700 нг, от приблизительно 200 нг до приблизительно 725 нг, от приблизительно 200 нг до приблизительно 750 нг, от приблизительно 200 нг до приблизительно 775 нг, от приблизительно 200 нг до приблизительно 800 нг, от приблизительно 200 нг до приблизительно 825 нг, от приблизительно 200 нг до приблизительно 850 нг, от приблизительно 200 нг до приблизительно 875 нг, от приблизительно 200 нг до приблизительно 900 нг, от приблизительно 200 нг до приблизительно 925 нг, от приблизительно 200 нг до приблизительно 950 нг, от приблизительно 200 нг до приблизительно 975 нг или от приблизительно 200 нг до приблизительно 1000 нг.
[070] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 250 нг до приблизительно 275 нг, от приблизительно 250 нг до приблизительно 300 нг, от приблизительно 250 нг до приблизительно 325 нг, от приблизительно 250 нг до приблизительно 350 нг, от приблизительно 250 нг до приблизительно 375 нг, от приблизительно 250 нг до приблизительно 400 нг, от приблизительно 250 нг до приблизительно 425 нг, от приблизительно 250 нг до приблизительно 450 нг, от приблизительно 250 нг до приблизительно 475 нг, от приблизительно 250 нг до приблизительно 500 нг, от приблизительно 250 нг до приблизительно 525 нг, от приблизительно 250 нг до приблизительно 550 нг, от приблизительно 250 нг до приблизительно 575 нг, от приблизительно 250 нг до приблизительно 600 нг, от приблизительно 250 нг до приблизительно 625 нг, от приблизительно 250 нг до приблизительно 650 нг, от приблизительно 250 нг до приблизительно 675 нг, от приблизительно 250 нг до приблизительно 700 нг, от приблизительно 250 нг до приблизительно 725 нг, от приблизительно 250 нг до приблизительно 750 нг, от приблизительно 250 нг до приблизительно 775 нг, от приблизительно 250 нг до приблизительно 800 нг, от приблизительно 250 нг до приблизительно 825 нг, от приблизительно 250 нг до приблизительно 850 нг, от приблизительно 250 нг до приблизительно 875 нг, от приблизительно 250 нг до приблизительно 900 нг, от приблизительно 250 нг до приблизительно 925 нг, от приблизительно 250 нг до приблизительно 950 нг, от приблизительно 250 нг до приблизительно 975 нг, от приблизительно 250 нг до приблизительно 1000 нг, от приблизительно 300 нг до приблизительно 325 нг, от приблизительно 300 нг до приблизительно 350 нг, от приблизительно 300 нг до приблизительно 375 нг, от приблизительно 300 нг до приблизительно 400 нг, от приблизительно 300 нг до приблизительно 425 нг, от приблизительно 300 нг до приблизительно 450 нг, от приблизительно 300 нг до приблизительно 475 нг, от приблизительно 300 нг до приблизительно 500 нг, от приблизительно 300 нг до приблизительно 525 нг, от приблизительно 300 нг до приблизительно 550 нг, от приблизительно 300 нг до приблизительно 575 нг, от приблизительно 300 нг до приблизительно 600 нг, от приблизительно 300 нг до приблизительно 625 нг, от приблизительно 300 нг до приблизительно 650 нг, от приблизительно 300 нг до приблизительно 675 нг, от приблизительно 300 нг до приблизительно 700 нг, от приблизительно 300 нг до приблизительно 725 нг, от приблизительно 300 нг до приблизительно 750 нг, от приблизительно 300 нг до приблизительно 775 нг, от приблизительно 300 нг до приблизительно 800 нг, от приблизительно 300 нг до приблизительно 825 нг, от приблизительно 300 нг до приблизительно 850 нг, от приблизительно 300 нг до приблизительно 875 нг, от приблизительно 300 нг до приблизительно 900 нг, от приблизительно 300 нг до приблизительно 925 нг, от приблизительно 300 нг до приблизительно 950 нг, от приблизительно 300 нг до приблизительно 975 нг, от приблизительно 300 нг до приблизительно 1000 нг, от приблизительно 400 нг до приблизительно 425 нг, от приблизительно 400 нг до приблизительно 450 нг, от приблизительно 400 нг до приблизительно 475 нг, от приблизительно 400 нг до приблизительно 500 нг, от приблизительно 400 нг до приблизительно 525 нг, от приблизительно 400 нг до приблизительно 550 нг, от приблизительно 400 нг до приблизительно 575 нг, от приблизительно 400 нг до приблизительно 600 нг, от приблизительно 400 нг до приблизительно 625 нг, от приблизительно 400 нг до приблизительно 650 нг, от приблизительно 400 нг до приблизительно 675 нг, от приблизительно 400 нг до приблизительно 700 нг, от приблизительно 400 нг до приблизительно 725 нг, от приблизительно 400 нг до приблизительно 750 нг, от приблизительно 400 нг до приблизительно 775 нг, от приблизительно 400 нг до приблизительно 800 нг, от приблизительно 400 нг до приблизительно 825 нг, от приблизительно 400 нг до приблизительно 850 нг, от приблизительно 400 нг до приблизительно 875 нг, от приблизительно 400 нг до приблизительно 900 нг, от приблизительно 400 нг до приблизительно 925 нг, от приблизительно 400 нг до приблизительно 950 нг, от приблизительно 400 нг до приблизительно 975 нг или от приблизительно 400 нг до приблизительно 1000 нг.
[071] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 500 нг до приблизительно 525 нг, от приблизительно 500 нг до приблизительно 550 нг, от приблизительно 500 нг до приблизительно 575 нг, от приблизительно 500 нг до приблизительно 600 нг, от приблизительно 500 нг до приблизительно 625 нг, от приблизительно 500 нг до приблизительно 650 нг, от приблизительно 500 нг до приблизительно 675 нг, от приблизительно 500 нг до приблизительно 700 нг, от приблизительно 500 нг до приблизительно 725 нг, от приблизительно 500 нг до приблизительно 750 нг, от приблизительно 500 нг до приблизительно 775 нг, от приблизительно 500 нг до приблизительно 800 нг, от приблизительно 500 нг до приблизительно 825 нг, от приблизительно 500 нг до приблизительно 850 нг, от приблизительно 500 нг до приблизительно 875 нг, от приблизительно 500 нг до приблизительно 900 нг, от приблизительно 500 нг до приблизительно 925 нг, от приблизительно 500 нг до приблизительно 950 нг, от приблизительно 500 нг до приблизительно 975 нг, от приблизительно 500 нг до приблизительно 1000 нг, от приблизительно 600 нг до приблизительно 625 нг, от приблизительно 600 нг до приблизительно 650 нг, от приблизительно 600 нг до приблизительно 675 нг, от приблизительно 600 нг до приблизительно 700 нг, от приблизительно 600 нг до приблизительно 725 нг, от приблизительно 600 нг до приблизительно 750 нг, от приблизительно 600 нг до приблизительно 775 нг, от приблизительно 600 нг до приблизительно 800 нг, от приблизительно 600 нг до приблизительно 825 нг, от приблизительно 600 нг до приблизительно 850 нг, от приблизительно 600 нг до приблизительно 875 нг, от приблизительно 600 нг до приблизительно 900 нг, от приблизительно 600 нг до приблизительно 925 нг, от приблизительно 600 нг до приблизительно 950 нг, от приблизительно 600 нг до приблизительно 975 нг, от приблизительно 600 нг до приблизительно 1000 нг, от приблизительно 700 нг до приблизительно 725 нг, от приблизительно 700 нг до приблизительно 750 нг, от приблизительно 700 нг до приблизительно 775 нг, от приблизительно 700 нг до приблизительно 800 нг, от приблизительно 700 нг до приблизительно 825 нг, от приблизительно 700 нг до приблизительно 850 нг, от приблизительно 700 нг до приблизительно 875 нг, от приблизительно 700 нг до приблизительно 900 нг, от приблизительно 700 нг до приблизительно 925 нг, от приблизительно 700 нг до приблизительно 950 нг, от приблизительно 700 нг до приблизительно 975 нг, от приблизительно 700 нг до приблизительно 1000 нг, от приблизительно 800 нг до приблизительно 825 нг, от приблизительно 800 нг до приблизительно 850 нг, от приблизительно 800 нг до приблизительно 875 нг, от приблизительно 800 нг до приблизительно 900 нг, от приблизительно 800 нг до приблизительно 925 нг, от приблизительно 800 нг до приблизительно 950 нг, от приблизительно 800 нг до приблизительно 975 нг или от приблизительно 800 нг до приблизительно 1000 нг.
[072] В аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, 1 мкг, приблизительно 2 мкг, приблизительно 3 мкг, приблизительно 4 мкг, приблизительно 5 мкг, приблизительно 6 мкг, приблизительно 7 мкг, приблизительно 8 мкг, приблизительно 9 мкг, приблизительно 10 мкг, приблизительно 15 мкг, приблизительно 20 мкг, приблизительно 25 мкг, приблизительно 30 мкг, приблизительно 35 мкг, приблизительно 40 мкг, приблизительно 45 мкг, приблизительно 50 мкг, приблизительно 55 мкг, приблизительно 60 мкг, приблизительно 65 мкг, приблизительно 70 мкг, приблизительно 75 мкг, приблизительно 80 мкг, приблизительно 85 мкг, приблизительно 90 мкг, приблизительно 95 мкг, приблизительно 100 мкг, приблизительно 110 мкг, приблизительно 120 мкг, приблизительно 130 мкг, приблизительно 140 мкг, приблизительно 150 мкг, приблизительно 160 мкг, приблизительно 170 мкг, приблизительно 180 мкг, приблизительно 190 мкг, приблизительно 200 мкг, приблизительно 210 мкг, приблизительно 220 мкг, приблизительно 230 мкг, приблизительно 240 мкг, приблизительно 250 мкг, приблизительно 260 мкг, приблизительно 270 мкг, приблизительно 280 мкг, приблизительно 290 мкг, приблизительно 300 мкг, приблизительно 310 мкг, приблизительно 320 мкг, приблизительно 330 мкг, приблизительно 340 мкг, приблизительно 350 мкг, приблизительно 360 мкг, приблизительно 370 мкг, приблизительно 380 мкг, приблизительно 390 мкг, приблизительно 400 мкг, приблизительно 410 мкг, приблизительно 420 мкг, приблизительно 430 мкг, приблизительно 440 мкг, приблизительно 450 мкг, приблизительно 460 мкг, приблизительно 470 мкг, приблизительно 480 мкг, приблизительно 490 мкг, приблизительно 500 мкг, приблизительно 510 мкг, приблизительно 520 мкг, приблизительно 530 мкг, приблизительно 540 мкг, приблизительно 550 мкг, приблизительно 560 мкг, приблизительно 570 мкг, приблизительно 580 мкг, приблизительно 590 мкг, приблизительно 600 мкг, приблизительно 610 мкг, приблизительно 620 мкг, приблизительно 630 мкг, приблизительно 640 мкг, приблизительно 650 мкг, приблизительно 660 мкг, приблизительно 670 мкг, приблизительно 680 мкг, приблизительно 690 мкг, приблизительно 700 мкг, приблизительно 710 мкг, приблизительно 720 мкг, приблизительно 730 мкг, приблизительно 740 мкг, приблизительно 750 мкг, приблизительно 760 мкг, приблизительно 770 мкг, приблизительно 780 мкг, приблизительно 790 мкг, приблизительно 800 мкг, приблизительно 810 мкг, приблизительно 820 мкг, приблизительно 830 мкг, приблизительно 840 мкг, приблизительно 850 мкг, приблизительно 860 мкг, приблизительно 870 мкг, приблизительно 880 мкг, приблизительно 890 мкг, приблизительно 900 мкг, приблизительно 910 мкг, приблизительно 920 мкг, приблизительно 930 мкг, приблизительно 940 мкг, приблизительно 950 мкг, приблизительно 960 мкг, приблизительно 970 мкг, приблизительно 980 мкг, приблизительно 990 мкг или приблизительно 1000 мкг.
[073] В других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, по меньшей мере 1 мкг, по меньшей мере 2 мкг, по меньшей мере 3 мкг, по меньшей мере 4 мкг, по меньшей мере 5 мкг, по меньшей мере 6 мкг, по меньшей мере 7 мкг, по меньшей мере 8 мкг, по меньшей мере 9 мкг, по меньшей мере 10 мкг, по меньшей мере 15 мкг, по меньшей мере 20 мкг, по меньшей мере 25 мкг, по меньшей мере 30 мкг, по меньшей мере 35 мкг, по меньшей мере 40 мкг, по меньшей мере 45 мкг, по меньшей мере 50 мкг, по меньшей мере 55 мкг, по меньшей мере 60 мкг, по меньшей мере 65 мкг, по меньшей мере 70 мкг, по меньшей мере 75 мкг, по меньшей мере 80 мкг, по меньшей мере 85 мкг, по меньшей мере 90 мкг, по меньшей мере 95 мкг, по меньшей мере 100 мкг, по меньшей мере 110 мкг, по меньшей мере 120 мкг, по меньшей мере 130 мкг, по меньшей мере 140 мкг, по меньшей мере 150 мкг, по меньшей мере 160 мкг, по меньшей мере 170 мкг, по меньшей мере 180 мкг, по меньшей мере 190 мкг, по меньшей мере 200 мкг, по меньшей мере 210 мкг, по меньшей мере 220 мкг, по меньшей мере 230 мкг, по меньшей мере 240 мкг, по меньшей мере 250 мкг, по меньшей мере 260 мкг, по меньшей мере 270 мкг, по меньшей мере 280 мкг, по меньшей мере 290 мкг, по меньшей мере 300 мкг, по меньшей мере 310 мкг, по меньшей мере 320 мкг, по меньшей мере 330 мкг, по меньшей мере 340 мкг, по меньшей мере 350 мкг, по меньшей мере 360 мкг, по меньшей мере 370 мкг, по меньшей мере 380 мкг, по меньшей мере 390 мкг, по меньшей мере 400 мкг, по меньшей мере 410 мкг, по меньшей мере 420 мкг, по меньшей мере 430 мкг, по меньшей мере 440 мкг, по меньшей мере 450 мкг, по меньшей мере 460 мкг, по меньшей мере 470 мкг, по меньшей мере 480 мкг, по меньшей мере 490 мкг, по меньшей мере 500 мкг, по меньшей мере 510 мкг, по меньшей мере 520 мкг, по меньшей мере 530 мкг, по меньшей мере 540 мкг, по меньшей мере 550 мкг, по меньшей мере 560 мкг, по меньшей мере 570 мкг, по меньшей мере 580 мкг, по меньшей мере 590 мкг, по меньшей мере 600 мкг, по меньшей мере 610 мкг, по меньшей мере 620 мкг, по меньшей мере 630 мкг, по меньшей мере 640 мкг, по меньшей мере 650 мкг, по меньшей мере 660 мкг, по меньшей мере 670 мкг, по меньшей мере 680 мкг, по меньшей мере 690 мкг, по меньшей мере 700 мкг, по меньшей мере 710 мкг, по меньшей мере 720 мкг, по меньшей мере 730 мкг, по меньшей мере 740 мкг, по меньшей мере 750 мкг, по меньшей мере 760 мкг, по меньшей мере 770 мкг, по меньшей мере 780 мкг, по меньшей мере 790 мкг, по меньшей мере 800 мкг, по меньшей мере 810 мкг, по меньшей мере 820 мкг, по меньшей мере 830 мкг, по меньшей мере 840 мкг, по меньшей мере 850 мкг, по меньшей мере 860 мкг, по меньшей мере 870 мкг, по меньшей мере 880 мкг, по меньшей мере 890 мкг, по меньшей мере 900 мкг, по меньшей мере 910 мкг, по меньшей мере 920 мкг, по меньшей мере 930 мкг, по меньшей мере 940 мкг, по меньшей мере 950 мкг, по меньшей мере 960 мкг, по меньшей мере 970 мкг, по меньшей мере 980 мкг, по меньшей мере 990 мкг или по меньшей мере 1000 мкг.
[074] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, не более 1 мкг, не более 2 мкг, не более 3 мкг, не более 4 мкг, не более 5 мкг, не более 6 мкг, не более 7 мкг, не более 8 мкг, не более 9 мкг, не более 10 мкг, не более 15 мкг, не более 20 мкг, не более 25 мкг, не более 30 мкг, не более 35 мкг, не более 40 мкг, не более 45 мкг, не более 50 мкг, не более 55 мкг, не более 60 мкг, не более 65 мкг, не более 70 мкг, не более 75 мкг, не более 80 мкг, не более 85 мкг, не более 90 мкг, не более 95 мкг, не более 100 мкг, не более 110 мкг, не более 120 мкг, не более 130 мкг, не более 140 мкг, не более 150 мкг, не более 160 мкг, не более 170 мкг, не более 180 мкг, не более 190 мкг, не более 200 мкг, не более 210 мкг, не более 220 мкг, не более 230 мкг, не более 240 мкг, не более 250 мкг, не более 260 мкг, не более 270 мкг, не более 280 мкг, не более 290 мкг, не более 300 мкг, не более 310 мкг, не более 320 мкг, не более 330 мкг, не более 340 мкг, не более 350 мкг, не более 360 мкг, не более 370 мкг, не более 380 мкг, не более 390 мкг, не более 400 мкг, не более 410 мкг, не более 420 мкг, не более 430 мкг, не более 440 мкг, не более 450 мкг, не более 460 мкг, не более 470 мкг, не более 480 мкг, не более 490 мкг, не более 500 мкг, не более 510 мкг, не более 520 мкг, не более 530 мкг, не более 540 мкг, не более 550 мкг, не более 560 мкг, не более 570 мкг, не более 580 мкг, не более 590 мкг, не более 600 мкг, не более 610 мкг, не более 620 мкг, не более 630 мкг, не более 640 мкг, не более 650 мкг, не более 660 мкг, не более 670 мкг, не более 680 мкг, не более 690 мкг, не более 700 мкг, не более 710 мкг, не более 720 мкг, не более 730 мкг, не более 740 мкг, не более 750 мкг, не более 760 мкг, не более 770 мкг, не более 780 мкг, не более 790 мкг, не более 800 мкг, не более 810 мкг, не более 820 мкг, не более 830 мкг, не более 840 мкг, не более 850 мкг, не более 860 мкг, не более 870 мкг, не более 880 мкг, не более 890 мкг, не более 900 мкг, не более 910 мкг, не более 920 мкг, не более 930 мкг, не более 940 мкг, не более 950 мкг, не более 960 мкг, не более 970 мкг, не более 980 мкг, не более 990 мкг или не более 1000 мкг.
[075] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 1 мкг до приблизительно 10 мкг, от приблизительно 1 мкг до приблизительно 20 мкг, от приблизительно 1 мкг до приблизительно 30 мкг, от приблизительно 1 мкг до приблизительно 40 мкг, от приблизительно 1 мкг до приблизительно 50 мкг, от приблизительно 1 мкг до приблизительно 60 мкг, от приблизительно 1 мкг до приблизительно 70 мкг, от приблизительно 1 мкг до приблизительно 80 мкг, от приблизительно 1 мкг до приблизительно 90 мкг, от приблизительно 1 мкг до приблизительно 100 мкг, от приблизительно 1 мкг до приблизительно 110 мкг, от приблизительно 1 мкг до приблизительно 120 мкг, от приблизительно 1 мкг до приблизительно 130 мкг, от приблизительно 1 мкг до приблизительно 140 мкг, от приблизительно 1 мкг до приблизительно 150 мкг, от приблизительно 5 мкг до приблизительно 10 мкг, от приблизительно 5 мкг до приблизительно 20 мкг, от приблизительно 5 мкг до приблизительно 30 мкг, от приблизительно 5 мкг до приблизительно 40 мкг, от приблизительно 5 мкг до приблизительно 50 мкг, от приблизительно 5 мкг до приблизительно 60 мкг, от приблизительно 5 мкг до приблизительно 70 мкг, от приблизительно 5 мкг до приблизительно 80 мкг, от приблизительно 5 мкг до приблизительно 90 мкг, от приблизительно 5 мкг до приблизительно 100 мкг, от приблизительно 5 мкг до приблизительно 110 мкг, от приблизительно 5 мкг до приблизительно 120 мкг, от приблизительно 5 мкг до приблизительно 130 мкг, от приблизительно 5 мкг до приблизительно 140 мкг, от приблизительно 5 мкг до приблизительно 150 мкг, от приблизительно 10 мкг до приблизительно 20 мкг, от приблизительно 10 мкг до приблизительно 30 мкг, от приблизительно 10 мкг до приблизительно 40 мкг, от приблизительно 10 мкг до приблизительно 50 мкг, от приблизительно 10 мкг до приблизительно 60 мкг, от приблизительно 10 мкг до приблизительно 70 мкг, от приблизительно 10 мкг до приблизительно 80 мкг, от приблизительно 10 мкг до приблизительно 90 мкг, от приблизительно 10 мкг до приблизительно 100 мкг, от приблизительно 10 мкг до приблизительно 110 мкг, от приблизительно 10 мкг до приблизительно 120 мкг, от приблизительно 10 мкг до приблизительно 130 мкг, от приблизительно 10 мкг до приблизительно 140 мкг, от приблизительно 10 мкг до приблизительно 150 мкг, от приблизительно 10 мкг до приблизительно 175 мкг, от приблизительно 10 мкг до приблизительно 200 мкг, от приблизительно 10 мкг до приблизительно 225 мкг, от приблизительно 10 мкг до приблизительно 250 мкг, от приблизительно 25 мкг до приблизительно 50 мкг, от приблизительно 25 мкг до приблизительно 75 мкг, от приблизительно 25 мкг до приблизительно 100 мкг, от приблизительно 25 мкг до приблизительно 125 мкг, от приблизительно 25 мкг до приблизительно 150 мкг, от приблизительно 25 мкг до приблизительно 175 мкг, от приблизительно 25 мкг до приблизительно 200 мкг, от приблизительно 25 мкг до приблизительно 225 мкг, от приблизительно 25 мкг до приблизительно 250 мкг, от приблизительно 50 мкг до приблизительно 75 мкг, от приблизительно 50 мкг до приблизительно 100 мкг, от приблизительно 50 мкг до приблизительно 125 мкг, от приблизительно 50 мкг до приблизительно 150 мкг, от приблизительно 50 мкг до приблизительно 175 мкг, от приблизительно 50 мкг до приблизительно 200 мкг, от приблизительно 50 мкг до приблизительно 225 мкг, от приблизительно 50 мкг до приблизительно 250 мкг, от приблизительно 75 мкг до приблизительно 100 мкг, от приблизительно 75 мкг до приблизительно 125 мкг, от приблизительно 75 мкг до приблизительно 150 мкг, от приблизительно 75 мкг до приблизительно 175 мкг, от приблизительно 75 мкг до приблизительно 200 мкг, от приблизительно 75 мкг до приблизительно 225 мкг или от приблизительно 75 мкг до приблизительно 250 мкг.
[076] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 100 мкг до приблизительно 125 мкг, от приблизительно 100 мкг до приблизительно 150 мкг, от приблизительно 100 мкг до приблизительно 175 мкг, от приблизительно 100 мкг до приблизительно 200 мкг, от приблизительно 100 мкг до приблизительно 225 мкг, от приблизительно 100 мкг до приблизительно 250 мкг, от приблизительно 100 мкг до приблизительно 275 мкг, от приблизительно 100 мкг до приблизительно 300 мкг, от приблизительно 100 мкг до приблизительно 325 мкг, от приблизительно 100 мкг до приблизительно 350 мкг, от приблизительно 100 мкг до приблизительно 375 мкг, от приблизительно 100 мкг до приблизительно 400 мкг, от приблизительно 100 мкг до приблизительно 425 мкг, от приблизительно 100 мкг до приблизительно 450 мкг, от приблизительно 100 мкг до приблизительно 475 мкг, от приблизительно 100 мкг до приблизительно 500 мкг, от приблизительно 100 мкг до приблизительно 525 мкг, от приблизительно 100 мкг до приблизительно 550 мкг, от приблизительно 100 мкг до приблизительно 575 мкг, от приблизительно 100 мкг до приблизительно 600 мкг, от приблизительно 125 мкг до приблизительно 150 мкг, от приблизительно 125 мкг до приблизительно 175 мкг, от приблизительно 125 мкг до приблизительно 200 мкг, от приблизительно 125 мкг до приблизительно 225 мкг, от приблизительно 125 мкг до приблизительно 250 мкг, от приблизительно 125 мкг до приблизительно 275 мкг, от приблизительно 125 мкг до приблизительно 300 мкг, от приблизительно 125 мкг до приблизительно 325 мкг, от приблизительно 125 мкг до приблизительно 350 мкг, от приблизительно 125 мкг до приблизительно 375 мкг, от приблизительно 125 мкг до приблизительно 400 мкг, от приблизительно 125 мкг до приблизительно 425 мкг, от приблизительно 125 мкг до приблизительно 450 мкг, от приблизительно 125 мкг до приблизительно 475 мкг, от приблизительно 125 мкг до приблизительно 500 мкг, от приблизительно 125 мкг до приблизительно 525 мкг, от приблизительно 125 мкг до приблизительно 550 мкг, от приблизительно 125 мкг до приблизительно 575 мкг, от приблизительно 125 мкг до приблизительно 600 мкг, от приблизительно 150 мкг до приблизительно 175 мкг, от приблизительно 150 мкг до приблизительно 200 мкг, от приблизительно 150 мкг до приблизительно 225 мкг, от приблизительно 150 мкг до приблизительно 250 мкг, от приблизительно 150 мкг до приблизительно 275 мкг, от приблизительно 150 мкг до приблизительно 300 мкг, от приблизительно 150 мкг до приблизительно 325 мкг, от приблизительно 150 мкг до приблизительно 350 мкг, от приблизительно 150 мкг до приблизительно 375 мкг, от приблизительно 150 мкг до приблизительно 400 мкг, от приблизительно 150 мкг до приблизительно 425 мкг, от приблизительно 150 мкг до приблизительно 450 мкг, от приблизительно 150 мкг до приблизительно 475 мкг, от приблизительно 150 мкг до приблизительно 500 мкг, от приблизительно 150 мкг до приблизительно 525 мкг, от приблизительно 150 мкг до приблизительно 550 мкг, от приблизительно 150 мкг до приблизительно 575 мкг, от приблизительно 150 мкг до приблизительно 600 мкг, от приблизительно 200 мкг до приблизительно 225 мкг, от приблизительно 200 мкг до приблизительно 250 мкг, от приблизительно 200 мкг до приблизительно 275 мкг, от приблизительно 200 мкг до приблизительно 300 мкг, от приблизительно 200 мкг до приблизительно 325 мкг, от приблизительно 200 мкг до приблизительно 350 мкг, от приблизительно 200 мкг до приблизительно 375 мкг, от приблизительно 200 мкг до приблизительно 400 мкг, от приблизительно 200 мкг до приблизительно 425 мкг, от приблизительно 200 мкг до приблизительно 450 мкг, от приблизительно 200 мкг до приблизительно 475 мкг, от приблизительно 200 мкг до приблизительно 500 мкг, от приблизительно 200 мкг до приблизительно 525 мкг, от приблизительно 200 мкг до приблизительно 550 мкг, от приблизительно 200 мкг до приблизительно 575 мкг, от приблизительно 200 мкг до приблизительно 600 мкг, от приблизительно 200 мкг до приблизительно 625 мкг, от приблизительно 200 мкг до приблизительно 650 мкг, от приблизительно 200 мкг до приблизительно 675 мкг, от приблизительно 200 мкг до приблизительно 700 мкг, от приблизительно 200 мкг до приблизительно 725 мкг, от приблизительно 200 мкг до приблизительно 750 мкг, от приблизительно 200 мкг до приблизительно 775 мкг, от приблизительно 200 мкг до приблизительно 800 мкг, от приблизительно 200 мкг до приблизительно 825 мкг, от приблизительно 200 мкг до приблизительно 850 мкг, от приблизительно 200 мкг до приблизительно 875 мкг, от приблизительно 200 мкг до приблизительно 900 мкг, от приблизительно 200 мкг до приблизительно 925 мкг, от приблизительно 200 мкг до приблизительно 950 мкг, от приблизительно 200 мкг до приблизительно 975 мкг, от приблизительно 200 мкг до приблизительно 1000 мкг.
[077] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 250 мкг до приблизительно 275 мкг, от приблизительно 250 мкг до приблизительно 300 мкг, от приблизительно 250 мкг до приблизительно 325 мкг, от приблизительно 250 мкг до приблизительно 350 мкг, от приблизительно 250 мкг до приблизительно 375 мкг, от приблизительно 250 мкг до приблизительно 400 мкг, от приблизительно 250 мкг до приблизительно 425 мкг, от приблизительно 250 мкг до приблизительно 450 мкг, от приблизительно 250 мкг до приблизительно 475 мкг, от приблизительно 250 мкг до приблизительно 500 мкг, от приблизительно 250 мкг до приблизительно 525 мкг, от приблизительно 250 мкг до приблизительно 550 мкг, от приблизительно 250 мкг до приблизительно 575 мкг, от приблизительно 250 мкг до приблизительно 600 мкг, от приблизительно 250 мкг до приблизительно 625 мкг, от приблизительно 250 мкг до приблизительно 650 мкг, от приблизительно 250 мкг до приблизительно 675 мкг, от приблизительно 250 мкг до приблизительно 700 мкг, от приблизительно 250 мкг до приблизительно 725 мкг, от приблизительно 250 мкг до приблизительно 750 мкг, от приблизительно 250 мкг до приблизительно 775 мкг, от приблизительно 250 мкг до приблизительно 800 мкг, от приблизительно 250 мкг до приблизительно 825 мкг, от приблизительно 250 мкг до приблизительно 850 мкг, от приблизительно 250 мкг до приблизительно 875 мкг, от приблизительно 250 мкг до приблизительно 900 мкг, от приблизительно 250 мкг до приблизительно 925 мкг, от приблизительно 250 мкг до приблизительно 950 мкг, от приблизительно 250 мкг до приблизительно 975 мкг, от приблизительно 250 мкг до приблизительно 1000 мкг, от приблизительно 300 мкг до приблизительно 325 мкг, от приблизительно 300 мкг до приблизительно 350 мкг, от приблизительно 300 мкг до приблизительно 375 мкг, от приблизительно 300 мкг до приблизительно 400 мкг, от приблизительно 300 мкг до приблизительно 425 мкг, от приблизительно 300 мкг до приблизительно 450 мкг, от приблизительно 300 мкг до приблизительно 475 мкг, от приблизительно 300 мкг до приблизительно 500 мкг, от приблизительно 300 мкг до приблизительно 525 мкг, от приблизительно 300 мкг до приблизительно 550 мкг, от приблизительно 300 мкг до приблизительно 575 мкг, от приблизительно 300 мкг до приблизительно 600 мкг, от приблизительно 300 мкг до приблизительно 625 мкг, от приблизительно 300 мкг до приблизительно 650 мкг, от приблизительно 300 мкг до приблизительно 675 мкг, от приблизительно 300 мкг до приблизительно 700 мкг, от приблизительно 300 мкг до приблизительно 725 мкг, от приблизительно 300 мкг до приблизительно 750 мкг, от приблизительно 300 мкг до приблизительно 775 мкг, от приблизительно 300 мкг до приблизительно 800 мкг, от приблизительно 300 мкг до приблизительно 825 мкг, от приблизительно 300 мкг до приблизительно 850 мкг, от приблизительно 300 мкг до приблизительно 875 мкг, от приблизительно 300 мкг до приблизительно 900 мкг, от приблизительно 300 мкг до приблизительно 925 мкг, от приблизительно 300 мкг до приблизительно 950 мкг, от приблизительно 300 мкг до приблизительно 975 мкг, от приблизительно 300 мкг до приблизительно 1000 мкг, от приблизительно 400 мкг до приблизительно 425 мкг, от приблизительно 400 мкг до приблизительно 450 мкг, от приблизительно 400 мкг до приблизительно 475 мкг, от приблизительно 400 мкг до приблизительно 500 мкг, от приблизительно 400 мкг до приблизительно 525 мкг, от приблизительно 400 мкг до приблизительно 550 мкг, от приблизительно 400 мкг до приблизительно 575 мкг, от приблизительно 400 мкг до приблизительно 600 мкг, от приблизительно 400 мкг до приблизительно 625 мкг, от приблизительно 400 мкг до приблизительно 650 мкг, от приблизительно 400 мкг до приблизительно 675 мкг, от приблизительно 400 мкг до приблизительно 700 мкг, от приблизительно 400 мкг до приблизительно 725 мкг, от приблизительно 400 мкг до приблизительно 750 мкг, от приблизительно 400 мкг до приблизительно 775 мкг, от приблизительно 400 мкг до приблизительно 800 мкг, от приблизительно 400 мкг до приблизительно 825 мкг, от приблизительно 400 мкг до приблизительно 850 мкг, от приблизительно 400 мкг до приблизительно 875 мкг, от приблизительно 400 мкг до приблизительно 900 мкг, от приблизительно 400 мкг до приблизительно 925 мкг, от приблизительно 400 мкг до приблизительно 950 мкг, от приблизительно 400 мкг до приблизительно 975 мкг, от приблизительно 400 мкг до приблизительно 1000 мкг.
[078] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 500 мкг до приблизительно 525 мкг, от приблизительно 500 мкг до приблизительно 550 мкг, от приблизительно 500 мкг до приблизительно 575 мкг, от приблизительно 500 мкг до приблизительно 600 мкг, от приблизительно 500 мкг до приблизительно 625 мкг, от приблизительно 500 мкг до приблизительно 650 мкг, от приблизительно 500 мкг до приблизительно 675 мкг, от приблизительно 500 мкг до приблизительно 700 мкг, от приблизительно 500 мкг до приблизительно 725 мкг, от приблизительно 500 мкг до приблизительно 750 мкг, от приблизительно 500 мкг до приблизительно 775 мкг, от приблизительно 500 мкг до приблизительно 800 мкг, от приблизительно 500 мкг до приблизительно 825 мкг, от приблизительно 500 мкг до приблизительно 850 мкг, от приблизительно 500 мкг до приблизительно 875 мкг, от приблизительно 500 мкг до приблизительно 900 мкг, от приблизительно 500 мкг до приблизительно 925 мкг, от приблизительно 500 мкг до приблизительно 950 мкг, от приблизительно 500 мкг до приблизительно 975 мкг, от приблизительно 500 мкг до приблизительно 1000 мкг, от приблизительно 600 мкг до приблизительно 625 мкг, от приблизительно 600 мкг до приблизительно 650 мкг, от приблизительно 600 мкг до приблизительно 675 мкг, от приблизительно 600 мкг до приблизительно 700 мкг, от приблизительно 600 мкг до приблизительно 725 мкг, от приблизительно 600 мкг до приблизительно 750 мкг, от приблизительно 600 мкг до приблизительно 775 мкг, от приблизительно 600 мкг до приблизительно 800 мкг, от приблизительно 600 мкг до приблизительно 825 мкг, от приблизительно 600 мкг до приблизительно 850 мкг, от приблизительно 600 мкг до приблизительно 875 мкг, от приблизительно 600 мкг до приблизительно 900 мкг, от приблизительно 600 мкг до приблизительно 925 мкг, от приблизительно 600 мкг до приблизительно 950 мкг, от приблизительно 600 мкг до приблизительно 975 мкг, от приблизительно 600 мкг до приблизительно 1000 мкг, от приблизительно 700 мкг до приблизительно 725 мкг, от приблизительно 700 мкг до приблизительно 750 мкг, от приблизительно 700 мкг до приблизительно 775 мкг, от приблизительно 700 мкг до приблизительно 800 мкг, от приблизительно 700 мкг до приблизительно 825 мкг, от приблизительно 700 мкг до приблизительно 850 мкг, от приблизительно 700 мкг до приблизительно 875 мкг, от приблизительно 700 мкг до приблизительно 900 мкг, от приблизительно 700 мкг до приблизительно 925 мкг, от приблизительно 700 мкг до приблизительно 950 мкг, от приблизительно 700 мкг до приблизительно 975 мкг, от приблизительно 700 мкг до приблизительно 1000 мкг, от приблизительно 800 мкг до приблизительно 825 мкг, от приблизительно 800 мкг до приблизительно 850 мкг, от приблизительно 800 мкг до приблизительно 875 мкг, от приблизительно 800 мкг до приблизительно 900 мкг, от приблизительно 800 мкг до приблизительно 925 мкг, от приблизительно 800 мкг до приблизительно 950 мкг, от приблизительно 800 мкг до приблизительно 975 мкг, от приблизительно 800 мкг до приблизительно 1000 мкг.
[079] В аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, приблизительно 1 мг, приблизительно 2 мг, приблизительно 3 мг, приблизительно 4 мг, приблизительно 5 мг, приблизительно 6 мг, приблизительно 7 мг, приблизительно 8 мг, приблизительно 9 мг, приблизительно 10 мг, приблизительно 15 мг, приблизительно 20 мг, приблизительно 25 мг, приблизительно 30 мг, приблизительно 35 мг, приблизительно 40 мг, приблизительно 45 мг, приблизительно 50 мг, приблизительно 55 мг, приблизительно 60 мг, приблизительно 65 мг, приблизительно 70 мг, приблизительно 75 мг, приблизительно 80 мг, приблизительно 85 мг, приблизительно 90 мг, приблизительно 95 мг, приблизительно 100 мг, приблизительно 110 мг, приблизительно 120 мг, приблизительно 130 мг, приблизительно 140 мг, приблизительно 150 мг, приблизительно 160 мг, приблизительно 170 мг, приблизительно 180 мг, приблизительно 190 мг, приблизительно 200 мг, приблизительно 210 мг, приблизительно 220 мг, приблизительно 230 мг, приблизительно 240 мг, приблизительно 250 мг, приблизительно 260 мг, приблизительно 270 мг, приблизительно 280 мг, приблизительно 290 мг, приблизительно 300 мг, приблизительно 310 мг, приблизительно 320 мг, приблизительно 330 мг, приблизительно 340 мг, приблизительно 350 мг, приблизительно 360 мг, приблизительно 370 мг, приблизительно 380 мг, приблизительно 390 мг, приблизительно 400 мг, приблизительно 410 мг, приблизительно 420 мг, приблизительно 430 мг, приблизительно 440 мг, приблизительно 450 мг, приблизительно 460 мг, приблизительно 470 мг, приблизительно 480 мг, приблизительно 490 мг, приблизительно 500 мг, приблизительно 510 мг, приблизительно 520 мг, приблизительно 530 мг, приблизительно 540 мг, приблизительно 550 мг, приблизительно 560 мг, приблизительно 570 мг, приблизительно 580 мг, приблизительно 590 мг, приблизительно 600 мг, приблизительно 610 мг, приблизительно 620 мг, приблизительно 630 мг, приблизительно 640 мг, приблизительно 650 мг, приблизительно 660 мг, приблизительно 670 мг, приблизительно 680 мг, приблизительно 690 мг, приблизительно 700 мг, приблизительно 710 мг, приблизительно 720 мг, приблизительно 730 мг, приблизительно 740 мг, приблизительно 750 мг, приблизительно 760 мг, приблизительно 770 мг, приблизительно 780 мг, приблизительно 790 мг, приблизительно 800 мг, приблизительно 810 мг, приблизительно 820 мг, приблизительно 830 мг, приблизительно 840 мг, приблизительно 850 мг, приблизительно 860 мг, приблизительно 870 мг, приблизительно 880 мг, приблизительно 890 мг, приблизительно 900 мг, приблизительно 910 мг, приблизительно 920 мг, приблизительно 930 мг, приблизительно 940 мг, приблизительно 950 мг, приблизительно 960 мг, приблизительно 970 мг, приблизительно 980 мг, приблизительно 990 мг, приблизительно 1000 мг, приблизительно 1250 мг, приблизительно 1500 мг, приблизительно 1750 мг, приблизительно 2000 мг, приблизительно 2250 мг, приблизительно 2500 мг, приблизительно 2750 мг или приблизительно 3000 мг.
[080] В других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, по меньшей мере 1 мг, по меньшей мере 2 мг, по меньшей мере 3 мг, по меньшей мере 4 мг, по меньшей мере 5 мг, по меньшей мере 6 мг, по меньшей мере 7 мг, по меньшей мере 8 мг, по меньшей мере 9 мг, по меньшей мере 10 мг, по меньшей мере 15 мг, по меньшей мере 20 мг, по меньшей мере 25 мг, по меньшей мере 30 мг, по меньшей мере 35 мг, по меньшей мере 40 мг, по меньшей мере 45 мг, по меньшей мере 50 мг, по меньшей мере 55 мг, по меньшей мере 60 мг, по меньшей мере 65 мг, по меньшей мере 70 мг, по меньшей мере 75 мг, по меньшей мере 80 мг, по меньшей мере 85 мг, по меньшей мере 90 мг, по меньшей мере 95 мг, по меньшей мере 100 мг, по меньшей мере 110 мг, по меньшей мере 120 мг, по меньшей мере 130 мг, по меньшей мере 140 мг, по меньшей мере 150 мг, по меньшей мере 160 мг, по меньшей мере 170 мг, по меньшей мере 180 мг, по меньшей мере 190 мг, по меньшей мере 200 мг, по меньшей мере 210 мг, по меньшей мере 220 мг, по меньшей мере 230 мг, по меньшей мере 240 мг, по меньшей мере 250 мг, по меньшей мере 260 мг, по меньшей мере 270 мг, по меньшей мере 280 мг, по меньшей мере 290 мг, по меньшей мере 300 мг, по меньшей мере 310 мг, по меньшей мере 320 мг, по меньшей мере 330 мг, по меньшей мере 340 мг, по меньшей мере 350 мг, по меньшей мере 360 мг, по меньшей мере 370 мг, по меньшей мере 380 мг, по меньшей мере 390 мг, по меньшей мере 400 мг, по меньшей мере 410 мг, по меньшей мере 420 мг, по меньшей мере 430 мг, по меньшей мере 440 мг, по меньшей мере 450 мг, по меньшей мере 460 мг, по меньшей мере 470 мг, по меньшей мере 480 мг, по меньшей мере 490 мг, по меньшей мере 500 мг, по меньшей мере 510 мг, по меньшей мере 520 мг, по меньшей мере 530 мг, по меньшей мере 540 мг, по меньшей мере 550 мг, по меньшей мере 560 мг, по меньшей мере 570 мг, по меньшей мере 580 мг, по меньшей мере 590 мг, по меньшей мере 600 мг, по меньшей мере 610 мг, по меньшей мере 620 мг, по меньшей мере 630 мг, по меньшей мере 640 мг, по меньшей мере 650 мг, по меньшей мере 660 мг, по меньшей мере 670 мг, по меньшей мере 680 мг, по меньшей мере 690 мг, по меньшей мере 700 мг, по меньшей мере 710 мг, по меньшей мере 720 мг, по меньшей мере 730 мг, по меньшей мере 740 мг, по меньшей мере 750 мг, по меньшей мере 760 мг, по меньшей мере 770 мг, по меньшей мере 780 мг, по меньшей мере 790 мг, по меньшей мере 800 мг, по меньшей мере 810 мг, по меньшей мере 820 мг, по меньшей мере 830 мг, по меньшей мере 840 мг, по меньшей мере 850 мг, по меньшей мере 860 мг, по меньшей мере 870 мг, по меньшей мере 880 мг, по меньшей мере 890 мг, по меньшей мере 900 мг, по меньшей мере 910 мг, по меньшей мере 920 мг, по меньшей мере 930 мг, по меньшей мере 940 мг, по меньшей мере 950 мг, по меньшей мере 960 мг, по меньшей мере 970 мг, по меньшей мере 980 мг, по меньшей мере 990 мг, по меньшей мере 1000 мг, по меньшей мере 1250 мг, по меньшей мере 1500 мг, по меньшей мере 1750 мг, по меньшей мере 2000 мг, по меньшей мере 2250 мг, по меньшей мере 2500 мг, по меньшей мере 2750 мг или по меньшей мере 3000 мг.
[081] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может составлять, например, не более 1 мг, не более 2 мг, не более 3 мг, не более 4 мг, не более 5 мг, не более 6 мг, не более 7 мг, не более 8 мг, не более 9 мг, не более 10 мг, не более 15 мг, не более 20 мг, не более 25 мг, не более 30 мг, не более 35 мг, не более 40 мг, не более 45 мг, не более 50 мг, не более 55 мг, не более 60 мг, не более 65 мг, не более 70 мг, не более 75 мг, не более 80 мг, не более 85 мг, не более 90 мг, не более 95 мг, не более 100 мг, не более 110 мг, не более 120 мг, не более 130 мг, не более 140 мг, не более 150 мг, не более 160 мг, не более 170 мг, не более 180 мг, не более 190 мг, не более 200 мг, не более 210 мг, не более 220 мг, не более 230 мг, не более 240 мг, не более 250 мг, не более 260 мг, не более 270 мг, не более 280 мг, не более 290 мг, не более 300 мг, не более 310 мг, не более 320 мг, не более 330 мг, не более 340 мг, не более 350 мг, не более 360 мг, не более 370 мг, не более 380 мг, не более 390 мг, не более 400 мг, не более 410 мг, не более 420 мг, не более 430 мг, не более 440 мг, не более 450 мг, не более 460 мг, не более 470 мг, не более 480 мг, не более 490 мг, не более 500 мг, не более 510 мг, не более 520 мг, не более 530 мг, не более 540 мг, не более 550 мг, не более 560 мг, не более 570 мг, не более 580 мг, не более 590 мг, не более 600 мг, не более 610 мг, не более 620 мг, не более 630 мг, не более 640 мг, не более 650 мг, не более 660 мг, не более 670 мг, не более 680 мг, не более 690 мг, не более 700 мг, не более 710 мг, не более 720 мг, не более 730 мг, не более 740 мг, не более 750 мг, не более 760 мг, не более 770 мг, не более 780 мг, не более 790 мг, не более 800 мг, не более 810 мг, не более 820 мг, не более 830 мг, не более 840 мг, не более 850 мг, не более 860 мг, не более 870 мг, не более 880 мг, не более 890 мг, не более 900 мг, не более 910 мг, не более 920 мг, не более 930 мг, не более 940 мг, не более 950 мг, не более 960 мг, не более 970 мг, не более 980 мг, не более 990 мг, не более 1000 мг, не более 1250 мг, не более 1500 мг, не более 1750 мг, не более 2000 мг, не более 2250 мг, не более 2500 мг, не более 2750 мг или не более 3000 мг.
[082] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 1 мг до приблизительно 10 мг, от приблизительно 1 мг до приблизительно 20 мг, от приблизительно 1 мг до приблизительно 30 мг, от приблизительно 1 мг до приблизительно 40 мг, от приблизительно 1 мг до приблизительно 50 мг, от приблизительно 1 мг до приблизительно 60 мг, от приблизительно 1 мг до приблизительно 70 мг, от приблизительно 1 мг до приблизительно 80 мг, от приблизительно 1 мг до приблизительно 90 мг, от приблизительно 1 мг до приблизительно 100 мг, от приблизительно 1 мг до приблизительно 110 мг, от приблизительно 1 мг до приблизительно 120 мг, от приблизительно 1 мг до приблизительно 130 мг, от приблизительно 1 мг до приблизительно 140 мг, от приблизительно 1 мг до приблизительно 150 мг, от приблизительно 5 мг до приблизительно 10 мг, от приблизительно 5 мг до приблизительно 20 мг, от приблизительно 5 мг до приблизительно 30 мг, от приблизительно 5 мг до приблизительно 40 мг, от приблизительно 5 мг до приблизительно 50 мг, от приблизительно 5 мг до приблизительно 60 мг, от приблизительно 5 мг до приблизительно 70 мг, от приблизительно 5 мг до приблизительно 80 мг, от приблизительно 5 мг до приблизительно 90 мг, от приблизительно 5 мг до приблизительно 100 мг, от приблизительно 5 мг до приблизительно 110 мг, от приблизительно 5 мг до приблизительно 120 мг, от приблизительно 5 мг до приблизительно 130 мг, от приблизительно 5 мг до приблизительно 140 мг, от приблизительно 5 мг до приблизительно 150 мг, от приблизительно 10 мг до приблизительно 20 мг, от приблизительно 10 мг до приблизительно 30 мг, от приблизительно 10 мг до приблизительно 40 мг, от приблизительно 10 мг до приблизительно 50 мг, от приблизительно 10 мг до приблизительно 60 мг, от приблизительно 10 мг до приблизительно 70 мг, от приблизительно 10 мг до приблизительно 80 мг, от приблизительно 10 мг до приблизительно 90 мг, от приблизительно 10 мг до приблизительно 100 мг, от приблизительно 10 мг до приблизительно 110 мг, от приблизительно 10 мг до приблизительно 120 мг, от приблизительно 10 мг до приблизительно 130 мг, от приблизительно 10 мг до приблизительно 140 мг, от приблизительно 10 мг до приблизительно 150 мг, от приблизительно 10 мг до приблизительно 175 мг, от приблизительно 10 мг до приблизительно 200 мг, от приблизительно 10 мг до приблизительно 225 мг, от приблизительно 10 мг до приблизительно 250 мг, от приблизительно 25 мг до приблизительно 50 мг, от приблизительно 25 мг до приблизительно 75 мг, от приблизительно 25 мг до приблизительно 100 мг, от приблизительно 25 мг до приблизительно 125 мг, от приблизительно 25 мг до приблизительно 150 мг, от приблизительно 25 мг до приблизительно 175 мг, от приблизительно 25 мг до приблизительно 200 мг, от приблизительно 25 мг до приблизительно 225 мг, от приблизительно 25 мг до приблизительно 250 мг, от приблизительно 50 мг до приблизительно 75 мг, от приблизительно 50 мг до приблизительно 100 мг, от приблизительно 50 мг до приблизительно 125 мг, от приблизительно 50 мг до приблизительно 150 мг, от приблизительно 50 мг до приблизительно 175 мг, от приблизительно 50 мг до приблизительно 200 мг, от приблизительно 50 мг до приблизительно 225 мг, от приблизительно 50 мг до приблизительно 250 мг, от приблизительно 75 мг до приблизительно 100 мг, от приблизительно 75 мг до приблизительно 125 мг, от приблизительно 75 мг до приблизительно 150 мг, от приблизительно 75 мг до приблизительно 175 мг, от приблизительно 75 мг до приблизительно 200 мг, от приблизительно 75 мг до приблизительно 225 мг или от приблизительно 75 мг до приблизительно 250 мг.
[083] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 100 мг до приблизительно 125 мг, от приблизительно 100 мг до приблизительно 150 мг, от приблизительно 100 мг до приблизительно 175 мг, от приблизительно 100 мг до приблизительно 200 мг, от приблизительно 100 мг до приблизительно 225 мг, от приблизительно 100 мг до приблизительно 250 мг, от приблизительно 100 мг до приблизительно 275 мг, от приблизительно 100 мг до приблизительно 300 мг, от приблизительно 100 мг до приблизительно 325 мг, от приблизительно 100 мг до приблизительно 350 мг, от приблизительно 100 мг до приблизительно 375 мг, от приблизительно 100 мг до приблизительно 400 мг, от приблизительно 100 мг до приблизительно 425 мг, от приблизительно 100 мг до приблизительно 450 мг, от приблизительно 100 мг до приблизительно 475 мг, от приблизительно 100 мг до приблизительно 500 мг, от приблизительно 100 мг до приблизительно 525 мг, от приблизительно 100 мг до приблизительно 550 мг, от приблизительно 100 мг до приблизительно 575 мг, от приблизительно 100 мг до приблизительно 600 мг, от приблизительно 125 мг до приблизительно 150 мг, от приблизительно 125 мг до приблизительно 175 мг, от приблизительно 125 мг до приблизительно 200 мг, от приблизительно 125 мг до приблизительно 225 мг, от приблизительно 125 мг до приблизительно 250 мг, от приблизительно 125 мг до приблизительно 275 мг, от приблизительно 125 мг до приблизительно 300 мг, от приблизительно 125 мг до приблизительно 325 мг, от приблизительно 125 мг до приблизительно 350 мг, от приблизительно 125 мг до приблизительно 375 мг, от приблизительно 125 мг до приблизительно 400 мг, от приблизительно 125 мг до приблизительно 425 мг, от приблизительно 125 мг до приблизительно 450 мг, от приблизительно 125 мг до приблизительно 475 мг, от приблизительно 125 мг до приблизительно 500 мг, от приблизительно 125 мг до приблизительно 525 мг, от приблизительно 125 мг до приблизительно 550 мг, от приблизительно 125 мг до приблизительно 575 мг, от приблизительно 125 мг до приблизительно 600 мг, от приблизительно 150 мг до приблизительно 175 мг, от приблизительно 150 мг до приблизительно 200 мг, от приблизительно 150 мг до приблизительно 225 мг, от приблизительно 150 мг до приблизительно 250 мг, от приблизительно 150 мг до приблизительно 275 мг, от приблизительно 150 мг до приблизительно 300 мг, от приблизительно 150 мг до приблизительно 325 мг, от приблизительно 150 мг до приблизительно 350 мг, от приблизительно 150 мг до приблизительно 375 мг, от приблизительно 150 мг до приблизительно 400 мг, от приблизительно 150 мг до приблизительно 425 мг, от приблизительно 150 мг до приблизительно 450 мг, от приблизительно 150 мг до приблизительно 475 мг, от приблизительно 150 мг до приблизительно 500 мг, от приблизительно 150 мг до приблизительно 525 мг, от приблизительно 150 мг до приблизительно 550 мг, от приблизительно 150 мг до приблизительно 575 мг, от приблизительно 150 мг до приблизительно 600 мг, от приблизительно 200 мг до приблизительно 225 мг, от приблизительно 200 мг до приблизительно 250 мг, от приблизительно 200 мг до приблизительно 275 мг, от приблизительно 200 мг до приблизительно 300 мг, от приблизительно 200 мг до приблизительно 325 мг, от приблизительно 200 мг до приблизительно 350 мг, от приблизительно 200 мг до приблизительно 375 мг, от приблизительно 200 мг до приблизительно 400 мг, от приблизительно 200 мг до приблизительно 425 мг, от приблизительно 200 мг до приблизительно 450 мг, от приблизительно 200 мг до приблизительно 475 мг, от приблизительно 200 мг до приблизительно 500 мг, от приблизительно 200 мг до приблизительно 525 мг, от приблизительно 200 мг до приблизительно 550 мг, от приблизительно 200 мг до приблизительно 575 мг, от приблизительно 200 мг до приблизительно 600 мг, от приблизительно 200 мг до приблизительно 625 мг, от приблизительно 200 мг до приблизительно 650 мг, от приблизительно 200 мг до приблизительно 675 мг, от приблизительно 200 мг до приблизительно 700 мг, от приблизительно 200 мг до приблизительно 725 мг, от приблизительно 200 мг до приблизительно 750 мг, от приблизительно 200 мг до приблизительно 775 мг, от приблизительно 200 мг до приблизительно 800 мг, от приблизительно 200 мг до приблизительно 825 мг, от приблизительно 200 мг до приблизительно 850 мг, от приблизительно 200 мг до приблизительно 875 мг, от приблизительно 200 мг до приблизительно 900 мг, от приблизительно 200 мг до приблизительно 925 мг, от приблизительно 200 мг до приблизительно 950 мг, от приблизительно 200 мг до приблизительно 975 мг, от приблизительно 200 мг до приблизительно 1000 мг, от приблизительно 200 мг до приблизительно 1250 мг, от приблизительно 200 мг до приблизительно 1500 мг, от приблизительно 200 мг до приблизительно 1750 мг, от приблизительно 200 мг до приблизительно 2000 мг, от приблизительно 200 мг до приблизительно 2250 мг, от приблизительно 200 мг до приблизительно 2500 мг, от приблизительно 200 мг до приблизительно 2750 мг или от приблизительно 200 мг до приблизительно 3000 мг.
[084] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 250 мг до приблизительно 275 мг, от приблизительно 250 мг до приблизительно 300 мг, от приблизительно 250 мг до приблизительно 325 мг, от приблизительно 250 мг до приблизительно 350 мг, от приблизительно 250 мг до приблизительно 375 мг, от приблизительно 250 мг до приблизительно 400 мг, от приблизительно 250 мг до приблизительно 425 мг, от приблизительно 250 мг до приблизительно 450 мг, от приблизительно 250 мг до приблизительно 475 мг, от приблизительно 250 мг до приблизительно 500 мг, от приблизительно 250 мг до приблизительно 525 мг, от приблизительно 250 мг до приблизительно 550 мг, от приблизительно 250 мг до приблизительно 575 мг, от приблизительно 250 мг до приблизительно 600 мг, от приблизительно 250 мг до приблизительно 625 мг, от приблизительно 250 мг до приблизительно 650 мг, от приблизительно 250 мг до приблизительно 675 мг, от приблизительно 250 мг до приблизительно 700 мг, от приблизительно 250 мг до приблизительно 725 мг, от приблизительно 250 мг до приблизительно 750 мг, от приблизительно 250 мг до приблизительно 775 мг, от приблизительно 250 мг до приблизительно 800 мг, от приблизительно 250 мг до приблизительно 825 мг, от приблизительно 250 мг до приблизительно 850 мг, от приблизительно 250 мг до приблизительно 875 мг, от приблизительно 250 мг до приблизительно 900 мг, от приблизительно 250 мг до приблизительно 925 мг, от приблизительно 250 мг до приблизительно 950 мг, от приблизительно 250 мг до приблизительно 975 мг, от приблизительно 250 мг до приблизительно 1000 мг, от приблизительно 300 мг до приблизительно 325 мг, от приблизительно 300 мг до приблизительно 350 мг, от приблизительно 300 мг до приблизительно 375 мг, от приблизительно 300 мг до приблизительно 400 мг, от приблизительно 300 мг до приблизительно 425 мг, от приблизительно 300 мг до приблизительно 450 мг, от приблизительно 300 мг до приблизительно 475 мг, от приблизительно 300 мг до приблизительно 500 мг, от приблизительно 300 мг до приблизительно 525 мг, от приблизительно 300 мг до приблизительно 550 мг, от приблизительно 300 мг до приблизительно 575 мг, от приблизительно 300 мг до приблизительно 600 мг, от приблизительно 300 мг до приблизительно 625 мг, от приблизительно 300 мг до приблизительно 650 мг, от приблизительно 300 мг до приблизительно 675 мг, от приблизительно 300 мг до приблизительно 700 мг, от приблизительно 300 мг до приблизительно 725 мг, от приблизительно 300 мг до приблизительно 750 мг, от приблизительно 300 мг до приблизительно 775 мг, от приблизительно 300 мг до приблизительно 800 мг, от приблизительно 300 мг до приблизительно 825 мг, от приблизительно 300 мг до приблизительно 850 мг, от приблизительно 300 мг до приблизительно 875 мг, от приблизительно 300 мг до приблизительно 900 мг, от приблизительно 300 мг до приблизительно 925 мг, от приблизительно 300 мг до приблизительно 950 мг, от приблизительно 300 мг до приблизительно 975 мг, от приблизительно 300 мг до приблизительно 1000 мг, от приблизительно 400 мг до приблизительно 425 мг, от приблизительно 400 мг до приблизительно 450 мг, от приблизительно 400 мг до приблизительно 475 мг, от приблизительно 400 мг до приблизительно 500 мг, от приблизительно 400 мг до приблизительно 525 мг, от приблизительно 400 мг до приблизительно 550 мг, от приблизительно 400 мг до приблизительно 575 мг, от приблизительно 400 мг до приблизительно 600 мг, от приблизительно 400 мг до приблизительно 625 мг, от приблизительно 400 мг до приблизительно 650 мг, от приблизительно 400 мг до приблизительно 675 мг, от приблизительно 400 мг до приблизительно 700 мг, от приблизительно 400 мг до приблизительно 725 мг, от приблизительно 400 мг до приблизительно 750 мг, от приблизительно 400 мг до приблизительно 775 мг, от приблизительно 400 мг до приблизительно 800 мг, от приблизительно 400 мг до приблизительно 825 мг, от приблизительно 400 мг до приблизительно 850 мг, от приблизительно 400 мг до приблизительно 875 мг, от приблизительно 400 мг до приблизительно 900 мг, от приблизительно 400 мг до приблизительно 925 мг, от приблизительно 400 мг до приблизительно 950 мг, от приблизительно 400 мг до приблизительно 975 мг, от приблизительно 400 мг до приблизительно 1000 мг, от приблизительно 400 мг до приблизительно 1250 мг, от приблизительно 400 мг до приблизительно 1500 мг, от приблизительно 400 мг до приблизительно 1750 мг, от приблизительно 400 мг до приблизительно 2000 мг, от приблизительно 400 мг до приблизительно 2250 мг, от приблизительно 400 мг до приблизительно 2500 мг, от приблизительно 400 мг до приблизительно 2750 мг или от приблизительно 400 мг до приблизительно 3000 мг.
[085] В еще других аспектах данного варианта реализации количество описанной в настоящем документе ранпирназы и/или амфиназы, содержащееся в фармацевтической композиции, может находиться в диапазоне, например, от приблизительно 500 мг до приблизительно 525 мг, от приблизительно 500 мг до приблизительно 550 мг, от приблизительно 500 мг до приблизительно 575 мг, от приблизительно 500 мг до приблизительно 600 мг, от приблизительно 500 мг до приблизительно 625 мг, от приблизительно 500 мг до приблизительно 650 мг, от приблизительно 500 мг до приблизительно 675 мг, от приблизительно 500 мг до приблизительно 700 мг, от приблизительно 500 мг до приблизительно 725 мг, от приблизительно 500 мг до приблизительно 750 мг, от приблизительно 500 мг до приблизительно 775 мг, от приблизительно 500 мг до приблизительно 800 мг, от приблизительно 500 мг до приблизительно 825 мг, от приблизительно 500 мг до приблизительно 850 мг, от приблизительно 500 мг до приблизительно 875 мг, от приблизительно 500 мг до приблизительно 900 мг, от приблизительно 500 мг до приблизительно 925 мг, от приблизительно 500 мг до приблизительно 950 мг, от приблизительно 500 мг до приблизительно 975 мг, от приблизительно 500 мг до приблизительно 1000 мг, от приблизительно 600 мг до приблизительно 625 мг, от приблизительно 600 мг до приблизительно 650 мг, от приблизительно 600 мг до приблизительно 675 мг, от приблизительно 600 мг до приблизительно 700 мг, от приблизительно 600 мг до приблизительно 725 мг, от приблизительно 600 мг до приблизительно 750 мг, от приблизительно 600 мг до приблизительно 775 мг, от приблизительно 600 мг до приблизительно 800 мг, от приблизительно 600 мг до приблизительно 825 мг, от приблизительно 600 мг до приблизительно 850 мг, от приблизительно 600 мг до приблизительно 875 мг, от приблизительно 600 мг до приблизительно 900 мг, от приблизительно 600 мг до приблизительно 925 мг, от приблизительно 600 мг до приблизительно 950 мг, от приблизительно 600 мг до приблизительно 975 мг, от приблизительно 600 мг до приблизительно 1000 мг, от приблизительно 700 мг до приблизительно 725 мг, от приблизительно 700 мг до приблизительно 750 мг, от приблизительно 700 мг до приблизительно 775 мг, от приблизительно 700 мг до приблизительно 800 мг, от приблизительно 700 мг до приблизительно 825 мг, от приблизительно 700 мг до приблизительно 850 мг, от приблизительно 700 мг до приблизительно 875 мг, от приблизительно 700 мг до приблизительно 900 мг, от приблизительно 700 мг до приблизительно 925 мг, от приблизительно 700 мг до приблизительно 950 мг, от приблизительно 700 мг до приблизительно 975 мг, от приблизительно 700 мг до приблизительно 1000 мг, от приблизительно 800 мг до приблизительно 825 мг, от приблизительно 800 мг до приблизительно 850 мг, от приблизительно 800 мг до приблизительно 875 мг, от приблизительно 800 мг до приблизительно 900 мг, от приблизительно 800 мг до приблизительно 925 мг, от приблизительно 800 мг до приблизительно 950 мг, от приблизительно 800 мг до приблизительно 975 мг, от приблизительно 800 мг до приблизительно 1000 мг, от приблизительно 800 мг до приблизительно 1250 мг, от приблизительно 800 мг до приблизительно 1500 мг, от приблизительно 800 мг до приблизительно 1750 мг, от приблизительно 800 мг до приблизительно 2000 мг, от приблизительно 800 мг до приблизительно 2250 мг, от приблизительно 800 мг до приблизительно 2500 мг, от приблизительно 800 мг до приблизительно 2750 мг или от приблизительно 800 мг до приблизительно 3000 мг.
[086] Описанная в настоящем документе фармацевтическая композиция может необязательно содержать фармацевтически приемлемый носитель, который облегчает процессинг активного ингредиента в фармацевтически приемлемых композициях. В контексте настоящего изобретения термин «фармакологически приемлемый носитель» является синонимом для термина «фармакологический носитель» и обозначает любой носитель, у которого по существу при введении отсутствуют продолжительные или перманентные неблагоприятные эффекты, и охватывает такие термины, как «фармакологически приемлемая среда-носитель, стабилизатор, разбавитель, добавка, вспомогательный ингредиент или вспомогательное вещество». Такой носитель обычно смешивают с активным соединением или допускают его разбавление указанным активным соединением или включение такого соединения в его состав, и он может представлять собой твердый, полутвердый или жидкий агент. Понятно, что активные ингредиенты могут быть растворимыми, или можно осуществить их доставку в виде суспензии в желаемом носителе или разбавителе. Можно применять любой из множества фармацевтически приемлемых носителей, включая, без ограничений, водные среды, такие как, например, вода, солевой раствор, глицин, гиалуроновая кислота и им подобные; твердые носители, такие как, например, маннит, лактоза, крахмал, стеарат магния, сахарин натрия, тальк, целлюлоза, глюкоза, сахароза, карбонат магния и им подобные; растворители; дисперсионные среды; покрывающие агенты; антибактериальные и противогрибковые агенты; изотонические и задерживающие абсорбцию агенты или любой другой неактивный ингредиент. Выбор фармакологически приемлемого носителя может зависеть от способа введения. За исключением того, что любой фармакологически приемлемый носитель является несовместимым с активным агентом, предусмотрено его применение в фармацевтически приемлемых композициях. Неограничивающие примеры конкретных применений таких фармацевтических носителей можно найти в Pharmaceutical Dosage Forms and Drug Delivery Systems (Howard C. Ansel et al., eds., Lippincott Williams and Wilkins Publishers, 7th ed. 1999); REMINGTON: THE SCIENCE AND PRACTICE OF PHARMACY (Alfonso R. Gennaro ed., Lippincott, Williams & Wilkins, 20th ed. 2000); Goodman and  The Pharmacological Basis of Therapeutics (Joel G. Hardman et al., eds., McGraw-Hill Professional, 10th ed. 2001) и в Handbook of Pharmaceutical Excipients (Raymond C. Rowe et al., APhA Publications, 4th edition 2003). Данные протоколы представляют собой обычные процедуры, и любые модификации находятся в пределах компетенции специалиста в данной области техники и приведенного в настоящем документе руководства.
The Pharmacological Basis of Therapeutics (Joel G. Hardman et al., eds., McGraw-Hill Professional, 10th ed. 2001) и в Handbook of Pharmaceutical Excipients (Raymond C. Rowe et al., APhA Publications, 4th edition 2003). Данные протоколы представляют собой обычные процедуры, и любые модификации находятся в пределах компетенции специалиста в данной области техники и приведенного в настоящем документе руководства.
[087] Фармацевтическая композиция, описанная в настоящем описании, может необязательно содержать, без ограничений, другие фармацевтически приемлемые компоненты (или фармацевтические компоненты), включая, без ограничений, буферы, консерванты, регуляторы тоничности, соли, антиоксиданты, агенты для регулирования осмоляльности, физиологические вещества, фармакологические вещества, объемообразующие агенты, эмульгирующие агенты, смачивающие агенты, подсластители или ароматизаторы и им подобные. Для получения описанной в настоящем документе фармацевтической композиции можно применять различные буферы и средства для регулирования рН, при условии, что поучающийся в результате препарат является фармацевтически приемлемым. Такие буферы включают, без ограничений, ацетатные буферы, цитратные буферы, фосфатные буферы, нейтральный забуференный солевой раствор, забуференный фосфатом солевой раствор и боратные буферы. Понятно, для регулирования рН композиции при необходимости можно применять кислоты или основания. Фармацевтически приемлемые антиоксиданты включают, без ограничений, метабисульфит натрия, тиосульфат натрия, ацетилцистеин, бутилированный гидроксианизол и бутилированный гидрокситолуол. Подходящие консерванты включают, без ограничений, бензалкония хлорид, хлорбутанол, тимеросал, ацетат фенилртути, нитрат фенилртути, стабилизированную оксихлорную композицию, такую как, например, PURITE® и хеланты, такие как, например, ДТПА или ДТПА-бисамид, кальция ДТПА, и СаNа ДТПА-бисамид. Многие из этих консервантов обладают бактерицидными свойствами. Регуляторы тоничности, применяемые в фармацевтической композиции, включают, без ограничений, соли, такие как, например, хлорид натрия, хлорид калия, маннит или глицерин и другие фармацевтически приемлемые регуляторы тоничности. Указанную фармацевтическую композицию можно представить в виде соли и ее можно получить при помощи многих кислот, включая, но не ограничиваясь ими, соляную, серную, уксусную, молочную, винную, яблочную, янтарную и т.д. Соли, как правило, более растворимы в водных или других протонных растворителях, чем соответствующие формы свободного основания. Понятно, что такие и другие вещества, известные в области фармакологии, могут содержаться в фармацевтической композиции.
[088] Описанную в настоящем документе фармацевтическую композицию можно приготовить для осуществления как местной, так и системной доставки с применением местного, офтальмологического, энтерального или парентерального путей введения. Кроме того, описанную в настоящем документе фармацевтическую композицию можно получить в виде жидкого состава, полутвердого состава или твердого состава. Описанный в настоящем документе состав можно получить так, чтобы образовывалась одна фаза, как, например, масло или твердое вещество. В альтернативном варианте описанный в настоящем документе состав можно получить так, чтобы образовывалось две фазы, как, например, коллоидный состав. Описанную в настоящем документе фармацевтическую композицию, предназначенную для такого введения, можно получить по любому способу, известному в данной области техники для получения фармацевтических композиций. Жидкие составы, подходящие для местного и офтальмологического введения, включают, без ограничений, растворы и эмульсии. Полутвердые составы, подходящие для местного и офтальмологического введения, включают, без ограничений, мази, кремы, мази, пены и гели. Твердые составы, подходящие для местного и офтальмологического введения, включают, без ограничений, гелевые имплантаты, имплантаты из твердого золя и твердые имплантаты.
[089] Описанный в настоящем документе состав может представлять собой одну простую систему или выступать как часть более сложной системы доставки лекарственного средства. Независимо от состава, описанная в настоящем документе ранпирназа и/или амфиназа, а также фармацевтически приемлемые вспомогательные вещества и компоненты, должны быть совместимы с офтальмологическим составом, поскольку глаз очень чувствителен к раздражителям. Это включает такие факторы, как осмолярность, рН, температура и другие. Описанный в настоящем документе состав может содержать предварительно оптимизированные офтальмологические растворы, содержащие смачивающие вещества, такие как слезозаменители Refresh или другие отпускаемые без рецепта (ОТС) слезозаменители, доступные на сегодняшний день. Если для увеличения продолжительности пребывания на поверхности глаза требуется более усовершенствованный состав, добавление совместных растворителей, поверхностно-активных веществ, осмотических агентов, комплексообразующих агентов (таких как циклодекстринов), буферов и вяжущих агентов или комбинаций из вышеуказанных веществ, успешно применялось ранее для других терапевтических средств. Кроме того, описанную в настоящем документе ранпирназу и/или амфиназу можно ввести в состав фармацевтической композиции в исходном виде, или ее можно ввести в состав одной фармацевтической композиции совместно по меньшей мере с одним терапевтическим соединением, описанным в настоящем документе.
[090] Описанную в настоящем документе ранпирназу и/или амфиназу можно приготовить в системе для доставки с контролируемым высвобождением, включая состав с замедленным высвобождением и состав с пролонгированным высвобождением. Поверхность глаза представляет собой твердую ткань-мишень для введения лекарственного средства, поскольку образование слезной жидкости немедленно разбавляет любой активный ингредиент. Кроме того, моргание - это еще один источник для немедленного разбавления и удаления любого активного доставляемого ингредиента. Применение системы для доставки с контролируемым высвобождением обеспечивает «сцепление» с поверхностью глаза с гарантией того, что описанная в настоящем документе ранпирназа и/или амфиназа остаются на ней в течение времени, достаточного для доставки требуемой дозы, необходимой для терапевтического эффекта. Такая система для доставки с контролируемым высвобождением может улучшать кинетику доставки описанной в настоящем документе ранпирназы и/или амфиназы, путем высвобождения с контролируемым по времени способом, потенциально минимизируя количество инстилляций, необходимых в течение курса лечения.
[091] Состав с пролонгированным высвобождением относится к высвобождению описанной в настоящем документе ранпирназы и/или амфиназы в течение периода времени меньшего, чем приблизительно через семь дней. Состав с замедленным высвобождением относится к высвобождению описанной в настоящем документе ранпирназы и/или амфиназы в течение периода от приблизительно семи дней или более.
[092] В аспектах данного варианта реализации состав с замедленным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу нулевого порядка в течение периода, например, приблизительно 7 дней, приблизительно 15 дней после введения, приблизительно 30 дней, приблизительно 45 дней, приблизительно 60 дней, приблизительно 75 дней или приблизительно 90 дней после введения. В других аспектах данного варианта реализации состав с замедленным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу нулевого порядка в течение периода, например, по меньшей мере 7 дней, по меньшей мере 15 дней, по меньшей мере 30 дней, по меньшей мере 45 дней, по меньшей мере 60 дней, по меньшей мере 75 дней или по меньшей мере 90 дней после введения. В еще других аспектах данного варианта реализации состав с замедленным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу первого порядка в течение периода, например, приблизительно 7 дней, приблизительно 15 дней после введения, приблизительно 30 дней, приблизительно 45 дней, приблизительно 60 дней, приблизительно 75 дней или приблизительно 90 дней после введения. В еще других аспектах данного варианта реализации состав с замедленным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу первого порядка в течение периода, например, по меньшей мере 7 дней, по меньшей мере 15 дней, по меньшей мере 30 дней, по меньшей мере 45 дней, по меньшей мере 60 дней, по меньшей мере 75 дней или по меньшей мере 90 дней после ведения.
[093] В аспектах данного варианта реализации состав с пролонгированным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу нулевого порядка в течение периода, например, приблизительно 1 день, приблизительно 2 дня, приблизительно 3 дня, приблизительно 4 дня, приблизительно 5 дней, приблизительно 6 дней или приблизительно 7 дней после введения. В других аспектах данного варианта реализации состав с пролонгированным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу нулевого порядка в течение периода, например, не более 1 дня, не более 2 дней, не более 3 дней, не более 4 дней, не более 5 дней, не более 6 дней или не более 7 дней после введения. В еще других аспектах данного варианта реализации состав с пролонгированным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу первого порядка в течение периода, например, приблизительно 1 день, приблизительно 2 дня, приблизительно 3 дня, приблизительно 4 дня, приблизительно 5 дней, приблизительно 6 дней или приблизительно 7 дней после введения. В еще других аспектах данного варианта реализации состав с пролонгированным высвобождением высвобождает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию с кинетикой высвобождения по существу первого порядка в течение периода, например, не более 1 дня, не более 2 дней, не более 3 дней, не более 4 дней, не более 5 дней, не более 6 дней или не более 7 дней после введения.
[094] Аспекты настоящего изобретения описывают, в частности, способ лечения индивидуума с вирусным конъюнктивитом. В одном варианте реализации указанный способ включает стадию введения индивидууму, нуждающемуся в этом, описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиций, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение указанного индивидуума. Другие аспекты настоящего изобретения раскрывают, в частности, применение ранпирназы и/или амфиназы, описанной в настоящем документе, для лечения индивидуума с вирусным конъюнктивитом.
[095] Аспекты настоящего изобретения описывают, в частности, лечение индивидуума, страдающего от вирусного конъюнктивита. В контексте настоящего изобретения термин «лечение» относится к уменьшению или устранению у индивидуума клинического симптома вирусного конъюнктивита; или к задерживанию или предотвращению у индивидуума клинического симптома вирусного конъюнктивита. Например, термин «лечение» может означать уменьшение симптома состояния, характеризующегося вирусным конъюнктивитом, например, по меньше мере на 20%, по меньше мере на 25%, по меньше мере на 30%, по меньше мере на 35%, по меньше мере на 40%, по меньше мере на 45%, по меньше мере на 50%, по меньше мере на 55%, по меньше мере на 60%, по меньше мере на 65%, по меньше мере на 70%, по меньше мере на 75%, по меньше мере на 80%, по меньше мере на 85%, по меньше мере на 90%, по меньше мере на 95% или по меньше мере на 100%. Фактические симптомы, ассоциированные с вирусным конъюнктивитом, хорошо известны, и их может определить специалист в данной области техники, принимая во внимание факторы, включая, без ограничений, продолжительность вирусного конъюнктивита, конкретный вирусный патоген и/или тяжесть вирусного конъюнктивита. Неограничивающие примеры симптомов, ассоциированных с вирусным конъюнктивитом, описанным в настоящем документе, включают покраснение склеры, отек склеры, покраснение внутреннего века, отек внутреннего века, текучесть внутреннего века, окулярный зуд (зуд в глазах), ощущение инородного тела (песок в глазах или поцарапанные глаза), жжение в глазах, боль в глазах, помутнение зрения, повышенную чувствительность к свету или светобоязнь, субэпителиальные инфильтраты, повышенную выработку слезной жидкости, водянистые выделения, слизисто-гнойные выделения и образование корочки на ресницах. Специалисты в данной области техники знают соответствующие симптомы или признаки, ассоциированные с конкретным типом вирусного конъюнктивита, и знают, каким образом определить, является ли индивидуум кандидатом на лечение, как это описано в настоящем документе.
[096] Аспекты настоящего изобретения включают, в частности, вирусный конъюнктивит. На сегодняшний день вирусный конъюнктивит является самым распространенным инфекционным заболеванием глаз. По оценкам на его долю приходится вплоть до 70% от общего числа случаев ежегодно наблюдаемого конъюнктивита. Описанный в настоящем документе вирусный конъюнктивит включает эпидемический кератоконъюнктивит, фарингоконъюнктивальную лихорадку, неспецифический спорадический фолликулярный конъюнктивит или хронический папиллярный конъюнктивит. Из семейств вирусов, которые вызывают заболевание у человека, аденовирусы ответственны за почти 90% случаев. Однако и другие вирусы, которые также могут быть ответственны за конъюнктивальную инфекцию, включают вирус простого герпеса (HSV), вирус ветряной оспы (VZV), пикорнавирус (энтеровирус 70, коксаки А24) и поксвирус (вирус контагиозного моллюска, осповакцины).
[097] Аденовирусы (члены семейства Adnoviridae) - это вирусы среднего размера (от 90 до 100 нм), без оболочки, с икосаэдрическим нуклеокапсидом, содержащим двухцепочечный ДНК-геном. Для аденовирусов характерно большое число хозяев среди позвоночных. Было установлено, что приблизительно 60 различных серотипов аденовирусов вызывает широкий спектр заболеваний у людей, от легких респираторных инфекций у детей (известных как простуда) до угрожающего жизни полиорганного заболевания у людей с ослабленной иммунной системой.
[098] Что касается вирусного конъюнктивита, то серотипы аденовирусов 3, 4, 7, 8, 11, 13, 19 и 37, по всей видимости, являются первичными возбудителями, хотя другие серотипы аденовируса также могут вызывать вирусный конъюнктивит. Серотипы аденовирусов 3, 7 и 11 классифицируют как аденовирус А человека; серотип 8, 13, 19 и 37 классифицируют как аденовирус D человека; и серотип 4 классифицируют как аденовирус Е человека. Из-за низкого врожденного иммунитета против аденовируса в общей популяции каждый индивидуум считается восприимчивым к инфекции. Кроме того, конъюнктивальные вирусные инфекции инициируют сильный иммунный ответ. Способность регулировать такой ответ поможет уменьшить многие клинические симптомы, ассоциированные с вирусным конъюнктивитом.
[099] С клинической точки зрения эти аденовирусы могут вызывать множественные различные синдромы, при этом наиболее распространенными являются эпидемический кератоконъюнктивит (ЕКС - в первую очередь серотипы 8, 19, 37) и фарингоконъюнктивальная лихорадка (PCF - прежде всего серотипы 3, 4, 7). Эпидемический кератоконъюнктивит (ЕКС) является одним из наиболее распространенных синдромов острого конъюнктивита с характерными клиническими признаками, такими как внезапное начало острого фолликулярного конъюнктивита с водянистыми выделениями, гиперемия (покраснение), хемоз и ипсилатеральная преаурикулярная лимфаденопатия. Поражение роговицы может происходить в форме диффузного, мелкого и/или поверхностного кератита, эпителиальных дефектов и даже помутнение субэпителия. В 20-50% случаев помутнение роговицы может сохраняться в течение нескольких недель или месяцев. Это явление может значительно снизить остроту зрения и вызвать симптомы бликов. Лечение в основном предназначено для контроля симптомов с применением холодных компрессов и слезозаменителей. Противовирусные глазные капли (такие как цидофовир) и циклоспориновые глазные капли были протестированы с клинической точки зрения, однако окончательного положительного эффекта не наблюдали. В очень конкретных случаях с тяжелым мембранным конъюнктивитом легкие кортикостероиды для местного применения можно применять для контроля воспаления.
[0100] ЕКС обычно представляет собой локальное заболевание. Инкубационный период составляет 2-14 дней, и лицо может оставаться заразным в течение 10-14 дней после появления симптомов. Симптомы имеют тенденцию продолжаться в течение 7-21 дней. Второй глаз, как правило, поражается в более чем 50% случаев в течение 7 дней после начала поражения первого. Во втором глазу признаки и симптомы обычно менее выражены. Оно имеет тенденцию к спонтанному разрешению без значительных осложнений. Однако в течение этого периода указанный пациент обычно находится в своем доме, чтобы не распространять инфекцию. В редких случаях рубцевание конъюнктивы и конъюнктивальные спайки могут возникать на фоне мембранного конъюнктивита.
[0101] Эпидемии ЕКС, как правило, происходят в закрытых учреждениях (таких, как школы, больницы, лагеря, дома сестер, рабочие места). Прямой контакт с глазными выделениями является основным способом передачи. Другими возможными способами передачи являются воздушно-капельный способ и, возможно, бассейны для плавания. Аденовирус можно выделить из глаз в течение 14 дней после появления клинических симптомов. Кроме того, хорошо документирована роль медицинских клиник в распространении указанного заболевания. Многие эпидемии начинались в офтальмологических амбулаториях при непосредственном контакте с зараженными инструментами для диагностики. Некоторые из причин передачи ЕКС-инфекции в больницах и клиниках включают в себя тот факт, что: (1) вирус может оставаться «жизнеспособным» в течение 5 недель; (2) вирус устойчив к стандартным дезинфицирующим средствам, таким как 70% изопропиловый спирт и аммиак; и (3) вирус «просачивается» из глаза за три (3) дня до и через четырнадцать (14) дней после появления симптомов.
[0102] Фарингоконъюнктивальная лихорадка (PCF) представляет собой острую и высокоинфекционную болезнь, характеризующуюся ассоциированными с ней системными проявлениями, такими как лихорадка, фарингит, острый фолликулярный конъюнктивит и региональная лимфоидная гиперплазия с болезненной увеличенной преаурикулярной аденопатией. Пациенты испытывают внезапное или постепенное начало лихорадки с температурой от 100°F до 104°F (приблизительно от 37,7°С до 40°С), продолжающейся вплоть до 10 дней. Миалгия, недомогание и нарушения в работе ЖКТ часто ассоциированы с лихорадкой. Фарингит может быть мягким или довольно болезненным. Первоначальные симптомы конъюнктивита варьируются от незначительного зуда и жжения до выраженного раздражения и слезотечения, но небольшой светобоязнью. Отек век может произойти в течение 48 часов. Признаки заболевания включают эпифору, конъюнктивальную гиперемию (покраснение) и хемоз, субконъюнктивальное кровоизлияние, фолликулярную или мягкую папиллярную конъюнктивальную реакцию и отек век. Может возникнуть образование мягкой корочки и выделений. PCF чаще всего является двусторонним (билатеральным), причем на одном глазу появление симптомов обычно начинается за 1-3 дня до появления симптомов на втором глазу. При двустороннем заболевании, первый глаз в целом поражается сильнее.
[0103] Вирусный конъюнктивит обладает двумя основными характеристиками, которые необходимо ослаблять, а именно наличие и репликация вируса и иммунный ответ хозяина, который приводит к клиническим симптомам. Для успешной терапии недостаточно действовать только в отношении одного из этих двух аспектов. Описанная в настоящем документе ранпирназа или амфиназа, по всей видимости, обладает как противовирусными, так и иммуномодулирующими механизмами действия.
[0104] В варианте реализации настоящего изобретения описан способ или применение лечения вирусного конъюнктивита, вызываемого аденовирусом В человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить вирусный конъюнктивит, вызываемый серотипом 3 аденовируса В человека, серотипом 7 аденовируса В человека, серотипом 11 аденовируса В человека или любой их комбинацией.
[0105] В варианте реализации настоящего изобретения описан способ или применение лечения эпидемического кератоконъюнктивита, вызываемого аденовирусом В человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить эпидемический кератоконъюнктивит, вызываемый серотипом 3 аденовируса В человека, серотипом 7 аденовируса В человека, серотипом 11 аденовируса В человека или любой их комбинацией.
[0106] В варианте реализации настоящего изобретения описан способ или применение лечения фарингоконъюнктивальной лихорадки, вызываемой аденовирусом В человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить фарингоконъюнктивальную лихорадку, вызываемую серотипом 3 аденовируса В человека, серотипом 7 аденовируса В человека, серотипом 11 аденовируса В человека или любой их комбинацией.
[0107] В варианте реализации настоящего изобретения описан способ или применение лечения вирусного конъюнктива, вызываемого аденовирусом D человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить вирусный конъюнктивит, вызываемый серотипом 8 аденовируса D человека, серотипом 13 аденовируса D человека, серотипом 19 аденовируса D человека, серотипом 37 аденовируса D человека или любой их комбинацией.
[0108] В варианте реализации настоящего изобретения описан способ или применение лечения эпидемического кератоконъюнктивита, вызываемого аденовирусом D человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить эпидемический кератоконъюнктивит, вызываемый серотипом 8 аденовируса D человека, серотипом 13 аденовируса D человека, серотипом 19 аденовируса D человека, серотипом 37 аденовируса D человека или любой их комбинацией.
[0109] В варианте реализации настоящего изобретения описан способ или применение лечения фарингоконъюнктивальной лихорадки, вызываемой аденовирусом D человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить фарингоконъюнктивальную лихорадку, вызываемую серотипом 8 аденовируса D человека, серотипом 13 аденовируса D человека, серотипом 19 аденовируса D человека, серотипом 37 аденовируса D человека или любой их комбинацией.
[0110] В варианте реализации настоящего изобретения описан способ или применение лечения вирусного конъюнктивита, вызываемого аденовирусом Е человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить вирусный конъюнктивит, вызываемый серотипом 4 аденовируса Е человека.
[0111] В варианте реализации настоящего изобретения описан способ или применение лечения эпидемического кератоконъюнктивита, вызываемого аденовирусом Е человека у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить эпидемический кератоконъюнктивит, вызываемый серотипом 4 аденовируса Е человека.
[0112] В варианте реализации настоящего изобретения описан способ или применение лечения фарингоконъюнктивальной лихорадки, вызываемой аденовирусом Е человека, у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума. В аспекте данного варианта реализации описанный в настоящем документе способ позволяет лечить фарингоконъюнктивальную лихорадку, вызываемую серотипом 4 аденовируса Е человека.
[0113] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления уровня вируса или титра вируса у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень вируса или титр вируса. В аспектах данного варианта реализации в описанном в настоящем документе способе вирус, уровень или титр которого уменьшают или подавляют, представляет собой аденовирус В человека, аденовирус D человека, аденовирус Е человека или любую их комбинацию. В других аспектах данного варианта реализации аденовирус В человека может представлять собой, например, серотип 3 аденовируса В человека, серотип 7 аденовируса В человека, серотип 11 аденовируса В человека или любую их комбинацию. В еще других аспектах данного варианта реализации аденовирус D человека может представлять собой, например, серотип 8 аденовируса D человека, серотип 13 аденовируса D человека, серотип 19 аденовируса D человека, серотип 37 аденовируса D человека или любую их комбинацию. В еще других аспектах данного варианта реализации аденовирус Е человека может представлять собой, например, серотип 4 аденовируса Е человека. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень вируса или титр вируса у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень вируса или титр вируса у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0114] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления уровня вируса или титра вируса у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень вируса или титр вируса. В аспектах данного варианта реализации в описанном в настоящем документе способе вирус, уровень или титр которого уменьшают или подавляют, представляет собой аденовирус В человека, аденовирус D человека, аденовирус Е человека или любую их комбинацию. В других аспектах данного варианта реализации аденовирус В человека может представлять собой, например, серотип 3 аденовируса В человека, серотип 7 аденовируса В человека, серотип 11 аденовируса В человека или любую их комбинацию. В еще других аспектах данного варианта реализации аденовирус D человека может представлять собой, например, серотип 8 аденовируса D человека, серотип 13 аденовируса D человека, серотип 19 аденовируса D человека, серотип 37 аденовируса D человека или любую их комбинацию. В еще других аспектах данного варианта реализации аденовирус Е человека может представлять собой, например, серотип 4 аденовируса Е человека. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень вируса или титр вируса у индивидуума например, по меньшей мере на меньшей мере 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень вируса или титр вируса у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0115] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления синтеза белка по меньшей мере в одной клетке индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет синтеза белка по меньшей мере в одной клетке. В аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет синтез белка по меньшей мере в одной клетке индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет синтез белка по меньшей мере в одной клетке индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0116] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления уровня тРНК по меньшей мере в одной клетке индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке индивидуума. В аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В других аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет синтез белка по меньшей мере в одной клетке индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0117] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления уровня индуцирующей воспаление молекулы у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень индуцирующей воспаление молекулы. В аспектах данного варианта реализации описанная в настоящем документе индуцирующая воспаление молекула представляет собой вещество Р (SP), пептид, связанный с геном кальцитонина (CGRP), глутамат или их комбинацию. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень индуцирующей воспаление молекулы у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет уровень индуцирующей воспаление молекулы у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0118] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления уровня индуцирующего воспаление простагландина у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень индуцирующего воспаление простагландина. В аспектах данного варианта реализации описанный в настоящем документе индуцирующий воспаление простагландин представляет собой 15dPGJ2. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень индуцирующего воспаление простагландина у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанные в настоящем документе способ или применение уменьшает или подавляет уровень индуцирующего воспаление простагландина у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0119] В варианте реализации настоящего изобретения описан способ или применение стимуляции или увеличения активности сигнального пути рецептора, активируемого пролифератором пероксисом (PPAR), у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение стимулирует или улучшает сигнальный путь PPAR. В аспектах данного варианта реализации активность сигнального пути PPAR, описанного в настоящем документе, представляет собой активность сигнального пути PPAR-α, активность сигнального пути PPAR-γ, активность сигнального пути PPAR-δ (также известный как PPAR-β) или любую их комбинацию. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение стимулирует или активность сигнального пути PPAR у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанные в настоящем документе способ или применение стимулирует или улучшает активность сигнального пути PPAR у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0120] В варианте реализации настоящего изобретения описан способ или применение для содействия установления изменения фенотипа M1 в М2 у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение индуцирует апоптоз клеток M1-макрофагов, способствует дифференцировке клеток М2-макрофагагов или и то, и другое, тем самым способствуя установлению изменения фенотипа M1 в М2. В варианте реализации настоящего изобретения описан способ или применение модуляции уровня Th1-цитокина и/или уровня Th2-цитокина у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет уровень интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки, увеличивает или улучшает уровень ИЛ-10, высвобождаемого из Th2-клетки или и то, и другое, посредством чего модулируется уровень Th1-цитокина и/или Th2-цитокина. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки, или увеличивает или улучшает уровень ИЛ-10, высвобождаемого из Th2-клетки или и то, и другое у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанный в настоящем документе способ или применение уменьшает или подавляет уровень интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки или увеличивает или улучшает уровень ИЛ-10, высвобождаемого из Th2-клетки или и то, и другое у индивидуума в диапазоне, от например, приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0121] В варианте реализации настоящего изобретения описан способ или применение уменьшения или подавления активности сигнального пути NFκB у индивидуума, нуждающегося в этом, путем введения указанному индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, при этом введение уменьшает или подавляет активность сигнального пути NFκB. В других аспектах данного варианта реализации описанный в настоящем документе способ или применение стимулирует или активность сигнального пути NFκB у индивидуума, например, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%. В еще других аспектах данного варианта реализации описанные в настоящем документе способ или применение стимулирует или улучшает активность сигнального пути NFκB у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
[0122] В аспектах настоящего изобретения предложено, в частности, введение описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции. В контексте настоящего изобретения термин «введение» относится к любому механизму доставки, который обеспечивает описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию для индивидуума, которое потенциально приводит к благоприятному результату с клинической, терапевтической или экспериментальной точек зрения. Фактический механизм доставки, применяемый для введения описанной в настоящем документе композиции индивидууму, может определить специалист в данной области техники, принимая во внимание факторы, включая, без ограничений, тип вирусного конъюнктивита, локализацию вирусного конъюнктивита, причину вирусного конъюнктивита, тяжесть вирусного конъюнктивита, степень желаемого облегчения для вирусного конъюнктивита, продолжительность желаемого облегчения для вирусного конъюнктивита, уровень вируса, титр вируса, репликацию вируса, синтез белка или тРНК, который необходимо уменьшить или подавить, конкретный сигнальный путь, индуцирующую воспаление молекулу, индуцирующий воспаление простагландин и/или цитокин, которые необходимо модулировать, конкретный вирусный патоген, применяемую ранпирназу и/или амфиназу, и/или фармацевтическую композицию, скорость выведения конкретной применяемой ранпирназы и/или амфиназы, фармакодинамику конкретной применяемой ранпирназы и/или амфиназы, природу других соединений, которые необходимо включить в указанную фармацевтическую композицию, конкретный путь введения, конкретные характеристики, историю и факторы риска указанного индивидуума, такие как, например, возраст, масса тела, общее состояние здоровья и им подобные или любую их комбинацию.
[0123] В одном варианте реализации введение индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции включает введение на поверхность конъюнктивы индивидуума, введение на поверхность глаза индивидуума или введение на поверхность конъюнктивы и/или глаза индивидуума.
[0124] В одном варианте реализации введение индивидууму описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции включает введение имплантата в конъюнктиву индивидуума, введение имплантата в глаз индивидуума или введение имплантата в конъюнктиву и/или глаз индивидуума.
[0125] Описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию можно вводить индивидууму, применяя методику поглощения клетками. Введение описанной в настоящем документе композиции с применением методики клеточного поглощения включает множество энтеральных или парентеральных методик, включая, без ограничений, офтальмологическое введение, пероральное введение в любой приемлемой форме, такой как, например, таблетка, жидкость, капсула, порошок или им подобные; местное введение в любой приемлемой форме, такой как, например, капли, спрей, кремы, гели или мази; внутрисосудистое введение в любой приемлемой форме, такой как, например, внутривенная инъекция, внутривенная инфузия, внутриартериальная инъекция, внутриартериальная инфузия и инсталляция с применением катетера в сосудистую сеть; пери- и внутритканевое введение в любой приемлемой форме, такой как, например, внутрибрюшинная инъекция, внутримышечная инъекция, подкожная инъекция, подкожная инфузия, внутриглазная инъекция, ретинальная инъекция или субретинальная инъекция или эпидуральная инъекция; внутрисуставное введение в любой приемлемой форме, такой как, например, установка катетера; и путем устройства для местного применения, такого как, например, имплантат, пластырь, таблетка, катетер, осмотический насос, суппозиторий, система биологически разрушаемой доставки, система доставки, не являющейся биологически разрушаемой, или другая имплантированная система с расширенным или медленным высвобождением. Список примеров биологически разлагаемых полимеров и способов их применения описаны, например, в Handbook of Biodegradable Polymers (Abraham J. Domb et al., eds., Overseas Publishers Association, 1997).
[0126] Описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию обычно вводят с применением офтальмологического состава и офтальмологическим путем доставки. Например, описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию можно получить в виде состава для местного применения, такого как, например, глазные капли, пробки, вставляемые в слезный канал, мазь в виде бальзама, мазь, лосьон, в виде состава для энтерального применения, такого как, например, таблетка, капсула, сироп или в виде состава для парентерального применения, такого как, например, пробка для инъекций или вставляемая вовнутрь глаза. Такие препараты можно вводить, например, офтальмологически посредством окулярной инсталляции, окулярной ирригации или имплантата для местного применения (пробки, вставляемой в слезный канал) или парентерально посредством внутриглазной инъекции или имплантата, интравитреальной инъекции, интракорнеальной инъекции или имплантата или субконъюнктивальной инъекции или имплантата.
[0127] Описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию вводят в количестве, достаточном для лечения вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшения уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляции или улучшения сигнала путь рецептора, активируемого пролифератора пероксисом (PPAR), содействия установлению изменения фенотипа M1 в М2, модуляции Th1- и Th2-цитокинов и/или уменьшения или подавления сигнал NFκB-пути. В аспектах данного варианта реализации количество вводимой ранпирназы и/или амфиназы, описанной в настоящем документе или вводимой фармацевтической композиции, описанной в настоящем документе, представляет собой количество, достаточное для уменьшения по меньшей мере одного физиологического состояния или симптома, ассоциированного с вирусным конъюнктивитом, эпидемическим кератоконъюнктивитом и/или фарингоконъюнктивальной лихорадкой, уменьшения уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействия установления изменения фенотипа M1 в М2, модуляции Th1- и Th2-цитокинов и/или уменьшения или подавления сигнал NFκB-пути. В контексте настоящего изобретения термин «достаточное количество» включает термин «эффективное количество», «эффективная доза», «терапевтически эффективное количество» или «терапевтически эффективная доза» и относится к минимальному количеству описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции для достижения желаемого терапевтического эффекта, и включает количество, достаточное для уменьшения по меньшей мере одного физиологического состояния или симптома, ассоциированного с вирусным конъюнктивитом, эпидемическим кератоконъюнктивитом и/или фарингоконъюнктивальной лихорадкой, количество, достаточное для уменьшения уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, количество, достаточное для стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), количество, достаточное для содействия установления изменения фенотипа M1 в М2, количество, достаточное для модуляции Th1- и Th2-цитокинов, и/или количество, достаточное для уменьшения или подавления сигнала NFκB-пути.
[0128] В аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции модулирует по меньшей мере одно физиологическое состояние или симптом, ассоциированный с лечением вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшая уровень индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимулируя или улучшая сигнал пути рецептора, активируемого пролифератором пероксисом (PPAR), способствуя установлению изменения фенотипа M1 в М2, модулируя Th1- и Th2-цитокины и/или уменьшая или подавляя сигнал NFκB-пути, например, по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90% или по меньшей мере на 100%. В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции модулирует по меньшей мере одно физиологическое состояние или симптом, ассоциированный с лечением вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшая уровень индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимулируя или улучшая сигнал пути рецептора, активируемого пролифератором пероксисом (PPAR), способствуя установлению изменения фенотипа M1 в М2, модулируя Th1- и Th2-цитокины и/или уменьшая или подавляя сигнал NFκB-пути, например, не более чем на 10%, не более чем на 20%, не более чем на 30%, не более чем на 40%, не более чем на 50%, не более чем на 60%, не более чем на 70%, не более чем на 80%, не более чем на 90% или не более чем на 100%. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции модулирует по меньшей мере одно физиологическое состояние или симптом, ассоциированный с лечением вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшая уровень индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимулируя или улучшая сигнал пути рецептора, активируемого пролифератором пероксисом (PPAR), способствуя установлению изменения фенотипа M1 в М2, модулируя Th1- и Th2-цитокины и/или уменьшая или подавляя сигнал NFκB-пути, например, от приблизительно на 10% до приблизительно 100%, от приблизительно на 10% до приблизительно 90%, от приблизительно на 10% до приблизительно 80%, от приблизительно на 10% до приблизительно 70%, от приблизительно на 10% до приблизительно 60%, от приблизительно на 10% до приблизительно 50%, от приблизительно на 10% до приблизительно 40%, от приблизительно на 20% до приблизительно 100%, от приблизительно на 20% до приблизительно 90%, от приблизительно на 20% до приблизительно 80%, от приблизительно на 20% до приблизительно 20%, от приблизительно на 20% до приблизительно 60%, от приблизительно на 20% до приблизительно 50%, от приблизительно на 20% до приблизительно 40%, от приблизительно на 30% до приблизительно 100%, от приблизительно на 30% до приблизительно 90%, от приблизительно на 30% до приблизительно 80%, от приблизительно на 30% до приблизительно 70%, от приблизительно на 30% до приблизительно 60% или от приблизительно на 30% до приблизительно 50%. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции модулирует по меньшей мере одно физиологическое состояние или симптом, ассоциированный с лечением вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшая уровень индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимулируя или улучшая сигнал пути рецептора, активируемого пролифератором пероксисом (PPAR), способствуя установлению изменения фенотипа M1 в М2, модулируя Th1- и Th2-цитокины и/или уменьшая или подавляя сигнал NFκB-пути в течение, например, по меньшей мере одной недели, по меньшей мере двух недель, по меньшей мере трех недель, по меньшей мере одного месяца, по меньшей мере двух месяцев, по меньшей мере трех месяцев, по меньшей мере четырех месяцев, по меньшей мере пяти месяцев, по меньшей мере шести месяцев, по меньшей мере семи месяцев, по меньшей мере восьми месяцев, по меньшей мере девяти месяцев, по меньшей мере десяти месяцев, по меньшей мере одиннадцати месяцев или по меньшей мере двенадцати месяцев.
[0129] Фактическое эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции для введения индивидууму может определить специалист в данной области техники, принимая во внимание факторы, включая, без ограничений, тип вирусного конъюнктивита, локализацию вирусного конъюнктивита, причину вирусного конъюнктивита, тяжесть вирусного конъюнктивита, степень желаемого облегчения для вирусного конъюнктивита, продолжительность желаемого облегчения для вирусного конъюнктивита, уровень вируса, титр вируса, репликацию вируса, синтез белка или тРНК, который необходимо уменьшить или подавить, конкретный сигнальный путь, индуцирующую воспаление молекулу, индуцирующий воспаление простагландин и/или цитокин, которые необходимо модулировать, конкретный вирусный патоген, применяемую ранпирназу и/или амфиназу, и/или фармацевтическую композицию, скорость выведения конкретной применяемой ранпирназы и/или амфиназы, фармакодинамику конкретной применяемой ранпирназы и/или амфиназы, природу других соединений, которые необходимо включить в указанную фармацевтическую композицию, конкретный путь введения, конкретные характеристики, историю и факторы риска указанного индивидуума, такие как, например, возраст, масса тела, общее состояние здоровья и им подобные или любую их комбинацию. Кроме того, в том случае, если применяют повторное введение описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, то фактическое терапевтически эффективное количество будет также зависеть от факторов, включая, без ограничений, частоту введения, период полувыведения ранпирназы и/или амфиназы или фармацевтической композиции или любую их комбинацию. Специалисту в данной области техники известно, что эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции можно экстраполировать по результатам анализов in vitro и исследований по введению in vivo с применением животных моделей до введения людям. Следует ожидать большое число изменений в необходимом эффективном количестве с учетом различия в эффективности различных путей введения. Например, следует ожидать, что при офтальмологическом введении в целом требуются более высокие уровни дозировки, чем при пероральном введении, и, как следует ожидать, при пероральном введении требуются более высокие уровни дозировки, чем при введении посредством внутривенной или интравитреальной инъекции. Вариации этих уровней дозировки можно корректировать с применением стандартных эмпирических подходов оптимизации, которые хорошо известны специалисту в данной области техники. Точные терапевтически эффективные уровни и схемы дозировки и образцы дозировки в предпочтительном варианте определяет лечащий врач с учетом вышеуказанных факторов.
[0130] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы в целом находится в диапазоне от приблизительно 0,001 мг/кг/день до приблизительно 100 мг/кг/день. В аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может составлять, например, по меньшей мере 0,001 мг/кг/день, по меньшей мере 0,01 мг/кг/день, по меньшей мере 0,1 мг/кг/день, по меньшей мере 1,0 мг/кг/день, по меньшей мере 5,0 мг/кг/день, по меньшей мере 10 мг/кг/день, по меньшей мере 15 мг/кг/день, по меньшей мере 20 мг/кг/день, по меньшей мере 25 мг/кг/день, по меньшей мере 30 мг/кг/день, по меньшей мере 35 мг/кг/день, по меньшей мере 40 мг/кг/день, по меньшей мере 45 мг/кг/день или по меньшей мере 50 мг/кг/день.
[0131] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,001 мг/кг/день до приблизительно 10 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 15 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 20 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 25 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 30 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 35 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 40 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 45 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 50 мг/кг/день, от приблизительно 0,001 мг/кг/день до приблизительно 75 мг/кг/день или от приблизительно 0,001 мг/кг/день до приблизительно 100 мг/кг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,01 мг/кг/день до приблизительно 10 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 15 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 20 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 25 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 30 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 35 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 40 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 45 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 50 мг/кг/день, от приблизительно 0,01 мг/кг/день до приблизительно 75 мг/кг/день или от приблизительно 0,01 мг/кг/день до приблизительно 100 мг/кг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,1 мг/кг/день до приблизительно 10 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 15 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 20 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 25 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 30 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 35 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 40 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 45 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 50 мг/кг/день, от приблизительно 0,1 мг/кг/день до приблизительно 75 мг/кг/день или от приблизительно 0,1 мг/кг/день до приблизительно 100 мг/кг/день.
[0132] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 1 мг/кг/день до приблизительно 10 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 15 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 20 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 25 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 30 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 35 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 40 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 45 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 50 мг/кг/день, от приблизительно 1 мг/кг/день до приблизительно 75 мг/кг/день или от приблизительно 1 мг/кг/день до приблизительно 100 мг/кг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 5 мг/кг/день до приблизительно 10 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 15 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 20 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 25 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 30 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 35 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 40 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 45 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 50 мг/кг/день, от приблизительно 5 мг/кг/день до приблизительно 75 мг/кг/день или от приблизительно 5 мг/кг/день до приблизительно 100 мг/кг/день.
[0133] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы в целом может находиться в диапазоне от приблизительно 0,001 мг/день до приблизительно 100 мг/день. В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может составлять, например, по меньшей мере 0,001 мг/день, по меньшей мере 0,01 мг/день, по меньшей мере 0,1 мг/день, по меньшей мере 1,0 мг/день, по меньшей мере 5,0 мг/день, по меньшей мере 10 мг/день, по меньшей мере 15 мг/день, по меньшей мере 20 мг/день, по меньшей мере 25 мг/день, по меньшей мере 30 мг/день, по меньшей мере 35 мг/день, по меньшей мере 40 мг/день, по меньшей мере 45 мг/день или по меньшей мере 50 мг/день.
[0134] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,001 мг/день до приблизительно 10 мг/день, от приблизительно 0,001 мг/день до приблизительно 15 мг/день, от приблизительно 0,001 мг/день до приблизительно 20 мг/день, от приблизительно 0,001 мг/день до приблизительно 25 мг/день, от приблизительно 0,001 мг/день до приблизительно 30 мг/день, от приблизительно 0,001 мг/день до приблизительно 35 мг/день, от приблизительно 0,001 мг/день до приблизительно 40 мг/день, от приблизительно 0,001 мг/день до приблизительно 45 мг/день, от приблизительно 0,001 мг/день до приблизительно 50 мг/день, от приблизительно 0,001 мг/день до приблизительно 75 мг/день или от приблизительно 0,001 мг/день до приблизительно 100 мг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,01 мг/день до приблизительно 10 мг/день, от приблизительно 0,01 мг/день до приблизительно 15 мг/день, от приблизительно 0,01 мг/день до приблизительно 20 мг/день, от приблизительно 0,01 мг/день до приблизительно 25 мг/день, от приблизительно 0,01 мг/день до приблизительно 30 мг/день, от приблизительно 0,01 мг/день до приблизительно 35 мг/день, от приблизительно 0,01 мг/день до приблизительно 40 мг/день, от приблизительно 0,01 мг/день до приблизительно 45 мг/день, от приблизительно 0,01 мг/день до приблизительно 50 мг/день, от приблизительно 0,01 мг/день до приблизительно 75 мг/день или от приблизительно 0,01 мг/день до приблизительно 100 мг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 0,1 мг/день до приблизительно 10 мг/день, от приблизительно 0,1 мг/день до приблизительно 15 мг/день, от приблизительно 0,1 мг/день до приблизительно 20 мг/день, от приблизительно 0,1 мг/день до приблизительно 25 мг/день, от приблизительно 0,1 мг/день до приблизительно 30 мг/день, от приблизительно 0,1 мг/день до приблизительно 35 мг/день, от приблизительно 0,1 мг/день до приблизительно 40 мг/день, от приблизительно 0,1 мг/день до приблизительно 45 мг/день, от приблизительно 0,1 мг/день до приблизительно 50 мг/день, от приблизительно 0,1 мг/день до приблизительно 75 мг/день или от приблизительно 0,1 мг/день до приблизительно 100 мг/день.
[0135] В других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 1 мг/день до приблизительно 10 мг/день, от приблизительно 1 мг/день до приблизительно 15 мг/день, от приблизительно 1 мг/день до приблизительно 20 мг/день, от приблизительно 1 мг/день до приблизительно 25 мг/день, от приблизительно 1 мг/день до приблизительно 30 мг/день, от приблизительно 1 мг/день до приблизительно 35 мг/день, от приблизительно 1 мг/день до приблизительно 40 мг/день, от приблизительно 1 мг/день до приблизительно 45 мг/день, от приблизительно 1 мг/день до приблизительно 50 мг/день, от приблизительно 1 мг/день до приблизительно 75 мг/день или от приблизительно 1 мг/день до приблизительно 100 мг/день. В еще других аспектах данного варианта реализации эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы может находиться в диапазоне, например, от приблизительно 5 мг/день до приблизительно 10 мг/день, от приблизительно 5 мг/день до приблизительно 15 мг/день, от приблизительно 5 мг/день до приблизительно 20 мг/день, от приблизительно 5 мг/день до приблизительно 25 мг/день, от приблизительно 5 мг/день до приблизительно 30 мг/день, от приблизительно 5 мг/день до приблизительно 35 мг/день, от приблизительно 5 мг/день до приблизительно 40 мг/день, от приблизительно 5 мг/день до приблизительно 45 мг/день, от приблизительно 5 мг/день до приблизительно 50 мг/день, от приблизительно 5 мг/день до приблизительно 75 мг/день или от приблизительно 5 мг/день до приблизительно 100 мг/день.
[0136] Дозирование может представлять собой однократную или множественную дозировку (серийное дозирование), и его легко может определить специалист в данной области техники. Например, лечение вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшение или подавление уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляция или улучшение сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействие установлению изменения фенотипа M1 в М2, модуляция Th1- и Th2-цитокинов и/или уменьшение или подавление сигнала NFκB-пути может включать однократное введение эффективного количества описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции. В качестве неограничивающего примера эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции можно вводить индивидууму один раз, например, в виде однократного применения. В альтернативном варианте лечение вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшение или подавление уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляция или улучшение сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействие установлению изменения фенотипа M1 в М2, модуляция Th1- и Th2-цитокинов и/или уменьшение или подавление сигнала NFκB-пути может включать многократные введения эффективного количества описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции, осуществляемые в течение периода времени, как, например, один или несколько раз в день, один раз в несколько дней, еженедельно, ежемесячно или ежегодно. В качестве неограничивающего примера описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию можно вводить индивидууму два, три, четыре, пять или шесть раз в день. Время введения может варьироваться от индивидуума к индивидууму в зависимости от таких факторов, как тяжесть симптомов у индивидуума. Например, эффективное количество описанной в настоящем документе ранпирназы и/или амфиназы или описанной в настоящем документе фармацевтической композиции можно вводить индивидууму от трех до шести раз в день в течение неопределенного периода времени или до тех пор, пока пациент больше не будет нуждаться в терапии. Для специалиста в данной области техники будет понятно, что можно отслеживать состояние указанного индивидуума на протяжении всего курса лечения и что эффективное количество описанной в настоящем документе вводимой ранпирназы и/или амфиназы или описанной в настоящем документе вводимой фармацевтической композиции можно соответствующим образом корректировать.
[0137] Способ или применение лечения описанного в настоящем документе вирусного конъюнктивита по существу влияет на инфицированные вирусом клетки. В аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита влияет, например, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 86%, по меньшей мере на 87%, по меньшей мере на 88%, по меньшей мере на 89%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% инфицированных вирусом клеток. В других аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита влияет, например, на не более чем 75%, не более чем 80%, по меньшей мере на 85%, не более чем на 86%, не более чем на 87%, по меньшей мере на 88%, не более чем на 89%, не более чем на 90%, не более чем на 91%, не более чем на 92%, не более чем на 93%, не более чем на 94%, не более чем на 95%, не более чем на 96%, не более чем на 97%, не более чем на 98% или не более чем на 99% инфицированных вирусом клеток. В еще других аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита влияет, например, от приблизительно на 75% до приблизительно 100%, от приблизительно на 80% до приблизительно 100%, от приблизительно на 85% до приблизительно 100%, от приблизительно на 90% до приблизительно 100%, от приблизительно на 95% до приблизительно 100%, от приблизительно на 75% до приблизительно 99%, от приблизительно на 80% до приблизительно 99%, от приблизительно на 85% до приблизительно 99%, от приблизительно на 90% до приблизительно 99%, от приблизительно на 95% до приблизительно 99%, от приблизительно на 75% до приблизительно 97%, от приблизительно на 80% до приблизительно 97%, от приблизительно на 85% до приблизительно 97%, от приблизительно на 90% до приблизительно 97% или от приблизительно на 95% до приблизительно 97% инфицированных вирусом клеток.
[0138] Способ или применение лечения описанного в настоящем документе вирусного конъюнктивита по существу не влияет на инфицированные не вирусом клетки. В аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита не влияет, например, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 86%, по меньшей мере на 87%, по меньшей мере на 88%, по меньшей мере на 89%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98% или по меньшей мере на 99% инфицированных не вирусом клеток. В других аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита не влияет, например, не более чем на 75%, не более чем на 80%, по меньшей мере на 85%, не более чем на 86%, не более чем на 87%, по меньшей мере на 88%, не более чем на 89%, не более чем на 90%, не более чем на 91%, не более чем на 92%, не более чем на 93%, не более чем на 94%, не более чем на 95%, не более чем на 96%, не более чем на 97%, не более чем на 98% или не более чем на 99% инфицированных не вирусом клеток. В еще других аспектах данного варианта реализации способ или применение лечения вирусного конъюнктивита не влияет, например, от приблизительно на 75% до приблизительно 100%, от приблизительно на 80% до приблизительно 100%, от приблизительно на 85% до приблизительно 100%, от приблизительно на 90% до приблизительно 100%, от приблизительно на 95% до приблизительно 100%, от приблизительно на 75% до приблизительно 99%, от приблизительно на 80% до приблизительно 99%, от приблизительно на 85% до приблизительно 99%, от приблизительно на 90% до приблизительно 99%, от приблизительно на 95% до приблизительно 99%, от приблизительно на 75% до приблизительно 97%, от приблизительно на 80% до приблизительно 97%, от приблизительно на 85% до приблизительно 97%, от приблизительно на 90% до приблизительно 97% или от приблизительно на 95% до приблизительно 97% инфицированных не вирусом клеток.
[0139] Описанную в настоящем документе ранпирназу и/или амфиназу или описанную в настоящем документе фармацевтическую композицию можно также вводить индивидууму в комбинации с другими терапевтическими соединениями для усиления общего терапевтического эффекта такого лечения. Применение нескольких соединений для лечения показания может усилить благоприятные эффекты, одновременно понижая присутствие побочных эффектов. Например, описанную в настоящем документе ранпирназу и/или амфиназу можно либо получить совместно, либо последовательно вводить с иммуномодулирующими лекарственными средствами, такими как стероиды, нестероидные противовоспалительные лекарственные средства (НПВЛС), циклоспорин А или другие терапевтические средства с целью улучшения иммуномодуляции, достигаемой при применении по отдельности ранпирназы и/или амфиназы. В качестве другого примера, описанную в настоящем документе ранпирназу и/или амфиназу можно либо получить совместно, либо последовательно вводить с антибиотиками, которые назначают в настоящий момент для лечения бактериального конъюнктивита.
[0140] Аспекты настоящего изобретения можно также описать следующим образом:
1. Способ лечения вирусного конъюнктивита у индивидуума, нуждающегося в этом, причем указанный способ включает введение на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение индивидуума.
2. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для лечения вирусного конъюнктивита.
3. Способ по варианту реализации 1 или применение по варианту реализации 2, причем указанный вирусный конъюнктивит представляет собой эпидемический кератоконъюнктивит, фарингоконъюнктивальную лихорадку, неспецифический спорадический фолликулярный конъюнктивит или хронический папиллярный конъюнктивит.
4. Способ уменьшения или подавления репликации вируса, инфицирующего индивидуума, нуждающегося в этом, причем указанный способ включает введение на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет репликацию указанного вируса, инфицирующего указанного индивидуума.
5. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для уменьшения или подавления репликации вируса, инфицирующего индивидуума.
6. Способ уменьшения или подавления синтеза белка по меньшей мере в одной клетке индивидуума, нуждающегося в этом, причем указанный способ включает введение на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет синтез белка по меньшей мере в одной клетке указанного индивидуума.
7. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для уменьшения или подавления синтеза белка по меньшей мере в одной клетке индивидуума.
8. Способ уменьшения или подавления уровня тРНК по меньшей мере в одной клетке индивидуума, нуждающегося этом, причем указанный способ включает введение на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке указанного индивидуума.
9. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, для уменьшения или подавления уровня тРНК по меньшей мере в одной клетке индивидуума.
10. Способ по любому одному из вариантов реализации 1, 3, 4, 6 или 8, применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9, при этом указанный вирусный конъюнктивит вызывается аденовирусом В человека.
11. Способ или применение по варианту реализации 10, при этом указанный аденовирус В человека представляет собой серотип 3 аденовируса В человека, серотип 7 аденовируса В человека, серотип 11 аденовируса В человека или любую их комбинацию.
12. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8, 10 или 11 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-11, при этом указанный вирусный конъюнктивит вызывается аденовирусом D человека.
13. Способ или применение по варианту реализации 12, при этом указанный аденовирус D человека представляет собой серотип 8 аденовируса D человека, серотип 13 аденовируса D человека, серотип 19 аденовируса D человека, серотип 37 аденовируса D человека или любую их комбинацию.
14. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-13 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-13, при этом указанный вирусный конъюнктивит вызывается аденовирусом Е человека.
15. Способ или применение по варианту реализации 14, при этом указанный аденовирус Е человека представляет собой серотип 4 аденовируса Е человека.
16. Способ уменьшения или подавления уровня индуцирующей воспаление молекулы у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет уровень индуцирующей воспаление молекулы у указанного индивидуума.
17. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, для уменьшения или подавления уровня индуцирующей воспаление молекулы.
18. Способ по варианту реализации 16 или применение по варианту реализации 17, при этом указанная индуцирующая воспаление молекула представляет собой вещество Р, пептид, связанный с геном кальцитонина, глутамат или их комбинацию.
19. Способ уменьшения или подавления уровня индуцирующего воспаление простагландина у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет уровень индуцирующего воспаление простагландина у указанного индивидуума.
20. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, для уменьшения или подавления уровня индуцирующего воспаление простагландина.
21. Способ по варианту реализации 19 или применение по варианту реализации 20, при этом указанный индуцирующий воспаление простагландин представляет собой 15dPGJ2.
22. Способ стимуляции или улучшения активности сигнального пути рецептора, активируемого пролифератором пероксисом (PPAR), у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение стимулирует или улучшает активность сигнального пути PPAR у указанного индивидуума.
23. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, для стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR).
24. Способ по варианту реализации 22 или применение по варианту реализации 23, при этом активность указанного сигнального пути PPAR представляет собой активность сигнального пути PPAR-α, активность сигнального пути PPAR-γ, активность сигнального пути PPAR-δ (также известный как PPAR-β) или любую их комбинацию.
25. Способ содействия установлению изменения фенотипа M1 в М2 у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение индуцирует апоптоз клеток M1-макрофагов, способствует дифференцировке клеток М2-макрофагов или и то, и другое, тем самым способствуя установлению изменения фенотипа M1 в М2 у указанного индивидуума.
26. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, для содействия установления изменению M1 в М2.
27. Применение по варианту реализации 26, которое индуцирует апоптоз клеток М1-макрофагов, способствует дифференцировке клеток М2-макрофагов или и то, и другое, тем самым способствуя установлению изменения фенотипа M1 в М2.
28. Способ модуляции уровня Th1-цитокина и/или уровня Th2-цитокина у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает уровни интерферона-гамма (ИФН-γ), фактора некроза опухоли-α (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки, повышает уровень ИЛ-10, высвобождаемого из Th2-клетки или и то, и другое, посредством чего модулируется уровень Th1-цитокина и/или Th2-цитокина у указанного индивидуума.
29. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для модуляции уровня Th1-цитокина и/или уровень Th2-цитокина.
30. Применение по варианту реализации 29, которое уменьшает уровни интерферона-гамма (ИФН-γ), фактора некроза опухоли-α (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки, увеличивает уровень ИЛ-10, высвобождаемого из Th2-клетки, или и то, и другое, посредством чего модулируются уровни Th1- и Th2-цитокинов.
31. Способ уменьшения или подавления активности сигнального пути NFκB у индивидуума, нуждающегося в этом, путем введения на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей терапевтически эффективное количество по меньшей мере одной ранпирназы и/или терапевтически эффективное количество по меньшей мере одной амфиназы, при этом введение уменьшает или подавляет активность сигнального пути NFκB у указанного индивидуума.
32. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу для уменьшения или подавления активности сигнального пути NFκB.
33. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28 или 31 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32, при этом по меньшей мере одна ранпирназа содержит аминокислотную последовательность SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26; последовательность, обладающую идентичностью аминокислотной последовательности по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% к SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26; или последовательность, обладающую идентичностью аминокислотной последовательности от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 97%, от приблизительно 80% до приблизительно 97%, от приблизительно 85% до приблизительно 97%, от приблизительно 90% до приблизительно 97% или от приблизительно 95% до приблизительно 97% к SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №; 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26.
34 Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30, 32 или 33, при этом по меньшей мере одна ранпирназа содержит аминокислотную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID N2: 25 или SEQ ID №: 26; или аминокислотную последовательность, содержащую не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11,12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26; или аминокислотную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26; или аминокислотную последовательность, содержащую не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 1, SEQ ID №: 2, SEQ ID №: 3, SEQ ID №: 4, SEQ ID №: 5, SEQ ID №: 6, SEQ ID №: 7, SEQ ID №: 8, SEQ ID №: 9, SEQ ID №: 10, SEQ ID №: 11, SEQ ID №: 12, SEQ ID №: 13, SEQ ID №: 14, SEQ ID №: 15, SEQ ID №: 16, SEQ ID №: 17, SEQ ID №: 18, SEQ ID №: 19, SEQ ID №: 20, SEQ ID №: 21, SEQ ID №: 22, SEQ ID №: 23, SEQ ID №: 24, SEQ ID №: 25 или SEQ ID №: 26.
35. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31, 33 или 34 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-34, при этом по меньшей мере одна амфиназа содержит аминокислотную последовательность SEQ ГО №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39; или последовательность, обладающую идентичностью аминокислотной последовательности по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98% или по меньшей мере 99% к SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39; или последовательность, обладающую идентичностью аминокислотной последовательности в диапазоне от приблизительно 75% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 85% до приблизительно 100%, от приблизительно 90% до приблизительно 100%, от приблизительно 95% до приблизительно 100%, от приблизительно 75% до приблизительно 99%, от приблизительно 80% до приблизительно 99%, от приблизительно 85% до приблизительно 99%, от приблизительно 90% до приблизительно 99%, от приблизительно 95% до приблизительно 99%, от приблизительно 75% до приблизительно 97%, от приблизительно 80% до приблизительно 97%, от приблизительно 85% до приблизительно 97%, от приблизительно 90% до приблизительно 97% или от приблизительно 95% до приблизительно 97% к SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39.
36. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-35 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-35, при этом по меньшей мере одна амфиназа содержит аминокислотную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39; или аминокислотную последовательность, содержащую не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 смежных делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39; или аминокислотную последовательность, содержащую по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39; или аминокислотную последовательность, содержащую не более 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 не являющихся смежными делеций, вставок и/или замен в аминокислотной последовательности по сравнению с SEQ ID №: 27, SEQ ID №: 28, SEQ ID №: 29, SEQ ID №: 30, SEQ ID №: 31, SEQ ID №: 32, SEQ ID №: 33, SEQ ID №: 34, SEQ ID №: 35, SEQ ID №: 36, SEQ ID №: 37, SEQ ID №: 38 или SEQ ID №: 39.
37. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-36 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-36, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовирусной активностью, которая уменьшает или подавляет уровень вируса или титр вируса у индивидуума.
38. Способ или применение по варианту реализации 37, при это введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет уровень вируса или титр вируса у индивидуума по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет уровень вируса или титр вируса у индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
39. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-38 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-38, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовирусной активностью, которая уменьшает или подавляет репликацию вируса.
40. Способ или применение по варианту реализации 39, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет репликацию вируса по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет репликацию вируса в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
41. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-40 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-40, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовирусной активностью, которая уменьшает или подавляет синтез белка в по меньшей мере одной клетке индивидуума.
42. Способ или применение по варианту реализации 41, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет синтез белка по меньшей мере в одной клетке индивидуума по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет синтез белкам по меньшей мере в одной клетке индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
43. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-42 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-42, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовирусной активностью, которая уменьшает или подавляет уровень тРНК по меньшей мере одной клетке индивидуума.
44. Способ или применение по варианту реализации 43, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке индивидуума по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке индивидуума в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
45. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-44 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-44, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая уменьшает уровень индуцирующей воспаление молекулы.
46. Способ или применение по варианту реализации 45, при этом индуцирующая воспаление молекула представляет собой вещество Р (SP), пептид, связанный с геном кальцитонина (CGRP), глутамат или их комбинацию.
47. Способ или применение по варианту реализации 45 или варианту реализации 46, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет уровень указанной индуцирующей воспаление молекулы по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет уровень индуцирующей воспаление молекулы в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
48. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-47 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-47, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая уменьшает уровень индуцирующего воспаление простагландина.
49. Способ или применение по варианту реализации 48, при этом указанный индуцирующий воспаление простагландин представляет собой 15dPGJ2.
50. Способ или применение по варианту реализации 48 или варианту реализации 49, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет уровень индуцирующего воспаление простагландина по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или уменьшает или подавляет уровень индуцирующего воспаление простагландина в диапазоне, например, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
51. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-50 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-50, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая стимулирует или улучшает активность сигнального пути PPAR.
52. Способ или применение по варианту реализации 51, при этом активность указанного сигнального пути PPAR представляет собой активность сигнального пути PPAR-α, активность сигнального пути PPAR-δ, активность сигнального пути PPAR-γ или их комбинацию.
53. Способ или применение по варианту реализации 51 или варианту реализации 52, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы стимулирует или улучшает активность сигнального пути PPAR по меньшей мере на 5%, по меньшей мере на 15%, по меньшей мере на 25%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%; или стимулирует или улучшает активность сигнального пути PPAR в диапазоне от приблизительно 5% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 25% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 80% до приблизительно 90%, от приблизительно 25% до приблизительно 80%, от приблизительно 50% до приблизительно 80%, от приблизительно 60% до приблизительно 80%, от приблизительно 70% до приблизительно 80%, от приблизительно 25% до приблизительно 70%, от приблизительно 50% до приблизительно 70%, от приблизительно 25% до приблизительно 60%, от приблизительно 50% до приблизительно 60% или от приблизительно 25% до приблизительно 50%.
54. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-53 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-53, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая способствует установлению изменению фенотипа M1 в М2.
55. Способ или применение по варианту реализации 53, при этом указанное установление изменения фенотипа M1 в М2 представляет собой индукцию апоптоза клеток М1-макрофагов, содействие дифференцировке клеток М2-макрофагов или их комбинацию.
56. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-55 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-55, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая модулирует уровень Th1-цитокина и/или Th2-цитокина.
57. Способ или применение по варианту реализации 56, при этом модуляция уровня указанного Th1-цитокина и/или указанного Th2-цитокина включает уменьшение уровня интерферона-гамма (ИФН-γ), фактора некроза опухоли-альфа (ФНО-α), интерлейкина-1b (ИЛ-1b), интерлейкина-12 (ИЛ-12) или их комбинации, высвобождаемой из Th1-клетки, увеличение уровня ИЛ-10, высвобождаемого из Th2-клетки, или их комбинацию.
58. Способ или применение по варианту реализации 56 или варианту реализации 57, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90% или уменьшает или подавляет уровень ИФН-γ, ФНО-α, ИЛ-1b, ИЛ-12 или их комбинации, высвобождаемой из Th1-клетки, в диапазоне от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
59. Способ или применение по любому одному из вариантов реализации 56-58, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы увеличивает или улучшает уровень ИЛ-10, высвобождаемого из Th2-клетки, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 35%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90% или по меньшей мере на 95%; или увеличивает или улучшает уровень ИЛ-10, высвобождаемого из Th2-клетки, в диапазоне от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
60. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-59 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-59, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы обладает противовоспалительной активностью, которая уменьшает или подавляет активность сигнального пути NFκB.
61. Способ или применение по варианту реализации 60, при этом введение или применение по меньшей мере одной ранпирназы и/или по меньшей мере одной амфиназы уменьшает или подавляет указанную активность сигнального пути NFκB по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90%; или уменьшает или подавляет активность сигнального пути NFκB в диапазоне от приблизительно 5% до приблизительно 100%, от приблизительно 10% до приблизительно 100%, от приблизительно 20% до приблизительно 100%, от приблизительно 30% до приблизительно 100%, от приблизительно 40% до приблизительно 100%, от приблизительно 50% до приблизительно 100%, от приблизительно 60% до приблизительно 100%, от приблизительно 70% до приблизительно 100%, от приблизительно 80% до приблизительно 100%, от приблизительно 10% до приблизительно 90%, от приблизительно 20% до приблизительно 90%, от приблизительно 30% до приблизительно 90%, от приблизительно 40% до приблизительно 90%, от приблизительно 50% до приблизительно 90%, от приблизительно 60% до приблизительно 90%, от приблизительно 70% до приблизительно 90%, от приблизительно 10% до приблизительно 80%, от приблизительно 20% до приблизительно 80%, от приблизительно 30% до приблизительно 80%, от приблизительно 40% до приблизительно 80%, от приблизительно 50% до приблизительно 80% или от приблизительно 60% до приблизительно 80%, от приблизительно 10% до приблизительно 70%, от приблизительно 20% до приблизительно 70%, от приблизительно 30% до приблизительно 70%, от приблизительно 40% до приблизительно 70% или от приблизительно 50% до приблизительно 70%.
62. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-61 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-61, при этом указанную фармацевтическую композицию получают для введения офтальмологическим путем.
63. Способ или применение по варианту реализации 62, при этом указанная фармацевтическая композиция дополнительно содержит по меньшей мере один фармацевтически приемлемый носитель и необязательно по меньшей мере один фармацевтически приемлемый компонент.
64. Способ или применение по варианту реализации 62 или варианту реализации 63, при этом офтальмологический состав представляет собой жидкий состав, коллоидный состав, полутвердый состав или твердый состав.
65. Способ или применение по любому одному из вариантов реализации 62-64, при этом указанный офтальмологический состав вводят посредством окулярной инстилляции, окулярной ирригации, внутриглазной инъекции, интракорнеальной инъекции, интравитреальной инъекции или субконъюнктивальной инъекции.
66. Способ или применение по любому одному из вариантов реализации 62-64, при этом указанный офтальмологический состав представляет собой систему для доставки с контролируемым высвобождением.
67. Способ или применение по варианту реализации 66, при этом указанная система для доставки с контролируемым высвобождением представляет собой состав с пролонгированным высвобождением или состав с замедленным высвобождением.
68. Способ или применение по любому одному из вариантов реализации 62-64, при этом указанный офтальмологический состав представляет собой глазной имплантат, офтальмологический имплантат, пробку, вставляемую в слезный канал, внутриглазной имплантат, интракорнеальный имплантат или субконъюнктивальный имплантат.
69. Способ по любому одному из вариантов реализации 1, 3, 4, 6, 8 или 10-16, 18, 19, 21, 22, 24, 25, 28, 31 или 33-68 или применение по любому одному из вариантов реализации 2, 3, 5, 7 или 9-15, 17, 18, 20, 21, 23, 24, 26, 27, 29, 30 или 32-68, в котором указанная ранпирназа содержит N-концевую блокированную пироглутаминовую кислоту или пирролидонкарбоновую кислоту.
70. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, в качестве лекарственного средства для лечения вирусного конъюнктивита.
71. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, в качестве лекарственного средства для уменьшения или подавления репликации вируса, инфицирующего индивидуума.
72. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, в качестве лекарственного средства для уменьшения или подавления синтеза белка по меньшей мере в одной клетке индивидуума.
73. Применение фармацевтической композиции, содержащей по меньшей мере одну ранпирназу и/или по меньшей мере одну амфиназу, в качестве лекарственного средства для уменьшения или подавления уровня тРНК по меньшей мере в одной клетке индивидуума.
ПРИМЕРЫ
[0141] Приведенные далее неограничивающие примеры предложены в иллюстративных целях только для того, чтобы облегчить более полное понимание примеров рассматриваемых в настоящее время вариантов реализации. Эти примеры не следует понимать как ограничивающие любые варианты реализации, описанные в настоящем описании, в том числе и относящиеся к ранпирназе, амфиназе, составам, содержащим ранпирназу и/или амфиназу, а также способы и применения для лечения вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшения уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействия установлению изменения фенотипа M1 в М2, модуляции Th1- и Th2-цитокинов и/или уменьшения или подавления сигнала NFκB-пути с применением ранпирназы, амфиназы или композиции, содержащей ранпирназу и/или амфиназу.
Пример 1
Противовирусное действие ранпирназы in vitro
[0142] Противовирусную активность ранпирназы оценивали с применением трех анализов in vitro. В каждом анализе для инфицирования клеток применяли аденовирус 5 человека (штамм AD5 NYS №98-1836) или аденовирус 8 человека (штамм 13306 Ad8) для определения того, может ли ранпирназа ингибировать цитопатические действия вируса в инфицированных клетках и/или может ли она уменьшать количество вирусов, полученных из таких инфицированных клеток.
[0143] Для оценки цитотоксичности in vitro проводили как регрессионный анализ цитопатического действия вируса (СРЕ), так и анализ на определение жизнеспособности клеток по оценке интенсивности поглощения лизосом, окрашенных нейтральным красным, так, как это по существу описано в публикации Repetto, et al., Neutral Red Uptake Assay for the Estimation of Cell Viability/Cytotoxicity, Nat. Protoc. 3: 1125-1131 (2008), содержание которой полностью включено в настоящее описание посредством ссылки. В 96-луночные планшеты высевали клетки МА-104 при концентрации 1×105 клеток/мл и инкубировали в течение ночи при 37°С в атмосфере 5% CO2. Ранпирназу серийно разводили в предписанной среде для исследования, применяя восемь полулогарифмических разведений. Каждое разведение добавляли к 5 лункам 96-луночного планшета с 80%-100% конфлюэнтными клетками, и затем три лунки с каждым из разведений инфицировали одним из двух вирусов для исследования. Две лунки оставляли неинфицированными в качестве контроля для определения токсичности. Шесть лунок в планшете оставляли в качестве контроля с неинфицированными, необработанными клетками, а шесть лунок в планшете инфицировали без обработки в качестве контроля с вирусом. 2',3'-дидезоксицитидин (ddC), известное активное соединение, анализировали параллельно в качестве положительного контроля. Планшеты для анализа инкубировали при 37°С в атмосфере 5% СО2. После того как при помощи микроскопических наблюдений было отмечено цитопатическое действие, проводили анализ уменьшения СРЕ, оценивая каждую лунку на цитопатическое действие по шкале 1-4 с оценкой 4, обозначающей, что во всех клетках наблюдали СРЕ. После завершения анализа уменьшения СРЕ, проводили анализ на определение поглощения лизосом, окрашенных нейтральным красным, заполняя каждую из лунок 0,011% (м/об.) нейтральным красным, прижизненным красителем. Затем планшеты инкубировали в течение 2 часов при 37°С в темноте. Раствор не включенного в клетки нейтрального красного удаляли из лунок, а включенный в клетки краситель затем элюировали, добавляя забуференный цитратом (по Сёренсену) этанол. Затем планшеты считывали на спектрофотометре при 540 нм для количественного определения нейтрального красного, поглощенного здоровыми клетками. Оптическую плотность исследуемых лунок преобразовывали в процент от контроля с клетками и нормировали к контролям с вирусом.
[0144] Концентрацию соединения для исследования, необходимую для ингибирования СРЕ на 50% или уменьшения поглощения нейтрального красного в клетках на 50% (ЕС50), рассчитывали методом регрессионного анализа. Токсичность соединения без присутствия вируса аналогичным образом рассчитывали по неинфицированным лункам, обработанным соединениями для исследования, по сравнению с контролями с необработанными клетками. Концентрацию соединения, которая бы вызывала 50% цитотоксических действий при отсутствии вируса (СС50), оценивали методом линейного регрессионного анализа. Индекс избирательности (SI) представляет собой величину СС50, деленную на ЕС50. Анализы повторяли с применением четырех 10-кратных разведений для проверки неэффективных результатов. В том случае, когда наблюдали противовирусную активность, применяли формат анализа на определение CPE/поглощения нейтрального красного с внесением в лунки планшета восемь полулогарифмических разведений в трех повторах, после чего из этих лунок собирали надосадочную жидкость для анализа на определение патогенного вируса, применяя анализ уменьшения урожая вируса в трех повторах для подтверждения и количественного определения противовирусной активности ранпирназы.
[0145] Анализ уменьшения урожая вируса применяли для определения фактических количеств вируса в присутствии и отсутствии указанного соединения для исследования; это подтверждающий анализ на определение противовирусной активности. После инкубации в течение 5 дней при 37°С в инкубаторе, продувающимся 5% СО2 (время, когда в контроле с инфицированными вирусом клетками наблюдали максимальную величину СРЕ), из каждой лунки для исследования удаляли аликвоту надосадочной жидкости. Репликатные лунки, содержащие каждую концентрацию соединения или контроля, объединяли и замораживали при -80°С. Образцы размораживали и разбавляли 10-кратным серийным разведением. Затем 100 мкл аликвоты каждого из разведений вносили в 4 репликатные лунки 96-луночных планшетов, засеянных соответствующими клетками для каждого штамма вируса. Планшеты инкубировали так, как это было указано выше до тех пор, пока СРЕ вируса не достигало своей конечной точки, затем каждую лунку оценивали с применением микроскопа по наличию СРЕ вируса. Титр вируса определяли на основе указанной конечной точки, применяя метод Рида-Мюнха. Лунки для исследования сравнивали с лунками, содержащими контроль с вирусом, а концентрацию соединения, необходимую для уменьшения урожая вируса на 90% или 1 log10 (ЕС90), рассчитывали методом регрессионного анализа.
[0146] Эксперименты показали, что было обнаружено, что ранпирназа не ингибирует любой из исследованных аденовирусов, независимо от применяемого анализа на определение противовирусной активности (Таблица 1). Например, более 100 мкг/мл ранпирназы требовалось для достижения ЕС50 в анализе на определение уменьшения СРЕ для клеток, инфицированных как Ad5, так и Ad8. Это контрастирует с ddC, для которого была достигнута ЕС50 при концентрации 2,1 мкг/мл. Аналогичным образом, этот анализ показал, что ранпирназа демонстрирует значимо высокую цитотоксичность по сравнению с ddC. Не является неожиданным то, что значения SI для ранпирназы были очень неудовлетворительными, в то время как значения для ddC были очень хорошими (0 в сравнении с >2400). Аналогичные результаты наблюдали в анализе на определение жизнеспособности клеток по оценке интенсивности поглощения лизосом, окрашенных нейтральным красным (Таблица 1).
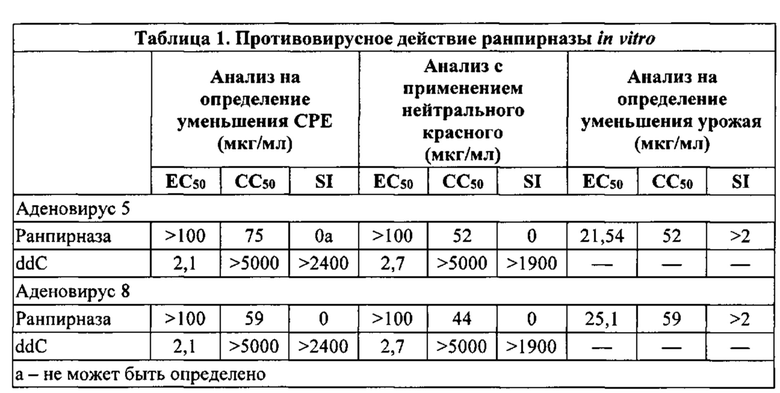
[0147] Действия описанной в настоящем документе ранпирназы или амфиназы in vitro, на другие серотипы аденовируса можно оценить способом, аналогичным описанному выше. Другие серотипы аденовируса включают, без ограничений, серотип 3 аденовируса В человека (Ad3), серотип 7 аденовируса В человека (Ad7), серотип 11 аденовируса В человека (Ad11), серотип 13 аденовируса D человека (Ad13), серотип 19 аденовируса D человека (Ad19), серотип 37 аденовируса D человека (Ad37) или серотип 4 аденовируса Е человека (Ad4). Кроме того, действия описанной в настоящем документе ранпирназы или амфиназы in vivo на другие вирусы можно оценить способом, аналогичным описанному выше. Другие вирусы включают, без ограничений, вирус простого герпеса (HSV), вирус ветряной оспы (VZV), пикорнавирус (энтеровирус 70, коксаки А24) или поксвирус (вирус контагиозного моллюска, осповакцины).
Пример 2
Цитотоксическое действие ранпирназы
[0148] Для подтверждения цитотоксического действия ранпирназы, анализ на определение уменьшения числа бляшек выполняли по существу так, как это описано, например, в публикации Romanowski, et al., The In Vitro and In Vivo Evaluation of ddC as a Topical Antiviral for Ocular Adnovirus Infections, Invest. Ophthalmol. Vis. Sci. 50: 5295-5299 (2009), которая полностью включено в настоящее описание посредством ссылки.
[0149] Для оценки цитотоксичности in vitro в 96-луночные планшеты высевали клетки А549 при концентрации 1×105 клеток/мл и инкубировали в течение ночи при 37°С в атмосфере 5% СО2. Проводили серийные разведения ранпирназы до концентраций 1,0 мкМ, 10 мкМ и 50 мкМ. После удаления среды для культивирования ткани 100 мкл каждого разведения добавляли к 3 лункам 96-луночного планшета с 80%-100% конфлюэнтными клетками. В качестве контроля в 6 лунок добавляли 100 мкл буфера для лизиса, содержащего 0,25% TRITON Х-100 (положительный контроль цитотоксичности), и в 6 лунок добавляли 100 мкл среды для культивирования ткани, не содержащей ранпирназу (отрицательный контроль цитотоксичности). Каждое лекарственное средство для исследования и лекарственное средство, представляющее собой контроль, инкубировали на монослоях А549 в течение двух дней при 37°С в атмосфере 5% СО2. Затем в каждую лунку добавляли аликвоту 100 мкл флуорометрического красителя, и указанные клетки инкубировали в течение 1 часа при 37°С в атмосфере 5% СО2. Флюорометрический краситель (ALAMARBLUE®, Invitrogen, Карлсбат, штат Калифорния) действует как индикатор окислительно-восстановительного потенциала, который восстанавливается до флуоресцентной формы метаболически активными живыми клетками. Затем флуоресценцию считывали при помощи планшета-ридера (Biotek Synergy 2, компания Biotek) с фильтром возбуждения 500/27 нм и фильтром излучения 620/40 нм при чувствительности 35. Цитотоксичность определяли по проценту оставшихся жизнеспособных клеток после воздействия на них ранпирназой (% цитотоксичности = 100 - [(медиана флуоресцентного лекарственного средства/медиана флуоресценции в отсутствие лекарственного средства)×100], где «лекарственное средство» представляло собой либо одну из трех концентраций ранпирназы, либо буфер для лизиса, а «отсутствие лекарственного средства» представляло собой отрицательный контроль. Наблюдаемые различия статистически оценивали с применение непараметрического дисперсионного анализа (ANOVA) по Краскелу-Уоллису и множественных сравнений Дункана, а значимость устанавливали на уровне достоверности Р≤0,05.
[0150] Эксперименты показали, что ранпирназа вызывала значимую цитотоксичность в клетках А549 через 2 дня обработки (Таблица 2). Например, обработка клеток А549 50 мкМ ранпирназой приводила к цитотоксичности приблизительно 75% клеток, что на 7% ниже, чем обработка буфером для лизиса, который служил положительным контролем. Хотя цитотоксичность снижалась приблизительно до 66% для 10 мкМ ранпирназы и приблизительно до 62% для 1 мкМ ранпирназы, эта степень цитотоксичности по-прежнему остается значимо высокой.
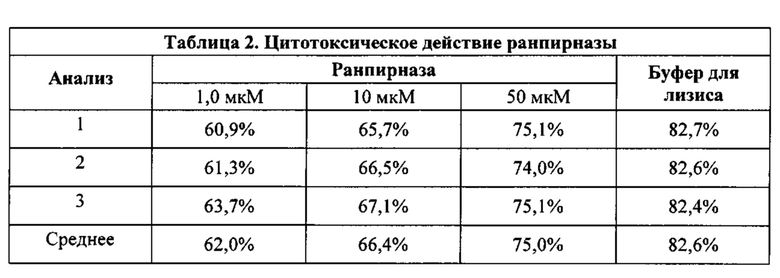
[0151] Чтобы еще больше расширить этот анализ для оценки того, при какой концентрации ранпирназа не является цитотоксической, был проведен дополнительный анализ на определения уменьшения числа бляшек при более низких концентрациях ранпирназы. Эти эксперименты проводились так, как это было описано выше, за исключением того, что применяемые концентрации ранпирназы составляли 0,001 мкМ, 0,01 мкМ, 0,1 мкМ, 1,0 мкМ, 10 мкМ и 50 мкМ.
[0152] Эксперименты подтвердили, что ранпирназа вызывала значимую цитотоксичность в клетках А549 через 2 дня обработки (Таблица 3). Например, обработка клеток А549 50 мкМ ранпирназой приводила к цитотоксичности приблизительно 87% клеток, что представляло собой такую же степень цитотоксичности, которую наблюдали при обработке буфером для лизиса, который служил положительным контролем. Хотя цитотоксичность снизилась приблизительно до 33% при обработке 10 мкМ ранпирназой и приблизительно до 15% при обработке 1 мкМ ранпирназой, такая степень цитотоксичности по-прежнему остается умеренно высокой. Более низкие степени цитотоксичности наблюдали при обработке 0,001 мкМ, 0,01 мкМ и 0,1 мкМ ранпирназой, находящейся в диапазоне от 3,2% до 7,4%. Тем не менее, поскольку любая степень цитотоксичности выше 2,5% считается проблематичной, даже при этих более низких концентрациях ранпирназа проявляла неудовлетворительную степень цитотоксичности. Это усугубляется тем фактом, что эти более низкие концентрации также представляют собой суб-терапевтические количества.
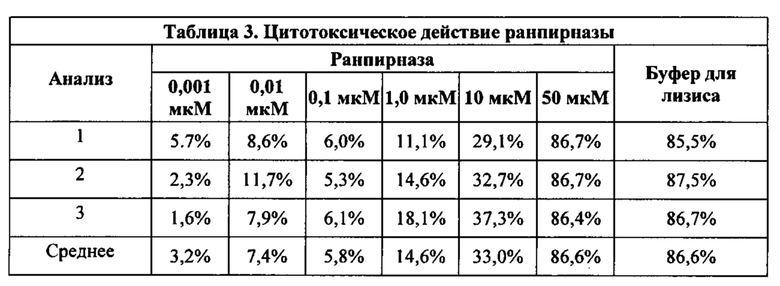
Пример 3
Противовирусные действия ранпирназы in vivo
[0153] Несмотря на неудовлетворительный профиль цитотоксичности ранпирназы, ее противовирусную активность оценивали in vivo с применением модели репликации вируса в глазе кролика. См., например, публикацию Romanowski, et al., The In Vitro and In Vivo Evaluation of ddC as a Topical Antiviral for Ocular Adenovirus Infections, Invest. Ophthalmol. Vis. Sci. 50: 5295-5299 (2009), которая полностью включена в настоящее описание посредством ссылки.
[0154] Для проведения данного анализа in vivo, 25 NZW-кроликов подвергали анестезии при помощи кетамина и ксилазина для общей анестезии и пропаракаина для местной анестезии. Затем каждому кролику локально инокулировали 50 мкл серотипа Ad5 аденовируса (3×107 БОЕ/мл) в оба глаза после скарификации эпителия роговицы (12 накрест штрихованных порезов 25 стерильными иглами). Кроликам закрывали глаза, и глаза нежно протирали в течение 5 секунд, чтобы обеспечить контакт вируса со всей поверхностью глаз. Инокуляция обоих глаз позволяла уменьшить количество животных, не подвергая сомнению статистическую достоверность. Спустя 24 часа кролики были случайным образом распределены в одну из пяти групп для местного лечения: (1А) 25 мкМ ранпирназа (n=5), (1 В) 2,5 мкМ ранпирназа (n=5), (1С) 0,25 мкМ ранпирназа (n=5), (1D) 0,9% солевой раствор в качестве отрицательного контроля (n=5) и (CDV) 0,5% цидофовир в качестве положительного контроля (n=4). Оба глаза контрольных кроликов обрабатывали ранпирназой и солевым раствором восемь раз в день на протяжении 9 дней, тогда как оба глаза кроликов в группе с цидофовиром обрабатывали два раза в день на протяжении 7 дней. Все растворы для местного применения (37 мкл капель) вводили при помощи электронной пипетки (EDP; Rainin, Окленд, штат Калифорния), установленной в режиме многократного дозирования. Забор мазков из глаз для восстановления аденовируса, полученного из слезной пленки и поверхностей роговицы и конъюнктивы после местной анестезии с применением пропаракаина, проводили по меньшей мере в течение 1 часа после введения окончательной дозы на 0, 1, 3, 4, 5, 7, 9, 11 и 14 день после инокуляции. Окулярные образцы, полученные из каждого глаза, по отдельности помещали в пробирки, содержащие 1 мл среды, и замораживали при -70°С до момента проведения анализа на определение числа вирусных бляшек.
[0155] У животных анализировали раздражение глаз с применением шкалы Драйзе для окулярных поражений. Классификация раздражения глаз оценивали у каждого кролика по двум глазам на день 3 и день 9, применяя общую оценку максимального среднего (MMTS, Таблица 4). См., например, публикацию Kay and Calandra, Interpretation of Eye Irritation Tests, J. Soc. Cos. Chem. 13: 281-289 (1962), содержание которой полностью включено в настоящее описание посредством ссылки. Показатель MMTS был следующим: 0,0-0,5, нет раздражения (N); 0,6-2,5, практически нет раздражения (PN); 2,6-15,0, минимальное раздражение (M1); 15,1-25,0, легкое раздражение (М2); 25,1-50,0, умеренное раздражение (М3); 50,1-80,0, серьезное раздражение (S); 80,1-100,0, чрезвычайное раздражение (Е); и 100,1-110,0, максимальное раздражение (MX).
[0156] Оценка раздражения глаз показана в Таблице 4. Ранпирназа также продемонстрировала зависимую от дозы токсичность в отношении окулярной ткани по сравнению с солевым раствором (отрицательный контроль) и CDV (положительный контроль) в окулярной модели кролика Ad5/NZW. Токсичность выражалась через повышенное воспаление поверхности глаз (покраснение конъюнктивы, хемоз и выделения), а токсичность в отношении роговицы проявлялась через помутнение роговицы. Лечение 25 мкМ ранпирназой продемонстрировало наибольшую токсичность в отношении окулярных тканей, за которой следовала концентрация ранпирназы в 2,5 мкМ. Концентрация ранпирназы в 0,25 мкМ продемонстрировала аналогичные оценки по шкале Драйзе для отрицательного и положительного противовирусного контроля. Эти экспериментальные результаты показывают, что лечение 0,25 мкМ ранпирназой показало отсутствие раздражения глаз по сравнению с контролем, представляющим собой как солевой раствор, так и цидофовир.
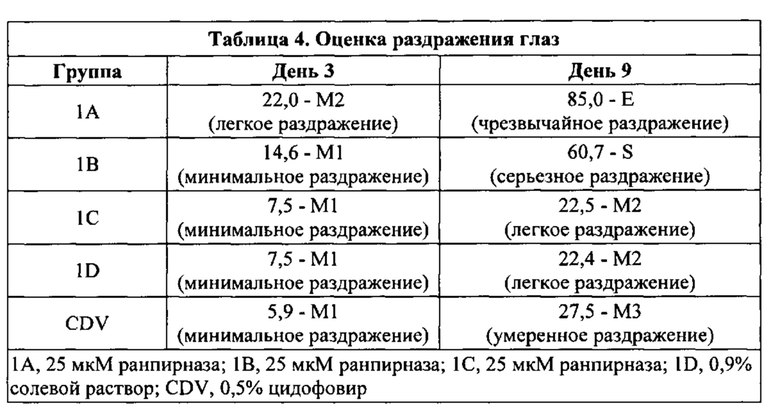
[0157] Животных также анализировали на 21 день для определения закупорки слезноносового протока, проводя тест с применением красителя Jones. На 21 день в каждый глаз капали каплю флюоресцеина натрия и измеряли время до появления красителя в ипсилатеральной ноздре. Считалось, что в глазе, при закапывании в который краситель не появлялся в ипсилатеральной ноздре через 5 минут, присутствует закупорка слезоносового протока. Этот анализ показал, что у кроликов, которые не получали лечение ранпирназой вне зависимости от ее концентрации, в результате наблюдали закупорку слезоносового протока. Аналогичным образом, у кроликов в группе с отрицательным и положительным контролем, также не наблюдали окклюзионные протоки.
[0158] Окулярные образцы анализировали на определение титра Ad5, проводя анализ на определение уменьшения числа бляшек. Образцы разбавляли в соотношении 1:10, и эти разведения инокулировали в дупликатные лунки 24-луночного мультипланшета, содержащего монослои А549. Вирус адсорбировали в течение 3 часов при 37°С в атмосфере 5% СО2-водяной пар и без постоянного раскачивания. После адсорбции в каждую лунку добавляли 1 мл среды плюс 0,5% метилцеллюлозы и указанные планшеты инкубировали при 37°С в атмосфере 5% СО2-водяной пар. Через 7 дней клетки окрашивали при помощи 0,5% генциановиолета, а число бляшек подсчитывали с применением препаровальной лупы (25-кратное увеличение). Затем рассчитывали титр вируса, и его выражали в бляшкообразующих единицах на миллилитр (БОЕ/мл). Данные, полученные в таком исследовании, анализировали с применением дисперсионного анализа (ANOVA) с использованием парных сравнений Фишера и Х2-анализов с применением статистического программного обеспечения True Epistat и/или Minitab. Значимость устанавливали на уровне достоверности Р≤0,05.
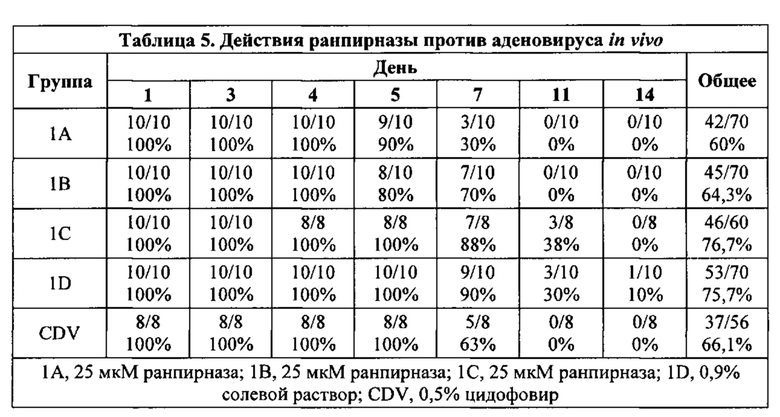
[0159] Оценка цитотоксичности показана в Таблице 5. Ранпирназа продемонстрировала зависимую от дозы противовирусную эффективность по сравнению с представляющим собой контроль солевым раствором (отрицательный) в окулярной модели кролика Ad5/NZW. Лечение с применением 25 мкМ ранпирназы продемонстрировало наибольшую противовирусную эффективность, за которой следовала концентрация ранпирназы в 2,5 мкМ. Эти концентрации ранпирназы демонстрировали аналогичную противовирусную активность по сравнению с положительным противовирусным контролем, 0,5% цидофовиром. Лечение с применением 0,25 мкМ ранпирназы продемонстрировало некоторую противовирусную эффективность, однако оно было столь же эффективным, как и более высокие концентрации Ранпирназа и 0,5% цидофовир.
[0160] Действия описанной в настоящем документе ранпирназы или амфиназы in vivo на другие серотипы аденовируса можно оценить способом, аналогичным описанному выше. Другие серотипы аденовируса включают, без ограничений, серотип 3 аденовируса В человека (Ad3), серотип 7 аденовируса В человека (Ad7), серотип 11 аденовируса В человека (Ad11), серотип 8 аденовируса D человека (Ad8), серотип 13 аденовируса D человека (Ad13), серотип 19 аденовируса D человека (Ad19), серотип 37 аденовируса D человека (Ad37) или серотип 4 аденовируса Е человека (Ad4). Кроме того, действия описанной в настоящем документе ранпирназы или амфиназы in vivo на другие вирусы можно оценить способом, аналогичным описанному выше. Другие вирусы включают, без ограничений, вирус простого герпеса (HSV), вирус ветряной оспы (VZV), пикорнавирус (энтеровирус 70, коксаки А24) или поксвирус (вирус контагиозного моллюска, осповакцины).
[0161] В заключение следует понимать, что хотя аспекты настоящего изобретения отмечены ссылкой на конкретные варианты реализации, специалист в данной области техники легко поймет, что эти описанные варианты реализации являются лишь иллюстрацией принципов описанного в настоящем документе объекта изобретения. Следовательно, следует понимать, что описанный объект изобретения не ограничивается конкретным соединением, композицией, статьей, устройством, методикой, протоколом и/или реагентом и т.д., описанным в настоящем документе до тех пор, пока это явным образом не указано. Кроме того, специалисты в данной области техники поймут, что некоторые изменения, модификации, перестановки, изменения, дополнения, исключения и их подкомбинации можно осуществить в соответствии с инструкциями, изложенными в настоящем документе, без отступления от сущности настоящего изобретения. Поэтому предполагается, что прилагаемая формула изобретения и формула изобретения, приведенная ниже, интерпретируются как включающие все такие изменения, модификации, перестановки, изменения, дополнения, исключения и подкомбинации, которые соответствуют сущности настоящего изобретения и входят в объем настоящего изобретения.
[0162] Некоторые варианты реализации настоящего изобретения, описанные в настоящем документе, включают наилучший способ, известный авторам настоящего изобретения, для выполнения настоящего изобретения. Разумеется, что вариации в этих описанных вариантах реализации станут очевидными для специалистов в данной области техники после ознакомления с предшествующим описанием. В настоящем изобретении предполагается, что квалифицированные специалисты используют такие соответствующие варианты, и авторы настоящего изобретения предполагают, что настоящее изобретение можно осуществить иначе, чем это конкретно описано в настоящем документе. Соответственно, настоящее изобретение включает все модификации и эквиваленты объекта настоящего изобретения, указанного в формуле изобретения, прилагаемой к настоящему документу, как это разрешено подлежащим применению законодательством. Кроме того, любая комбинация вышеописанных вариантов реализации во всех возможных их вариациях охватывается настоящим изобретением до тех пор, пока контекст явным образом не указывает на иное.
[0163] Группировки альтернативных вариантов реализации, элементов или стадий настоящего изобретения являются ограничивающими объектами. Каждый член группы может упоминаться и заявляться индивидуально или в любой комбинации с другими членами группы, описанными в настоящем документе. Предполагается, что по меньшей мере один член группы можно включить или удалить из группы по причинам, связанным с удобством и/или патентоспособностью. В том случае, когда происходит такое включение или удаление, считается, что описание содержит группу, модифицированную таким образом, чтобы выполнить письменное описание всех групп Маркуша, представленных в прилагаемой формуле изобретения.
[0164] До тех пор, пока не указано иное, все числа, выражающие характеристику, элемент, количество, параметр, свойство, термин и т.д., применяемые в настоящем описании и формуле изобретения следует понимать как модифицированные во всех случаях термином «примерно». В контексте настоящего изобретения термин «примерно» означает, что характеристика, элемент, количество, параметр, свойство или термин, квалифицированный таким образом, включают в себя диапазон от плюс/минус десять процентов выше и ниже значения указанного признака, элемента, количества, параметра, свойства или термина. Соответственно до тех пор, пока не указано обратное, числовые параметры, указанные в описании и прилагаемой формуле изобретения, являются приблизительными, и они могут варьироваться. Например, поскольку приборы для масс-спектрометрии могут незначительно варьироваться при определении массы данного анализируемого вещества, термин «примерно» в контексте массы иона или соотношения масса/заряда иона относится к +/- 0,50 единиц атомной массы. По меньшей мере, и не в качестве попытки ограничить применение доктрины эквивалентов в объеме формулы изобретения, каждую числовую индикацию следует по меньшей мере интерпретировать с учетом количества зарегистрированных значащих цифр и применения методов обычного округления.
[0165] Применение терминов «можно» (may) или «может» (can) в отношении варианта реализации или аспекта варианта реализации также несет в себе альтернативное значение «можно не» (may not)» или «не может» (cannot). Таким образом, если в настоящем описании описано, что вариант реализации или аспект варианта реализации можно включить или он может быть включен как часть объекта настоящего изобретения, тогда также явным образом подразумевается отрицательное ограничение или исключающее условие, что означает, что вариант реализации или аспект варианта реализации можно не включать или он может быть не включен как часть объекта настоящего изобретения. Аналогичным образом применение термина «необязательно» применительно к варианту реализации или аспекту варианта реализации означает, что такой вариант реализации или аспект варианта реализации можно включить как часть объекта настоящего изобретения или он может быть включен как часть объекта настоящего изобретения. Независимо от того, применяется ли такое отрицательное ограничение или исключающее условие, оно будет установлено, несмотря на то, упоминается ли отрицательное ограничение или исключающее условие в заявленном объекте изобретения или нет.
[0166] Несмотря на то, что числовые диапазоны и значения, определяющие широкий объем настоящего изобретения, являются приблизительными, числовые диапазоны и значения, указанные в конкретных примерах, приведены как можно точнее. Однако любой числовой диапазон или значение, тем не менее, содержит определенные погрешности, которые необязательно проистекают из стандартных отклонений, обнаруживаемых при их соответствующей проверке измерений. Упоминание числовых диапазонов и значений в настоящем документе просто предназначено для использования в качестве сокращенного метода индивидуальной ссылки для каждого отдельного числового значения, находящегося в пределах указанного диапазона. До тех пор, пока не указано иное, каждое индивидуальное значение числового диапазона включено в настоящее описание так, как если бы оно индивидуальным образом было описано в настоящем документе.
[0167] Формы единственного числа и аналогичные ссылки, применяемые в контексте описания настоящего изобретения (особенно в контексте последующей формулы изобретения), следует толковать как охватывающие как единичное, так и множественное число до тех пор, пока в настоящем документе не указано иное или оно явным образом противоречит контексту. Кроме того, порядковые индикаторы, такие как «первый», «второй», «третий» и т.д., применялись для того, чтобы различать идентифицированные элементы, и это не указывает или не подразумевает требуемое или ограниченное число таких элементов; и не указывает на конкретную позицию или порядок таких элементов до тех пор, пока явным образом не указано иное. Все способы, описанные в настоящем документе, можно выполнить в любом подходящем порядке до тех пор, пока не указано иное или оно явным образом противоречит контексту. Применение любого и всех предложенных в настоящем документе примеров или иллюстративных примеров (например, «таких как») предназначено просто для лучшего освещения настоящего изобретения, и не накладывает ограничение на объем настоящего изобретения, описанного далее. Ни одно из выражений настоящего описания не следует толковать как указание на любой незаявленный элемент, необходимый для практики настоящего изобретения.
[0168] Конкретные варианты реализации, описанные в настоящем документе, можно дополнительно ограничить в формуле изобретения, применяя выражения «состоящий из» или «по существу состоящий из». При применении в формуле изобретения, независимо от того, вносится ли он в поправку или добавляется в нее, переходный термин «состоящий из» исключает любой элемент, стадию или ингредиент, не указанный в формуле изобретения. Переходящий термин «по существу состоящий из» ограничивает объем пункта до определенных материалов или стадий и тех элементов, которые существенным образом не влияют на основную и новую характеристику(-ки). Варианты реализации настоящего изобретения, заявленные таким образом, по существу или явным образом описаны и включены в настоящий документ.
[0169] Все патенты, патентные публикации и другие публикации, на которые есть ссылка и которые идентифицированы в настоящем документе, индивидуально и явным образом полностью включены в настоящее описание посредством ссылки с целью описания и раскрытия, например, композиций и методик, описанных в таких публикациях, которые можно было бы применять в связи с настоящим изобретением. Эти публикации предоставлены исключительно для их описания с даты подачи настоящей заявки. Ничто в этом отношении не следует толковать как признание того, что авторы настоящего изобретения имеют право датировать задним числом такое описание в силу притязания или по любой другой причине. Все заявления о дате или представлении в отношении содержания этих документов основаны на информации, доступной для заявителей, и это не делает каких-либо допущений относительно правильности дат или содержания этих документов.
[0170] Наконец, терминология, применяемая в настоящем документе, служит для цели описания только конкретных вариантов реализации и она не предназначена для ограничения объема настоящего изобретения, который определяется исключительно формулой изобретения. Соответственно, настоящее изобретение не ограничено только тем, что представлено и описано.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ ГЛАЗА | 2016 |
|
RU2739392C2 |
| СПОСОБЫ И ПРОДУКТЫ ДЛЯ ЭКСПРЕССИИ БЕЛКОВ В КЛЕТКАХ | 2013 |
|
RU2711249C2 |
| АНТИТЕЛА ПРОТИВ PD-1 | 2015 |
|
RU2711141C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18А2 И ЕГО ПРИМЕНЕНИЕ | 2017 |
|
RU2793445C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ СНИЖЕНИЯ ИММУНОГЕННОСТИ С ПОМОЩЬЮ НЕ ПРИВОДЯЩИХ К ДЕПЛЕЦИИ В-КЛЕТОЧНЫХ ИНГИБИТОРОВ | 2020 |
|
RU2821892C2 |
| ВАКЦИНА | 2012 |
|
RU2640258C2 |
| ЛЕЧЕНИЕ РАКОВЫХ ЗАБОЛЕВАНИЙ С ПРИМЕНЕНИЕМ АНТИ-NKG2A СРЕДСТВ | 2015 |
|
RU2721271C2 |
| ЛЕЧЕНИЕ ВОСПАЛИТЕЛЬНЫХ, АУТОИММУННЫХ И НЕЙРОДЕГЕНЕРАТИВНЫХ НАРУШЕНИЙ ИММУННОДЕПРЕССИВНЫМИ ПОЛИПЕТИДАМИ, ЯВЛЯЮЩИМИСЯ ПРОИЗВОДНЫМИ ТАТ | 2013 |
|
RU2653754C2 |
| АНТИ-C5 АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2774716C2 |
| Нейтрализующие антитела к вирусу гриппа B и пути их применения | 2015 |
|
RU2711932C2 |
Изобретение относится к области биотехнологии. В настоящем описании описаны ранпирназа и амфиназа, композиции, содержащие ранпирназу и/или амфиназу, а также способы и применения для лечения вирусного конъюнктивита, эпидемического кератоконъюнктивита и/или фарингоконъюнктивальной лихорадки, уменьшения или подавления уровня вируса или титра вируса, уменьшения или подавления репликации вируса, уменьшения или подавления синтеза белка, уменьшения или подавления уровня тРНК, уменьшения или подавления уровня индуцирующей воспаление молекулы и/или индуцирующего воспаление простагландина, стимуляции или улучшения сигнала пути рецептора, активируемого пролифератором пероксисом (PPAR), содействия установлению изменения фенотипа M1 в М2, модуляции Th1- и Th2-цитокинов и/или уменьшения или подавления сигнала NFκB-пути с применением ранпирназы, амфиназы или композиции, содержащей ранпирназу и/или амфиназу. 17 з.п. ф-лы, 7 табл., 3 пр.
1. Способ лечения вирусного конъюнктивита у индивидуума, нуждающегося в этом, при этом указанный способ включает введение на поверхность конъюнктивы и/или глаза указанного индивидуума фармацевтической композиции, содержащей по меньшей мере одну ранпирназу, при этом однократная доза указанной композиции содержит по меньшей мере одну ранпирназу в количестве не более 15 мкг, и при этом указанная композиция приготовлена для введения один, два, три, четыре, пять или шесть раз в день, и причем введение уменьшает симптом, ассоциированный с вирусным конъюнктивитом, посредством чего происходит лечение указанного индивидуума.
2. Способ по п. 1, в котором указанный вирусный конъюнктивит представляет собой эпидемический кератоконъюнктивит, фарингоконъюнктивальную лихорадку, неспецифический спорадический фолликулярный конъюнктивит или хронический папиллярный конъюнктивит.
3. Способ по любому из пп. 1-2, в котором указанный вирусный конъюнктивит вызван аденовирусом В человека, аденовирусом D человека, аденовирусом Е человека или любой их комбинацией.
4. Способ по п. 3, в котором указанный аденовирус В человека представляет собой аденовирус B человека серотипа 3, аденовирус В человека серотипа 7, аденовирус В человека серотипа 11 или любую их комбинацию.
5. Способ по п. 3, в котором указанный аденовирус D человека представляет собой аденовирус D человека серотипа 8, аденовирус D человека серотипа 13, аденовирус D человека серотипа 19, аденовирус D серотипа 37 человека или любую их комбинацию.
6. Способ по п. 3, в котором указанный аденовирус Е человека представляет собой аденовирус Е человека серотипа 4.
7. Способ по любому из пп. 1-6, в котором введение по меньшей мере одной ранпирназы обеспечивает противовирусную активность, которая уменьшает или подавляет уровень вируса или титр вируса у индивидуума.
8. Способ по любому из пп. 1-6, в котором введение по меньшей мере одной ранпирназы обеспечивает противовирусную активность, которая уменьшает или подавляет репликацию вируса.
9. Способ по любому из пп. 1-6, в котором введение по меньшей мере одной ранпирназы обеспечивает противовирусную активность, которая уменьшает или подавляет синтез белка по меньшей мере в одной клетке индивидуума.
10. Способ по любому из пп. 1-6, в котором введение по меньшей мере одной ранпирназы обеспечивает противовирусную активность, которая уменьшает или подавляет уровень тРНК по меньшей мере в одной клетке индивидуума.
11. Способ по любому из пп. 1-10, в котором указанная фармацевтическая композиция приготовлена в виде офтальмологического состава для применения при введении офтальмологическим путем.
12. Способ по п. 11, в котором указанная фармацевтическая композиция дополнительно содержит по меньшей мере один фармацевтически приемлемый носитель и необязательно по меньшей мере один фармацевтически приемлемый компонент.
13. Способ по п. 11 или 12, в котором указанный офтальмологический состав представляет собой жидкий состав, коллоидный состав, полутвердый состав или твердый состав.
14. Способ по любому из пп. 11-13, в котором указанный офтальмологический состав вводят посредством окулярной инстилляции, окулярной ирригации, внутриглазной инъекции, интракорнеальной инъекции, интравитреальной инъекции или субконъюнктивальной инъекции.
15. Способ по любому из пп. 11-14, в котором указанный офтальмологический состав представляет собой систему для доставки с контролируемым высвобождением.
16. Способ по п. 15, в котором указанная система доставки с контролируемым высвобождением представляет собой состав с пролонгированным высвобождением или состав с замедленным высвобождением.
17. Способ по любому из пп. 11-16, в котором указанный офтальмологический состав представляет собой глазной имплантат, офтальмологический имплантат, пробку, вставляемую в слезный канал, внутриглазной имплантат, интракорнеальный имплантат или субконъюнктивальный имплантат.
18. Способ по любому из пп. 1-17, в котором указанная ранпирназа содержит N-концевую блокированную пироглутаминовую кислоту или пирролидонкарбоновую кислоту.
| WO 2015110429 A1, 30.07.2015 | |||
| US 8518399 B2, 27.08.2013 | |||
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ КОНЪЮНКТИВИТОВ | 1993 |
|
RU2093165C1 |
| US 20020151499 A1, 17.10.2002. | |||
Авторы
Даты
2020-10-01—Публикация
2016-09-25—Подача