Изобретение относится к области медицины, а именно к ревматологии, иммунологии и биотехнологии, и может быть использовано для совершенствования метода лечения ревматоидного артрита.
В патогенезе ревматоидного артрита (РА) ведущее значение имеют аутоиммунные реакции, в результате которых в организме человека продуцируются некоторые аномальные продукты клеток иммунной системы. К таким веществам относится ревматоидный фактор (РФ). Представляющий собой иммуноглобулины человека классов М, G, А, направленные против Fc-фрагмента IgG человека. Эти антитела в организме синтезируются плазматическими клетками синовиальной оболочки и оттуда попадают в кровь. Взаимодействуя с аутоантигеном, они образуют циркулирующие иммунные комплексы (ЦИК). Оседающие, главным образом, в синовиальной оболочке суставов. ЦИК вызывают повышение активности медиаторов воспаления, нарушают микроциркуляцию, активируют хемотаксис лейкоцитов и процессы фагоцитоза ЦИК лейкоцитами и макрофагами. В процессе фагоцитоза повреждаются лизосомы нейтрофилов и макрофагов, высвобождаются лизосомальные ферменты, которые разрушают клеточные структуры. Образуются новые аутоантигены и патологический процесс приобретает характер цепной реакции. Важное патогенетическое значение большинство авторов придают РФ класса IgG, так он составляет около 80% всех иммуноглобулинов человека и животных (Введение в иммунологию Цхалтубо-Кутаисское отделение грузинского научного общества иммунологов/Под. ред. Р.И. Сепиашвили - Цхалтубо-Кутаиси 1987 С.31.), (Bond A., Cooke А.С, Sumar N., Hay F.C. Glycosylation of IgG in the MRL/Ipr model of rheumatoid arthritis // Eur. Fed. Immunol. Soc. 10 th Meet., Edinburgh, 10-12 Sept., 1990: Abstr.-Edinburgh, 1990. - P. 103.).
В настоящее время определение РФ класса IgG в крови человека широко используется в медицинской диагностической практике, особенно для обследования пациентов с подозрением на ревматоидный артрит, для мониторинга течения РА, контроля эффективности проводимых лечебных мероприятий. Больные РА, имеющие высокий уровень РФ в крови, склонны к более агрессивному течению болезни и худшему исходу, чем слабоположительные по РФ. Высокий титр РФ ассоциируется с рядом аутоиммунных заболеваний и присутствием внесуставных проявлений и ревматических узлов (Новиков Д.К. Справочник по клинической иммунологии и аллергологии./ Д.К. Новиков - Минск: Беларусь, 1987. С. 223; Смердова М.А. Ревматоидный фактор в лабораторной диагностике /М.А. Смердова, Е.Ю.Косова /Информационный бюллетень Новости «Вектор-Бест» - 2000 - Т. 3, №17. - С. 5-7).
Таким образом, РФ принадлежит важнейшая роль в иммунопатогенезе развития ревматоидного артрита. Это диктует необходимость разработки и внедрения новых методов целенаправленной патогенетической терапии, способствующих непосредственной элиминации ревматоидного фактора из крови больных РА или угнетения его синтеза В -клетками.
Известен метод удаления указанных антител методом этапного плазмафереза, при котором проводится удаление плазмы больного в экстракорпоральном контуре малыми порциями по 300 мл с последующей инфузией пациенту изотонических солевых растворов и изоонкотических донорских белковых препаратов (Митысовская Н.П., Досин Ю.М., Лабань Ф.Н. и соавт.). Динамика иммунологических показателей больных ревматоидным артритом в процессе плазмафереза /Научно-практическая ревматология. - 2000. - №4. - С. 75.). Недостатком этого метода является его низкая избирательность и специфичность. При осуществлении такой процедуры вместе с ревматоидным фактором удаляются необходимые для организма альбумин, гормоны, нормальные иммуноглобулины, лекарственные препараты. Кроме того используемые белковые препараты являются чужеродными для организма, приводя к развитию аллергических реакций, дороги в цене, что затрудняют их широкому использованию.
Существует метод удаления ревматоидных факторов из крови путем пропускания ее через иммуносорбент, представляющий собой нерастворимый инертный носитель (агарозный гель в форме сефарозы CL-2B или сефарозы CL-4B), к которому после активации бромцианом ковалентно пришивается нативный или химически модифицированный иммуноглобулин G человека. Указанный способ имеет ряд недостатков. Сефароза имеет крайне высокую стоимость и поэтому не может найти широкого применения для приготовления иммуносорбентов в клинической практике. Бромциан, используемый для активации данного носителя, является высокотоксичным соединением, работа с ним представляет опасность для исследователя. При приготовлении сефарозы из агарозы существенная часть активных групп носителя, к которым впоследствии присоединяется иммуноглобулин G, блокируется поперечной сшивкой геля. В процессе образования ковалентных связей между матрицей и лигандом происходит частичное блокирование активных центров молекулы антигена. Вследствие указанных причин, плотность антигенных детерминант на поверхности иммуносорбента, используемого в прототипе, оказывается недостаточной, что приводит к недостаточной эффективности удаления ревматоидных факторов из крови (Эфферентные методы в медицине. М.: Медицина 1989 С. 64).
Наиболее близким к предложенному по принципу действия и достигаемому результату является способ удаления ревматоидного фактора из крови путем пропускания ее через иммуносорбент с иммобилизированным цельным нативным IgG человека, причем в качестве носителя используют железосодержащие полиакриламидные гранулы. В нашей лаборатории был получен подобный препарат (Гонтарь И.П., Заводовский Б.В., Липницкий С.А., Зборовский А.Б. «Способ очистки крови от ревматоидного фактора»/патент №2027192, 1995 г.).
Как известно человеческий иммуноглобулин состоит из Fab и Fc фрагментов, причем фрагмент Fab составляет примерно 2/3 иммуноглобулина IgG, a Fc - 1/3 (Иммунология А. Ройт, Дж. Бростофф, Д. Мейл - Москва «Мир» 2000 С. 97-112).
В работе была повышена сорбционная и специфическая емкость препарата путем разделения человеческого иммуноглобулина IgG на фрагменты Fc и Fab, и с последующей работой только с фракцией содержащей Fc фрагмент. Для разделения IgG человека на соответствующие фрагменты, мы использовали методику расщепление папаином.
Техническим результатом является повышение сорбционной и специфической емкости препарата для удаления ревматоидного фактора из крови путем разделения человеческого иммуноглобулина IgG на фрагменты Fc и Fab, и последующей работой только с фракцией содержащей Fc фрагмент.
В работе использовали 150 мг IG (1 ампула-1,5 мл, производитель: Микроген НПО Вирион г. Томск) и 1,5 мг меркурипапаина в 10 мл 0,1 М фосфатного буфера с рН 7,0, содержащего ЭДТА и цистеин. Инкубировали смесь 16 ч. При 37°С и против дистиллированной воды, затем диализировали при перемешивании в течение 48 ч. При 4°С. Продукты расщепления подвергали диализу против 0,01 М ацетатного буфера с рН=5,5 и затем проводили хроматографию на КМ-целлюлозе. Фрагменты IgG человека элюировали после папаинового гидролиза в градиенте фосфатного буфера 0,01-0,9 М с рН5,5 при длине волны 280 нм. Хроматографию выполняли при комнатной температуре для предотвращения кристаллизации Fc -фрагмента. Были получены две фракции содержащие Fab-фрагменты иммуноглобулина G и одна фракция - Fc-фрагменты (Иммунологические методы под редакцией Г. Фримеля - Москва «Медицина» 1987 С. 417-423). Для адекватного сравнения сорбционной емкости двух сорбентов были получены одинаковые гранулы как на основе IgG, так и на основе Fc -фрагментов.
Пример 1. Получение полиакриламидных гранул с магнитными свойствами с иммобилизированным нативным иммуноглобулином G человека.
В 2 мл нативного иммуноглобулина G человека, содержащего 200 мг белка растворяли соответственно 100 мг и 300 мг метиленбисакриламида и акриламида (Реанал, Венгрия).
В сосуд, содержащий 100 мл гексана и 0,5 мл эмульгатора СПЭН-85, подавали под давлением 0,2-1 атм газообразный азот по трубке сечением 0,8 мм таким образом, чтобы создавать интенсивное перемешивание в течение 5 мин. В колбу для полимеризации вносили 1 мл физиологического раствора с 200 мг окиси железа с гидрофильными свойствами и 10 мг персульфата аммония, через 1-2 мин. Добавляли 2 мл раствора, содержащего мономеры акриламида, метиленбисакриламида, IgG человека и 20 мкл NNN N-тетраметилендиамина (ТЭМЭД). После завершения полимеризации гранулы в течение 10-15 мин. отмывали ацетоном и физиологическим раствором с детергентом Твин-20 от непрореагировавших мономеров, эмульгатора и гексана. Гранулы имели стандартную сферическую форму с размером частиц геля 10-100 мкм. Соотношение полимерный носитель-железо = 2:1 (в пересчете на сухую массу).
Пример 2. Получение полиакриламидных гранул с магнитными свойствами с иммобилизированными Fc-фрагментами иммуноглобулина G человека.
Данный вид полиакриламидных гранул с магнитными свойствами и иммобилизированным Fc-фрагментами иммуноглобулина G человека получали аналогичным образом см. пример 1., только вместо 200 мг нативного иммуноглобулина G, брали 200 мг Fc- фрагмента этого иммуноглобулина, предварительно полученного при гидролизе папаином и его последующей очистки.
Пример 3. Сорбция ревматоидного фактора из крови больных ревматоидным артритом.
Для проведения сорбции использовали оригинальное устройство, создающее осевой и поперечный градиент магнитного поля напряженностью 4000-5000 Э, которое позволяет удерживать гранулы во взвешенном состоянии, одновременно перемещая их в различных направлениях (поперечном, продольном), что способствовало большему контакту иммуносорбента с кровью и препятствовало адгезии гранул друг с другом (Гонтарь И.П, Заводовский Б.В.., Зборовский А.Б., Зборовская И.А., Кабаков А.П., Самарин Н.В. «Способ проведения экстракорпоральной иммуносорбции»/ патент на изобретение №2098140, 1997 г.).
В колонку объемом 10 мл, оборудованного электромагнитом, вносили магнитоуправляемые полиакриламидные гранулы (МПГ) с иммобилизированным иммуноглобулином G человека при постоянной рециркуляции при t=370 с помощью насоса «MICROPERPEX» (LKB, Швеция) со скоростью 10 мл в час.. Используя эту колонку, была проведена обработка in vitro гепаринизированной крови 10 больных РА с высокой степенью активности основного заболевания. Через колонку перфузировали 20 мл нативной гепаринизированной крови со скоростью 10 мл/ч. После окончания перфузии МПГ отмывали от несвязавшихся белков забуференным физиологическим раствором рН 7,4 и проводили десорбцию РФ с сорбента 1 М глицин-HCI буфером рН2,2 двукратно по 10 мин. В качестве контроля использовали 10 сывороток крови практически здоровых лиц. Концентрацию ревматоидного фактора определяли непрямым твердофазным иммуноферментным методом (ИФА) на полистироловых планшетах (ELISA-тест) по классической методике, описанной в ряде источников литературы (Иммунологические методы / Под ред. Г. Фримеля: Пер. с англ.- М.: Медицина, 1987. - С. 472), (Bampton J., Park J., Kyle K. et al. Measurement of IgM, IgA and IgG rheumatoid factors by ELISA and comparison with other methods // Ann. Rheum. Diseases. - 1982. - Vol. 9 - P. 359-365.). Была также проведена проверка травматичности форменных элементов (эритроцитов, лейкоцитов, тромбоцитов). До и после сорбции определяли содержание их по общепринятым методикам (Лабораторные методы исследования в клинике /Под ред. Меньшикова В.В. - М.: Медицина., 1987. - С. 458). Количество форменных элементов крови достоверно не изменялось. Значения всех исследуемых показателей для каждого образца измеряли двукратно до и после перфузии.
Аналогично провели адсорбцию ревматоидного фактора, используя сорбент с иммобилизированным Fc-фрагментом иммуноглобулина G.
Средняя величина оптической плотности у доноров для IgG составила 0,036±0,004, была определена верхняя граница нормальных показателей оптической плотности для IgG-РФ, определяемая как М+2σ составила 0,08.
Динамика плазменной концентрации ревматоиного фактора в том и другом случае приведена в таблице 1.
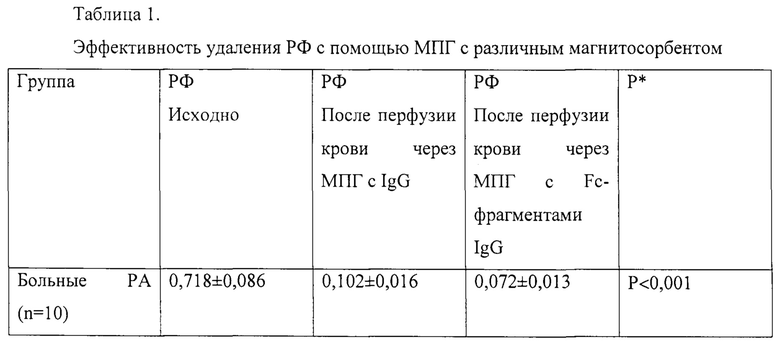
Эффективность удаления РФ с помощью МПГ на основе нативного IgG и Fc -фрагмента была определена в процессе длительности проведения этой процедуры (мин). Было выявлено, что сорбция РФ на основе Fc -фрагмента проходила быстрее, более чем в 2 раза, чем на основе нативного IgG (таб. 2, 3)

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ КРОВИ ОТ РЕВМАТОИДНОГО ФАКТОРА | 1991 |
|
RU2027192C1 |
| ПРИМЕНЕНИЕ Fc-ФРАГМЕНТОВ ИММУНОГЛОБУЛИНА КЛАССА G В КАЧЕСТВЕ АНТИГЕНА ДЛЯ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА, СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2385164C1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2366958C2 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ ДНК-СОДЕРЖАЩИХ ИММУННЫХ КОМПЛЕКСОВ С ПОМОЩЬЮ КОМБИНИРОВАННОГО СОРБЕНТА | 2010 |
|
RU2441674C1 |
| СПОСОБ ОДНОВРЕМЕННОГО УДАЛЕНИЯ ИНТЕРЛЕЙКИНА-12 И ИНТЕРЛЕЙКИНА-23 ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ С ПОМОЩЬЮ МАГНИТОУПРАВЛЯЕМЫХ ГРАНУЛ | 2017 |
|
RU2670674C1 |
| СОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУНОГЛОБУЛИНОВ | 2006 |
|
RU2325172C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ РЕВМАТОИДНОГО АРТРИТА | 2006 |
|
RU2313096C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРДИОЛИПИНОВОГО ИММУНОСОРБЕНТА | 1994 |
|
RU2092189C1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ ДНК-СОДЕРЖАЩИХ ИММУННЫХ КОМПЛЕКСОВ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2356585C2 |
| ВЫСОКОАФФИННЫЕ И АГРЕГАЦИОННО СТАБИЛЬНЫЕ АНТИТЕЛА НА ОСНОВЕ ВАРИАБЕЛЬНЫХ ДОМЕНОВ VL И ПРОИЗВОДНОГО VHH | 2014 |
|
RU2609627C2 |
Изобретение относится к области фармацевтики, а именно к способу получения препарата для удаления ревматоидного фактора из крови больных ревматоидным артритом. Способ включает пропускание крови через сорбент, представляющий собой полиакриламидные железосодержащие гранулы, в которых в результате эмульсионной полимеризации иммобилизован Fc-фрагмент иммуноглобулина G, полученный при папаиновом гидролизе и очистке нативного человеческого иммуноглобулина G. Изобретение обеспечивает повышение сорбционной и специфической емкости препарата для удаления ревматоидного фактора из крови путем разделения человеческого иммуноглобулина IgG на фрагменты Fc и Fab и последующей работы только с фракцией, содержащей Fc фрагмент. 3 табл., 3 пр.
Способ получения препарата для удаления ревматоидного фактора из крови больных ревматоидным артритом, включающий пропускание крови через сорбент, представляющий собой полиакриламидные железосодержащие гранулы, отличающийся тем, что в результате эмульсионной полимеризации в гранулы иммобилизуют Fc-фрагмент иммуноглобулина G, полученный при папаиновом гидролизе и очистке нативного человеческого иммуноглобулина G.
| СПОСОБ ОЧИСТКИ КРОВИ ОТ РЕВМАТОИДНОГО ФАКТОРА | 1991 |
|
RU2027192C1 |
| ПРИМЕНЕНИЕ Fc-ФРАГМЕНТОВ ИММУНОГЛОБУЛИНА КЛАССА G В КАЧЕСТВЕ АНТИГЕНА ДЛЯ ЛЕЧЕНИЯ РЕВМАТОИДНОГО АРТРИТА, СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2385164C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СПЕЦИФИЧЕСКИХ ИММУНОГЛОБУЛИНОВ G К КОНЪЮГАТУ ФОРМАЛЬДЕГИД - СЫВОРОТОЧНЫЙ ЧЕЛОВЕЧЕСКИЙ АЛЬБУМИН В СЫВОРОТКЕ КРОВИ | 2010 |
|
RU2473908C2 |
| СПОСОБ ПРОВЕДЕНИЯ ЭКСТРАКОРПОРАЛЬНОЙ ИММУНОСОРБЦИИ | 1994 |
|
RU2098140C1 |
| ЗБОРОВСКИЙ А.Б | |||
| Возможности использования иммобилизированных наносистем в ревматологии // Ревматология | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Веникодробильный станок | 1921 |
|
SU53A1 |
Авторы
Даты
2020-12-23—Публикация
2020-03-23—Подача