Изобретение относится к области медицины, а именно к ревматологии, иммунологии и биотехнологии, и может быть использовано для совершенствования лечения псориатического артрита и псориаза.
Известно, что ведущим звеном патогенеза многих аутоиммунных заболеваний, включая псориатический артрит (ПсА), является активация клеточного иммунитета с поляризацией по типу Th1 и Th17 [Молочков В.А., Бадокин В.В., Альбанова В.И. и др. Псориаз и псориатический артрит.: Товарищество научных изданий КМК. Авторская академия, 2007-332 с].
При ПсА, как и при других заболеваниях, сопровождающихся иммунными нарушениями, наблюдается патологическое образование интерлейкина-12 (ИЛ-12) и интерлейкина-23 (ИЛ-23). О роли ИЛ-12 в патогенезе артрита свидельствует ряд клинических исследований. Было выявлено, что уровень ИЛ-12 коррелирует с уровнями ФНО, ИЛ-8 и ИЛ-10. Повышенное содержания ИЛ-1, ИЛ-2, ИЛ-10, ИФН& и ФНО обнаружено в синовиальной ткани у пациентов с ПсА.
ИЛ-12 и ИЛ-23 представляют собой гетеродимерные цитокины, состоящие из двух субъединиц гликозилированных протеинов, связанных дисульфидными мостиками и имеющих общую для обоих цитокинов субъединицу р40. При связывании общей субъединицы р40 с субъединицей р35 образуется ИЛ-12, а с субъединицей р19- ИЛ23, каждая из этих субъединиц названа в соответствии со своей молекулярной массой. Эти цитокины продуцируются преимущественно макрофагами, дендритными клетками. Они оказывают действие путем связывания с двухцепочечными гетеродимерными рецепторными комплексами, экспрессируемыми на поверхности CD4+Т-лимфоцитов и естественных киллеров (NК-клеток). Через общую субъединицу р40 ИЛ-12 и ИЛ-23 связываются с цепью 1 рецептора к ИЛ-12. Специфичность сигнала обеспечивается связыванием уникальной субъединицы каждого цитокина с уникальной субъединицей рецепторного комплекса: ИЛ-12р35 связывается с рецептором 2 к ИЛ-12, а ИЛ-23р19 связывается с рецептором к ИЛ-23, запуская внутриклеточную сигнализацию и активируя клетки, несущие эти рецепторы. ИЛ-23 стимулирует Th17-лимфоциты, которые начинают продуцировать провоспалительные факторы, включая ИЛ-17, которые в свою очередь, также стимулируют образование других провоспалительных агентов [Toti D.C., Feldman S.R. Interleukin-12, interleukin-23, and psoriasis: current prospects. J. Am Acad Dermatol 2007; 57:1059-68.].
В настоящее время для лечения ПсА широко используется парентеральное введение ингибитора ИЛ-12 и ИЛ-23: моноклональные антитела к ИЛ-12 и ИЛ-23 (устекинумаб, CILAG, Швейцария). Этот коммерческий препарат - ингибитор интерлейкина, представляющий собой человеческие моноклональные антитела класса IgG1k, продуцируемые рекомбинантной клеточной линией и проходящие многоступенчатую очистку, включая инактивацию и удаление вирусных частиц. Устекинумаб обладает высоким сродством и специфичностью к субъединице р40 интерлейкинов человека ИЛ-12 и ИЛ-23. Препарат блокирует биологическую активность ИЛ-12 и ИЛ-23, предотвращая их связывание с рецептором ИЛ-12R-бетта1, экспрессируемый на поверхности иммунных клеток. Устекинумаб связывается с субъединицей р40 ИЛ-12 и ИЛ-23, одновременно нейтрализуя обе молекулы. Для этого препарата убедительно показан выраженный положительный лечебный эффект: быстрое и выраженное снижение активности заболевания, а также значительное замедление деструкции суставов. Однако существующие ингибиторы ИЛ-12 и ИЛ-23 обладают большим количеством побочных эффектов, связанных с введением иммуногенных молекул в организм пациента (синтез антител к ингибиторам ИЛ-12 и ИЛ-23, частые аллергические и инфузионные реакции). Кроме того, высокая стоимость имеющихся в настоящее время препаратов значительно ограничивает их применение для одного и того же больного.
Удобным инструментом подавления активности цитокинов (ИЛ-12 ИЛ-23) при аутоиммунных заболеваниях является сорбция этих цитокинов крови с помощью магнитоуправляемых гранул. Известен метод удаления цитокинов с помощью углеродного сорбента с локально модифицированной аминокапроновой кислотой поверхностью. В дальнейшем данный способ обозначается как прототип [Долгих Т.И., Пьянова Л.Г., Бакланова О.И. и соавт.: Адсорбция цитокинов на поверхности модифицированного углеродного сорбента in vitro при перитоните. Общая реаниматология 2009, V; 6.-66-69 с]. Согласно последнему, сорбция цитокинов из биологических жидкостей осуществлялась через твердофазный носитель (модифицированной поверхности углеродного адсорбента аминокапроновой кислотой с последующей ее поликонденсацией).
Через колонку заполненную сорбентом пропускали плазму больных, где до и после сорбции определяли содержание цитокинов методом иммуноферментного анализа с помощью тест-систем ООО «Протеиновый контур» (Санкт-Петербург, Россия).
Модифицирование поверхности углеродного адсорбента аминокапроновой кислотой приводило к увеличению содержания поверхностных функциональных групп (кислород -и азотсодержащих), тем самым повышая эффективность сорбции ряда цитокинов только за счет различной гидрофобности, однако такая сорбция не является селективной. Снижение содержания цитокинов в результате данной процедуры составляло 92,64%. Однако предложенный в прототипе носитель не является магнитоуправляемым, что затрудняет удержание сорбента во взвешенном состоянии в сорбционной колонке без магнитного поля, в результате чего, в процессе адсобции происходит уплотнение слоя носителя, следствием чего и является травматизация форменных элементов и частичная потеря углеродного сорбента.
Иммобилизация цитокинов, примененная в прототипе, как правило, препятсвует получению сорбентов с максимально высокой емкостью и регенерация такого сорбента обычно затруднена.
Решаемая задача состоит в разработке способа снижения содержания цитокинов (ИЛ-12, ИЛ-23) путем пропускания биологических жидкостей через предварительно полученный методом эмульсионной полимеризации в потоке газообразного азота оригинальный сорбент, представляющий собой магнитоуправляемые полиакриламидные гранулы (МПГ) с иммобилизированными антителами к ИЛ-12 и ИЛ-23, что обеспечивает более выраженное снижение концентрации цитокинов в перфузируемой крови по сравнению с прототипом, а также возможность многократного использования разработанных нами гранул.
Получение МПГ производится следующим способом. В сосуд, содержащий гексан и эмульгатор, подается под давлением по трубке химически инертный газ таким образом, чтобы создавать интенсивное перемешивание. В колбу для полимеризации вносится раствор окиси железа с гидрофильными свойствами и персульфат аммония, затем добавляется раствор, содержащий мономеры акриамида, метиленбисакриламида, NNN'N'-тетраметилендиамина и антител к ИЛ-12 и ИЛ-23 (устекинумаб). После завершения полимеризации МПГ отмывают от непрореагировавших мономеров, эмульгатора и гексана. Далее МПГ вносят в колонку и через нее перфузируется биологическая жидкость, например нативная гепаринизированная кровь. Регенерация препарата производится путем пропускания через колонку 1М буфера глицин-HCI рН 2,2 дважды по 10 мин.
Пример 1. Получение МПГ с иммобилизированными антителами к ИЛ-12 и ИЛ-23 В 2 мл 0,15М раствора натрия хлорида растворяли соответственно 300 мг и 100 мг акриламида и метиленбисакриламида (Reanal, Венгрия), после чего к такому раствору добавляли 0,4 мг моноклональных антител к ИЛ-12 и ИЛ-23. В сосуд, содержащий 100 мл гексана и 0,5 мл эмульгатора СПЭН-85, подавали под давлением 0,2-1 атм газообразный азот по трубке сечением 0,8 мм таким образом, чтобы создавать интенсивное перемешивание в течение 5 мин. В колбу для полимеризации вносили 1 мл физиологического раствора рН 7,4 с 200 мг окиси железа с гидрофильными свойствами и 10 мг персульфата аммония. Через 1-2 мин. Добавляли 2 мл вышеупомянутого раствора, содержащего мономеры акриламида, метиленбисакриламида, иммобилизируемое вещество (антитела к ИЛ-12 и ИЛ-23), а также 20 мкл NNN'N' - тетраметилэтилендиамина.
После завершения полимеризации гранулы в течение 10-15 мин. отмывали ацетоном и физиологическим раствором с детергентом Твин-20 (0,05%) от непрореагировавших мономеров, эмульгатора и гексана. Гранулы имели стандартную сферическую форму с размером частиц геля 10-100 мкм. Соотношение полимерный носитель : железо = 2:1 (в пересчете на сухую массу).
Пример 2. Определение удельной сорбционной емкости МПГ Для МПГ с иммобилизированными антителами к ИЛ-12 и ИЛ-23, полученных согласно примеру 1, определяли удельную сорбционную емкость.
С этой целью через мини-колонку с объемом рабочей камеры 0,2 мл, заполненную МПГ, пропускали растворы ИЛ-12 и ИЛ-23 (1 мл) с возрастающими концентрациями, после перфузии каждого раствора МПГ заменяли, контур промывали 1 М глицин-HCI буфером, рН 2,2 и стандартным фосфатно-солевым буферным раствором. Концентрацию ИЛ-12 и ИЛ-23 в пропущенных через МПГ растворах определяли методом ИФА с использованием коммерческих наборов (Bender Med.Systems, США для ИЛ-12, Bender Med.Systems, Vienna, Austria для ИЛ-23)). При изучении растворов ИЛ-12 и ИЛ-23 с исходными концентрациями 5, 10, 50, 100, 500, 1500 пг/мл после перфузии через МПГ ИЛ-12 и ИЛ-23 практически не определялись. В растворе ИЛ-12 и ИЛ-23 с исходной концентрацией 1500 пг/мл конечная концентрация ИЛ-12 и ИЛ-23 составила 24,3пг/мл. Следовательно, сорбционная емкость МПГ составила 7,38 нг/мл ИЛ-12 и ИЛ-23 сорбента. Сопоставление данного параметра МПГ с прототипом не представляется возможным ввиду отсутствия данных о концентрациях ИЛ-12 и ИЛ-23 в описании прототипа.
Пример 3. Перфузия крови через МПГ
В колонку объемом 10 мл, оборудованную электромагнитом, вносили МПГ с иммобилизированными антителами к ИЛ-12 и ИЛ-23. Используя колонку, проведена обработка in vitro гепаринизированной крови 10 больных псориатический артритом различной степени активности, которым в течение 12 месяцев не проводилось парентеральное введение ингибиторов цитокинов (ИЛ-12 и ИЛ-23) (устекинумаба). Через колонку перфузировали 20 мл нативной гепаринизированной крови со скоростью 10 мл/ч. В качестве контроля выступала перфузия крови 10 здоровых доноров, параметры процедуры перфузии были аналогичными. После окончания перфузии МПГ отмывали от несвязавшихся белков забуференным физиологическим раствором рН 7,4 и проводили регенерацию 1 М глицин-HCI буфером рН 2,2 двукратно по 10 мин. Концентрацию цитокинов (ИЛ-12 и ИЛ-23) плазмы крови определяли методом ИФА с использованием коммерческих наборов (Bender Med. Systems, США для ИЛ-12 и Bender Med.Systems, Viennna, Austria для Ил-23), также оценивали содержание форменных элементов крови (эритроцитов, лейкоцитов, тромбоцитов). Значения всех исследуемых показателей для каждого образца измеряли двукратно- до и после перфузии.
Динамика плазменной концентрации ИЛ-12 доноров и больных ПсА в результате осуществления заявляемого способа приведена в таблице 1, ИЛ-23 - в таблице 2, динамика форменных элементов - в таблице 3. Из таблиц 1 и 2 видно, что при перфузии через магнитоуправляемый сорбент достигается значимое снижение содержания ИЛ-12 от исходного на 99,8% (для здоровых лиц) и 99.9% (для больных ПсА) от исходного, а снижение концентрации ИЛ-23 для для больных ПсА - 99,9%. [Shibata S1, Tada Y, Komine M, Hattori N, Osame S, Kanda N, Watanabe S, Saeki H, Tamaki K. Anti-cyclic citrullinated peptide antibodies and IL-23p19 in psoriatic arthritis. J Dermatol Sci. 2009 Jan; 53(1):34-9.]. Поэтому максимально возможное снижение уровня цитокинов имеет большое практическое значение, так как играют ведущую роль в патогенезе ПсА. При перфузии же через прототип, концентрация цитокинов уменьшается на 92,64% от исходного. В прототипе используются чистый углеродный гемосорбент и тот же сорбент, обработанный аминокапроновой кислотой с последующей поликонденсацией. Оба типа сорбентов на микрофотографии имеют структуры игольчатой формы, способные травмировать форменные элементы крови. Поэтому мы дополнительно провели количественную оценку степени травматизации форменных элементов с помощью заявляемого образца.
При использовании заявляемого нами способа содержание форменных элементов крови достоверно не изменяется, что является дополнительным преимуществом перед прототипом [таб. 3]. Следовательно, полученные при сопоставлении с прототипом данные свидетельствуют о более значительном снижении концентрации цитокинов в плазме крови как здоровых лиц, так и больных ПсА при использовании заявляемого способа.
После использования МПГ регенерировали 1М глицин-HCI буфером, рН 2,2. После первой регенерации потеря сорбционной емкости составила 15%. При последующих повторных регенерациях (9 раз) статистически значимых изменений удельной сорбционной емкости не происходило.
СПОСОБ УДАЛЕНИЯ ИНТЕРЛЕЙКИНА-12 ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ С ПОМОЩЬЮ МАГНИТОУПРАВЛЯЕМЫХ ГРАНУЛ
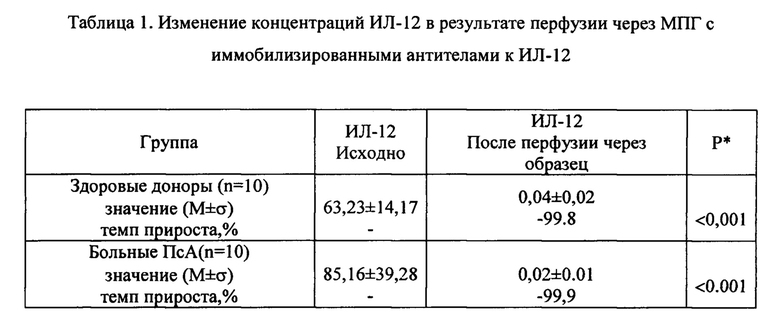
* - парный критерий Стьюдента
СПОСОБ УДАЛЕНИЯ ИНТЕРЛЕЙКИНА-23 ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ С ПОМОЩЬЮ МАГНИТОУПРАВЛЯЕМЫХ ГРАНУЛ

* - парный критерий Стьюдента

*р<0,05 - по сравнению с исходными значениями
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ КРОВИ ОТ ДНК-СОДЕРЖАЩИХ ИММУННЫХ КОМПЛЕКСОВ С ПОМОЩЬЮ КОМБИНИРОВАННОГО СОРБЕНТА | 2010 |
|
RU2441674C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ДЛЯ УДАЛЕНИЯ РЕВМАТОИДНОГО ФАКТОРА ИЗ КРОВИ БОЛЬНЫХ РЕВМАТОИДНЫМ АРТРИТОМ | 2020 |
|
RU2739352C1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2366958C2 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ ДНК-СОДЕРЖАЩИХ ИММУННЫХ КОМПЛЕКСОВ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2356585C2 |
| ГОМОДИМЕР Р40 ИНТЕРЛЕЙКИНА-12 | 1994 |
|
RU2135584C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЧИСТКИ ФИЗИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2010 |
|
RU2448897C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРДИОЛИПИНОВОГО ИММУНОСОРБЕНТА | 1994 |
|
RU2092189C1 |
| СОРБЕНТ ДЛЯ УДАЛЕНИЯ ИММУНОГЛОБУЛИНОВ | 2008 |
|
RU2389022C2 |
| ПЕПТИД-АНТАГОНИСТ АКТИВНОСТИ ИНТЕРЛЕЙКИНА-15 | 2009 |
|
RU2506270C2 |
| Сорбент для сочетанного удаления из плазмы человека атерогенных липопротеидов и С-реактивного белка | 2019 |
|
RU2700605C1 |
Изобретение относится к медицине, а именно к иммунологии и биотехнологии. Осуществляют пропускание крови через гранулированный препарат с иммобилизированными сконцентрированными моноклональными антителами к интерлейкину-12 и интерлейкину-23. При этом для иммобилизации антител к ИЛ-12 и ИЛ-23 используют полиакриламидный носитель с магнитными свойствами при соотношении носитель : железо 2:1, который гранулируют методом эмульсионной полимеризации. Способ позволяет обеспечить более выраженное снижение концентрации цитокинов в перфузионной крови без изменения содержания форменных элементов крови, позволяет многократно использовать используемые гранулы. 3 пр., 3 табл.
Способ одновременного удаления интерлейкина-12 (ИЛ-12) и интерлейкина-23 (ИЛ-23), включающий пропускание крови через гранулированный препарат с иммобилизированными сконцентрированными моноклональными антителами к интерлейкину-12 и интерлейкину-23, отличающийся тем, что для иммобилизации антител к ИЛ-12 и ИЛ-23 используют полиакриламидный носитель с магнитными свойствами при соотношении носитель : железо 2:1, который гранулируют методом эмульсионной полимеризации.
| ДОЛГИХ Т.И | |||
| Адсорбция цитокинов на поверхности модифицированного углеродного сорбента in vitro при перитоните | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ ДНК-СОДЕРЖАЩИХ ИММУННЫХ КОМПЛЕКСОВ С ПОМОЩЬЮ КОМБИНИРОВАННОГО СОРБЕНТА | 2010 |
|
RU2441674C1 |
| МАГНИТНЫЕ ЧАСТИЦЫ, СПОСОБ ИХ ИЗГОТОВЛЕНИЯ, КОМПОЗИЦИОННЫЙ МАГНИТНЫЙ МАТЕРИАЛ И СПОСОБ УДАЛЕНИЯ ЗАГРЯЗНЯЮЩИХ ИОНОВ ИЗ ВОДНОГО РАСТВОРА | 1995 |
|
RU2113277C1 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2366958C2 |
| Устройство, регулирующее степень подогрева воды в регенераторах при паровых турбинах | 1926 |
|
SU4953A1 |
| ГОЛЕНКИНА Е.А | |||
| и др | |||
| Иммуномагнитные сорбенты в селекции Т-лимфоцитов человека | |||
| Российский биотерапевтический журнал | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
Авторы
Даты
2018-10-24—Публикация
2017-05-02—Подача