Изобретение относится к способу определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор)) или ингибиторов HMG-CoA-редуктазы (статины), включающему стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, и
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови с заданным пороговым значением, и
- где в случае, когда определенный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, тогда индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), и
- где в случае, когда установленный уровень hGH и/или его изоформ является более низким, чем указанный заданный пороговый уровень, тогда индивидуума идентифицируют как не имеющего сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
Применение биомаркеров для стратификации пациентов, страдающих или имеющих риск развития сердечно-сосудистого заболевания, для успешного фармакологического вмешательства, в основном, известно. Однако до настоящего времени оно было ограничено биомаркерами, ассоциированными с воздействующей на сосуды или воспалительной активностью, например, WO/2010/128071, Richards AM, et al. Australia-New Zealand Heart Failure Group. Journal of the American College of Cardiology 2001, 37(7):1781-1787 и Ridker et al: The New England journal of medicine 2008, 359(21):2195-2207.
Гормон роста человека (hGH) в этом контексте никогда не описывался. Известно только, что относительно повышенные уровни hGH в плазме в нормальной популяции (особенно у мужчин) ассоциированы с увеличенным риском развития характерных сердечных неблагоприятных явлений, WO/2014/108396.
В настоящем описании авторы описывают, что повышенные уровни Hgh и/или его изоформ в плазме у индивидуумов ассоциированы с успехом терапии антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), в то время как такая терапия не является эффективной у пациентов с относительно низкими уровнями hGH и/или его изоформ в плазме. Таким образом, измерение hGH и/или его изоформ у индивидуумов является пригодным для стратификации пациентов для фармакологической терапии.
Настоящее изобретение относится к способу определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, снижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), включающему стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, и
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови с заданным пороговым значением, и
- где в случае, когда установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, тогда индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), и
- где в случае, когда установленный уровень hGH и/или его изоформ является более низким, чем указанный заданный пороговый уровень, тогда индивидуума идентифицируют как не имеющего сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
В одном конкретном варианте осуществления указанный индивидуум не имеет гипертензии (по меньшей мере >140 мм рт. ст. (систолическое) на 90 мм рт. ст. (диастолическое)).
В одном конкретном варианте осуществления указанного индивидуума еще не лечили антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
В одном варианте осуществления снижение сосудистого риска посредством снижения кровяного давления у индивидуума означает предупреждение тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у указанного индивидуума.
В одном конкретном варианте осуществления способа указанный индивидуум имел острый инфаркт миокарда или острую сердечную недостаточность в пределах последних 2 недель, предпочтительно в пределах последней одной недели, предпочтительно в пределах последних 36 часов.
В одном конкретном варианте осуществления способа согласно изобретению указанный индивидуум никогда не имел тяжелого неблагоприятного сердечно-сосудистого явления и никогда не имел никакого сердечно-сосудистого заболевания. В другом конкретном варианте осуществления способа согласно изобретению указанный индивидуум имеет бляшку в сонной артерии, но не имеет симптомов заболевания сонной артерии. Общепринятым способом обнаружения присутствия атеросклеротического заболевания и мониторинга его регрессии, остановки или прогрессирования является измерение толщины внутренней-средней оболочки (IMT) (de Groot et al., Nature Reviews Cardiology 5, 280-288 (May 2008) | doi:10,1038/ncpcardio1163). Она представляет собой толщину внутренней оболочки и средней оболочки, двух наиболее внутренних слоев стенки артерии. Измерение обычно проводят посредством внешнего ультразвука и иногда посредством внутренних инвазивных ультразвуковых катетеров. FDA одобрила IMT в качестве заместительного маркера атеросклеротического заболевания для применения в клинических испытаниях. Размер IMT ассоциирован с исходом сердечно-сосудистого заболевания и его изменения с течением времени (статистически значимое изменение IMT в год) ассоциированы с эффективностью лекарственных средств (de Groot et al., Nature Reviews Cardiology 5, 280-288 (May 2008) | doi:10,1038/ncpcardio1163; Hedblad et al., Circulation. 2001;103:1721-1726.)
Указанное тяжелое неблагоприятное сердечно-сосудистое явление или сердечно-сосудистое заболевание могут быть выбраны из группы, включающей сердечную недостаточность, атеросклероз, гипертензию, кардиомиопатию, инфаркт миокарда и инсульт.
В одном варианте осуществления изобретения указанным индивидуумом является мужчина.
В одном варианте осуществления способа согласно изобретению указанный способ используют для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления или предупреждения сердечно-сосудистого заболевания.
Указанное тяжелое неблагоприятное сердечно-сосудистое явление может быть выбрано из группы, включающей инфаркт миокарда, острую сердечную недостаточность, инсульт и смерть от сердечно-сосудистой патологии.
Образец крови может быть выбран из группы, включающей цельную кровь, сыворотку и плазму.
В одном варианте осуществления изобретения образец крови представляет собой образец крови, взятый натощак.
Образец, взятый натощак, означает образец, который был взят от индивидуума, который не употреблял никакую пищу или солюбилизированные питательные вещества в течение по меньшей мере 8 часов перед взятием образца крови. В конкретном варианте осуществления такой образец, взятый натощак, получают от индивидуума в период от 7:00 до 11:30 после голодания индивидуума в течение по меньшей мере 8 часов.
В другом варианте осуществления уровни гормона роста (hGH) натощак означают уровень гормона роста (hGH), определенный в крови, сыворотке или плазме индивидуумов в состоянии натощак, которые не принимали пищу в течение 12 ч перед взятием образца. В указанном варианте осуществления индивидуум в состоянии натощак означает индивидуума, который не принимал пищу в течение 12 ч перед взятием образца.
Термин "индивидуум", как используют в рамках изобретения, относится к живому человеческому или нечеловеческому организму. Предпочтительно в рамках настоящего изобретения индивидуумом является человек. Индивидуум может быть здоровым или заболевшим, если нет иных указаний. Термин "повышенный уровень" означает уровень выше определенного порогового уровня.
В одном конкретном варианте осуществления изобретения способ измерения или анализ, которые используют для определения уровня hGH и/или его изоформ, имеет аналитическую чувствительность, которая является достаточной для количественного определения нижнего 95-го процентиля нормального диапазона от показателя здоровых мужчин в состоянии натощак предпочтительно в возрасте по меньшей мере 40 лет с CV между анализами, который не превышает 20%. Пример такого анализа описан в WO/2014/108396.
Чувствительность анализа можно определять посредством "аналитической" чувствительности анализа, которую определяют как концентрация hGH (данные стандартной кривой) при срединном сигнале, например, для 20 определений в образце с истощенным hGH+2 стандартных отклонения (SD).
Альтернативно чувствительность анализа можно определять посредством "функциональной" чувствительности анализа, которая отражает в большей степени предел обнаружения в повседневных клинических условиях. Функциональную чувствительность анализа определяют как определение коэффициента вариации (CV) между анализами в плазме (образцах пациента) в различных индивидуальных образцах с различными концентрациями hGH. Функциональная чувствительность анализа представляет собой наиболее низкую концентрацию hGH с CV между анализами менее 20%.
Чувствительность анализа может зависеть от используемого способа калибровки и используемого анализа hGH. Различные анализы hGH могут обнаруживать различные наборы изоформ hGH, что приводит к различным количественным результатам, что означает различные пороговые значения и необходимую чувствительность в зависимости от используемого анализа и способа калибровки.
Для преодоления этой возможной гетерогенности различных анализов hGH в калибровку анализа можно вносить поправку путем коррелирования величин hGH в плазме отдельных индивидуумов. Если наклон кривой коррелирования отличается от 1, тогда в величины hGH (калибровка) можно вносить поправку на дифференциальный коэффициент, что приводит к сравнимой калибровке, анализу со сравнимой чувствительностью и сравнимым пороговым значениям.
Описанное выше внесение поправки можно проводить для сравнения результатов, полученных с помощью различных анализов.
Анализ, описанный в примере 1, в основном распознает изоформу 1 hGH и откалиброван с помощью рекомбинантного гормона роста человека (код NIBSC 98/574, National Institute for Biological Standards and Control, Herfordshire, Великобритания).
В конкретном способе по изобретению указанный уровень гормона роста (hGH) и/или его изоформы натощак в жидкости организма определяют с помощью сверхчувствительного анализа, имеющего аналитическую чувствительность анализа (которую определяют как концентрация hGH при срединном сигнале для 20 определений в образце с истощенным hGH+2 стандартных отклонения (SD)) менее 100 пг/мл, предпочтительно менее 50 пг/мл, предпочтительно менее 30 пг/мл, предпочтительно менее 20 пг/мл, предпочтительно менее 10 пг/мл, предпочтительно менее 5 пг/мл, предпочтительно 2 пг/мл. Результат измерения hGH выражают в нг/мл (1 нг/мл=2,6 мЕ/л).
Альтернативно, сверхчувствительный анализ имеет функциональную чувствительность анализа (см. выше) менее 400 пг/мл, предпочтительно менее 200 пг/мл, предпочтительно менее 120 пг/мл, предпочтительно менее 80 пг/мл, предпочтительно менее 40 пг/мл, предпочтительно менее 20 пг/мл, предпочтительно менее 10 пг/мл, наиболее предпочтительно менее 8,5 пг/мл. Результаты измерения hGH выражают в нг/мл.
Анализ может представлять собой иммуноанализ или другой способ обнаружения, например, масс-спектрометрию.
Для иммунизации и калибровки авторы настоящего изобретения использовали рекомбинантный гормон роста человека (код NIBSC 98/574, National Institute for Biological Standards and Control, Herfordshire, Великобритания).
В одном варианте осуществления изобретения указанный анализ проводят, как описано в примере 1.
Указанный анализ может быть селективным в отношении одной конкретной изоформы hGH, или он может быть специфичным в отношении или определяет более одного или все секретируемые изомеры hGH, выбранные из группы, включающей изоформу 1, изоформу 2, изоформу 3 и изоформу 4 hGH (см. SEQ ID NO: 1-4) в указанной жидкости организма.
Изоформы гормона роста (hGH) могут быть выбраны из группы, включающей изоформу 1 hGH (22 кДа), изоформу 2 hGH, изоформу 3 hGH и изоформу 4 hGH.
Последовательности изоформ:
SEQ ID NO.1: изоформа 1 hGH (22 кДа)
MATGSRTSLLLAFGLLCLPWLQEGSAFPTIPLSRLFДНКMLRAHRLHQLAFDTYQEFEEA
YIPKEQKYSFLQNPQTSLCFSESIPTPSNREETQQKSNLELLRISLLLIQSWLEPVQFLR
SVFANSLVYGASDSNVYDLLKDLEEGIQTLMGRLEDGSPRTGQIFKQTYSKFDTNSHNDD
ALLKNYGLLYCFRKDMDKVETFLRIVQCRSVEGSCGF
SEQ ID NO.2: изоформа 2 hGH
MATGSRTSLLLAFGLLCLPWLQEGSAFPTIPLSRLFДНКMLRAHRLHQLAFDTYQEFNPQ
TSLCFSESIPTPSNREETQQKSNLELLRISLLLIQSWLEPVQFLRSVFANSLVYGASDSN
VYDLLKDLEEGIQTLMGRLEDGSPRTGQIFKQTYSKFDTNSHNDDALLKNYGLLYCFRKD
MDKVETFLRIVQCRSVEGSCGF
SEQ ID NO.3: изоформа 3 hGH
MATGSRTSLLLAFGLLCLPWLQEGSAFPTIPLSRLFДНКMLRAHRLHQLAFDTYQEFEEA
YIPKEQKYSFLQNPQTSLCFSESIPTPSNREETQQKSNLELLRISLLLIQTLMGRLEDGS
PRTGQIFKQTYSKFDTNSHNDDALLKNYGLLYCFRKDMDKVETFLRIVQCRSVEGSCGF
SEQ ID NO.4: изоформа 4 hGH
MATGSRTSLLLAFGLLCLPWLQEGSAFPTIPLSRLFДНКMLRAHRLHQLAFDTYQEFEEA
YIPKEQKYSFLQNPQTSLCFSESIPTPSNREETQQKSNLELLRISLLLIQSWLEPVQIFK
QTYSKFDTNSHNDDALLKNYGLLYCFRKDMDKVETFLRIVQCRSVEGSCGF
В одном конкретном варианте осуществления изобретения способ измерения, который используют для определения уровня hGH и/или его изоформ, представляет собой анализ, имеющий чувствительность анализа по меньшей мере 50 пг/мл.
В одном конкретном варианте осуществления изобретения способ измерения, который используют для определения уровня hGH и/или его изоформ, представляет собой иммуноанализ, имеющий чувствительность анализа по меньшей мере 50 пг/мл.
В одном варианте осуществления изобретения заданный пороговый уровень составляет более 330 пг/мл, предпочтительно более 1370 пг/мл. В одном варианте осуществления изобретения заданный пороговый уровень составляет более 330 пг/мл, предпочтительно более 1370 пг/мл у индивидуума, который имел острый инфаркт миокарда в пределах последних 2 недель, предпочтительно в пределах последней одной недели, предпочтительно в пределах последних 36 часов.
В одном варианте осуществления пороговое значение может быть определено следующим образом:
- Сравнение концентрации hGH и/или его изоформ в жидкости организма, полученной от указанного индивидуума, со срединным значением уровней hGH и/или его изоформ в жидкости организма, полученной из набора заданных образцов в случайным образом отобранной группе индивидуумов, имеющих сравнимое исходное состояние с указанным индивидуумом,
- Сравнение концентрации hGH и/или его изоформ в жидкости организма, полученной от указанного индивидуума, с квантилем уровней hGH и/или его изоформ в жидкости организма, полученным для набора заданных образцов в группе индивидуумов, имеющих сравнимое исходное состояние с указанным индивидуумом,
- Вычисление на основе анализа пропорциональных рисков Кокса или с использованием вычисления индексов риска, таких как NRI (суммарный индекс переклассификации) или IDI (интегрированный индекс дискриминации).
Специалисту в данной области будет понятно, что заданное пороговое значение необходимо рассматривать в контексте используемого анализа, используемых способов калибровки и других факторов.
Настоящее изобретение относится к способу, в котором уровень, предпочтительно уровень натощак, гормона роста (hGH) и/или его изоформ определяют с использованием соединения, связывающегося с гормоном роста (hGH) и/или его изоформами.
В одном варианте осуществления изобретения указанное связывающееся соединение выбрано из группы, включающей антитело, фрагмент антитела или каркас не на основе Ig, связывающиеся с гормоном роста (hGH) и/или его изоформами.
В одном конкретном варианте осуществления изобретения используют иммуноанализ, который включает по меньшей мере два антитела, которые связываются с hGH и/или его изоформами.
Согласно изобретению, диагностическое связывающееся соединение выбрано из группы, состоящей из антител, например IgG, типичного полноразмерного иммуноглобулина или фрагментов антител, содержащих по меньшей мере F-вариабельный домен тяжелой и/или легкой цепей, например, химически связанных антител (антигенсвязывающий фрагмент), включающих, но не ограничивающихся ими, Fab-фрагменты, включающие Fab-миниантитела, одноцепочечное Fab-антитело, одновалентное Fab-антитело с эпитопными метками, например Fab-V5Sx2; двухвалентный Fab (миниантитело), димеризованный с доменом CH3; двухвалентный Fab или поливалентный Fab, например, образованный посредством мультимеризации с помощью гетерологичного домена домен, например посредством димеризации доменов dHLX, например Fab-dHLX-FSx2; F(ab')2-фрагменты, scFv-фрагменты, мультимеризованные поливалентные или/и мультиспецифические scFv-фрагменты, двухвалентные и/или биспецифические диантитела, BITE® (биспецифическое соединение, связывающее T-клетки), трифункциональные антитела, поливалентные антитела, например, из класса, отличающегося от G; однодоменные антитела, например, наноантитела, происходящие из иммуноглобулинов животных семейства верблюжьих или рыб.
В предпочтительном варианте осуществления каждое из по меньшей мере двух антител, которые связываются с hGH и/или его изоформами, обладает аффинностью в отношении hGH и/или его изоформ по меньшей мере 107 M-1, предпочтительно 108 M-1, предпочтительно константа аффинности превышает 109 M-1, наиболее предпочтительно превышает 1010 M-1. Специалисту в данной области известно, что возможна компенсация более низкой аффинности с использованием более высокой дозы соединений, и эта мера не приведет к выходу за пределы объема изобретения. Аффинность связывания можно определять с использованием способа Biacore, предлагаемого в качестве сервисного анализа, например, в Biaffin, Kassel, Германия (http://www.biaffin.com/de/).
Для определения аффинности антител кинетику связывания hGH с иммобилизованным антителом определяли посредством поверхностного плазмонного резонанса без метки с использованием системы Biacore 2000 (GE Healthcare Europe GmbH, Freiburg, Германия). Обратимую иммобилизацию антител проводили с использованием антитела против Fc мыши, ковалентно связанного при высокой плотности с поверхностью сенсора CM5 в соответствии с инструкциями изготовителя (набор для улавливания антител мыши; GE Healthcare) {Lorenz et al.,"Functional Antibodies Targeting IsaA of Staphylococcus aureus Augment Host Immune Response and Open New Perspectives for Antibacterial"; Antimicrob Agents Chemother. 2011 January; 55(1): 165-173}.
В дополнение к антителам, в данной области хорошо известны другие биополимерные каркасы, образующие комплекс с молекулой-мишенью, и их используют для получения высокоспецифичных к мишени биополимеров. Примерами являются аптамеры, шпигельмеры, антикалины и конотоксины. Не-Ig каркасы могут представлять собой белковые каркасы, и их можно использовать в качестве миметиков, антител, поскольку они способны связываться с лигандами или антигенами. Не-Ig каркасы могут быть выбраны из группы, включающей не-Ig каркасы на основе тетранектина (например, описанные в US 2010/0028995), каркасы на основе фибронектина (например, описанные в EP 1266 025; каркасы на основе липокалинов (например, описанные в WO 2011/154420); каркасы на основе убиквитина (например, описанные в WO 2011/073214), каркасы на основе трансферрина (например, описанные в US 2004/0023334), каркасы на основе белка A (например, описанные в EP 2231860), каркасы на основе анкириновых повторов (например, описанные в WO 2010/060748), каркасы на основе микробелков, предпочтительно микробелков, образующих цистиновый узел (например, описанные в EP 2314308), каркасы на основе домена Fyn SH3 (например, описанные в WO 2011/023685), каркасы на основе A-домена EGFR (например, описанные в WO 2005/040229) и каркасы на основе домена Kunitz (например, описанные в EP 1941867).
В одном варианте осуществления изобретения может предусматриваться так называемый POC-тест (исследование по месту лечения), который представляет собой технологию, позволяющую проведение исследования в течение менее чем 1 часа вблизи пациента без необходимости в полностью автоматизированной системе анализа. Одним примером этой технологии является иммунохроматографическая технология исследования.
В одном варианте осуществления изобретения такой анализ представляет собой сэндвич-иммуноанализ с использованием любого типа технологии обнаружения, включая, но не ограничиваясь ими, ферментную метку, хемилюминесцентную метку, электрохемилюминесцентную метку, предпочтительно полностью автоматизированный анализ. В одном варианте осуществления изобретения такой анализ представляет собой сэндвич-анализ с ферментной меткой. Примеры автоматизированного или полностью автоматизированного анализа включают анализы, которые можно использовать для одной из следующих систем: Roche Elecsys®, Abbott Architect®, Siemens Centauer®, Brahms Kryptor®, Biomerieux Vidas®, Alere Triage®.
Для анализов и способов по настоящему изобретению известны и могут использоваться различные иммуноанализы, которые включают: радиоиммунный анализ ("RIA"), однородный иммуноферментный анализ ("EMIT"), твердофазный иммуноферментный анализ ("ELISA"), анализ реактивации апофермента ("ARIS"), иммуноанализ с импрегнированным субстратом и иммунохроматографический анализ.
В одном варианте осуществления изобретения по меньшей мере одно из указанных двух связывающих соединений является меченным для обнаружения.
Предпочтительные способы обнаружения включают иммуноанализ в различных форматах, например, таких как радиоиммунный анализ (RIA), хемилюминесцентный и флуоресцентный иммуноанализ, твердофазный иммуноферментный анализ (ELISA), гранульные матрицы на основе Luminex, анализы белков на микрочипах и форматы быстрых тестов, например, такие как тесты на иммунохроматографической полоске.
В предпочтительном варианте осуществления указанная метка выбрана из группы, включающей хемилюминесцентную метку, ферментную метку, флуоресцентную метку, радиоактивную йодную метку.
Анализы могут представлять собой гомогенные или гетерогенные анализы, конкурентные или неконкурентные анализы. В одном варианте осуществления анализ имеет форму сэндвич-анализа, который представляет собой неконкурентный иммуноанализ, в котором молекула, подлежащая обнаружению и/или количественному определению, связана с первым антителом и со вторым антителом. Первое антитело может быть связано с твердой фазой, например, гранулами, поверхностью лунки или другого контейнера, чипом или полоской, а второе антитело представляет собой антитело, которое является меченным, например, красителем, радиоактивным изотопом или реакционноспособной или каталитически активной частью. Затем количество меченого антитела, связанного с анализируемым соединением, измеряют подходящим способом. Основные композиции и методики, вовлеченные в "сэндвич-анализ", являются общепризнанными и известны специалисту в данной области {Ludvigsson J, Andersson E, Ekbom A, Feychting M, Kim J-L, Reuterwall C, et al. External review and validation of the Swedish national inpatient register. BMC Public Health. 2011;11(1):450}.
В другом варианте осуществления анализ включает две улавливающих молекулы, предпочтительно антитела, обе из которых присутствуют в качестве дисперсий в жидкой реакционной смеси, где первый компонент для мечения связан с первой улавливающей молекулой, где указанный первый компонент для мечения является частью системы мечения на основе тушения или усиления флуоресценции или хемилюминесценции, и второй компонент для мечения указанной маркирующей системы связан со второй улавливающей молекулой, так что при связывании обеих улавливающих молекул с анализируемым соединением генерируется поддающийся обнаружению сигнал, который позволяет обнаружение образовавшихся сэндвич-комплексов в растворе, содержащем образец.
В другом варианте осуществления указанная система мечения включает редкоземельные криптаты или редкоземельные хелаты в комбинации с флуоресцентным красителем или хемилюминесцентным красителем, в частности, красителем типа цианина.
В контексте настоящего изобретения флуоресцентные анализы включают применение красителей, которые могут быть выбраны из группы, например, включающей FAM (5-или 6-карбоксифлуоресцеин), VIC, NED, флуоресцеин, флуоресцеинизотиоцианат (FITC), IRD-700/800, цианиновые красители, такие как CY3, CY5, CY3.5, CY5.5, Cy7, ксантен, 6-карбокси-2',4',7',4,7-гексахлорфлуоресцеин (HEX), TET, 6-карбокси-4',5'-дихлор-2',7'-диметоксифлуоресцеин (JOE), N,N,N',N'-тетраметил-6-карбоксиродамин (TAMRA), 6-карбокси-X-родамин (ROX), 5-карбоксиродамин-6G (R6G5), 6-карбоксиродамин-6G (RG6), родамин, родамин зеленый, родамин красный, родамин 110, красители BODIPY, такие как BODIPY TMR, орегоновый зеленый, кумарины, такие как умбеллиферон, бензимиды, такие как хехст 33258; фенантридины, такие как техасский красный, якимский желтый, Alexa Fluor, PET, бромид этидия, красители акридиния, красители на основе карбазола, красители на основе феноксазина, порфириновые красители, полиметиновые красители и т.д.
В контексте настоящего изобретения анализы на основе хемилюминесценции включают применение красителей на основе физических принципов, описанных для хемилюминесцентных материалов в {D'Agostino RB, Sr., Vasan RS, Pencina MJ, Wolf PA, Cobain M, Massaro JM, et al. General cardiovascular risk profile for use in primary care: the Framingham Heart Study. Circulation. 2008;117(6):743-53. Epub 2008/01/24}. Предпочтительными хемилюминесцентными красителями являются сложные эфиры акридиния.
Как упоминается в настоящем описании, "анализ" или "диагностический анализ" может представлять собой анализ любого типа, используемый в области диагностики. Такой анализ может быть основан на связывании анализируемого соединения, подлежащего обнаружению, с одним или несколькими улавливающими зондами с определенной аффинностью. Что касается взаимодействия между улавливающими молекулами и молекулами-мишенями или представляющими интерес молекулами, константа аффинности предпочтительно превышает 108 M-1.
В контексте настоящего изобретения "связывающие молекулы" представляют собой молекулы, которые можно использовать для связывания молекул-мишеней или представляющих интерес молекул, т.е. анализируемых соединений (т.е. в контексте настоящего изобретения hGH и/или его изомеров) из образца. Таким образом, связывающие молекулы должны иметь надлежащую форму, как пространственно, так и с точки зрения поверхностных характеристик, таких как заряд поверхности, гидрофобность, гидрофильность, присутствие или отсутствие доноров и/или акцепторов Льюиса, для специфического связывания молекул-мишеней или представляющих интерес молекул. Таким образом, связывание может быть опосредовано, например, ионными, ван-дер-ваальсовыми, пи-пи, сигма-пи, гидрофобными или водородными взаимодействиями или комбинацией двух или более из вышеупомянутых взаимодействий между улавливающими молекулами и молекулами-мишенями или представляющими интерес молекулами. В контексте настоящего изобретения связывающие молекулы могут быть выбраны из группы, например, включающей молекулу нуклеиновой кислоты, молекулу углевода, молекулу PNA, белок, антитело, пептид или гликопротеин. Предпочтительно, связывающие молекулы представляют собой антитела, включая их фрагменты, с достаточной аффинностью к мишени или представляющей интерес молекуле, и включая рекомбинантные антитела или рекомбинантные фрагменты антител, а также химически и/или биохимически модифицированные производные указанных антител или фрагментов, происходящие из вариантов цепей длиной по меньшей мере 12 аминокислот.
Хемилюминесцентная метка может представлять собой метку на основе сложного эфира акридиния, стероидные метки, включая изолюминоловые метки, и т.п.
Ферментные метки могут представлять собой лактатдегидрогеназу (LDH), креатинкиназу (CPK), щелочную фосфатазу, аспартатаминотрансферазу (AST), аланинаминотрансферазу (ALT), кислую фосфатазу, глюкоза-6-фосфатдегидрогеназу и т.д.
В одном варианте осуществления изобретения по меньшей мере одно из указанных двух связывающих соединений связано с твердой фазой, такой как магнитные частицы и полистироловые поверхности.
В одном варианте осуществления анализов для определения уровня гормона роста (hGH) и/или его изоформ в образце в соответствии с настоящим изобретением, такой анализ представляет собой сэндвич-анализ, предпочтительно, полностью автоматизированный анализ. Он может представлять собой полностью автоматизированный или ручной ELISA. Он может представлять собой так называемый POC-тест (исследование по месту лечения). Примеры автоматизированного или полностью автоматизированного анализа включают анализы, которые можно использовать для одной из следующих систем: Roche Elecsys®, Abbott Architect®, Siemens Centauer®, Brahms Kryptor®, Biomerieux Vidas®, Alere Triage®. Примеры форматов исследования приведены выше.
В одном варианте осуществления анализов для определения уровня гормона роста (hGH) и/или его изоформ в образце в соответствии с настоящим изобретением по меньшей мере одно из указанных двух связывающих соединений является меченным для обнаружения. Примеры меток приведены выше.
В одном варианте осуществления анализов для определения уровня гормона роста (hGH) и/или его изоформ в образце в соответствии с настоящим изобретением по меньшей мере одно из указанных двух связывающих соединений связано с твердой фазой. Примеры твердых фаз приведены выше.
В одном варианте осуществления анализов для определения уровня гормона роста (hGH) и/или его изоформ в образце в соответствии с настоящим изобретением указанная метка выбрана из группы, включающей хемилюминесцентную метку, ферментную метку, флуоресцентную метку, радиоактивную йодную метку.
Кроме того, настоящее изобретение относится к набору, включающему систему анализа в соответствии с настоящим изобретением, где компоненты указанной системы анализа могут находиться в одном или нескольких контейнерах.
В одном варианте осуществления изобретения уровень hGH и/или его изоформ определяют с помощью масс-спектрометрии.
В одном конкретном варианте осуществления указанные способы в соответствии с настоящим изобретением используют для мониторинга сосудистого риска у указанного индивидуума. Таким образом, настоящее изобретение также относится к способу определения по меньшей мере два раза, предпочтительно ежегодно, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), включающему стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, и
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови с заданным пороговым значением, и
- где в случае, когда установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, тогда индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), и
- где в случае, когда установленный уровень hGH и/или его изоформ является более низким, чем указанный заданный пороговый уровень, тогда индивидуума идентифицируют как не имеющего сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
В указанном способе мониторинга упомянутые выше стадии способа проводят по меньшей мере один раз в год.
Кроме того, в одном варианте осуществления изобретения способ в соответствии с настоящим изобретением может включать:
- рекомендацию введения антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- рекомендацию воздержаться от терапии антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
Кроме того, в одном варианте осуществления изобретения способ в соответствии с настоящим изобретением может включать:
- введение антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- воздержание от терапии антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
В одном варианте осуществления изобретения лекарственное средство от гипертензии выбрано из группы, включающей ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB) и блокатор бета-адренорецепторов (бета-блокатор), статины и их комбинацию, а также комбинацию с другими лекарственными средствами, например, такими как диуретики.
В одном варианте осуществления изобретения ингибитор ангиотензинпревращающего фермента (ингибитор ACE) выбран из группы, включающей беназеприл, каптоприл, цилазаприл, эналаприл, фосиноприл, имидаприл, лизиноприл, моэксиприл, периндоприл, квинаприл, рамиприл, спираприл, трандолаприл и зофеноприл.
В одном варианте осуществления изобретения блокатор рецепторов ангиотензина (ARB) выбран из группы, включающей азилсартан, азилсартанмедоксомил, кандесартан, кандесартанцилексетил, эпросартан, фимасартан, ирбесартан, лозартан, милфасартан, олмесартан, помисартан, пратосартан, риписартан, саприсартан, тасосартан, телмисартан и валсартан.
В одном варианте осуществления изобретения блокатор бета-адренорецепторов (бета-блокатор) выбран из группы, включающей атенолол, бизопролол, метопролол, небиволол, эсмолол, бетоксалол, ацебутолол, целипролол, пропранолол, бупранолол, тимолол, карведилол, соталол, надолол, пиндолол, окспренолол, алпренолол и картеолол.
В одном варианте осуществления изобретения статин выбран из группы, включающей аторвастатин, флувастатин, ловастатин, питавастатин, правастатин, розувастатин, симвастатин, церивастатин и мервастатин (компактин) и их комбинации, а также комбинации с другими лекарственными средствами.
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и где указанный индивидуум идентифицирован способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, и где индивидуум способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств и где указанный индивидуум не имеет гипертензию.
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изформ превышает указанное пороговое значение, и где указанный индивидуум идентифицирован способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, и где указанный индивидуум не имеет гипертензию и где указанный ингибитор ангиотензинпревращающего фермента (ингибитор ACE) выбран из группы, включающей беназеприл, каптоприл, цилазаприл, эналаприл, фосиноприл, имидаприл, лизиноприл, моэксиприл, периндоприл, квинаприл, рамиприл, спираприл, трандолаприл и зофеноприл.
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и где указанный индивидуум идентифицирован способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств и где указанный индивидуум не имеет гипертензии и где указанный блокатор рецепторов ангиотензина (ARB) выбран из группы, включающей азилсартан, азилсартанмедоксомил, кандесартан, кандесартанцилексетил, эпросартан, фимасартан, ирбесартан, лозартан, милфасартан, олмесартан, помисартан, пратосартан, риписартан, саприсартан, тасосартан, телмисартан и валсартан.
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и где указанный индивидуум идентифицирован способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, и где указанный индивидуум не имеет гипертензии и где указанный статин выбран из группы, включающей: аторвастатин, флувастатин, ловастатин, питавастатин, правастатин, розувастатин, симвастатин, церивастатин и мервастатин (компактин).
Настоящее изобретение относится к антигипертензивному лекарственному средству (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и где указанный индивидуум идентифицирован способами по настоящему изобретению как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, и где указанный индивидуум не имеет гипертензии и где указанный блокатор бета-адренорецепторов (бета-блокатор) выбран из группы, включающей атенолол, бизопролол, метопролол, небиволол, эсмолол, бетоксалол, ацебутолол, целипролол, пропранолол, бупранолол, тимолол, карведилол, соталол, надолол, пиндолол, окспренолол, алпренолол и картеолол.
Большинство из описанных выше активных соединений может быть составлено в различных солевых формах. Фармацевтически приемлемые соли можно получать с использованием обычных методик. Таким образом, изобретение также относится ко всем фармацевтически приемлемым солям вышеупомянутых активных соединений.
Такие солевые формы могут представлять собой обычные соли щелочных металлов и кислотно-аддитивные соли, полученные путем конвертирования с помощью соответствующих органических или неорганических кислот. Кислоты, которые образуют соли активных соединений, включают серную кислоту, сульфоновую кислоту, фосфорную кислоту, азотистую кислоту, азотную кислоту, перхлорную кислоту, бромистоводородную кислоту, хлористоводородную кислоту, муравьиную кислоту, уксусную кислоту, пропионовую кислоту, янтарную кислоту, щавелевую кислоту, глюкуроновую кислоту (в левовращающей и правовращающей форме), молочную кислоту, яблочную кислоту, виннокаменную кислоту, (гидроксималоновую, гидроксипропионоваядиугольную кислоту), фумаровую кислоту, лимонную кислоту, аскорбиновую кислоту, малеиновую кислоту, малоновую кислоту, гидроксималеиновую кислоту, пировиноградную кислоту, фенилуксусную кислоту (o-, м-, п-) толуиловую кислоту, бензойную кислоту, п-аминобензойную кислоту, салициловую, п-аминосалициловую кислоту, метилсульфоновую, этилсульфоновую, гидроксиметилсульфоновую кислоту, этиленсульфоновую кислоту, п-толуолсульфоновую, нафталинсульфоновую, нафтиламиносульфоновую кислоту, сульфаниловую кислоту, камфорсульфоновую кислоту, хинную кислоту, o-метилминдальную кислоту, пикриновую кислоту (2,4,6-тринитрофенол), адипиновую кислоту, аминокислоты, такие как метионин, триптофан, аргинин и особенно кислые аминокислоты, такие как глутамин или аспарагиновая кислота.
В случае, когда в указанных активных соединениях присутствуют кислотные заместители, также можно получать основно-аддитивные соли, в частности, с щелочными металлами, а также с аминокислотами. Таким образом, предусматриваются соли щелочных металлов, таких как соль натрия, калия, лития, или соль магния, кальция, алкиламиносоли или соли, образованные с аминокислотами, например, с такими аминокислотами, как щелочной лизин.
Предпочтительные конкретные соли в соответствии с изобретением выбирают из группы, включающей сульфат, бисульфат, нитрат, фосфат, гидрофосфат, гидрохлорид, гидробромид, гидройодид, ацетат, тартрат, лактат, цитрат, глюконат, фумарат, малеат, гидроксилмалеат, сукцинат, памоат, бензоат, пропионат, пируват, оксалат, малонат, циннамат, салицилат, алкилсульфонат, арилсульфонат и аралкилсульфонат.
Подходящими солями активных соединений являются все кислотно-аддитивные соли или все соли с основаниями. Конкретно могут быть упомянуты фармакологически переносимые неорганические и органические кислоты и основания, традиционно используемые в фармацевтике.
Подходящими солями являются, с одной стороны, нерастворимые в воде и, особенно, растворимые в воде кислотно-аддитивные соли с кислотами, например, такими как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, азотная кислота, серная кислота, уксусная кислота, лимонная кислота, D-глюконовая кислота, бензойная кислота, 2-(4-гидроксибензоил)бензойная кислота, масляная кислота, сульфосалициловая кислота, малеиновая кислота, лауриновая кислота, яблочная кислота такая как (-)-L-яблочная кислота или (+)-D-яблочная кислота, фумаровая кислота, янтарная кислота, щавелевая кислота, виннокаменная кислота, такая как (+)-L-виннокаменная кислота или (-)-D-виннокаменная кислота или мезо-виннокаменная кислота, эмбоновая кислота, стеариновая кислота, толуолсульфоновая кислота, метансульфоновая кислота или 3-гидрокси-2-нафтойная кислота, причем кислоты используются при получении соли - в зависимости от того, является ли кислота одноосновной или многоосновной и в зависимости от того, какая соль является желательной - в эквимолярном количественном соотношении или в другом соотношении. Кроме того, пригодными солями вышеупомянутых активных соединений являются глутамат и аспартат.
Фармакологически непереносимые соли, которые могут быть получены, например, в качестве продуктов или побочных продуктов процесса получения соединений в соответствии с настоящим изобретением в промышленном масштабе, конвертируют в фармакологически переносимые соли способами, известными специалисту в данной области.
Термин "фармацевтически приемлемый" в контексте изобретения означает, что соответствующие производные, функциональные эквиваленты, соли, сольваты, гидраты, эксципиенты, носитель, разбавители и растворители согласно изобретению являются безопасными и эффективными для применения у млекопитающих и обладают желаемой биологической активностью и/или функцией, соответственно.
Ниже приведены отдельные варианты осуществления изобретения:
1) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), включающий стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, и
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови с заданным пороговым значением, и
- где в случае, когда установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, тогда индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), и
- где в случае, когда установленный уровень hGH и/или его изоформ является более низким, чем указанный заданный пороговый уровень, тогда индивидуума идентифицируют как не имеющего сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
2) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно положению 1, где указанный индивидуум не имеет гипертензии (по меньшей мере >140 мм рт. ст. (систолическое) на 90 мм рт. ст. (диастолическое)).
3) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно положению 1 или 2, где указанный образец крови взят от индивидуума, которого еще не лечили антигипертензивными лекарственными средствами.
4) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно положению 1, 2 или 3, где снижение сосудистого риска путем понижения кровяного давления у индивидуума означает предупреждение тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у указанного индивидуума.
5) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из положений 1-4, где указанный индивидуум никогда не имел тяжелого неблагоприятного сердечно-сосудистого явления и никогда не имел никакого сердечно-сосудистого заболевания.
6) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из положений 1-4, где указанный индивидуум имел острый инфаркт миокарда или острую сердечную недостаточность в пределах последних 2 недель, предпочтительно в пределах последней одной недели, предпочтительно в пределах последних 36 часов.
7) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из положений 1-6, где указанное антигипертензивное лекарственное средство выбрано из группы, включающей ингибитор ангиотензинпревращающего фермента (ACE ингибитор), блокатор рецепторов ангиотензина (ARB) и блокатор бета-адренорецепторов (бета-блокатор), статины или их комбинации.
8) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где образец крови выбран из группы, включающей цельную кровь, сыворотку и плазму.
9) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где образец крови представляет собой образец, взятый натощак.
10) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где способ измерения, который используют для определения уровня hGH и/или его изоформ, имеет чувствительность по меньшей мере 50 пг/мл.
11) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где способ измерения, который используют для определения уровня hGH и/или его изоформ, представляет собой иммуноанализ, обладающий чувствительностью анализа по меньшей мере 50 пг/мл.
12) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где заданный пороговый уровень составляет 1370 пг/мл, предпочтительно 330 пг/мл.
13) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из положений 1-12, где уровень hGH и/или его изоформ определяют с помощью иммуноанализа, который включает по меньшей мере два антитела, которые связываются с hGH и/или его изоформами.
14) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно положению 11, где каждое из по меньшей мере двух антител, которые связываются с hGH и/или его изоформами, обладают аффинностью в отношении hGH и/или его изоформ, которая составляет по меньшей мере 108 M-1.
15) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где указанный способ используют для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления, и/или сердечно-сосудистого заболевания, и/или предварительной стадии сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у указанного индивидуума, выбранных из группы, включающей сердечную недостаточность, атеросклероз, гипертензию, кардиомиопатию, инфаркт миокарда и инсульт.
16) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где способ дополнительно включает:
- рекомендацию введения антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- рекомендацию воздержаться от терапии антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
17) Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств согласно любому из предшествующих положений, где способ дополнительно включает:
- введение антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- воздержание от терапии антигипертензивными лекарственными средствами (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины), у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
18) Антигипертензивное лекарственное средство (например ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения в способе предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, и где указанного индивидуума идентифицируют способами согласно любому из положений 1-17 как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
19) Антигипертензивное лекарственное средство (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины) для применения в способе предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, и где указанный индивидуум идентифицирован способами согласно любому из положений 1-17 как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, где указанной индивидуум не имеет гипертензии.
Примеры
Пример 1, анализ us-hGH
Измерение в образцах плазмы проводили с использованием анализа hGH, как описано ранее в WO/2014/108396. Измерение проводили с помощью сверхчувствительного хемилюминесцентного иммуноанализа (см. пример 1, анализ us-hGH). Предел обнаружения составлял 2 пг/мл, функциональная чувствительность анализа составляла 8,5 пг/мл. Результат измерения hGH выражали в нг/мл (1 нг/мл=2,6 мЕ/л).
Химические реагенты
Если нет иных указаний, приобретали химические реагенты категории p.a. от Merck (Darmstadt, Германия).
Антиген
Для иммунизации и для калибровки использовали рекомбинантный гормон роста человека (код NIBSC 98/574, National Institute for Biological Standards and Control, Herfordshire, Великобритания).
Разработка антител
Моноклональные антитела мыши против hGH были разработаны UNICUS (Karlsburg, Германия).
Антитела получали следующим способом:
Мышей BALB/c иммунизировали посредством 100 мкг hGH на 0 и 14 сутки (эмульгированный в 100 мкл полного адъюванта Фрейнда) и 50 мкг на 21 и 28 сутки (в 100 мкл неполного адъюванта Фрейнда). За трое суток до проведения эксперимента по слиянию животным вводили 50 мкг конъюгата, растворенного в 100 мкл физиологического раствора, вводимого в качестве одной внутрибрюшинной и одной внутривенной инъекции.
Спленоциты от иммунизированной мыши и клетки миеломной клеточной линии SP2/0 подвергали слиянию с 1 мл 50% полиэтиленгликоля в течение 30 с при 37°C. После промывания клетки высевали в 96-луночные планшеты для культивирования клеток. Гибридные клоны отбирали путем выращивания в среде HAT [культуральная среда RPMI 1640, дополненная 20% эмбриональной телячьей сывороткой и добавкой HAT]. Через две недели среду HAT заменяли средой HT на три пассажа, а затем возвращались к нормальной среде для культивирования клеток.
Супернатанты клеточных культур сначала подвергали скринингу в отношении антигенспецифических IgG-антител через три недели после слияния. Микрокультуры с положительными результатам исследования переносили в 24-луночные планшеты для увеличения в количестве. После повторного исследования выбранные культуры клонировали и переклонировали с использованием способа лимитирующих разведений и определяли изотипы (Lane, R.D. "A short-duration polyethylene glycol fusiontechnique for increasing production of monoclonal antibody-secreting hybridomas", J. Immunol. Meth. 81: 223-228; (1985) - Ziegler, B. et al. "Glutamate decarboxylase (GAD) is not detectable on the surface of rat islet cells examined by cytofluorometry and complement-dependent antibody-mediated cytotoxicity of monoclonal GAD antibodies", Horm. Metab. Res. 28: 11-15, (1996)).
Получение моноклональных антител
Авторы настоящего изобретения выбрали 5 антител для дальнейшего исследования.
Антитела получали стандартными способами получения антител (Marx et al., Monoclonal Antibody Production (1997), ATLA 25, 121) и очищали хроматографией с белком A. Чистота антител составляла >95%, исходя из анализа с помощью SDS гель-электрофореза.
Мечение и нанесение антител
Все антитела метили сложным эфиром акридиния по следующей методике:
Меченное соединение (метка): 100 мкг (100 мкл) антитела (1 мг/мл в PBS, pH 7,4) смешивали с 10 мкл акридиния NHS-сложного эфира (1 мг/мл в ацетонитриле, InVent GmbH, германия) (EP 0353971) и инкубировали в течение 20 мин при комнатной температуре. Меченное антитело очищали ВЭЖХ с гель-фильтрацией на Bio-Sil SEC 400-5 (Bio-Rad Laboratories, Inc., США) Очищенное меченое антитело разбавляли в (300 ммоль/л фосфата калия, 100 ммоль/л NaCl, 10 ммоль/л Na-EDTA, 5 г/л бычьего сывороточного альбумина, pH 7,0). Конечная концентрация составляла приблизительно 800000 относительных световых единиц (RLU) меченого соединения (приблизительно 20 нг меченого антитела) на 200 мкл. Хемилюминесцению сложного эфира акридиния измеряли с использованием AutoLumat LB 953 (Berthold Technologies GmbH & Co. KG).
Антитело твердой фазы (нанесенное антитело):
Твердая фаза: Полистироловые пробирки (Greiner Bio-One International AG, Австрия) покрывали (18 ч при комнатной температуре) антителом (1,5 мкг антитела/0,3 мл 100 ммоль/л NaCl, 50 ммоль/л Tris/HCl, pH 7,8). После блокирования 5% бычьим сывороточным альбумином пробирки промывали PBS, pH 7,4, и сушили в вакууме.
Иммуноанализ hGH:
50 мкл образца (или калибратора) распределяли пипетками в покрытые пробирки, после добавления меченного антитела (200 мкл) пробирки инкубировали в течение 2 ч при 18-25°C. Не связавшуюся метку удаляли путем промывания 5 раз (каждый раз по 1 мл) раствором для промывания (20 ммоль/л PBS, pH 7,4, 0,1% Triton X 100). Измерение количества связавшегося с пробиркой меченого антитела проводили с использованием LB 953. Использовали фиксированную концентрацию hGH, составлявшую 1 нг/мл. Соотношение сигнала (RLU в концентрации 1 нг hGH/мл) и шума (RLU без us-hGH) для различных комбинаций антител приведено ниже. Все антитела были способны генерировать сэндвич-комплекс с любым другим антителом. Затем пару антител с наиболее высоким соотношением сигнала и шума (наилучшей чувствительностью) использовали для проведения иммуноанализа us-hGH: антитело против hGH G12 использовали в качестве нанесенного на пробирку антитела и антитело против hGH H4 использовали в качестве меченого антитела.
Результаты определения соотношения сигнала и шума для различных пар антител против hGH
Калибровка:
Калибровку анализа проводили с использованием разведений рекомбинантного hGH (международный стандарт ВОЗ, код NIBSC 98/574), разбавленного в 20 мМ K2PO4, с 6 мМ EDTA, 0,5% BSA, 50 мкМ амастатином, 100 мкМ лейпептином, pH 8,0 (фиг.1).
Описание анализа
Аналитическая чувствительность анализа (среднее значение относительных световых единиц для 20 определений в свободном от hGH образце плюс 2 S.D.) составляла 2 пг/мл hGH и функциональная чувствительность анализа (см. выше) составила 8,5 пг/мл. Выделение и разведение составляли >85% в диапазоне измерений 5-10000 пг/мл hGH. Коэффициент корреляции для N=997 образцов между анализом us-hGH и анализом hGH, специфичным к рекомбинантному hGH (22 кДа), составил r=0,98, и r, составляющий 0,95, был определен для анализа, предпочтительно распознающего изоформы hGH, естественным образом продуцированные гипофизом (Bidlingmaier M, Suhr J, Ernst A, Wu Z, Keller A, Strasburger CJ, et al. High-sensitivity chemiluminescence immunoassays for detection of growth hormone doping in sports. Clinical chemistry. 2009;55(3):445-53. Epub 2009/01/27). Эти данные указывают на пригодность измерений всех изоформ hGH в рамках настоящего изобретения.
Пример 2. Исследуемая выборка
Авторы настоящего изобретения исследовали 953 пациентов STEMI и NSTEMI, поступивших в University Hospitals of Leicester NHS trust между августом 2004 года и апрелем 2007 года. Это наблюдательное исследование группы согласовывалось с Хельсинкской декларацией и было одобрено местным этическим комитетом; от пациентов получали письменное информированное согласие. AMI диагностировали, если пациент имел уровень сердечного тропонина I выше 99-го процентиля с по меньшей мере одним из следующих: боль в груди длительностью >20 минут или диагностические серийные электрокардиографические изменения, состоящие из новых патологических волн Q или ST-сегмента и изменения T-волны. Пациентов с известной злокачественной опухолью, заместительной терапией почек или хирургической операцией в течение предшествующего месяца, исключали. Оцененную скорость гломерулярной фильтрации (eGFR) вычисляли по упрощенной формуле модификации диеты при почечной болезни (Smilde TD, van Veldhuisen DJ, Navis G, Voors AA, Hillege HL. Drawbacks and prognostic value formulas estimating renal function in patients with chronic heart failure and systolic dysfunction. Circulation 2006;114:1572-80). Всем пациентам проводили стандартное медикаментозное лечение, и реваскуляризацию проводили в соответствии с мнением лечащего врача.
Образцы плазмы: взятие образцов плазмы (антикоагулированных посредством EDTA и апротинина) проводили после отдыха в постели в течение 15 минут сразу после диагностирования и в течение 36 ч после появления симптомов. Плазму хранили при -80°C до анализа в одной партии для слепого определения уровня hGH в плазме.
Пример 3. Анализ
Эффективность лечения пациентов с острым инфарктом миокарда различными лекарственными средствами анализировали в зависимости от концентрации hGH у пациентов, которую определяли в период максимально 36 часов после появления симптомов. Анализируемые лекарственные средства представляли собой a) ингибитор ангиотензинпревращающего фермента (ACE) или блокатор рецепторов ангиотензина (ARB), и b) бета-блокатор. Конечным результатом определения эффективности было появление тяжелых неблагоприятных сердечно-сосудистых явлений (MACE) в течение одного года после появления симптомов. MACE определяли как комбинацию следующих конечных результатов: смерть по любой причине, госпитализация вследствие сердечной недостаточности или повторный острый инфаркт миокарда (re-AMI).
Ингибитор ангиотензинпревращающего фермента (ACE) или блокатор рецепторов ангиотензина (ARB):
Группа пациентов состояла из 953 случаев с 245 конечными результатами в виде MACE в течение 1 года. Различные клинические переменные были ассоциированы с прогнозированием MACE в течение одного года, как определяли с помощью регрессионного анализа Кокса (таблица 1). Когда к статистической модели добавляли концентрации hGH (таблица 2), hGH был независимым прогностическим фактором для MACE, и, неожиданно, также взаимодействие hGH и лечения посредством ACE/ARB. Анализ Каплана-Мейера возникновения MACE в зависимости от лечения посредством ACE/ARB проводили для группы пациентов после разделения на тертили hGH, т.е. пациент с низкой (<330 пг/мл), средней (330-1370 пг/мл) и высокой концентрациями (>1370 пг/мл) hGH. Число MACE для подгрупп представлено в таблице 3. Как показано в таблице 4, эффект лечения посредством ACE/ARB на MACE зависел от тертилей hGH и был значимым только для тертилей 2 и 3 hGH, которые представляют собой среднюю и высокую концентрации hGH. Эффект был более выраженным в 3 тертиле hGH, чем во 2 тертиле hGH. На фиг.2-4 представлены соответствующие графики Каплана-Мейера для трех тертилей hGH.
Таблица 1: Многопараметрический регрессионный анализ Кокса для прогнозирования MACE в пределах 1 года.
Таблица 2: Многопараметрический регрессионный анализ Кокса для прогнозирования MACE в пределах 1 года, включающий hGH и взаимодействие с терапией ACE/ARB
Обобщение обработки случаев MACE в зависимости от лечения ACE/ARB у пациентов с низкой (тертиль 1), средней (тертиль 2) и высокой (тертиль 3) концентрациями hGH.
Таблица 4: Статистическое сравнение эффекта лечения ACE/ARB на MACE в зависимости от тертилей hGH
Бета-блокаторы
В той же группе пациентов многопараметрический регрессионный анализ Кокса выявил также значимое взаимодействие hGH и лечения бета-блокаторами для прогнозирования MACE в пределах 1 года (таблица 5).
Анализ Каплана-Мейера встречаемости MACE в зависимости от лечения бета-блокаторами проводили для выборки пациентов после разделения на тертили hGH, которые относятся к пациентам с низкой, умеренной и высокой концентрациями hGH. Количество MACE для подгрупп представлено в таблице 6. Как показано в таблице 7, эффект лечения бета-блокаторами на MACE зависел от тертилей hGH и был значимым только для тертилей 2 и 3 hGH, т.е. для средней и высокой концентраций hGH. Эффект был более выраженным в тертиле 3 hGH, чем в тертиле 2 hGH. На фиг.5-7 представлены соответствующие графики Каплана-Мейера для трех тертилей hGH.
Таблица 5: Многопараметрический регрессионный анализ Кокса для прогнозирования MACE в пределах 1 года, включающий hGH и взаимодействие с терапией бета-блокатором
Таблица 6
Обобщение обработки случаев MACE в зависимости от лечения бета-блокатором у пациентов с низкой (тертиль 1), средней (тертиль 2) и высокой (тертиль 3) концентрациями hGH.
Таблица 7: Статистическое сравнение эффекта лечения бета-блокатором на MACE в зависимости от тертилей hGH
Характеристики 953 пациентов с AMI согласно тертилям hGH при поступлении приведены в таблице 8
<330
330-1370
>1370
Характеристики 953 пациентов с AMI согласно тертилям hs-GH при поступлении. Числовые данные приведены в качестве n (%). Значения P приведены для критериев Крускала-Уоллиса или Хи-квадрат для непрерывных или категорийных переменных, соответственно. Приведены числа (%) или среднее значение ±SD.
*ARB=Блокатор рецепторов ангиотензина 2
В ходе наблюдения в течение 2 лет произошло 281 MACE, являющихся первичными комбинированными конечными результатами (включая 117 смертей, 71 госпитализаций HF и 93 re-AMI). Пациенты с MACE имели более высокие уровни GH при поступлении (срединное значение [диапазон], 910 [40-26 280] пг/мл) по сравнению с выжившими пациентами без явлений (590 [20-21 600], p<0,0005 с использованием критерия Манна-Уитни). В таблице 8 также иллюстрируется более высокая распространенность MACE у пациентов с более высокими уровнями GH.
В таблице 9 описаны одномерные отношения рисков для различных факторов, способов терапии и биомаркеров, которые влияли на исход MACE через 2 года. В многопараметрическом анализе исследовали отдельные способы терапии и их взаимодействие с уровнями GH. Возраст, класс Killip >1, eGFR оставались во всех моделях независимыми прогностическими факторами вместе с уровнями GH. Терапия бета-блокаторами была ассоциирована с более низкими MACE (p=0,03) и продемонстрировала значительное взаимодействие с уровнями GH (p=0,047, таблица 9). Терапия посредством ACE/ARB также продемонстрировала значительное взаимодействие с уровнями GH (p=0,016, таблица 9).
Анализ выживаемости Каплана-Мейера использовали для визуализации взаимодействий способов терапии с бета-блокатором или ACE/ARB в зависимости от тертилей GH (фиг.8). Для терапии бета-блокатором существовали значимые отличия в показателях MACE между пациентами, которым было назначено это лечение, по сравнению с пациентами, которым не было назначено это лечение, во 2-м (p=0,009) и 3-м тертилях GH (p<0,0005). Для лечения ACE/ARB существовали значимые отличия в показателях MACE между пациентами, которым было назначено это лечение, по сравнению с пациентами, которым не было назначено это лечение, во 2-м (p=0,001) и 3-м тертилях GH (p<0,0005). Напротив, для обоих способов лечения не было отличий в показателях MACE между пациентами, которым было назначено это лечение, или пациентами, которым не было назначено это лечение, в самом низком тертиле GH.
Таблица 9
Регрессионный анализ Кокса для MACE через 2 года после AMI. Результаты многопараметрического анализа представлены для моделей 1 и 2, которые включали клинические переменные и hGH, c взаимодействием hGH с бета-блокаторами (модель 1) или ACE/ARB (модель 2).
Пример 4. Исследование диеты Malmö и злокачественной опухоли
Исследование диеты Malmö и злокачественной опухоли - сердечно-сосудистая выборка (MDC-CC) представляет собой проспективную выборку, исследованную в ранние 90-е. Дальнейшие детали об этом исследовании могут быть найдены в более ранних публикациях (Berglund et al. 1993. Journal of Internal Medicine 233: 45-51). Авторы настоящего изобретения провели кросс-секционный анализ взаимосвязи между hs-GH и толщиной внутренней-средней оболочки (IMT) в MDC-CC. В множественных регрессионных моделях с IMT в качестве зависимой переменной и стандартизованной величиной натурального логарифма hs-GH в качестве независимой переменной, авторы настоящего изобретения проанализировали 4425 индивидуумов из этой выборки с величинами как hs-GH, так и средней IMT в общей сонной артерии (IMTcca), и 3397 участников с величинами максимальной IMT в области бифуркации (IMTbulb). Использовали отдельные модели для IMTcca и IMTbulb, и в них вносили поправку либо на пол и возраст, либо на набор традиционных сердечно-сосудистых факторов риска: пол, возраст, курение на текущий момент, систолическое кровяное давление, антигипертензивная терапия, BMI, LDL-C, HDL-C и сахарный диабет.
Ультразвуковое исследование сонной артерии проводили на исходном уровне. В кратком изложении, заданный участок бифуркации правой сонной артерии сканировали в отношении присутствия бляшек и максимальной IMT в области бифуркации (IMTbulb), и измеряли среднюю IMT в общей сонной артерии (IMTcca). В первоначальной кросс-секционной регрессионной модели из 3397 (1957 женщины, 58%) индивидуумов в MDC-CC hs-GH демонстрировал значимую положительную корреляцию с IMTbulb во всей выборке (P=0,003) и у мужчин (P=0,003) (таблица 10). Эта ассоциация оставалась по существу неизменной при внесении поправки на традиционные сердечно-сосудистые факторы риска (P=0,002 и P=0,005, соответственно). Результаты для женщин не были значимыми. Уровни hs-GH натощак не были ассоциированы с IMTcca у 4425 индивидуумов (2658 женщин, 60%), которые были доступными в этом анализе.
Более высокие уровни hs-GH натощак были ассоциированы с увеличенной IMT в луковице сонной артерии у мужчин. Взаимосвязь между hs-GH и IMT в луковице сонной артерии соответствует предыдущим результатам более высоких величин hs-GH натощак, ассоциированных с сердечно-сосудистым заболеванием, которые также преимущественно наблюдали у мужчин (Hallgren et al. 2014. JACC 64: 1452-1460; Maison et al. 1998. BMJ [Clinical Research ed] 316: 1132-1133). IMTbulb является надежным показателем атеросклероза (Naqvi and Lee. 2014. JACC Cardiovasc Imaging 7: 1025-1038), и эти данные, таким образом, подтверждают гипотезу о связи между hs-GH и сердечно-сосудистыми заболеваниями, опосредуемыми атеросклерозом.
Таблица 10: Линейная регрессия с IMT на исходном уровне в исследовании MDC-CC в качестве зависимой переменной и hs-GH в качестве независимой. В одной приближенной модели вносили поправку на пол и возраст, а в другой модели дополнительно вносили поправку на традиционные сердечно-сосудистые факторы риска.
Приближенные модели с внесенной поправкой на пол и возраст. В модель с внесенной поправкой вносили поправку на: пол, возраст, систолическое кровяное давление, антигипертензивную терапию, сахарный диабет, курение в текущий момент, BMI, LDL-C и HDL-C. Коэффициенты β выражены в качестве приращения стандартизованных величин натурального логарифма IMT на 1 приращение стандартизованных величин натурального логарифма hs-GH. Сокращенные обозначения: IMTcca, среднее значение толщины средней оболочки в общей сонной артерии. IMTbulb, максимальная величина толщины средней оболочки в области бифуркции сонной артерии.
Пример 5, BCAPS
Описание исследования
Исследование снижения уровня холестерина β-блокаторами на бессимптомные бляшки (BCAPS) представляло собой рандомизированное, двойное слепое, плацебо-контролируемое одноцентровое клиническое испытание, которое происходило между 1994 и 1999 годами. Подробное описание BCAPS может быть найдено в оригинальной статье (Hedblad et al. 2001. Circulation 103: 1721-1726), в настоящем описании приведено только краткое обобщенное изложение. Исходная исследуемая выборка состояла из 361 мужчин и 432 женщин (всего n=793) в возрасте от 49 до 70 лет, привлеченных из MDC-CC. Индивидуумы, включенные в BCAPS, имели бляшку в правой сонной артерии, но не имели симптомов болезни сонных артерий. Критериями исключения были: инфаркт миокарда, стенокардия или инсульт в течение предшествующих 3 месяцев; предшествующая хирургическая операция в правой сонной артерии; регулярное применение β-блокаторов или статинов; кровяное давление >160 (систолическое) или >95 (диастолическое) мм рт. ст.; общий холестерин >8,0 ммоль/л; гипергликемия, предположительно требующая лечения инсулином; и состояния, которые по мнению исследователя делали участника непригодным для испытания.
Все участники предоставляли письменное согласие, и исследование было одобрено этическим комитетом Lund University.
Исследование состояло из 4 различных групп лечения и участников случайным образом распределяли в 1 из следующих групп: плацебо/плацебо, метопролол CR/XL (25 мг один раз в сутки)/плацебо, флувастатин (40 мг один раз в сутки)/плацебо или метопролол CR/XL (25 мг один раз в сутки)/флувастатин (40 мг один раз в сутки).
Период лечения составлял 36 месяца. Взятие образцов крови, полученных натощак, проводили на исходном уровне и через 12, 24 и 36 месяцев. Количественное определение HDL-C, общего холестерина и TG проводили по стандартным методикам в Department of Clinical Chemistry, University Hospital of Malmö. Уровни LDL-C вычисляли по формуле Фридвальда. Уровни GH измеряли в сохраненных образцах плазмы, взятых натощак, который были сразу заморожены до -80°C при различных обследованиях. Ряд образцов, сохраненных в морозильной камере, отсутствовал или имел недостаточное количество плазмы для анализа hs-GH. Индивидуумов, у которых либо исходная величина GH, либо величина GH через 12 месяцев, отсутствовала, исключали из дальнейшего анализа. После внесения поправок исследование состояло из 472 индивидуумов. Количественное определение во всех образцах проводили с использованием иммуноанализа hs-hGH, как описано выше.
Ультразвуковое исследование
Ультразвуковое исследование сонной артерии проводили на исходном уровне, через 18 и 36 месяцев (Hedblad et al. 2001. Circulation 103: 1721-1726). В кратком изложении, заданный участок в области бифуркации правой сонной артерии сканировали в отношении наличия бляшек, и измеряли максимальную IMT в области бифуркации (IMTbulb) и среднюю IMT в общей сонной артерии (IMTcca).
Статистический анализ
В анализах, в которых сравнивали группы лечения, группы представляли собой либо 4 группы рандомизации, либо их делили на 2 группы, которые представляли собой флувастатин против не флувастатина (т.е. плацебо) или метопролол против не метопролола. Поскольку известно, что hs-GH натощак различается у мужчин и женщин, все модели выполняли отдельно для мужчин и женщин, а также в комбинации. Во все модели вносили поправки на возраст, пол (если пол не был уже разделен) и натуральный логарифм исходного уровня hs-GH натощак.
Для исследования того, влияло ли на уровень hs-GH натощак лечение флувастатином или метопрололом, авторы настоящего изобретения провели множественный регрессионный анализ с ΔGH (величина исходного уровня, вычтенная из величины через 12 месяцев) в качестве зависимой переменной и группами лечения в качестве независимых переменных.
Затем авторы настоящего изобретения проанализировали, влияет ли hs-GH на эффект лечения различными лекарственными средствами на IMT в серии множественных регрессионных моделей с IMT через 36 месяцев в качестве зависимой переменной. В этих анализах более крупные группы рандомизации использовали для достижения большей мощности. Для оценки этого взаимодействия была создана величина взаимодействия между группами лечения, умноженная на ΔGH или натуральный логарифм hs-GH, в зависимости от модели. Небольшое количество индивидуумов было утрачено в ходе наблюдения, и они не могли выполнить ультразвуковое исследование IMT через 36 месяцев. При анализе IMT, для этих индивидуумов использовали последние значения IMT (т.е. через 18 месяцев), и в анализ вносили поправку на время между измерениями IMT. Кроме того, в модели вносили поправку на натуральный логарифм IMT на исходном уровне.
Все анализы проводили в SPSS (версия 22.0.0, SPSS Inc., Chicago, Ill). Статистически значимым считали 2-стороннее значение P менее 0,05.
Результаты
Исходные характеристики 472 индивидуумов в исследуемой выборке BCAPS представлены в таблице 11. Женщины во всех группах имели более высокие величины hs-GH на исходном уровне по сравнению с мужчинами. Индивидуумы, у которых hs-GH нельзя было измерить вследствие отсутствующих образцов либо на исходном уровне, либо через 12 месяцев, не отличались их исходными характеристиками. Отсутствующие образцы были равномерно распределены по группам лечения, однако чаще в группе отсутствующих образцов было больше образцов мужчин, чем женщин. Это привело к незначительному отличию соотношения мужчины/женщины в двух из четырех групп лечения (таблица 11).
В линейных регрессионных моделях изменение уровней hs-GH через 12 месяцев по сравнению с исходным уровнем (ΔGH) сопоставляли против различных групп лечения (таблица 12). При анализе всей выборки ни один из результатов анализа не был значимым. У мужчин лечение флувастатином/метопрололом имело значимую отрицательную корреляцию c ΔGH по сравнению с плацебо (P=0,015). Также существовала значимая отрицательная корреляция между ΔGH и лечением флувастатином по сравнению с плацебо (P=0,046). Среди женщин корреляция была положительной и значимой для флувастатина/метопролола (P=0,010) и имела пограничную значимость для флувастатина (P=0,051).
Мужчины, которых лечили флувастатином, имели более высокое снижение hs-GH в течение 12 месяцев по сравнению с индивидуумами, которых не лечили флувастатином. У мужчин лечение метопрололом/флувастатином по сравнению с плацебо/плацебо было на значимом уровне ассоциировано с более высоким снижением hs-GH на протяжении лечения в течение 12 месяцев независимо от исходного уровня hs-GH. Более того, когда всех мужчин, которым вводили флувастатин (метопролол/флувастатин и плацебо/флувастатин), сравнивали со всеми индивидуумами без лечения флувастатином, лечение флувастатином также было ассоциировано со снижением hs-GH более чем на 12 месяцев, что указывает, что уровень hs-GH натощак у мужчин снижается путем лечения флувастатином. Однако в этом контексте следует отметить, что изменение hs-GH на протяжении 12 месяцев в группе флувастатин/плацебо не отличалось на значимом уровне от группы плацебо/плацебо.
Таблица 11: Клинические характеристики исследуемой выборки в BCAPS.
Сокращенные обозначения: LDL-C, липопротеин низкой плотности-холестерин; HDL-C, липопротеин высокой плотности-холестерин; IMT, толщина средней оболочки.
Отсутствующие величины IMTbulb: плацебо/плацебо, n=3; метопролол/плацебо, n=3; флувастатин/метопролол, n=5; флувастатин/плацебо, n=8.
Отсутствующие величины HDL-C и LDL-C: плацебо/плацебо, n=1; метопролол/флувастатин n=1.
Таблица 12: Множественные линейные регрессионные модели для ΔGH (12 месяцев-исходный уровень) против различных групп лечения
В модели вносили поправку на: возраст и стандартизованные величины натурального логарифма hs-GH на исходном уровне. Кроме того, вносили поправку на пол в подгруппе "Все".
Использовали три различных модели: во "всех группах" каждую из различных групп лечения сравнивали против плацебо. Во "всех с флувастатином" индивидуумов, которым вводили флувастатин, сравнивали против индивидуумов, которым не вводили флувастатин, и наоборот для "всех с метопрололом". Коэффициенты β выражены как приращение ΔGH для рассматриваемого лекарственного средства по сравнению с плацебо.
Описание чертежей
На фиг.1 представлена типичная кривая доза/сигнал в анализе us-hGH.
Фиг.2: график Каплана-Мейера для эффективности лечения посредством ACE/ARB на MACE у пациентов с концентрациями hGH в 1 тертиле.
Фиг.3: график Каплана-Мейера для эффективности лечения посредством ACE/ARB на MACE у пациентов с концентрациями hGH во 2 тертиле.
Фиг.4: график Каплана-Мейера для эффективности лечения посредством ACE/ARB на MACE у пациентов с концентрациями hGH в 3 тертиле.
Фиг.5: график Каплана-Мейера для эффективности лечения бета-блокатором на MACE у пациентов с концентрациями hGH в 1 тертиле.
Фиг.6: график Каплана-Мейера для эффективности лечения бета-блокатором на MACE у пациентов с концентрациями hGH в 2 тертиле.
Фиг.7: график Каплана-Мейера для эффективности лечения бета-блокатором на MACE у пациентов с концентрациями hGH в 3 тертиле.
Фиг.8: график Каплана-Мейера для эффективности лечения бета-блокатором или ACE/ARB на MACE у пациентов c концентрациями hGH в 1, 2 и 3 тертилях, соответственно.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> sphingotec GmbH
<120> ОПРЕДЕЛЕНИЕ hGH ДЛЯ ПРИМЕНЕНИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ТЯЖЕЛОГО НЕБЛАГОПРИЯТНОГО СЕРДЕЧНО-СОСУДИСТОГО ЯВЛЕНИЯ ИЛИ СЕРДЕЧНО-СОСУДИСТОГО ЗАБОЛЕВАНИЯ У ИНДИВИДУУМА
<130> S75037WO
<150> 14187366.1
<151> 2014-10-01
<160> 4
<170> PatentIn version 3.3
<210> 1
<211> 217
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Ala Thr Gly Ser Arg Thr Ser Leu Leu Leu Ala Phe Gly Leu Leu
1 5 10 15
Cys Leu Pro Trp Leu Gln Glu Gly Ser Ala Phe Pro Thr Ile Pro Leu
20 25 30
Ser Arg Leu Phe Asp Asn Ala Met Leu Arg Ala His Arg Leu His Gln
35 40 45
Leu Ala Phe Asp Thr Tyr Gln Glu Phe Glu Glu Ala Tyr Ile Pro Lys
50 55 60
Glu Gln Lys Tyr Ser Phe Leu Gln Asn Pro Gln Thr Ser Leu Cys Phe
65 70 75 80
Ser Glu Ser Ile Pro Thr Pro Ser Asn Arg Glu Glu Thr Gln Gln Lys
85 90 95
Ser Asn Leu Glu Leu Leu Arg Ile Ser Leu Leu Leu Ile Gln Ser Trp
100 105 110
Leu Glu Pro Val Gln Phe Leu Arg Ser Val Phe Ala Asn Ser Leu Val
115 120 125
Tyr Gly Ala Ser Asp Ser Asn Val Tyr Asp Leu Leu Lys Asp Leu Glu
130 135 140
Glu Gly Ile Gln Thr Leu Met Gly Arg Leu Glu Asp Gly Ser Pro Arg
145 150 155 160
Thr Gly Gln Ile Phe Lys Gln Thr Tyr Ser Lys Phe Asp Thr Asn Ser
165 170 175
His Asn Asp Asp Ala Leu Leu Lys Asn Tyr Gly Leu Leu Tyr Cys Phe
180 185 190
Arg Lys Asp Met Asp Lys Val Glu Thr Phe Leu Arg Ile Val Gln Cys
195 200 205
Arg Ser Val Glu Gly Ser Cys Gly Phe
210 215
<210> 2
<211> 202
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Met Ala Thr Gly Ser Arg Thr Ser Leu Leu Leu Ala Phe Gly Leu Leu
1 5 10 15
Cys Leu Pro Trp Leu Gln Glu Gly Ser Ala Phe Pro Thr Ile Pro Leu
20 25 30
Ser Arg Leu Phe Asp Asn Ala Met Leu Arg Ala His Arg Leu His Gln
35 40 45
Leu Ala Phe Asp Thr Tyr Gln Glu Phe Asn Pro Gln Thr Ser Leu Cys
50 55 60
Phe Ser Glu Ser Ile Pro Thr Pro Ser Asn Arg Glu Glu Thr Gln Gln
65 70 75 80
Lys Ser Asn Leu Glu Leu Leu Arg Ile Ser Leu Leu Leu Ile Gln Ser
85 90 95
Trp Leu Glu Pro Val Gln Phe Leu Arg Ser Val Phe Ala Asn Ser Leu
100 105 110
Val Tyr Gly Ala Ser Asp Ser Asn Val Tyr Asp Leu Leu Lys Asp Leu
115 120 125
Glu Glu Gly Ile Gln Thr Leu Met Gly Arg Leu Glu Asp Gly Ser Pro
130 135 140
Arg Thr Gly Gln Ile Phe Lys Gln Thr Tyr Ser Lys Phe Asp Thr Asn
145 150 155 160
Ser His Asn Asp Asp Ala Leu Leu Lys Asn Tyr Gly Leu Leu Tyr Cys
165 170 175
Phe Arg Lys Asp Met Asp Lys Val Glu Thr Phe Leu Arg Ile Val Gln
180 185 190
Cys Arg Ser Val Glu Gly Ser Cys Gly Phe
195 200
<210> 3
<211> 179
<212> БЕЛОК
<213> Homo sapiens
<400> 3
Met Ala Thr Gly Ser Arg Thr Ser Leu Leu Leu Ala Phe Gly Leu Leu
1 5 10 15
Cys Leu Pro Trp Leu Gln Glu Gly Ser Ala Phe Pro Thr Ile Pro Leu
20 25 30
Ser Arg Leu Phe Asp Asn Ala Met Leu Arg Ala His Arg Leu His Gln
35 40 45
Leu Ala Phe Asp Thr Tyr Gln Glu Phe Glu Glu Ala Tyr Ile Pro Lys
50 55 60
Glu Gln Lys Tyr Ser Phe Leu Gln Asn Pro Gln Thr Ser Leu Cys Phe
65 70 75 80
Ser Glu Ser Ile Pro Thr Pro Ser Asn Arg Glu Glu Thr Gln Gln Lys
85 90 95
Ser Asn Leu Glu Leu Leu Arg Ile Ser Leu Leu Leu Ile Gln Thr Leu
100 105 110
Met Gly Arg Leu Glu Asp Gly Ser Pro Arg Thr Gly Gln Ile Phe Lys
115 120 125
Gln Thr Tyr Ser Lys Phe Asp Thr Asn Ser His Asn Asp Asp Ala Leu
130 135 140
Leu Lys Asn Tyr Gly Leu Leu Tyr Cys Phe Arg Lys Asp Met Asp Lys
145 150 155 160
Val Glu Thr Phe Leu Arg Ile Val Gln Cys Arg Ser Val Glu Gly Ser
165 170 175
Cys Gly Phe
<210> 4
<211> 171
<212> БЕЛОК
<213> Homo sapiens
<400> 4
Met Ala Thr Gly Ser Arg Thr Ser Leu Leu Leu Ala Phe Gly Leu Leu
1 5 10 15
Cys Leu Pro Trp Leu Gln Glu Gly Ser Ala Phe Pro Thr Ile Pro Leu
20 25 30
Ser Arg Leu Phe Asp Asn Ala Met Leu Arg Ala His Arg Leu His Gln
35 40 45
Leu Ala Phe Asp Thr Tyr Gln Glu Phe Glu Glu Ala Tyr Ile Pro Lys
50 55 60
Glu Gln Lys Tyr Ser Phe Leu Gln Asn Pro Gln Thr Ser Leu Cys Phe
65 70 75 80
Ser Glu Ser Ile Pro Thr Pro Ser Asn Arg Glu Glu Thr Gln Gln Lys
85 90 95
Ser Asn Leu Glu Leu Leu Arg Ile Ser Leu Leu Leu Ile Gln Ser Trp
100 105 110
Leu Glu Pro Val Gln Ile Phe Lys Gln Thr Tyr Ser Lys Phe Asp Thr
115 120 125
Asn Ser His Asn Asp Asp Ala Leu Leu Lys Asn Tyr Gly Leu Leu Tyr
130 135 140
Cys Phe Arg Lys Asp Met Asp Lys Val Glu Thr Phe Leu Arg Ile Val
145 150 155 160
Gln Cys Arg Ser Val Glu Gly Ser Cys Gly Phe
165 170
<---
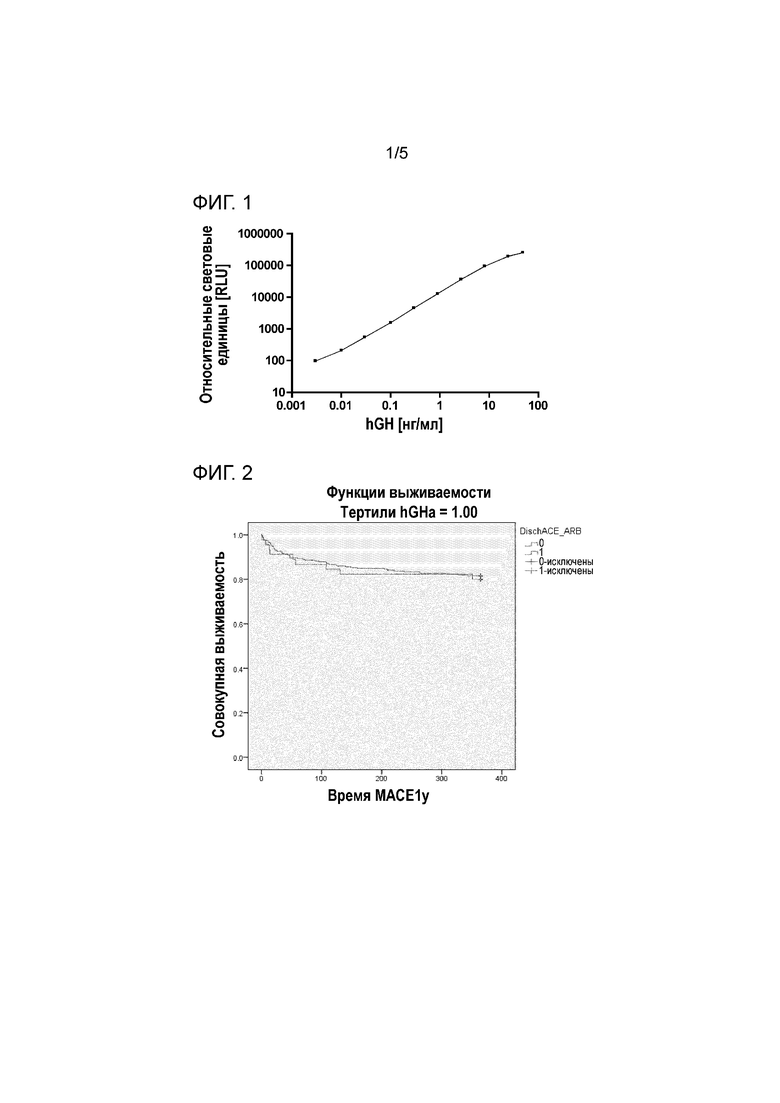




Настоящая группа изобретений относится к медицине, а именно к кардиологии и эндокринологии, и касается предупреждения тяжелого неблагоприятного сердечно-сосудистого явления. Для этого определяют уровень hGH и/или его изоформ в образце крови указанного индивидуума и сравнивают его с заданным пороговым значением. В том случае, когда установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством антигипертензивных лекарственных средств. Это обеспечивает стратификацию пациентов для своевременной фармакотерапии, что, в свою очередь, позволяет предупредить развитие тяжелого течения сердечно-сосудистой патологии.4 н. и 19 з.п. ф-лы, 12 табл., 5 пр., 8 ил.
1. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, включающих ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, включающий стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, и
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови с заданным пороговым значением, и
- где в случае, когда установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, тогда индивидуума идентифицируют как имеющего сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, включающих ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, и
- где в случае, когда установленный уровень hGH и/или его изоформ является более низким, чем указанный заданный пороговый уровень, тогда индивидуума идентифицируют как не имеющего сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, включающих ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины.
2. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по п. 1, где указанный индивидуум не имеет гипертензию (по меньшей мере >140 мм рт.ст. (систолическое) на 90 мм рт.ст. (диастолическое)).
3. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по п. 1 или 2, где образец крови взят от индивидуума, которого еще не лечили антигипертензивными лекарственными средствами.
4. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по пп. 1, 2 или 3, где снижение сосудистого риска путем понижения кровяного давления у индивидуума означает предупреждение тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у указанного индивидуума.
5. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из пп.1-4, где указанный индивидуум никогда не имел тяжелого неблагоприятного сердечно-сосудистого явления и никогда не имел никакого сердечно-сосудистого заболевания.
6. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из пп. 1-4, где указанный индивидуум имел острый инфаркт миокарда или острую сердечную недостаточность в пределах последних 2 недель, предпочтительно в пределах последней одной недели, предпочтительно в пределах последних 36 часов.
7. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из пп. 1-6, где указанное антигипертензивное лекарственное средство выбрано из группы, включающей ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB) и блокатор бета-адренорецепторов (бета-блокатор), статин или их комбинации.
8. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где образец крови выбран из группы, включающей цельную кровь, сыворотку и плазму.
9. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где образец крови представляет собой образец, взятый натощак.
10. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где способ измерения, который используют для определения уровня hGH и/или его изоформ, имеет чувствительность по меньшей мере 50 пг/мл.
11. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где способ измерения, который используют для определения уровня hGH и/или его изоформ, представляет собой иммуноанализ, имеющий чувствительность по меньшей мере 50 пг/мл.
12. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где заданный пороговый уровень представляет собой 330 пг/мл или выше, предпочтительно 1370 пг/мл или выше.
13. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из пп. 1-12, где уровень hGH и/или его изоформ определяют с помощью иммуноанализа, который включает по меньшей мере два антитела, которые связываются с hGH и/или его изоформами.
14. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по п. 11, где каждое из по меньшей мере двух антител, которые связываются с hGH и/или его изоформами, обладает аффинностью в отношении hGH и/или его изоформ, которая составляет по меньшей мере 108 M-1.
15. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где указанный способ используют для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у указанного индивидуума, выбранных из группы, включающей сердечную недостаточность, атеросклероз, гипертензию, кардиомиопатию, инфаркт миокарда и инсульт.
16. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где способ дополнительно включает:
- рекомендацию введения антигипертензивных лекарственных средств, включающих ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- рекомендацию воздержаться от терапии антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
17. Способ определения того, имеет ли индивидуум сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств по любому из предшествующих пунктов, где способ дополнительно включает:
- введение антигипертензивных лекарственных средств, включающих ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, индивидууму, у которого установленный уровень hGH и/или его изоформ превышает указанное заданное пороговое значение, и который идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, или
- воздержание от терапии антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, у индивидуума, у которого установленный уровень hGH и/или его изоформ является более низким, чем указанное заданное пороговое значение, и который идентифицирован как не имеющий сосудистого риска, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
18. Применение антигипертензивного лекарственного средства, включающего ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, и где указанный индивидуум идентифицирован способами по любому из пп. 1-17 как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств.
19. Применение антигипертензивного лекарственного средства, включающего ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, для предупреждения тяжелого неблагоприятного сердечно-сосудистого явления и/или сердечно-сосудистого заболевания у индивидуума, у которого установленный уровень hGH и/или его изоформ превышает указанный заданный пороговый уровень, и где указанный индивидуум идентифицирован способами по любому из пп. 1-17 как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств, где указанный индивидуум не имеет гипертензии.
20. Способ мониторинга ответа на терапию у индивидуума с сосудистым риском, которого лечат антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, включающий стадии:
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, взятом в момент времени X1, с антигипертензивными лекарственными средствами, и
- определение уровня hGH и/или его изоформ в образце крови указанного индивидуума, взятом в момент времени X2, с антигипертензивными лекарственными средствами, и
- где момент времени X1 представляет собой момент времени либо до начала терапии, либо после начала терапии, но в любом случае раньше, чем момент времени X2, и
- где момент времени X2 представляет собой момент времени после начала терапии и в любом случае позже, чем момент времени X1,
- сравнение установленного уровня hGH и/или его изоформ в указанном образце крови, взятом в момент времени X1, с установленным уровнем hGH и/или его изоформ в указанном образце крови, взятом в момент времени X2,
- где более низкий уровень hGH и/или его изоформ в указанном образце крови, взятом в момент времени X2, по сравнению с уровнем hGH и/или его изоформ в указанном образце крови, взятом в момент времени X1, указывает на ответ на терапию.
21. Способ мониторинга ответа на терапию у индивидуума с сосудистым риском, которого лечат антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, по п. 20, где установленный уровень hGH и/или его изоформ в указанном образце крови, взятом в момент времени X1, превышает заданный пороговый уровень, и индивидуум идентифицирован как имеющий сосудистый риск, который может быть снижен посредством терапии, понижающей кровяное давление, с помощью антигипертензивных лекарственных средств (например, ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины).
22. Способ мониторинга ответа на терапию у индивидуума, имеющего сосудистый риск, которого лечат антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, по п. 20 или 21, где момент времени X1 представляет собой момент времени до начала терапии.
23. Способ мониторинга ответа на терапию у индивидуума, имеющего сосудистый риск, которого лечат антигипертензивными лекарственными средствами, включающими ингибитор ангиотензинпревращающего фермента (ингибитор ACE), блокатор рецепторов ангиотензина (ARB), блокатор бета-адренорецепторов (бета-блокатор) и/или статины, по любому из пп. 20-22, где момент времени X2 представляет собой 12 месяцев, 24 месяца или 36 месяцев после момента времени X1.
| РАКОВЫЙ МАРКЕР И ТЕРАПЕВТИЧЕСКАЯ МИШЕНЬ | 2008 |
|
RU2529797C2 |
| MAISON P | |||
| et al | |||
| "Growth hormone as a risk for ptemature mortality in healthy subjects: data from the Paris prospective study" | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Способ амидирования жидких сульфохлоридов ароматического ряда | 1921 |
|
SU316A1 |
| BANGALORE S | |||
| et al | |||
| "Beta-Blockers for primary prevention of heart failure in patients with hypertension" | |||
| Journal of the American college of cardiology, 2008, | |||
Авторы
Даты
2021-01-12—Публикация
2015-10-01—Подача