Изобретение относится к медицине, в частности к хирургии, онкологии, трансплантологии и может быть использовано при проведении методик, связанных с необходимостью изоляции долевого сосудистого кровотока печени и ее селективной перфузии.
В настоящее время разработка комбинированных методов лечения с применением регионарной химиотерапии больных с множественными билобарными поражениями печени остается актуальной проблемой (С.В. Козлов и др., Ю.И. Патютко, 2014). В этой связи, широкое распространение получили методы высокодозной изолированной химиоперфузии печени. (Т. Voron et al. 2013, М.С. Burgmans et al. 2015, T.J. Vogl и др., 2017). Основными недостатками указанных методик являются: вынужденный блок кровотока в нижней полой вене (НПВ) и необходимость формирования кава-кавального шунта, высокая себестоимость проведения закрытых методик и, наконец, утечки перфузата в системный кровоток. Кроме того, в доступной литературе отсутствуют сведения о возможности проведения перфузионных методик, связанных с сосудистой изоляцией одной из долей печени или комбинирования их с хирургическими методами лечения.
Известен способ изолированной перфузии печени (способ изолированной гипертермической химиоперфузии печени, патент РФ №2664631, А61Р 35/00, А61K 38/36, А61K 38/19, А61В 17/00 опубл. 21.09.2018). В этом способе изолируют печень от системного кровотока, формируют перфузионный контур и выполняют перфузию пораженной метастазами печени противоопухолевым препаратом. Однако этот способ не предусматривает возможности перфузии отдельных долей печени, в связи с чем, в ряде случаев, ограничиваются возможности его применения.
Предложен способ изолированной долевой ретроградной перфузии печени в эксперименте, целью которого является выполнение последовательных оперативных приемов, позволяющих изолировать долевой кровоток печени и провести ее селективную перфузию необходимым фармпрепаратом. Данный способ предлагается применять в онкологии, в качестве химиорегионарной терапии как усовершенствованный метод лечения злокачественных поражений или в комбинации с методиками этапных резекций печени, так называемых, операциях «ех vivo», а также в трансплантологии.
Поставленная задача решается тем, что в способе изолированной долевой ретроградной перфузии печени в эксперименте, после эксплантации трупной печени определяют долю для перфузии необходимым препаратом (далее по тексту «перфузируемая доля»); после чего, лигируют круглую связку печени, мобилизуют воротную вену (ВВ), ее правую (ПВ), левую (ЛВ) ветви, собственную печеночную артерию (СПА), ее правую (ПА) и левую (ЛА) ветви и ретропеченочный сегмент (PC) НПВ с перевязкой коротких вен печени; далее, выполняют холецистэктомию; затем, последовательно устанавливают канюли внешним диаметром от 2 до 4 мм в ветвь СПА и канюли внешним диаметром от 6 до 12 мм в ветвь ВВ перфузируемой доли с использованием сосудистых турникетов; после чего, на стороне перфузируемой доли участвующие в венозном оттоке печеночные вены отжимают у их оснований для исключения утечки перфузата в НПВ; далее, формируют перфузионный контур путем присоединения систем притока (от резервуара с перфузатом к препарату) к артериальным канюлям, оттока (от препарата к резервуару) - к венозным, в состав контура также включают резервуар с раствором для перфузии, резервуар для сбора отработанного перфузата на выходе из контура (в случаях формирования разомкнутого контура), перфузионный насос, термостатическую баню и соединители (для подключения инфузионных фильтров, разветвителей, удлинителей, тройников для инфузионных систем); после чего выполняют изолированную ретроградную долевую перфузию печени в режиме: направление перфузии -приток на ветвь СПА, отток от ветви ВВ перфузируемой доли; скорость потока - 110-650 мл/мин, длительность - 20-60 мин, температура перфузата -37-43°С; далее во время перфузии с целью определения междолевой границы и контроля сосудистой изоляции перфузируемой доли вводят растворы различных водорастворимых красителей (например: 0,05% бриллиантового зеленого, 1% сини митиленовой, 0,4% фуксина основного и т.д.) общим объемом 20-50 мл/мин; по завершению перфузии препарат печени подвергают исследованию и утилизируют согласно требованиям руководящих документов.
Технические характеристики канюль, а также состав контура, вводимого раствора и параметры перфузии определяют в зависимости от реальных требований и выбирают оптимальные.
Представленные значения диаметра сосудистых канюль определяются необходимостью поддержания должных скоростных показателей, и не могут быть больше диаметра используемых сосудов. Поскольку создать адекватные гидродинамические условия на трупной ткани затруднительно, то, чем выше диаметр венозной канюли, установленной в ветви ВВ, тем эффективнее отток перфузата из печени и, следовательно, меньше сопротивление току перфузата в сосудистом русле перфузируемой доли. В связи с этим, диаметр канюль в ветвях СПА (4-6 мм) всегда больше такового, чем канюль, установленных в ветви ВВ (6-12 мм). При использовании канюль меньшего диаметра проведение перфузии на препарате печени затруднительно.
Скоростные параметры перфузии были максимально приближены к физиологическим. Однако производилась их поправка с учетом работы на трупной ткани. Так, при скорости менее 110 мл/мин снижалась эффективность перфузии, о чем свидетельствовал характер распространения перфузата по сосудистому руслу. Увеличение же скорости потока перфузата выше 650 мл/мин приводило к повреждению паренхимы трупной печени, что влияло на качество исследования. Длительность перфузии и гипертермия в эксперименте определялась в соответствии с требованиями клинической практики.
Объем вводимого раствора водорастворимого красителя от 20 до 50 мл/мин определялся скоростными показателями перфузии и морфометрическими характеристиками препарата. Однако, введение меньшего объема снижало информативность исследования, что выражалось в слабом окрашивании сосудистого русла. Введение большего объема, по нашим данным, экономически не целесообразно.
Использование данного способа позволяет качественно изолировать долевой кровоток печени с целью проведения ее ретроградной селективной перфузии раствором необходимого препарата. Основным преимуществом способа является простота применения, поскольку он не требует дополнительного поиска путей оттока перфузата и связанного с этим увеличением объема хирургического вмешательства и анестезиологического пособия. Практически весь объем оперативного этапа проводится в воротах печени, без необходимости формирования кава-кавального шунта. С точки зрения анатомо-физиологических особенностей, перфузат стремится по пути наименьшего сопротивления, что объясняет свободный артерио-портальный ток перфузата при блокировании кровооттока по печеночным венам. В тоже время это приводит к минимизации рисков утечки в контралатеральную долю при наличии внутрипеченочных артериальных сообщений. Внедрение данного способа в клиническую практику позволит усовершенствовать прежние и предложить новые методики комбинированного лечения множественных билобарных поражений печени, а также создать основу для использования трансплантационных технологий в абдоминальной, в том числе «ех vivo» хирургии.
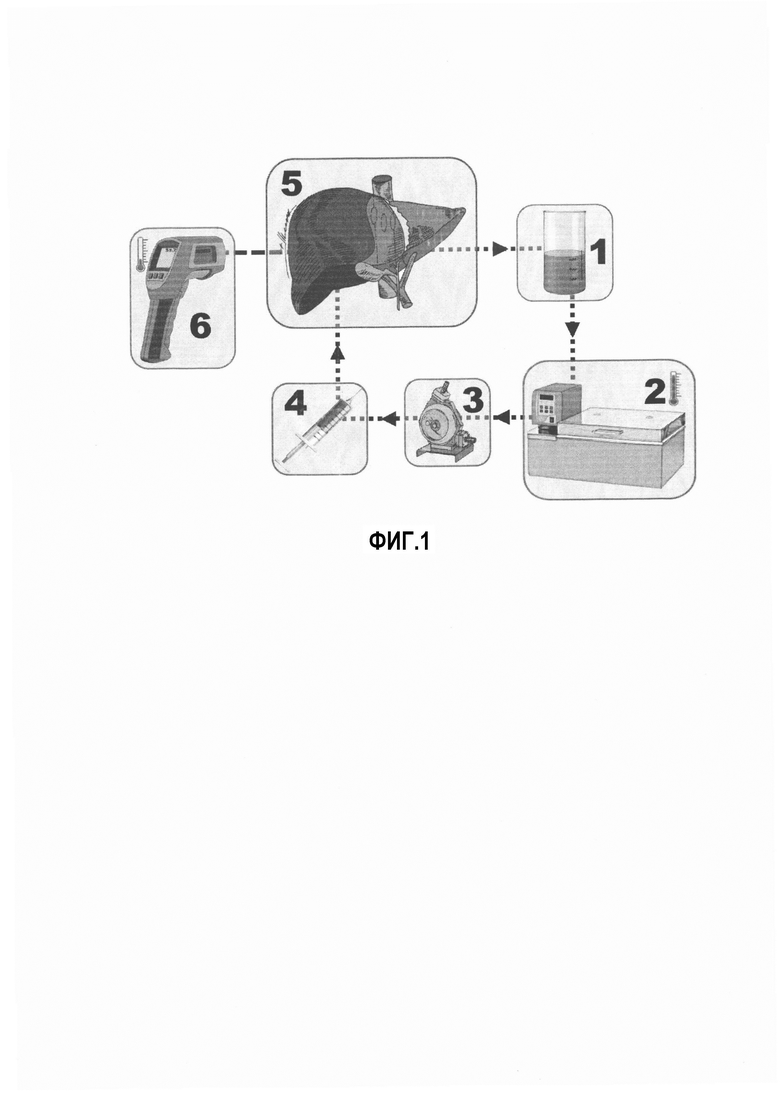
Изобретение поясняется фиг. 1, на которой показана схема перфузионного контура для проведения изолированной долевой ретроградной перфузии печени в эксперименте, и приводятся экспериментальные примеры, которые поясняются фиг. 1, фиг. 2, фиг. 3, фиг. 4.
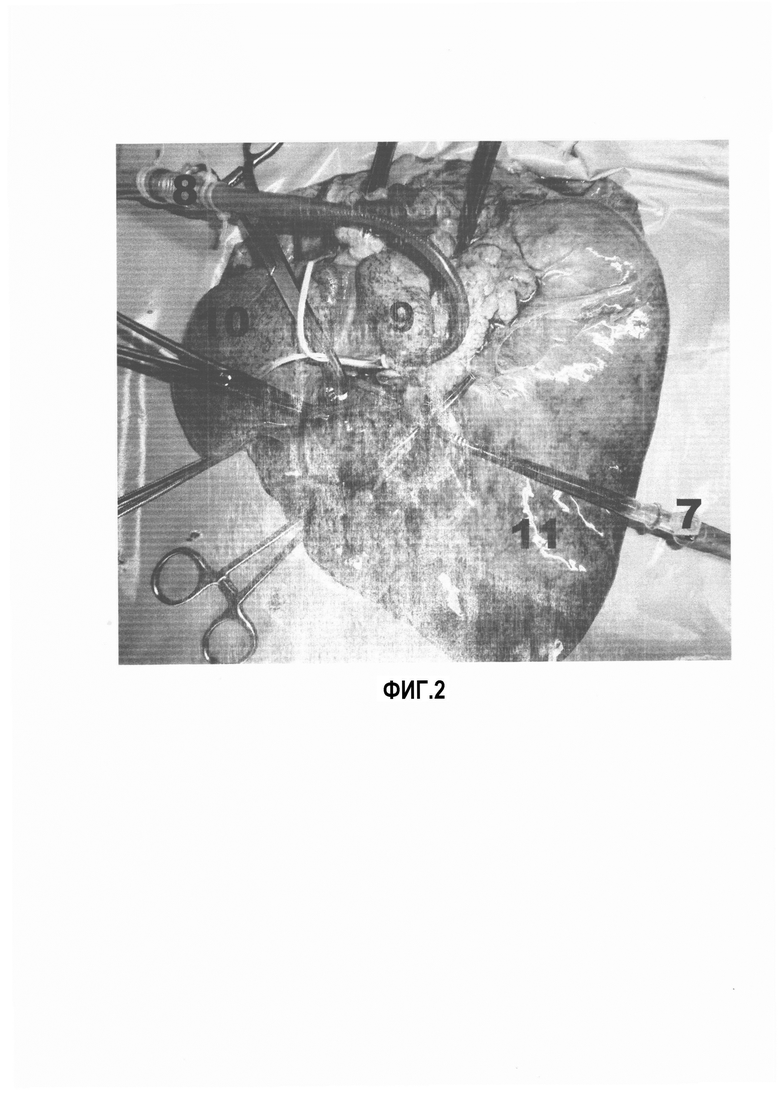
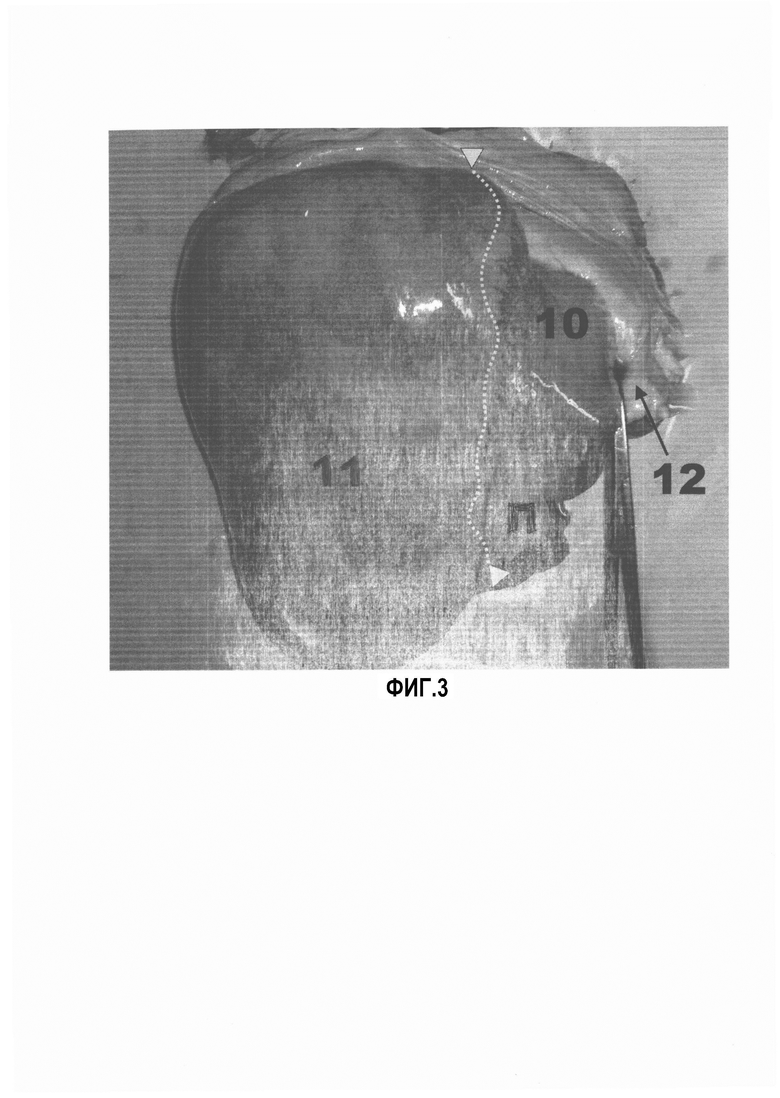
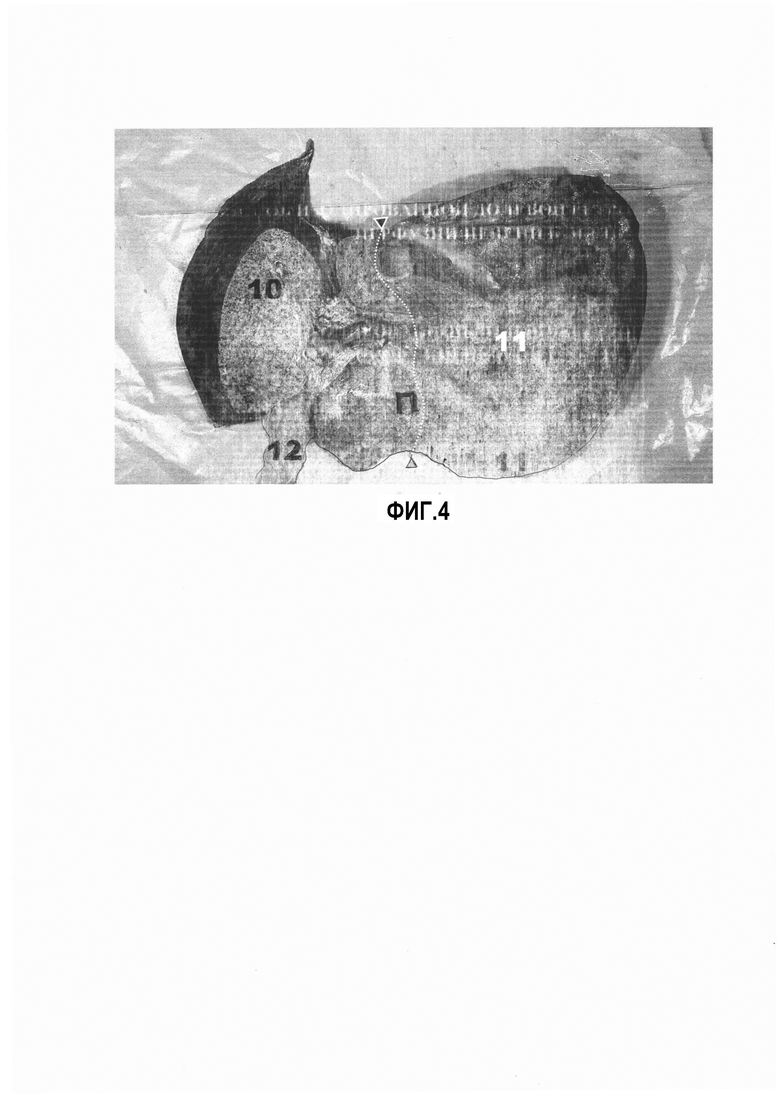
На фиг. 2 продемонстрирован порядок установки сосудистых канюль, их фиксации и характер распространения красителя после проведения изолированной ретроградной перфузии левой доли. На фиг. 3 показан внешний вид препарата со стороны его диафрагмальной поверхности после проведения изолированной ретроградной перфузии левой доли. На фиг. 4 показан препарат, подвергшийся анатомическому исследованию после проведения изолированной ретроградной перфузии правой доли печени.
Как показано на фиг. 1, сначала выполняют подготовку к перфузии препарата печени 5. Далее, формируют перфузионный контур путем присоединения систем притока к канюле, установленной в ветвь СПА, и оттока - к канюле, установленной в ветвь ВВ перфузируемой доли -пунктирные линии со стрелками. В состав контура также включают резервуар с перфузатом 1. По направлению притока раствора к перфузируемой доле устанавливается термостатическая баня 2. Движение перфузата в контуре создает перистальтический (центробежный) насос 3, направление потока обозначено стрелками. При необходимости, инъекции препаратов выполняют посредством соединителей 4. С целью контроля температуры перфузируемой доли, выполняется термометрия 6.
Пример №1 - изолированная ретроградная перфузия левой доли печени. Поясняется фиг. 1, фиг. 2, фиг. 3.
Препарат печени №15 эксплантирован из небальзамированного трупа пациента Р., умершего от заболевания, не связанного напрямую с исследуемым органом.
На первом этапе, после предварительной подготовки препарата, выполнили мобилизацию необходимых сосудистых образований (PC НПВ, ВВ, СПА, их ветви), пережали круглую связку и лигировали короткие вены печени. После чего последовательно установили артериальную канюлю 7 на фиг. 2 в ЛА и венозную канюлю 8 на фиг. 2 в ЛВ (артериальная 6 Fr, венозная канюля 12 Fr Maquet, Германия) с проведением фиксации сосудистыми обтяжками. Для исключения утечки перфузата в НПВ из сосудистого русла левой доли во время перфузии, мобилизовали и пережали основание общего ствола левой, средней печеночных вен.
Вторым этапом сформировали замкнутый перфузионный контур как показано на фиг. 1, в состав которого включили резервуар с перфузатом 1 на фиг. 1, термостатическую баню 2 на фиг. 1., насос перистальтический «LOIP ls-301» (фирмы ОАО «Лабораторное оборудование и приборы», Россия) 3 на фиг. 1, приобретенный при поддержке правительства Санкт-Петербурга (диплом ПСП №18787) и соединители для инъекций 4 на фиг. 1. Контроль подъема температуры оценивали в начале и в конце перфузии с помощью контактного термометра 6 на фиг. 1.
Третьим этапом провели ретроградную изолированную перфузию левой доли печени 10 на фиг. 2, фиг. 3 в следующем режиме: скорость потока - 230 мл/мин, длительность - 34 мин, температура перфузата - 41°С. Во время перфузии, с целью определения междолевой границы и контроля утечки перфузата в правую долю печени 11 на фиг. 2, фиг. 3, в артериальную канюлю 7 на фиг. 2 посредством соединителя для инъекций 4 на фиг. 1 вводили 20 мл/мин 1% раствора сини митиленовой, в результате чего определялась междолевая граница печени - пунктирная линия, ограниченная треугольниками на фиг. 3, которая проходила на расстоянии 4-12 см от серповидной и круглой связки печени 12 на фиг. 3, в проекции линии идущей от правого края вырезки НПВ к правому краю ложа желчного пузыря, проекция которого представлена П на фиг. 2, фиг. 3. На висцеральной поверхности печени выявленная междолевая граница проходила по дорсальной части первого сегмента печени 9 на фиг. 2, непосредственно по средней части собственно ворот печени и по левому краю ложа желчного пузыря, проекция которого П на фиг. 2, 3. Во время процедуры перфузат поступал в артериальное русло через канюлю 7 на фиг. 2 и беспрепятственно выводился через канюлю, установленную в ЛВ 8 на фиг. 2. Утечки красителя в просвет НПВ и в контралатеральную долю при условии наличия положительного гидродинамического давления в перфузируемой доли не наблюдалось. В конце перфузии при выполнении сравнительной термометрии отмечалась значимая разница в показателях между правой (перфузируемой) и левой долями печени.
Далее, с помощью монополярного электрокоагулятора выполнили удаление желчного пузыря, проекция которого обозначена П на фиг. 2, фиг. 3.
По окончанию перфузии препарат подвергли анатомическому исследованию, которое показало распространение красителя лишь в пределах левой доли печени 10 на фиг. 2, фиг. 3.
Пример №2 - изолированная ретроградная перфузия правой доли печени. Поясняется фиг. 1, фиг. 4.
Препарат печени №27 эксплантирован из небальзамированного трупа пациента К., умершего от заболевания, не связанного напрямую с исследуемым органом.
На первом этапе, после предварительной подготовки препарата выполнили мобилизацию необходимых сосудистых образований (PC НПВ, ВВ, СПА, их ветви), лигировали круглую связку и короткие вены печени. После чего последовательно установили артериальную канюлю в ПА и венозную канюлю в ПВ (артериальная 6 Fr, венозная канюля 12 Fr Maquet, Германия) с фиксацией сосудистыми обтяжками. Для исключения утечки перфузата в НПВ из сосудистого русла правой доли во время перфузии, мобилизовали и пережали основание средней и правой печеночных вен.
Вторым этапом сформировали замкнутый перфузионный контур как показано на фиг. 1, в состав которого включили резервуар с перфузатом 1 на фиг. 1, термостатическую баню 2 на фиг. 1., насос перистальтический «LOIP ls-301» (фирмы ОАО «Лабораторное оборудование и приборы», Россия) 3 на фиг. 1, приобретенный при поддержке правительства Санкт-Петербурга (диплом ПСП №18787) и соединители для инъекций 4 на фиг. 1. Контроль подъема температуры оценивали в начале и в конце перфузии с помощью контактного термометра 6 на фиг. 1.
Третьим этапом провели ретроградную изолированную перфузию правой доли печени 11 на фиг. 4 в следующем режиме: скорость потока - 320 мл/мин, длительность - 20 мин, температура перфузата - 37°С. Во время перфузии, с целью определения междолевой границы и контроля утечки перфузата в правую долю печени 11 на фиг. 4, в артериальную канюлю посредством соединителя для инъекций 4 на фиг. 1 вводили 20 мл/мин 1% раствора сини митиленовой, в результате чего определялась междолевая граница печени - пунктирная линия, ограниченная треугольниками на фиг. 4, которая проходила на расстоянии 2-9,5 см от серповидной и круглой связки печени 12 на фиг. 4, в проекции линии идущей от левого края вырезки НПВ к середине ложа желчного пузыря, проекция которого представлена П на фиг. 4. Во время процедуры перфузат поступал через артериальную канюлю, установленную в ПА, и беспрепятственно выводился через канюлю, установленную в ПВ. Утечки красителя в просвет НПВ и в контралатеральную долю при условии наличия положительного гидродинамического давления в перфузируемой доли не наблюдалось. В конце перфузии при выполнении термометрии отмечалась значимая разница в показателях между правой (перфузируемой) и левой долями печени.
Далее, с помощью монополярного электрокоагулятора выполнили удаление желчного пузыря, проекция которого обозначена П на фиг. 4. По окончанию перфузии препарат подвергли анатомическому исследованию, которое показало распространение красителя в пределах правой доли печени 11 на фиг. 4 и его отсутствие в контралатеральной -левой доле 10 на фиг. 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗОЛИРОВАННОЙ ДОЛЕВОЙ АРТЕРИО-КАВАЛЬНОЙ ПЕРФУЗИИ ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ | 2019 |
|
RU2726591C1 |
| СПОСОБ ИЗОЛИРОВАННОЙ ДОЛЕВОЙ ПОРТО-КАВАЛЬНОЙ ПЕРФУЗИИ ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2747908C1 |
| СПОСОБ ИЗОЛИРОВАННОЙ ЛЕВОСТОРОННЕЙ ДОЛЕВОЙ УМБИЛИКО-КАВАЛЬНОЙ ПЕРФУЗИИ ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ | 2021 |
|
RU2765846C1 |
| СПОСОБ ИЗОЛИРОВАННОЙ ЛЕВОСТОРОННЕЙ ДОЛЕВОЙ АРТЕРИО-УМБИЛИКАЛЬНОЙ ПЕРФУЗИИ ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ | 2021 |
|
RU2765017C1 |
| СПОСОБ ИЗОЛИРОВАННОЙ ХИМИОПЕРФУЗИИ ПЕЧЕНИ | 2021 |
|
RU2784944C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ АРТЕРИО-ПОРТО-КАВАЛЬНОЙ ИЗОЛИРОВАННОЙ ХИМИОПЕРФУЗИИ ПЕЧЕНИ | 2023 |
|
RU2826473C2 |
| Способ хирургического лечения рака правой почки с опухолевым тромбозом нижней полой вены тип 3-4 в условиях вено-венозного обходного шунтирования и in situ нормотермической изолированной перфузии печени | 2024 |
|
RU2837006C2 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ ИЗОЛИРОВАННОЙ ГИПЕРТЕРМИЧЕСКОЙ ХИМИОПЕРФУЗИИ ПЕЧЕНИ | 2022 |
|
RU2796774C2 |
| Способ изолированной гипертермической химиоперфузии печени | 2017 |
|
RU2664631C1 |
| СПОСОБ ОДНОВРЕМЕННОЙ АРТЕРИОВЕНОЗНОЙ ГИПЕРТЕРМИЧЕСКОЙ ХИМИОПЕРФУЗИИ ПЕЧЕНИ | 2021 |
|
RU2767705C2 |
Изобретение относится к медицине, в частности к хирургии, онкологии, трансплантологии. После эксплантации трупной печени определяют перфузируемую долю; после чего лигируют круглую связку печени, мобилизуют воротную вену, ее правую и левую ветви, собственную печеночную артерию, ее правую и левую ветви, и ретропеченочный сегмент нижней полой вены с перевязкой коротких вен печени. Далее выполняют холецистэктомию. Затем последовательно устанавливают канюли внешним диаметром от 2 до 4 мм в ветвь собственной печеночной артерии и канюли внешним диаметром от 6 до 12 мм в ветвь воротной вены перфузируемой доли с использованием сосудистых турникетов. После чего на стороне перфузируемой доли участвующие в венозном оттоке печеночные вены отжимают у их оснований для исключения утечки перфузата в нижней полой вене. Далее формируют перфузионный контур путем присоединения систем притока от резервуара с перфузатом к препарату, к артериальным канюлям, оттока - от печени к резервуару - к венозным канюлям, перфузионному насосу, термостатической бане и соединителям для подключения инфузионных фильтров, разветвителей, удлинителей, тройников для инфузионных систем. После чего выполняют изолированную ретроградную долевую перфузию печени в режиме: направление перфузии - приток на ветвь собственной печеночной артерии, отток от ветви воротной вены перфузируемой доли. Скорость потока - 110-650 мл/мин, длительность - 20-60 мин, температура перфузата - 37-43°С. Далее во время перфузии с целью определения междолевой границы и контроля сосудистой изоляции перфузируемой доли вводят раствор водорастворимого красителя общим объемом 20-50 мл/мин. По завершении перфузии препарат печени подвергают исследованию и утилизируют. Способ позволяет создать основу для использования трансплантационных технологий в абдоминальной «ех vivo» хирургии, качественно изолировать долевой кровоток печени с целью проведения ее ретроградной селективной перфузии раствором необходимого препарата, а также не требует дополнительного поиска путей оттока перфузата и связанного с этим увеличения объема хирургического вмешательства и анестезиологического пособия. 4 ил., 2 пр.
Способ изолированной долевой ретроградной перфузии печени в эксперименте, отличающийся тем, что после эксплантации трупной печени определяют перфузируемую долю; после чего лигируют круглую связку печени, мобилизуют воротную вену, ее правую и левую ветви, собственную печеночную артерию, ее правую и левую ветви, и ретропеченочный сегмент нижней полой вены с перевязкой коротких вен печени; далее выполняют холецистэктомию; затем последовательно устанавливают канюли внешним диаметром от 2 до 4 мм в ветвь собственной печеночной артерии и канюли внешним диаметром от 6 до 12 мм в ветвь воротной вены перфузируемой доли с использованием сосудистых турникетов; после чего на стороне перфузируемой доли участвующие в венозном оттоке печеночные вены отжимают у их оснований для исключения утечки перфузата в нижней полой вене; далее формируют перфузионный контур путем присоединения систем притока от резервуара с перфузатом к препарату, к артериальным канюлям, оттока - от печени к резервуару - к венозным канюлям, перфузионному насосу, термостатической бане и соединителям для подключения инфузионных фильтров, разветвителей, удлинителей, тройников для инфузионных систем; после чего выполняют изолированную ретроградную долевую перфузию печени в режиме: направление перфузии - приток на ветвь собственной печеночной артерии, отток от ветви воротной вены перфузируемой доли; скорость потока - 110-650 мл/мин, длительность - 20-60 мин, температура перфузата - 37-43°С; далее во время перфузии с целью определения междолевой границы и контроля сосудистой изоляции перфузируемой доли вводят раствор водорастворимого красителя общим объемом 20-50 мл/мин; по завершении перфузии препарат печени подвергают исследованию и утилизируют.
| Способ изолированной гипертермической химиоперфузии печени | 2017 |
|
RU2664631C1 |
| Рыбаков А.С | |||
| ИЗОЛИРОВАННАЯ ДОЛЕВАЯ АРТЕРИО-ПОРТАЛЬНАЯ ПЕРФУЗИЯ ПЕЧЕНИ В ЭКСПЕРИМЕНТЕ, Известия Российской Военно-медицинской академии | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Т | |||
| Пишущая машина | 1922 |
|
SU37A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| С | |||
| Джино-прядильная машина | 1922 |
|
SU173A1 |
| Тягун В.С | |||
| и др., ОЦЕНКА СОСУДИСТОЙ ИЗОЛЯЦИИ ПРИ ПРОВЕДЕНИИ ЭКСПЕРИМЕНТАЛЬНОЙ АРТЕРИО-УМБИЛИКАЛЬНОЙ ПЕРФУЗИИ ЛЕВОЙ ДОЛИ ПЕЧЕНИ, Белые ночи 2019 | |||
Авторы
Даты
2021-01-15—Публикация
2020-03-05—Подача