Настоящее изобретение относится к новым хелатообразующим агентам, которые могут быть использованы в широком диапазоне значений pH и, в частности, в щелочных или нейтральных средах, и к соответствующим хелатам металлов, в частности, к хелатам железа. Настоящее изобретение также относится к способу получения хелатообразующих агентов и соответствующих хелатов металлов, более конкретно, к получению фенольных аминокислот и их производных, подходящих для применения в качестве хелатообразующих агентов, и к соответствующим хелатам металлов.
Уровень техники
Альфа-имино-о-гидроксифенилуксусные кислоты и их производные следующей общей формулы:
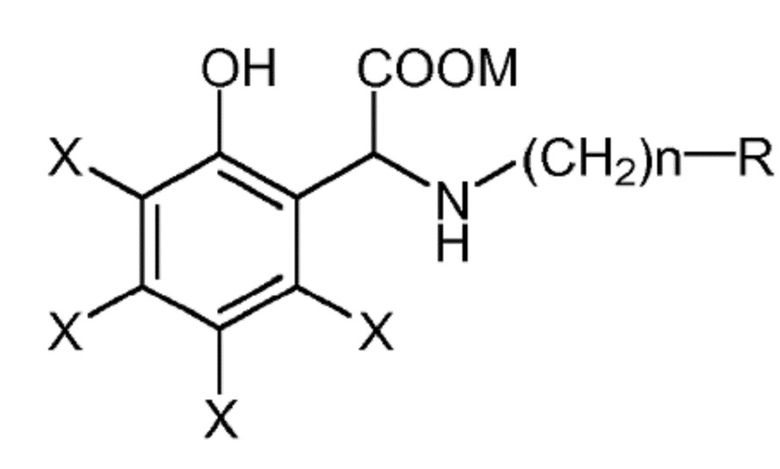
в которой X представляет собой H, -COOH, -NO2, -Cl, -CH3, -NH2 или SO3H; R представляет собой -COOH, -CH2OH, или -SH; n представляет собой целое число от 1 до 10, предпочтительно 1 или 2; и M представляет собой H или катион металла, предпочтительно щелочного металла, или основного органического соединения, такого как амин или аминоспирт, известны в качестве соединений, способных к комплексообразованию с катионами металлов, в частности, с катионами железа, с образованием устойчивых хелатов, подходящих для устранения дефицита указанных металлов в растениях, выращиваемых на кислых и щелочных почвах.
Несколько способов получения вышеупомянутых или родственных соединений раскрыты, например, в документах US3567752, GB1418888 и US3825592. Тем не менее, в указанных документах раскрыты способы, в которых вода и/или другие растворители использованы в качестве растворителя, и некоторые из способов протекают с применением опасных реагентов. Выходы, достигаемые в указанных способах, не являются настолько высокими, насколько это желательно. В частности, в документе US3567752 [2-(о-гидроксифенил)]-2-гидроксиэтилглицин получен в несколько стадий, включая применение 1,2-дихлорэтана в качестве растворителя и цианистого водорода в качестве одного из реагентов.
Несмотря на описания в указанных документах предшествующего уровня техники, предложение улучшенных хелатообразующих соединений по-прежнему представляет собой огромный интерес в промышленности. Кроме того, представляет собой интерес предложение улучшенного способа получения альфа-имино-о-гидроксифенилуксусных кислот и их производных с повышенными выходами и региоселективностями.
Сущность изобретения
Авторы настоящего изобретения обнаружили новые хелатообразующие соединения, которые являются подходящими для применения в обеспечении доступности для растений катионов металлов, в частности, железа. Кроме того, свободный хелатообразующий агент согласно настоящему изобретению может также обеспечивать солюбилизацию и доступность для растений следов металлов, в частности, железа, которые уже присутствуют в почвах, в частности, в кислых и щелочных почвах.
Соответственно, первый аспект настоящего изобретения относится к хелатообразующему соединению формулы (I´):
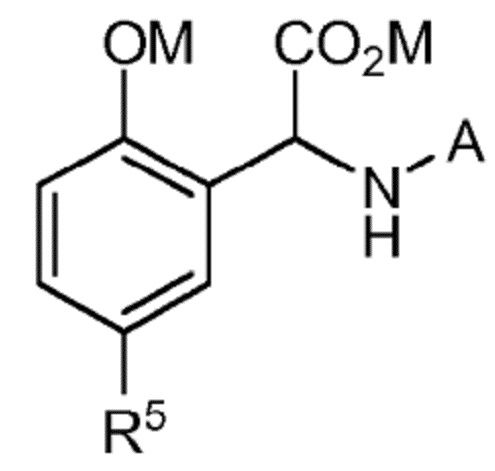 (I´)
(I´)
в которой R5 выбран из группы, состоящей из -H, -OM, -COOM, -NH2, -SO3M, (C1-C4)алкила и галогена; и
A представляет собой радикал, имеющий по меньшей мере 3 атома С и выбранный из группы, состоящей из:
i) радикала формулы (i):
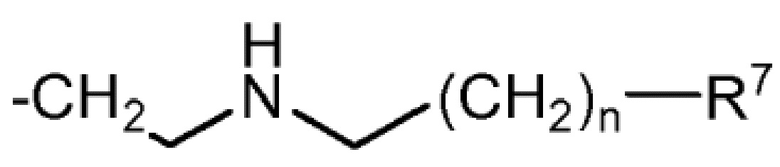 (i)
(i)
в которой R7 выбран из группы, состоящей из -OM и -COOM, и n составляет 0, 1 или 2; и
где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ или K+, и NH4+;
ii) радикала формулы (ii):
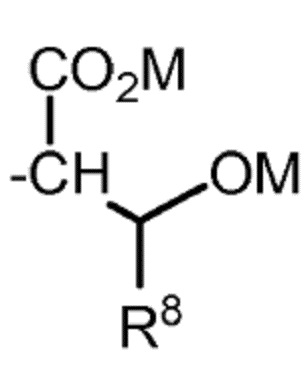 (ii)
(ii)
в которой R8 выбран из группы, состоящей из -H и (C1-C4)алкила; и
где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ или K+, и NH4+; или
iii) радикала формулы (iii):
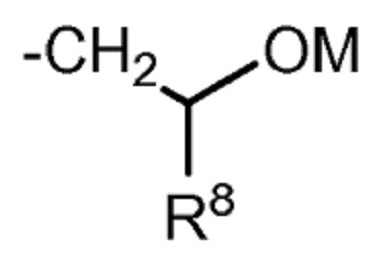 (iii)
(iii)
в которой R8 представляет собой (C1-C4)алкил; и
где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ или K+, и NH4+.
Соединения согласно настоящему изобретению способны к комплексообразованию с катионами металлов, в частности, с катионами железа, с образованием устойчивых хелатов, которые являются подходящими для устранения дефицита указанных металлов в растениях, в частности, в растениях, выращиваемых на кислых и щелочных почвах. Таким образом, хелаты металлов, в частности, хелаты железа, образованные соединениями формулы (I´), которые определены выше, также составляют часть настоящего изобретения.
Соответственно, еще один аспект настоящего изобретения относится к хелату металла, в частности, хелату железа, образованному одним из хелатообразующих соединений, которые определены выше.
Неожиданно, по сравнению с известными аналогичными хелатными соединениями, хелатные соединения согласно настоящему изобретению имеют более высокую устойчивость. Следовательно, хелат и хелатообразующие соединения согласно настоящему изобретению являются более эффективными в обеспечении доступности железа для растений. С этим также связана более высокая эффективность хелатообразующего агента согласно настоящему изобретению в обеспечении солюбилизации и доступности для растений следов железа, которое уже присутствует в почвах, в частности, в кислых и щелочных почвах. Следующий аспект настоящего изобретения относится к способу получения хелатов одного из металлов, в частности, хелатов железа, как описано выше, предусматривающему добавление соли металла к хелатообразующим соединениям, которые определены выше.
Другой аспект настоящего изобретения относится к композиции, содержащей хелатообразующее соединение формулы (I´), представленное выше, или соответствующий хелат металла, в частности, соответствующий хелат железа, вместе с приемлемыми для сельского хозяйства носителями.
Следующий аспект настоящего изобретения относится к применению соединения формулы (I´) или соответствующего хелата металла для устранения дефицита металлов, в частности, железа, в растениях посредством обеспечения доступности катионов металла для растений, в частности, для растений, выращиваемых на кислых и щелочных почвах.
Следующий аспект настоящего изобретения относится к способу получения соединения формулы (I´), которое определено выше, причем способ предусматривает реакцию соединения формулы (II´):
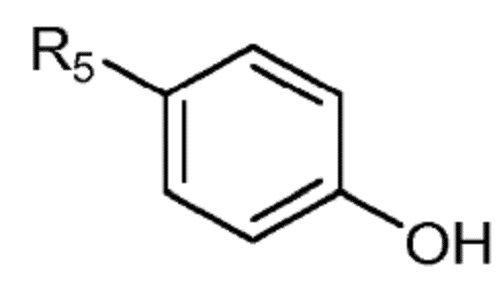 (II´)
(II´)
в которой R5 представляет собой H или CH3,
a-i) с соединением следующей формулы:
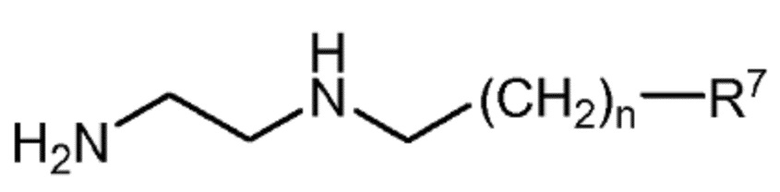
в которой R7 выбран из группы, состоящей из -OM и -COOM, и n составляет 0, 1 или 2, и M независимо выбран из группы, состоящей из H, щелочного металла и NH4+; или
a-ii) с соединением следующей формулы:
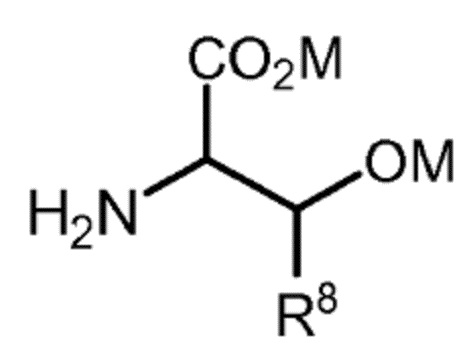
в которой R8 выбран из группы, состоящей из -H и (C1-C4)алкила, и M независимо выбран из группы, состоящей из H, щелочного металла и NH4+; или
a-iii) с соединением следующей формулы:
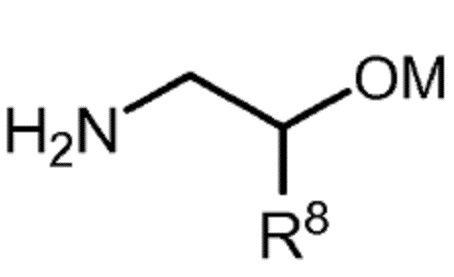
в которой R8 выбран из группы, состоящей из -H и (C1-C4)алкила, и M независимо выбран из группы, состоящей из H, щелочного металла и NH4+;
и
b) с глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 моль в расчете на 1 моль глиоксиловой кислоты.
Преимущественно способ согласно настоящему изобретению преодолевает или сокращает до минимума недостатки известных способов получения указанного типа вышеупомянутых соединений (на основе применения воды и/или других растворителей в качестве растворителя, или на основе применения опасных реагентов). Кроме того, новый способ преимущественно обеспечивает получение упомянутых соединений с высокими выходами и региоселективностями, причем применяемые условия реакции позволяют легко увеличивать масштаб до промышленного уровня, избегая применения вредных реагентов, исключая некоторые технологические стадии и, таким образом, уменьшая расходы.
Способ согласно настоящему изобретению также является применимым для получения других α-имино-о-гидроксифенилуксусных кислот и их производных. Соответственно, часть настоящего изобретения также составляет способ получения соединения формулы (I):
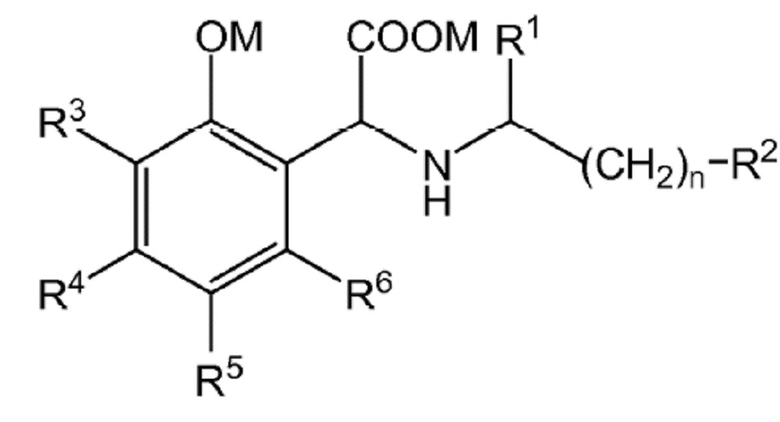 (I)
(I)
в которой R1 выбран из группы, состоящей из H, -OM, -CH3, -COOM, -CH2OH, -CH(CH3)(OH) и -NH2;
R2 выбран из группы, состоящей из -H, -OM, -COOM, -NH2, -СН3СН(NН2)(СН2)3OН, -NH2(CH2)mCOOM, -CONH2, -NHC(NH2)2, -SH, -SCH3, -CH(CH3)2, -CH(CH3)(OH), -СН(СН3)(СНСН2СН3), -PhOH, -Ph, 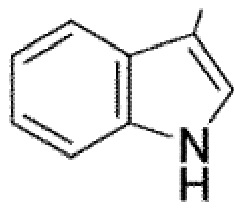 и -NH2(CH2)mOM, где m составляет 1 или 2;
и -NH2(CH2)mOM, где m составляет 1 или 2;
R3, R4, R5 и R6 независимо выбраны из группы, состоящей из -H, -OM, -COOM, -NH2, -SO3M, (C1-C4)алкила и галогена, в частности, Cl или F;
где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+, и n составляет от 0 до 1,
причем способ предусматривает реакцию соединение формулы (II):
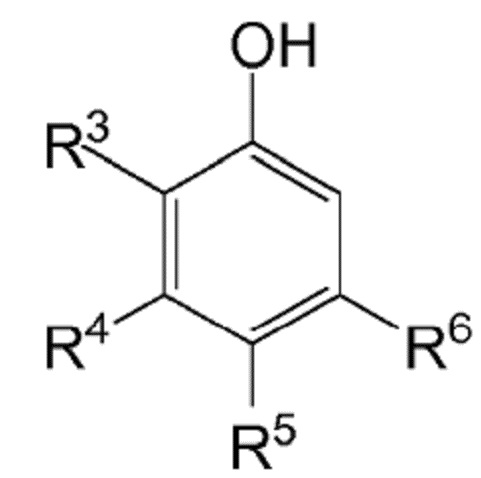 (II)
(II)
в которой R3, R4, R5 и R6 являются такими, как определено выше, с соединением формулы (III):
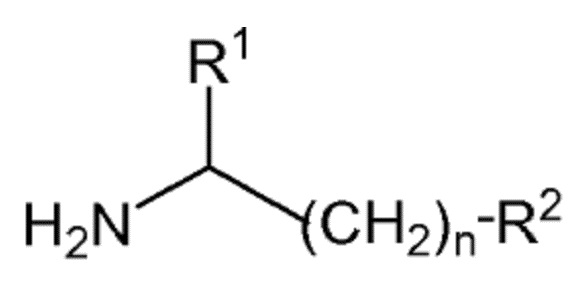 (III)
(III)
в которой R1, R2 и n являются такими, как определено выше, и глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 моль в расчете на 1 моль глиоксиловой кислоты.
Подробное описание изобретения
Термин "алкил" означает неразветвленный или разветвленный насыщенный углеводородный радикал, который содержит число атомов углерода, указанное в описании или формуле изобретения. Таким образом, термин "(C1-C4)алкил" означает неразветвленный или разветвленный насыщенный углеводородный радикал, содержащий от 1 до 4 атомов углерода. Примеры включают в себя такие радикалы, как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил.
Как определяет Международный союз чистой и прикладной химии (IUPAC), хелатообразование включает в себя образование или присутствие двух или более отдельных координационных связей между полидентатным (образующим множество связей) лигандом (таким как хелатообразующие соединения, описанные выше и ниже в настоящем документе) и единственным центральным атомом металла. Термин "хелат металла", который использован в настоящем документе, означает координационное соединение, в котором атом или ион металла связан с хелатообразующим агентом, как определено выше и ниже, в двух или более точках лиганда с образованием гетероциклического кольца, содержащего атом металла.
Термин "фенольное соединение", который использован в настоящем документе, означает соединение, представленное формулой (II):
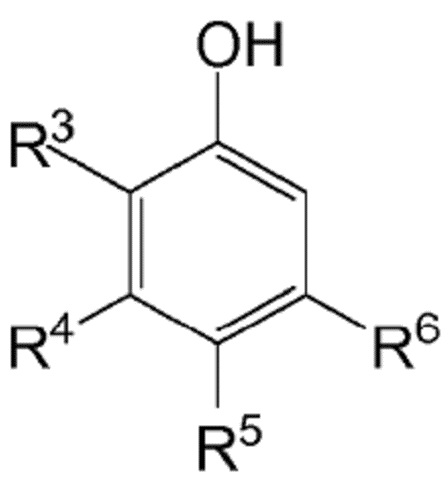 (II)
(II)
в которой R3, R4, R5 и R6 являются такими, как определено выше. В частности, R3, R4, R5 и R6 представляют собой H, и R5 представляет собой H или CH3.
Как упомянуто выше, первый аспект настоящего изобретения относится к хелатообразующему соединению формулы (I´):
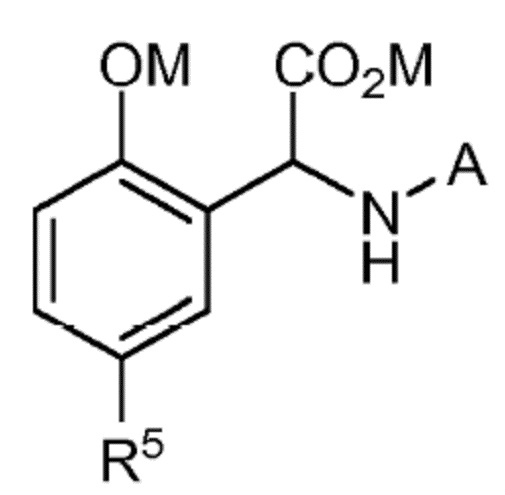 (I´)
(I´)
в которой R5, M и A являются такими, как определено выше.
Согласно конкретному варианту осуществления соединение формулы (I´) представляет собой:
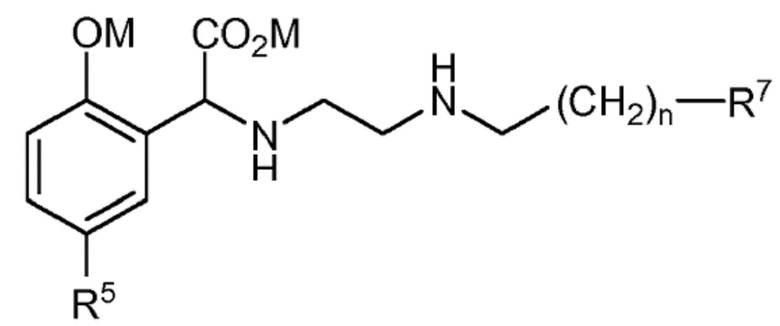
где R7 выбран из группы, состоящей из -OM и -COOM, и n составляет 0, 1 или 2; и
где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+.
Согласно другому конкретному варианту осуществления соединение формулы (I´) представляет собой:
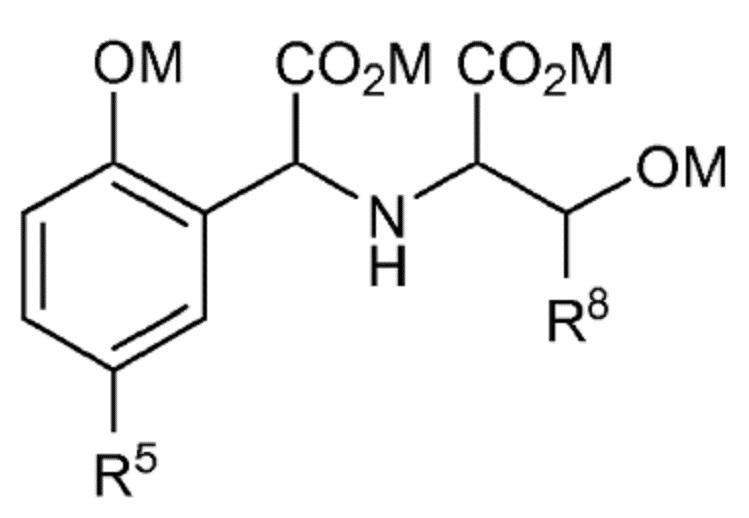
где R8 выбран из группы, состоящей из -H, (C1-C4)алкил; и
где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+.
Согласно другому конкретному варианту осуществления соединение формулы (I´) представляет собой:
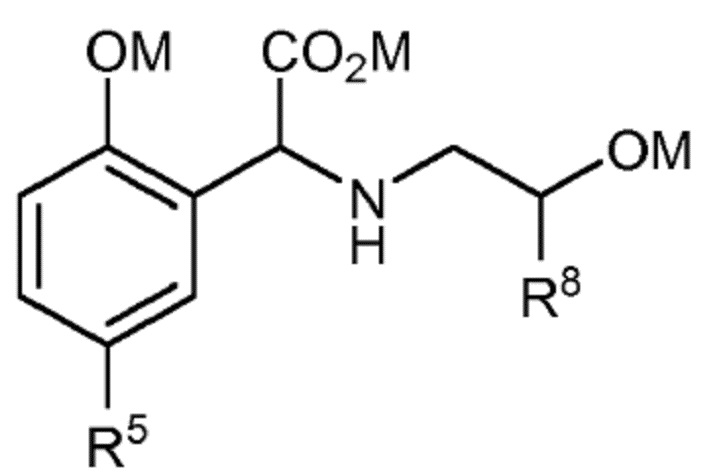
где R8 представляет собой (C1-C4)алкил; и
где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+.
Согласно другому конкретному варианту осуществления соединение формулы (I´) выбрано из группы, состоящей из:
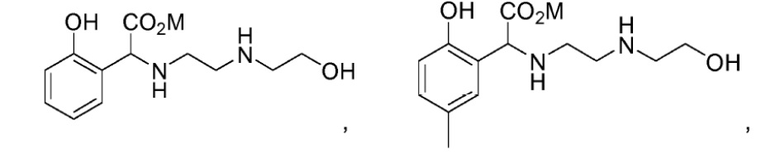
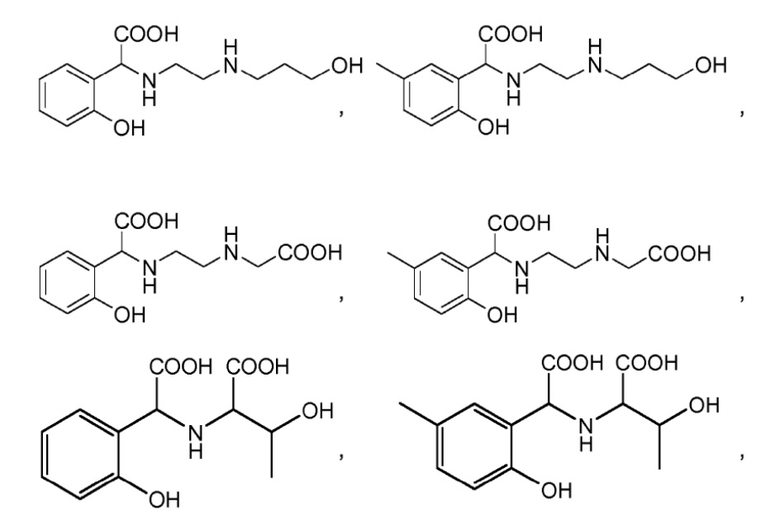
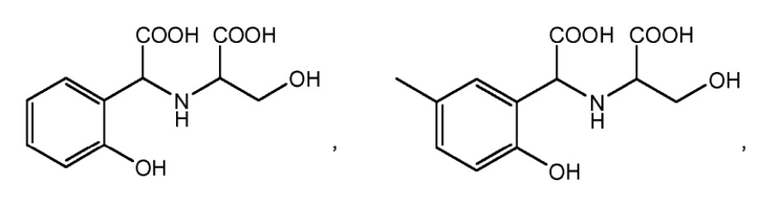
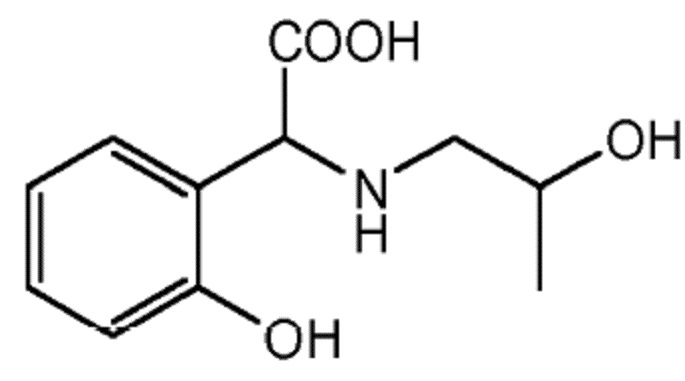 или
или 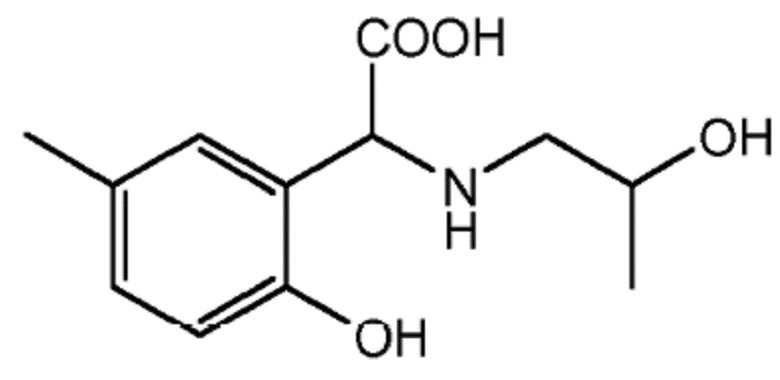
где гидроксильные группы (-OH) могут присутствовать в форме -OM, где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+. В частности, M представляет собой H. Часть настоящего изобретения также составляет хелат металла, образованный упомянутым соединением. В частности, хелат металла представляет собой хелат железа.
Соединения согласно настоящему изобретению, то есть соединения формулы (I´), в частности, соединения, перечисленные выше, способны осуществлять комплексообразование с катионами металлов, в частности, с катионами железа, с образованием устойчивых хелатов, которые являются подходящими для устранения дефицита указанных металлов в растениях, в частности, в растениях, выращиваемых на кислых и щелочных почвах. Устойчивость хелатных соединений согласно настоящему изобретению является выше, чем устойчивость уже известных хелатных соединений.
Хелаты металлов, образованные хелатообразующими соединениями, определенными выше, могут быть получены посредством добавления соли металла к соединениям, которые определены выше. В частности, получение хелата железа(III) может быть осуществлено посредством добавления соли железа(III), такой как сульфат железа, нитрат железа или трихлорид железа, в водный раствор, упомянутый выше, и установления pH на уровне от 8 до 9 с помощью основания, такого как KOH, NaOH, К2СО3 и NH3. Хелат железа(III) выделяют посредством удаления воды в процессе дистилляции при пониженном давлении.
Количество катионов металла, добавляемых к хелатообразующему соединению, составляет от 0,5 до 3 моль по отношению к хелатообразующему соединению. В частности, катион металла представляет собой Fe2+ или Fe3+.
Как упомянуто выше, часть настоящего изобретения составляет также композиция, содержащая хелатообразующее соединение формулы (I´), определенное выше, в частности, конкретные соединения, представленные выше, или соответствующий хелат металла, в частности, соответствующий хелат железа, вместе с приемлемыми для сельского хозяйства носителями.
Подходящие для сельского хозяйства носители, которые могут быть применены в получении сельскохозяйственных композиций согласно настоящему изобретению, хорошо известны специалистам в данной области техники. Например, жидкие носители, которые могут быть использованы, содержат воду. Вода представляет собой обычно выбираемый носитель для разбавления концентратов.
Кроме того, как упомянуто выше, авторы настоящего изобретения обнаружили преимущественный способ получения соединения формулы (I):
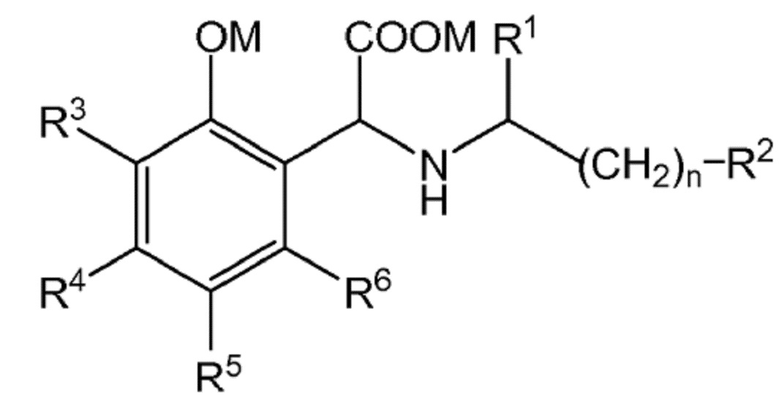 (I)
(I)
которое определено выше, причем способ предусматривает реакцию соединения формулы (II):
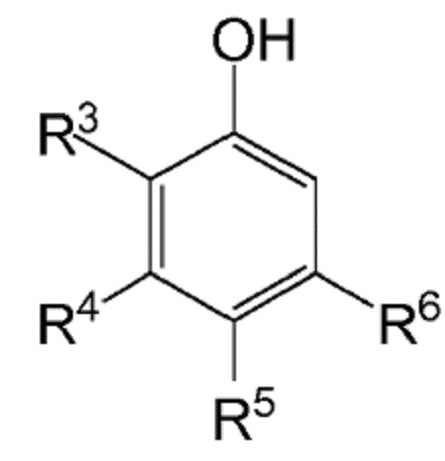 (II)
(II)
которое определено выше, с соединением формулы (III):
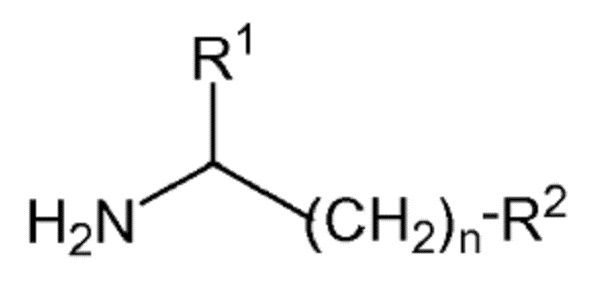 (III)
(III)
которое определено выше, и глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 г/г глиоксиловой кислоты.
Указанный способ обеспечивает получение конечного соединения с аминокислотным заместителем в орто-положении по отношению к группе -OM, в частности, -OH, с более высокими выходами и селективностями, чем способы, известные в технике, причем образование пара-изомера сокращается до минимума.
В частности, способ согласно настоящему изобретению предусматривает реакцию фенольного соединения, в частности, фенола или фенольного соединения, которое определено выше и содержит заместитель в пара-положении, с соединением формулы (III), которое определено выше, в частности, с аминокислотой или аминоспиртом. Реакция происходит в присутствии основания, такого как KOH, NaOH, K2CO3 и NH3. Наконец, добавляют глиоксиловую кислоту или ее соль, такую как глиоксилат натрия, поддерживая реакционную смесь при температуре от 50°C до 100°C. Более конкретно, используют от 3 до 30 моль фенольного соединения, от 0,5 до 2 моль соединения формулы (III), которое определено выше, от 0,5 до 2 моль основания и от 0,5 до 2 моль глиоксиловой кислоты или ее соли. Еще более конкретно, используют 10 моль фенольного соединения, 1 моль соединения формулы (III), которое определено выше, 1 моль основания и 1 моль глиоксиловой кислоты или ее соли.
Такое же фенольное соединение, которое использовано в качестве реагента, используют и в качестве растворителя, то есть в реакционную смесь не добавляют никакие другие растворители, кроме воды, содержащейся в растворах основания или глиоксиловой кислоты, используемых в реакции. Это имеет преимущество исключения некоторых технологических стадий, таких как осаждение и очистка конечного продукта. Кроме того, получают более высокие выходы и региоселективности. Когда реакция завершается, в частности, после ее проведения в течение от 2 до 7 часов, вода может быть добавлена в неочищенную реакционную смесь для получения водного раствора конечного соединения.
Согласно конкретному варианту осуществления способа настоящего изобретения R1 выбран из группы, состоящей из H, -OM, -CH3, -COOM, -CH2OH, -CH(CH3)(OH) и NH2; R2 выбран из группы, состоящей из -H, -OM, -COOM, -NH2, -CH3CH(NH2)(CH2)3OH, -NH2(CH2)mCOOM и -NH2(CH2)mOM, где m составляет 1 или 2; R3, R4 и R6 представляют собой H; и R5 независимо выбран из группы, состоящей из -H, -OH, -COOM, -NH2, -SO3M, (C1-C4)алкила; где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+, и n составляет 0 или 1.
Согласно другому конкретному варианту осуществления способа настоящего изобретения R1 выбран из группы, состоящей из -H, -OM, -CH3, -COOM, -CH2OH, -CH(CH3)(OH) и -NH2; R2 выбран из группы, состоящей из -H, -OM, -COOM, -NH2, -CH3CH(NH2)(CH2)3OH, -NH2(CH2)mCOOM и -NH2(CH2)mOM, где m составляет 1 или 2; R3, R4 и R6 представляют собой H; и R5 независимо выбран из группы, состоящей из -H, -OH, -COOM, -NH2, -SO3M, (C1-C4)алкила; где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+, и n составляет 0 или 1.
Согласно следующему конкретному варианту осуществления способа настоящего изобретения, R1 представляет собой H; R2 представляет собой -OH, -COOM, -NH2, -NH2(CH2)mCOOM и -NH2(CH2)mOM; R3, R4 и R6 представляют собой H; и R5 независимо выбран из группы, состоящей из H, -CH3 и -SO3H; где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+; m составляет 1 или 2; и n составляет 0 или 1, при том условии, что если n составляет 0, R2 представляет собой -COOM, и если n составляет 1, R2 представляет собой -NH2, -NH2(CH2)mCOOM, или -NH2(CH2)mOM, где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+.
Согласно следующему конкретному варианту осуществления способа настоящего изобретения, получают соединение формулы (IV):
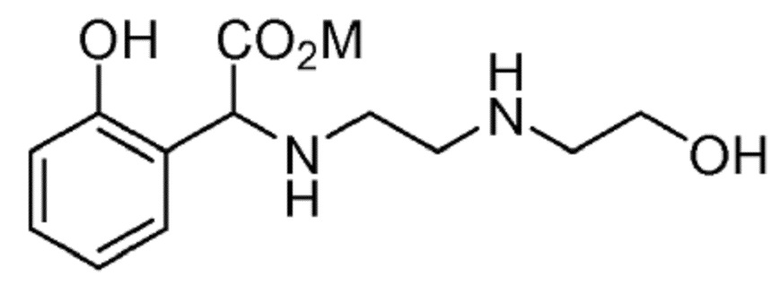 (IV)
(IV)
или формулы (V):
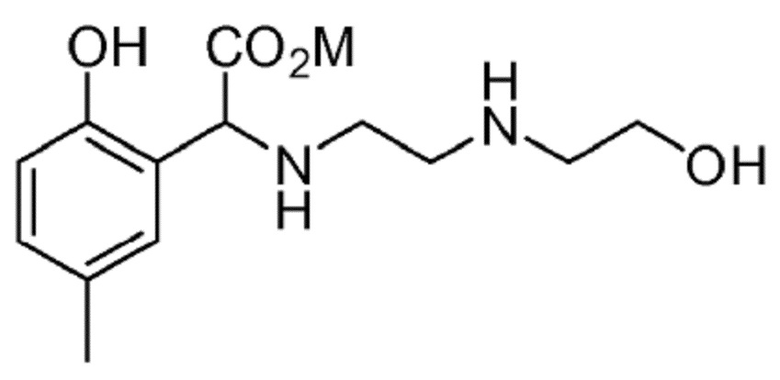 (V)
(V)
в которой M выбран из группы, состоящей из H и щелочного металла, такого как Na+ и K+, и, в частности, M представляет собой H; причем способ предусматривает реакцию соединения формулы (II´):
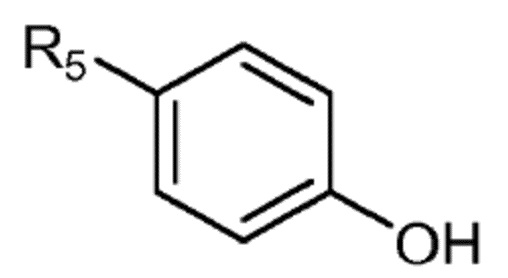 (II´)
(II´)
в которой R5 представляет собой H или CH3,
с аминоэтилэтаноламином и глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 моль в расчете на 1 моль глиоксиловой кислоты.
Согласно следующему конкретному варианту осуществления способа настоящего изобретения получают соединение формулы (I´):
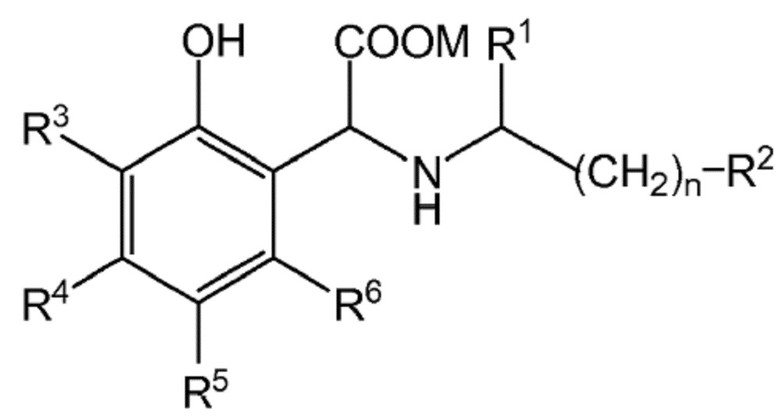 (I´)
(I´)
причем соединение формулы (II) представляет собой:
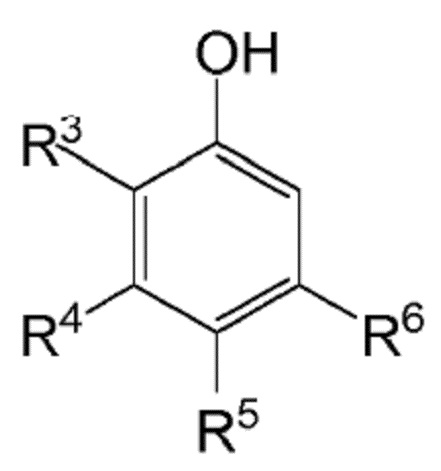 (II)
(II)
где R1, R2, R3, R4, R5, R6, n, m и M являются такими, как определено выше.
Согласно следующему конкретному варианту осуществления способа настоящего изобретения получают соединение формулы (I´), которое определено выше, где R3, R4 и R6 представляют собой H, и R5 представляет собой H, -CH3 или -SO3H, причем способ предусматривает реакцию соединение формулы (II´):
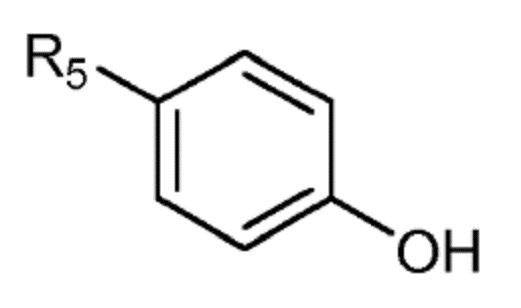 (II´)
(II´)
в которой R5 является таким, как определено выше, с соединением формулы (III):
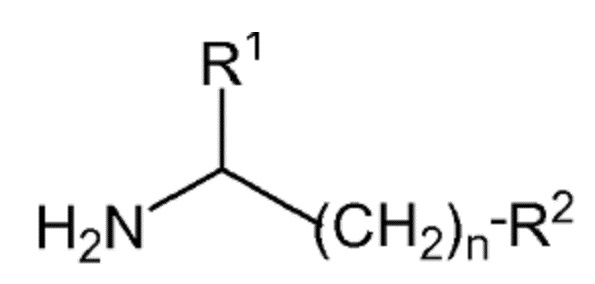 (III)
(III)
в которой R1 представляет собой H, R2 представляет собой -OH, -COOM, -NH2, -NH2(CH2)mCOOM, и -NH2(CH2)mOM, где M независимо выбран из группы, состоящей из H, щелочного металла, такого как Na+ и K+, и NH4+; m составляет 1 или 2; и n составляет 0 или 1; при том условии, что если n составляет 0, R2 представляет собой -COOM, и если n составляет 1, R2 представляет собой -NH2, -NH2(CH2)mCOOM и -NH2(CH2)mOM;
и с глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 моль в расчете на 1 моль глиоксиловой кислоты.
Конечное соединение может быть выделено посредством экстракции органическим растворителем, таким как хлороформ, и последующего удаления растворителя посредством дистилляции при пониженном давлении. В качестве альтернативы, вышеупомянутый водный раствор, содержащий рассматриваемое соединение, может быть непосредственно использован для образования хелата железа.
Получаемые соединения могут быть количественно определены посредством потенциометрического титрования аминогрупп, посредством измерения красно-фиолетового соединения, получаемого после добавления соли железа(III) при pH от 3 до 7, методами ВЭЖХ и спектрофотометрии.
Соединения формулы (II) и формулы (III), определенные выше, имеются в продаже или могут быть получены из имеющихся в продаже соединений традиционными способами, известными любому специалисту в данной области техники.
Во всем тексте описания и формулы изобретения выражение "включать в себя" и его вариации не предназначены для исключения других технических признаков, добавок, компонентов или стадий. Кроме того, выражение "включать в себя" распространяется на случай "состоящий из".
Следующие примеры представлены в качестве иллюстрации, и они не предназначены для ограничения настоящего изобретения. Кроме того, настоящее изобретение распространяется на все возможные комбинации конкретных и предпочтительных вариантов осуществления, описанных в настоящем документе.
Примеры
Пример 1. Получение моноэтаноламин-N-2-гидроксифенилуксусной кислоты (MEAHA)
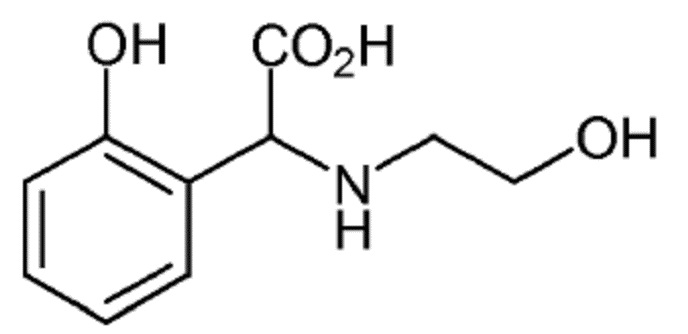
К 940 г (10 моль) фенола при 40°C медленно добавляли 61 г (1 моль) моноэтаноламина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°С. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент MEAHA. Образование хелата Fe-MEAHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент MEAHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 2. Получение моноэтаноламин-N-2-гидрокси-5-метил-фенилуксусной кислоты (CREMEAHA)
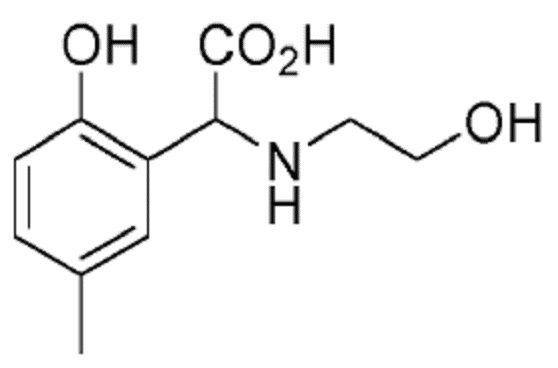
К 1080 г (10 моль) п-крезола при 40°C медленно добавляли 61 г (1 моль) моноэтаноламина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент CREMEAHA. Образование хелата Fe-CREMEAHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент CREMEAHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 3. Получение аминоэтилэтаноламин-N-2-гидроксифенилуксусной кислоты (NEAHA)
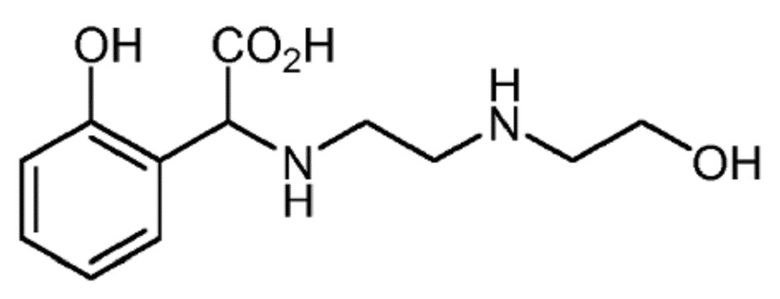
К 940 г (10 моль) фенола при 40°C медленно добавляли 106 г (1 моль) аминоэтилэтаноламина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент NEAHA. Образование хелата Fe-NEAHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент NEAHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 7 до 8 мас.%.
Пример 4. Получение аминоэтилэтаноламин-N-2-гидрокси-5-метилфенилуксусной кислоты (CRENEAHA)
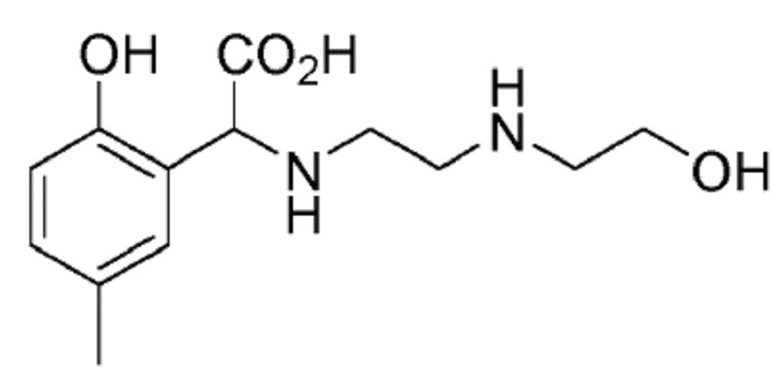
К 1180 г (10 моль) п-крезола при 40°C медленно добавляли 106 г (1 моль) аминоэтилэтаноламина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент CRENEAHA. Образование хелата Fe-CRENEAHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент CRENEAHA, добавляли 62,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 7-8 мас.%.
Пример 5. Получение соединения формулы (VI) (GLYHA)
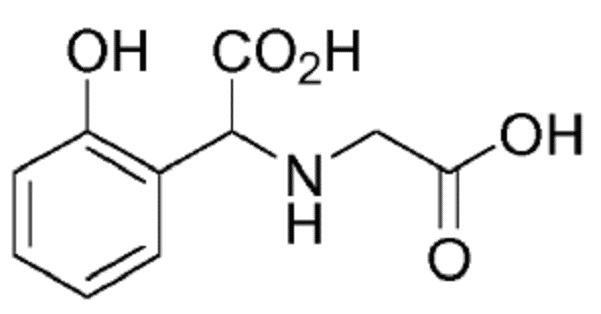 (VI)
(VI)
К 940 г (10 моль) фенола при 40°C медленно добавляли 75 г (1 моль) глицина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент GLYHA. Образование хелата Fe-GLYHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент GLYHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 6. Получение соединения формулы (VII) (CREGLYHA)
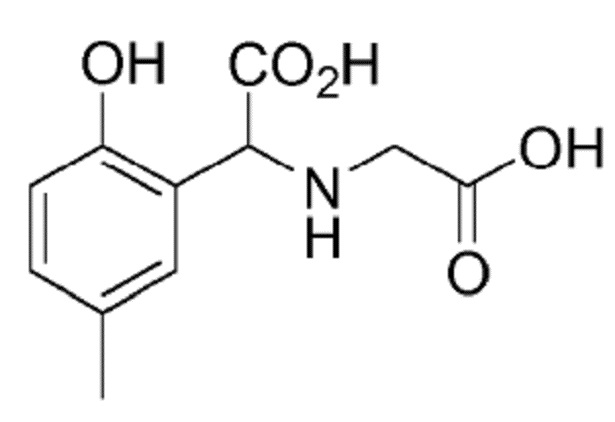 (VII)
(VII)
К 1180 г (10 моль) п-крезола при 40°C медленно добавляли 75 г (1 моль) глицина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент CREGLYHA. Образование хелата Fe-CREGLYHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент CREGLYHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 7. Получение соединения формулы (VIII) (ASPHA)
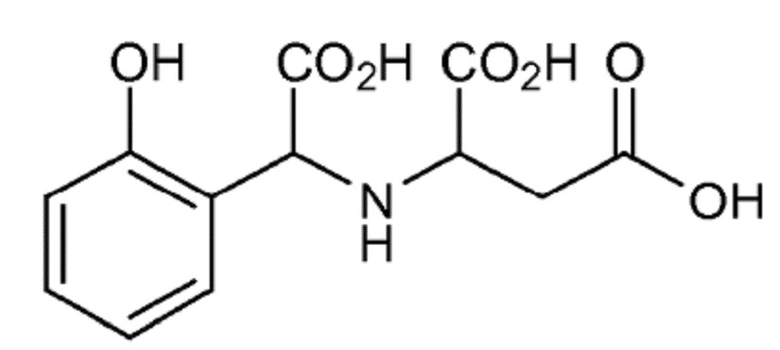 (VIII)
(VIII)
К 940 г (10 моль) фенола при 40° С медленно добавляли 133 г (1 моль) аспарагиновой кислоты, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент ASPHA. Образование хелата Fe-ASPHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент ASPHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 8. Получение соединения формулы (IX) (CREASPHA)
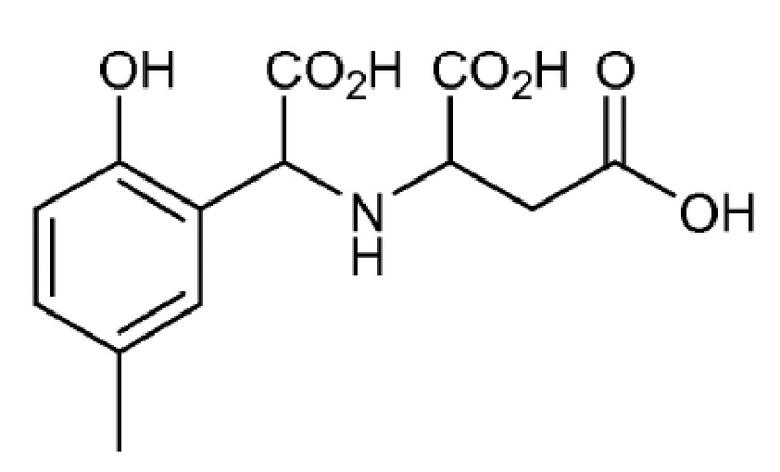 (IX)
(IX)
К 1180 г (10 моль) п-крезола при 40°C медленно добавляли 133 г (1 моль) аспарагиновой кислоты, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент CREASPHA. Образование хелата Fe-CREASPHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент CREASPHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 9. Получение карбокси(2-гидроксифенил)метил)серина (SERHA)
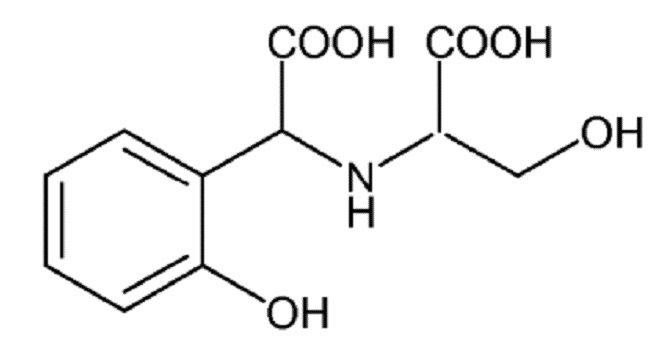
К 940 г (10 моль) фенола при 40°C медленно добавляли 105 г (1 моль) серина, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°C. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент SERHA. Образование хелата Fe-SERHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент SERHA, добавляли 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 10. Получение 2-(2-гидроксифенил)-2-((2-гидроксипропил)амино)уксусной кислоты (AMPHA)
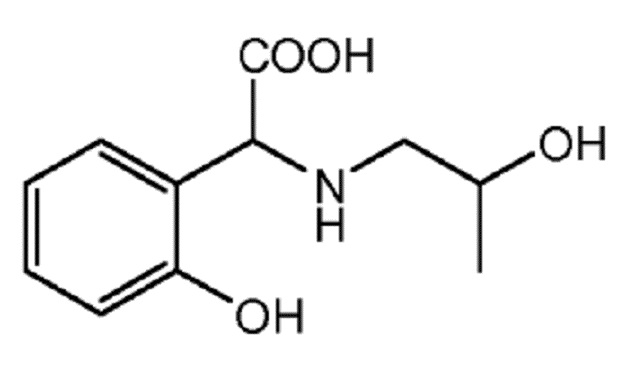
К 940 г (10 моль) фенола при 40°C медленно добавляли 75 г (1 моль) 1-амино-2-пропанола, не допуская увеличения температуры выше 45°C. После завершения добавления реакционную смесь выдерживали для охлаждения и добавляли 80 г (1 моль) водного раствора 50 мас.% гидроксида натрия. После охлаждения неочищенной реакционной смеси до 35°C медленно и непрерывно добавляли 148 г (1 моль) водного раствора 50 мас.% глиоксиловой кислоты, поддерживая температуру ниже 40°C в течение всей реакции. Затем смесь выдерживали для реакции в течение от 2 до 4 часов при температуре от 70 до 75°С. Наконец, добавляли 90 г (5 моль) воды и водную фазу дважды экстрагировали 1120 г (10 моль) хлорбензола. Водная фаза содержала хелатообразующий агент AMPHA. Образование хелата Fe-AMPHA затем осуществляли непосредственно в полученном водном растворе.
Для хелатообразования в полученный выше водный раствор, содержащий хелатообразующий агент AMPHA, 162,3 г (1 моль) FeCl3 и 240-320 г (3-4 моль) водного раствора 50 мас.% гидроксида натрия до достижения pH от 8 до 9 добавляли.
Наконец, после удаления воды посредством дистилляции при пониженном давлении получали хелат железа в форме порошка/микрогранул темно-коричневого цвета. Содержание железа в продукте составляло от 8 до 9 мас.%.
Пример 11. Устойчивость хелатов
Константу устойчивости хелатного соединения Fe3+ в примере 4 (CRENEAHA) определяли спектрофотометрически посредством титрования раствора 2,22•10-4 М (12,5 мг/л) при I = 0,10 М (NaCl) раствором 0,1 M NaOH от pH 2,7 до pH 12,0 и измерения изменения поглощения при 480 нм.
Константу устойчивости хелатного соединения Fe3+ в примере 2 (CREMEAHA) определяли спектрофотометрически посредством титрования раствора 4,49•10-4 М (12,5 мг/л) при I = 0,10 М (NaCl) раствором 0,1 M NaOH от pH 2,7 до pH 12,0 и измерения изменения поглощения при 480 нм.
Константы устойчивости определяли, сокращая до минимума разность между вычисленным поглощением и экспериментальным поглощением посредством изменения констант устойчивости Fe3+. Каждый анализ повторяли четыре раза. Значение константы устойчивости для каждого соединения не зависит от концентрации раствора, используемого для осуществления спектрофотометрического титрования.
Константы устойчивости, полученные для системы, содержащей хелатообразующий агент и Fe3+ в соотношении 1:1, представлены ниже в таблице 1:
Таблица 1
FeHL представляет собой преимущественное соединение при pH < 4,0, FeL представляет собой преимущественное соединение при pH от 4 до 6,5, и FeOHL представляет собой преимущественное соединение при pH > 6,5.
Может быть сделан вывод, что хелат Fe3+, полученный в примере 4 (из соединения CRENEAHA), имеет более высокую устойчивость, в частности, при высоком pH, чем хелат Fe3+, полученный в примере 2 (из CREMEAHA). Следовательно, хелатные соединения согласно настоящему изобретению являются более эффективными в обеспечении доступности железа для растений. С этим также связана более высокая эффективность хелатообразующего агента согласно настоящему изобретению в солюбилизации и обеспечении доступности для растений следов железа, уже присутствующих в почвах, в частности, в кислых и щелочных почвах.
Список документов, процитированных в заявке
1. US3567752
2. GB1418888
3. US3825592
Группа изобретений относится к биотехнологии и сельскому хозяйству. Предложены новый хелатообразующий агент формулы (I'): 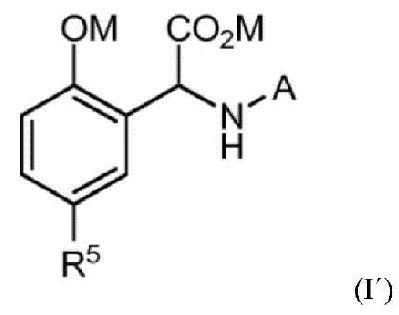 , где A представляет собой
, где A представляет собой 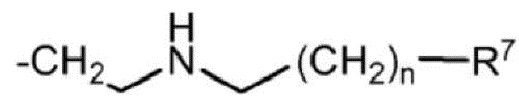 , соответствующий хелат железа, сельскохозяйственные композиции на их основе, способ получения хелатообразующих агентов и соответствующих хелатов металлов, а также их применение для устранения дефицита железа в растениях посредством обеспечения доступности катиона железа для растений. Предложенные хелатные соединения имеют высокую устойчивость, могут быть использованы в широком диапазоне значений pH, в частности в щелочных или нейтральных средах, и являются эффективными в обеспечении доступности железа для растений. 8 н. и 1 з.п. ф-лы, 1 табл., 11 пр.
, соответствующий хелат железа, сельскохозяйственные композиции на их основе, способ получения хелатообразующих агентов и соответствующих хелатов металлов, а также их применение для устранения дефицита железа в растениях посредством обеспечения доступности катиона железа для растений. Предложенные хелатные соединения имеют высокую устойчивость, могут быть использованы в широком диапазоне значений pH, в частности в щелочных или нейтральных средах, и являются эффективными в обеспечении доступности железа для растений. 8 н. и 1 з.п. ф-лы, 1 табл., 11 пр.
1. Соединение формулы (I'):
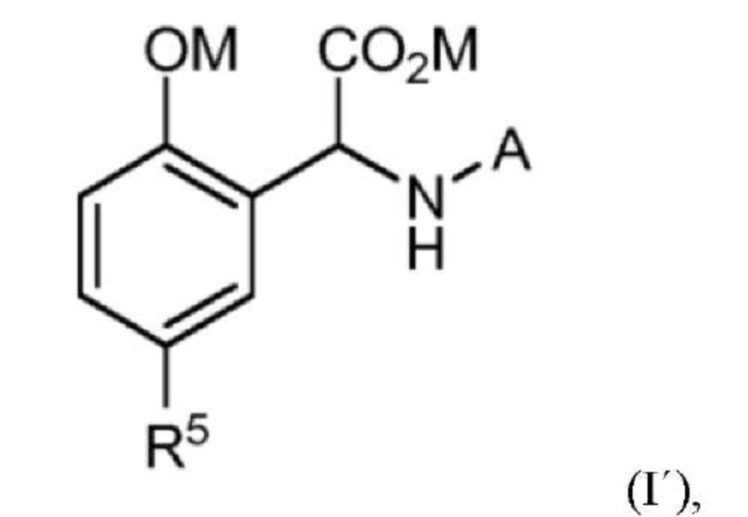
в которой R5 выбран из группы, состоящей из -H, -OM, -COOM, -NH2, -SO3M, (С1-С4)алкила и галогена; и
A представляет собой радикал формулы (i):
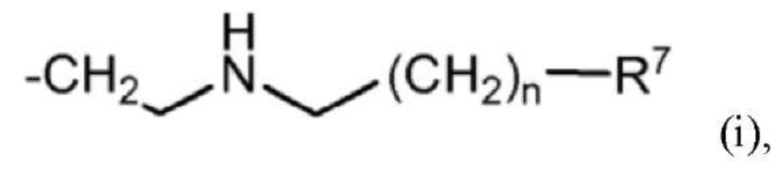
в которой R7 выбран из группы, состоящей из -OM и -COOM, и n составляет 0, 1 или 2; и
где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+.
2. Соединение по п. 1, которое представляет собой:
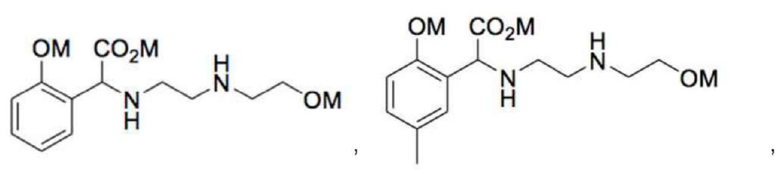
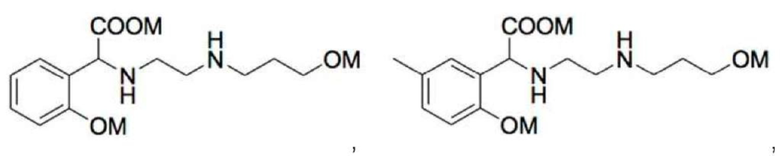
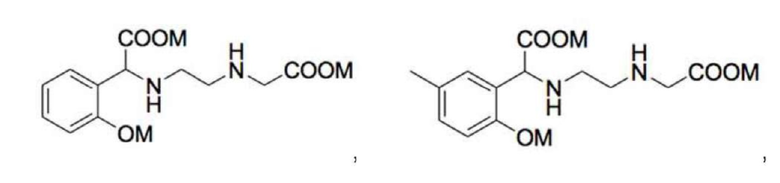
где M независимо выбран из группы, состоящей из H, щелочного металла и NH4+.
3. Хелат железа на основе соединения по п. 1 или 2 для устранения дефицита железа в растениях, получаемый добавлением соли железа к соединению по п. 1 или 2, где хелат представляет собой координационное соединение, в котором катион железа связан с соединением по п. 1 или 2 в двух или более точках с образованием гетероциклического кольца, содержащего атом железа.
4. Сельскохозяйственная композиция для устранения дефицита железа в растениях, содержащая соединение по п. 1 или 2 вместе с приемлемыми в сельском хозяйстве носителями.
5. Сельскохозяйственная композиция для устранения дефицита железа в растениях, содержащая хелат железа по п. 3 вместе с приемлемыми в сельском хозяйстве носителями.
6. Применение соединения по п. 1 или 2 для устранения дефицита железа в растениях посредством обеспечения доступности катиона железа для растений.
7. Применение хелата железа по п. 3 для устранения дефицита железа в растениях посредством обеспечения доступности катиона железа для растений.
8. Способ получения соединения формулы (I') по п. 1, причем способ предусматривает реакцию соединения формулы (II'):
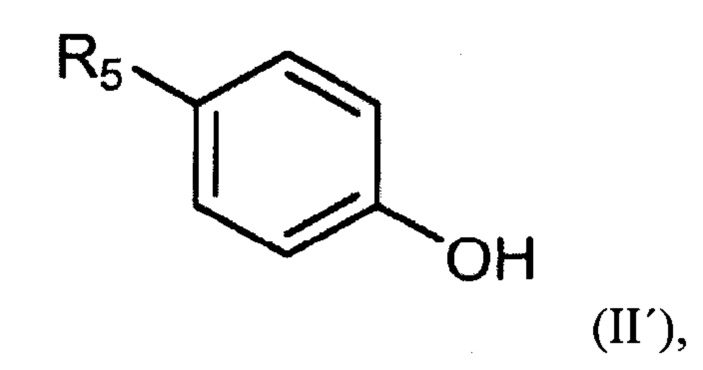
в которой R5 представляет собой H или CH3,
а) с соединением следующей формулы:
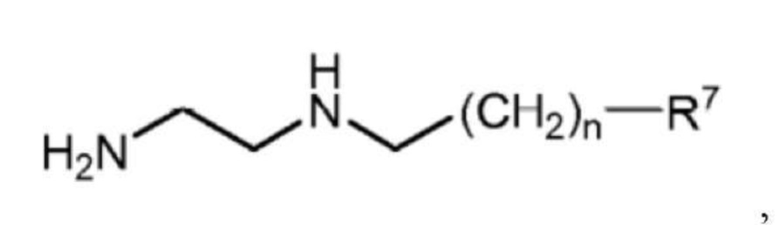
в которой R7 выбран из группы, состоящей из -OM и -COOM, и n составляет 0, 1 или 2, и M независимо выбран из группы, состоящей из H, щелочного металла и NH4+;
и
b) с глиоксиловой кислотой или ее солью в присутствии основания, без добавления органического растворителя, и в присутствии воды в количестве от 1 до 13,3 моль в расчете на 1 моль глиоксиловой кислоты, с получением соединения формулы (I') по п. 1.
9. Способ получения хелата железа по п. 3, включающий осуществление способа по п. 8 и дополнительно добавление соли железа к соединению формулы (I') по п. 1 или 2.
| US 3567752 A, 02.03.1971 | |||
| Дифференциальный усилитель с регулируемым коэффициентом усиления | 1987 |
|
SU1418888A1 |
| US 3825592 A, 23.07.1974 | |||
| Устройство для подгонки сопротивлений проволочных резисторов | 1975 |
|
SU561226A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРИРОВАННОГО РАСТВОРА ХЕЛАТА ЖЕЛЕЗА И ХЕЛАТ ЖЕЛЕЗА | 2005 |
|
RU2278868C1 |
Авторы
Даты
2021-01-15—Публикация
2016-12-21—Подача