ОБЛАСТЬ ТЕХНИКИ
[1]. Настоящее изобретение относится к улучшенному рекомбинантному вектору для вакцинации для лечения или вакцинации против вируса гепатита В (ВГВ), а также к фармацевтическим композициям или вакцинам, содержащим указанный рекомбинантный вектор. Настоящее изобретение также относится к рекомбинантному вектору для вакцинации для применения в способе вакцинации против ВГВ, а также к наборам для вакцинации против ВГВ.
УРОВЕНЬ ТЕХНИКИ
[2]. Более 240 миллионов человек страдают от хронической инфекции вирусом гепатита В (ВГВ). Одобренные способы лечения включают применение аналогов нуклеозидов (нуклеотидов) и α-интерферона. Аналоги нуклеозидов (нуклеотидов) позволяют регулироать, но не излечивать гепатит В и требуют дорогостоящего долгосрочного лечения, потенциально связанного с появлением резистентных вирусов. Терапия с применением α-интерферона ограничена побочными эффектами и способствует выздоровлению только у 15-20% пациентов.
[3]. Вирус подразделяется на четыре основных серотипа (adr, adw, ayr, ayw), которые индуцируют различные гуморальные ответы на основании антигенных эпитопов, присутствующих на белках оболочки вируса, и на (по меньшей мере) восемь генотипов (A-I) в соответствии с общей изменчивостью нуклеотидной последовательности генома. Генотипы имеют различное географическое распределение и используются для отслеживания эволюции и передачи вируса. Различия между генотипами влияют на степень тяжести заболевания, течение и вероятность осложнений, а также ответ на лечение и, возможно, вакцинацию. Помимо этого существуют подгенотипы, например, А1-5. В Центральной Европе и США преобладающим генотипом является А2. Однако только 1% инфицированных людей являются носителями подгенотипа А2, в то время как большинство пациентов являются носителями генотипа В, С или D ВГВ. Было показано, что стандартные вакцины против ВГВ обеспечивают лучшую защиту от ВГВ, (под)генотип которого аналогичен тому, который применяли в качестве антигенов ВГВ, содержащихся в вакцине, чем от других (под)генотипов.
[4]. Хорошо известно, что адаптивная иммунная система хозяина необходима для эффективного контроля ВГВ. Нейтрализующие антитела, направленные к малому поверхностному антигену ВГВ (HBsAg), предотвращают распространение вируса в неинфицированные гепатоциты, и сероконверсия по HBsAg с появлением антител к HBs представляет собой клиническую конечную точку инфекции ВГВ (Rehermann and Nascimben, Nat Rev Immunol 2005; 5:215-29). У пациентов, организм которых устраняет вирус, развиваются сильные ответы, опосредованные поликлональными и полиспецифичными CD8+ и CD4+ Т-клетками, тогда как хроническая инфекция связана с истощением и прогрессирующей дисфункцией противовирусных Т-клеток (Rehermann et al., J Exp Med 1995; 181:1047-58). Важная роль Т-клеток в контроле инфекции подтверждена клиническим наблюдением о том, что хроническая инфекция ВГВ разрешалась у реципиентов трансплантата костного мозга, которые получали костный мозг от доноров, иммунных к ВГВ (Ilan et al., Gastroenterology 1993; 104:1818-21). На основании этих наблюдений были разработаны терапевтические вакцинации для активации ответов эндогенных ВГВ-специфичных Т-клеток. Однако многочисленные клинические попытки, предпринятые с участием пациентов с хронической инфекцией, оказывали лишь временное действие на иммунные ответы на ВГВ и не контролировали ВГВ (Kutscher et al,. Microb Biotechnol 2012; 5:270-82)). Длительное воздействие высоких уровней циркулирующих вирусных антигенов, по-видимому, является основным препятствием для иммунотерапевтических подходов, поскольку они индуцируют развитие толерантности и дисфункции эффекторных клеток.
[5]. Помимо этого комбинирование терапевтической вакцинации с антивирусным лечением, которое контролирует виремию, но не влияет на уровни циркулирующих антигенов, не улучшало эффективность вакцины и клинический исход (Michel et al., J Hepatol 2011; 54:1286-96).
[6]. Для того чтобы облегчить разработку новых стратегий иммунотерапии, была создана линия ВГВ-трансгенных мышей (HBVtg), модель вертикально переданной хронической инфекции ВГВ (Guidotti et al., J Virol 1995; 69:6158-69). Мыши линии HBVtg реплицируют ВГВ в гепатоцитах, вырабатывают HBcAg, HBsAg и антиген е гепатита В (HBeAg) и высвобождают инфекционный вирус в кровь (Guidotti et al., J Virol 1995; 69:6158-69). Экспрессия антигенов ВГВ начинается с рождения, и мыши являются иммунологически толерантными к белкам, кодируемым ВГВ (Shimizu et al., J Immunol 1998; 161:4520-9), однако данная толерантность может быть нарушена (Buchmann et al., Vaccine 2013; 31:1197-203).
[7]. Модифицированный вирус осповакцины Анкара (MVA) относится к вирусу осповакцины, который является членом рода ортопоксвирусов в семействе Poxviridae. MVA создан путем 516 последовательных пассирований штамма Анкара вируса осповакцины (CVA) на фибробластах из куриного эмбриона (см. обзор Mayr, A., et al. Infection 3, 6-14 (1975)). В результате такого длительного пассирования геном полученного вируса MVA был лишен приблизительно 31 тыс. п. о. своей геномной последовательности и в этой связи был описан как вирус, репликация которого строго ограничена птичьими клетками-хозяевами (Meyer, Н. et al., J. Gen. Virol. 72, 1031-1038 (1991)). На разных моделях на животных было показано, что полученный MVA был значительно авирулентным (Mayr, А. & Danner, К., Dev. Biol. Stand. 41: 225-34 (1978)), но все же вызывал защитные иммунные ответы на поксвирусы. В этой связи штамм MVA испытывали в клинических исследованиях в качестве вакцины для иммунизации против черной оспы человека (Mayr et al., Zbl. Bakt. Hyg. I, Abt. Org. В 167, 375-390 (1987); Stickl et al., Dtsch. med. Wschr. 99, 2386-2392 (1974)). Эти исследования включали более 120000 человек, включая пациентов с высоким риском, и доказали, что, по сравнению с вакцинами на основе вируса осповакцины, MVA имел уменьшенную вирулентность и хорошо переносился и при этом вызывал надлежащий специфичный иммунный ответ.
[8]. В течение последующих десятилетий MVA был модифицирован для применения в качестве вирусного вектора для экспрессии рекомбинантных генов или в качестве рекомбинантной вакцины (Sutter, G. et al., Vaccine 12: 1032-40 (1994)). Были описаны штаммы MVA для разработки вакцин или фармацевтических препаратов. См. патенты США №№6761893 и 6193752. Упомянутые штаммы способны к репродуктивной репликации в отдельных клетках и линиях клеток из вида, отличного от человека, особенно в фибробластах из куриного эмбриона (CEF), но не способны к значительной репродуктивной репликации в линиях клеток человека, которые, как известно, позволяют реплицировать другие известные штаммы вируса осповакцины.
[9]. На основании изложенного выше в данной области техники существует потребность в разработке улучшенных средств и способов, которые можно применять при терапевтической вакцинации против ВГВ. Указанные средства и способы должны одновременно вызывать ответы нейтрализующих антител и ответы полиспецифичных Т-клеток, направленные к нескольким подтипам ВГВ.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[10]. Настоящее изобретение относится к новому рекомбинантному вектору для вакцинации для лечения или вакцинации против вируса гепатита В (ВГВ), а также к фармацевтическим композициям или вакцинам, содержащим указанный MVA. Настоящее изобретение также относится к способу вакцинации против ВГВ с применением указанного рекомбинантного MVA. Предполагается, что средства и способы согласно настоящему изобретению индуцируют у субъекта гуморальный ответ, а также ответ Т-клеток на ВГВ, и также предполагается, что индуцированный иммунный ответ эффективен против широкого разнообразия генотипов и серотипов ВГВ.
[11]. В настоящей заявке «рекомбинантный вектор для вакцинации» относится к ослабленному вирусу или бактерии. В данном случае термин «вектор» относится к вирусу или бактерии, используемой в качестве носителя. Как правило, указанный ослабленный вирус или бактерию используют для введения нуклеиновой кислоты, кодирующей антигены, в клетки субъекта.
[12]. Рекомбинантный вектор для вакцинации согласно настоящему изобретению может представлять собой ослабленный штамм Salmonella. Однако в другом варианте могут быть использованы другие прокариотические микроорганизмы, такие как ослабленные штаммы Escherichia coli, Shigella, Yersinia, Lactobacillus, Mycobacteria, Listeria или Vibrio. Примеры подходящих штаммов микроорганизмов включают Salmonella typhimurium, Salmonella typhi, Salmonella dublin, Salmonella enteretidis, Shigella flexeneri, Shigella sonnel. Ослабленные штаммы Salmonella являются одними из наиболее хорошо охарактеризованных носителей для мукозных вакцин. Рекомбинантные штаммы Salmonella, которые были ослаблены, однако остаются инвазивными, использовали в качестве векторов для пероральных вакцин для переноса защитных эпитопов нескольких патогенов в лимфоидную ткань, ассоциированную со слизистой оболочкой, индуцируя тем самым иммунные ответы в слизистой оболочке, системные ответы и ответы цитотоксических Т-лимфоцитов (CTL) на носитель и на чужеродные антигены.
[13]. Помимо этого рекомбинантный вектор для вакцинации согласно настоящему изобретению может представлять собой ослабленный штамм Salmonella, вектор на основе ЦМВ, ВВС, аденовирусный вектор или вектор на основе вируса кори.
[14]. Рекомбинантный вектор для вакцинации согласно настоящему изобретению может представлять собой вирусный вектор, который может представлять собой инфекционную вирусную частицу, которая также является носителем для введения гена в клетку. Вирусные векторы для вакцинации известны специалистам в данной области техники. В частности, в область настоящего изобретения включен поксвирусный вектор. Рекомбинантный поксвирус может представлять собой поксвирус, который получен с помощью стандартных способов генной инженерии. Согласно предпочтительному варианту реализации настоящего изобретения рекомбинантный вектор для вакцинации согласно настоящему изобретению представляет собой MVA.
[15]. MVA является особенно подходящим в качестве векторной системы. Было показано, что MVA эффективно индуцировал гуморальный ответ и клеточный иммунный ответ в течение короткого периода времени после вакцинации против, например, вируса черной оспы. Было установлено, что MVA является безопасным. Известно, что MVA способен индуцировать иммунный ответ даже у субъектов с ослабленным иммунитетом.
[16]. Однако, помимо преимуществ MVA при его использовании в качестве вакцины против ВГВ, важнейшей задачей для вакцины против ВГВ является способность индуцировать как гуморальный, так и клеточный иммунный ответ и что данный иммунный ответ предпочтительно направлен к нескольким генотипам и/или серотипам ВГВ. Выбор вектора, схемы вакцинации и антигенов ВГВ может способствовать эффективности вакцинации.
[17]. В область настоящего изобретения включено применение комбинации антигенов ВГВ из разных генотипов и/или серотипов ВГВ. Указанная комбинация привела не только к полиспецифичному иммунному ответу на несколько штаммов ВГВ, но и к более сильному иммунному ответу на каждый генотип ВГВ по сравнению с вакцинами, содержащими только антигены из одного генотипа ВГВ. Фактически, применяя средства и способы согласно настоящему изобретению, авторы настоящего изобретения смогли даже преодолеть иммунную толерантность у субъектов с низкими, средними и даже высокими уровнями антигена.
[18]. Вакцины на основе MVA являются предпочтительными по нескольким причинам. Например, предпочтительный штамм MVA, MVA-F6 (Sutter and Staib, 2003. Curr. Drug Targets Infect. Disord. 3:263-271), хорошо размножается в первичных фибробластах из куриного эмбриона (CEF) и не реплицируется в клетках человека. В клетках человека вирусные гены, а также модифицированный трансген экспрессируются, но инфекционный вирус не вырабатывается. Ограниченный ряд хозяев MVA может объяснить невирулентный фенотип, наблюдаемый в условиях in vivo в широком диапазоне видов млекопитающих, включая человека. В многочисленных исследованиях токсичности было показано, что MVA является безопасным. Конструкция, получение и применение рекомбинантного MVA описаны в данной области техники, например, в WO 97/02355, Sutter and Staib, 2003 (см. выше) и WO 2003/008533.
[19]. В область настоящего изобретения включен рекомбинантный вектор для вакцинации, предпочтительно модифицированный вирус осповакцины Анкара (MVA), экспрессирующий один или более антигенов вируса гепатита В (ВГВ). Один или более антигенов могут быть выбраны из белка оболочки (HBs-антиген) ВГВ, ядерного белка (НВс-антиген) ВГВ или домена RT полимеразы ВГВ. Белок оболочки может представлять собой, например, белок оболочки из серотипа adw ВГВ, например, генотипа А серотипа adw ВГВ, например, генотипа А2 серотипа adw2 ВГВ. Ядерный белок может представлять собой, например, ядерный белок из серотипа ayw ВГВ, например, генотипа D серотипа ayw ВГВ.
[20]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению может экспрессировать более одного белка оболочки, причем более чем один белок оболочки может представлять собой белок оболочки из разных генотипов или серотипов ВГВ. Например, MVA согласно настоящему изобретению может экспрессировать белок оболочки генотипа А серотипа adw ВГВ, а также белок оболочки генотипа С. Аналогичным образом, MVA согласно настоящему изобретению может экспрессировать более одного ядерного белка, причем более чем один ядерный белок может представлять собой ядерный белок из разных генотипов или серотипов ВГВ. Например, MVA согласно настоящему изобретению может экспрессировать ядерный белок генотипа D серотипа ayw ВГВ, а также ядерный белок генотипа С.
[21]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению также может экспрессировать полимеразу ВГВ или домен RT полимеразы ВГВ. Указанная полимераза может представлять собой полимеразу любого генотипа или серотипа. Полимераза может предпочтительно представлять собой полимеразу из генотипа D ВГВ.
[22]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению может экспрессировать (а) белок оболочки (HBs-антиген) из серотипа adw вируса гепатита В, причем белок оболочки предпочтительно представляет собой большой белок оболочки или малый белок оболочки из генотипа А серотипа adw вируса гепатита В; предпочтительно малый белок оболочки и (b) ядерный белок (НВс-антиген) из серотипа ayw вируса гепатита В, причем ядерный белок предпочтительно представляет собой белок из генотипа D серотипа ayw вируса гепатита В; и по меньшей мере один из следующих: (с) белок оболочки (HBs-антиген) из вируса гепатита В, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1, (d) ядерный белок (НВс-антиген) из вируса гепатита В, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2, и/или (е) домен RT полимеразы вируса гепатита В, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3. Следует понимать, что MVA согласно настоящему изобретению может экспрессировать три, предпочтительно четыре или наиболее предпочтительно пять антигенов ВГВ, таких как антигены (а), (b), (с), антигены (a), (b), (d) или антигены (а), (b), (е), антигены (а), (b), (с), (d), антигены (а), (b), (с), (е), антигены (a), (b), (d), (е) или антигены (а), (b), (с), (d), (е).
[23]. В настоящей заявке термин «белок оболочки», «HBs-антиген» или «HBsAg» ВГВ относится к поверхностному антигену вируса гепатита В (ВГВ). «Белок оболочки», «HBs-антиген» или «HBsAg» может относиться к любому из трех вариантов: малому, среднему и большому белку оболочки, которые транслируются с различных мРНК. Общим для всех трех вариантов является детерминантный эпитоп «а», который расположен в положениях кодонов 124-147 в пределах основной гидрофильной области (MHR) гена S. Указанный детерминантный эпитоп «а» является одной из основных мишеней антител к HBs во время первоначального иммунного ответа при остром гепатите В. Термин «белок оболочки», «HBs-антиген» или «HBsAg» может необязательно относиться к иммуногенному фрагменту белка оболочки. Иммуногенный фрагмент белка оболочки относится к белкам или пептидам, полученным из любого полноразмерного белка оболочки, который является укороченным с N-конца и/или С-конца, т.е. лишен по меньшей мере одной из N-концевых и/или С-концевых аминокислот. Такой фрагмент содержит предпочтительно по меньшей мере 70, предпочтительно по меньшей мере 80, предпочтительно по меньшей мере 90, предпочтительно по меньшей мере 100, более предпочтительно по меньшей мере 125, наиболее предпочтительно по меньшей мере 150 последовательных аминокислот первичной последовательности белка оболочки и обычно является иммуногенным. Как правило, такой иммуногенный фрагмент содержит, по сравнению с полноразмерным белком, по меньшей мере аминокислоты с 99 по 168, соответствующие положениям аминокислот малого белка оболочки.
[24]. В настоящей заявке термин «ядерный белок» или «НВс-антиген» ВГВ относится к структурному белку нуклеокапсида. Полноразмерный ядерный белок содержит 183 аминокислоты и состоит из домена сборки (аминокислоты с 1 по 149) и домена, связывающего нуклеиновую кислоту (аминокислоты со 150 по 183). Домен, связывающий нуклеиновую кислоту, содержащий 34 остатка, является чрезвычайно основным и содержит 17 остатков аргинина, что соответствует его функции. Ядерный белок является димером в растворе; такие димеры самопроизвольно собираются с образованием икосаэдрических капсидов. Следует понимать, что усеченные ядерные белки, содержащие только аминокислоты с 1 по 149, также способны образовывать капcиды. Термин «ядерный белок» или «НВс-антиген» может необязательно относиться к иммуногенному фрагменту ядерного белка. Иммуногенный фрагмент ядерного белка относится к белкам или пептидам, полученным из любого полноразмерного ядерного белка, который укорочен с N-конца и/или С-конца, т.е. лишен по меньшей мере одной из N-концевых и/или С-концевых аминокислот. Такой фрагмент содержит предпочтительно по меньшей мере 100, более предпочтительно 125, наиболее предпочтительно 149 или более последовательных аминокислот первичной последовательности ядерного белка и обычно является иммуногенным. Как правило, такой иммуногенный фрагмент содержит, по сравнению с полноразмерным ядерным белком, по меньшей мере аминокислоты с 18 по 143, соответствующие положениям последовательности, представленной в SEQ ID NO: 11. Типичным примером является фрагмент ядерного белка, который состоит из аминокислот 1-149 полноразмерного ядерного белка, последовательность которого представлена в SEQ ID NO: 11.
[25]. В настоящей заявке термин «иммуногенный» относится к способности конкретного вещества, такого как антиген или эпитоп, провоцировать иммунный ответ в организме человека или животного. Другими словами, иммуногенность - это способность индуцировать гуморальный и/или клеточный иммунный ответ. Способность антигена вызывать иммунные ответы называется иммуногенностью, которая может представлять собой гуморальные и/или опосредованные клетками иммунные ответы. Не желая быть связанными соответствием какой-либо теории, авторы настоящего изобретения полагают, что любой природный HBs-антиген, НВс-антиген или полимераза из ВГВ обладает иммуногенностью. Помимо этого предполагается, что многие варианты природного HBs-антигена, НВс-антигена или полимеразы из ВГВ, в которых одна или более аминокислот заменены, удалены или вставлены по сравнению с природной последовательностью, являются иммуногенными. В качестве иллюстративного примера иммуногенный вариант природного HBs-антигена представляет собой HBs-антиген, в котором детерминантный эпитоп «а» заменен детерминантой «а» из HBs-антигена другого серотипа. Как правило, последовательность иммуногенного варианта природного HBs-антигена, НВс-антигена или полимеразы может быть на 90% идентична аминокислотной последовательности природного HBs-антигена, НВс-антигена или полимеразы.
[26]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению содержит белок оболочки из серотипа adw вируса гепатита В. Такой белок оболочки может представлять собой малый, средний или большой белок оболочки, причем предпочтительным является малый или большой белок оболочки, причем наиболее предпочтительным является малый белок оболочки. Белок оболочки предпочтительно представляет собой белок генотипа А серотипа adw (A/adw), предпочтительно A2/adw2 ВГВ. Однако любой природный или модифицированный белок оболочки, обладающий иммуногенностью природного белка оболочки adw ВГВ, подходит для настоящего изобретения. Предпочтительные белки оболочки содержат последовательность, которая по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 8, или предпочтительно содержит или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 8. Белок оболочки также может содержать дополнительные аминокислоты на N- или С-конце. Предпочтительно белок оболочки содержит 30 или менее, предпочтительно 25 или менее, предпочтительно 20 или менее, предпочтительно 15 или менее, предпочтительно 10 или менее, предпочтительно 5 или менее, предпочтительно 4 или менее, предпочтительно 3 или менее, предпочтительно 2 или менее, предпочтительно 1 или менее дополнительных аминокислот на N-конце и/или С-конце. Указанные аминокислоты предпочтительно представляют собой фрагменты сайтов саморасщепления, таких как Р2А или Т2А, которые описаны в Kim et al. 2011, PLoS ONE, 6(4):e18556. Соответственно, белок оболочки необязательно содержит дополнительный пролин на N-конце и/или дополнительную последовательность GSGATNFSLLKQAGDVEENPG (SEQ ID NO: 9) на С-конце. Соответственно, белок оболочки может содержать последовательность, представленную в SEQ ID NO: 10.
[27]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению содержит ядерный белок из серотипа ayw вируса гепатита В. Ядерный белок предпочтительно представляет собой белок генотипа D/ayw ВГВ. Любой природный или модифицированный ядерный белок, обладающий иммуногенностью природного ядерного белка серотипа ayw ВГВ, подходит согласно настоящему изобретению. Согласно предпочтительным вариантам реализации настоящего изобретения ядерный белок представляет собой фрагмент полноразмерного ядерного белка, состоящий из аминокислот 1-149 полноразмерного белка. Предпочтительные ядерные белки содержат последовательность, которая по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 11, или предпочтительно содержит или состоит из аминокислотной последовательности, представленной в SEQ ID NO: 11. Ядерный белок также может содержать дополнительные аминокислоты на N- или С-конце. Предпочтительно ядерный белок содержит 30 или менее, предпочтительно 25 или менее, предпочтительно 20 или менее, предпочтительно 15 или менее, предпочтительно 10 или менее, предпочтительно 5 или менее, предпочтительно 4 или менее, предпочтительно 3 или менее, предпочтительно 2 или менее, предпочтительно 1 или менее дополнительных аминокислот на N-конце и/или С-конце. Указанные аминокислоты предпочтительно представляют собой фрагменты сайтов саморасщепления, таких как Р2А или Т2А. Соответственно, ядерный белок необязательно содержит дополнительный пролин на N-конце и/или дополнительную последовательность, представленную в SEQ ID NO: 12, на своем С-конце. Фрагмент ядерного белка, состоящий из аминокислот 1-149 полноразмерного белка и имеющий С-концевую последовательность, описанную в настоящем документе, как полагают, по-прежнему обладает способностью собираться с образованием капсидов, и дополнительная С-концевая последовательность, как предполагают, не препятствует образованию капсида.
[28]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению может содержать иммуногенный белок оболочки (HBs-антиген) из вируса гепатита В, который по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентичен аминокислотной последовательности, представленной в SEQ ID NO: 1. SEQ ID NO: 1 представляет собой консенсусную последовательность больших белков оболочки из штаммов генотипа С, которая была создана на основании сопоставления 500 последовательностей ВГВ, представляющих штаммы ВГВ, распространенные во всем мире. Иллюстративным примером является иммуногенный белок оболочки, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 4, которая на 99% идентична последовательности, представленной в SEQ ID NO: 1, соответствующей последовательности, полученной из предполагаемого препре-S белка ВГВ с номером доступа в GenBank ABV02797 (версия ABV02797.1 GI:157057635 от 12 сентября 2007 г.), где А-детерминанта (наиболее важная последовательность-мишень для антител к HBs) была модифицирована с получением ayw (для образования антител, направленных к серотипу ayw) путем замены 2 аминокислот. Существование штамма ВГВ, содержащего последовательность, которая по существу аналогична последовательности, представленной в SEQ ID NO: 4, гарантирует, что существенные процессы (сворачивание/процессинг/представление) являются функциональными для кодируемого белка. Следовательно, согласно настоящему изобретению иммуногенный белок оболочки, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1, представляет собой белок оболочки, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 4. Более того, консенсусная последовательность для белков оболочки из штаммов генотипа С очень сходна с консенсусной последовательностью белков оболочки из штаммов генотипа В. Поскольку иммуногенный белок оболочки основан на консенсусной последовательности белка оболочки для штаммов генотипа С, которая в то же время очень сходна с консенсусной последовательностью белка оболочки из штаммов генотипа В, этот иммуногенный белок оболочки способен индуцировать иммунный ответ против широкого спектра штаммов по меньшей мере генотипа В и генотипа С. Следует понимать, что иммуногенный белок оболочки, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1, необязательно также относится к его иммуногенному фрагменту, последовательность которого по меньшей мере на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична последовательности соответствующего фрагмента, представленной в SEQ ID NO: 1. Белок оболочки также может содержать дополнительные аминокислоты на N- или С-конце. Предпочтительно белок оболочки содержит 30 или менее, предпочтительно 25 или менее, предпочтительно 20 или менее, предпочтительно 15 или менее, предпочтительно 10 или менее, предпочтительно 5 или менее, предпочтительно 4 или менее, предпочтительно 3 или менее, предпочтительно 2 или менее, предпочтительно 1 или менее дополнительных аминокислот на N-конце и/или С-конце. Указанные аминокислоты предпочтительно представляют собой фрагменты сайтов саморасщепления, таких как Р2А или Т2А. Соответственно, белок оболочки необязательно содержит дополнительный пролин на N-конце и/или дополнительную последовательность GSGEGRGSLLTCGDVEENPG (SEQ ID NO: 13) на своем С-конце. Соответственно, белок оболочки может содержать последовательность, представленную в SEQ ID NO: 14.
[29]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению также может содержать иммуногенный ядерный белок (НВс-антиген) из вируса гепатита В, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2. SEQ ID NO: 2 представляет собой консенсусную последовательность ядерных белков из штаммов генотипа С, которая была получена на основании сопоставления 500 последовательностей ВГВ, представляющих штаммы ВГВ, распространенные во всем мире. Иллюстративным примером является иммуногенный ядерный белок, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 5, которая на 100% идентична последовательности, представленной в SEQ ID NO: 2, которая по существу идентична последовательности, полученной из капсидного белка ВГВ с номером доступа в GenBank NP_647607 (вариант NP_647607.1 GI:21326588 от 9 июля 2015 года). Соответственно, согласно настоящему изобретению иммуногенный ядерный белок, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2, представляет собой белок оболочки, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 5. Помимо этого консенсусная последовательность для штаммов генотипа С идентична консенсусной последовательности штаммов генотипа В. Поскольку иммуногенный белок оболочки основан на консенсусной последовательности белка оболочки для штаммов генотипа С, которая идентична консенсусной последовательности белка оболочки для штаммов генотипа В, упомянутый иммуногенный белок оболочки способен индуцировать иммунный ответ на широкий спектр штаммов по меньшей мере генотипа В и генотипа С. Следует понимать, что иммуногенный ядерный белок, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2, необязательно также относится к его иммуногенному фрагменту, последовательность которого по меньшей мере на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична последовательности соответствующего фрагмента, представленной в SEQ ID NO: 2. В качестве иллюстративного примера такой иммуногенный фрагмент может представлять собой фрагмент, последовательность которого на 90% идентична последовательности аминокислот с 1 по 149, представленной в SEQ ID NO: 2. Ядерный белок также может содержать дополнительные аминокислоты на N- или С-конце. Предпочтительно ядерный белок содержит 30 или менее, предпочтительно 25 или менее, предпочтительно 20 или менее, предпочтительно 15 или менее, предпочтительно 10 или менее, предпочтительно 5 или менее, предпочтительно 4 или менее, предпочтительно 3 или менее, предпочтительно 2 или менее, предпочтительно 1 или менее дополнительных аминокислот на N-конце и/или С-конце. Упомянутые аминокислоты предпочтительно представляют собой фрагменты сайтов саморасщепления, таких как Р2А или Т2А. Соответственно, ядерный белок необязательно содержит дополнительный пролин на N-концевом конце. Ядерный белок может дополнительно необязательно содержать дополнительную последовательность, представленную в SEQ ID NO: 9 или 13, на своем С-конце. Соответственно, ядерный белок может содержать последовательность, представленную в SEQ ID NO: 15.
[30]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению также может содержать иммуногенный домен RT полимеразы вируса гепатита В, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3. SEQ ID NO: 3 представляет собой консенсусную последовательность доменов RT из штаммов генотипа А, В, С и D, которая была получена на основании сопоставления 500 последовательностей ВГВ, представляющих штаммы ВГВ, распространенные по всему миру. Иллюстративным примером такого иммуногенного домена RT полимеразы является белок с аминокислотной последовательностью, представленной в SEQ ID NO: 6, последовательность которого на 97% идентична последовательности, представленной в SEQ ID NO: 3. SEQ ID NO: 6 соответствует аминокислотной последовательности домена RT из полимеразы, полученной из неполной полимеразы ВГВ с номером доступа в GenBank AFY09280 (версия AFY09280.1 GI:425891330 от 31 января 2013 г.). SEQ ID NO: 6 является типичным примером, поскольку она представляет собой природный домен RT полимеразы, который имеет самое высокое сходство с полученной консенсусной последовательностью генотипов А, В, С и D. Существование штамма ВГВ с указанной последовательностью гарантирует, что существенные процессы (складывание/процессинг/представление) являются функциональными для кодируемого домена RT. Соответственно, согласно настоящему изобретению иммуногенный домен RT, последовательность которого по меньшей мере приблизительно на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3, представляет собой белок оболочки, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотой последовательности, представленной в SEQ ID NO: 6. Поскольку домен RT полимеразы содержит несколько высококонсервативных эпитопов и поскольку домен RT полимеразы, содержащийся в MVA согласно настоящему изобретению, основан на консенсусной последовательности домена RT для генотипа А, В, С и D, указанный иммуногенный домен RT полимеразы способен индуцировать иммунный ответ на широкий спектр штаммов по меньшей мере генотипа А, В, С и D. Согласно настоящему изобретению также предусмотрено, что домен RT полимеразы может входить в состав полноразмерной полимеразы. Соответственно, в область настоящего изобретения также включена полноразмерная полимераза или усеченная полноразмерная полимераза, содержащая иммуногенный домен RT. Следует понимать, что иммуногенный домен RT полимеразы, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3, необязательно также относится к его иммуногенному фрагменту, последовательность которого по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97% предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно на 100% идентична последовательности соответствующего фрагмента, представленной в SEQ ID NO: 3. Домен RT полимеразы также может содержать дополнительные аминокислоты на N- или С-конце. Предпочтительно домен RT содержит 30 или менее, предпочтительно 25 или менее, предпочтительно 20 или менее, предпочтительно 15 или менее, предпочтительно 10 или менее, предпочтительно 5 или менее, предпочтительно 4 или менее, предпочтительно 3 или менее, предпочтительно 2 или менее, предпочтительно 1 или менее дополнительных аминокислот на N-конце и/или С-конце. Указанные аминокислоты предпочтительно являются фрагментами сайтов саморасщепления, таких как Р2А или Т2А. Соответственно, домен RT необязательно содержит дополнительный пролин на N-конце. Ядерный белок может необязательно дополнительно содержать дополнительную последовательность, представленную в SEQ ID NO: 13, на своем С-конце. Соответственно, домен RT может содержать последовательность, представленную в SEQ ID NO: 16.
[31]. Рекомбинантный вектор для вакцинации, описанный в настоящем документе, предпочтительно MVA, также может содержать или дополнительно экспрессировать молекулу CD70. Предпочтительно CD70 представляет собой CD70 человека.
[32]. Белок CD70 является лигандом для CD27 и также известен как CD27L. Это трансмембранный белок типа II, который экспрессируется на высокоактивных лимфоцитах (например, в Т- и В-клеточных лимфомах). Он также экспрессируется на почечноклеточной карциноме и оценивается как опухолевая мишень. Экспрессия CD70-лиганда обычно тщательно регулируется, однако если CD27L конститутивно экспрессируется на В-клетках, то развивается обширный и эффективный пул Т-клеток, сходных с клетками памяти (Arens, R. et al 2004 J Exp Med 199(11) 1595-605). При хронических вирусных инфекциях передача сигналов с участием CD70 может иметь значение для клинического исхода.
[33]. CD27/CD70 является членом суперсемейства рецепторов факторов некроза опухолей/факторов некроза опухолей (TNFR/TNF), хорошо известного своими свойствами профилирования Т-клеток. Помимо CD27/CD70 это семейство включает CD30/CD30L, CD40/CD40L, OX40/OX40L, 4-1BB/4-1BBL, GITR/GITRL и Fas/FasL. Роль CD70, помимо других членов, таких как OX40L и 4-1BBL, в отношении первичных и вторичных ответов Т-клеток была исследована в широком диапазоне моделей инфекционных заболеваний (Hendrick et al., "CD27 is required for generation and long-term maintenance of T-cell immunity," Nature Immunol. l(5):433-440 (2000); Matter et al., "Virus-induced polyclonal B-cell activation improves protective CTL memory via retained CD27 expression on memory CTL," Eur. J. Immunol. 35(11):3229-3239 (2005); A. Schildknecht et al., "Priming of CD8+ T-cell responses by pathogens typically depends on CD70-mediated interactions with dendritic cells," Eur. J. Immunol. 37(3):716-728 (2007)). Интересно отметить, что активация костимулирующих молекул, включая, помимо других, CD70 на дендритных клетках («DC»), может быть индуцирована комбинированной стимуляцией TLR/CD40 (Sanchez et al., "Combined TLR/CD40 stimulation mediates potent cellular immunity by regulating dendritic cell expression of CD70 in vivo," J. Immunol. 178(3): 1564-1572 (2007).
[34]. Следовательно, согласно настоящему изобретению последовательность CD70 по меньшей мере приблизительно на 90%, предпочтительно по меньшей мере приблизительно на 91%, предпочтительно по меньшей мере приблизительно на 92%, предпочтительно по меньшей мере приблизительно на 93%, предпочтительно по меньшей мере приблизительно на 94%, предпочтительно по меньшей мере приблизительно на 95%, предпочтительно по меньшей мере приблизительно на 96%, предпочтительно по меньшей мере приблизительно на 97%, предпочтительно по меньшей мере приблизительно на 98%, предпочтительно по меньшей мере приблизительно на 99%, предпочтительно приблизительно на 100% идентична аминокислотной последовательности, представленной в SEQ ID NO: 26.
[35]. Рекомбинантный вектор для вакцинации, предпочтительно MVA, согласно настоящему изобретению оптимизирован для терапевтической вакцинации против широкого спектра ВГВ и содержит антигенные последовательности из нескольких часто встречающихся генотипов ВГВ. Соответственно, указанный MVA способен индуцировать иммунный ответ против ВГВ различных генотипов и серотипов. Авторы настоящего изобретения обнаружили неожиданный факт, что, по сравнению с MVA-вакциной, которая содержит только антиген(ы) D/ayw ВГВ, комбинация HBs-антигена из A/adw ВГВ с НВс-антигеном из D/ayw ВГВ будет не только индуцировать полиспецифичный иммунный ответ на генотипы А и D ВГВ, но также будет индуцировать еще более сильный ответ Т-клеток на D/ayw ВГВ. Помимо этого MVA согласно настоящему изобретению также может экспрессировать HBs-антиген или НВс-антиген, которые основаны на консенсусной последовательности штаммов генотипа С ВГВ. Упомянутые консенсусные последовательности штаммов генотипа С ВГВ также очень сходны или даже идентичны консенсусной последовательности штаммов генотипа В. Это означает, что MVA согласно настоящему изобретению, содержащий одну или обе из указанных последовательностей, дополнительно индуцирует полиспецифичный иммунный ответ на штаммы по меньшей мере генотипа В и генотипа С. Помимо этого MVA согласно настоящему изобретению может экспрессировать домен RT полимеразы, который основан на консенсусной последовательности штаммов генотипа А, В, С и D и содержит высококонсервативные антигены. Соответственно, введение указанного домена RT в MVA будет дополнительно способствовать индукции полиспецифичного иммунного ответа на ВГВ по меньшей мере генотипов А, В, С и D. Следовательно, MVA согласно настоящему изобретению представляет собой эффективную вакцину против ВГВ по меньшей мере генотипов А, В, С и D.
[36]. Термин «антиген» относится к молекуле, которая содержит один или более эпитопов, которые стимулируют иммунную систему хозяина, чтобы вызвать клеточный антигенспецифичный иммунный ответ или гуморальный ответ. Антигены могут включать белки, полипептиды, антигенные фрагменты белка и т.п. Помимо этого антиген может быть получен из любого известного вируса, бактерии, паразита, приона, растений, простейших или грибов и может представлять собой целый организм. Термин также включает опухолевые антигены. В настоящую заявку также включены синтетические антигены, такие как полиэпитопы, фланкирующие эпитопы и другие антигены, полученные рекомбинантными или синтетическими способами. Согласно предпочтительному варианту реализации настоящего изобретения антиген согласно настоящему изобретению представляет собой полипептид или белок.
[37]. В отношении термина «эпитоп» термин «антиген» относится к (более длинной) последовательности, в частности к (более длинной) аминокислотной последовательности или последовательности белка, тогда как выражение «антигенный эпитоп» или «эпитоп антигена» включает участок более короткой последовательности из более длинной последовательности. Соответственно, термин «антиген» включает эпитопы. Термин «антиген» также включает варианты белков, полипептидов, а также антигенных фрагментов белка, описанных в настоящем документе. Помимо этого термин «антиген» включает последовательности, идентичные нативной последовательности, а также модификацию нативной последовательности, такую как делеции, добавления, вставки и замены. Предпочтительно аминокислотная последовательность варианта антигена по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60% или 65%, по меньшей мере приблизительно на 70% или 75%, по меньшей мере приблизительно на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88% или 89%, более типично по меньшей мере приблизительно на 90%, 91%, 92%, 93% или 94% и даже более типично по меньшей мере приблизительно на 95%, 96%, 97%, 98% или 99%, наиболее типично по меньшей мере приблизительно на 99% идентична аминокислотной последовательности эталонного антигена (т.е. антигена, из которого он получен).
[38]. Эпитоп, также называемый в настоящем документе «антигенный эпитоп», является частью антигена, которая все еще вызывает иммунный ответ у хозяина. Однако эпитоп не ограничен точной последовательностью антигена, из которого он получен. Соответственно, термин «эпитоп» включает последовательности, идентичные нативной последовательности, а также модификацию нативной последовательности, такую как делеции, добавления, вставки и замены. Предпочтительно аминокислотная последовательность варианта эпитопа по меньшей мере приблизительно на 50%, по меньшей мере приблизительно на 60% или 65%, по меньшей мере приблизительно на 70% или 75%, по меньшей мере приблизительно на 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88% или 89%, более типично по меньшей мере приблизительно на 90%, 91%, 92%, 93% или 94% и даже более типично по меньшей мере приблизительно на 95%, 96%, 97%, 98% или 99%, наиболее типично по меньшей мере приблизительно на 99% идентична аминокислотной последовательности эталонного эпитопа (т.е. эпитопа, из которого он получен).
[39]. Методики определения идентичности последовательностей между двумя последовательностями нуклеиновых кислот и аминокислотными последовательностями известны в данной области техники. Две или более последовательностей (полинуклеотидных или аминокислотных) можно сравнить, определив их «процент идентичности». Процент идентичности двух последовательностей, независимо от того, являются они нуклеиновыми или аминокислотными последовательностями, представляет собой число точных совпадений между двумя сопоставленными последовательностями, деленное на длину более коротких последовательностей и умноженное на 100.
[40]. «Процент идентичности аминокислотных последовательностей (%)» по отношению к антигенам или эпитопам, описанным в настоящем документе, определяется как процент аминокислотных остатков в последовательности-кандидате, которые идентичны аминокислотным остаткам в эталонной последовательности (т.е. антигену или эпитопу из которого она получена), после сопоставления последовательностей и введения пробелов, если необходимо, для достижения максимального процента идентичности последовательностей, и без учета каких-либо консервативных замен как части идентичности последовательностей. Сопоставление для определения процента идентичности аминокислотных последовательностей может быть достигнуто различными способами, которые входят в компетенцию специалиста в данной области техники, например, с использованием общедоступного компьютерного программного обеспечения, такого как BLAST, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для измерения сопоставления, включая любые алгоритмы, необходимые для достижения максимального сопоставления по всей длине сравниваемых последовательностей.
[41]. Аналогичные принципы применимы к «проценту идентичности нуклеотидных последовательностей (%)», с необходимыми изменениями.
[42]. Например, подходящий способ сопоставления последовательностей нуклеиновых кислот обеспечивается алгоритмом поиска локальной гомологии Смита и Уотермана (1981), Advances in Applied Mathematics 2: 482-489. Этот алгоритм можно применять к аминокислотным последовательностям, используя оценочную матрицу, разработанную Dayhoff, Atlas of Protein Sequences and Structure, M.O. Dayhoff ed., 5 suppl. 3:353-358, National Biomedical Research Foundation, Washington, D.C., USA, и нормированную Gribskov (1986), Nucl. Acids Res. 14(6): 6745-6763. Примерные варианты реализации данного алгоритма для определения процента идентичности последовательностей предоставлены Genetics Computer Group (Мэдисон, Висконсин, США) в приложении «BestFit». Параметры по умолчанию для этого способа описаны в Висконсиновском руководстве для пакета программ для анализа последовательностей, версия 8 (1995) (доступно от Genetics Computer Group, Мэдисон, Висконсин, США). Предпочтительный способ установления процента идентичности применительно к настоящему изобретению заключается в использовании пакета программ MPSRCH, защищенных авторским правом Эдинбургского университета, разработанного John F. Collins и Shane S. Sturrok, и распространяемого IntelliGenetics, Inc. (Маунтин-Вью, Калифорния, США). Из этого набора пакетов можно использовать алгоритм Смита-Уотермана, где параметры по умолчанию используются для оценочной таблицы (например, штраф за открытие гэпа - 12, штраф за продолжение гэпа - 1 и штраф за гэп - 6). Значение «совпадение» в полученных данных отражает «идентичность последовательностей». Другие подходящие программы для вычисления процента идентичности или сходства между последовательностями обычно известны в данной области техники, например, другая программа сопоставления представляет собой BLAST, которая используется с параметрами по умолчанию. Например, BLASTN и BLASTP могут быть использованы со следующими параметрами по умолчанию: генетический код = стандартно; фильтр = нет; цепь = обе; отсечение = 60; ожидание = 10; матрица = BLOSUM62; описания = 50 последовательностей; сортировка = высокие балы; базы данных = нерезервированные, GenBank + EMBL + DDBJ + PDB + GenBank CDS translations + Swiss protein + Spupdate + PIR. Подробную информацию об указанных программах можно найти по следующему веб-адресу: http://wvw.ncbi.nlm.gov/cgi-bin/BLAST.
[43]. Нуклеиновые кислоты, кодирующие антигены ВГВ в MVA согласно настоящему изобретению, могут быть включены в отдельные кассеты экспрессии или предпочтительно все вместе находятся в одной кассете экспрессии. В настоящей заявке термин «кассета экспрессии» включает последовательности ДНК, а также РНК, которые способны направлять экспрессию определенной нуклеотидной последовательности в соответствующей клетке-хозяине. В целом кассета экспрессии содержит промотор, функционально соединенный с представляющим интерес полинуклеотидом, который необязательно функционально соединен с сигналом терминации и/или другими регуляторными элементами. Кассета экспрессии может содержать нуклеотидную последовательность, регулирующую транскрипцию. Кассета экспрессии также может содержать последовательности, необходимые для правильной трансляции нуклеотидной последовательности. Кассета экспрессии может представлять собой кассету, которая является природной, но была получена в рекомбинантной форме, пригодной для гетерологичной экспрессии. Кодирующая область обычно кодирует представляющий интерес белок. Кассета экспрессии, содержащая представляющую интерес полинуклеотидную последовательность, также может быть химерной, это означает, что по меньшей мере один из ее компонентов является гетерологичным в отношении по меньшей мере одного из других ее компонентов. Как правило, кассета экспрессии согласно настоящему изобретению не встречается в природе (т.е. является гетерологичной или экзогенной, или чужеродной) в геноме MVA и способна к транскрипции в инфицированных клетках.
[44]. Экспрессия нуклеотидной последовательности в кассете экспрессии может находиться под контролем конститутивного промотора или индуцируемого промотора, который инициирует транскрипцию только если клетка-хозяин подвергается воздействию какого-либо конкретного внешнего стимула. В кассетах экспрессии согласно настоящему изобретению промотор предпочтительно представляет собой промотор поксвируса. Подходящий промотор поксвируса может представлять собой природный промотор или синтетический промотор. В качестве иллюстративного примера промотор поксвируса представляет собой промотор Pr7.5, гибридный ранний/поздний промотор, промотор PrS, синтетический или природный ранний или поздний промотор, такой как один из промоторов, описанных в WO 2010/102822 или WO 2005/054484, или промотор ATI вируса коровьей оспы. Например, промотор поксвируса представляет собой Р7.5 (SEQ ID NO: 17) (Endo et al. J Gen Virol. 1991 Mar;72 ( Pt 3):699-703). Однако предпочтительные промоторы представляют собой промоторы, которые сильнее, чем Р7.5, например промотор РН5, описанный в US 2011/0064769, имеющий последовательность, представленную в SEQ ID NO: 18.
[45]. Последовательности нуклеиновых кислот, кодирующих антиген или его эпитоп, предпочтительно оптимизированы по кодонам. Последовательность нуклеиновой кислоты «оптимизированная по кодонам» относится к последовательности нуклеиновой кислоты, содержащей кодоны, которые заменены кодонами, предпочтительными для желаемой клетки-хозяина, предпочтительно клетки-хозяина человека. Последовательность нуклеиновой кислоты превращают в последовательность нуклеиновой кислоты, оптимизированную по кодонам, которая имеет идентичную транслируемую полипептидную последовательность, но с альтернативным использованием кодонов, в частности кодонов, которые наиболее часто используются в организме-мишени. Способ создания оптимизированной по кодонам последовательности нуклеиновой кислоты антигена обычно включает идентификацию кодонов в природной последовательности антигена, которые обычно не связаны с активно экспрессируемыми генами в организме-мишени, и замену их кодонами, которые, как известно, широко используются при экспрессии генов организма-мишени. Оптимизированная по кодонам последовательность нуклеиновой кислоты может демонстрировать улучшенную экспрессию по сравнению с природной последовательностью в желаемой клетке-хозяине. Возможность индукции улучшенной выработки белка оптимизированной по кодонам последовательностью, по сравнению с неоптимизированной последовательностью, может быть проверена квалифицированным специалистом.
[46]. Оптимизация кодонов исключает использование редких кодонов для желаемого хозяина, поскольку редкие кодоны могут блокировать или уменьшать экспрессию кодируемого белка. Помимо этого предпочтительно избегают использования замен, которые могут вводить сигнальную нуклеиновую кислоту для желаемого хозяина. Такие сигналы включают, но не ограничиваются ими, сигналы сплайсинга, сигналы терминации и сигналы инициирования. В зависимости от типа используемого вектора предпочтительно избегают использования последовательностей мотивов, включающих, например, сигнал ранней терминации транскрипции вируса осповакцины, который не следует избегать во многих других векторах, внутренние ТАТА-боксы, хи-сайты и сайты посадки рибосомы; АТ-богатые и GC-богатые последовательности; элементы последовательности ARE, INS и CRS; повторяющиеся последовательности и вторичные структуры РНК; (скрытый) донорный сайт сплайсинга и акцепторный сайт сплайсинга и точки ветвления; и сигналы ранней терминации транскрипции осповакцины: (TTTTTNT).
[47]. Методики оптимизации кодонов известны в данной области техники. Замена нуклеотидов различными нуклеотидами относится к технической или искусственной замене нуклеотидов другими нуклеотидами. Предпочтительно замененные нуклеотиды не изменяют кодируемую аминокислотную последовательность. Замена может быть выполнена путем идентификации кодонов в двух гомологичных нуклеотидных последовательностях, кодирующих аналогичные аминокислоты, и изменения кодонов в одной из двух гомологичных нуклеотидных последовательностей так, что кодоны продолжают кодировать аналогичные аминокислоты. Изменения могут быть сделаны в одной или обеих гомологичных нуклеотидных последовательностях.
[48]. Согласно настоящему изобретению все антигены ВГВ предпочтительно транслируются как одна полипептидная цепь, содержащая несколько антигенов. Антигенные последовательности на полипептидной цепи предпочтительно разделены последовательностями сайтов саморасщепления. Соответственно, полипептидная цепь, содержащая несколько антигенов, будет посттрансляционно расщеплена на несколько полипептидных цепей, причем каждая из нескольких полипептидных цепей может содержать один антиген ВГВ. Преимущество такого подхода состоит в том, что все антигены ВГВ экспрессируются приблизительно на эквимолярных уровнях. Предпочтительное расположение для полипептидной цепи, содержащей несколько антигенов, от N-конца к С-концу, является следующим: белок оболочки из A/adw ВГВ, сайт Р2А, ядерный белок из D/ayw ВГВ, сайт Р2А, иммуногенный домен RT полимеразы из вируса гепатита В, описанный в настоящем документе, сайт Т2А, иммуногенный белок оболочки (HBs-антиген) гепатита В, описанный в настоящем документе, сайт Т2А, иммуногенный белок (HBs-антиген) гепатита В, описанный в настоящем документе. Согласно предпочтительному варианту реализации настоящего изобретения полипептидная цепь, содержащая несколько антигенов, содержит последовательность, представленную в SEQ ID NO: 7. Как показано на Фигуре 16В, два разных белка оболочки будут расположены в клеточной мембране и могут быть секретированы как субвирусные частицы. Такие субвирусные частицы могут содержать оба белка оболочки, которые принадлежат к различным генотипам ВГВ, и могут поглощаться антигенпредставляющими клетками, что может увеличить индуцированный иммунный ответ. Ядерные частицы могут образовывать пустые капсиды, причем пустые капсиды могут также содержать ядерные белки, которые принадлежат к различным генотипам ВГВ. Такой капсид вызовет иммунный ответ на несколько генотипов ВГВ. Полимераза будет разрушена в протеасоме и представлена с участием HLA. Дополнительное преимущество компоновки, описанной в настоящем документе, состоит в том, что большинство из белков, подвергшихся частичному процессингу, т.е. белков, в которых участок саморасщепления не был расщеплен, будут включены в секретируемые вирусоподобные частицы, которые предположительно увеличивают иммунный ответ, в частности усиливают и расширяют адаптивный иммунный ответ (см. Фиг. 18).
[49]. В область настоящего изобретения включен рекомбинантный MVA, содержащий гены ВГВ, включенные в ряд сайтов вставки в геноме MVA. Термин «ряд сайтов вставки» означает, что гены ВГВ, кодирующие антигены ВГВ, соответственно, могут быть вставлены в один или более разных сайтов вставки в геноме MVA, при этом предпочтительным является один и тот же сайт вставки. Другими словами, например, первый сайт вставки отличается от второго сайта вставки.
[50]. В качестве иллюстративного примера гены ВГВ могут быть вставлены в межгенные области (IGR) MVA. Подходящая IGR может быть выбрана из IGR 07/08, IGR 44/45, IGR 64/65, IGR 88/89, IGR 136/137 и IGR 148/149. Однако предпочтительно гены ВГВ вставлены в природные сайты делеции I, II, III, IV, V или VI MVA, причем предпочтительно по меньшей мере один или предпочтительно все гены ВГВ вставлены в природный сайт делеции III. В качестве иллюстративного примера все гены ВГВ могут быть включены в одну кассету экспрессии в одной открытой рамке считывания, описанную в настоящем документе, при этом одну кассету экспрессии вставляют в природный сайт делеции III.
[51]. Рекомбинантный вирус MVA может быть получен стандартными способами, известными в данной области техники. Способы получения рекомбинантных поксвирусов или вставки экзогенных кодирующих последовательностей в поксвирусный геном хорошо известны специалисту в данной области техники. Например, способы описаны в следующих ссылках: Molecular Cloning, A laboratory Manual. Second Edition. By J. Sambrook, E.F. Fritsch and T. Maniatis. Cold Spring Harbor Laboratory Press. 2003: где описаны стандартные методы молекулярной биологии, такие как клонирование ДНК, выделение ДНК и РНК, Вестерн-блоттинг, методики ОТ-ПЦР и ПЦР-амплификации. В Virology Methods Manual. Edited by Brian W J Mahy and Hillar О Kangro. Academic Press. 1996: описаны методики обращения и манипуляции с вирусами. В Molecular Virology: А Practical Approach. Edited by AJ Davison and RM Elliott. The Practical Approach Series. IRL Press at Oxford University Press. Oxford 1993. Chapter 9: Expression of genes by Vaccinia virus vectors. Current Protocols in Molecular Biology. Publisher: John Wiley and Son Inc. 1998. Chapter 16, section IV: Expression of proteins in mammalian cells using vaccinia viral vector: описаны методики и технологии обращения, манипуляции и генной инженерии MVA.
[52]. Для получения рекомбинантных поксвирусов в соответствии с настоящим изобретением могут быть применены различные способы. Последовательность ДНК, которая должна быть вставлена в вирус, может быть помещена в плазмидную конструкцию Е. coli, в которую была вставлена ДНК, гомологичная участку ДНК поксвируса. Последовательность ДНК, подлежащая вставке, может быть отдельно лигирована с промотором. Связка промотор-ген может быть помещена в плазмидную конструкцию так, что связка промотор-ген фланкирована на обоих концах ДНК, которая гомологична последовательности ДНК, фланкирующей область ДНК поксвируса, содержащую несущественный локус. Полученная плазмидная конструкция может быть амплифицирована путем размножения в бактериях Е. coli и выделена. Выделенная плазмида, содержащая последовательность ДНК, которая должна быть введена, может быть трансфецирована в клеточную культуру, например, фибробласты из куриного эмбриона (CEF), наряду с заражением этой культуры поксвирусом. Рекомбинация между гомологичной поксвирусной ДНК в плазмиде и вирусном геноме, соответственно, обеспечивает получение поксвируса, модифицированного присутствием чужеродных последовательностей ДНК.
[53]. Клетка из подходящей культуры клеток, например, культуры клеток CEF, может быть инфицирована поксвирусом. Затем инфицированную клетку можно трансфецировать первым плазмидным вектором, содержащим чужеродный ген или гены, предпочтительно под транскрипционным контролем элемента поксвируса, управляющего экспрессией. Как объяснялось выше, плазмидный вектор также содержит последовательности, способные направлять встраивание экзогенной последовательности в выбранную часть поксвирусного генома. Плазмидный вектор также необязательно содержит кассету, содержащую маркер и/или селективный ген, функционально соединенный с промотором поксвируса. Подходящий маркер или селективные гены включают, например, гены, кодирующие зеленый флуоресцентный белок, β-галактозидазу, неомицинфосфорибозилтрансферазу или другие маркеры. Использование селективных или маркерных кассет упрощает идентификацию и выделение полученного рекомбинантного поксвируса. Однако рекомбинантный поксвирус также может быть идентифицирован с помощью технологии ПЦР. Впоследствии другая клетка может быть инфицирована рекомбинантным поксвирусом, полученным, как описано выше, и трансфецирована вторым вектором, содержащим второй чужеродный ген или гены. В том случае, если указанный ген может быть введен в другой сайт вставки поксвирусного генома, второй вектор также отличается по поксвирусным гомологичным последовательностям, направляющим интеграцию второго чужеродного гена или генов в геном поксвируса. После гомологичной рекомбинации может быть выделен рекомбинантный вирус, содержащий два или более чужеродных генов. Для введения дополнительных чужеродных генов в рекомбинантный вирус этапы инфицирования и трансфекции можно повторять с использованием рекомбинантного вируса, выделенного на предыдущих этапах, для инфицирования, и с использованием дополнительного вектора, содержащего дополнительный чужеродный ген или гены, для трансфекции.
[54]. В другом варианте этапы инфицирования и трансфекции, описанные выше, взаимозаменяемы, т.е. подходящая клетка сначала может быть трансфецирована плазмидным вектором, содержащим чужеродный ген, и затем инфицирована поксвирусом. В качестве другой альтернативы каждый чужеродный ген также можно ввести в разные вирусы, совместно инфицировать клетку всеми полученными рекомбинантными вирусами и подвергнуть скринингу для выявления рекомбинанта, содержащего все чужеродные гены. Третьим альтернативным вариантом является лигирование геномной ДНК и чужеродных последовательностей в условиях in vitro и восстановление геномной ДНК рекомбинантного вируса осповакцины с использованием вспомогательного вируса. Четвертым альтернативным вариантом является гомологичная рекомбинация в Е. coli или другом виде бактерий между геномом вируса осповакцины, клонированным в виде бактериальной искусственной хромосомы (ВАС), и линейной чужеродной последовательностью, фланкированной последовательностями ДНК, которые гомологичны последовательностям, фланкирующим желаемый сайт интеграции в геноме вируса осповакцины.
[55]. Поскольку репликация рекомбинантного вируса MVA в соответствии с настоящим изобретением значительно ограничена и, соответственно, сильно ослаблена, он является идеальным кандидатом для лечения широкого круга млекопитающих, включая людей и даже людей с ослабленным иммунитетом. Более того, получение вакцин на основе MVA до известной степени не зависит от существующих производственных мощностей для стандартных вакцин, поскольку MVA можно удобно культивировать в клетках CEF. Соответственно, вакцина на основе MVA согласно настоящему изобретению может быть получена в больших количествах за короткий промежуток времени. Помимо этого вакцины на основе вектора MVA согласно настоящему изобретению могут доставлять несколько антигенов ВГВ и тем самым позволяют одновременно индуцировать высокий уровень гуморального и клеточного иммунитета. Соответственно, согласно настоящему изобретению также обеспечена фармацевтическая композиция, а также вакцина для индукции иммунного ответа в организме живого животного, включая человека.
[56]. Вакцина предпочтительно содержит вирусы MVA в диапазоне концентраций от 104 до 109 ЦПД50/мл, предпочтительно в диапазоне концентраций от 105 до 5×108 ЦПД50/мл, более предпочтительно в диапазоне концентраций от 106 до 108 ЦПД50/мл и наиболее предпочтительно в диапазоне концентраций от 107 до 108 ЦПД50/мл.
[57]. Предпочтительная доза вакцинации для человека содержит от 106 до 109 ЦПД50, наиболее предпочтительно доза составляет 106 ЦПД50 или 107 ЦПД50, или 108 ЦПД50.
[58]. Фармацевтическая композиция обычно может содержать одну или более фармацевтически приемлемых и/или одобренных добавок, таких как носители, антибиотики, консерванты, адъюванты, разбавители и/или стабилизаторы. Подходящие вспомогательные вещества могут представлять собой воду, физиологический раствор, глицерин, этанол, смачивающие или эмульгирующие агенты, вещества, забуферивающие рН, или т.п. Подходящие носители обычно включают большие, медленно метаболизируемые молекулы, такие как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот, липидные агрегаты или т.п.
[59]. Термин «фармацевтически приемлемый» означает нетоксичный материал, который не оказывает отрицательного влияния на эффективность биологической активности MVA в соответствии с настоящим изобретением. Характеристики носителя будут зависеть от пути введения. Фармацевтическая композиция может дополнительно содержать другие агенты, которые повышают активность или используются при лечении. Подходящие дополнительные факторы и/или агенты могут быть включены в фармацевтическую композицию для применения в способе иммунизации в соответствии с настоящим изобретением, чтобы получить синергетический эффект или уменьшить до минимума побочные эффекты. Методики приготовления и введения MVA в соответствии с настоящим изобретением можно найти в «Remington's Pharmaceutical Sciences» (Muck Publishing Gompany, Easton, PA, последнее издание).
[60]. Для получения вакцин рекомбинантный MVA согласно настоящему изобретению может быть превращен в физиологически приемлемую форму. Этот этап можно осуществлять на основании опыта получения поксвирусных вакцин, применяемых для вакцинации против черной оспы (как описано в Stickl, Н. et al. [1974] Dtsch. med. Wschr. 99, 2386-2392).
[61]. Например, очищенный вирус можно хранить при -80°С с титром 5×108 ЦПД50/мл, приготовленным в растворе, содержащем приблизительно 10 мМ Трис, 140 мМ NaCl, рН=7,4. Чтобы получить инъекционную форму вакцины, например, 102-108 частиц вируса могут быть лиофилизованы в 100 мл забуференного фосфатом физиологического раствора (ФСБ) в присутствии 2% пептона и 1% альбумина человека в ампуле, предпочтительно в стеклянной ампуле. В другом варианте инъекционные формы вакцины могут быть получены путем ступенчатой сублимационной сушки вируса в составе. Такой состав может содержать дополнительные добавки, такие как маннит, декстран, сахар, глицин, лактоза или поливинилпирролидон, или другие вспомогательные вещества, такие как антиоксиданты или инертный газ, стабилизаторы или рекомбинантные белки (например, сывороточный альбумин человека), подходящие для введения в условиях in vivo. Затем стеклянную ампулу герметично запечатывают и хранят в диапазоне температур от 4°С до комнатной температуры в течение нескольких месяцев. Однако ампулу предпочтительно хранят при температуре ниже -20°С, если ампула не должна быть использована в ближайшее время.
[62]. Для вакцинации или терапии лиофилизат может быть растворен в водном растворе, предпочтительно физиологическом растворе или трис-содержащем буфере, и может быть введен системно или местно, т.е. с помощью парентерального, подкожного, внутривенного, внутримышечного или любого другого пути введения, известного квалифицированному специалисту. Способ введения, доза и количество введений могут быть оптимизированы специалистами в данной области техники известным образом.
[63]. Следует понимать, что предпочтительная вакцина или фармацевтическая композиция содержит рекомбинантный MVA согласно настоящему изобретению, описанный в настоящем документе. Также следует понимать, что рекомбинантный MVA согласно настоящему изобретению может применяться при терапии или вакцинации, предпочтительно терапевтической вакцинации, предпочтительно против ВГВ.
[64]. Рекомбинантный MVA согласно настоящему изобретению может предпочтительно применяься для изготовления лекарственного средства или вакцины, которые можно применять для лечения и/или предотвращения патологического состояния, такого как инфекционное заболевание или гепатит В.
[65]. Согласно настоящему изобретению дополнительно обеспечен способ вакцинации против гепатита В. Способ вакцинации может представлять собой способ терапевтической вакцинации, т.е. для лечения заболевания. В способе вакцинации согласно настоящему изобретению вирус MVA, экспрессирующий белок оболочки из серотипа adw ВГВ, описанный в настоящем документе, и вирус MVA, экспрессирующий ядерный белок из серотипа ayw ВГВ, описанный в настоящем документе, вводят субъекту. Субъектом может быть любой субъект, определенный в настоящем документе, предпочтительно человек. Субъект предпочтительно нуждается во введении. В способе вакцинации согласно настоящему изобретению белок оболочки из серотипа adw ВГВ и ядерный белок из серотипа ayw ВГВ могут быть экспрессированы двумя различными MVA, причем каждый из MVA экспрессирует либо белок оболочки, либо ядерный белок. В данном случае субъекту должны быть введены оба MVA. Однако белок оболочки из серотипа adw ВГВ и ядерный белок из серотипа ayw ВГВ также могут быть экспрессированы одним и тем же MVA. В данном случае субъекту должен быть введен только один MVA. Следует понимать, что последний вариант является предпочтительным.
[66]. Помимо этого в область настоящего изобретения включен вирус MVA, экспрессирующий белок оболочки из серотипа adw ВГВ, описанный в настоящем документе, который дополнительно экспрессирует молекулу CD70, и вирус MVA, экспрессирующий ядерный белок из серотипа ayw ВГВ, описанный в настоящем документе, который дополнительно экспрессирует молекулу CD70, который вводят субъекту. Субъектом может быть любой субъект, определенный в настоящем документе, предпочтительно человек. Субъект предпочтительно нуждается во введении. Помимо этого субъектом предпочтительно является пациент, имеющий хронический гепатит В, который нуждается в лечебной терапии. В способе вакцинации согласно настоящему изобретению белок оболочки из серотипа adw ВГВ и молекула CD70 и ядерный белок из серотипа ayw ВГВ и молекула CD70 могут быть экспрессированы двумя различными MVA, причем каждый из MVA экспрессирует либо белок оболочки и CD70, либо ядерный белок и CD70. В данном случае субъекту должны быть введены оба MVA. Однако белок оболочки из серотипа adw ВГВ, ядерный белок из серотипа ayw ВГВ и молекула CD70 также могут быть экспрессированы одним и тем же MVA. В этом случае субъекту должен быть введен только один MVA. Следует понимать, что последний вариант является предпочтительным.
[67]. Также следует понимать, что способ вакцинации согласно настоящему изобретению включает введение MVA согласно настоящему изобретению субъекту и что MVA предпочтительно обеспечен в эффективной дозе.
[68]. Способ вакцинации согласно настоящему изобретению может включать по меньшей мере два этапа вакцинации. Согласно настоящему изобретению иммунный ответ индуцируют с помощью схем первичной вакцинации/стимулирующей вакцинации, в которых «свободные» белки, такие как белок оболочки из a/adw ВГВ и/или ядерный белок из D/ayw ВГВ, используются для первичной вакцинации, причем один или более рекомбинантных MVA согласно настоящему изобретению применяют по меньшей мере для одной стимулирующей вакцинации.
[69]. Следовательно, на первом этапе (первичная вакцинация) субъекту может быть введена «белковая вакцина». В настоящей заявке термин «белковая вакцина» относится к композиции, содержащей белок оболочки из A/adw ВГВ и/или ядерный белок из D/ayw ВГВ, предпочтительно белок оболочки и ядерный белок. Оба, белок оболочки и ядерный белок, являются предпочтительно «свободными» белками, это означает, что они предпочтительно не входят в состав вирусных частиц. Белок оболочки и ядерный белок могут присутствовать в двух композициях, которые вводят по отдельности или в комбинации друг с другом. Белок оболочки и ядерный белок также могут быть включены в одну композицию. Белок оболочки или ядерный белок, содержащийся в «белковой вакцине», может рекомбинантно вырабатываться микроорганизмом, например, бактериальной или грибковой клеткой.
[70]. Следует понимать, что «белковая вакцина» предпочтительно по существу не содержит вирусных частиц, в частности, по существу не содержит MVA. В данном случае «по существу не содержит» означает, что белковая вакцина содержит менее 103 ЦПД50/мл, предпочтительно менее 102 ЦПД50/мл, предпочтительно менее 101 ЦПД50/мл, предпочтительно менее 100 ЦПД50/мл, предпочтительно менее 10-1 ЦПД50/мл, предпочтительно менее 10-2 ЦПД50/мл. Белковая вакцина может дополнительно содержать подходящий адъювант. В настоящей заявке термин «адъювант» относится к веществу, которое усиливает, увеличивает или стимулирует иммунный ответ хозяина (опосредованный антителами и/или клетками) на антиген или его фрагмент. Подходящие адъюванты известны специалисту в данной области техники. Предпочтительный адъювант выбран из группы, включающей поли-ди(натрийкарбоксилатэтилфенокси)фосфазен (РСЕР), иммуностимулирующий олигонуклеотид, агонист Toll-подобного рецептора (TLR), сапонин или их комбинации, при этом агонист TLR предпочтительно представляет собой агонист TLR3, агонист TLR4, агонист TLR7, агонист TLR8 или агонист TLR9, и при этом иммуностимулирующий олигонуклеотид предпочтительно представляет собой поли-I/C, поли-ICLC (стабилизированная форма поли-I/C), CpG, лиганд RIG-I, лиганд STING, циклический ди-АМФ, циклический ди-ЦМФ, циклический ди-ГМФ, агонист TLR7, агонист TLR8, CTA1DD или dmLT или их комбинации. Однако авторы настоящего изобретения обнаружили, что если белковая вакцина содержит адъювант, не содержащий алюминия, такой как, например, адъювант CpG или РСЕР, способ вакцинации согласно настоящему изобретению будет индуцировать более сильный ответ Т-клеток. Этот вывод является неожиданным, поскольку стандартные вакцины, содержащие антигены ВГВ, такие как Engerix-B, как правило, содержат адъювант, содержащий алюминий, такой как гидроксид алюминия. Следовательно, описанная в настоящем документе белковая вакцина предпочтительно содержит адъювант CpG или РСЕР или оба указанных адъюванта. Согласно настоящему изобретению дополнительно обеспечен вирусный вектор, предпочтительно вирусный вектор MVA, причем адъювант представляет собой циклический ди-АМФ.
[71]. На следующем этапе (стимулирующая вакцинация) один или более рекомбинантных MVA, описанных в настоящем документе, вводят субъекту. Один или более рекомбинантных MVA могут быть включены в фармацевтическую композицию или вакцину, описанную в настоящем документе.
[72]. Как правило, рекомбинантный MVA вводят через по меньшей мере приблизительно 1 день после первичной вакцинации, предпочтительно через по меньшей мере приблизительно 5 дней, предпочтительно через по меньшей мере приблизительно 1 неделю, предпочтительно через приблизительно от 1 недели до приблизительно 8 недель, предпочтительно через приблизительно от 2 недель до приблизительно 5 недель, предпочтительно через приблизительно от 3 недель до приблизительно 4 недель.
[73]. Помимо этого согласно настоящему изобретению схема вакцинации включает две или более стимулирующих вакцинаций после первичной вакцинации. Согласно предпочтительному варианту реализации настоящего изобретения белковая вакцина используется для первичной вакцинации и первой стимулирующей вакцинации. Помимо этого согласно настоящему изобретению может быть проведен второй, третий или дополнительный этап стимулирующей вакцинации с использованием белковой вакцины. После стимулирующей вакцинации с применением белковых вакцин стимулирующую вакцинацию проводят путем введения одного или более рекомбинантных MVA, описанных в настоящем документе. Помимо этого согласно настоящему изобретению после первого введения рекомбинантного MVA может быть проведено второе, третье или дополнительное введение (дополнительные стимулирующие вакцинации).
[74]. В данном случае первую стимулирующую вакцинацию с применением белковой вакцины проводят через по меньшей мере приблизительно 1 день после предыдущего этапа вакцинации, предпочтительно через по меньшей мере приблизительно 5 дней, предпочтительно через по меньшей мере приблизительно 1 неделю, предпочтительно через приблизительно от 1 недели до приблизительно 8 недель, предпочтительно через приблизительно от 2 недель до приблизительно 5 недель, предпочтительно через приблизительно от 3 недель до приблизительно 4 недель. Любую последующую стимулирующую вакцинацию с применением рекомбинантного MVA или белковой вакцины затем проводят через по меньшей мере приблизительно 1 день после предыдущей вакцинации, предпочтительно через по меньшей мере приблизительно 5 дней, предпочтительно через по меньшей мере приблизительно 1 неделю, предпочтительно через приблизительно от 1 недели до приблизительно 8 недель, предпочтительно через приблизительно от 2 недель до приблизительно 5 недель, предпочтительно через приблизительно от 3 недель до приблизительно 4 недель.
[75]. Способ вакцинации согласно настоящему изобретению может дополнительно включать лечение субъекта с применением миРНК и/или мшРНК перед первичной/стимулирующей вакцинацией. Подходящие миРНК или мшРНК предназначены для нацеленного воздействия на гены ВГВ, уменьшая тем самым экспрессию генов-мишеней ВГВ у субъекта, инфицированного ВГВ. Предпочтительно миРНК и/или мшРНК нацелены на 3'-области РНК, кодирующих гены-мишени ВГВ. Согласно предпочтительному варианту реализации настоящего изобретения целевые 3'-области РНК, кодирующие гены-мишени ВГВ, расположены в направлении 5'-конца относительно полиА-концов РНК (т.е. целевая область расположена в направлении 5'-конца относительно полиА-хвоста или, другими словами, в направлении от 5'-конца к 3'-концу сначала располагается целевая область, за которой следует полиА-хвост). Предполагается, что при использовании миРНК мишенью является по меньшей мере один ген ВГВ. Однако в предпочтительном варианте реализации мишенями являются все гены ВГВ. Одна миРНК или мшРНК может быть использована для нацеленного воздействия на ген ВГВ. Однако для нацеленного воздействия на ген ВГВ также можно использовать более одной миРНК и/или мшРНК. Предполагается, что указанное лечение с применением миРНК и/или мшРНК снижает экспрессию (т.е. трансляцию) целевого гена (генов) по меньшей мере приблизительно на 1%, 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80% или 85%, предпочтительно по меньшей мере приблизительно на 90%. Упомянутое лечение субъекта с применением миРНК и/или мшРНК можно проводить в течение периода от 1 дня до 20 недель, от 1 недели до 19 недель, от 2 недель до 18 недель, от 3 недель до 17 недель, от 4 недель до 16 недель, от 5 недель до 15 недель, от 6 недель до 14 недель, от 7 недель до 13 недель, предпочтительно приблизительно за 8 недель до начала первичной/стимулирующей вакцинации. Авторы настоящего изобретения обнаружили неожиданный факт, что указанное лечение с применением миРНК и/или мшРНК до начала первичной/стимулирующей вакцинации увеличивает индуцированный ответ Т-клеток после первичной/стимулирующей вакцинации.
[76]. В способе иммунизации в соответствии с настоящим изобретением будет использовано терапевтически эффективное количество белковой вакцины или рекомбинантного MVA. Терапевтически эффективная доза также относится к такому количеству соединения/ингредиента, которое является достаточным для улучшения симптомов, например, лечения, заживления, предотвращения или улучшения таких состояний. Согласно предпочтительному варианту реализации настоящего изобретения иммунизация может быть профилактической и/или терапевтической. Эффективные дозы согласно настоящему изобретению для воздействия на иммунный ответ варьируются в зависимости от множества различных факторов, включая тип антигена или вакцины, способы введения, целевой сайт, независимо от того, является ли субъект человеком или животным, и является ли лечение профилактическим или терапевтическим. Предпочтительные дозы рекомбинантного MVA раскрыты в настоящем документе.
[77]. Согласно настоящему изобретению обеспечены способы иммунизации субъекта-животного, включая птиц. Предпочтительно животное представляет собой млекопитающее, включая крыс, кроликов, свиней, мышей и человека, включая введение дозы MVA субъекту. Наиболее предпочтительно субъект является человеком. Согласно одному варианту реализации настоящего изобретения субъект является взрослым.
[78]. Введение можно осуществлять с помощью любого пути введения, определенного квалифицированным специалистом. Предпочтительно введение представляет собой парентеральное введение, введение через энтеральные слизистые оболочки, предпочтительно внутримышечное, внутривенное, подкожное (например, путем царапин или инъекций), назальное (например, путем ингаляции) или оральное введение. Предпочтительными способами введения являются парентеральное введение или введение через слизистую оболочку.
[79]. Помимо этого согласно настоящему изобретению обеспечен способ введения, который является внутримышечным, причем указанный способ введения включает введение адъюванта. Предпочтительно адъювант содержит циклический ди-АМФ.
[80]. Помимо этого в область настоящего изобретения также включен способ введения, который представляет собой подкожное или внутримышечное введение, причем указанный способ введения включает введение адъюванта. Предпочтительно адъювант содержит поли-I/C или лиганд RIG-I.
[81]. В область настоящего изобретения также включены способы вакцинации, описанные выше, причем вектор для вакцинации не является MVA, а представляет собой один или более штаммов Salmonella, которые экспрессируют тот же антиген(ы), как и MVA. Следовательно, способ вакцинации, описанный в настоящем документе, применим, с необходимыми изменениями, для способов вакцинации с использованием штамма Salmonella. Указанный способ вакцинации предпочтительно представляет собой способ вакцинации через слизистую оболочку, в котором белковая вакцина предпочтительно содержит адъювант CTA1DD или dmLT.
[82]. В область настоящего изобретения также включено любое соединение, раскрытое в способах, описанных в настоящем документе, для применения в указанных способах. Например, в область настоящего изобретения включен рекомбинантный MVA для применения в способе вакцинации, описанном в настоящем документе.
[83]. В область настоящего изобретения также включена фармацевтическая композиция или вакцина, содержащая один или более из рекомбинантных векторов для вакцинации согласно настоящему изобретению. Как уже упоминалось, «вакцина» может применяться для предотвращения или лечения патологического состояния у субъекта. Упомянутый термин включает субъединичные вакцины, т.е. вакцинные композиции, содержащие антигены, которые отделены и обособленны от целого организма, с которым антиген связан в природных условиях, а также композиции, содержащие рекомбинантный поксвирус согласно настоящему изобретению, несущий, среди прочего, антиген и/или его эпитоп. Вакцина может содержать один или более дополнительных компонентов, которые усиливают иммунологическую активность активного компонента, или вакцина может быть лишена указанных компонентов. Вакцина может дополнительно содержать дополнительные компоненты, типичные для фармацевтических композиций. Вакцина согласно настоящему изобретению предпочтительно предназначена для применения у человека и/или применения в ветеринарии.
[84]. Вакцина или композиция согласно настоящему изобретению, например, вакцина, содержащая вирус MVA, обычно может содержать один или более фармацевтически приемлемых носителей, добавок, антибиотиков, консервантов, адъювантов, разбавителей и/или стабилизаторов. Подходящие вспомогательные вещества могут представлять собой воду, физиологический раствор, глицерин, этанол, смачивающие или эмульгирующие агенты, вещества, забуферивающие рН, или т.п. Подходящие носители, как правило, представляют собой крупные, медленно метаболизируемые молекулы, такие как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот, липидные агрегаты или т.п. Другие носители, описанные в US 2011/0052627 Col. 7, также могут быть добавлены к композиции.
[85]. В область настоящего изобретения также включен набор, содержащий по меньшей мере два флакона/контейнера для первичной/стимулирующей иммунизации, причем по меньшей мере один флакон/контейнер содержит белковую вакцину, описанную в настоящем документе, с первой инокуляцией (первичная инокуляция), и необязательно дополнительные флаконы для дополнительных инокуляций (стимулирующих инокуляций), при этом дополнительный флакон предпочтительно содержит рекомбинантный вектор для вакцинации согласно настоящему изобретению. Набор также содержит по меньшей мере один дополнительный флакон/контейнер, содержащий рекомбинантный вектор для вакцинации, описанный в настоящем документе, по меньшей мере для дополнительной инокуляции («стимулирующая инокуляция»). Набор может дополнительно содержать инструкции для введения субъекту рекомбинантного вектора для вакцинации.
[86]. Согласно настоящему изобретению предпочтительным субъектом является человек. В инструкциях может быть указано, что белковая вакцина, определенная в настоящем документе, и/или рекомбинантный вектор для вакцинации должен быть введен субъекту в виде нескольких (т.е., 2, 3, 4, 5, 6 и т.д.) дозировок в определенные моменты времени (например, через по меньшей мере 4 недели, по меньшей мере 6 недель, по меньшей мере 8 недель после предыдущего введения). Предпочтительно в инструкциях указано, что белковая вакцина и/или рекомбинантный вектор для вакцинации должен быть введен в виде по меньшей мере 3 или по меньшей мере 4 дозировок.
[87]. В область настоящего изобретения включен набор, описанный в настоящем документе, причем вакцина (вакцины), содержащаяся в наборе, пригодна для парентерального введения. Белковая вакцина в указанном наборе может предпочтительно содержать адъювант РСЕР и/или CpG, и рекомбинантный вектор для вакцинации может предпочтительно представлять собой MVA согласно настоящему изобретению.
[88]. В область настоящего изобретения также включен набор, описанный в настоящем документе, причем вакцина (вакцины), содержащаяся в наборе, пригодна для введения через слизистую оболочку. Белковая вакцина в указанном наборе может предпочтительно содержать адъювант CTA1DD, dmLT, РСЕР, цикло-ди-АМФ, цикло-ди-ЦМФ, цикло-ди-ГМФ или их комбинации, и рекомбинантный вектор для вакцинации может предпочтительно представлять собой штамм Salmonella, вектор на основе ЦМВ, ВВС, аденовирусный вектор или вектор на основе вируса кори, предпочтительно штамм Salmonella согласно настоящему изобретению.
[89]. Помимо этого в область настоящего изобретения также включен набор, описанный в настоящем документе, причем вакцина (вакцины), содержащаяся в наборе, пригодна для введения через слизистую оболочку. Белковая вакцина в указанном наборе предпочтительно может содержать адъювант CTA1DD, dmLT, РСЕР, поли-I/C, лиганд RIG-I, цикло-ди-АМФ, цикло-ди-ЦМФ, цикло-ди-ГМФ или их комбинации, и рекомбинантный вектор для вакцинации может предпочтительно представлять собой штамм Salmonella согласно настоящему изобретению или предпочтительно штамм Salmonella, вектор на основе ЦМВ, ВВС, аденовирусный вектор или вектор на основе вируса кори.
[90]. Согласно настоящему изобретению также обеспечен набор, в котором белковая композиция подходит для внутримышечного введения. Предпочтительно композиция содержит по меньшей мере один адъювант, который представляет собой циклический ди-АМФ.
[91]. В область настоящего изобретения также включен набор, в котором белковая композиция подходит для подкожного или внутримышечного введения. Предпочтительно композиция содержит по меньшей мере один адъювант, который представляет собой поли-I/C.
[92]. Согласно настоящему изобретению также обеспечена клетка (хозяин), содержащая рекомбинантный MVA, описанный в настоящем документе. Примеры клеток, чувствительных к поксвирусам, включают, но не ограничиваются ими, клетки линий COS, HEK-293, ВНК, СНО, ТМ4, CVI, VERO-76, HELA, MDCK, BRL ЗА и NIH/3T3. Для MVA предпочтительными клетками являются клетки линий CEF и ВНК. Дополнительные линии клеток известны специалистам в данной области техники. Введение поксвирусной конструкции в клетку может быть осуществлено путем трансфекции фосфатом кальция, электропорации, инфекции и других способов, известных в данной области техники и описанных в стандартных лабораторных руководствах, таких как Current Protocols in Molecular Biology John Wiley & Sons, Inc. New York.
[93]. Согласно настоящему изобретению также обеспечена клетка (хозяин), инфицированная рекомбинантным поксвирусом. Соответственно, клетку (хозяина) можно инфицировать вирусным вектором MVA и трансфецировать другим вектором, например, плазмидным вектором, содержащим ген, подлежащий вставке, предпочтительно под транскрипционным контролем MVA или элемента, контролирующего экспрессию, или промотора поксвируса, такого как синтетический промотор PrS. Как описано выше, плазмидный вектор содержит последовательности, способные направлять вставку гетерологичной последовательности в выбранную часть генома поксвируса, такие как последовательности, фланкирующие один из природных сайтов делеции или межгенные области.
[94]. В настоящей заявке термин «около» или «приблизительно» означает в пределах отклонения на 20%, например, в пределах отклонения на 10% или в пределах отклонения на 5% от заданного значения или диапазона.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[95]. Фиг. 1: Первичная белковая вакцинация/стимулирующая вакцинация MVA является высоко иммуногенной. (А) Открытые рамки считывания гена S и ядерного белка подтипа ayw ВГВ были вставлены в сайт делеции III (del III) генома MVA под контролем поксвирусных промоторов Р7.5 и РН5, соответственно. (В) Мыши дикого типа (n=3) были вакцинированы один раз (0 день, закрашенные столбики) или дважды (0 и 21 день, заштрихованные столбики) с применением MVA-S (1×108 и.е.), MVA-ядерный белок (1×108 и.е.) или MVAwt (1×108 и.е.). На 8 день (после первичной вакцинации) или 27 (после стимулирующей вакцинации) спленоциты стимулировали пептидами, полученными из HBsAg (S190 и S208) или HBcAg (С93), и исследовали экспрессию ИФН-γ с помощью внутриклеточного окрашивания цитокинов (ICS). (С) Мышей линии C57BL/6 вакцинировали с применением 12 мкг рекомбинантного HBsAg или HBcAg. В качестве адъюванта использовали CpG. На 8 день спленоциты стимулировали пептидами, полученными из HBsAg или HBcAg, и исследовали экспрессию ИФН-γ с помощью внутриклеточного окрашивания цитокинов (ICS). (D) У мышей линии C57BL/6 проводили первичную вакцинацию с применением 12 мкг рекомбинантного HBcAg или HBsAg, содержащего в качестве адъюванта CpG, и на 21 день стимулировали с применением MVA-ядерного белка (1×108 и.е.) или MVA-S (1×108 и.е.). На 27 день спленоциты стимулировали пептидами, полученными из HBsAg или HBcAg, и исследовали экспрессию ИФН-γ с помощью внутриклеточного окрашивания цитокинов. Сыворотки исследовали для определения антител к HBs с помощью иммунологического количественного исследования (средняя панель) или антител к НВс с помощью конкурентного ИФА (правая панель). Значения частоты ИФН-γ-вырабатывающих Т-клеток представлены после вычитания неспецифичного сигнала. S/CO - соотношение сигнал/уровень отсечения; и.е. - инфекционные единицы.
[96]. Фиг. 2: Ответы ВГВ-специфичных антител и CD4+ Т-клеток, индуцированные вакцинацией, обратно пропорциональны уровню антигенемии. (A-D) Мышей линии HBVtg с низким, средним и высоким уровнем антигенемии (n=4) иммунизировали с применением HBsAg или HBcAg, содержащего в качестве адъюванта CpG. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S (1×108 и.е.) или MVA-ядерный белок (1×108 и.е.), соответственно. На 27 день (6 день после стимулирующей вакцинации) сыворотки исследовали для определения (А) антител к HBs и (В) антител к НВс. (С) Спленоциты и (D) связанные с печенью лимфоциты мышей линии HBVtg с низким уровнем антигенемии стимулировали с применением HBsAg и исследовали для определения ИФН-γ-экспрессирующих CD4+ Т-клеток с помощью внутриклеточного окрашивания цитокинов. Значения частоты ИФН-γ-вырабатывающих Т-клеток представлены после вычитания неспецифичного сигнала. S/CO - соотношение сигнал/уровень отсечения; отриц. - отрицательный; и.е. - инфекционные единицы.
[97]. Фиг. 3: Частота ВГВ-специфичных CD8+ Т-клеток, индуцированных вакцинацией, обратно пропорциональна уровню антигенемии. Мышей линии HBVtg с низким, средним и высоким уровнем антигенемии (n=4) иммунизировали с применением 12 мкг HBsAg или HBcAg, содержащего в качестве адъюванта CpG. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S (1×108 и.е.) или MVA-ядерный белок (1×108 и.е.). На 27 день после стимулирующей вакцинации спленоциты (А) и связанные с печенью лимфоциты (В) стимулировали с применением HBsAg (S109 и S208)- или HBcAg (С93)-специфичных пептидов и исследовали для определения экспрессии ИФН-γ с помощью внутриклеточного окрашивания цитокинов. На верхней и средней панелях представлены результаты типичных животных, на нижней панели представлены значения частоты ИФН-γ-вырабатывающих Т-клеток после вычитания неспецифичного сигнала. И.е. - инфекционные единицы.
[98]. Фиг. 4: Функциональность индуцированных вакцинацией ВГВ-специфичных CD8+ Т-клеток. Мышей дикого типа, а также мышей линии HBVtg с низким и средним уровнем антигенемии иммунизировали с применением HBsAg, содержащего в качестве адъюванта CpG. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S (1×108 и.е.). На 6 день после стимулирующей вакцинации S-специфичные селезеночные CD8+ Т-клетки (А) исследовали для определения экспрессии CD 107а и ИФН-γ. (В) S-специфичные CD8+ Т-клетки из селезенки или печени исследовали для определения экспрессии ИФН-γ, ИЛ-2 и ФНО-α после стимуляции пептидом S190. (С) Окрашивание мультимеров в S190-специфичных CD8+ Т-клетках и совместное окрашивание для оценки поверхностной экспрессии CD127 и KLRG-1. И.е. -инфекционные единицы.
[99]. Фиг. 5: Гетерологичная вакцинация нарушает толерантность Т-клеток у мышей линии HBVtg с высоким уровнем антигенемии. (А) Открытые рамки считывания гена S подтипов ayw и adw помещали в сайт делеции III (del III) генома MVA под контролем сильного промотора поксвируса РН5. (B)-(D) Мышей линии HBVtg с высоким уровнем антигенемии (n>4) вакцинировали с применением 16 мкг HBsAg (подтип ayw или adw) и 16 мкг HBcAg (подтип ayw) совместно с указанными адъювантами на 0 и 14 день. На 28 день мышей подвергали стимулирующей вакцинации с применением MVA-PH5-S (5×107 и.е.; подтип ayw или adw) и MVA-ядерный белок (5×107 и.е.). На 6 день после стимулирующей вакцинации (В) спленоциты (левая панель) и связанные с печенью лимфоциты (LAL, правая панель) выделяли, стимулировали пептидами S109 и S208 (подтип adw, если указано) или С93 и исследовали для оценки экспрессии ИФН-γ с помощью внутриклеточного окрашивания цитокинов. (С) Спленоциты и LAL стимулировали с применением С-концевого пула HBsAg-специфичных 15-мерных пептидов (включающих аминокислоты с 145 по 226, подтип ayw) и исследовали для определения ИФН-γ-экспрессирующих CD4+ Т-клеток с помощью ICS. (D) Типичный график флуоресцентно-активированной сортировки клеток (FACS) для S208-специфичных CD8+ Т-клеток, экспрессирующих ИФН-γ, исследовали для того чтобы оценить экспрессию ФНО-α и ИЛ-2. Среднее значение ± станд. ошиб. сред. частоты Т-клеток, вырабатывающих ИФН-γ, представлено после вычитания неспецифичного сигнала. Ns - недостоверно. *р<0,05, **р <0,01 t-тест Стьюдента; и.е. - инфекционные единицы.
[100]. Фиг. 6: Гетерологичная вакцинация индуцирует сероконверсию у мышей линии HBVtg с высоким уровнем антигенемии. (A)-(D) Мышей линии HBVtg с высоким уровнем антигенемии (n>4) вакцинировали с применением 16 мкг HBcAg (подтип ayw) и 16 мкг HBsAg (подтип ayw или adw, как указано) с добавлением адъюванта CpG и РСЕР на 0 и 14 день. На 28 день мышей подвергали стимулирующей вакцинации с применением MVA-PH5-S (5×107 и.е.; подтип ayw или adw) и MVA-ядерный белок (5×107 и.е.). В качестве контроля 5 мышей линии HBVtg с высоким уровнем антигенемии вакцинировали адъювантами CpG и РСЕР на 0 и 14 день с последующей стимулирующей вакцинацией с применением 1×108 MVA-wt. На 6 день после стимулирующей вакцинации сыворотки исследовали для определения присутствия (А) антител к HBs или (В) антител к НВс. (С) Сыворотки мышей линии HBVtg, положительные на присутствие HBs, исследовали для определения способности нейтрализовать HBsAg подтипа ayw. (D) Представлены уровни HBsAg в сыворотке крови до и после вакцинации. Представлено среднее значение ± станд. ошиб. сред. Ns - недостоверно; S/CO - соотношение сигнал/уровень отсечения. **р<0,01 t-тест Стьюдента.
[101]. Фиг. 7: Экспрессия антигенов ВГВ векторами MVA. (А) и (В) Клетки мыши линии NIH-3T3 инфицировали MVA-S, MVA-ядерный белок или MVA-wt (при MOI=10). Через 16 ч после инфицирования (А) общие клеточные лизаты исследовали для оценки экспрессии HBsAg и HBcAg с помощью Вестерн-блоттинга. (В) Секретируемый HBsAg в супернатанте определяли с помощью HBsAg-специфичного ИФА. S/CO - соотношение сигнал/уровень отсечения.
[102]. Фиг. 8: Вакцинация с применением HBsAg с добавлением адъюванта CpG. Мышей линии HBVtg с высоким уровнем антигенемии иммунизировали с применением 12 мкг HBsAg, содержащего CpG в качестве адъюванта. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S. На 0, 27, 35, 42, 49 и 56 день после первичной иммунизации сыворотки исследовали для определения уровней HBsAg и анти-HBs. S/CO - соотношение сигнал/уровень отсечения.
[103]. Фиг. 9: Сравнение адъювантов для первичной вакцинации белковой вакциной. (А)-(С) Мышей дикого типа вакцинировали с применением 16 мкг HBsAg (подтип ayw) и 16 мкг HBcAg (подтип ayw) совместно с указанным адъювантом(ами) на 0 день. На 28 день мышей подвергали стимулирующей вакцинации с применением MVA-PH5-S (5×107 и.е.; подтип ayw) и MVA-ядерный белок (5×107 и.е.). На 6 день после стимулирующей вакцинации сыворотки исследовали, чтобы определить присутствие (А) антител к HBs и (В) антител к НВс. (С) На 6 день после стимулирующей вакцинации спленоциты исследовали методом ICS после стимуляции HBsAg (S190 и S208adw)- или HBcAg (С93)-специфичными пептидами. Столбики представляют процент (среднее ± станд. ошиб. сред.) клеток CD8+, имеющих положительные результаты окрашивания ИФН-γ, после вычитания неспецифичного сигнала. И.е. - инфекционные единицы.
[104]. Фиг. 10: Группировка мышей линии HBVtg. Мышей группировали в соответствии с их уровнями антигена, которые, в случае мышей линии HBVtg, коррелируют с титрами вируса, определенными в сыворотке.
[105]. Фиг. 11: Пептиды, использованные для стимуляции Т-клеток. В таблице приведены последовательности пептидов, использованных для определения ответов CD8+ Т-клеток, ограниченных аллелями мыши Kb/Kd MHS-I. Пул S использовали для общего определения ответов CD4+ и CD8+ Т-клеток мышей и человека.
[106]. Фиг. 12: Графический обзор схемы вакцинации из примера 4. Мышей линии HBVtg с высоким уровнем антигенемии (≥4) вакцинировали с применением 16 мкг HBsAg (подтип ayw или adw) и 16 мкг HBcAg (подтип ayw) совместно с указанными адъювантами на 0 и 14 день. На 28 день мышей подвергали стимулирующей вакцинации с применением MVA-PH5-S (5×107 и.е.; подтип ayw или adw) и MVA-ядерный белок (5×107 и.е.). На 6 день после стимулирующей вакцинации (В) спленоциты (левая панель) и связанные с печенью лимфоциты (LAL, правая панель) выделяли и стимулировали пептидами S109 и S208 (подтип adw, если указано) или С93, и исследовали для определения экспрессии ИФН-γ с помощью внутриклеточного окрашивания цитокинов (ICS).
[107]. Фиг. 13: Корреляция окрашивания мультимеров и внутриклеточных цитокинов ВГВ-специфичных CD8+ Т-клеток. Мышей линии HBVtg иммунизировали с применением 12 мкг HBsAg, содержащего в качестве адъюванта CpG. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S. Ответы ВГВ-специфичных Т-клеток детектировали на 28 день с помощью окрашивания мультимеров S190 или с помощью ICS после повторной стимуляции пептидом S190 в условиях ex vivo.
[108]. Фиг. 14: Детектирование сывороточных иммунных комплексов. Мышей линии HBVtg иммунизировали с применением HBsAg, содержащего в качестве адъюванта CpG. На 21 день мышей подвергали стимулирующей вакцинации с применением MVA-S (1×108 и.е.). На 6 день после стимулирующей вакцинации сыворотки исследовали для определения антител к HBs, HBsAg и HBsAg в осажденных иммунных комплексах. И.е. - инфекционные единицы; nd - не поддающийся детектированию.
[109]. Фиг. 15: Сравнение различных вакцинных адъювантов. Мышей дикого типа CH57BL/6 иммунизировали с применением HBcAg и HBsAg, связанных в комплекс в разных адъювантных составах. 1: CpG плюс гидроксид алюминия; 2: полифосфазен РСЕР плюс квасцы; 3: РСЕР плюс CpG плюс квасцы; 4: только CpG; 5: только РСЕР; 6: CpG плюс РСЕР. На 28 день всех животных подвергали стимулирующей вакцинации с применением MVA, экспрессирующего ядерный белок и S подтипа adw. На Фиг. 15А-В представлены гуморальные ответы на HBs (Фиг. 15А) и НВс (Фиг. 15В) через 28 дней (только первичная вакцинация белковой вакциной) и 34 дня (первичная вакцинация белковой вакциной плюс стимулирующая вакцинация MVA). На Фиг. 15C-D представлены ответы CD8+ Т-клеток на эпитопы S и ядерного белка после первичной вакцинации (Фиг. 15С) и после стимулирующей вакцинации MVA (Фиг. 15D). На Фиг. 15Е представлены результаты количественного исследования нейтрализации, при котором подтип ayw ВГВ инкубировали с указанными разведениями сыворотки перед инфицированием, и секрецию HBsAg инфицированными клетками измеряли через 4, 7 и 10 дней.
[110]. Фиг. 16: Полиантигенная открытая рамка считывания. На Фиг. 16А представлена структура полиантигенной полипептидной цепи, представленной в SEQ ID NO: 7. На Фиг. 16В схематически изображено образование субвирусных частиц, содержащих антигены HBs A/adw и C/ayw. На Фиг. 16С схематически изображено образование пустых капсидов, содержащих антигены НВс D/ayw и C/ayw.
[111]. Фиг. 17: Схематическая иллюстрация полностью расщепленных белков, полученных из полиантигенной полипептидной цепи, представленной в SEQ ID NO: 7, и их дальнейший путь.
[112]. Фиг. 18: Схематическая иллюстрация частично нерасщепленных белков, полученных из полиантигенной полипептидной цепи, представленной в SEQ ID NO: 7, и их ожидаемый дальнейший путь. Предполагается, что большая часть частично нерасщепленных белков увеличивает иммунный ответ (особенно усиливает и расширяет адаптивный иммунный ответ) за счет включения в секретируемые вирусоподобные частицы/филаменты.
[113]. Фиг. 19: Аминокислотная последовательность малого белка оболочки A2/adw2 ВГВ, включая С-концевой липкий конец (SEQ ID NO: 10). Подчеркнутая последовательность соответствует аминокислотной последовательности малого белка оболочки A2/adw2 ВГВ без С-концевого липкого конца (SEQ ID NO: 8). С-концевой липкий конец представляет собой фрагмент расщепления Р2А, который соответствует последовательности, представленной в SEQ ID NO: 9.
[114]. Фиг. 20: Аминокислотная последовательность фрагмента ядерного белка 1-149 D/ayw ВГВ, включая N- и С-концевые липкие концы (SEQ ID NO: 12). Подчеркнутая последовательность соответствует аминокислотной последовательности фрагмента ядерного белка 1-149 D/ayw ВГВ без N- и С-концевых липких концов (SEQ ID NO: 11). С-концевой липкий конец представляет собой фрагмент расщепления Р2А, который соответствует последовательности, представленной в SEQ ID NO: 9.
[115]. Фиг. 21: Аминокислотная последовательность домена RT полимеразы ВГВ, включая N- и С-концевые липкие концы (SEQ ID NO: 16). Подчеркнутая последовательность соответствует аминокислотной последовательности домена RT полимеразы ВГВ без N- и С-концевых липких концов (SEQ ID NO: 6). С-концевой липкий конец представляет собой фрагмент расщепления Т2А, который соответствует последовательности, представленной в SEQ ID NO: 13.
[116]. Фиг. 22: Аминокислотная последовательность большого белка оболочки C/ayw ВГВ, включая N- и С-концевые липкие концы (SEQ ID NO: 14). Подчеркнутая последовательность соответствует аминокислотной последовательности большого белка оболочки C/ayw ВГВ без N- и С-концевых липких концов (SEQ ID NO: 4). С-концевой липкий конец представляет собой фрагмент расщепления Т2А, который соответствует последовательности, представленной в SEQ ID NO: 13.
[117]. Фиг. 23: Аминокислотная последовательность ядерного белка C/ayw ВГВ, включая N-концевой липкий конец (SEQ ID NO: 15). Подчеркнутая последовательность соответствует аминокислотной последовательности ядерного белка C/ayw ВГВ без N-концевых липких концов (SEQ ID NO: 5).
[118]. Фиг. 24: Аминокислотная последовательность консенсусной последовательности домена RT полимеразы ВГВ (SEQ ID NO: 3).
[119]. Фиг. 25: Аминокислотная последовательность консенсусной последовательности большого белка оболочки штаммов генотипа С ВГВ (SEQ ID NO: 1).
[120]. Фиг. 26: Аминокислотная последовательность консенсусной последовательности ядерного белка штаммов генотипа С ВГВ (SEQ ID NO: 2).
[121]. Фиг. 27: Комбинация РНК-интерференции и терапевтической вакцинации. (А) Дизайн эксперимента. Трансгенные мыши HBVxfs получали ВГВ-специфичную миРНК (siHBV), нецелевую миРНК (siNEG) или не подвергались обработке. Восемь недель спустя все мыши получали первичную вакцинацию белковой вакциной - стимулирующую терапевтическую иммунизацию MVA с применением ядерного белка ВГВ и поверхностных антигенов (HBcAg и HBsAg). (В) Схематическая иллюстрация ВГВ-специфичной конструкции миРНК/мшРНК.
[122]. Фиг. 28: Уровни антигена ВГВ и гуморальный ответ, а также ответы CD8+ Т-клеток. (А) Кинетика сывороточного уровня HBeAg и HBeAg. (В) Антитела к HBs в сыворотке мышей на момент умерщвления (91 день, 13 неделя (W)). (С) Ответы CD8+ Т-клеток, измеренные в печени и селезенке после первичной/стимулирующей вакцинации.
[123]. Фиг. 29: Оценка оптимальной дозировки MVA. Мышей линии HBVtg с низким и средним уровнем антигенемии группировали в соответствии с уровнями HBeAg в сыворотке крови. (А). Группы мышей линии HBVtg (n=3-4) дважды иммунизировали с двухнедельным интервалом с применением 15 мкг частиц HBcAg, содержащих в качестве адъюванта цикло-ди-АМФ. На 28 день мышей подвергали стимулирующей вакцинации с применением 4 различных дозировок MVA-ядерный белок (3×106, 1×107, 3×107, 1×108 БОЕ, соответственно). Сыворотки мышей через 0 и 35 дней (7 день после стимулирующей вакцинации) исследовали для определения HBsAg, HBeAg, антител к HBs и антител к НВс (В) и уровней АЛТ (С). (D) На 35 день спленоциты и связанные с печенью лимфоциты мышей линии HBVtg выделяли и стимулировали пептидом B8R, полученным из MVA, или пептидом с93, полученным из HBcAg, и исследовали для определения ИФН-γ-экспрессирующих CD8+ Т-клеток с помощью внутриклеточного окрашивания цитокинов. Значения частоты ИФН-γ-вырабатывающих Т-клеток представлены после вычитания неспецифичного сигнала. В/м - внутримышечная иммунизация; S/CO - соотношение сигнал/уровень отсечения; БОЕ - бляшкообразующие единицы; U - единицы; ME - международные единицы.
[124]. Фиг. 30: Оценка цикло-ди-АМФ в качестве адъюванта для первичной иммунизации белковой вакциной. Мышей линии HBVtg со средним и высоким уровнем антигенемии группировали в соответствии с уровнями HBeAg в сыворотке крови. (А). Группы мышей линии HBVtg (n=7) иммунизировали с двухнедельным интервалом с применением смеси 15 мкг частиц HBsAg и 15 мкг HBcAg, содержащей в качестве адъюванта цикло-ди-АМФ, или комбинации CpG/PCEP. На 28 день мышей подвергали стимулирующей вакцинации с применением 108 MVA-S/ядерный белок. В качестве контролей использовали мышей линии HBVtg (n=4), получивших две инъекции цикло-ди-АМФ и стимулированных «пустым» MVA (MVAwt). Сыворотки мышей через 0 и 34 дня (6 день после стимулирующей вакцинации) исследовали для определения уровней АЛТ (В), HBsAg, HBeAg, антител к HBs и антител к НВс (C-D). (Е) На 34 день спленоциты и связанные с печенью лимфоциты мышей линии HBVtg (n=4) выделяли, стимулировали пептидом с93, полученным из HBcAg, или пептидом s208, полученным из HBsAg, и исследовали для определения ИФН-γ-экспрессирующих CD8+ Т-клеток с помощью внутриклеточного окрашивания цитокинов. Значения частоты ИФН-γ-вырабатывающих Т-клеток представлены после вычитания неспецифичного сигнала. В/м - внутримышечная иммунизация; S/CO - соотношение сигнал/уровень отсечения; БОЕ - бляшкообразующие единицы; ME - международные единицы.
[125]. Фиг. 31: Оценка оптимального пути доставки для различных адъювантов: цикло-ди-АМФ, поли-I/C и лиганд RIG-I. Мышей линии HBVtg с низким и средним уровнем антигенемии группировали в соответствии с уровнями HBeAg в сыворотке крови. (А) Группы мышей линии HBVtg (n=5) иммунизировали с двухнедельным интервалом с применением смеси 15 мкг частиц HBsAg и 15 мкг HBcAg, содержащей в качестве адъюванта цикло-ди-АМФ, поли-I/C или лиганд RIG-I. На 28 день мышей подвергали стимулирующей вакцинации с применением 6×107 MVA-S/ядерный белок. Иммунизации осуществляли исключительно внутримышечным путем, или первичную белковую иммунизацию осуществляли путем подкожного введения с последующей внутрибрюшинной стимулирующей иммунизацией. Сыворотки мышей через 0 и 34 дня (6 день после стимулирующей вакцинации) исследовали для определения HBsAg, HBeAg, антител к HBs и антител к НВс (А). Массу мышей линии HBVtg контролировали еженедельно в течение эксперимента (В). (С) На 34 день спленоциты и связанные с печенью лимфоциты мышей линии HBVtg выделяли и стимулировали пептидом B8R, полученным из MVA, пептидом s208, полученным из HBsAg, или пептидом с93, полученным из HBcAg. Затем клетки исследовали для определения ИФН-γ-экспрессирующих CD8+ Т-клеток с помощью внутриклеточного окрашивания цитокинов. Значение частоты ИФН-γ-вырабатывающих Т-клеток представлены после вычитания неспецифичного сигнала. В/м, п/к, в/б - внутримышечная, подкожная, внутрибрюшинная иммунизация, соответственно; S/CO - соотношение сигнал/уровень отсечения; БОЕ - бляшкообразующие единицы; ME - международные единицы.
[126]. Фиг. 32: Оценка новой конструкции MVA (MVA HBVvac) у мышей линии C57BL/6. (А) Схематическое представление конструкций MVA-S/ядерный белок и MVA-HBVVac. (В) Исследование методом Вестерн-блоттинга лизатов из клеток, вырабатывающих указанные клоны MVA. Окрашивание негликозилированного и гликозилированного S с использованием поликлональных антител. (С) В группах мышей линии C57BL/6 (n=5) проводили первичную вакцинацию с применением смеси 20 мкг частиц HBsAg и 20 мкг HBcAg, содержащей в качестве адъюванта цикло-ди-АМФ. Через две недели мышей подвергали стимулирующей вакцинации с применением 6×107 MVA-S/ядерный белок или 6×107 MVA-HBVvac, экспрессирующего HBsAg, HBcAg и домен RT полимеразы ВГВ. (D) Сыворотки мышей на 21 день (через 7 дней после стимулирующей вакцинации) исследовали для определения антител к HBs и антител к НВс. (Е) На 21 день спленоциты выделяли и стимулировали с применением пептидов B8R, полученных из MVA, HBsAg-, HBcAg- и ВГВ RT-специфичных пептидов и пулов пептидов. В качестве отрицательного контроля использовали пептид SIINFEKL, полученный из овальбумина. Затем клетки исследовали для определения ИФН-γ-экспрессирующих CD8+ Т-клеток путем внутриклеточного окрашивания цитокинов. Красные стрелки указывают на положительные ответы RT-специфичных CD8+ Т-клеток. В/м - внутримышечная иммунизация, соответственно; S/CO - соотношение сигнал/уровень отсечения; БОЕ - бляшкообразующие единицы; ME - международные единицы.
[127]. Фиг. 33: Нуклеотидная последовательность конструкции рекомбинантного вектора для вакцинации (rMVA), дополнительно экспрессирующего CD70 (SEQ ID NO: 27). Различные домены указанной конструкции изображены следующим образом: Del III-фланкирующая последовательность 1, промотор mH5, белок НВсоге, Р2А, молекула CD70 человека, IRES (EMCV), eGFP, Del III-фланкирующая последовательность 2.
[128]. Фиг. 34: Оценка MVA, экспрессирующего CD70, у мышей линии C57BL/6. (А) Схематическое изображение конструкций MVA-ядерный белок и MVA-ядерный белок-CD70. Оба вектора экспрессируют последовательность ядерного белка генотипа D ВГВ и GFP, чтобы обеспечить более легкую очистку. MVA-ядерный белок-CD70 дополнительно экспрессирует ген CD70. (В) В группах мышей линии C57BL/6 (n=6-7) проводили однократную первичную вакцинацию путем внутримышечной инъекции 20 мкг частиц HBcAg, содержащих в качестве адъюванта РСЕР и CpG. Через три недели мышей подвергали стимулирующей вакцинации с применением 108 и.е. MVA-ядерный белок или 108 и.е. MVA-ядерный белок-CD70 или 108 и.е. MVA-дикого типа (MVAwt), которые вводили внутрибрюшинно. (С) На 35 день спленоциты выделяли и стимулировали с применением пептида B8R, полученного из MVA, или ядерного белка С93. В качестве отрицательного контроля использовали пептид SIINFEKL, полученный из овальбумина. Затем клетки исследовали для определения ИФН-γ-экспрессирующих CD8+ Т-клеток с помощью внутриклеточного окрашивания цитокинов. Данные представлены как среднее значение ± станд. откл. сред, для каждой группы. Точки указывают значения, определенные у отдельных мышей. И.е. - инфекционные единицы.
[129]. Фиг. 35: Оценка MVA, экспрессирующего CD70, у мышей трансгенных по генам ВГВ. (А) Схематическое изображение конструкций MVA-ядерный белок и MVA-ядерный белок-CD70. Оба вектора экспрессируют последовательность ядерного белка генотипа D ВГВ и GFP, чтобы обеспечить более легкую очистку. MVA-ядерный белок-CD70 дополнительно экспрессирует ген CD70. (В) В группах трансгенных мышей с увеличенным в 1,3 раза размером генома (n=5-6) проводили однократную первичную вакцинацию путем внутримышечной инъекции 20 мкг частиц HBcAg, содержащих в качестве адъюванта РСЕР и CpG, и через три недели стимулировали с применением 108 и.е. MVA-ядерный белок или 108 MVA-ядерный белок-CD70, которые вводили путем внутрибрюшинной инъекции. В качестве контроля использовали 2 мышей, получивших, соответственно, 108 MVA дикого типа (MVAwt). (С) На 35 день связанные с печенью лимфоциты (LAL) выделяли и стимулировали с применением пептида B8R, полученного из MVA, или ядерного пептида С93. В качестве отрицательного контроля использовали нестимулированные клетки. Клетки исследовали методом проточной цитометрии после внутриклеточного окрашивания цитокинов для определения ИФН-γ (красный) и ИЛ-2 (синий). Представлены графики FACS для трех типичных животных.
ПРИМЕРЫ
[130]. Линии мышей и варианты вакцинации
[131]. Мышей линии C57BL/6 дикого типа (wt) и ВГВ-трансгенных мышей (линия HBV1.3.32 (Guidotti et al., J Virol 1995; 69:6158-69) (генотип D подтип ayw ВГВ), любезно предоставленных F. Chisari, Институт Скриппса, Ла-Йолла, Калифорния, США, получали путем разведения на собственной базе в особых условиях без патогенов в соответствии с институциональными руководящими принципами. Для белковой вакцинации мышей иммунизировали подкожно, используя рекомбинантный HBsAg из дрожжей или HBcAg из Е. coli (АРР Latvijas  , Рига, Латвия), смешанный с 31,91 мкг синтетического фосфотиоат-модифицированного CpG, ODN 1668, и/или 25 или 50 мкг поли-ди(карбоксилатэтилфенокси)фосфазена (РСЕР) в 50 мкл ФСБ. Для вакцинации с использованием MVA мышей вакцинировали путем внутрибрюшинной инъекции 1×108 инфекционных единиц соответствующего рекомбинантного MVA в 500 мкл ФСБ.
, Рига, Латвия), смешанный с 31,91 мкг синтетического фосфотиоат-модифицированного CpG, ODN 1668, и/или 25 или 50 мкг поли-ди(карбоксилатэтилфенокси)фосфазена (РСЕР) в 50 мкл ФСБ. Для вакцинации с использованием MVA мышей вакцинировали путем внутрибрюшинной инъекции 1×108 инфекционных единиц соответствующего рекомбинантного MVA в 500 мкл ФСБ.
[132]. Внутриклеточное окрашивание цитокинов, окрашивание мультимеров и количественное исследование дегрануляции
[133]. Спленоциты и связанные с печенью лимфоциты (LAL) выделяли, как описано ранее (Stress et al., Hepatology 2012; 56:873-83) и стимулировали с использованием H2-kb-или Н-2Db-расщепленных пептидов (Фигура 10) (jpt Peptide Technologies, Берлин, Германия) или рекомбинантного HBsAg (любезно предоставленного Rheinbiotech-Dynavax, Дюссельдорф, Германия) в течение 5 ч в присутствии 1 мг/мл брефелдина А (Sigma-Aldrich, Тауфкирхен, Германия). Клетки окрашивали для выявления живых/мертвых клеток с помощью моноазида бромида этидия (Invitrogen, Карлсруэ, Германия) и блокировали aнти-CD16/CD32-Fc-Block (BD Biosciences, Гейдельберг, Германия). Поверхностные маркеры окрашивали РВ-конъюгированным антителом к CD8a и ФЭ-конъюгированным антителом к CD4 (eBiosciences, Эхинг, Германия). Внутриклеточное окрашивание цитокинов (ICS) проводили с помощью FITC-конъюгированного антитела к ИФН-γ (XMG1.2), ФЭ-Су7-конъюгированного антитела к ФНО-α и АРС-конъюгированного антитела к ИЛ-2 (eBiosciences, Эхинг, Германия) с использованием набора Cytofix/Cytoperm (BD Biosciences, Гейдельберг, Германия) в соответствии с рекомендациями производителя.
[134]. Для количественного исследования дегрануляции спленоциты стимулировали пептидом в присутствии монензина, брефелдина А, FITC-конъюгированного антитела к CD 107а и АРС-конъюгированного антитела к CD107b в течение 5 часов с последующим окрашиванием поверхности с использованием Pacific Blue CD8a, и внутриклеточное окрашивание цитокинов проводили с использованием PerCP-Су5.5 ИФН-γ (eBiosciences, Эхинг, Германия) с помощью набора Cytofix/Cytoperm (BD Biosciences, Гейдельберг, Германия) в соответствии с рекомендациями производителя.
[135]. Для окрашивания мультимеров спленоциты и LAL окрашивали с использованием ФЭ-конъюгированных мультимеров S190 (VWLSVIWM, SEQ ID NO: 19) или MVA B8R (TSYKFESV, SEQ ID NO: 20) в течение 20 минут с последующим окрашиванием Pacific Blue CD8a, FITC KLRG1 и APC CD 127 (eBiosciences, Эхинг, Германия) в присутствии антитела к рецептору Fc (клон 2.4G2) в течение 20 минут. Данные получали методом флуоресцентно-активированной сортировки клеток (FACS) на aFACSCanto II (BD Biosciences, Гейдельберг, Германия) и анализировали с использованием программного обеспечения FlowJo (Treestar, Эшланд, США).
[136]. Серологический анализ
[137]. Уровни HBsAg, HBeAg, антител к HBs и антител к НВс в сыворотке крови определяли в разведениях 1:20 с использованием устройства для количественного исследования AXSYM™ (Abbott Laboratories, Эбботт-Парк, Иллинойс, США). Количественное определение титров ВГВ в сыворотке крови с помощью ПЦР в режиме реального времени проводили, как описано ранее (Untergasser et al., Hepatology 2006; 43:539-47).
[138]. Количественное исследование нейтрализации
[139]. Клетки HepaRG, дифференцированные и культивированные, как описано (Lucifora et al., J Hepatol 2011; 55:996-1003), инфицировали с применением 200 ДНК-содержащих частиц ВГВ в оболочке/клеток (подтип ayw) в двух повторах в присутствии последовательного разведения сывороток от вакцинированных мышей (1:33, 1:100, 1:333 и 1:1000). В качестве положительного контроля использовали 0,8 международной единицы антитела Hepatect™ CP (Biotest Pharma GmbH, Драйайх, Германия). Через 24 часа после инфицирования клетки трижды промывали ФСБ и добавляли 1 мл среды для дифференцировки. Супернатанты собирали на 4, 7 и 10 день после инфицирования, и HBsAg детектировали в разведениях 1:20 с помощью иммуноанализа.
[140]. Статистический анализ
[141]. Статистические анализы проводили с использованием программного обеспечения Prism5 (GraphPad, Сан-Диего, США). Результаты представлены как среднее значение ± стандартная ошибка среднего. Различия между группами анализировали для определения статистической значимости с использованием двухсторонних t-тестов Стьюдента.
[142]. Получение вакцин MVA
[143]. Рекомбинантный MVA получали путем гомологичной рекомбинации и выбора ряда хозяев, как описано ранее (Staib et al., Biotechniques 2003; 34:694-6, 698, 700). Полные открытые рамки считывания HBcAg (генотип D подтип ayw) и HBsAg (генотип D подтип ayw или adw) клонировали в MVA-переносящие плазмиды pIIIΔHR-PH5 или pIIIΔHR-Р7.5, помещая тем самым белки ВГВ под контроль ранних/поздних ВОВ-специфичных промоторов РН5 (HBcAg ayw/HBsAg ayw/HBsAg adw) или P7.5 (HBsAg ayw). После конструирования каждого вируса проверяли экспрессию гена, последовательность вставленной ДНК и чистоту вируса. Для получения вакцинных препаратов MVA размножали стандартными способами в CEF, очищали с помощью ультрацентрифугирования через сахарозу, восстанавливали в 1 мМ Трис-HCl, рН=9,0 и титровали в соответствии со стандартной методологией (Staib et al., Methods Mol Biol 2004; 269:77-100).
[144]. Иммуноблоттинг
[145]. Фибробласты мыши линии NIH-3T3 (CRL-1658) культивировали в среде RPMI 1640, дополненной 10% фетальной сыворотки теленка (ФСТ), 100 ед./мл пенициллина и 100 мкг/мл стрептомицина. Клетки собирали в буфере для лизиса (50 мМ Трис-HCl [рН=8,0], 150 мМ NaCl, 1% Nonidet Р-40, 0,02% NaN3 и 100 мкг/мл фенилметилсульфонилфторида) через 16 ч после инфицирования, разделяли с помощью электрофореза в 12% ДСН-ПААГ (SDS-PAGE) и переносили на нитроцеллюлозную мембрану путем блоттинга (0,45 мкМ, Bio-Rad, Мюнхен, Германия). Мембраны инкубировали при 4°С в присутствии антитела к НВс (антисыворотка Н800, любезно предоставленная Н. Schaller), антитела к HBs (Murex HBsAg версия 3, Abbott, Эбботт-Парк, Иллинойс, США) или антитела к актину (Sigma, Мюнхен, Германия), разведенных в соотношениях 1:10000, 1:50 и 1:10000, соответственно. Меченые пероксидазой хрена вторичные антитела мыши и антитела кролика (Dianova, Гамбург, Германия) использовали в разведении 1:5000 в течение 1 ч при 21°С. Антитела разводили в забуференном фосфатом физиологическом растворе, содержащем 5% обезжиренного молока. Усиленную хемилюминесценцию использовали в соответствии с указаниями производителя (Roche, Манхейм, Германия).
[146]. Секретируемый HBsAg в супернатанте культивируемых клеток количественно определяли с использованием Abbott AxSYM HBsAg (Abbott Laboratories, Эбботт-Парк, Иллинойс, США).
[147]. Пример 1: Первичная белковая вакцинация/стимулирующая вакцинация MVA индуцирует сильный иммунитет против ВГВ
[148]. Две вакцины MVA, экспрессирующие HBs (MVA-S) или НВс (MVA-ядерный белок), получали из генотипа D подтипа ayw ВГВ (Фиг. 1А). Результаты HBsAg-специфичного Вестерн-блоттинга и ИФА подтвердили правильную экспрессию белка из любого MVA (Фиг. 7А, В).
[149]. Для оценки иммуногенности мышей линии C57BL/6 (wt) иммунизировали путем внутрибрюшинной инъекции MVA-S, MVA-ядерный белок или MVAwt (108 инфекционных единиц), и частоту ИФН-γ-вырабатывающих CD8+ Т-клеток определяли с помощью внутриклеточного окрашивания цитокинов (ICS) на 8 день после иммунизации. Введение путем в/б инъекции использовали, поскольку планировалось системное распределение MVA. Иммунизация с применением MVA-S, MVA-ядерный белок и MVAwt индуцировала сопоставимые ответы CD8+ Т-клеток на иммунодоминантный B8R-пептид, полученный из MVA, который был усилен после второй иммунизации (Фиг. 1В). Напротив, не было обнаружено ответов ВГВ-специфичных CD8+ Т-клеток (Фиг. 1В).
[150]. Для того чтобы индуцировать ВГВ-специфичный иммунитет, проводили гетерологичные первичные/стимулирующие вакцинации. Мыши получали 12 мкг частиц рекомбинантного HBsAg или HBcAg (подтип ayw) с CpG в качестве адъюванта. Через 8 дней после вакцинации с применением HBsAg частота селезеночных CD8+ Т-клеток, секретирующих ИФН-γ в ответ на стимуляцию пептидами S190 и S208, составляла приблизительно 0,6%, тогда как ответы CD8+ Т-клеток на С93 после иммунизации HBcAg не детектировались (Фиг. 1С). Стимулирующая вакцинация на 21 день с применением MVA-S или MVA-ядерный белок способна индуцировать высокую частоту HBsAg- или HBcAg-специфичных CD8+ Т-клеток, а также высокие титры антител к HBs или антител к НВс, соответственно (Фиг. 1D). В совокупности полученные данные указывают на то, что для индукции ВГВ-специфичных Т-клеток требовалась гетерологичная первичная/стимулирующая вакцинация.
[151]. Пример 2: Высокий уровень антигенемии предотвращает индукцию ВГВ-специфичного иммунитета
[152]. Для того чтобы исследовать влияние нагрузки антигеном ВГВ на индукцию ВГВ-специфичных иммунных ответов, трансгенных (HBVtg) мышей HBV1.3.32 разделяли на группы с низким, средним и высоким уровнем антигенемии в соответствии с уровнями HBeAg в сыворотке крови перед вакцинацией (Фиг. 10). Через 6 дней после стимулирующей вакцинации титры антител к HBs у мышей, получавших HBsAg/MVA-S, были выше в группе с низким уровнем антигенемии, по сравнению с мышами из группы со средним уровнем антигенемии, и не поддавались детектированию у мышей в группе с высоким уровнем антигенемии (Фиг. 2А). Даже через 35 дней после стимуляции с применением MVA-S мыши с высоким уровнем антигенемии не имели детектируемых титров антител к HBs, и уровни HBsAg оставались низкими (Фиг. 11). Чтобы изучить возможность образования комплексов антител к HBs с избыточными количествами HBsAg, которые, соответственно, могут избегать детектирования, 131 осажденный белковый комплекс растворяли с мочевиной и повторяли иммуноанализ. Таким способом были обнаружены иммунные комплексы HBsAg-антитело к HBs у вакцинированных мышей линии HBVtg с высоким и средним уровнем антигенемии, но не с низким уровнем антигенемии (Фиг. 14). Однако HBcAg-специфичные антитела детектировали в сыворотках крови мышей, вакцинированных HBcAg/MVA-ядерный белок, из всех групп, при этом также наблюдали тенденцию обратной корреляции титров с уровнем антигенемии (Фиг. 2В). Для того чтобы исследовать индуцированный вакцинацией ответ CD4+ Т-клеток спленоциты и связанные с печенью лимфоциты (LAL) стимулировали с применением HBsAg. Несмотря на то, что у мышей дикого типа была обнаружена высокая частота HBsAg-специфичных CD4+ Т-клеток, ВГВ-специфичные CD4+ Т-клетки не были обнаружены ни в одной из групп мышей линии HBVtg (Фиг. 2С, D).
[153]. Также как и в случае титров антител, была обнаружена обратная корреляция между антигенемией и ответами специфичных к ВГВ CD8+ Т-клеток. У мышей с высоким уровнем антигенемии иммунизация с применением HBsAg/MVA-S, а также HBcAg/MVA-ядерный белок не индуцировала детектируемые HBsAg- или HBcAg-специфичные CD8+ Т-клетки ни на периферии (в селезенке), ни в печени, месте репликации ВГВ (Фиг. 3А, В). У мышей со средней или низкой нагрузкой HBeAg развились ответы S190- и S208-специфичных CD8+ Т-клеток на HBsAg/MVA-S и ответы С93-специфичных Т-клеток на вакцинацию HBcAg/MVA-C. Частота ВГВ-специфичных CD8+ Т-клеток, которую детектировали у мышей с низким уровнем антигенемии, была выше, чем у мышей со средним уровнем антигенемии. Важно отметить, что частота MVA B8R-специфичных CD8+ Т-клеток не зависела от антигенемии и была сопоставима между всеми группами, что указывает на равную эффективность вакцинации (Фиг. 3А, В).
[154]. При хронической инфекции и устойчивости антигена могут вырабатываться CD8+ Т-клетки с истощенным, нефункциональным фенотипом. В таких условиях количество антигенспецифичных Т-клеток в значительной степени недооценивается при функциональных тестах, таких как выработка ИФН-γ. В этой связи проводили окрашивание S190-, С93- и B8R-специфичных мультимеров, которое не выявило детектируемых уровней ВГВ-специфичных CD8+ Т-клеток в селезенке или печени иммунизированных мышей с высоким уровнем антигенемии, в то время как CD8+ Т-клетки, положительные на присутствие мультимеров B8R, легко поддавались детектированию. Полученные результаты указывают на то, что вакцина действительно не была способна индуцировать ВГВ-специфичные Т-клетки в этой группе. В группах с низким и средним уровнем антигенемии для ответов, специфичных в отношении S190 ВГВ и MVA-B8R, было характерно аналогичное соотношение мультимер-положительных и ИФН-γ-положительных CD8+ Т-клеток (Фиг. 13). В совокупности уровни антигена ВГВ влияют на то, насколько эффективно гетерологичная первичная/стимулирующая вакцинация может индуцировать ВГВ-специфичные антитела, а также ответы Т-клеток.
[155]. Пример 3: Антигенемия влияет на качество индуцированных вакцинацией ответов
[156]. Важные эффекторные функции CD8+ Т-клеток включают выработку ИЛ-2 и ФНО-α, помимо ИФН-γ, а также способность к дегрануляции в ответ на стимуляцию пептидом, которую можно исследовать с помощью оценки поверхностной экспрессии CD107а. При стимуляции пептидом S190 ИФН-γ+ S190-специфичные селезеночные CD8+ Т-клетки, индуцированные у мышей дикого типа и мышей линии HBVtg с низким уровнем антигенемии при иммунизации HBsAg/MVA-S, дегранулировали в аналогичных соотношениях (72,3 и 73,4%, соответственно) (Фиг. 4А), также наблюдали сопоставимую экспрессию ИЛ-2 и ФНО-α в CD8+ Т-клетках селезенки и печени, полученных от мышей со средним уровнем антигенемии, которые также были способны к дегрануляции при стимуляции пептидом, хотя и в меньшей степени (62%), но не экспрессировали ИЛ-2 (Фиг. 4В).
[157]. Чтобы определить статус дифференцировки мультимерсвязывающих клеток и их способность к пролиферации, проводили окрашивание CD127 и KLRG-1. Вакцинация мышей дикого типа и мышей линии HBVtg с низким уровнем антигенемии индуцировала высокий процент S190-специфичных CD 127+ KLRG-1-мультимерсвязывающих клеток в печени и селезенке, которые считаются временными предшественниками долгоживущих клеток, способными пролиферировать и давать новое потомство эффекторных клеток (Фиг. 4С). Однако у мышей со средним уровнем антигенемии данные клетки с трудом поддавались детектированию (Фиг. 4С). Полученные данные указывают на то, что экспрессия антигена ВГВ уменьшает полифункциональность CD8+ Т-клеток и, в частности, секрецию ИЛ-2 эффекторными клетками и их способность к пролиферации.
[158]. Пример 4. Сравнение адъювантов для первичной белковой вакцинации
[159]. Для того чтобы исследовать способность полифосфазенового адъюванта РСЕР усиливать иммуностимулирующий эффект CpG, РСЕР использовали вместо CpG или добавляли к CpG для состава белковой вакцины и комбинации HBsAg и HBcAg.
[160]. Мышей дикого типа вакцинировали с применением 16 мкг HBsAg (подтип ayw) и 16 мкг HBcAg (подтип ayw) с соответствующим адъювантом(-ами) на 0 день. На 28 день мышей подвергали стимулирующей вакцинации с применением MVA-PH5-S (5×107 и.е., подтип ayw) и MVA-ядерный белок (5×107 и.е.). На 6 день после стимулирующей вакцинации сыворотки исследовали для определения антител к HBs (Фиг. 9А) и антител к НВс (Фиг. 9В). На 6 день после стимулирующей вакцинации спленоциты исследовали методом ICS после стимуляции HBsAg (S190 и S208adw)- или HBcAg (С93)-специфичными пептидами (Фиг. 9С). Столбики представляют процент (среднее значение ± станд. ошиб. сред.) клеток CD8+, имеющих положительные результаты окрашивания ИФН-γ, после вычитания неспецифичного сигнала. И.е. - инфекционные единицы.
[161]. Использование РСЕР (по отдельности или в комбинации с CpG) обеспечивало преимущества при индукции антител к HBs и антител к НВс, по сравнению с CpG по отдельности, после первичной белковой вакцинации/стимулирующей вакцинации MVA у мышей дикого типа, тогда как ответы CD8+ Т-клеток были сопоставимы (Фиг. 9А-С).
[162]. Пример 5: Сравнение комбинаций адъювантов
[163]. На следующем этапе определяли влияние различных адъювантов на гуморальные и клеточные иммунные ответы. В этой связи у мышей линии СН57В1/6 дикого типа проводили первичную вакцинацию с применением частиц HBcAg и HBsAg, которые комбинировали в разных составах, содержащих адъюванты. В группах 1-3 (n=3) HBsAg связывали в комплекс с гидроксидом алюминия и комбинировали с HBcAg, CpG или полифосфазеновым адъювантом или обоими. Группы 4-6 (n=3) вакцинировали с использованием частиц HBcAg и HBsAg, содержащих в качестве адъюванта CpG или полифосфазен, или оба адъюванта, но без соединений алюминия. На 28 день всех животных подвергали стимулирующей иммунизации с применением MVA, экспрессирующего ядерный белок и S подтипа adw.
[164]. Гуморальный ответ на HBs и НВс определяли через 28 дней (только для первичной белковой вакцинации) и через 34 дня (белковая вакцинация плюс стимулирующая вакцинация MVA). На Фиг. 15А и 15В показано, что гуморальные ответы, в частности на HBs, неожиданно были значительно более выраженными, если соединения алюминия не были использованы. На Фиг. 15C-D показаны ответы CD8+ Т-клеток на эпитопы S и ядерного белка после первичной белковой вакцинации (Фиг. 15С) и после стимулирующей вакцинации MVA (Фиг. 15D).
[165]. Ответы Т-клеток детектировали непосредственно после первичной белковой вакцинации, если вакцинные составы не содержали алюминия. Интересно отметить, что после стимулирующей вакцинации MVA у всех мышей во всех группах (о чем свидетельствуют B8R-специфичные ответы) с равной эффективностью развились ответы Т-клеток, специфичные в отношении ядерного белка, в то время как животные, вакцинированные без алюминия, снова имели гораздо более выраженные ответы S-специфичных CD8+ Т-клеток.
[166]. Пример 6: Вакцинация с применением гетерологичного подтипа HBsAg нарушает толерантность Т-клеток и индуцирует сильную выработку антител у мышей линии HBVtg с высоким уровнем антигенемии
[167]. Сыворотки мышей исследовали для определения их способности к нейтрализации после вакцинации. Мыши, вакцинированные HBsAg подтипа adw, смогли перекрестно нейтрализовать подтип ayw ВГВ даже при высоких разведениях вплоть до 1:1000 (Фиг. 15Е).
[168]. На следующем этапе усиливали иммуногенность гетерологичной первичной белковой вакцинации/стимулирующей вакцинации MVA для преодоления толерантности в присутствии более высокой нагрузки антигеном ВГВ.
[169]. Чтобы проверить, улучшит ли более сильный антигенный стимул эффективность вакцинации, разрабатывали новые MVA, экспрессирующие HBsAg, под контролем более сильного промотора РН5 (Фиг. 5А), и проводили вторую белковую вакцинацию на 14 день (Фиг. 12). Помимо этого сравнивали HBsAg подтипа ayw (идентичен мышам HBVtg) и adw. Помимо этого РСЕР добавляли к CpG для состава белковой вакцины и комбинировали HBsAg и HBcAg во время первичной и стимулирующей вакцинации, чтобы получить иммунные ответы на несколько антигенов ВГВ. Применение данной модифицированной схемы вакцинации (первичная вакцинация с применением комбинации HBsAg/HBcAg, содержащей в качестве адъюванта CpG и РСЕР, на 0 и 14 день с последующей стимулирующей вакцинацией на 28 день с использованием MVA-S/MVA-ядерный белок, которые экспрессируют антигены под контролем более сильного промотора РН5) позволило нарушить толерантность у мышей линии HBVtg с высоким уровнем антигенемии и индуцировать HBsAg- и HBcAg-специфичные CD8+ и CD4+ Т-клетки (Фиг. 5В, С).
[170]. На следующем этапе изучали, улучшит ли частичное несоответствие между вакциной и целевым антигеном эффективность вакцины (Schirmbeck et al., Eur J Immunol 2003; 33:3342-52). Любой вакцинный антиген, Sayw или Sadw, индуцировал CD8+ Т-клетки, нацеленные к обоим подтипам (Фиг. 5В), согласно результатам определения с использованием пептида S208, специфичного для подтипа (Фиг. 11). Однако гетерологичная Sadw-содержащая вакцина индуцировала более сильные ответы CD8+ Т-клеток и детектируемые ответы CD4+ Т-клеток (Фиг. 5В, С). Аналогично более ранним наблюдениям для S-специфичных CD8+ Т-клеток, полученным у мышей со средним уровнем антигенемии (Фиг. 4В), было обнаружено, что селезеночные S208-специфичные CD8+ Т-клетки секретируют ИФН-γ и в некоторой степени ФНО-α, однако имеют лишь незначительную экспрессию ИЛ-2 (Фиг. 5D).
[171]. Примечательно, что только Sadw-содержащий вакцинный состав, но не вакцинный состав, содержащий Sayw, был способен индуцировать детектируемые уровни антител к HBs у мышей с высоким уровнем антигенемии (Фиг. 6А), тогда как оба состава индуцировали антитела к НВс (Фиг. 6В). Важно отметить, что антитела к HBs, вырабатываемые при введении Sadw, были способны нейтрализовать частицы ВГВ подтипа ayw (Фигура 6С). Одновременно с индукцией нейтрализующих антител к HBs в группе вакцинации с применением Sadw уровни HBsAg значительно снижались до низких уровней (Фиг. 6D). В совокупности полученные данные указывают на то, что модифицированная схема вакцинации действительно позволила нарушить толерантность В- и Т-клеток у мышей линии HBVtg.
[172]. Пример 7. Полиспецифичный иммунный ответ, индуцируемый полиантигенным MVA
[173]. На следующем этапе проводили сравнение индукции иммунных ответов на один, два и более антигенов ВГВ с использованием полиантигенного MVA. Был обнаружен неожиданный факт, что гуморальные, а также клеточные иммунные ответы на S или S и Pol были улучшены при совместной экспрессии ядерного белка вакцинным вектором MVA.
[174]. Пример 8: Комбинация РНК-интерференции и терапевтической вакцинации
[175]. ВГВ-трансгенных мышей линии HBVxfs, экспрессирующих антигены ВГВ с высоким титром, обрабатывали ВГВ-специфичными миРНК, нацеленными на 3'-область всех РНК ВГВ. Обработка миРНК снизила уровни HBeAg и HBsAg на 90%. Через 8 недель животных вакцинировали с применением первичной белковой вакцины/стимулирующей вакцины MVA-ВГВ, чтобы индуцировать антитела к HBs и ВГВ-специфичные Т-клетки (Фиг. 27). В качестве белковой вакцины использовали частицы HBsAg и HBcAg, содержащие в качестве адъюванта CpG и РСЕР. Вектор для вакцинирования MVA экспрессировал полную открытую рамку считывания S и ядерных белков ВГВ. В качестве контролей использовали мышей, которые не получали миРНК, не были вакцинированы, и мышей, которые не получали миРНК и не были вакцинированы.
[176]. Через 6 дней после стимулирующей вакцинации мышей умерщвляли и определяли уровни HBeAg и HBsAg, а также титры антител к HBs (Фиг. 28А, В). Т-клетки выделяли из печени и селезенки, стимулировали ВГВ-специфичными пептидами в условиях ex vivo, окрашивали для оценки экспрессии ИФН-γ методом ICS и исследовали методом проточной цитометрии (Фиг. 28С).
[177]. Пример 9: Оценка оптимальной дозы MVA
[178]. В первой группе экспериментов оценивали самую низкую дозировку MVA для гетерологичной первичной белковой вакцинации/стимулирующей вакцинации MVA, которая могла обладать удовлетворительной иммуногенностью и могла бы нарушить иммунную толерантность у мышей линии HBVtg. Соответственно, группы мышей HBVtg с низким и средним уровнем антигенемии дважды иммунизировали с двухнедельным интервалом с применением 15 мкг частиц HBcAg, содержащих в качестве адъюванта бис-3',5'-циклический димерный аденозинмонофосфат (цикло-ди-АМФ). На 28 день мышей подвергали стимулирующей вакцинации с применением 4 различных дозировок MVA-ядерный белок (3×106, 1×107, 3×107, 1×108 БОЯ, соответственно) (Фиг. 29А). Гуморальные и клеточные иммунные ответы, вызванные схемами иммунизации, в которых применяли различные дозировки MVA, оценивали через 7 дней после стимулирующей иммунизации (35 день).
[179]. Сыворотки мышей через 0 и 35 дней (7 день после стимулирующей вакцинации) исследовали для определения HBsAg, HBeAg, антител к HBs и антител к НВс (Фиг. 29В). Все схемы иммунизации вызывали аналогичные уровни антител к НВс, которые детектировали в сыворотке мышей линии HBVtg на 35 день. Помимо этого все группы мышей имели значительное снижение HBsAg в крови. Этот эффект не был опосредован антителами к HBs, поскольку схема иммунизации не включала HBsAg, что имеет существенное значение для сероконверсии HBsAg в модели HBVtg. Интересно отметить, что мыши линии HBVtg из групп, которые получали более высокие дозировки MVA-ядерный белок (3×107 и 1×108 БОЯ) в качестве стимулирующей вакцинации, имели значительно сниженные уровни HBeAg в сыворотке крови (Фиг. 29В). Более того, небольшое повышение уровня аланинаминотрансферазы печени (АЛТ) наблюдали также в группах мышей, которые получали более высокие дозировки MVA-ядерный белок (3×107 и 1×108 БОЯ) (Фиг. 29С). Полученные данные свидетельствуют о том, что протоколы иммунизации в двух указанных группах мышей приводили к подавлению репликации ВГВ в печени, возможно, вследствие повышенной активности Т-клеток, специфичных в отношении HBcAg. Действительно, окрашивание внутриклеточного ИФН-γ в связанных с печенью лимфоцитах (LAL) и спленоцитах выявило, что мыши линии HBVtg, которые были иммунизированы более высокими дозировками MVA-ядерный белок, могли иметь более эффективные ответы ВГВ-специфичных CD8+ Т-клеток, особенно в печени (Фиг. 29D). Одновременно с этим ответы MVA-специфичных CD8+ Т-клеток не были значительно увеличены при введении более высокой дозировки MVA, использованной для иммунизации.
[180]. На основании полученных результатов можно сделать вывод о том, что дозировка MVA-ядерный белок 3×107 БОЯ в случае гетерологичной первичной белковой вакцинации/стимулирующей вакцинации MVA является достаточной для нарушения иммунной толерантности у мышей HBVtg с низким и средним уровнем антигенемии.
[181]. Пример 10: Оценка цикло-ди-АМФ в качестве адъюванта для первичной белковой вакцинации
[182]. Отсутствие безопасного и эффективного адъюванта, индуцирующего сбалансированный ответ Th1/Th2 CD4+ Т-клеток, может являться препятствием для начала клинических исследований. Более того, активация недавно идентифицированного цитоплазматического рецептора распознавания структур, STING, является интересной альтернативой терапевтической вакцинации. В этой связи исследовали эффективность цикло-ди-АМФ как потенциального нового адъюванта для терапевтической вакцины против гепатита В. С этой целью группы мышей линии HBVtg со средним и высоким уровнем антигенемии (n=7) дважды получили первичную белковую вакцину и стимулирующую вакцину MVA. Частицы HBsAg и HBcAg для первичной белковой вакцинации комбинировали и добавляли адъювант цикло-ди-АМФ или ранее установленную комбинацию CpG с полифосфазенами (РСЕР). На 28 день мышей подвергали стимулирующей вакцинации с применением смеси MVA-S/ядерный белок (Фиг. 30А). В качестве контролей использовали мышей HBVtg (n=4), которые получали инъекцию цикло-ди-АМФ и «пустой» MVA (MVAwt). Эффективность вакцинных препаратов в отношении индукции гуморального и клеточного иммунного ответа сравнивали на 34 день (через 6 дней после стимулирующей вакцинации).
[183]. Ни один из протоколов иммунизации с применением цикло-ди-АМФ или CpG/PCEP не влиял на уровни HBeAg в сыворотке крови мышей HBVtg с высоким уровнем антигенемии (Фиг. 30С). Оба испытываемых вакцинных состава индуцировали значительный гуморальный ответ на НВс. Однако иммунизация с применением цикло-ди-АМФ вызывала значительно более высокие титры антител к НВс по сравнению со схемой CpG/PCEP (р<0,05) (Фиг. 30С). Интересно отметить, что оба протокола иммунизации привели к сероконверсии по HBsAg с появлением антител к HBs у всех исследованных мышей линии HBVtg (Фиг. 30D). Высокие уровни антител к HBs, вызванные вакцинами, содержащими в качестве адъюванта цикло-ди-АМФ или CpG/PCEP, связывали циркулирующий HBsAg и удаляли его из сыворотки крови мышей. Напротив, мыши линии HBVtg, которые получали только цикло-ди-АМФ, с последующей стимулирующей вакцинацией MVAwt, не вырабатывали антитела к HBs, и уровни HBsAg в сыворотке крови этих мышей оставались неизменными. Важно отметить, что оба вакцинных состава индуцировали значительные ответы HBsAg-специфичных (s208) и HBcAg-специфичных (с93) CD8+ Т-клеток, которые детектировали в селезенке (р<0,05) и, в частности, в связанных с печенью лимфоцитах у мышей линии HBVtg (р<0,05) (Фиг. 30Е), которые сопровождались повреждением печени легкой степени тяжести, вызванным Т-клетками, вследствие увеличения АЛТ (Фиг. 30В). Отсутствовали статистически значимые различия величины ответов ВГВ-специфичных CD8+ Т-клеток, вызванных схемами с применением цикло-ди-АМФ или CpG/PCEP.
[184]. Учитывая полученные данные, цикло-ди-АМФ считается эффективным адъювантом для терапевтической первичной белковой вакцинации/стимулирующей вакцинации MVA даже у мышей линии HBVtg с высоким уровнем антигенемии.
[185]. Пример 11: Оценка оптимального пути доставки для различных адъювантов: цикло-ди-АМФ, поли-LCIC и лиганд RIG-I.
[186]. Для того чтобы выбрать подходящий адъювант для первичной белковой иммунизации для терапевтической первичной белковой вакцинации/стимулирующей вакцинации MVA проводили расширенный скрининг. Задача заключалась в том, чтобы сравнить эффективность цикло-ди-АМФ с двумя потенциальными новыми адъювантами для терапевтической вакцины против гепатита В: поли-LCIC и лигандом RIG-I. Помимо этого изучали различные протоколы иммунизации, чтобы найти наиболее эффективный способ применения. С этой целью в группах мышей линии HBVtg с низким и средним уровнем антигенемии (n=5) дважды проводили первичную белковую вакцинацию и стимулирующую вакцинацию MVA (Фиг. 30А). Частицы HBsAg и HBcAg для первичной белковой вакцинации комбинировали и добавляли адъювант цикло-ди-АМФ, поли-LCIC или лиганд RIG-I. На 28 день мышей подвергали стимулирующей вакцинации с применением смеси MVA-sAg и MVA-ядерный белок. Иммунизацию проводили с помощью только внутримышечного (в/м) пути введения либо первичную белковую вакцинацию проводили путем подкожного введения (п/к) с последующей стимулирующей вакцинацией путем внутрибрюшинного (в/б) введения. Эффективность различных составов вакцин и путей их применения сравнивали в отношении индукции гуморальных и клеточных иммунных ответов на 34 день (через 6 дней после стимулирующей вакцинации).
[187]. Все протоколы вакцинации эффективно снижали уровни HBsAg в сыворотках крови мышей линии HBVtg. Это было связано с тем, что все исследованные адъюванты и пути доставки могли вызывать высокие титры антител к HBs, которые образовывали комплексы с HBsAg в крови мышей. Аналогичным образом, уровни индуцированных антител к НВс были сопоставимы между группами мышей, при этом способ внутримышечной иммунизации имел тенденцию к усилению индукции антител к НВс. Тем не менее, более низкий уровень репликации ВГВ, который детектировали опосредовано на основании уровней HBeAg, наблюдали только в группах мышей линии HBVtg, которые получали цикло-ди-АМФ посредством в/м или п/к/в/б пути введения, или поли-LCIC посредством в/м пути введения (Фиг. 31А). К сожалению, внутримышечная иммунизация с применением поли-LCIC была единственным исследованным протоколом, который привел к значительной потере массы тела у мышей линии HBVtg (Фиг. 31В). Цикло-ди-АМФ также можно рассматривать как более эффективный адъювант при индукции ответов HBcAg-специфичных (с93) и HBsAg-специфичных (s208) CD8+ Т-клеток в селезенке и особенно в печени иммунизированных мышей линии HBVtg, независимо от того, какой путь введения был использован (Фиг. 31С). Интересно отметить, что поли-LCIC привел к интенсивному внутрипеченочному ответу HBcAg-специфичных CD8+ Т-клеток при внутримышечной доставке, тогда как при доставке п/к или в/б путем происходила индукция ответов преимущественно HBsAg-специфичных (s208) CD8+ Т-клеток. Лиганд RJG-I был способен индуцировать специфичные к ВГВ гуморальные ответы, но не смог индуцировать первичные ВГВ-специфичные ответы CD8+ Т-клеток. Ответы MVA-специфичных CD8+ Т-клеток, используемых в качестве контролей, были сопоставимы во всех иммунизированных группах в селезенке и печени, что указывает на равную эффективность вакцинации.
[188]. Полученные данные свидетельствуют о том, что цикло-ди-АМФ является очень эффективным адъювантом, поли-LCIC демонстрирует промежуточную эффективность и лиганд RIG-I недостаточно эффективен для терапевтической первичной белковой вакцинации/стимулирующей вакцинации MVA. Цикло-ди-АМФ был одинаково эффективным при введении в/м, а также п/к/в/б путем.
[189]. Пример 12: Оценка новой конструкции MVA (MVA-HBVvac) у мышей линии C57BL/6.
[190]. Помимо этого оценивали иммуногенность недавно сконструированного полицистронного MVA, экспрессирующего HBsAg, HBcAg (последовательности, охватывающие основные генотипы А, В, С, D ВГВ) и домен RT полимеразы ВГВ (MVA-HBVvac), в условиях in vivo. Была создана схема двух полицистронных вакцинных конструкций: HBVVac, включающей ядерный белок и S ВГВ всех основных генотипов ВГВ, а также домен RT полимеразы ВГВ, и C/S (C/S), экспрессирующей ядерный белок и S ВГВ (Фиг. 32А). Экспрессию белка подтверждали методом Вестерн-блоттинга. На Фиг. 32В представлены результаты оценки экспрессии S различными рекомбинантными клонами MVA, экспрессирующими HBVVAc или S/C.
[191]. В группах мышей линии C57BL/6 (n=5) сначала проводили первичную вакцинацию с применением смеси частиц HBsAg и HBcAg, содержащей в качестве адъюванта цикло-ди-АМФ. Через две недели мышей подвергали стимулирующей вакцинации с применением смеси MVA-S и MVA-ядерный белок или равным количеством нового MVA-HBVvac. Мышей умерщвляли на 21 день для оценки ВГВ-специфичного гуморального и клеточного иммунного ответа (Фиг. 32С).
[192]. Новый полицистронный MVA вызывал значительные гуморальные ответы на HBs и НВс, сравнимые со смесью комбинации конструкций MVA-S и MVA-ядерный белок (Фиг. 32D). Помимо этого иммунизация MVA-HBVvac вызывала сильные HBsAg-специфичные (s190, s208 и Spool) и HBcAg-специфичные (с93, Cpool) ответы CD8+ Т-клеток (определяемые путем исследования спленоцитов), которые были сходны по величине с ответами, индуцированными смесью MVA-S и MVA-ядерный белок (Фиг. 32Е). Помимо этого иммунизация с применением MVA-HBVvac приводила к детектированию слабых ответов RT-специфичных CD8+ Т-клеток для пептидов RT61, RT333 и пула пептидов RT 2 (обозначенных стрелками), даже несмотря на то, что белок RT не использовали для первичной иммунизации.
[193]. Полученные данные свидетельствуют о том, что полицистронный MVA (MVA-HBVvac) экспрессировал все ожидаемые белки и показал превосходную иммуногенность у мышей линии C57BL/6 в условиях in vivo.
[194]. Пример 13: Увеличение иммуногенности конструкций MVA путем совместной экспрессии CD70
[195]. Для улучшения иммуногенности векторов для вакцинации на основе MVA в условиях in vivo конструировали вектор MVA, который экспрессирует CD70 бицистронным способом (Фиг. 34А).
[196]. В группах мышей линии C57BL/6 (n=6-7) проводили первичную вакцинацию с применением частиц HBcAg, содержащих в качестве адъюванта CpG и РСЕР. Через две недели у мышей проводили стимулирующую вакцинацию с применением MVA-ядерный белок или аналогичного количества MVA-ядерный белок-CD70, экспрессирующего CD70, или MVA дикого типа в качестве контроля (Фиг. 34В). Мышей умерщвляли на 35 день, чтобы оценить специфичные для ВГВ гуморальные и клеточные иммунные ответы. Несмотря на то, что гуморальные иммунные ответы были идентичны после стимулирующей вакцинации с применением MVA-ядерный белок и MVA-ядерный белок-CD70, CD8+ Т-клеточные ответы на MVA (B8R)-специфичный цитокин были незначительными, и были значительно увеличены в отношении ВГВ (С93)-специфичного цитокина у мышей, которые получили стимулирующую вакцинацию с применением MVA-ядерный белок-CD70 (Фиг. 34С). Повторный эксперимент дал идентичные результаты.
[197]. В третьем эксперименте вакцинировали группы ВГВ-трансгенных мышей, которые были выведены на основе ядра C57BL/6 (n=5-6). У этих животных иммунная толерантность может быть нарушена при терапевтической вакцинации. После однократной первичной вакцинации с применением частиц HBcAg, содержащих в качестве адъюванта CpG и РСЕР, у мышей проводили стимулирующую вакцинацию с применением MVA-ядерный белок или аналогичного количества MVA-ядерный белок-CD70, экспрессирующего CD70 (Фиг. 35А и В). Мышей, вакцинированных MVA дикого типа, использовали в качестве контроля. Мышей умерщвляли на 35 день для оценки MVA- и ВГВ-специфичных ответов Т-клеток. CD8+ Т-клетки, отсортированные из связанных с печенью лимфоцитов, имели более выраженную секрецию ИФН-γ и ИЛ-2 при повторной стимуляции с применением MVA- и ВГВ-специфичных пептидов, соответственно, когда мышей вакцинировали с применением MVA-ядерный белок-CD70 по сравнению с мышами, вакцинированными с применением MVA-ядерный белок. У мышей, стимулированных с применением MVAwt, детектировали MVA-специфичные, но не ВГВ-специфичные ответы Т-клеток (Фиг. 35С).
[198]. В отношении вышеприведенных результатов, можно сделать вывод, что совместная экспрессия CD70 с ВГВ-специфичным антигеном значительно увеличивала MVA- и ВГВ-специфичные ответы Т-клеток в условиях in vivo.
[199]. Настоящее изобретение, иллюстративно описанное в настоящем документе, может быть реализовано подходящим способом в отсутствие какого-либо элемента или элементов, ограничения или ограничений, конкретно не раскрытых в настоящем документе. Следовательно, например, термины «содержащий», «включая», «заключающий» и т.д. следует толковать расширено и без ограничений. Помимо этого используемые в настоящем документе термины и выражения использовали как описательные термины, а не ограничивающие, и использование указанных терминов и выражений не предназначено для исключения любых эквивалентов представленных и описанных признаков или их частей, однако следует понимать, что возможны различные модификации в объеме заявленного изобретения. Соответственно, следует понимать, что, несмотря на то, что настоящее изобретение было конкретно раскрыто с помощью примерных вариантов реализации и дополнительных признаков, модификации и изменения объектов согласно настоящему изобретению, предусмотренных в настоящем документе, могут быть применены специалистами в данной области техники и что такие модификации и изменения находятся в пределах объема настоящего изобретения.
[200]. Настоящее изобретение было описано в настоящем документе в общих чертах и в целом. Каждый из более узких видов и субродовых группировок, входящих в общее описание, также является частью настоящего изобретения. Это включает в себя общее описание настоящего изобретения с оговоркой или отрицательным ограничением, удаляющим какой-либо объект из рода, независимо от конкретного упоминания удаленного материала в настоящем документе.
[201]. Другие варианты реализации настоящего изобретения охватываются формулой настоящего изобретения. Помимо этого в тех случаях, когда признаки или аспекты настоящего изобретения описаны в терминах групп Маркуша, специалисты в данной области техники поймут, что настоящее изобретение также описано тем самым в терминах любого отдельного члена или подгруппы членов группы Маркуша.
[202]. Содержание всех документов и патентных документов, цитируемых в настоящем документе, полностью включено посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В (ВАРИАНТЫ) | 2015 |
|
RU2603729C2 |
| РЕКОМБИНАНТНАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В (ВАРИАНТЫ) | 2003 |
|
RU2238105C1 |
| Способ оценки уровня антител, специфичных к различным вариантам HBsAg вируса гепатита В | 2016 |
|
RU2616236C1 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ КОКЛЮША, ДИФТЕРИИ, СТОЛБНЯКА И ВИРУСНОГО ГЕПАТИТА В И Д | 2003 |
|
RU2233673C1 |
| ПОЛИЭПИТОПНАЯ ВАКЦИНА 4-ГО ПОКОЛЕНИЯ ПРОТИВ ГЕПАТИТА В И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2011 |
|
RU2469741C1 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ИММУНОПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В И Д, СТОЛБНЯКА И ДИФТЕРИИ | 2003 |
|
RU2233672C1 |
| Мутантные полимеразы вируса гепатита В | 2012 |
|
RU2625021C2 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ Hansenula polymorpha - ПРОДУЦЕНТ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В СЕРОТИПА "ayw" | 2015 |
|
RU2586511C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК РНВS, ОБЕСПЕЧИВАЮЩАЯ БИОСИНТЕЗ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В, СПОСОБ КОНСТРУИРОВАНИЯ ПЛАЗМИДЫ, ШТАММ ДРОЖЖЕЙ PICHIA PASTORIS PS103 (PHBS) - ПРОДУЦЕНТ УКАЗАННОГО АНТИГЕНА | 2000 |
|
RU2201452C2 |
| РЕКОМБИНАНТНЫЙ ШТАММ ДРОЖЖЕЙ Hansenula polymorpha - ПРОДУЦЕНТ МУТАНТНОГО ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА В (ВАРИАНТЫ) | 2015 |
|
RU2586513C1 |

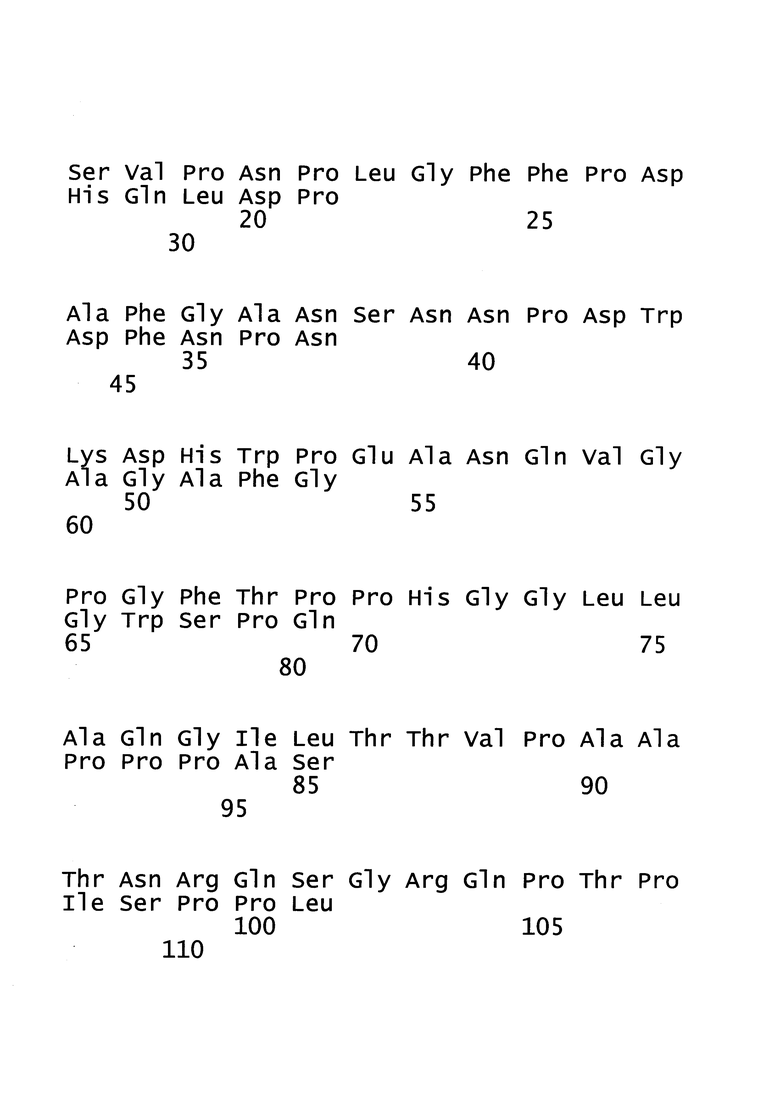






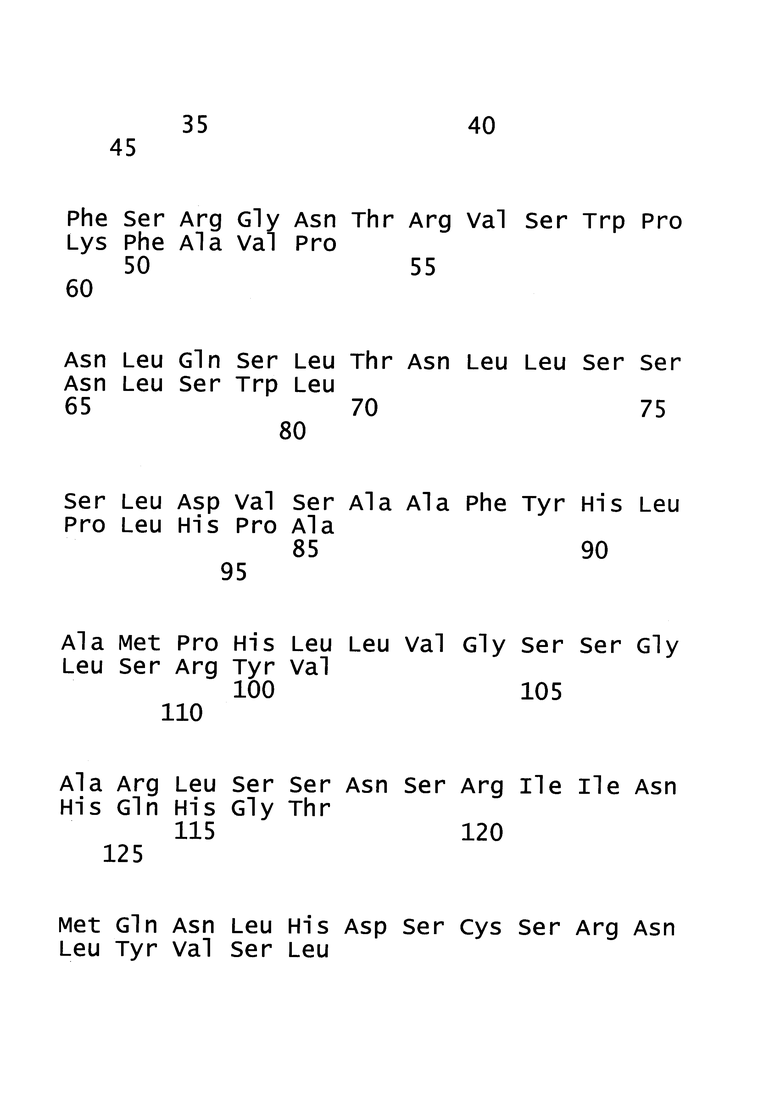



















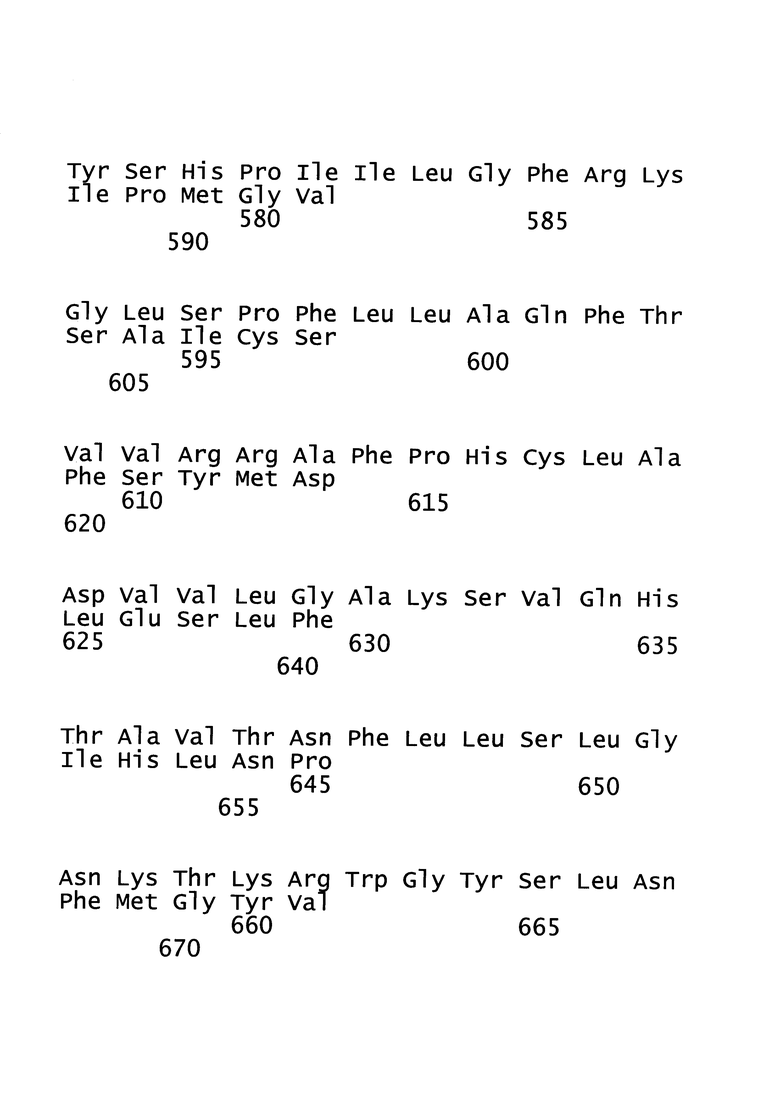








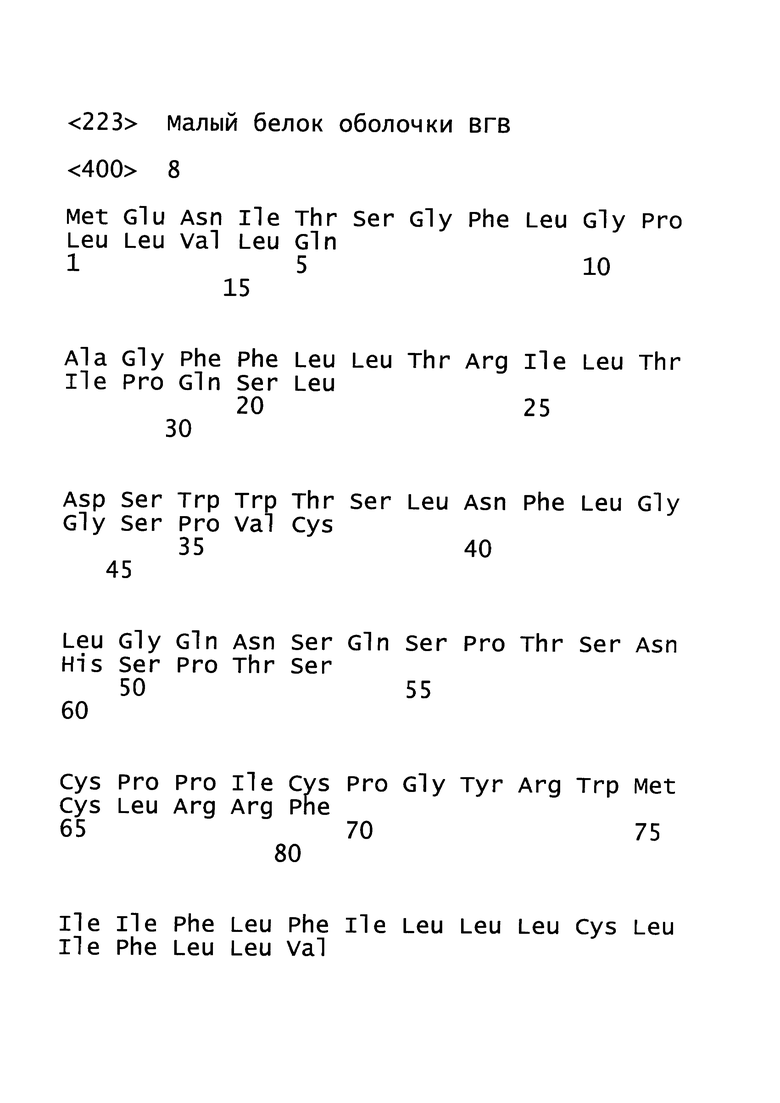










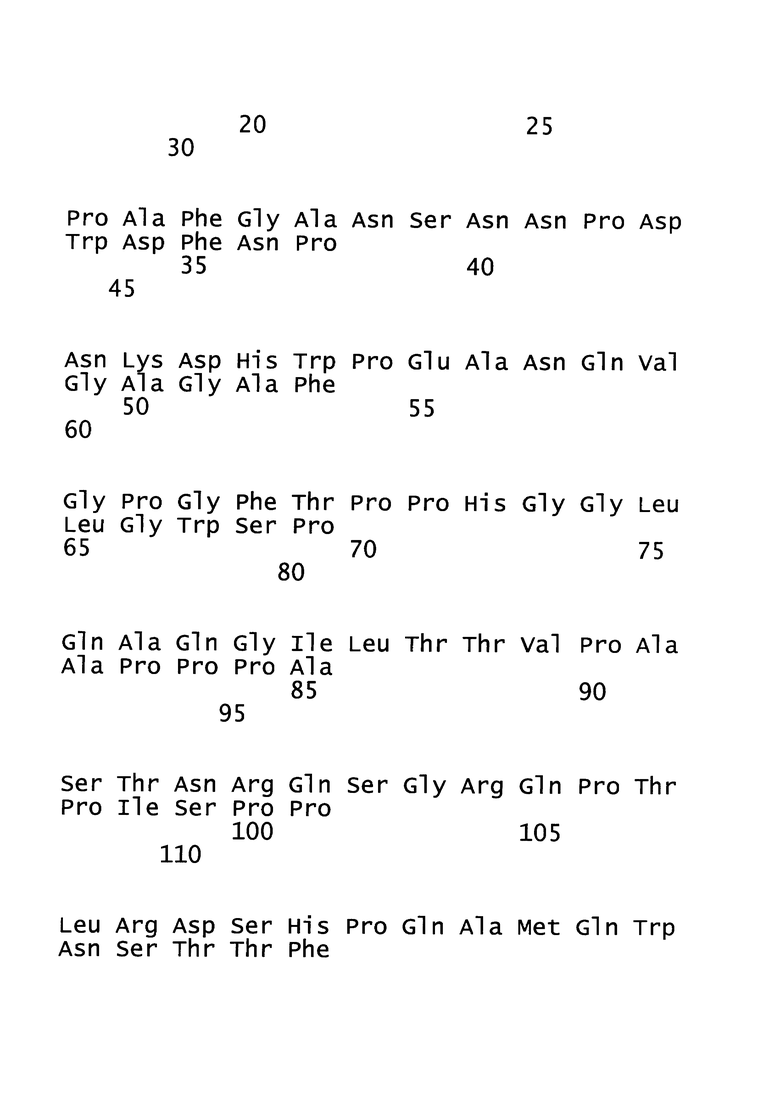


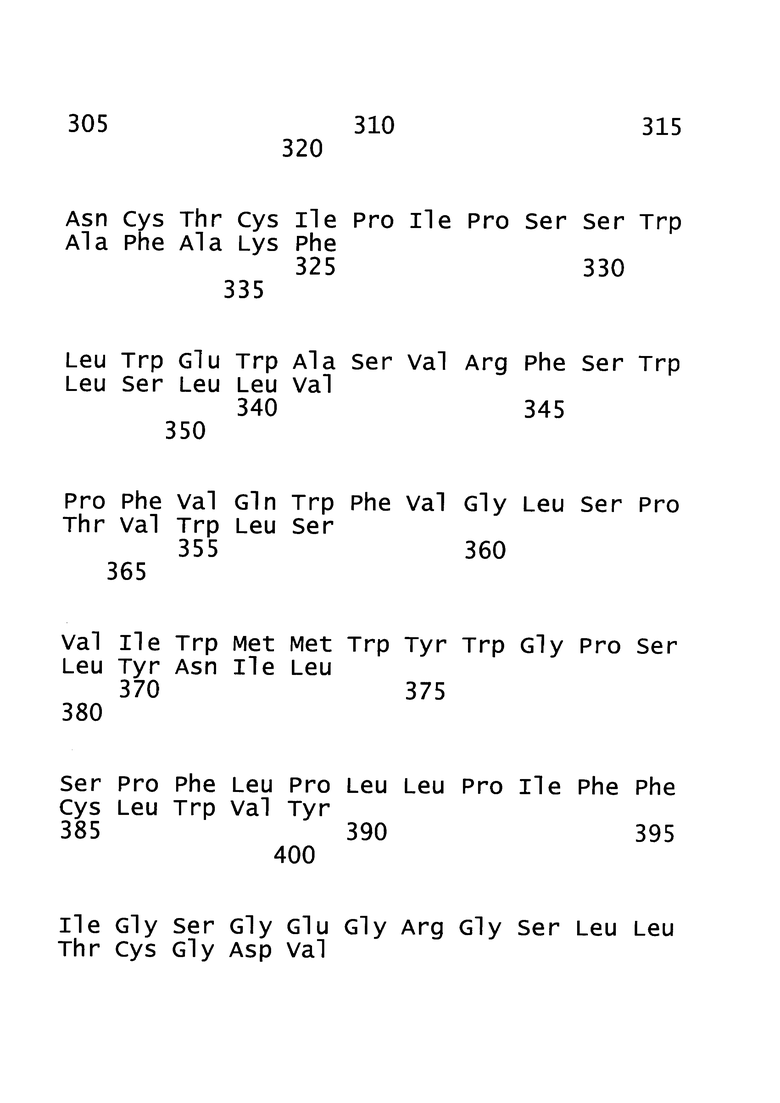

























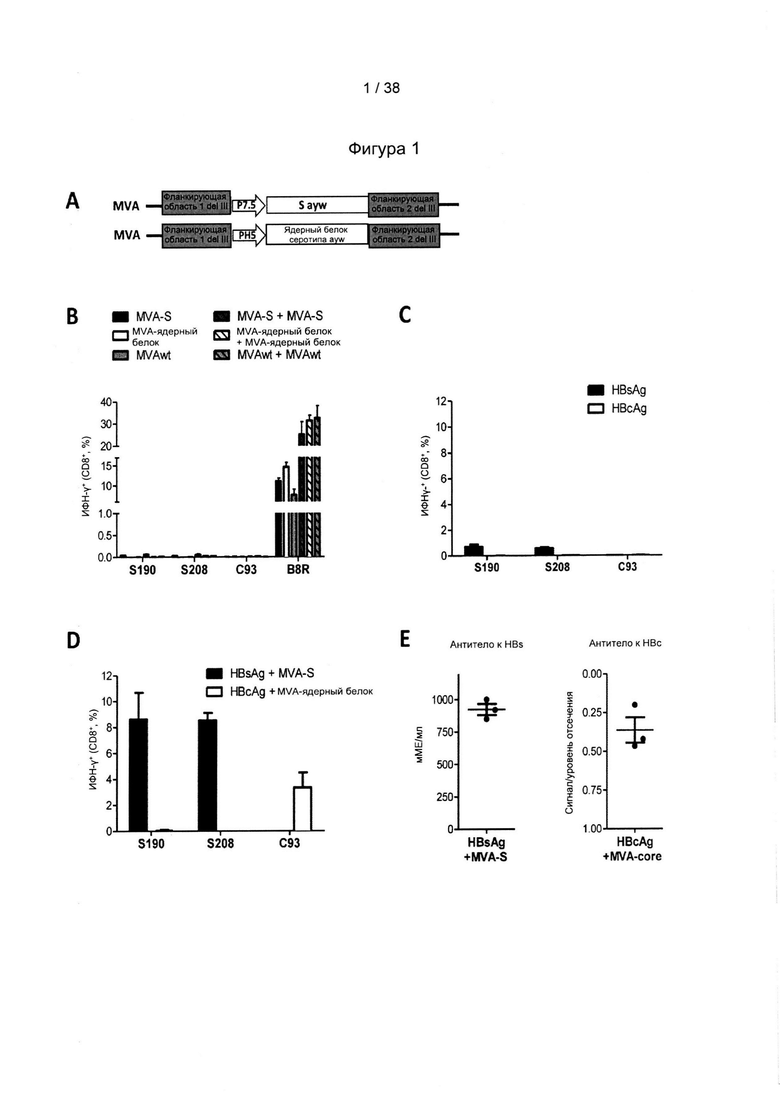
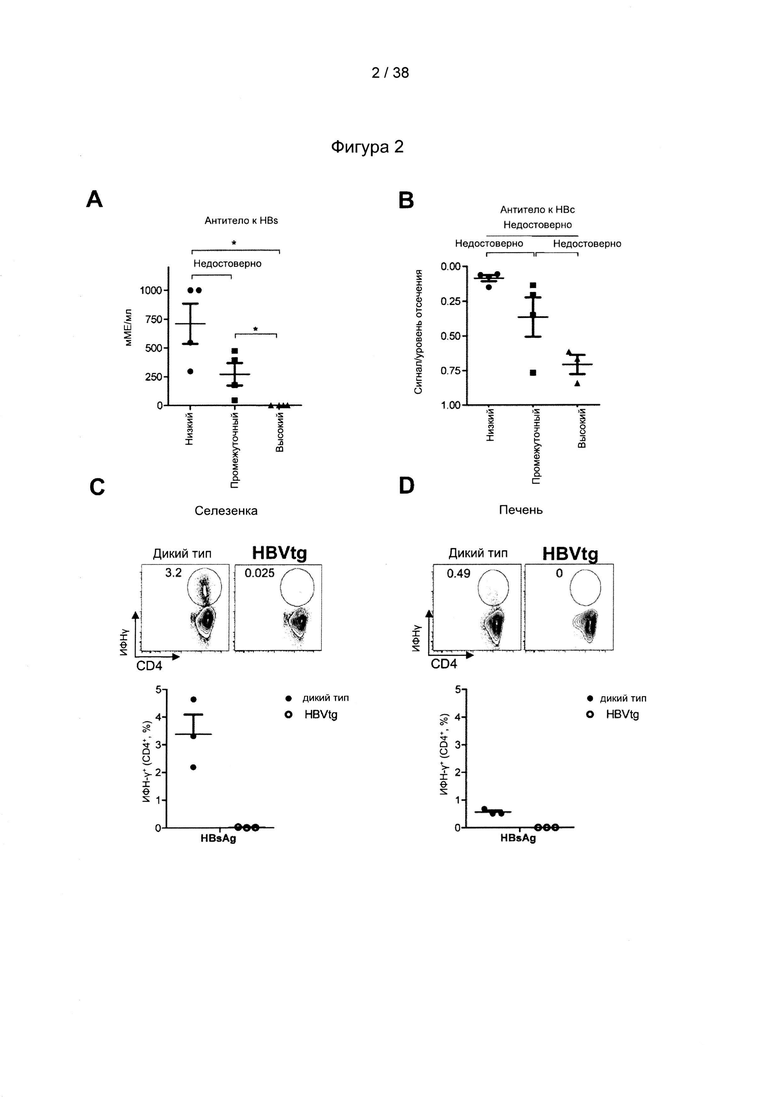
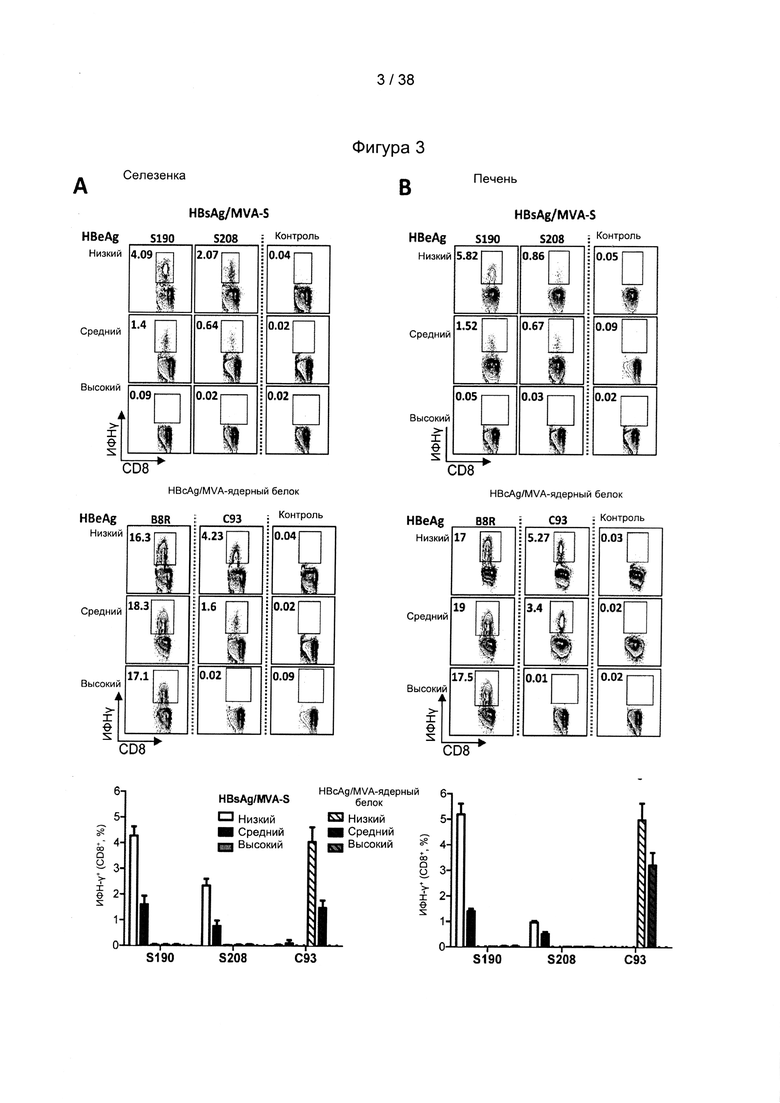
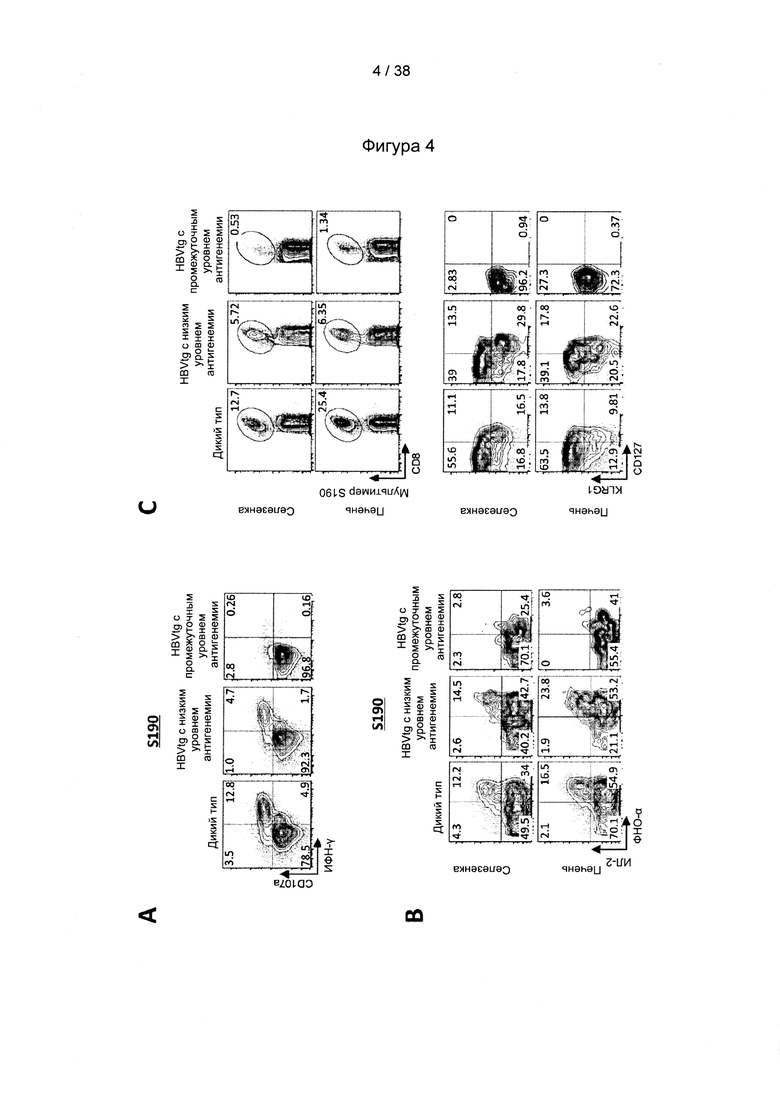
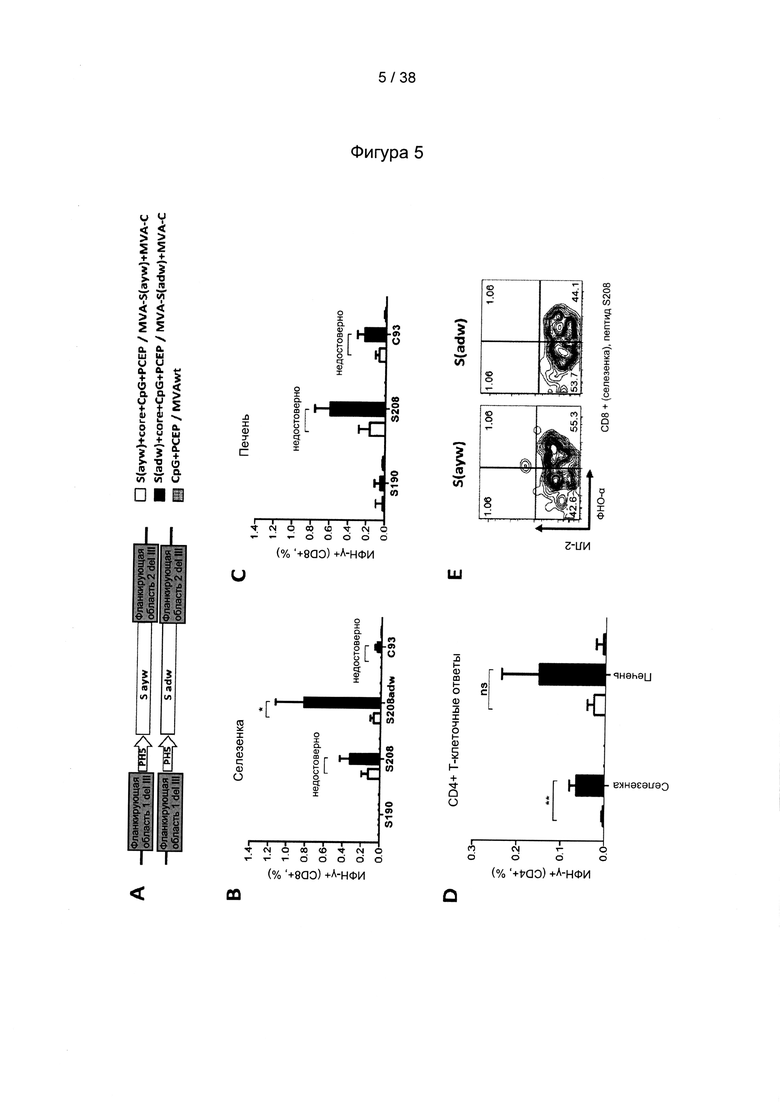
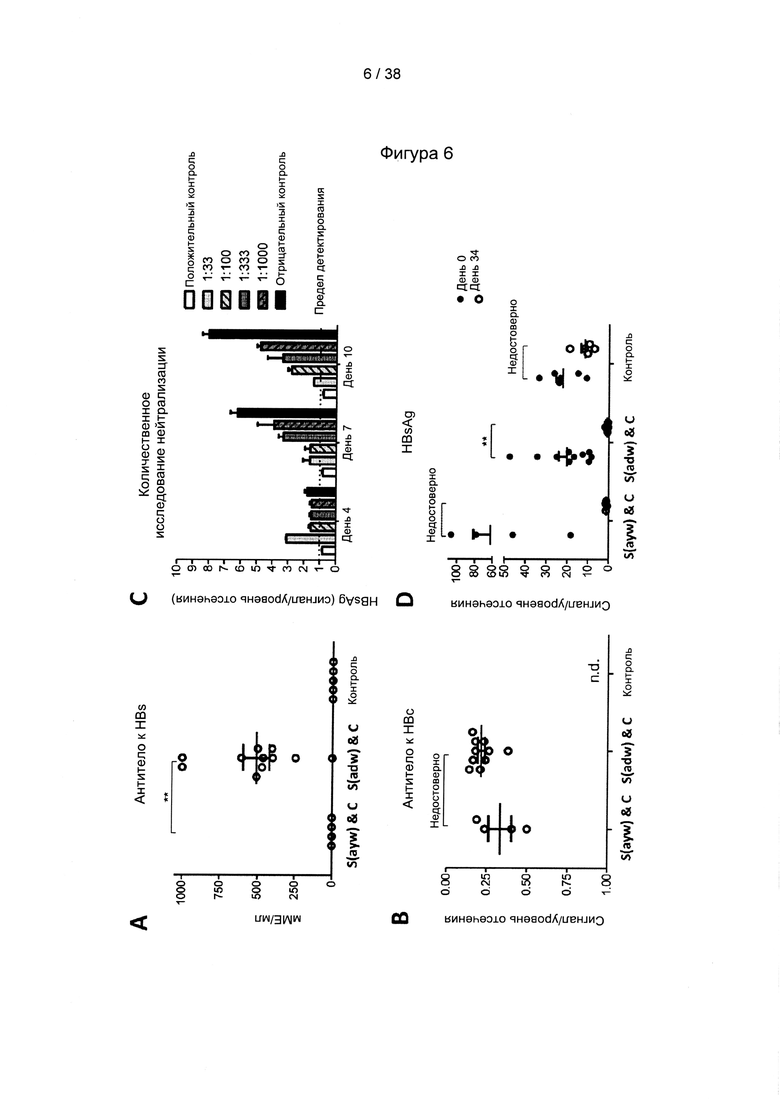
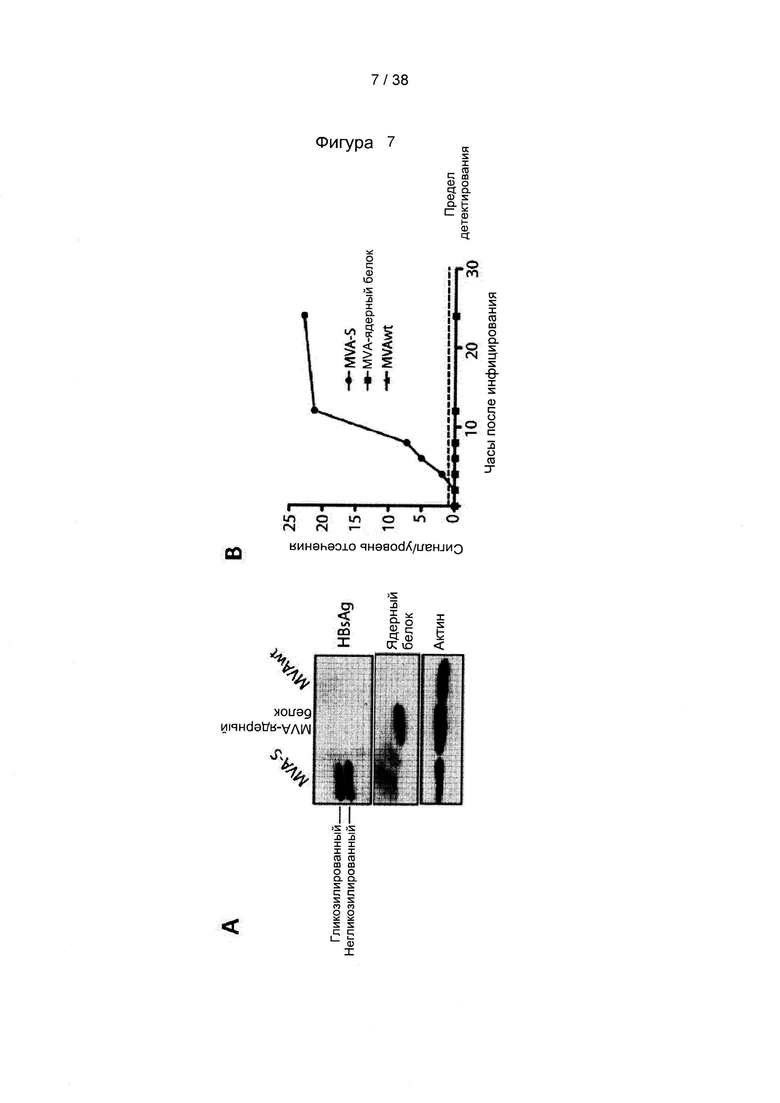
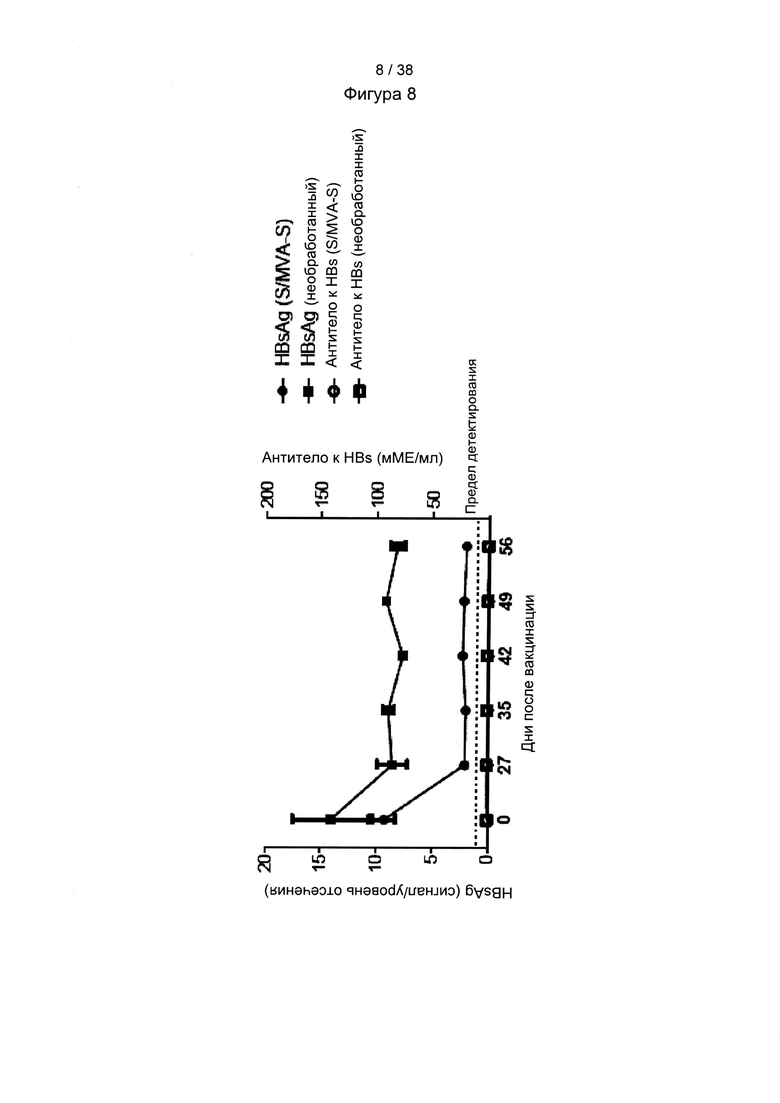
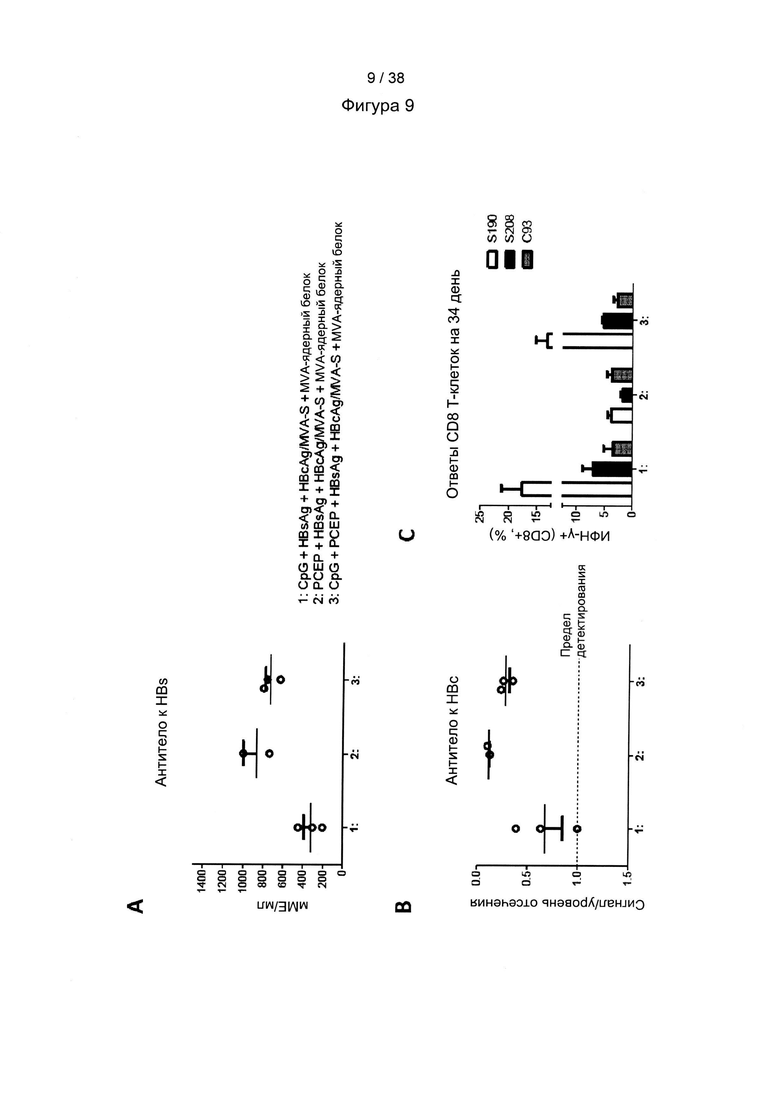
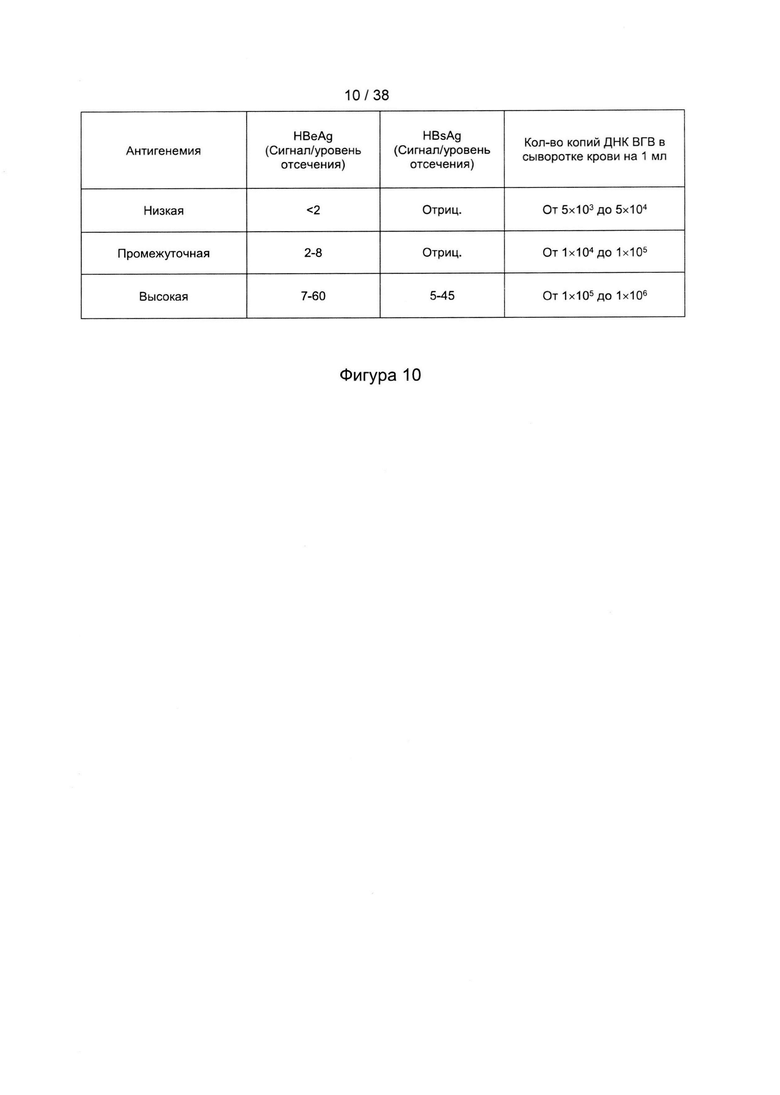
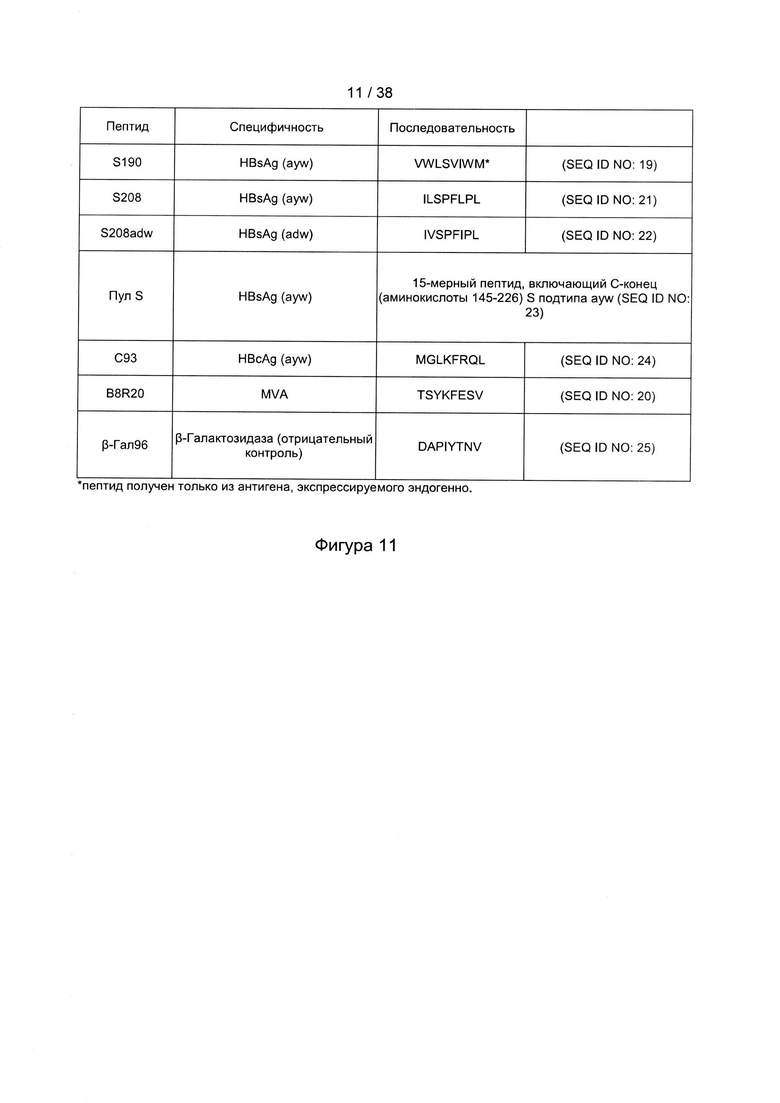
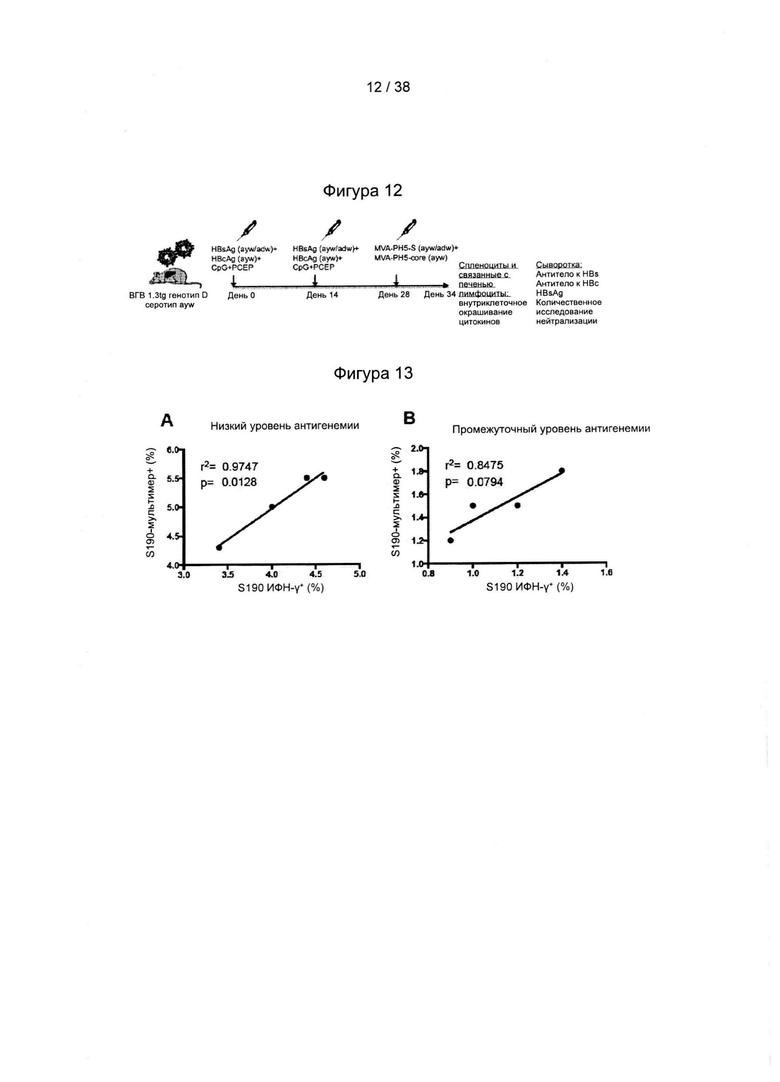
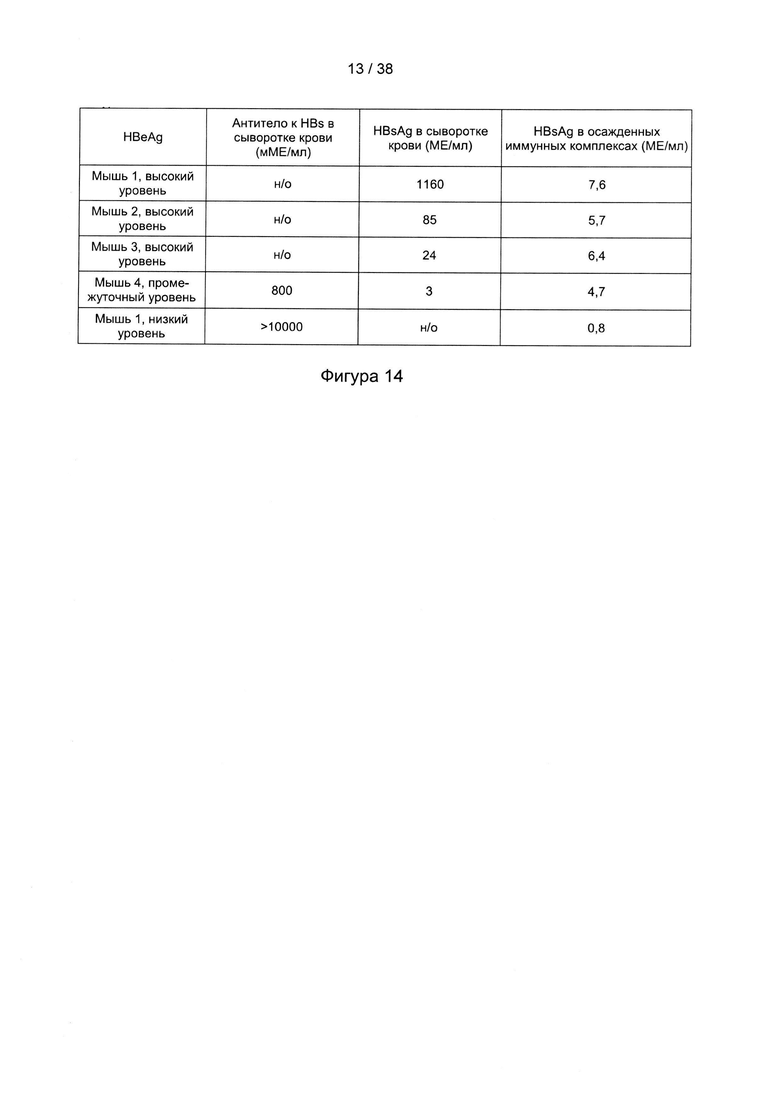
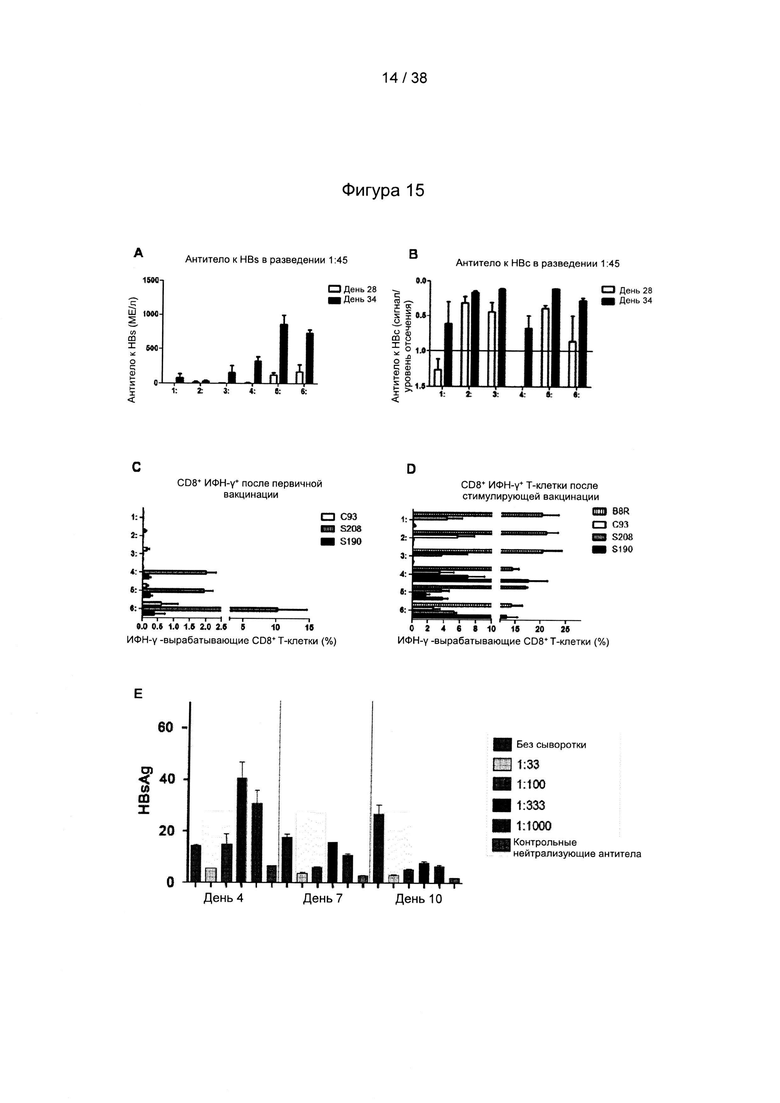
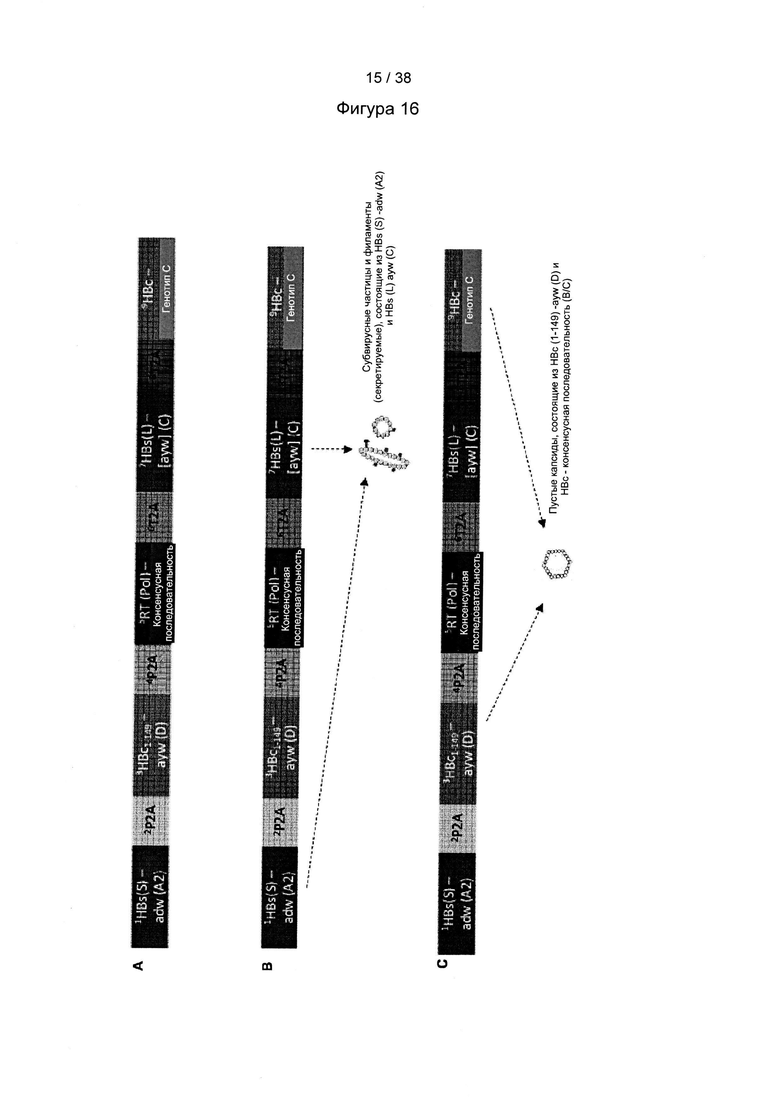





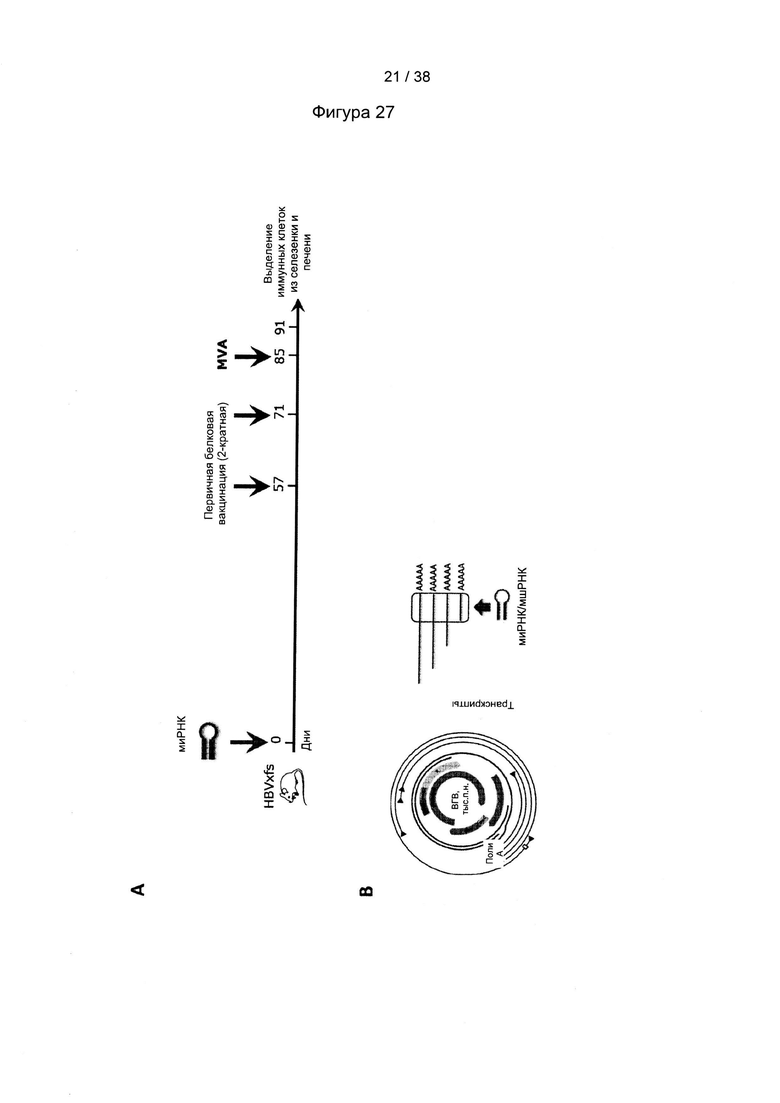

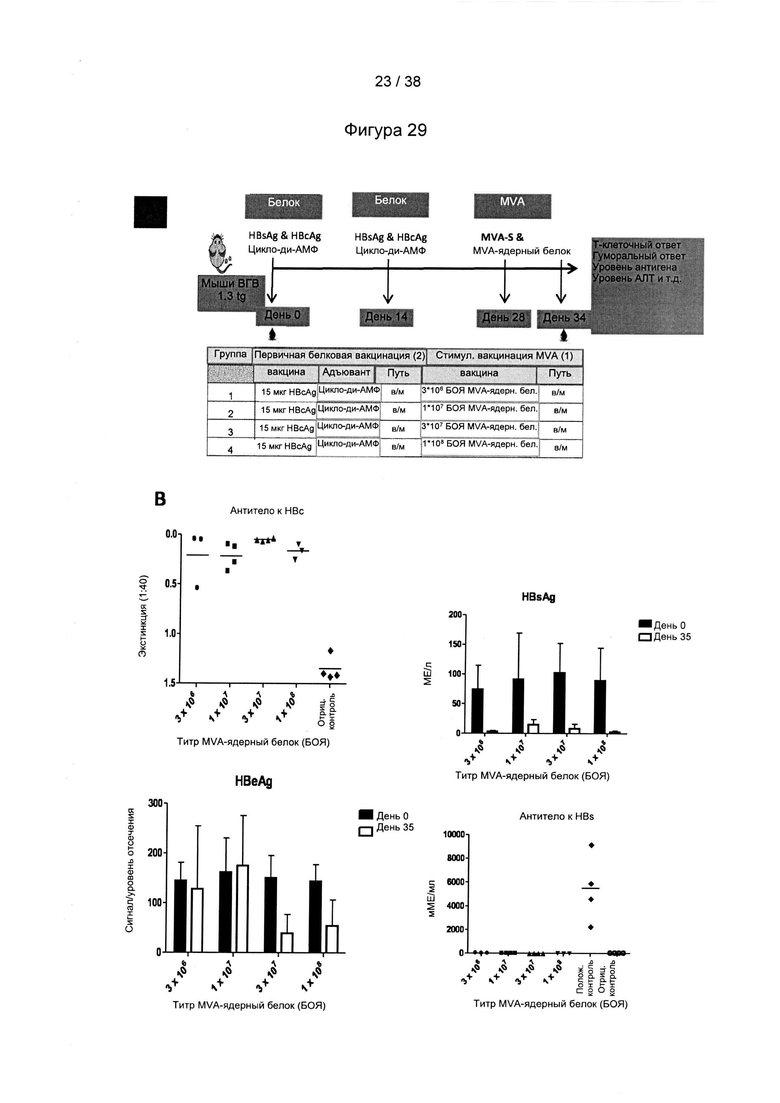
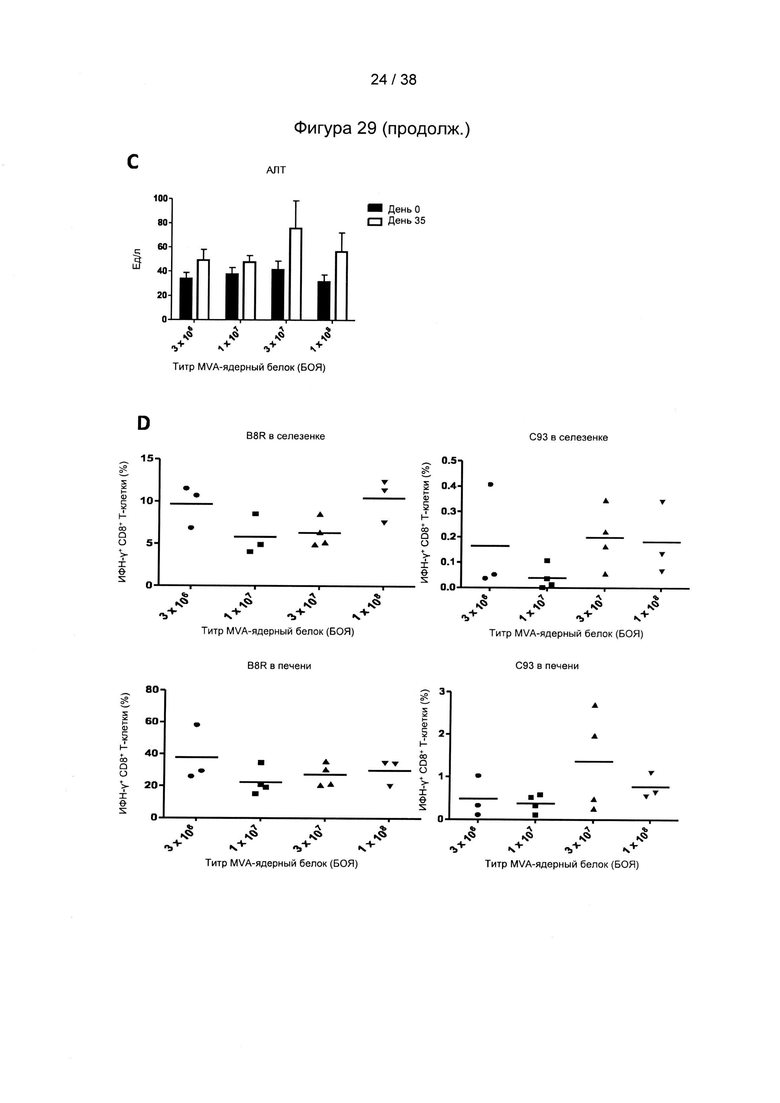
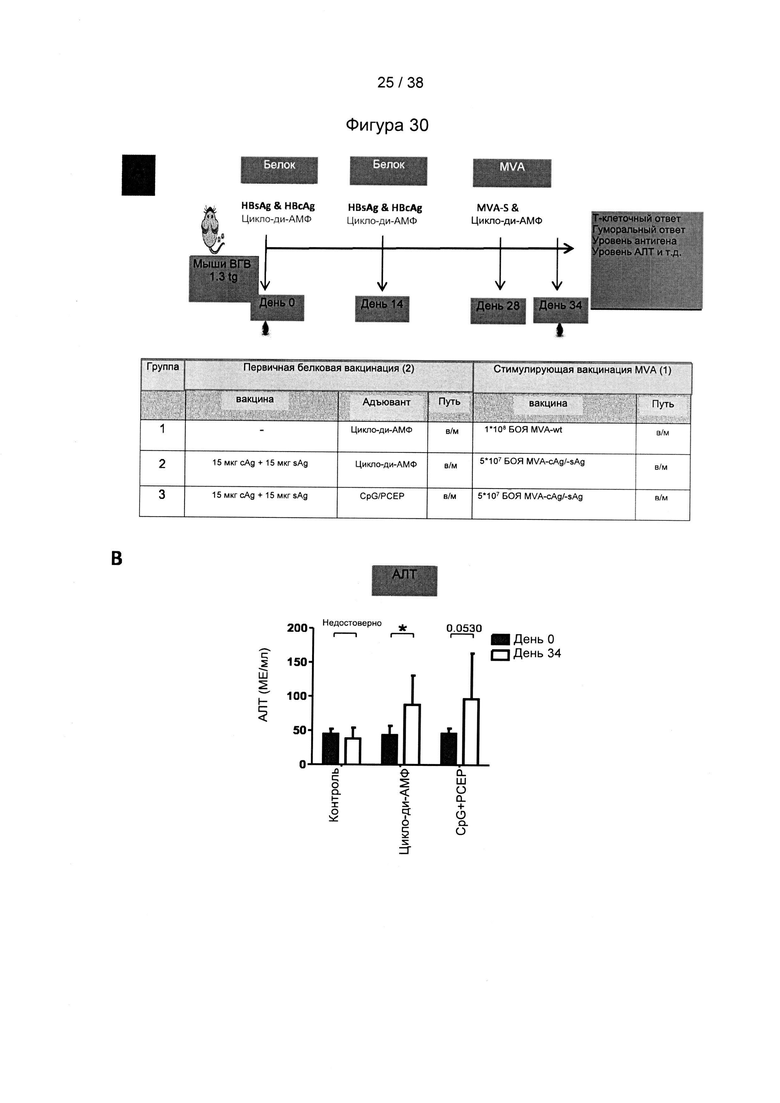
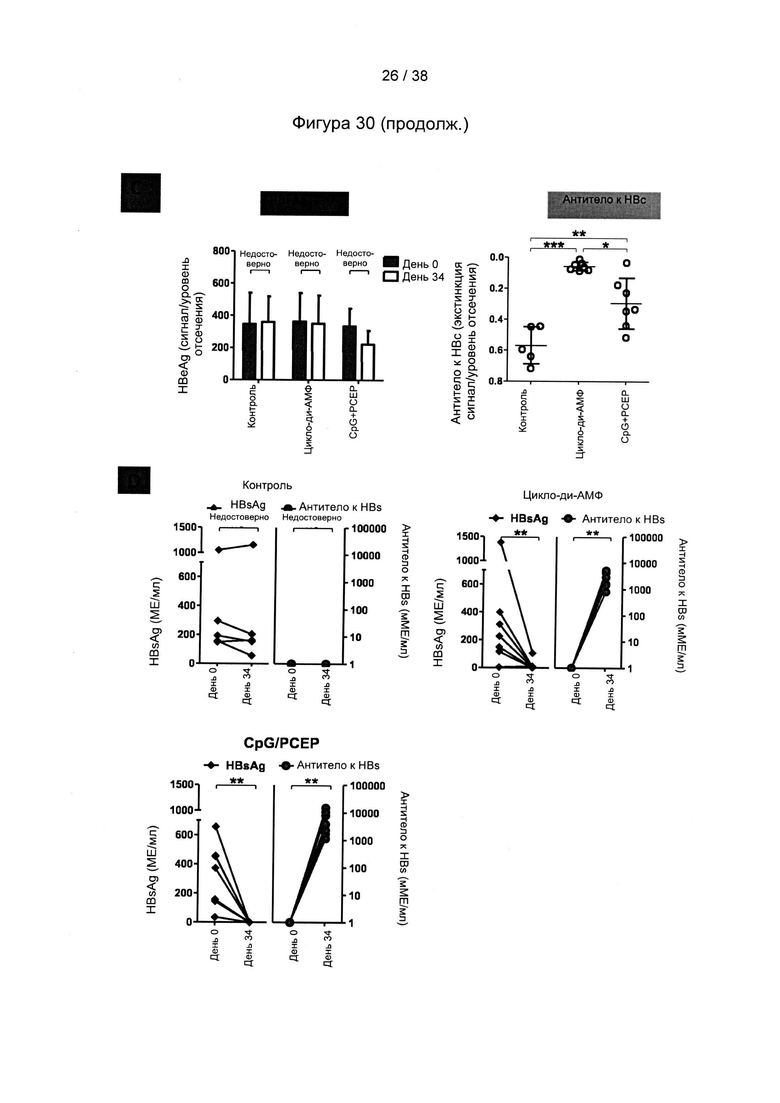
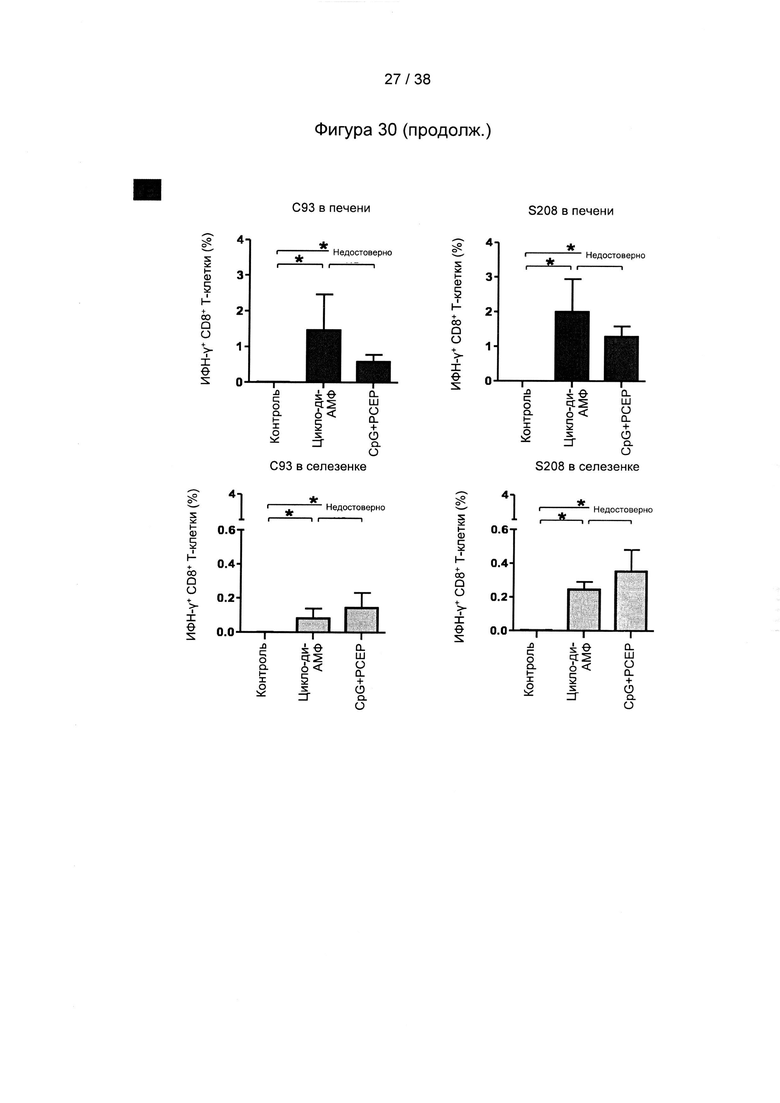
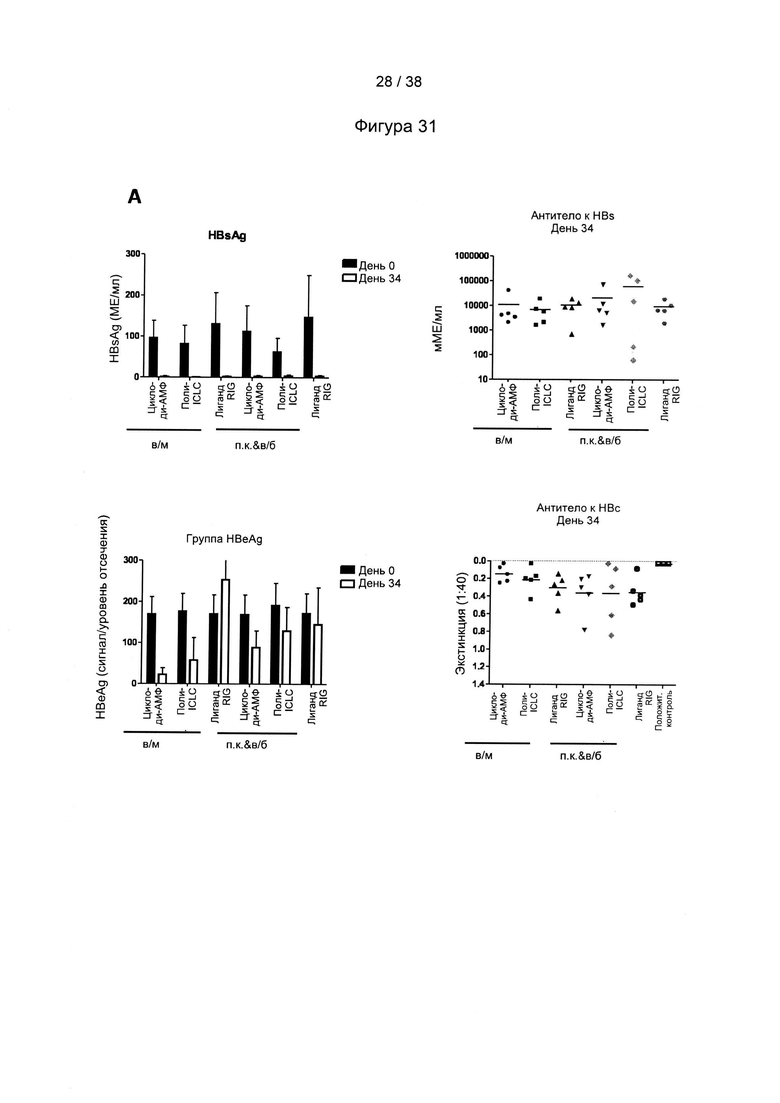
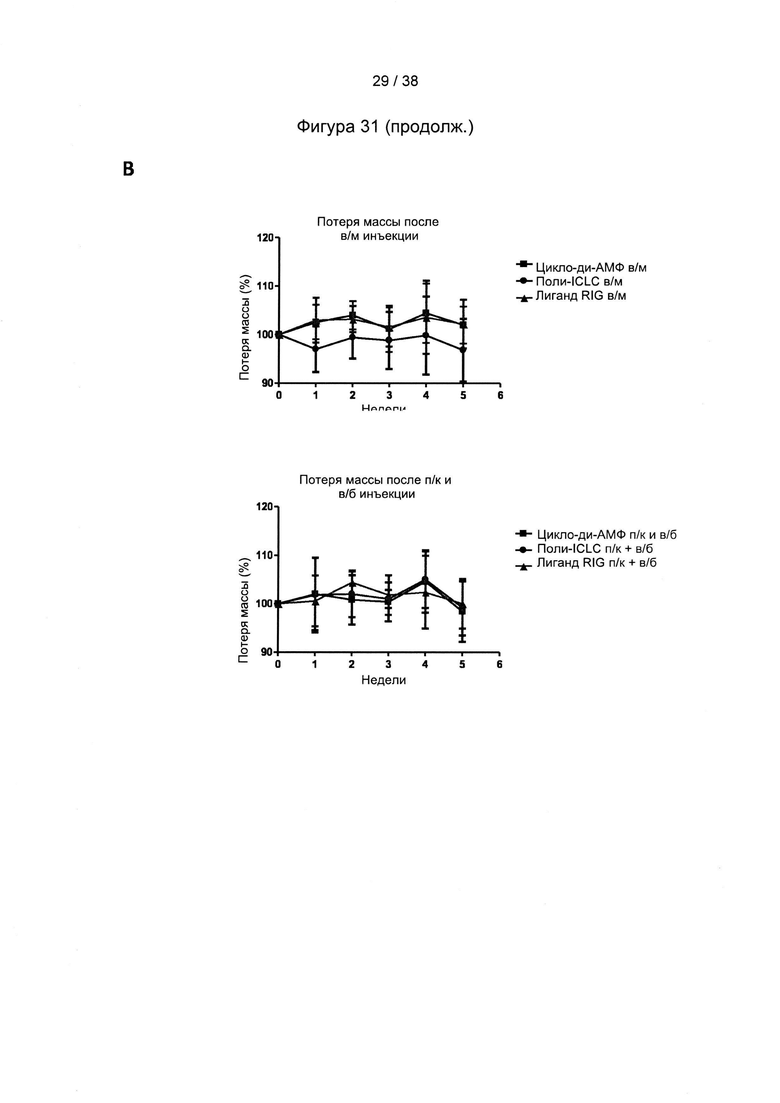
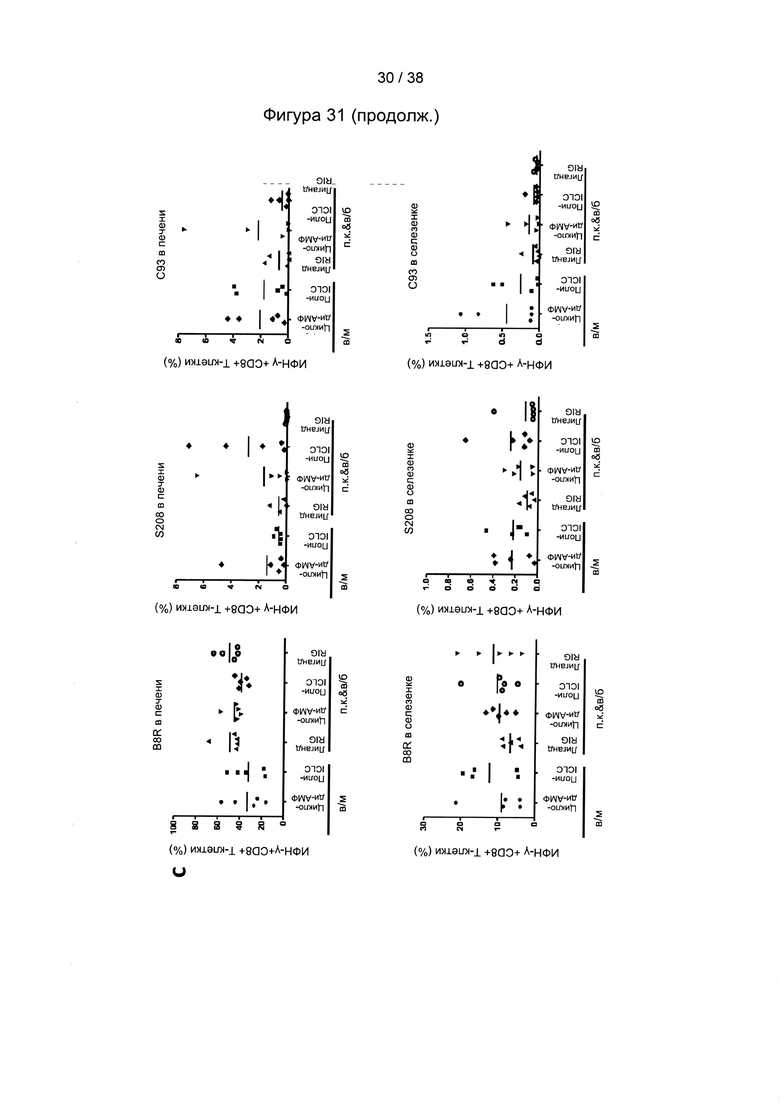
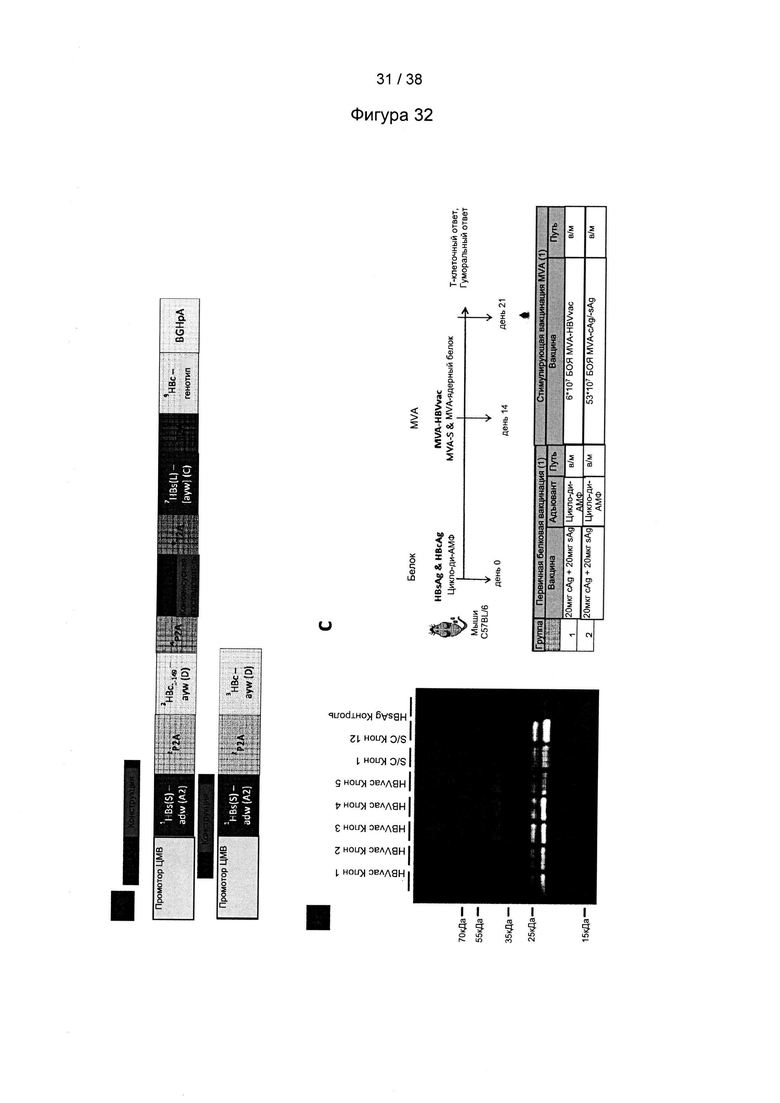
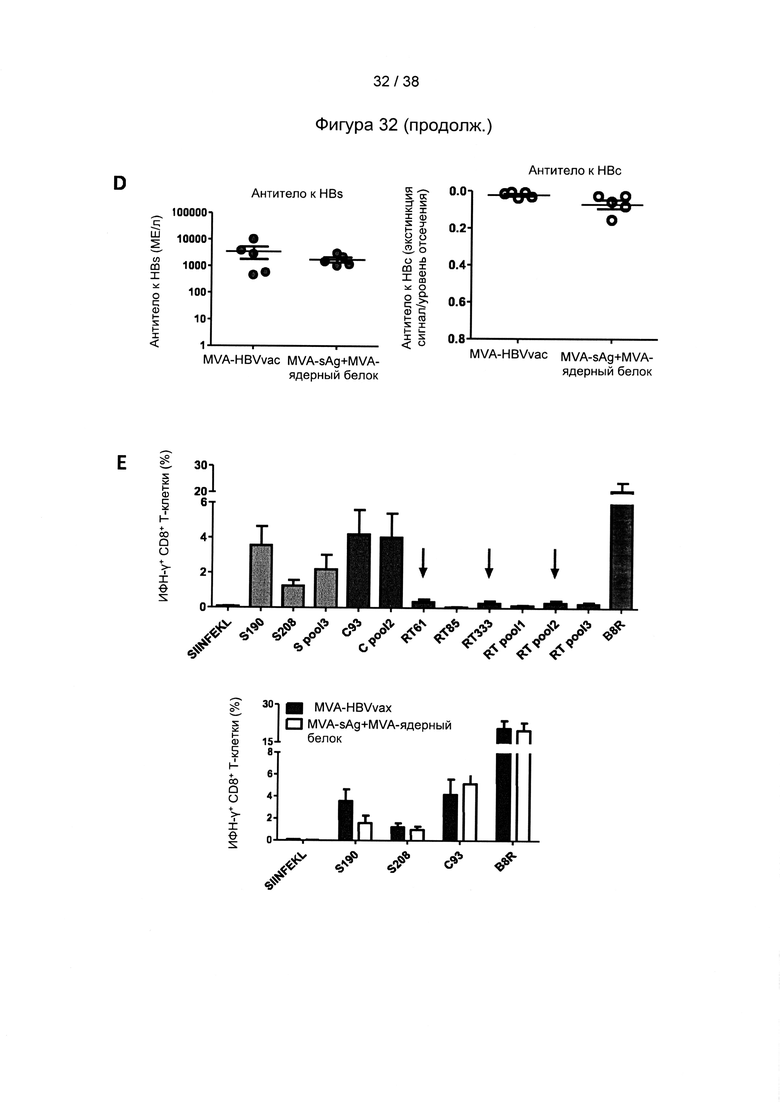


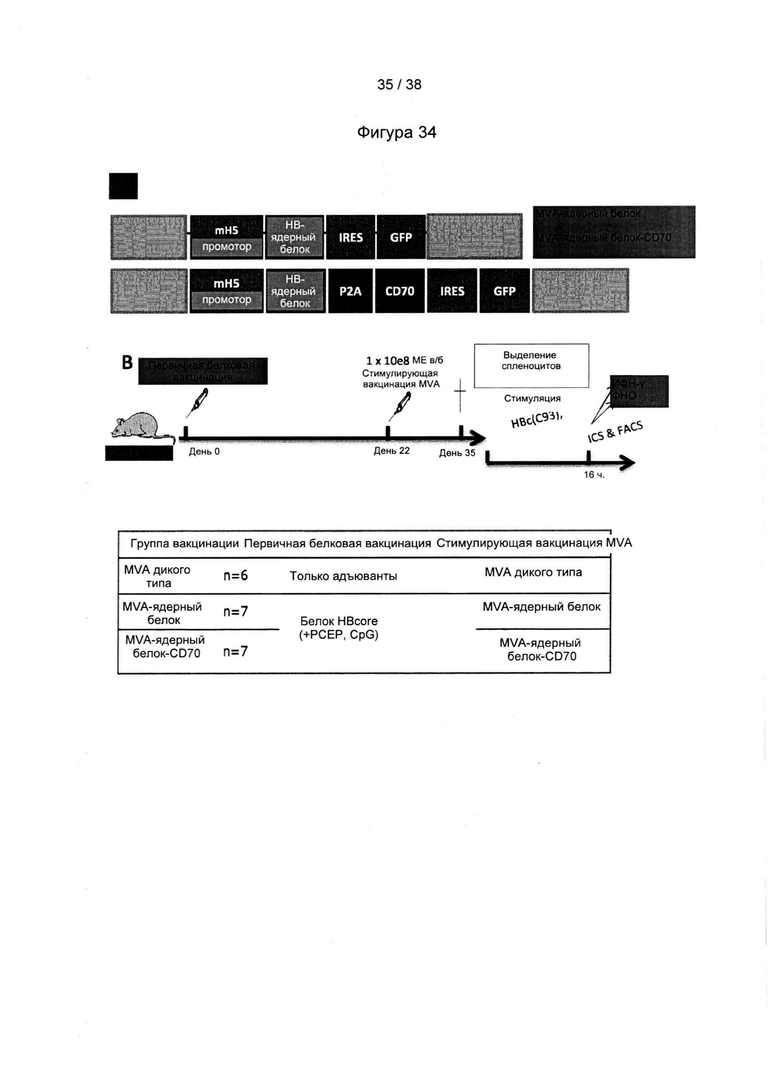
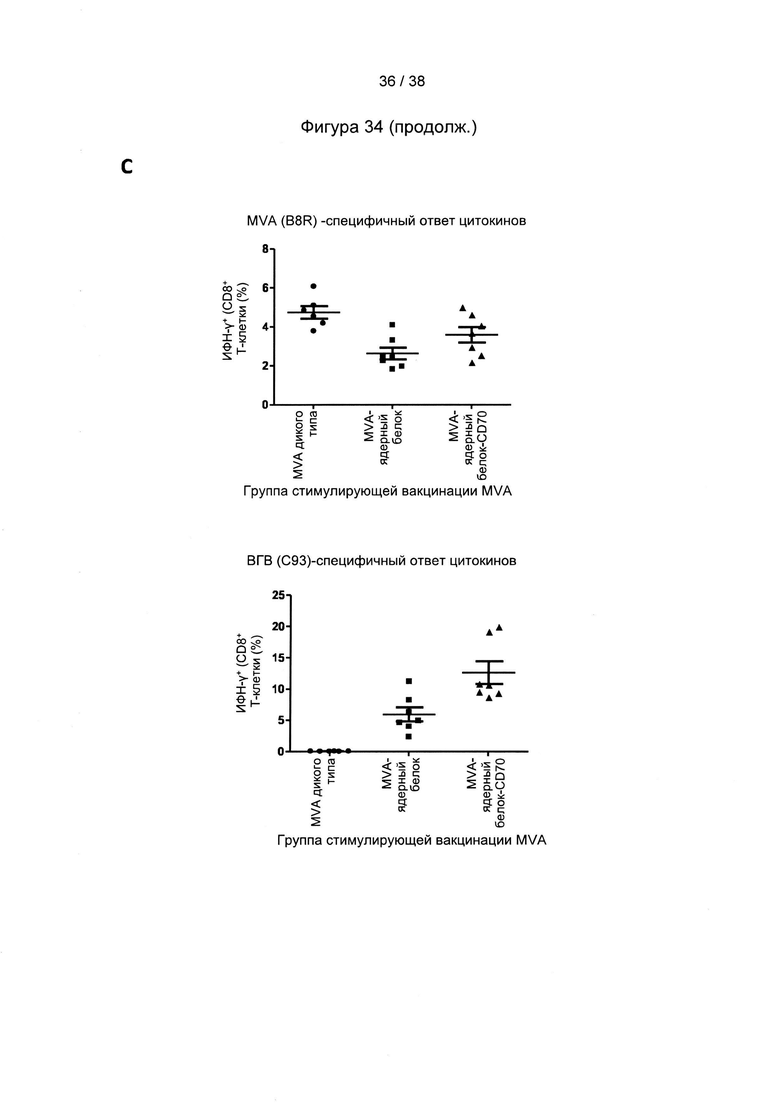
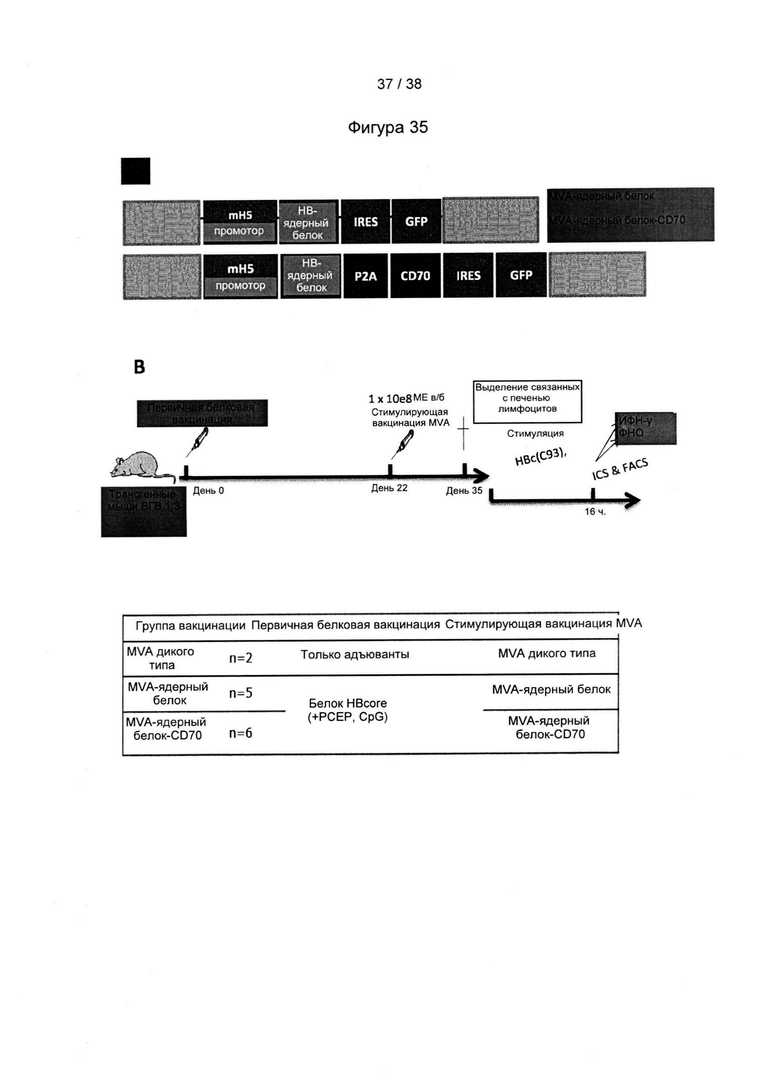

Изобретение относится к биотехнологии. Описан рекомбинантный вектор для вакцинации против вируса гепатита B, экспрессирующий: белок оболочки (антиген HBs) из серотипа adw вируса гепатита B (ВГВ), причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, при этом указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и ядерный белок (антиген НВс) из серотипа ayw вируса гепатита B, причем указанный ядерный белок содержит или состоит из аминокислот 1-149 антигена HBc, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B; и по меньшей мере одно из следующих: иммуногенный белок оболочки (антиген HBs) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1; и/или иммуногенный ядерный белок (антиген НВс) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2; и/или иммуногенный домен RT полимеразы из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3. Изобретение расширяет арсенал средств для лечения гепатита В. 7 н. и 33 з.п. ф-лы, 13 пр., 35 ил.
1. Рекомбинантный вектор для вакцинации против вируса гепатита B, экспрессирующий:
(a) белок оболочки (антиген HBs) из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, при этом указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и
(b) ядерный белок (антиген НВс) из серотипа ayw вируса гепатита B, причем указанный ядерный белок содержит или состоит из аминокислот 1-149 антигена HBc, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B;
и по меньшей мере одно из следующих:
(c) иммуногенный белок оболочки (антиген HBs) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1; и/или
(d) иммуногенный ядерный белок (антиген НВс) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2; и/или
(e) иммуногенный домен RT полимеразы из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3.
2. Рекомбинантный вектор для вакцинации по п. 1, отличающийся тем, что указанный антиген HBs согласно (с) и/или антиген НВс согласно (d) является/являются антигеном (антигенами) генотипа C вируса гепатита B.
3. Рекомбинантный вектор для вакцинации по п. 1 или 2, отличающийся тем, что последовательность указанного иммуногенного антигена HBs согласно (с) по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 4, и/или последовательность указанного иммуногенного антигена НВс согласно (d) по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 5, и/или последовательность указанного иммуногенного домена RT полимеразы согласно (е) по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 6.
4. Рекомбинантный вектор для вакцинации по любому из предшествующих пунктов, отличающийся тем, что указанный ядерный белок из серотипа ayw вируса гепатита B согласно (b) представляет собой усеченный с C-конца ядерный белок, содержащий или состоящий из аминокислот 1-149 антигена НВс из генотипа D серотипа ayw вируса гепатита B.
5. Рекомбинантный вектор для вакцинации по любому из предшествующих пунктов, дополнительно экспрессирующий
(f) CD70.
6. Рекомбинантный вектор для вакцинации по п. 5, отличающийся тем, что указанный CD70 представляет собой CD70 человека.
7. Рекомбинантный вектор для вакцинации по п. 5 или 6, отличающийся тем, что последовательность указанного CD70 по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 26.
8. Рекомбинантный вектор для вакцинации по любому из предшествующих пунктов, отличающийся тем, что указанный рекомбинантный вектор для вакцинации представляет собой вирус, вирусоподобную частицу или бактерию.
9. Рекомбинантный вектор для вакцинации по любому из предшествующих пунктов, отличающийся тем, что указанный рекомбинантный вектор для вакцинации представляет собой модифицированный вирус осповакцины Ankara (вирус MVA).
10. Рекомбинантный вектор для вакцинации по любому из пп. 1-6, отличающийся тем, что указанный рекомбинантный вектор представляет собой ослабленный штамм Salmonella, вектор на основе цитомегаловируса (ЦМВ), вируса везикулярного стоматита (ВВС), аденовирусный вектор или вектор на основе вируса кори.
11. Рекомбинантный вектор для вакцинации по п. 1, причем указанный рекомбинантный вектор для вакцинации представляет собой вирус MVA, отличающийся тем, что по меньшей мере одна, предпочтительно по меньшей мере две, предпочтительно по меньшей мере три, предпочтительно по меньшей мере четыре, предпочтительно пять последовательностей нуклеиновых кислот, кодирующих (a), (b), (c), (d) и/или (е), включены в одну кассету экспрессии.
12. Рекомбинантный вектор для вакцинации по п. 11, отличающийся тем, что по меньшей мере одна из нуклеиновых кислот, кодирующих (a), (b), (c), (d) и/или (е), находится под контролем поксвирусного промотора, причем указанный поксвирусный промотор предпочтительно представляет собой P7.5 или PH5.
13. Рекомбинантный вектор для вакцинации по п. 11, отличающийся тем, что указанная кассета экспрессии кодирует аминокислотную последовательность, представленную в SEQ ID NO: 7.
14. Рекомбинантный вектор для вакцинации по п. 1, причем указанный рекомбинантный вектор для вакцинации представляет собой вирус MVA, и при этом последовательность нуклеиновой кислоты, кодирующая по меньшей мере один из (а), (b), (c), (d) и/или (е), вставлена в сайт делеции I (del I), сайт делеции II (del II), сайт делеции III (del III), сайт делеции IV (del IV), сайт делеции V (del V) или сайт делеции VI (del VI), предпочтительно сайт делеции III (del III) генома MVA.
15. Применение рекомбинантного вектора для вакцинации по п. 1 в терапии или вакцинации против гепатита B.
16. Применение по п. 15, отличающееся тем, что указанное применение заключается в способе вакцинации против гепатита B, причем указанное применение включает:
(i) введение субъекту
(a') белка оболочки из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, при этом указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и/или
(b') ядерного белка (антиген HBc) из серотипа ayw вируса гепатита B, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B; и
(ii) введение указанному субъекту указанного рекомбинантного вектора для вакцинации.
17. Способ вакцинации против гепатита B, причем указанный способ включает:
(i) введение субъекту
(a') белка оболочки из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, причем указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и/или
(b') ядерного белка (антиген HBc) из серотипа ayw вируса гепатита B, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B; и
(ii) введение указанному субъекту рекомбинантного вектора для вакцинации по любому из пп.1-14, причем указанный рекомбинантный вектор для вакцинации представляет собой вирус MVA.
18. Способ по п. 17, отличающийся тем, что указанный рекомбинантный вектор для вакцинации дополнительно экспрессирует CD70.
19. Способ по п. 17, отличающийся тем, что указанный способ вакцинации представляет собой способ терапевтической вакцинации.
20. Способ по п. 17, отличающийся тем, что этап (i) способа вакцинации представляет собой этап первичной вакцинации, и этап (ii) способа вакцинации представляет собой этап стимулирующей вакцинации.
21. Способ по п. 17, отличающийся тем, что указанный белок оболочки и/или ядерный белок в (i) вводят совместно с по меньшей мере одним адъювантом, причем указанный адъювант предпочтительно выбран из группы, состоящей из поли-ди(натрийкарбоксилатэтилфенокси)фосфазена (PCEP), иммуностимулирующего олигонуклеотида, агониста Toll-подобного рецептора (TLR), сапонина или их комбинаций, при этом указанный агонист TLR предпочтительно представляет собой агонист TLR3, агонист TLR4, агонист TLR7, агонист TLR8 или агонист TLR9, и при этом указанный иммуностимулирующий олигонуклеотид предпочтительно представляет собой поли-I/C, CpG, лиганд RIG-I, лиганд STING, циклический ди-АМФ, циклический ди-ЦМФ, циклический ди-ГМФ, агонист TLR7, агонист TLR8, CTA1DD или dmLT.
22. Способ по п. 21, отличающийся тем, что указанный адъювант представляет собой PCEP и/или адъювант CpG.
23. Способ по п. 21, отличающийся тем, что указанный адъювант представляет собой циклический ди-АМФ.
24. Способ по п. 17, отличающийся тем, что этап (i) проводят за по меньшей мере приблизительно 1 день до проведения этапа (ii), предпочтительно за по меньшей мере приблизительно 5 дней, предпочтительно за по меньшей мере приблизительно 1 неделю, предпочтительно за приблизительно от 1 недели до приблизительно 8 недель, предпочтительно за приблизительно от 2 недель до приблизительно 5 недель, предпочтительно за приблизительно от 3 недель до приблизительно 4 недель.
25. Способ по п. 17, отличающийся тем, что указанный способ вакцинации дополнительно включает после этапа (i) и до проведения этапа (ii):
(i') введение субъекту
(a') белка оболочки из генотипа A вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, при этом указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и/или
(b') ядерного белка (антиген HBc) из генотипа D вируса гепатита B, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B,
при этом этап (i') предпочтительно представляет собой этап стимулирующей вакцинации.
26. Способ по п. 25, отличающийся тем, что этап (i) проводят за по меньшей мере приблизительно 1 день до проведения этапа (i'), предпочтительно за по меньшей мере приблизительно 5 дней, предпочтительно за по меньшей мере приблизительно 1 неделю, предпочтительно за приблизительно от 1 недели до приблизительно 8 недель, предпочтительно за приблизительно от 2 недель до приблизительно 5 недель, предпочтительно за приблизительно от 3 недель до приблизительно 4 недель, и при этом этап (i') проводят за по меньшей мере приблизительно 1 день до проведения этапа (ii), предпочтительно за по меньшей мере приблизительно 5 дней, предпочтительно за по меньшей мере приблизительно 1 неделю, предпочтительно за приблизительно от 1 недели до приблизительно 8 недель, предпочтительно за приблизительно от 2 недель до приблизительно 5 недель, предпочтительно за приблизительно от 3 недель до приблизительно 4 недель.
27. Способ по п. 17, отличающийся тем, что указанное введение осуществляют парентеральным путем или через слизистую оболочку.
28. Способ по п. 27, отличающийся тем, что указанное введение осуществляют внутримышечным путем, и при этом этап (i) и/или (i') включает введение адъюванта, причем указанный адъювант содержит циклический ди-АМФ.
29. Способ по п. 27, отличающийся тем, что указанное введение осуществляют подкожным или внутримышечным путем, и при этом этап (i) и/или (i') включает введение адъюванта, причем указанный адъювант содержит поли-I/C или лиганд RIG-I.
30. Фармацевтическая композиция для вакцинации против вируса гепатита B, содержащая рекомбинантный вектор для вакцинации по любому из пп. 1-14.
31. Фармацевтическая композиция по п. 30, отличающаяся тем, что указанный рекомбинантный вектор для вакцинации представляет собой вирус MVA или штамм Salmonella.
32. Фармацевтическая композиция по п. 30 или 31, отличающаяся тем, что указанная вакцина представляет собой вакцину для парентерального введения или введения через слизистую оболочку.
33. Набор для вакцинации против вируса гепатита B, содержащий:
(i) белковую композицию, содержащую:
(a) белок оболочки из генотипа A вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, причем указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и/или
(b) ядерный белок (антиген HBc) из генотипа D вируса гепатита B, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B;
(ii) вакцину по любому из пп. 30-32.
34. Набор по п. 33, отличающийся тем, что указанная белковая композиция подходит для парентерального введения, причем указанная композиция предпочтительно содержит по меньшей мере один адъювант, который представляет собой адъювант PCEP и/или CpG.
35. Набор по п. 33, отличающийся тем, что указанная белковая композиция подходит для введения через слизистую оболочку, причем указанная композиция предпочтительно содержит адъювант, выбранный из группы, состоящей из CTA1DD, dmLT, PCEP, поли-I/C, лиганда RIG-I, цикло-ди-АМФ, цикло-ди-ЦМФ и цикло-ди-ГМФ или их комбинаций.
36. Набор по п. 33, отличающийся тем, что указанная белковая композиция подходит для внутримышечного введения, причем указанная композиция предпочтительно содержит по меньшей мере один адъювант, который представляет собой циклический ди-АМФ.
37. Набор по п. 33, отличающийся тем, что указанная белковая композиция подходит для подкожного или внутримышечного введения, причем указанная композиция предпочтительно содержит по меньшей мере один адъювант, который представляет собой поли-I/C.
38. Способ вакцинации против гепатита B, причем указанный способ включает:
(i) введение субъекту:
(a') белка оболочки (антиген HBs) из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, причем указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и/или
(b') ядерного белка (антиген HBc) из серотипа ayw вируса гепатита B, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B; и
(ii) введение указанному субъекту вируса MVA, экспрессирующего
(а) белок оболочки (антиген HBc) из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, причем указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и вируса MVA, экспрессирующего
(b) ядерный белок (антиген HBc) из серотипа ayw вируса гепатита B, причем указанный ядерный белок содержит или состоит из аминокислот 1-149 антигена HBc, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B.
39. Способ по п. 38, отличающийся тем, что указанный вирус MVA, экспрессирующий (a), и/или указанный вирус MVA, экспрессирующий (b), дополнительно экспрессирует CD70.
40. Кассета экспрессии, содержащая нуклеиновую кислоту, кодирующую:
(a) белок оболочки (HBs-антиген) из серотипа adw вируса гепатита B, причем указанный белок оболочки предпочтительно представляет собой малый или большой белок оболочки из генотипа A серотипа adw вируса гепатита B, причем указанный малый или большой белок оболочки предпочтительно представляет собой малый белок оболочки; и
(b) ядерный белок (HBc-антиген) из серотипа ayw вируса гепатита B, причем указанный ядерный белок содержит или состоит из аминокислот 1-149 антигена HBc, причем указанный ядерный белок предпочтительно представляет собой ядерный белок из генотипа D серотипа ayw вируса гепатита B;
и по меньшей мере один из следующего:
(c) иммуногенный белок оболочки (HBs-антиген) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 1; и/или
(d) иммуногенный ядерный белок (HBc-антиген) из вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 2; и/или
(e) иммуногенный домен RT полимеразы вируса гепатита B, последовательность которого по меньшей мере на 90% идентична аминокислотной последовательности, представленной в SEQ ID NO: 3.
| WO2009056535 A2, 07.05.2009 | |||
| US2008267996 A1,30.10.2008 | |||
| US6235288 B1, 22.05.2001. |
Авторы
Даты
2021-01-21—Публикация
2017-01-12—Подача