Область техники, к которой относится изобретение
Изобретение относится к применению соединений для стимуляции роста и/или ингибирования или замедления выпадения волос у людей, и к композициям для такого применения, включающим такие соединения в качестве активных веществ.
Предшествующий уровень техники
Термин “сандаловое дерево” относится к классу древесины из деревьев рода Santalum. Эфирное масло сандалового дерева обычно экстрагируют путем паровой дистилляции древесины из зрелых сандаловых деревьев, и оно является хорошо известным компонентом для парфюмерии.
Среди множества различных применений в области косметологии, в основном связанных с его ценным запахом, масло сандалового дерева также является предметом патентных публикаций, касающихся фармакопейных и эмпирических препаратов для целого ряда различных применений, включая обычное лечение выпадения волос и перхоти, таких как, например, патентная публикация CN1075250A, описывающая лекарственный экстракт, определяемый по сути как средство китайской медицины, включающий сандаловое дерево, смешанное с цветочным бутоном магнолии, цветком розы, корнем лакрицы, порошком коры пиона, кемпферией, сиренью, травой копытня, женьшенем и корнем дудника.
CN102000293 и CN103735443 описывают аналогичные средства китайской медицины, которые в первом документе состоят из смеси сандалового дерева, корней и корневища дудника, семян кемпферии, талька, базилика священного, натурального индиго и аралии, а во втором документе состоят из смеси из сандалового дерева, корня горца остроконечного, сосновых игл и шалфея многокорневищного, для нанесения на волосы.
Для по существу аналогичного типичного использования индийская патентная публикация IN00177MU2002A описывает композицию для профилактики выпадения волос, которая включает масло сандалового дерева, смешанное с кокосовым маслом, эвкалиптовым маслом, гвоздичным маслом, маслом лаванды и розмариновым маслом.
Для таких эмпирических препаратов конкретная роль каждого ингредиента, смешанного в итоговом масле, не определена в таких публикациях, так что не определяется конкретная функция ингредиента масла сандалового дерева в смесях, в качестве ароматизатора или, возможно, чего-то иного.
В любом случае основными компонентами сандалового масла являются α-санталол и β-санталол, которые являются спиртами, демонстрирующими в основе цепь сесквитерпенового типа. Структурной формулой α-санталола является:
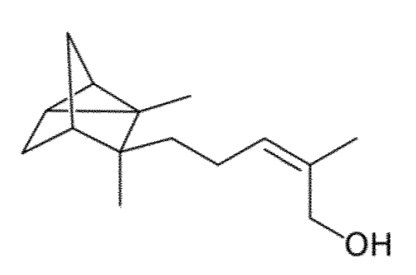
а структурной формулой β-санталола:
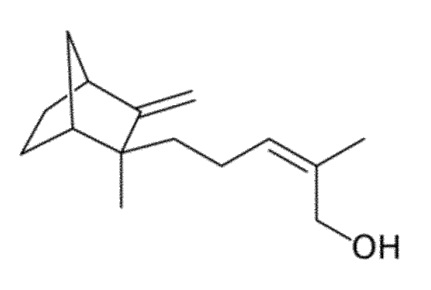
характеризующаяся терминальной трициклогепт-3-ильной или бициклогепт-2-ильной группой, соответственно.
С другой стороны, соединение, известное как сандалор, представляет собой синтетическое душистое вещество, имеющее аромат, подобный сандаловому дереву, и, следовательно, используемое в парфюмерных средствах, смягчающих средствах и средствах для очистки кожи как менее дорогой ингредиент, имитирующий запах сандалового дерева. Сандалор, а также структурно подобное соединение, называемое брахманолом, представляют собой спирты, имеющие химическую структуру, совершенно отличную от указанных ингредиентов натурального масла сандалового дерева, то есть α-санталола и β-санталола.
Фактически, сандалор или сандал пентанол, имеющий формулу:
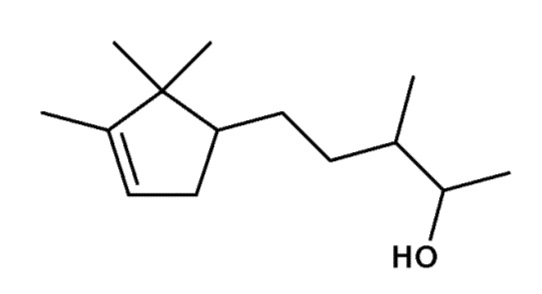
и брахманол или сандал циклопентан, имеющий формулу:
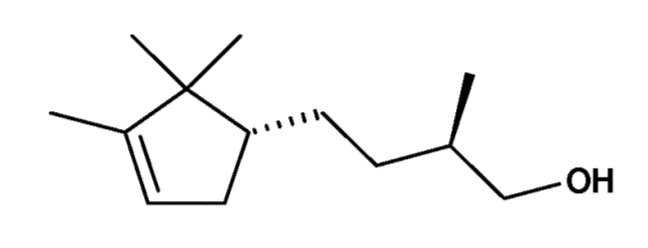
являются синтетическими молекулами, которые характеризуются концевой циклопентен-1-ильной группой и не имеют сесквитерпеновой цепи. Они также являются предметом патентных публикаций, касающихся обработки волос косметическими композициями, такими как шампуни и кондиционеры для волос, однако они применяются просто как ароматические вещества, на самом деле с конкретной целью использования их свойства имитировать ценный аромат сандалового дерева. Например, EP1561476 описывает дезодорантные композиции для улучшения дезодорирующих эффектов, где среди широкого ряда веществ и широкого спектра применений также описано использование сандалора и брахманола в качестве дезодорирующих ароматических веществ в средствах для ухода за волосами, таких как шампуни, кондиционеры, ополаскиватели для волос, красители для волос, агенты для химической завивки, воск, аэрозоль для волос и мусс. Ароматизаторы природного происхождения, используемые в качестве ароматизаторов в ЕР1561476, включают масло сандалового дерева, а сандалор и брахманол определяются в качестве торговых наименований вышеуказанных материалов, что означает, что в соответствии с этим документом нет различия между ароматом, обеспечиваемым натуральным экстрактом, и его синтетическими заменителями.
EP1346720 относится к дезодорантной композиции для окрашивания волос, имеющей аналогичный объем.
В таких публикациях не упоминаются даже общем виде такие синтетические ароматические вещества для лечения выпадения волос, или для стимуляции роста волос.
В соответствии с Busse et al., “A Synthetic Sandalwood Odorant Induces Wound-Healing Processes in Human Keratinocytes via the Olfactory Receptor OR2AT4”, Journal of Investigative Dermatology, 2014, 134: 2823-2832, сандалор и брахманол были идентифицированы в качестве агонистов кожного обонятельного рецептора OR2AT4, и как было установлено, индуцируют сигналы Са2+ в культивируемых кератиноцитах человека. Долговременная стимуляция кератиноцитов сандалором положительно влияет на пролиферацию клеток, миграцию и регенерацию монослоев кератиноцитов в анализе заживления царапины in vitro, а стимуляция сандалором усиливает заживление раны эпидермиса в органных культурах кожи человека.
Согласно Busse et al., было доказано, что натуральное масло сандалового дерева и другие синтетические ароматизаторы сандалового дерева не являются агонистами обонятельного рецептора OR2AT4 и не проявляют такого эффекта заживления раны эпидермиса.
Экспрессия обонятельных рецепторов (ОР) не ограничивается эпителием носа, но также отмечается в других тканях человека, см. Feldmesser E, Olender T, Khen M, Yanai I, Ophir R, Lancet D., “Widespread ectopic expression of olfactory receptor genes”. BMC Genomics. 2006 May 22;7:121; Zhang X, Firestein S., “Nose thyself: individuality in the human olfactory genome”. Genome Biol. 2007;8(11):230; Flegel C, Manteniotis S, Osthold S, Hatt H, Gisselmann G., “Expression profile of ectopic olfactory receptors determined by deep sequencing”. PLoS One. 2013;8(2):55368). Многочисленные исследования описывают физиологическую роль ОР в различных типах клеток человека (Kang N, Koo J. “Olfactory receptors in non-chemosensory tissues”. BMB Rep. 2012 Nov;45(11):612-22), таких как сперматозоиды (Spehr M, Gisselmann G, Poplawski A, Riffell JA, Wetzel CH, Zimmer RK, Hatt H. “Identification of a testicular odorant receptor mediating human sperm chemotaxis”. Science. 2003 Mar 28;299(5615):2054-8; Veitinger T, Riffell JR et al, “Chemosensory Ca2+ dynamics correlate with diverse behavioural phenotypes in human sperm”. J Biol Chem. 2011 May 13;286(19):17311-25), эпителиальные клетки простаты (Neuhaus EM, Zhang W, Gelis L, Deng Y, Noldus J, Hatt H. “Activation of an Olfactory Receptor Inhibits Proliferation of Prostate Cancer Cells”. J Biol Chem. 2009;284(24):16218-16225), и энтерохромаффинные клетки кишечника (Braun T, Voland P, Kunz L, Prinz C, Gratzl M. “Enterochromaffin cells of the human gut: sensors for spices and odorants”. Gastroenterology. 2007 May;132(5):1890-901).
Изложение сущности изобретения
В соответствии с настоящим изобретением неожиданно было обнаружено, что рост волос можно стимулировать, и что выпадение волос можно ингибировать или замедлить на коже головы человека с использованием соединений общей формулы (I):

где
R1 и R2 образуют вместе двойную связь, или R1 и R2 образуют вместе циклопропильную группу;
R3, R4 являются одинаковыми или различными, и независимо выбраны из водорода, метила, или R3 и R4 вместе образуют двойную связь;
R5, R6 являются одинаковыми или различными, и независимо выбраны из водорода, метила; или R5 и R6 вместе образуют двойную связь, или R5 и R6 вместе образуют циклопропильную группу;
R7 представляет собой метил или этил;
R8 представляет собой водород или метил.
В рамках нового применения в соответствии с настоящим изобретением предпочтительные соединения формулы (I), включая вышеупомянутый сандал пентанол (соединение 1) и сандал циклопентан (соединение 5), приведены в следующей таблице:
Таблица
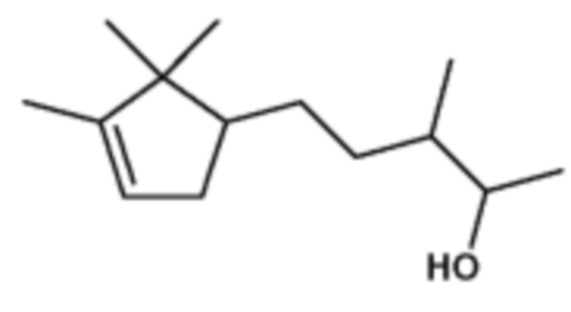
210,36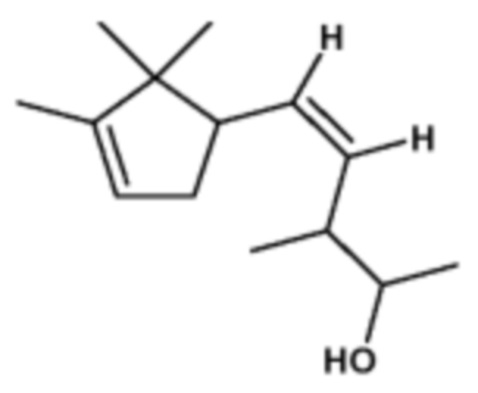
208,35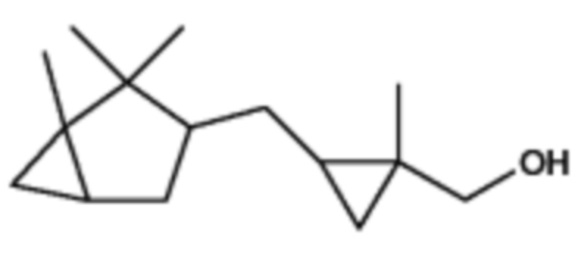
222,37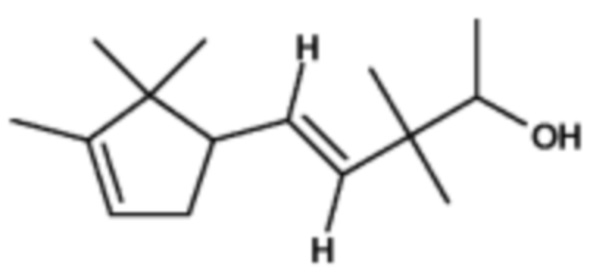
222,37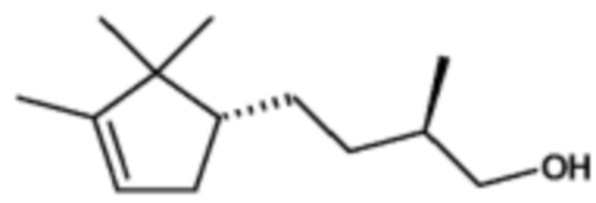
196,34
208,35
194,32
Предметом изобретения являются также композиции, используемые для стимуляции роста волос и/или ингибирования или замедления выпадения волос, подходящие для местного применения на коже головы человека, где одно или несколько соединений формулы (I) используют в качестве активных веществ, предпочтительно в количестве от 0,1 до 10% по массе (масс.%), в сочетании с ингредиентами, подходящими для местного применения.
Композиции по изобретению пригодны как для косметического, так и терапевтического применения для стимуляции роста волос и/или для лечения выпадения волос на волосистой части кожи головы человека, где по меньшей мере одно соединение общей формулы (I) входит в качестве активного ингредиента.
Подробное описание изобретения
Для лучшего понимания характеристик и преимуществ изобретения ниже описаны его не ограничивающие практические примеры. Компоненты названы в соответствии с номенклатурой INCI.
Примеры
Пример 1
Лосьон
Пример 2
Маска перед мытьем шампунем
Пример 3
Укрепляющий гель для укладки волос
Пример 4
Укрепляющий кондиционер для волос
Пример 5
Оздоравливающий шампунь
Пример 6
Мусс
Краткое описание чертежей
Со ссылкой на фиг. 1-5 соответствующих чертежей.
На фиг. 1 показаны изображения иммунофлуоресценции, взятые от образцов тканей кожи волосистой части головы человека и волосяных фолликулов (HF).
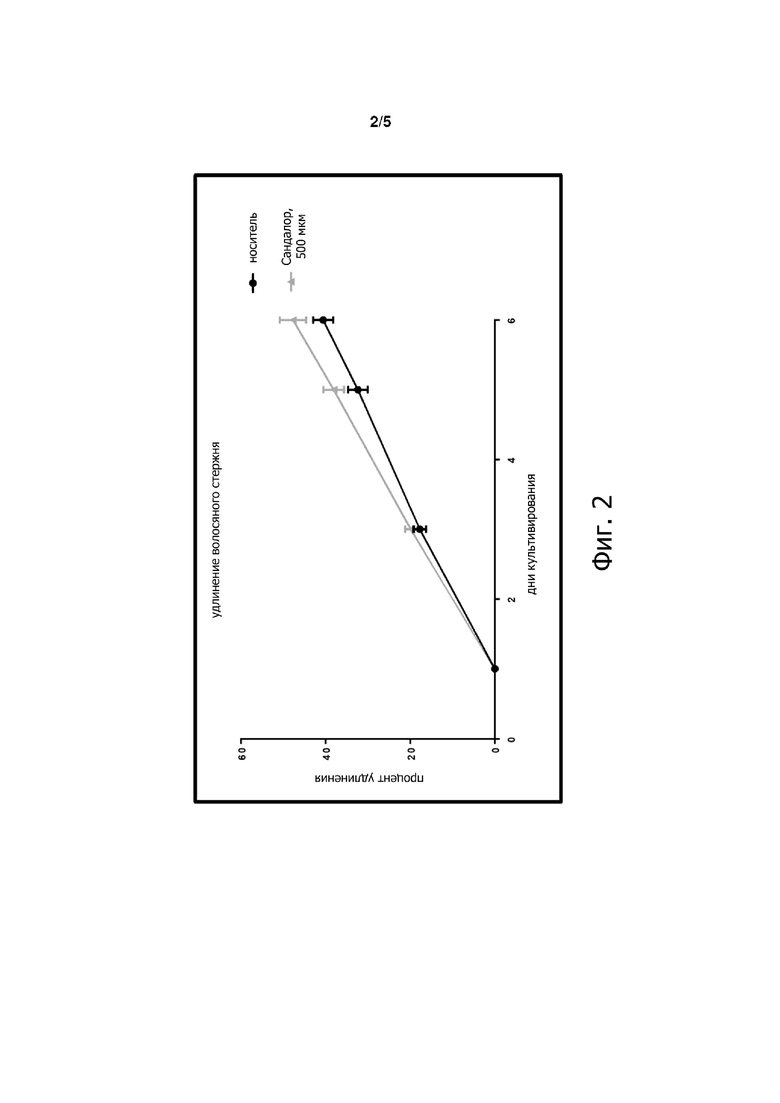
На фиг. 2 показана диаграмма, относящаяся к удлинению волосяного стержня.
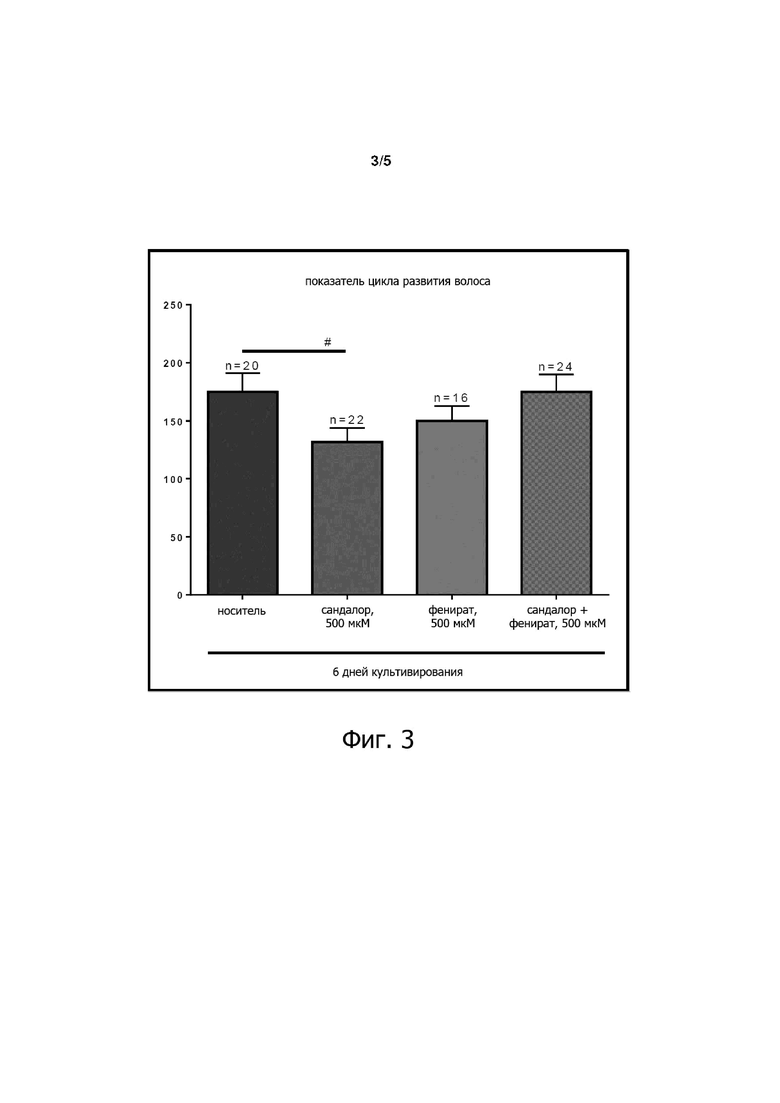
На фиг. 3 показана диаграмма, относящаяся к циклу роста волоса, с конкретной ссылкой на фазу катагена.
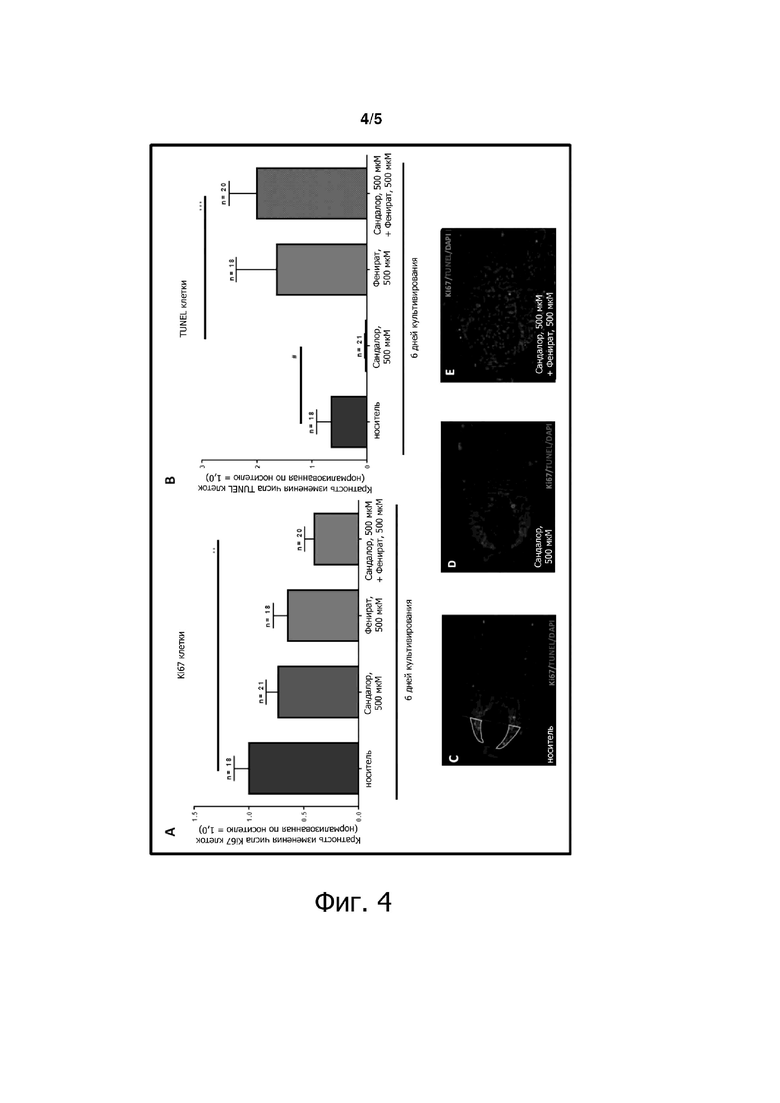
На фиг. 4 показана диаграмма, относящаяся к пролиферации кератиноцитов матрикса волоса и к апоптозу.
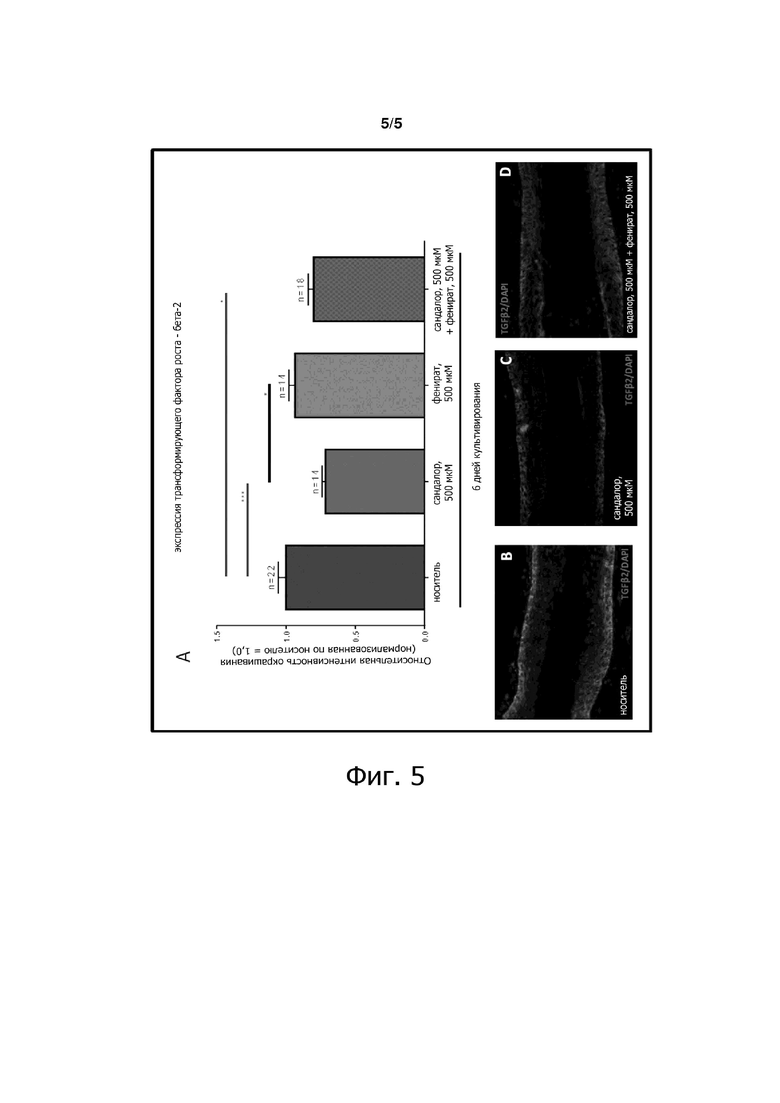
На фиг. 5 показана диаграмма, относящаяся к катаген-стимулирующему фактору роста TGF-β2.
На фиг. 1-5 приведены результаты, полученные в следующем экспериментальном исследовании, и таким образом, подробно изложены в следующем описании.
Экспериментальное исследование
Указанное соединение 1 в соответствии с изобретением, то есть сандал пентанол, было выбрано из соединений формулы (I), которые должны быть испытаны для экспериментальных целей следующим образом. Сандал пентанол обозначен как Сандалор на диаграммах фиг. 2-5.
Дизайн исследования
В качестве первого этапа использовали стандартную иммунофлуоресценцию срезов тканей волосистой части головы человека от здоровых доноров с целью установления экспрессии OR2АT4 в волосяных фолликулах волосистой части головы человека (HF).
Затем для того, чтобы оценить, может ли стимуляция OR2AT4 влиять на рост волос человека, микропрепараты HF обрабатывали сандал пентанолом с концентрацией 500 мкМ в качестве агониста, и проводили измерение удлинения волосяного стрежня (см. Philpottetal., 1990). Кроме того, проводили анализ киназы, чтобы установить, какие сигнальные пути вовлечены в специфическую стимуляцию OR2AT4 сандал пентанолом.
Впоследствии, чтобы подтвердить, что анаген-пролонгирующий эффект сандал пентанола является специфичным, осуществляли культивирование HF с применением сандал пентанола в качестве агониста, и специфического антагониста фенирата (феноксиэтил-изобутирата), синтетического ароматического вещества, см. Busse et al., ссылку, упомянутую выше.
HF обрабатывали носителем, сандал пентанолом, фениратом или смесью сандал пентанола и фенирата. Для анализа изменения волосяного цикла выполняли Ki67/TUNEL и использовали для оценки показателей цикла развития волоса и пролиферации и апоптоза кератиноцитов волосяной матрицы.
Кроме того, исследовали TGFβ2, мощный индуктор катагена, по отношению к вышеуказанным соединениям.
Для осуществления понижающей регуляции экспрессии OR2AT4 в человеческих HF и изучения его влияния на рост волос, HF трансфицировали OR2AT4-миРНК.
Использовали количественную ПЦР в режиме реального времени и (иммуно)гистоморфометрический анализ для подтверждения успешной миРНК-опосредуемой понижающей регуляции гена и белка OR2AT4 в микропрепаратах HF. Наконец, для того, чтобы исследовать, как нокаут OR2AT4 влияет на рост волос человека, использовали Ki67/TUNEL иммунофлуоресценцию для количественного анализа показателей цикла развития волоса и пролиферации и апоптоза кератиноцитов волосяной матрицы. Чтобы проверить, может ли нокдаун влиять на индукцию катагена, анализировали экспрессияю TGF-β2 путем иммунофлуоресценции.
Материалы и методы
Образцы тканей
Кожу волосистой части головы здорового человека с височной и затылочной областей получали от здоровых доноров (в возрасте 38-69 лет) при выполнении рутинной хирургической операции по подтяжке лица после получения информированного согласия и разрешения этического комитета.
Иммунофлуоресценция
Готовили срезы залитых реактивом ОСТ образцов (толщиной 6 мкм) посредством криостата. Срезы фиксировали 4% параформальдегидом, предварительно инкубировали с 10% козьей сывороткой (для OR2AT4) или 5% козьей сывороткой + 0,3% Тритон X-100 (для расщепления каспазой-3) и инкубировали с соответствующим первичным антителом при 4°C в течение ночи (1/100 для OR2AT4 и 1/400 для расщепления каспазой-3). Инкубацию с вторичным антителом проводили при комнатной температуре в течение 45 мин. Окраску DAPI (1 мкг/мл) проводили с целью визуализации ядер. Для TGF-β2 образцы фиксировали в ацетоне и блокировали эндогенные пероксидазы 3% H2O2. Этот этап сопровождался этапом блокирования авидина-биотина и предварительной инкубацией с буфером TNB (Трис-HCl + NaCl + казеин). Соответствующее первичное антитело инкубировали при 4°С в течение ночи (1/1000 для TGF-β2). Инкубацию с вторичным антителом проводили при комнатной температуре в течение 45 минут перед применением набора для тирамидной амплификации сигнала (Perkin Elmer). Окрашивание DAPI проводили для визуализации ядер. Для окрашивания апоптотических и пролиферирующих клеток использовали набор Аpoptag-kit (MerckMilipore) в соответствии с инструкциями производителя, с последующим окрашиванием Ki67. Первичное антитело инкубировали в течение ночи (Ki67, 1/20) после TdT-ферментного этапа. Вторичное антитело инкубировали в течение 45 минут при комнатной температуре после этапа анти-дигоксигенина с флуоресцентной меткой из набора Аpoptag kit. Окрашивание DAPI проводили для визуализации ядер. Отрицательный контроль осуществляли, не используя первичное антитело. Изображения получали с применением флуоресцентного микроскопа Keyence (Осака, Япония), сохраняя постоянное время выдержки при получении изображения для последующего анализа.
Органная культура волосяных фолликулов
Образцы волосистой кожи головы человека были получены после процедуры подтяжки лица и использованы в тот же день для получения микропрепаратов HF волосистой части головы человека в фазе анагена VI. Микропрепараты HF волосистой части кожи головы человека культивировали при 37°C в атмосфере 5% CO2 в минимальной среде Уильяма Е (Gibco, Life technologies) с добавлением 2 мМ L-глутамина (Gibco), 10 нг/мл гидрокортизона (Sigma-Aldrich), 10 пг/мл инсулина (Sigma-Aldrich) и 1% смеси пенициллина/стрептомицина (Gibco) (WEM), как описано ранее (Philpott, 1990; Kloepper, 2010; Langan et al, 2015).
1) Химическая стимуляция микропрепаратов человеческих HF с OR2AT4 сандал пентанолом (агонистом) и фениратом (антагонистом).
После 24 часов инкубации среду WEM заменяли, и HF обрабатывали соответствующими веществами в течение 6 дней в соответствующих экспериментальных условиях. HF обрабатывали носителем (0,1% ДМСО), сандал пентанолом (500 мкМ), фениратом (в отношении 1:1 к агонисту), или смесью сандал пентанола + фенирата.
Фенират добавляли за 30 минут до сандал пентанола. Удлинение волосяного стрежня измеряли ежедневно с применением инвертированного бинокулярного микроскопа (Philpott et al., 1990), и заменяли среду для культивирования каждые два дня. HF встраивали в криоматрикс (Fisher Scientific) и подвергали мгновенному замораживанию в жидком азоте. Готовили срезы толщиной 6 мкм с помощью криостата, и хранили их при -80°С для дальнейшего иммуногистохимического анализа.
Количественная (иммуно)гистоморфометрия
Интенсивность окрашивания оценивали в точно определенных контрольных областях с помощью количественной (иммуно)гистоморфометрии, как описано ранее (Bertolini et al., 2014) с использованием программного обеспечения NIH IMAGE (NIH, Бетесда, Мэриленд, США).
Статистический анализ
Все данные выражены в виде среднего значения ± SEM (стандартной ошибки среднего значения) и были проанализированы с помощью одностороннего дисперсионного анализа или критерия Краскела-Уоллиса, когда сравнивали более двух групп, и t-теста Стьюдента или теста Манна-Уитни, когда обработку сандал пентанолом сравнивали с обработкой носителем (программное обеспечение Graph Pad Prism 6, Graph Pad Software, Сан-Диего, Калифорния, США).
Результаты
Результаты описаны со ссылкой на прилагаемые чертежи на фиг. 1-5.
1) Человеческие HF экспрессируют обонятельный рецептор 2АТ4
Во-первых, исследовали наличие обонятельного рецептора 2AT4 (OR2AT4) в HF. OR2AT4 был обнаружен в кератиноцитах наружной оболочки волосяной луковицы (ORS) HF кожи головы человека, как показано посредством иммунофлуоресценции на фиг. 1. Изображения (A)-(D) на фиг. 1 представляют собой иммунофлуоресценцию OR2AT4 в HF в волосистой части кожи головы человека (см. изображение A и соответствующие увеличения) и микропрепаратах HF (см. изображения B-D и соответствующие увеличения) от трех разных доноров (n = 3). CTS обозначает оболочку из соединительной ткани, DP - дермальный гребень, HM - матрицу волоса, IRS - внутреннее корневое влагалище, ORS - наружное корневое влагалище, HS - волосяной стержень, HB - волосяную луковицу, HF - волосяные фолликулы. Пунктирные линии обозначают IRS (внутреннее корневое влагалище), ORS (наружное корневое влагалище) и DP (дермальный гребень).
На фиг. 1 показано, что OR2AT4 экспрессируется в супрабульбарных кератиноцитах ORS HF волосистой части головы в фазе анагена, и в супрабульбарных и бульбарных ORS, и в кератиноцитах кончиков волосяной матрицы в микропрепаратах HF в фазе анагена.
Микропрепараты HF в фазе анагена (модель Philpott) выявили OR2AT4 клетки в волосяной луковице, а именно в ORS и на кончиках волосяной матрицы (HM), см. фиг. 1B, в дополнение к характерной супрабульбарной интрафолликулярной экспрессии, см. фиг. 1D.
2) Специфическая стимуляция OR2AT4 сандал пентанолом стимулирует удлинение волосяного стержня и ингибирует путь передачи апоптотического сигнала.
Чтобы проверить, может ли активация OR2AT4 влиять на цикл развития человеческих HF, микропрепараты человеческих HF специфически стимулировали потенциальным агонистом сандал пентанолом. Эффект лечения сандал пентанолом оценивали путем измерения удлинения волосяного стержня при сравнении с обработкой носителем.
Удлинение HF измеряли в культивируемых микропрепаратах HF. Определяли среднее значение ± SEM, n = 18 HF для каждого донора, 2 донора, t-критерий Стьюдента, Graph Pad Prism 6. Несмотря на различия между отдельными индивидуумами, результаты показали, что сандал пентанол в концентрации 500 мкМ стимулирует удлинение волосяного стержня культивируемых микропрепаратов HF, полученных от двух доноров, как показано на диаграмме фиг. 2, демонстрирующей процент удлинения по дням культивирования для сандалора по сравнению с носителем.
3) Активация OR2AT4 сандал пентанолом существенно замедляет индукцию катагена и снижает апоптоз в кератиноцитах волосяной матрицы человека.
Для исследования специфичности влияния на рост волос стимуляции OR2AT4 сандал пентанолом, микропрепараты HF культивировали с сандал пентанолом и/или фениратом, и проводили анализ стадий цикла развития волоса, как описано ранее (Kloepper, 2010; Langan et al, 2015). Оценку цикла развития волоса проводили для HF в опытной группе и при обработке носителем спустя 6 дней культивирования. N = 16-24 HF для 3 пациентов, среднее значение ± SEM, тест Краскела-Уоллиса и тест множественных сравнений Данна в качестве апостериорного критерия, ns, тест Манна-Уитни, #p <0,05, Graph Pad Prism 6.
Полученные результаты указывают, что специфическая стимуляция OR2AT4 сандал пентанолом в концентрации 500 мкМ замедляет индукцию катагена в обработанных HF, по сравнению с носителем, спустя 6 дней культивирования, как показано на диаграмме фиг. 3. Напротив, обработка фениратом по отдельности и смесью сандал пентанола с фениратом не приводит к продлению фазы анагена в обработанных HF, по сравнению с носителем. Данные позволяют предположить, что стимуляция OR2AT4 сандал пентанолом стимулирует задержку катагена, в то время как этим эффектам противодействует ингибирование OR2AT4 с использованием фенирата.
Подводя итог, на фиг. 3 показано, что соединение по изобретению значительно замедляет развитие катагена.
4) Сандал пентанол значительно уменьшает апоптоз кератиноцитов матрицы волос.
Что касается свидетельства, показанного на фиг. 4, то для исследования влияния сандал пентанола на пролиферацию и апоптоз кератиноцитов матрицы волос проводили окрашивание Ki67/TUNEL. Пролиферирующие (диаграмма с фиг. 4А) и апоптотические (диаграмма с фиг. 4В) кератиноциты волосяной матрицы подсчитывали в волосяной матрице обработанных и необработанных HF. Примерные изображения Ki67/TUNEL показаны на фиг. 4С-4Е. Приведены среднее значение ± SEM, n = 18-21 HF от 3 пациентов, тест Краскела-Уоллиса и тест множественных сравнений Данна в качестве апостериорного критерия, ** p <0,01, *** p <0,001, тест Манна-Уитни #p <0,05, Graph Pad Prism 6.
После культивирования в течение 6 дней пролиферация кератиноцитов волосяной матрицы не изменялась в HF, обработанных сандал пентанолом или фениратом по отдельности. Однако, совместное применение специфического антагониста OR2AT4 фенирата вместе с сандал пентанолом индуцировала существенное снижение пролиферации кератиноцитов волосяной матрицы, как показано на фиг. 4А.
Обработка сандал пентанолом значительно уменьшала апоптоз кератиноцитов волосяной матрицы, в то время как совместное применение сандал пентанола + фенирата значительно повышало апоптоз кератиноцитов волосяной матрицы, как показано на фиг. 4В.
5) Специфическая стимуляция OR2AT4 сандал пентанолом значительно уменьшала катаген-стимулирующий фактор роста TGF-β2.
Со ссылкой на доказательства на фиг. 5, для дополнительного исследования влияния ОR агониста и антагониста на рост HF оценивали экспрессию релевантного катаген-стимулирующего фактора роста во время физиологического цикла развития HF человека, т.е. TGF-β2 (Soma et al., 2002), в проксимальных OR. После 6 дней обработки сандал пентанолом наблюдалось значительное снижение экспрессии TGF-β2 на белковом уровне, в то время как не отмечено изменения при блокировании рецептора фениратом. В этом случае совместное применение сандал пентанола с фениратом показало сопоставимый результат с применением сандал пентанола по отдельности, как показано на диаграмме на фиг. 5А. Экспрессию TGF-β2 измеряли в ORS кератиноцитах в обработанных и необработанных HF.
Соответствующие примерные снимки иммунофлуоресценции TGF-β2 показаны на фиг. 5, B (носитель), C (сандалор), D (сандалор + фенират).
Экспрессию TGF-β2 определяли количественно с использованием Image J. Среднее значение ± SEM, n = 14-22 HF от 2 пациентов, тест множественных сравнений Краскела-Уоллиса и Данна в качестве апостериорного теста, *p <0,05, ***p <0,001 и тест Манна-Уитни, ns. Graph Pad Prism 6.
Выводы
Вышеприведенные результаты показывают, что OR2AT4 является модулятором роста волос, а соединение по изобретению представляет собой анаген-пролонгирующий агент. Стимуляция OR2AT4 соединением по изобретению повышает удлинение стержня волоса и замедляет переход в фазу катагена, в то время как этот эффект не достигается с ингибитором OR2AT4 фениратом, и в значительной степени подавляется, когда соединение по изобретению применяют совместно с фениратом.
Стимуляция OR2AT4 соединением по изобретению модулирует пути передачи апоптотического сигнала и существенно снижает апоптоз кератиноцитов волосяной матрицы человека, в то время как этот эффект не достигается с помощью фенирата, и по существу подавляется, когда соединение по изобретению совместно применяют с фениратом.
Стимуляция OR2AT4 соединением по изобретению значительно уменьшает релевантный катаген-стимулирующий фактор роста TGF-β2, в то время как этот эффект не достигается с помощью фенирата.
В общих чертах экспериментальные данные показывают, что соединения формулы (I), как определено выше, могут быть эффективно использованы для стимуляции роста волос и/или ингибирования или замедления выпадения волос на волосистой части головы человека.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ ИЛИ КОСМЕТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АЛОПЕЦИИ | 2013 |
|
RU2635627C2 |
| КОМПОЗИЦИЯ ДЛЯ РОСТА И УЛУЧШЕНИЯ СОСТОЯНИЯ ВОЛОС | 2024 |
|
RU2831552C1 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ ЗЕАКСАНТИНА, ОБЛАДАЮЩЕГО СПЕЦИФИЧЕСКОЙ АНТИАПОПТОЗНОЙ АКТИВНОСТЬЮ ДЛЯ КАСПАЗЫ-3, И КОМПОЗИЦИИ, ЕГО СОДЕРЖАЩИЕ | 2009 |
|
RU2504366C2 |
| СОСТАВ ПРЕПАРАТА ДЛЯ СТИМУЛЯЦИИ РОСТА ВОЛОС | 2023 |
|
RU2812523C1 |
| ЭКСТРАКТ ЛЕСПЕДЕЦЫ ГОЛОВЧАТОЙ ДЛЯ ПРИМЕНЕНИЯ В ОБЛАСТИ УХОДА ЗА ВОЛОСАМИ | 2019 |
|
RU2799324C2 |
| СРЕДСТВА, СТИМУЛИРУЮЩИЕ РОСТ ВОЛОС | 2005 |
|
RU2342384C2 |
| ЭКСТРАКТ СЕМЯНОК SILYBUM MARIANUM (L.) GAERTN. ДЛЯ СТИМУЛЯЦИИ РОСТА ВОЛОС | 2020 |
|
RU2834029C2 |
| Композиция для предупреждения выпадения волос или стимуляции роста волос | 2019 |
|
RU2794988C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УЛУЧШЕНИЯ КАЧЕСТВА ВОЛОС С ПРИМЕНЕНИЕМ ЭКСТРАКТА ЕЖЕВИКИ | 2014 |
|
RU2678099C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИЧЕСКОГО ИЛИ ТЕРАПЕВТИЧЕСКОГО ЛЕЧЕНИЯ СОСТОЯНИЙ, СВЯЗАННЫХ С ИЗМЕНЕНИЕМ КОЛИЧЕСТВА ВОЛОС | 2018 |
|
RU2716159C2 |

Изобретение относится к косметическому применению 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ола, а также композиции, содержащей 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ол, в качестве активного начала в количестве от 0,1 до 10% по массе (масс.%), в сочетании с ингредиентами, пригодными для местного применения, для стимуляции роста волос и/или ингибирования или замедления выпадения волос на волосистой части головы человека. Кроме того, изобретение относится к применению 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ола для изготовления лекарственного средства от выпадения волос на волосистой части головы человека, а также к применению фармацевтической композиции, содержащей 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ол, в качестве активного начала для лечения выпадения волос на волосистой части головы человека в количестве от 0,1 до 10% по массе (масс.%), в сочетании с ингредиентами, пригодными для местного применения. Технический результат – получение эффективного средства для стимуляции роста волос и/или для лечения выпадения волос на волосистой части кожи головы человека. 4 н. и 6 з.п. ф-лы, 5 ил., 1 табл., 6 пр.
1. Косметическое применение 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ола для стимуляции роста волос и/или ингибирования или замедления выпадения волос на волосистой части головы человека.
2. Косметическое применение композиции, содержащей 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ол, в качестве активного начала в количестве от 0,1 до 10% по массе (масс.%), в сочетании с ингредиентами, пригодными для местного применения, для стимуляции роста волос и/или ингибирования или замедления выпадения волос на волосистой части головы человека.
3. Косметическое применение по п. 2, где композиция представляет собой лосьон, имеющий следующий состав:
4. Косметическое применение по п. 2, где композиция представляет собой маску перед мытьем шампунем, имеющую следующий состав:
5. Косметическое применение по п. 2, где композиция представляет собой укрепляющий гель для укладки волос, имеющий следующий состав:
6. Косметическое применение по п. 2, где композиция представляет собой укрепляющий кондиционер для волос, имеющий следующий состав:
7. Косметическое применение по п. 2, где композиция представляет собой оздоравливающий шампунь, имеющий следующий состав:
8. Косметическое применение по п. 2, где композиция представляет собой мусс, имеющий следующий состав:
9. Применение 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ола для изготовления лекарственного средства от выпадения волос на волосистой части головы человека.
10. Применение фармацевтической композиции, содержащей 3-метил-5-(2,2,3-триметилциклопент-3-ен-1-ил)пентан-2-ол, в качестве активного начала для лечения выпадения волос на волосистой части головы человека в количестве от 0,1 до 10% по массе (масс.%), в сочетании с ингредиентами, пригодными для местного применения.
| Мост | 1986 |
|
SU1346720A1 |
| US 4052341 А1, 04.10.1977 | |||
| EP 1238650 А2, 11.09.2002 | |||
| Видоизменение охарактеризованной в патенте № 904 русской печи с плитой и дымооборотами | 1929 |
|
SU20293A1 |
| ЕР 2916878 А1, 16.09.2015 | |||
| US 7879910 B1, 01.02.2011 | |||
| В.Г | |||
| Беликов "Фармацевтическая химия", учебное пособие, 2007, Москва, "МЕДпресс-информ", стр.27-29. | |||
Авторы
Даты
2021-01-22—Публикация
2017-05-19—Подача