Настоящее изобретение относится к области иммунодиагностики.
Более конкретно, настоящее изобретение относится к антителу, набору и способам in vitro диагностики болезни Альцгеймера и/или предрасположенности субъекта к развитию болезни Альцгеймера или когнитивных расстройств при старении.
ДНК-связывающий домен (DBD) человеческого белка p53 (aa 101-306) характеризуется высокой конформационной гибкостью и содержит один ион Zn2+, координируемый тремя цистеинами (остатки 176, 238 и 242) и одним гистидином (остаток 179). В изоформе дикого типа человеческого белка p53 линейный эпитоп aa 282-297 замаскирован и, следовательно, недоступен для распознавания эпитоп-специфическим антителом.
Однако из-за высокой гибкости домена DBD белок p53 может принимать несколько конформаций, которые также характеризуют его биологическую активность.
В конформации дикого типа белок p53 может связывать консенсусные последовательности ДНК и транскрибировать/подавлять экспрессию целевых генов. В этой конформации у белка обнажается эпитоп, который распознается коммерчески доступным конформационно-специфическим антителом PAb1620.
Существует несколько классов конформационных изменений состояния р53, которые соответствуют различным конформационно измененным изоформам. Некоторые мутации в гене р53 вызывают конформационное изменение белка, соответствующее конформационно измененной изоформе, которая может быть распознана коммерчески доступными конформационно-специфическими антителами.
Дополнительные конформационно измененные изоформы могут быть также получены в результате посттрансляционных модификаций, таких как реакции окисления и/или нитрования, которые изменяют третичную структуру белка дикого типа.
Buizza L. et al. ʺConformational altered p53 as an early marker of oxidative stress in Alzheimerʹs diseaseʺ, PlosOne 7(1):e29789) и Uberti D et al. (ʺIdentification of a mutant-like conformation of p53 in fibroblasts from sporadic Alzheimerʹs disease patientsʺ, Neurobiology of Aging 27 (2006) 1193-1201) идентифицировали экспрессию мутированного белка р53 у пациентов с болезнью Альцгеймера, причем такая идентификация была выполнена с использованием анти-p53 антитела PAb240, которое связывается с криптотопом на аминокислотных остатках 213-217 белка р53, не обнаруживаемых в белке р53 дикого типа.
Авторы настоящего изобретения неожиданно обнаружили античеловеческое p53 антитело с обнаженным линейным эпитопом aa 282-297, которое оказалось способным специфически и селективно распознавать конформационно измененную изоформу белка, полученную посредством посттрансляционных модификаций.
Авторы настоящего изобретения также неожиданно обнаружили, что изоформа белка р53, распознаваемая антителом по изобретению, специфически экспрессируется у пациентов с болезнью Альцгеймера. В частности, конформационно-измененная изоформа, распознаваемая антителом по изобретению, экспрессируется в более высоких количествах в биологических образцах пациентов с болезнью Альцгеймера, в частности, в образцах клеток крови, нейронных клетках или других типах клеток, а также в образцах биологических жидкостей, таких как, например, кровь, плазма, сыворотка, слюна, моча.
Авторы настоящего изобретения также обнаружили, что такая конформационно-измененная изоформа, распознаваемая антителом по изобретению, также экспрессируется в биологических образцах субъектов с легкими когнитивным нарушением (ЛКН, MCI).
Следовательно, антитело по изобретению является полезным диагностическим и прогностическим инструментом для диагностики болезни Альцгеймера и для определения предрасположенности субъекта с легким когнитивным нарушением (ЛКН, MCI) к развитию болезни Альцгеймера.
Наконец, авторы изобретения обнаружили, что экспрессия изоформы белка p53, положительной по отношению к антителу по изобретению, статистически значимым образом коррелирует с возрастом и когнитивными нарушениями у исследуемых субъектов.
Следовательно, антитело по изобретению также может быть использовано для определения предрасположенности субъекта к развитию когнитивных нарушений при старении.
Таким образом, первой задачей настоящего изобретения является предоставление антитела против человеческого р53, отличающегося тем, что оно распознает линейный эпитоп с последовательностью RRTEEENLRKKGEPHH (SEQ ID NO: 1), представленной в ДНК-связывающем домене (DBD) человеческого p53, причем указанный линейный эпитоп находится между аминокислотными остатками в положениях 282-297 аминокислотной последовательности человеческого p53.
Получение антитела по изобретению описано ниже в экспериментальной части.
В предпочтительном варианте осуществления антитело по изобретению представляет собой моноклональное антитело.
Антитело по настоящему изобретению может быть получено любым хорошо известным методом получения поликлональных или моноклональных антител. В экспериментальной части в качестве примера описано антитело, полученное путем иммунизации животных (мышей) антигеном, состоящим из пептида с последовательностью CRTEEENLRKKGEPHH (SEQ ID NO: 2), конъюгированного с бычьим сывороточным альбумином в качестве носителя, а метод получения гибридомы приведен в качестве примера.
Как упоминалось ранее, антитело по настоящему изобретению специфически распознает изоформу человеческого белка p53, которая, как было показано, коррелирует с болезнью Альцгеймера и развитием когнитивных нарушений при старении. Таким образом, такое антитело является полезным диагностическим и прогностическим инструментом.
Способ in vitro определения изоформы, конформационно измененной посттрансляционной модификацией белка р53, свойственной болезни Альцгеймера, а также диагностические и прогностические способы, определенные в прилагаемой формуле изобретения, которые являются неотъемлемой частью настоящего описания, также являются частью настоящего изобретения.
Набор для иммунодиагностики, определенный в прилагаемой формуле изобретения, также является частью настоящего изобретения.
Для реализации способов и набора по изобретению может быть использован любой хорошо известный способ иммуноанализа, такой как, например, иммунопреципитационный анализ, ИФА (ELISA) или РИА, иммунофлюоресценция, Вестерн-блоттинг, FACS-анализ, иммуноцитохимия/иммуногистохимия.
Следующие неограничивающие примеры приведены для иллюстрации объема изобретения, определяемого прилагаемой формулой изобретения.
Пример 1
1a. Иммунизация
Для иммунизации использовали здоровых, без каких-либо нарушений, мышей в возрасте 6/8 недель. Пептид, используемый в качестве антигена для продуцирования антител, имел следующие признаки:
Последовательность: ʺN-конецʺ CRTEEENLRKKGEPHH ʺС-конецʺ (SEQ ID NO: 2)
Длина: 16 аминокислот
Молекулярный вес: 1960,94
Чистота: 96,4%
Форма: лиофилизированный порошок
Конъюгация: конъюгировали с BSA глутаральдегидным методом
Последовательность белка p53 (SEQ ID NO: 3) приведена на фиг.1, где ДНК-связывающий домен (DBD) выделен серым цветом, линейный эпитоп, распознаваемый антителом 2D3A8, подчеркнут.
Первую инъекцию выполняли путем эмульгирования антигена (50 мкг) в полном адъюванте Фрейнда (ПАФ). Подкожные инъекции вводили животному в 2-3 местах. Дополнительные инъекции 50 мкг антигена, эмульгированного в неполном адъюванте Фрейнда (НАФ), проводили с интервалами в 3 недели. Титр антител оценивали методом ELISA.
В анализе ELISA оценивали титр антитела, присутствующий в сыворотке 5 мышей после третьей инъекции вышеописанного пептида. Кровь иммунизированных мышей собирали из хвостовых вен. Величины оптической плотности, полученные после спектрофотометрического считывания, давали важную информацию о титрах антител, присутствующих у разных мышей. Животным вводили дополнительные инъекции, чтобы титр антител достиг достаточно высокого уровня. Для первого слияния была выбрана мышь с лучшим титром антител.
1b. Получение гибридом
Осуществляли слияние спленоцитов животных с клетками мышиной миеломы (линия клеток SP2/O). Продукты слияния подвергали скринингу на наличие антигена, чтобы выбрать клоны, продуцирующие антитела. Продолжали выращивать эти клоны. Первый скрининг проводили методом ELISA. Положительные клоны помечали как ʺродительские клоныʺ и замораживали после 3 пассажей. На планшеты для ELISA наносили антиген, и затем добавляли супернатант продукта слияния. В качестве положительного контроля в ELISA (пример 2) использовали сыворотку иммунизированных животных.
Пример 2
После слияния мышиных спленоцитов, имеющих лучший титр антитела, с клетками мышиной миеломы проводили анализ ELISA для оценки продуктов слияния. 96-луночный планшет ELISA покрывали антигеном, и в каждую лунку добавляли серийные разведения супернатанта из различных клонов для оценки продуцирования ими антител спектрофотометрическим считыванием. Клоны с наивысшей оптической плотностью при 450 нм (OD450нм) переносили в 24-луночные планшеты, и после их роста повторяли анализ ELISA, клоны с самым высоким продуцированием антител переносили в 6-луночные планшеты, выращивали и снова тестировали методом ELISA. Процедуру повторяли также для клонов, перенесенных в культуральные колбы. Эти последовательные анализы позволили определить лучшие клоны, которые в последний раз были протестированы с помощью ELISA, методом предельного разведения, с целью подтверждения наличия реального антительного ответа у положительных клонов.
Проверенное антитело очищали от надосадочной жидкости клона с самым высоким значением OD450нм и, следовательно, с лучшим титром антител. Это антитело для краткости назвали ʺклон 2D3A8ʺ.
Пример 3
Изучение экспрессии конформационно измененной изоформы белка р53, распознаваемой антителом 2D3A8, у пациентов со спорадической и семейной болезнью Альцгеймера и ЛКН.
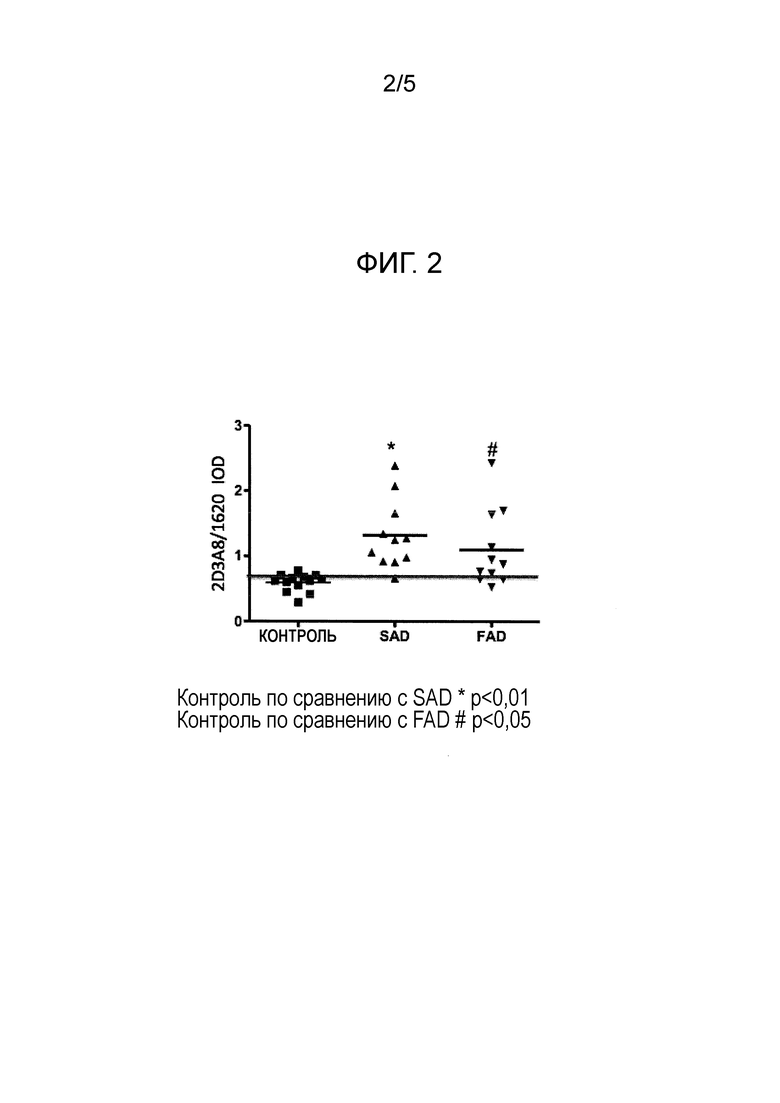
В иммортализованных В-лимфоцитах пациентов, у которых диагностировали спорадическую форму болезни Альцгеймера (SAD) и семейную форму болезни Альцгеймера (FAD), оценивали конформационное состояние р53 методом иммунопреципитации, используя два конформационно специфических антитела, которые распознают изоформу дикого типа белка (PAb 1620) и конформационно измененную изоформу (2D3A8). Затем иммунопреципитат визуализировали Вестерн-блоттингом с помощью поликлонального антитела против р53 (CM1). Экспериментальные данные представлены в виде отношения интенсивности полос, положительных к антителам 2D3A8 и PAb1620 того же образца.
В образцах SAD и FAD отношение 2D3A8/1620 было значительно выше по сравнению с лимфоцитами пациентов, страдающих слабоумием (Фиг. 2).
Следовательно, антитело 2D3A8 может различать конформационно измененную изоформу р53, специфически экспрессируемую в иммортализованных лимфоцитах пациентов со спорадической (SAD) и семейной (FAD) формами болезни Альцгеймером.
Пример 4
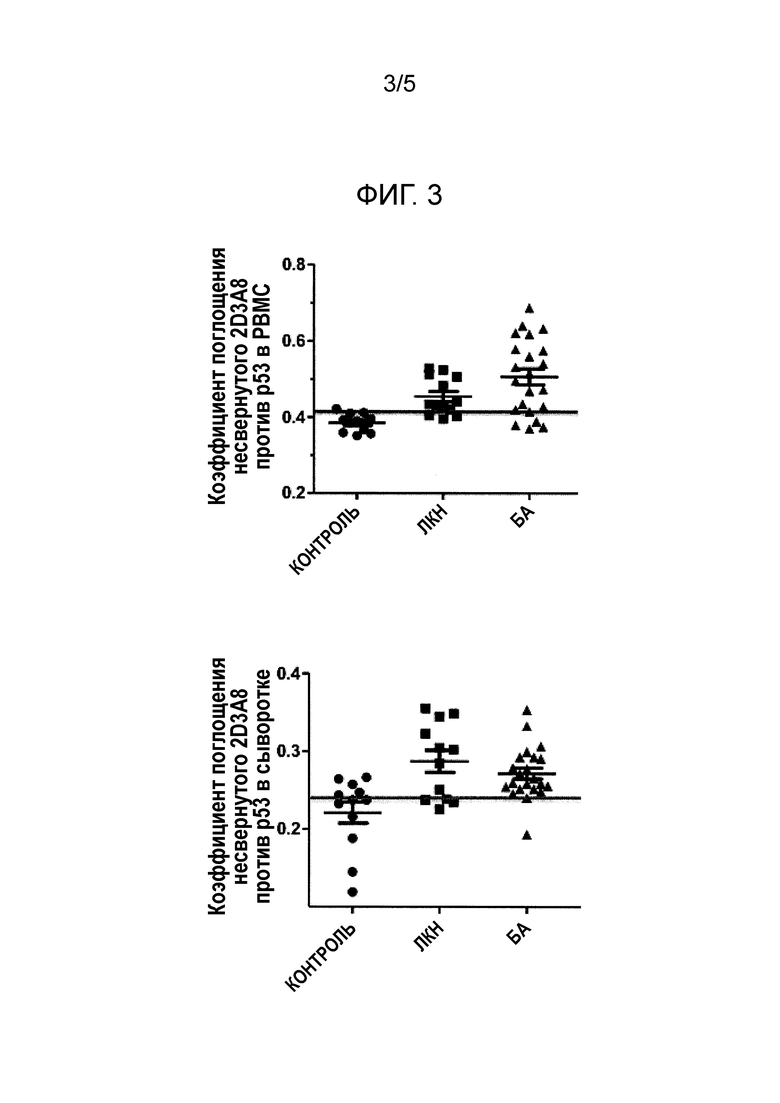
В образцах свежей крови пациентов с диагнозом болезни Альцгеймера и субъектов с легким когнитивным нарушением, диагностированным как ЛКН, методом ELISA оценивали конформационно измененную изоформу р53, распознаваемую антителом 2D3A8 (2D3A8-положительный р53). Также оценивали здоровых субъектов той же возрастной группы без симптомов деменции.
2D3A8-положительный р53 был обнаружен как в клетках крови (РВМС), так и в сыворотке одних и тех же пациентов или субъектов. С помощью антитела 2D3A8 можно с высокой степенью специфичности распознавать пациентов с болезнью Альцгеймера. Следует отметить, что сывороточные уровни 2D3A8-положительного р53, экспрессируемые у субъектов с легкими когнитивными нарушениями, оказались статистически более высокими, чем уровни изоформы белка, присутствующие у контрольных субъектов. В РВМС и сыворотке пациентов с болезнью Альцгеймера уровень 2D3A8-положительной изоформы р53 статистически значимо превышал уровень в контроле (Фиг. 3).
Пример 5
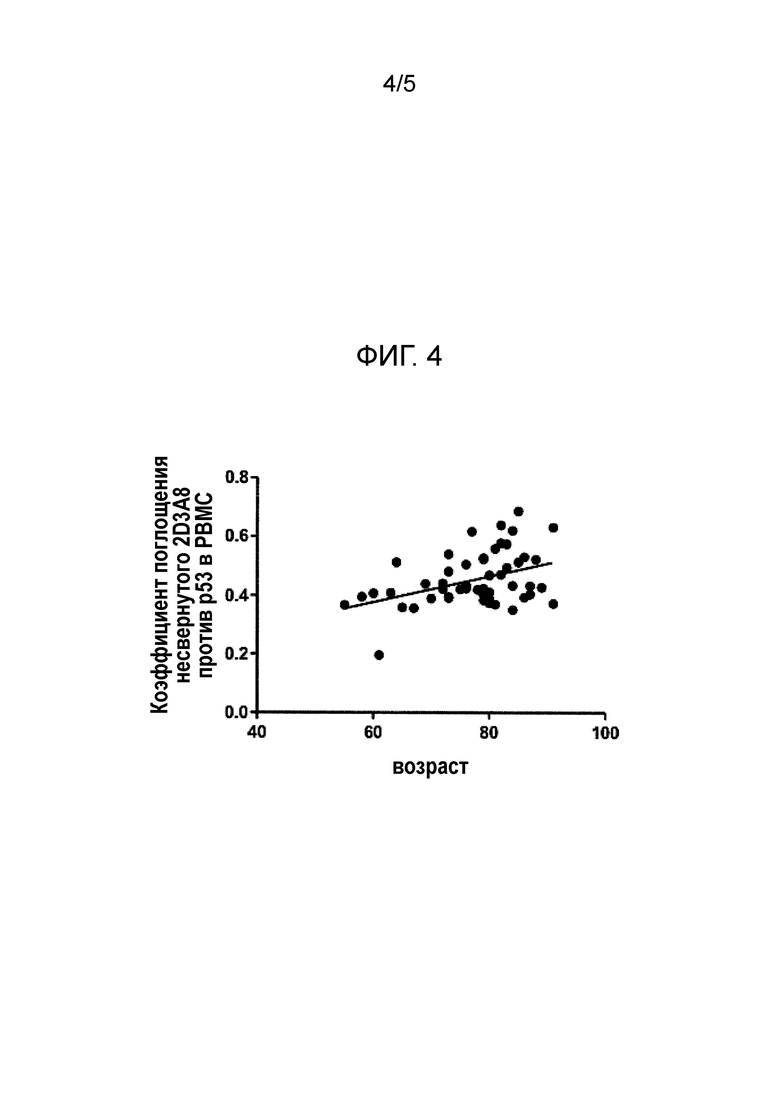
2D3A8-положительная изоформа p53 коррелирует с возрастом.
При старении экспрессия 2D3A8-положительного р53 в клетках крови (РВМС) статистически значимо возрастает (Фиг. 4).
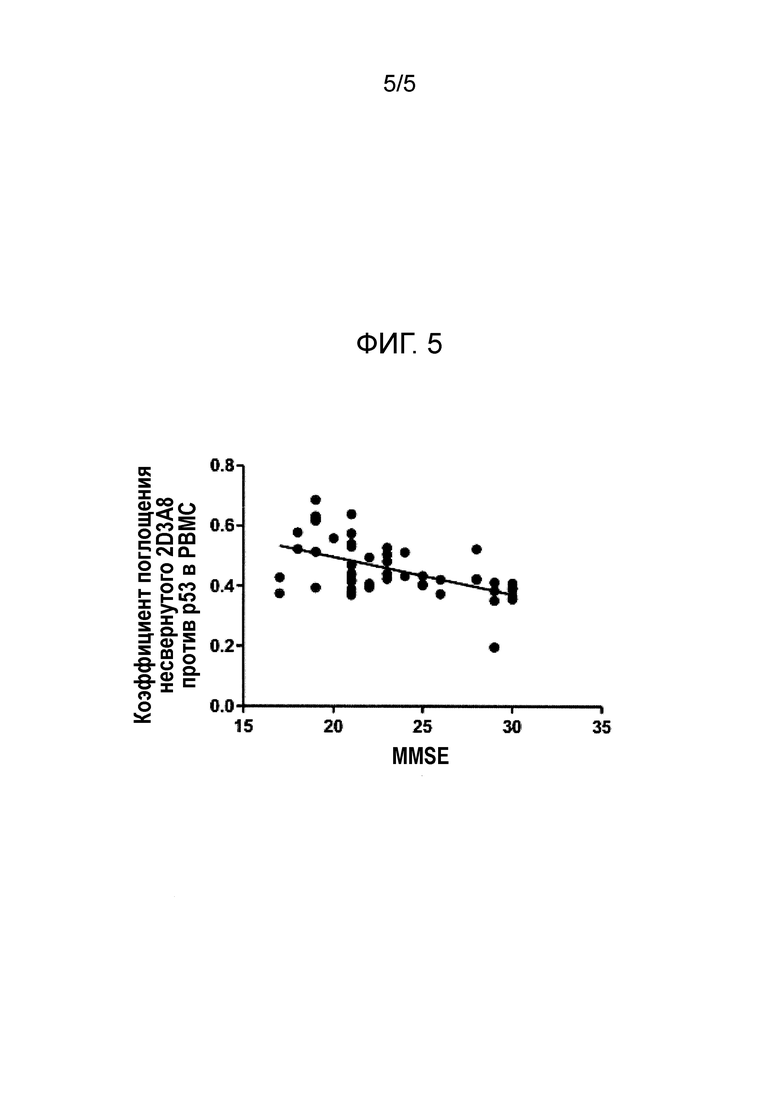
Более того, экспрессия 2D3A8-положительного p53 коррелирует с когнитивным статусом, измеренным с помощью хорошо известного нейропсихологического теста MMSE. Уровень 2D3A8-положительной изоформы p53 увеличивается с уменьшением баллов, полученных в тесте MMSE, т.е. он увеличивается с прогрессированием когнитивных нарушений (Фиг. 5).
| название | год | авторы | номер документа |
|---|---|---|---|
| ИЗОФОРМЫ ТРОПОМИОЗИНА, СВЯЗАННЫЕ С БОЛЕЗНЬЮ АЛЬЦГЕЙМЕРА И УМЕРЕННЫМИ КОГНИТИВНЫМИ НАРУШЕНИЯМИ | 2013 |
|
RU2661022C2 |
| ТЕРАПИЯ И ДИАГНОСТИКА НА ОСНОВЕ БЕЛКОВ ТАУ-ОПОСРЕДУЕМОЙ ПАТОЛОГИИ ПРИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2012 |
|
RU2645259C2 |
| ПЕПТИДЫ, СПОСОБНЫЕ РЕАКТИВИРОВАТЬ МУТАНТЫ Р53 | 2014 |
|
RU2693487C2 |
| МОНОКЛОНАЛЬНОЕ ТЕЛО ПРОТИВ АМИЛОИДА БЕТА | 2008 |
|
RU2571856C2 |
| СПОСОБ IN VITRO-ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА С ПОМОЩЬЮ МОНОКЛОНАЛЬНОГО АНТИТЕЛА | 2006 |
|
RU2416619C2 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ ADDL И ЕГО ПРИМЕНЕНИЯ | 2011 |
|
RU2567808C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2603078C2 |
| ЭПИТОП, СПЕЦИФИЧНЫЙ К ОЛИГОМЕРУ АМИЛОИДА БЕТА, И АНТИТЕЛА | 2011 |
|
RU2644335C2 |
| ПЕПТИДНАЯ ВАКЦИНА ДЛЯ ПРЕДУПРЕЖДЕНИЯ И ИММУНОТЕРАПИИ ДЕМЕНЦИИ АЛЬЦГЕЙМЕРОВСКОГО ТИПА | 2013 |
|
RU2696566C2 |
| АНТИТЕЛА К БЕТА-АМИЛОИДУ | 2013 |
|
RU2651486C2 |

Изобретение относится к области биохимии, в частности к антителу, которое специфично связывается с человеческим белком p53. Также раскрыты способ получения указанного антитела, способ in vitro определения изоформы человеческого белка p53, с которым связывается указанное антитело, способ in vitro диагностики болезни Альцгеймера и способ in vitro определения предрасположенности субъекта, страдающего легким когнитивным нарушением, к развитию болезни Альцгеймера с помощью указанного антитела. Раскрыт набор для иммуноанализа, содержащий указанное антитело. Изобретение позволяет эффективно лечить болезнь Альцгеймера, ассоциированную с белком p53. 7 н. и 3 з.п. ф-лы, 5 пр., 5 ил.
1. Антитело, которое специфично связывается с человеческим белком p53, отличающееся тем, что оно связывается с линейным эпитопом человеческого p53 с последовательностью RRTEEENLRKKGEPHH (SEQ ID NO: 1), где указанное антитело получено посредством иммунизации животного, не являющегося человеком, пептидом с последовательностью SEQ ID NO: 2.
2. Антитело по п.1, представляющее собой моноклональное антитело.
3. Способ получения антитела по любому из пп.1, 2, отличающийся этапами:
(i) иммунизации животного, не являющегося человеком, иммуногеном, содержащим пептид человеческого белка p53 с последовательностью CRTEEENLRKKGEPHH (SEQ ID NO: 2), необязательно конъюгированный с носителем, где носителем предпочтительно является бычий сывороточный альбумин; и
(ii) выделения антитела, полученного при иммунизации.
4. Набор для иммуноанализа, содержащий по меньшей мере антитело по любому из пп.1, 2 и средство для обнаружения связывания указанного антитела с человеческим белком p53.
5. Способ in vitro определения изоформы человеческого белка p53 в образце, полученном от субъекта, причем указанная изоформа обладает обнаженным линейным эпитопом человеческого p53 с последовательностью SEQ ID NO: 1 и конформационно изменена посредством посттрансляционной модификации по отношению к человеческому белку p53 дикого типа, причем способ отличается тем, что образец приводят в контакт с по меньшей мере одним антителом по любому из пп.1, 2 и обнаруживают в образце иммунокомплекс человеческого белка p53 и антитела.
6. Способ in vitro диагностики болезни Альцгеймера у субъекта, отличающийся этапами:
(i) приведения в контакт биологического образца субъекта с по меньшей мере одним антителом против человеческого p53 по любому из пп.1, 2 в условиях, подходящих для образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом; и
(ii) обнаружения образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом,
причем образование иммунокомплекса указывает на болезнь Альцгеймера.
7. Способ in vitro определения предрасположенности субъекта, страдающего легким когнитивным нарушением, к развитию болезни Альцгеймера, отличающийся этапами:
(i) приведения в контакт биологического образца субъекта с по меньшей мере одним антителом против человеческого p53 по любому из пп.1, 2 в условиях, подходящих для образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом; и
(ii) обнаружения образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом,
причем образование иммунокомплекса указывает на предрасположенность к развитию болезни Альцгеймера.
8. Способ in vitro определения предрасположенности субъекта к развитию когнитивной слабости при старении, отличающийся этапами:
(i) приведения в контакт биологического образца субъекта с по меньшей мере одним антителом против человеческого p53 по любому из пп.1, 2 в условиях, подходящих для образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом; и
(ii) обнаружение образования иммунокомплекса между человеческим белком p53 и по меньшей мере одним антителом,
причем образование иммунокомплекса указывает на предрасположенность к развитию когнитивной слабости при старении.
9. Способ in vitro по любому из пп.5-8, в котором биологическим образцом является кровь, плазма, сыворотка, слюна, моча, нейронные клетки, клетки крови или другие типы клеток.
10. Способ in vitro по любому из пп.5-9, в котором обнаружение проводят методом иммунопреципитации, иммуноанализа, предпочтительно ИФА (ELISA) или РИА, или анализом иммунофлюоресценции, Вестерн-блоттингом, FACS-анализом или методами иммуноцитохимии/иммуногистохимии.
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ РАКА | 1996 |
|
RU2174409C2 |
| US 8703734 B2, 22.04.2014 | |||
| US 7833513 B2, 16.11.2010 | |||
| WO 2007123723 A2, 01.11.2007 | |||
| WALTERS D.M | |||
| and et.al., Clinical, Molecular and Genetic Validation of a Murine Orthotopic Xenograft Model of Pancreatic Adenocarcinoma Using Fresh Human Specimens, 2013, PLOS ONE, V.8, pp.1-10. | |||
Авторы
Даты
2021-01-28—Публикация
2015-09-25—Подача