УРОВЕНЬ ТЕХНИКИ
В связи с увеличением продолжительности жизни связанные со слабоумием заболевания становятся в глобальном масштабе основной статьей расходов медицинского характера для медицинских бюджетов и являются стрессом для лиц, осуществляющих уход за страдающими этими заболеваниями пациентами, и для семей пациентов. Болезнь Альцгеймера (AD) представляет собой наиболее распространенную нейродегенеративную патологию, и для поиска способов лечения и улучшенных способов диагностики для скрининга и лечения пациентов постоянно прилагаются усилия. Хотя психометрические тесты, такие как краткая оценка когнитивных функций, как правило, хорошо предсказывают AD, вскрытие остается единственным однозначным способом диагностики болезни Альцгеймера. Потеря памяти является обычным феноменом среди пожилых людей. Если тяжелая потеря памяти является преобладающим симптомом, то это состояние называется умеренным когнитивным нарушением (MCI) и часто рассматривается как очень ранняя стадия AD. На этой стадии лечение может быть более эффективным, чем на более поздней стадии. Скорость перехода пациентов с MCI в клиническую AD составляет 50% в течение 3 лет (Karas et al., 2008). В настоящее время в диагностической медицине все активнее применяют белковые биомаркеры. Идентификация белков биомаркеров AD, особенно тех, которые присутствуют в легкодоступных биологических жидкостях, таких как кровь и моча, представляют желаемую и эффективную альтернативу современным способам диагностики. Тропомиозин представляет собой волокнистую молекулу, которая состоит из двух альфа-спиралей. Он широко распространен во всех типах клеток, где он регулирует сокращение актиновых и миозиновых мышечных филаментов. У млекопитающих дифференциальный сплайсинг четырех высококонсервативных генов может привести к более чем 40 изоформам (Schevzov et al., 2005). Кроме того, каждая изоформа может в различной степени подвергаться посттрансляционным модификациям, в том числе фосфорилированию и гликозилированию. Два наиболее распространенных аналитических метода, используемых в разделении и идентификации белков, представляют собой двухмерный гель-электрофорез (2-D DIGE) и 2D вестерн-блоттинг. В ЕР 2293075 с использованием 2-D DIGE для выявления возможных биомаркеров AD в образцах тромбоцитов были выявлены две изоформы тропомиозина, обозначенные как номер доступа Swissprot/UniProt Р07951 и номер доступа NCBI/Genbank ВАВ14554/AK023385.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает способы и наборы для обнаружения связанных с MCI и AD изоформ тропомиозина, включающих экзон 1а и, необязательно, экзон 9d. В соответствии с первым аспектом изобретение обеспечивает способ для содействия диагностике болезни Альцгеймера (AD) или умеренных когнитивных нарушений (MCI) in vitro, включающий определение уровня экспрессии одной или более изоформ тропомиозина, соответствующих Р09493-3 и/или Р09493-1, в образце от пациента.
В соответствии со вторым аспектом изобретение обеспечивает набор, включающий зонды, которые связывают изоформы тропомиозина Р09493-3 и Р09493-1, где первый зонд связывает общий эпитоп Р09493-3 и Р09493-1, который не включает экзон 1а, и второй зонд специфически связывает экзон 1а.
В соответствии с третьим аспектом изобретение обеспечивает агент, который изменяет уровни концентрации одной или более изоформ тропомиозина Р09493-3 и Р09493-1, для применения в лечении AD или MCI.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 показывает окрашивание рутением антител против экзонов 1а и 9d;
Фиг. 2 показывает оценку методом 2D вестерн-блоттинга антитела против экзона 1а; и
Фиг. 3 показывает оценку методом 2D вестерн-блоттинга антитела против экзона 9d.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если не указано иное, ссылка на экзоны 1а и 9d относится к последовательностям аминокислот, показанным ниже:
экзон 1: -Leu-Asp-Lys-Glu-Asn-Ala-Leu-Asp-Arg-Ala-Glu-Gln-Ala-Glu-Ala-Asp-Lys-Lys-Ala-Ala- (SEQ ID NO: 1)
экзон 9d: -Glu-Lys-Val-Ala-His-Ala-Lys-Glu-Glu-Asn-Leu-Ser-Met-His-Gln-Met-Leu-Asp-Gln-Thr-Leu-Leu-Glu-Leu-Asn-Asn-Met- (SEQ ID NO: 2)
Термины "пациент" и "субъект" в настоящем документе применяются взаимозаменяемо и относятся к любому животному (например, млекопитающему), включая, но не ограничиваясь людьми, приматами, не являющимися людьми, собаками, кошками, грызунами и подобными животными, которые должны быть подвержены диагностике. Предпочтительно, субъект или пациент является человеком. Термины "лекарство" и "агент" в настоящем документе применяются взаимозаменяемо и относятся к химическому или биологическому веществу, которое оказывает эффект на биологическую систему. В настоящем документе термин "изоформы тропомиозина" включает все белки на основе тропомиозина, включая белки, образованные в результате дифференциального сплайсинга генов, и формы с пост-трансляционными модификациями. Три изоформы тропомиозина, соответствующие пятнам 2, 3 и 4 на Фиг. 1, 2 и 3, на основании данных 2D-WB и масс-спектрометрии были соотнесены с номером доступа UniprotKB (UniprotKB; www.uniprot.org/uniprot) Р09493-3; ссылка на Р09493-3 в настоящем документе, таким образом, подразумевает пятна 2, 3 и 4, если не указано иное. Ссылка на Р09493 в настоящем документе подразумевает Р09493-3 (пятна 2, 3 и 4) и Р09493-1; ссылка на Р09493-1 в настоящем документе соответствует описанию в UniprotKB и соответствует пятну 1.
В соответствии с первым аспектом изобретение обеспечивает способ для содействия диагностике умеренных когнитивных нарушений (MCI) и/или болезни Альцгеймера (AD), включающий обнаружение и измерение уровня экспрессии одной или более изоформ, выбранных из Р09493 и/или ее аналогов с пост-трансляционными модификациями, в образце от пациента in vitro. В предпочтительном варианте воплощения, изоформы тропомиозина, которые должны быть обнаружены и измерены, соответствуют одной или более из изоформ Р09493-3 (пятна 2, 3 и 4). В настоящем документе уровень экспрессии или экспрессионный уровень относится к количеству конкретного белка или мРНК, кодирующей белок. Р09493 может быть использован с другими биомаркерами MCI и AD для увеличения диагностических возможностей тестов на AD или MCI. Белки биомаркеры не применяют отдельно от других методов диагностики, и специалисту в данной области техники известно, что при применении Р09493 в диагностике MCI или AD диагностика также будет включать клиническую оценку пациента с применением физических и когнитивных тестов, таких как MMSE, для содействия в классификации пациентов как имеющих AD или MCI. В зависимости от диагностических возможностей биомаркеров, применяемых вместе с Р09493 (оцененных, например, с помощью анализа кривой ROC, по чувствительности и специфичности), возможно, биохимический тест с биомаркерами станет главным диагностическим инструментом для диагностики AD или MCI. Изоформы тропомиозина для обнаружения включают экзон 1а и, необязательно, экзон 9d; изоформы тропомиозина Р09493-3 включают экзоны 1а и 9d, в то время как изоформа тропомиозина Р09493-1 включает экзон 1а, но не экзон 9d. Изоформы тропомиозина для обнаружения и измерения предпочтительно происходят из тромбоцитов из образца крови пациента. Для пациентов с MCI и AD было показано, что концентрация Р09493 значительно увеличена по сравнению с контрольным значением.
Предпочтительно, контрольное значение представляет собой концентрацию Р09493 в образце, предпочтительно образце тромбоцитов, полученном от здорового субъекта. Альтернативно, контроль может представлять собой ссылочное значение. Тромбоциты, которые используют в измерении для потенциальных пациентов с AD и здоровых контролей, предпочтительно получены с помощью способа, описанного в ЕР 1891445, который описывает способ, который приводит к выделению неактивированных тромбоцитов из образца крови. Контрольные данные также могут представлять собой значения для образцов, полученных от пациентов с MCI/AD до наступления MCI/AD. Применение наборов контрольных данных, которые были ранее получены и архивированы, является обычной практикой в таких способах диагностики с биомаркерами. В предпочтительном варианте воплощения увеличение уровня экспрессии одной или более изоформ тропомиозина по сравнению с контрольным значением является показателем AD или MCI. Способ согласно изобретению необязательно может дополнительно включать лечение пациента, у которого была диагностирована AD или MCI (или для которого способ согласно изобретению показал вероятность AD или MCI), агентом, который изменяет уровень концентрации Р09493.
Во втором аспекте изобретение обеспечивает набор, включающий первый зонд, который специфически распознает экзон 1а, и второй зонд, который специфически распознает общий эпитоп Р09493-3 и Р09493-1, который не включает экзон 1а, для применения в диагностике MCI и AD. Для целей диагностики AD или MCI второй зонд может быть специфичным к экзону 9d. Специфичность подразумевает, что в пределах диапазона обнаружения теста зонды по существу обнаруживают только Р09493, т.е. любое связывание зондами белков, отличающихся от Р09493, находится на таком низком уровне, который не влияет на результат диагностики. Зонды предпочтительно представляют собой антитела.
В настоящем документе термин "антитело" относится к иммуноглобулину, который специфически распознает эпитоп на мишени, что определяется характеристиками связывания вариабельных доменов тяжелой и легкой цепей иммуноглобулина (VНS и VLS), более конкретно, их определяющих комплементарность районов (CDRs). В уровне техники известно множество потенциальных форм антител, которые могут включать, без ограничения, множество интактных моноклональных антител или смеси поликлональных антител, включая интактные моноклональные антитела, фрагменты антител (например, фрагменты Fab, 
Третий аспект изобретения направлен на применение агента, который изменяет уровень концентрации Р09493; такое применение относится к лечению для облегчения или подавления симптомов MCI и AD.
Изобретение также обеспечивает способ лечения MCI и/или AD, включающий (i) определение, является ли уровень экспрессии одной или более изоформ тропомиозина, соответствующих Р09493-3 и/или Р09493-1, в образце от пациента увеличенным по сравнению с контролем; и (ii) введение агента, который изменяет уровень концентрации Р09493.
Содержание всех публикаций, цитированных в настоящем документе, включено в настоящий документ посредством ссылки.
Изобретение проиллюстрировано со ссылкой на прилагаемые чертежис помощью следующих неограничивающих примеров.
ПРИМЕРЫ
Способы
Популяция для исследования
Пациенты с болезнью Альцгеймера: в исследование были включены сорок семь пациентов с AD. Набор нейрофизиологических тестов CERAD (Консорциум для разработки регистра болезни Альцгеймера) проводили в день взятия образцов крови. Никто из пациентов не подвергался лечению препаратами против AD, например ингибиторами ацетилхолинэстеразы или мемантином. Более того, пациенты с деменцией не получали систематическое хроническое лечение антипсихотическими лекарствами, которое могло повлиять на экспрессию Мао-В. Чтобы исключить другие причины когнитивных нарушений (например, инсульт или опухоль), все пациенты прошли структурную визуализацию сканированием мозга (магнитно-резонансная томография), за исключением двух пациентов, которые вместо этого подверглись компьютерной томографии (клаустрофобия, металлический имплантат). На основе критериев CERAD (http://cerad.mc.duke.edu/Assesment.htm/), например истории болезни, визуализации мозга и набора нейрофизиологических тестов CERAD, были поставлены следующие диагнозы: 47 AD (9 подтверждены аутопсией). Посмертное невропатологическое обследование проводили всего для 13 пациентов. Пациенты умерли через 10-18 месяцев после отбора образцов крови. Для 9 из 47 пациентов с клиническим подозрением на AD клинический диагноз был подтвержден невропатологическим обследованием и у четырех из 13 пациентов сосудистая деменция (VD) соответствовала невропатологическим критериям для деменции смешанного типа (AD и VD). Невропатологическое обследование в соответствии со стандартным протоколом включало окрашивание гематоксилином/эозином, модифицированную импрегнацию по Бильшовскому и иммуногистохимический анализ на белок тау (антитело АТ-8, Innogenetics, Ghent, Belgium), β-амилоид (клон 4G8, Signet Labs, Dedham, MA) и альфа-синуклеин (моноклональные и поликлональные антитела, Chemicon, Temecula, СА). Невропатологический диагноз ставили в соответствии с признанным патологоанатомическим единым критерием для AD, включающим шкалу CERAD. Образцы от пациентов с AD продемонстрировали невропатологическую картину CERAD С и стадий по Braak V/VI, что соответствовало высокой вероятности AD в соответствии с критерием «деменции» института NIA-Reagan. Контроли: соответствующая по полу и возрасту группе с AD контрольная группа из 49 субъектов без признаков нейродегенеративного заболевания или когнитивных нарушений. Всех субъектов опрашивали, и опытные психологи проводили их нейропсихологическое обследование (MMSE). Все индивидуумы, включенные в исследование, были некурящими. Умеренные когнитивные нарушения определяли в соответствии с Petersen et al. (1999 & 2004).
Этические аспекты исследования
Методика исследования была одобрена местной комиссией по вопросам этики, и исследование проводили в соответствии с принципами Хельсинкской декларации в редакции 2000 г. От каждого субъекта или от его представителя после объяснения целей и процедуры исследования было получено информированное согласие.
Получение образцов
Кровь собирали без стаза из латеральной подкожной вены руки в вакуумные пробирки (Greiner Bio-One GmbH, Kremsmunster, Austria), содержащие 0,129 моль/л цитрата натрия в качестве антикоагулянта (соотношение для смешивания с кровью 1: 9). Первую пробирку с собранной кровью отбраковывали, чтобы исключить какое-либо загрязнение тканью при венепункции. Дифференциальную гемограмму измеряли с использованием анализатора крови MicroDiff 18 (Coulter Electronics, Miami, FL, USA). Выделение тромбоцитов и выделение белка проводили, как описано ранее [31]. Кратко, осадок растворяли в денатурирующем буфере для образцов 2-D, содержащем 7 М мочевину, 2 М тиомочевину, 4% CHAPS, 20 мМ Трис-HCl (pH 8,5) при встряхивании в течение ночи при 4°C. На 100×106 тромбоцитов использовали семьдесят микролитров буфера для образцов. Концентрацию белка в растворенных образцах определяли в трех повторах с помощью набора для анализа белка с кумасси бриллиантовым голубым с BSA в качестве стандартного белка (Pierce Biotechnology, Rockford, IL, USA). При соответствующем разбавлении компоненты буфера для образцов 2-D не мешают анализу белка. Таким образом, образцы разбавляли 1:20 в PBS и 5% буфера для образцов 2-D добавляли к стандартам BSA. Внутренние стандарты для анализа 2D DIGE получали, отбирая то же количество общего белка от каждого из образцов для исследования. Аликвоты внутреннего стандарта и индивидуальные образцы для исследования хранили при -80°C. Мечение белка флуоресцентным цианиновым красителем (CyDyes, GE Healthcare, Uppsala, Sweden) проводили до электрофореза в соответствии с инструкциями производителя с минимальными изменениями. Соотношение CyDye к белку было уменьшено до 5 пмоль красителя на мкг белка. Внутренний стандарт метили Су2, а образцы метили альтернативно Су3 или Су5. Для ПЦР с обратной транскрипцией в реальном времени (qRT-PCR) общую РНК экстрагировали из подвергнутых гель-фильтрации тромбоцитов, как описано ранее.
Электрофорез 2D DIGE и анализ изображения геля
Электрофорез и обработку изображения геля проводили, как описано ранее. Кратко, 24 см pH 4-7 9 IPG-Drystrips пассивно регидратировали в модифицированном растворе для регидратации (7 М мочевина, 2 М тиомочевина, 4% CHAPS, 70 мМ DTT и 0,5% амфолитов с pH 4-7), включающем меченный красителем образец. Затем с помощью пассивной регидратации было нанесено 25 мкг меченного красителем белка. Изоэлектрофокусирование проводили до достижения 30 киловольт-часов. Во втором направлении проводили 11,5% SDS-PAGE (35 В в течение 1 ч, 50 В в течение 1,5 ч и, наконец, ПО В в течение 16,5 ч при 10°C), и гели сканировали при разрешении 100 мкм с помощью сканера Typhoon 9410 (GE Healthcare, Uppsala, Sweden). Обнаружение пятен на изображениях гелей проводили с помощью модуля Differential In-gel Analysis программного обеспечения DeCyder (версия 6.00.28; GE Healthcare, Uppsala, Sweden), устанавливая количество пятен 2500. Каждый гель добавляли в соответствующую рабочую среду и группу и выравнивали с эталонным гелем с помощью модуля Biological Variation Analysis программного обеспечения DeCyder (версия 6.01.02). Процедура анализа изображения геля описана в подробностях ранее.
Идентификация белков
Белки идентифицировали с помощью масс-спектрометрии. Получение гидролизатов белка трипсином для последующих стадий проводили, как описано ранее. Пептиды наносили на колонку Zorbax 300SB-C8 (5 мкм, 0,3 мм×5 мм) и разделяли с помощью нанопроточной жидкостной хроматографии (система 1100 Series LC, Agilent, Palo Alto, CA) на колонке Zorbax 300SB-C18 (5 мкм, 75 мкм×150 мм) при скорости потока 250 нл/мин с помощью градиента от 0,2% муравьиной кислоты и 3% ацетонитрила до 0,2% муравьиной кислоты и 45% ацетонитрила в течение 12 мин. Идентификацию пептидов проводили методом тандемной масс-спектрометрии с фрагментацией (MS/MS) с масс-спектрометром ионной ловушкой (ХСТ - Plus, Agilent), оснащенным ортогональным источником ионов с нанораспылением. Данные MS/MS интерпретировали с помощью программного обеспечения Spectrum Mill MS Proteomics Workbench (версия A.03.03, Agilent), поиск проводили в базе данных SwissProt для белков человека (версия 14.3, включающая 20328 записей), устанавливая для предшественника отклонение массы 1,5 Да, допустимое отклонение массы продукта 0,7 Да и минимальную интенсивность совпавших пиков (% SPI) 70%, и одно пропущенное расщепление. Из-за предшествующей химической модификации карбамидометилирование цистеинов установили в качестве постоянной модификации. Уровень ложноположительных результатов для пептидов с оценкой более 13 составлял менее 1%, что давало достоверность более 99,9% для белков, которые идентифицировали по двум или более пептидам с оценкой более 13.
Получение антител
Овец ежемесячно иммунизировали пептидами с последовательностями, соответствующими H-Cys-Leu-Asp-Lys-Glu-Asn-Ala-Leu-Asp-Arg-Ala-Glu-Gln-Ala-Glu-Ala-Asp-Lys-Lys-Ala-Ala-NH2 и H-Cys-Glu-Lys-Val-Ala-His-Ala-Lys-Glu-Glu-Asn-Leu-Ser-Met-His-Gln-Met-Leu-Asp-Gln-Thr-Leu-Leu-Glu-Leu-Asn-Asn-Met-OH, конъюгированными с бычьим сывороточным альбумином (BSA) через N-концевые остатки цистеина. Полученные иммуногены ежемесячно вводили взрослым овцам для получения поликлональных антител. Затем были выделены лимфоциты, которые сливали с клетками гетеромиеломы. Супернатанты из полученных гибридом скринировали на присутствие специфичных к экзонам антител с применением основанных на ELISA анализах, в которых планшеты для микротитрования были покрыты полноразмерным белком. Положительные гибридомы клонировали для получения стабильных линий. Антитела, вырабатываемые полученными моноклональными гибридомами, очищали, характеризовали методом одномерного и двумерного вестерн-блоттинга (ID и 2D WB) и применяли для разработки сэндвич-иммуноанализа на биочипах. Анализ применяли в анализаторе Evidence Investigator, который использует технологию микроматричных биочипов на основе принципов иммуноанализа ELISA (Fitzgerald et al., 2005).
Анализ методом двумерного вестерн-блоттинга
Для анализа методом 2D вестерн-блоттинга 30 мкг осажденного ТС А и растворенного в мочевине/тиомочевине/CHAPS белка тромбоцитов разделяли в первом направлении с помощью IEF на 24 см IPG полоске с pH 4-7 (GE Healthcare). Разделение во втором направлении проводили методом SDS PAGE в геле 13×16 см, и разделенные белки переносили на нитроцеллюлозную мембрану (Pall, East Hills, NY). Весь белок на мембране окрашивали с помощью флуоресцентного красителя на основе рутений-(II)-трис-(батофенантролин дисульфоната) (RuBPS). Затем мембрану блокировали 5% раствором обезжиренного сухого молока в PBS, содержащим 0,3% Tween-20 (PBS-T), в течение 2 часов. Связанные с AD изоформы тропомиозина обнаруживали, инкубируя мембрану: а) для обнаружения анти-1а экзона применяли HRP-меченное антитело анти-1а экзон (1/1000), инкубация в течение 1 ч, обнаружение с помощью Luminol PLUS/пероксид, экспозиция 10 с; b) для обнаружения анти-9 с1 экзона применяли HRP-меченное антитело анти-9d экзон (1/1000), инкубация в течение 1 ч, обнаружение с помощью Luminol PLUS/ пероксид, экспозиция 30 с - 1 мин.
Результаты
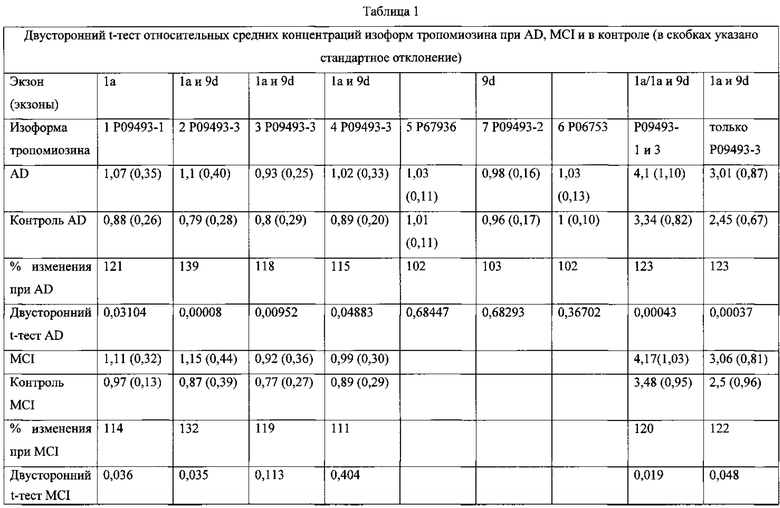
Специфичное к экзону 9d антитело для захвата выбирали для иммобилизации на поверхности биочипа, и специфичное к экзону 1а обнаруживающее антитело конъюгировали с пероксидазой хрена для получения трейсера для анализа. Разработанный с использованием этих иммунореагентов иммуноанализ на биочипе имел специфичность к трем из четырех связанных с AD и MCI изоформ тропомиозина Р09493. Анализы методом ID и 2D вестерн-блоттинга подтвердили, что антитела, полученные к экзонам 1а и 9d, связывают пятна 2, 3 и 4 (Фиг. 1). Также было показано, что каждая из изоформ тропомиозина, уровень которых был повышен в образцах AD и MCI, включала экзон 1а. Уровень четырех других изоформ тропомиозина, определенных методом масс-спектрометрии, соответствующих пятнам 5, 6, 7 и 8 (Фиг. 1), которые не включали экзон 1а, не был повышен в образцах AD и MCI. Чувствительность анализа составляла <10 нг/мл (диапазон измерения 0-700 нг/мл), и точность в пределах одного измерения составляла <10% для стандартных концентраций. При используемых экспериментальных условиях пятно 1 имело pI=4,5 и MW=~37 кДа, пятно 2 имело pI=4,5 и MW=~37 кДа, пятно 3 имело pI=4,6 и MW=~35 кДа, и пятно 4 имело pI=4,56 и MW=-~33 кДа. В выделенных из крови тромбоцитах были обнаружены уровни до 12 мкг/мл. Таблица 1 (строка % изменения) подтверждает, что уровни изоформ тропомиозина Р09493, соответствующие пятнам 1, 2, 3 и 4, отдельно и в комбинации, повышены у пациентов с AD и MCI по сравнению с контролем. t-Тест подтвердил, что пятно 2 и комбинация всех четырех пятен значительно повышены у пациентов с AD и MCI по сравнению с контролем (P<0,05). Результаты этого исследование указывают, что обнаружение и измерение в образце от пациента с подозрением на AD или MCI повышения уровня изоформ тропомиозина Р09493-3 и Р09493-1 in vitro предсказывают AD и MCI.
Ссылки
Karas et al. (2008). Am. J. Neuroradiol, 29 (5): 944-949
Schevzov G. et al. (2005). J. Histochem. Cytochem., 53 (5): 557-570
Fitzgerald et al. (2005). Clin. Chem., 51 (7): 1165-1176
Petersen et al. (1999). Arch. Neurol, 56 (3): 303-308
Petersen et al. (2004). J. Intern. Med. 256 (3): 183-194.
| название | год | авторы | номер документа |
|---|---|---|---|
| Лактоферрин, используемый при диагностике или прогнозировании болезни Альцгеймера или диагностике болезни Паркинсона | 2016 |
|
RU2745602C2 |
| Новый биомаркер для диагностики болезни Альцгеймера, обнаруженный в полученных из крови экзосомах, и способ диагностики болезни Альцгеймера с его использованием | 2021 |
|
RU2826381C1 |
| АНТИТЕЛО, КОТОРОЕ РАСПОЗНАЕТ ПЕПТИД Т14 АСНЕ | 2016 |
|
RU2729491C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2015 |
|
RU2720468C2 |
| Способ оценки риска развития болезни Альцгеймера с использованием панели белков крови | 2021 |
|
RU2794040C1 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ГИПЕРФОСФОРИЛИРОВАННОМУ ТАУ-БЕЛКУ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2727911C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К ГИПЕРФОСФОРИЛИРОВАННОМУ ТАУ-БЕЛКУ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2760875C1 |
| ГУМАНИЗИРОВАННОЕ МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ Aβ и ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2783528C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АПОЛИПОПРОТЕИНА Е4 | 2017 |
|
RU2779197C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛО ПРОТИВ ПРОТОФИБРИЛЛ АБЕТА И ИНГИБИТОР БЕТА-СЕКРЕТАЗЫ ВАСЕ1 ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2017 |
|
RU2786476C2 |



Изобретение относится к способу обнаружения пациентов с подозрением на болезнь Альцгеймера (AD) или умеренные когнитивные нарушения (MCI) in vitro, включающему сравнение уровня экспрессии изоформы тропомиозина Р09493-3 в образце от пациента с контрольным значением, где увеличение уровня экспрессии Р09493-3 является показателем AD или MCI. 2 н. и 4 з.п. ф-лы, 3 ил., 1 табл.
1. Способ обнаружения пациентов с подозрением на болезнь Альцгеймера (AD) или умеренные когнитивные нарушения (MCI) in vitro, включающий сравнение уровня экспрессии изоформы тропомиозина Р09493-3 в образце от пациента с контрольным значением, где увеличение уровня экспрессии Р09493-3 является показателем AD или MCI.
2. Способ по п. 1, где способ дополнительно содержит определение уровня экспрессии изоформы тропомиозина Р09493-1 в образце.
3. Способ по п. 1 или 2, где увеличение уровня экспрессии одной или более изоформ тропомиозина по сравнению с контрольным значением является показателем AD или MCI.
4. Способ по п. 1 или 2, где образец от пациента представляет собой образец крови, сыворотки, плазмы или тромбоцитов.
5. Набор для обнаружения пациентов с подозрением на болезнь Альцгеймера (AD) или умеренные когнитивные нарушения (MCI), включающий зонды, которые связывают изоформу тропомиозина Р09493-3, где первый зонд специфически связывает экзон 9d, и второй зонд специфически связывает экзон 1а.
6. Набор по п. 5, где зонды представляют собой антитела.
| WO 2011067610 A1, 09.06.2011 | |||
| WO 2004113568 A3, 29.12.2004 | |||
| WO 2012053255 A1, 26.04.2012 | |||
| WO 2005050219 A1, 02.06.2005 | |||
| WO 2007149798 A3, 27.12.2007. |
Авторы
Даты
2018-07-11—Публикация
2013-07-08—Подача