ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Для настоящей заявки испрашивается приоритет предварительной заявки США №61/310,167, поданной 3 марта 2010, которая целиком включена в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к новым конформационным эпитопам олигомеров Абета, к композициям антител, имеющих отношение к указанным эпитопам, и способам их применения.
УРОВЕНЬ ТЕХНИКИ
Болезнь Альцгеймера (БА) - распространенное нейродегенеративное заболевание (сопровождающееся нарушениями памяти и познания), ассоциированное с накоплением в мозге внеклеточных бляшек, состоящих преимущественно из пептидов Абета (1-40), Aβ (1-42) и Aβ (1-43) (также обозначаемых как амилоид β или Aβ), которые являются протеолитическими продуктами амилоидного белка-предшественника (APP). К тому же, в внутри клеток гибнущих нейронов образуются нейрофибриллярные узлы, состоящие преимущественно из аномально фосфорилированного тау белка (белка нейронов, ассоциированного с микротрубочками). Aβ (1-41) является доминирующим видом в амилоидных бляшках больных БА.
Наследственные формы БА могут быть вызваны мутациями в гене АРР или в генах пресенилина 1 или 2, белковые продукты которых включены в процессинг APP до Aβ. Аллельные варианты аполипопротеина E также влияют на возраст возникновения обеих форм БА - спорадической и наследственной. Совсем недавно было выяснено, что отдельные молекулярные разновидности Aβ, в которых пептид представлен в виде олигомера, опосредуют основной компонент нейротоксичности, наблюдающейся при БА и в моделях болезни на мышах (Walsh et al. 2002). Токсичность олигомера Аβ может проявляться в дисфункции нейронных рецепторов инсулина (Zhao et al. 2008) и в препятствовании нормальной синаптической функции, в частности, в гиппокампе, путем эктопической активации глутаматэргических рецепторов (De Felice et al. 2007; Nimmrich et al. 2008). Сообщалось о наномолярной аффинности связывания при взаимодействии между олигомерами Aβ и нормальной клеточной изоформой белка-приона PrPC (Lauren et al. 2009). Более того, взаимодействие между PrPC и различными токсичными сигнальными путями (Solforosi et al. Lefebvre-Roque et al. 2007), включая субъединицы рецептора глутамата (Khosravani et al. 2008), может приводить к объединенному механизму токсичности олигомеров Аβ.
Хорошо известно, что иммунное распознавание Aβ может приводить как к развитию патологии, так и к улучшению поведения трансгенных мышей, экспрессирующих человеческий мутантный амилоидный белок-предшественник. Однако существует опасность, присущая лечению людей «неселективной» иммунотерапией Aβ. Например, у примерно 10% пациентов, получающих вакцину против болезни Альцгеймера, содержащую неселективный иммуноген Aβ, возникает аутоиммунный менингоэнцефалит (Gelinas et al. 2004; Robinson et al. 2004; Broytman and Malter 2004; Mathews and Nixon 2003). И хотя в итоге менингоэнцефалопатия возникала, очевидно, в связи с клеточной иммунной активацией по отношению к Aβ, также было показано, что пассивно введенные при инфузии моноклональные антитела против Aβ (МАТ), обособленные от клеточного иммунного ответа, ассоциировались с микрокровоизлияниями в мозге (Goni and Sigurdsson 2005). Другой риск неселективной иммунизации Aβ - это иммунное распознавание родительских белков APP, экспонированных на поверхности нейронов мозга и циркулирующих моноцитов (Jung et al. 1996; Jung et al. 1990). Такое распознавание мембранной молекулы клеточной поверхности может спровоцировать лизис или помешать функционированию внеклеточного домена белка APP, включая трофическую активность (Morimoto et al. 1998; Mileusnic et al. 2005; Mileusnic et al. 2005).
Другая проблема с «неспецифическим» распознаванием пептида Aβ состоит в том, что пептид Аβ является единственным предшественником токсичных молекулярных разновидностей Aβ - олигомеров Aβ. Было показано, что олигомеры Aβ способны вызывать гибель клеточных линий и нейронов в культуре (Lambert et al.2007; Lacor et al. 2007; Ronicke et al. 2008) Balducci et al. 2012; Shankar et al. 2008; Selcoe 2008; Klyubin et al. 2005; Walsh et al. 2002; Wamg et al. 2002). Специфические олигомеры Aβ были идентифицированы как пептиды, которые коррелируют с началом нарушений памяти у мышей и которые после очистки и введения нормальным молодым крысам вызывают негативные поведенческие нарушения, наблюдаемые у мышей (Lesne et al. 2006). Похожие исследования показали, что PrPC может выступать в качестве рецептора для олигомеров Aβ и может преобразовывать их токсичные эффекты в синаптические нарушения LTP (Lauren et al. 2009).
Хотя в прошлом были созданы вакцины Aβ и моноклональные антитела против пептидов Aβ, ни для одного из них к настоящему времени не доказано, что с их использованием достигается желаемый терапевтический эффект без дополнительного возникновения серьезных побочных эффектов у животных и/или людей. Существует терапевтическая необходимость в разработке биологических препаратов, которые бы блокировали или замедляли развитие заболевания и не оказывали негативные и потенциально летальные воздействия на организм человека. Эта необходимость особенно очевидна ввиду роста общей продолжительности жизни популяции и роста числа пациентов, у которого ежегодно диагностируется болезнь Альцгеймера. Было бы желательно идентифицировать иммунологические эпитопы, являющиеся болезнь-специфическими эпитопами (БСЭ), и разработать иммунотерапию, специфически нацеленную на токсичные олигомерные молекулярные разновидности Aβ. Также желательно разработать иммунотерапию, нацеленную на токсичные олигомерные молекулярные разновидности Aβ, и избежать аутоиммунного распознавания APP на поверхности клеток. Такие БСЭ-эпитопы могут стать целями для иммунотерапии и профилактических вакцин, специфически нейтрализующих токсичность белков-мишеней. Также желательно разработать диагностические инструменты, обеспечивающие идентификацию населения с риском развития БА для дифференциальной диагностики и возможности отличить БА от других синдромов слабоумия и для мониторинга ответа биологических маркеров на терапию БА.
Также желательно предоставить болезнь-специфический эпитоп, уникальный для токсической олигомерной молекулярной разновидности Aβ.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Целью настоящего изобретения является устранение либо минимизация, по крайней мере, одного недостатка предшествующих эпитопов, антител, композиций и методов диагностики, лечения и профилактики болезни Альцгеймера.
В первом аспекте настоящее изобретение частично основано на неожиданном открытии нового структурного эпитопа в Aβ с полезными свойствами для селективного присоединения антител.
В одном из вариантов реализации настоящего изобретения предоставляется циклический пептид, полученный из Aβ и содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ.
В другом варианте реализации настоящего изобретения предоставляется антигенный пептид, содержащий эпитоп, который содержит конформационно напряженную циклическую конфигурацию, эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ.
В другом варианте реализации настоящего изобретения предоставляется антигенный пептид, содержащий эпитоп, который содержит конформационно напряженную циклическую конфигурацию, эпитоп, содержащий аминокислотную последовательность, соответствующую последовательности SEQ ID NO: 1, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ.
В одном аспекте эпитоп антигенного пептида соответствует остаткам с 25 по 29 олигомерного Аβ (1-40) или олигомерного Aβ (1-42).
В другом варианте реализации настоящего изобретения предоставляется изолированное антитело, которое специфично связывается с циклическим пептидом - производным Aβ, циклическим пептидом, содержащим конформационный эпитоп, имеющий аминокислотную последовательность, по крайней мере, SNK, соответствующую гидрофильному и доступному антителам шарнирному участку олигомерного Aβ.
В еще одном варианте реализации настоящего изобретения оно представляет собой изолированное антитело, которое специфично связывается с циклическим пептидом, полученным из Aβ, циклическим пептидом, содержащим конформационный эпитоп, содержащий аминокислотную последовательность, соответствующую последовательности SEQ ID NO: 1, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ.
В одном аспекте изолированное антитело специфически связывается с большей аффинностью с олигомерными формам Aβ и, чем с не олигомерными формами Aβ.
В еще одном аспекте изолированное антитело является моноклональным.
В еще одном аспекте изолированное антитело является гуманизированным.
В другом варианте реализации настоящего изобретения предоставляется иммуноконъюгат, содержащий изолированное антитело, которое специфически связывается с циклическим пептидом, полученным из Аβ, содержащим конформационный эпитоп, содержащим, по крайней мере, аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ, конъюгированное с детектируемой меткой.
В другом аспекте предоставляется нуклеиновая кислота, кодирующая изолированное антитело.
В еще одном варианте реализации настоящего изобретения предоставляется композиция, содержащая терапевтически эффективное количество изолированных антител, которые специфически связываются с циклическим пептидом, полученным из Aβ, циклическим пептидом, содержащим конформационный эпитоп, содержащий по крайней мере, аминокислотную последовательность SNK, соответствующую экспоинрованному в раствор и доступному для антител шарнирному участку олигомерного Aβ; и фармацевтически приемлемый адъювант.
В другом варианте реализации настоящего изобретения предоставляется антиолигомерная вакцинная композиция, содержащая антигенный пептид, который содержит эпитоп, содержащий конформационно напряженную циклическую конфигурацию, эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ; и фармацевтически приемлемый адъювант.
В еще одном аспекте предоставляется способ лечения либо профилактики болезни Альцгеймера у пациентов, нуждающихся в вышеупомянутом лечении, включающем введение фармацевтически эффективного количества изолированного антитела или иммуноконъюгата.
В еще одном аспекте предоставляется способ лечения и профилактики болезни Альцгеймера у пациентов, нуждающихся в вышеупомянутом лечении, включающий введение вакцины.
В еще одном аспекте предоставляется способ диагностики болезни Альцгеймера у пациентов с подозрением на болезнь Альцгеймера, включающий следующие стадии: а) получение биологического образца у пациента; б) контакт биологического образца с изолированным антителом на протяжении времени и при условиях, достаточных для формирования комплексов антиген-антитело в образце и в) определение наличия комплекса антиген-антитело в образце, где наличие комплекса означает диагностирование болезни Альцгеймера у пациента.
В еще одном варианте реализации настоящего изобретения предоставляется набор, состоящий из изолированного антитела и конъюгата, содержащего антиген, связанный с соединением, генерирующим сигнал.
В другом аспекте набор включает один детектирующий агент или более.
В другом варианте реализации настоящего изобретения предоставляется продукт производства, включающий: изолированное антитело, конъюгат, содержащий антиген, связанный с соединением, генерирующим сигнал, и инструкцию по применению для диагностики болезни Альцгеймера.
В еще одном аспекте предоставляется применение антитела или иммуноконъюгата для лечения и профилактики болезни Альцгеймера.
В еще одном аспекте предоставляется использование вакцины для лечения и профилактики болезни Альцгеймера.
В другом варианте реализации предоставляются изолированные антитела, способные связываться с циклическим пептидом, полученным из Aβ, содержащим аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ. В отдельном аспекте данне антитела связывают олигомерные формы Aβ с большей аффинностью, чем не олигомерные формы Aβ.
В еще одном варианте реализации настоящего изобретения предоставляется способ профилактики развития или прогрессирования БА у объекта, способ, включающий введение объекту терапевтически эффективного количества антигенного пептида, который содержит эпитоп, содержащий конформационо напряженную циклическую конфигурацию, содержащую аминокислотную последовательность SNK, соответствующую экспонированному в раствор и доступному для антител шарнирному участку олигомерного Aβ. При введении антигенный пептид вызывает иммунную реакцию против олигомерного Aβ. Вырабатываемые антитела способны специфически связываться с олигомерным Aβ. В определенных вариантах реализации данные антитела связывают олигомерные формы Aβ с большей аффинностью, чем не олигомерные формы Aβ.
Другие аспекты и черты настоящего изобретения будут очевидны для специалиста в данной области из нижеследующего описания частных вариантов реализации с сопроводительными иллюстрациями.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Варианты реализации настоящего изобретения будут описаны с использованием примеров, со ссылками на прилагаемые Фигуры.
Фиг.1 графически иллюстрирует результаты динамического рассеяния света, демонстрирующие динамические свойства мономерного Aβ.
Фиг.2 графически иллюстрирует результаты динамического рассеяния света, демонстрирующие динамические свойства олигомерного Aβ.
Фиг.3 графически иллюстрирует результаты динамического рассеяния света, демонстрирующие динамические свойства олигомерного Aβ.
Фиг.4 представляет собой трехмерную модель дисульфид-циклизованного пептида, содержащего эпитоп SNK.
Фиг.5 графически иллюстрирует результаты типичного аналитического цикла Biacore™ для скрининга анти-SNK моноклональных антител, связывающихся с конформационным пептидом, содержащим SNK.
Фиг.6 графически иллюстрирует сенсограмму наложения Biacore™, которая демонстрирует связывание конъюгированных с БСА линейных или циклических пептидов, содержащих эпитоп SNK, со специфичными к линейным формам (3F5, 3G2), специфичными к циклическим формам (5E3, 5D8) и специфичными к промежуточным формам (4D11, 4D12) моноклональными антителами и способность этих антител к связыванию с синтетическими олигомерами Aβ 1-42.
Фиг.7 графически иллюстрирует сенсограмму наложения Biacore™, которая демонстрирует связывание конъюгированных с БСА линейных или циклических пептидов, содержащих эпитоп SNK, со специфичными к линейным формам (3F5, 3G2), специфичными к циклическим формам (5E3, 5D8) и специфичными к промежуточным формам (4D11, 4D12) моноклональными антителами и способность этих антител к связыванию с синтетическими олигомерами Aβ 1-42.
Фиг.8 графически иллюстрирует результаты анализа Biacore™, которые демонстрируют связывание синтетических олигомеров Aβ 1-42 с моноклональным антителом 5E3, специфичным к циклическим формам, при разных концентрациях.
Фиг.9 представляет собой результат проточной цитометрии, который демонстрирует сравнительный анализ связывания с клетками меченных антител 6E10 и негативного контроля с белком APP, расположенным на поверхности клеток.
Фиг.10 представляет собой результат проточной цитометрии, который демонстрирует сравнительный анализ связывания с клетками меченных антител 5E3 и негативного контроля с белком APP, расположенным на поверхности клеток.
Фиг.11 графически иллюстрирует результаты анализа нейрональной токсичности, которые демонстрируют степень выживаемости клеток, инкубированных с холостым контролем, растворимыми мономерным и олигомерным Aβ 1-40 в присутствии и в отсутствие антител 5E3 в разных концентрациях.
Фиг.12 иллюстрирует результаты иммуноблотинга, которые демонстрируют гомогенизированные в солевом трис-буферном растворе (TBS) ткани мозга, фракционированные в трис-трициновых гелях, и проанализированные методом иммуноблотинга с пан-Aβ антителами 6E10.
Фиг.13 иллюстрирует результаты иммуноблотинга, которые демонстрируют гомогенизированные в солевом трис-буферном растворе (TBS) ткани мозга, фракционированные в трис-трициновых гелях, и проанализированные методом иммуноблотинга с антителами 5E3.
Фиг.14 изображает результаты статического рассеяния света для определения полимеризации Aβ в присутствии («5E3») и в отсутствие («C») антитела 5E3; и
Фиг.15 иллюстрирует нуклеотидную последовательность тяжелой и легкой цепей антитела 5ЕЗ в обоих прочтениях (5’ и 3’).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В общих чертах, настоящее изобретение представляет собой новый пептидный эпитоп с ограниченной подвижностью, полученный из Aβ, далее именуемый как «новый эпитоп» или «новый конформационный эпитоп», и композиции антител, имеющих отношение к указанному эпитопу. Антитела, способные связываться с новым конформационным эпитопом, полезны в качестве как диагностических, так и терапевтических агентов при лечении болезни Альцгеймера. Новый конформационно напряженный пептидный эпитоп Aβ, полезен для вакцин для профилактики БА и родственных видов слабоумия. Антитела, способные к связыванию с новым конформационным эпитопом также полезны для диагностики, лечения и профилактики слабоумий, родственных с болезнью Альцгеймера.
Любые термины, определение которых здесь прямо не приводится, должны пониматься как имеющие то значение, которое обычно ассоциируется с ними в рамках области техники, к которой относится данное изобретение.
Используемый здесь термин «выделенное антитело» используется для обозначения антител, способных связываться с новым конформационным эпитопом, которые обладают высокой степенью чистоты и являются свободными от постороннего клеточного материала, включая другие антитела и фрагменты антител, имеющие другую антигенную специфичность. Изолированное антитело, специфически связывающееся с новым конформационным эпитопом, может, тем не менее, иметь перекрестную реактивность к другим антигенам. Специалисту в данной области техники очевидно, что экспериментальные условия могут быть оптимизированы для получения антитела с максимальным специфическим связыванием. Термин «антитело» считается включающим его фрагменты, которые также специфически реагируют с новым конформационным эпитопом в соответствии с настоящим изобретением. Антитела могут быть фрагментированы с использованием традиционных методов, и отбор фрагментов по их пригодности проводится таким же образом, как описано выше. Фрагменты могут быть получены, например, путем обработки антител пепсином. Полученные фрагменты могут быть в дальнейшем обработаны для восстановления дисульфидных связей.
Термин «объект», используемый здесь, относится к животному, такому как птица или млекопитающее. Конкретные животные включают крыс, мышей, собак, коров, овец, лошадей, свиней или приматов. Объектом может также быть человек, альтернативно обозначаемым как пациент.Объектом может также быть трансгенное животное. Объектом может также быть грызун, такой как мышь или крыса.
Термин «эпитоп», используемый здесь, относится к участку молекулы, который может распознаваться специфичным антителом, или который индуцирует образование специфичных антител.
Термин «конформационный эпитоп», используемый здесь, относится к эпитопу, в котором аминокислотная последовательность имеет особенную трехмерную структуру. Антитела, которые специфически связываются с конформационно-специфичным эпитопом, распознают пространственное расположение аминокислот конформационно-специфичного эпитопа.
Термин Aβ, используемый здесь, может попеременно обозначать «амилоид бета», «амилоид β» или «Aβ». Амилоид бета - это пептид, состоящий из 39-43 аминокислот, который представляется основным компонентом амилоидных бляшек в мозге больных болезнью Альцгеймера. Было показано, что олигомеризация Аβ является ключевым звеном нейротоксичности при болезни Альцгеймера, как описано в данной заявке.
Термин «большая аффинность», используемый здесь, относится к степени связывания антитела, когда антитело X связывается с мишенью Y более сильно и с меньшей константой диссоциации, чем с мишенью Z, и в этом контексте антитело X имеет большую аффинность по отношению к мишени Y, чем к Z. Подобным образом, термин «меньшая аффинность» относится к степени связывания антитела, когда антитело X связывается с мишенью Y менее сильно и с большей константой диссоциации, чем с мишенью Z, и в этом контексте антитело X имеет меньшую аффинность по отношению к мишени Y, чем к Z.
Термин «мономер Aβ», используемый здесь, относится к изолированной линейной форме пептида Aβ (X-Y), предпочтительно, к форме пептида Aβ (X-Y), который не вовлечен в существенные нековалентные взаимодействия с другими пептидами Aβ.
Термин «олигомер Aβ», используемый здесь, относится к изолированной форме пептида Aβ, в которой предшественник мономера Aβ нековалентно связан в упорядоченную трехмерную структуру из не менее чем 50 мономеров.
Термин «фибрилла Aβ», используемый здесь, относится к молекулярной структуре, которая содержит агрегаты нековалетно связанных, индивидуальных пептидов Aβ (X-Y), которые под электронным микроскопом имеют фибриллярную структуру. Фибриллярная структура является типичной структурой «бета перекреста», для которой не существует теоретической верхней границы размера мультимеров, и фибриллы могут содержать тысячи мономеров.
Термин «антиген», используемый здесь, относится к молекуле, такой как белок, полипептид или их фрагмент, содержащей один эпитоп или более, которая будет вызывать в иммунной системе хозяина развитие гуморального и/или клеточного антиген-специфичного ответа. Этот термин используется взаимозаменяемо с термином «иммуноген». Антитела, такие как анти-идиотипические антитела или их фрагменты и синтетические пептидные мимотопы, которые могут имитировать антиген или антигенную детерминанту, также включены в определение термина антиген, используемым здесь. Аналогично олигонуклеотиды или полинуклеотиды, экспрессирующие антиген или антигенную детерминанту in vivo, например, при применении иммунизации ДНК, также включены в приведенное здесь определение антигена.
Номенклатура, используемая для описания пептидов настоящего изобретения, следует общепринятой практике, когда аминогруппа представляется слева, а карбоксигруппа - справа от каждого остатка аминокислоты. В последовательностях, представляющих избранные специфичные варианты реализации настоящего изобретения, амино- и карбокси-терминальные группы, даже конкретно не показанные, будут пониматься находящимися в форме, которую они принимают при физиологических значениях pH, если не указано другое.
В настоящем описании с целью пояснения приведено множество деталей для обеспечения исчерпывающего понимания вариантов реализации настоящего изобретения. Однако для специалиста в данной области техники эти специфические детали не являются обязательными.
Структура олигомеров Aβ на атомном уровне окончательно не выяснена из-за ограниченных возможностей кристаллографии и ЯМР в растворе и твердых телах. Биохимические, биофизические и иммунохимические данные свидетельствуют о фибриллярно/олигомерной модели, в которой мономеры Aβ упакованы в широкие β-шпильки, формирующие стерические структуры «застежки-молнии» (Luhrs et al. 2005; Sawaya et al. 2007; Rauk 2009). Естественным путем возникающие мономерные пептиды Aβ подвергаются конформационным изменениям во время агрегации, включающей фолдинг и формирование шпильки из стерических олигомерных структур Аβ по типу «застежки-молнии». Aβ (1-42) имеет большую склонность к агрегации β-слоев. Подробная структура олигомерных Aβ неизвестна, однако структуры олигомеров Aβ были охарактеризованы, используя комбинацию стимуляции молекулярной динамики, атомной силовой микроскопии и изучения замещения водорода амидной группы. Структура олигомеров Aβ (1-42) и Aβ (1-40) была проанализирована, используя вышеназванные методы. Ориентация β-слоев в олигомерах Aβ, как известно специалисту в данной области техники, включает внутримолекулярные солевые мостики между остатками D23 и K28. В этой конфигурации остаток K28 ориентирован преимущественно внутрь с образованием солевого мостика между D23 и K28 и стабилизирует поворот шпильки (Lurs et al. 2005; Rauk 2008).
Изучение предложенных структур олигомеров Aβ, известных в данной области техники, было проведено для идентификации участков, против которых может быть специфически направлен иммунный ответ и против которых могут быть созданы специфичные к олигомерам Aβ антитела. Исследование моделей олигомеров Aβ иллюстрирует три участка, имеющих гидрофильные, потенциально доступные для антител остатки, доступные для связывания: N-конец пептида олигомера Aβ, который распознается MAT 6E10 (остатки 4-9, последовательность FRHDSG, идентифицированная как SEQ ID NO: 2); смешанный полярно-гидрофобный домен в N-терминальной трети пептида олигомера Аβ (последовательность LVFFAEDV, идентифицированная как SEQ ID NO: 3), который распознается MAT 4G8 (остатки 17-24); и поворотный домен с ограниченной подвижностью пептида олигомера Aβ, содержащий остатки 25-29 (последовательность GSNKG). Поворотный домен с ограниченной подвижностью эпитопа, содержащего остатки SNK 26-28, является конформационно напряженным и не может присутствовать в линейном Aβ или APP. Поэтому нельзя ожидать, что антитела, направленные против этих конформационно напряженных эпитопов, будут присоединяться к линейному Aβ или APP; они являются антителами, специфичными к олигомеру Aβ.
Была проведена запись изображения моделирования с помощью молекулярной динамики циклического пептида, связанного дисульфидными связями, содержащего остатки 25-29 (CGSNKGC); неприродные цистеины были добавлены для образования в дисульфидного мостика. Моделирование показывает, что боковая цепь лизина 28 ориентирована вовне, как показано на Фиг.4, в отличие от ориентированной внутрь боковой цепи лизина 28, прогнозированной в ссылке Lurs et al. (2005) и Rauk (2008). Неожиданное открытие внешней ориентации остатка лизина 28 согласуется с высокой иммуногенностью этого циклического пептида, содержащего остатки 25-29 (CGSNKGC), в котором поверхность лизина экспонирована в растворитель, увеличена и заряжена посредством ε-аминогруппы. Антитела, мишенью которых является конформационный циклический эпитоп, содержащий, по крайней мере, остатки SNK, как было продемонстрировано в вышеописанных примерах, эффективно нейтрализуют токсичность олигомеров Aβ (см., например, Фиг.11). Неожиданное открытие внешней ориентации остатка лизина 28 согласуется также с аутентичными олигомерами Aβ, которые также демонстрируют схожую ориентацию боковой цепи лизина в растворитель в доступной для антител форме. Остатки серина 26, аспарагина 27 и лизина 28, т.е. SNK, локализированные в шарнирном участке олигомера Aβ, являются заряженными или полярными и имеют большую иммуногенность, чем маленькие неполярные аминокислоты. Циклическая конформация остатков SNK, локализированных в шарнирном участке олигомера Aβ, образует новый конформационный эпитоп, являющийся гидрофильным и доступным для связывания антителами. Следующие примеры, описанные ниже, подтверждают пригодность конформационно напряженного эпитопа SNK олигомеров Aβ для связывания. Открытие этого нового структурно напряженного эпитопа на поверхности олигомеров Aβ имеет преимущественные свойства для селективного связывания антител.
Новый конформационный эпитоп может в дальнейшем включать нативный глицин, локализированный на любом конце последовательности эпитопа SNK. Новый конформационный эпитоп может в дальнейшем включать нативные остатки глицина на обоих концах последовательности эпитопа. В одном из аспектов, остатки нативного глицина вносят ограниченный вклад в иммуногенность нового конформационного эпитопа либо не вносить в нее какой-либо вклад, однако остатки глицина могут ослаблять стерическую напряженность, возникающую при циклизации пептида. В аминокислотной структурной формуле каждый остаток может быть в общих чертах представлен с помощью однобуквенного или трехбуквенного обозначения, соответствующего тривиальному названию аминокислоты, в соответствии с Таблицей 1.
Эпитоп на поверхности олигомеров Aβ содержит сильно полярные/заряженные остатки, которые являются гидрофильными и конформационно напряженными. Эпитоп содержит по крайней мере остатки 26-28, SNK, в циклической напряженной конформационно конфигурации. В другом аспекте эпитоп содержит остатки 25-28, GSNK, в циклической конформационно напряженной конфигурации. В еще одном аспекте эпитоп содержит остатки 26-29, SNKG, в циклической конформационно напряженной конфигурации. В еще одном аспекте эпитоп содержит остатки 25-29, GSNKG (последовательность SEQ ID NO: 1), в циклической конформационно напряженной конфигурации.
В одном аспекте структура нового конформационно-специфичного эпитопа зависит от относительно жесткой пространственной организации аминокислотных остатков.
В отличие от известных эпитопов, идентифицированных как последовательности SEQ ID NO: 2 и SEQ ID NO: 3, с которыми связываются известные антитела 6E10 и 4G8 соответственно, которые экспрессируются на экспонированной в раствор поверхности олигомеров Aβ и на поверхности клеток, поддерживающих экспрессию родительских белков APP (как нейронов, так и моноцитов), новый конформационный эпитоп, имеющий конформационно напряженную циклическую конфигурацию, не присутствует на молекулярной поверхности APP, и таким образом ограничивает аутоиммунное распознавание APP. Мотив GSNKG, присущий APP, локализованному на поверхности нейронов и моноцитов, по большей части не структурирован. Конформационно специфичные антитела, связывающиеся с новым конформационным эпитопом, содержащим конформационно напряженную циклическую конфигурацию, обладают ограниченной способностью, либо не обладают способностью к распознаванию не структурированного мотива GSNKG белка APP на поверхности клеток, как показано ниже в Примерах. Антитела, распознающие новый конформационный эпитоп, демонстрируют незначительную реакцию, либо отсутствие реакции с мономерным Aβ. В другом аспекте антитела, распознающие новый конформационный эпитоп, демонстрируют незначительную реакцию, либо отсутствие реакции с фибриллярным Aβ из-за стерического уплотнения эпитопа и/или других нежелательных аспектов.
Антитела к новому конформационному эпитопу представлены в еще одном аспекте настоящего изобретения. Анализ показывает, что антитела, связывающиеся с новым конформационным эпитопом, имеющим конформационно напряженную циклическую конфигурацию, распознают нелинейную структуру эпитопа между субъединицами в участке аминокислот 25-29 олигомеров Aβ. Специфичность антител к новому конформационному эпитопу делает возможным специфически направлять действие антител на олигомерную форму Aβ и таким образом ограничивать их связывание с мономерными Aβ и APP, которые, как известно, воздействуют на нейрональную и иммунную функцию и повышают способность антител к связыванию, поскольку мономерный Aβ представлен в значительно больших количествах, чем олигомерный Aβ.
Антитела, способные к связыванию с новым конформационным эпитопом, полезны как диагностические и как терапевтические агенты в лечении болезни Альцгеймера, а вакцины для профилактики БА представляют собой другой аспект настоящего изобретения.
Антитела, специфически связывающиеся с циклическим пептидом, содержащим новый конформационный эпитоп, производный Aβ, как показано здесь, включают антитела, синтезированные с помощью дисульфидного циклического пептида, содержащего новый конформационный эпитоп.
Для применения в качестве терапевтического средства антитело, специфически связывающееся с циклическим пептидом, производным Aβ, где циклический пептид содержит конформационный эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, могут быть созданы с применением стандартных, хорошо разработанных способов производства антител. Терапевтическая композиция содержит антитело, специфически связывающееся с циклическим пептидом, производным Aβ, где циклический пептид содержит конформационный эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, в комбинации с фармацевтически приемлемым вспомогательным веществом. Такое терапевтическое средство может быть введено пациенту, нуждающемуся в терапии или профилактике болезни Альцгеймера. В одном из аспектов такое терапевтическое средство может отсрочить начало болезни Альцгеймера.
Выражение «фармацевтически приемлемый» означает приемлемый для применения в фармацевтической и ветеринарной областях, т.е. не являющийся неприемлемо токсичным или не подходящим иным образом. Примерами фармацевтически приемлемых вспомогательных веществ являются вещества, которые обычно используются в лекарствах на основе пептидов - такие как растворители, формообразующие вещества и подобные им. Для общего руководства по лекарственным формам можно обратиться к «Remington’s: The Science and Practice of Pharmacy», 21st Ed., Lippincott Williams & Wilkins, 2005». Выбор вспомогательного вещества зависит от назначенного способа введения композиции. В одном из вариантов реализации настоящего изобретения компоненты предназначены для введения путем инфузии или инъекции подкожным либо внутримышечным, либо внутривенным путем и, соответственно, применяются в форме водных стерильных и апирогенных растворов, которые могут быть буферными или изотоническими. Таким образом, компоненты могут быть введены в дистиллированной воде или, что предпочтительнее, в солевом растворе, фосфатном буферном растворе или в 5% растворе декстрозы. Композицию для орального введения посредством таблеток, капсул или суспензий готовят, используя вспомогательные компоненты, включающие сахара, такие как лактоза, глюкоза и сахароза, крахмалы, такие как кукурузный крахмал и картофельный крахмал, целлюлозу и ее производные, включая карбоксиметилцеллюлозу натрия, этилцеллюлозу и ацетаты целлюлозы, порошковые трагаканты, солод, желатин, тальк, стеариновые кислоты, стеарат магния, сульфат кальция, растительные масла, такие как арахисовое масло, масло семян хлопка, сезама, оливковое и кукурузное масла, полиолы, такие как пропиленгликоль, глицерин, сорбитол, маннитол и полиэтиленгликоль, агар, альгиновые кислоты, воду, изотонические солевые и фосфатные буферные растворы. Также могут присутствовать увлажняющие агенты, смазывающие вещества, такие как лаурилсульфат натрия, стабилизаторы, таблетирующие агенты, антиоксиданты, консерванты, окрашивающие агенты и вкусовые агенты. Кремы, лосьоны и мази могут быть приготовлены для местного применения с использованием подходящей основы, например, триглицеридов. Такие кремы, лосьоны и мази могут также содержать поверхностно-активные агенты. Также могут быть приготовлены аэрозольные композиции, например, для назального введения, с использованием подходящих вспомогательных пропеллентов. Другие вспомогательные вещества также могут быть включены в композицию в зависимости от того, каким способом она будет введена, например, антимикробные агенты могут быть добавлены в композицию для предотвращения микробного роста на протяжении долгого периода хранения. Терапевтические композиции обычно должны быть стерильными и стабильными в условиях производства и хранения.
При использовании в качестве вакцины антигенный пептид, содержащий конформационно напряженный эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, в комбинации с фармацевтически приемлемым вспомогательным веществом, после введения вызывает образование антител, специфично направленных на связывание олигомерного Aβ. Эти антитела специфично связываются с эпитопом, содержащим, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ. Вакцина содержит антигенный пептид, содержащий конформационно напряженный эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, в комбинации с фармацевтически приемлемым вспомогательным веществом. Вакцина блокирует развитие амилоидоза мозга путем нейтрализации олигомерного Aβ и действует в качестве профилактики развития БА. Когда олигомерные Aβ заблокированы, также блокируется опосредованная ими токсичность. Такая токсичность может включать, например, синаптическую дисфункцию и смерть нейрональных клеток. В другом аспекте антитела, образующиеся при введении вакцины, описанной выше, замедляют размножение олигомерного Aβ, поскольку такие антитела препятствуют агрегации мономеров Aβ в токсичные формы олигомера Aβ. В еще одном аспекте антитела, образующиеся при введении вакцины, описанной выше, блокируют размножение олигомерного Aβ, поскольку такие антитела препятствуют агрегации мономеров Aβ в токсичные формы олигомера Aβ.
Примеры фармацевтически приемлемых вспомогательных веществ могут включать гидроксид алюминия, квасцы, Alhydrogel™ (тригидрат алюминия) или другие соли, содержащие алюминий, виросомы, нуклеиновые кислоты, содержащие мотив CpG, сквалены, масла, MF59, QS21, разнообразные сапонины, вирус-подобные частицы, монофосфорил-липид A / дикориномиколат трегалозы, агонисты toll-like рецепторов, кополимеры, такие как полиоксипропилен и полиоксиэтилен или подобные.
Вакцина может быть введена пациентам из группы риска развития болезни Альцгеймера, например, людям преклонного возраста из группы риска со скрытой мутацией, провоцирующей БА.
В одном из вариантов реализации настоящего изобретения для лечения с помощью вакцины субъекты иммунизируют по схеме, которая может варьировать в пределах от одного раза в день до одного раза в неделю, одного раза в месяц, одного раза в год, одного раза в десять лет. Типичный режим заключается в иммунизации с последующими повторными инъекциями с интервалами в 6 недель. Другой режим заключается в иммунизации с последующими повторными инъекциями через 1, 2 и 12 месяцев. В качестве альтернативы повторные инъекции могут варьировать в зависимости от иммунного ответа и физиологических условий объекта. Антиолигомерная вакцина может быть введена для иммунизации в дозах, варьирующих от около 0,0001 микрограмма до 10 грамм, от около 0,01 микрограмма до около 1 грамма, около 1 микрограмма до около 1 мг, и около 100 до 250 микрограмм на лечение. В одном из вариантов реализации терапевтическое введение вакцины осуществляется в следующие моменты времени (либо чаще): 0 месяцев, 2 месяца; 6 месяцев; 9 месяцев; и/или 12 месяцев. В одном режиме введение дозы осуществляют через 2, 6, 9 и 12 месяцев после первой иммунизации. В другом режиме дозы вводятся через 2 и 4 недели после первой иммунизации, а затем вводятся каждый месяц. В альтернативном режиме дозы варьируют в зависимости от физиологического состояния субъекта и/или от ответа субъекта на предшествующую иммунизацию. Путь введения включает внутримышечные и внутрибрюшинные инъекции, но не ограничивается ими. В одном из вариантов реализации композиция инъецируется в дельтовидную мышцу.
При использовании настоящего изобретения в качестве диагностического биомаркера, либо биомаркера ответа на лечение подходящий биологический образец собирают у пациента; образец приводят в контакт с антителом, специфически связывающимся с циклическим пептидом, производным Aβ, где циклический пептид содержит эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, на протяжении времени и при условиях, достаточных для формирования комплексов антиген-антитело в образце; затем определяется наличие комплексов. Если комплексы выявлены, это означает диагноз БА у пациента. Подходящий для этой цели биологический образец может быть представлен тканями, клетками и биологическими жидкостями, включая, например, спинномозговую жидкость (СМЖ) и кровь.
Применение антител, связывающихся с новым конформационным эпитопом, имеет большое значение для диагностики БА. С целью выявления субъектов, являющихся кандидатами для лечения с помощью антител или композиции вакцины настоящего изобретения, настоящее изобретение также предоставляет эпитоп для диагностических методов in vitro и in vivo.
Для определения наличия олигомерного Aβ в любом предоставленном образце настоящее изобретение предоставляет способ определения, в котором образец, предположительно содержащий олигомерный Aβ, обрабатывается с помощью антитела или его фрагмента, ответственного за связывание, которое селективно связывается с новым конформационным эпитопом, уникально представленным на олигомерном Aβ, родственном мономерному Aβ и белку APP; затем определяется формирование комплекса антиген/антитело, наличие которого является индикатором наличия в образце олигомерного Aβ. Наличие комплекса антиген/антитело означает диагноз БА у пациента.
При применении in vitro способ определения влечет за собой анализ биологического образца жидкости организма или ткани или образца органа субъекта, обычно субъекта, предположительно имеющего БА. Образец ткани или органа, например, полученный из твердой или полутвердой ткани или органа, может быть выпарен, экстрагирован или каким-либо иным образом переведен в жидкую форму. Биологический образец или образцы могут быть изъяты у субъекта в любое удобное время, включая время до того, как у субъекта было диагностировано или заподозрено наличие БА или родственного вида слабоумия, на протяжении терапевтического режима лечения или устранения симптомов болезни или расстройства, после смерти субъекта (независимо от ее причины или ее предполагаемой причины). Биологический образец поочередно может включать пожертвованную в рамках донорства жидкость организма или ткань (такую как кровь, плазму или тромбоциты), полученную при помощи централизованной организации или учреждения кровоснабжения.
Наличие олигомерного Aβ в образце подтверждается, если антитело образует детектируемый комплекс антиген/антитело. Образование такого комплекса может быть обнаружено с использованием широкого спектра методик, включающих ELISA, РИА, проточную цитометрию, Вестерн блоттинг, иммуногистохимию и подобные им. Для обнаружения комплекса и, таким образом, подтверждения наличия нового конформационного эпитопа в образце, антитело предпочтительно должно представлять собой меченное антитело, помеченное путем конъюгации или слияния с агентом, который можно обнаружить визуально или с применением инструментов. Агент или метка способны к продукции сигнала, который обнаруживается прямым или не прямым способом. Например, метка может быть рентгеноконтрастной или изотопной, такой как 3H, 14C, 32P, 35S, 123I, 125I, 131I; флуоресцентным (флуорофор) или хемилюминисцентым (хромофор) компонентом, таким как изотиоцианат флуоресцеина, родамин или люциферин; ферментом, таким как щелочная фосфатаза, бета-галоктозидаза или пероксидаза хрена; визуализирующим агентом или ионом металла. В качестве альтернативы новый конформационный эпитоп может быть обнаружен с использованием меченного вторичного реагента, который связывается с эпитоп-специфичным антителом, например, используя меченное антитело, которое связывается с эпитоп-специфичным антителом, для непрямого обнаружения эпитопа. Наличие комплекса антиген/антитело может быть обнаружено и непрямым методом, который не требует присутствия в растворе двух агентов. Например, комплекс можно обнаружить непрямым методом, используя проточную цитофлуориметрию, при которой антитело связывается с эпитопом, присутствующим на поверхности интактной клетки, и образует комплекс антиген/антитело. Было бы также предпочтительно, чтобы комплекс антиген/антитело можно было идентифицировать с применением методов, не основанных на использовании антител, например, методов, которые позволяют разделять белки на основании их размера, заряда и подвижности - таких как электрофорез, хроматография, масс-спектроскопия и подобные им.
В подобном варианте реализации меченные антитела согласно настоящему изобретению или меченные формы их фрагментов, ответственных за связывание, могут быть использованы in vivo для визуализации олигомерного Aβ, с которым связывается антитело. В этой связи настоящее изобретение представляет собой антитело или его фрагмент, связанное с агентом, позволяющим проводить визуализацию in vivo, таким как изотопы технеция, гадолиния и подобные.
В еще одном аспекте предмет производства (также обозначаемый как коммерческая упаковка) представляет собой фармацевтическую композицию в упаковочном материале. Композиция содержит фармацевтически приемлемое вспомогательное вещество и терапевтически эффективное количество конформационно-чувствительного антитела, которое специфично связывается с циклическим пептидом, производным Aβ, где циклический пептид содержит эпитоп, содержпщий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ. Упаковочный материал может содержать маркировку, указывающую, что композиция полезна для лечения болезни Альцгеймера. Упаковочным материалом может быть любой подходящий материал, обычно используемый для упаковки фармацевтических агентов, включая, например, стекло, пластик, фольгу и картон.
В еще одном аспекте предмет производства представляет собой фармацевтическую композицию в упаковочном материале. Композиция содержит пептид, содержащий конформационно напряженный эпитоп, содержащий, по крайней мере, аминокислотную последовательность SNK, соответствующую шарнирному участку олигомерного Aβ, в комбинации с фармацевтически приемлемым вспомогательным веществом, как представлено в настоящем документе. Композиция может включать физиологически или фармацевтически приемлемые наполнители, а упаковочный материал может включать маркировку, указывающую на активные компоненты композиции (т.е. пептид). Маркировка может также включать назначение композиции, например, использование в качестве терапевтического или профилактического реагента или в качестве композиции для индукции у субъекта иммунного ответа с целью продукции антисыворотки или антител, специфичных к олигомерному Aβ, для использования в составе набора, представленного здесь.
В еще одном варианте реализации настоящее изобретение представляет собой набор, содержащий композицию, которая содержит пептид, представленный здесь, вместе с инструкцией по применению компонента композиции для производства или скрининга конформационно-чувствительных антител для идентификации олигомерного Aβ. Набор может быть полезным для получения и/или идентификации специфичных к олигомерному Aβ антител или антисыворотки, а инструкция может включать, например, концентрации доз, интервалы доз, предпочтительные методы введения, методы иммунологического скрининга и тестирования и подобное.
В другом варианте реализации настоящее изобретение представляет собой набор для приготовления медикамента, содержащего композицию, которая содержит один пептид или более, вместе с инструкцией по его применению. Инструкция может содержать серии шагов для приготовления лекарства, которое было бы полезно для стимулирования терапевтического или профилактического иммунного ответа у объекта, которому оно было введено. Набор может также содержать инструкцию по применению лекарства в лечении, для терапии, профилактики или ослабления одного или более симптомов БА или родственных видов слабоумия, которая включает, например, концентрации доз, интервалы доз, предпочтительные методы введения и подобное.
В еще одном варианте реализации настоящее изобретение представляет собой набор для диагностики БА или родственных видов слабоумия. Набор содержит одно или более конформационно-чувствительное селективное антитело или антисыворотку, представленных здесь, вместе с инструкцией по применению. Антитела также могут быть связанными с детектирующим реагентом. Примеры детектирующих реагентов включают вторичные антитела, такие как антимышиные антитела, антикроличьи антитела и подобные им. Такие вторичные антитела могут быть связанными с ферментом, который, при наличии подходящего субстрата, обеспечивает прохождение детектируемой колориметрической или хемилюминисцентной реакции. Набор может также содержать реагенты для проведения реакции детектирования, включая ферменты, такие как протеиназа К, блокирующий буфер, гомогенизирующий буфер, буфер для выделения, буфер для разведения и подобные им.
В еще одном варианте реализации настоящее изобретение представляет собой набор для определения наличия олигомерного Aβ в биологических образцах. Набор содержит одно или более конформационно-чувствительное антитело или антисыворотку, которые специфически связываются с олигомерным Aβ, вместе с инструкцией по применению. Антитела также могут быть связанными с детектирующим реагентом. Примеры детектирующих реагентов включают вторичные антитела, такие как антимышиные антитела, антикроличьи антитела и подобные. Такие вторичные антитела могут быть связанны с ферментом, который, при наличии подходящего субстрата, обеспечивает прохождение детектируемой колориметрической или хемилюминисцентной реакции. Набор может также содержать реагенты для проведения реакции детектирования, включая ферменты, такие как протеиназа К, блокирующий буфер, гомогенизирующий буфер, буфер для выделения, буфер для разведения и подобные. им
Для получения конформационно-чувствительных антител могут быть использованы подходящие методы, включая использование поликлональной антисыворотки или моноклональных антител. Для получения поликлональных антител млекопитающее (например, мышь, хомяк или кролик) может быть иммунизировано с помощью иммуногенной формы нового конформационного эпитопа, который вызывает образование антител у млекопитающего. Например, связанный дисульфидной связью циклизованный пептид, содержащий последовательность нового конформационного эпитопа, может быть получен напряженным в конформационной петле с использованием дисульфидной связи между цистеинами на C и N-концах пептида. Связанный дисульфидной связью циклизованный пептид может быть синтезирован с использованием общепринятых методик, и введен в млекопитающее.
Приемы наделения пептида иммуногенностью хорошо известны в данной области техники и включают, например, конъюгацию с носителями. Пептид может быть введен в присутствии адъюванта. За развитием иммунизации можно следить путем измерения титров антител в плазме или сыворотке. Для оценки уровня антител может быть применен стандартный метод ELISA или другая процедура иммуноанализа с использованием иммуногена в качестве антигена. После иммунизации может быть получена антисыворотка и, при необходимости, поликлональные антитела могут быть изолированы из сыворотки.
Для получения моноклональных антител у иммунизированного животного отбирают антитело-продуцирующие клетки (B-лимфоциты) и объединяют их с клетками миеломы путем процедур стандартного слияния соматических клеток для формирования бессмертных клеток гибридомы. Такие методики хорошо известны в данной области техники (например, методика получения гибридомы, изначально разработанная Kohler and Milstein (Nature 256, 495-497 (1975)), также как и другие способы, такие как методика получения В-клеточной гибридомы человека (Kozbor et al, Immunol. Today 4, 72 (1983)), способ получения моноклональных антител человека методом EBV-гибридомы (Cole et al., Monoclonal Antibodies in Cancer Therapy (1985) Allen R. Bliss, Inc., pages 77-96), и способ скрининга библиотек комбинаторных антител (Huse et al., Science 246, 1275 (1989)). Клетки гибридомы могут быть отобраны иммунохимически для продукции антител, специфически реакционноспособных по отношению к новому конформационному эпитопу, и монокланальные антитела могут быть изолированы.
Типичное антитело состоит из двух «тяжелых цепей» иммуноглобулина (Ig) и двух «легких цепей» Ig и может быть представлено как имеющее общее Y-образную форму. Существует несколько различных типов тяжелых цепей, что определяет классы или изотипы антител. У млекопитающих существует пять типов тяжелых цепей иммуноглобулинов: γ, δ, α, μ, ε которые определяют классы иммуноглобулинов: IgG, IgD, IgA, IgM и IgE, соответственно. У млекопитающих существует два типа легких цепей: каппа (κ) цепь и лямбда (λ) цепь.
Каждая тяжелая цепь содержит два участка: константный участок, являющийся одинаковым для всех иммуноглобулинов одного класса, но различающийся у иммуноглобулинов разных классов (тяжелые цепи λ, α и δ имеют константный регион, состоящий из трех тандемных иммуноглобулиновых доменов (CH1, CH2, CH3) и имеют шарнирный участок, придающий гибкость; тяжелые цепи μ и ε имеют константный участок, состоящий из четырех доменов); и вариабельный участок (VH), который отличается у иммуноглобулинов, вырабатываемых разными В-клетками, но является одинаковым для иммуноглобулинов, вырабатываемых одной и той же В-клеткой или клоном В-клеток. Вариабельный домен любой тяжелой цепи состоит из одного иммуноглобулинового домена. Эти домены имеют длину около 110 аминокислот.
Каждая легкая цепь состоит из двух тандемных иммуноглобулиновых доменов: одного константного (CL) домена и одного вариабельного (VL), важных для связывания антигена.
Некоторые части антитела имеют уникальные функции. Плечи Y-образного антитела, например, содержат сайты, которые могут связать два антигена (обычно идентичных) и таким образом распознать специфичные чужеродные объекты. Этот участок антитела называют «Fab» участок (Fab-фрагмент, Aг-связывающий фрагмент). Он состоит из одного константного и одного вариабельного домена от каждой тяжелой и легкой цепи антитела. На N-конце мономера антитела находится «паратоп», сформированный вариабельными доменами тяжелых и легких цепей. Вариабельные домены также обозначаются как FV-участок и являются наиболее важным участком для связывания с антигеном. Вариабельные петли β-слоев, по три на легкой (VL) и тяжелой (VH) цепях, отвечают за специфичное связывание с антигеном. Эти петли обозначаются как участки, определяющие комплементарность («CDR-участки»).
Участки, определяющие комплементарность («CDR-участки»), являются участками антитела, в которых данные белки являются комплементарными по форме антигену. Таким образом, CDR-участки определяют аффинность и специфичность связывания белков со специфичными антигенам. CDR-участки являются наиболее вариабельной частью молекулы и вносят вклад в разнообразие молекул антител, что позволяет антителам распознавать широкий репертуар антигенов.
В аминокислотной последовательности вариабельного домена антигенного рецептора находятся три CDR-участка (CDR1, CDR2 и CDR3), расположенные не последовательно. Поскольку антигенный рецептор обычно состоит их двух вариабельных доменов (находящихся на двух разных полипептидных цепях, тяжелой и легкой цепях), существует шесть CDR-участков для каждого антигенного рецептора, которые могут совместно контактировать с антигеном. Одиночная молекула антитела имеет два антигенных рецептора и, таким образом, содержит двенадцать CDR-участков.
Основание Y-образного антитела играет роль в модуляции активности клеток иммунной системы. Этот участок называют Fc-участок (Fc-фрагмент, кристаллизирующийся фрагмент); он состоит из двух тяжелых цепей, которые содержат по два или три константных домена в зависимости от класса антитела. Fc-фрагмент обеспечивает то, что каждое антитело вызывает развитие соответствующего иммунного ответа на введение антигена путем связывания со специфичным классом Fc-рецепторов и других молекул иммунной системы, таких как белки комплемента. Тем самым опосредуются различные физиологические эффекты, включая распознавание опсонизированных частиц, лизис клеток или дегрануляцию тучных клеток, базофилов или эозинофилов.
Есть несколько способов определения CDR-участков в аминокислотной последовательности. Наиболее часто используется определение «Kabat», основанное на выявлении различий в последовательностях. Существует также определение «Chotia», основанное на расположении участков структурных петель. Определение «AbM» является компромиссным между этими двумя определениями и используется в программном обеспечении Oxford Molecular’s AbM antibody modelling. «Контактное» определение основано на анализе доступных кристаллических структур комплексов.
Специалист в данной области техники может легко идентифицировать CDR-участки в любой предложенной последовательности, содержащей CDR-участки, используя известные паттерны и методы выравнивания последовательностей. В другом аспекте для идентификации CDR-участков может быть также использовано моделирование или другие методы, известные специалисту в данной области техники. Существуют хорошо известные руководства, например, расположенное на следующем веб-сайте (http://www.bioinf.org.uk/abs/), для помощи специалисту в идентификации CDR-участков в последовательности антитела.
Тяжелая и легкая цепи антитела 5E3 были секвенированы. Последовательность тяжелой цепи и последовательность легкой цепи соответствуют последовательностям, представленным на Фиг.15. Специалисту в данной области техники очевидно, что части указанной последовательности, являющиеся детерминантами связывания антигена, могут быть перенесены в рамку считывания другого антитела, например, для создания «химерного» или «гуманизированного» антитела.
Специалист в данной области техники может легко совместить последовательности с 3’ и 5’ -концов, приведенные на Фиг.15, для получения консенсусной последовательности (например, используя доступные пакеты программ, такие как GCG или Sequencher) и может проверить признаки последовательности, необходимые для выявления различий. Любое упомянутое различие может быть разрешено методом повторного секвенирования. Различия, например, в среднем стоп-кодоне, расположенном в нуклеотидной последовательности, будут разрешены специалистом в данной области техники как, очевидно, неправильно прочитанные нуклеотиды. В данной области техники хорошо известно, что последовательности аминокислот и нуклеотидов, кодирующие ошибки или неточности чтения, могут возникать, когда метод секвенирования считывает одно или более оснований некорректно, приводя к неточному прочтению. Из-за не предсказуемости молекулярной биологии ни один из лабораторных методов секвенирования ДНК не является совершенно точным; все они допускают случайные механические ошибки при чтении оснований. Такие ошибки чтения становятся очевидными, когда прочитанная последовательность сравнивается с другими прочтениями или с последовательностью сравнения.
«Химерные» антитела также рассматроиваются в рамках данного изобретения. Химерные антитела могут содержать последовательности двух разных антител. Они могут содержать последовательности антител двух разных видов. Молекулы химерного антитела могут включать, например, антиген-связывающий домен антитела мыши, крысы или другого вида и константный пептидный участок человека. Для создания химерных антител, содержащих вариабельный участок иммуноглобулина, который распознает новый конформационный эпитоп изобретения, могут быть использованы соответствующие методы (см., например, Morrison et al., Proc. Natl Acad. Sci. U.S.A. 81,6851 (1985); Takeda et al., Nature 314, 452 (1985), Cabilly et al, Патент США No. 4,816,567; Boss et al. Патент США No. 4,816,397; Tanaguchi et al., Европейский патент EP 171496; Европейский патент 0173494, Патент Великобритании GB 21770966) 4,816,397; Tanaguchi et al., Европейский патент EP 171496; Европейский патент 0173494, Патент Великобритании GB 21770966))
«Гуманизированные антитела» содержат последовательности антитела вида, отличного от человека, последовательность белка которого была изменена для повышения его схожести с вариантами антитела, которые обычно образуются у человека. В некоторых случаях они могут рассматриваться как особый подтип химерных антител. Однако «гуманизация» обычно рассматривается как процесс, отличный от простого создания химеры. Процесс гуманизации может включать создание химеры мышь-человек на начальном этапе (например, мышиный Fab-фрагмент может быть объединен с Fc-фрагментом человека). После этого химера может быть гуманизирована селективным изменением последовательности аминокислот в Fab-части молекулы. Процесс обычно является «селективным» в отношении сохранения специфичности, для которой антитело было изначально создано. Например, помимо CDR-участков, части последовательности Fab, которые отличаются от аналогичных последовательностей человека, могут быть мутированы путем замены соответствующих индивидуальных аминокислот. Это осуществляется на уровне ДНК путем мутагенеза. Возможно создать гуманизированное антитело и без создания химерного промежуточного продукта. «Прямое» создание гуманизированного антитела может быть осуществлено путем вставки соответствующего сегмента, кодирующего CDR-участок (ответственный за желаемые свойства связывания), в «каркас» антитела человека. Как описано выше, это достигается с помощью методов рекомбинантной ДНК с использованием экспрессии соответствующего вектора в клетках млекопитающих. То есть после того как, например, в мыши создают антитело, которое демонстрирует желаемые свойства, ДНК, кодирующая это антитело, может быть изолирована, клонирована в вектор и секвенирована. Затем может быть определена последовательность ДНК, соответствующая CDR-участкам антитела. Однажды определив точную последовательность желаемого CDR-участка, можно разработать стратегию вставки этой последовательности соответствующим образом в конструкцию, содержащую ДНК различных вариантов антитела человека. Эта стратегия может также включать синтез линейных фрагментов ДНК, основываясь на прочтенной последовательности CDR-участков. Могут быть созданы библиотеки различий в последовательности с использованием синтетических олигонуклеотидных праймеров, содержащих такие различия. Среди полученной в результате этого совокупности клонов можно в дальнейшем провести скрининг для выявления оптимизированных гуманизированных клонов антител, используя известные методы.
В некоторых вариантах реализации настоящего изобретения моноклональные или химерные антитела, специфически реагирующие с новым конформационным эпитопом изобретения, представленным здесь, могут быть затем гуманизированы путем создания химер константного участка человека, в котором части вариабельного участка, в частности, консервативные участки рамок считывания антиген-связывающего домена, имеют человеческое происхождение и только гипервариабельные участки имеют не человеческое происхождения. Такие молекулы иимуноглобулинов могут быть созданы с использованием методик, известных в данной области техники (см., например, Teng et al, Proc. Natl. Acad. Sci. U.S.A.., 80, 7308-7312 (1983); Kozbor et al, Immunology Today, 4, 7279 (1983); Olsson et al., Meth. Enzymol., 92, 3-16 (1982)), и PCT Publication W092/06193 или Европейский патент 0239400). Гуманизированные антитела также могут быть произведены коммерчески (Scotgen Limited, 2 Holly Road, Twickenham, Middlesex, Great Britain).
В одном аспекте настоящее изобретение представляет собой химерное гуманизированное антитело, содержащее тяжелую и/или легкую цепи последовательности 5E3, или его часть или части. Части могут быть детерминантами антигенного связывания. В некоторых вариантах реализации детерминанты могут содержать последовательности CDR-участков 5E3. Эти антитела связываются с тем же эпитопом, что и 5E3. Они также могут связываться с эпитопом, который, по крайней мере, частично совпадает с эпитопом, с которым связывается 5Е3.
В некоторых вариантах реализации настоящего изобретения химерное или гуманизированное антитело может содержать последовательность CDR-участков, по большей части идентичную последовательности CDR-участков 5E3. В некоторых вариантах реализации антитела могут содержать изменения в консервативной последовательности в сравнении с последовательностями 5E3.
«Замена консервативной аминокислоты» среди распространенных аминокислот иллюстрируется заменой аминокислот в каждой из следующих групп: (1) глицин, аланин, валин, лейцин и изолейцин; (2) фенилаланин, тирозин и троптофан; (3) серии и треонин; (4) аспарагиновая и глутаминовая кислоты; (5) глутамин и аспарагин и (6) лизин, аргинин, гистидин.
Таблица BLOSUM62, хорошо известная в данной области техники, является матрицей аминокислотных замен, производной 2000 локальных множественных выравниваний сегментов белковой последовательности, представляющей высоко консервативные участки более чем 500 групп родственных белков (См. Henikoff and Henikoff, Proc. Nat’I Acad. Sci. USA 89:10915 (1992)). Соответственно, частота замен BLOSUM62 может быть использована для определения консервативных аминокислотных замен, которые могут быть включены в аминокислотную последовательность настоящего изобретения. Хотя возможно создать аминокислотные замены, основываясь исключительно на химических свойствах (что обсуждалось выше), выражение «консервативная аминокислотная замена» предпочтительно относится к заменам, со значениями BLOSUM62 большими, чем -1. Например, аминокислотная замена консервативна, если замена характеризуется значениями BLOSUM62 0, 1, 2 или 3. Согласно этой системе, предпочтительные консервативные аминокислотные замены характеризуются значениями BLOSUM62, по крайней мере, 1 (например, 1, 2 или 3), тогда как более предпочтительные консервативные аминокислотные замены характеризуются значениями BLOSUM62, по крайней мере, 2 (т.е. 2 или 3).
В некоторых вариантах реализации настоящего изобретения антитело может содержать последовательность CDR, в которой по крайней мере 70%, по крайней мере 75%, по крайней мере 80%, по крайней мере 85%, по крайней мере 90% идентичны последовательности CDR 5E3. Они также могут быть по крайней мере на 91%, по крайней мере на 92%, по крайней мере на 93%, по крайней мере на 94%, по крайней мере на 95%, по крайней мере на 96%, по крайней мере на 97%, по крайней мере на 98%, по крайней мере на 99% или более чем на 99% идентичны последовательностям CDR 5E3.
Стандартные методики рекомбинантной ДНК и молекулярного клонирования, используемые при создании антител, хорошо известны в данной области техники и более полно описаны в Sambrook, J., Fritsch, E.F. and Maniatis, T., Molecular Cloning: A Laboratory Manual; Cold Spring Harbor Laboratory Press: Cold Spring Harbor, 1989 (здесь и далее «Sambrook»).
Термин «рекомбинантный» относится к искусственной комбинации двух во всех других случаях разделенных сегментов последовательности, созданной, например, путем химического синтеза или путем манипулирования изолированными участками нуклеиновых кислот, используя технологии генной инженерии.
Доза композиции или ее компонентов определенного варианта реализации изобретения может варьировать в зависимости от способа введения (оральное, внутривенное введение, ингаляция или подобные) и от формы, в которой вводится композиция или ее компоненты (раствор, контролированное высвобождение или подобное). Определение соответствующих дозировок является прерогативой специалиста в данной области техники.
«Фармацевтически приемлемый носитель» включает в себя любой из перечисленных компонентов: все растворители, дисперсионные среды, оболочки, антибактериальные и антигрибковые агенты, изотонические и препятствующие всасыванию агенты и подобные физиологически совместимые агенты. Примеры фармацевтически приемлемых носителей включают одно или более из следующих веществ: вода, солевой раствор, фосфатный буферный раствор, декстроза, глицерин, этанол и подобные, а также их комбинации.
Во многих случаях будет предпочтительно включение в композицию изотонических агентов, таких как сахара, полиспирты (такие как маннитол, сорбитол), натрия хлорид. Фармацевтически приемлемые носители могут, кроме того, содержать небольшие количества вспомогательных веществ, таких как увлажняющие агенты, эмульгаторы, консерванты или буферы, повышающие срок годности или эффективность антитела или его частей.
Фармацевтическая композиция изобретения может включать «эффективное количество», «терапевтически эффективное количество» или «профилактически эффективное количество» антитела или части антитела настоящего изобретения. «Терапевтически эффективное количество» означает количество, являющееся эффективным в необходимых дозах и на протяжении необходимого периода времени для достижения желаемого терапевтического результата. Терапевтически эффективное количество антитела или части антитела может быть определено специалистом в данной области техники и может варьировать в зависимости от различных факторов, таких как состояние болезни, возраст, пол, вес индивидуума и способность антитела или части антитела вызывать желаемый ответ у индивидуума. Терапевтически эффективным количеством также должно быть такое количество, в котором терапевтически целебный эффект превосходит любые токсические или пагубные эффекты антитела или части антитела. «Профилактически эффективное количество» означает количество, являющееся эффективным в необходимых дозах и на протяжении необходимого периода времени для достижения желаемого профилактического результата. Поскольку профилактическая доза применяется к объекту на ранних стадиях возникновения заболевания или до его возникновения, профилактически эффективное количество обычно бывает меньшим, чем терапевтически эффективное количество. Эффективное количество может быть вычислено на основании соотношения масса/масса (т.е. микрограммы или миллиграммы на килограмм объекта), или может быть вычислено на основании соотношения масса/объем (т.е. концентрация, микрограммы или миллиграммы на миллилитр). При использовании единицы масса/объем, антитело может присутствовать в количестве от около 0,1 мкг/мл до около 20 мг/мл, или в любом количестве, промежуточным между ними, например, 0,1; 0,5; 1; 2; 5; 10; 15; 20; 25; 30; 35; 40; 50; 60; 70; 80; 90; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 1500; 2000; 5000; 10000; 20000 мкг/мл или в любом количестве между ними; или от около 1 мкг/мл до около 2000 мкг/мл или в любом количестве между ними, например, 1,0; 2,0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 1500; 2000 мкг/мл или в любом количестве между ними; или от около 10 мкг/мл до около 1000 мкг/мл или в любом количестве между ними, например, 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/мл или в любом количестве между ними; или от около 30 мкг/мл до около 1000 мкг/мл или в любом количестве между ними, например, 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/мл.
Количества и/или концентрации могут быть рассчитаны на основании соотношения масса/масса (т.е. микрограммы или миллиграммы на килограмм объекта), или могут быть вычислены на основании соотношения масса/объем (т.е. концентрация, микрограммы или миллиграммы на миллилитр). При использовании единицы масса/объем, антитело или петид может присутствовать в количестве от около 0,1 мкг/мл до около 20 мг/мл, или в любом количестве между ними, например, 0,1; 0,5; 1; 2; 5; 10; 15; 20; 25; 30; 35; 40; 50; 60; 70; 80; 90; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 1500; 2000; 5000; 10000; 20000 мкг/мл или в любом количестве между ними; или от около 1 мкг/мл до около 2000 мкг/мл или в любом количестве между ними, например, 1,0; 2,0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 1500; 2000 мкг/мл или в любом количестве между ними; или от около 10 мкг/мл до около 1000 мкг/мл или в любом количестве между ними, например, 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/мл или в любом количестве между ними; или от около 30 мкг/мл до около 1000 мкг/мл или в любом количестве между ними, например, 0,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/мл.
Антитела настоящего изобретения могут быть включены в фармацевтическую композицию, подходящую, например, для парентерального введения. Предпочтительно антитело будет приготовлено как раствор для инъекций, содержащий эффективное количество антитела. Инъецируемый раствор может состоять из жидкой или лиофилизированной дозированной формы во флаконах прозрачного или темного стекла, ампулах или преднаполненных шприцах. Для приготовления фармацевтической композиции может быть использован любой подходящий буфер. Примеры таких буферов включают сукцинат натрия, цитрат натрия, фосфат натрия или фосфат калия, но не ограничиваются ими. В лиофилизированную дозированную форму могут быть включены криопротекторы и агенты, увеличивающие объем. Как для жидкой, так и для лиофилизированной дозированной формы могут быть использованы стабилизаторы.
Композиции, предназначенные для различного применения изобретения, включая терапевтические композиции, могут вводиться в дозе, содержащей эффективное количество антитела или пептида. Доза может содержать от около 0,1 мкг/кг до около 20 мг/кг (в зависимости от массы объекта), например, 0,1; 0,5; 1; 2; 5; 10; 15; 20; 25; 30; 35; 40; 50; 60; 70; 80; 90; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 1500; 2000; 5000; 10000; 20000 мкг/кг или в любом количестве между ними; или от около 1 мкг/кг до около 2000 мкг/мл или в любом количестве между ними, например, 1,0; 2,0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000; 2000 мкг/мл или в любом количестве между ними; или от около 10 мкг/кг до около 1000 мкг/кг или в любом количестве между ними, например, 10,0; 15,0; 20,0; 25,0; 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/кг или в любом количестве между ними; или от около 30 мкг/кг до около 1000 мкг/кг или в любом количестве между ними, например, 30,0; 35,0; 40,0; 50,0; 60,0; 70,0; 80,0; 90,0; 100; 120; 140; 160; 180; 200; 250; 500; 750; 1000 мкг/кг.
Специалист в данной области техники способен при необходимости перевести представленные данные, касающиеся массы объекта, концентрации фармацевтической композиции, индивидуальных компонентов или их комбинации, объема фармацевтической композиции, индивидуальных компонентов или их комбинации, в формат, подходящий для предпочтительного применения.
Фармацевтические композиции согласно настоящему изобретению могут находиться в различных формах. Эти формы включают, например, жидкую, полутвердую, твердую дозированную форму, такую как жидкий раствор (например, инъецируемый и инфузионный раствор), дисперсия или суспензия, таблетки, пилюли, порошки, липосомы и суппозитории. Предпочитаемая форма зависит от предназначенного способа введения и терапевтического применения. Типичные предпочтительные композиции изготавливаются в форме инъеционных или инфузионных растворов, таких как композиции, схожие с используемыми для пассивной иммунизации людей другими антителами. Предпочитаемым способом введения является парентеральный (например, внутривенный, подкожный, внутрибрюшинный, внутримышечный). В предпочтительном варианте реализации антитело вводится путем внутривенной инфузии или инъекции. В другом предпочтительном варианте реализации антитело вводится путем внутримышечной или подкожной инъекции.
Антитела согласно настоящему изобретению могут вводиться различными методами, известными в данной области техники, хотя для многих терапевтических применений предпочтительным путем/способом введения является подкожная инъекция, внутривенная инъекция или инфузия. Как очевидно специалисту в данной области техники, путь и/или способ введения может варьировать в зависимости от желаемых результатов. В частных вариантах реализации активный компонент может быть приготовлен с носителем, защищающим компонент от быстрого высвобождения; это могут быть, например, формы с контролируемым выходом, включая имплантаты, трансдермальные повязки и микроинкапсулированные системы доставки. Также могут использоваться такие биодеградирующие, биосовместимые полимеры как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие методы приготовления таких форм запатентованы или общеизвестны специалисту в данной области техники. См., например, Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
В частных вариантах реализации антитело согласно настоящему изобретению может быть введено орально, например, вместе с инертным растворителем или с ассимилируемым съедобным носителем. Компонент (и другие ингредиенты, если это необходимо) могут также быть заключенными в твердые или мягкие оболочные желатиновые капсулы, спрессоваными в таблетки или напрямую включенными в питание объекта. Для орального терапевтического введения компоненты могут включаться вместе с наполнителем и использоваться в форме нерастворимых таблеток, буккальных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, брикетов и подобного. Для введения компонента изобретения иным способом, кроме парентерального введения, может возникнуть необходимость покрыть компонент материалом (или вводить компонент совместно с материалом), предотвращающим его инактивацию.
В фармацевтические композиции могут также включаться вспомогательные активные компоненты. В частных вариантах реализации антитело согласно настоящему изобретению может быть приготовлено как часть лекарственной формы и/или может быть введено совместно с одним или более дополнительными терапевтическими агентами, полезными для терапии БА и родственных видов слабоумия. Например, одно из антител согласно настоящему изобретению или часть этого антитела может быть приготовлено как часть лекарственной формы и/или может быть введено совместно с одним или более дополнительными антителами, которые связываются с другими мишенями.
В частных вариантах реализации настоящего изобретения антитело согласно настоящему изобретению или его фрагмент может быть связано с носителем, повышающим его срок годности, известным в данной области техники. Такие носители включают Fc-домен, полиэтиленгликоль (ПЭГ) и декстран. но не ограничиваются ими. Такие носители описаны, например, в Заявке на Патент США Ser. No. 09/428,082 и в опубликованной Заявке No. WO 99/25044, которые включены в качестве ссылки для любых целей.
В одном из вариантов реализации изобретения оно представляет собой антигенный пептид, содержащий эпитоп, который имеет конформационно напряженную циклическую конфигурацию, эпитоп, который содержит аминокислотную последовательность, по крайне мере, SNK, эпитоп, соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ.
В другом варианте реализации изобретения оно представляет собой антигенный пептид, содержащий эпитоп, который имеет конформационно напряженную циклическую конфигурацию, эпитоп, который содержит аминокислотную последовательность SEQ ID NO: 1, эпитоп, соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ.
В еще одном варианте реализации изобретения оно представляет собой антитела, способные связываться с циклическим пептидом, производным Aβ, циклическим пептидом, содержащим конформационный эпитоп который имеет конформационно напряженную циклическую конфигурацию, эпитоп, который содержит аминокислотную последовательность, по крайне мере, SNK, эпитоп, соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ.
В еще одном варианте реализации изобретения оно представляет собой антитела способные связываться с циклическим пептидом, производным Aβ, циклическим пептидом, содержащим конформационный эпитоп, который имеет конформационно напряженную циклическую конфигурацию, эпитоп, который содержит аминокислотную последовательность SEQ ID NO: 1, соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ.
В частных вариантах реализации такие антитела могут связываться с олигомерными формами Aβ с большей аффинностью, чем с не олигомерными формами Aβ.
В другом варианте реализации настоящее изобретение представляет собой способ лечения объекта, имеющего болезнь Альцгеймера или подозрение на нее, способ, включающий введение объекту терапевтически эффективного количества антитела, способного связываться с циклическим пептидом, производным Aβ, где циклический пептид содержит конформационный эпитоп, имеющий аминокислотную последовательность, по крайне мере, SNK, и соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ. В частных вариантах реализации антитело может связываться с олигомерными формами Aβ с большей аффинностью, чем с не олигомерными формами Aβ.
В еще одном варианте реализации оно представляет собой способ профилактики развития или прогрессии БА у объекта, способ, включающий введение объекту терапевтически эффективного количества антитела, способного связываться с циклическим пептидом, производным Aβ, где циклический пептид содержит конформационный эпитоп, имеющий аминокислотную последовательность, по крайне мере, SNK, и соответствующий гидрофильному и доступному антителу шарнирному участку олигомерного Aβ. В частных вариантах реализации настоящего изобретения антитело может связываться с олигомерными формами Aβ с большей аффинностью, чем с не олигомерными формами Aβ.
Другие аспекты изобретения будут понятны из условий приведенного ниже описания предпочтительных вариантов реализации изобретения. Специалисту в данной области техники очевидно, что другие варианты реализации также возможны и что детали изобретения могут быть модифицированы, исходя из концепции изобретения. Таким образом, фигуры и примеры являются иллюстративными способами практического применения настоящего изобретения и не ограничивают объем настоящего изобретения.
ПРИМЕРЫ
Пример 1: Очистка и агрегация Aβ, а также характеристика олигомеров.
Трансформация, экспрессия и очистка.
Клетки E. coli BL21 (DE3) pLysS и E. coli DH5α трансформировали с помощью конструкции, кодирующей Aβ 1-40. Клетки E. coli из культуры объемом 1 л ресуспендировали в 25 мл лизирующего буфера (50 мМ Трис-HCl, pH 8,0+1 мМ этилендиаминтетрауксусная кислота (ЭДТА)) для получения гомогенизированной суспензии (ингибиторы протеаз не добавляли). Суспензию переносили в центрифужную пробирку вместимостью 40 мл (JA-20), помещали на лед и подвергали ультразвуковой обработке в течение 3 мин при интенсивности 6 (т.е. максимальной для маленькой УЗ-установки) и периодичностью 50 Гц с последующим центрифугированием в течение 10 мин при 18000 g при температуре 4°C. Процесс УЗ-обработки повторяли трижды. Растворимую фракцию отбирали после каждого цикла УЗ-обработки и анализировали методом электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (ДСН-ПААГ) (в данном случае преципитация ТХУ необязательна). Затем осадок ресуспендировали в 12,5 мл буфера, содержащего 8 M мочевину, 10 мМ Трис-HCl, pH 8,0 и 1 мМ ЭДТА, с последующим дополнительным шагом УЗ-обработки и центрифугирования (18000 об./мин в течение 10 мин). Полученный раствор затем разводили в 4 раза (добавлением 37,5 мл 10 мМ Трис, pH 8,0+1 мМ ЭДТА). Белковый раствор затем инкубировали с ДЕАЕ-целлюлозой (052, Whatman) (предварительно регенерированной 0,5 н NaOH в течение 15 мин с последующей промывкой водой и 0,5 М HCl, с последующими несколькими промывками водой и концентрированным буферным раствором (50 мМ Трис-HCl, pH 8,0+1 мМ ЭДТА)) и затем уравновешивали буфером для очистки (25 мМ Трис-HCl, pH 8,0+1 мМ ЭДТА). При этом происходило связывание пептида со смолой при условиях аккуратного перемешивания (т.е. в пробирке фалкон с магнитной мешалкой внутри, поставленной на магнитное перемешивающее устройство) в течение 20 мин. Несвязанный белок отбирали из раствора после центрифугирования в течение 1 мин при 1200 об./мин для седиментации осадка. Осадок отбирали с помощью пипетки.
Было проведено несколько промывок для удаления фракций, по 5 мин инкубации каждая, с краткой стадией центрифугирования (в течение 1 мин при 1200 об./мин) раствором следующего состава: 25 мМ ТрисHCl, pH 8,0+1 мМ EDTA с использованием, соответственно 0, 50, 75, 100, 125, 150, 200, 250, 300, 500 мМ NaCI. Элюированные фракции помещали на лед для предотвращения образования мономерной формы пептидов.
С этой целью 250 мкл отобранных фракций были проанализированы с помощью ДСН-ПААГ после преципитации ТХУ. Для преципитации ТХУ образцы инкубировали в 20% трихлоруксусной кислоте (ТХУ) по крайней мере 30 мин на льду, затем центрифугировали в течение 15 мин при 14000 об./мин. Ацетон удаляли, осадки оставляли для подсушивания. Осадок повторно растворяли с помощью красителя, окрашивающего белки, и анализировали по 8-10 мкл полученного раствора методом ДСН-ПААГ.
Методика агрегации Aβ и олигомеризации Aβ.
Для достижения мономеризации Aβ очищенный Aβ диализовали против воды miliQ и лиофилизировали. После лиофилизации Aβ восстанавливали в одном объеме ТХУ или муравьиной кислоты и высушивали для образования мономерного молекулярного слоя в стеклянной пробирке. Мономерный Aβ был ресуспендирван в 5 мМ фосфатном буферном растворе (ФБР), pH около 6,8, для поддержания Аβ в мономерной форме.
Для достижения олигомеризации Aβ в качестве исходного материала использовали мономерный Aβ; его инкубировали в количестве 200 мкМ в УЗ бане в течение 12 ч при температуре 33°C. Процедура приводила к образованию олигомеров Aβ чаще, чем фибрилл Aβ.
Характеристика олигомеров.
Размер олигомера был охарактеризован с помощью метода динамического рассеяния света (ДРС), общеизвестной методики, которую можно использовать для определения размера профиля распространения частиц в суспензии. В случае если источником света является лазер, и он является монохроматическим и когерентным, наблюдается зависимая от времени флуктуация интенсивности рассеяния. Эти флуктуации являются результатом того, что маленькие молекулы в растворе подвергаются Броуновскому движению и, таким образом, расстояние между рассеивающими свет частицами в растворе постоянно меняется со временем. Когда свет ударяется о маленькие частицы, он рассеивается во всех направлениях, что составляет процесс, известный как рассеяние Рэлея. Рассеянный свет затем подвергается конструктивной либо деструктивной интерференции со стороны окружающих частиц, в ходе чего меняется интенсивность флуктуации, содержащая информацию о временном масштабе движения частиц. Метод ДРС был использован для определения размера распространения Абета в образце в растворе и для подтверждения того, что Абета присутствует в мономерной либо в олигомерной форме.
Фиг.1 иллюстрирует, что образец Aβ, проанализированный методом ДРС, является мономерным Aβ. Коммерчески доступный Aβ (1-40) (50 мкМ) инкубировали в 5 мМ ФБР при температуре 10°C. Вычисляли радиус гидратации (Rh), который составил менее 1 нм. Эти результаты соотносятся с прогнозируемым значением Rh мономерного Aβ, составляющим менее 1 нм, который, как очевидно специалисту в данной области техники, типичен для мономерного Aβ.
Фиг.2 иллюстрирует, что образец Aβ, проанализированный методом ДРС, является олигомерным Aβ. Коммерчески доступный Aβ (1-40) (80 мкМ) инкубировали в 150 мМ ФБР при температуре 10°C. Результаты демонстрируют квазимонодисперсное распределение. Вычисляли радиус гидратации (Rh), который составил 200 нм. Эти результаты соотносятся с прогнозируемым значением Rh олигомерного Aβ, составляющим от 100 до 200 нм, который, как очевидно специалисту в данной области техники, типичен для мономерного Aβ.
Фиг.3 иллюстрирует, что образец Aβ, проанализированный методом ДРС, является олигомерным Аβ. Коммерчески доступный Aβ (1-40) (50 мкМ) инкубировали в 150 мМ ФБР при температуре 10°C. Результаты демонстрируют квазимонодисперсное распределение. Вычисляли радиус гидратации (Rh), который составил менее 190 нм. Эти результаты соотносятся с прогнозируемыми значениями для олигомерного Aβ.
Пример 2: Получение циклического пептида, содержащего конформационно напряженный эпитоп
Циклический пептид, содержащий новый конформационный эпитоп, был создан в конформации напряженной петли, используя дисульфидную связь между остатками цистеина, расположенными на N- и C-концах этого пептида. В последовательность GSNKG были добавлены два не нативных цистеина: один на C-конце и один на N-конце. Эти два цистеина были окислены в контролируемых условиях для формирования дисульфидной связи.
Структура циклического пептида была создана для имитации «шарнирной» конформации и ориентации шарнирного участка олигомеров Aβ, содержащего новый конформационный эпитоп.
Фиг 4 иллюстрирует трехмерную модель дисульфидно-циклизованного пептида, содержащего новый конформационный эпитоп SNK.
Специалисту в данной области техники очевидно, что существуют и другие методы формирования конформационно напряженного эпитопа. Например, пептид может быть циклизован путем образования связи между двумя остатками пептида с образованием замкнутой петли. Циклические пептиды могут быть описаны как гомодетные (когда все связи являются пептидными связями) или гетеродетные (когда существуют как пептидные связи, так и другие типы связей, такие как сложноэфирные, эфирные, амидные или дисульфидные связи внутри циклического пептида). Пептиды могут быть циклизованы с использованием химических или ферментативных методов. Патент США 2009/0215172 описывает рекомбинантные белки, катализирующие циклизацию пептидов от «головы» до «хвоста» с помощью амидных связей, не зависимо от последовательности пептида. Распознавание последовательностей в препептидах, окружающих интересующий пептид, вызывает циклизацию. Bourne et al (Methods in Molecular Biology, 2005 298:151-166) описывает комбинаторные методы приготовления сетей циклических пептидов путем использования безопасного захватывающего линкера и выбранной процедуры. Патент США 2004/0014100 содержит методику получения циклических пептидов in vivo. Патент США 2010/0240865, Патент США 2010/0137559 и Патент США 7,569,541 описывают различные методы циклизации пептидов; например, пептиды могут быть циклизованы путем окисления тиол- или меркаптан-содержащих остатков на С-конце, на N-конце или в середине пептида. Примерами тиол-содержащих остатков являются цистеин, гомоцистеин, пеницилламин. В некоторых вариантах реализации первый тиол-содержащий остаток является цистеином. В еще одних вариантах реализации оба (и первый, и второй) тиол-содержащие остатки являются цистеинами. Два тиол-содержащих остатка в пептиде могут быть окислены для формирования димерной аминокислоты цистеина, связанной дисульфидными связью. Для достижения такой тиол-дисульфидной конверсии может быть использовано множество окисляющих реагентов, например, кислород (воздух), диметил сульфоксид, окисленный глутатион, феррицианид калия, трифторацетат таллия (III) или другие окисляющие реагенты, известные специалисту в данной области техники, и соответствующие методы, известные специалисту в данной области техники. Примеры таких методов описаны в PCT Publication W001/92466, and Andreu et al., 1994. Methods in Molecular Biology 35:91.
Пример 3: Получение и скрининг специфичных к олигомеру Aβ моноклональных антител.
Моноклональные антитела (МАТ) к специфичному олигомеру Аβ конформационному эпитопу (SEQ ID NO: 1) были созданы путем получения антител, направленных на эпитоп с конформацией, напряженной в петле, используя дисульфидную связь между цистеинами на N- и С-концах этого пептида, как описано в Примере 2.
Мыши BALB/C были иммунизированы новым конформационно напряженным в петле эпитопом (CLE), обозначаемым далее как GSNKG-CLE, связанным с множественным антигенным пептидом (МАП) или с гемоцианином лимфы улитки (ГЛУ), которые использовали для эпитопов, специфичных к PrP и неправильно свернутым SOD1 (Paramithiotis et al. 2003; Rakhit et al. 2007). Сыворотка мыши подвергалась скринингу с помощью GSNKG-CLE, связанного с бычьим сывороточным альбумином (БСА); затем у мышей со специфичным и сильным взаимодействием с GSNKG-CLE и не структурированным растворимым Аβ выделяли клетки селезенки и осуществляли их слияние с миеломой для получения гибридомы, после чего проводили скрининг полученной гибридомы. Позитивно отобранные IgG-секретирующие клоны использовали для крупномасштабного производства с последовательной характеристикой иммунологическими методами с применением циклических и линейных GSNKG-БСА, синтетических олигомеров Аβ и олигомеров Аβ, выделенных из мозга БА.
Были созданы моноклональные антитела (МАТ) против циклических пептидов GSNKG-БСА и был проведен их предварительный скрининг методом пептидной ELISA в отношении параметров связывания. Некоторые антитела, созданные против циклических пептидов GSNKG, распознавали предпочтительно циклические пептиды, некоторые антитела распознавали линейные пептиды, а некоторые антитела распознавали как циклические, так и линейные пептиды. Способность антител распознавать линейные и циклические пептиды может быть связана, например, с иммунным распознаванием циклического пептида, который был частично или полностью линеаризован путем восстановления цистеиновых мостиков in vivo. Антитела, созданные против промежуточных пептидов GSNKG, представляют собой антитела, которые распознают и циклический, и линейный пептид. Основываясь на результатах ELISA, для дальнейших анализов были отобраны следующие клоны IgG: два антитела, специфичных к циклическим пептидам (5D8, 5E3), два антитела, специфичных к линейным пептидам (3F5, 3G2), и два антитела промежуточной специфичности (4011, 4012). Для дальнейшего анализа была использована платформа Biacore™, которая использует оптический феномен поверхностного плазмонного резонанса для мониторинга биомолекулярных взаимодействий в режиме реального времени и без необходимости мечения.
На Фиг.5 представлены показательные результаты, полученные с помощью платформы Biacore™. Моноклональные антитела были выделены из супернатанта культуры тканей и были ковалентно иммобилизованы на сенсорный чип СМ5 с помощью кроличьих антимышиных Fc-специфичных антител (RAMFc). Затем анализировали связывание антитела с конъюгированными с БСА пептидами GSNKG (линейными и циклическими) и олигомерным Aβ (1-42) путем пропускания этих аналитов через захватывающие МАТ. Полученные результаты, характеризующие связывание, сравнивали с результатами, полученными в проточной ячейке, содержащей иммобилизованные RAMFc, но не содержащей присоединенные МАТ, в растворителе образца (буферном солевом растворе Hepes, содержащем 1 мг/мл карбоксиметилдекстран), которые использовали как холостой образец. К тому же, полученные результаты были нормализованы против количества захваченных МАТ для того, чтобы обеспечить точность сравнения между несколькими МАТ.
На Фиг.6 и Фиг.7 представлены итоговые сенсограммы Biacore™, демонстрирующие отобранные с помощью ELISA клоны, предпочитающие линейный пептид (3F5, 3G2), не связавшиеся ни с линейными, ни с циклическими пептидами, связанными с БСА на чипах Biacore™; отобранные с помощью ELISA клоны, предпочитающие промежуточные пептиды (4011, 4012), связавшиеся как с циклическими, так и с линейными пептидами на чипах Biacore™; а также отобранные с помощью ELISA клоны, связавшиеся преимущественно с циклическим пептидом, связанным с БСА на чипах Biacore™. Циклические клоны 5E3 и 5D8 демонстрируют наиболее сильное связывание с олигомером Aβ (1-42) и циклическими пептидами, при этом также демонстрирует незначительное связывание с линейными пептидами, сопоставимое с промежуточными клонами, либо не демонстрируют его. Данные иллюстрируют, что антитела 5E3 демонстрируют наиболее сильное связывание с олигомером 1-42, хотя с циклическим пептидом связываются оба антитела, и 5E3, и 5D8. Эти результаты свидетельствуют, что при скрининге антител, произведенном с использованием циклического пептида из Примера 2, репертуар циклически-специфичных антител демонстрировал предпочтительное распознавание антителом эпитопа олигомерного Aβ.
Фиг.8 демонстрирует, что связывание с олигомером Aβ (1-42) MAT 5E3, клона, связывающегося преимущественно с циклическим пептидом, происходит в концентрационно-зависимом режиме. Это наблюдение демонстрирует доступный и конформационно напряженный эпитоп в олигомере Aβ, который является титруемым и совместимым с аутентичным иммунологическими взаимодействиями антиген-антитело. Таким образом, анализ с помощью Biacore™ демонстрирует, что циклический пептид GSNKG и полноразмерный олигомерный Aβ (1-42) имеют общую молекулярную черту, конформационно напряженный эпитоп, который особым образом распознается конформационно-чувствительным MAT 5E3.
МАТ, специфичные к олигомеру Aβ (1-42), могут быть также проанализированы с терапевтической целью на клеточных и животных моделях БА, а также для нейтрализации активности в нейрофизиологических анализах синаптической функции, ослабляемой олигомером Aβ.
Пример 4: Анализ методом проточной цитометрии.
Анализ методом проточной цитометрии проводили для определения степени связывания антитела с белком APP на поверхности клеток.
Здоровые взрослые мыши Black/6 были умерщвлены в камере, содержащей диоксид углерода. Мозг незамедлительно извлекали и промывали фосфатным буферным раствором (ФБР) с последующим погружением в ФБР + 1% бычью фетальную сыворотку (БФС). Отдельные суспензии клеток были получены путем крошения мозга анатомическими ножницами и серийного пропускания через сита с диаметром отверстий 100 мкм и 70 мкм. Клетки инкубировали в ФБР + 1% БФС для блокирования 30 мин при комнатной температуре. Клетки затем по отдельности инкубировали (или не инкубировали) в 100 мкл ФБР + 1% БФС плюс 10 мкг/мл или 1 мкг/мл 6E10 и 5E3. Через 1 ч при комнатной температуре клетки дважды промывали (400 g, 5 мин) и ресуспендировали в ФБР + 1% БФС с добавлением антимышиных антител, конъюгированных с аллофикоцианином (АФЦ) или флуоресцеином (ФИТЦ); оба конъюгата использовали в разведении 1:1000. Помимо чистого контроля, некоторые клетки инкубировали вместе с вторичными антителами для контроля неспецифичного взаимодействия. Вторичные антитела инкубировали с образцом 30 мин при комнатной температуре, после чего клетки промывали и либо немедленно анализировали, либо фиксировали на ночь в 4% параформальдегиде при 4°C. Для сбора данных использовали проточный цитометр A BD LSRII, для анализа данных использовали программу FlowJo.
На Фиг.9 и Фиг.10 представлены результаты анализа методом проточной цитометрии. Фиг.9 представляет собой график, полученный методом проточной цитометрии, демонстрирующий сравнение связывания меченных пан-Aβ антител 6E10 и вторичных антител негативного контроля с белком APP, расположенным на поверхности клеток. Фиг.10 демонстрирует сравнение связывания меченных антител 5E3 и вторичных антител негативного контроля с белком APP, расположенным на поверхности клеток. Антитела 6Е10, меченные ФИТЦ, представленные на Фиг.9, демонстрируют значительную степень связывания с APP, расположенным на поверхности клеток. Антитела 5E3, меченные ФИТЦ, представленные на Фиг.10, напротив, демонстрируют очень низкую степень связывания с клетками в сравнении с контролем. Эти результаты ясно показывают, что 5E3, меченные ФИТЦ, демонстрируют значительно меньшее связывание с АРР на поверхности клеток в сравнении с 6E10, меченным ФИТЦ. Результаты этих анализов демонстрируют, что конформационно напряженный специфичный олигомеру новый конформационный эпитоп не присутствует на клеточной поверхности нейронов, которая представлена линейным неструктурированным нативным мотивом GSNKG нативного APP. Отсутствие конформационно напряженного нового конформационного эпитопа на поверхности клеток свидетельствует о том, что иммунный ответ, возникающий против используемого в лечении болезни Альцгеймера циклического эпитопа, не будет нацелен на нативные APP. Эти результаты свидетельствуют, что антитела, специфически связывающиеся с циклическим эпитопом GSNKG олигомерного Aβ, имеют предпочитаемый профиль безопасности в сравнении с известными антителами 6E10.
Пример 5: Нейрональный анализ.
Анализ нейрональной токсичности проводился для определения степени выживаемости клеток на клетках, инкубированных с холостым контролем (среда), с растворимым (линейным) и олигомерным Аβ (1-40) в присутствии и при отсутствии антител 5Е3 в разных концентрациях. Холостой контроль обрабатывали только сывороткой (без антител).
Нейроны выращивали в лунках 96-луночного планшета, содержащих по 10000 крысиных первичных нейронов на каждую лунку, обработанную поли-L-Лизином (ScienCell #0403; 2 микрограмм/см2, 1 ч, 37 градусов Цельсия, промытых трижды ФБР), и содержащую по 0,2 мл нейрональной среды (ScienCell #1521). Культуральную среду меняли каждый день на протяжении 7 дней. Растворимые и олигомерные Aβ (1-40) инкубировали 4 ч в отсутствии или при наличии антител 5E3 в разных концентрациях (см. Фиг.11) в нейрональной среде при комнатной температуре на перемешивающем устройстве. 0,2 мл этой смеси добавляли к нейронам после их отделения от среды. Через 24 ч измеряли выживаемость клеток, используя Roche Cell Proliferation kit II (#11465015001) в соответствии с инструкцией производителя. Оптическую плотность измеряли с помощью плашечного считывающего устройства.
Фиг.11 иллюстрирует результаты анализа нейрональной токсичности. Аβ токсичен по отношению к нейронам в обеих, линейной и мономерной конфигурациях, а также в олигомерной конфигурации. Антитела 5E3, направленные против конформационно напряженного эпитопа Aβ, как было показано, имели протекторный эффект по отношению к олигомерным формам Aβ. Антитела 5E3 не имели протекторного эффекта по отношению к линейному Aβ. Эти результаты показывают конформационную специфичность связывания антитела 5E3.
Пример 6: Анализ методом иммуноблотинга.
Анализ методом иммуноблотинга проводили для определения относительного связывания антител 6E10 и 5E3 с APP, мономерные Aβ и олигомерные Aβ.
Гомогенизация.
Образцы тканей мозга взвешивали и последовательно погружали в объем свежего трисового буферного раствора (ТБР) на льду (с добавлением 5 мМ этилен гликоль тетрауксусной кислоты (ЕГТА), 5 мМ ЭДТА и смеси ингибиторов протеаз) таким образом, чтобы конечная концентрация тканей мозга была 20%. Ткань гомогенизировали в этом буфере, используя механический гомогенизатор, следующим образом: ткань помещали в гомогенизатор трижды на 30 сек и держали по 30 сек на льду между каждой стадией гомогенизации. Гомогенизированные в ТБР образцы помещали на ультрацентрифугу (70000 g, 90 мин). Супернатант отбирали и хранили при температуре -80°C.
Концентрацию белка в гомогенатах ТБР определяли, используя белковый анализ ВСА. В некоторых случаях эквивалентное количество белка разделяли на фракции методом ДСН-ПААГ, используя Трис-Трициновые 4-20% гели после кипячения в Трис-Трициновом буфере для образцов (Invitrogen), и переносили на 0,2 мкМ поливинилиден флоридные (ПВДФ) мембраны. После переноса мембраны погружали в ФБР и кипятили 2 раза по 3 мин каждую для теплового восстановления эпитопа. Мембраны использовали для иммуноблотинга, применяя либо антитела E610, либо антитела 5E3, специфичные к олигомеру, в качестве первичных антител. Оба антитела использовались в концентрации 1 мкг/мл.
Фиг.12 иллюстрирует результаты иммуноблотинга, демонстрирующие ткань мозга, гомогенизированную в ТБР, фракционированную на Трис-Трициновых гелях и проанализированную методом иммуноблотинга с пан- Aβ антителами 6E10. Очевидна реакция антител с APP и с мономерными формами Aβ, а также незначительная реактивность к полосе олигомера Aβ.
Фиг.13 иллюстрирует результаты иммуноблотинга для антитела 5Е3. Антитело 5E3 специфически распознает олигомерные виды массой около 45-55 кДа, очевидно, стабильные в ДСН, что свидетельствует о сильном нековалентном взаимодействии мономеров Aβ в олигомерных видах. Не наблюдалось никакой реакции с мономерными формами Aβ, хотя при иммуноблотинге выявлена некоторая ограниченная реакция с APP, что, предположительно, связано с денатурацией и частичной нативной и не нативной ренатурацией мембраны для иммуноблотинга. Пан-Aβ антитела 6E10 показали ограниченное распознавание олигомерных видов либо его отсутствие. Результаты анализа Biacore™, которые обсуждались в Примере 3 (основываясь на эмпирической формуле Biacore™ и принимая коэффициент стехиометрии между 5E3 и AB42 за 1), находятся в соответствии с результатами иммуноблотинга, демонстрирующими, что виды Aβ (1-42), которые связываются с 5E3, находятся в промежуточной форме между декамером и тридекамером, которая имеет молекулярную массу 4,0-4,3 кДа на мономер. При этом данные Biacore™ определяют молекулярную массу олигомерных видов равной около 50 кДа, что соответствует молекулярной массе основных полос, выявляемых с помощью MAT 5E3.
Пример 7: Анализ ингибирования образования олигомера Aβ.
Анализ ингибирования Aβ был проведен для определения способности антител 5E3 вызывать ослабление размножения олигомеров Aβ.
Статическое рассеяние света (CPC) - метод физической химии, который измеряет интенсивность рассеянного света для получения средней молекулярной массы (Mw) макромолекулы, такой как полимер или белок. Измерение интенсивности рассеяния под разными углами позволяет рассчитать квадратный корень радиуса, также называемого радиусом циркуляции (Rg). Измеряя интенсивность рассеивания для многих образцов в различных концентрациях, может быть рассчитан второй вириальный коэффициент A2. Для экспериментов по статическому рассеянию света монохроматический свет высокой интенсивности (обычно лазер) направляют в раствор, содержащий макромолекулы. Для измерения интенсивности рассеяния под одним или несколькими углами (θ) при данной длине волны (X) используют один или несколько детекторов.
Для измерения средней молекулярной массы напрямую, без калибровки, исходя из интенсивности рассеивания света, должны быть известны интенсивность лазера, квантовая эффективность детектора, общей объем рассеяния и пространственный угол детектора. Поскольку на практике это трудно достижимо, все коммерческие инструменты откалиброваны используют известное сильное рассеяние, например толуола, поскольку соотношение Рэлея для толуола и некоторых других растворителей было измерено, используя абсолютный рассеивающий свет инструмент.
Фиг.14 иллюстрирует способность антитела 5E3 угнетать агрегацию мономера Aβ в токсичную форму олигомера Aβ. Образование олигомера Аβ было изучено в отсутствии 5ЕЗ («C» на Фиг.14)) или в присутствии 5E3 («5E3» на Фиг.14). Aβ (1-40) коммерческого происхождения 23 (мкМ) был инкубирован при температуре 39°C в реакционной смеси объемом 150 мкл с антителами 5E3 (2,0 мкМ). Сдвиг интенсивности CPC, отмеченный с помощью стрелки, соответствовал вкладу антител 5E3 в интенсивность рассеяния. Фиг.14 иллюстрирует, что в результате инкубирования с антителами 5E3 существенно снижается образование олигомеров Aβ.
Этот ингибирующий полимеризацию эффект подтверждает терапевтическую роль антитела 5E3, а также гуманизированных и химерных антител, родственных ему, а также нового конформационного эпитопа самого по себе, например, при создании вакцин.
Пример 8: Определение олигомера Aβ в биологических образцах.
Было предположено, что очищенные антитела 5E3 могут быть использованы для определения олигомеров Aβ в биологических образцах, таких как гомогенаты тканей, включая мозг. Такое определение, которое можно проводить, используя различные способы определения, включая платформу Biacore™, может иметь диагностическое и/или прогностическое значение.
Пример 9: Терапия 5E3 и родственными антителами и вакцинами.
Терапия антителами 5E3 может быть полезной для специфичного и/или селективного очищения токсического олигомера Aβ и может быть полезной при терапии и/или предотвращении появления или развития болезней, связанных с токсичностью олигомера Aβ, таких как болезнь Альцгеймера. Человеческие либо гуманизированные антитела, направленные на тот же эпитоп, что и 5E3, будут полезны для терапии и/или профилактики болезни Альцгеймера. В другом аспекте эпитоп, совпадающий с эпитопом, распознаваемым антителом 5E3, будет полезен для терапии и/или профилактики болезни Альцгеймера.
Аналогично, описанный новый конформационный эпитоп будет, очевидно, полезным для того, чтобы вызывать специфичный иммунный ответ к олигомеру Aβ, что является полезным для терапии или профилактики, например, болезни Альцгеймера.
Вышеописанные варианты реализации являются только примерами. Изменения, модификации и вариации, являющиеся результатами частных вариантов реализации настоящего изобретения в данной области техники, неотделимы от объема изобретения, исключительно определяемого изложенными в нем притязаниями.
Список литературы
Gelinas, D.S., et al., Immunotherapy for Alzheimer’s disease. Proc Natl Acad Sci USA, 2004. 101 Suppl 2: p.14657-62.
Robinson, S.R., et al., Lessons from the AN 1792 Alzheimer vaccine: lest we forget. Neurobiol Aging, 2004. 25(5): p.609-15.
Broytman, O. and J.S. Malter, Anti-Abeta: The good, the bad, and the unforeseen. J Neurosci Res, 2004. 75(3): p.301-6.
Mathews, P.M. and R.A. Nixon, Setback for an Alzheimer’s disease vaccine: lessons learned. Neurology, 2003. 61 (1): p.7-8.
Goni, F. and E.M. Sigurdsson, New directions towards safer and effective vaccines for Alzheimer's disease. Curr Opin Mol Ther, 2005. 7(1): p.17-23.
Jung, S.S., J. Nalbantoglu, and N.R. Cashman, Alzheimer’s beta-amyloid precursor protein is expressed on the surface of immediately ex vivo brain cells: a flow cytometric study. J Neurosci Res, 1996. 46(3): p.336-48.
Jung, S.S., S. Gauthier, and N.R. Cashman, Beta-amyloid precursor protein is detectable on monocytes and is increased in Alzheimer's disease. Neurobiol Aging, 1999. 20(3): p.249-57. Morimoto, T., et al., Involvement of amyloid precursor protein in functional synapse formation in cultured hippocampal neurons. J Neurosci Res, 1998. 51 (2): p.185-95.
Mileusnic, R., C.L. Lancashire, and S.P. Rose, Amyloid precursor protein: from synaptic plasticity to Alzheimer's disease. Ann N Y Acad Sci, 2005. 1048: p.149-65.
Mileusnic, R., et al., APP is required during an early phase of memory formation. Eur J Neurosci, 2000. 12(12): p.4487-95.
Lambert, M.P., et al., Monoclonal antibodies that target pathological assemblies of Abeta. J Neurochem, 2007. 100(1): p.23-35.
Lacor, P.N., et al., Abeta oligomer-induced aberrations in synapse composition, shape, and density provide a molecular basis for loss of connectivity in Alzheimer's disease. J Neurosci, 2007. 27(4): p.796-807.
Ronicke, R., et al., Abeta mediated diminution of MTT reduction-an artefact of single cell culture? PLoS One, 2008. 3(9): p. e3236.
Balducci, C, et al., Synthetic amyloid-beta oligomers impair long-term memory independently of cellular prion protein. Proc Natl Acad Sci USA. 2010, 107(5): p.2295-300.
Shankar, G.M., et al., Amyloid-beta protein dimers isolated directly from Alzheimer’s brains impair synaptic plasticity and memory. Nat Med, 2008. 14(8): p.837-42.
Selkoe, D.J., Soluble oligomers of the amyloid beta-protein impair synaptic plasticity and behavior. Behav Brain Res, 2008. 192(1): p.106-3.
Klyubin, I., et al., Amyloid beta protein immunotherapy neutralizes Abeta oligomers that disrupt synaptic plasticity in vivo. Nat Med, 2005. 11 (5): p.556-61.
Walsh, D.M., et al., Naturally secreted oligomers of amyloid beta protein potently inhibit hippocampal long-term potentiation in vivo. Nature, 2002. 416(6880): p.535-9.
Wang, H.W., et al., Soluble oligomers of beta amyloid (1-42) inhibit long-term potentiation but not long-term depression in rat dentate gyrus. Brain Res, 2002. 924(2): p.133-40.
Lesne, S., et al., A specific amyloid-beta protein assembly in the brain impairs memory. Nature, 2006. 440(7082): p.352-7.
Lauren, J., et al., Cellular prion protein mediates impairment of synaptic plasticity by amyloidbeta oligomers. Nature, 2009. 457(7233): p.1 128-32.
Luhrs, T., et al, 3D structure of Alzheimer's amyloid-beta(1-42) fibrils. Proc Natl Acad Sci USA, 2005. 102(48): p.17342-7.
Rauk, A., Why is the amyloid beta peptide of Alzheimer's disease neurotoxic? Dalton Trans, 2008(10): p.1273-82.
| название | год | авторы | номер документа |
|---|---|---|---|
| УЛУЧШЕННЫЕ СЕЛЕКТИВНЫЕ В ОТНОШЕНИИ ПРОТОФИБРИЛЛ АНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2429244C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА И ИХ ПРИМЕНЕНИЯ | 2006 |
|
RU2432362C2 |
| МОНОКЛОНАЛЬНОЕ ТЕЛО ПРОТИВ АМИЛОИДА БЕТА | 2008 |
|
RU2571856C2 |
| АНТИТЕЛА ПРОТИВ ГЛОБУЛОМЕРА Аβ, ИХ АНТИГЕНСВЯЗЫВАЮЩИЕ ЧАСТИ, СООТВЕТСТВУЮЩИЕ ГИБРИДОМЫ, НУКЛЕИНОВЫЕ КИСЛОТЫ, ВЕКТОРЫ, КЛЕТКИ-ХОЗЯЕВА, СПОСОБЫ ПОЛУЧЕНИЯ УКАЗАННЫХ АНТИТЕЛ, КОМПОЗИЦИИ, СОДЕРЖАЩИЕ УКАЗАННЫЕ АНТИТЕЛА, ПРИМЕНЕНИЯ УКАЗАННЫХ АНТИТЕЛ И СПОСОБЫ ИСПОЛЬЗОВАНИЯ УКАЗАННЫХ АНТИТЕЛ | 2006 |
|
RU2442793C2 |
| ВАКЦИНА ПРОТИВ ИНТЕРМЕДИАТА С АМИЛОИДНЫМ СВОРАЧИВАНИЕМ | 2009 |
|
RU2546234C2 |
| ПРИМЕНЕНИЕ МИМОТОПОВ ДЛЯ ЛЕЧЕНИЯ БЕТТА-АМИЛОИДОЗОВ | 2009 |
|
RU2553345C2 |
| БЕЗОПАСНЫЕ И ФУНКЦИОНАЛЬНЫЕ ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА | 2011 |
|
RU2607368C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗОВ | 2009 |
|
RU2491953C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2008 |
|
RU2434639C2 |
| АКТИВНАЯ ИММУНИЗАЦИЯ ДЛЯ СОЗДАНИЯ АНТИТЕЛ К РАСТВОРИМОМУ А-БЕТА | 2004 |
|
RU2390350C2 |





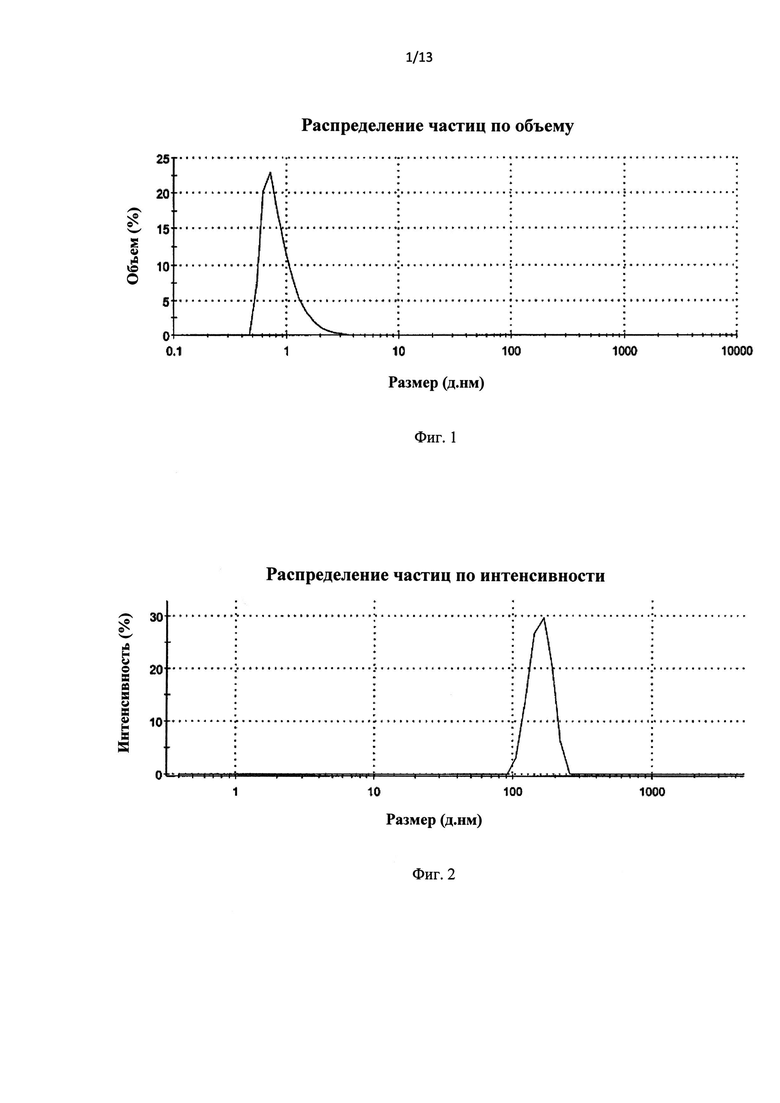
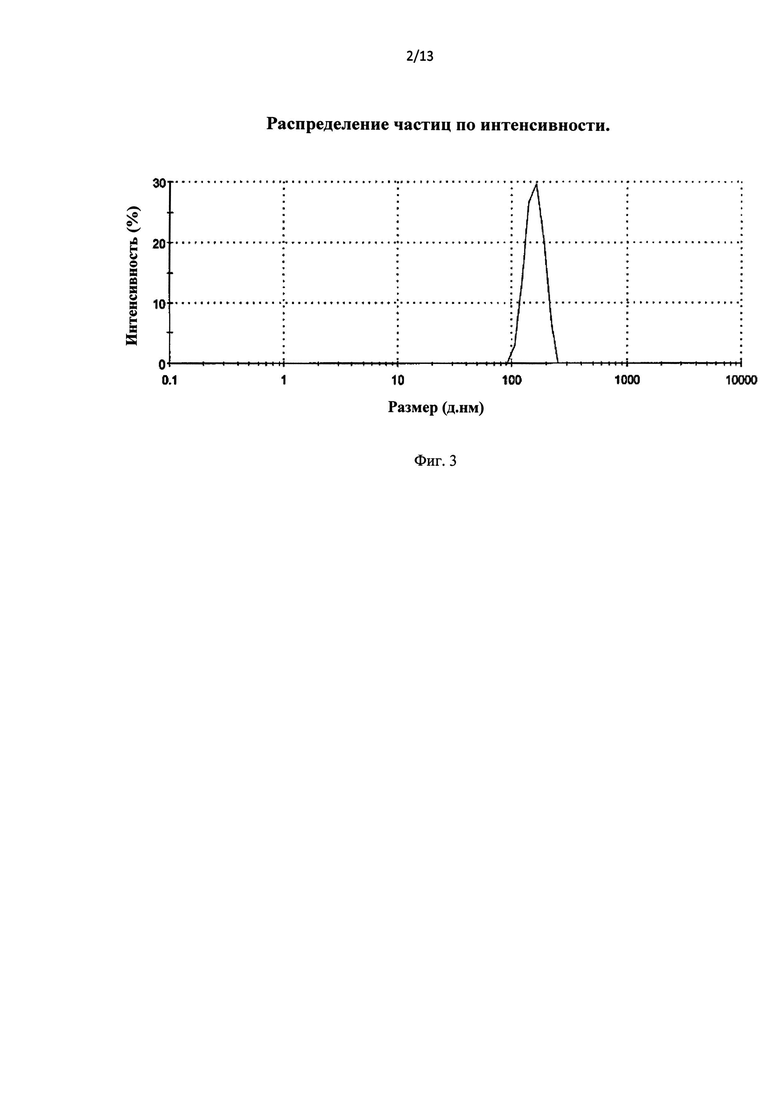
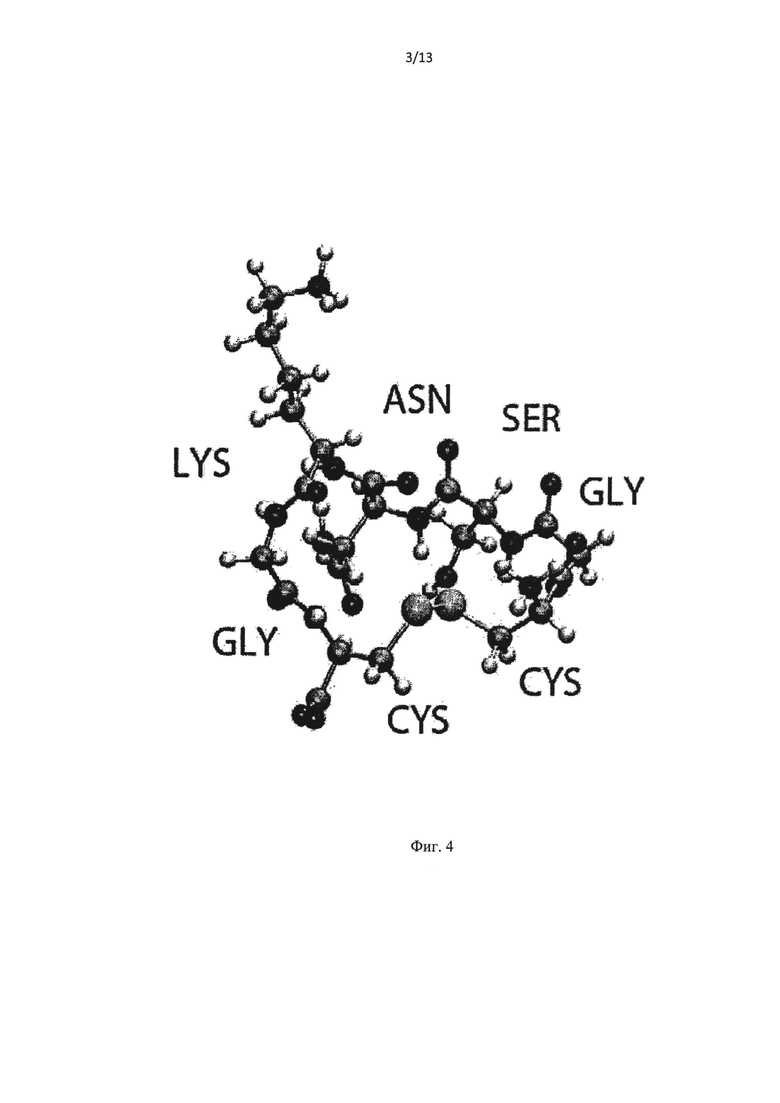
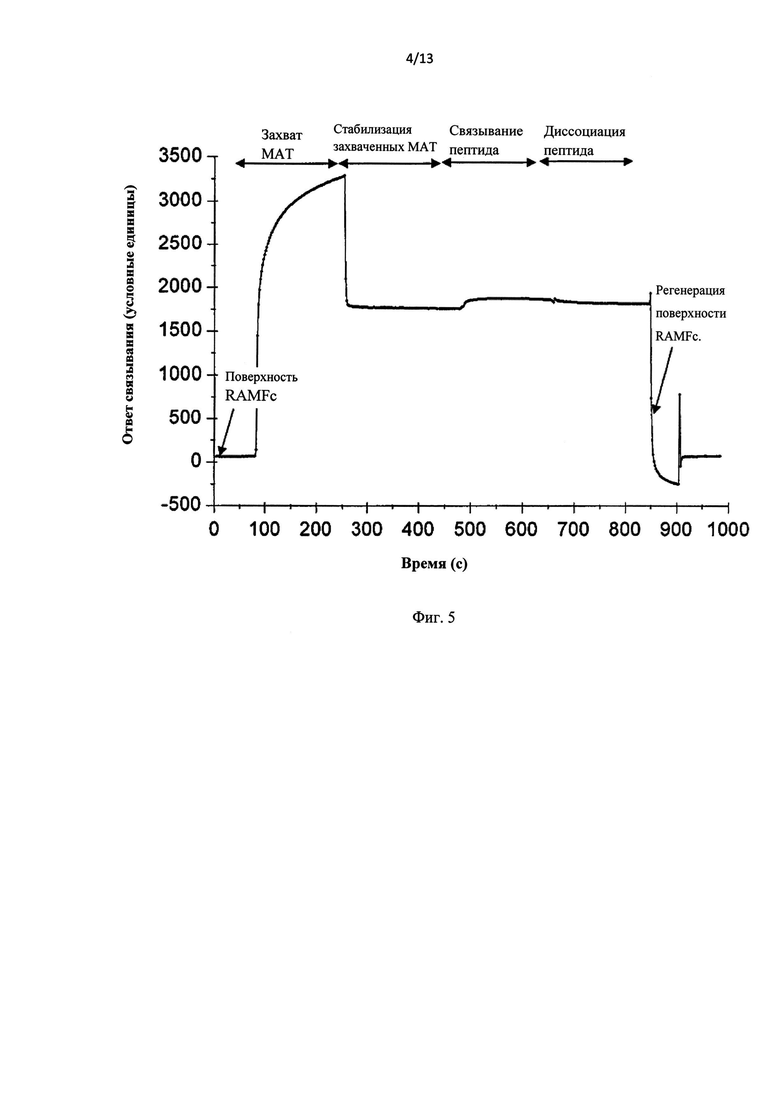
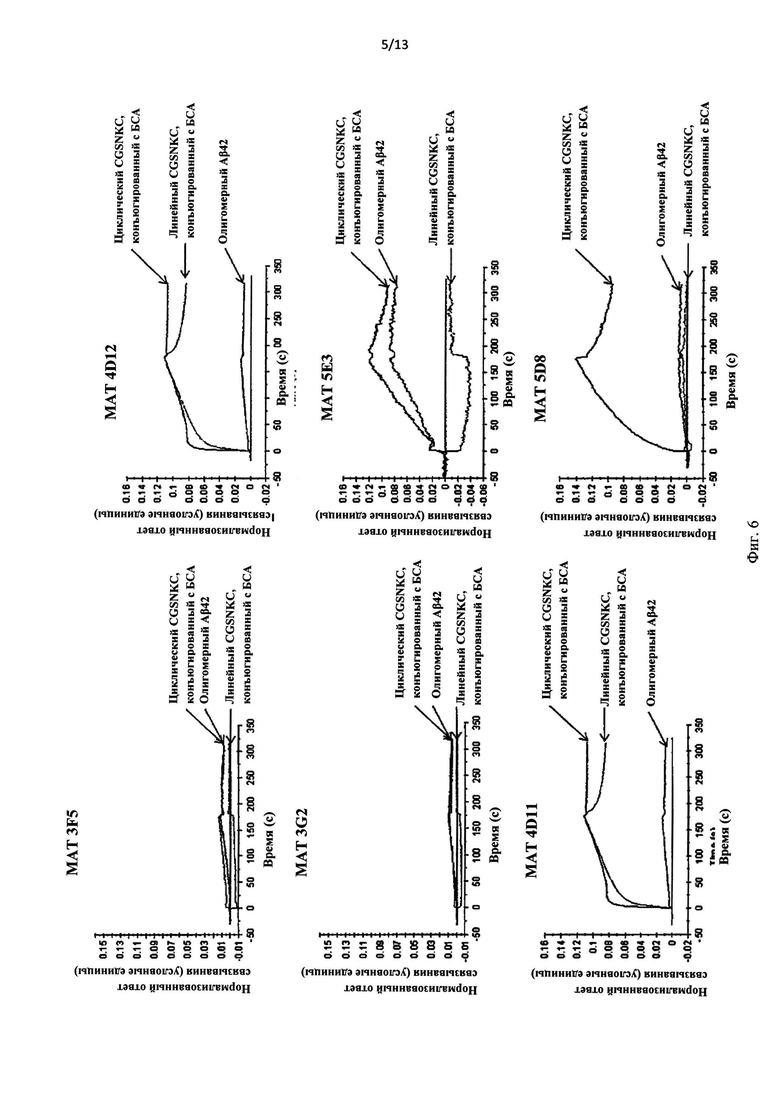
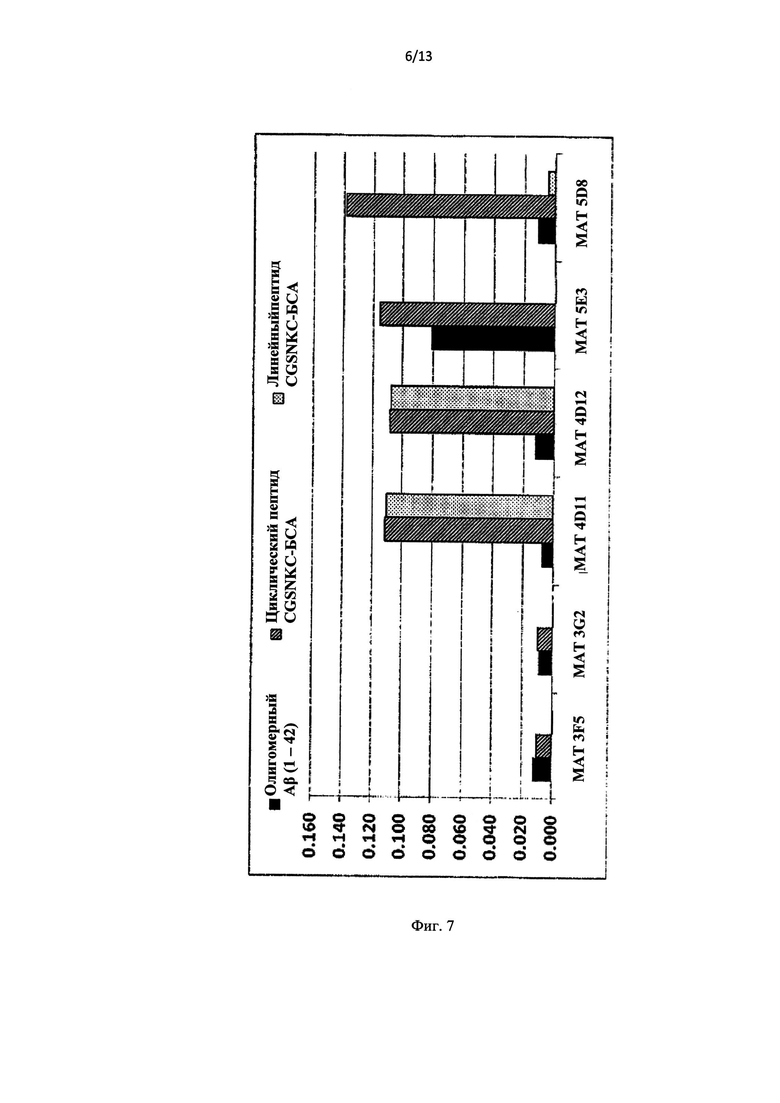
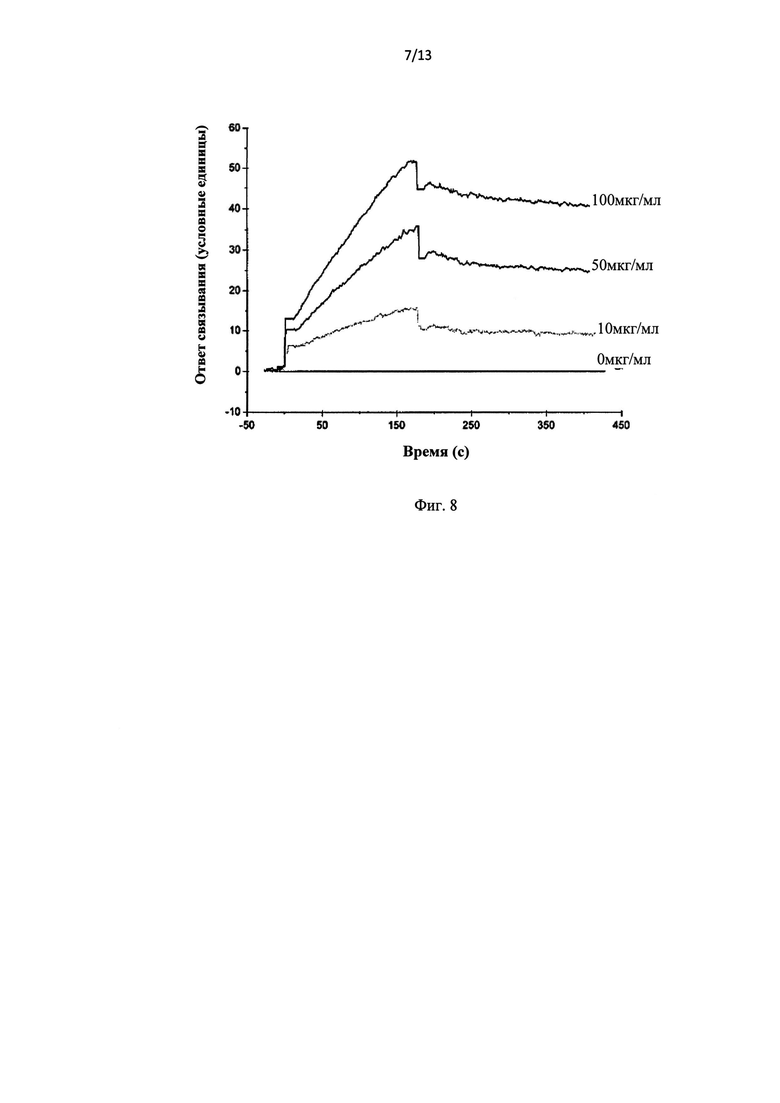
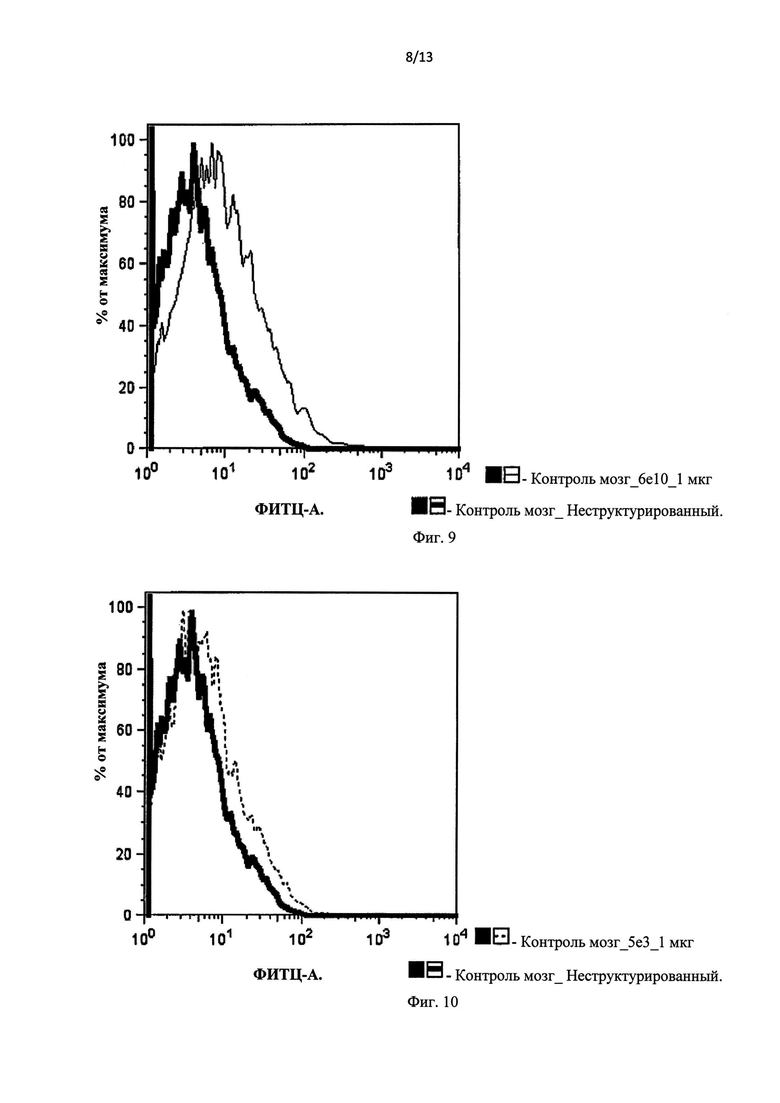
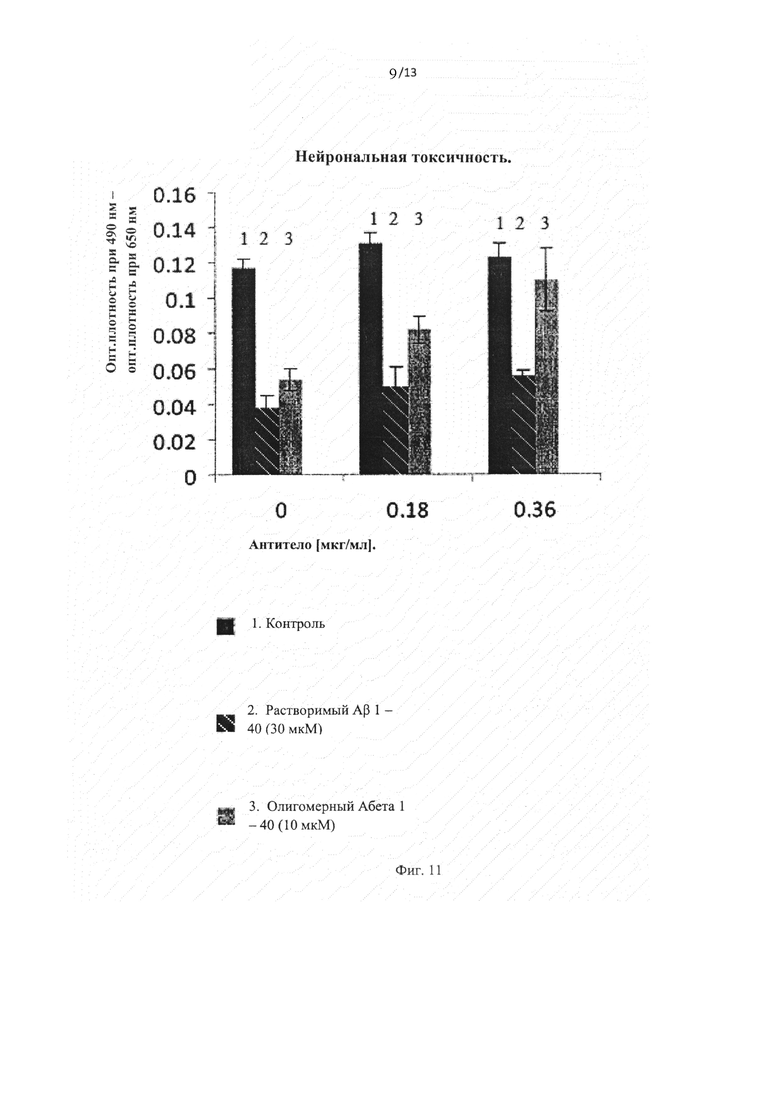
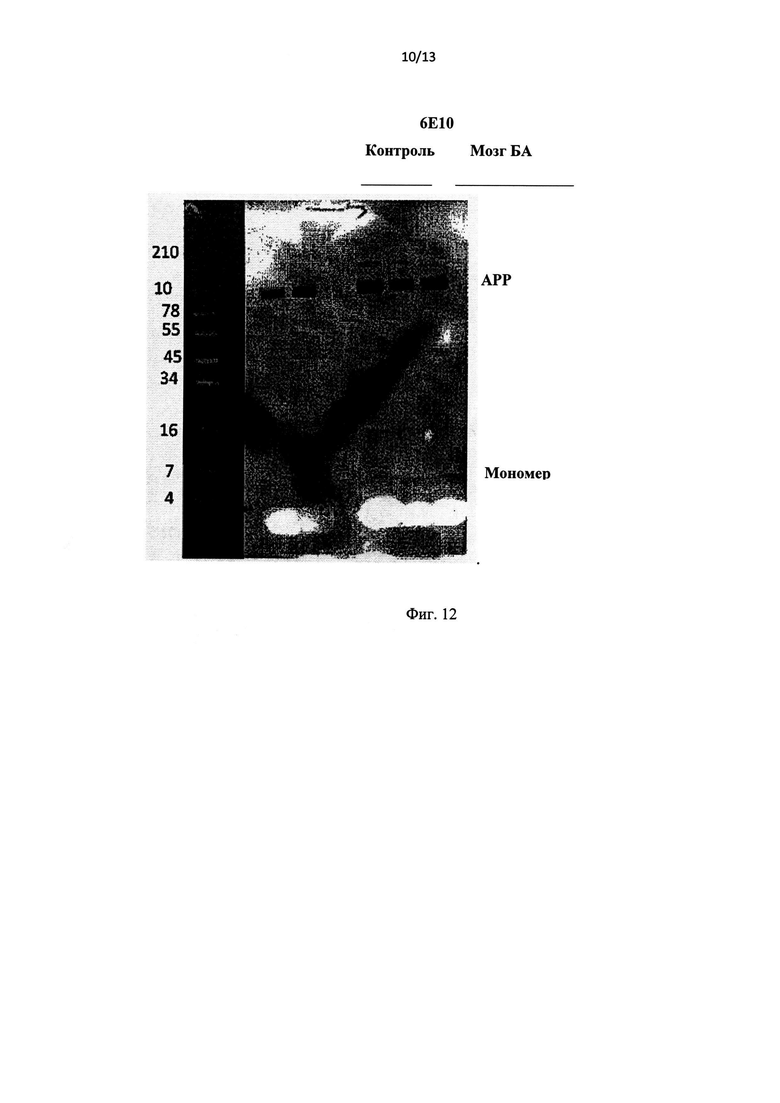
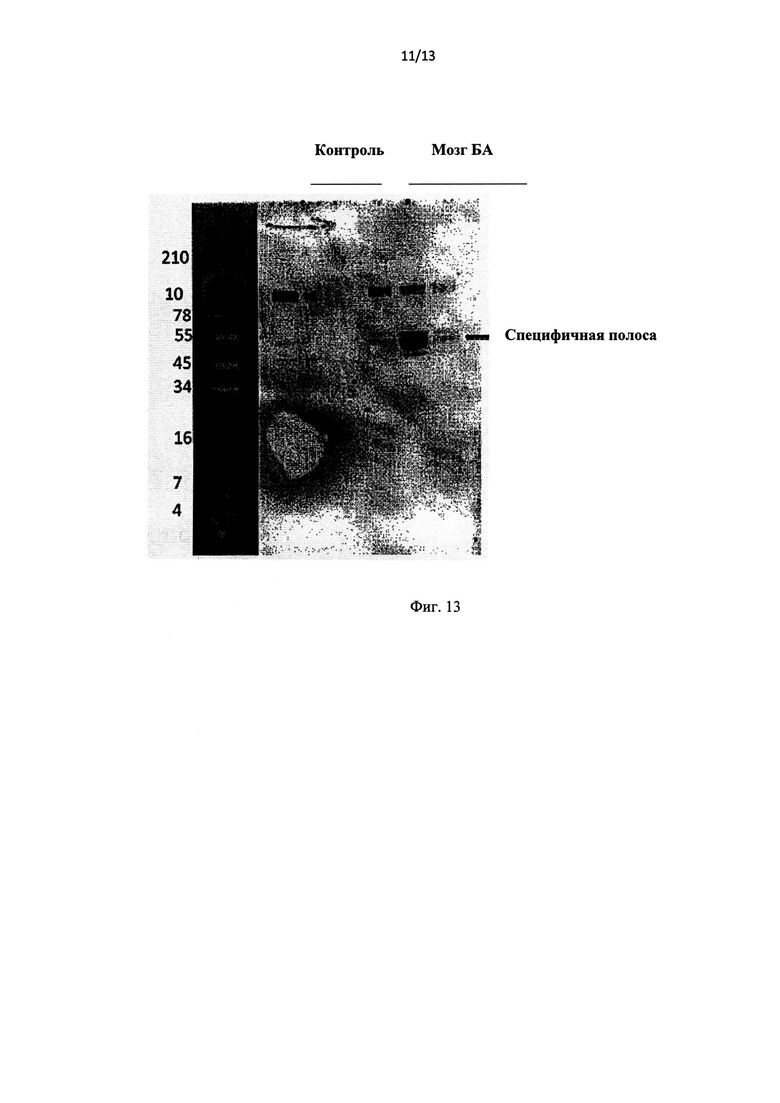
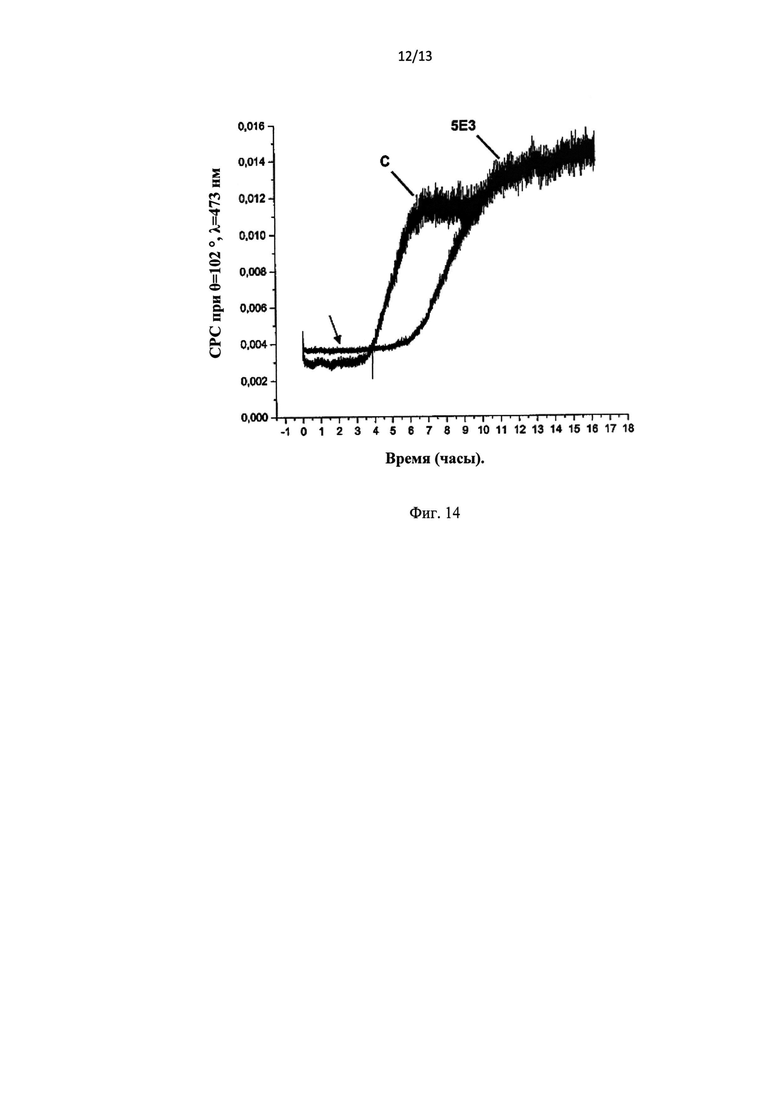

Данное изобретение относится к области иммунологии. Предложено изолированное антитело, которое обладает способностью специфично связываться с амилоидом бета (Аβ), а также антигенные циклические пептиды, способные вызывать специфический иммунный ответ против олигомерного Аβ. Описаны: иммуноконъюгат, композиции, а также применение антитела, иммуноконъюгата и вакцинной композиции для лечения или профилактики болезни Альцгеймера. Кроме того, рассмотрены способы лечения или профилактики болезни Альцгеймера, способ и набор для диагностики болезни Альцгеймера, а также нуклеиновая кислота, кодирующая изолированное антитело. Настоящее изобретение может найти дальнейшее применение в терапии и диагностике заболеваний, связанных с амилоидом бета. 13 н. и 9 з.п. ф-лы, 15 ил., 1 табл., 9 пр. 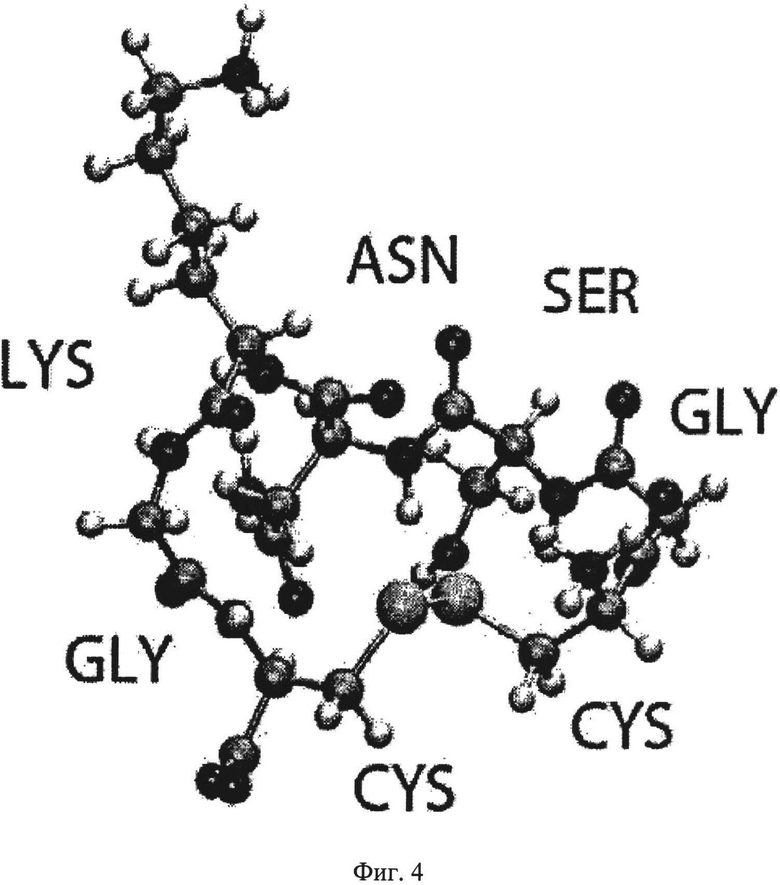
1. Изолированное антитело, специфически связывающееся с конформационным эпитопом, присутствующим на циклическом пептиде, причем указанный конформационный эпитоп имеет аминокислотную последовательность, состоящую из по меньшей мере SNK, где K (лизин) конформационного эпитопа экспонирован в раствор, причем указанное антитело обладает способностью специфично связываться с амилоидом бета (Аβ), причем указанное антитело содержит последовательности CDR (участков, определяющих комплементарность), кодируемых последовательностями нуклеиновой кислоты SEQ ID NO: 4 и 6, причем указанное антитело специфически с большей аффинностью связывается с олигомерной формой Аβ, чем с не олигомерной формой Аβ.
2. Изолированное антитело по п. 1, отличающееся тем, что указанное антитело является моноклональным.
3. Изолированное антитело по п. 1, отличающееся тем, что указанное антитело является гуманизированным.
4. Изолированное антитело по п. 1, отличающееся тем, что указанный эпитоп соответствует экспонированному в раствор доступному антителам шарнирному участку олигомерного Аβ.
5. Изолированное антитело по п. 1, дополнительно содержащее детектируемую метку, выбранную из группы, состоящей из рентгеноконтрастного соединения, радиоизотопа, флюорофора, хромофора, фермента, иона металла и любых их комбинаций.
6. Изолированное антитело по п. 1, которое связано с носителем, увеличивающим время полужизни.
7. Изолированное антитело по п. 6, отличающееся тем, что носитель, увеличивающий время полужизни, выбран из группы, состоящей из Fc-домена, полиэтиленгликоля (ПЭГ), декстрана и любых их комбинаций.
8. Антигенный циклический пептид, способный вызывать специфический иммунный ответ против олигомерного Аβ, причем указанный антигенный пептид содержит конформационный эпитоп, имеющий аминокислотную последовательность, состоящую по меньшей мере из SNK, причем K (лизин) конформационного эпитопа экспонирован в раствор, и при этом указанный конформационный эпитоп соответствует экспонированному в раствор, доступному антителам шарнирному участку олигомерного Аβ.
9. Антигенный циклический пептид, способный вызывать специфический иммунный ответ против олигомерного Aβ, причем указанный антигенный пептид содержит конформационный эпитоп, имеющий аминокислотную последовательность GSNKG (SEQ ID NO: 1), причем K (лизин) конформационного эпитопа экспонирован в раствор, и при этом указанный конформационный эпитоп соответствует экспонированному в раствор, доступному антителам шарнирному участку олигомерного Аβ.
10. Антигенный пептид по п. 8 или 9, отличающийся тем, что указанный экспонированный в раствор, доступный антителам шарнирный участок олигомерного Аβ соответствует остаткам с 25 по 29 олигомерного Аβ (1-40) или олигомерного Аβ (1-42).
11. Иммуноконъюгат для лечения или предотвращения болезни Альцгеймера, содержащий изолированное антитело по любому из пп. 1-3, дополнительно содержащий детектируемую метку.
12. Композиция для лечения или предотвращения болезни Альцгеймера, содержащая терапевтически эффективное количество изолированного антитела по любому из пп. 1-3 и фармацевтически приемлемое вспомогательное вещество или носитель.
13. Композиция вакцины против олигомеров Аβ, содержащая антигенный пептид по любому из пп. 8-10 и фармацевтически приемлемый адъювант.
14. Способ лечения или профилактики болезни Альцгеймера у пациента, нуждающегося в указанном лечении, включающий введение фармацевтически эффективного количества изолированного антитела по любому из пп. 1-3 или иммуноконъюгата по п. 11.
15. Способ лечения и профилактики болезни Альцгеймера у пациента, нуждающегося в указанном лечении, включающий введение вакцинной композиции по п. 13.
16. Способ диагностики болезни Альцгеймера у пациента, у которого предполагается наличие болезни Альцгеймера, включающий следующие шаги:
а) введение в контакт биологического образца, взятого у пациента, с антителом по любому из пп. 1-3 на протяжении времени и при условиях, достаточных для формирования комплексов антиген/антитело в образце; и
б) определение присутствия комплексов антиген/антитело в образце, где наличие комплексов означает диагноз болезни Альцгеймера у пациента.
17. Набор для диагностики болезни Альцгеймера, включающий в себя:
антитело по любому из пп. 1-3; и
конъюгат, содержащий антиген, присоединенный к соединению, генерирующему сигнал.
18. Набор по п. 17, включающий один или более агентов для детекции.
19. Набор по п. 17 или 18, дополнительно включающий инструкцию по применению для диагностики болезни Альцгеймера.
20. Применение антитела по любому из пп. 1-3 или иммуноконъюгата по п. 11 для лечения или профилактики болезни Альцгеймера.
21. Применение вакцинной композиции по п. 13 для лечения или профилактики болезни Альцгеймера.
22. Нуклеиновая кислота, кодирующая изолированное антитело по любому из пп. 1-3, причем последовательность указанной нуклеиновой кислоты идентифицирована в последовательностях SEQ ID NO: 4 и 6.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| O’NUALLAIN B | |||
| et al | |||
| "Human plasma contains cross-reactive Aβ conformer-specific IgG antibodies." Biochemistry, 2008, 47: 12254-12256 | |||
| ПОПОВА М.С., СТЕПАНИЧЕВ М.Ю., "Индукция клеточного цикла, амилоид-бета и свободные радикалы в механизме развития нейродегенеративных процессов в мозге." Нейрохимия, 2008, 25(3): 170-178. | |||
Авторы
Даты
2018-02-08—Публикация
2011-03-03—Подача