ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННУЮ ЗАЯВКУ
[001] Настоящая заявка испрашивает преимущество приоритета предварительной заявки на патент США №62/291446, поданной 4 февраля 2016 г., полное содержание которой включено в данный документ посредством ссылки.
ВКЛЮЧЕНИЕ ПЕРЕЧНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ ПОСРЕДСТВОМ ССЫЛКИ
[002] Перечень последовательностей в виде текстового файла в формате ASCII размером 38 Кб под названием 34634_10232US01_SequenceListing, созданный 2 февраля 2017 г. и поданный в Ведомство по патентам и товарным знакам США через EFS-Web, включен в данный документ посредством ссылки.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[003] Согласно данным Всемирной организации здравоохранения (WHO) главной причиной смерти ежегодно являются сердечно-сосудистые заболевания. В частности, согласно оценкам в 2012 году от сердечно-сосудистых заболеваний умерло 17,5 миллиона человек, что составляет приблизительно 31% от всех случаев смерти во всем мире. Сердечно-сосудистые заболевания включают нарушения со стороны сердца и системы крови и характеризуются наличием нескольких ассоциированных факторов риска, которые включают прежде всего поведенческие факторы риска, такие как употребление табака и/или алкоголя, неправильное питание и ожирение, а также отсутствие физической активности. Такие поведенческие факторы риска включают, например, высокое кровяное давление, высокий уровень сахара в крови и/или высокие уровни липидов в крови. Липиды (жир), которые включают как холестерин, так и триглицериды, являются нерастворимыми в крови и переносятся кровотоком с помощью липопротеинов. При наличии высоких уровней липидов в крови может увеличиваться риск развития сердечно-сосудистого заболевания и требуется контроль с помощью средств медицины и в некоторых случаях хирургическое вмешательство.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[004] Настоящее изобретение охватывает понимание того, что для обеспечения улучшенных систем in vivo для идентификации и разработки новых терапевтических средств и/или режимов терапии, которые можно применять для лечения метаболических нарушений, в некоторых вариантах осуществления характеризующихся нарушением метаболизма липидов, желательным является конструирование животных, отличных от человека. Настоящее изобретение также охватывает понимание того, что для обеспечения улучшенных систем in vivo для идентификации и разработки новых терапевтических средств, которые можно применять для лечения сердечно-сосудистых заболеваний, нарушений или состояний, желательным является конструирование животных, отличных от человека. Дополнительно, настоящее изобретение также охватывает понимание того, что животные, отличные от человека, имеющие сконструированный ген ангиопоэтин-подобного белка 8 (Angptl8) и/или иным образом экспрессирующие, содержащие (например, в крови) или продуцирующие человеческий или гуманизированный полипептид ангиопоэтин-подобный белок 8, являются желательными, например, для применения в идентификации и разработке терапевтических средств, которые можно применять для лечения гипертриглицеридемии.
[005] В некоторых вариантах осуществления предусмотрены животные, отличные от человека, имеющие геном, содержащий сконструированный ген Angptl8, при этом данный сконструированный ген Angptl8 содержит генетический материал от двух различных видов (например, человека и вида, отличного от человека). В некоторых вариантах осуществления такой сконструированный ген Angptl8 содержит генетический материал, который кодирует один или более суперспиральных доменов человеческого полипептида ANGPTL8. В некоторых вариантах осуществления такой сконструированный ген Angptl8 содержит генетический материал, который кодирует полную или неполную N-концевую область человеческого полипептида ANGPTL8. Таким образом, в некоторых вариантах осуществления сконструированный ген Angptl8 животного, отличного от человека, описанного в данном документе, кодирует полипептид Angptl8, имеющий последовательность, являющуюся полностью или практически полностью человеческой. В различных вариантах осуществления полипептид Angptl8, экспрессируемый животным, отличным от человека, описанным в данном документе, экспрессируется под контролем промотора, отличного от человеческого (например, промотора Angptl8, отличного от человеческого).
[006] В некоторых вариантах осуществления предусмотрено животное, отличное от человека, геном которого содержит ген Angptl8, содержащий эндогенную часть и человеческую часть, где эндогенная и человеческая части функционально связаны с регуляторными элементами Angptl8, отличными от человеческих.
[007] В некоторых вариантах осуществления предусмотрено животное, отличное от человека, которое экспрессирует человеческий полипептид ANGPTL8 под контролем регуляторных элементов Angptl8, отличных от человеческих.
[008] В некоторых вариантах осуществления эндогенная часть гена Angptl8 включает или содержит эндогенный промотор Angptl8, отличный от человеческого. В некоторых вариантах осуществления эндогенная часть гена Angptl8 включает или содержит 3'-концевую область или последовательность, расположенную непосредственно ниже 3'-концевой нетранслируемой области эндогенного гена Angptl8, отличного от человеческого, в эндогенном локусе Angptl8, отличном от человеческого.
[009] В некоторых вариантах осуществления эндогенная часть гена Angptl8 включает или содержит 5'-концевую и/или 3'-концевую нетранслируемые области (UTR). В некоторых вариантах осуществления эндогенная часть гена Angptl8 содержит 5'-концевую и/или 3'-концевую нетранслируемые области (UTR) и дополнительно содержит стартовый кодон ATG эндогенного Angptl8. В некоторых вариантах осуществления каждая из 5'-концевой и 3'-концевой UTR эндогенного гена Angptl8 имеет последовательность, практически идентичную или идентичную соответствующим 5'-концевой и 3'-концевой UTR, присутствующим в гене Angptl8 грызуна. В некоторых определенных вариантах осуществления каждая из 5'-концевой и 3'-концевой UTR эндогенного гена Angptl8 имеет последовательность, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичную соответствующим 5'-концевым и 3'-концевым UTR, присутствующим в SEQ ID NO:1 или SEQ ID NO:3.
[0010] В некоторых вариантах осуществления ген Angptl8, описанный в данном документе, кодирует полипептид, имеющий последовательность, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичную SEQ ID NO:6 или SEQ ID NO:8. В некоторых вариантах осуществления ген Angptl8, описанный в данном документе, кодирует полипептид, имеющий последовательность, практически идентичную или идентичную SEQ ID NO:6 или SEQ ID NO:8.
[0011] В некоторых вариантах осуществления человеческая часть включает или содержит полные или неполные экзоны 1-4 человеческого гена ANGPTL8. В некоторых вариантах осуществления полные или неполные экзоны 1-4 человеческого гена ANGPTL8 по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичны соответствующим полным или неполным экзонам 1-4, присутствующим в последовательности mRNA человеческого ANGPTL8 под SEQ ID NO:5. В некоторых вариантах осуществления полные или неполные экзоны 1-4 человеческого гена ANGPTL8 практически идентичны или идентичны соответствующим полным или неполным экзонам 1-4, присутствующим в последовательности mRNA человеческого ANGPTL8 под SEQ ID NO:5. В некоторых вариантах осуществления человеческая часть дополнительно содержит 3'-концевую UTR человеческого гена ANGPTL8. В некоторых вариантах осуществления человеческая часть содержит последовательность, являющуюся кодон-оптимизированной для экспрессии у животного, отличного от человека.
[0012] В некоторых вариантах осуществления человеческий полипептид ANGPTL8 включает или содержит аминокислотную последовательность, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичную аминокислотным остаткам 22-198 в SEQ ID NO:6 или SEQ ID NO:8. В некоторых вариантах осуществления человеческий полипептид ANGPTL8 включает или содержит аминокислотную последовательность, практически идентичную или идентичную аминокислотным остаткам 22-198 в SEQ ID NO:6 или SEQ ID NO:8.
[0013] В некоторых вариантах осуществления человеческий полипептид ANGPTL8 кодируется последовательностью, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичной SEQ ID NO:9. В некоторых вариантах осуществления человеческий полипептид ANGPTL8 кодируется последовательностью, практически идентичной или идентичной SEQ ID NO:9. В некоторых вариантах осуществления человеческий полипептид ANGPTL8 кодируется последовательностью, являющейся кодон-оптимизированной.
[0014] В некоторых вариантах осуществления человеческий полипептид ANGPTL8 представляет собой вариант человеческого полипептида ANGPTL8. В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 характеризуется аминокислотной заменой R59W. В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 характеризуется аминокислотной заменой Q121X. В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 характеризуется более низкими уровнями холестерина липопротеинов низкой плотности (LDL) и/или холестерина липопротеинов высокой плотности (HDL) в плазме крови или ассоциирован с ними. В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 характеризуется повышенными уровнями триглицеридов или ассоциирован с ними. В некоторых вариантах осуществления человеческий полипептид ANGPTL8 кодируется последовательностью нуклеиновой кислоты, размещенной в эндогенном локусе Angptl8, отличном от человеческого.
[0015] В некоторых вариантах осуществления предусмотрены выделенные клетка или ткань, отличные от человеческой, геном которых содержит ген Angptl8, описанный в данном документе. В некоторых вариантах осуществления клетка представляет собой лимфоцит. В некоторых вариантах осуществления клетка выбрана из B-клетки, дендритной клетки, макрофага, моноцита и T-клетки. В некоторых вариантах осуществления ткань выбрана из жировой ткани, ткани мочевого пузыря, головного мозга, молочной железы, костного мозга, глаза, сердца, кишечника, почки, печени, легкого, лимфатического узла, мышцы, поджелудочной железы, плазмы крови, сыворотки крови, кожи, селезенки, желудка, вилочковой железы, яичка, яйцеклетки и их комбинации.
[0016] В некоторых вариантах осуществления предусмотрена иммортализованная клетка, созданная, образованная или полученная из выделенной клетки, отличной от человеческой, описанной в данном документе.
[0017] В некоторых вариантах осуществления предусмотрена эмбриональная стволовая клетка (ES), отличная от человеческой, геном которой содержит ген Angptl8, описанный в данном документе. В некоторых вариантах осуществления эмбриональная стволовая клетка, отличная от человеческой, представляет собой эмбриональную стволовую клетку грызуна. В некоторых определенных вариантах осуществления эмбриональная стволовая клетка грызуна представляет собой эмбриональную стволовую клетку мыши и получена из линии 129, линии C57BL или их помеси. В некоторых определенных вариантах осуществления эмбриональная стволовая клетка грызуна представляет собой эмбриональную стволовую клетку мыши и является помесью линий 129 и C57BL.
[0018] В некоторых вариантах осуществления предусмотрено применение эмбриональной стволовой клетки, отличной от человеческой, описанной в данном документе, для получения животного, отличного от человека. В некоторых определенных вариантах осуществления эмбриональная стволовая клетка, отличная от человеческой, представляет собой эмбриональную стволовую клетку мыши и применяется для получения мыши, содержащей ген (или локус) Angptl8, описанный в данном документе. В некоторых определенных вариантах осуществления эмбриональная стволовая клетка, отличная от человеческой, представляет собой эмбриональную стволовую клетку крысы и применяется для получения крысы, содержащей ген (или локус) Angptl8, описанный в данном документе.
[0019] В некоторых вариантах осуществления предусмотрен эмбрион, отличный от человеческого, содержащий описанную в данном документе эмбриональную стволовую клетку, отличную от человеческой, созданный из нее, полученный из нее или полученный за счет нее. В некоторых определенных вариантах осуществления эмбрион, отличный от человеческого, представляет собой эмбрион грызуна; в некоторых вариантах осуществления - эмбрион мыши; в некоторых вариантах осуществления - эмбрион крысы.
[0020] В некоторых вариантах осуществления предусмотрено применение эмбриона, отличного от человеческого, описанного в данном документе, для получения животного, отличного от человека. В некоторых определенных вариантах осуществления эмбрион, отличный от человеческого, представляет собой эмбрион мыши и применяется для получения мыши, содержащей ген (или локус) Angptl8, описанный в данном документе. В некоторых определенных вариантах осуществления эмбрион, отличный от человеческого, представляет собой эмбрион крысы и применяется для получения крысы, содержащей ген (или локус) Angptl8, описанный в данном документе.
[0021] В некоторых вариантах осуществления предусмотрен набор, содержащий выделенные клетку или ткань, отличные от человеческой, описанную в данном документе, иммортализованную клетку, описанную в данном документе, эмбриональную стволовую клетку, отличную от человеческой, описанную в данном документе, эмбрион, отличный от человеческого, описанный в данном документе, или животное, отличное от человека, описанное в данном документе.
[0022] В некоторых вариантах осуществления предусмотрен набор, описанный в данном документе, для применения в производстве и/или разработке лекарственного средства (например, антитела или его антигенсвязывающего фрагмента) для терапии или диагностики.
[0023] В некоторых вариантах осуществления предусмотрен набор, описанный в данном документе, для применения в производстве и/или разработке лекарственного средства (например, антитела или его антигенсвязывающего фрагмента) для лечения, предупреждения или уменьшения интенсивности проявлений заболевания, нарушения или состояния.
[0024] В некоторых вариантах осуществления предусмотрены трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор, описанные в данном документе. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор содержат полный или неполный ген (или локус) Angptl8, описанный в данном документе. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор содержат фрагмент ДНК, содержащий полный или неполный ген (или локус) Angptl8, описанный в данном документе. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор содержат ген (или локус) Angptl8, содержащий любую из SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:15, SEQ ID NO:16 и SEQ ID NO:17. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор содержат ген (или локус) Angptl8, содержащий SEQ ID NO:15, SEQ ID NO:16 и SEQ ID NO:17. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор дополнительно содержат один или более селективных маркеров. В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор дополнительно содержат один или более сайтов сайт-специфической рекомбинации (например, loxP, Frt или их комбинации). В некоторых определенных вариантах осуществления трансген, конструкция на основе нуклеиновой кислоты, ДНК-конструкция или нацеливающийся вектор изображены на фигуре 3.
[0025] В некоторых вариантах осуществления предусмотрено применение трансгена, конструкции на основе нуклеиновой кислоты, ДНК-конструкции или нацеливающегося вектора, описанных в данном документе, для получения эмбриональной стволовой клетки, отличной от человеческой, клетки, отличной от человеческой, эмбриона, отличного от человеческого, и/или животного, отличного от человека.
[0026] В некоторых вариантах осуществления предусмотрен способ получения животного, отличного от человека, которое экспрессирует человеческий полипептид ANGPTL8 с эндогенного гена Angptl8, при этом способ включает (a) помещение геномного фрагмента в эндогенный ген Angptl8 в эмбриональной стволовой клетке, отличной от человеческой, при этом указанный геномный фрагмент содержит нуклеотидную последовательность, которая кодирует полный или неполный человеческий полипептид ANGPTL8; (b) получение эмбриональной стволовой клетки, отличной от человеческой, образованной на (a); и (c) создание животного, отличного от человека, с применением эмбриональной стволовой клетки, отличной от человеческой, из (b).
[0027] В некоторых вариантах осуществления нуклеотидная последовательность содержит полные или неполные экзоны 1-4 человеческого гена ANGPTL8. В некоторых вариантах осуществления нуклеотидная последовательность дополнительно содержит 3'-концевую UTR человеческого гена ANGPTL8. В некоторых вариантах осуществления нуклеотидная последовательность кодирует зрелую форму (т.е. не имеющую сигнального пептида) человеческого полипептида ANGPTL8. В некоторых вариантах осуществления нуклеотидная последовательность кодирует аминокислоты 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8. В некоторых вариантах осуществления нуклеотидная последовательность содержит один или более селективных маркеров. В некоторых вариантах осуществления нуклеотидная последовательность содержит один или более сайтов сайт-специфической рекомбинации. В некоторых вариантах осуществления нуклеотидная последовательность содержит ген рекомбиназы и селективный маркер, фланкированные сайтами распознавания для рекомбиназы, при этом сайты распознавания для рекомбиназы ориентированы для направления вырезания. В некоторых вариантах осуществления ген рекомбиназы функционально связан c промотором, который управляет экспрессией гена рекомбиназы в дифференцированных клетках и не управляет экспрессией гена рекомбиназы в недифференцированных клетках. В некоторых вариантах осуществления ген рекомбиназы функционально связан c промотором, который является транскрипционно компетентным и регулируемым в процессе развития. В некоторых вариантах осуществления промотор, который является транскрипционно компетентным и регулируемым в процессе развития, представляет собой или содержит SEQ ID NO:12, SEQ ID NO:13 или SEQ ID NO:14; в некоторых определенных вариантах осуществления промотор, который является транскрипционно компетентным и регулируемым в процессе развития, представляет собой или содержит SEQ ID NO:12. В некоторых вариантах осуществления нуклеотидная последовательность содержит одну или более последовательностей, являющихся кодон-оптимизированными для экспрессии у животного, отличного от человека. В некоторых вариантах осуществления способа получения животного, отличного от человека, которое экспрессирует человеческий полипептид ANGPTL8 с эндогенного гена Angptl8, способ дополнительно включает стадию разведения грызуна, полученного на (c), для того, чтобы создать грызуна, гомозиготного по экспрессии человеческого полипептида ANGPTL8 с эндогенного гена Angptl8.
[0028] В некоторых вариантах осуществления предусмотрен способ получения животного, отличного от человека, геном которого содержит ген Angptl8, кодирующий человеческий полипептид ANGPTL8, при этом способ включает модификацию генома животного, отличного от человека, таким образом, чтобы он содержал ген Angptl8, кодирующий человеческий полипептид ANGPTL8 под контролем регуляторных последовательностей Angptl8 животного, отличного от человека, за счет чего обеспечивается получение указанного животного, отличного от человека.
[0029] В некоторых вариантах осуществления ген Angptl8 модифицируют таким образом, чтобы он содержал полные или неполные экзоны 1-4 человеческого гена ANGPTL8. В некоторых вариантах осуществления ген Angptl8 модифицируют таким образом, чтобы он содержал полные или неполные экзоны 1-4 человеческого гена ANGPTL8, и модифицируют таким образом, чтобы он дополнительно содержал 3'-концевую UTR человеческого гена ANGPTL8.
[0030] В некоторых вариантах осуществления предусмотрено животное, отличное от человека, получаемое (созданное, полученное или образованное) посредством любого из способов, описанных в данном документе.
[0031] В некоторых вариантах осуществления предусмотрен способ оценки эффективности лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, в снижении уровней триглицеридов, при этом способ включает стадии введения лекарственного средства животному, отличному от человека, описанному в данном документе, и проведения анализа для определения одного или более свойств снижения уровней триглицеридов у лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8.
[0032] В некоторых вариантах осуществления предусмотрен способ оценки фармакокинетических свойств лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, при этом способ включает стадии введения лекарственного средства животному, отличному от человека, описанному в данном документе, и проведения анализа для определения одного или более фармакокинетических свойств лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8.
[0033] В некоторых вариантах осуществления лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, является антагонистом ANGPTL8. В некоторых вариантах осуществления лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, является агонистом ANGPTL8. В некоторых вариантах осуществления лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, представляет собой антитело к ANGPTL8. В некоторых вариантах осуществления лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, вводят грызуну внутривенно, внутрибрюшинно или подкожно.
[0034] В некоторых вариантах осуществления предусмотрено животное, отличное от человека, геном которого содержит сконструированный ген Angptl8, содержащий эндогенную часть, которая содержит 5'-концевую UTR эндогенного гена Angptl8, и человеческую часть, которая содержит полные или неполные экзоны 1-4 и 3'-концевую UTR человеческого гена ANGPTL8, где человеческая часть функционально связана со стартовым кодоном ATG эндогенного Angptl8, отличного от человеческого, и функционально связана с эндогенным промотором Angptl8, отличным от человеческого, и где животное, отличное от человека, экспрессирует человеческий полипептид ANGPTL8 в своей сыворотке крови. Сконструированный ген Angptl8 также может содержать 3'-концевую UTR эндогенного гена Angptl8 и/или 3'-концевую последовательность, расположенную непосредственно ниже 3'-концевой UTR эндогенного гена Angptl8 в эндогенном локусе Angptl8, или быть соединенным с ними или располагаться перед ними.
[0035] В некоторых вариантах осуществления предусмотрена модель гипертриглицеридемии на животных, отличных от человека, где животное, отличное от человека, экспрессирует человеческий полипептид ANGPTL8, описанный в данном документе.
[0036] В некоторых вариантах осуществления предусмотрена модель гипертриглицеридемии на животных, отличных от человека, где животное, отличное от человека, имеет геном, содержащий ген Angptl8, описанный в данном документе.
[0037] В некоторых вариантах осуществления предусмотрены животное, отличное от человека, или клетка, отличная от человеческой, описанные в данном документе, для применения в производстве и/или разработке лекарственного средства для терапии или диагностики.
[0038] В некоторых вариантах осуществления предусмотрено применение животного, отличного от человека, или клетки, отличной от человеческой, описанных в данном документе, в производстве и/или разработке лекарственного средства или вакцины для применения в медицине, как, например, для применения в качестве лекарственного препарата.
[0039] В некоторых вариантах осуществления предусмотрено животное, отличное от человека, или клетка, отличная от человеческой, описанные в данном документе, для применения в производстве лекарственного препарата для лечения, предупреждения или уменьшения интенсивности проявлений заболевания, нарушения или состояния. В некоторых вариантах осуществления заболевание, нарушение или состояние представляют собой гипертриглицеридемию. В некоторых вариантах осуществления заболевание, нарушение или состояние представляют собой сердечно-сосудистое заболевание, нарушение или состояние.
[0040] В некоторых вариантах осуществления предусмотрено применение животного, отличного от человека, или клетки, отличной от человеческой, описанных в данном документе, в производстве лекарственного препарата для лечения заболевания, нарушения или состояния, характеризующихся нарушением метаболизма липидов.
[0041] В некоторых вариантах осуществления предусмотрено применение животного, отличного от человека, или клетки, отличной от человеческой, описанных в данном документе, в производстве и/или разработке антитела, которое связывается с человеческим ANGPTL8.
[0042] В различных вариантах осуществления регуляторные элементы Angptl8, отличные от человеческих, включают промотор Angptl8, отличный от человеческого; в некоторых определенных вариантах осуществления - эндогенный промотор Angptl8, отличный от человеческого.
[0043] В различных вариантах осуществления ген Angptl8, описанный в данном документе, представляет собой гуманизированный ген Angptl8.
[0044] В различных вариантах осуществления человеческая часть гена Angptl8 кодирует аминокислотную последовательность, кодируя при этом, помимо прочего, аминокислотную последовательность человеческого полипептида ANGPTL8, которая отвечает за связывание с липидами или связывание с ANGPTL3.
[0045] В различных вариантах осуществления человеческая часть полипептида Angptl8 содержит аминокислотную последовательность суперспирального(суперспиральных) домена(доменов) или N-концевую область человеческого полипептида ANGPTL8.
[0046] В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, экспрессируют человеческий полипептид ANGPTL8, выявляемый в сыворотке крови животного, отличного от человека. В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, не экспрессируют эндогенный полипептид Angptl8 в сыворотке крови животного, отличного от человека, на выявляемом уровне.
[0047] В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат ген (или локус) Angptl8, который содержит SEQ ID NO:9 или SEQ ID NO:11. В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат ген (или локус) Angptl8, который содержит SEQ ID NO:15 и SEQ ID NO:18.
[0048] В различных вариантах осуществления животное, отличное от человека, описанное в данном документе, представляет собой грызуна; в некоторых вариантах осуществления - мышь; в некоторых вариантах осуществления - крысу. В некоторых вариантах осуществления мышь, описанная в данном документе, выбрана из группы, состоящей из линии 129, линии BALB/C, линии C57BL/6 и линии смешанного происхождения 129xC57BL/6; в некоторых определенных вариантах осуществления - линии C57BL/6.
[0049] Используемые в настоящей заявке термины «приблизительно» и «примерно» используются в качестве эквивалентов. Предполагается, что все числа, используемые в настоящей заявке, вместе с термином «приблизительно/примерно» или без него охватывают любые нормальные отклонения, понятные специалисту в соответствующей области техники.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0050] Графические материалы, включенные в данный документ, которые состоят из нижеследующих фигур, приведены только в иллюстративных целях, а не для ограничения.
[0051] На фигуре 1 показана типичная схема геномной организации отличного от человеческого (например, мышиного) и человеческого генов ангиопоэтин-подобного белка 8 (ANGPTL8) без соблюдения масштаба. Экзоны пронумерованы под каждым экзоном. Нетранслируемые области (незакрашенные прямоугольники) также указаны для каждого гена. Относительные части кодирующей последовательности, которые кодируют сигнальные пептиды, указаны над экзоном 1 для каждого гена.
[0052] На фигуре 2 показано выравнивание типичных аминокислотных последовательностей человеческого ANGPTL8 (hANGPTL8, SEQ ID NO:6), мышиного Angptl8 (mAngptl8, SEQ ID NO:4), крысиного Angptl8 (rAngptl8, SEQ ID NO:2) и сконструированного Angptl8 (engAngptl8; SEQ ID NO:8). Звездочкой (*) указаны идентичные аминокислоты; двоеточием (:) указаны консервативные замены; точкой (.) указаны полуконсервативные замены; пробелом указаны неконсервативные замены; аминокислотными остатками в рамке указан сигнальный пептид.
[0053] На фигуре 3 показана типичная схема иллюстративного способа гуманизации гена Angptl8, отличного от человеческого, без соблюдения масштаба. Вверху: нацеливающийся вектор, полученный согласно примеру 1, для вставки в мышиный локус Angptl8 посредством гомологичной рекомбинации; внизу: целевой мышиный локус Angptl8 после вставки нацеливающегося вектора посредством гомологичной рекомбинации и опосредованного рекомбиназой удаления селекционной кассеты. Выбранные месторасположения участков сочленения нуклеотидов отмечены линией под каждым участком сочленения, и каждый из них указан с помощью SEQ ID NO.
[0054] На фигуре 4 показана типичная схема геномной организации мышиного и человеческого генов ангиопоэтин-подобного белка 8 (ANGPTL8) без соблюдения масштаба, на которой указаны примерные месторасположения зондов, используемых в анализе, описанном в примере 1. Значения длины иллюстративного синтетического фрагмента ДНК, используемого при гуманизации эндогенного мышиного гена Angptl8, и соответствующей делеции указаны под каждым соответствующим геном и описаны в примере 1.
[0055] На фигуре 5 показаны типичные уровни триглицеридов, общего холестерина, холестерина липопротеинов низкой плотности (LDL-C) и холестерина липопротеинов высокой плотности (HLD-C) у мышей дикого типа (WT) и мышей, гомозиготных по гуманизированному гену Angptl8 (ANGPTL8hum/hum), описанных в примере 2. Уровни липидов представлены в мг/дл в плазме крови, отделенной от венозной крови.
[0056] На фигуре 6 показана типичная тканеспецифическая (в ткани печени и жировой ткани) экспрессия человеческого ANGPTL8 у мышей, гомозиготных по гуманизированному гену Angptl8, описанных в примере 3. Уровни экспрессии показаны в виде числа ридов на тысячу оснований транскрипта на миллион картированных ридов (RPKM).
[0057] На фигуре 7 показаны типичные уровни триглицеридов в сыворотке крови мышей, гомозиготных по гуманизированному гену Angptl8, описанных в примере 4, до и после введения антитела к ANGPTL8 или контроля (изотипически сходного человеческого IgG с несоответствующей специфичностью). Уровни триглицеридов в сыворотке крови представлены в мг/дл до (предварительный отбор) и после (после введения) обработки антителом.
[0058] Фигуры 8A-8K. В последовательностях mRNA кодирующая последовательность указана жирным шрифтом, а последовательные экзоны в тех случаях, когда они указаны, разделены чередующимся подчеркнутым текстом; в сконструированных последовательностях mRNA человеческие последовательности заключены в круглые скобки. В аминокислотных последовательностях сигнальные последовательности указаны подчеркнутым шрифтом. 8A. mRNA Angptl8 Rattus norvegicus (SEQ ID NO:1, эталонная последовательность NCBI NM_001271710.1). 8B. Аминокислотная последовательность Angptl8 Rattus norvegicus (SEQ ID NO:2, эталонная последовательность NP_001258639.1). 8C. mRNA Angptl8 Mus musculus (SEQ ID NO:3, эталонная последовательность NCBI NM_001080940.1). 8D. Аминокислотная последовательность Angptl8 Mus musculus (SEQ ID NO:4, эталонная последовательность NCBI NP_001074409.1). 8E. mRNA ANGPTL8 Homo sapiens (SEQ ID NO:5, эталонная последовательность NCBI NM_018687.6). 8F. Аминокислотная последовательность Homo sapiens ANGPTL8(SEQ ID NO:6, эталонная последовательность NCBI NP_061157.3). 8G. Иллюстративная сконструированная mRNAAngptl8 (SEQ ID NO:7). 8H. Иллюстративная сконструированная аминокислотная последовательность Angptl8(SEQ ID NO:8). 8I. Иллюстративный синтетический фрагмент ДНК для конструирования гена Angptl8, отличного от человеческого (SEQ ID NO:9; ~ 2383 п.о. охватывают экзоны 1-4 и 3'-концевую UTR человеческого гена ANGPTL8). 8J. Иллюстративный сконструированный аллель Angptl8, содержащий селекционную кассету (SEQ ID NO:10; человеческая последовательность указана жирным шрифтом в верхнем регистре, последовательность селекционной кассеты указана шрифтом в нижнем регистре, и мышиная последовательность указана обычным шрифтом в верхнем регистре). 8K. Иллюстративный сконструированный аллель Angptl8 после опосредованного рекомбиназой вырезания селекционной кассеты (SEQ ID NO:11, человеческая последовательность указана жирным шрифтом в верхнем регистре, последовательность, оставшаяся после опосредованного рекомбиназой удаления селекционной кассеты, указана шрифтом в нижнем регистре, и мышиная последовательность указана обычным шрифтом в верхнем регистре).
[0059] Фигура 9A. Показана нуклеотидная последовательность, охватывающая вышерасположенную точку вставки, в которой указана эндогенная мышиная последовательность (заключенная ниже в круглые скобки с выделенным жирным шрифтом стартовым кодоном ATG), смежная с человеческой геномной последовательностью ANGPTL8 в точке вставки.
[0060] Фигура 9B. Показана нуклеотидная последовательность, охватывающая 5'-конец самоудаляющейся кассеты устойчивости к неомицину, в которой указана человеческая геномная последовательность ANGPTL8, смежная с последовательностью кассеты (заключенной ниже в круглые скобки с выделенным курсивом сайтом XhoI и выделенным жирным шрифтом сайтом loxP) ниже точки вставки.
[0061] Фигура 9C. Показана нуклеотидная последовательность, охватывающая нижерасположенную точку вставки на 3'-конце самоудаляющейся кассеты устойчивости к неомицину, в которой указана последовательность кассеты (заключенная ниже в круглые скобки с выделенным жирным шрифтом сайтом loxP, выделенным подчеркиванием сайтом распознавания I-CeuI и выделенным курсивом сайтом распознавания NheI), смежная с мышиной геномной последовательностью Angptl8.
[0062] Фигура 9D. Показана нуклеотидная последовательность, охватывающая нижерасположенную точку вставки, после удаления кассеты устойчивости к неомицину (между 3'-концевой UTR человеческого ANGPTL8 и 3'-концевой UTR мышиного Angptl8 остаются 77 п.о.), в которой указаны человеческая и мышиная геномные последовательности, расположенные рядом с оставшейся последовательностью кассеты (заключенной ниже в круглые скобки с выделенными курсивом сайтами распознавания XhoI и NheI, выделенным жирным шрифтом сайтом loxP и выделенным подчеркиванием сайтом рестрикции I-CeuI).
ОПРЕДЕЛЕНИЯ
[0063] Настоящее изобретение не ограничено конкретными способами и условиями эксперимента, описанными в данном документе, поскольку такие способы и условия могут изменяться. Также следует понимать, что терминология, используемая в данном документе, предназначена только для целей описания конкретных вариантов осуществления и не подразумевается как ограничивающая, поскольку объем настоящего изобретения определяется формулой изобретения.
[0064] Если не определено иное, все термины и фразы, используемые в данном документе, имеют значения, которые данные термины и фразы приобрели в данной области техники, если в контексте, в котором используется термин или фраза, четко не указано или четко не видно противоположное. Хотя при практическом осуществлении или тестировании настоящего изобретения можно применять любые способы и материалы, сходные с описанными в данном документе или эквивалентные им, в данном документе описаны только конкретные способы и материалы. Все патентные и непатентные публикации, упомянутые в данном документе, включены в данный документ посредством ссылки.
[0065] Термин «примерно», применяемый в данном документе в отношении одного или более значений, представляющих интерес, относится к значению, сходному с указанным эталонным значением. В некоторых вариантах осуществления термин «примерно» или «приблизительно» относится к диапазону значений, находящихся в пределах 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или меньше в любую сторону (большую или меньшую) от указанного эталонного значения, если иное не указано или иное не очевидно из контекста (за исключением случаев, в которых такое число будет превышать 100% от возможного значения).
[0066] Термин «биологически активный», используемый в данном документе, относится к характеристике любого средства, обладающего активностью в биологической системе in vitro или in vivo (например, в организме). Например, средство, которое в случае присутствия в организме обладает биологическим эффектом в этом организме, считается биологически активным. В конкретных вариантах осуществления, в которых белок или полипептид являются биологически активными, часть этого белка или полипептида, обладающая по меньшей мере одним общим с данным белком или полипептидом видом биологической активности, обычно называется «биологически активной» частью.
[0067] Термин «сравнимый», используемый в данном документе, относится к двум или более средствам, объектам, ситуациям, наборам условий и т.д., которые могут не быть идентичными друг другу, но которые являются достаточно сходными для обеспечения возможности сравнения между ними таким образом, чтобы на основании наблюдаемых различий или сходств можно было сделать обоснованные выводы. Специалисту в данной области техники будет понятно из контекста, какая степень идентичности необходима в любых заданных обстоятельствах для двух или более таких средств, объектов, ситуаций, наборов условий и т.д., чтобы считать их сравнимыми.
[0068] Термин «консервативный», используемый в данном документе, относится к случаям, описывающим консервативную аминокислотную замену, в том числе замену аминокислотного остатка другим аминокислотным остатком, имеющим R-группу боковой цепи со сходными химическими свойствами (например, зарядом или гидрофобностью). Как правило, консервативная аминокислотная замена практически не будет изменять функциональные свойства белка, представляющие интерес, например, способность рецептора связываться с лигандом. Примеры групп аминокислот, которые имеют боковые цепи со сходными химическими свойствами, включают алифатические боковые цепи, такие как у глицина (Gly, G), аланина (Ala, A), валина (Val, V), лейцина (Leu, L) и изолейцина (Ile, I); алифатические боковые цепи с гидроксильными группами, такие как у серина (Ser, S) и треонина (Thr, T); амидосодержащие боковые цепи, такие как у аспарагина (Asn, N) и глутамина (Gln, Q); ароматические боковые цепи, такие как у фенилаланина (Phe, F), тирозина (Tyr, Y) и триптофана (Trp, W); основные боковые цепи, такие как у лизина (Lys, K), аргинина (Arg, R) и гистидина (His, H); кислые боковые цепи, такие как у аспарагиновой кислоты (Asp, D) и глутаминовой кислоты (Glu, E); и серосодержащие боковые цепи, такие как у цистеина (Cys, C) и метионина (Met, M). Группы консервативных аминокислотных замен включают, например, валин/лейцин/изолейцин (Val/Leu/Ile, V/L/I), фенилаланин/тирозин (Phe/Tyr, F/Y), лизин/аргинин (Lys/Arg, K/R), аланин/валин (Ala/Val, A/V), глутамат/аспартат (Glu/Asp, E/D) и аспарагин/глутамин (Asn/Gln, N/Q). В некоторых вариантах осуществления консервативная аминокислотная замена может представлять собой замену любого нативного остатка в белке аланином, используемую, например, в аланин-сканирующем мутагенезе. В некоторых вариантах осуществления производят консервативную замену, которая имеет положительное значение в матрице логарифмической функции правдоподобия PAM250, раскрытой в Gonnet et al., 1992, Science 256:1443-1445. В некоторых вариантах осуществления замена представляет собой умеренно консервативную замену, где замена имеет неотрицательное значение в матрице логарифмической функции правдоподобия PAM250.
[0069] Термин «контроль», используемый в данном документе, относится к понятному в данной области техники значению «контроля», являющемуся стандартом, с которым сравнивают результаты. Как правило, контроли применяют для повышения целостности в экспериментах путем разделения переменных для того, чтобы сделать вывод об этих переменных. В некоторых вариантах осуществления контроль представляет собой реакцию или анализ, проводимые одновременно с тестовыми реакцией или анализом для обеспечения объекта сравнения. Как используется в данном документе, «контроль» может относиться к «контрольному животному». «Контрольное животное» может иметь модификацию, описанную в данном документе, модификацию, отличную от описанной в данном документе, или не иметь модификации (т.е. в случае животного дикого типа). В одном эксперименте применяют «тест» (т.е. тестируемую переменную). Во втором эксперименте «контроль» (т.е. тестируемую переменную) не применяют. В некоторых вариантах осуществления контроль представляет собой исторический контроль (т.е. тест или анализ, проведенный ранее, или количество или результат, известные заранее). В некоторых вариантах осуществления контроль представляет собой или включает напечатанную или иным образом сохраненную запись. Контроль может представлять собой положительный контроль или отрицательный контроль.
[0070] Термин «разрушение», используемый в данном документе, относится к результату события гомологичной рекомбинации с молекулой ДНК (например, с эндогенной гомологичной последовательностью, такой как ген или локус гена). В некоторых вариантах осуществления разрушение может приводить к вставке, делеции, замене, замещению, миссенс-мутации или сдвигу рамки считывания в последовательности(последовательностях) ДНК или любой их комбинации или может быть представлено таковыми. Вставки могут включать вставку полных генов или фрагментов генов, например, экзонов, которые могут иметь происхождение, отличное от такого происхождения для эндогенной последовательности (например, гетерологичной последовательности). В некоторых вариантах осуществления разрушение может приводить к повышению экспрессии и/или активности гена или продукта гена (например, белка, кодируемого геном). В некоторых вариантах осуществления разрушение может приводить к уменьшению экспрессии и/или активности гена или продукта гена. В некоторых вариантах осуществления разрушение может приводить к изменению последовательности гена или кодируемого продукта гена (например, кодируемого белка). В некоторых вариантах осуществления разрушение может приводить к усечению или фрагментации гена или кодируемого продукта гена (например, кодируемого белка). В некоторых вариантах осуществления разрушение может приводить к удлинению гена или кодируемого продукта гена; в некоторых таких вариантах осуществления разрушение может приводить к сборке слитого белка. В некоторых вариантах осуществления разрушение может влиять на уровень экспрессии, но не на активность гена или продукта гена. В некоторых вариантах осуществления разрушение может влиять на активность, но не на уровень экспрессии гена или продукта гена. В некоторых вариантах осуществления разрушение может не оказывать значительный эффект в отношении уровня экспрессии гена или продукта гена. В некоторых вариантах осуществления разрушение может не оказывать значительный эффект в отношении активности гена или продукта гена. В некоторых вариантах осуществления разрушение может не оказывать значительный эффект ни в отношении уровня экспрессии, ни в отношении активности гена или продукта гена.
[0071] Термины «определение», «измерение», «установление», «оценка», «анализ» и «анализирование» используются в данном документе взаимозаменяемо для обозначения любой формы измерения и включают определение присутствия или отсутствия элемента. Эти термины включают количественные и/или также качественные определения. Анализ может быть относительным или абсолютным. «Анализ на наличие» может представлять собой определение количества чего-либо присутствующего и/или определение того, присутствует или отсутствует ли это.
[0072] Термины «эндогенный локус» или «эндогенный ген», используемые в данном документе, относятся к генетическому локусу, обнаруживаемому в исходном или эталонном организме до введения изменения, разрушения, делеции, вставки, модификации, замещения или замены, описанных в данном документе. В некоторых вариантах осуществления эндогенный локус имеет последовательность, обнаруживаемую в природе. В некоторых вариантах осуществления эндогенный локус представляет собой локус дикого типа. В некоторых вариантах осуществления эталонный организм представляет собой организм дикого типа. В некоторых вариантах осуществления эталонный организм представляет собой сконструированный организм. В некоторых вариантах осуществления эталонный организм представляет собой организм, выведенный в лаборатории (будь то организм дикого типа либо сконструированный).
[0073] Термин «эндогенный промотор», используемый в данном документе, относится к промотору, связанному в естественных условиях, например, в организме дикого типа, с эндогенным геном.
[0074] Термин «сконструированный», используемый в данном документе, относится в целом к аспекту проведения манипуляций человеком. Например, в некоторых вариантах осуществления полинуклеотид может считаться «сконструированным» в том случае, если две или более последовательности, которые не соединены друг с другом в этом порядке в природе, подвергнуты манипуляции человеком для непосредственного соединения друг с другом в сконструированном полинуклеотиде. В некоторых таких конкретных вариантах осуществления сконструированный полинуклеотид может содержать регуляторную последовательность, которая обнаруживается в природе в функциональной связи с первой кодирующей последовательностью, но не в функциональной связи со второй кодирующей последовательностью, соединенную с ними человеком таким образом, чтобы она была функционально связанной со второй кодирующей последовательностью. В качестве альтернативы или дополнительно, в некоторых вариантах осуществления первая и вторая последовательности нуклеиновых кислот, каждая из которых кодирует элементы или домены полипептидов, которые в природе не соединены друг с другом, могут быть соединены друг с другом в одном сконструированном полинуклеотиде. Аналогично, в некоторых вариантах осуществления клетка или организм могут считаться «сконструированными» в том случае, если они были подвергнуты манипуляции таким образом, чтобы их генетическая информация была изменена (например, был введен новый генетический материал, который ранее отсутствовал, или ранее присутствовавший генетический материал был изменен или удален). Как понятно специалистам в данной области техники и что является для них общепринятой практикой, потомство сконструированного полинуклеотида или клетки, как правило, по-прежнему называют «сконструированным», даже если фактическую манипуляцию проводили на предшествующем объекте. Кроме того, как будет понятно специалистам в данной области техники, доступно множество методик, посредством которых можно осуществлять «конструирование», описанное в данном документе. Например, в некоторых вариантах осуществления «конструирование» может предусматривать отбор или разработку (например, последовательностей нуклеиновых кислот, полипептидных последовательностей, клеток, тканей и/или организмов) путем использования компьютерных систем, запрограммированных для проведения анализа или сравнения или, в иных случаях, для анализа, рекомендации и/или отбора последовательностей, изменений и т.д. В качестве альтернативы или дополнительно, в некоторых вариантах осуществления «конструирование» может предусматривать применение методик химического синтеза in vitro, и/или технологий рекомбинантных нуклеиновых кислот, таких как, например, амплификация (например, посредством полимеразной цепной реакции), гибридизация, мутация, трансформация, трансфекция нуклеиновых кислот и т.д., и/или любой из множества методик контролируемого спаривания. Как будет понятно специалистам в данной области техники, множество таких общепринятых методик (например, для рекомбинантной ДНК, синтеза олигонуклеотидов и культивирования и трансформации тканей [например, электропорации, липофекции и т.д.]) хорошо известно из уровня техники и описано в различных общих и более специализированных литературных источниках, которые цитируются и/или обсуждаются во всем настоящем описании. См., например, Sambrook et al., Molecular Cloning: A Laboratory Manual (2d ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989).
[0075] Термин «ген», используемый в данном документе, относится к последовательности ДНК в хромосоме, которая кодирует продукт (например, РНК-продукт и/или полипептидный продукт). В некоторых вариантах осуществления ген содержит кодирующую последовательность (т.е. последовательность, которая кодирует конкретный продукт). В некоторых вариантах осуществления ген содержит некодирующую последовательность. В некоторых конкретных вариантах осуществления ген может содержать как кодирующую (например, экзонную), так и некодирующую (например, интронную) последовательность. В некоторых вариантах осуществления ген может содержать одну или более регуляторных последовательностей (например, промоторы, энхансеры и т.д.) и/или интронных последовательностей, которые, например, могут контролировать или влиять на один или более аспектов экспрессии гена (например, специфичную для типа клеток экспрессию, индуцируемую экспрессию и т.д.). Для ясности отметим, что используемый в настоящей заявке термин «ген» обычно обозначает часть нуклеиновой кислоты, которая кодирует полипептид; при этом данный термин может необязательно охватывать регуляторные последовательности, как будет понятно из контекста специалистам в данной области техники. Это определение не подразумевает исключение применения термина «ген» к единицам экспрессии, не кодирующим белок, но скорее поясняет то, что в большинстве случаев термин, используемый в данном документе, относится к нуклеиновой кислоте, кодирующей полипептид.
[0076] Термин «гетерологичный», используемый в данном документе, относится к средству или объекту из другого источника. Например, при использовании по отношению к полипептиду, гену или продукту гена, присутствующим в конкретной клетке или конкретном организме, данный термин поясняет, что соответствующий полипептид, ген или продукт гена 1) были сконструированы человеком; 2) были введены в клетку или организм (или их предшественника) человеком (например, посредством генной инженерии) и/или 3) в естественных условиях не вырабатываются соответствующими клеткой или организмом (например, соответствующим типом клетки или типом организма) или отсутствует в них.
[0077] Термин «клетка-хозяин», используемый в данном документе, относится к клетке, в которую были введены гетерологичные (например, экзогенные) нуклеиновая кислота или белок. Специалистам в данной области техники при прочтении данного раскрытия будет понятно, что такие термины относятся не только к конкретной рассматриваемой клетке, но также используются для обозначения потомства такой клетки. Поскольку в последующих поколениях вследствие влияния мутаций или окружающей среды могут происходить определенные модификации, такое потомство в действительности может не быть идентичным родительской клетке, но по-прежнему включается в объем термина «клетка-хозяин», используемого в данном документе. В некоторых вариантах осуществления клетка-хозяин представляет собой или включает прокариотическую или эукариотическую клетку. Как правило, клетка-хозяин представляет собой любую клетку, подходящую для приема и/или выработки гетерологичных нуклеиновой кислоты или полипептида, независимо от того, к какому царству живой природы относится клетка. Иллюстративные клетки включают клетки прокариот и эукариот (одноклеточных или многоклеточных), бактериальные клетки (например, штаммов E. coli, Bacillus spp., Streptomyces spp. и т.д.), клетки микобактерий, клетки грибов, клетки дрожжей (например, S. cerevisiae, S. pombe, P. pastoris, P. methanolica и т.д.), растительные клетки, клетки насекомых (например, SF-9, SF-21, клетки насекомых, инфицированные бакуловирусами, клетки Trichoplusiani и т.д.), клетки животных, отличных от человека, клетки человека или продукты слияния клеток, такие как, например, гибридомы или квадромы. В некоторых вариантах осуществления клетка представляет собой клетку человека, нечеловекообразной обезьяны, человекообразной обезьяны, хомяка, крысы или мыши. В некоторых вариантах осуществления клетка является эукариотической и выбрана из следующих клеток: CHO (например, CHO K1, CHO-DXB11, Veggie-CHO), COS (например, COS-7), клетки сетчатки, Vero, CV1, клетки почки (например, HEK293, 293 EBNA, MSR 293, MDCK, HaK, BHK), HeLa, HepG2, WI38, MRC 5, Colo205, HB 8065, HL-60 (например, BHK21), Jurkat, Daudi, A431 (эпидермальной), CV-1, U937, 3T3, L-клетки, клетки C127, SP2/0, NS-0, MMT 060562, клетки Сертоли, клетки BRL 3A, клетки HT1080, клетки миеломы, опухолевой клетки и линии клеток, происходящей из вышеупомянутых клеток. В некоторых вариантах осуществления клетка содержит один или более вирусных генов, например, клетка сетчатки, которая экспрессирует вирусный ген (например, клетка PER.C6™). В некоторых вариантах осуществления клетка-хозяин представляет собой или включает выделенную клетку. В некоторых вариантах осуществления клетка-хозяин является частью ткани. В некоторых вариантах осуществления клетка-хозяин является частью организма.
[0078] Термин «гуманизированный» используется в данном документе в соответствии с его понятным в данной области техники значением для обозначения нуклеиновых кислот или полипептидов, структуры которых (т.е. нуклеотидные или аминокислотные последовательности) содержат части, практически соответствующие или идентичные структурам конкретного гена или полипептида, обнаруживаемого в природе у животного, отличного от человека, а также содержат части, отличающиеся от обнаруживаемых в соответствующем конкретном гене или белке, отличном от человеческого, и вместо этого более близко соответствующие сравнимым структурам, обнаруживаемым в соответствующем человеческом гене или полипептиде. В некоторых вариантах осуществления «гуманизированный» ген представляет собой ген, который кодирует полипептид, имеющий практически такую же аминокислотную последовательность, как и у человеческого полипептида (например, у человеческого белка или его части, например, у его характерной части). Например, в случае мембранного рецептора «гуманизированный» ген может кодировать полипептид, имеющий внеклеточную часть, имеющую полностью или частично такую же аминокислотную последовательность, как и у человеческой внеклеточной части, и остальную часть последовательности, такую же, как и у полипептида, отличного от человеческого (например, мышиного). В случае секретируемого полипептида «гуманизированный» ген может кодировать полипептид, имеющий зрелый пептид, имеющий полностью или частично такую же последовательность, как и у человеческого зрелого пептида, и сигнальную последовательность, такую же, как и у пептида, отличного от человеческого (например, мышиного). В некоторых вариантах осуществления гуманизированный ген содержит по меньшей мере часть последовательности ДНК человеческого гена. В некоторых вариантах осуществления гуманизированный ген содержит полную последовательность ДНК человеческого гена или последовательность ДНК человеческого гена, которая кодирует зрелый пептид или полипептид, соответствующий зрелому человеческому пептиду или полипептиду. В некоторых вариантах осуществления гуманизированный полипептид содержит последовательность, имеющую часть, присутствующую в человеческом полипептиде. В некоторых вариантах осуществления гуманизированный полипептид содержит полную последовательность человеческого полипептида и экспрессируется из эндогенного локуса животного, отличного от человека, который соответствует гомологу или ортологу человеческого гена.
[0079] Термин «идентичность», используемый в данном документе применительно к сравнению последовательностей, относится к идентичности, определяемой с помощью ряда различных алгоритмов, известных из уровня техники, которые можно применять для измерения идентичности нуклеотидных и/или аминокислотных последовательностей. В некоторых вариантах осуществления значения идентичности, описанные в данном документе, определяют с помощью выравнивания ClustalW v. 1.83 (медленного), в котором используются штраф за открытие гэпа 10,0, штраф за продление гэпа 0,1, а также с помощью матрицы сходства Gonnet (MACVECTOR™ 10.0.2, MacVector Inc., 2008).
[0080] Термин «in vitro», используемый в данном документе, относится к событиям, которые происходят в искусственной среде, например, в пробирке или реакционном сосуде, в культуре клеток и т.д., а не в многоклеточном организме.
[0081] Термин «in vivo», используемый в данном документе, относится к событиям, которые происходят в многоклеточном организме, таком как человек и/или животное, отличное от человека. В контексте систем на основе клетки данный термин можно использовать для обозначения событий, которые происходят в пределах живой клетки (в противоположность, например, системам in vitro).
[0082] Термин «выделенный», используемый в данном документе, относится к веществу и/или объекту, которые были (1) отделены по меньшей мере от некоторых компонентов, с которыми они были связаны при первоначальной выработке (будь то в природе и/или в условиях проведения эксперимента), и/или (2) разработаны, выработаны, получены и/или произведены человеком. Выделенные вещества и/или объекты могут быть отделены от приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или больше чем приблизительно 99% других компонентов, с которыми они были первоначально связаны. В некоторых вариантах осуществления выделенные средства являются чистыми на приблизительно 80%, на приблизительно 85%, на приблизительно 90%, на приблизительно 91%, на приблизительно 92%, на приблизительно 93%, на приблизительно 94%, на приблизительно 95%, на приблизительно 96%, на приблизительно 97%, на приблизительно 98%, на приблизительно 99% или больше чем на приблизительно 99%. Как используется в данном документе, вещество является «чистым», если оно практически не содержит других компонентов. В некоторых вариантах осуществления, как будет понятно специалистам в данной области техники, вещество может по-прежнему считаться «выделенным» или даже «чистым» после объединения с определенными другими компонентами, такими как, например, один или более носителей или наполнителей (например, буфер, растворитель, вода и т.д.); в таких вариантах осуществления процент выделения или чистоты вещества рассчитывают без учета таких носителей или наполнителей. В качестве лишь одного примера, в некоторых вариантах осуществления биологический полимер, такой как полипептид или полинуклеотид, встречающийся в природе, считается «выделенным», если: a) он ввиду своего происхождения или источника получения не связан с некоторыми или всеми компонентами, сопровождающими его в его нативном состоянии в природе; b) он практически не содержит других полипептидов или нуклеиновых кислот того же вида от вида, который вырабатывает их в природе; или c) он экспрессируется или иным образом связан с компонентами в клетке или другой системе экспрессии, не принадлежащей к виду, который вырабатывает его в природе. Таким образом, например, в некоторых вариантах осуществления полипептид, синтезируемый химическим путем или синтезируемый в клеточной системе, отличной от той, которая вырабатывает его в природе, считается «выделенным» полипептидом. В качестве альтернативы или дополнительно, в некоторых вариантах осуществления полипептид, который был подвергнут одной или более методикам очистки, может считаться «выделенным» полипептидом в той степени, в которой он был отделен от других компонентов: a) с которыми он связан в природе и/или b) с которыми он был связан при первоначальной выработке.
[0083] Термин «локус» или «локусы», используемый в данном документе, включает конкретное(конкретные) месторасположение(месторасположения) гена (или значимой последовательности), последовательность ДНК, последовательность, кодирующую полипептид, или положение в хромосоме генома организма. Например, «локус Angptl8» может относиться к конкретному месторасположению гена Angptl8, последовательности ДНК Angptl8, последовательности, кодирующей Angptl8, или положению Angptl8 в хромосоме генома организма, которое было идентифицировано как то, в котором находится такая последовательность. «Локус Angptl8» может содержать регуляторный элемент гена Angptl8, в том числе без ограничения энхансер, промотор, 5'-концевую и/или 3'-концевую UTR или их комбинацию. Специалистам в данной области техники будет понятно, что в некоторых вариантах осуществления хромосомы могут содержать несколько сотен или даже несколько тысяч генов и демонстрировать физическую совместную локализацию сходных генетических локусов при сравнении разных видов. Такие генетические локусы могут быть описаны как имеющие общую синтению.
[0084] Термин «животное, отличное от человека», используемое в данном документе, относится к любому позвоночному организму, который не является человеком. В некоторых вариантах осуществления животное, отличное от человека, является круглоротым, костной рыбой, хрящевой рыбой (например, акулой или скатом), земноводным пресмыкающимся, млекопитающим и птицей. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является млекопитающим. В некоторых вариантах осуществления млекопитающее, отличное от человека, является приматом, козой, овцой, свиньей, собакой, коровой или грызуном. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является мелким млекопитающим, например, из надсемейства Dipodoidea или Muroidea. В некоторых вариантах осуществления генетически модифицированное животное, описанное в данном документе, является грызуном. В некоторых вариантах осуществления грызун, описанный в данном документе, выбран из мыши, крысы и хомяка. В некоторых вариантах осуществления грызун, описанный в данном документе, выбран из надсемейства Muroidea. В некоторых вариантах осуществления генетически модифицированное животное, описанное в данном документе, относится к семейству, выбранному из Calomyscidae (например, мышевидные хомячки), Cricetidae (например, хомяки, крысы и мыши Нового света, полевки), Muridae (настоящие мыши и крысы, песчанки, иглистые мыши, косматые хомяки), Nesomyidae (лазающие мыши, скальные мыши, белохвостые крысы, малагасийские крысы и мыши), Platacanthomyidae (например, колючие сони) и Spalacidae (например, слепыши, бамбуковые крысы и цокоры). В некоторых определенных вариантах осуществления генетически модифицированный грызун, описанный в данном документе, выбран из настоящей мыши или крысы (семейство Muridae), песчанки, иглистой мыши и косматого хомяка. В некоторых определенных вариантах осуществления генетически модифицированная мышь, описанная в данном документе, является представителем семейства Muridae. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является грызуном. В некоторых определенных вариантах осуществления грызун, описанный в данном документе, выбран из мыши и крысы. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является мышью.
[0085] В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является грызуном, который является мышью линии C57BL, выбранной из C57BL/A, C57BL/An, C57BL/GrFa, C57BL/KaLwN, C57BL/6, C57BL/6J, C57BL/6ByJ, C57BL/6NJ, C57BL/10, C57BL/10ScSn, C57BL/10Cr и C57BL/Ola. В некоторых определенных вариантах осуществления мышь, описанная в данном документе, принадлежит к линии 129, выбранной из группы, состоящей из линии 129P1, 129P2, 129P3, 129X1, 129S1 (например, 129S1/SV, 129S1/SvIm), 129S2, 129S4, 129S5, 129S9/SvEvH, 129/SvJae, 129S6 (129/SvEvTac), 129S7, 129S8, 129T1, 129T2 (см., например, Festing et al., 1999, Mammalian Genome 10:836; Auerbach, W. et al., 2000, Biotechniques 29(5):1024-1028, 1030, 1032). В некоторых определенных вариантах осуществления генетически модифицированная мышь, описанная в данном документе, является помесью вышеупомянутой линии 129 и вышеупомянутой линии C57BL/6. В некоторых определенных вариантах осуществления мышь, описанная в данном документе, является помесью вышеупомянутых линий 129 или помесью вышеупомянутых линий BL/6. В некоторых определенных вариантах осуществления линия 129 в помеси, описанной в данном документе, представляет собой линию 129S6 (129/SvEvTac). В некоторых вариантах осуществления мышь, описанная в данном документе, принадлежит к линии BALB, например, к линии BALB/c. В некоторых вариантах осуществления мышь, описанная в данном документе, является помесью линии BALB и другой вышеупомянутой линии.
[0086] В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является крысой. В некоторых определенных вариантах осуществления крыса, описанная в данном документе, выбрана из крысы линии Wistar, линии LEA, линии Sprague Dawley, линии Fischer, F344, F6 и Dark Agouti. В некоторых определенных вариантах осуществления линия крыс, описанная в данном документе, представляет собой помесь двух или более линий, выбранных из группы, состоящей из Wistar, LEA, Sprague Dawley, Fischer, F344, F6 и Dark Agouti.
[0087] Термин «нуклеиновая кислота», используемый в данном документе, в своем самом широком смысле относится к любому соединению и/или веществу, которое включено или может быть включено в состав олигонуклеотидной цепи. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой соединение и/или вещество, которое включено или может быть включено в состав олигонуклеотидной цепи с помощью фосфодиэфирной связи. Как будет очевидно из контекста, в некоторых вариантах осуществления «нуклеиновая кислота» относится к отдельным остаткам нуклеиновой кислоты (например, нуклеотидам и/или нуклеозидам); в некоторых вариантах осуществления «нуклеиновая кислота» относится к олигонуклеотидной цепи, содержащей отдельные остатки нуклеиновой кислоты. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит РНК; в некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит ДНК. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой один или более остатков природной нуклеиновой кислоты, содержит их или состоит из них. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой один или более аналогов нуклеиновой кислоты, содержит их или состоит из них. В некоторых вариантах осуществления аналог нуклеиновой кислоты отличается от «нуклеиновой кислоты» тем, что в нем не используется фосфодиэфирный остов. Например, в некоторых вариантах осуществления «нуклеиновая кислота» представляет собой одну или более «пептидных нуклеиновых кислот», которые известны из уровня техники и имеют в остове пептидные связи вместо фосфодиэфирных связей, содержит их или состоит из них, и они считаются находящимися в пределах объема настоящего изобретения. В качестве альтернативы или дополнительно, в некоторых вариантах осуществления «нуклеиновая кислота» имеет одну или более фосфоротиоатных и/или 5'-N-фосфорамидитных связей вместо фосфодиэфирных связей. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой один или более природных нуклеозидов (например, аденозин, тимидин, гуанозин, цитидин, уридин, дезоксиаденозин, дезокситимидин, дезоксигуанозин и дезоксицитидин), содержит их или состоит из них. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой один или более аналогов нуклеозидов (например, 2-аминоаденозин, 2-тиотимидин, инозин, пирролопиримидин, 3-метиладенозин, 5-метилцитидин, C5-пропинилцитидин, C5-пропинилуридин, 2-аминоаденозин, C5-бромуридин, C5-фторуридин, C5-йодуридин, C5-пропинилуридин, C5-пропинилцитидин, C5-метилцитидин, 2-аминоаденозин, 7-дезазааденозин, 7-дезазагуанозин, 8-оксоаденозин, 8-оксогуанозин, O(6)-метилгуанин, 2-тиоцитидин, метилированные основания, интеркалированные основания и их комбинации), содержит их или состоит из них. В некоторых вариантах осуществления «нуклеиновая кислота» содержит один или более модифицированных сахарных остатков (например, 2’-фторрибозу, рибозу, 2’-дезоксирибозу, арабинозу и гексозу) по сравнению с таковыми сахарными остатками в природных нуклеиновых кислотах. В некоторых вариантах осуществления «нуклеиновая кислота» имеет нуклеотидную последовательность, которая кодирует функциональный продукт гена, такой как РНК или белок. В некоторых вариантах осуществления «нуклеиновая кислота» содержит один или более интронов. В некоторых вариантах осуществления «нуклеиновую кислоту» получают посредством одного или более из выделения из природного источника, ферментативного синтеза путем полимеризации на основе комплементарной матрицы (in vivo или in vitro), воспроизведения в рекомбинантной клетке или системе и химического синтеза. В некоторых вариантах осуществления «нуклеиновая кислота» имеет длину по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 20, 225, 250, 275, 300, 325, 350, 375, 400, 425, 450, 475, 500, 600, 700, 800, 900, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000 или больше остатков. В некоторых вариантах осуществления «нуклеиновая кислота» является однонитевой; в некоторых вариантах осуществления «нуклеиновая кислота» является двухнитевой. В некоторых вариантах осуществления «нуклеиновая кислота» имеет нуклеотидную последовательность, содержащую по меньшей мере один элемент, который кодирует полипептид или является комплементарным по отношению к последовательности, которая кодирует полипептид. В некоторых вариантах осуществления «нуклеиновая кислота» обладает ферментативной активностью.
[0088] Термин «функционально связанный», используемый в данном документе, относится к расположению рядом, при котором описанные компоненты находятся во взаимосвязи, позволяющей им функционировать надлежащим образом. Контролирующая последовательность, «функционально связанная» с кодирующей последовательностью, лигирована с ней таким образом, что экспрессия кодирующей последовательности достигается в условиях, совместимых с функционированием контролирующих последовательностей. «Функционально связанные» последовательности включают как последовательности, контролирующие экспрессию, смежные с геном, представляющим интерес, так и последовательности, контролирующие экспрессию, действующие по транс-типу или на некотором расстоянии, осуществляя контроль над геном, представляющим интерес. Термин «последовательность, контролирующая экспрессию», используемый в данном документе, относится к полинуклеотидным последовательностям, необходимым для осуществления экспрессии и процессинга кодирующих последовательностей, с которыми они лигированы. «Последовательности, контролирующие экспрессию» включают соответствующие последовательности для инициации и терминации транскрипции, промоторные и энхансерные последовательности; сигналы для эффективного процессинга РНК, такие как сигналы сплайсинга и полиаденилирования; последовательности, стабилизирующие цитоплазматическую mRNA; последовательности, повышающие эффективность трансляции (т.е. консенсусную последовательность Козак); последовательности, повышающие стабильность белка; и, при необходимости, последовательности, усиливающие секрецию белка. Природа таких контролирующих последовательностей различается в зависимости от организма-хозяина. Например, у прокариот такие контролирующие последовательности обычно включают промотор, сайт связывания рибосом и последовательность для терминации транскрипции, тогда как у эукариот такие контролирующие последовательности, как правило, включают промоторы и последовательность для терминации транскрипции. Термин «контролирующие последовательности» подразумевает включение компонентов, наличие которых является существенным для экспрессии и процессинга, и также может включать дополнительные компоненты, наличие которых является преимущественным, например, лидерные последовательности и последовательности-партнеры по слиянию.
[0089] Термины «пациент» или «субъект», используемые в данном документе, относятся к любому организму, которому вводят или могут вводить предусмотренную композицию, например, для экспериментальных, диагностических, профилактических, косметических и/или терапевтических целей. Типичные пациенты включают животных (например, млекопитающих, таких как мыши, крысы, кролики, приматы, отличные от человека, и/или люди). В некоторых вариантах осуществления пациент является животным, отличным от человека. В некоторых вариантах осуществления пациент или субъект (например, пациент, являющийся животным, отличным от человека) может иметь модификацию, описанную в данном документе, модификацию, отличную от описанной в данном документе, или не иметь модификации (т.е. в случае пациента, являющегося животным, отличным от человека, дикого типа). В некоторых вариантах осуществления животное, отличное от человека, страдает от одного или более нарушений или состояний или восприимчиво к ним. В некоторых вариантах осуществления у животного, отличного от человека, проявляются один или более симптомов заболевания, нарушения или состояния. В некоторых вариантах осуществления у животного, отличного от человека, было диагностировано одно или более заболеваний, нарушений или состояний.
[0090] Термин «полипептид», используемый в данном документе, относится к любой полимерной цепи из аминокислот. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, встречающуюся в природе. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, не встречающуюся в природе. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, которая содержит части, встречающиеся в природе отдельно друг от друга (т.е. из двух или более различных организмов, например, человеческую и отличную от человеческой части). В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, которая является сконструированной в том смысле, что она разработана и/или получена в результате действий человека.
[0091] Термины «промотор» или «промоторная последовательность», используемые в данном документе, относятся к регуляторной области ДНК, способной связываться с РНК-полимеразой в клетке (например, непосредственно или с помощью других связанных с промотором полипептидов или веществ) и инициировать транскрипцию кодирующей последовательности. Промоторная последовательность, как правило, связана на своем 3'-конце с сайтом инициации транскрипции и простирается против хода транскрипции (в 5'-направлении), включая минимальное количество оснований или элементов, необходимых для инициации транскрипции на любом уровне. Промотор может быть функционально соединен или функционально связан с последовательностями, контролирующими экспрессию, в том числе с энхансерными и репрессорными последовательностями, или с нуклеиновой кислотой, представляющей интерес, подлежащей экспрессии. В некоторых вариантах осуществления промотор может быть индуцируемым. В некоторых вариантах осуществления индуцируемый промотор может быть однонаправленным или двунаправленным. В некоторых вариантах осуществления промотор может представлять собой конститутивный промотор. В некоторых вариантах осуществления промотор может представлять собой гибридный промотор, в котором последовательность, содержащая область, регулирующую транскрипцию, получена из одного источника, а последовательность, содержащая область инициации транскрипции, получена из второго источника. Системы для соединения контролирующих элементов с кодирующими последовательностями в трансгене хорошо известны из уровня техники. Например, общие методики молекулярной биологии и рекомбинантных ДНК описаны в Principles of Gene Manipulation: An Introduction to Genetic Manipulation, 5th Ed., ed. By Old, R.W. and S.B. Primrose, Blackwell Science, Inc., 1994; Molecular Cloning: A Laboratory Manual, 2nd Ed., ed. by Sambrook, J. et al., Cold Spring Harbor Laboratory Press: 1989.
[0092] Термин «рекомбинантный», используемый в данном документе, подразумевает обозначение полипептидов, разрабатываемых, конструируемых, получаемых, экспрессируемых, создаваемых или выделяемых с помощью рекомбинантных способов, таких как полипептиды, экспрессируемые с помощью рекомбинантного вектора экспрессии, вводимого путем трансфекции в клетку-хозяина, полипептиды, выделяемые из комбинаторной библиотеки рекомбинантных человеческих полипептидов (Hoogenboom H. R., 1997, TIB Tech. 15:62-70; Azzazy H., and Highsmith W. E., 2002, Clin. Biochem. 35:425-45; Gavilondo J. V., and Larrick J. W., 2002, BioTech. 29:128-45; Hoogenboom H., and Chames P., 2000, Immunology Today 21:371-8), антитела, выделяемые из животного (например, мыши), трансгенного по генам человеческих иммуноглобулинов (см., например, Taylor, L. D. et al., 1992, Nucl. Acids Res. 20:6287-95; Kellermann S-A., and Green L. L., 2002, Curr. Opin. Biotechnol. 13:593-7; Little M. et al., 2000, Immunol. Today 21:364-370; Murphy, A.J. et al., 2014, Proc. Natl. Acad. Sci. U.S.A. 111(14):5153-8), или полипептиды, получаемые, экспрессируемые, создаваемые или выделяемые любыми другими способами, предусматривающими сшивку выбранных элементов последовательностей друг с другом. В некоторых вариантах осуществления один или более из таких выбранных элементов последовательностей обнаруживаются в природе. В некоторых вариантах осуществления один или более из таких выбранных элементов последовательностей разрабатывают in silico. В некоторых вариантах осуществления один или более из таких выбранных элементов последовательностей получают в результате мутагенеза (например, in vivo или in vitro) известного элемента последовательности, например, из природного или синтетического источника. Например, в некоторых вариантах осуществления рекомбинантный полипептид состоит из последовательностей, обнаруживаемых в геноме организма-источника, представляющего интерес (например, человека, мыши и т.д.). В некоторых вариантах осуществления рекомбинантный полипептид имеет аминокислотную последовательность, полученную в результате мутагенеза (например, in vitro или in vivo, например, у животного, отличного от человека), так что аминокислотные последовательности рекомбинантных полипептидов представляют собой последовательности, которые хоть и происходят из последовательностей полипептидов и являются родственными им, но в естественных условиях могут не существовать в геноме животного, отличного от человека, in vivo.
[0093] Термин «замещение», используемый в данном документе, относится к процессу, посредством которого «замещаемую» последовательность нуклеиновой кислоты (например, ген), обнаруживаемую в локусе хозяина (например, в геноме), удаляют из этого локуса, а другую, «замещающую» нуклеиновую кислоту, располагают на ее месте. В некоторых вариантах осуществления замещаемая последовательность нуклеиновой кислоты и замещающие последовательности нуклеиновых кислот сравнимы друг с другом в том, что, например, они являются гомологичными друг другу и/или содержат соответствующие элементы (например, элементы, кодирующие белок, регуляторные элементы и т.д.). В некоторых вариантах осуществления замещаемая последовательность нуклеиновой кислоты содержит одно или более из промотора, энхансера, донорного сайта сплайсинга, акцепторного сайта сплайсинга, интрона, экзона, нетранслируемой области (UTR); в некоторых вариантах осуществления замещающая последовательность нуклеиновой кислоты содержит одну или более кодирующих последовательностей. В некоторых вариантах осуществления замещающая последовательность нуклеиновой кислоты является гомологом замещаемой последовательности нуклеиновой кислоты. В некоторых вариантах осуществления замещающая последовательность нуклеиновой кислоты является ортологом замещаемой последовательности. В некоторых вариантах осуществления замещающая последовательность нуклеиновой кислоты представляет собой или содержит человеческую последовательность нуклеиновой кислоты. В некоторых вариантах осуществления замещающая последовательность нуклеиновой кислоты представляет собой или содержит сконструированную последовательность нуклеиновой кислоты. В некоторых вариантах осуществления, в том числе в тех, в которых замещающая последовательность нуклеиновой кислоты представляет собой или содержит человеческую последовательность нуклеиновой кислоты, замещаемая последовательность нуклеиновой кислоты представляет собой или содержит последовательность от грызуна (например, мышиную или крысиную последовательность). Последовательность нуклеиновой кислоты, размещенная таким образом, может содержать одну или более регуляторных последовательностей, которые являются частью исходной последовательности нуклеиновой кислоты, используемой для получения последовательности, размещенной таким образом (например, промоторы, энхансеры, 5'-концевые или 3'-концевые нетранслируемые области и т.д.). Например, в различных вариантах осуществления замещение представляет собой замену эндогенной последовательности гетерологичной последовательностью, что в результате приводит к выработке продукта гена с последовательности нуклеиновой кислоты, размещенной таким образом (содержащей гетерологичную последовательность), но не к экспрессии с эндогенной последовательности; при этом эндогенная геномная последовательность замещается последовательностью нуклеиновой кислоты, которая кодирует полипептид, имеющий функцию, сходную с таковой у полипептида, кодируемого эндогенной последовательностью (например, эндогенная геномная последовательность кодирует полипептид Angptl8, а фрагмент ДНК кодирует один или более полных или неполных человеческих полипептидов ANGPTL8). В различных вариантах осуществления эндогенный ген или его фрагмент замещают соответствующим человеческим геном или его фрагментом. Соответствующий человеческий ген или его фрагмент представляет собой человеческий ген или его фрагмент, который является ортологом замещаемого эндогенного гена или его фрагмента или практически сходным или одинаковым с ним по структуре и/или функции.
[0094] Термин «эталон», используемый в данном документе, описывает стандартные или контрольные средство, когорту, индивидуума, популяцию, образец, последовательность или значение, с которыми сравнивают средство, животное, когорту, индивидуума, популяцию, образец, последовательность или значение, представляющие интерес. В некоторых вариантах осуществления эталонные средство, когорту, индивидуума, популяцию, образец, последовательность или значение тестируют и/или определяют практически одновременно с тестированием или определением средства, когорты, индивидуума, популяции, образца, последовательности или значения, представляющих интерес. В некоторых вариантах осуществления эталонные средство, когорта, индивидуум, популяция, образец, последовательность или значение представляют собой исторический эталон, необязательно воплощенный в материальной форме. В некоторых вариантах осуществления эталон может относиться к контролю. Используемый в данном документе термин «эталон» может относиться к «эталонному животному». «Эталонное животное» может иметь модификацию, описанную в данном документе, модификацию, отличную от описанной в данном документе, или не иметь модификации (т.е. в случае животного дикого типа). Как будет понятно специалистам в данной области техники, эталонные средство, животное, когорту, индивидуума, популяцию, образец, последовательность или значение, как правило, определяют или характеризуют в условиях, сравнимых с условиями, используемыми для определения или получения характеристик средства, животного (например, млекопитающего), когорты, индивидуума, популяции, образца, последовательности или значения, представляющих интерес.
[0095] Термин «практически», используемый в данном документе, относится к качественному состоянию проявления полной или практически полной меры или степени выраженности характеристики или свойства, представляющих интерес. Специалисту в области биологии будет понятно, что биологические и химические явления редко, если это вообще происходит, продолжаются до окончания и/или протекают до завершения или достижения или избегания абсолютного результата. Таким образом, термин «практически» используется в данном документе для охвата потенциального отсутствия завершенности, присущего многим биологическим и химическим явлениям.
[0096] Термин «практически гомологичный», используемый в данном документе, относится к сравнению между аминокислотными последовательностями или последовательностями нуклеиновых кислот. Как будет понятно специалистам в данной области техники, две последовательности обычно считаются «практически гомологичными», если они содержат гомологичные остатки в соответствующих положениях. Гомологичные остатки могут являться идентичными остатками. В качестве альтернативы, гомологичные остатки могут являться неидентичными остатками с соответствующими сходными структурными и/или функциональными характеристиками. Например, как хорошо известно специалистам в данной области техники, определенные аминокислоты, как правило, классифицируют как «гидрофобные» или «гидрофильные» аминокислоты и/или как имеющие «полярные» или «неполярные» боковые цепи. Замена одной аминокислоты другой того же типа часто может считаться «гомологичной» заменой. Типичное распределение аминокислот по категориям обобщено ниже.
[0097] Из уровня техники хорошо известно, что аминокислотные последовательности или последовательности нуклеиновых кислот можно сравнивать с помощью любого из множества алгоритмов, в том числе алгоритмов, доступных в коммерческих компьютерных программах, таких как BLASTN для нуклеотидных последовательностей и BLASTP, BLAST с гэпами и PSI-BLAST для аминокислотных последовательностей. Такие иллюстративные программы описаны в Altschul et al., 1990, Basic local alignment search tool, J. Mol. Biol., 215(3): 403-410; Altschul et al., 1996, Methods Enzymol. 266:160-80; Altschul et al., 1997, Nucleic Acids Res. 25:3389-3402; Baxevanis et al., 1998 Bioinformatics: A Practical Guide to the Analysis of Genes and Proteins, Wiley; и Misener et al. (eds.) (1999) Bioinformatics Methods and Protocols (Methods in Molecular Biology, Vol. 132), Humana Press. В дополнение к идентификации гомологичных последовательностей, программы, упомянутые выше, как правило, дают представление о степени гомологии. В некоторых вариантах осуществления две последовательности считаются практически гомологичными, если по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше их соответствующих остатков являются гомологичными на протяжении рассматриваемого фрагмента из остатков. В некоторых вариантах осуществления рассматриваемый фрагмент представляет собой полную последовательность. В некоторых вариантах осуществления рассматриваемый фрагмент содержит по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17 или больше остатков. В некоторых вариантах осуществления рассматриваемый фрагмент содержит смежные остатки вдоль полной последовательности. В некоторых вариантах осуществления рассматриваемый фрагмент содержит прерывисто расположенные остатки вдоль полной последовательности. В некоторых вариантах осуществления рассматриваемый фрагмент содержит по меньшей мере 10, 15, 20, 25, 30, 35, 40, 45, 50 или больше остатков.
[0098] Термин «практически идентичный», используемый в данном документе, относится к сравнению между аминокислотными последовательностями или последовательностями нуклеиновых кислот. Как будет понятно специалистам в данной области техники, две последовательности обычно считаются «практически идентичными», если они содержат идентичные остатки в соответствующих положениях. Из уровня техники хорошо известно, что аминокислотные последовательности или последовательности нуклеиновых кислот можно сравнивать с помощью любого из множества алгоритмов, в том числе алгоритмов, доступных в коммерческих компьютерных программах, таких как BLASTN для нуклеотидных последовательностей и BLASTP, BLAST с гэпами и PSI-BLAST для аминокислотных последовательностей. Такие иллюстративные программы описаны в Altschul et al., 1990, Basic local alignment search tool, J. Mol. Biol., 215(3): 403-410; Altschul et al., 1996, Methods Enzymol. 266:160-80; Altschul et al., 1997, Nucleic Acids Res. 25:3389-3402; Baxevanis et al., 1998, Bioinformatics: A Practical Guide to the Analysis of Genes and Proteins, Wiley; Misener et al., (eds.) (1999) Bioinformatics Methods and Protocols (Methods in Molecular Biology, Vol. 132), Humana Press. В дополнение к идентификации идентичных последовательностей, программы, упомянутые выше, как правило, дают представление о степени идентичности. В некоторых вариантах осуществления две последовательности считаются практически идентичными, если по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше их соответствующих остатков являются идентичными на протяжении рассматриваемого фрагмента из остатков. В некоторых вариантах осуществления рассматриваемый фрагмент представляет собой полную последовательность. В некоторых вариантах осуществления рассматриваемый фрагмент содержит по меньшей мере 10, 15, 20, 25, 30, 35, 40, 45, 50 или больше остатков.
[0099] Термины «нацеливающийся вектор» или «нацеливающаяся конструкция», используемые в данном документе, относятся к молекуле полинуклеотида, содержащей нацеливающуюся область. Нацеливающаяся область содержит последовательность, идентичную или практически идентичную последовательности в клетке-, ткани- или животном-мишени, и обеспечивает интеграцию нацеливающейся конструкции в некоторое положение в геноме клетки, ткани или животного посредством гомологичной рекомбинации. Также включены нацеливающиеся области, которые нацеливаются с помощью сайтов распознавания для сайт-специфической рекомбиназы (например, сайтов loxP и/или Frt). В некоторых вариантах осуществления нацеливающаяся конструкция дополнительно содержит последовательность нуклеиновой кислоты или ген, представляющие особенный интерес, селектируемый маркер, контрольные и/или регуляторные последовательности, а также другие последовательности нуклеиновой кислоты, обеспечивающие возможность рекомбинации, опосредованной добавлением экзогенных белков, которые способствуют или содействуют рекомбинации с участием таких последовательностей. В некоторых вариантах осуществления нацеливающаяся конструкция дополнительно содержит полный или неполный ген, представляющий интерес, где ген, представляющий интерес, является гетерологичным геном, который кодирует полный или неполный полипептид, имеющий функцию, сходную с таковой у белка, кодируемого эндогенной последовательностью. В некоторых вариантах осуществления нацеливающаяся конструкция дополнительно содержит полный или неполный гуманизированный ген, представляющий интерес, где гуманизированный ген, представляющий интерес, кодирует полный или неполный полипептид, имеющий функцию, сходную с таковой у полипептида, кодируемого эндогенной последовательностью. В некоторых вариантах осуществления нацеливающаяся конструкция дополнительно содержит полный или неполный сконструированный ген, представляющий интерес, где сконструированный ген, представляющий интерес, кодирует полный или неполный полипептид, имеющий функцию, сходную с таковой у полипептида, кодируемого эндогенной последовательностью.
[00100] Термин «вариант», используемый в данном документе, относится к объекту, демонстрирующему значительную структурную идентичность с эталонным объектом, но структурно отличающемуся от эталонного объекта по наличию или уровню одного или более химических фрагментов по сравнению с эталонным объектом. Во многих вариантах осуществления «вариант» также отличается функционально от своего эталонного объекта. Как правило, то, уместно ли считать конкретный объект «вариантом» эталонного объекта, зависит от степени его структурной идентичности с эталонным объектом. Как будет понятно специалистам в данной области техники, любой биологический или химический эталонный объект имеет определенные характерные структурные элементы. «Вариант» по определению представляет собой отличающийся химический объект, имеющий один или более общих таких характерных структурных элементов. В качестве лишь нескольких примеров, малая молекула может иметь характерный сердцевинный структурный элемент (например, макроциклическую сердцевину) и/или один или более характерных «подвешенных» фрагментов, так что вариант малой молекулы имеет общие с ней сердцевинный структурный элемент и характерные «подвешенные» фрагменты, но отличается по другим «подвешенным» компонентам и/или по типам связей (одинарные по сравнению с двойными, E по сравнению с Z и т.д.), присутствующих в сердцевине, полипептид может иметь характерный элемент последовательности, состоящий из множества аминокислот, имеющих определенные положения по отношению друг к другу в линейном или трехмерном пространстве и/или способствующих осуществлению конкретной биологической функции, нуклеиновая кислота может иметь характерный элемент последовательности, состоящий из множества нуклеотидных остатков, имеющих определенные положения по отношению друг к другу в линейном или трехмерном пространстве. Например, «вариант полипептида» может отличаться от эталонного полипептида вследствие одного или более различий в аминокислотной последовательности и/или одного или более различий в химических фрагментах (например, углеводах, липидах и т.д.), прикрепленных ковалентной связью к полипептидному остову. В некоторых вариантах осуществления «вариант полипептида» демонстрирует общую идентичность последовательности с эталонным полипептидом, составляющую по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97% или 99%. В качестве альтернативы или дополнительно, в некоторых вариантах осуществления «вариант полипептида» не имеет по меньшей мере одного характерного элемента последовательности, общего с эталонным полипептидом. В некоторых вариантах осуществления эталонный полипептид обладает одним или более видами биологической активности. В некоторых вариантах осуществления «вариант полипептида» обладает одним или более видами биологической активности, общими с эталонным полипептидом. В некоторых вариантах осуществления у «варианта полипептида» отсутствует один или более видов биологической активности эталонного полипептида. В некоторых вариантах осуществления «вариант полипептида» демонстрирует пониженный уровень одного или более видов биологической активности по сравнению с эталонным полипептидом. Во многих вариантах осуществления полипептид, представляющий интерес, считается «вариантом» исходного или эталонного полипептида, если полипептид, представляющий интерес, имеет аминокислотную последовательность, идентичную такой последовательности у исходной молекулы, за исключением небольшого количества изменений в конкретных положениях в последовательности. У варианта, как правило, заменены меньше 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% остатков по сравнению с исходной молекулой. В некоторых вариантах осуществления «вариант» имеет 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замененный остаток по сравнению с исходной молекулой. «Вариант» часто имеет очень небольшое количество (например, меньше 5, 4, 3, 2 или 1) замененных функциональных остатков (т.е. остатков, принимающих участие в конкретной биологической активности). Кроме того, «вариант», как правило, имеет не более 5, 4, 3, 2 или 1 добавления или делеции и часто не имеет добавлений или делеций по сравнению с исходной молекулой. Более того, любые добавления или делеции обычно охватывают меньше чем приблизительно 25, приблизительно 20, приблизительно 19, приблизительно 18, приблизительно 17, приблизительно 16, приблизительно 15, приблизительно 14, приблизительно 13, приблизительно 10, приблизительно 9, приблизительно 8, приблизительно 7, приблизительно 6 и зачастую охватывают меньше чем приблизительно 5, приблизительно 4, приблизительно 3 или приблизительно 2 остатка. В некоторых вариантах осуществления исходный или эталонный полипептид обнаруживается в природе. Как будет понятно специалистам в данной области техники, множество вариантов конкретного полипептида, представляющего интерес, можно зачастую обнаружить в природе, особенно если полипептид, представляющий интерес, представляет собой полипептид возбудителя инфекции.
[00101] Термин «вектор», используемый в данном документе, относится к молекуле нуклеиновой кислоты, способной переносить другую нуклеиновую кислоту, с которой она связана. В некоторых вариантах осуществления векторы способны к внехромосомной репликации и/или экспрессии нуклеиновых кислот, с которыми они соединены, в клетке-хозяине, такой как эукариотическая и/или прокариотическая клетка. Векторы, способные управлять экспрессией функционально связанных генов, называются в данном документе «векторами экспрессии».
[00102] Термин «дикий тип», используемый в данном документе, имеет понятное в данной области техники значение, которое относится к объекту, обладающему структурой и/или активностью, обнаруживаемой в природе в «нормальном» (в противоположность мутантному, болезненному, измененному и т.д.) состоянии или окружении. Специалистам в данной области техники будет понятно, что гены и полипептиды дикого типа часто существуют в нескольких различных формах (например, аллелях).
ПОДРОБНОЕ ОПИСАНИЕ ОПРЕДЕЛЕННЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[00103] В настоящем изобретении предусмотрены, помимо прочего, улучшенные и/или сконструированные животные, отличные от человека, имеющие гетерологичный генетический материал, кодирующий ангиопоэтин-подобный белок 8 (ANGPTL8), для определения терапевтической эффективности модуляторов ANGPTL8 (например, антител к ANGPTL8) для лечения метаболических нарушений и анализов с измерением метаболизма липидов (например, триглицеридов), гомеостаза глюкозы, различных эффектов в отношении веса и состава тела и расхода энергии. Предполагается, что такие животные, отличные от человека, обеспечивают улучшение определения терапевтической эффективности модуляторов ANGPTL8 и их потенциала блокирования ANGPTL8. Таким образом, настоящее изобретение является особенно применимым для разработки терапевтических средств, противодействующих ANGPTL8, для лечения заболеваний, нарушений или состояний, обусловленных или характеризующихся различными метаболическими нарушениями, в том числе дисфункцией метаболизма триглицеридов, нарушением толерантности к глюкозе и дислипидемией (Zhang and Abou-Samra, Cardiovascular Diabetology 2014, 13:133). В частности, настоящее изобретение охватывает конструирование гена Angptl8, отличного от человеческого (например, мышиного), приводящее в результате к экспрессии человеческого полипептида ANGPTL8 в сыворотке крови животного, отличного от человека. Такие животные, отличные от человека, способны обеспечивать животную модель in vivo для определения эффективности терапевтических средств, противодействующих ANGPTL8, в лечении метаболических нарушений и/или сердечно-сосудистых заболеваний, нарушений и/или состояний. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, демонстрируют повышенные уровни триглицеридов по сравнению с животными, отличными от человека, дикого типа. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, обеспечивают животную модель in vivo для изучения метаболизма липопротеинов. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, обеспечивают животную модель in vivo для изучения гипертриглицеридемии.
[00104] В некоторых вариантах осуществления полипептиды Angptl8, экспрессируемые (или секретируемые) животным, отличным от человека, описанным в данном документе, содержат последовательность, соответствующую аминокислотам 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8. В некоторых вариантах осуществления полипептиды Angptl8, кодируемые генетическим материалом в геноме животных, отличных от человека, описанных в данном документе, содержат последовательность, соответствующую сигнальному пептиду мышиного полипептида Angptl8. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат в эндогенном локусе Angptl8 ген Angptl8, который содержит генетический материал от животного, отличного от человека, и гетерологичного вида (например, человека). В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат сконструированный ген Angptl8, где сконструированный ген Angptl8 содержит полные или неполные экзоны 1-4 человеческого гена ANGPTL8. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат сконструированный ген Angptl8, где сконструированный ген Angptl8 содержит кодирующую часть экзона 1 и экзоны 2-4 человеческого гена ANGPTL8. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат сконструированный ген Angptl8, где сконструированный ген Angptl8 содержит кодирующую часть экзона 1 (или кодирующую часть экзона 1 без стартового кодона), экзон 2, экзон 3 и экзон 4 (который содержит 3'-концевую UTR) человеческого гена ANGPTL8. В некоторых определенных вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат сконструированный ген Angptl8, где сконструированный ген Angptl8 содержит ~ 2383 п.о. человеческого гена ANGPTL8, соответствующие человеческому гену ANGPTL8 от кодирующей части экзона 1, начинающейся непосредственно после стартового кодона, до экзона 4, содержащего 3'-концевую UTR (например, ~ 256 п.о.), включительно. В некоторых вариантах осуществления животные, отличные от человека, описанные в данном документе, содержат сконструированный ген Angptl8 в эндогенном локусе Angptl8, где сконструированный ген Angptl8 содержит 5'-концевую UTR эндогенного гена Angptl8, кодирующую часть экзона 1, экзон 2, экзон 3 и экзон 4 (который содержит 3'-концевую UTR) человеческого гена ANGPTL8, функционально связанные с эндогенным промотором Angptl8; и в некоторых вариантах осуществления при создании такого сконструированного гена Angptl8 кодирующая часть экзона 1, экзоны 2-3 и кодирующая часть экзона 4 эндогенного гена Angptl8 в указанном эндогенном локусе Angptl8 были удалены. В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, не экспрессируют полный или неполный эндогенный полипептид Angptl8 на выявляемом уровне.
[00105] Различные аспекты настоящего изобретения подробно описаны в нижеследующих разделах. Использование разделов не подразумевает ограничения настоящего изобретения. Каждый раздел можно применять в отношении любого аспекта настоящего изобретения. В настоящей заявке использование «или» означает «и/или», если не указано иное.
Ангиопоэтин-подобный белок 8 (ANGPTL8)
[00106] ANGPTL8 (также называемый TD26, RIFL, липазином, C19orf80 и бетатрофином) является недавно обнаруженным представителем семейства ANGPTL, вовлеченным в метаболизм как триглицеридов, так и глюкозы. Филогенетический анализ выявил, что ANGPTL8 является близкородственным по отношению к ANGPTL3 и ANGPTL4 (Fu, Z. et. al., 2013, Biochem. Biophys. Res. Commun. 430:1126-31; Quagliarini F. et al; 2012, PNAS 109:19751-19756). ANGPTL8 представляет собой секретируемый полипептид, экспрессируемый преимущественно в ткани печени и жировой ткани, и, в отличие от родственных представителей семейства ANGPTL3 и ANGPTL4, не имеет C-концевого фибриноген-подобного домена, но содержит N-концевой суперспиральный домен, подобно другим представителям семейства ANGPTL (Mattijssen F.,and Kersten S, Biochim Biophys Acta 1821, 2012:782-789).
[00107] Сверхэкспрессия ANGPTL8 в печени ассоциирована с гипертриглицеридемией, тогда как инактивация Angptl8 вызывает снижение уровней триглицеридов в плазме крови (Quagliarini, F. et. al., 2012, Proc. Natl. Acad. Sci. USA 109(48):19751-6; Wang, Y. et. al., 2013, Proc. Natl. Acad. Sci. USA 110:16109-14). Несмотря на сообщения о том, что ANGPTL8 участвует в регуляции метаболизма липидов, механизм, отвечающий за это, по-прежнему является предметом обсуждений. В качестве лишь одного примера, один механизм обосновывает это тем, что ANGPTL8 ингибирует активность липопротеинлипазы, в результате чего снижается гидролиз триглицеридов и очищение от них (Zhang, R. et.al., 2012, Biochem. Biophys. Res. Commun. 424:786-92). ANGPTL8 согласно сообщениям также играет роль в пролиферации бета-клеток и увеличении массы бета-клеток у мышей, у которых инсулинорезистентность была индуцирована антагонистом инсулиновых рецепторов S961 (Yi, P. et. al. 2013, Cell 153:747-58). Однако, последующие исследования выявили, что ANGPTL8 не является необходимым для функционирования бета-клеток или роста бета-клеток в ответ на инсулинорезистентность. Кроме того, при сверхэкспрессии ANGPTL8 не увеличивается площадь, занимаемая бета-клетками, и не улучшается гликемический контроль (Gusarova, V. et. al., 2014, Cell 159:691-6). Поскольку сверхэкспрессия ANGPTL8 в печени ассоциирована с гипертриглицеридемией, а инактивация Angptl8 приводит в результате к снижению уровней триглицеридов в плазме крови, то ингибитор или антагонист ANGPTL8 может оказаться эффективным в лечении заболевания, характеризующегося в том числе повышенными уровнями триглицеридов, такого как, без ограничения, гипертриглицеридемия. Согласно одному сообщению в случае использования мышей дикого типа моноклональное антитело к липазину уменьшало уровни триглицеридов в сыворотке крови при внутрибрюшинной инъекции (Zhang, R., 2015, Endocrine Society's 97th Annual Meeting, Presentation No. OR13-6, March 5-8, San Diego, CA).
[00108] Для разработки практических средств целенаправленной терапии для будущего лечения пациентов-людей, страдающих от гипертриглицеридемии и других заболеваний, нарушений или состояний, характеризующихся повышенными уровнями триглицеридов и липидов, требуется более основательное и доскональное понимание функций, опосредованных ANGPTL8, и регуляторного пути ANGPTL8 в метаболизме липидов, гомеостазе глюкозы, эффекте в отношении веса тела, состава тела, расхода энергии и сердечно-сосудистой функции.
Последовательности ANGPTL8
[00109] ANGPTL8 (также называемый TD26, RIFL, липазином, C19orf80 и бетатрофином) является представителем белков семейства ангиопоэтинов. Термин «ANGPTL8», используемый в данном документе, относится к человеческому полипептиду ANGPTL8 и в некоторых вариантах осуществления к человеческому полипептиду ANGPTL8 без сигнального пептида (например, к полипептиду, содержащему аминокислотную последовательность, приведенную в 22-198 SEQ ID NO:6). Иллюстративные аминокислотные последовательности (содержащие сигнальный пептид) и последовательности mRNA человеческого ANGPTL8 можно найти соответственно под номерами доступа в GenBank NP_061157.3 (SEQ ID NO:6) и NM_018687.6 (SEQ ID NO:5) (см. фигуры 8D и 8E). N-концевые суперспиральные домены человеческого ANGPTL8 охватывают аминокислотные остатки ~77-134 и 156-193 в SEQ ID NO:6.
[00110] Иллюстративные последовательности Angptl8 грызунов (например, крысиного и мышиного), человеческого и сконструированного Angptl8 приведены на фигурах 8A-8H. Иллюстративный синтетический фрагмент ДНК для конструирования гена Angptl8, отличного от человеческого, описанного в данном документе, также приведен на фигуре 8I. В последовательностях mRNA кодирующая последовательность указана жирным шрифтом, а последовательные экзоны в тех случаях, когда они указаны, разделены чередующимся подчеркнутым текстом; в сконструированных последовательностях mRNA человеческие последовательности заключены в круглые скобки. В аминокислотных последовательностях сигнальные последовательности указаны подчеркнутым шрифтом.
ДНК-конструкции и получение животных, отличных от человека, имеющих гуманизированный ген ANGPTL8
[00111] Как правило, молекулу полинуклеотида, содержащую полный или неполный ген Angptl8 (например, гетерологичный или сконструированный ген Angptl8), вставляют в вектор, предпочтительно ДНК-вектор, с целью репликации молекулы полинуклеотида в подходящей клетке-хозяине.
[00112] В зависимости от размера ген Angptl8 или последовательность, кодирующую Angptl8, можно клонировать непосредственно из источников cDNA, доступных от коммерческих поставщиков, или разработать in silico на основе опубликованных последовательностей, доступных в GenBank. В качестве альтернативы, гетерологичные последовательности Angptl8 из генов, представляющих интерес (например, гетерологичного гена Angptl8), можно получить из библиотек искусственных бактериальных хромосом (BAC). Библиотеки BAC содержат вставки со средним размером 100-150 т.о. и способны нести вставки размером до 300 т.о. (Shizuya, H. et al., 1992, Proc. Natl. Acad. Sci., U.S.A. 89:8794-7; Swiatek, P.J. and T. Gridley, 1993, Genes Dev. 7:2071-84; Kim, U.J. et al., 1996, Genomics 34:213-8; включенные в данный документ посредством ссылки). Например, геномные библиотеки BAC для человека и мыши были сконструированы и являются коммерчески доступными (например, Invitrogen, Карлсбад, Калифорния). Геномные библиотеки BAC также могут служить источником гетерологичных последовательностей Angptl8, а также областей, контролирующих транскрипцию.
[00113] В качестве альтернативы, гетерологичные последовательности Angptl8 можно выделять, клонировать и/или переносить из искусственных хромосом дрожжей (YAC). Полный гетерологичный ген или локус можно клонировать и помещать в одну или несколько YAC. Если используются несколько YAC и они содержат перекрывающиеся гомологичные области, их можно рекомбинировать в штаммах дрожжей-хозяев с получением единой конструкции, представляющей полный локус. Плечи YAC можно дополнительно модифицировать с помощью селекционных кассет для клеток млекопитающих путем их усовершенствования таким образом, чтобы содействовать введению конструкций в эмбриональные стволовые клетки или эмбрионы с помощью способов, известных из уровня техники и/или описанных в данном документе.
[00114] Иллюстративные последовательности mRNA и аминокислотные последовательности для использования в конструировании гуманизированного гена Angptl8 у животного, отличного от человека, приведены выше. Другие гетерологичные последовательности Angptl8 также можно найти в базе данных GenBank или в других базах данных последовательностей, известных из уровня техники.
[00115] ДНК-конструкции, содержащие последовательности Angptl8, описанные в данном документе, в некоторых вариантах осуществления содержат геномные последовательности (или последовательности cDNA) человеческого ANGPTL8, кодирующие по меньшей мере приблизительно аминокислоты 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8, функционально связанные с регуляторными последовательностями, отличными от человеческих (например, промотором грызуна), для экспрессии у трансгенного животного, отличного от человека. В некоторых вариантах осуществления ДНК-конструкции, содержащие последовательности Angptl8, описанные в данном документе, содержат геномные последовательности (или последовательности cDNA) человеческого ANGPTL8, кодирующие по меньшей мере приблизительно аминокислоты 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8, функционально связанные с промотором Angptl8, отличным от человеческого, и одну или более нетранслируемых областей Angptl8, отличных от человеческих (например, 5'-концевых и/или 3'-концевых UTR). Человеческие и/или отличные от человеческих последовательности Angptl8, включенные в ДНК-конструкции, описанные в данном документе, могут быть идентичными или практически идентичными человеческим и/или отличным от человеческих последовательностям Angptl8, обнаруживаемым в природе (например, геномным), искусственными (например, синтетическими) или могут быть сконструированы человеком. В некоторых вариантах осуществления последовательности Angptl8 являются синтетическими по происхождению и содержат последовательность или последовательности, обнаруживаемые в человеческом гене ANGPTL8, обнаруживаемом в природе. Например, ДНК-конструкция может содержать синтетическую ДНК, которая соответствует экзонам 1-4 человеческого гена ANGPTL8 и которая кодирует по меньшей мере приблизительно аминокислоты 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8, функционально связанную с регуляторными (например, промотором) и некодирующими (например, одной или более UTR, отличными от человеческих) последовательностями Angptl8, отличными от человеческих, таким образом, что полученная в результате ДНК-конструкция кодирует полипептид Angptl8, имеющий последовательность, являющуюся полностью или практически полностью человеческой. В качестве альтернативы, ДНК-конструкция может содержать синтетическую ДНК, которая соответствует генетическому материалу, кодирующему функциональную часть человеческого полипептида ANGPTL8 (например, один или более суперспиральных доменов, N-концевую область), функционально связанную с регуляторными (например, промотором) и кодирующими (например, одним или более экзонами, отличными от человеческих) последовательностями Angptl8, отличными от человеческих, таким образом, что полученная в результате ДНК-конструкция кодирует полипептид Angptl8, имеющий человеческую и отличную от человеческой части. В некоторых вариантах осуществления последовательности Angptl8 содержат последовательность, в естественных условиях связанную с гетерологичным геном Angptl8 (т.e. человеческим геном ANGPTL8). В некоторых вариантах осуществления последовательности Angptl8 содержат последовательность, которая в естественных условиях не связана с гетерологичным геном Angptl8. В некоторых вариантах осуществления последовательности Angptl8 содержат последовательность, которая оптимизирована для экспрессии у животного, отличного от человека. В некоторых вариантах осуществления каждая из гетерологичных последовательностей Angptl8, функционально связанных с последовательностями Angptl8, отличными от человеческих, кодирует часть полипептида Angptl8, присутствующую в природе в отдельном полипептиде. Если дополнительные последовательности применимы в оптимизации экспрессии гетерологичных последовательностей Angptl8, то такие последовательности можно клонировать с использованием существующих последовательностей в качестве зондов. Дополнительные последовательности, необходимые для максимального увеличения экспрессии гетерологичного гена Angptl8 или гетерологичной последовательности, кодирующей Angptl8, можно получить из геномных последовательностей или других источников в зависимости от требуемого результата.
[00116] ДНК-конструкции можно получать с помощью способов, известных из уровня техники. Например, ДНК-конструкцию можно получить в качестве части большей плазмиды. Такое получение позволяет эффективно клонировать и отбирать правильные конструкции, как это известно из уровня техники. Фрагменты ДНК, содержащие одну или более нуклеотидных кодирующих последовательностей, описанных в данном документе, можно расположить между подходящими сайтами рестрикции в плазмиде так, чтобы их можно было легко выделить из остальных последовательностей плазмиды для включения в состав генома требуемого животного.
[00117] Различные способы, используемые для получения плазмид и организмов-хозяев, которые их содержат, известны из уровня техники. В отношении других систем экспрессии, подходящих как для прокариотических, так и для эукариотических клеток, а также общих процедур рекомбинации см. Principles of Gene Manipulation: An Introduction to Genetic Manipulation, 5th Ed., ed. By Old, R.W. and S.B. Primrose, Blackwell Science, Inc., 1994; Molecular Cloning: A Laboratory Manual, 2nd Ed., ed. by Sambrook, J. et al., Cold Spring Harbor Laboratory Press: 1989.
[00118] Предусмотрены животные, отличные от человека, которые экспрессируют полные или неполные человеческие полипептиды ANGPTL8 в сыворотке крови животных, отличных от человека, в результате генетической модификации эндогенного локуса (например, локуса Angptl8), кодирующего полипептид Angptl8, у животного, отличного от человека. Подходящие примеры, описанные в данном документе, включают грызунов, в частности, мышей.
[00119] Гуманизированный ген Angptl8 в некоторых вариантах осуществления содержит генетический материал от гетерологичного вида (например, человека), при этом гуманизированный ген Angptl8 кодирует полипептид Angptl8, который содержит часть, кодируемую генетическим материалом от гетерологичного вида. В некоторых вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит геномную ДНК гетерологичного вида, кодирующую полипептид Angptl8, который экспрессируется в сыворотке крови животного, отличного от человека, где полипептид Angptl8 имеет последовательность, являющуюся полностью или практически полностью человеческой. Также предусмотрены животные, отличные от человека, эмбрионы и клетки, отличные от человеческих, а также нацеливающиеся конструкции для получения животных, отличных от человека, а также эмбрионов и клеток, отличных от человеческих, содержащих указанный гуманизированный ген Angptl8.
[00120] В некоторых вариантах осуществления эндогенный ген Angptl8 подвергают делеции. В некоторых вариантах осуществления эндогенный ген Angptl8 изменяют, при этом часть эндогенного гена Angptl8 замещают гетерологичной последовательностью (например, полной или неполной последовательностью человеческого ANGPTL8). В некоторых вариантах осуществления весь или практически весь эндогенный ген Angptl8 замещают гетерологичным геном (например, полным или неполным человеческим геном ANGPTL8). В некоторых вариантах осуществления часть гетерологичного гена Angptl8 вставляют в эндогенный ген Angptl8, отличный от человеческого, в эндогенном локусе Angptl8. В некоторых вариантах осуществления гетерологичный ген представляет собой человеческий ген. В некоторых вариантах осуществления модификацию или гуманизацию проводят в отношении одной из двух копий эндогенного гена Angptl8, что приводит к получению животного, отличного от человека, являющегося гетерозиготным относительно гуманизированного гена Angptl8. В других вариантах осуществления предусмотрено животное, отличное от человека, являющееся гомозиготным по гуманизированному гену Angptl8.
[00121] В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, содержит полный или неполный человеческий ген ANGPTL8 в эндогенном локусе Angptl8, отличном от человеческого. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, содержит полный или неполный человеческий ген ANGPTL8 в месторасположении, отличном от эндогенного локуса Angptl8, отличного от человеческого. Таким образом, животных, отличных от человека, описанных в данном документе, можно охарактеризовать как имеющих гуманизированный или гетерологичный ген Angptl8. Замещенный, вставленный, модифицированный или измененный ген Angptl8 в эндогенном локусе Angptl8 или полипептид, экспрессируемый с такого гена, можно выявить с помощью множества способов, включающих, например, ПЦР, вестерн-блоттинг, Саузерн-блоттинг, полиморфизм длин рестрикционных фрагментов (RFLP) или анализ приобретения или потери аллеля. Гуманизированный или гетерологичный ген Angptl8, произвольным образом вставленный в геном животного, отличного от человека, можно выявить с помощью этих же или сходных способов. В некоторых вариантах осуществления животное, отличное от человека, описанное в данном документе, является гетерозиготным относительно гуманизированного или гетерологичного гена Angptl8, описанного в данном документе.
[00122] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, включает ген Angptl8, имеющий кодирующую часть экзона 1 (начинающуюся от стартового кодона ATG или непосредственно после него и простирающуюся до 3'-конца экзона 1) и экзоны 2-4 человеческого гена ANGPTL8.
[00123] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, включает ген Angptl8, который имеет первый, второй, третий и четвертый экзоны, каждый из которых имеет последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную первому, второму, третьему и четвертому экзонам, присутствующим в SEQ ID NO:5 или SEQ ID NO:7.
[00124] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, включает ген Angptl8, который имеет первый, второй, третий и четвертый экзоны, каждый из которых имеет последовательность, практически идентичную или идентичную первому, второму, третьему и четвертому экзонам, присутствующим в SEQ ID NO:5 или SEQ ID NO:7.
[00125] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную SEQ ID NO:10 или SEQ ID NO:11.
[00126] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит последовательность, практически идентичную или идентичную SEQ ID NO:10 или SEQ ID NO:11.
[00127] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, представляет собой или содержит SEQ ID NO:10или SEQ ID NO:11.
[00128] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит 5'-концевую нетранслируемую область, имеющую последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную 5'-концевой нетранслируемой области, присутствующей в SEQ ID NO:1 или SEQ ID NO:3, и/или 3'-концевую нетранслируемую область, имеющую последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную 3'-концевой нетранслируемой области, присутствующей в SEQ ID NO:1 или SEQ ID NO:3.
[00129] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит 5'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 5'-концевой нетранслируемой области, присутствующей в SEQ ID NO:1 или SEQ ID NO:3, и/или 3'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 3'-концевой нетранслируемой области, присутствующей в SEQ ID NO:1 или SEQ ID NO:3.
[00130] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит 5'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 5'-концевой нетранслируемой области эндогенного гена Angptl8, отличного от человеческого, и/или 3'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 3'-концевой нетранслируемой области человеческого гена ANGPTL8. В конкретных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит 5'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 5'-концевой нетранслируемой области, присутствующей в SEQ ID NO:1 или SEQ ID NO:3, и/или 3'-концевую нетранслируемую область, имеющую последовательность, практически идентичную или идентичную 3'-концевой нетранслируемой области, присутствующей в SEQ ID NO:5 или SEQ ID NO:7.
[00131] В конкретных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит 5'-концевую нетранслируемую область эндогенного гена Angptl8, отличного от человеческого (например, мышиного или крысиного), кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, которые содержат 3'-концевую UTR человеческого гена ANGPTL8.
[00132] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит нуклеотидную кодирующую последовательность (например, последовательность cDNA), по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную нуклеотидной кодирующей последовательности, присутствующей в SEQ ID NO:5 или SEQ ID NO:7.
[00133] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, содержит нуклеотидную кодирующую последовательность (например, последовательность cDNA), практически идентичную или идентичную нуклеотидной кодирующей последовательности, присутствующей в SEQ ID NO:5 или SEQ ID NO:7.
[00134] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, кодирует полипептид Angptl8, идентичный или практически идентичный человеческому полипептиду ANGPTL8. В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, кодирует полипептид Angptl8, идентичный или практически идентичный полноразмерному человеческому белку ANGPTL8, транслируемому с человеческого гена ANGPTL8 (который содержит человеческий сигнальный пептид ANGPTL8 или первую 21 аминокислоту человеческого полноразмерного белка ANGPTL8).
[00135] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, кодирует полипептид Angptl8, имеющий аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную аминокислотной последовательности, присутствующей в SEQ ID NO:6 или SEQ ID NO:8.
[00136] В различных вариантах осуществления гуманизированный ген Angptl8, описанный в данном документе, кодирует полипептид Angptl8, имеющий аминокислотную последовательность, практически идентичную или идентичную аминокислотной последовательности, присутствующей в SEQ ID NO:6 или SEQ ID NO:8.
[00137] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную аминокислотным остаткам 22-198 в SEQ ID NO:6 или SEQ ID NO:8.
[00138] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, практически идентичную или идентичную аминокислотным остаткам 22-198 в SEQ ID NO:6 или SEQ ID NO:8.
[00139] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную аминокислотным остаткам 77-134 в SEQ ID NO:6 или SEQ ID NO:8.
[00140] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, практически идентичную или идентичную аминокислотным остаткам 77-134 в SEQ ID NO:6 или SEQ ID NO:8.
[00141] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную аминокислотным остаткам 156-193 в SEQ ID NO:6 или SEQ ID NO:8.
[00142] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, практически идентичную или идентичную аминокислотным остаткам 156-193 в SEQ ID NO:6 или SEQ ID NO:8.
[00143] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную аминокислотным остаткам 22-60 в SEQ ID NO:6 или SEQ ID NO:8.
[00144] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит аминокислотную последовательность, практически идентичную или идентичную аминокислотным остаткам 22-60 в SEQ ID NO:6 или SEQ ID NO:8.
[00145] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит один или более суперспиральных доменов, где указанные один или более суперспиральных доменов содержат аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную одному или более суперспиральным доменам, присутствующим в SEQ ID NO:6 или SEQ ID NO:8.
[00146] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, содержит один или более суперспиральных доменов, где указанные один или более суперспиральных доменов содержат аминокислотную последовательность, практически идентичную или идентичную одному или более суперспиральным доменам, присутствующим в SEQ ID NO:6 или SEQ ID NO:8.
[00147] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, имеет N-концевую область, причем эта N-концевая область содержит аминокислотную последовательность, по меньшей мере на 50% (например, на 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или больше) идентичную N-концевой области, присутствующей в SEQ ID NO:6 или SEQ ID NO:8.
[00148] В различных вариантах осуществления полипептид Angptl8, вырабатываемый животным, отличным от человека, описанным в данном документе, имеет N-концевую область, причем эта N-концевая область содержит аминокислотную последовательность, практически идентичную или идентичную N-концевой области, присутствующей в SEQ ID NO:6 или SEQ ID NO:8.
[00149] Предусмотрены композиции и способы получения животных, отличных от человека, которые экспрессируют человеческий или гуманизированный полипептид Angptl8, в том числе конкретные полиморфные формы, аллельные варианты (например, с различиями по отдельным аминокислотам) или изоформы, полученные в результате альтернативного сплайсинга, в том числе композиции и способы получения животных, отличных от человека, которые экспрессируют такие полипептиды под контролем человеческого промотора и человеческой регуляторной последовательности. В некоторых вариантах осуществления также предусмотрены композиции и способы получения животных, отличных от человека, которые экспрессируют такие белки под контролем промотора, отличного от человеческого, и регуляторной последовательности, отличной от человеческой. В некоторых вариантах осуществления также предусмотрены композиции и способы получения животных, отличных от человека, которые экспрессируют такие белки под контролем эндогенного промотора и эндогенной регуляторной последовательности. В некоторых определенных вариантах осуществления эндогенные промоторы и эндогенные регуляторные последовательности представляют собой эндогенные промоторы грызунов и эндогенные регуляторные последовательности грызунов. Способы включают вставку генетического материала, кодирующего полный или неполный человеческий полипептид ANGPTL8, в точное месторасположение в геноме животного, отличного от человека, которое соответствует эндогенному гену Angptl8, за счет чего обеспечивается создание гуманизированного гена Angptl8, который экспрессирует полипептид Angptl8, являющийся полностью или частично человеческим. В некоторых вариантах осуществления способы включают вставку геномной ДНК, соответствующей полным или неполным экзонам 1-4 человеческого гена ANGPTL8, в эндогенный ген Angptl8 животного, отличного от человека, за счет чего обеспечивается создание гуманизированного гена, кодирующего белок Angptl8, который содержит человеческую часть, содержащую аминокислоты, кодируемые вставленными экзонами.
[00150] При необходимости кодирующую область генетического материала или полинуклеотидной (полинуклеотидных) последовательности (последовательностей), кодирующую полный или неполный человеческий (или гуманизированный) полипептид ANGPTL8, можно модифицировать таким образом, чтобы она содержала кодоны, оптимизированные для экспрессии в клетках животного, отличного от человека (см., например, патенты США №№5670356 и 5874304). Кодон-оптимизированные последовательности представляют собой синтетические последовательности и предпочтительно кодируют полипептид (или биологически активный фрагмент полноразмерного полипептида, обладающий практически такой же активностью, как и полноразмерный полипептид), идентичный кодируемому исходным полинуклеотидом, не являющимся кодон-оптимизированным. В некоторых вариантах осуществления кодирующая область генетического материала, кодирующая полный или неполный человеческий (или гуманизированный) полипептид ANGPTL8, может содержать последовательность, измененную для оптимизации частоты использования кодонов для конкретного типа клеток (например, клетки грызуна). Например, кодоны геномной ДНК, соответствующие полным или неполным экзонам 1-4 человеческого гена ANGPTL8, подлежащим вставке в эндогенный ген Angptl8 животного, отличного от человека (например, грызуна), можно оптимизировать для экспрессии в клетке животного, отличного от человека. Такая последовательность может быть описана как кодон-оптимизированная последовательность.
[00151] Способы получения трансгенных животных, отличных от человека, в том числе с помощью нокаутов и нокинов, хорошо известны из уровня техники (см., например, Gene Targeting: A Practical Approach, Joyner, ed., Oxford University Press, Inc. (2000)). Например, получение трансгенных грызунов может необязательно предусматривать разрушение генетических локусов одного или более эндогенных генов грызуна (или сегментов генов) и введение одного или более гетерологичных генов (или последовательностей, кодирующих Angptl8) в геном грызуна, в некоторых вариантах осуществления в то же месторасположение, в котором находился эндогенный ген грызуна (или сегменты гена).
[00152] В некоторых вариантах осуществления гетерологичные (например, человеческие или гуманизированные) гены Angptl8 или гетерологичные последовательности, кодирующие Angptl8, описанные в данном документе, произвольным образом вводят в геном грызуна. В таких вариантах осуществления грызунов, имеющих, содержащих или иным образом несущих произвольным образом введенные гетерологичные (или гуманизированные) гены Angptl8 или гетерологичные последовательности, кодирующие Angptl8, можно охарактеризовать как имеющие гетерологичный трансген Angptl8 или гетерологичную трансгенную конструкцию Angptl8. Как правило, трансген и/или трансгенная конструкция содержит, помимо прочего, последовательность нуклеиновой кислоты (кодирующую, например, полный или неполный полипептид, представляющий интерес), которую человек вводит в клетку, отличную от человеческой (например, эмбриональную стволовую клетку грызуна), с помощью способов, описанных в данном документе или иным образом известных из уровня техники. Кроме того, трансген может быть частично или полностью гетерологичным, т.е. чужеродным, для животного, отличного от человека, или клетки, отличной от человеческой, в которую его вводят. Трансген может дополнительно содержать одну или более последовательностей, регулирующих транскрипцию, и любую другую нуклеиновую кислоту, такую как интроны или промоторы (например, конститутивные, тканеспецифические и т.д.), которые могут быть необходимы для экспрессии выбранной последовательности нуклеиновой кислоты. В некоторых вариантах осуществления гетерологичные (или гуманизированные) гены Angptl8 или гетерологичные последовательности, кодирующие Angptl8, описанные в данном документе, вводят в эндогенный ген Angptl8 в геноме грызуна; в некоторых определенных вариантах осуществления эндогенный локус гена Angptl8 изменяют, модифицируют или конструируют таким образом, чтобы он содержал человеческие последовательности (или фрагменты гена) ANGPTL8, функционально связанные с одной или более последовательностями (или фрагментами гена) Angptl8, отличными от человеческих.
[00153] Как описано в данном документе, гетерологичные (или гуманизированные) гены Angptl8 или гетерологичные последовательности, кодирующие Angptl8, функционально связаны с последовательностями, контролирующими экспрессию, такими как промотор, для управления экспрессией гетерологичного (или гуманизированного) Angptl8 у животных, отличных от человека. В некоторых вариантах осуществления такие промоторы представляют собой промоторы Angptl8, отличные от человеческих (например, промоторы Angptl8 грызунов). Специалистам в данной области техники после прочтения настоящего раскрытия будет понятно, что другие промоторы, отличные от человеческих, могут быть функционально связаны с гетерологичными последовательностями Angptl8, вставленными в геном животных, отличных от человека, описанных в данном документе, независимо от того, размещены ли такие гетерологичные последовательности Angptl8 в том же месторасположении, в котором находился эндогенный ген, отличный от человеческого, или произвольным образом интегрированы в геном животного, отличного от человека. В некоторых вариантах осуществления промотор, отличный от человеческого, представляет собой или содержит конститутивный промотор. В некоторых вариантах осуществления промотор, отличный от человеческого, представляет собой или содержит вирусный промотор (например, промотор вируса обезьян, промотор вируса простого герпеса, промотор вируса папилломы, промотор аденовируса, промотор ретровируса и т.д.). В некоторых вариантах осуществления промотор, отличный от человеческого, представляет собой промотор млекопитающего. Подходящие примеры промоторов, которые можно использовать в соответствии с настоящим изобретением, включают без ограничения промоторы SRα, промоторы CMV человека или мышей, промоторы EF1α и ранние промоторные области SV40. Другие промоторы, контролирующие экспрессию желаемых полипептидов тканеспецифическим образом, известны из уровня техники и при необходимости могут использоваться в способах, описанных в данном документе. Кроме того, промоторы можно выбрать в зависимости от желаемого типа клеток для экспрессии. Иллюстративные промоторы можно найти, например, в Villa-Komaroff et al., 1978, Proc. Natl. Acad. Sci. U.S.A. 75:3727-31; Benoist et al., 1981, Nature 290:304-10; Wagner et al., 1981, Proc. Natl. Acad. Sci. U.S.A. 78:1441-5; Brinster et al., 1982, Nature 296:39-42; DeBoer et al., 1983, Proc. Natl. Acad. Sci. U.S.A. 80:21-5; Boshart et al., 1985, Cell 41:521-30; Foecking et al., 1986, Gene 45:101-5; Takebe et al., 1988, Mol. Cell. Bio. 8:466-72.
[00154] В подходе с гуманизацией гена Angptl8 используют относительно минимальную модификацию взаимодействий эндогенного белка и передачи сигнала с его помощью, в результате чего у животного, отличного от человека, в различных вариантах осуществления наблюдаются естественные функции и активность, опосредованные Angptl8, поскольку геномные последовательности Angptl8 модифицируются в одном фрагменте и, таким образом, сохраняют нормальные функциональные свойства благодаря включению необходимых регуляторных последовательностей. Кроме того, в различных вариантах осуществления модификация не влияет на секрецию функционального полипептида Angptl8 в сыворотке крови и сохраняет нормальные функции и/или взаимодействия посредством связывания с различными липидами (например, триглицеридами).
[00155] Схематическая иллюстрация (без соблюдения масштаба) геномной организации эндогенного мышиного гена Angptl8 и человеческого гена ANGPTL8 приведена на фигуре 1. Иллюстративный способ гуманизации эндогенного мышиного гена Angptl8 с помощью геномного фрагмента, содержащего экзоны 1-4 и 3'-концевую UTR человеческого гена ANGPTL8, приведен на фигуре 3. Как проиллюстрировано, синтетический фрагмент ДНК размером 2383 п.о., соответствующий экзонам 1-4 и 3'-концевой UTR человеческого гена ANGPTL8, вставляют в место расположения последовательности эндогенного локуса мышиного гена Angptl8 размером 1576 п.о. посредством гомологичной рекомбинации с использованием нацеливающейся конструкции. Синтетический фрагмент ДНК размером 2383 п.о. можно клонировать непосредственно из человеческой ДНК или синтезировать из исходной последовательности (например, имеющей № доступа в GenBank NM_018687.6, SEQ ID NO:5). Эта геномная ДНК содержит часть гена, кодирующую по меньшей мере приблизительно аминокислотные остатки 22-198 человеческого полипептида ANGPTL8, отвечающие за связывание с липидами.
[00156] Животное, отличное от человека (например, мышь), имеющее гуманизированный ген Angptl8 в эндогенном локусе Angptl8, можно получить любым способом, известным из уровня техники. Например, можно получить нацеливающийся вектор, с помощью которого вводят полный или неполный человеческий ген ANGPTL8 вместе с селективным маркерным геном. На фигуре 3 проиллюстрирован нацеливающийся вектор, который содержит эндогенный локус Angptl8 генома мыши, содержащий вставку синтетического фрагмента ДНК размером 2383 п.о., который соответствует экзонам 1-4 (в частности, кодирующей части экзона 1, экзону 2, экзону 3 и экзону 4, который содержит 3'-концевую UTR) человеческого гена ANGPTL8. Как проиллюстрировано, нацеливающаяся конструкция содержит 5'-концевое гомологичное плечо, содержащее последовательность, расположенную выше экзона 1 (т.е. содержащую стартовый кодон ATG) эндогенного мышиного гена Angptl8 (~ 79 т.о.), за которым расположены синтетический фрагмент ДНК размером 2383 п.о., селекционная кассета устойчивости к лекарственному средству (например, ген устойчивости к неомицину, фланкированный с обеих сторон последовательностями loxP; ~ 5 т.о.) и 3'-концевое гомологичное плечо, содержащее 3'-концевую UTR эндогенного мышиного гена Angptl8 (~ 148 т.о.). Нацеливающаяся конструкция содержит самоудаляющуюся селекционную кассету устойчивости к лекарственному средству (например, ген устойчивости к неомицину, фланкированный последовательностями loxP; см. патенты США №№8697851, 8518392 и 8354389, все из которых включены в данный документ посредством ссылки). В результате электропорации в эмбриональных стволовых клетках создается модифицированный эндогенный ген Angptl8, содержащий 2383 п.о. человеческого гена ANGPTL8 (т.е. кодирующую часть экзона 1, экзон 2, экзон 3 и экзон 4, который содержит 3'-концевую UTR) на месте 1576 п.о. эндогенного гена Angptl8 дикого типа, которые содержатся в нацеливающемся векторе. В результате создания гуманизированного гена Angptl8 клетка или животное, отличное от человека, экспрессируют гуманизированный полипептид Angptl8, содержащий аминокислоты, кодируемые синтетическим фрагментом ДНК размером 2383 п.о. Селекционную кассету устойчивости к лекарственному средству удаляют способом, зависимым от стадии развития, т.е. у потомства, происходящего от мышей, клетки зародышевой линии которых содержат гуманизированный ген Angptl8, описанный выше, будет утрачиваться селективный маркер из дифференцированных клеток в ходе развития (см. нижнюю часть фигуры 3).
[00157] Иллюстративные промоторы, которые могут быть функционально связаны с селекционными кассетами устойчивости к лекарственным средствам и/или генами рекомбиназ, содержащимися в нацеливающихся векторах, описанных в данном документе, приведены ниже. Дополнительные подходящие промоторы, которые можно использовать в нацеливающихся векторах, описанных в данном документе, включают промоторы, описанные в патентах США №№8697851, 8518392 и 8354389; все из которых включены в данный документ посредством ссылки. Иллюстративные промоторные последовательности включают промотор гена протамина 1 (Prm1) (SEQ ID NO:12), промотор Blimp1 размером 1 т.о. (SEQ ID NO:13) и промотор Blimp1 размером 2 т.о. (SEQ ID NO:14).
[00158] В некоторых вариантах осуществления животное, отличное от человека, имеющее гуманизированный ген Angptl8, описанный в данном документе, можно охарактеризовать как трансгенное по гуманизированному гену Angptl8 или как животное, отличное от человека, трансгенное по Angptl8. Такие описания используются в данном документе взаимозаменяемо и относятся к любому животному, отличному от человека, не встречающемуся в природе, у которого одна или более клеток животного, отличного от человека, содержат полную или неполную гетерологичную последовательность нуклеиновой кислоты Angptl8 и/или последовательность, кодирующую Angptl8, описанную в данном документе. В некоторых вариантах осуществления полную или неполную гетерологичную последовательность нуклеиновой кислоты Angptl8 и/или последовательность, кодирующую Angptl8, вводят в клетку напрямую или опосредованно путем введения в клетку-предшественника, путем преднамеренной генетической манипуляции, как, например, путем микроинъекции, или путем инфицирования рекомбинантным вирусом. В таких вариантах осуществления генетическая манипуляция не включает классические методики скрещивания, а скорее направлена на введение рекомбинантной(рекомбинантных) молекулы(молекул) ДНК, которые содержат полную или неполную гетерологичную последовательность нуклеиновой кислоты Angptl8 и/или последовательность, кодирующую Angptl8, описанную в данном документе. Такая молекула может интегрироваться в хромосому или может представлять собой внехромосомную реплицирующуюся ДНК. Описанные в данном документе трансгенные животные, отличные от человека, включают животных, которые являются гетерозиготными или гомозиготными по полной или неполной гетерологичной последовательности нуклеиновой кислоты Angptl8 и/или последовательности, кодирующей Angptl8, и/или животных, которые имеют одну или несколько копий полной или неполной гетерологичной последовательности нуклеиновой кислоты Angptl8 и/или последовательности, кодирующей Angptl8, описанной в данном документе.
[00159] Трансгенного животного-основателя, отличного от человека, можно идентифицировать на основании наличия гуманизированного гена Angptl8 в его геноме и/или экспрессии полипептидов Angptl8, содержащих аминокислоты, кодируемые вставленным генетическим материалом, в тканях или клетках животного, отличного от человека. Затем трансгенного животного-основателя, отличного от человека, можно использовать для разведения дополнительных животных, отличных от человека, несущих гуманизированный ген Angptl8, за счет чего обеспечивается создание ряда животных, отличных от человека, каждое из которых несет одну или более копий гуманизированного гена Angptl8. Более того, трансгенных животных, отличных от человека, несущих гуманизированный ген Angptl8, при необходимости можно дополнительно скрещивать с другими трансгенными животными, отличными от человека, несущими другие трансгены (например, гены человеческих иммуноглобулинов).
[00160] Также можно получать таких трансгенных животных, отличных от человека, которые содержат выбранные системы, позволяющие регулировать экспрессию гуманизированного гена Angptl8 (или гуманизированного трансгена Angptl8) или управлять ей. Иллюстративные системы включают систему рекомбинации Cre/loxP из бактериофага P1 (см., например, Lakso, M. et al., 1992, Proc. Natl. Acad. Sci. U.S.A. 89:6232-6) и систему рекомбинации FLP/Frt из S. cerevisiae (O’Gorman, S. et al, 1991, Science 251:1351-5). Таких животных можно получать путем конструирования «двойных» трансгенных животных, например, путем спаривания двух трансгенных животных, одно из которых содержит трансген, содержащий выбранную модификацию (например, гуманизированный ген или трансген Angptl8), а другое содержит трансген, кодирующий рекомбиназу (например, рекомбиназу Cre).
[00161] Хотя варианты осуществления, в которых используется гуманизированный ген Angptl8 у мыши (т.е. у мыши с геном Angptl8, кодирующим полипептид Angptl8, имеющий полную или неполную человеческую последовательность), широко обсуждаются в данном документе, также предусмотрены другие животные, отличные от человека, которые содержат гуманизированный ген Angptl8. В некоторых вариантах осуществления такие животные, отличные от человека, содержат гуманизированный ген Angptl8, функционально связанный с промотором Angptl8 грызуна. В некоторых вариантах осуществления такие животные, отличные от человека, содержат гуманизированный ген Angptl8, функционально связанный с эндогенным промотором Angptl8; в некоторых вариантах осуществления - с эндогенным промотором Angptl8 грызуна. В некоторых вариантах осуществления такие животные, отличные от человека, экспрессируют гуманизированный полипептид Angptl8 из эндогенного локуса, где гуманизированный полипептид Angptl8 содержит по меньшей мере аминокислотные остатки 22-60, 77-134, 156-193 или 22-198 человеческого полипептида ANGPTL8. Такие животные, отличные от человека, включают любых из тех, которых можно подвергнуть генетической модификации для экспрессии полипептида Angptl8, раскрытого в данном документе, в том числе, например, млекопитающих, например, мышь, крысу, кролика, свинью, бычьих (например, корову, быка, буйвола), оленя, овцу, козу, курицу, кошку, собаку, хорька, примата (например, игрунку, макака-резуса) и т.д. Например, для тех животных, отличных от человека, для которых подходящие генетически модифицируемые ES-клетки являются труднодоступными, используют другие способы для получения животного, отличного от человека, содержащего генетическую модификацию. Такие способы включают, например, модификацию генома клеток, отличных от ES-клеток (например, фибробласта или индуцированной плюрипотентной клетки), и использование переноса ядер соматических клеток (SCNT) для переноса генетически модифицированного генома в подходящую клетку, например, в энуклеированный ооцит, и вынашивание модифицированной клетки (например, модифицированного ооцита) животным, отличным от человека, в подходящих условиях с образованием эмбриона.
[00162] Например, крысиная плюрипотентная и/или тотипотентная клетка может быть получена из крысы любой линии, в том числе, например, линии крыс ACI, линии крыс Dark Agouti (DA), линии крыс Wistar, линии крыс LEA, линии крыс Sprague Dawley (SD) или линии крыс Fischer, такой как Fisher F344 или Fisher F6. Крысиные плюрипотентные и/или тотипотентные клетки также могут быть получены из линии, происходящей из помеси двух или более линий, перечисленных выше. Например, крысиная плюрипотентная и/или тотипотентная клетка может быть получена из линии DA или линии ACI. Линия крыс ACI характеризуется наличием окраски «черный агути» с белыми брюхом и лапами и гаплотипаRT1av1. Такие линии доступны из множества источников, в том числе Harlan Laboratories. Примером линии крысиных ES-клеток из крысы ACI является крысиная ES-клетка ACI.G1. Линия крыс Dark Agouti (DA) характеризуется наличием окраски «агути» и гаплотипаRT1av1. Такие крысы доступны из множества источников, в том числе Charles River и Harlan Laboratories. Примерами линии крысиных ES-клеток из крысы DA являются линия крысиных ES-клеток DA.2B и линия крысиных ES-клеток DA.2C. В некоторых случаях крысиные плюрипотентные и/или тотипотентные клетки получены из инбредной линии крыс. См., например, публикацию заявки на патент США № 2014-0235933 A1, включенную в данный документ посредством ссылки.
[00163] Способы модификации генома животного, отличного от человека (например, генома свиньи, коровы, грызуна, курицы и т.д.), включают, например, использование нуклеазы с «цинковыми пальцами» (ZFN), эффекторной нуклеазы, подобной активатору транскрипции (TALEN), или белка Cas (т.e. системы CRISPR/Cas) для модификации генома таким образом, чтобы он содержал гуманизированный ген Angptl8.
Способы, в которых используются животные, отличные от человека, имеющие гуманизированный ген ANGPTL8
[00164] Настоящее изобретение, помимо прочего, основывается на понимании того, что создание системы in vivo, в которой используются молекулы, регулирующие метаболизм липидов, можно осуществлять с использованием гуманизированного гена Angptl8, описанного в данном документе. Такая система in vivo позволяет разрабатывать терапевтические средства и/или режимы терапии, которые направлены на уменьшение интенсивности эффектов дисфункции метаболизма липидов у пациентов-людей. Кроме того, такая система in vivo также обеспечивает разработку терапевтических средств и/или режимов терапии, которые направлены на изменение ассоциированной с ангиопоэтином регуляции метаболизма липидов при гипертриглицеридемии и/или сердечно-сосудистых заболеваниях, нарушениях или состояниях.
[00165] Животные, отличные от человека, описанные в данном документе, обеспечивают улучшенную систему in vivo и источник биологических материалов (например, клеток), экспрессирующих человеческий (или гуманизированный) ANGPTL8, которые являются применимыми во множестве анализов. В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для разработки терапевтических средств, которые нацеливаются на человеческий ANGPTL8 и/или модулируют передачу сигнала с помощью человеческого ANGPTL8 (например, нарушая взаимодействия с партнерами человеческого ANGPTL8 по связыванию, такими как ANGPTL3). В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для скрининга и разработки терапевтических средств-кандидатов (например, антител), которые блокируют взаимодействие человеческого ANGPTL8 с человеческим ANGPTL3. В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения профиля связывания антагонистов и/или агонистов человеческого ANGPTL8 у животного, отличного от человека, описанного в данном документе; в некоторых вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения эпитопа или эпитопов для одного или более терапевтических антител-кандидатов, которые связываются с человеческим ANGPTL8.
[00166] В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения фармакокинетических профилей антител к ANGPTL8. В различных вариантах осуществления каждое из одного или более животных, отличных от человека, описанных в данном документе, и одного или более контрольных или эталонных животных, отличных от человека, подвергают воздействию одного или более терапевтических антител-кандидатов к ANGPTL8 в различных дозах (например, 0,1 мг/кг, 0,2 мг/кг, 0,3 мг/кг, 0,4 мг/кг, 0,5 мг/кг, 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг, 7,5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг, 25 мг/кг, 30 мг/кг, 40 мг/кг или 50 мг/кг или больше). Дозы терапевтических антител-кандидатов можно вводить посредством любого желаемого пути введения, в том числе парентерального и непарентерального путей введения. Парентеральные пути включают, например, внутривенный, внутриартериальный, интрапортальный, внутримышечный, подкожный, внутрибрюшинный, интраспинальный, интратекальный, интрацеребровентрикулярный, внутричерепной, интраплевральный или другие пути инъекции. Непарентеральные пути включают, например, пероральный, интраназальный, трансдермальный, внутрилегочный, ректальный, трансбуккальный, вагинальный, внутриглазной. Введение также можно осуществлять посредством непрерывной инфузии, местного введения, замедленного высвобождения из имплантатов (гелей, мембран и т.п.) и/или внутривенной инъекции. У животных, отличных от человека (гуманизированных и контрольных), отбирают кровь в различные моменты времени (например, 0 ч., 6 ч., 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 7 дней, 8 дней, 9 дней, 10 дней, 11 дней или до 30 или больше дней). Можно проводить различные анализы для определения фармакокинетических профилей вводимых терапевтических антител-кандидатов с использованием образцов, полученных от животных, отличных от человека, описанных в данном документе, в том числе без ограничения анализы уровня общего IgG, гуморального ответа на терапевтические средства, агглютинации и т.д.
[00167] В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для измерения терапевтического эффекта блокирования или модулирования передачи сигнала с помощью человеческого ANGPTL8 и эффекта в отношении экспрессии генов в результате клеточных изменений. В различных вариантах осуществления животное, отличное от человека, описанное в данном документе, или клетки, выделенные из него, подвергают воздействию терапевтического средства-кандидата, которое связывается с человеческим полипептидом ANGPTL8 (или частью человеческого полипептида ANGPTL8) у животного, отличного от человека, и по истечении последующего периода времени анализируют в отношении эффектов, оказываемых на ANGPTL8-зависимые процессы, например, на метаболизм триглицеридов, активность липопротеинлипазы и поглощение различных липопротеинов (например, липопротеинов низкой плотности LDL).
[00168] Животные, отличные от человека, описанные в данном документе, экспрессируют человеческий (или гуманизированный) полипептид ANGPTL8, поэтому можно создавать клетки, линии клеток и культуры клеток, служащие в качестве источника человеческого ANGPTL8 для применения в анализах связывания и функциональных анализах, например, для анализа связывания или функции антагониста или агониста ANGPTL8, в частности, если антагонист или агонист является специфичным к последовательности или эпитопу человеческого ANGPTL8 или, в качестве альтернативы, специфичным к последовательности или эпитопу человеческого ANGPTL8, которые подвергаются ассоциации с ANGPTL3. В различных вариантах осуществления эпитопы ANGPTL8, с которыми связываются терапевтические антитела-кандидаты, можно определять с применением клеток, выделенных из животных, отличных от человека, описанных в данном документе. В различных вариантах осуществления человеческий (или гуманизированный) полипептид ANGPTL8, экспрессируемый животным, отличным от человека, описанным в данном документе, может содержать вариант аминокислотной последовательности. В различных вариантах осуществления животные, отличные от человека, описанные в данном документе, экспрессируют человеческий (или гуманизированный) вариант ANGPTL8. В различных вариантах осуществления вариант является полиморфным в положении аминокислоты, ассоциированном со связыванием с лигандом. В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения эффекта связывания с лигандом посредством взаимодействия с полиморфным вариантом человеческого ANGPTL8. Иллюстративные варианты человеческого полипептида ANGPTL8 включают вариант, характеризующийся аминокислотной заменой R59W (Quagliarini, F. et al., 2012, Proc. Nat. Acad. Sci. U.S.A. 109(48):19751-6) или Q121X (Clapham et al., BMC Endocr Disord. 2016, 16:7). В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 ассоциирован с более низкими уровнями холестерина липопротеинов низкой плотности (LDL) и/или холестерина липопротеинов высокой плотности (HDL) в плазме крови. В некоторых вариантах осуществления вариант человеческого полипептида ANGPTL8 ассоциирован с более низкими уровнями триглицеридов и/или холестерина HDL в плазме крови.
[00169] Клетки животных, отличных от человека, описанных в данном документе, можно выделять и использовать для конкретной цели или можно поддерживать в культуре в течение многих поколений. В различных вариантах осуществления клетки животного, отличного от человека, описанного в данном документе, иммортализуют (например, посредством применения вируса) и поддерживают в культуре в течение неопределенного времени (например, в серийных культурах).
[00170] Животные, отличные от человека, описанные в данном документе, обеспечивают систему in vivo для оценки фармакокинетических свойств лекарственного средства (например, модулятора ANGPTL8). В различных вариантах осуществления лекарственное средство можно доставлять или вводить одному или более животным, отличным от человека, описанным в данном документе, с последующим мониторингом животных, отличных от человека (или клеток, выделенных из них), или проведением одного или более анализов в их отношении для определения эффекта лекарственного средства в отношении животного, отличного от человека. Фармакокинетические свойства включают без ограничения характер переработки лекарственного средства в различные метаболиты в организме животного (или выявляемое наличие или отсутствие одного или более метаболитов лекарственных средств, в том числе токсичных метаболитов), период полувыведения лекарственного средства, уровни циркулирующего в крови лекарственного средства после введения (например, концентрацию лекарственного средства в сыворотке крови), гуморальный ответ на лекарственное средство (например, выработку антител к лекарственным средствам), всасывание и распределение лекарственного средства, путь введения, пути выведения и/или клиренс лекарственного средства. В некоторых вариантах осуществления мониторинг фармакокинетических и фармакодинамических свойств лекарственных средств проводят у животных, отличных от человека, описанных в данном документе, или посредством их использования.
[00171] В некоторых вариантах осуществления проведение анализа включает определение эффекта в отношении фенотипа и/или генотипа животного, отличного от человека, которому вводят лекарственное средство. В некоторых вариантах осуществления проведение анализа включает определение изменчивости лекарственного средства от партии к партии. В некоторых вариантах осуществления проведение анализа включает определение различий между эффектами лекарственного средства при введении животному, отличному от человека, описанному в данном документе, и эталонному животному, отличному от человека. В различных вариантах осуществления эталонные животные, отличные от человека, могут иметь модификацию, описанную в данном документе, модификацию, отличную от описанной в данном документе, или не иметь модификации (т.е. в случае животного, отличного от человека, дикого типа).
[00172] Иллюстративные параметры, которые можно измерять у животных, отличных от человека (или в клетках, выделенных из них, и/или с их применением), для оценки фармакокинетических свойств лекарственного средства включают без ограничения агглютинацию, аутофагию, клеточное деление, гибель клеток, комплементзависимый гемолиз, целостность ДНК, титр антител, специфичных к лекарственному средству, метаболизм лекарственного средства, экспрессию генов, определяемую с помощью микроматриц, метаболическую активность, митохондриальную активность, окислительный стресс, фагоцитоз, биосинтез белка, разрушение белка, секрецию белка, стрессовую реакцию, концентрацию лекарственного средства в целевой ткани, концентрацию лекарственного средства в нецелевой ткани, транскрипционную активность и т.п. В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения фармацевтически эффективной дозы лекарственного средства.
[00173] Животные, отличные от человека, описанные в данном документе, обеспечивают систему in vivo для анализа и тестирования лекарственного средства или вакцины. В различных вариантах осуществления лекарственное средство-кандидата или вакцину-кандидата можно вводить одному или более животным, отличным от человека, описанным в данном документе, с последующим мониторингом животных, отличных от человека, для определения одного или более из иммунного ответа на лекарственное средство или вакцину, профиля безопасности лекарственного средства или вакцины или эффекта в отношении заболевания или состояния. Иллюстративные способы, применяемые для определения профиля безопасности, включают измерения токсичности, оптимальной концентрации дозы, эффективности лекарственного средства или вакцины и возможных факторов риска. Такие лекарственные средства или вакцины можно улучшать и/или разрабатывать у таких животных, отличных от человека.
[00174] Эффективность вакцины можно определять с помощью ряда способов. Вкратце, животных, отличных от человека, описанных в данном документе, вакцинируют с помощью способов, известных из уровня техники, и затем заражают вакциной, или вакцину вводят уже инфицированному животному, отличному от человека. Ответ животного(животных), отличного(отличных) от человека, на вакцину можно измерять путем мониторинга животного(животных), отличного(отличных) от человека (или клеток, выделенных из них), и/или проведения одного или более анализов в их отношении для определения эффективности вакцины. Ответ животного(животных), отличного(отличных) от человека, на вакцину затем сравнивают с ответом контрольных животных, используя один или более количественных показателей, известных из уровня техники и/или описанных в данном документе.
[00175] Эффективность вакцины можно дополнительно определять с помощью анализов нейтрализации вируса. Вкратце, животных, отличных от человека, описанных в данном документе, иммунизируют, и у них собирают сыворотку крови в различные дни после иммунизации. Серийные разведения сыворотки крови предварительно инкубируют с вирусом, и в ходе этого периода времени антитела в сыворотке крови, специфичные к вирусу, связываются с ним. Смесь вирус/сыворотка крови затем добавляют к пермиссивным клеткам для определения инфицирующей способности с помощью анализа бляшкообразования или анализа микронейтрализации. Если антитела в сыворотке крови нейтрализуют вирус, то наблюдается меньшее количество бляшек или более низкое количество относительных люциферазных единиц по сравнению с контрольной группой.
[00176] В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют в исследованиях эффективности для определения эффекта терапевтических средств, противодействующих ANGPTL8 (например, антител к ANGPTL8), in vivo в отношении уровней циркулирующих в крови триглицеридов. Например, у животных, отличных от человека, описанных в данном документе, производят забор крови перед введением терапевтических средств-кандидатов или контролей, и при необходимости их распределяют по различным группам обработки. Терапевтические средства-кандидаты или контроли вводят в желаемой дозе, и забор крови производят в последовательные дни после введения. Используя собранную сыворотку крови, можно измерить уровни триглицеридов, глюкозы и/или инсулина в плазме крови. Также при необходимости можно измерить уровни терапевтических средств-кандидатов. Иллюстративные анализы, которые можно применять для выявления различных молекул, включаю ELISA-анализы и другие, описанные в Wang, Y. et al., 2013, Proc. Nat. Acad. Sci. U.S.A. 110(40):16109-114; Quagliarini, F. et al., 2012, Proc. Nat. Acad. Sci. U.S.A. 109(48):19751-6.
[00177] В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют для определения активности липопротеинлипазы (LPL) после обработки терапевтическими средствами, противодействующими ANGPTL8 (например, антителами к ANGPTL8). Например, у животных, отличных от человека, описанных в данном документе, производят забор крови перед введением терапевтических средств-кандидатов или контролей, и при необходимости их включают в различные группы обработки. Терапевтические средства-кандидаты или контроли вводят в желаемой дозе, и забор крови производят в последовательные дни после введения. По истечении достаточного периода времени (например, нескольких дней) животным, отличным от человека, вводят антикоагулянт (например, гепарин) для того, чтобы LPL высвободился с поверхностей эндотелия сосудов, и вскоре после этого от животных, отличных от человека, получают кровь. Гепаринизированную плазму крови фракционируют для отделения LPL с помощью хроматографии на гепарин-сефарозе, и активность LPL анализируют с помощью субстрата липазы. Общие способы и анализы описаны, например, в Wang, Y. et al., 2013, Proc. Nat. Acad. Sci. U.S.A. 110(40):16109-114; Quagliarini, F. et al., 2012, Proc. Nat. Acad. Sci. U.S.A. 109(48):19751-6.
[00178] В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, используют в тестах толерантности к липидам для определения очищения от триглицеридов с помощью острой жировой нагрузки после обработки терапевтическими средствами, противодействующими ANGPTL8 (например, антителами к ANGPTL8). Например, у животных, отличных от человека, описанных в данном документе, производят забор крови перед введением терапевтических средств-кандидатов или контролей, и их включают в различные группы обработки. Терапевтические средства-кандидаты или контроли вводят в желаемой дозе. Через несколько дней животных, отличных от человека, подвергают режиму воздержания от приема пищи после введения липидной эмульсии (например, в концентрации 20%) в соответствии с весом тела. В крови, собранной у животных, отличных от человека, в каждой группе обработки, определяют уровни триглицеридов в плазме крови. Общие способы и анализы описаны, например, в Wang, Y. et al., 2013, Proc. Nat. Acad. Sci. U.S.A. 110(40):16109-114; Quagliarini, F. et al., 2012, Proc. Nat. Acad. Sci. U.S.A. 109(48):19751-6.
[00179] Животные, отличные от человека, описанные в данном документе, обеспечивают улучшенную систему in vivo для разработки и получения характеристик терапевтических средств-кандидатов для применения при гипертриглицеридемии. В различных вариантах осуществления животных, отличных от человека, описанных в данном документе, можно подвергать специфическому режиму кормления (например, с перекармливанием или воздержанием от приема пищи) с последующим введением одного или более терапевтических средств-кандидатов. В некоторых вариантах осуществления терапевтические средства-кандидаты могут включать полиспецифическое антитело (например, биспецифическое антитело) или коктейль из антител; в некоторых вариантах осуществления использование терапевтических средств-кандидатов включает комбинированную терапию, такую как, например, последовательное или одновременное введение доз моноспецифических антител. Животных, отличных от человека, можно подвергать режиму кормления в течение периода времени, достаточного для того, чтобы уровни ANGPTL8 были высокими в одном или более месторасположениях (например, в ткани печени и/или жировой ткани) в организме животного, отличного от человека. Уровни триглицеридов, глюкозы и/или инсулина в плазме крови, а также активность липопротеинлипазы и т.д. можно измерять как до, так и после введения терапевтического(терапевтических) средства-кандидата(средств-кандидатов). При необходимости у животного, отличного от человека, также можно измерять цитотоксичность терапевтических средств-кандидатов.
[00180] Животных, отличных от человека, описанных в данном документе, можно использовать для разработки одной или более моделей заболевания для установления или оценки эффективности терапевтических средств-кандидатов и/или режимов терапии (например, монотерапии, комбинированной терапии, тестирования в диапазоне доз и т.д.) в лечении заболеваний, нарушений или состояний, поражающих людей. У животных, отличных от человека, описанных в данном документе, можно сформировать различные болезненные состояния с последующим введением одной или более молекул-кандидатов (например, лекарственных средств, целенаправленно воздействующих на ANGPTL8) для того, чтобы можно было определить эффективность одной или более молекул-кандидатов при болезненном состоянии. Животных, отличных от человека, можно поместить в различные группы обработки в зависимости от дозы таким образом, чтобы можно было определить оптимальную дозу или диапазон доз, коррелирующих с эффективным лечением сформировавшегося заболевания. В некоторых вариантах осуществления модели заболеваний включают сердечно-сосудистые заболевания, нарушения или состояния.
[00181] Молекулы-кандидаты можно вводить животным, отличным от человека, в моделях заболеваний с помощью любого способа введения, в том числе парентеральных и непарентеральных путей введения. Парентеральные пути включают, например, внутривенный, внутриартериальный, интрапортальный, внутримышечный, подкожный, внутрибрюшинный, интраспинальный, интратекальный, интрацеребровентрикулярный, внутричерепной, интраплевральный или другие пути инъекции. Непарентеральные пути включают, например, пероральный, интраназальный, трансдермальный, внутрилегочный, ректальный, трансбуккальный, вагинальный, внутриглазной. Введение также можно осуществлять посредством непрерывной инфузии, местного введения, замедленного высвобождения из имплантатов (гелей, мембран и т.п.) и/или внутривенной инъекции. В тех случаях, когда у животных, отличных от человека, описанных в данном документе, оценивают комбинированную терапию, молекулы-кандидаты можно вводить посредством одного и того же пути введения или посредством различных путей введения. В тех случаях, когда у животных, отличных от человека, описанных в данном документе, оценивают режим дозирования, молекулы-кандидаты можно вводить раз в два месяца, раз в месяц, раз в три недели, раз в две недели, еженедельно, ежедневно, с переменными интервалами и/или в повышающихся концентрациях для определения режима дозирования, при котором у животного, отличного от человека, у которого были сформированы одна или более моделей заболеваний, демонстрируется желаемый терапевтический или профилактический эффект.
Наборы
[00182] В настоящем изобретении дополнительно предусмотрены упаковка или набор, содержащие один или более контейнеров, заполненных по меньшей мере одним животным, отличным от человека, клеткой, отличной от человеческой, фрагментом ДНК (или ДНК-конструкцией) и/или нацеливающимся вектором, описанными в данном документе. Наборы можно использовать в любом применимом способе (например, в способе исследования). Необязательно связанным с таким(такими) контейнером(контейнерами) может быть уведомление в форме, предписанной правительственным органом, регулирующим производство, применение или продажу фармацевтических препаратов или биологических продуктов, при этом данное уведомление отражает (а) одобрение органом, регулирующим производство, применение или продажу, для введения человеку, (b) указания по применению и/или договор, который регулирует передачу материалов и/или биологических продуктов (например, животного, отличного от человека, или клеток, отличных от человеческих, описанных в данном документе) между двумя или более организациями, или как первое, так и второе.
[00183] Другие признаки настоящего изобретения станут очевидными из следующего описания иллюстративных вариантов осуществления, которые приведены в иллюстративных целях и не подразумеваются как ограничивающие его.
ПРИМЕРЫ
[00184] Следующие примеры приведены для того, чтобы обеспечить специалистов в данной области техники описанием того, как создавать и применять способы и композиции по настоящему изобретению, и не подразумеваются как ограничивающие объем того, что авторы настоящего изобретения рассматривают в качестве своего изобретения. Если не указано иное, температура указана по Цельсию, а давление является атмосферным или близким к нему.
Пример 1. Модификация эндогенного гена ангиопоэтин-подобного белка 8
[00185] В данном примере демонстрируются иллюстративные способы модификации эндогенного гена Angptl8 у млекопитающего, отличного от человека, такого как грызун (например, мышь), таким образом, чтобы указанный эндогенный ген Angptl8 кодировал человеческий полипептид ANGPTL8. Способы, описанные в данном примере, можно при необходимости использовать для модификации эндогенного гена Angptl8 животного, отличного от человека, с помощью любой человеческой последовательности (например, варианта) или комбинации человеческих последовательностей (или фрагментов последовательностей). В данном примере для модификации эндогенного гена ANGPTL8 мыши использовали синтетический фрагмент ДНК размером 2383 п.о., содержащий экзоны 1-4 (без стартового кодона ATG) человеческого гена ANGPTL8, присутствующего в GenBank под номером доступа NM_018687.6 (SEQ ID NO:5). Выравнивание последовательностей мышиного, человеческого и иллюстративного человеческого полипептида ANGPTL8, экспрессируемого грызуном, описанным в данном документе, с сигнальным пептидом, указанным в рамке для каждой последовательности, изображено на фигуре 2. На фигуре 3 показан нацеливающийся вектор для модификации эндогенного гена Angptl8 грызуна таким образом, чтобы он кодировал человеческий полипептид ANGPTL8, который был сконструирован с использованием технологии VELOCIGENE® (см., например, патент США №6586251 и Valenzuela et al., 2003, Nature Biotech. 21(6):652-659; включенные в данный документ посредством ссылки).
[00186] Вкратце, искусственную бактериальную хромосому (BAC) клона RP23-198h22 для мыши (Invitrogen) модифицировали с удалением последовательности, содержащейся от точки, находящейся непосредственно ниже стартового кодона ATG эндогенного Angptl8, до точки, находящейся за стоп-кодоном на расстоянии 9 п.о. (т.е. экзона 1 без 11 5'-концевых нуклеотидов, экзонов 2-3 и 5'-концевой части экзона 4 до точки, находящейся за стоп-кодоном на расстоянии 9 п.о., включительно), и вставкой от точки, находящейся сразу ниже стартового кодона ATG человеческого ANGPTL8, до точки, находящейся за 3'-концевой UTR человеческого ANGPTL8 (т.е. от кодирующей части экзона 1, начинающейся сразу ниже стартового кодона ATG, до экзона 4 включительно), с использованием синтетического фрагмента ДНК размером 2383 п.о., кодирующего человеческий полипептид ANGPTL8. Эндогенную ДНК, содержащую 5'-концевую и 3'-концевую нетранслируемые области (UTR), а также стартовый кодон ATG эндогенного Angptl8, сохраняли. Таким образом, экзоны 1-4 человеческого гена ANGPTL8 без стартового кодона человеческого ANGPTL8 подвергали внутрирамочному слиянию со стартовым кодоном ATG эндогенного Angptl8. Анализ последовательности синтетического фрагмента ДНК размером 2383 п.о. (т.e. соответствующего экзонам 1-4 человеческого гена ANGPTL8) подтвердил наличие всех экзонов и сигналов сплайсинга человеческого ANGPTL8. Анализ последовательности выявил, что последовательность соответствует эталонному геному и транскрипту ANGPTL8 NM_018687.6.
[00187] Синтетический фрагмент ДНК размером 2383 п.о. синтезировали в Genescript Inc. (Пискатауэй, Нью-Джерси) и клонировали в плазмидный вектор с геном устойчивости к ампициллину. Использовали уникальные сайты распознавания для ферментов рестрикции для лигирования самоудаляющейся кассеты устойчивости к неомицину размером ~4996 п.о., фланкированной сайтами распознавания для рекомбиназы (loxP-hUb1-em7-Neo-pA-mPrm1-Crei-loxP; см. патенты США №№8697851, 8518392 и 8354389, все из которых включены в данный документ посредством ссылки). Последующий отбор в бактериальных клетках проводили посредством посева на агаровую среду, содержащую неомицин. Нацеливающийся вектор линеаризировали перед гомологичной рекомбинацией с BAC клона RP23-198H22 для мыши. По замыслу участок сочленения между фрагментом человеческого ANGPTL8 размером 2383 п.о. и нижерасположенной мышиной последовательностью содержал 3'-концевую UTR человеческого ANGPTL8 с расположенной за ней 3'-концевой UTR мышиного Angptl8 (фигура 3). Полученный нацеливающийся вектор содержал в направлении от 5'- к 3'-концу 5'-концевое гомологичное плечо, содержащее ~79 т.о. мышиной геномной ДНК из BAC клона RP23-198h22, синтетический фрагмент ДНК размером 2383 п.о. (соответствующий экзонам 1-4 человеческого гена ANGPTL8), самоудаляющуюся кассету устойчивости к неомицину, фланкированную сайтами loxP, и ~148 т.о. мышиной геномной ДНК из BAC клона RP23-198h22.
[00188] Модифицированную BAC клона bMQ-400O17, описанную выше, использовали для электропорации мышиных эмбриональных стволовых (ES) клеток с созданием модифицированных ES-клеток, содержащих эндогенный ген Angptl8, гуманизированный от экзона 1 (за вычетом стартового кодона ATG) до экзона 4, содержащего 3'-концевую UTR человеческого ANGPTL8 (т.е. с делецией 1576 п.о. эндогенного гена Angptl8 и вставкой 2383 п.о. последовательности, кодирующей человеческий ANGPTL8), включительно. ES-клетки с положительным результатом нацеливания, содержащие модифицированный ген Angptl8, идентифицировали с помощью анализа (Valenzuela et al., выше), в котором выявляли наличие последовательностей человеческого ANGPTL8 (например, экзонов 1-4) и подтверждали потерю и/или сохранение последовательностей мышиного Angptl8 (например, экзонов 1-4 и/или 5'-концевой и 3'-концевой UTR). В таблице 1 приведены праймеры и зонды, которые использовались для подтверждения модификации эндогенного гена Angptl8, описанной выше (фигура 4).
[00189] Нуклеотидная последовательность, охватывающая вышерасположенную точку вставки, в которой указана эндогенная мышиная последовательность (заключенная ниже в круглые скобки с выделенным жирным шрифтом стартовым кодоном ATG), смежная с человеческой геномной последовательностью ANGPTL8 в точке вставки, содержит следующее: (AAGGCAGCCG CAGCGGCCCG GGAACCACAC CCACGAAACT GTCAGCCATG) CCAGTGCCTG CTCTGTGCCT GCTCTGGGCC CTGGCAATGG TGACCCGGCC (SEQ ID NO: 15) (фигура 9A). См. также фигуру 3.
[00190] Нуклеотидная последовательность, охватывающая 5'-конец самоудаляющейся кассеты устойчивости к неомицину, в которой указана человеческая геномная последовательность ANGPTL8, смежная с последовательностью кассеты (заключенной ниже в круглые скобки с выделенным курсивом сайтом XhoI и выделенным жирным шрифтом сайтом loxP) ниже точки вставки, содержит следующее: GGGAGACCCC ACCCAGCATG ATGTATGAAT ACCTCCCATT CAAGTGCCCA (CTCGAG ATAACTTCG TATAATGTAT GCTATACGAA GTTAT ATGCATGGCC TCCGCGCCGG GTTTTGGCGC CTCCCGCGGG CGCCCCCCTC CTCACGGCGA GCGCTGCCAC GTCAGACGAA GGGCGCAGCG AGCGTCCTGA) (SEQ ID NO:16) (фигура 9B). См. также фигуру 3.
[00191] Нуклеотидная последовательность, охватывающая нижерасположенную точку вставки на 3'-конце самоудаляющейся кассеты устойчивости к неомицину, в которой указана последовательность кассеты (заключенная ниже в круглые скобки с выделенным жирным шрифтом сайтом loxP, выделенным подчеркиванием сайтом распознавания I-CeuI и выделенным курсивом сайтом распознавания NheI), смежная с мышиной геномной последовательностью Angptl8, содержит следующее: (TTTCACTGCAT TCTAGTTGTG GTTTGTCCAA ACTCATCAAT GTATCTTATC ATGTCTGGA ATAACTTCGTATAATGTATGCTATACGAAGTTAT GCTAGTAACTATAACGGTCCTAAGGTAGCGA GCTAGC) GATGCCACCGA GGACCAGTTGT GCTGCAAGGAA CACTGAAGCG CTCCACC (SEQ ID NO:17) (фигура 9C). См. также фигуру 3.
[00192] Нуклеотидная последовательность, охватывающая нижерасположенную точку вставки, после удаления кассеты устойчивости к неомицину (между 3'-концевой UTR человеческого ANGPTL8 и 3'-концевой UTR мышиного Angptl8 остаются 77 п.о.), в которой указаны человеческая и мышиная геномные последовательности, расположенные рядом с оставшейся последовательностью кассеты (заключенной ниже в круглые скобки с выделенными курсивом сайтами распознавания XhoI и NheI, выделенным жирным шрифтом сайтом loxP и выделенным подчеркиванием сайтом рестрикции I-CeuI), содержит следующее: GGGAGACCCC ACCCAGCATG ATGTATGAAT ACCTCCCATT CAAGTGCCCA (GTCGAG ATAACTTCGTATAATGTATGCTATACGAAGTTAT GCTAGTAACTATAACGGTCCTAAGGTAGCGA GCTAGC) GATGCCACCG AGGACCAGTT GTGCTGCAAG GAACACTGAA GCGCTCCACC (SEQ ID NO:18) (фигура 9D). См. также фигуру 3.
[00193] Положительные клоны ES-клеток затем использовали для имплантации самкам мышей с помощью способа VELOCIMOUSE® (см., например, патент США №7294754 и Poueymirou et al., 2007, Nature Biotech. 25(1):91-99) для создания выводка детенышей, содержащих вставку экзонов 1-4 человеческого ANGPTL8 (в том числе 3'-концевую UTR человеческого ANGPTL8 ) в эндогенном локусе Angptl8 мыши. Для мышей, содержащих экзоны 1-4 человеческого ANGPTL8 (т.е. синтетический фрагмент ДНК размером 2383 п.о.) на месте экзонов 1-4 эндогенного Angptl8, вновь проводили подтверждение и идентификацию путем генотипирования ДНК, выделенной из отрезанных фрагментов хвостов, с помощью ранее описанного анализа (Valenzuela et al., выше), выявившего наличие последовательностей человеческого ANGPTL8 (фигура 4). Детенышей генотипировали, и для получения характеристик отбирали когорты животных, гетерозиготных по последовательностям человеческого ANGPTL8.
Пример 2. Экспрессия человеческого ANGPTL8 у животных, отличных от человека
[00194] В данном примере демонстрируется, что животные, отличные от человека (например, грызуны), содержащие сконструированный ген Angptl8 согласно примеру 1, экспрессируют (или секретируют) человеческий (или гуманизированный) полипептид ANGPTL8, выявляемый в плазме крови животного, отличного от человека. В частности, как описано ниже, животные, отличные от человека, имеющие сконструированный ген Angptl8, демонстрируют повышенные уровни триглицеридов по сравнению с животными, отличными от человека, дикого типа (например, грызунами дикого типа), содержащими ген Angptl8 дикого типа.
[00195] Вкратце, у мышей дикого типа (n = 9) и мышей, гомозиготных по сконструированному гену Angptl8 (n = 8), в состоянии не натощак собирали венозную кровь из ретроорбитального сплетения в пробирки с EDTA. Плазму крови выделяли путем центрифугирования собранной крови при 4000 об./мин. в течение 10 минут. Плазму крови анализировали в отношении экспрессии человеческого ANGPTL8 с помощью ELISA-анализа с использованием антитела к ANGPLT8.
[00196] Данные демонстрировали, что человеческий ANGPTL8 секретировался в плазму крови мышей, гомозиготных по гуманизированному гену Angptl8. В частности, уровень экспрессии белка для человеческого ANGPTL8 в среднем составлял приблизительно 400 нг/мл у всех гуманизированных мышей, у которых была собрана кровь. Таким образом, грызуны, содержащие сконструированный ген Angptl8 согласно примеру 1, экспрессируют (и секретируют) человеческий ANGPTL8 в плазме крови на выявляемом уровне. В частности, такая экспрессия (или секреция) человеческого ANGPTL8 у этих животных находится под контролем регуляторных элементов Angptl8 грызуна (например, промотора Angptl8 грызуна).
[00197] В другом эксперименте плазму крови от мышей дикого типа и мышей, гомозиготных по сконструированному гену Angptl8 (описанному выше), собранную в состоянии не натощак, также использовали для определения уровней липидов в плазме крови.
[00198] Вкратце, уровни липидов в плазме крови (триглицеридов, общего холестерина, холестерина липопротеинов низкой плотности [LDL-C], холестерина липопротеинов высокой плотности [HDL-C]) измеряли с помощью биохимического анализатора сыворотки крови DVIA® 1800 (Siemens) согласно спецификации производителя. Типичные результаты приведены на фигуре 5.
[00199] Как показано на фигуре 5, грызуны, имеющие сконструированный ген Angptl8, описанный в данном документе, демонстрируют повышенные уровни триглицеридов по сравнению с грызунами дикого типа.
Пример 3. Тканевая экспрессия человеческого ANGPTL8 у животных, отличных от человека
[00200] В данном примере демонстрируется, что животные, отличные от человека (например, грызуны), содержащие сконструированный ген Angptl8 согласно примеру 1, экспрессируют (или секретируют) человеческий (или гуманизированный) полипептид ANGPTL8, выявляемый в различных тканях животного, отличного от человека. В частности, как описано ниже, животные, отличные от человека, имеющие сконструированный ген Angptl8, демонстрируют экспрессию человеческого ANGPTL8 в ткани печени и жировой ткани.
[00201] Вкратце, получение РНК и картирование ридов, полученных в ходе секвенирования РНК, выполняли согласно описанному ранее (Mastaitis, J. et al., 2015, Proc. Natl. Acad. Sci. U.S.A. 112(6):1845-9) с использованием тканей от мышей, гомозиготных по сконструированному гену Angptl8, описанных в примере 1, которые были собраны в условиях возобновленного кормления. Типичные результаты приведены на фигуре 6.
[00202] Как показано на фигуре 6, экспрессию человеческого ANGPTL8 идентифицировали в ткани печени и жировой ткани (например, в белой жировой ткани, подкожной жировой клетчатке и буром жире) мышей с гуманизированным Anptl8. В данном примере демонстрируется, что конструирование мышиного гена Angptl8, описанного в данном документе, в результате приводит к тканеспецифической экспрессии человеческого полипептида ANGPTL8 и, таким образом, обеспечивает животную модель in vivo для определения эффективности терапевтических средств, противодействующих ANGPTL8, в снижении уровней триглицеридов in vivo.
Пример 4. Эффективность модуляторов ANGPTL8in vivo
[00203] В данном примере демонстрируется, что животных, отличных от человека (например, грызуны), модифицированных таким образом, чтобы они содержали гуманизированный ген Angptl8 согласно примеру 1, можно использовать в анализе in vivo для скрининга модуляторов Angptl8 (например, антител к ANGPTL8) в отношении их эффективности снижения уровней триглицеридов. В данном примере типичные антитела к ANGPTL8 подвергают скринингу у мышей, гомозиготных по гуманизированному гену Angptl8, для определения эффективности терапии моноклональными антителами в снижении повышенных уровней триглицеридов.
[00204] Вкратце, мышей, гомозиготных по сконструированному гену Angptl8 (описанных выше), предварительно отбирали за 5 дней до проведения эксперимента и сортировали по группам обработки (n = 5 на группу обработки) на основании их уровней триглицеридов таким образом, чтобы средний уровень триглицеридов в целом по каждой группе был одинаковым. Антитела к ANGPTL8 или контроль (изотипически сходный контрольный человеческий IgG4 с несоответствующей специфичностью) вводили в дозе 10 мг/кг путем подкожной инъекции в день 0 исследования. У мышей производили забор крови через 4 дня после инъекции, и уровни триглицеридов в сыворотке крови определяли с помощью биохимического анализатора сыворотки крови ADVIA® 1800 (Siemens). Результаты выражали в виде среднего значения ± SEM для всех тестируемых антител в каждой группе. Типичные результаты приведены на фигуре 7.
[00205] Как показано на фигуре 7, терапия антителами к ANGPTL8 значительно снижала уровни циркулирующих в крови триглицеридов по сравнению с контрольным антителом. Кроме того, эти данные позволяют предположить, что мыши, содержащие сконструированный ген Angptl8, описанные в примере 1, экспрессируют человеческий ANGPTL8 и могут использоваться при скрининге терапевтических средств в отношении лечения повышенных уровней триглицеридов. В целом настоящее изобретение демонстрирует, что животные, отличные от человека, предусмотренные в данном документе, представляют систему in vivo для оценки эффективности антител к ANGPTL8 в снижении уровней триглицеридов и в некоторых вариантах осуществления обеспечивают животную модель гипертриглицеридемии in vivo.
ЭКВИВАЛЕНТЫ
[00206] При наличии описанных таким образом некоторых аспектов по меньшей мере одного варианта осуществления настоящего изобретения будет понятно, что различные изменения, модификации и улучшения без труда придут на ум специалистам в данной области техники. Подразумевается, что такие изменения, модификации и улучшения являются частью настоящего изобретения, и подразумевается, что они находятся в пределах сущности и объема настоящего изобретения. Соответственно, вышеприведенные описание и графические материалы представлены исключительно в качестве примера, и настоящее изобретение подробно описано в нижеследующей формуле изобретения.
[00207] Порядковые термины, такие как «первый», «второй», «третий» и т.д., используемые в формуле изобретения для модификации элемента формулы изобретения, сами по себе не означают какой-либо приоритет, предшествование или порядок расположения одного элемента формулы изобретения перед другим или временной порядок, в котором выполняются действия способа, но используются исключительно в качестве отметок для проведения различий между одним элементом формулы изобретения, имеющим определенное название, и другим элементом, имеющим такое же название (за исключением используемого порядкового термина), для проведения различий между элементами формулы изобретения.
[00208] Формы единственного числа, используемые в данном документе в описании и формуле изобретения, если четко не указано противоположное, следует понимать как охватывающие определяемые объекты в форме множественного числа. Признаки, раскрытые в пунктах формулы изобретения или частях описания, в которых содержится «или» между одним или более членами группы, считаются охваченными, если один, более одного или все члены группы присутствуют в указанном продукте или способе, используются в них или иным образом имеют отношение к ним, если не указано противоположное или иное не очевидно из контекста. Настоящее изобретение охватывает варианты осуществления, в которых только один член группы присутствует в указанном продукте или способе, используется в них или иным образом имеет отношение к ним. Настоящее изобретение также охватывает варианты осуществления, в которых более одного или все члены группы присутствуют в указанном продукте или способе, используются в них или иным образом имеют отношение к ним. Кроме того, следует понимать, что настоящее изобретение охватывает все варианты, комбинации и перестановки, в которых одно или более ограничений, элементов, условий, описательных терминов и т.д. из одного или более перечисленных пунктов формулы изобретения входят в другой пункт формулы изобретения, зависимый от того же основного пункта формулы изобретения (или, в зависимости от того, что применимо, любого другого пункта формулы изобретения), если не указано иное или если специалисту в данной области техники не будет очевидным возникновение противоречия или несоответствия. В тех случаях, когда элементы представлены в виде перечней (например, в виде группы Маркуша или в аналогичном формате), следует понимать, что также раскрыта каждая подгруппа элементов, и любой(любые) элемент(элементы) можно исключить из группы. Следует понимать, что, как правило, в тех случаях, когда настоящее изобретение или аспекты настоящего изобретения рассматриваются как включающие конкретные элементы, признаки и т.д., определенные варианты осуществления настоящего изобретения или аспектов настоящего изобретения состоят из таких элементов, признаков и т.д. или состоят главным образом из них. В целях простоты эти варианты осуществления не были в каждом случае специально недвусмысленно изложены в данном документе. Также следует понимать, что любой вариант осуществления или аспект настоящего изобретения может быть явным образом исключен из формулы изобретения независимо от упоминания конкретного исключения в описании.
[00209] Специалистам в данной области техники будут понятны типичные среднеквадратические отклонения или ошибки, присущие значениям, получаемым в анализах или других процессах, описанных в данном документе. Публикации, веб-сайты и другие справочные материалы, упоминаемые в данном документе для описания предпосылок настоящего изобретения и для предоставления дополнительных подробностей, относящихся к его практическому осуществлению, настоящим включены в данный документ посредством ссылки.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> РЕДЖЕНЕРОН ФАРМАСЬЮТИКАЛС, ИНК.
<120> ЖИВОТНЫЕ, ОТЛИЧНЫЕ ОТ ЧЕЛОВЕКА, ИМЕЮЩИЕ СКОНСТРУИРОВАННЫЙ ГЕН ANGPTL8
<130> 34634PCT (10232WO01)
<150> 62/291,446
<151> 2016-02-04
<160> 30
<170> PatentIn версии 3.5
<210> 1
<211> 878
<212> ДНК
<213> Rattus norvegicus
<400> 1
atacccccga gactgtccac catggttgtg cctattctct gcctcctatg ggccatagca 60
acagcagtgc gacctgcccc agtggcccct ctcggtggtc cagagccggc ccaatatgaa 120
gagttgaccc tgctctttca cggggcccta cagctaggtc aggccctcaa tggtgtgtac 180
aaagccacgg aagctcgcct gacagaagct gggcgcaacc tgggcctttt tgaccaagca 240
ctggaatttc tgggaagaga ggtcaatcag ggccgggatg caacacggga gcttcgcacc 300
agcttgtcgg agattcaggc agaagaggac actttacacc ttcgagcaga agccacagcc 360
cgatcgctga gggaagtggc ccgggcccag catgctctgc ggaacagtgt acggagacta 420
caagtgcagc tgagaggtgc ctggctaggc caagcccacc aagaatttga gaatttaaag 480
gatcgagccg ataagcagaa ccacctcttg tgggctctca ctggccacgt gcagcgacag 540
cagcgtgaga tggcagagca gcaacagtgg ctgcggcaga tccagcagag actccacatg 600
gcagccctcc cagcctgaga ctacctggat gccactgagg accagttgtg ctgcagggaa 660
cactgaatgc gctccaccgg gcctatctat gagcagggcc gacagagctg gctgcccatc 720
agctagactt ggccggtgca ccccgcttcc tggcagagca gagacagaag caagcaggcg 780
ggatggaagg cagaagacag ccccgtggag aaggctggag aaggacatga gctcccttat 840
gccccacacc ccacaataaa aaagaggcaa tctataaa 878
<210> 2
<211> 198
<212> БЕЛОК
<213> Rattus norvegicus
<400> 2
Met Val Val Pro Ile Leu Cys Leu Leu Trp Ala Ile Ala Thr Ala Val
1 5 10 15
Arg Pro Ala Pro Val Ala Pro Leu Gly Gly Pro Glu Pro Ala Gln Tyr
20 25 30
Glu Glu Leu Thr Leu Leu Phe His Gly Ala Leu Gln Leu Gly Gln Ala
35 40 45
Leu Asn Gly Val Tyr Lys Ala Thr Glu Ala Arg Leu Thr Glu Ala Gly
50 55 60
Arg Asn Leu Gly Leu Phe Asp Gln Ala Leu Glu Phe Leu Gly Arg Glu
65 70 75 80
Val Asn Gln Gly Arg Asp Ala Thr Arg Glu Leu Arg Thr Ser Leu Ser
85 90 95
Glu Ile Gln Ala Glu Glu Asp Thr Leu His Leu Arg Ala Glu Ala Thr
100 105 110
Ala Arg Ser Leu Arg Glu Val Ala Arg Ala Gln His Ala Leu Arg Asn
115 120 125
Ser Val Arg Arg Leu Gln Val Gln Leu Arg Gly Ala Trp Leu Gly Gln
130 135 140
Ala His Gln Glu Phe Glu Asn Leu Lys Asp Arg Ala Asp Lys Gln Asn
145 150 155 160
His Leu Leu Trp Ala Leu Thr Gly His Val Gln Arg Gln Gln Arg Glu
165 170 175
Met Ala Glu Gln Gln Gln Trp Leu Arg Gln Ile Gln Gln Arg Leu His
180 185 190
Met Ala Ala Leu Pro Ala
195
<210> 3
<211> 887
<212> ДНК
<213> Mus musculus
<400> 3
tgtcagccat ggctgtgctt gctctctgcc tcctgtggac cttagcatca gcagtgcgac 60
ccgctccagt ggcccctctg ggtggtccag agccagctca atatgaagag ctgaccctgc 120
tctttcacgg ggccctgcag ctaggccagg ccctcaatgg cgtgtacaga gccacagagg 180
ctcgcctgac agaagctggg cacagcctgg gcctctatga cagagcactg gaattcctgg 240
ggacagaagt caggcagggc caggatgcca cacaggagct tcgcaccagc ctgtcggaga 300
ttcaggtgga agaggacgct ttacaccttc gagctgaagc cacagcccga tcactggggg 360
aagtggcccg ggcccagcag gctctgcggg acactgtacg gagactacaa gtgcagctga 420
gaggcgcctg gctcggtcaa gcccaccaag aatttgagac cttaaaggct cgagctgata 480
agcagagcca cctcttatgg gctctcactg gccacgtgca gcgacagcag cgggagatgg 540
cagagcagca acagtggctg cgacagatcc agcagagact ccacacagca gccctcccag 600
cctgagacta cctggatgcc accgaggacc agttgtgctg caaggaacac tgaagcgctc 660
caccaggccc atgaacaggg ctgacagagc cggctgccca tcagctggac ctggccagtg 720
caccccgctt cctggcagag cggagacaga agcaagcagg cgggatggaa ggcagaagac 780
agagccctgt ggaggagggc tggaaaaaga cacgagcccc cttatgccca cacaccccac 840
aataaaagag aacagaggca atctaaaaaa aaaaaaaaaa aaaaaaa 887
<210> 4
<211> 198
<212> БЕЛОК
<213> Mus musculus
<400> 4
Met Ala Val Leu Ala Leu Cys Leu Leu Trp Thr Leu Ala Ser Ala Val
1 5 10 15
Arg Pro Ala Pro Val Ala Pro Leu Gly Gly Pro Glu Pro Ala Gln Tyr
20 25 30
Glu Glu Leu Thr Leu Leu Phe His Gly Ala Leu Gln Leu Gly Gln Ala
35 40 45
Leu Asn Gly Val Tyr Arg Ala Thr Glu Ala Arg Leu Thr Glu Ala Gly
50 55 60
His Ser Leu Gly Leu Tyr Asp Arg Ala Leu Glu Phe Leu Gly Thr Glu
65 70 75 80
Val Arg Gln Gly Gln Asp Ala Thr Gln Glu Leu Arg Thr Ser Leu Ser
85 90 95
Glu Ile Gln Val Glu Glu Asp Ala Leu His Leu Arg Ala Glu Ala Thr
100 105 110
Ala Arg Ser Leu Gly Glu Val Ala Arg Ala Gln Gln Ala Leu Arg Asp
115 120 125
Thr Val Arg Arg Leu Gln Val Gln Leu Arg Gly Ala Trp Leu Gly Gln
130 135 140
Ala His Gln Glu Phe Glu Thr Leu Lys Ala Arg Ala Asp Lys Gln Ser
145 150 155 160
His Leu Leu Trp Ala Leu Thr Gly His Val Gln Arg Gln Gln Arg Glu
165 170 175
Met Ala Glu Gln Gln Gln Trp Leu Arg Gln Ile Gln Gln Arg Leu His
180 185 190
Thr Ala Ala Leu Pro Ala
195
<210> 5
<211> 888
<212> ДНК
<213> Homo sapiens
<400> 5
ataccttaga ccctcagtca tgccagtgcc tgctctgtgc ctgctctggg ccctggcaat 60
ggtgacccgg cctgcctcag cggcccccat gggcggccca gaactggcac agcatgagga 120
gctgaccctg ctcttccatg ggaccctgca gctgggccag gccctcaacg gtgtgtacag 180
gaccacggag ggacggctga caaaggccag gaacagcctg ggtctctatg gccgcacaat 240
agaactcctg gggcaggagg tcagccgggg ccgggatgca gcccaggaac ttcgggcaag 300
cctgttggag actcagatgg aggaggatat tctgcagctg caggcagagg ccacagctga 360
ggtgctgggg gaggtggccc aggcacagaa ggtgctacgg gacagcgtgc agcggctaga 420
agtccagctg aggagcgcct ggctgggccc tgcctaccga gaatttgagg tcttaaaggc 480
tcacgctgac aagcagagcc acatcctatg ggccctcaca ggccacgtgc agcggcagag 540
gcgggagatg gtggcacagc agcatcggct gcgacagatc caggagagac tccacacagc 600
ggcgctccca gcctgaatct gcctggatgg aactgaggac caatcatgct gcaaggaaca 660
cttccacgcc ccgtgaggcc cctgtgcagg gaggagctgc ctgttcactg ggatcagcca 720
gggcgccggg ccccacttct gagcacagag cagagacaga cgcaggcggg gacaaaggca 780
gaggatgtag ccccattggg gaggggtgga ggaaggacat gtaccctttc atgcctacac 840
acccctcatt aaagcagagt cgtggcatct caaaaaaaaa aaaaaaaa 888
<210> 6
<211> 198
<212> БЕЛОК
<213> Homo sapiens
<400> 6
Met Pro Val Pro Ala Leu Cys Leu Leu Trp Ala Leu Ala Met Val Thr
1 5 10 15
Arg Pro Ala Ser Ala Ala Pro Met Gly Gly Pro Glu Leu Ala Gln His
20 25 30
Glu Glu Leu Thr Leu Leu Phe His Gly Thr Leu Gln Leu Gly Gln Ala
35 40 45
Leu Asn Gly Val Tyr Arg Thr Thr Glu Gly Arg Leu Thr Lys Ala Arg
50 55 60
Asn Ser Leu Gly Leu Tyr Gly Arg Thr Ile Glu Leu Leu Gly Gln Glu
65 70 75 80
Val Ser Arg Gly Arg Asp Ala Ala Gln Glu Leu Arg Ala Ser Leu Leu
85 90 95
Glu Thr Gln Met Glu Glu Asp Ile Leu Gln Leu Gln Ala Glu Ala Thr
100 105 110
Ala Glu Val Leu Gly Glu Val Ala Gln Ala Gln Lys Val Leu Arg Asp
115 120 125
Ser Val Gln Arg Leu Glu Val Gln Leu Arg Ser Ala Trp Leu Gly Pro
130 135 140
Ala Tyr Arg Glu Phe Glu Val Leu Lys Ala His Ala Asp Lys Gln Ser
145 150 155 160
His Ile Leu Trp Ala Leu Thr Gly His Val Gln Arg Gln Arg Arg Glu
165 170 175
Met Val Ala Gln Gln His Arg Leu Arg Gln Ile Gln Glu Arg Leu His
180 185 190
Thr Ala Ala Leu Pro Ala
195
<210> 7
<211> 877
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Иллюстративный сконструированный полинуклеотид Angpt18
<400> 7
tgtcagccat gccagtgcct gctctgtgcc tgctctgggc cctggcaatg gtgacccggc 60
ctgcctcagc ggcccccatg ggcggcccag aactggcaca gcatgaggag ctgaccctgc 120
tcttccatgg gaccctgcag ctgggccagg ccctcaacgg tgtgtacagg accacggagg 180
gacggctgac aaaggccagg aacagcctgg gtctctatgg ccgcacaata gaactcctgg 240
ggcaggaggt cagccggggc cgggatgcag cccaggaact tcgggcaagc ctgttggaga 300
ctcagatgga ggaggatatt ctgcagctgc aggcagaggc cacagctgag gtgctggggg 360
aggtggccca ggcacagaag gtgctacggg acagcgtgca gcggctagaa gtccagctga 420
ggagcgcctg gctgggccct gcctaccgag aatttgaggt cttaaaggct cacgctgaca 480
agcagagcca catcctatgg gccctcacag gccacgtgca gcggcagagg cgggagatgg 540
tggcacagca gcatcggctg cgacagatcc aggagagact ccacacagcg gcgctcccag 600
cctgaatctg cctggatgga actgaggacc aatcatgctg caaggaacac ttccacgccc 660
cgtgaggccc ctgtgcaggg aggagctgcc tgttcactgg gatcagccag ggcgccgggc 720
cccacttctg agcacagagc agagacagac gcaggcgggg acaaaggcag aggatgtagc 780
cccattgggg aggggtggag gaaggacatg taccctttca tgcctacaca cccctcatta 840
aagcagagtc gtggcatctc aaaaaaaaaa aaaaaaa 877
<210> 8
<211> 198
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Иллюстративный сконструированный полипептид Angpt18
<400> 8
Met Pro Val Pro Ala Leu Cys Leu Leu Trp Ala Leu Ala Met Val Thr
1 5 10 15
Arg Pro Ala Ser Ala Ala Pro Met Gly Gly Pro Glu Leu Ala Gln His
20 25 30
Glu Glu Leu Thr Leu Leu Phe His Gly Thr Leu Gln Leu Gly Gln Ala
35 40 45
Leu Asn Gly Val Tyr Arg Thr Thr Glu Gly Arg Leu Thr Lys Ala Arg
50 55 60
Asn Ser Leu Gly Leu Tyr Gly Arg Thr Ile Glu Leu Leu Gly Gln Glu
65 70 75 80
Val Ser Arg Gly Arg Asp Ala Ala Gln Glu Leu Arg Ala Ser Leu Leu
85 90 95
Glu Thr Gln Met Glu Glu Asp Ile Leu Gln Leu Gln Ala Glu Ala Thr
100 105 110
Ala Glu Val Leu Gly Glu Val Ala Gln Ala Gln Lys Val Leu Arg Asp
115 120 125
Ser Val Gln Arg Leu Glu Val Gln Leu Arg Ser Ala Trp Leu Gly Pro
130 135 140
Ala Tyr Arg Glu Phe Glu Val Leu Lys Ala His Ala Asp Lys Gln Ser
145 150 155 160
His Ile Leu Trp Ala Leu Thr Gly His Val Gln Arg Gln Arg Arg Glu
165 170 175
Met Val Ala Gln Gln His Arg Leu Arg Gln Ile Gln Glu Arg Leu His
180 185 190
Thr Ala Ala Leu Pro Ala
195
<210> 9
<211> 2383
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Иллюстративный синтетический фрагмент ДНК для конструирования гена
Angpt18, отличного от человеческого
<400> 9
ccagtgcctg ctctgtgcct gctctgggcc ctggcaatgg tgacccggcc tgcctcagcg 60
gcccccatgg gcggcccaga actggcacag catgaggagc tgaccctgct cttccatggg 120
accctgcagc tgggccaggc cctcaacggt gtgtacagga ccacggaggg acggctgaca 180
aaggccagga acagcctggg tctctatggc cgcacaatag aactcctggg gcaggaggtc 240
agccggggcc gggatgcagc ccaggaactt cgggcaagcc tgttggagac tcaggtgggc 300
accgtagctg cgacactgtg gggtggccag gagtccaaag aggagttcgt gtctagggta 360
accaaccatc ctggtttgcc caggactgaa gggattcctg ggatacaaga ttttcagcga 420
taaactcagg caagtcctta ggtacacaaa gatgagttgg acatcctact agtgacccac 480
tgtttattaa gcagatggag gaggatattc tgcagctgca ggcagaggcc acagctgagg 540
tgctggggga ggtggcccag gcacagaagg tgctacggga cagcgtgcag cggctagaag 600
tccagctgag gagcgcctgg ctgggccctg cctaccgaga atttgaggtc ttaaaggtaa 660
ggagctcccc caaccctagt gggctgagac cctgatttcc ggccagaact cgcttctgca 720
ccttgagtcc caaagacctc ccagatcagc ctcccagctc tgtggcctct accctgcatg 780
tccccagaca aaactcaagt ccttttgtgt gcctcagttt cccttttgtg tgcctcagtt 840
gcaaataagg gcaacacctg atatctcaca gtagggccag gtactcaatg caggtaaaat 900
attcagcatg gggcgggcac acagttggtg ctcaataaat tctttttttt tttttttttg 960
agacagagtc tcactgttgc ccaggctgga gtgcagtggt gtgatcttgg ctcactgcaa 1020
cctccacctc ctaggttcaa gtgattctcc tgcctcagcc tcctgagtag ctggaattac 1080
aggtgcacca gctaattttt gtatttttta gtagagatgg gatttcacca tgttggccag 1140
gctggtctcg aactcctgac ctcaagggat ctgcctgcct cggtttccca aagtgctggg 1200
attacaggtg tgagccacta cacctggcca ataaattctt actactagag aaactggtaa 1260
cattttgtga gcacccagta agtacccagc actgttctat gccctttaat aatccatatg 1320
atggccgggc atggtggctc atgcctgtaa tcccagcact ttgggtagct aaggtgggtg 1380
gaacacttaa ggtcaggagt tcgagaccac cctggccaac atggtgaaac cccgtctcta 1440
ctaaaaatac aaaaaattag ctgggcgtgg tggcacatgc ctgtagtccc agctactcag 1500
gaggcttagg taggagaatc gcttgaacct gggaggtgga ggttgcagtg agctgagatc 1560
gtgtcattgc actcagcctg ggtgacagag agagactcaa aaaaaaaaaa aaatccatag 1620
gatgttcatc acctccccat gaagtgagtc ctattttatc cccattttac agatggggaa 1680
actgaggcca aagagcattg ttgacttgct gggtcacaca gatacaatga ggggctgggg 1740
cagagggtca ggggatggga ggtgaggtgg ctgtcggctg aggtttccat tctgaccccc 1800
acaggctcac gctgacaagc agagccacat cctatgggcc ctcacaggcc acgtgcagcg 1860
gcagaggcgg gagatggtgg cacagcagca tcggctgcga cagatccagg agaggtgagc 1920
ctggcagggg tttggcaggc agggcagttg gatggggggc gcacagggca gctggaaagg 1980
ggccccctca cctgggctga gccacatctc cctccccaga ctccacacag cggcgctccc 2040
agcctgaatc tgcctggatg gaactgagga ccaatcatgc tgcaaggaac acttccacgc 2100
cccgtgaggc ccctgtgcag ggaggagctg cctgttcact gggatcagcc agggcgccgg 2160
gccccacttc tgagcacaga gcagagacag acgcaggcgg ggacaaaggc agaggatgta 2220
gccccattgg ggaggggtgg aggaaggaca tgtacccttt catgcctaca cacccctcat 2280
taaagcagag tcgtggcatc tcacccaggg tgtctgtgtg tgtccttggc ttagggagac 2340
cccacccagc atgatgtatg aatacctccc attcaagtgc cca 2383
<210> 10
<211> 7473
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Иллюстративный сконстурированный аллель Angptl8,содержащий селекционную
кассету
<400> 10
cacgaaactg tcagccatgc cagtgcctgc tctgtgcctg ctctgggccc tggcaatggt 60
gacccggcct gcctcagcgg cccccatggg cggcccagaa ctggcacagc atgaggagct 120
gaccctgctc ttccatggga ccctgcagct gggccaggcc ctcaacggtg tgtacaggac 180
cacggaggga cggctgacaa aggccaggaa cagcctgggt ctctatggcc gcacaataga 240
actcctgggg caggaggtca gccggggccg ggatgcagcc caggaacttc gggcaagcct 300
gttggagact caggtgggca ccgtagctgc gacactgtgg ggtggccagg agtccaaaga 360
ggagttcgtg tctagggtaa ccaaccatcc tggtttgccc aggactgaag ggattcctgg 420
gatacaagat tttcagcgat aaactcaggc aagtccttag gtacacaaag atgagttgga 480
catcctacta gtgacccact gtttattaag cagatggagg aggatattct gcagctgcag 540
gcagaggcca cagctgaggt gctgggggag gtggcccagg cacagaaggt gctacgggac 600
agcgtgcagc ggctagaagt ccagctgagg agcgcctggc tgggccctgc ctaccgagaa 660
tttgaggtct taaaggtaag gagctccccc aaccctagtg ggctgagacc ctgatttccg 720
gccagaactc gcttctgcac cttgagtccc aaagacctcc cagatcagcc tcccagctct 780
gtggcctcta ccctgcatgt ccccagacaa aactcaagtc cttttgtgtg cctcagtttc 840
ccttttgtgt gcctcagttg caaataaggg caacacctga tatctcacag tagggccagg 900
tactcaatgc aggtaaaata ttcagcatgg ggcgggcaca cagttggtgc tcaataaatt 960
cttttttttt ttttttttga gacagagtct cactgttgcc caggctggag tgcagtggtg 1020
tgatcttggc tcactgcaac ctccacctcc taggttcaag tgattctcct gcctcagcct 1080
cctgagtagc tggaattaca ggtgcaccag ctaatttttg tattttttag tagagatggg 1140
atttcaccat gttggccagg ctggtctcga actcctgacc tcaagggatc tgcctgcctc 1200
ggtttcccaa agtgctggga ttacaggtgt gagccactac acctggccaa taaattctta 1260
ctactagaga aactggtaac attttgtgag cacccagtaa gtacccagca ctgttctatg 1320
ccctttaata atccatatga tggccgggca tggtggctca tgcctgtaat cccagcactt 1380
tgggtagcta aggtgggtgg aacacttaag gtcaggagtt cgagaccacc ctggccaaca 1440
tggtgaaacc ccgtctctac taaaaataca aaaaattagc tgggcgtggt ggcacatgcc 1500
tgtagtccca gctactcagg aggcttaggt aggagaatcg cttgaacctg ggaggtggag 1560
gttgcagtga gctgagatcg tgtcattgca ctcagcctgg gtgacagaga gagactcaaa 1620
aaaaaaaaaa aatccatagg atgttcatca cctccccatg aagtgagtcc tattttatcc 1680
ccattttaca gatggggaaa ctgaggccaa agagcattgt tgacttgctg ggtcacacag 1740
atacaatgag gggctggggc agagggtcag gggatgggag gtgaggtggc tgtcggctga 1800
ggtttccatt ctgaccccca caggctcacg ctgacaagca gagccacatc ctatgggccc 1860
tcacaggcca cgtgcagcgg cagaggcggg agatggtggc acagcagcat cggctgcgac 1920
agatccagga gaggtgagcc tggcaggggt ttggcaggca gggcagttgg atggggggcg 1980
cacagggcag ctggaaaggg gccccctcac ctgggctgag ccacatctcc ctccccagac 2040
tccacacagc ggcgctccca gcctgaatct gcctggatgg aactgaggac caatcatgct 2100
gcaaggaaca cttccacgcc ccgtgaggcc cctgtgcagg gaggagctgc ctgttcactg 2160
ggatcagcca gggcgccggg ccccacttct gagcacagag cagagacaga cgcaggcggg 2220
gacaaaggca gaggatgtag ccccattggg gaggggtgga ggaaggacat gtaccctttc 2280
atgcctacac acccctcatt aaagcagagt cgtggcatct cacccagggt gtctgtgtgt 2340
gtccttggct tagggagacc ccacccagca tgatgtatga atacctccca ttcaagtgcc 2400
cactcgagat aacttcgtat aatgtatgct atacgaagtt atatgcatgg cctccgcgcc 2460
gggttttggc gcctcccgcg ggcgcccccc tcctcacggc gagcgctgcc acgtcagacg 2520
aagggcgcag cgagcgtcct gatccttccg cccggacgct caggacagcg gcccgctgct 2580
cataagactc ggccttagaa ccccagtatc agcagaagga cattttagga cgggacttgg 2640
gtgactctag ggcactggtt ttctttccag agagcggaac aggcgaggaa aagtagtccc 2700
ttctcggcga ttctgcggag ggatctccgt ggggcggtga acgccgatga ttatataagg 2760
acgcgccggg tgtggcacag ctagttccgt cgcagccggg atttgggtcg cggttcttgt 2820
ttgtggatcg ctgtgatcgt cacttggtga gtagcgggct gctgggctgg ccggggcttt 2880
cgtggccgcc gggccgctcg gtgggacgga agcgtgtgga gagaccgcca agggctgtag 2940
tctgggtccg cgagcaaggt tgccctgaac tgggggttgg ggggagcgca gcaaaatggc 3000
ggctgttccc gagtcttgaa tggaagacgc ttgtgaggcg ggctgtgagg tcgttgaaac 3060
aaggtggggg gcatggtggg cggcaagaac ccaaggtctt gaggccttcg ctaatgcggg 3120
aaagctctta ttcgggtgag atgggctggg gcaccatctg gggaccctga cgtgaagttt 3180
gtcactgact ggagaactcg gtttgtcgtc tgttgcgggg gcggcagtta tggcggtgcc 3240
gttgggcagt gcacccgtac ctttgggagc gcgcgccctc gtcgtgtcgt gacgtcaccc 3300
gttctgttgg cttataatgc agggtggggc cacctgccgg taggtgtgcg gtaggctttt 3360
ctccgtcgca ggacgcaggg ttcgggccta gggtaggctc tcctgaatcg acaggcgccg 3420
gacctctggt gaggggaggg ataagtgagg cgtcagtttc tttggtcggt tttatgtacc 3480
tatcttctta agtagctgaa gctccggttt tgaactatgc gctcggggtt ggcgagtgtg 3540
ttttgtgaag ttttttaggc accttttgaa atgtaatcat ttgggtcaat atgtaatttt 3600
cagtgttaga ctagtaaatt gtccgctaaa ttctggccgt ttttggcttt tttgttagac 3660
gtgttgacaa ttaatcatcg gcatagtata tcggcatagt ataatacgac aaggtgagga 3720
actaaaccat gggatcggcc attgaacaag atggattgca cgcaggttct ccggccgctt 3780
gggtggagag gctattcggc tatgactggg cacaacagac aatcggctgc tctgatgccg 3840
ccgtgttccg gctgtcagcg caggggcgcc cggttctttt tgtcaagacc gacctgtccg 3900
gtgccctgaa tgaactgcag gacgaggcag cgcggctatc gtggctggcc acgacgggcg 3960
ttccttgcgc agctgtgctc gacgttgtca ctgaagcggg aagggactgg ctgctattgg 4020
gcgaagtgcc ggggcaggat ctcctgtcat ctcaccttgc tcctgccgag aaagtatcca 4080
tcatggctga tgcaatgcgg cggctgcata cgcttgatcc ggctacctgc ccattcgacc 4140
accaagcgaa acatcgcatc gagcgagcac gtactcggat ggaagccggt cttgtcgatc 4200
aggatgatct ggacgaagag catcaggggc tcgcgccagc cgaactgttc gccaggctca 4260
aggcgcgcat gcccgacggc gatgatctcg tcgtgaccca tggcgatgcc tgcttgccga 4320
atatcatggt ggaaaatggc cgcttttctg gattcatcga ctgtggccgg ctgggtgtgg 4380
cggaccgcta tcaggacata gcgttggcta cccgtgatat tgctgaagag cttggcggcg 4440
aatgggctga ccgcttcctc gtgctttacg gtatcgccgc tcccgattcg cagcgcatcg 4500
ccttctatcg ccttcttgac gagttcttct gaggggatcc gctgtaagtc tgcagaaatt 4560
gatgatctat taaacaataa agatgtccac taaaatggaa gtttttcctg tcatactttg 4620
ttaagaaggg tgagaacaga gtacctacat tttgaatgga aggattggag ctacgggggt 4680
gggggtgggg tgggattaga taaatgcctg ctctttactg aaggctcttt actattgctt 4740
tatgataatg tttcatagtt ggatatcata atttaaacaa gcaaaaccaa attaagggcc 4800
agctcattcc tcccactcat gatctataga tctatagatc tctcgtggga tcattgtttt 4860
tctcttgatt cccactttgt ggttctaagt actgtggttt ccaaatgtgt cagtttcata 4920
gcctgaagaa cgagatcagc agcctctgtt ccacatacac ttcattctca gtattgtttt 4980
gccaagttct aattccatca gacctcgacc tgcagcccct agcccgggcg ccagtagcag 5040
cacccacgtc caccttctgt ctagtaatgt ccaacacctc cctcagtcca aacactgctc 5100
tgcatccatg tggctcccat ttatacctga agcacttgat ggggcctcaa tgttttacta 5160
gagcccaccc ccctgcaact ctgagaccct ctggatttgt ctgtcagtgc ctcactgggg 5220
cgttggataa tttcttaaaa ggtcaagttc cctcagcagc attctctgag cagtctgaag 5280
atgtgtgctt ttcacagttc aaatccatgt ggctgtttca cccacctgcc tggccttggg 5340
ttatctatca ggacctagcc tagaagcagg tgtgtggcac ttaacaccta agctgagtga 5400
ctaactgaac actcaagtgg atgccatctt tgtcacttct tgactgtgac acaagcaact 5460
cctgatgcca aagccctgcc cacccctctc atgcccatat ttggacatgg tacaggtcct 5520
cactggccat ggtctgtgag gtcctggtcc tctttgactt cataattcct aggggccact 5580
agtatctata agaggaagag ggtgctggct cccaggccac agcccacaaa attccacctg 5640
ctcacaggtt ggctggctcg acccaggtgg tgtcccctgc tctgagccag ctcccggcca 5700
agccagcacc atgggtaccc ccaagaagaa gaggaaggtg cgtaccgatt taaattccaa 5760
tttactgacc gtacaccaaa atttgcctgc attaccggtc gatgcaacga gtgatgaggt 5820
tcgcaagaac ctgatggaca tgttcaggga tcgccaggcg ttttctgagc atacctggaa 5880
aatgcttctg tccgtttgcc ggtcgtgggc ggcatggtgc aagttgaata accggaaatg 5940
gtttcccgca gaacctgaag atgttcgcga ttatcttcta tatcttcagg cgcgcggtct 6000
ggcagtaaaa actatccagc aacatttggg ccagctaaac atgcttcatc gtcggtccgg 6060
gctgccacga ccaagtgaca gcaatgctgt ttcactggtt atgcggcgga tccgaaaaga 6120
aaacgttgat gccggtgaac gtgcaaaaca ggctctagcg ttcgaacgca ctgatttcga 6180
ccaggttcgt tcactcatgg aaaatagtga tcgctgccag gatatacgta atctggcatt 6240
tctggggatt gcttataaca ccctgttacg tatagccgaa attgccagga tcagggttaa 6300
agatatctca cgtactgacg gtgggagaat gttaatccat attggcagaa cgaaaacgct 6360
ggttagcacc gcaggtgtag agaaggcact tagcctgggg gtaactaaac tggtcgagcg 6420
atggatttcc gtctctggtg tagctgatga tccgaataac tacctgtttt gccgggtcag 6480
aaaaaatggt gttgccgcgc catctgccac cagccagcta tcaactcgcg ccctggaagg 6540
gatttttgaa gcaactcatc gattgattta cggcgctaag gtaaatataa aatttttaag 6600
tgtataatgt gttaaactac tgattctaat tgtttgtgta ttttaggatg actctggtca 6660
gagatacctg gcctggtctg gacacagtgc ccgtgtcgga gccgcgcgag atatggcccg 6720
cgctggagtt tcaataccgg agatcatgca agctggtggc tggaccaatg taaatattgt 6780
catgaactat atccgtaacc tggatagtga aacaggggca atggtgcgcc tgctggaaga 6840
tggcgattga tctagataag taatgatcat aatcagccat atcacatctg tagaggtttt 6900
acttgcttta aaaaacctcc cacacctccc cctgaacctg aaacataaaa tgaatgcaat 6960
tgttgttgtt aaacctgccc tagttgcggc caattccagc tgagcgtgcc tccgcaccat 7020
taccagttgg tctggtgtca aaaataataa taaccgggca ggggggatct aagctctaga 7080
taagtaatga tcataatcag ccatatcaca tctgtagagg ttttacttgc tttaaaaaac 7140
ctcccacacc tccccctgaa cctgaaacat aaaatgaatg caattgttgt tgttaacttg 7200
tttattgcag cttataatgg ttacaaataa agcaatagca tcacaaattt cacaaataaa 7260
gcattttttt cactgcattc tagttgtggt ttgtccaaac tcatcaatgt atcttatcat 7320
gtctggaata acttcgtata atgtatgcta tacgaagtta tgctagtaac tataacggtc 7380
ctaaggtagc gagctagcga tgccaccgag gaccagttgt gctgcaagga acactgaagc 7440
gctccaccag gcccatgaac agggctgaca gag 7473
<210> 11
<211> 2554
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Иллюстративный сконстурированный аллель Angptl8 после опосредованного рекомбиназой
удаления селекционной кассеты
<400> 11
cacgaaactg tcagccatgc cagtgcctgc tctgtgcctg ctctgggccc tggcaatggt 60
gacccggcct gcctcagcgg cccccatggg cggcccagaa ctggcacagc atgaggagct 120
gaccctgctc ttccatggga ccctgcagct gggccaggcc ctcaacggtg tgtacaggac 180
cacggaggga cggctgacaa aggccaggaa cagcctgggt ctctatggcc gcacaataga 240
actcctgggg caggaggtca gccggggccg ggatgcagcc caggaacttc gggcaagcct 300
gttggagact caggtgggca ccgtagctgc gacactgtgg ggtggccagg agtccaaaga 360
ggagttcgtg tctagggtaa ccaaccatcc tggtttgccc aggactgaag ggattcctgg 420
gatacaagat tttcagcgat aaactcaggc aagtccttag gtacacaaag atgagttgga 480
catcctacta gtgacccact gtttattaag cagatggagg aggatattct gcagctgcag 540
gcagaggcca cagctgaggt gctgggggag gtggcccagg cacagaaggt gctacgggac 600
agcgtgcagc ggctagaagt ccagctgagg agcgcctggc tgggccctgc ctaccgagaa 660
tttgaggtct taaaggtaag gagctccccc aaccctagtg ggctgagacc ctgatttccg 720
gccagaactc gcttctgcac cttgagtccc aaagacctcc cagatcagcc tcccagctct 780
gtggcctcta ccctgcatgt ccccagacaa aactcaagtc cttttgtgtg cctcagtttc 840
ccttttgtgt gcctcagttg caaataaggg caacacctga tatctcacag tagggccagg 900
tactcaatgc aggtaaaata ttcagcatgg ggcgggcaca cagttggtgc tcaataaatt 960
cttttttttt ttttttttga gacagagtct cactgttgcc caggctggag tgcagtggtg 1020
tgatcttggc tcactgcaac ctccacctcc taggttcaag tgattctcct gcctcagcct 1080
cctgagtagc tggaattaca ggtgcaccag ctaatttttg tattttttag tagagatggg 1140
atttcaccat gttggccagg ctggtctcga actcctgacc tcaagggatc tgcctgcctc 1200
ggtttcccaa agtgctggga ttacaggtgt gagccactac acctggccaa taaattctta 1260
ctactagaga aactggtaac attttgtgag cacccagtaa gtacccagca ctgttctatg 1320
ccctttaata atccatatga tggccgggca tggtggctca tgcctgtaat cccagcactt 1380
tgggtagcta aggtgggtgg aacacttaag gtcaggagtt cgagaccacc ctggccaaca 1440
tggtgaaacc ccgtctctac taaaaataca aaaaattagc tgggcgtggt ggcacatgcc 1500
tgtagtccca gctactcagg aggcttaggt aggagaatcg cttgaacctg ggaggtggag 1560
gttgcagtga gctgagatcg tgtcattgca ctcagcctgg gtgacagaga gagactcaaa 1620
aaaaaaaaaa aatccatagg atgttcatca cctccccatg aagtgagtcc tattttatcc 1680
ccattttaca gatggggaaa ctgaggccaa agagcattgt tgacttgctg ggtcacacag 1740
atacaatgag gggctggggc agagggtcag gggatgggag gtgaggtggc tgtcggctga 1800
ggtttccatt ctgaccccca caggctcacg ctgacaagca gagccacatc ctatgggccc 1860
tcacaggcca cgtgcagcgg cagaggcggg agatggtggc acagcagcat cggctgcgac 1920
agatccagga gaggtgagcc tggcaggggt ttggcaggca gggcagttgg atggggggcg 1980
cacagggcag ctggaaaggg gccccctcac ctgggctgag ccacatctcc ctccccagac 2040
tccacacagc ggcgctccca gcctgaatct gcctggatgg aactgaggac caatcatgct 2100
gcaaggaaca cttccacgcc ccgtgaggcc cctgtgcagg gaggagctgc ctgttcactg 2160
ggatcagcca gggcgccggg ccccacttct gagcacagag cagagacaga cgcaggcggg 2220
gacaaaggca gaggatgtag ccccattggg gaggggtgga ggaaggacat gtaccctttc 2280
atgcctacac acccctcatt aaagcagagt cgtggcatct cacccagggt gtctgtgtgt 2340
gtccttggct tagggagacc ccacccagca tgatgtatga atacctccca ttcaagtgcc 2400
cactcgagat aacttcgtat aatgtatgct atacgaagtt atgctagtaa ctataacggt 2460
cctaaggtag cgagctagcg atgccaccga ggaccagttg tgctgcaagg aacactgaag 2520
cgctccacca ggcccatgaa cagggctgac agag 2554
<210> 12
<211> 680
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Промотор гена протамина 1 (Prm1)
<400> 12
ccagtagcag cacccacgtc caccttctgt ctagtaatgt ccaacacctc cctcagtcca 60
aacactgctc tgcatccatg tggctcccat ttatacctga agcacttgat ggggcctcaa 120
tgttttacta gagcccaccc ccctgcaact ctgagaccct ctggatttgt ctgtcagtgc 180
ctcactgggg cgttggataa tttcttaaaa ggtcaagttc cctcagcagc attctctgag 240
cagtctgaag atgtgtgctt ttcacagttc aaatccatgt ggctgtttca cccacctgcc 300
tggccttggg ttatctatca ggacctagcc tagaagcagg tgtgtggcac ttaacaccta 360
agctgagtga ctaactgaac actcaagtgg atgccatctt tgtcacttct tgactgtgac 420
acaagcaact cctgatgcca aagccctgcc cacccctctc atgcccatat ttggacatgg 480
tacaggtcct cactggccat ggtctgtgag gtcctggtcc tctttgactt cataattcct 540
aggggccact agtatctata agaggaagag ggtgctggct cccaggccac agcccacaaa 600
attccacctg ctcacaggtt ggctggctcg acccaggtgg tgtcccctgc tctgagccag 660
ctcccggcca agccagcacc 680
<210> 13
<211> 1052
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Промотор Blimp1 размером 1 т. о.
<400> 13
tgccatcatc acaggatgtc cttccttctc cagaagacag actggggctg aaggaaaagc 60
cggccaggct cagaacgagc cccactaatt actgcctcca acagctttcc actcactgcc 120
cccagcccaa catccccttt ttaactggga agcattccta ctctccattg tacgcacacg 180
ctcggaagcc tggctgtggg tttgggcatg agaggcaggg acaacaaaac cagtatatat 240
gattataact ttttcctgtt tccctatttc caaatggtcg aaaggaggaa gttaggtcta 300
cctaagctga atgtattcag ttagcaggag aaatgaaatc ctatacgttt aatactagag 360
gagaaccgcc ttagaatatt tatttcattg gcaatgactc caggactaca cagcgaaatt 420
gtattgcatg tgctgccaaa atactttagc tctttccttc gaagtacgtc ggatcctgta 480
attgagacac cgagtttagg tgactagggt tttcttttga ggaggagtcc cccaccccgc 540
cccgctctgc cgcgacagga agctagcgat ccggaggact tagaatacaa tcgtagtgtg 600
ggtaaacatg gagggcaagc gcctgcaaag ggaagtaaga agattcccag tccttgttga 660
aatccatttg caaacagagg aagctgccgc gggtcgcagt cggtgggggg aagccctgaa 720
ccccacgctg cacggctggg ctggccaggt gcggccacgc ccccatcgcg gcggctggta 780
ggagtgaatc agaccgtcag tattggtaaa gaagtctgcg gcagggcagg gagggggaag 840
agtagtcagt cgctcgctca ctcgctcgct cgcacagaca ctgctgcagt gacactcggc 900
cctccagtgt cgcggagacg caagagcagc gcgcagcacc tgtccgcccg gagcgagccc 960
ggcccgcggc cgtagaaaag gagggaccgc cgaggtgcgc gtcagtactg ctcagcccgg 1020
cagggacgcg ggaggatgtg gactgggtgg ac 1052
<210> 14
<211> 2008
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Промотор Blimp1 размером 2 т. о.
<400> 14
gtggtgctga ctcagcatcg gttaataaac cctctgcagg aggctggatt tcttttgttt 60
aattatcact tggacctttc tgagaactct taagaattgt tcattcgggt ttttttgttt 120
tgttttggtt tggttttttt gggttttttt tttttttttt tttttggttt ttggagacag 180
ggtttctctg tatatagccc tggcacaaga gcaagctaac agcctgtttc ttcttggtgc 240
tagcgccccc tctggcagaa aatgaaataa caggtggacc tacaaccccc cccccccccc 300
ccagtgtatt ctactcttgt ccccggtata aatttgattg ttccgaacta cataaattgt 360
agaaggattt tttagatgca catatcattt tctgtgatac cttccacaca cccctccccc 420
ccaaaaaaat ttttctggga aagtttcttg aaaggaaaac agaagaacaa gcctgtcttt 480
atgattgagt tgggcttttg ttttgctgtg tttcatttct tcctgtaaac aaatactcaa 540
atgtccactt cattgtatga ctaagttggt atcattaggt tgggtctggg tgtgtgaatg 600
tgggtgtgga tctggatgtg ggtgggtgtg tatgccccgt gtgtttagaa tactagaaaa 660
gataccacat cgtaaacttt tgggagagat gatttttaaa aatgggggtg ggggtgaggg 720
gaacctgcga tgaggcaagc aagataaggg gaagacttga gtttctgtga tctaaaaagt 780
cgctgtgatg ggatgctggc tataaatggg cccttagcag cattgtttct gtgaattgga 840
ggatccctgc tgaaggcaaa agaccattga aggaagtacc gcatctggtt tgttttgtaa 900
tgagaagcag gaatgcaagg tccacgctct taataataaa caaacaggac attgtatgcc 960
atcatcacag gatgtccttc cttctccaga agacagactg gggctgaagg aaaagccggc 1020
caggctcaga acgagcccca ctaattactg cctccaacag ctttccactc actgccccca 1080
gcccaacatc ccctttttaa ctgggaagca ttcctactct ccattgtacg cacacgctcg 1140
gaagcctggc tgtgggtttg ggcatgagag gcagggacaa caaaaccagt atatatgatt 1200
ataacttttt cctgtttccc tatttccaaa tggtcgaaag gaggaagtta ggtctaccta 1260
agctgaatgt attcagttag caggagaaat gaaatcctat acgtttaata ctagaggaga 1320
accgccttag aatatttatt tcattggcaa tgactccagg actacacagc gaaattgtat 1380
tgcatgtgct gccaaaatac tttagctctt tccttcgaag tacgtcggat cctgtaattg 1440
agacaccgag tttaggtgac tagggttttc ttttgaggag gagtccccca ccccgccccg 1500
ctctgccgcg acaggaagct agcgatccgg aggacttaga atacaatcgt agtgtgggta 1560
aacatggagg gcaagcgcct gcaaagggaa gtaagaagat tcccagtcct tgttgaaatc 1620
catttgcaaa cagaggaagc tgccgcgggt cgcagtcggt ggggggaagc cctgaacccc 1680
acgctgcacg gctgggctgg ccaggtgcgg ccacgccccc atcgcggcgg ctggtaggag 1740
tgaatcagac cgtcagtatt ggtaaagaag tctgcggcag ggcagggagg gggaagagta 1800
gtcagtcgct cgctcactcg ctcgctcgca cagacactgc tgcagtgaca ctcggccctc 1860
cagtgtcgcg gagacgcaag agcagcgcgc agcacctgtc cgcccggagc gagcccggcc 1920
cgcggccgta gaaaaggagg gaccgccgag gtgcgcgtca gtactgctca gcccggcagg 1980
gacgcgggag gatgtggact gggtggac 2008
<210> 15
<211> 100
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 15
aaggcagccg cagcggcccg ggaaccacac ccacgaaact gtcagccatg ccagtgcctg 60
ctctgtgcct gctctgggcc ctggcaatgg tgacccggcc 100
<210> 16
<211> 150
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 16
gggagacccc acccagcatg atgtatgaat acctcccatt caagtgccca ctcgagataa 60
cttcgtataa tgtatgctat acgaagttat atgcatggcc tccgcgccgg gttttggcgc 120
ctcccgcggg cgcccccctc ctcacggcga 150
<210> 17
<211> 181
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 17
tttcactgca ttctagttgt ggtttgtcca aactcatcaa tgtatcttat catgtctgga 60
ataacttcgt ataatgtatg ctatacgaag ttatgctagt aactataacg gtcctaaggt 120
agcgagctag cgatgccacc gaggaccagt tgtgctgcaa ggaacactga agcgctccac 180
c 181
<210> 18
<211> 177
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Синтетический полинуклеотид
<400> 18
gggagacccc acccagcatg atgtatgaat acctcccatt caagtgccca gtcgagataa 60
cttcgtataa tgtatgctat acgaagttat gctagtaact ataacggtcc taaggtagcg 120
agctagcgat gccaccgagg accagttgtg ctgcaaggaa cactgaagcg ctccacc 177
<210> 19
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 19
ggtgttggtg gcaggtaaga gt 22
<210> 20
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 20
tgaggaaatg gtaaacccag aacaga 26
<210> 21
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 21
tggtgtgtca tcagggtatg tttc 24
<210> 22
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 22
tgagcctggt gggattactc t 21
<210> 23
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 23
tagcagtgga agttgcctag gtcc 24
<210> 24
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 24
ccgtcaaggc cagtgctt 18
<210> 25
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 25
gcaagcctgt tggagactca g 21
<210> 26
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 26
caccgtagct gcgacactgt gg 22
<210> 27
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 27
agacacgaac tcctctttgg a 21
<210> 28
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 28
tgggctgagc cacatctc 18
<210> 29
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 29
cagactccac acagcggcgc t 21
<210> 30
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> синтетический олигонуклеотид
<400> 30
tcagttccat ccaggcagat tc 22
<---
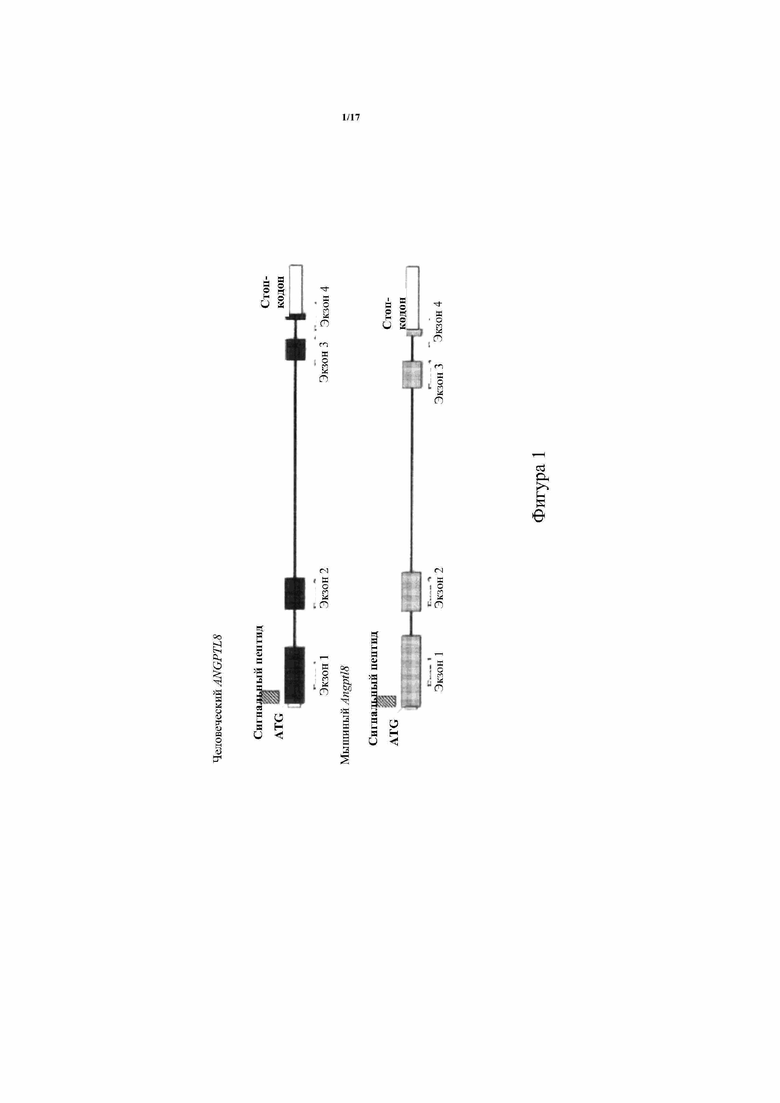

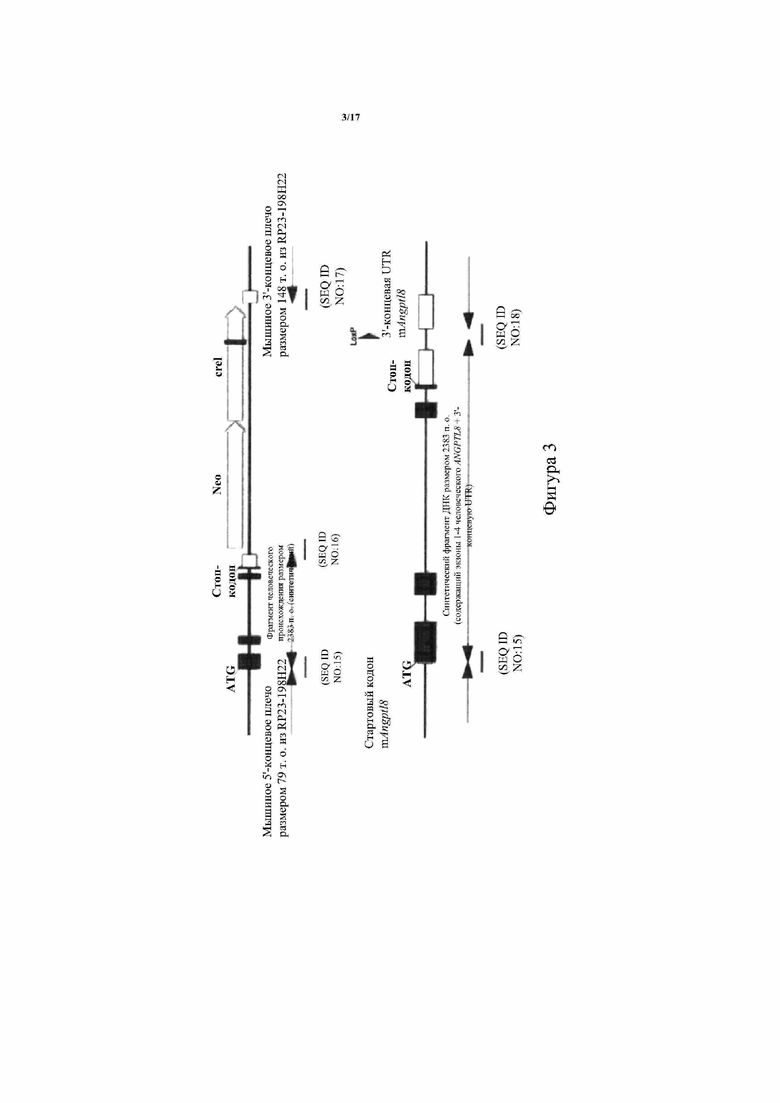
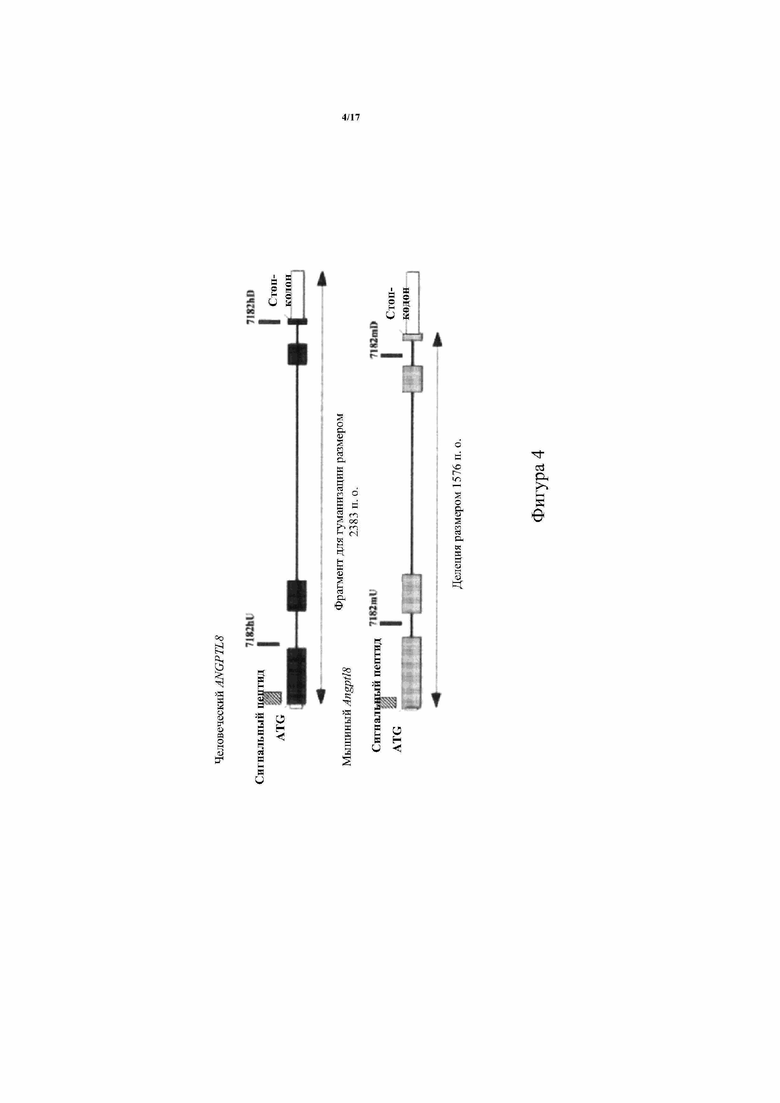

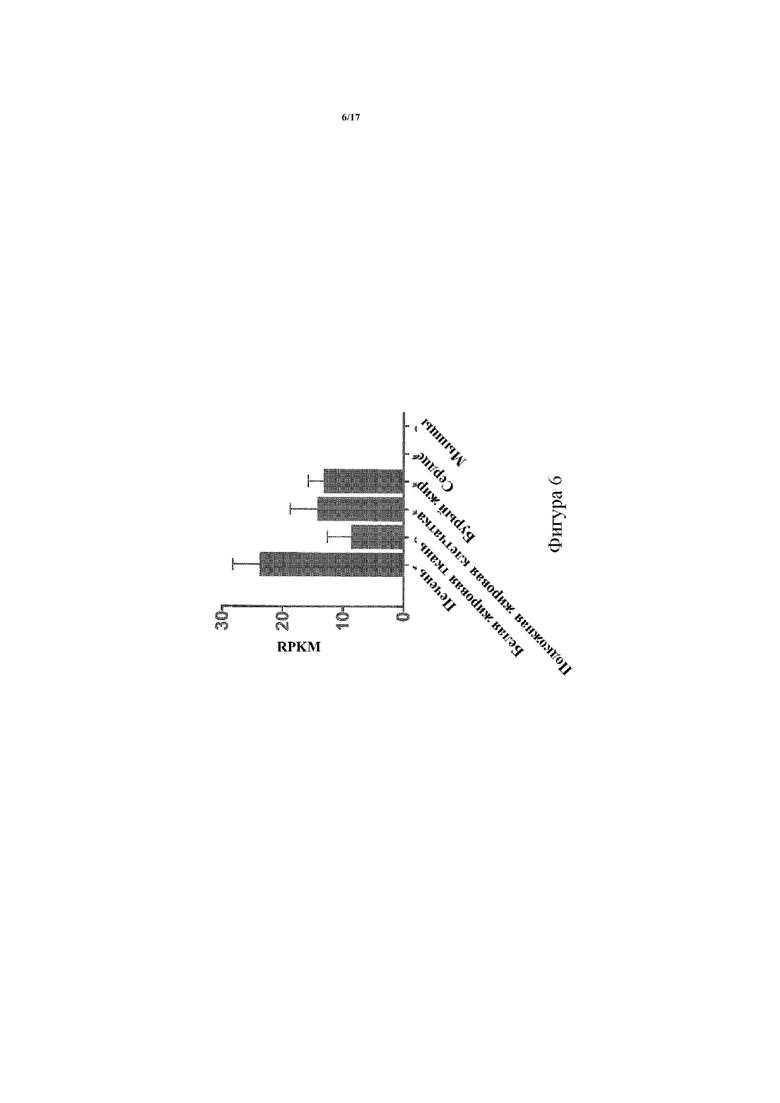











Изобретение относится к области биохимии, в частности к грызуну для экспрессии человеческого белка ANGPTL8, геном которого содержит сконструированный ген ангиопоэтин-подобного белка 8 (Angptl8) в эндогенном локусе Angptl8, а также к его клетке, ткани и эмбриону. Также раскрыт способ получения грызуна, экспрессирующего человеческий полипептид ANGPTL8 с эндогенного гена Angptl8. Изобретение также относится к способу оценки эффективности лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, а также к способу оценки фармакокинетических свойств лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, предусматривающему использование вышеуказанного грызуна. Изобретение эффективно для идентификации и разработки новых терапевтических средств, которые можно применять для лечения сердечно-сосудистых заболеваний, нарушений или состояний. 9 н. и 11 з.п. ф-лы, 9 ил., 1 табл., 4 пр.
1. Грызун для экспрессии человеческого белка ANGPTL8, при этом геном грызуна содержит сконструированный ген ангиопоэтин-подобного белка 8 (Angptl8), в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, при этом сконструированный ген Angptl8 кодирует человеческий белок ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, при этом человеческий белок ANGPTL8 экспрессируется у грызуна из сконструированного гена Angptl8, и при этом грызун является мышью или крысой.
2. Грызун по п. 1, где сконструированный ген Angptl8 содержит эндогенную 3' нетранслируемую область (UTR) эндогенного гена Angptl8 грызуна.
3. Грызун по п. 1, где человеческий белок ANGPTL8 содержит аминокислотную последовательность, приведенную в SEQ ID NO: 6.
4. Грызун по п. 1, где человеческий полипептид ANGPTL8 содержит аминокислотные остатки 22-198 в SEQ ID NO: 6.
5. Грызун по любому из пп. 1-4, где грызун является крысой.
6. Грызун по любому из пп. 1-4, где грызун является мышью.
7. Выделенная клетка грызуна для экспрессии человеческого белка ANGPTL8, содержащая сконструированный ген Angptl8 в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, при этом сконструированный ген Angptl8 кодирует человеческий белок ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, и при этом клетка грызуна является мышиной клеткой или крысиной клеткой.
8. Выделенная ткань грызуна для экспрессии человеческого белка ANGPTL8, при этом геном ткани содержит сконструированный ген Angptl8 в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, при этом сконструированный ген Angptl8 кодирует человеческий белок ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, и при этом ткань грызуна является мышиной тканью или крысиной тканью.
9. Эмбриональная стволовая клетка (ES) грызуна для получения грызуна, который экспрессирует человеческий белок ANGPTL8, содержащая сконструированный ген Angptl8 в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, при этом сконструированный ген Angptl8 кодирует человеческий белок ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, и при этом ES клетка грызуна является мышиной ES клеткой или крысиной ES клеткой.
10. Эмбрион грызуна для получения грызуна, который экспрессирует человеческий белок ANGPTL8, содержащий ES клетку грызуна по п. 9, при этом эмбрион грызуна является мышиным эмбрионом или крысиным эмбрионом.
11. Способ получения грызуна, экспрессирующего человеческий полипептид ANGPTL8 с эндогенного гена Angptl8, при этом способ включает
(a) вставку нуклеиновой кислоты, кодирующей человеческий полипептид ANGPTL8 в эндогенный локус Angptl8 в ES клетке грызуна, тем самым формируя сконструированный ген Angptl8 в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, при этом сконструированный ген Angptl8 кодирует человеческий полипептид ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, и при этом ES клетка грызуна является мышиной ES клеткой или крысиной ES клеткой; и
(b) получение грызуна с применением ES клетки грызуна полученной на стадии (a),
при этом геном грызуна содержит сконструированный ген Angptl8, который кодирует человеческий полипептид ANGPTL8, при этом человеческий полипептид ANGPTL8 экспрессируется у грызуна из сконструированного гена Angptl8, и при этом грызун является мышью или крысой.
12. Способ по п. 11, где человеческий полипептид ANGPTL8 содержит аминокислотные остатки 22-198 в SEQ ID NO: 6.
13. Способ получения грызуна, который экспрессирует человеческий полипептид ANGPTL8, при этом способ включает модификацию генома грызуна для содержания в модифицированном геноме сконструированного гена Angptl8 в эндогенном локусе Angptl8, при этом сконструированный ген Angptl8 содержит 5' нетранслируемую часть экзона 1 эндогенного гена Angptl8 грызуна, кодирующую часть экзона 1 человеческого гена ANGPTL8 и экзоны 2-4 человеческого гена ANGPTL8, и при этом сконструированный ген Angptl8 кодирует человеческий полипептид ANGPTL8 и функционально связан с эндогенным промотором Angptl8 грызуна в эндогенном локусе Angptl8, за счет чего обеспечивается получение указанного грызуна, где грызун является мышью или крысой.
14. Способ по п. 13, где человеческий полипептид ANGPTL8 содержит аминокислотные остатки 22-198 в SEQ ID NO: 6.
15. Способ оценки эффективности лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, в снижении уровней триглицеридов, при этом способ включает стадии: введения лекарственного средства грызуну по п.1; и проведения анализа для определения того, снижает ли лекарственное средство уровни триглицеридов у указанного грызуна.
16. Способ оценки фармакокинетических свойств лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8, при этом способ включает стадии: введения лекарственного средства грызуну по п.1; и проведения анализа для определения одного или более фармакокинетических свойств лекарственного средства, целенаправленно воздействующего на человеческий ANGPTL8.
17. Способ по п. 15 или 16, где лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, является антагонистом ANGPTL8.
18. Способ по п. 15 или 16, где лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, является агонистом ANGPTL8.
19. Способ по п. 15 или 16, где лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, представляет собой антитело к ANGPTL8.
20. Способ по п. 15 или 16, где лекарственное средство, целенаправленно воздействующее на человеческий ANGPTL8, вводят грызуну внутривенно, внутрибрюшинно или подкожно.
| WO 2006098887 A2, 21.09.2006 | |||
| ANNY DEVOY et al., Genomically humanized mice: technologies and promises, Nat Rev Genet., 2012, Vol.13, N.1, pp | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| WO 2015179317 A2, 26.11.2015 | |||
| WO 2015196051 A1, 23.12.2015 | |||
| GINA M | |||
| PELOSO et al., Association of Low-Frequency and Rare Coding-Sequence Variants with Blood Lipids and Coronary Heart Disease in | |||
Авторы
Даты
2021-02-05—Публикация
2017-02-03—Подача