Родственная заявка
Настоящая заявка претендует на приоритет по Предварительной заявке на патент U.S. No. 61/794,818, поданной 15 марта 2013 г., которая полностью включена сюда путем ссылки.
Уровень техники
Современные подходы к генной терапии нейродегенеративных заболеваний не дают возможности включать и выключать экспрессию введенного терапевтического гена. Кроме того, существующие подходы не дают возможности дозировать экспрессию терапевтического гена после введения. Имеется насущная потребность в регулируемых промоторах.
Сущность изобретения
В некоторых воплощениях настоящим изобретением предусмотрена выделенная последовательность промотора, включающая (или состоящая из) нуклеиновую кислоту длиной от 500 до 1700 нуклеотидов, которая по меньшей мере на 90% идентична SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7. В некоторых воплощениях промотор на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% идентичен SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6 или SEQ ID NO: 7.
В некоторых воплощениях настоящим изобретением предусмотрена экспрессионная кассета, содержащая описанный выше промотор, функционирующий в трансформированных клетках, который функционально связан с заданным сегментом ДНК, кодирующим белок или РНК-транскрипт. В некоторых воплощениях заданный сегмент ДНК содержит ген селектируемого маркера или ген-репортер. В некоторых воплощениях заданный сегмент ДНК кодирует терапевтическую композицию. В некоторых воплощениях терапевтическая композиция представляет собой молекулу РНКи.
В некоторых воплощениях настоящим изобретением предусмотрен вектор, содержащий описанную выше экспрессионную кассету. В некоторых воплощениях вектор представляет собой вектор на базе аденоассоциированного вируса (AAV).
В некоторых воплощениях настоящим изобретением предусмотрены трансформированные клетки, содержащие описанную выше экспрессионную кассету или описанный выше вектор. В некоторых воплощениях клетки-хозяева представлены эукариотическими клетками. В некоторых воплощениях эукариотические клетки представлены клетками животных (напр., клетками млекопитающих, как-то клетками человека).
В некоторых воплощениях настоящим изобретением предусмотрен способ получения трансформированных клеток, включающий стадии (i) введения в клетки рекомбинантной ДНК, содержащей описанный выше промотор, функционально связанный с сегментом ДНК, с тем, чтобы получить трансформированные клетки, и (ii) идентификации или отбора линии трансформированных клеток. В некоторых воплощениях рекомбинантная ДНК экспрессируется с тем, чтобы придать характерный фенотип трансформированным клеткам. В некоторых воплощениях трансформированные клетки проявляют существенное усиление экспрессии гена-репортера при введении в клетки, полученные от пациентов с болезнью Хантингтона, по сравнению с клетками, полученными от контрольных индивидов.
В некоторых воплощениях настоящим изобретением предусмотрены трансформированные клетки, полученные описанным выше способом.
В некоторых воплощениях настоящим изобретением предусмотрены трансформированные клетки, содержащие описанный выше выделенный промотор.
В некоторых воплощениях настоящим изобретением предусмотрены трансформированные клетки, содержащие описанную выше экспрессионную кассету.
В некоторых воплощениях настоящим изобретением предусмотрен способ лечения нейродегенеративных заболеваний у млекопитающих, включающий введение (а) описанного выше вектора или (b) описанных выше трансформированных клеток.
Краткое описание чертежей
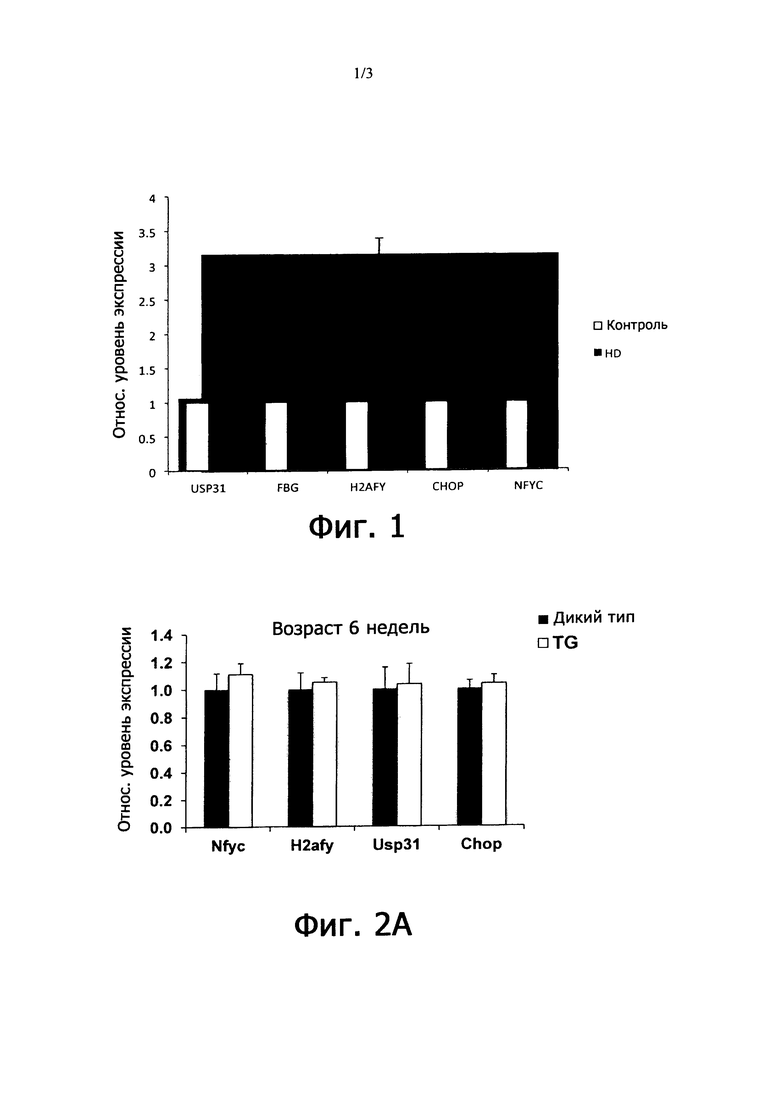
Фиг. 1. Анализ экспрессии у пяти промоторов свидетельствует о положительной регуляции их эндогенных транскриптов в посмертном материале мозга пациентов с болезнью Хантингтона по сравнению со здоровыми контрольными лицами.
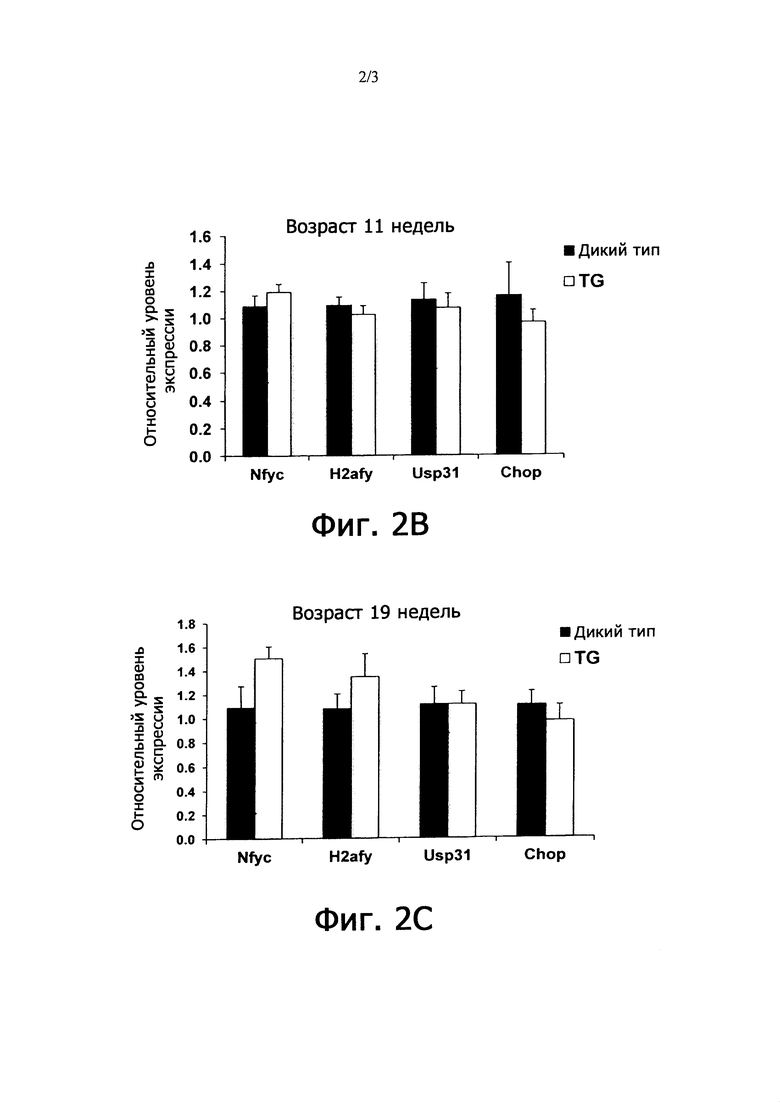
Фиг. 2A-2C. Положительная регуляция эндогенных транскриптов в мозге мышей с болезнью Хантингтона в возрасте 6 недель (фиг. 2A), 11 недель (фиг. 2B) и 19 недель (фиг. 2C).
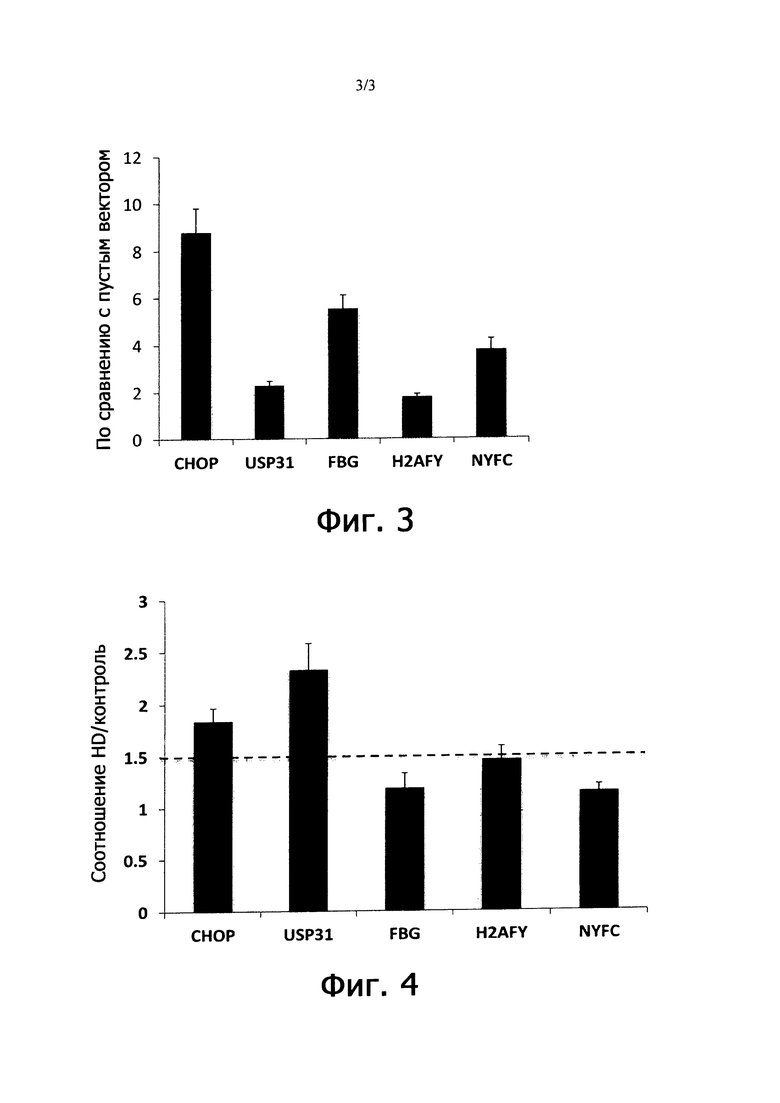
Фиг. 3. Активность клонированных последовательностей промоторов генов.
Фиг. 4. Индукция клонированных последовательностей промоторов генов по данным экспрессии гена-репортера (люциферазы).
Раскрытие сущности изобретения
Настоящим изобретением предусмотрено использование последовательностей промоторов генов, которые могут активировать, усиливать или подавлять экспрессию генетической последовательности при возникновении или при патологическом прогрессировании нейродегенеративных заболеваний. Данное изобретение прямо применимо в области генной терапии. Оно имеет потенциальную коммерческую ценность в качестве инструмента при разработке подходов регулируемой генной терапии для нейродегенеративных заболеваний. Данным изобретением предусмотрено средство, которым можно дозировать или регулировать экспрессию терапевтических генов по ходу заболевания на основании состояния или скорости прогрессирования нейродегенеративного заболевания. Например, во время прогрессирования заболевания промоторные последовательности гена могут активировать экспрессию терапевтического гена. Если же терапия остановит прогрессирование заболевания, то активность промоторной последовательности гена ослабеет, что приведет к снижению/ограничению экспрессии терапевтического гена. Данный регулируемый заболеванием динамический подход к экспрессии терапевтических генов является уникальным и востребованным в области генной терапии.
Изобретение применимо к области генной терапии. Оно удовлетворяет потребность в регулировании и/или дозировании терапевтических генов после доставки в мозг. Анализ экспрессии генов показал, что при возникновении и/или при прогрессировании нейродегенеративных заболеваний действует целый ряд промоторных последовательностей генов с тем, чтобы включать, усиливать, подавлять или выключать экспрессию генов. Авторы настоящего изобретения установили и клонировали последовательности промоторов генов, которые активируют и/или повышают экспрессию генов при прогрессировании нейродегенеративных заболеваний на клеточных и животных моделях нейродегенеративных заболеваний. Эти промоторные последовательности генов также могут активировать и/или усиливать экспрессию гена-репортера при прогрессировании нейродегенеративных заболеваний на моделях нейродегенеративных заболеваний. Этот подход уникален и отличается от существующих систем, применяющихся для искусственного регулирования экспрессии терапевтических генов, тем, что он полагается на связанные с нейродегенеративными заболеваниями молекулярные события для модулирования экспрессии терапевтических генов. Эти события, а тем самым и активность промоторных последовательностей определенных генов, контролируются/индуцируются внутриклеточными и/или внеклеточными сигналами, зависящими от возникновения и/или прогрессирования заболевания.
Авторы настоящего изобретения установили, клонировали и протестировали активность семи различных последовательностей промоторов генов на клетках тканевых культур, полученных из контрольных индивидов или индивидов, несущих мутацию гена болезни Хантингтона (т.е. нейродегенеративного заболевания). Эксперименты показали, что эти промоторные последовательности генов могут вызывать значительное усиление экспрессии гена-репортера при введении в клетки, полученные от пациентов с болезнью Хантингтона, по сравнению с клетками, полученными от контрольных индивидов. Кроме того, введение искусственного фактора стресса типа ингибитора протеасом или про-воспалительное воздействие приводит к повышению активности у промоторных последовательностей генов, судя по экспрессии контролируемых эндогенно транскриптов или гена-репортера в культивируемых клетках. Кроме того, на моделях болезни Хантингтона (т.е. нейродегенеративного заболевания) мы обнаружили в мозге мышей зависимое от прогрессирования заболевания повышение активности этих промоторных последовательностей генов при измерении методом количественного ПЦР-анализа регулируемых эндогенно транскриптов генов.
Последовательности промоторов
В некоторых воплощениях изобретения предусмотрены последовательности следующих промоторов, активирующих и/или усиливающих экспрессию генов: убиквитин-специфичной пептидазы 31 (USP31, SEQ ID NO: 1), гамма-FBG (SEQ ID NO: 2), представителя Y семейства гистонов Н2А (H2AFY, SEQ ID NO: 3), ядерного фактора транскрипции Y-гамма (NYFC, SEQ ID NO: 4), индуцируемого повреждением ДНК транскрипта 3 (CHOP, SEQ ID NO:5), некодирующей РНК 38A (локус 38A, SEQ ID NO: 6) и некодирующей РНК 17A (17A, SEQ ID NO: 7).
Идентификатор гена: USP31 (SEQ ID NO: 1)
GGAGGTCATATACTAGTTGATTTTGGACtaaaggcatcccaaagatgtactattttttgctccctgcactatttttttttaatggaaccaacgtttaaaaataggatttctgccttctcttaaaacatcagatgatctggtaacgctgagctcctgttctcacatgggaacaactggctggagctgagtggcagccacctctttagaaagatgttaatttgaagtctgctatagtccccatcattccttatatttcccccaacactgagacccaagtcacttgaaagtcaatatgatgattcaaacaccaggattcttcactcatttgtgggtttgtgacctgtgatatttgtggattcgtgacctttggtttagaggtcaagtataggggttgtaaataaaacttgggtttgaatcagataagaactgtaccaatctcaaagacggtgaattaaagattaaagaaaatattgcatgcttggcataatgtgtggaacacaacagctattgtaaacacccagtaggaatgtaagctgcaagagggcaggtagaaaccgtgctaatttaatccgctggggatatgacatttgattctaatttaataggtttaattctttgcaatatccccagtaactgctgaatgaatgagtgagtgaatgaatgaatggaatgatgaatgatgggagagcccggaggagttttaaaggctggaatgaaaaggaaagtagttatgataacagcgtttcgctgggactccaaggtgcagccaggaagaaaagcccgctgggacgtgccagggtctgtgactgcgctccgctggcacccagagggtaggtatctgcaacgtcccttgggagccagacagggctgacttgcccaggacctgtcagggccatgtccaccagctcttgcacggtctggtaactgacagcatcctgattcctgcacgttcccgcctctgccatctgaccagcaaagacagagacccaccccggggatccaccatccaacgggagcccagccttttcctccaagccgggacggcgcccacactagacatggcctccctcgggcttcacgcagcaggaccgcgcccgcagcctccaggcatcgcgtccggctggagaggcagctaccgtcccacagtgaacatggcggccgaggcggcttcagcgccgggcgggcggcgccgggaggcacgtcacgtgagcggctcagctgggcggaccgcgcgcgcgcccgctggccccgccggccgccgctcgctcgctggctcggctgcgctttgaggtgtgtggggcgtcgagcccccgggcccggtgaggcgcggcgctgcgggatgcggcggcggccgtggcggggccgcgggccgggcgggcgggcgcggtgatgagtgtctgcggccgccgccatgtccaaggtaacggcgcctgggtccgggccgccggcggcggcgagcgggaaggagaagcgctccttcagcaagcggctgtttcggagcggccgcgctggcggcggcggcgcggggggccccggggcgtccgggccggccgcgccttcctcgccctcctcgccctcctctgcacgctcggtgggcAGCTTCATGAGCCGCGTTCTCAAG
Идентификатор гена: гамма-FBG (SEQ ID NO: 2)
TGAGAAGTGAGAGCCTATGAACATGGttgacacagagggacaggaatgtatttccagggtcattcattcctgggaatagtgaactgggacatgggggaagtcagtctcctcctgccacagccacagattaaaaataataatgttaactgatccctaggctaaaataatagtgttaactgatccctaagctaagaaagttcttttggtaattcaggtgatggcagcaggacccatcttaaggatagactaggtttgcttagttcgaggtcatatctgtttgctctcagccatgtactggaagaagttgcatcacacagcctccaggactgccctcctcctcacagcaatggataatgcttcactagcctttgcagataattttggatcagagaaaaaaccttgagctgggccaaaaaggaggagcttcaacctgtgtgcaaaatctgggaacctgacagtataggttgggggccaggatgaggaaaaaggaacgggaaagacctgcccacccttctggtaaggaggccccgtgatcagctccagccatttgcagtcctggctatcccaggagcttacataaagggacaattggagcctgagaggtGACAGTGCTGACACTACAAGGCTCGG
Идентификатор гена: H2AFY (SEQ ID NO: 3)
CCAAGATCAGCTCTTGGAGGAGTGtagactttaattccacctggtggtccctacagaacggagagtccttgcccaaaggcacagagaaggatggaacaacaatgtggtgtgtgggggagggtctctgcacctttcctgacatcttttcttcgggagatcctcatagaaccataatgctttgttttgggaccagaagcatcataagcatcatcatttttccagcttcatctcctgttactttccccttcacccattctactccaacctcacactcgctctgtcttgactattttggacacactcctaccccagcctttgcacttgctattcctcatgctcggcgcagttcttccccagacatccacacggcttgctccctcaatttcttcaggctttaaatgttactttctcatagaggccttctcttgtatttgagcctcactcttatctcacacttcctattccccttctccgccttatttttctccaccccatggagaccctctgacacattctcccgtttgtctgtctttcccccacgagactgcaaactacaggagggcagagatttctgcctgttctcttggctgtttcatatccagcacccaaatcgatgtatgacacaaaatacgttctcagtacttaatcgaattaacgaatgcatgaatggcaggtattggacattgttttgcaaactcttaaagtaaggtgtaaagcatcccggtgaggtggaggttactgccgctgcgattcccgcgcagcctgaggactggggggtgggggtgggggtctctaattacctccataatccccagtagcggcactttaaacttcacatcaaccctgagggatgtgtattattatccaaatttagttcacagctggatggagaagtggcttccggctccacactttggagggaggggagtagagggcaggcccccatttaagtacccgggatggggcaccaatgccttcaggcggtaaaccaatttaggaagacgtggcgggctttgtggcggctcctcctctttcggcctgtccgcagtttttaaaaaacgtgtgtgatgataaggaatcactgtctacattagtaattcccaacttgggtccgaaagtgaacttttgctgaagcgaagtagctaaccgcttccatgtgcaaggcaggttccagacttcggggtgaggaggattaactgaaggaccccaggggaaccgggtgcgcagtaattgatcttggggcagaccagggcttggcggtggcctgtatctaaagacagcggggtctctgaggcggggcaggggggagttggcattgactggggagggaagagcgatcGCTGGTAACAGCCATTGTGCCTTC
Идентификатор гена: NYFC (SEQ ID NO: 4)
GTGCCTGATGTGAGATTTATTGAAACTGGatttgaaaacaattttcctgaattcaagtcgagggtttactccactattctcaattactttatcaccagggttataaacccaaaggaagtgagtaacaacagtgtgattttattgaggacccatgcaacactagtctcagaaaggctccagtgtcatttgtaaaattcaaggttaccatcagcagaggcagtcattcctctctgcgcttgttacctaatgcactaactctcactgtaggtaattccattcaagacacatttgatgactatacctacaggttttgaagttattcggatggggttttgacacttactagctgtggggacttagatcaagttacttaacctttttgagcttcagttttatcatttgtaaaatggatacaatcctgatgcctttggaccaagtggtcacggaaatgaaagagataagtatgaaaaaatccatgctcatagtagctgtggtttccaactgcgtgataaaacttteaaatctgcattcaaataagaacaactatgtcgacgtaaggttacaagctaactattcttggtaagtactgttctttattctagaggacatcactttacagtttggtgctaaatgctcttttatgaatttaaggtgccagtagctgtctacttgaacggcatgcttaatctggaacgccatgtcgaccttcatcccccagttctttctccccaaattaaaaacacaaatacacacacacgcccctacttagttcctaaaactcaagggcacgcgcacacacctacttatttcctaaaattcaagctcgcaccaaggagatccacaaggataggcagggtggtggaggtcactgggcagcgcctccggatcccccgaaagggggcggggtcaaaactcagatctcgagctcccgaaagggggcggggttaaaactctcagatctcattccgcctccctctgtcgtcgccccttcccaattctcgcgagacctcaaggagcacagcttctgcgcaccgcacgatactgggagtccaggcgccaagggagggggaagggaaaaggggaaacggtgcaaacggcgtggccgccatcttgcttgtgcccccgcttcgcgcgcgctccgttctccgtgacgcacacttccccctcccctccgccgcgcctgggcctctgcattgcccgactccgtaggagcgcgggggcggctcctgctcttcctggactcctgagcagaggtgtgtgagtgtgcgggagtttctgtgcgagggtgatagggaagcggcggcggggggaggggcagcgcttccCGCCTTCGCCAGAGACCTCACTTC
Идентификатор гена: CHOP (SEQ ID NO: 5)
CTTTTGGGAGATtTACGGGGCTAGAACAGGAGACCACCCccgtttttttgtttgtttgttttgttttttgttmggtgaaacgtagtctcgctctgtcacccaggctggagtgcagtggcgcgatctcggtcactgcaacatccgcctccagggttcaagcgattcttctgcctctgcctccagagtagctgggattacaggcgcgcatcaccacacccggctaatttttgtatttttagtagagacggggtttcaccatgttggtcaggctgatctcgaactcctgacctcaagtgatccgctctcctcagcctcccaaagtgctgggattacaggcgtaagccactgagcccggccaggagacctctttaagaagactcgagatgtcgacaatcccagtggatggataccaactttaaaaagaaaagttcaaaaggcctatgtgcccattagctgggaggggccaagaaatatgggagtcccttatagtgggggtaaaacggcgggtaaagctaggtgggcggaacagcagcttctgggggagacaagcggcaaagaggctcacgaccgactaggggcgaccaaggctgatagccgttggggccgttgggcgccgggagctggcgccccgccctctctcctctcccccaccctccgcacctcccaccaccctcggtgtcccctgcgcgtgcgcgtgcagacaccggttgccaaacattgcatcatccccgcccccctttcctcccctccccccccgctacactcccctccgcgcgcgcgcatgactcacccacctcctccgtgaagcctcgtgacccaaagccacttccgggtccgacactacgtcgaccccctagcgagagggagcgacgggggcggtgccgcggggctcctgagtggcggatgcgagggacggggcggggccaatgccggcgtgccactttctgattggtaggttttggggtcccgcccctgagaggagggcaaggccatggtaaaagattacagccaggcgctcCCGAGGTCAGAGACTTAAGTCTAAGgcaCTG AGCGTATC
Идентификатор гена: локус 38A (SEQ ID NO: 6)
TAATAACAACATATCTGAAAAAGACGCtttaaaatcccatttatgaaagcataaaaatagttagaaataaatttaaccataaaggtgaaatatttgtataccgataactataaacctttgataaaaaaagttgaagaagAcacatataaatagaataatattctgtgttcatgaatcaaaaaatttaacaatgttaaaatgtctgtattaaccaaagcaatatacaaattcaatgcaatttctatcaaaatttcaaggatatgcatcacagaaatagaaaaaaaattcttgaaattcatatggaaccacagacacataaaaacagaataggcaaaggaacaatgagaaagcaaaacaaagcttgaggcatcacacttcctaagttaaaattatattgcaaagctacagtaatcaaaaacagtatacaaatggcatgaaaacgaaaatgtggaccaacggaacagaatatagagagccagaaacttaactaaTTTTcaacaagGGTACCAACAGGACACCCTGAA
Идентификатор гена: локус 17A (SEQ ID NO: 7)
ATTTCCACCAGCAACACACAAGGGTTCCAGTTTCTCCACATCTTCACCAACACTTGTGGTTTTGCTTTTTGGTAATAGCCATGCTAATGGGTGTGAACAAGAAGTGCTTTAAGCATCTCCTAAAGCGGAAGAAACTGAGGCCCAGAGAAGGGAAGAATCACACGAGAGATTGAGGTCACAAGCAAGTCAGTGATAGAGCAGGACCTGGAAGCTGGATCCCCTAACCCCAGCCTAGTTCTTGCTACTAAAACCCAAAATCCAGTTTCCATTGCTATATGTCAGAGGGTGCACAGCCATGGCCACAGGCCAGATACAGACTTTAAGTTTATTTGGTTTGATCCTTACTTTCTTTTTTTTTTAATTCAAAATAGTATCAACATTTAAAAATTAGGGGATTTTATATTTTAAAAGTCTAAATTTCTGATTTCTCCCCTCAAAAATCAGAAGGTCTGGTAACCCTTGACCCACATTCTAACTCAGCAACCAACTATTACTGTCTTTTGTTTTGTTTTGTTCTGTTGAGACAAGGTCTTGTTCTGTCACCCAGGCTGGAGTACGGTGGCGTGATCACGGCTCACTGCAGTCTTGAACTCCTGGGCTCAAGCAAGCCCCCCGTCTTGGCCTCCCAAAGCTCTGGGATTACAGGTGTGAGCCCACGCCCAGCCCTATCATTCTGTAATATCCTTCCACACAGGCTAGTTCACACACTGGCTGGTCCTGGTAACACTGGAGTTTGCAGCCCTTTGCTTTTCACATCCATAGATATTCCTCATTCTGAGTGTCAGTAGACACATAGTTACGTGTAACATCATAGGCAGGTTCCATACTTCTTTCCTCTTTCCTTTACTCTATATTGTCTTTGAATATCTTAGCTATTTCCTCACCATAAAAGTGAAATAATGTTGCAAATAAATAGTGCAAAATATTAACAAAGACACAATTGAATAGCCTG
“Промотор” означает такую последовательность нуклеотидов, которая обычно находится выше (с 5′стороны от) своей кодирующей последовательности и контролирует экспрессию кодирующей последовательности тем, что обеспечивает распознавание РНК-полимеразой и других факторов, необходимых для правильной транскрипции.
“Промоторы” включают в себя минимальные промоторы, то есть короткие последовательности ДНК, состоящие из TATA-бокса и других последовательностей, служащих для определения сайта инициации транскрипции, к которым добавляются регуляторные элементы для управления экспрессией. К “промоторам” также относятся последовательности нуклеотидов, включающие минимальный промотор плюс регуляторные элементы, которые способны контролировать экспрессию кодирующей последовательности или функциональной РНК. Такой тип последовательности промотора состоит из проксимальных и более дистальных вышерасположенных элементов, которые зачастую называются энхансерами. Соответственно, “энхансер” представляет собой последовательность ДНК, которая может стимулировать активность промотора и может быть собственным элементом промотора или гетерологичным элементом, вставленным для повышения уровня или тканевой специфичности промотора. Он способен работать в обеих ориентациях (нормальной или отраженной) и даже при перемещении его выше или ниже от промотора. И энхансеры, и другие вышерасположенные элементы промоторов связываются со специфичными к последовательности ДНК-связывающими белками, которые опосредуют их эффекты. Промоторы могут происходить целиком из природного гена либо состоять из различных элементов, происходящих из различных природных промоторов, или даже состоять из синтетических сегментов ДНК. Промотор также может содержать последовательности ДНК, которые участвуют в связывании белковых факторов, контролирующих эффективность инициации транскрипции в ответ на физиологические или онтогенетические условия.
В настоящем изобретении “биологически активный” означает то, что промотор обладает по меньшей мере 0,1%, 10%, 25%, 50%, 75%, 80%, 85% и даже 90% или больше, напр., 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% активности промотора CCT по SEQ ID NO: 1 или SEQ ID NO: 2. Активность промотора может быть определена методами, хорошо известными в данной области. Например, см. Sambrook et al., Molecular Cloning: A Laboratory Manual (1989). Промоторы по настоящему изобретению, которые не идентичны SEQ ID NO: 1 или SEQ ID NO: 2, но сохраняют сравнимую биологическую активность, называются вариантами промоторов. Нуклеотидные последовательности по изобретению включают как природные последовательности, так и рекомбинантные формы.
Изобретение охватывает композиции из выделенных или практически очищенных нуклеиновых кислот. В контексте настоящего изобретения “выделенная” или “очищенная” молекула ДНК или РНК есть такая молекула ДНК или РНК, которая существует отдельно от своего природного окружения и поэтому не является природным продуктом. Выделенные молекулы ДНК или РНК могут существовать в очищенном виде или же вне своего природного окружения, как-то, к примеру, в трансгенных клетках-хозяевах. Например, “выделенная” или “очищенная” молекула нуклеиновой кислоты или её биологически активная часть будет практически свободной от другого клеточного материала или культуральной среды при получении её рекомбинантными методами либо практически свободной от химических предшественников или других химических веществ при её синтезе химическим путем. В одном воплощении “выделенная” нуклеиновая кислота свободна от тех последовательностей, которые в природе фланкируют эту нуклеиновую кислоту (то есть последовательностей, расположенных на 5′- и 3′-концах нуклеиновой кислоты) в геномной ДНК того организма, из которого происходит нуклеиновая кислота. Например, в различных воплощениях выделенная молекула нуклеиновой кислоты может содержать менее чем 5 т.о., 4 т.о., 3 т.о., 2 т.о., 1 т.о., 0,5 т.о. или 0,1 т.о. из последовательностей нуклеотидов, которые в природе фланкируют эту молекулу нуклеиновой кислоты в геномной ДНК тех клеток, из которых происходит нуклеиновая кислота. Фрагменты и варианты приведенных нуклеотидных последовательностей также охватываются настоящим изобретением. Под “фрагментом” или “частью” подразумевается вся длина или же неполная длина нуклеотидной последовательности.
Термин “нуклеиновая кислота” относится к дезоксирибонуклеиновым кислотам (ДНК) или рибонуклеиновым кислотам (РНК) и их полимерам в одноцепочечном либо двухцепочечном виде, состоящим из мономеров (нуклеотидов), содержащих сахар, фосфат и основание, представленное пурином либо пиримидином. Если это специально не оговорено, термин охватывает и нуклеиновые кислоты, содержащие известные аналоги природных нуклеотидов, которые обладают такими же свойствами связывания, как и стандартные нуклеиновые кислоты, и подвергаются метаболизму таким же образом, как и природные нуклеотиды. Если не указано иначе, данная последовательность нуклеиновой кислоты также охватывает её консервативно модифицированные варианты (напр., замены кодонов на соответствующие вырожденные кодоны) и комплементарные последовательности, наряду с приведенными в явном виде последовательностями. В частности, замена кодонов на соответствующие вырожденные кодоны может осуществляться путем создания последовательностей, в которых третье положение у одного или нескольких выбранных (или всех) кодонов замещено на различные основания и/или остатками дезоксиинозина. “Фрагмент нуклеиновой кислоты” представляет собой часть данной молекулы нуклеиновой кислоты.
“Природный”, “нативный” или “дикого типа” применяется для описания таких объектов, которые встречаются в природе, в отличие от полученных искусственным путем. Например, белковая или нуклеотидная последовательность, присутствующая в организме (включая вирусы), которая может быть выделена из природного источника и которая не подвергалась преднамеренной модификации человеком в лаборатории, является природной.
Векторы и экспрессионные кассеты
В некоторых воплощениях настоящим изобретением предусмотрены векторы и экспрессионные кассеты, содержащие описанные выше промоторы.
Векторы
“Вектор” служит для обозначения, среди прочего, любых вирусных векторов, а также любых плазмид, космид, фаговых или бинарных векторов в двухцепочечной либо одноцепочечной, линейной или кольцевой форме, которые могут и самостоятельно передаваться или мобилизироваться и могут трансформировать прокариотические или эукариотические организмы путем встраивания в клеточный геном или же существуют внехромосомно (напр., автономно реплицирующиеся плазмиды с ориджином репликации).
Выбор и оптимизация конкретного экспрессирующего вектора для экспрессии определенной терапевтической композиции (напр., белка) в клетке может осуществляться путем получения последовательности нуклеиновой кислоты, кодирующей белок, возможно, с одним или несколькими соответствующими контролирующими участками (напр., промотором, встроенной последовательностью); получения векторной конструкции, включающей вектор, в который вставляется последовательность нуклеиновой кислоты, кодирующая белок; трансфекции или трансдукции культивируемых клеток in vitro векторной конструкцией; и определения того, присутствует ли белок в культивируемых клетках.
Векторы для клеточной генной терапии включают вирусы, как-то дефектные по репликации вирусы. Дефектные по репликации ретровирусы способны направлять синтез всех белков вириона, но не способны производить инфекционные частицы. Соответственно, эти генетически измененные ретровирусные экспрессирующие векторы в общем применимы для высокоэффективной трансдукции последовательностей нуклеиновых кислот в культивируемые клетки, в частности, применимы в способе по настоящему изобретению. Такие ретровирусы к тому же применимы для эффективной трансдукции последовательностей нуклеиновых кислот в клетки in vivo. Ретровирусы широко применялись для передачи материала нуклеиновой кислоты в клетки. Методики получения дефектных по репликации ретровирусов (в том числе стадии включения экзогенного материала нуклеиновой кислоты в плазмиды, трансфекцию пакующей линии клеток плазмидами, продукции рекомбинантных ретровирусов пакующей линией клеток, сбор вирусных частиц из среды тканевой культуры и инфицирование вирусными частицами клеток мишени) хорошо известны в данной области.
Преимущество использования ретровирусов для генной терапии состоит в том, что вирусы вставляют последовательность нуклеиновой кислоты, кодирующую требуемый белок, в геном клетки-хозяина, тем самым позволяя передачу последовательности нуклеиновой кислоты, кодирующей искомый белок, потомству клетки при её делении. Промоторные последовательности в области LTR могут повысить экспрессию вставленной кодирующей последовательности в различных типах клеток.
Другим вирусным кандидатом, применимым в качестве экспрессирующего вектора для трансформации клеток, являются аденовирусы (Ad), которые представляют собой вирусы с двухцепочечной ДНК. Аденовирусы инфекционны в широком диапазоне типов клеток, включая, к примеру, мышечные и эндотелиальные клетки. Аденовирусы – это вирусы с двухцепочечной линейной ДНК и геномом в 36 т.о. Некоторые особенности аденовирусов сделали их полезными в качестве средств доставки трансгенов для терапевтического применения, как-то облегчение доставки генов in vivo. Рекомбинантные аденовирусные векторы, как оказалось, способны эффективно переносить гены in situ в клетки паренхимы различных органов, включая легкие, мозг, поджелудочную железу, желчный пузырь и печень. Это позволяет использовать эти векторы в способах лечения наследственных генетических заболеваний типа муковисцидоза, где векторы могут быть доставлены в органы мишени.
Подобно ретровирусам, геном аденовирусов можно приспособить для применения в качестве экспрессирующего вектора для генной терапии, то есть путем удаления генетической информации, контролирующей выработку самого вируса. Поскольку аденовирусы функционируют внехромосомно, то у рекомбинантных аденовирусов по теории не может возникать проблема инсерционного мутагенеза.
Для создания рекомбинантных аденовирусов традиционно применялось несколько подходов. Один подход включает прямое лигирование фрагментов, полученных при рестрикции эндонуклеазами, содержащих последовательность искомой нуклеиновой кислоты, с частями генома аденовируса. С другой стороны, искомая последовательность нуклеиновой кислоты может быть вставлена в дефектный аденовирус посредством гомологической рекомбинации. Нужные рекомбинанты идентифицируют при скрининге индивидуальных бляшек, образующихся на посеве из комплементационных клеток.
Примеры подходящих векторов включают ДНК-вирусы (напр., аденовирусы), лентивирусные, аденоассоциированные вирусные (AAV), полиовирусные, векторы на основе HSV или вируса Moloney мышей, вирусные векторы из вируса саркомы Harvey, вируса саркомы Rous, MPSV или гибридные векторы на основе транспозонов. В одном воплощении вектор представлен AAV. AAV представляет собой небольшой непатогенный вирус из семейства Parvoviridae. AAV отличается от других представителей этого семейства своей зависимостью от вируса-хелпера для репликации. Геном AAV примерно в 5 т.о. состоит из одного сегмента одноцепочечной ДНК положительной либо отрицательной полярности. Концы генома представлены короткими инвертированными концевыми повторами, которые могут складываться в шпильковые структуры и служить в качестве начала репликации вирусной ДНК. Физически вирион парвовируса не имеет оболочки, а его икосаэдрический капсид имеет диаметр примерно 20 нм.
На сегодняшний день идентифицировано и выделено много серологически различных AAVs из человека или приматов. Например, геном AAV2 имеет длину в 4680 нуклеотидов и содержит две открытые рамки считывания (ORFs). Левая ORF кодирует неструктурные белки Rep: Rep 40, Rep 52, Rep 68 и Rep 78, которые участвуют в регуляции репликации и транскрипции наряду с продукцией одноцепочечных геномов потомства. Было показано, что Rep 68/78 также обладает NTP-связывающей активностью, а также ДНК- и РНК-геликазной активностью. Белки Rep содержат сигналы ядерной локализации, а также несколько потенциальных сайтов фосфорилирования. Мутация одного из этих киназных сайтов приводит к потере репликационной активности.
Концы генома представлены короткими инвертированными концевыми повторами (ITR), которые могут складываться в T-образные шпильковые структуры, служащие в качестве начала репликации вирусной ДНК. В пределах участков ITR было описано два элемента, которые важны для функционирования ITR: повторяющийся мотив GAGC и сайт концевого разрешением (trs). Повторяющийся мотив, как было показано, связывает Rep, когда ITR находится в линейной либо шпилечной конформации. Это связывание служит для расположения Rep68/78 для расщепления по сайту trs, которое происходит сайт- и ните-специфичным образом. Векторы из AAV имеют несколько особенностей, которые делают их привлекательными для переноса генов, как-то широкий спектр хозяев, способность к трансдукции как делящихся, так и неделящихся клеток in vitro и in vivo, и способность к поддержанию высоких уровней экспрессии трансдуцированных генов.
В некоторых воплощениях вирусным вектором является вектор из AAV. Термин вектор “AAV” относится к аденоассоциированным вирусам и может применяться для обозначения самого природного вируса дикого типа или его производных. Этот термин охватывает все подтипы, серотипы и псевдотипы, а также природные и рекомбинантные формы, за исключением случаев, когда требуется иное. В настоящем изобретении термин “серотип” относится к таким AAV, которые определяются и отличаются от других AAVs по способности капсидного белка к реакции с определенными антисыворотками, напр., существует 8 известных серотипов AAVs у приматов, от AAV1 до AAV8. Например, серотип AAV9 относится к таким AAV, которые содержат белки капсида, кодируемые геном cap AAV9, и геном, содержащий последовательности 5′- и 3′-ITR одного и того же серотипа AAV9. В некоторых воплощениях вектор AAV представлен AAV9.
Сокращение “rAAV” означает рекомбинантный аденоассоциированный вирус, который также называют рекомбинантным вектором AAV (или “вектором rAAV”). В одном воплощении экспрессирующие векторы AAV конструируют известными методами так, чтобы по крайней мере обеспечить в качестве функционально связанных компонентов в направлении транскрипции контролирующие элементы, включая участок инициации транскрипции, искомую ДНК и участок терминации транскрипции. Контролирующие элементы выбирают так, чтобы они были функциональными в клетках млекопитающих. Полученная конструкция, которая содержит функционально связанные компоненты, фланкируется (5′ и 3′) функциональными последовательностями ITR AAV.
Под “инвертированными концевыми повторами аденоассоциированного вируса” или “ITRs AAV” понимаются признанные в данной области участки, находящиеся на каждом конце генома AAV, которые функционируют вместе в cis-положении в качестве начала репликации ДНК и в качестве сигналов упаковки для вируса.
Нуклеотидные последовательности участков ITR AAV известны. В настоящем изобретении “ITRs AAV” не обязательно должны иметь приведенную нуклеотидную последовательность дикого типа, но могут быть изменены, напр., путем вставки, делеции или замены нуклеотидов. Кроме того, ITRs AAV могут происходить из любого из нескольких серотипов AAV, включая, без ограничения, AAV1, AAV2, AAV3, AAV4, AAV5, AAV7 и т.д. Кроме того, 5′- и 3′-ITRs, фланкирующие данную нуклеотидную последовательность в векторе из AAV, не обязательно должны быть одинаковыми или происходить из одного и того же серотипа или изолята AAV, если только они функционируют должным образом, то есть позволяют вырезать и выделить искомую последовательность из генома клеток-хозяев или вектора.
Нуклеиновые кислоты, кодирующие терапевтические композиции, могут быть встроены в вектор AAV стандартными методами лигирования типа тех, что описаны в Sambrook and Russell, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY (2001). Например, лигирование может проводиться в 20 мМ трис-Cl рН 7,5, 10 мМ MgCl2, 10 мМ DTT, 33 мкг/мл BSA, 10 мМ-50 мМ NaCl и либо 40 мкМ АТФ, 0,01-0,02 единиц (Weiss) ДНК-лигазы T4 при 0°C (для лигирования “по липким концам”), либо 1 мМ АТФ, 0,3-0,6 единиц (Weiss) ДНК-лигазы T4 при 14°C (для лигирования “по тупым концам”). Межмолекулярное лигирование “по липким концам” обычно проводится при общей концентрации ДНК в 30-100 мкг/мл (общая концентрация концов 5-100 нМ). Векторы AAV, содержащие ITRs, описаны, напр., в U.S. Pat. No. 5,139,941. В частности, в нем описано несколько векторов AAV, доступных из Американской коллекции типовых культур (“ATCC”) под номерами доступа 53222, 53223, 53224, 53225 и 53226.
В некоторых воплощениях у аденоассоциированных вирусов упаковывается полный геном, то есть примерно такого же размера, как и природный геном, не слишком большой и не слишком маленький. В некоторых воплощениях AAV не является самокомплементарным вектором AAV.
Вирусный вектор также содержит промотор для контролирования транскрипции гетерологичного гена. Промотор может быть индуцируемым промотором для контроля транскрипции терапевтической композиции. Система экспрессии должна подходить для введения млекопитающим-реципиентам.
В некоторых воплощениях вводятся вирусные частицы. Вирусные частицы являются термостабильным, устойчивыми к растворителям, детергентам, изменениям pH и температуры и могут концентрироваться в градиентах CsCl. AAV не связаны с какими-либо патогенными событиями, а трансдукция векторами AAV не оказывала каких-либо продолжительных отрицательных эффектов на рост или дифференцировку клеток. ITRs оказались единственными cis-элементами, необходимыми для упаковки, что позволяет полное извлечение вирусных генов для создания векторных систем.
В некоторых воплощениях настоящим изобретением предусмотрен вектор, содержащий экспрессионную кассету, содержащую промотор, функционально связанный с интересующей последовательностью. “Экспрессионная кассета” в настоящем изобретении означает последовательность нуклеиновой кислоты, способную направлять экспрессию определенной последовательности нуклеотидов в подходящих клетках-хозяевах, которая включает промотор, функционально связанный с искомой последовательностью нуклеотидов, который может быть функционально связан с сигналами терминации. Кодирующая область обычно кодирует заданную функциональную РНК, например, молекулу РНКи. Экспрессионная кассета, включающая в себя искомую последовательность нуклеотидов, может быть химерной.
В некоторых воплощениях настоящего изобретения предусмотрен вектор, кодирующий интересующую молекулу типа выделенной молекулы РНКи. В настоящем изобретении термин “кодируется” применяется в широком смысле, аналогично термину “включающий” в патентной терминологии. К молекулам РНКи относятся миРНК, кшРНК и другие небольшие молекулы РНК, которые способны модулировать экспрессию гена мишени, например, посредством РНК-интерференции. К таким коротким РНК относятся, без ограничения, кшРНК и микроРНК).
Термин “функционально связанный” относится к ассоциации последовательностей нуклеиновых кислот на одном фрагменте нуклеиновой кислоты с тем, что на функцию одной из последовательностей влияет другая. Например, регуляторная последовательность ДНК считается “функционально связанной с” или “ассоциированной с” последовательностью ДНК, кодирующей РНК или полипептид, если две последовательности располагаются таким образом, что регуляторная последовательность ДНК влияет на экспрессию кодирующей последовательности ДНК (то есть кодирующая последовательность или функциональная РНК находится под транскрипционным контролем промотора). Кодирующие последовательности могут быть функционально связаны с регуляторными последовательностями в смысловой или антисмысловой ориентации. Нуклеиновая кислота является “функционально связанной”, если она находится в функциональной взаимосвязи с другой последовательностью нуклеиновой кислоты. Как правило, “функционально связанные” означает, что связанные друг с другом последовательности ДНК являются смежными. Однако энхансеры не должны быть смежными. Связывание осуществляется путем лигирования в подходящих сайтах рестрикции. Если таких сайтов нет, то в соответствии с обычной практикой используются синтетические олигонуклеотидные адаптеры или линкеры. Кроме того, в экспрессирующем векторе могут соединяться множественные копии кодирующих ферменты нуклеиновых кислот. Такие множественные нуклеиновые кислоты могут разделяться линкерами.
“Экспрессия” относится к транскрипции и/или трансляции эндогенного гена или трансгена в клетках. Например, в случае антисмысловых конструкций экспрессия может означать транскрипцию только антисмысловой ДНК. Кроме того, экспрессия означает транскрипцию и стабильную аккумуляцию смысловой (мРНК) или функциональной РНК. Экспрессия также может означать продукцию белка.
“Экспрессионная кассета” в настоящем изобретении означает последовательность нуклеиновой кислоты, способную направлять экспрессию определенной последовательности нуклеотидов в подходящих клетках-хозяевах, которая включает промотор, функционально связанный с искомой последовательностью нуклеотидов, который функционально связан с сигналами терминации. Как правило, она также содержит последовательности, необходимые для правильной трансляции последовательности нуклеотидов. Кодирующая область обычно кодирует нужный белок, но также может кодировать нужную функциональную РНК, к примеру, антисмысловую РНК или нетранслируемую РНК, в смысловой или антисмысловой ориентации. Экспрессионная кассета, содержащая нужную последовательность нуклеотидов, может быть химерной, что означает, что по крайней мере один из её компонентов гетерологичен по отношению к по меньшей мере одному из других её компонентов. Экспрессионная кассета также может иметь природное происхождение, но получена в рекомбинантном виде, применимом для гетерологической экспрессии. Такие экспрессионные кассеты должны содержать участок инициации транскрипции, связанный с нужной последовательностью нуклеотидов. Такая экспрессионная кассета может быть снабжена несколькими рестрикционными сайтами для вставки нужных генов под транскрипционным контролем регуляторных участков. Экспрессионная кассета может дополнительно содержать гены селектируемых маркеров.
Настоящим изобретением также предусмотрены клетки млекопитающих, содержащие описанный здесь вектор. Клетки могут быть клетками человека и могут происходить из мозга, селезенки, почек, легких, сердца или печени. Клетки могут быть представлены популяцией стволовых клеток или клеток-предшественников.
Нуклеиновые кислоты, кодирующие терапевтическую композицию
Настоящим изобретением предусмотрен способ введения терапевтической композиции. В некоторых воплощениях терапевтическая композиция представлена трансгеном, то есть геном, кодирующим полипептид, который является чужеродным для того ретровируса, из которых был изначально получен вектор, и обладает полезной биологической активностью в том организме, в который она вводится (напр., терапевтического гена). В настоящем изобретении термин “терапевтический ген” означает такой ген, экспрессия которого желательна в клетках для обеспечения терапевтического эффекта, напр., для лечения заболевания.
Способы применения
Настоящим изобретением предусмотрен способ лечения нейродегенеративных заболеваний типа генетических заболеваний, таких как болезнь Хантингтона, амиотрофический боковой склероз, наследственная спастическая гемиплегия, первичный боковой склероз, спинальная мышечная атрофия, болезнь Кеннеди, болезнь Альцгеймера, болезнь полиглутаминовых повторов или очаговых поражений типа болезни Паркинсона, путем введения вектора, содержащего описанные выше выделенные промоторы.
Некоторые аспекты изобретения касаются полинуклеотидов, полипептидов, векторов и генетически измененных клеток (модифицированных in vivo) и их применения. В частности, изобретение касается способа генной или белковой терапии, который дает возможность системного введения терапевтически эффективной дозы терапевтического средства.
Далее изобретение будет проиллюстрировано на следующем неограничительном примере.
Пример 1
Для этого эксперимента использовали посмертные образцы ткани мозга человека, полученные от 6 различных пациентов с болезнью Хантингтона или 5 контрольных здоровых лиц, для анализа активности 5 различных промоторов полимеразы 2. Экстрагировали РНК и анализировали ее посредством количественной ПЦР для измерения количества эндогенного РНК-транскрипта, вырабатываемого посредством этих промоторов. У всех пяти промоторов отмечалась значительная положительная регуляция в мозге пациентов с болезнью Хантингтона по сравнению со здоровыми лицами. См. фиг. 1.
Мышей дикого типа и мышей HD забивали в возрасте 6 и 11 недель (до появления симптомов) и 19 недель (с симптомами). Выделяли тотальную РНК из образцов полосатого тела и определяли экспрессию мышиных генов Nfyc, H2afy, Usp31 и Chop методом кПЦР в реальном времени. В возрасте 6 и 11 недель ни один из генов не проявлял положительной регуляции, тогда как в возрасте 19 недель значительно усиливалась экспрессия Nfyc и H2afy. Количество исследованных мышей составляло по 4 на группу. См. фиг. 2A-2C.
Каждую из промоторных последовательностей генов клонировали перед геном-репортером, кодирующим люциферазу светлячков. Эти конструкции подвергали кратковременной экспрессии в культивируемых клетках человека для проверки их транскрипционной активности в исходных условиях. См. фиг. 3.
Конструкции с промоторами, подвергали кратковременной трансфекции в контрольные или полученные при болезни Хантингтона клетки культивируемых фибробластов. При болезни Хантингтона отмечалось повышение активности клонированных промоторных последовательностей генов в фибробластах по сравнению с контрольными фибробластами. См. фиг. 4.
Все публикации, патенты и патентные заявки включены в настоящее описание путем ссылки. Хотя в предшествующем описании настоящее изобретение было описано на определенных предпочтительных воплощениях и многие детали приводились в целях иллюстрации, однако специалистам в данной области должно быть ясно, что изобретение допускает дополнительные воплощения, а некоторые из описанных здесь деталей могут существенно различаться, не отходя от основных принципов изобретения.
Использование форм единственного числа в контексте описания изобретения следует понимать как охватывающее как единственное, так и множественное число, если здесь не указано иначе или явно не противоречит контексту. Термины “включающий в себя”, “имеющий”, “включающий” и “содержащий” следует понимать как открытые термины (т.е. означающие “включая, но не ограничиваясь этим”), если не указано иначе. При этом указание диапазонов значений должно служить всего лишь кратким способом указания по отдельности каждого отдельного значения, попадающего в этот диапазон, если не указано иначе, а каждое отдельное значение включено в описание, как если бы оно было приведено индивидуально. Все описанные здесь способы могут выполняться в любом подходящем порядке, если не указано иначе или же явно не противоречит контексту. Использование всевозможных примеров или приведение здесь типичных выражений (напр., “такой как”) служит всего лишь для лучшего раскрытия изобретения и не накладывает ограничений на объем изобретения, если не заявлено иное. Ни одно выражение в описании не следует понимать как указывающее на какой-нибудь незаявленный элемент как существенный для практического применения изобретения.
Здесь описаны воплощения настоящего изобретения, включая наилучший способ, известный авторам изобретения, для осуществления изобретения. При прочтении вышеприведенного описания рядовым специалистам могут стать очевидными вариации этих воплощений. Авторы изобретения ожидают, что профессионалы будут использовать такие вариации надлежащим образом, а также полагают, что изобретение может осуществляться иначе, чем конкретно описано здесь. Соответственно, настоящее изобретение включает все модификации и эквиваленты тематики, приведенной в прилагаемой формуле изобретения, насколько это разрешается действующим законодательством. Кроме того, изобретение охватывает любые комбинации вышеописанных элементов во всех возможных вариантах, если не указано иначе или же явно не противоречит контексту.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> UNIVERSITY OF IOWA RESEARCH FOUNDATION
<120> PROMOTER COMPOSITIONS
<130> 17023.135WO1
<140> PCT/US2014/021357
<141> 2014-03-06
<150> 61/794,818
<151> 2013-03-15
<160> 7
<170> PatentIn version 3.5
<210> 1
<211> 1622
<212> DNA
<213> Homo sapiens
<400> 1
ggaggtcata tactagttga ttttggacta aaggcatccc aaagatgtac tattttttgc 60
tccctgcact attttttttt taatggaacc aacgtttaaa aataggattt ctgccttctc 120
ttaaaacatc agatgatctg gtaacgctga gctcctgttc tcacatggga acaactggct 180
ggagctgagt ggcagccacc tctttagaaa gatgttaatt tgaagtctgc tatagtcccc 240
atcattcctt atatttcccc caacactgag acccaagtca cttgaaagtc aatatgatga 300
ttcaaacacc aggattcttc actcatttgt gggtttgtga cctgtgatat ttgtggattc 360
gtgacctttg gtttagaggt caagtatagg ggttgtaaat aaaacttggg tttgaatcag 420
ataagaactg taccaatctc aaagacggtg aattaaagat taaagaaaat attgcatgct 480
tggcataatg tgtggaacac aacagctatt gtaaacaccc agtaggaatg taagctgcaa 540
gagggcaggt agaaaccgtg ctaatttaat ccgctgggga tatgacattt gattctaatt 600
taataggttt aattctttgc aatatcccca gtaactgctg aatgaatgag tgagtgaatg 660
aatgaatgga atgatgaatg atgggagagc ccggaggagt tttaaaggct ggaatgaaaa 720
ggaaagtagt tatgataaca gcgtttcgct gggactccaa ggtgcagcca ggaagaaaag 780
cccgctggga cgtgccaggg tctgtgactg cgctccgctg gcacccagag ggtaggtatc 840
tgcaacgtcc cttgggagcc agacagggct gacttgccca ggacctgtca gggccatgtc 900
caccagctct tgcacggtct ggtaactgac agcatcctga ttcctgcacg ttcccgcctc 960
tgccatctga ccagcaaaga cagagaccca ccccggggat ccaccatcca acgggagccc 1020
agccttttcc tccaagccgg gacggcgccc acactagaca tggcctccct cgggcttcac 1080
gcagcaggac cgcgcccgca gcctccaggc atcgcgtccg gctggagagg cagctaccgt 1140
cccacagtga acatggcggc cgaggcggct tcagcgccgg gcgggcggcg ccgggaggca 1200
cgtcacgtga gcggctcagc tgggcggacc gcgcgcgcgc ccgctggccc cgccggccgc 1260
cgctcgctcg ctggctcggc tgcgctttga ggtgtgtggg gcgtcgagcc cccgggcccg 1320
gtgaggcgcg gcgctgcggg atgcggcggc ggccgtggcg gggccgcggg ccgggcgggc 1380
gggcgcggtg atgagtgtct gcggccgccg ccatgtccaa ggtaacggcg cctgggtccg 1440
ggccgccggc ggcggcgagc gggaaggaga agcgctcctt cagcaagcgg ctgtttcgga 1500
gcggccgcgc tggcggcggc ggcgcggggg gccccggggc gtccgggccg gccgcgcctt 1560
cctcgccctc ctcgccctcc tctgcacgct cggtgggcag cttcatgagc cgcgttctca 1620
ag 1622
<210> 2
<211> 630
<212> DNA
<213> Homo sapiens
<400> 2
tgagaagtga gagcctatga acatggttga cacagaggga caggaatgta tttccagggt 60
cattcattcc tgggaatagt gaactgggac atgggggaag tcagtctcct cctgccacag 120
ccacagatta aaaataataa tgttaactga tccctaggct aaaataatag tgttaactga 180
tccctaagct aagaaagttc ttttggtaat tcaggtgatg gcagcaggac ccatcttaag 240
gatagactag gtttgcttag ttcgaggtca tatctgtttg ctctcagcca tgtactggaa 300
gaagttgcat cacacagcct ccaggactgc cctcctcctc acagcaatgg ataatgcttc 360
actagccttt gcagataatt ttggatcaga gaaaaaacct tgagctgggc caaaaaggag 420
gagcttcaac ctgtgtgcaa aatctgggaa cctgacagta taggttgggg gccaggatga 480
ggaaaaagga acgggaaaga cctgcccacc cttctggtaa ggaggccccg tgatcagctc 540
cagccatttg cagtcctggc tatcccagga gcttacataa agggacaatt ggagcctgag 600
aggtgacagt gctgacacta caaggctcgg 630
<210> 3
<211> 1363
<212> DNA
<213> Homo sapiens
<400> 3
ccaagatcag ctcttggagg agtgtagact ttaattccac ctggtggtcc ctacagaacg 60
gagagtcctt gcccaaaggc acagagaagg atggaacaac aatgtggtgt gtgggggagg 120
gtctctgcac ctttcctgac atcttttctt cgggagatcc tcatagaacc ataatgcttt 180
gttttgggac cagaagcatc ataagcatca tcatttttcc agcttcatct cctgttactt 240
tccccttcac ccattctact ccaacctcac actcgctctg tcttgactat tttggacaca 300
ctcctacccc agcctttgca cttgctattc ctcatgctcg gcgcagttct tccccagaca 360
tccacacggc ttgctccctc aatttcttca ggctttaaat gttactttct catagaggcc 420
ttctcttgta tttgagcctc actcttatct cacacttcct attccccttc tccgccttat 480
ttttctccac cccatggaga ccctctgaca cattctcccg tttgtctgtc tttcccccac 540
gagactgcaa actacaggag ggcagagatt tctgcctgtt ctcttggctg tttcatatcc 600
agcacccaaa tcgatgtatg acacaaaata cgttctcagt acttaatcga attaacgaat 660
gcatgaatgg caggtattgg acattgtttt gcaaactctt aaagtaaggt gtaaagcatc 720
ccggtgaggt ggaggttact gccgctgcga ttcccgcgca gcctgaggac tggggggtgg 780
gggtgggggt ctctaattac ctccataatc cccagtagcg gcactttaaa cttcacatca 840
accctgaggg atgtgtatta ttatccaaat ttagttcaca gctggatgga gaagtggctt 900
ccggctccac actttggagg gaggggagta gagggcaggc ccccatttaa gtacccggga 960
tggggcacca atgccttcag gcggtaaacc aatttaggaa gacgtggcgg gctttgtggc 1020
ggctcctcct ctttcggcct gtccgcagtt tttaaaaaac gtgtgtgatg ataaggaatc 1080
actgtctaca ttagtaattc ccaacttggg tccgaaagtg aacttttgct gaagcgaagt 1140
agctaaccgc ttccatgtgc aaggcaggtt ccagacttcg gggtgaggag gattaactga 1200
aggaccccag gggaaccggg tgcgcagtaa ttgatcttgg ggcagaccag ggcttggcgg 1260
tggcctgtat ctaaagacag cggggtctct gaggcggggc aggggggagt tggcattgac 1320
tggggaggga agagcgatcg ctggtaacag ccattgtgcc ttc 1363
<210> 4
<211> 1349
<212> DNA
<213> Homo sapiens
<400> 4
gtgcctgatg tgagatttat tgaaactgga tttgaaaaca attttcctga attcaagtcg 60
agggtttact ccactattct caattacttt atcaccaggg ttataaaccc aaaggaagtg 120
agtaacaaca gtgtgatttt attgaggacc catgcaacac tagtctcaga aaggctccag 180
tgtcatttgt aaaattcaag gttaccatca gcagaggcag tcattcctct ctgcgcttgt 240
tacctaatgc actaactctc actgtaggta attccattca agacacattt gatgactata 300
cctacaggtt ttgaagttat tcggatgggg ttttgacact tactagctgt ggggacttag 360
atcaagttac ttaacctttt tgagcttcag ttttatcatt tgtaaaatgg atacaatcct 420
gatgcctttg gaccaagtgg tcacggaaat gaaagagata agtatgaaaa aatccatgct 480
catagtagct gtggtttcca actgcgtgat aaaactttaa aatctgcatt caaataagaa 540
caactatgtc gacgtaaggt tacaagctaa ctattcttgg taagtactgt tctttattct 600
agaggacatc actttacagt ttggtgctaa atgctctttt atgaatttaa ggtgccagta 660
gctgtctact tgaacggcat gcttaatctg gaacgccatg tcgaccttca tcccccagtt 720
ctttctcccc aaattaaaaa cacaaataca cacacacgcc cctacttagt tcctaaaact 780
caagggcacg cgcacacacc tacttatttc ctaaaattca agctcgcacc aaggagatcc 840
acaaggatag gcagggtggt ggaggtcact gggcagcgcc tccggatccc ccgaaagggg 900
gcggggtcaa aactcagatc tcgagctccc gaaagggggc ggggttaaaa ctctcagatc 960
tcattccgcc tccctctgtc gtcgcccctt cccaattctc gcgagacctc aaggagcaca 1020
gcttctgcgc accgcacgat actgggagtc caggcgccaa gggaggggga agggaaaagg 1080
ggaaacggtg caaacggcgt ggccgccatc ttgcttgtgc ccccgcttcg cgcgcgctcc 1140
gttctccgtg acgcacactt ccccctcccc tccgccgcgc ctgggcctct gcattgcccg 1200
actccgtagg agcgcggggg cggctcctgc tcttcctgga ctcctgagca gaggtgtgtg 1260
agtgtgcggg agtttctgtg cgagggtgat agggaagcgg cggcgggggg aggggcagcg 1320
cttcccgcct tcgccagaga cctcacttc 1349
<210> 5
<211> 1059
<212> DNA
<213> Homo sapiens
<400> 5
cttttgggag atttacgggg ctagaacagg agaccacccc cgtttttttg tttgtttgtt 60
ttgttttttg tttttggtga aacgtagtct cgctctgtca cccaggctgg agtgcagtgg 120
cgcgatctcg gtcactgcaa catccgcctc cagggttcaa gcgattcttc tgcctctgcc 180
tccagagtag ctgggattac aggcgcgcat caccacaccc ggctaatttt tgtattttta 240
gtagagacgg ggtttcacca tgttggtcag gctgatctcg aactcctgac ctcaagtgat 300
ccgctctcct cagcctccca aagtgctggg attacaggcg taagccactg agcccggcca 360
ggagacctct ttaagaagac tcgagatgtc gacaatccca gtggatggat accaacttta 420
aaaagaaaag ttcaaaaggc ctatgtgccc attagctggg aggggccaag aaatatggga 480
gtcccttata gtgggggtaa aacggcgggt aaagctaggt gggcggaaca gcagcttctg 540
ggggagacaa gcggcaaaga ggctcacgac cgactagggg cgaccaaggc tgatagccgt 600
tggggccgtt gggcgccggg agctggcgcc ccgccctctc tcctctcccc caccctccgc 660
acctcccacc accctcggtg tcccctgcgc gtgcgcgtgc agacaccggt tgccaaacat 720
tgcatcatcc ccgcccccct ttcctcccct ccccccccgc tacactcccc tccgcgcgcg 780
cgcatgactc acccacctcc tccgtgaagc ctcgtgaccc aaagccactt ccgggtccga 840
cactacgtcg accccctagc gagagggagc gacgggggcg gtgccgcggg gctcctgagt 900
ggcggatgcg agggacgggg cggggccaat gccggcgtgc cactttctga ttggtaggtt 960
ttggggtccc gcccctgaga ggagggcaag gccatggtaa aagattacag ccaggcgctc 1020
ccgaggtcag agacttaagt ctaaggcact gagcgtatc 1059
<210> 6
<211> 524
<212> DNA
<213> Homo sapiens
<400> 6
taataacaac atatctgaaa aagacgcttt aaaatcccat ttatgaaagc ataaaaatag 60
ttagaaataa atttaaccat aaaggtgaaa tatttgtata ccgataacta taaacctttg 120
ataaaaaaag ttgaagaaga cacatataaa tagaataata ttctgtgttc atgaatcaaa 180
aaatttaaca atgttaaaat gtctgtatta accaaagcaa tatacaaatt caatgcaatt 240
tctatcaaaa tttcaaggat atgcatcaca gaaatagaaa aaaaattctt gaaattcata 300
tggaaccaca gacacataaa aacagaatag gcaaaggaac aatgagaaag caaaacaaag 360
cttgaggcat cacacttcct aagttaaaat tatattgcaa agctacagta atcaaaaaca 420
gtatacaaat ggcatgaaaa cgaaaatgtg gaccaacgga acagaatata gagagccaga 480
aacttaacta attttcaaca agggtaccaa caggacaccc tgaa 524
<210> 7
<211> 952
<212> DNA
<213> Homo sapiens
<400> 7
atttccacca gcaacacaca agggttccag tttctccaca tcttcaccaa cacttgtggt 60
tttgcttttt ggtaatagcc atgctaatgg gtgtgaacaa gaagtgcttt aagcatctcc 120
taaagcggaa gaaactgagg cccagagaag ggaagaatca cacgagagat tgaggtcaca 180
agcaagtcag tgatagagca ggacctggaa gctggatccc ctaaccccag cctagttctt 240
gctactaaaa cccaaaatcc agtttccatt gctatatgtc agagggtgca cagccatggc 300
cacaggccag atacagactt taagtttatt tggtttgatc cttactttct ttttttttta 360
attcaaaata gtatcaacat ttaaaaatta ggggatttta tattttaaaa gtctaaattt 420
ctgatttctc ccctcaaaaa tcagaaggtc tggtaaccct tgacccacat tctaactcag 480
caaccaacta ttactgtctt ttgttttgtt ttgttctgtt gagacaaggt cttgttctgt 540
cacccaggct ggagtacggt ggcgtgatca cggctcactg cagtcttgaa ctcctgggct 600
caagcaagcc ccccgtcttg gcctcccaaa gctctgggat tacaggtgtg agcccacgcc 660
cagccctatc attctgtaat atccttccac acaggctagt tcacacactg gctggtcctg 720
gtaacactgg agtttgcagc cctttgcttt tcacatccat agatattcct cattctgagt 780
gtcagtagac acatagttac gtgtaacatc ataggcaggt tccatacttc tttcctcttt 840
cctttactct atattgtctt tgaatatctt agctatttcc tcaccataaa agtgaaataa 900
tgttgcaaat aaatagtgca aaatattaac aaagacacaa ttgaatagcc tg 952
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2015 |
|
RU2711147C2 |
| ВАРИАНТ СРЕДСТВА ДЛЯ RNAi | 2018 |
|
RU2789647C2 |
| ВЕКТОРНЫЕ КОМПОЗИЦИИ С МОДИФИЦИРОВАННЫМ АДЕНОАССОЦИИРОВАННЫМ ВИРУСОМ | 2013 |
|
RU2679843C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ МОЗГА | 2014 |
|
RU2664471C2 |
| Синергетическое действие SMN1 и miR-23a при лечении спинальной мышечной атрофии | 2021 |
|
RU2839898C2 |
| ОПТИМИЗИРОВАННЫЕ ГЕНЫ И ЭКСПРЕССИОННЫЕ КАССЕТЫ CLN1, И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2764919C2 |
| Нуклеиновая кислота, имеющая промоторную активность, и ее применение | 2022 |
|
RU2818112C2 |
| Кодон-оптимизированная нуклеиновая кислота, которая кодирует белок SMN1, и ее применение | 2020 |
|
RU2742837C1 |
| МИНИ-БЕЛОК USH2A, НУКЛЕИНОВАЯ КИСЛОТА, КОДИРУЮЩАЯ МИНИБЕЛОК USH2A, И СОДЕРЖАЩИЙ ЕЕ ЭКСПРЕССИОННЫЙ ВЕКТОР ДЛЯ ГЕННОЙ ТЕРАПИИ | 2023 |
|
RU2822884C1 |
| НУКЛЕАЗА PaCas9 | 2018 |
|
RU2706298C1 |
Группа изобретений относится к области генной терапии. Предложена экспрессионная кассета для лечения болезни Хантингтона, содержащая промотор, состоящий из нуклеиновой кислоты длиной от 500 до 1700 нуклеотидов, которая по меньшей мере на 98% идентична полинуклеотидной последовательности из по меньшей мере 500 нуклеотидов в SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 7. Промотор функционально связан с заданным сегментом ДНК, содержащим терапевтический ген, кодирующий белок или гетерологичный РНК-транскрипт. Также предложены экспрессионный вектор, трансформированная клетка млекопитающих, содержащая экспрессионную кассету или экспрессионный вектор, способ ее получения. Применение экспрессионной кассеты для экспрессии терапевтического гена при возникновении или при патологическом прогрессировании болезни Хантингтона активирует и/или усиливает экспрессию указанного терапевтического гена. 6 н. и 14 з.п. ф-лы, 4 ил., 1 пр.
1. Экспрессионная кассета для лечения болезни Хантингтона, содержащая промотор, состоящий из нуклеиновой кислоты длиной от 500 до 1700 нуклеотидов, которая по меньшей мере на 98% идентична полинуклеотидной последовательности из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 7, где промотор функционально связан с заданным сегментом ДНК, содержащим терапевтический ген, кодирующий белок или гетерологичный РНК-транскрипт, где промотор активирует и/или усиливает экспрессию указанного терапевтического гена при возникновении или при патологическом прогрессировании болезни Хантингтона.
2. Экспрессионная кассета по п. 1, где нуклеиновая кислота имеет по меньшей мере 99% идентичности с полинуклеотидной последовательностью из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 7.
3. Экспрессионная кассета по п. 2, где нуклеиновая кислота имеет 100% идентичности с полинуклеотидной последовательностью из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 1, SEQ ID NO: 2 или SEQ ID NO: 7.
4. Экспрессионная кассета по п. 1, где нуклеиновая кислота длиной от 1500 до 1700 нуклеотидов имеет по меньшей мере 98% идентичности с полинуклеотидной последовательностью из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 1.
5. Экспрессионная кассета по п. 1, где нуклеиновая кислота длиной от 600 до 800 нуклеотидов имеет по меньшей мере 98% идентичности с полинуклеотидной последовательностью из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 2.
6. Экспрессионная кассета по п. 1, где нуклеиновая кислота длиной от 900 до 1700 нуклеотидов имеет по меньшей мере 98% идентичности с полинуклеотидной последовательностью из по меньшей мере 500 нуклеотидов, представленной в SEQ ID NO: 7.
7. Экспрессионная кассета по любому из пп. 1-6, где заданный сегмент ДНК содержит ген селектируемого маркера или ген-репортер.
8. Экспрессионная кассета по любому из пп. 1-6, где указанный терапевтический ген кодирует молекулу РНКи.
9. Экспрессионный вектор, включающий в себя экспрессионную кассету по любому из пп. 1-7.
10. Экспрессионный вектор по п. 9, где вектор представляет собой аденоассоциированный вирусный (AAV) вектор.
11. Трансформированная клетка млекопитающих, содержащая экспрессионную кассету по любому из пп. 1-6 или экспрессионный вектор по п. 9 или 10 для экспрессии указанного заданного сегмента ДНК, кодирующего указанный терапевтический ген, где если клетка млекопитающих является клеткой человека, то эта клетка из мозга, селезенки, почек, легких, сердца или печени.
12. Трансформированная клетка млекопитающих по п. 11, где клетка млекопитающих представлена клеткой человека.
13. Способ получения трансформированных клеток млекопитающих, включающий стадии (i) введения в клетки млекопитающих рекомбинантной ДНК, содержащей экспрессионную кассету по любому из пп. 1-6, и (ii) идентификации или отбора линии трансформированных клеток млекопитающих.
14. Способ по п. 13, где рекомбинантная ДНК экспрессируется с тем, чтобы придать характерный фенотип трансформированным клеткам млекопитающих.
15. Способ по п. 13, где трансформированные клетки млекопитающих проявляют значительное повышение экспрессии сегмента ДНК при введении в клетки млекопитающих, полученные от пациентов с болезнью Хантингтона, по сравнению с клетками млекопитающих, полученными от контрольных индивидов.
16. Трансформированная клетка млекопитающих, содержащая экпрессионную кассету по любому из пп. 1-7 для экспрессии сегмента ДНК, где сегмент ДНК экспрессируется таким образом, чтобы придать характерный фенотип трансформированным клеткам млекопитающих или чтобы обеспечить существенное усиление экспрессии гена-репортера у трансформированной клетки млекопитающих, где если клетка млекопитающих является клеткой человека, то эта клетка из мозга, селезенки, почек, легких, сердца или печени.
17. Экспрессионный вектор по п. 9 или 10, используемый для экспрессии указанного терапевтического гена для лечения болезни Хантингтона у млекопитающих.
18. Трансформированная клетка по п. 16, используемая для экспрессии указанного терапевтического гена для лечения болезни Хантингтона у млекопитающих.
19. Трансформированная клетка по п. 11, используемая для экспрессии указанного терапевтического гена для лечения болезни Хантингтона у млекопитающих.
20. Применение экспрессионной кассеты по любому из пп. 1-6 для экспрессии указанного терапевтического гена при возникновении или при патологическом прогрессировании болезни Хантингтона.
| MASSONE S | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Механический грохот | 1922 |
|
SU41A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| RIBAN ET AL: "Gene therapy in epilepsy", | |||
Авторы
Даты
2021-02-05—Публикация
2014-03-06—Подача