Изобретение относится к медицине, а именно к экспериментальной онкологии, и касается способа трансплантации скаффолда из сплава титана с заселенной культурой опухолевых клеток в нижнюю челюсть иммунодефицитных мышей для получения ортотопической модели опухолевого процесса в костях и мягких тканях нижнечелюстной и шейной области, позволяющей наиболее адекватно повторить клиническую картину туморогенеза.
Достижением последних десятилетий в клинической практике является трансплантация тканей и органов, выращенных из культур клеток на специальных подложках - скаффолдах. Данный способ считается более совершенным по сравнению с имплантацией эндопротезов, не способных к сращиванию с окружающими тканями. Соответствие характеристик трансплантируемых клеток микроокружению в организме реципиента и форма имплантата, организованная при помощи скаффолда, позволяют ему максимально точно повторить восполняемый орган или его часть. Скаффолды благодаря своей пористой структуре способны надежно закрепляться выращиваемым на них клеткам, а также окружающей ткани реципиента, в том числе и костной, которая врастает в поровое пространство (см. Vacanti J.P., Vacanti С.А. The history and scope of tissue engineering, in principles of tissue engineering // Academic Press. - 2000. - P. 3-8).
Подобные конструкции должны обладать определенной внешней формой и внутренней структурой (см. Yang S., Leong K.F., Du Z., Chua C.K. The design of scaffolds for use in tissue engineering. Part I. traditional factors // Tissue Eng. - 2001. - 7(6). - P. 679-689; см. Hollister S., Lin C., Saito E., Schek R., Taboas J., Williams J. Engineering craniofacial scaffolds // Orthod Craniofac Res. -2005. - 8(3). - P. 162-173).
Существует опыт применения имплантатов из керамики и полимеров (см. Chang B.S., Lee С.K., Hong K.S., Youn H.J., Ryu H.S., Chung S.S. Osteoconduction at porous hydroxyapatite with various pore configurations // Biomaterials. - 2000. - 21(12). - P. 1291-1298; см. Nagashima Т., Ohshima Y., Takeuchi H. Osteoconduction in porous hydroxyapatite ceramics grafted into the defect of the lamina in experimental expansive open-door laminoplasty in the spinal canal // Nippon Seikeigekagakkai Zasshi. - 1995. - 69(4). - P. 222-230). Однако они не обладают достаточной жесткостью и могут легко трансформироваться (см. Kalita S.J., Bose S., Hosick H.L., Bandyopadhyay A. Development of controlled porosity polymer-ceramics composite scaffolds via fused deposition modeling // Mater Sci Eng (C). - 2003. - 23. - P. 611-620; см. Zhang R., Ma P.X. Poly(a-hydroxyl acids)/hydroxyapatite porous composites for bone-tissue engineering. I. Preparation and morphology // J Biomed Mater Res. - 1999. - 44. - P. 446-155).
По этой причине наиболее распространенными материалами для скаффолдов и эндопротезов являются сплавы из титана (см. Lueck R.A., Galante J.O., Rostoker W., Ray R.D. Development of an open pore metallic implant to permit attachment to bone // Surg Forum. - 1969. - 20. - P. 456-457; см. Welsh R.P., Pilliar R.M., Macnab I. Surgical implants. The role of surface porosity in fixation to bone and acrylic // J Bone J Surg Am. - 1971. - 53(5). - P. 963-977.).
Титановые сплавы обладают значительными преимуществами благодаря их механическим свойствам в сравнении с другими металлами, высокому индексу прочности, их химической иннертности, коррозионной стойкости и совместимостью с живыми тканями (см. Liu X.Y., Chu Р.K., Ding С.Х. Surface modification of titanium, titanium alloys, and related materials for biomedical applications // Mater Sci Eng R Rep. - 2004. - 47: 49e121; см. Geetha M., Singh A.K., Asokamani R., Gogia A.K. Ti based biomaterials, the ultimate choice for orthopaedic implants e a review // Prog Mater Sci. - 2009. - 54: 397e425). Исследования in vitro биосовместимости титановых подложек показали не только их нетоксичность, но и положительное влияние на клетки: клеточную адгезию, пролиферацию, дифференциацию и миграцию (см. Lia J.P., Wijna J.R., Blitterswijka С.A., Groota K. Porous Ti6A14V scaffold directly fabricating by rapid prototyping: Preparation and in vitro experiment // Biomaterials. - 2006. - 27. - P. 1223-1235).
Известен способ трансплантации крысам скаффолдов из TA6V, содержащего костные морфогенетические белки ВМР-2 и культуру миобластов С2С12, между мышцами и апоневротическим слоем (см. Guillot R., Gilde F., Becquart P., Sailhan F., Lapeyrere A., Logeart-Avramoglou D., Picart C. The stability of BMP loaded polyelectrolyte multilayer coatings on titanium // Biomaterials. - 2013. - 34: 5737e5746). Преимуществом этого способа является покрытие скаффолда костными морфогенетическими белками, вызывающими остеиндукцию. Недостатком метода является имплантация скаффолда в мышечном слое без какого-либо закрепления, из-за чего трансплантант может во время мышечной работы перемещаться, вызывая болевые ощущения и мешая быстрому заживлению послеоперационной раны и сращению с окружающими тканями.
Известен способ трансплантации скаффолда цилиндрической формы с первичными мышиными остеобластами МС3Т3-Е1 в просверленное отверстие диафизарной части бедренной кости кролика (см. Fu Q., Hong Y., Liu X., Fan H., Zhang X. A hierarchically graded bioactive scaffold bonded to titanium substrates for attachment to bone // Biomaterials. - 2011. - 32. - 7333e7346). Преимущество данного способа заключается в надежной фиксации скаффолда. Данная модель наиболее проста и не способна продемонстрировать тканезамещение в наиболее сложных по форме костях.
Известен способ трансплантации скаффолда с заселенными мышиными остеобластами МС3Т3-Е1 в нижнюю челюсть кроликов, в которой предварительно был сделан прямоугольный дефект (см. Cao Н., Fenga L., WuaZh., Houb W., Li Sh., Hao Y., Wua L. Effect of low-intensity pulsed ultrasound on the biological behavior of osteoblasts on porous titanium alloy scaffolds: An in vitro and in vivo study // Materials Science and Engineering. - 2017. - С 80. - P. 7-17; Feng L., Liu X., Cao H., Qin L., Hou W., Wu L. A Comparison of 1- and 3.2-MHz Low-Intensity Pulsed Ultrasound on Osteogenesison Porous Titanium Alloy Scaffolds An In Vitro and In Vivo Study // J Ultrasound Med. - 2019. - 38. - P. 191-202). При этом скаффолд вкладывался в полученное углубление кости без закрепления, что является ненадежным способом фиксации имплантируемого материала.
Существенным недостатком перечисленных выше способов является создание либо аллогенной модели, либо ксеногенной, но с мышиными клетками, а не человеческими. Подобные модели не способны адекватно отражать процессы, протекающие в организме человека. Эту задачу способны решать ксеногенные модели с использованием скаффолдов и человеческих культур клеток, в том числе и опухолевых - с целью моделирования опухолевого процесса в различных тканях.
Техническим результатом предлагаемого изобретения является разработка способа трансплантации скаффолда из сплава титана с заселенной культурой опухолевых клеток в нижнюю челюсть иммунодефицитных мышей для получения ортотопической модели опухолевого роста в костях и мягких тканях нижнечелюстной и шейной области мышей, наиболее адекватно отражающей клиническую картину развития злокачественных новообразований в данной анатомической области у человека.
Технический результат изобретения достигается тем, что разрез кожи производят параллельно телу нижней челюсти на протяжении 15 мм, начало разреза расположено на средней линии тела на расстоянии 5 мм от нижней губы, отодвигая анатомическим пинцетом подкожную мышцу шеи, осуществляют тупое выделение жевательной мышцы, которую рассекают параллельно телу нижней челюсти, при помощи хирургического бура производят повреждение надкостницы и верхнего слоя костной ткани тела нижней челюсти диаметром 2 мм и глубиной 1 мм в области жевательного гребня, прошивают лигатурой скаффолд из сплава титана с заселенной культурой опухолевых клеток и обвивают этой же лигатурой тело нижней челюсти, завязывают узел, сшивают разрезанную жевательную мышцу одним узловым швом, ушивают послеоперационную рану непрерывным швом.
Способ осуществляют следующим образом.
Предварительно скаффолд заселяют необходимой культурой опухолевых клеток человека, после чего инкубируют в стандартных условиях (в СО2-инкубаторе при температуре плюс 37°С).
Реципиентами опухолевого материала являются иммунодефицитные мыши Balb/c Nude.
Для осуществления трансплантации животных вводят в наркоз. Для этого используют в качестве премедикации ксилазин концентрацией 20 мг/мл. Мышей наркотизируют при помощи золетила концентрацией 22,57 мг/мл.
Для обеспечения доступа к нижней челюсти делают разрез кожи параллельно телу нижней челюсти на протяжении 15 мм. Разрез начинается на средней линии тела на расстоянии 5 мм от нижней губы. Отодвигая анатомическим пинцетом подкожную мышцу шеи, осуществляют тупое выделение жевательной мышцы. Последнюю рассекают параллельно телу нижней челюсти. С помощью хирургического бура повреждают надкостницу и верхний слой костной ткани тела нижней челюсти диаметром 2 мм и глубиной 1 мм в области жевательного гребня. Скаффолд из сплава титана с заселенной культурой опухолевых клеток прошивают лигатурой, которой также обвивают тело нижней челюсти, завязывают узел. Разрезанную жевательную мышцу сшивают одним узловым швом. Послеоперационную рану ушивают непрерывным швом.
Изобретение иллюстрируется фигурами (1-7).
На Фиг. 1 изображено повреждение надкостницы и верхнего слоя костной ткани тела нижней челюсти иммунодефицитной мыши Balb/c Nude при помощи хирургического бура.
На Фиг. 2 показано обвитие лигатурой тела нижней челюсти иммунодефицитной мыши Balb/c Nude.
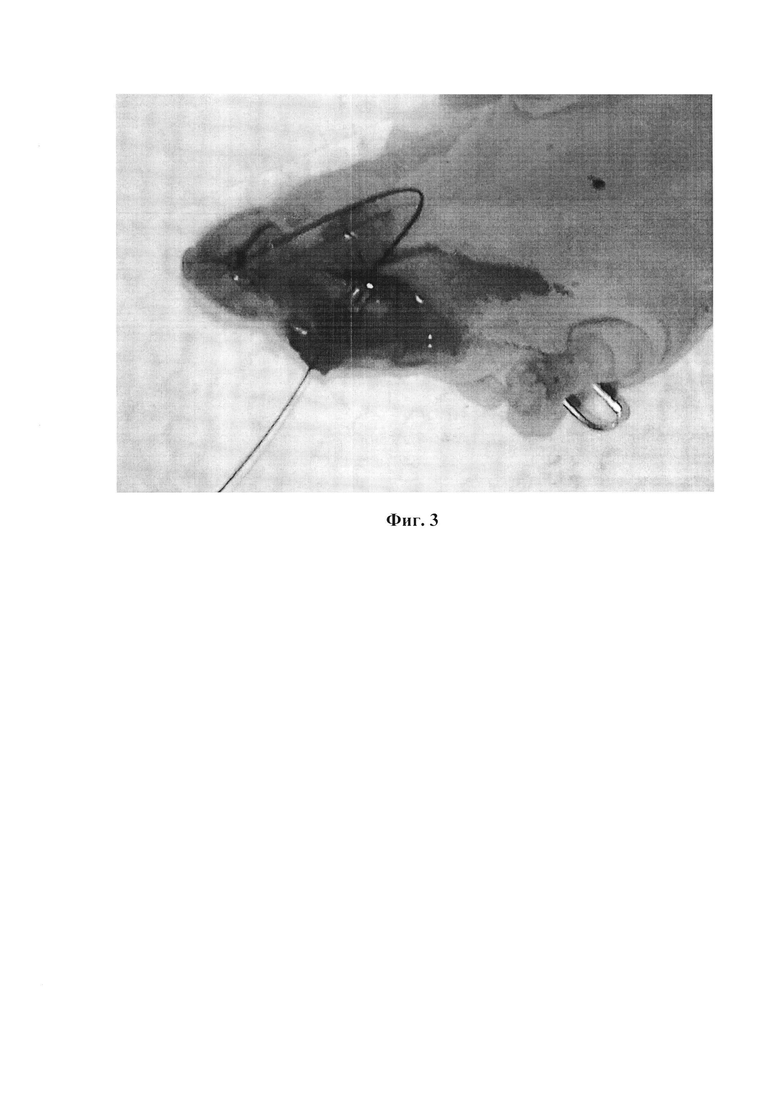
На Фиг. 3 изображено расположение скаффолда из сплава титана с заселенной культурой опухолевых клеток на нижней челюсти иммунодефицитной мыши Balb/c Nude.
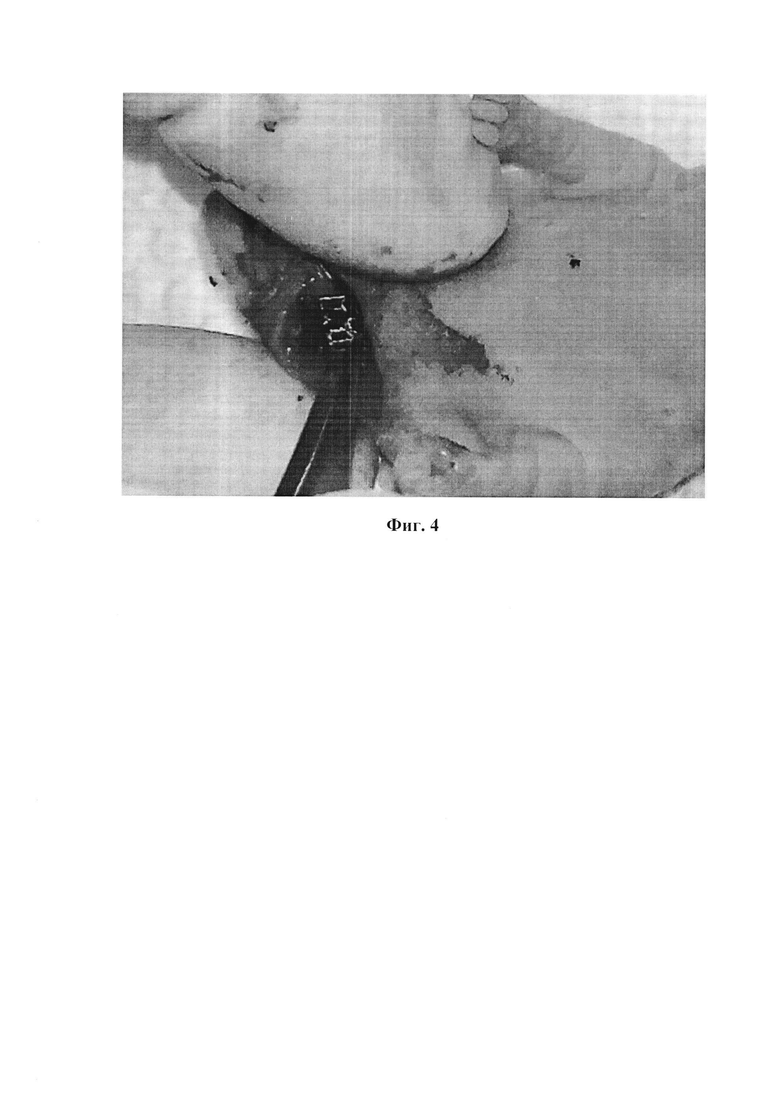
На Фиг. 4 изображена фиксация скаффолда из сплава титана с заселенной культурой опухолевых клеток на теле нижней челюсти иммунодефицитной мыши Balb/c Nude при помощи лигатуры.
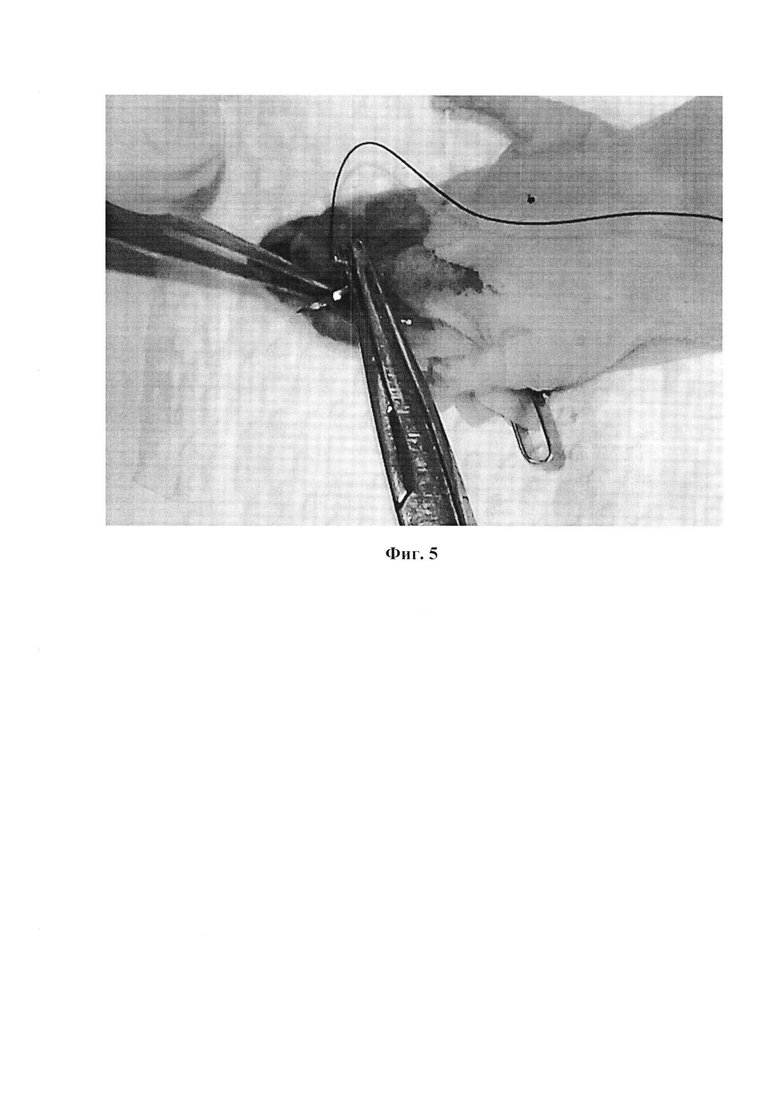
На Фиг. 5 показано ушитие жевательной мышцы иммунодефицитной мыши Balb/c Nude.
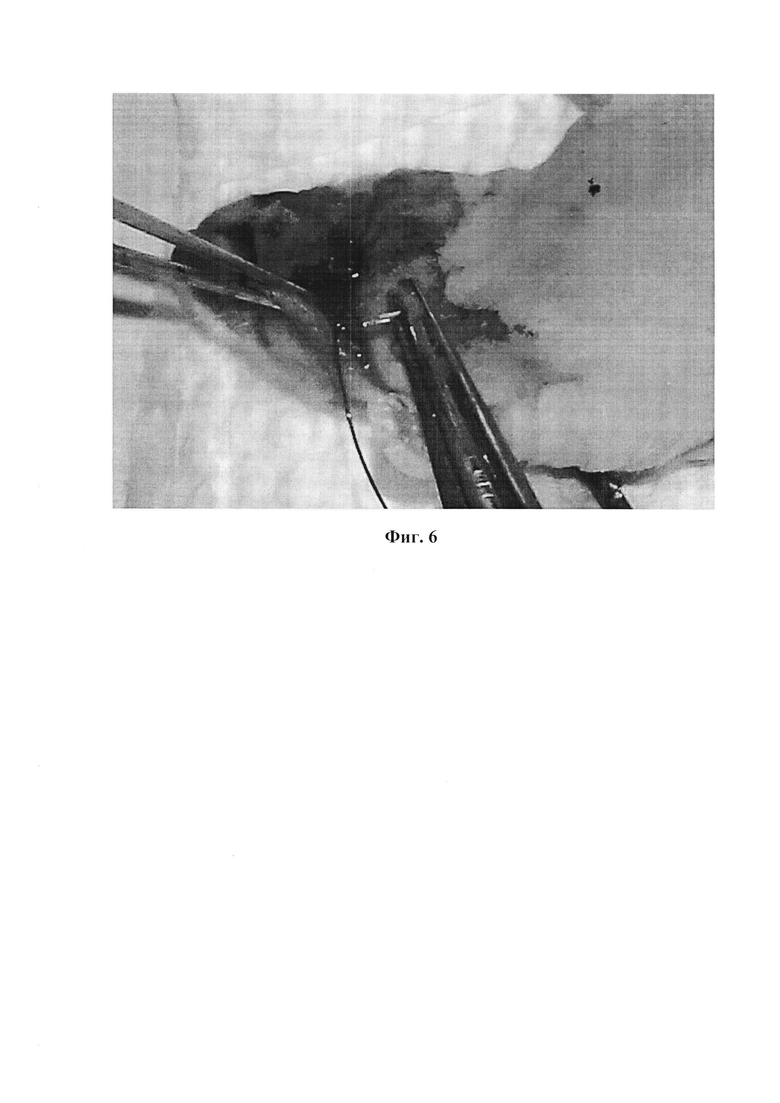
На Фиг. 6 изображено ушитие послеоперационной раны у иммунодефицитной мыши Balb/c Nude.
На Фиг. 7 изображен финальный вид иммунодефицитной мыши Balb/c Nude после трансплантации скаффолда из сплава титана с заселенной культурой опухолевых клеток.
Данным способом произведена трансплантация скаффолдов из сплава титана с заселенной культурой опухолевых клеток в нижнюю челюсть 30 иммунодефицитным мышам Balb/c Nude.
Приводим пример применения способа.
Данным способом была прооперирована самка мыши линии Balb/c Nude возрастом 7 недель массой 23 г.
Скаффолд заселили культурой клеток остеосаркомы человека HOS, после чего инкубировали их в стандартных условиях (в СО2-инкубаторе при температуре плюс 37°С) в течение 3 суток.
Наркоз животного осуществляли с использованием ксилазина концентрацией 20 мг/мл и золетила концентрацией 22,57 мг/мл. Для обеспечения доступа к нижней челюсти разрезали кожу мыши параллельно телу нижней челюсти на протяжении 15 мм. Разрез начинался на средней линии тела на расстоянии 5 мм от нижней губы. Отодвигая анатомическим пинцетом подкожную мышцу шеи, осуществили тупое выделение жевательной мышцы, которую рассекали параллельно телу нижней челюсти. Используя хирургический бур, повредили надкостницу и верхний слой костной ткани тела нижней челюсти диаметром 2 мм и глубиной 1 мм в области жевательного гребня. Скаффолд из сплава титана с заселенной культурой опухолевых клеток прошивали лигатурой, которой также обвивали тело нижней челюсти, завязали узел. Разрезанную жевательную мышцу сшивали одним узловым швом. Послеоперационную рану ушивали непрерывным швом.
Технико-экономическая эффективность данного способа заключается в том, что он позволяет создать ортотопическую модель злокачественного роста в костях и мягких тканях нижнечелюстной и шейной области, трансплантируя опухолевые клетки в костную ткань, и исключает элиминацию опухолевого материала, создавая оптимальные условия для роста имплантируемых клеток.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА ОПУХОЛИ ТОЛСТОЙ КИШКИ ЧЕЛОВЕКА В СЛЕПУЮ КИШКУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2020 |
|
RU2727868C1 |
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА НЕЙРОЭНДОКРИННОЙ ОПУХОЛИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА В ПОДЖЕЛУДОЧНУЮ ЖЕЛЕЗУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2019 |
|
RU2725273C1 |
| Способ трансплантации фрагмента опухоли толстой кишки человека в нисходящий отдел толстой кишки иммунодефицитных мышей | 2020 |
|
RU2753144C1 |
| СПОСОБ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ КУЛЬТУРЫ ОПУХОЛЕВЫХ КЛЕТОК ПИЩЕВОДА ЧЕЛОВЕКА В ШЕЙНЫЙ ОТДЕЛ ПИЩЕВОДА ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2019 |
|
RU2713798C1 |
| Способ имплантации углеродного имплантата на основе аморфного углерода в бедренную кость мыши линии Balb/c | 2022 |
|
RU2799127C1 |
| Способ создания ксенографта рака пищевода внутригрудной локализации на иммунодефицитных мышах | 2020 |
|
RU2738308C1 |
| Способ доступа к телу желудка иммунодефицитных мышей при ортотопической трансплантации фрагмента опухоли желудка человека | 2022 |
|
RU2790950C1 |
| Способ создания ортотопической модели саркомы мягких тканей человека, прорастающей в кость, на иммунодефицитных мышах линии BALB/C NUDE | 2023 |
|
RU2818462C1 |
| СПОСОБ СОЗДАНИЯ ОРТОТОПИЧЕСКОЙ МОДЕЛИ САРКОМЫ МЯГКИХ ТКАНЕЙ ЧЕЛОВЕКА, ПРОРАСТАЮЩЕЙ В ТРУБЧАТУЮ КОСТЬ, НА ИММУНОДИФИЦИТНЫХ МЫШАХ ЛИНИИ BALB/C NUDE | 2024 |
|
RU2838798C1 |
| Способ получения ортотопической PDX-модели плоскоклеточного рака пищевода человека для исследования лучевой терапии в эксперименте | 2021 |
|
RU2760084C1 |



Изобретение относится к медицине, а именно к экспериментальной онкологии, и может быть использовано для трансплантации скаффолда из сплава титана с заселенной культурой опухолевых клеток в нижнюю челюсть иммунодефицитных мышей для получения ортотопической модели опухолевого процесса в костях и мягких тканях нижнечелюстной и шейной области. Способ включает наркоз иммунодефицитных мышей, рассечение кожи и мышц нижней челюсти, послойное ушитие послеоперационной раны. Разрез кожи производят параллельно телу нижней челюсти на протяжении 15 мм. Начало разреза расположено на средней линии тела на расстоянии 5 мм от нижней губы. Отодвигая анатомическим пинцетом подкожную мышцу шеи, осуществляют тупое выделение жевательной мышцы, которую рассекают параллельно телу нижней челюсти. При помощи хирургического бура производят повреждение надкостницы и верхнего слоя костной ткани тела нижней челюсти диаметром 2 мм и глубиной 1 мм в области жевательного гребня. Прошивают лигатурой скаффолд из сплава титана с заселенной культурой опухолевых клеток и обвивают этой же лигатурой тело нижней челюсти. Завязывают узел, сшивают разрезанную жевательную мышцу одним узловым швом, ушивают послеоперационную рану непрерывным швом. Способ обеспечивает создание адекватной клинической картины туморогенеза, позволяет создать ортотопическую модель злокачественного роста в костях и мягких тканях нижнечелюстной и шейной области, трансплантируяопухолевые клетки в костную ткань, и исключает элиминацию опухолевого материала, создавая оптимальные условия для роста имплантируемых клеток за счет использования скаффолда из сплава титана с заселенной культурой опухолевых клеток. 5 ил.
Способ трансплантации скаффолда из сплава титана с заселенной культурой опухолевых клеток в нижнюю челюсть иммунодефицитных мышей, включающий наркоз иммунодефицитных мышей, рассечение кожи и мышц нижней челюсти, послойное ушитие послеоперационной раны, отличающийся тем, что разрез кожи производят параллельно телу нижней челюсти на протяжении 15 мм, начало разреза расположено на средней линии тела на расстоянии 5 мм от нижней губы, отодвигая анатомическим пинцетом подкожную мышцу шеи, осуществляют тупое выделение жевательной мышцы, которую рассекают параллельно телу нижней челюсти, при помощи хирургического бура производят повреждение надкостницы и верхнего слоя костной ткани тела нижней челюсти диаметром 2 мм и глубиной 1 мм в области жевательного гребня, прошивают лигатурой скаффолд из сплава титана с заселенной культурой опухолевых клеток и обвивают этой же лигатурой тело нижней челюсти, завязывают узел, сшивают разрезанную жевательную мышцу одним узловым швом, ушивают послеоперационную рану непрерывным швом.
| СПОСОБ ТРАНСПЛАНТАЦИИ ФРАГМЕНТА ОПУХОЛИ ТОЛСТОЙ КИШКИ ЧЕЛОВЕКА В СЛЕПУЮ КИШКУ ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2020 |
|
RU2727868C1 |
| СПОСОБ ОРТОТОПИЧЕСКОЙ ТРАНСПЛАНТАЦИИ КУЛЬТУРЫ ОПУХОЛЕВЫХ КЛЕТОК ПИЩЕВОДА ЧЕЛОВЕКА В ШЕЙНЫЙ ОТДЕЛ ПИЩЕВОДА ИММУНОДЕФИЦИТНЫХ МЫШЕЙ | 2019 |
|
RU2713798C1 |
| Митрошин А | |||
| Н | |||
| и др | |||
| Современные представления о применении скаффолдов в регенеративной медицине (обзор литературы) // Известия ВУЗов | |||
| Поволжский регион | |||
| Медицинские науки | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Топочная решетка для многозольного топлива | 1923 |
|
SU133A1 |
| Li J, Wen J, Li B, Li W, Qiao W, Shen J, Jin W, Jiang X, Yeung KWK, Chu PK | |||
| Valence State | |||
Авторы
Даты
2021-02-10—Публикация
2020-09-30—Подача