[001] Изобретение относится к способу получения кислотных гидроксидов и оксидов циркония, композиций, содержащих кислотные гидроксиды и оксиды циркония, а также к использованию этих гидроксидов и оксидов при изготовлении катализаторов и сорбентов.
[002] УРОВЕНЬ ТЕХНИКИ
[003] Благодаря хорошо известным амфотерным свойствам, гидроксид циркония обладает высокой способностью селективной адсорбции широкого ряда различных токсичных анионов, таких как фосфаты и арсенаты.
[004] Оксиды циркония, как со стабилизаторами, так и без них, находят применение в различных каталитических процессах, включая применение катализа в сфере экологии, автомобильной и химической промышленности. Также изучена каталитическая активность ZrO2 в таких имеющих важное значение реакциях, как синтез метанола и других углеводородов из СО и Н2, СО2 и Н2 или дегидратация спиртов.
[005] Гидроксид циркония также широко используют в качестве подложки для металлов. Его вводят в подложки с целью стабилизации металла или повышения устойчивости металла к спеканию. Было обнаружено, что стабилизированный гидроксид циркония, содержащий сульфат- или вольфрамат-ионы, обладает сверхкислотными свойствами, обуславливающими его высокую активность по изомеризации углеводородов или конверсии метанола в углеводороды. Установлено, что введение кремния в гидроксид циркония путем замещения повышает кислотность смешанного оксида, образующегося из гидроксида. Получаемые материалы обладают высокой каталитической активностью при высокой температуре и в настоящее время проходят испытания в качестве многообещающих катализаторов окисления метана для двигателей, работающих на сжиженном природном газе (СПГ). Что касается этой технологической области, ссылки на элементарные формы различных легирующих добавок, как правило, истолковываются как включающие соответствующие оксиды. Так, например, понятие «кремний» охватывает силикат и коллоидный оксид кремния, «вольфрам» включает вольфрамат и т.д.
[006] Коммерческому успеху в области катализа материалы на основе гидроксида циркония обязаны, главным образом, способности изменять свои физические и химические свойства при использовании усовершенствованных способов обработки и введении других стабилизаторов. Благодаря этому возможна тонкая настойка основных параметров подложки катализатора. В разных вариантах применения требуются различные сочетания свойств, однако, наличие большой площади поверхности, характеризующейся высокой термической стойкостью и пористостью, является предварительным требованием для большей части вариантов применения катализаторов. При модификации способа производства, направленной на улучшение морфологии продукта, также наблюдается изменение баланса кислотно-основных свойств. Существенное влияние на эти свойства оказывает и введение легирующих добавок, таких как оксид кремния, алюминий, сульфат, фосфат, молибден, олово, вольфрам, ниобий и титан.
[007] Так, понятно, что пористость является важным, но не решающим критерием эффективности катализатора. Равным образом, существенный вклад в конечные рабочие характеристики катализатора вносит кислотность поверхности, на которую, например, в гидроксиде циркония влияет количество и соотношение конечных и мостиковых ОН-групп. Это означает, что для оценки пригодности катализатора для определенного варианта применения важно определение силы кислотных центров, а также их концентрации и типа (кислота Брэнстеда/Льюиса). Для характеризации кислотных свойств твердой поверхности используют и другие методики, включая визуальное изменение цвета; спектрофотометрию; титрование аминами и т.д.
[008] Адсорбция газообразных оснований, в частности, пиридина, в сочетании с анализом методом инфракрасной (ИК) спектроскопии общепризнана и является обычной практикой определения типа кислоты на поверхности. Для этого имеется две причины. Во-первых, это помогает оценить общую концентрацию кислотных центров на поверхности катализатора, так как количество основания, адсорбированного из газовой фазы, строго соответствует концентрации кислотных центров на твердой поверхности. Во-вторых, различные полосы поглощения ИК излучения, соответствующие образованию различных комплексов, позволяют определить природу активных центров на поверхности оксида циркония.
[009] Другим хорошо известным и широко используемым методом характеризации кислотно-основных центров на поверхности оксида является термопрограммированная десорбция (temperature-programmed desorption - TPD). TPD позволяет определить количество и силу активных центров на поверхности гидроксида циркония, а это имеет решающее значение для понимания и прогнозирования рабочих характеристик катализатора.
[0010] Свойства гидроксидов и оксидов циркония часто жестко определяются способом получения. В WO 2004/096713 описан способ производства оксидов циркония и смешанных оксидов на основе циркония. Способ включает осаждение гидроксида циркония из водного раствора соли циркония посредством реакции со щелочью в присутствии регулируемого количества сульфат-анионов при температуре не более 50°С. Гидроксид затем обжигают, получая, по существу, не содержащий сульфата оксид циркония. В публикации заявки на патент Японии № Н11-292538 и 2000-247641 описано производство гидроксида циркония из основного сульфата циркония путем добавления в суспензию сульфата основания. Однако, способы, представленные в этих документах, не приводят к получению гидроксида циркония с улучшенными, соответствующими настоящему изобретению, параметрами объема пор, размера пор и площади поверхности.
[0011] Улучшенные параметры пористости аморфного гидроксида циркония и способ его производства описаны в WO 2007/088326. Гидроксид характеризуется площадью поверхности, по меньшей мере, 300 м2/г, общим объемом пор, по меньшей мере, 0,70 см3/г и средним размером пор 5 нм - 15 нм. Его получают способом, включающим следующие стадии: (а) приготовление водного раствора, содержащего сульфат-анионы и соль циркония в определенном соотношении, (b) охлаждение раствора до менее, чем 25°С, (c) добавление щелочи с целью осаждения аморфного гидроксида циркония, (d) фильтрация и промывка осажденного гидроксида циркония водой или щелочью с целью удаления остаточных сульфата и хлорида, (e) гидротермическая обработка гидроксида циркония под давлением менее 3 бар изб., и (f) сушка гидроксида циркония.
[0012] Несмотря на улучшенные параметры пористости аморфного материала, описанного в WO 2007/088326, ведутся поиски возможностей для улучшения термостойкости обожженных материалов, синтеза специализированных пористых/кристаллических структур (включая достижение определенного размера пор и содержания фаз) и получения определенных (кислотно-основных) свойств поверхности.
[0013] СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0014] В соответствии с изобретением, им обеспечиваются гидроксиды циркония или оксиды циркония, определяемые в описании аспектов изобретения, изложенных ниже. Во всех аспектах изобретения гидроксиды циркония и оксиды циркония могут быть определены как кислотные. Большая часть кислотных центров гидроксидов циркония и оксидов циркония также может являться льюисовскими кислотными центрами. Это может быть продемонстрировано посредством наиболее интенсивных пиков спектра диффузного отражения с Фурье-преобразованием (DRIFT) для гидроксидов циркония в диапазоне 1700-1400 см-1, лежащих около 1600-1620 см-1 и около 1440-1450 см-1. Более конкретно, гидроксиды циркония и оксиды циркония могут иметь больше льюисовских кислотных центров, чем кислотных центров Брэнстеда. Это может быть продемонстрировано посредством пиков спектра DRIFT, лежащих около 1600-1620 см-1 и около 1530-1550 см-1. В контексте изобретения термин «кислотные центры» используется для указания на кислотные частицы, доступные для реакции. Они могут включать кислотные центры Брэнстеда, т.е., доноры протонов (например, протон на терминальной поверхности ОН-групп, SO3H-групп или других поверхностных групп) и льюисовские кислотные центры, т.е., акцепторы электронов (например, атомы Zr). Оксид циркония или гидроксид циркония могут включать, в пересчете на оксид, до 30% вес., более конкретно, до 16% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан или олово. Следует отметить, что все оксиды циркония и гидроксиды циркония включают, в пересчете на оксид, около 1,5-2% вес. оксида или гидроксида гафния в качестве примеси. Он не включается в количество «случайных примесей», указываемое ниже.
[0015] В соответствии с одним из аспектов изобретения, им обеспечивается гидроксид циркония, включающий, в пересчете на оксид, менее 0,1% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан или олово, при этом, гидроксид циркония является пористым, и в отношении пор с диаметром до 155 нм, по меньшей мере, 70% объема его пор образовано порами диаметром 3,5-155 нм, измеренным методом BJH (Баррета-Джойнера-Халенды). В частности, гидроксид циркония может включать, в пересчете на оксид, менее 0,1% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан, олово, редкоземельный металл или иттрий. Более конкретно, в отношении пор с диаметром до 155 нм, по меньшей мере, 75% объема его пор может быть образовано порами диаметром 3,5-155 нм, измеренным методом BJH. В частности, в отношении пор с диаметром до 155 нм, менее 30% объема его пор может быть образовано порами диаметром менее 3,5 нм, измеренным методом BJH, более конкретно, менее 25%. В контексте изобретения, диаметр пор 3,5-155 нм считается мезопористым/макропористым, а диаметр пор менее 3,5 нм считается микропористым.
[0016] В частности, гидроксид циркония может характеризоваться общим объемом пор, измеренным методом физической адсорбции N2, по меньшей мере, 0,75 см3/г, более конкретно, по меньшей мере, 0,80 см3/г. В частности, гидроксид циркония может характеризоваться средним диаметром пор, по меньшей мере, 6,0 нм, более конкретно, по меньшей мере, 6,5 нм.
[0017] В частности, оксид циркония может включать, по меньшей мере, 80% вес. моноклинной фазы при измерении методом дифракционного рентгеновского анализа (X-ray diffraction - XRD) после обжига при 450°С на воздухе в течение 2 часов, более конкретно, по меньшей мере, 82% вес.
[0018] В частности, гидроксид циркония может характеризоваться кислотным заполнением, по меньшей мере, 1300 мкмоль/г, измеренным по TPD пропиламина. Более конкретно, гидроксид циркония может иметь Тmax менее 365°С, еще более конкретно, менее 360°С, измеренную по TPD пропиламина.
[0019] Этот аспект изобретения также относится к оксидам циркония, которые получены или могут быть получены из гидроксидов циркония, определенных выше, как правило, путем обжига (например, при температуре 450°С или выше). Более конкретно, изобретением обеспечивается оксид циркония, включающий, в пересчете на оксид, менее 0,1% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан или олово, имеющей удельную площадь поверхности, по меньшей мере, 50 м2/г после обжига при 600°С на воздухе в течение 2 часов, более конкретно, по меньшей мере, 52 м2/г. Более конкретно, оксид циркония может включать, в пересчете на оксид, менее 0,1% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан, олово, редкоземельный металл или иттрий. Более конкретно, оксид циркония может характеризоваться кислотным заполнением, по меньшей мере, 100 мкмоль/г, измеренным по TPD пропиламина после обжига при 600°С на воздухе в течение 2 часов. Более конкретно, оксид циркония может характеризоваться общим объемом пор, измеренным методом физической адсорбции N2, по меньшей мере, 0,35 см3/г после обжига при 600°С на воздухе в течение 2 часов. В частности, оксид циркония может характеризоваться средним диаметром пор, по меньшей мере, 25,0 нм после обжига при 600°С на воздухе в течение 2 часов. Более конкретно, оксид циркония может характеризоваться основностью, определяемой по поглощению СО2, по меньшей мере, 14 мкмоль/г при 400-600°С, при измерении методом TPD, еще более конкретно, по меньшей мере, 16 мкмоль/г после обжига при 600°С на воздухе в течение 2 часов.
[0020] Кроме того, этот аспект изобретения также относится к оксиду циркония, включающему, в пересчете на оксид, менее 0,1% вес. легирующей добавки, содержащей один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан или олово, имеющему удельную площадь поверхности, по меньшей мере, 15 м2/г после обжига при 900°С на воздухе в течение 2 часов, более конкретно, по меньшей мере, 16 м2/г. В частности, оксид циркония может характеризоваться общим объемом пор, измеренным методом физической адсорбции N2, по меньшей мере, 0,10 см3/г после обжига при 900°С на воздухе в течение 2 часов. Более конкретно, оксид циркония может характеризоваться средним диаметром пор, по меньшей мере, 26,0 нм после обжига при 900°С на воздухе в течение 2 часов.
[0021] Более конкретно, гидроксид циркония или оксид циркония может быть, в пересчете на оксид, чистым, по меньшей мере, на 98% вес., еще более конкретно, чистым, по меньшей мере, на 99% вес. (исключая упомянутую выше примесь оксида или гидроксида гафния).
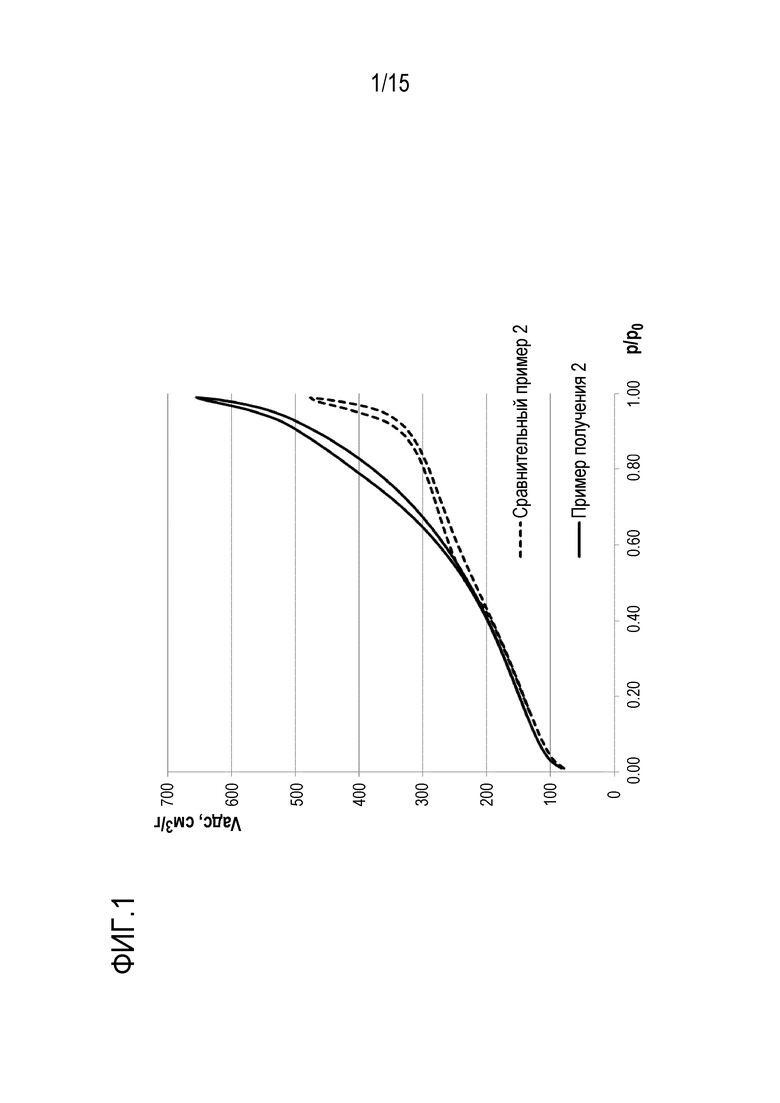
[0022] Гидроксиды циркония или соответствующие обожженные оксиды также имеют такие благоприятные физические характеристики, как большой объем пор, в частности, связанный с порами, размер которых лежит в диапазоне 3,5-50 нм. Кроме того, они могут характеризоваться изотермой адсорбции-десорбции азота IV типа с петлей гистерезиса Н3 с мезопористостью при Р/Р0>0,6.
[0023] В соответствии со вторым аспектом изобретения, им обеспечивается легированный оксид циркония, включающий, в пересчете на оксид, 0,1-30% вес. гидроксида или оксида кремния, при этом, оксид циркония характеризуется поглощением NH3, по меньшей мере, 3,5 мкмоль/м2, измеренным методом TPD, после обжига при 850°С в течение 2 часов. Более конкретно, легированный кремнием оксид циркония может характеризоваться поглощением NH3, по меньшей мере, 4,0 мкмоль/м2, измеренным методом TPD, еще более конкретно, по меньшей мере, 4,25 мкмоль/м2 после обжига при 850°С на воздухе в течение 2 часов. В частности, легированный кремнием оксид циркония может характеризоваться поглощением NH3, по меньшей мере, 330 мкмоль/г, измеренным методом TPD, более конкретно, по меньшей мере, 360 мкмоль/г после обжига при 850°С на воздухе в течение 2 часов. В частности, легированный кремнием оксид циркония может характеризоваться Тmax, по меньшей мере, 280°С, измеренной по TPD NH3, более конкретно, по меньшей мере, 285°С после обжига при 850°С на воздухе в течение 2 часов. Как указано выше, этот оксид может быть получен из соответствующего гидроксида циркония, как правило, путем обжига (например, при температуре 450°С или выше).
[0024] В частности, легированный кремнием оксид циркония может характеризоваться кислотным заполнением, по меньшей мере, 170 мкмоль/г, измеренным по TPD пропиламина, после обжига при 850°С на воздухе в течение 2 часов.
[0025] Кроме того, этот аспект изобретения также относится к легированному кремнием гидроксиду циркония, имеющему удельную площадь поверхности, по меньшей мере, 540 м2/г, общий объем пор, измеренный по физической адсорбции N2, по меньшей мере, 0,90 см3/г и, после обжига при 850°С на воздухе в течение 2 часов, поглощением NH3, по меньшей мере, 3,5 мкмоль/м2, измеренным методом TPD.
[0026] Более конкретно, легированный кремнием гидроксид циркония или легированный кремнием оксид циркония может включать, в пересчете на оксид, 1-10% вес. гидроксида или оксида кремния, более конкретно, 1-5% вес., еще более конкретно, 2,5-4,5% вес. В частности, остальное в легированном кремнием оксиде циркония может составлять, в пересчете на оксид, оксид циркония и случайные примеси в количестве до 0,3% вес.
[0027] В соответствии с третьим аспектом изобретения, им обеспечивается легированный гидроксид циркония, включающий, в пересчете на оксид, 0,1-30% вес. гидроксида или оксида вольфрама с удельной площадью поверхности, по меньшей мере, 400 м2/г. Более конкретно, гидроксид или оксид вольфрама может иметь удельную площадь поверхности, по меньшей мере, 450 м2/г, еще более конкретно, по меньшей мере, 450 м2/г.
[0028] В частности, легированный вольфрамом гидроксид циркония может характеризоваться общим объемом пор, измеренным методом физической адсорбции N2, по меньшей мере, 0,7 см3/г, более конкретно, по меньшей мере, 0,8 см3/г.
[0029] В частности, этот аспект изобретения также относится к легированным вольфрамом оксидам циркония, которые получены или могут быть получены из легированных вольфрамом гидроксидов циркония, описанных выше, как правило, путем обжига (например, при температуре 450°С или выше). Более конкретно, изобретением обеспечивается легированный вольфрамом оксид циркония, включающий, в пересчете на оксид, 0,1-30% вес. гидроксида или оксида вольфрама, характеризующийся поглощением NH3, по меньшей мере, 4,30 мкмоль/м2, измеренным методом TPD после обжига при 700°С на воздухе в течение 2 часов. Более конкретно, легированный вольфрамом оксид циркония может характеризоваться поглощением NH3, по меньшей мере, 420 мкмоль/г, измеренным методом TPD, еще более конкретно, по меньшей мере, 460 мкмоль/г, после обжига при 700°С на воздухе в течение 2 часов.
[0030] В частности, легированный вольфрамом оксид циркония может характеризоваться кислотным заполнением, по меньшей мере, 260 мкмоль/г, более конкретно, по меньшей мере, 280 мкмоль/г, измеренным по TPD пропиламина после обжига при 700°С на воздухе в течение 2 часов.
[0031] Более конкретно, легированный вольфрамом гидроксид циркония или легированный вольфрамом оксид циркония может включать, в пересчете на оксид, 12-20% вес. гидроксида или оксида вольфрама, еще более конкретно, 14-18% вес. В частности, остальное в легированном вольфрамом оксиде циркония может составлять, в пересчете на оксид, оксид циркония и случайные примеси в количестве до 0,3% вес.
[0032] В соответствии с четвертым аспектом изобретения, им обеспечивается легированный гидроксид циркония, включающий, в пересчете на оксид, 0,1-30% вес. сульфата, более конкретно, 1-12% вес., еще более конкретно, 1-10% вес., с удельной площадью поверхности, по меньшей мере, 375 м2/г. Более конкретно, легированный сульфатом гидроксид циркония может иметь удельную площадь поверхности, по меньшей мере, 400 м2/г.
[0033] В частности, легированный сульфатом гидроксид циркония может иметь общий объем пор, измеренный методом физической адсорбции N2, по меньшей мере, 0,50 см3/г, более конкретно, по меньшей мере, 0,60 см3/г. В частности, легированный сульфатом гидроксид циркония может иметь средний диаметр пор, по меньшей мере, 5,5 нм, более конкретно, по меньшей мере, 6,0 нм.
[0034] В частности, этот аспект изобретения также относится к легированным сульфатом оксидам циркония, которые получены или могут быть получены из легированных сульфатом гидроксидов циркония, описанных выше, как правило, путем обжига (например, при температуре 450°С или выше). Более конкретно, изобретением обеспечивается легированный сульфатом оксид циркония, включающий, в пересчете на оксид, 0,1-30% вес. сульфата, характеризующийся поглощением NH3, по меньшей мере, 800 мкмоль/г, измеренным методом TPD, более конкретно, по меньшей мере, 850 мкмоль/г, еще более конкретно, по меньшей мере, 900 мкмоль/г после обжига при 600°С на воздухе в течение 2 часов. В частности, легированный сульфатом оксид циркония может включать, в пересчете на оксид, 1-12% вес. сульфата, более конкретно, 1-10% вес.
[0035] В частности, легированный сульфатом оксид циркония может характеризоваться кислотным заполнением, по меньшей мере, 800 мкмоль/г, более конкретно, по меньшей мере, 900 мкмоль/г, измеренным по TPD пропиламина после обжига при 600°С на воздухе в течение 2 часов.
[0036] Более конкретно, легированный сульфатом оксид циркония может иметь удельную площадь поверхности, по меньшей мере, 140 м2/г после обжига при 600°С на воздухе в течение 2 часов, еще более конкретно, по меньшей мере, 150 м2/г. В частности, оксид циркония может иметь общий объем пор, измеренный методом физической адсорбции N2, по меньшей мере, 0,30 см3/г после обжига при 600°С на воздухе в течение 2 часов, более конкретно, по меньшей мере, 0,32 см3/г. Более конкретно, оксид циркония может иметь средний диаметр пор, по меньшей мере, 8,5 нм, более конкретно, по меньшей мере, 9,0 нм после обжига при 600°С на воздухе в течение 2 часов.
[0037] Настоящее изобретение относится к кислотным гидроксидам циркония и кислотным оксидам циркония, с регулируемыми кислотно-основными свойствами, как в объеме, так и на поверхности.
[0038] В некоторых вариантах осуществления изобретения, легированный кремнием, вольфрамом, сульфатом, фосфатом, ниобием, алюминием, молибденом, титаном или оловом гидроксид или оксид циркония может включать дополнительную легирующую добавку, а именно, предназначенную для стабилизации объемной формы. Дополнительная легирующая добавка может включать гидроксид или оксид редкоземельного элемента или гидроксид или оксид иттрия или гидроксид или оксид любого другого переходного металла, еще не упомянутого. Эта дополнительная легирующая добавка может присутствовать в концентрации, в пересчете на оксид, менее 25% вес., более конкретно, от 0,1 до 25% вес. В частности, общее содержание циркония в гидроксиде циркония или оксиде циркония не должно быть менее 50% вес. в пересчете на оксид. В некоторых вариантах осуществления гидроксиды циркония настоящего изобретения включают менее 5% вес. гидроксида церия, более конкретно, менее 2% вес. гидроксида церия, еще более конкретно, менее 1% вес. гидроксида церия. В некоторых вариантах осуществления изобретения гидроксиды циркония, по существу, не содержат церий.
[0039] Как указано выше, гидроксид циркония или дополнительно стабилизированные или легированные гидроксиды циркония могут быть подвергнуты обжигу до соответствующих оксидов. Эти оксиды также обладают кислотными свойствами, однако, некоторые из них также могут характеризоваться сильной основностью. Температура, при которой проводят обжиг, зависит от легирующей добавки, добавленной в композицию. Для некоторых легирующих добавок слишком высокая температура будет приводить к убыли легирующей добавки в композиции. Например, для композиций, содержащих сульфат, температура обжига должна быть менее 650°С, более конкретно, составлять 400-650°С. Для композиций, содержащих вольфрам, температура обжига должна быть менее 850°С, более конкретно, составлять 400-1000°С, более конкретно, 450-800°С.
[0040] В частности, гидроксиды циркония могут быть, по существу, аморфными при измерении методом XRD. Более конкретно, гидроксиды циркония могут характеризоваться размером частиц d50, измеренным методом спектроскопии лазерного рассеяния, менее 100 мкм, более конкретно, 10-50 мкм.
[0041] Для возможности использования в области катализа или сорбции, описываемые композиции могут включать менее 250 частей на миллион Na и/или менее 250 частей на миллион К, более конкретно, менее 200 частей на миллион, еще более конкретно, менее 125 частей на миллион. В некоторых вариантах осуществления изобретения содержание Na и/или К может быть менее 50 частей на миллион.
[0042] В соответствии с пятым аспектом изобретения, им обеспечивается катализатор, подложка катализатора или сорбент, включающие любой из гидроксидов циркония и/или оксидов циркония, описанных выше.
[0043] В соответствии с дополнительным аспектом изобретения, им обеспечивается способ получения гидроксида циркония, при этом, способ включает стадии, на которых:
(а) соль циркония растворяют в водной кислоте,
(b) в полученный раствор или золь добавляют один или несколько комплексообразующих агентов, при этом, один или несколько комплексообразующих агентов представляют собой органическое соединение, включающее, по меньшей мере, одну из следующих функциональных групп: амин, органосульфат, сульфонат, гидроксил, простой эфир или группу карбоновой кислоты,
(с) нагревают раствор или золь, полученный на стадии (b),
(d) добавляют сульфатирующий агент,
(e) добавляют основание с целью получения гидроксида циркония и
(f) необязательно, добавляют легирующую добавку.
[0044] Когда гидроксиды циркония, необязательно, содержащие легирующую добавку, получают этим способом, образующиеся материалы характеризуются большим процентным содержанием мезопор, чем возможно было достичь ранее. Кроме того, может быть обеспечена повышенная термостойкость, в частности, для нелегированных гидроксидов циркония, обжигаемых при 900°С. Нелегированные гидроксиды циркония также могут характеризоваться более высоким процентным содержанием моноклинной фазы.
[0045] В некоторых вариантах осуществления изобретения соль циркония может представлять собой основный карбонат циркония или гидроксид циркония. В определенных вариантах осуществления изобретения основный карбонат циркония (ZBC) является предпочтительным, так как легко растворяется в минеральных кислотах, выпускается серийно, а образующиеся карбонат-анионы являются нестойкими, следовательно, не затрудняют последующие реакции. Некоторые альтернативные анионы могут оказывать неблагоприятное воздействие на окружающую среду. В некоторых вариантах осуществления изобретения водная кислота может представлять собой соляную кислоту, серную кислоту, азотную кислоту или уксусную кислоту, в частности, водная кислота является азотной кислотой. Без связи с какой-либо теорией полагают, что хотя могут быть использованы другие кислоты, нитрат-ионы, образующиеся из азотной кислоты, особенно хорошо координируются с ионами циркония в водном растворе.
[0046] В частности, на стадии (а) молярное отношение ионов циркония к нитрат-ионам в растворе или золе может составлять от 1:0,8 до 1:2, более конкретно, от 1:0,8 до 1:1,5.
[0047] В контексте изобретения термин «комплексообразующий агент» используется для обозначения лиганда, соединяющегося с цирконием. В некоторых вариантах осуществления изобретения на стадии (b) комплексообразующий агент может являться карбоновой кислотой, дикарбоновой кислотой, альфа-гидроксикарбоновой кислотой, аминокислотой, органосульфатом или многоатомным спиртом. В частности, комплексообразующий агент может быть мультидентатным, в частности бидентатным, лигантом. Многоатомный спирт может представлять собой полисахарид, например, крахмал. В частности, комплексообразующий агент может являться альфа-гидроксикарбоновой кислотой. Как правило, комплексообразующий агент включает полярную группу (т.е., амин, органосульфат, сульфонат, гидроксид, простой эфир или группу карбоновой кислоты), которая координируется с цирконием, и одну или несколько углеводородных групп. В некоторых вариантах осуществления изобретения одна или несколько углеводородных групп может включать один или несколько ароматических заместителей, более конкретно, один или несколько фенильных заместителей. Без связи с какой-либо теорией полагают, что мультидентатные лиганды эффективно координируются с ионами металла. Сочетание различных функциональных групп в одной и той же молекуле может быть благоприятно для взаимодействия с различным координационным окружением на ионе металла, обеспечивая как стерический, так и электронный эффект. Таким образом, в зависимости от природы размера пор и пористой структуры, могут быть использованы комплексообразующие агенты с разными углеводородными группами. Например, альфа-гидроксикарбоновые кислоты могут представлять собой ароматическую (например, фенил-) или неароматическую альфа-гидроксикарбоновую кислоту, более конкретно, миндальную или бензиловую или молочную кислоту, более конкретно, миндальную кислоту.
[0048] В частности, на стадии (а) образовавшийся раствор может быть нагрет. В частности, раствор может быть нагрет до температуры более 25°С, более конкретно, по меньшей мере, до 40°С, еще более конкретно, по меньшей мере, до 50°С, более конкретно, до температуры, лежащей в диапазоне 50-70°С. Более конкретно, раствор может быть нагрет, примерно, до 60°С.
[0049] Необязательно, на стадии (а) рН раствора может быть увеличен (т.е., частично нейтрализован) путем добавления основания. Это увеличение рН также может быть описано как снижение свободной кислотности. В частности, увеличение рН может быть выполнено до нагревания раствора. Более конкретно, основание может представлять собой гидроксид натрия, карбонат натрия, гидрокарбонат натрия, гидроксид аммония, карбонат аммония, гидрокарбонат аммония, гидроксид калия, карбонат калия и/или гидрокарбонат калия.
[0050] В частности, стадия (b) может дополнительно включать добавление в нагретый раствор воды, обычно, деионизированной воды. Более конкретно, на стадии (b) после добавления комплексообразующего агента раствор характеризуется эквивалентным содержанием циркония 5-25% вес. в пересчете на ZrO2, более конкретно, 10-20% вес., еще более конкретно, 12-16% вес. в пересчете на ZrO2. Эквивалентное содержание циркония в пересчете на ZrO2 означает, например, что 100 г 15% по весу раствора будет иметь то же содержание циркония, что и 15 г ZrO2.
[0051] Более конкретно, на стадии (с) нагревание может включать нагревание раствора или золя до температуры 60-100°С, более конкретно, 80-100°С на 1-15 часов. В частности, нагревание может проводиться в течение 1-5 часов. Более конкретно, на стадии (с) температура раствора или золя может быть увеличена со скоростью 0,1-1,5°С/мин. В контексте изобретения указание скорости нагревания включает как линейную (т.е., постоянную) скорость нагревания, так и нелинейную скорость нагревания (например, быстрое начальное нагревание с последующим более медленным нагреванием). Эту стадию нагревания обычно проводят с целью благоприятствования оптимальному размеру полимера/олигомера для приготовления мезопористого порошка.
[0052] В частности, на стадии (d) раствор или золь может быть оставлен для охлаждения или охлажден перед добавлением сульфатирующего агента. Более конкретно, раствор или золь может быть оставлен для охлаждения или охлажден до температуры менее 40°С, более конкретно, менее 30°С. Возможными сульфатирующими агентами являются водорастворимые соли сульфат, бисульфат сульфит, бисульфит. В частности, сульфатирующим агентом может являться серная кислота. Сульфатирующий агент может быть добавлен так, чтобы молярное отношение ионов циркония к сульфат-ионам составляло от 1:0,05 до 1:1. После добавление сульфата на стадии (d) способ может включать стадию отделения твердой фазы от раствора или золя, например, путем фильтрации.
[0053] На стадии (е) рН раствора или золя может быть увеличен до рН>8 путем добавления основания. Основание может представлять собой гидроксид натрия, карбонат натрия, гидрокарбонат натрия, гидроксид аммония, карбонат аммония, гидрокарбонат аммония, гидроксид калия, карбонат калия и/или гидрокарбонат калия. Более конкретно, на стадии (е) добавление основания направлено на образование осадка гидроксида циркония. рН раствора или золя, подучаемый в результате, зависит от используемого основания. В частност-и, основание может быть либо гидроксидом аммония, либо гидроксидом щелочного металла, более конкретно, гидроксидом натрия. Для гидроксида аммония максимальный рН, который может быть достигнут, обычно составляет около рН 10,5-11. Для гидроксидов щелочных металлов рН может быть доведен до рН 11-13 или более.
[0054] Стадия (е) может быть проведена при любой температуре, при которой раствор или золь не замерзает, т.е., от -5°С до 95°С, более конкретно, от 10°С до 80°С.
[0055] В некоторых вариантах осуществления изобретения способ после стадии (е) может включать стадию (f) добавления легирующей добавки. Новизной способа настоящего изобретения является то, что легирующие добавки добавляют после стадии (е), а не осаждают их совместно с гидроксидом циркония на стадии (е). В частности, легирующая добавка может представлять собой любой материал, стабилизирующий тетрагональную фазу оксида циркония, например, как поверхностный стабилизатор или объемный стабилизатор. Эта фаза оксида циркония может обеспечивать улучшенные каталитические свойства. Легирующая добавка также может быть использована для повышения кислотности материала. Более конкретно, легирующая добавка может включать один или несколько из следующих элементов: кремний, сульфат, фосфат, вольфрам, ниобий, алюминий, молибден, титан или олово. Еще более конкретно, легирующая добавка может включать один или несколько из следующих элементов: сульфат, кремний или вольфрам. Сульфат может быть добавлен в форме серной кислоты, сульфата аммония, сульфата натрия или других сульфатов; кремний может быть добавлен в форме оксида кремния, например, водного коллоидного оксида кремния или силиката натрия; вольфрам может быть добавлен в форме вольфрамата, такого как вольфрамат натрия или метавольфрамат аммония. Стадия (f) может быть проведена на любом этапе способа после стадии (е) и перед стадией сушки, описываемой ниже.
[0056] В некоторых вариантах осуществления изобретения способ после стадии (е) и перед или после стадии (f) может включать стадию (g) тепловой обработки гидроксида циркония. Тепловая обработка может представлять собой гидротермическую обработку. Гидротермическая обработка может включать нагревание раствора или золя до температуры 50-250°С, более конкретно, 100-250°С на 0,5-24 часа в автоклаве.
[0057] Более конкретно, между стадиями (е) и (g) и/или после стадии (g) и до или после стадии (f) способ может включать стадии отделения, например, путем фильтрации и промывки гидроксида циркония. Эти стадии могут быть проведены с целью удаления хлорид-ионов, сульфат-ионов, фосфат-ионов, нитрат-ионов, ацетат-ионов, ионов натрия, ионов калия, ионов аммония и/или органического остатка, если это нужно. Для композиций, в которые сульфат или фосфат не добавляли в качестве легирующей добавки, содержание сульфат- или фосфат-ионов может быть снижено до 0,3% вес. или менее, более конкретно, до 0,1% вес. или менее. Содержание натрия, калия и хлорид-ионов может быть снижено до 0,05% вес. или менее, каждого, более конкретно, 0,01% вес. или менее, каждого, еще более конкретно, 0,005% вес. или менее, каждого.
[0058] Затем ионы щелочного металла могут быть удалены на дополнительной стадии повторного суспендирования промытого гидроксида циркония и добавления минеральной кислоты. В частности, минеральная кислота может представлять собой азотную кислоту или серную кислоту, более конкретно, азотную кислоту. Концентрация азотной кислоты может составлять, примерно, от 10% до 60% вес. рН раствора, как правило, доводят до рН менее 9, предпочтительно, до рН 6,5-9. После необязательной дополнительной стадии фильтрации способ может включать необязательную стадию повторного диспергирования осадка в водной среде и нагревания полученной диспергированной суспензии или влажного кека до температуры в диапазоне от 100°С до 350°С, более конкретно, от 100°С до 200°С. Это может быть осуществлено, например, в герметичном реакционном резервуаре, таком как автоклав, или, до 100°С, в открытом резервуаре.
[0059] В некоторых вариантах осуществления изобретения способ после стадии (е) или после стадий (f) или (g), если они проводятся, может включать стадию (h) сушки гидроксида циркония. В частности, это может быть выполнено как сушка в печи, распылительная сушка или вакуумная сушка. Сушка может быть проведена в окислительной, инертной (например, N2) или восстановительной атмосфере. Более конкретно, гидроксид циркония может быть высушен при температуре 50-200°С. Если используется вакуум, температура сушки может лежать на нижнем конце этого диапазона. Без вакуума могут потребоваться температуры, лежащие на верхнем конце диапазона, например, 100-150°С.
[0060] В некоторых вариантах осуществления изобретения способ после стадии (g) или после стадии (е) или (f), если стадия (f) и/или (g) не проводится, может включать стадию (h) обжига гидроксида циркония с получением оксида циркония. Более конкретно, стадия обжига может быть осуществлена при температуре 400-1100°С, более конкретно, 600-850°С. Стадия обжига может проводиться в течение 0,5-15 часов, более конкретно, 2-8 часов, еще более конкретно, 2-3 часов. Стадия обжига может быть осуществлена в любой газообразной атмосфере. В частности, стадия обжига может быть осуществлена в атмосфере неподвижного или проточного воздуха, хотя также может быть использована восстановительная или нейтральная атмосфера. В способе настоящего изобретения воздушная атмосфера, вообще, является предпочтительной, поскольку может способствовать удалению органических соединений. Нейтральная атмосфера, вообще, определяется как атмосфера, которая ни окисляет, ни восстанавливает композицию, находящуюся в этой атмосфере. Это может быть выполнено путем удаления из атмосферы воздуха или удаления кислорода. Дополнительным примером нейтральной атмосферы является атмосфера азота. Кроме того, атмосфера обжига может состоять из газообразных продуктов сгорания, образующихся в отапливаемой газом печи. Время выдержки при температуре может зависеть от термической массы, подвергаемой обжигу, и выбор адекватного времени выдержки при температуре необходим для согласования требуемой степени кристалличности, гомогенности, кислотности и образования микроструктуры твердого материала. После обжига оксид циркония (который может быть легированным) может быть подвергнут формованию или прессованию, например, путем гранулирования, зернения, таблетирования или экструдирования. Эти стадии формования или прессования, необязательно, могут включать добавление связующего.
[0061] Способ может включать необязательную дополнительную стадию дезагрегации или размола гидроксида циркония или оксида циркония. Это может быть выполнено в отношении порошка гидроксида или оксида циркония или в отношении гидроксида или оксида циркония в форме суспензии (т.е., «влажного») в водной или неводной жидкости. Эта стадия может быть осуществлена с использованием известных способов, таких как просеивание, грохочение, размол во встречном потоке воздуха, ударное измельчение, размол в шаровой мельнице, и т.п.
[0062] Изобретение также относится к композициям, которые могут быть получены описанным выше способом, и вариантам использования получаемых материалов, которые включают, помимо прочего, катализаторы, подложки или прекурсоры катализаторов, связующие, функциональные связующие, покрытия и сорбенты.
[0063] Далее изобретение описано со ссылкой на следующие фигуры, которые не подразумевают ограничения объема заявленного изобретения, и на которых:
На фиг. 1 показаны изотермы адсорбции азота для кислотных гидроксидов циркония сравнительного примера 2 и примера получения 2,
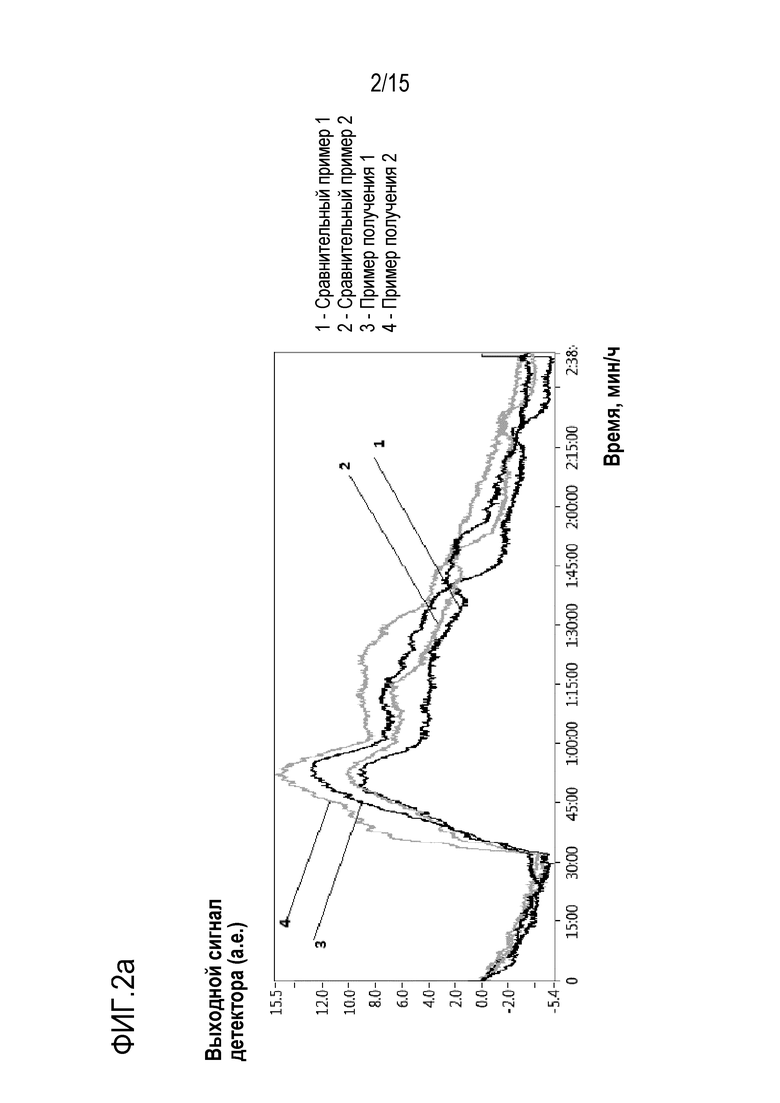
На фиг. 2а показаны профили NH3-TPD для кислотных оксидов циркония сравнительных примеров 1 и 2 и примеров получения 1 и 2 после обжига при 600°С/2 часа,
На фиг. 2b показаны профили CO2-TPD для кислотных оксидов циркония сравнительных примеров 1 и 2 и примеров получения 1 и 2 после обжига при 600°С/2 часа,
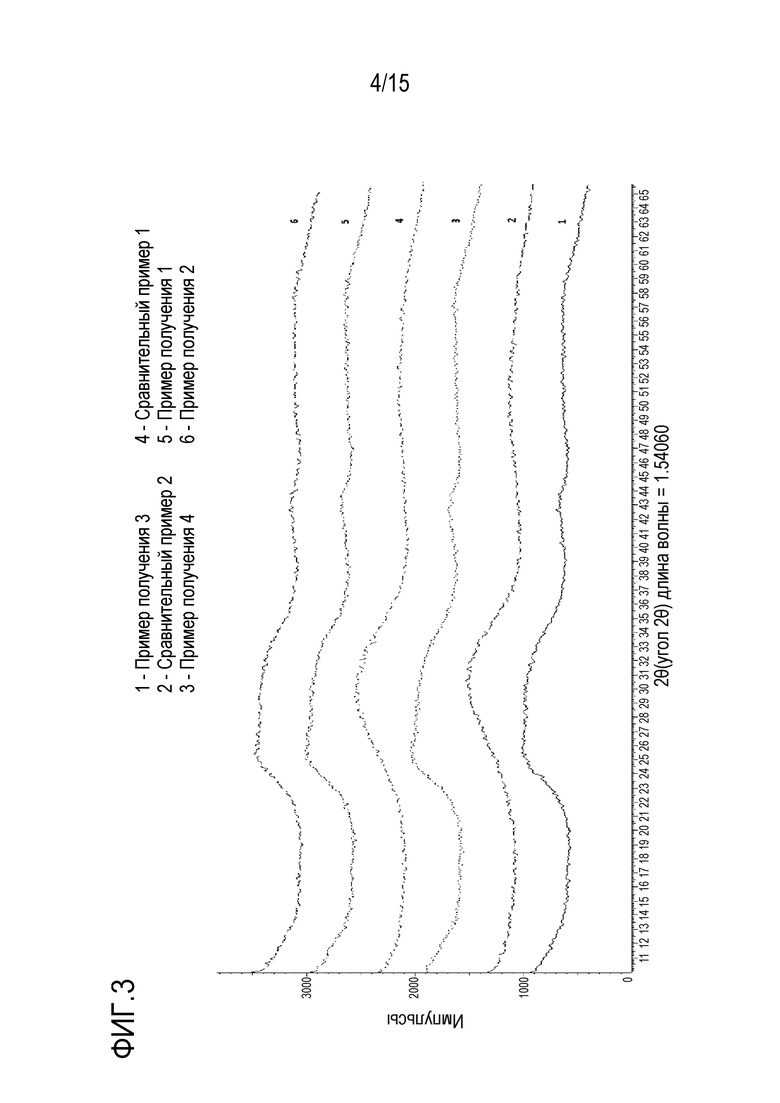
На фиг. 3 приведены данные XRD для кислотных гидроксидов циркония сравнительных примеров 1 и 2 и примеров получения 1-4 после сушки при 110°С,
На фиг. 4 приведены данные XRD для кислотных оксидов циркония сравнительных примеров 1 и 2 и примеров получения 1 и 2 после обжига при 450°С/2 часа,
На фиг. 5 приведены данные TPD-MS, демонстрирующие интенсивность при 41 а.е.м. как функцию температуры для а) свежих материалов сравнительных примеров 1, 2 и 5 и примеров получения 1 и 2; и b) легированных материалов после обжига сравнительных примеров 4 и 8 и примеров получения 5, 6 и 7,
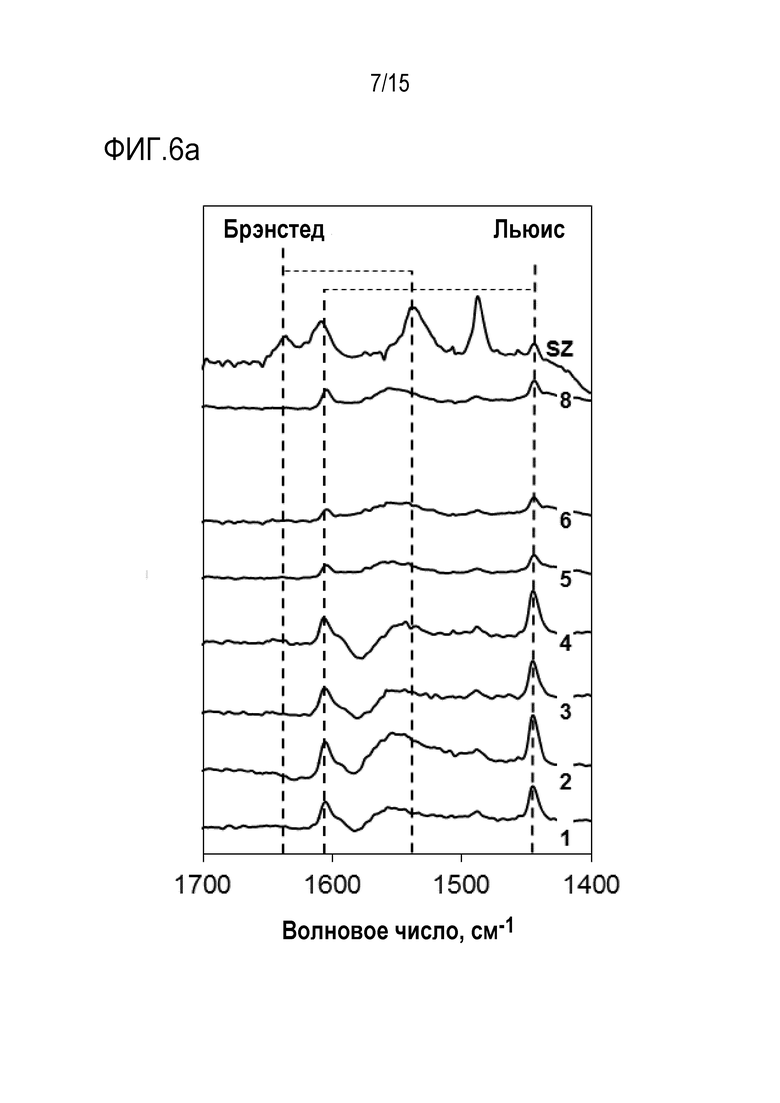
На фиг. 6 представлен спектр DRIFT образцов насыщенного пиридином кислотного оксида циркония, полученных при 100°С in vacuo для а) свежих и обожженных образцов гидроксида циркония примеров получения 1 и 2 и сравнительных примеров 1, 2 и 5; и b) легированных оксидов циркония после обжига примеров получения 5-7 и сравнительных примеров 4, 5 и 8.
На фиг. 7 показаны профили NH3-TPD для стабилизированных вольфрамом оксидов циркония сравнительных примеров 3 и 4 и примеров получения 5 и 8 после обжига при 700°С/2 часа,
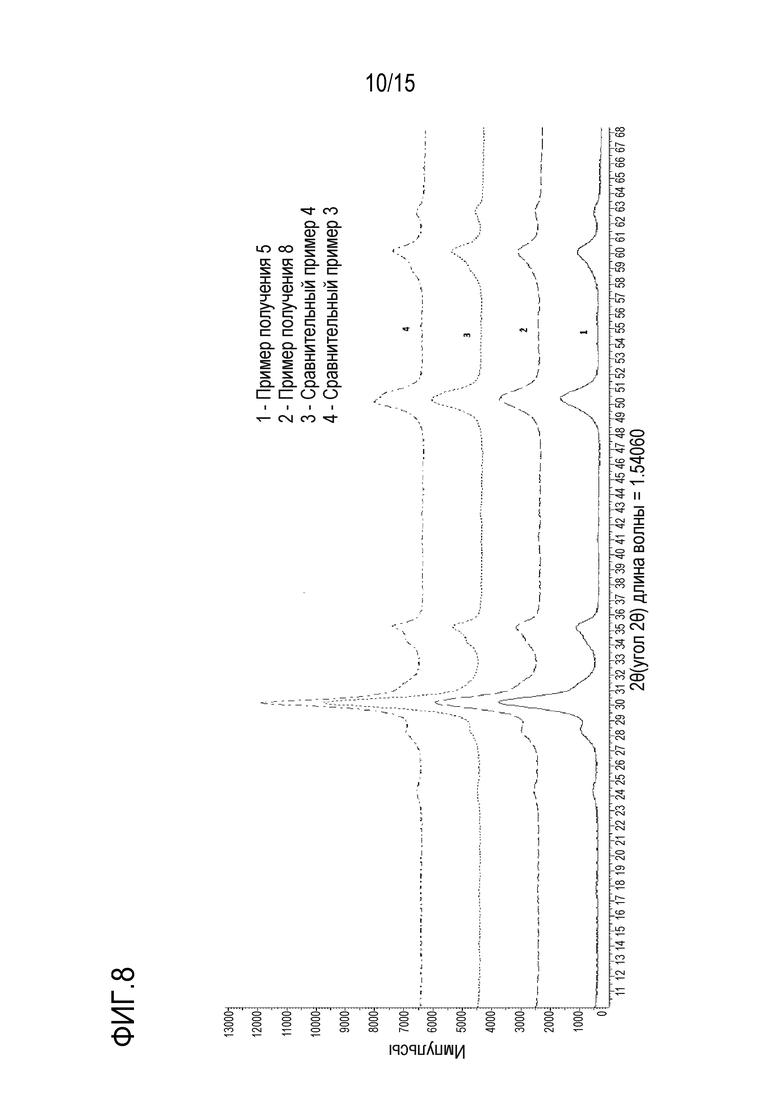
На фиг. 8 приведены данные XRD для стабилизированных вольфрамом оксидов циркония сравнительных примеров 3 и 4 и примеров получения 5 и 8 после обжига при 700°С/2 часа,
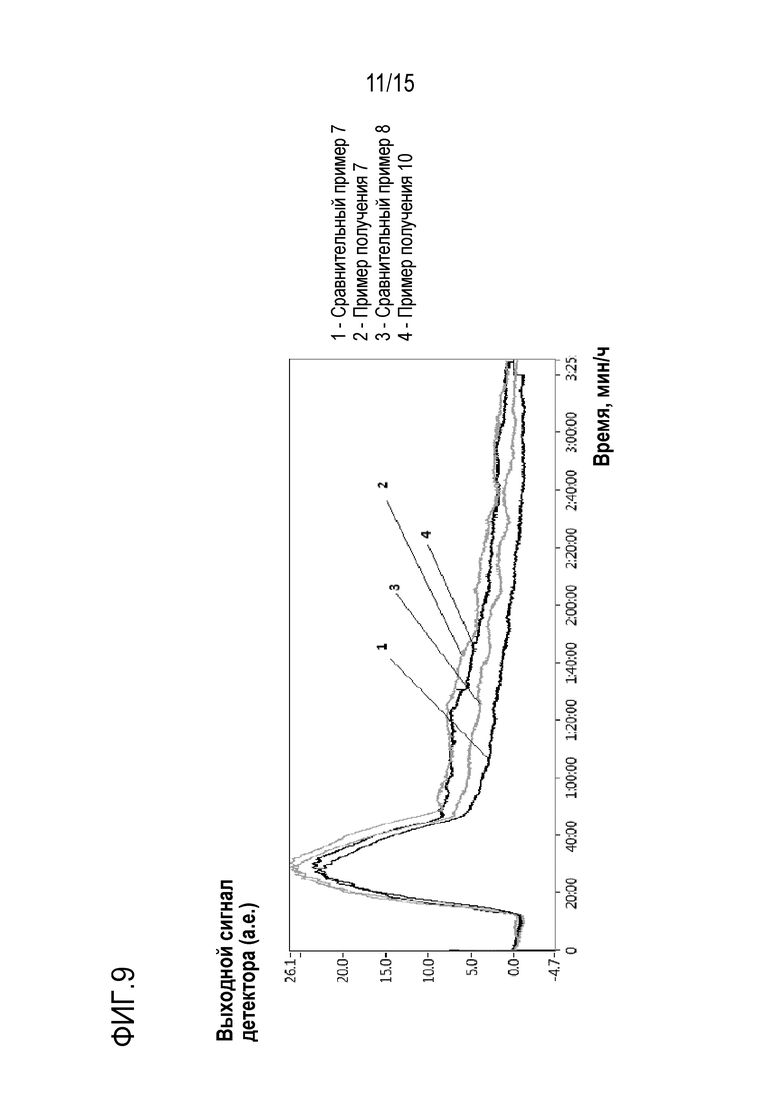
На фиг. 9 показаны профили NH3-TPD для стабилизированных кремнием оксидов циркония сравнительных примеров 7 и 8 и примеров получения 7 и 10 после обжига при 850°С/2 часа,
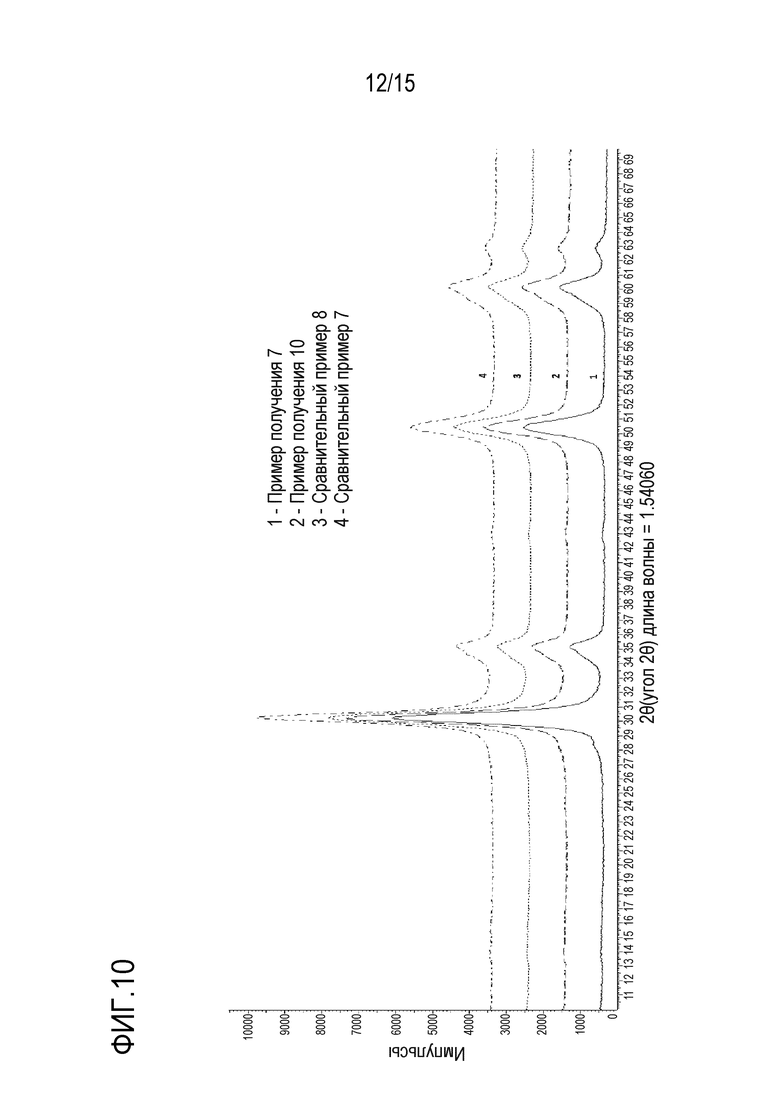
На фиг. 10 приведены данные XRD для стабилизированных кремнием оксидов циркония сравнительных примеров 7 и 8 и примеров получения 7 и 10 после обжига при 850°С/2 часа,
На фиг. 11 показаны профили NH3-TPD для стабилизированных сульфатом оксидов циркония сравнительных примеров 5 и 6 и примеров получения 6, 9, 11 и 12 после обжига при 600°С/2 часа,
На фиг. 12 приведены данные XRD для стабилизированных сульфатом оксидов циркония сравнительных примеров 5 и 6 и примеров получения 6 и 9 после обжига при 600°С/2 часа, и
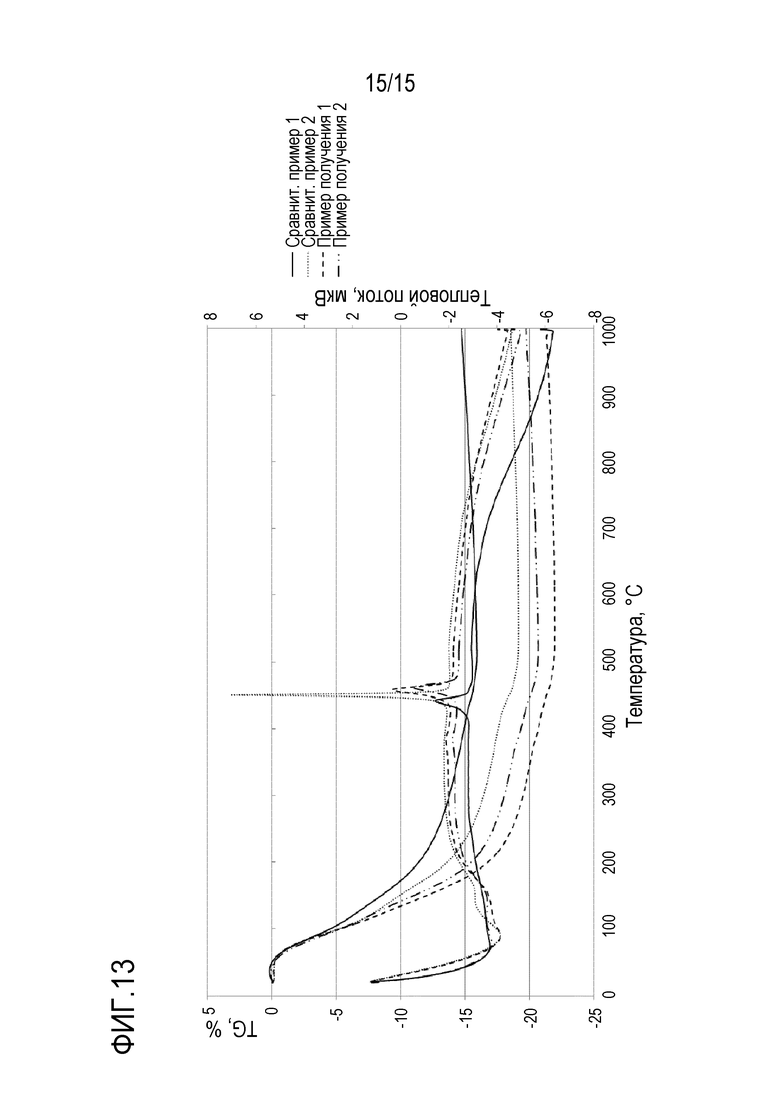
На фиг. 13 показаны профили TG-DTA для кислотных гидроксидов циркония сравнительных примеров 1 и 2 и примеров получения 1 и 2 после сушки при 110°С.
[0064] Далее изобретение описано для примера со ссылкой на нижеследующие примеры.
[0065] Сравнительный пример 1
[0066] Приготовили суспензию основного сульфата циркония в деионизированной воде, содержащую эквивалент 200 г ZrO2. По каплям добавляли 28% вес. водный гидроксид натрия до тех пор, пока рН раствора не достиг 13. Полученный осажденный гидроксид циркония отфильтровали и промыли. Влажный кек повторно суспендировали в деионизированной воде с получением 2000 г суспензии и подвергли гидротермической обработке при 1 бар изб. в течение 1 часа, после чего высушили при 110°С.
[0067] Сравнительный пример 2
[0068] Образец приготовили в соответствии со способом, описанным в патенте ЕР 1984301 В1. То есть, 394,84 г 20% вес. водной серной кислоты, 18,28 г деионизированной воды и 966,18 г оксихлорида циркония (20,7% вес. ZrO2) смешали и охладили до 2°С. Затем по каплям добавляли 10% вес. водный гидроксид натрия до тех пор, пока рН раствора не достиг 8. Затем добавили 28% вес. водный гидроксид натрия с получением рН раствора 13. Образовавшийся осажденный гидроксид циркония отфильтровали и промыли. Влажный кек повторно суспендировали в деионизированной воде и подвергали гидротермической обработке при 1 бар изб. в течение 1 часа, после чего высушили при 110°С.
[0069] Сравнительный пример 3
[0070] Образец приготовили в соответствии со сравнительным примером 1 за исключением того, что перед гидротермической обработкой в 2000 г суспензии добавляли 8% вес. водный раствор вольфрамата натрия до содержания 15,8% вес. WO3 в пересчете на оксид в готовом гидроксиде циркония. рН этой суспензии довели до 6,7 азотной кислотой, полученную суспензию отфильтровали и промыли деионизированной водой.
[0071] Сравнительный пример 4
[0072] Образец приготовили в соответствии со сравнительным примером 2 за исключением того, что перед гидротермической обработкой добавили 328 г 8% вес. водного раствора вольфрамата натрия до содержания 15,8% вес. WO3 в пересчете на оксид в готовом гидроксиде циркония. рН суспензии довели до 6,7 азотной кислотой, полученную суспензию отфильтровали и промыли деионизированной водой.
[0073] Сравнительный пример 5
[0074] Образец приготовили в соответствии со сравнительным примером 1 за исключением того, что перед гидротермической обработкой 390 г влажного кека суспендировали в деионизированной воде и добавили 127,1 г 20% вес. водной серной кислоты до содержания 10% вес. SO3 в пересчете на оксид в готовом гидроксиде циркония.
[0075] Сравнительный пример 6
[0076] Образец приготовили в соответствии со сравнительным примером 2 за исключением того, что перед гидротермической обработкой 977 г влажного кека суспендировали в деионизированной воде и добавили 180,9 г 20% вес. водной серной кислоты до содержания 10% вес. SO3 в пересчете на оксид в готовом гидроксиде циркония.
[0077] Сравнительный пример 7
[0078] К 1761,22 г суспензии, полученной в соответствии со сравнительным примером 1, перед гидротермической обработкой добавили 24,17 г 30% вес. раствора коллоидного оксида кремния (Ludox AS-30). Затем по каплям добавляли водный 28% вес. гидроксид натрия до достижения рН раствора 11. Полученный осажденный смешанный гидроксид циркония отфильтровали и промыли. Влажный кек повторно суспендировали и подвергали гидротермической обработке при 1 бар изб. в течение 5 часов, после чего высушили при 110°С.
[0079] Сравнительный пример 8
[0080] Образец приготовили в соответствии со сравнительным примером 2 за исключением того, что перед гидротермической обработкой 900 г промытого влажного кека суспендировали в деионизированной воде и добавили 22,6 г 30% вес. раствора коллоидного оксида кремния (Ludox AS-30).
[0081] Пример получения 1
[0082] 537,63 г основного карбоната циркония (содержащего 37,2% ZrO2) растворили в 490,81 г разбавленной азотной кислоты (до целевого отношения NO3/Zr 1,2). Этот раствор затем нагрели до 60°С. В раствор добавили 2,759 г миндальной кислоты и 390,8 г воды. Этот раствор нагревали при 94°С 2 часа.
[0083] Полученный раствор смешали с 465,31 г деионизированной воды, затем к смеси добавили 394,84 г 20% вес. водной серной кислоты. рН полученного раствора довели до 13,0 разбавленным раствором гидроксида натрия. Полученную суспензию отфильтровали и промыли. Влажный кек подвергали гидротермической обработке при 1 бар изб. в течение 1 часа, после чего высушили при 110°С.
[0084] Пример получения 2
[0085] 537,63 г основного карбоната циркония (содержащего 37,2% ZrO2) растворили в 490,81 г разбавленной азотной кислоты (до целевого отношения NO3/Zr 1,45). Этот раствор затем нагрели. В раствор добавили 2,759 г миндальной кислоты и 390,8 г воды. Этот раствор нагрели до 94°С.
[0086] Полученный раствор смешали с 564,01 г деионизированной воды, затем к смеси добавили 394,84 г 20% вес. водной серной кислоты. рН полученного раствора довели до 13,0 разбавленным раствором гидроксида натрия. Полученную суспензию отфильтровали и промыли. Влажный кек подвергали гидротермической обработке при 1 бар изб. в течение 1 часа, после чего высушили при 110°С.
[0087] Пример получения 3
[0088] Образец приготовили в соответствии с методикой, описанной в примере приготовления 1, но использовали меньшее количество миндальной кислоты - 1,226 г.
[0089] Пример получения 4
[0090] Образец приготовили в соответствии с методикой, описанной в примере приготовления 2, но использовали меньшее количество миндальной кислоты - 1,226 г.
[0091] Пример получения 5
[0092] Образец приготовили в соответствии с примером получения 1 за исключением того, что перед гидротермической обработкой 1891,2 г суспензии смешали с 258 г 8% вес. водного раствора вольфрамата натрия до содержания 15,8% вес. WO3 в пересчете на оксид в готовом гидроксиде циркония. рН суспензии довели до 6,7 разбавленной азотной кислотой, полученную суспензию отфильтровали и промыли деионизированной водой.
[0093] Пример получения 6
[0094] Образец приготовили в соответствии с методикой, описанной в примере получения 1, за исключением того, что после гидротермической обработки, но перед сушкой добавили разбавленную серную кислоту. Образец затем высушили при 110°С, получив конечное содержание SO3 в пересчете на оксид 10% вес.
[0095] Пример получения 7
[0096] Образец влажного кека гидроксида циркония получили в соответствии с примером получения 1. Перед гидротермической обработкой добавили 12,46 г 30% вес. раствора коллоидного оксида кремния (Ludox AS-30). Образец затем высушили при 110°С, получив конечное содержание SiO2 в пересчете на оксид 3,5%.
[0097] Пример получения 8
[0098] Образец приготовили в соответствии с методикой, описанной в примере получения 5, но использовали другое соотношение исходных реагентов, так что NO3/Zr=1,45.
[0099] Пример получения 9
[00100] Образец приготовили в соответствии с методикой, описанной в примере получения 6, но использовали другое соотношение исходных реагентов, так что NO3/Zr=1,45.
[00101] Пример получения 10
[00102] Образец приготовили в соответствии с методикой, описанной в примере получения 7, но использовали другое соотношение исходных реагентов, так что NO3/Zr=1,45.
[00103] Пример получения 11
[00104] Образец приготовили в соответствии с методикой, описанной в примере получения 1, за исключением того, что до гидротермической обработки в 1812,7 г промытой суспензии рН довели до 6,5 разбавленной серной кислотой. Конечное содержание SO3 в пересчете на оксид составило 6,5% вес.
[00105] Пример получения 12
[00106] 28 г образца, полученного в соответствии с методикой, описанной в примере получения 1, смешали с разбавленной серной кислотой. Затем провели дополнительную сушку при 110°С в течение 3 часов, получив конечное содержание SO3 в пересчете на оксид 10% вес.
[00107] Материалы и методы анализа
[00108] Полученные в различных примерах образцы подвергли анализу в состоянии после получения, некоторые образцы также обжигали при различных температурах в неподвижном воздухе в течение 2 часов в аналитических целях. Содержание Na, определенное методом жидкостной ионообменной хроматографии (Methrom IC 761), во всех случаях было менее 200 частей на миллион.
[00109] Процентное содержание SO3 измеряли при помощи Eltra Carbon Sulfur Analyzer CS800.
[00110] Параметры пористости
[00111] Удельную площадь поверхности, диаметр пор и общий объем пор измеряли по адсорбции жидкого азота при -196°С при помощи Micromeritics TriStar 3020. Перед проведением анализа образцы дегазировали при 90°С под вакуумом 30 мин. Удельная площадь поверхности: Удельную площадь поверхности измеряли методом ВЕТ (Брунауэр-Эммет-Теллер) по нескольким точкам. Общий объем пор: Измерение объема пор проводили во время десорбции при р/р°=0,9814. Распределение пор по размерам и средний диаметр пор: Определение распределения пор по размерам выполняли методом BJH (ветвь десорбции) как «Средняя ширина как функция инкрементного объема пор» в диапазоне от 1,7 до 300 нм. Долю мезо+макро- или микропор в % оценивали на основании графиков размера пор, полученных методом BJH.
[00112] Размер частиц
[00113] Распределение частиц по размерам определяли методом спектроскопии лазерного рассеяния при помощи Microtrac X100 оборудованного блоком ASVR. Для подтверждения достоверности результатов сначала проводили анализ стандартного образца. Блок ASVR автоматически заполнялся до заданного уровня 0,05% дисперсантом Nopcosant K, затем добавляли, приблизительно, 0,100 г сухого образца и 60 сек проводили обработку внутренним ультразвуковым датчиком, установленным на 40 Вт⋅с. Время предварительной циркуляции составляло 30 сек, время измерения - 50 сек. Измерение для образца проводили 3 раза (по теории рассеяния Ми) и получали приводимый далее усредненный результат.
[00114] Термогравиметрический анализ (TGA)
[00115] Эксперименты TG-DTA (термогравиметрический анализ - дифференциально-термический анализ) (измерение потери веса образца (TG) и экзотермического DTA сигнала (например, температуры кристаллизации)) проводили с использованием прибора Setsys-EVO-DTA. 50 мг образца помещали в тигель (100 мкл, Pt) и нагревали до температуры в диапазоне 20-1000°С со скоростью нагревания 10°С/мин в атмосфере 20% О2/Не (расход 20 мл/мин). Проведение эксперимента и анализ данных осуществляли с использованием программного обеспечения Data Acquisition Setsys-1750 CS Evol.
[00116] Дифракционный рентгеновский анализ (XRD)
[00117] Порошковый XRD кристаллографический фазовый анализ материалов на основе оксида циркония проводили при помощи Bruker D8 Advance X-ray diffusion system (программное обеспечение Diffrac. EVA, геометрия Bragg-Brentano, детектор LYNXEYE, Cu излучение (λ=1.5418Å) в диапазоне 2θ от 10° до 70°, 0,015° за один шаг, время шага 0,2 с, Ni фильтр 0,02 мм, прикладываемая мощность 40 мВ/40мА). Количественный фазовый анализ проводили для рентгенограмм образцов оксида циркония при помощи программного обеспечения TOPAS (версия 4.2). Для идентификации пиков использовали эталонные материалы (тетрагональный оксид циркония/моноклинный оксид циркония, поставляемый Bruker). Оценка данных включала поиск пика, ручное/автоматическое устранение фона и сглаживание данных. Определение размера кристаллитов проводили методом Scherrer, К=0,9.
[00118] Потеря веса при прокаливании (LOI)
[00119] Потери веса при прокаливании (Loss over ignition - LOI) определяли при помощи блока Vecsrar в воздушной атмосфере при постоянном потоке. Образцы (2 г) нагревали со скоростью 3°С/мин до заданной температуры (как правило, 1000°С, но для образцов, легированных вольфрамом - до 800°С) и выдерживали при этой температуре, по меньшей мере, 60 мин и до тех пор, пока не наступало постоянство веса во времени.
[00120] Измерение кислотности (для предварительно обожженных образцов)
[00121] NH3/СО2 - термопрограммированная десорбция (TPD) -Измерения проводили при помощи прибора AMI200. 0,2 г образца нагревали от температуры окружающей среды до температуры эксперимента (нелегированные образцы=600°С; сульфатированные=544°С; вольфрамированные=700°С; легированные оксидом кремния=800°С) в потоке аргона (20 мл/мин) со скоростью 20°С/мин. При этой температуре образец выдерживали 45 мин, затем охлаждали до 100°С. Затем над образцом пропускали поток 5% NH3/Не (или 5% СО2/Не) при 100°С в течение 3 мин (20 мл/мин). Образец затем продували гелием при 100°С 1 час с целью удаления из системы неадсорбированного NН3 или СО2 и обеспечения постоянной нулевой линии для детектора теплопроводности (thermal-conductivity detector - TCD). Эксперимент TPD проводили при температуре от 100°С до максимальной температуры эксперимента при 10°С/мин в потоке гелия (20 мл/мин) и времени выдерживания 2 часа. Поглощение NH3 и СО2 фиксировали в соответствии с выходным сигналом TCD. Количественный анализ осуществляли на основании импульсной калибровки, при этом, серию импульсов известного объема (527 мкл) 5% NH3/He или 5% СО2/Не инжектировали в поток гелия-носителя и фиксировали выходной сигнал TCD.
[00122] Адсорбция полиамина/термогравиметрический анализ/масс-спектрометрия (TGA-MS) -Этот анализ осуществляли путем воздействия на образцы полиамином в течение ночи. Избыток полиамина удаляли при помощи вакуума при 30°С, затем проводили термопрограммированную десорбцию при помощи Mettler Toledo TGA/DSC 2 STARe System, оборудованной масс-спектрометром Pfeiffer Vacuum ThermoStarTM GSD 301 T3. Число кислотных центров рассчитывали на основании потери веса в диапазоне температуры 200-800°С, принимая во внимание изменение веса чистых образцов.
[00123] Внешняя адсорбция пиридина - Этот анализ проводили, пропитывая образцы чистым пиридином. Избыток пиридина удаляли в вакуумной печи при 30°С в течение ночи. Образцы затем разбавляли (10% вес. в KBr) и загружали в моделирующую окружающую среду ячейку, оборудованную ИК-спектрометром диффузного отражения с Фурье-преобразованием (diffuse reflectance infrared Fourier transform - DRIFT). Перед проведением измерений образцы подвергали дополнительной сушке под вакуумом при 100°С в течение 15 мин для удаления влаги, физически адсорбированной во время воздействия воздуха.
[00124] Результаты испытаний
[00125] Результаты испытаний представлены в таблицах 1-7, размещенных ниже. В таблицах показано следующее:
Таблица 1 - различные свойства кислотных гидроксидов циркония
Таблица 2 - поверхностные свойства кислотных гидроксидов циркония после обжига при 600°С в течение 2 часов, измеренные методом NH3/СО2-TPD
Таблица 3 - XRD фазовый анализ образцов после обжига при 450°С в течение 2 часов
Таблица 4 - поверхностные свойства кислотных гидроксидов циркония, свежих и после обжига при 600°С в течение 2 часов, измеренные по TPD пропиламина
Таблица 5 - поверхностные свойства стабилизированных вольфрамом кислотных гидроксидов циркония после обжига при 700°С в течение 2 часов, измеренные методом NH3-TPD
Таблица 6 - поверхностные свойства стабилизированных оксидом кремния кислотных гидроксидов циркония после обжига при 850°С в течение 2 часов, измеренные методом NH3-TPD
Таблица 7 - поверхностные свойства стабилизированных сульфатом кислотных гидроксидов циркония после обжига при 600°С в течение 2 часов, измеренные методом NH3-TPD.
[00126] Способ настоящего изобретения демонстрирует повышенную термостойкость нелегированных гидроксидов циркония и соответствующих оксидов после обжига при высокой температуре (900°С), сохраняющих достаточную пористость со значительной долей мезопор. Материалы на основе обожженного нелегированного гидроксида циркония характеризуются большим влиянием моноклинной фазы, что может быть важным для определенных вариантов использования этих материалов. Пористость легированных гидроксидов также повышена по сравнению с испытанными контрольными образцами. Общее существенное увеличение кислотности (сила кислотных центров) отмечено для обоих типов материалов (нелегированных/легированных).
[00127] Что касается кислотности: концентрация кислотных центров, их сила и тип подтверждены методом адсорбции пропиламина/TGA-MS (фиг. 5) и внешней адсорбции пиридина (DRIFT) (фиг. 6). Данные (площадь пика), представленные на фиг. 5а, подтверждают значительно более высокое кислотное заполнение образцов нелегированных гидроксидов циркония по сравнению с серийным сульфатированным оксидом циркония - хорошо известной суперкислотой. Кроме того, сильная кислотность всех образцов подтверждена по температуре высвобождения пропена (41 а.е.м.). Было обнаружено, что кислотная сила увеличивается от образцов 1 и 2 (сравнительных, центр пика около 368°С) к соответствующим изобретению образцу 3 (352°С) и 4 (423°С). Полученные данные показали, что материалы настоящего изобретения характеризуются сильной кислотностью даже без добавления стабилизирующих легирующих добавок, что выделяет их, как уникальные среди других хорошо известных оксидов циркония.
[00128] Спектры DRIFT пропитанных пиридином образцов (фиг. 6) подтверждают льюисовскую кислотную природу испытанных образцов в силу присутствия пика поглощения на 1446 и 1604 см-1 - основной характеристики льюисовских кислотных центров.
[00129] Легированные материалы (сульфатом, вольфрамом или оксидом кремния и т.д.) продемонстрировали сходные тенденции в отношении кислотности и пористости. Отмечено значительное улучшение (увеличение пористости на 30%, кислотности (измеренной методом NH3-TPD) -на 25% (таблицы 5, 6 и 7)) по сравнению со стандартными промышленными сортами, что указывает на положительное влияние на каталитическую активность и делает эти материалы конкурентоспособными на рынке гетерогенных катализаторов.
Таблица 1
м2/г
низкий/высокий ультразвуковой диапазон
крист, °C
600°C/
2 ч
м2/г
2 ч
мл/г
600°C/
2 ч
нм
Mакрo
2 ч
м2/г
2 ч
мл/г
900°C/
2 ч
нм
Таблица 2
мкмоль/г
мкмоль/м2
oC
мкмоль/г
мкмоль/м2
мкмоль/г
при T=
400-600°C
Таблица 3
Таблица 4
Таблица 5
2 ч,
м2/г
2 ч,
мл/г
700°C/
2 ч,
нм
oC
Таблица 6
2 ч,
м2/г
2 ч,
мл/г
850°C/
2 ч,
нм
oC
Таблица 7
2 ч,
м2/г
2 ч,
мл/г
600°C/
2 ч,
нм
2 ч, мкмоль/г
2 ч, мкмоль /м2
2 ч,
oC
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ НА ОСНОВЕ ЦЕРИЯ, ЦИРКОНИЯ И ВОЛЬФРАМА, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАТАЛИЗЕ | 2011 |
|
RU2549573C2 |
| ПОДЛОЖКА КАТАЛИЗАТОРА ИЗ ОКСИДА АЛЮМИНИЯ, УСТОЙЧИВАЯ К СЕРЕ | 2011 |
|
RU2615991C2 |
| ПОДЛОЖКА КАТАЛИЗАТОРА ИЗ ОКСИДА АЛЮМИНИЯ | 2011 |
|
RU2566748C2 |
| СОСТАВ НА ОСНОВЕ ОКСИДОВ ЦЕРИЯ, НИОБИЯ И, ВОЗМОЖНО, ЦИРКОНИЯ И ЕГО ПРИМЕНЕНИЕ В КАТАЛИЗЕ | 2011 |
|
RU2551381C2 |
| КОМПОЗИЦИИ НА ОСНОВЕ ОКСИДА ЦИРКОНИЯ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ТРОЙНЫХ КАТАЛИЗАТОРОВ | 2016 |
|
RU2727187C2 |
| КОМПОЗИЦИЯ ДИОКСИДА КРЕМНИЯ-ОКСИДА АЛЮМИНИЯ С УЛУЧШЕННОЙ СТАБИЛЬНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2019 |
|
RU2801455C2 |
| КАТАЛИЗАТОР АМИНИРОВАНИЯ, ЕГО ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2021 |
|
RU2837051C1 |
| КАТАЛИЗАТОР КРЕКИНГА ТЯЖЕЛЫХ ОСТАТКОВ НЕФТИ, ВЯЗКОЙ И ВЫСОКОВЯЗКОЙ НЕФТИ | 2019 |
|
RU2691650C1 |
| МОЛЕКУЛЯРНОЕ СИТО, ЕГО ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2017 |
|
RU2732141C2 |
| КОМПОЗИЦИЯ С ПОВЫШЕННОЙ КИСЛОТНОСТЬЮ НА ОСНОВЕ ОКСИДОВ ЦИРКОНИЯ, КРЕМНИЯ И, ПО МЕНЬШЕЙ МЕРЕ, ОДНОГО ДРУГОГО ЭЛЕМЕНТА, ВЫБРАННОГО ИЗ ТИТАНА, АЛЮМИНИЯ, ВОЛЬФРАМА, МОЛИБДЕНА, ЦЕРИЯ, ЖЕЛЕЗА, ОЛОВА, ЦИНКА И МАРГАНЦА | 2007 |
|
RU2425711C2 |







Изобретение может быть использовано при изготовлении катализаторов и сорбентов. Предложен гидроксид циркония, включающий в пересчете на оксид до 30% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, и имеющий кислотные центры, при этом указанный гидроксид циркония имеет больше льюисовских кислотных центров, чем кислотных центров Бренстеда. Способ получения гидроксида циркония включает стадии, на которых основный карбонат циркония растворяют в водном растворе азотной кислоты, в полученный раствор или золь добавляют комплексообразующий агент, при этом указанный комплексообразующий агент представляет собой миндальную кислоту. Затем нагревают полученный раствор или золь, добавляют сульфатирующий агент, основание, легирующую добавку, содержащую кремний, сульфат или вольфрам. Предложены оксид циркония, способ его получения, а также продукт для использования в катализе, связующее, покрытие и сорбент, включающие гидроксид циркония или оксид циркония. Изобретение позволяет повысить термостойкость продукта, предназначенного для использования в катализе, такого как катализатор, подложка катализатора, предшественник катализатора. 8 н. и 25 з.п. ф-лы, 13 ил., 7 табл., 12 пр.
1. Гидроксид циркония, включающий в пересчете на оксид до 30% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, и имеющий кислотные центры, при этом указанный гидроксид циркония имеет больше льюисовских кислотных центров, чем кислотных центров Бренстеда.
2. Гидроксид циркония по п. 1, включающий в пересчете на оксид менее 0,1% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, при этом гидроксид циркония является пористым, и в отношении пор с диаметром до 155 нм по меньшей мере 70% объема его пор образовано порами диаметром 3,5-155 нм, измеренным методом Баррета-Джойнера-Халенды.
3. Гидроксид циркония по п. 2, в котором в отношении пор с диаметром до 155 нм по меньшей мере 75% объема пор образовано порами диаметром 3,5-155 нм, измеренным методом Баррета-Джойнера-Халенды.
4. Гидроксид циркония по п. 1, включающий в пересчете на оксид 0,1-30% вес. сульфата с удельной площадью поверхности по меньшей мере 375 м2/г.
5. Гидроксид циркония по п. 4, имеющий общий объем пор, измеренный методом физической адсорбции N2, по меньшей мере 0,50 см3/г.
6. Гидроксид циркония по п. 4 или 5, включающий в пересчете на оксид 1-12% вес. сульфата.
7. Гидроксид циркония по п. 1, включающий в пересчете на оксид 0,1-30% вес. гидроксида вольфрама с удельной площадью поверхности по меньшей мере 400 м2/г.
8. Гидроксид циркония по п. 7, имеющий общий объем пор, измеренный методом физической адсорбции N2, по меньшей мере 0,7 см3/г.
9. Гидроксид циркония по п. 7 или 8, включающий в пересчете на оксид 12-20% вес. гидроксида вольфрама.
10. Гидроксид циркония по п. 1, включающий одну или несколько дополнительных легирующих добавок, выбранных из гидроксида редкоземельного элемента, гидроксида иттрия или гидроксида другого переходного металла, при этом общее содержание циркония в гидроксиде циркония составляет не менее 50% вес. в пересчете на оксид.
11. Способ получения гидроксида циркония по любому из пп. 1-11, при этом способ включает стадии, на которых:
(а) основный карбонат циркония растворяют в водном растворе азотной кислоты,
(b) в полученный раствор или золь добавляют комплексообразующий агент, при этом указанный комплексообразующий агент представляет собой миндальную кислоту,
(с) нагревают раствор или золь, полученный на стадии (b),
(d) добавляют сульфатирующий агент,
(e) добавляют основание с целью получения гидроксида циркония и
(f) добавляют легирующую добавку в количестве, необходимом для обеспечения содержания указанной легирующей добавки в получаемом в результате гидроксиде циркония до 30% вес. в пересчете на оксид, при этом указанная легирующая добавка содержит кремний, сульфат или вольфрам.
12. Способ по п. 11, в котором на стадии (с) раствор или золь нагревают до температуры 60-100°С.
13. Способ по п. 11 или 12, в котором сульфатирующим агентом является серная кислота.
14. Способ по любому из пп. 11-13, в котором на стадии (е) рН раствора или золя увеличивают до рН более 8.
15. Оксид циркония, включающий в пересчете на оксид до 30% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, и имеющий кислотные центры, при этом указанный оксид циркония имеет больше льюисовских кислотных центров, чем кислотных центров Бренстеда.
16. Оксид циркония по п. 15, включающий в пересчете на оксид менее 0,1% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, и включающий по меньшей мере 80% вес. моноклинной фазы при измерении методом дифракционного рентгеновского анализа после обжига при 450°С на воздухе в течение 2 ч.
17. Оксид циркония по п. 15, включающий в пересчете на оксид менее 0,1% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, и имеющий удельную площадь поверхности по меньшей мере 15 м2/г после обжига при 900°С на воздухе в течение 2 ч.
18. Оксид циркония по п. 17, имеющий общий объем пор, измеренный методом физической адсорбции N2, по меньшей мере 0,10 см3/г после обжига при 900°С на воздухе в течение 2 ч.
19. Оксид циркония по п. 15, включающий в пересчете на оксид менее 0,1% вес. легирующей добавки, содержащей кремний, сульфат или вольфрам, характеризующийся поглощением СО2 по меньшей мере 14 мкмоль/г при 400-600°С, при измерении методом термопрограммированной десорбции, после обжига при 600°С в течение 2 ч.
20. Оксид циркония по п. 15, включающий в пересчете на оксид 0,1-30% вес. сульфата, характеризующийся поглощением NH3 по меньшей мере 800 мкмоль/г, измеренным методом термопрограммированной десорбции, после обжига при 600°С на воздухе в течение 2 ч.
21. Оксид циркония по п. 20, включающий в пересчете на оксид 1-12% вес. сульфата.
22. Оксид циркония по п. 15, включающий в пересчете на оксид 0,1-30% вес. оксида вольфрама, характеризующийся поглощением NH3 по меньшей мере 420 мкмоль/г, измеренным методом термопрограммированной десорбции, после обжига при 700°С на воздухе в течение 2 ч.
23. Оксид циркония по п. 15, включающий в пересчете на оксид 0,1-30% вес. оксида кремния, при этом оксид циркония характеризуется поглощением NH3 по меньшей мере 330 мкмоль/г, измеренным методом термопрограммированной десорбции, после обжига при 850°С в течение 2 часов.
24. Оксид циркония по п. 23, включающий в пересчете на оксид 1-10% вес. оксида кремния.
25. Оксид циркония по п. 15, включающий одну или несколько дополнительных легирующих добавок, выбранных из оксида редкоземельного элемента, оксида иттрия или оксида другого переходного металла, при этом общее содержание циркония в оксиде циркония составляет не менее 50% вес. в пересчете на оксид.
26. Способ получения оксида циркония по любому из пп. 15-25, при этом способ включает стадии, на которых:
(а) основный карбонат циркония растворяют в водном растворе азотной кислоты,
(b) в полученный раствор или золь добавляют комплексообразующий агент, при этом указанный комплексообразующий агент представляет собой миндальную кислоту,
(с) нагревают раствор или золь, полученный на стадии (b),
(d) добавляют сульфатирующий агент,
(e) добавляют основание с целью получения гидроксида циркония и
(f) добавляют легирующую добавку в количестве, необходимом для обеспечения содержания указанной легирующей добавки в получаемом в результате гидроксиде циркония до 30% вес. в пересчете на оксид, при этом указанная легирующая добавка содержит кремний, сульфат или вольфрам,
(h) обжигают гидроксид циркония с получением оксида циркония.
27. Способ по п. 26, в котором на стадии (с) раствор или золь нагревают до температуры 60-100°С.
28. Способ по п. 26 или 27, в котором сульфатирующим агентом является серная кислота.
29. Способ по любому из пп. 26-28, в котором на стадии (е) рН раствора или золя увеличивают до рН более 8.
30. Продукт, предназначенный для использования в катализе, включающий гидроксид циркония по любому из пп. 1-10 или оксид циркония по любому из пп. 15-25, при этом указанный продукт выбирают из группы, состоящей из катализатора, подложки катализатора и предшественника катализатора.
31. Связующее, включающее гидроксид циркония по любому из пп. 1-10 или оксид циркония по любому из пп. 15-25.
32. Покрытие, включающее гидроксид циркония по любому из пп. 1-10 или оксид циркония по любому из пп. 15-25.
33. Сорбент, включающий гидроксид циркония по любому из пп. 1-10 или оксид циркония по любому из пп. 15-25.
| US 20160151768 A1, 02.06.2016 | |||
| REDDY B | |||
| M | |||
| et al | |||
| Influence of alumina and titania on the structure and catalytic properties of sulfated zirconia: Beckmann rearrangement, Journal of Molecular Catalysis A: Chemical, 2009, vol | |||
| Телефонно-осведомительный аппарат | 1921 |
|
SU306A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| WO 2014089131 A1, 12.06.2014 | |||
| ANDERSON J | |||
| A | |||
| et al | |||
| Influence of Si/Zr ratio on the formation of | |||
Авторы
Даты
2021-02-16—Публикация
2017-01-30—Подача