Изобретение относится к области приготовления катализаторов, используемых в процессах нефтехимического синтеза, в частности реакции получения синтетических углеводородов путем каталитического превращения синтез-газа по реакции Фишера-Тропша.
Синтез Фишера-Тропша - это гетерогенный каталитический процесс, который является одним из перспективных способов получения синтетических моторных топлив и сырья для получения пластмасс, каучуков, спиртов и других органических соединений. Промышленными катализаторами синтеза Фишера-Тропша являются катализаторы на основе железа, в первую очередь это обусловлено их низкой стоимостью и широким распределением получаемых продуктов. В то же время, последние исследования показывают, что использование марганца в качестве активной добавки к железо и кобальтсодержащим катализаторам улучшает селективность по целевым продуктам [S. Gao, N. Liu, J. Liu, W. Chen, X. Liang, Y. Yuan, "Synthesis of higher alcohols by CO hydrogenation over catalysts derived from LaCo1-xMnxO3 perovskites: Effect of the partial substitution of Co by Mn", Fuel, vol. 261, no. 1, pp. 1-12, 2020 - (1)]. В то же время для усовершенствования процесса получения синтетических углеводородов реакцией Фишера-Тропша требуется разработка новых эффективных, селективных и стабильных катализаторов. Общеизвестно, что помимо состава катализатора большое влияние на каталитические характеристики и функциональные свойства оказывает способ получения, а именно, исходные реагенты, виды растворителя, тип используемого комплексообразователя, температура получения.
Оксиды со структурой перовскита (АВО3, где А - редкоземельный металл, В - переходный металл) из-за своей дешевизны, активности, термической и механической устойчивости являются перспективными катализаторами для процессов нефтехимического синтеза, включая синтез Фишера-Тропша. Данные оксиды могут быть модифицированы путем полного или частичного замещения А или В катионов, что позволяет в широких пределах варьировать состав, улучшать поверхностные и каталитические характеристики, тем самым создавать материалы с заданными функциональными свойствами. Традиционным способом получения данного класса соединений является керамический метод синтеза, он позволяет получать чистые однофазные целевые соединения, однако использование длительных и высотемпературных условий прокаливания приводит к уменьшению удельной площади поверхности и агрегации частиц катализатора, что в свою очередь приводит к снижению каталитической активности.
Известен способ приготовления [RU 2468863 Катализатор на основе Fe для синтеза Фишера-Тропша, способ его приготовления и применения - (2)] катализатора для получения углеводородов из синтез-газа реакцией Фишера-Тропша. Описанный катализатор состоит из железа - используемого в качестве главного компонента и содержит оксиды меди и серебра, а также благородные металлы Pt, Pd, Ru и Rh. Достоинствами способа приготовления является простота получения, а использование полученного катализатора в процессе Фишера-Тропша приводит к увеличению селективности по целевым продуктам, в то же время данный катализатор имеет ряд недостатков, главный из которых использование благородных металлов, что приводит к существенному удорожанию катализатора.
Наиболее близким к предложенному способу, является способ приготовления оксида со структурой перовскита [CN 102942225 2013 Preparation method of GdFeO3 nanocrystallines - (3)] который может быть использован в качестве катализатора получения углеводородов реакцией Фишера-Тропша. По решаемой задаче и достигаемому техническому результату этот способ выбран в качестве прототипа. Способ включает следующие стадии: растворение нитратов Gd(NO3)3⋅6H2O, Fe(NO3)3⋅9H2O в этиленгликоле (1:1:40-120), выпаривание при 60-80°С в течение 2-4 часов до образования золя, сушку полученного золя при 120-160°С в течение 6-10 часов, с последующей гомогенизацией полученного порошка и трехкратное прокаливание в муфельной печи при 300-500°С с промежуточным измельчением. Прокаливание в муфельной печи при 600-900°С в течение 2-8 часов. Промывание водой и этанолом, сушку в печи при 60-80°С в течение 5-6 часов. Известный способ позволяет получать частицы размером 60-100 нм.
В то же время прототип имеет ряд недостатков, среди которых большое количество повторяющихся этапов прокаливания и промывки, использование большого количества реагентов (комплексообразователя - этиленгликоля и этанола для промывки) и длительных высокотемпературных режимов обработки, все это приводит к удорожанию целевого соединения.
Техническим результатом заявленного изобретения является упрощение процесса получения, за счет сокращения числа стадий прокаливания, снижение экономических затрат на приготовление катализатора за счет уменьшения количества используемых реагентов, сокращения времени и температуры термической обработки.
Указанный технический результат достигается тем, что в способе приготовления катализатора для получения углеводородов путем реакции Фишера-Тропша, заключающемся в растворении солей-предшественников, добавлении комплексообразователя, выпаривании раствора, прокаливании в муфельной печи, в соответствии с заявленным изобретением, в качестве дополнительной соли-предшественника используют нитрат марганца Mn(NO3)2⋅3H2O, соли-предшественники Gd(NO3)3⋅6H2O, Mn(NO3)2⋅3H2O, Fe(NO3)3⋅9H2O, взятые в мольном соотношении 1:х:(1-х), где х=0.1-0.9, перед добавлением комплексообразователя растворяют в деионизированной воде, в качестве комплексообразователя используют моногидрат лимонной кислоты, взятый в весовом соотношении к смеси нитратов от 1.8:1 до 3.5:1, после полного растворения моногидрата лимонной кислоты добавляют раствор аммиака до установления рН от 5.5 до 6.5, а полученный после выпаривания порошок прокаливают при 430°С в течение 2-х часов и 1-2 часа при температуре 650-850°С.
Общими с прототипом признаками заявленного способа приготовления катализаторов включает следующие стадии: растворение солей-предшественников Gd(NO3)3⋅6H2O и Fe(NO3)3⋅9H2O, добавление комплексообразователя, выпаривание раствора и прокаливание полученного порошка в муфельной печи.
Отличительными от прототипа признаками заявленного способа приготовления катализатора являются:
1. Использование в качестве дополнительной соли-предшественника нитрата марганца Mn(NO3)2⋅3H2O
2. Соли-предшественники Gd(NO3)3⋅6H2O, Mn(NO3)2⋅3H2O, Fe(NO3)3⋅9H2O, взятые в мольном соотношении 1:х:(1-х), где х=0.1-0.9, перед добавлением комплексообразователя растворяют в деионизированной воде
3. В качестве комплексообразователя используют моногидрат лимонной кислоты, взятый в весовом соотношении к смеси нитратов от 1.8:1 до 3.5:1
4. После полного растворения моногидрата лимонной кислоты добавляют раствор аммиака до установления рН от 5.5 до 6.5
5. Полученный после выпаривания порошок прокаливают при 430°С в течение 2 часов и 1-2 часа при температуре 650-850°С.
Сущность заявленного способа приготовления катализаторов заключатся в растворении солей-предшественников Gd(NO3)3⋅5H2O, Fe(NO3)3⋅9H2O, Mn(NO3)2⋅3H2O, взятых в мольном соотношении 1:х:(1-х), где х=0.1-0.9, в деионизированной воде, добавлении комплексообразователя - моногидрата лимонной кислоты, взятой в весовом соотношении к смеси нитратов от 1.8:1 до 3.5:1, до полного растворения моногидрата лимонной кислоты, добавлении раствора аммиака при комнатной температуре, до установления рН от 5.5 до 6.5 и образования золя, выпаривании полученного раствора, при постоянном перемешивании при температуре 120°С до полного удаления воды, прокаливании порошка при 430°С в течение 2 часов, гомогенизации порошка с последующим таблетированием, прокаливании 1-2 часа при температуре 650-850°С.
Заявленный способ позволяет приготовить катализатор состава, соответствующего формуле GdMnxFe1-xO3, где х=0.1-0.9.
Для приготовленных предложенным способов образцов катализатора проводили определение фазового состава, морфологии поверхности и тестирование каталитической активности в реакции получения углеводородов путем каталитического превращения синтез-газа по реакции Фишера-Тропша.
Рентгенофазовый анализ образцов проведен при комнатной температуре, на приборе Rigaku «MiniFlex II», с CuKα излучением, интервал сканирования углов - 2θ=20-80°, скорость сканирования - 10°/мин. Для идентификации фаз использована база данных PDF2. Морфологию поверхности катализаторов исследовали с использованием сканирующего микроскопа (ZeissMerlin и ZeissSupra 40VP). Удельная площадь поверхности была определена методом адсорбции азота при -196°С на адсорбционном анализаторе QuadrasorbSI. Каталитические свойства образцов, полученных описанным способом, анализировали в реакции получения углеводородов из синтез-газа реакцией Фишера-Тропша. Испытания были проведены в проточной каталитической установке с U-образным кварцевым реактором, при атмосферном давлении, температура реакции - при 350°С, скорость подачи смеси - 1,0 л/ч, состав исходной смеси - СО: Н2=1:2. Перед началом опыта реактор отжигали воздухом, и нагревали до 400°С. Затем засыпали катализатор в реактор и в потоке водорода проводили восстановление при 400°С.
Количественная интерпретация полученных результатов была проведена методом абсолютной калибровки с использованием программы Хроматэк Аналитик 2.5. Скорости образования продуктов реакции измерялись после достижения в системе стационарного состояния, о котором судили по постоянству площадей хроматографических пиков.
Селективность по i-компоненту Si при данной температуре рассчитывали по формуле:
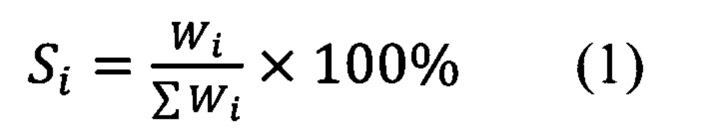
Wi - выход i-го продукта реакции на 1 г катализатора, моль/час*г; ∑Wi - сумма выходов i-х продуктов реакции на 1 г катализатора, моль/час*г.
Погрешность в определении каждого компонента не превышала 5% и складывалась из погрешности измерения температуры и погрешности измерения скорости подачи реакционной смеси.
Сущность изобретения иллюстрируется нижеприведенными примерами (1-3), таблицей (1) и чертежами (Фиг. 1-Фиг. 6).
Пример 1 иллюстрирует способ приготовления катализатора состава GdMn0.1Fe0.9O3.
В качестве солей-предшественников использовали: Gd(NO3)3⋅6H2O (квалификации "ХЧ"), Mn(NO3)2⋅3H2O (квалификации "ХЧ"), Fe(NO3)3⋅9H2O (квалификации "Ч"). Нитраты, взятые в мольном соотношении 1:0.1:0.9, растворяли в деионизированной воде, затем колба помещалась на магнитную мешалку с терморегулятором. К полученному раствору нитратов при постоянном перемешивании добавляли моногидрат лимонной кислоты в весовом соотношении 1.8:1. После полного растворения моногидрата лимонной кислоты, для установления рН раствора на уровне 6.5, при комнатной температуре добавляли раствор аммиака и при этом наблюдали образование золя. Далее проводили выпаривание раствора при температуре ~120°С до полного удаления воды и образования порошка черного цвета. Затем температуру поднимали до 430°С и прокаливали полученный порошок в течение 2 часов. Полученный порошок гомогенизировали перетиранием в агатовой ступке с последующим таблетированием, затем прокаливали в печи при температуре 650°С в течение 2 часов.
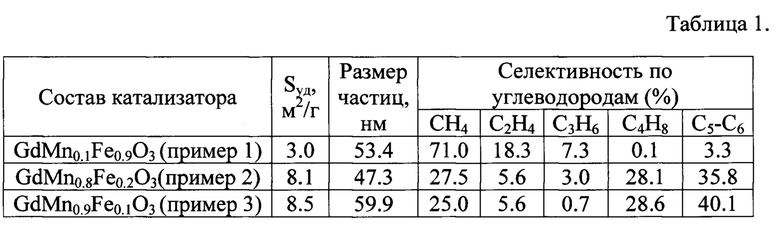
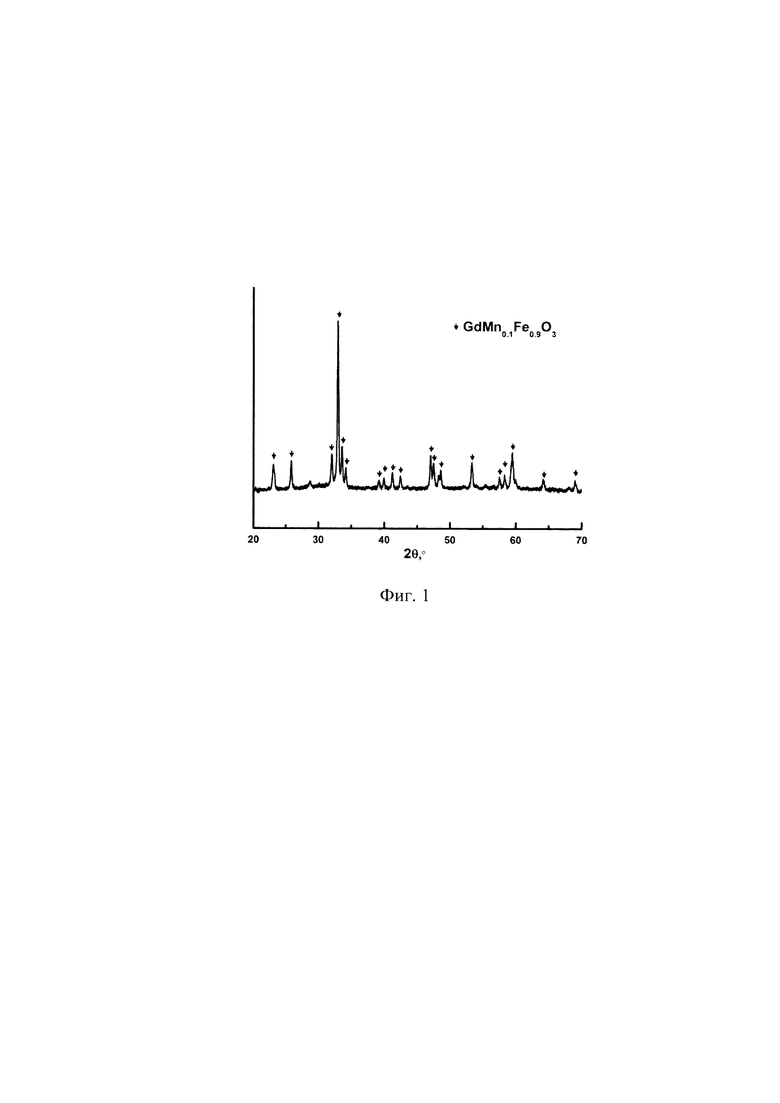
На Фиг. 1 представлены результаты исследования фазового состава приготовленного катализатора, установлено, что указанные условия прокаливания достаточны для образования оксида со структурой перовскита, значение удельной площади поверхности приведены в таблице 1.
На Фиг. 2 приведена микрофотография поверхности приготовленного катализатора, на которой видно, что полученный образец обладает пористой поверхностью, а размер частиц катализатора составляет ~ 50-60 нм.
Результаты исследования каталитических свойств, а именно, значения селективности по продуктам при температуре 400°С, приведены в таблице 1.
Таким образом, приведенный пример демонстрирует, что применение заявленного способа позволяет существенно упростить получение оксида с развитой морфологией, который может быть использован в качестве катализатора для получения углеводородов.
Пример 2 иллюстрирует способ приготовления катализатора состава GdMn0.8Fe0.2O3.
В качестве солей-предшественников использовали: Gd(NO3)3⋅6H2O (квалификации "ХЧ"), Mn(NO3)2⋅3H2O (квалификации "Ч"), Fe(NO3)3⋅9H2O (квалификации "Ч"). Нитраты, взятые мольном соотношении 1:0.8:0.2, растворяли в деионизированной воде, затем колба помещалась на магнитную мешалку с терморегулятором. К полученному раствору солей-предшественников при постоянном перемешивании добавляли моногидрат лимонной кислоты в весовом соотношении : моногидрат лимонной кислоты : нитраты (3:1). После полного растворения моногидрата лимонной кислоты, при комнатной температуре добавляли раствор аммиака до установления рН раствора на уровне 5.5 и образования золя. Далее проводили выпаривание раствора при температуре ~120°С, до полного удаления воды и образования порошка черного цвета. Затем температуру поднимали до 430°С и прокаливали полученный порошок в течение 2 часов. Полученный порошок гомогенизировали в агатовой ступке и таблетировали, затем прокаливали в муфельной печи при температуре 700°С 1 час.
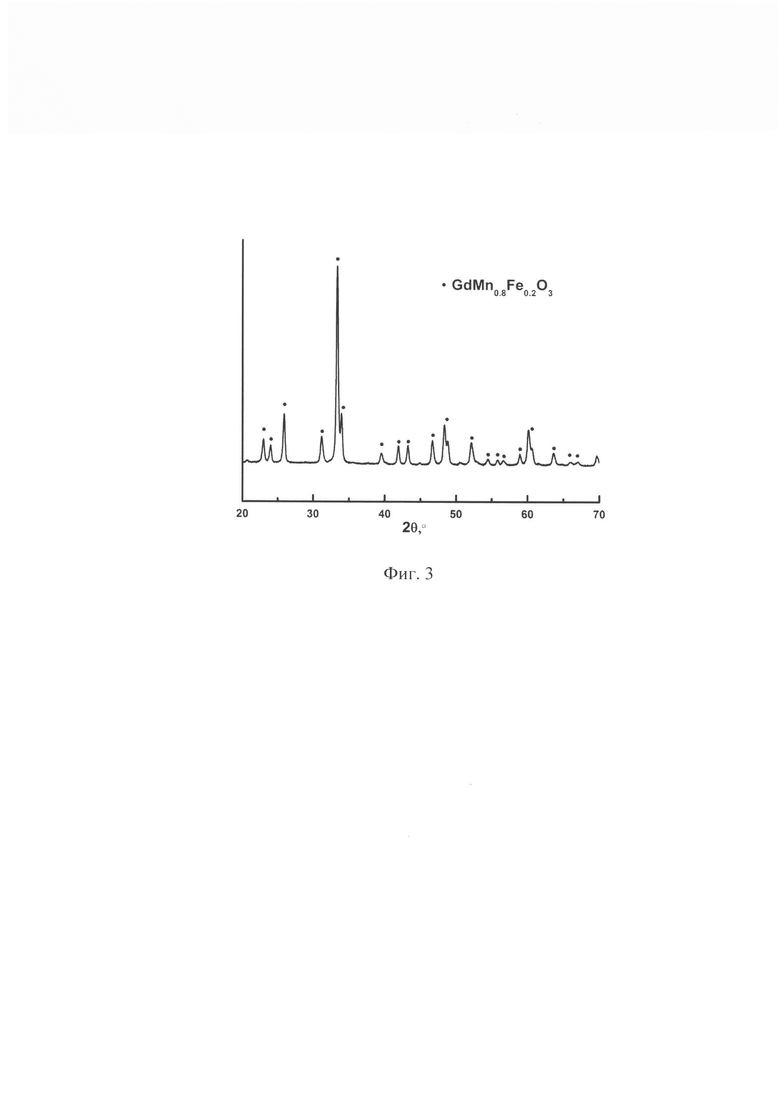
Данные исследования фазового состава, приведенные на Фиг. 3 подтверждают присутствие только целевого соединения со структурой перовскита. На Фиг. 4 приведена микрофотография полученного образца катализатора, частицы которого имеет размер в диапазоне 50-200 нм и образуют пористую поверхность, данные исследования удельной площади поверхности приведены в таблице 1.
Результаты изучения каталитических характеристик полученного оксида, приготовленного по описанному способу, приведены в таблице 1.
Пример 3 иллюстрирует способ приготовления катализатора состава - GdMn0.9Fe0.1O3.
В качестве солей-предшественников использовали: Gd(NO3)3⋅6H2O (квалификации "ХЧ"), Mn(NO3)2⋅3H2O (квалификации "Ч"), Fe(NO3)3⋅9H2O (квалификации "Ч"). Нитраты, взятые мольном соотношении 1:0.9:0.1 растворяли в деионизированной воде, затем колба помещалась на магнитную мешалку с терморегулятором. К полученному раствору солей при постоянном перемешивании добавляли моногидрат лимонной кислоты в весовом соотношении: моногидрат лимонной кислоты: нитраты (3.5:1). После полного растворения многидрата лимонной кислоты, при комнатной температуре добавляли раствор аммиака до установления рН раствора на уровне 6 и образования золя, после чего проводили выпаривание раствора при температуре ~120°С до полного удаления воды и образования порошка черного цвета. Затем нагревали до 430°С и прокаливали полученный порошок в течение 2 часов. Полученный порошок гомогенизировали в агатовой ступке и таблетировали, затем прокаливали в муфельной печи при температуре 850°С 1 час.
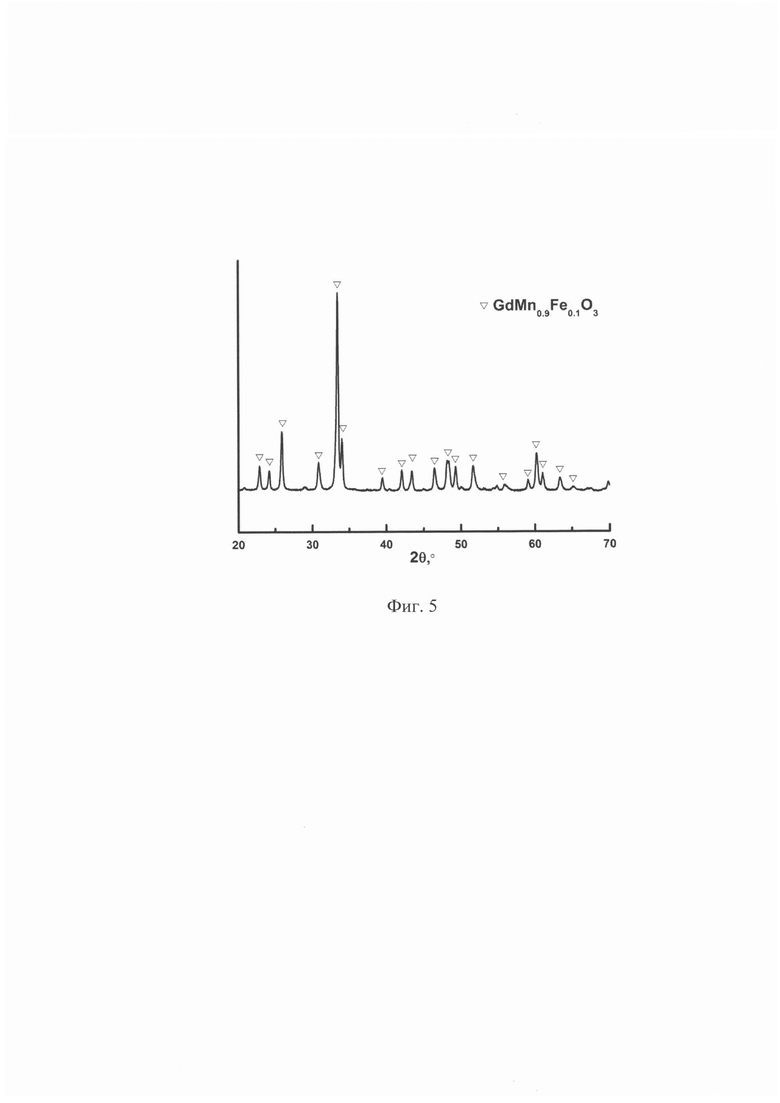
На Фиг. 5 приведены результаты рентгенофазового анализа образца катализатора. Рентгенограмма полученного соединения показала наличие только однофазного целевого оксида.
На Фиг. 6 приведена микрофотография GdMn0.9Fe0.1O3, свидетельствующая о том, что приготовленный катализатор имеет частицы размером порядка 100 нм. В таблице 1 приведена удельная площадь поверхности.
Результаты изучения каталитической активности, полученного по описанному способу катализатора, приведены в таблице 1.
Приведенные выше примеры подтверждают возможность использования заявленного способа приготовления катализаторов с частицами размером 50-200 нм для получения углеводородов процессом Фишера-Тропша.
Техническим результатом заявленного изобретения является упрощение процесса получения, за счет сокращения числа стадий прокаливания, снижение экономических затрат на приготовление катализатора за счет уменьшения количества используемых реагентов, сокращения времени и температуры термической обработки. Заявленный способ позволяет получать однофазные оксиды с заданными характеристиками, таким как: развитая морфология поверхности, высокая каталитическая активность, термическая и механическая стабильность.
Использование заявленного изобретения предполагается на предприятиях нефтегазового сектора, таких как ПАО «Газпром нефть», ПАО «Лукойл», ОАО «Салаватнефтеоргсинтез», ЗАО «Промышленные катализаторы».
Источники информации
1. S. Gao, N. Liu, J. Liu, W. Chen, X. Liang, Y. Yuan, "Synthesis of higher alcohols by CO hydrogenation over catalysts derived from LaCo1-xMnxO3 perovskites: Effect of the partial substitution of Co by Mn", Fuel, vol. 261, no. 1, pp. 1-12, 2020.
2. Патент RU 2468863 C1 2010 Катализатор на основе Fe для синтеза Фишера-Тропша, способ его приготовления и применения.
3. Патент CN 102942225 2013 Preparation method of GdFeO3 nanocrystallines - прототип.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ приготовления катализаторов для получения синтез-газа путем углекислотной конверсии метана | 2018 |
|
RU2690496C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРОВСКИТОВ | 2009 |
|
RU2440292C2 |
| КАТАЛИЗАТОРЫ | 2012 |
|
RU2603136C2 |
| СПОСОБ АКТИВАЦИИ МЕТАЛЛОКСИДНЫХ КАТАЛИЗАТОРОВ СИНТЕЗА УГЛЕРОДНЫХ НАНОМАТЕРИАЛОВ | 2010 |
|
RU2443470C2 |
| КАТАЛИЗАТОРЫ | 2010 |
|
RU2517700C2 |
| ВЫСОКОСЕЛЕКТИВНЫЙ КАТАЛИЗАТОР ДЛЯ ПРОИЗВОДСТВА ФРАКЦИЙ ВЫСОКОКАЧЕСТВЕННОГО БЕНЗИНА ИЗ СИНТЕЗ-ГАЗА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2011 |
|
RU2484897C1 |
| КАТАЛИЗАТОРЫ | 2011 |
|
RU2551433C1 |
| ПОЛУЧЕНИЕ НИЗКОМОЛЕКУЛЯРНЫХ ОЛЕФИНОВ ИЗ СИНТЕЗ-ГАЗА | 2010 |
|
RU2558954C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОБАЛЬТОВОГО КАТАЛИЗАТОРА СИНТЕЗА ЖИДКИХ УГЛЕВОДОРОДОВ ПО МЕТОДУ ФИШЕРА-ТРОПША | 2012 |
|
RU2493913C1 |
| КАТАЛИЗАТОРЫ | 2012 |
|
RU2591702C2 |



Предложен способ приготовления катализатора для получения углеводородов реакцией Фишера-Тропша, заключающийся в растворении солей-предшественников, добавлении комплексообразователя, выпаривании раствора, прокаливании в муфельной печи, где в качестве дополнительной соли-предшественника используют нитрат марганца Mn(NO3)2⋅2H2O, перед добавлением комплексообразователя соли-предшественники Gd(NO3)3⋅H2O, Mn(NO3)2⋅3H2O, Fe(NO3)3⋅9H2O, взятые в мольном соотношении 1:х:(1-х), где х=0.1-0.9, растворяют в деионизированной воде, в качестве комплексообразователя используют моногидрат лимонной кислоты, взятый в весовом соотношении к смеси нитратов от 1.8:1 до 3.5:1, после полного растворения моногидрата лимонной кислоты добавляют раствор аммиака до установления рН от 5.5 до 6.5, а полученный после выпаривания порошок прокаливают при 430°С в течение 2 часов и 1-2 часа при температуре 650-850°С. Технический результат - упрощение процесса получения, за счет сокращения числа стадий прокаливания, снижение экономических затрат на приготовление катализатора за счет уменьшения количества используемых реагентов, сокращения времени и температуры термической обработки. 1 табл., 6 ил.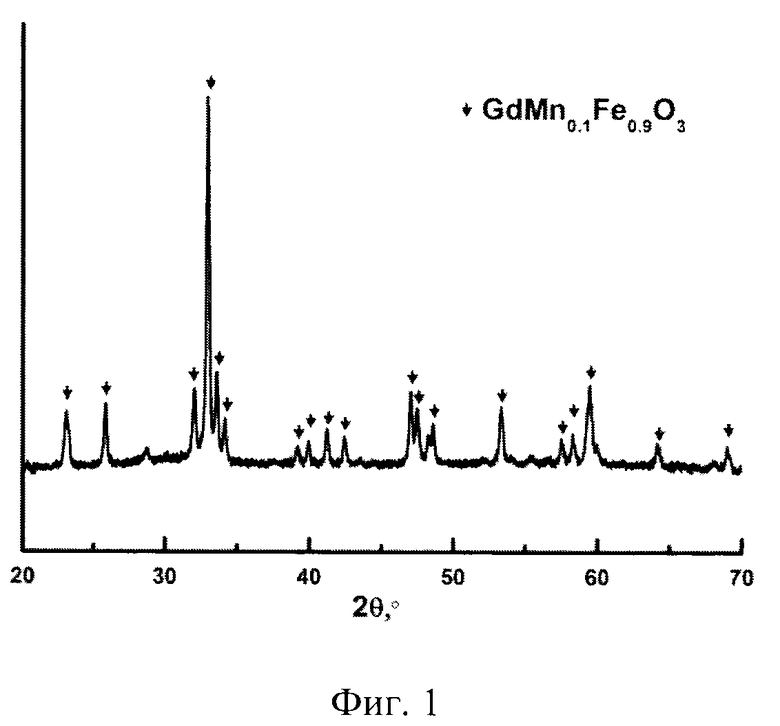
Способ приготовления катализатора для получения углеводородов реакцией Фишера-Тропша, заключающийся в растворении солей-предшественников, добавлении комплексообразователя, выпаривании раствора, прокаливании в муфельной печи, отличающийся тем, что в качестве дополнительной соли-предшественника используют нитрат марганца Mn(NO3)2⋅2H2O, перед добавлением комплексообразователя соли-предшественники Gd(NO3)3⋅H2O, Mn(NO3)2⋅3H2O, Fe(NO3)3⋅9H2O, взятые в мольном соотношении 1:х:(1-х), где х=0.1-0.9, растворяют в деионизированной воде, в качестве комплексообразователя используют моногидрат лимонной кислоты, взятый в весовом соотношении к смеси нитратов от 1.8:1 до 3.5:1, после полного растворения моногидрата лимонной кислоты добавляют раствор аммиака до установления рН от 5.5 до 6.5, а полученный после выпаривания порошок прокаливают при 430°С в течение 2 часов и 1-2 часа при температуре 650-850°С.
| CN 102942225 A, 27.02.2013 | |||
| CN 101185885 A, 27.02.2013 | |||
| CN 103933991 A, 23.07.2014 | |||
| КАТАЛИЗАТОРЫ | 2010 |
|
RU2517700C2 |
Авторы
Даты
2021-03-15—Публикация
2019-12-02—Подача