Изобретение относится к области химической инженерии, в частности к технологии очистки воды твердыми адсорбентами. В современном уровне техники твердые адсорбенты применяют в качестве заполняющей среды в слое колонки для удаления путем адсорбции катионов тяжелых металлов и, в частности, ртути из питьевой и сточной воды.
Загрязнение ртутью считается одной из наиболее важных экологических проблем вследствие ее подвижности на различных этапах жизненного цикла и подтвержденной высокой токсичности. Воздействие ртути может быть особенно вредным в зависимости от полученной дозы, химической формы ртути, синергетического эффекта с другими токсичными веществами и состояния здоровья человека. В частности, основными наблюдаемыми эффектами являются хроническое отравление, различные репродуктивные, генетические, неврологические и психиатрические проблемы, а также побочные эффекты, проявляемые в почках, крови, моче и конечностях. Исходя из опасений, связанных со здоровьем человека в отношении поглощения ртути из питьевой воды, допустимый предел общей концентрации ртути, предложенный Всемирной организацией здравоохранения в 1971 году и с тех пор постепенно применяемый во всем мире, составляет 0,001 мг/л.
Присутствие ртути в воздухе, воде и почве связано как с природными процессами, так и с антропогенной деятельностью. В частности, природные процессы включают выщелачивание горных пород минералами, содержащими ртуть, и выбросы в атмосферу в результате вулканической или геотермальной активности. Основные антропогенные выбросы происходят при сжигании ископаемого топлива, металлургии, добыче золота, сжигании отходов, а также при производстве цемента, едкого натра, бумаги и краски. В зависимости от кислотности, окислительно-восстановительного потенциала и концентрации других анионов, ртуть может встречаться в двухвалентной форме в природных водах и в трех формах: Hg2+, HgOH+ и Hg(OH)2. Однако при обычных значениях рН от 6 до 8, доминирующая форма представляет собой Hg(OH)2.
Способы удаления и поглощения ртути можно подразделить на способы, направленные на очистку воды (главным образом сточных вод), в которых основное внимание уделяется ионным формам ртути, и способы, применяемые для очистки газовой фазы, которые обычно сосредоточены на летучей металлической форме (Hg0). Ряд способов удаления ртути, таких как фитопоглощение, биоадсорбция, искусственные заболоченные земли и осаждение отстаиванием, не могут быть применены к воде, предназначенной для потребления человеком, из-за невозможности обрабатывать большие потоки и главным образом из-за большого объема токсичных сточных вод, даже если они обнаруживают приемлемые фиксированные и эксплуатационные расходы. По понятным причинам они не могут быть применены для удаления ртути из отработанных газов. Применение ионообменных смол, мембран из оксида алюминия, полимерных волокон и отгонки воздухом показывает большую эффективность в удалении ртути. Однако они не соответствуют требованиям в отношении эксплуатационных расходов и их неспособности обрабатывать большие объемы воды. Широкий спектр способов удержания ртути также применяли для ее удаления из газовых потоков и, в частности, из отработанных газов. В число этих способов входит применение электростатических или обычных фильтров, которые вместе с отделением твердых примесей, также удаляют долю ртути. Каталитическое окисление и добавление реагентов амальгамации, а также распыление адсорбентов синергетически применяют для поглощения ртути, с последующим отделением на электростатических фильтрах.
Однако наиболее распространенным способом удаления ртути, как из газовых, так и из водных потоков, является применение адсорбирующих материалов и, в основном, активированного угля. Эффективность активированного угля главным образом основана на большой удельной площади поверхности, в то время как тот факт, что он удерживает ртуть слабыми связями, позволяет предположить, что он не имеет подходящей плотности зарядов на своей поверхности и значительной окислительной способности элементарной ртути, увеличивая, таким образом, возможность последующего выщелачивания. Кроме того, эффективность активированного угля считается недостаточной для соблюдения новых экологических норм как для питьевой воды, где допустимый предел ртути составляет 1 мкг/л, так и для отработанных газов, где предел допустимых выбросов ртути составляет 50 мкг/м3.
В результате в последние годы исследования были сосредоточены на разработке адсорбентов на основе простых или композиционных неорганических материалов. Однако подавляющее большинство неорганических адсорбентов для удаления ртути применяется для очищения отработанных газов, и часто отмечается, что их эффективность значительно снижается при очистке воды, поскольку молекулы воды способствуют уменьшению активных центров. Эти случаи можно выделить:
- в композиционные материалы из двух или более фаз, которые действуют последовательно на стадии окисления ртути и на стадии ее поглощения; и
- в однофазовые материалы, где удержание и возможное окисление ртути происходит на поверхности одного и того же материала.
Первый подход описан S. Yang et al., Journal of Hazardous Materials 186 (2011) 508, где композиционный материал из марганца/маггемита (Mn/γ-Fe2О3) применяли для окисления ртути из газового потока, а затем для ее удержания из марганца или маггемита. Способность сохранять окисленную форму является результатом ее отрицательной поверхностной нагрузки. Максимальная емкость составляет 3,54 мг/г, которая уменьшается до 0,52 мг/г при достижении допустимого предела ртути (50 мкг/м3) в выходящем потоке (300 °С).
Песок с адсорбированным марганцем, по-видимому, хорошо подходит для очистки воды от тяжелых металлов, как показано в D.A. Atwood and M.K. Zaman, Structure and Bonding, Vol. 120, Springer-Verlag, 163. Однако при пропуске пресной воды наблюдается выщелачивание адсорбированной ртути.
Аналогичным случаем является бинарный оксид марганца/циркония (MnOx/ZrО2), описанный в M.M. Wiatros-Motyka et al., Fuel 109 (2013) 559. В указанном материале применяется окислительная способность оксида марганца, в то время как роль оксида циркония не выяснена авторами, но, вероятно, он обеспечивает дополнительные сайты физической адсорбции. Приведенные данные о емкости материала не соответствуют фактическим условиям применения, поскольку определенная максимальная адсорбционная емкость (8,4 мг/г) соответствует чрезмерно высокой концентрации в выходящем потоке, составляющей 3000 мг рт.ст./м3.
Комбинация оксида марганца и оксида алюминия (MnOx/Al2O3) описана в публикации F. Scala et al., Fuel 108 (2013) 13 и R.A. Jadhav et al., Topical review for U.S. Department of Energy (2005) для очистки горячего воздуха от ртути. В первом случае выход, описанном для концентрации ртути в выходящем потоке приблизительно 0,1 мг/м3, составляет 3,7 мг/г при 200 °С, тогда как десорбция ртути наблюдается при более высоких температурах. Следовательно, материал не может достичь предела выбросов газов, при очень слабой поглощающей способности. Напротив, во второй статье приводятся доказательства, подтверждающие способность снижать концентрацию ртути в выходящем потоке ниже 50 мкг/м3 при температуре 100 °С. Адсорбционная емкость относительно низкая (0,15 мг/г) и быстро уменьшается при повышении температуры до 200 °С.
Серию бинарных материалов на основе оксида титана (TiО2) применяли в публикациях Y. Li et al., Fuel Processing Technology 89 (2008) 567 (SiО2/TiО2), H. Li et al. (2011) 186 и Applied Catalysis B: Environmental 111-112 (2012) 381 (SiО2/TiО2/V2O5 и MnOx-CeO2/TiО2), Q. Wan et al., Chemical Engineering Journal 170 (2011) TiО2) и S. wu et al., Fuel 85 (2006) 213 (Fe2О3/TiО2), пытаясь применить его каталитическое влияние на окисление ртути. Однако обнаружено, что в этих случаях необходимо активировать поверхность оксида титана ультрафиолетовым излучением вместе с сосуществованием сероводорода или соляной кислоты в потоке газа для стабилизации окисленной ртути. Вследствие данных ограничений способ несет значительное воздействие от других компонентов газового потока. Кроме того, во всех случаях, хотя материалы смогли снизить концентрацию ртути ниже предела допустимых выбросов, данные об эффективной работе и емкости ртути являются неполными, так как они относятся к большому количеству материала и времени контакта с газовым потоком.
Применение оксида железа (Fe2O3) в качестве активного компонента описано в публикации Z. Tan et al., Chemical Engineering Journal 195-196 (2012) 218 в бинарном материале с оксидом кремния (SiО2), который представляет собой относительно низкий выход (85 %) при адсорбции ртути из газового потока. В этом случае окислению способствует присутствие кислорода.
Магнитные ферритовые наночастицы, в качестве материала для очистки воды от ртути предложены в CN 102908992, CN 102872913 и CN 102432085. Наночастицы либо покрыты активными группами адсорбции ртути (родамином, крахмалом), либо включены с наночастицами палладия в углеродные нанотрубки. В дополнение к высокой стоимости и несовместимости родамина и крахмала с питьевой водой, эти материалы демонстрируют практически нулевую эффективность удержания ртути.
Большая часть усилий направлена на повышение эффективности активированного угля путем включения неорганических легирующих примесей (MnО2, ZnCl2, FeCl3, CuCl2) или путем активации их поверхности путем окисления озоном, перекисью водорода, азотной кислотой и перманганатом калия, как описано в публикации Y. Zheng et al., Progress in Energy and Combustion Science 38 (2012) 599. Эти материалы, даже несмотря на повышение способности удаления ртути для соответствующего активированного угля, демонстрируют емкость, не превышающую 1 мг/г ртути при концентрации в выходящем потоке 50 мкг рт.ст./м3.
В документе US 8263525 В1 раскрыта твердая подложка из углеродных наночастиц и последовательное функциональное покрытие из диоксида кремния и сульфида, которое обеспечивает значительно более высокую эффективность в удалении ртути из воды по сравнению с соответствующими коммерческими продуктами. Представленные данные показывают, что материал достигает насыщения после 2 часов обработки воды при концентрации ртути 100 мг/л. Хотя емкость материала до насыщения относительно высока (50 мг/г), можно легко сделать вывод, что его нельзя применять к питьевой воде, где концентрация в выходящем потоке должна быть менее 1 мкг/л.
Второй способ включает применение металлов, таких как Ir, Pt, Pd, Rh, Ti и Ru, описанных в публикации E.J. Granite et al., Industrial and Engineering Chemistry Research 45 (2006) 4844. Данные материалы, способные образовывать амальгамы с ртутью, экспериментально проверяли на связывание ртути из потока горячего воздуха. Результаты показали, что показатели эффективности для Pt достигали 100%, для Ir 93%, а показатели эффективности для остальных материалов не превышала 65%, в то время как соответствующие значения адсорбционной емкости составляли менее 0,5 мг/г. Если принять во внимание стоимость данных благородных материалов, то их применение в больших масштабах не допускается.
В US 20130152788 A1 раскрыт ряд соединений сульфида металла (например, CuS), которые получают осаждением соответствующих предшественников и неорганического или органического источника серы и применяют для удаления ртути из газов или жидкостей. Эти материалы имеют низкую себестоимость, однако, согласно измерениям, предусмотренным только для адсорбции газа, емкость материала соответствует высоким концентрациям в выходящем потоке (от 150 до 200 мкг/м3).
В документе US 20130089479 A1 раскрыт синтез неорганических оксидов на основе сульфида на основе диоксида кремния общей формы (SiO2)x(OH)yMzSaFB, где M представляет собой катион металлоида, S представляет собой сульфидную соль, F представляет собой органосилан и B представляет собой гигроскопичный оксид или гидроксид щелочного металла. Данные комплексные соединения применяют для нейтрализации ртути с применением сульфидных групп, в то же время захватывая оставшиеся ингибирующие соединения, встречающиеся в отработанных газах, с применением других компонентов. Ожидали, что и стоимость сырья, и способ получения будут достаточно высокими, но даже тесты не показали высокой способности удаления ртути.
Однофазовые материалы с относительно высокой плотностью катионов на поверхности оказались весьма эффективными в адсорбции ртути из газов. Феррит марганца (Fe3-xMnxО4) и нестехиометрический титан-магнетит (Fe3-xTixО4) были изучены в публикациях S. Yang et al., Environmental Science and Technology 45 (2011) 1540 и S. Yang et al., Applied Materials and Interfaces 3 (2011) 209, где окисление ртути из Ti и Mn4+, соответственно, подтверждали, а затем ртуть адсорбировали на поверхности материала. Данные материалы получают совместным осаждением из солей железа и марганца или титана. Максимальная адсорбционная емкость достигает 4,0 и 5,1 мг/г соответственно в потоке газа при температуре 250 °С. Однако, когда концентрация ртути в выходящем потоке составляет менее 0,05 мг/м3, эффективная емкость составляет менее 0,2 мг/м3.
Неорганические адсорбенты, описанные в вышеупомянутых публикациях в качестве материалов для удаления ртути, имеют следующие недостатки:
- практически не существует материала, предназначенного для очистки питьевой воды от ртути. Кроме того, нет доказательств эффективности разработанных неорганических адсорбентов в удалении ртути из горячих газовых потоков.
- А именно, их способы синтеза являются дорогостоящими, поскольку они работают в периодическом режиме в течение длительного времени контакта и часто при длительном нагревании. Кроме того, некоторые из применяемых материалов имеют высокую ценность.
- Несмотря на заявленные высокие показатели поглощения ртути, указанные выходы не соответствуют законодательным ограничениям по питьевой воде и выбросам газа
- Низкая эффективность обусловлена тем, что в композиции не предусмотрено, чтобы поверхность материала имела повышенную плотность отрицательных зарядов, что необходимо для необратимой адсорбции положительно заряженных ионов Hg2+, обнаруженных в воде.
- Аналогичным образом, окислительная способность не оптимизирована, что приводит к частичной адсорбции ртути путем физической адсорбции в форме Hg0, что снижает выход и допускает последующее выщелачивание ртути.
- Представленные данные указывают на то, что при применении указанных материалов ожидается постепенное выщелачивание ртути в окружающую среду, причем о соответствующих испытаниях на выщелачивание обычно не сообщается.
Таким образом, разработка ртутного адсорбента с низкой себестоимостью, высокой окислительной способностью элементарной ртути и, прежде всего, высокой плотностью отрицательных зарядов на его поверхности будет идеальным решением для удаления ртути для питьевой воды и газовых потоков при концентрациях ниже допустимого предела для питьевой воды (1 мкг/л), а также предела допустимых выбросов (50 мкг/м3), соответственно, с применением адсорбционного слоя.
Некоторыми из данных характеристик обладает четырехвалентный фероксигит марганца, раскрытый в WO/2012/042282 и в публикации S. Tresintsi et al., Environmental Science and Technology 47 (2013) 9699, предназначенный для удаления мышьяка и других тяжелых металлов, а также ртути из питьевой воды. Данный материал состоит из оксигидроксида железа с четырехвалентным марганцем, который придает ему высокий потенциал окисления, и в то же время его получают в непрерывном режиме при температуре окружающей среды из недорогих материалов предшественников, таких как FeSО4 и KMnО4. Однако его синтез в водном растворе осуществляют в кислых условиях (рН от 4 до 7), что приводит к высокой плотности положительных зарядов на поверхности, определяемой значением изоэлектрической точки, превышающим значение 7. Это условие, хотя оно и максимизирует эффективность удаления отрицательно заряженных оксианионов мышьяка, ограничивает как способ, так и связывание положительно заряженных катионов ртути вследствие электростатического отталкивания.
Настоящее изобретение основано на новом подходе к способу синтеза четырехвалентного фероксигита марганца (Fe1-xMnxOOH, при 0,05<x<0,25), который имеет в качестве основной характеристики отрицательно заряженную поверхность (изоэлектрическая точка менее 5,5) и высокую эффективность удаления ртути из воды при сохранении окислительной способности и низкой себестоимости. Для этой цели, получение осуществляют в двухступенчатом проточном реакторе непрерывного действия в щелочных условиях (pH от 7 до 12) и условиях сильного окисления.
Настоящее изобретение решает вышеуказанные проблемы следующим образом:
- Материал обладает очень высокой способностью поглощения ртути из воды, и в то же время способен снижать остаточную концентрацию после обработки ниже допустимого предела, составляющего 1 мкг/л.
- Материал синтезируют в проточном реакторе непрерывного действия с высокой производительностью из недорогого сырья при температуре окружающей среды. Синтез в щелочных условиях незначительно влияет на стоимость из-за увеличения количества добавляемого основного раствора по сравнению с соответствующим материалом, раскрытым в WO/2012/042282.
- Получение материала в щелочной среде (при повышенной концентрации ОН-) обеспечивает высокую плотность отрицательных зарядов на его поверхности и в результате высокую адсорбционную емкость в отношении положительно заряженных форм ртути, преобладающих в воде.
- Окислительный потенциал, обусловленный присутствием четырехвалентного марганца, способствует полному окислению элементарной ртути в отработанных газах, а также в природном газе на месте добычи, и поглощения ртути в виде Hg2+. Таким образом, достигается максимальная эффективность удаления на единицу массы адсорбента, но в то же время данное явление необратимо, а выщелачивание ртути в окружающую среду практически невозможно.
Настоящее изобретение может быть полностью понято из нижеследующего описания способа синтеза, фигур и примеров осуществления способа синтеза абсорбирующего материала.
Прилагаемые фигуры описывают:
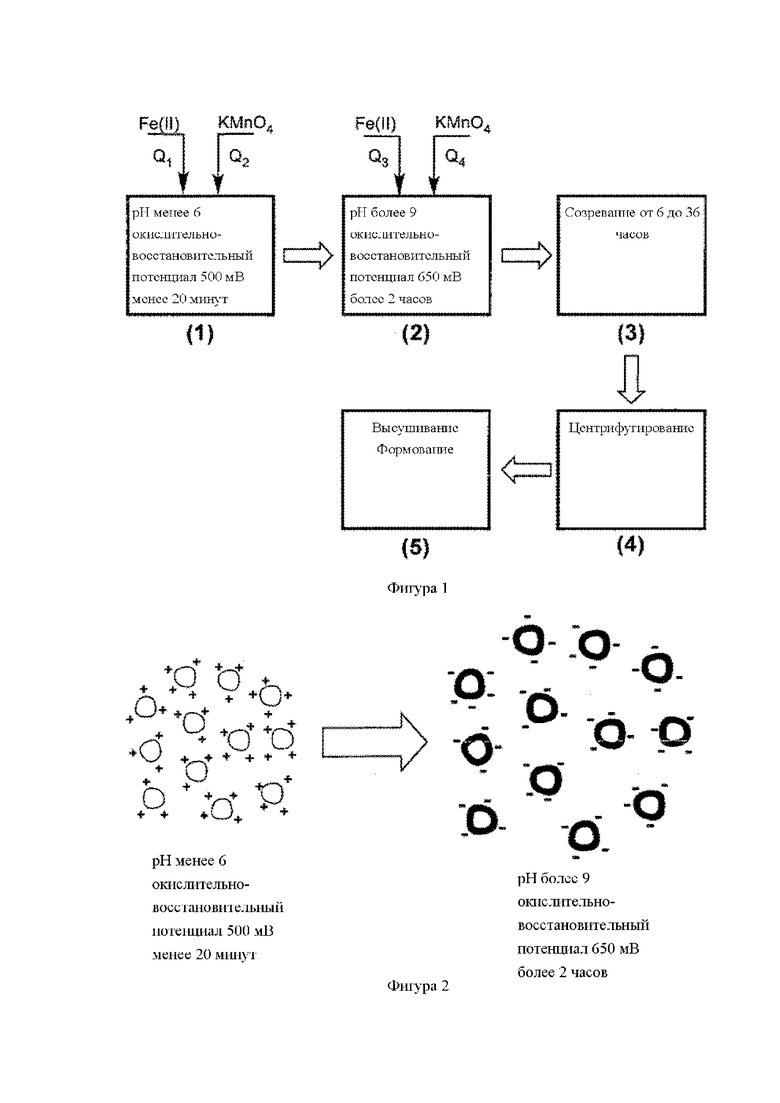
- Блок схему способа синтеза адсорбирующего материала в соответствии с описанным способом (Фигура 1).
- Схему способа выращивания гранул материала на двух стадиях реакции (Фигура 2).
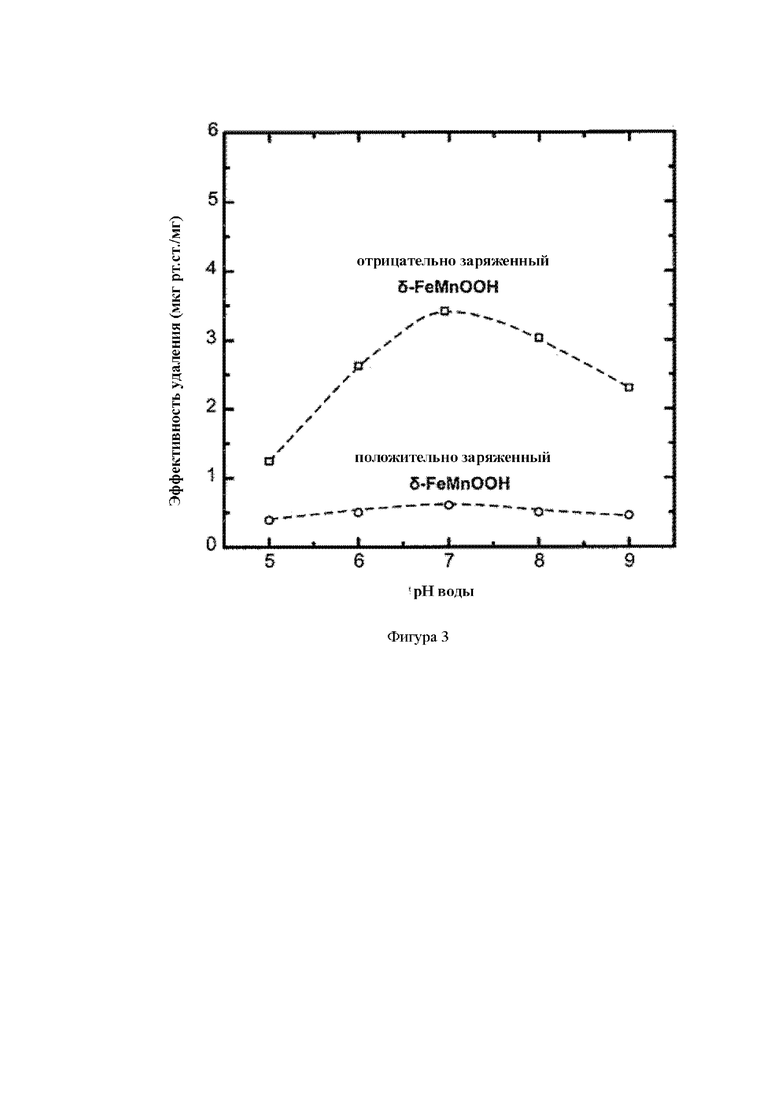
- График корреляции адсорбционной емкости для ртути в воде с различными значениями pH (от 5 до 9), при достижении остаточной концентрации до предела, составляющего 1 мкг/л, отрицательно заряженного δ-Fe0,75Mn0,25ООH (значение pH конечного синтеза составляет 9) по сравнению с материалом, полученным полностью в кислой среде (pH 4) (Фигура 3).
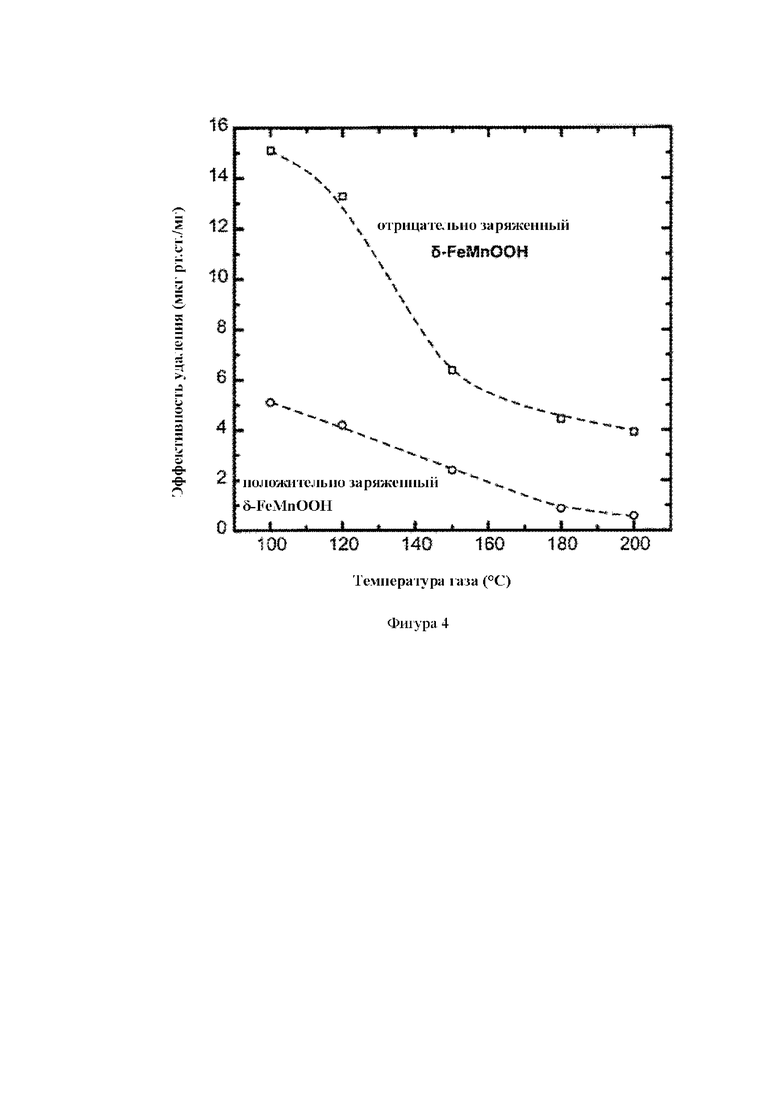
- График корреляции адсорбционной емкости в отношении Hg0 отрицательно заряженного δ-Fe0,75Mn0,25ООH (значение pH конечного синтеза составляет 9) при остаточной концентрации, равной пределу, составляющим 50 мкг/м3, в зависимости от температуры газового потока, по сравнению с материалом, полученным полностью в кислой среде (рН 4) (Фигура 4).
- График корреляции адсорбционной емкости для ртути в воде с различными значениями pH (от 5 до 9), при достижении остаточной концентрации до предела, составляющего 1 мкг/л, отрицательно заряженного δ-Fe0,75Mn0,25ООH (значение pH конечной композиции составляет 9) по сравнению с материалом, полученным полностью в кислой среде (pH 4) (Фигура 3).
- График корреляции адсорбционной емкости Hg0 отрицательно заряженного δ-Fe0,75Mn0,25ООH (значение pH конечной композиции составляет 9) при остаточной концентрации, равной пределу, составляющему 50 мкг/м3, в зависимости от температуры газового потока, по сравнению с материалом, полученным полностью в кислой среде (рН 4) (Фигура 4).
Целью настоящего изобретения является получение материала на основе четырехвалентного фероксигита марганца[δ-Fe(1-x)MnxOOH, при 0,05<x<0,25] с изоэлектрической точкой менее 5,5 и высокой плотностью отрицательных зарядов на его поверхности (более или равно 1,5 ммоль H+/г), обеспечивающей высокую адсорбционную емкость в отношении ртути, содержащейся в воде, а также высокую адсорбционную емкость в отношении других тяжелых металлов с валентностью большей или равной +2. Данная цель достигнута способом реакции солей Fe(II) и Mn(VII) в двухступенчатых проточных реакторах непрерывного действия, следующими реакциями:
- В первом реакторе соли Fe(II), которые используют в качестве источника железа, осаждают с помощью KMnО4 в среде от слабокислой до нейтральной для осуществления реакции образования зародыша δ-Fe(1-x)MnxOOH. рH доводят до постоянного значения от 5до 6, добавляя раствор одного из реагентов NaOH, NaHCO3, Na2CO3, KOH, KHCО3, K2CO3, в то время как высокий окислительно-восстановительный потенциал регулируют до постоянного значения 500±50 мВ добавлением KMnО4, который используют в качестве источника марганца. С соответствующим регулированием скорости потоков FeSO4 или FeCl2 и KMnO4, время реакции в первом реакторе не превышает 20 мин, что позволяет образовывать центр фероксигита марганца, но не полного образования положительной поверхностной структуры.
Во втором реакторе для достижения слабощелочных условий значение pH повышают в диапазоне от 9 до 10, добавлением NaOH или KOH, в то время как окислительно-восстановительный потенциал поддерживают в дипазоне 650±50 мВ добавлением KMnО4, с соответствующим регулированием скорости потоков FeSO4 или FeCl2 и KMnO4, так что реакция роста нанокристаллов четырехвалентного фероксигита марганца в среде с высоким pH и окислительно-восстановительным потенциалом приведет к увеличению отрицательного поверхностного заряда, который необходим для поглощения положительно заряженных ионов, таких как ртуть и другие тяжелые металлы.
- Затем осуществляют процесс созревания в резервуаре для перемешивания, где формируются гранулы неправильной формы с удельной поверхностью от 100 м2/г до 300 м2/г.
Более конкретно, способ синтеза однофазного адсорбента на основе четырехвалентного фероксигита марганца, где от 0,05 до 25 % железа изоморфно замещено атомами марганца, с высоким отрицательным зарядом при значении рН природных вод, соответствующего изоэлектрической точке ниже 5,5, и с удельной поверхностью от 100 до 300 м2/г, осуществляют следующим образом:
Применяют два проточных реактора непрерывного действия с мешалкой, расположенных последовательно. Время удержания в первом реакторе не превышает 20 мин (фигура 1), а во втором реакторе составляет по меньшей мере 2 часа. Количество полученного продукта зависит от потока реагентов железа и марганца Q1, Q2 в первом реакторе и Q3, Q4 и Q5 во втором реакторе, соответственно. Потоки Q3 и Q4 могут в 0-5 раз превосходить потоки Q1 и Q2, соответственно.
В реактор (1) непрерывным потоком одновременно добавляют водный раствор FeSО4 или FeCl2 в концентрации от 1 до 50 г/л и водный раствор KMnО4 в концентрации от 1 до 20 г/л. Контроль отношения скорости потоков растворов Fe(II) и KMnО4 осуществляют путем достижения требуемого окислительно-восстановительного потенциала 500±50 мВ, который необходим для образования зародыша типа Fe(1-x)MnxOOH с процентным содержанием Mn(IV) в диапазоне 12±1 мас.%. Продукт реакции поступает в реактор (2) и добавляют новый раствор FeSО4 или FeCl2 в концентрации от 1 до 50 г/л и раствор KMnО4 в концентрации от 1 до 20 г/л. Контроль отношения потоков растворов Fe(II) и KMnО4 осуществляют путем поддержания требуемого окислительно-восстановительного потенциала 650±50 мВ в реакторе (2). В обоих реакторах (1) и (2) на протяжении всей реакции значение рН регулируют в диапазоне от 5 до 6 в первом реакторе и от 9 до 10 во втором реакторе, добавлением одного или более щелочных реагентов NaOH, Na2CO3, KOH и K2CO3. Оптимальное осуществление достигают при значении рН реакции равном 9 и окислительно-восстановительном потенциале равном 650 мВ.
Выходящий поток из реактора (2) хранится в чане-сгустителе (3) при медленном перемешивании в течение от 6 до 36 часов, где достигается максимизация и балансировка отрицательного поверхностного заряда. В этих условиях созревание гранул приводит к образованию аморфных нанокристаллов, не способствуя их агломерации в состоянии вторичной структуры, что наблюдается при созревании в кислых условиях.
Осадок после сгущения обезвоживают центрифугированием (4) и либо формируют в гранулы размером от 250 до 2500 мкм и высушивают при температуре от 100 до 150 °С, либо сначала высушивают при температуре от 100 до 150 °С, а затем измельчают до гранул размером менее 50 мкм (5).
Адсорбционный материал можно применять для поглощения ртути из воды, а также других тяжелых металлов, таких как кадмий, свинец, никель, кобальт, ванадий, медь, марганец и железо, предпочтительно в адсорбционном слое. Применение данного материала относится к устройствам для очистки питьевой воды для бытового, промышленного и потребительского назначения, для обработки промышленных и коммунальных сточных вод, а также для очистки отработанных газов и природного газа.
Способом, описанным выше, четырехвалентный фероксигит марганца может быть образован при значении рН от 3 до 12. Однако при pH менее 8 адсорбционная емкость в отношении ртути и других тяжелых металлов резко снижается, поскольку постепенно начинает преобладать положительный поверхностный заряд, который отталкивает одноименные положительно заряженные ионы металлов.
В частности, отрицательно заряженный четырехвалентный фероксигит марганца в твердом состоянии имеет удельную площадь поверхности от 200 до 300 м2/г и размер гранулы от 250 до 2500 мкм. Его максимальная адсорбционная емкость (qmax) для воды со значением pH от 7 до 8 превышает 80 мкг рт.ст./мг при температуре 20 °C. В дополнение, скорость удаления элементарной ртути из газового потока до насыщения превышает 50 мкг/мг.
Способность (параметр q) материала поглощать ртуть из природных вод со значением pH от 6 до 8 и в то же время снижать остаточную концентрацию до предела, составляющему 1 мкг/л, показана на графике фигуры 3. Измерения относятся к фероксигиту марганца с процентом замещения 25 %. В данных экспериментах исследуемая вода была получена в соответствии со стандартом Национального Научного Фонда США (NSF), и ее состав соответствует характеристикам большинства типов природных вод, поскольку включает все параметры, которые препятствуют адсорбции ртути. В частности, включает 88,8 мг/л Na+, 40 мг/л Ca2+, 12,7 мг/л Mg2+, 183 мг/л HCО3-, 50 мг/л SO42-, 71 мг/л CI-, 2 мг/л N-NО3-, 1 мг/л F-, 0,04 мг/л P-PО43- и 20 мг/л SiO2. Было установлено, что значение q1 для удаления ртути из воды в соответствии с NSF при pH, равном 7, при 20 °C составляет 2,8 мкг/мг. Соответственно, удельная адсорбционная емкость (q50) для элементарной ртути из газового потока при 120 °C и при равновесной концентрации 50 мкг/м3, которая является пределом допустимого выброса, составляла 13,3 мкг/мг для времени контакта 0,1 с.
Пример 1 осуществления способа
Раствор FeSО4 Н2О в концентрации 45 г/л подают со скоростью потока Q1=2 м3/ч и смешивают с раствором KMnО4 в концентрации 15 г/л, который подают со скоростью потока Q2=2 м3/ч, в реакторе с мешалкой (1) объемом 1 м3. Скорость потока KMnО4 меняют таким образом, чтобы сохранять величину окислительно-восстановительного потенциала в реакторе (1) на уровне 500±50 мВ. рН реакционной смеси доводят до значения 5,5±0,1 добавлением 30 мас.% раствора NaOH.
Продукт реакции, выходящий из реактора (1), поступает в реактор с мешалкой (2) объемом 16 м3, где добавляют раствор FeSО4 H2O в концентрации 45 г/л со скоростью потока Q3=2 м3/ч и раствор KMnО4 в концентрации 15 г/л со скоростью потока Q4=2 м3/ч. Окислительно-восстановительный потенциал в реакторе (2) регулируют в диапазоне 650±50 мВ добавлением KMnО4, а pH доводят до значения 9±0,1 добавлением 30 мас.% раствора NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают с помощью центрифуги или фильтр-пресса, доводят до размера от 250 до 2500 мкм и высушивают при температуре 110 °C. Полученный материал имеет структуру Fe0,75Mn0,25OOH и валентность марганца составляет 4. При применении указанного материала в адсорбционной колонке с временем контакта 3 минуты, адсорбционная емкость в отношении Hg2+ составляет 2,8 мкг/мг в воде, соответствующей стандарту NSF с pH 7 и равновесной концентрацией 1 мкг/л.
Пример 2 осуществления способа
Раствор FeSО4 Н2О в концентрации 15 г/л подают со скоростью потока Q1=3 м3/ч и смешивают с раствором KMnО4 в концентрации 15 г/л, который подают со скоростью потока Q2=1 м3/ч, в реакторе с мешалкой (1) объемом 1 м3. Скорость потока KMnО4 регулируют таким образом, чтобы сохранять величину окислительно-восстановительного потенциала в реакторе (1) на уровне 500±50 мВ. рН реакционной смеси доводят до значения 5,5±0,1 добавлением 5 мас.% раствора K2CO3.
Продукт реакции, выходящий из реактора (1), поступает в реактор с мешалкой (2) объемом 32 м3, где добавляют раствор FeSО4 H2O в концентрации 15 г/л со скоростью потока Q3=9 м3/ч и раствор KMnО4 в концентрации 15 г/л со скоростью потока Q4=3 м3/ч. Окислительно-восстановительный потенциал в реакторе (2) регулируют в диапазоне 650±50 мВ добавлением KMnО4, а pH доводят до значения 9±0,1 добавлением 30 мас.% раствора KOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают с помощью центрифуги или фильтр-пресса, доводят до размера от 250 до 2500 мкм и высушивают при температуре 110 °C. Полученный материал имеет структуру Fe0,75Mn0,25OOH и валентность марганца составляет 4. При применении указанного материала в адсорбционной колонке с временем контакта 3 минуты, адсорбционная емкость в отношении Hg2+ составляет 2,8 мкг/мг в воде, соответствующей стандарту NSF с pH 7 и равновесной концентрацией 1 мкг/л.
Пример 3 осуществления способа
Раствор FeSО4 Н2О в концентрации 30 г/л подают со скоростью потока Q1=4 м3/ч и смешивают с раствором KMnО4 в концентрации 20 г/л, который подают со скоростью потока Q2=2 м3/ч, в реакторе с мешалкой (1) объемом 2 м3. Скорость потока KMnО4 регулируют таким образом, чтобы сохранять величину окислительно-восстановительного потенциала в реакторе (1) на уровне 500±50 мВ. рН реакционной смеси доводят до значения 5,5±0,1 добавлением 30 мас.% раствора NaOH.
Продукт реакции, выходящий из реактора (1), поступает в реактор с мешалкой (2) объемом 24 м3, где добавляют раствор FeSО4 H2O в концентрации 30 г/л, который подают со скоростью потока Q3=4 м3/ч и раствор KMnО4 в концентрации 20 г/л, который подают со скоростью потока Q4=2 м3/ч. Окислительно-восстановительный потенциал в реакторе (2) регулируют в диапазоне 650±50 мВ добавлением KMnО4, а pH доводят до значения 9±0,1 добавлением 30 мас.% раствора NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при перемешивании, затем его механически обезвоживают с помощью центрифуги или фильтр-пресса, доводят до размера менее 50 мкм и высушивают при температуре 110 °C. Полученный материал имеет структуру Fe0,75Mn0,25OOH и валентность марганца составляет 4. При применении указанного материала в адсорбционной колонке с временем контакта 0,01 секунды, адсорбционная емкость в отношении Hg2+ составляет 13,3 мкг/мг при равновесной концентрации 50 мкг/м3 в потоке газообразного азота.
Пример 4 осуществления способа
Раствор FeCl2 в концентрации 36 г/л подают со скоростью потока Q1=12 м3/ч и смешивают с раствором KMnО4 в концентрации 15 г/л, который подаюь со скоростью потока Q2=4 м3/ч, в реакторе с мешалкой (1) объемом 5 м3. Скорость потока KMnО4 регулируют таким образом, чтобы сохранять величину окислительно-восстановительного потенциала в реакторе (1) на уровне 500±50 мВ.
Продукт реакции, выходящий из реактора (1), поступает в реактор с мешалкой (2) объемом 16 м3, где добавляют раствор FeSО4 H2O в концентрации 45 г/л, который подают со скоростью потока Q3=6 м3/ч и раствор KMnО4 в концентрации 15 г/л, который подают со скоростью потока Q4=2 м3/ч. Окислительно-восстановительный потенциал в реакторе (2) регулируют в диапазоне 650±50 мВ добавлением KMnО4, а pH доводят до значения 9±0,1 добавлением 30 мас.% раствора NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при перемешивании, затем его механически обезвоживают с помощью центрифуги или фильтр-пресса, высушивают при температуре 110 °C и доводят до размера менее 50 мкм. Полученный материал имеет структуру Fe0,75Mn0,25OOH и валентность марганца составляет 4. Применение указанного материала путем инжекции в поток газообразного азота, содержащего Hg0 до 400 мкг/м3, привело к снижению концентрации ртути ниже предела допустимых выбросов 50 мкг/м3.
Пример осуществления способа 5
Осуществляют способ, описанный в примере 3, за исключением того, что в реактор (2) не добавляют дополнительные реагенты. Полученный материал имеет структуру Fe0,75Mn0,25OOH и валентность марганца составляет 4. При применении указанного материала в адсорбционной колонке с временем контакта 0,01 секунды, адсорбционная емкость в отношении элементарной ртути Hg0 составляет 10,6 мкг/мг при равновесной концентрации 50 мкг/м3 в потоке газообразного азота при температуре 120 °C.
Способ, описанный данным изобретением, осуществляют в лабораторных или промышленных масштабах в зависимости от производительности проточного реактора непрерывного действия.
Продукт, полученный способом получения по настоящему изобретению, может применяться для поглощения ртути и других тяжелых металлов, таких как кадмий, свинец, никель, кобальт, ванадий, медь, марганец и железо, из водного раствора или элементарной ртути из газового потока, предпочтительно в адсорбционном слое или в виде порошка в распылительной системе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СИНТЕЗА ЧЕТЫРЕХВАЛЕНТНОГО ФЕРОКСИГИТА МАРГАНЦА ДЛЯ УДАЛЕНИЯ МЫШЬЯКА ИЗ ВОДЫ | 2011 |
|
RU2587085C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦИНКА | 2002 |
|
RU2298585C9 |
| СПОСОБ УДАЛЕНИЯ БАРИЯ ИЗ ВОДЫ | 2009 |
|
RU2524230C2 |
| МИКРОБИОЛОГИЧЕСКИЙ СПОСОБ ТРАНСМУТАЦИИ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ПРЕВРАЩЕНИЯ ИЗОТОПОВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ | 2014 |
|
RU2563511C2 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ УГЛЕРОД-КРЕМНЕЗЕМИСТЫХ ЧЕРНОСЛАНЦЕВЫХ РУД | 2011 |
|
RU2477327C1 |
| СПОСОБ ЙОД-ЙОДИДНОЙ ПЕРЕРАБОТКИ ЗОЛОТОСОДЕРЖАЩЕГО СЫРЬЯ | 2019 |
|
RU2702250C1 |
| ОРГАНИЧЕСКИ МОДИФИЦИРОВАННЫЕ МИНЕРАЛЬНЫЕ МИКРОЧАСТИЦЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2790024C2 |
| СПОСОБ ОБРАБОТКИ СТОЧНЫХ ВОД | 2018 |
|
RU2743954C1 |
| СПОСОБ БЕЗРЕАГЕНТНОГО ИЗМЕНЕНИЯ ФИЗИКО-ХИМИЧЕСКИХ СВОЙСТВ ВОДЫ И/ИЛИ ВОДНЫХ РАСТВОРОВ | 2000 |
|
RU2155717C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛИЗИРУЮЩЕГО РАСТВОРА | 1999 |
|
RU2166335C1 |
Изобретение относится к области химической инженерии, в частности к технологии очистки воды твердыми адсорбентами. В частности, изобретение относится к способу синтеза абсорбирующего материала, состоящего из фазового четырехвалентного фероксигита марганца δ-Fe(1-x)MnxOOH с отрицательно заряженной поверхностью гранулы, в которой от 0,05 до 25% железа изоморфно замещено атомами марганца. Получение осуществляют в двух проточных реакторах непрерывного действия с мешалкой, расположенных последовательно, при слабокислых условиях в первом реакторе (pH от 5 до 6) и слабощелочных условиях во втором реакторе (pH от 9 до 10) и окислительно-восстановительном потенциале от 600 до 700 мВ. Материал может быть применен для поглощения ртути, а также других тяжелых металлов из потоков воды и горячего газа. Обеспечивается высокая эффективность удаления ртути из воды при сохранении окислительной способности и низкой себестоимости. 4 н. и 3 з.п. ф-лы, 4 ил., 5 пр.
1. Способ синтеза четырехвалентного фероксигита марганца, который представляет собой δ-Fe(1-x)MnxOOH, где x составляет от 0,05 до 0,25, характеризующийся тем, что способ осуществляют в двух проточных реакторах непрерывного действия с мешалкой, расположенных последовательно, при слабокислых условиях в первом реакторе и слабощелочных условиях во втором реакторе и высоком окислительно-восстановительном потенциале для получения материала с высокой плотностью отрицательных зарядов на поверхности, который выполняют посредством следующих стадий:
i) для осуществления реакции образования зародыша δ-Fe(1-x)MnxOOH в реактор (1) в качестве источника железа добавляют FeSО4 или FeCl2 в концентрации от 1 до 50 г/л и в качестве источника марганца добавляют KMnО4 в концентрации от 1 до 20 г/л, рН доводят до слабокислого значения в диапазоне от 5 до 6 добавлением одного или более чем одного из реагентов NaOH, NaHCO3, Na2CO3, KOH, KHCО3, K2CO3, в то же время окислительно-восстановительный потенциал доводят до значения в диапазоне от 450 до 550 мВ с соответствующим регулированием скорости потоков FeSО4 или FeCl2 и KMnO4, затем
ii) реакция роста нанокристаллов с отрицательно заряженной поверхностью продолжается в реакторе (2) посредством дополнительного добавления реагентов FeSО4 или FeCl2 и KMnO4, pH в реакторе (2) доводят до щелочного значения в диапазоне от 9 до 10 добавлением одного или комбинации более чем одного из реагентов NaOH, KOH и в то же время окислительно-восстановительный потенциал доводят до значения в диапазоне от 600 до 700 мВ с соответствующим регулированием скорости потоков FeSО4 или FeCl2 и KMnO4, и
iii) время удержания реакции составляет максимум 20 минут в реакторе (1) и по меньшей мере 2 часа в реакторе (2), и
iv) продукт, выходящий из реактора (2), направляют в чан-сгуститель (3), где при медленном перемешивании в течение от 6 до 36 часов формируются гранулы неправильной формы с удельной поверхностью от 100 м2/г до 300 м2/г, высоким отрицательным поверхностным зарядом, который представляет собой более 1,5 ммоль Н+/г, и изоэлектрической точкой менее 5,5.
2. Способ по п. 1, характеризующийся тем, что оптимального осуществления достигают при значении рН реакции, равном 9, и окислительно-восстановительном потенциале, равном 650 мВ.
3. Способ по п. 1 или 2, характеризующийся тем, что полученный материал подвергают механическому обезвоживанию (4), формированию в гранулы размером предпочтительно от 250 до 2500 мкм и высушиванию при температуре от 100 до 150 °С (5).
4. Способ по п. 1 или 2, характеризующийся тем, что материал, полученный после осуществления способа, механически обезвоживают (4), высушивают при температуре от 100 до 150 °С и формируют в гранулы размером предпочтительно менее 50 мкм (5).
5. Однофазный адсорбирующий материал на основе отрицательно заряженного четырехвалентного фероксигита марганца, который представляет собой δ-Fe(1-x)MnxOOH, полученный согласно способу по пп. 1-4, характеризующийся тем, что от 0,05 до 25 % железа изоморфно замещено атомами марганца, с удельной поверхностью от 100 до 300 м2/г, плотностью отрицательного поверхностного заряда более 1,5 ммоль H+/г и изоэлектрической точкой менее 5,5.
6. Применение адсорбирующего материала по п. 5 для поглощения ртути и других тяжелых металлов, таких как кадмий, свинец, никель, кобальт, ванадий, медь и марганец, из воды в адсорбционном слое.
7. Применение адсорбирующего материала по п. 5 для поглощения ртути и других тяжелых металлов, таких как кадмий, свинец, никель, кобальт, ванадий, медь и марганец, из отработанных газов и природного газа в адсорбционном слое или в виде порошка в распылительной системе.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| СИСТЕМА ДЛЯ ЗАЩИТЫ ПОВЕРХНОСТЕЙ НАГРЕВА ПАРОПЕРЕГРЕВАТЕЛЯ ОТ ПЕРЕГРЕВА ПРИ УВЕЛИЧЕНИИ ПОДАЧИ ТОПЛИВА В ТОПКУ ПАРОВОГО КОТЛА | 2000 |
|
RU2168677C1 |
| RU 2009132501 A, 10.03.2011 | |||
| Способ очистки газов от ртути | 1990 |
|
SU1747129A1 |
Авторы
Даты
2021-03-16—Публикация
2017-07-12—Подача