Изобретение относится к области химической инженерии, в частности к технологии очистки воды твердыми абсорбентами. В современном уровне техники твердые адсорбенты применяют как заполняющую среду в слое колонки для удаления адсорбцией тяжелых металлов и в особенности мышьяка из питьевой воды и отходов.
Присутствие мышьяка (As) в питьевой воде является одной из наиболее важных и наиболее распространенных проблем загрязнения воды. Доказано, что долгосрочное потребление воды с повышенной концентрацией мышьяка связано с риском сердечно-сосудистых заболеваний, сахарного диабета, также как и рака кожи, легких и мочевого пузыря, и, как следствие, к увеличению смертности. Предел общей концентрации мышьяка в питьевой воде был установлен до значения 10 мкг/л с 2001 года в США и с 1998 года в странах Европейского Союза. Появление мышьяка в основном является проблемой, возникающей в подземных водах, образующихся из природных источников (аллювиальных отложений и минеральных вод) или в результате антропогенной деятельности. Как правило, мышьяк встречается в форме пятивалентных As(V) оксианионов [H2AsO4 -/HAsO4 2-] или в незаряженной форме трехвалентного As(III) H3AsO3 в соотношении, определяющемся окислительно-восстановительными свойствами среды и кислотностью (pH). В частности, окислительные условия способствуют присутствию отрицательно заряженных оксианионов As(V), в то время как в восстановительной среде доминирует незаряженная форма As(III). Степень окисления мышьяка напрямую связана с его токсичностью, так как As(III) в 60 раз более токсичен, чем As(V).
Способы удаления мышьяка подразделяют на относительно селективные и неселективные. Неселективные (нанофильтрация, обратный осмос) не являются предпочтительными по причине их высокой стоимости и изменения состава воды. Среди относительно селективных способов удаления мышьяка основными являются соосаждение с трехвалентным железом и адсорбция. Более конкретно, несмотря на то, что соосаждение имеет относительно низкую стоимость эксплуатации, оно требует высокоспециализированного контроля работы, в том числе контролируемого добавления такого химического реагента, как трехвалентное железо, а также сгущения и обезвоживания полученного осадка, содержащего удаленный мышьяк. По этой причине применение расходуемых адсорбентов в настоящее время является основной тенденцией, так как представляет собой наиболее простой способ удаления мышьяка.
Большинство способов адсорбции мышьяка относятся к применению слоев колонки, включающих активированный оксид алюминия (Al2O3), оксид титана (TiO2) или оксигидроксиды железа. В последние годы, как правило, предпочтительным является применение оксигидроксидов железа в адсорбционном слое по следующим причинам:
- удовлетворительная адсорбционная емкость, которую они демонстрируют
- снижение концентрации мышьяка до уровня ниже 1 мкг/л
- процесс требует минимального контроля в течение операции
- выполнение требований выщелачивания для безопасной утилизации насыщенных оксигидроксидов на свалках в качестве инертных отходов
Однако оксигидроксиды железа способны удалить только ионные формы As(V) [H2AsO4 -/HAsO4 2-], в то время как их вклад по сравнению с незаряженными формами As(III) в составе H3AsO3 очень ограничен. Потребность в удалении As(III) делает оксигидроксиды железа менее конкурентоспособными, поскольку стоимость очистки становится значительно выше по причине низкой адсорбционной емкости в отношении As(III), а также необходимости добавления дополнительного этапа окисления для As(III). Главным образом существуют два подхода к преодолению проблемы удаления As(III) с помощью адсорбентов:
1. применение двух соединений, первое из которых (MnO2) окисляет As(III) до As(V), а второе (оксигидроксид железа) сорбирует полученный As(V),
2. применение смешанного соединения (железо/трехвалентный марганцевый оксигидроксид), которое действует как окисляющий реагент на As(III) и одновременно как адсорбирующая среда для образовавшегося As(V).
В рамках первого подхода для эффективного удаления As(III), как и As(V), применяют двухфазные адсорбенты на основе оксигидроксида железа и оксида марганца (MnO2). Роль MnO2 состоит в окислении As(III) до As(V), который за тем адсорбируется и связывается оксигидроксидом железа. Процедурой получения таких материалов является осаждение марганца в форме MnO2 путем восстановления KMnO4 в щелочной среде (pH>7) и его присоединение к оксигидроксиду железа.
Соответственно ЕР 2168677 описывает методику синтеза и применение способа удаления As(III) двухфазным железо-марганцевым оксидом. Выработка данного материала происходит на месте эксплуатации на носителе в результате реакции сульфата железа (FeSO4), или треххлористого железа (FeCl3), или сульфата марганца (MnSO4) с перманганатом калия (KMnO4). Данный патент относится к синтезу смеси двух различных материалов: гидроксида железа и MnO2. Данный адсорбент успешно окисляет As(III) с помощью MnO2 и адсорбирует полученный As(V) с помощью фазы гидроксида железа. Дополнительная информация, полученная тем же исследователем, представлена в публикациях G. Zhang et al., Water Research 41 (2007) 1921 и G. Zhang et al., Journal of Hazardous Materials 168 (2009) 820, где способ синтеза двухфазного железо-марганцевого оксида описан реакцией FeSO4 с KMnO4 при pH 7-8, протекающей в реакторе периодического действия. Структуру продукта характеризуют как смесь оксигидроксида железа и MnO2 в аморфном состоянии. Окислительная способность MnO2 позволяет улучшить адсорбцию As(III) оксигидроксидом железа, хотя максимальная адсорбционная емкость, по-видимому, намного ниже в отношении As(V), чем в отношении As(III). Окончательно материалы, о которых сообщается в трех вышеуказанных документах, содержат MnO2, адсорбционная емкость которого в отношении As(V) является очень низкой, и увеличение его процентного содержания при синтезе двухфазного оксида является причинной снижения общей адсорбционной емкости и увеличения стоимости очистки.
Аналогично, в публикации Н. Zeng et al., Water Research, 42 (2008) 4629 представлено исследование адсорбента на основе оксигидроксида железа, содержащего около 20% марганца. Материал состоит из двух отдельных фаз: оксигидроксид железа (ферригидрит) и MnO2 в форме бернессита. Кроме того, марганцевая фаза расположена во внутренней части материала далеко от поверхности, таким образом, происходит контакт с очищенной водой, а также ожидаемое окислительное действие является ограниченным.
Способ удаления As(III), в котором в качестве первого этапа применяют слой колонки, содержащий MnO2, для окисления As(III) до As(V) с последующим этапом осаждения с Fe(III), при котором происходит связывание As(V), описан в US 2010/0051555. Однако применение данного способа является достаточно сложным и требующим контроля двух основных способов удаления мышьяка: процесса адсорбции и гораздо более сложного осаждения с Fe(III). Для второго способа требуется (1) контролируемое добавление химического реагента Fe(III), (2) стадия фильтрации осадка, (3) еще одна сложная стадия обработки железного осадка (содержащего удаленный мышьяк) со сгущением и механическим обезвоживанием.
При втором подходе удаление мышьяка осуществляют трехвалентным марганцем, замещающим оксигидроксид железа. В целом, в связанных по тематике публикациях описан процесс приготовления таких материалов в результате периодических процессов при щелочных условиях (pH-12), высоких температурах и длительном времени реакции (>1 дня) с тем, чтобы сделать возможным окисление Mn(II) до Mn(III) барботирующим атмосферным кислородом и включение Mn(III) в структуру оксигидроксида железа.
Применяя данный способ в публикации S.S. Mohanty et al., Chemistry and Ecology, 24 (2008) 23 исследовали ряд марганцевых ферригидритов, в которых атомы железа замещены на атомы марганца в процентном соотношении от 0 до 100%. Для синтеза два раствора - марганца и трехвалентного железа соосаждались при значении pH около 12 и барботировании кислородом при температуре 70°C при длительности реакции 24 часа. Периодический режим, высокие значения pH и температуры, а также длительность реакции ответственны за повышенную энергию и расход реагентов, а также за низкую производительность процесса. Очень мало информации предоставлено для реагентов, и поскольку в соответствии с конкретными условиями реакции (барботаж кислорода, pH 12) параллельного осаждения Fe(III) и окисления-осаждения Mn(II) не ожидается (М. Stumm and J. Morgan, Aquatic Chemistry: An introduction emphasizing chemical equilibria in natural waters 2nd Ed., 1981), не известно, будет ли образовываться железо-марганцевый оксигидроксид. Более того, отсутствуют какие-либо измерения, подтверждающие наличие фазы железо-марганцевого гидроксида. Однако наиболее важным недостатком данных материалов являлась низкая адсорбционная емкость (q10) при равновесной концентрации, равной максимальному уровню загрязнения 10 мкг/л, что составляет не более чем 1 мкг As(V)/Mr при pH 7, при отсутствии данных по адсорбционной емкости в отношении As(III), который характерен для твердых веществ данной категории.
В публикации Х Sun et al., Clays and Clay Minerals, 47 (1999) 474 получали оксигидроксид железа (гетит), в котором атомы железа частично замещены атомами марганца (0-10%). Марганцевый гетит получали при периодическом режиме путем соосаждения трехвалентного нитрата железа [Fe(NO3)3] и двухвалентного нитрата марганца в сильнощелочной среде в присутствии 0,3 М NaOH и с длительным химическим созреванием в течение 15 дней при высокой температуре 60°C для того, чтобы окислить Mn(II) до Mn(III) кислородом. В данной публикации с применением рентгеновской спектроскопии исследовали окисление As(III) вместе с восстановлением Mn(II). Результаты показали, что скорость окисления As(III) очень низкая, и, как было измерено при комнатной температуре, через 5 дней только 20% As(III) было окислено до As(V). Кроме того, окисление As(III) сочетается с восстановлением Mn(III) до растворимого Mn(II), что ухудшает качество очищенной воды.
В публикации Р. Lakshmipathiraj et al., Journal of Colloid and Interface Science, 304 (2006) 317 изучали адсорбционную способность в отношении трехвалентного и пятивалентного мышьяка, частично замещенного марганцем оксигидроксида железа в процентном соотношении 13% (Mn0,13Fe0,87OOH). Для его синтеза FeSO4 и MnSO4 применяли вместе с Na2CO3 и сурфактантом SLS при pH 10-12 для того, чтобы обеспечить условия для параллельного осаждения железа и марганца. При данных условиях и при барботировании кислородом образовывалась промежуточная зеленая ржавчинная карбонатная соль, после чего замещение атомов на Mn(III) приводило к образованию (Mn0,13Fe0,87OOH).
Восстановление Mn(III) в соответствии с реакцией:
2Mn3++As3+→2Mn2++As5+
приводит к выщелачиванию Mn(II) в очищенную воду. Представленные измерения демонстрируют, что адсорбционная емкость материала по сравнению с обычными адсорбентами на основе оксигидроксида железа на порядок ниже (qmax=5.72 мкг/мг) в отношении As(V) и в 2-3 раза ниже (qmax=4.58 мкг/мг) в отношении As(III) в дистиллированной воде при pH 7.
Синтез оксигидроксида железа, где атомы железа частично заменены на Mn(III), как описано в вышеуказанной публикации, имеет следующие недостатки:
- Высокая стоимость производства по причине применения периодического режима, а также по причине высокой температуры, сильнощелочного pH и длительного времени реакции в целях обеспечения окисления Mn(11) до Mn(III) мягким окислителем, таким как кислород.
- Получение оксигидроксидов при высоких значениях pH (высокой концентрации гидроксила) в присутствии ограниченного количества положительных зарядов на их поверхности, что влечет за собой низкую адсорбционную емкость относительно As(V) оксид-ионов.
- Низкая окислительная способность Mn(III) вместе с низкой скоростью окисления As(III) соответственно является причиной низкой адсорбции As(III).
- Помимо этого окисление As(III) посредством Mn(III) является причиной выщелачивания Mn(II) в очищенную воду.
Настоящее изобретение относится к способу синтеза адсорбционного материала, состоящего из однофазного четырехвалентного марганцевого фероксигита [Fe(1-x)MnxOOH, при 0,05<х<0,25], в котором от 0,05 до 25% атомов железа заменены атомами Mn(V) в проточном реакторе непрерывного действия при слабокислых условиях (pH 4-7) и высоком окислительно-восстановительном потенциале (300-800 мВ) с последующей стадией сгущения.
Настоящее изобретение решает указанные проблемы следующими способами:
- Адсорбент состоит из единственной фазы, которая способна эффективно адсорбировать как As(V) так и As(III), поскольку одна и та же структура способна окислять As(III) и затем адсорбировать его в единую структуру оксигидроксида.
- При этом окисление As(III) посредством Mn(IV) и, следовательно, адсорбция As(V) на оксигидроксид является очень быстрым способом. Кроме того, полученный Mn(III) остается в структуре фероксигита в трехвалентном состоянии без выщелачивания в воду.
- Его получение в кислой среде (высокой концентрации Н+) обеспечивает высокую плотность положительных зарядов на его поверхности и в результате высокую адсорбционную емкость в отношении оксид-ионов мышьяка.
- Получение в проточном реакторе непрерывного действия при слабокислых условиях и температуре окружающей среды обеспечивает высокую производительность при низкой стоимости и хорошем контроле параметров синтеза.
- Кроме того, легкий и точный контроль pH и, что еще более важно, окислительно-восстановительного потенциала позволяет получать материалы с варьированием замещения Fe на Mn в процентном соотношении, в диапазоне от 0,05 до 25%, что эквивалентно варьированию содержания марганца в диапазоне от 0,2 до 13% и содержанию железа от 50 до 35% в сухом материале соответственно. В зависимости от процента замещения Mn возможно контролировать процент конечной адсорбции As(III), сохраняя адсорбцию As(V) на высоком уровне.
Настоящее изобретение может быть понято из нижеследующего аналитического описания способа синтеза, фигур и примеров применения способа синтеза адсорбционного материала.
Прилагаемые фигуры описывают:
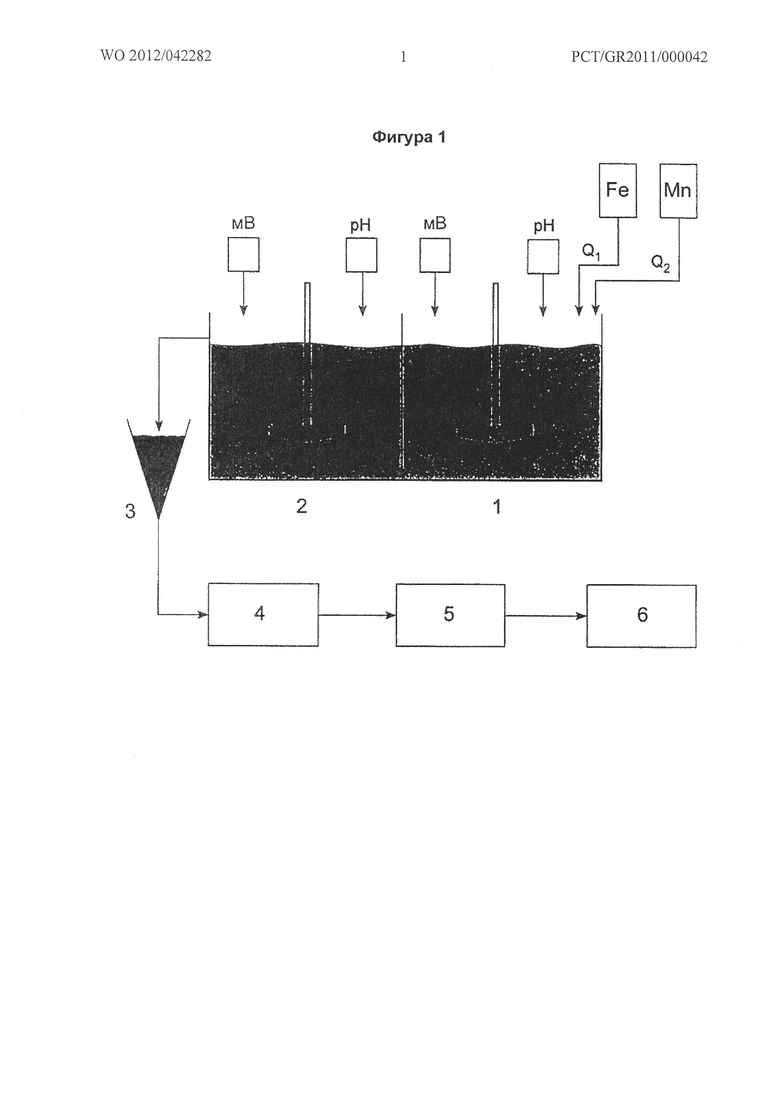
- Блок схема способа синтеза адсорбента в соответствии с описанным способом (Фигура 1).
- Схема способа выращивания гранул материала с полой архитектурой (Фигура 2).
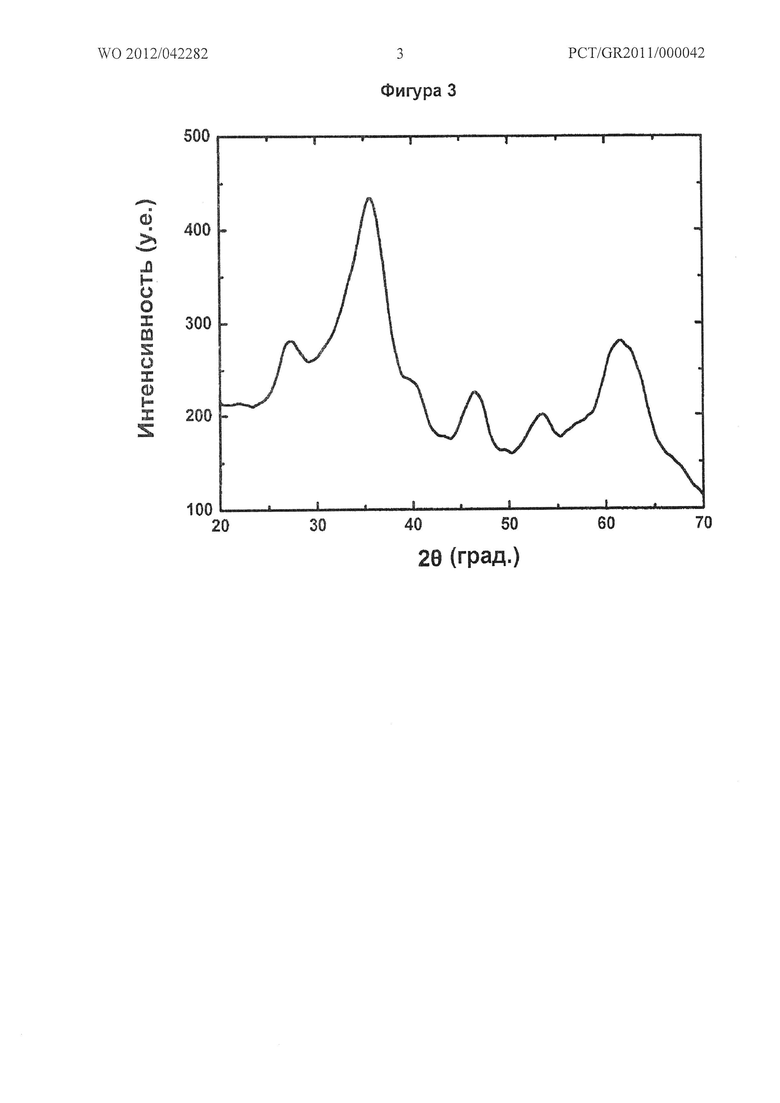
- График ДРЛ (дифракции рентгеновских лучей), который подтверждает, что структурой продукта является четырехвалентный марганцевый фероксигит (Фигура 3).
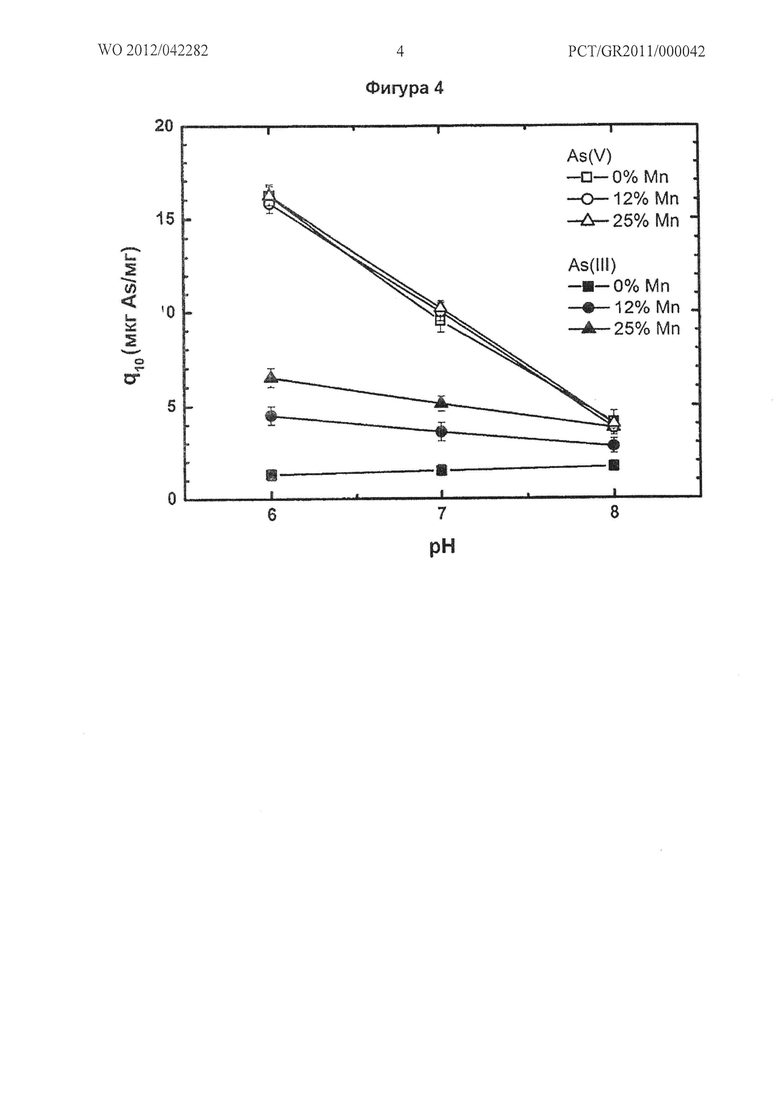
- График корреляции емкости адсорбента для As(III) и As(V) с процентом Mn и pH воды (Фигура 4).
Целью настоящего изобретения является получение адсорбента на основе четырехвалентного марганцевого фероксигита [Fe(1-x)MnxOOH, при 0,05<х<0,25] с полой сферической архитектурой, обеспечивающей высокую адсорбционную емкость в отношении мышьяка, в особенности в отношении As(III), а также других тяжелых металлов, содержащихся в воде. Данная цель достигается способом реакции солей Fe(II) и Mn(II) в двухступенчатом проточном реакторе непрерывного действия:
- в слабокислой среде, где pH доводят до постоянного значения в диапазоне 4-7 добавлением растворов NaOH, NaHCO3, Na2CO3, КОН, KHCO3, К2СО3
- и при управляемом высоком окислительно-восстановительном потенциале, доведенным до постоянного уровня в диапазоне 300-800 мВ добавлением сильных окислителей KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8
с последующим применением способа химического созревания в смесительном баке.
Более конкретно, способ синтеза адсорбента на основе четырехвалентного марганцевого фероксигита [Fe(1-x)MnxOOH, при 0,05<х<0,25] осуществляют следующим образом:
Применяют проточный реактор непрерывного действия с мешалкой с двумя ступенями (1) и (2) (Фигура 1). Время удержания в каждой ступени составляет по меньшей мере 30 минут. Количество полученного продукта зависит от потока железного и марганцевого реагентов Q1 и Q2 при условии времени удержания реакции по меньшей мере 30 минут для каждого из двух реакторов. В реактор (1) одновременно добавляют водный раствор FeSO4 или FeCl2 в концентрации 1-100 г/л и водный раствор KMnO4, или MnSO4, или MnCl2, или Mn(NO3)2 в концентрации 1-100 г/л. Контроль отношения потоков Fe(II) и Mn(VII) или Mn(II), а также концентрации раствора Mn позволяет получить материалы с процентным содержанием Mn(IV), варьирующим в пределах 0,2-13 масс. %, и имеющие структуру типа Fe(1-x)MnxOOH, при 0,05<х<0,25.
В обоих реакторах (1) и (2) во время реакции значение pH доводят до постоянного значения в диапазоне 4-7 с оптимальным значением pH от 5,5 до 6, добавлением одного или более щелочных реагентов NaOH, NaHCO3, Na2CO3, КОН, KHCO3, K2CO3. В то же время окислительно-восстановительный потенциал корректируют до постоянного уровня в диапазоне 300-800 мВ добавлением раствора одного или более сильных окислительных реагентов KMnO4, ClO2, NaClO2, (2KHSO5·KHSO4·K2SO4), Na2S2O8, K2S2O8, с оптимальным значением окислительно-восстановительного потенциала от 600 до 650 мВ при оптимальном значении pH.
Полученная смесь выходит из оттока реактора (2) и ее удерживают в чане-сгустителе при медленном перемешивании в течение 1-48 часов, с целью обеспечить преобразование геометрии гранул из неправильной формы в полую сферическую. Механизмом, объясняющим формирование полой сферической геометрии гранул, является первоначальное получение микропористых сфер материала, состоящих из агрегатов частиц разного размера, поглощение более мелких частиц, расположенных в центре, более крупными расположенными в оболочке гранулы, и в результате формирование пористой сферической гранулы с полостью (Фигура 2). Данный способ описан как механизм созревания по Отсвальду, и его выход и, как следствие, диаметр полостей зависит от времени удержания в чане-сгустителе.
Осадок после сгущения механически обезвоживают (4), формируют до размеров 250-2500 мкм (5) и высушивают (6) (Фигура 1).
Адсорбционный материал может быть применен для адсорбции всех форм мышьяка из воды, а также других тяжелых металлов, таких как ванадия, сурьмы, ртути, никеля и свинца, преимущественно в слое колонки. Применение данного материала относится к устройствам для очистки воды для бытового, промышленного и коммунального водоснабжения, а также очистки промышленных и коммунальных сточных вод.
В соответствии со способом, описанным выше, четырехвалентный марганцевый фероксигит может быть образован при диапазоне pH 4-9. Однако при pH выше 7 адсорбционная емкость в отношении As(III) и As(V) резко снижается.
На графике ДРЛ для материала с процентом замещения 25% (Fe0,75Mn0,25ООН), приведенном в Фигуре 3, был обнаружен оксигидроксид железа со структурой ферокситта, в котором атомы железа частично заменены на четырехвалентный марганец.
Корректировка окислительно-восстановительного потенциала до значений более 600 мВ не имеет серьезного влияния на адсорбционную емкость материала, но повышает стоимость получения в связи с потреблением окислителя. Наоборот, его корректировка до значений менее 300 мВ приводит к низкой валентности марганца [Mn(III)] в фероксигите, то есть более низкой адсорбционной емкости в отношении As(III).
Более конкретно, в состоянии твердого вещества четырехвалентный марганцевый фероксигит имеет удельную поверхность 100-300 м2/г и размер гранул 250-2500 мкм. Его максимальная адсорбционная емкость (qmax) при pH 6-8 и в среде 10 мМ NaCl составляет 48-87 мкг As(III)/мг и 62-117 мкг As(V)/мг.
Способность материала адсорбировать As(III) и As(V) из природной воды с pH 6-8 и в то же время снижать остаточную концентрацию до предела 10 мкг/л (параметра q10) показана на графике Фигуры 4. Измерения относятся к адсорбентам с процентом замещения 0%, 12% и 25%. В данном эксперименте исследуемая вода была получена в соответствии со стандартом NSF (National Science Foundation, Национального Научного Фонда США), и по своему составу она соответствует характеристике большинства типов природной воды, включая большинство параметров, влияющих на адсорбцию мышьяка. Состав воды, приготовленной по стандарту NSF, включает 88,8 мг/л Na+, 40 мг/л Са2+, 12,7 мг/л Mg2+, 183 мг/л HCO3 -, 50 мг/л SO4 2-, 71 мг/л Cl-, 2 мг/л NO3 --N, 1 мг/л F-, 0,04 мг/л PO4 3--Р и 20 мг/л SiO2. Максимальные значения q10 обнаруживаются при pH воды 6 в отношении As(V) при 18 мкг/мг для Fe0,88Mn0,12OOH, и в отношении As(III) при 7,5 мкг/мг для Fe0,75Mn0,25OOH. По-видимому, изменение содержания Mn(IV) в фероксигите серьезно не влияет на адсорбционную способность в отношении As(V), но, напротив, при уменьшении концентрации Mn(IV) адсорбционная емкость в отношении As(III) снижается до минимального значения, полученного для нулевой концентрации Mn(IV). Этот факт делает возможным получение фероксигита с композицией, соответствующей конкретным качествам очищенной воды в отношении соотношения концентраций [As(V)]/[As(III)].
Пример 1 применения способа
Раствор FeSO4 H2O в концентрации 45 г/л подводят потоком Q1=1 м3/ч и смешивают с раствором KMnO4 в концентрации 15 г/л при потоке Q2=1 м3/ч в реактор с мешалкой (1) объемом 2 м2. Поток KMnO4 регулируют таким образом, чтобы сохранить величину окислительно-восстановительного потенциала в диапазоне 625±25 мВ. pH реакционной смеси доводят до 5,5±0,1 добавлением раствора NaOH с концентрацией 30% масс./масс. Аналогичные окислительно-восстановительный потенциал и pH поддерживают во втором реакторе (2) путем добавления небольших количеств KMnO4 и NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают, например, с помощью центрифуги или фильтр-пресса, формируют до размера 250-2500 мкм и высушивают при температуре 110°C. Полученный продукт имеет тип структуры Fe0,75Mn0,26ООН и валентность марганца 4,0. Адсорбционная емкость в отношении As(V) составляет 11 мкг/мг, а в отношении As(III) 5 мкг/мг в воде, соответствующей стандарту NSF с pH 7,0.
Пример 2 применения способа
Раствор FeSO4 H2O в концентрации 45 г/л подводят потоком Q1=2 м3/ч и смешивают с раствором KMnO4 в концентрации 23 г/л при потоке Q2=0,5 м3/ч в реактор с мешалкой (2) объемом 2 м3. Окислительно-восстановительный потенциал доводят до значения в диапазоне 625±25 мВ добавлением раствора 2KHSO5·KHSO4·K2SO4 в концентрации 100 г/л. pH реакционной смеси доводят до 5,5±0,1 добавлением раствора NaOH с концентрацией 30% масс./масс. Аналогичные окислительно-восстановительный потенциал и pH поддерживаются во втором реакторе (2) путем добавления небольших количеств 2KHSO5·KHSO4·K2SO4 и NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают, например, с помощью центрифуги или фильтр-пресса, формируют до размера 250-2500 мкм и высушивают при температуре 110°C. Полученный продукт имеет тип структуры Fe0,88Mn0,12OOH и валентность марганца 4,0. Адсорбционная емкость в отношении As(V) составляет 11 мкг/мг, а в отношении As(III) 3,5 мкг/мг в воде, соответствующей стандарту NSF с pH 7,0.
Пример 3 применения способа
Раствор FeSO4 H2O в концентрации 40 г/л и MnSO4 H2O в концентрации 5,5 г/л подводят потоком Q1=20 м3/ч в реактор с мешалкой (1) объемом 20 м3. Окислительно-восстановительный потенциал доводят до значения в диапазоне 625±25 мВ добавлением раствора NaClO2 с концентрацией 25% масс./масс. pH реакционной смеси доводят до 5,5±0,1 добавлением раствора NaOH с концентрацией 30% масс./масс. Аналогичные окислительно-восстановительный потенциал и pH поддерживают во втором реакторе (2) путем добавления небольших количеств NaClO2 и NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают, например, с помощью центрифуги или фильтр-пресса, формируют до размера 250-2500 мкм и высушивают при температуре 110°C. Полученный продукт имеет тип структуры Fe0,88Mn0,12OOH и валентность марганца 4,0. Адсорбционная емкость в отношении As(V) составляет 11 мкг/мг, а в отношении As(III) 5 мкг/мг в воде, соответствующей стандарту NSF с pH 7,0.
Способ, который описывается данным изобретением, может применяться в лабораторных или промышленных масштабах в зависимости от производительности проточного реактора непрерывного действия.
Продукт, полученный описанным способом синтеза по данному изобретению, может применяться для адсорбции мышьяка, в особенности форм As(III), а также других тяжелых металлов, включая ванадий, сурьму, ртуть никель и свинец, предпочтительно в слое колонки или в форме дисперсного порошка.
Пример 4 применения способа
Раствор FeSO4 H2O в концентрации 40 г/л и MnSO4 H2O в концентрации 2,1 г/л подводят потоком Q1=20 м3/ч в реактор с мешалкой (1) объемом 20 м3. Окислительно-восстановительный потенциал доводят до значения в диапазоне 800±25 мВ добавлением раствора NaClO2 с концентрацией 25% масс./масс. рН реакционной смеси доводят до 4±0,1 путем добавления раствора NaOH с концентрацией 30% масс./масс. Аналогичные окислительно-восстановительный потенциал и рН поддерживают во втором реакторе (2) путем добавления небольших количеств NaClO2 и NaOH. Продукт из оттока реактора (2) поступает в чан-сгуститель, где его оставляют на 24 часа при медленном перемешивании, затем его механически обезвоживают, например, с помощью центрифуги или фильтр-пресса, формируют до размера 250-2500 мкм и высушивают при температуре 110°С. Полученный продукт имеет тип структуры Fe0,95Mn0,05OOH и валентность марганца 4,0. Адсорбционная емкость в отношении As(V) составляет 15 мкг/мг, а в отношении As(III) 3,5 мкг/мг в воде, соответствующей стандарту NSF с рН 7,0.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СИНТЕЗА ОТРИЦАТЕЛЬНО ЗАРЯЖЕННОГО ФЕРОКСИГИТА МАРГАНЦА ДЛЯ СЕЛЕКТИВНОГО УДАЛЕНИЯ РТУТИ ИЗ ВОДЫ | 2017 |
|
RU2744898C2 |
| МИКРОБИОЛОГИЧЕСКИЙ СПОСОБ ТРАНСМУТАЦИИ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ И ПРЕВРАЩЕНИЯ ИЗОТОПОВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ | 2014 |
|
RU2563511C2 |
| СПОСОБ ПЕРЕРАБОТКИ МАРГАНЦЕВОГО СЫРЬЯ | 1992 |
|
RU2054494C1 |
| СПОСОБ ОЧИСТКИ ВОДЫ ОТ СОЕДИНЕНИЙ МЫШЬЯКА | 2019 |
|
RU2725315C1 |
| КАТАЛИТИЧЕСКИЙ СОРБЕНТ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД | 2016 |
|
RU2617492C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ МЕТАЛЛИЧЕСКОГО ЦИНКА ИЗ ТВЕРДЫХ МЕТАЛЛУРГИЧЕСКИХ ОТХОДОВ | 2021 |
|
RU2830268C1 |
| СОРБЦИОННЫЙ МАТЕРИАЛ ДЛЯ ОЧИСТКИ ВОДНЫХ СРЕД ОТ ТЯЖЁЛЫХ МЕТАЛЛОВ | 2023 |
|
RU2838228C1 |
| СПОСОБ ХИМИЧЕСКОЙ ДЕЗАКТИВАЦИИ ОБОРУДОВАНИЯ АТОМНЫХ ЭЛЕКТРИЧЕСКИХ СТАНЦИЙ | 2007 |
|
RU2340965C1 |
| УСТРОЙСТВО ДЛЯ ФИЛЬТРАЦИИ ВОД РАЗЛИЧНОГО ГЕНЕЗИСА И СПОСОБ ПОДГОТОВКИ СОРБИРУЮЩЕГО МАТЕРИАЛА | 2011 |
|
RU2484021C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ ЦИНКА | 2002 |
|
RU2298585C9 |

Настоящее изобретение относится к способу синтеза адсорбционного материала, состоящего из однофазного четырехвалентного марганцевого фероксигита (δ-Fe(1-x)MnxOOH), в котором 0,05-25% железа изоморфно замещено атомами марганца. Синтез проводят в проточном реакторе непрерывного действия при слабокислых условиях (рН 4-7) и высоком окислительно-восстановительном потенциале (300-800 мВ). Полученный сорбент рекомендован для удаления как пятивалентного, так и трехвалентного мышьяка. 3 н. и 2 з.п. ф-лы, 4 ил., 4 пр.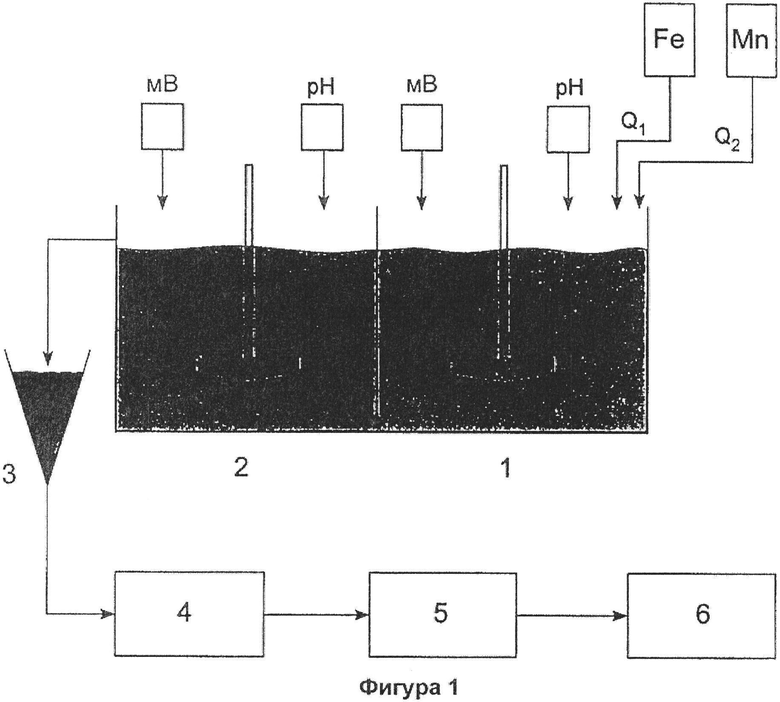
1. Способ синтеза четырехвалентного марганцевого фероксигита (δ-Fe(1-x)MnxOOH), где х составляет от 0,05 до 0,25, отличающийся тем, что его проводят в проточном реакторе непрерывного действия при слабокислых условиях и контролируемом окислительно-восстановительном потенциале и осуществляют посредством следующих стадий:
i) в реактор (1) в качестве источника железа добавляют FeSO4 или FeCl2, в качестве источника марганца добавляют KMnO4, или MnSO4, или MnCl2, или Mn(NO3)2 в концентрации 1-100 г/л, рН для реакции доводят до слабокислого значения в диапазоне 4-7 добавлением одного или более из следующих реагентов: NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3, в то же время окислительно-восстановительный потенциал доводят до значения в диапазоне 300-800 мВ добавлением одного или комбинации более чем одного из следующих реагентов: KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8;
ii) далее реакцию завершают в реакторе (2), значение рН в реакторе (2) также доводят до слабокислого значения в диапазоне 4-7 добавлением одного или более из следующих реагентов: NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3, и в то же время окислительно-восстановительный потенциал доводят до значения в диапазоне 300-800 мВ добавлением одного или более чем одного из следующих реагентов: KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8;
время удержания в каждом из двух реакторов должно быть по меньшей мере 30 минут;
iii) затем после выхода продукта из реактора (2) его направляют в чан-сгуститель и оставляют там при медленном перемешивании в течение 1-48 часов.
2. Способ синтеза четырехвалентного марганцевого фероксигита (δ-Fe(1-x)MnxOOH) по п. 1, отличающийся тем, что для оптимального осуществления способа рН реакционной смеси доводят до значения 5,5 с варьированием 0,5 и окислительно-восстановительный потенциал доводят до значения 600 мВ с варьированием 50 мВ.
3. Способ синтеза четырехвалентного марганцевого фероксигита (δ-Fe(1-х)MnxOOH) по пп. 1 и 2, отличающийся тем, что продукт после осуществления способа механически обезвоживают (4), формируют в гранулы размером предпочтительно 250-2500 мкм (5) и высушивают при температуре 100-200°С (6).
4. Адсорбционный материал, полученный согласно способу по пп. 1-3, отличающийся тем, что он состоит из однофазного четырехвалентного марганцевого фероксигита (δ-Fe(1-x)MnxOOH), где х составляет от 0,05 до 0,25, в котором 0,05-25% железа изоморфно замещено атомами марганца, с геометрией от неправильных сфер до полых сфер, с удельной поверхностью от 100 м2/г до 300 м2/г и размером гранул предпочтительно 250-2500 мкм.
5. Применение адсорбционного материала по п. 4, полученного в соответствии со способом по пп. 1-3, для удаления трехвалентного и/или пятивалентного мышьяка из воды в слое колонки или в форме дисперсного порошка.
| CN 101024160 A, 29.08.2007 | |||
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ИОНОВ МЕТАЛЛОВ | 1984 |
|
SU1443340A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ИОНОВ МЕТАЛЛОВ | 1984 |
|
SU1443341A1 |
| Сорбент ионов металлов | 1984 |
|
SU1143456A1 |
| СПОСОБ ОБРАБОТКИ ВОДЫ | 2002 |
|
RU2228304C1 |
| НОВИКОВ В.Г., Ионообменные свойства рудных минералов железомарганцевых образований мирового океана, автореферат дисс | |||
| на соиск | |||
| уч | |||
| степ | |||
| докт.геол-.мин | |||
| наук, Москва 2007. | |||
Авторы
Даты
2016-06-10—Публикация
2011-09-26—Подача