Область изобретения
Настоящее изобретение относится к способу извлечения цинка из цинковой руды с использованием выщелачивающего раствора на основе галогенида. Изобретение относится также к способу удаления марганца из растворов галогенида цинка и другого металла и, особенно, растворов галогенида цинка и/или свинца. Кроме того, изобретение относится к способу удаления серебра и/или ртути из растворов галогенидов металлов, особенно растворов хлорида цинка или меди(I) (например, в гидрометаллургическом способе получения цинка или меди).
Предпосылки создания изобретения
Существующий способ получения цинка включает кальцинирование руды, содержащей цинк, с последующим выщелачиванием кислым сульфатом и затем электролитическим выделением цинка из щелока от выщелачивания. Способ кальцинирования происходит с образованием загрязняющих примесей на основе серы, которые должны быть удалены из отходящих газов печи кальцинирования. Кроме того, если руда содержит высокие уровни примесей, это может оказывать вредное действие на электролиз и чистоту получаемого цинка. Например, многие цинковые руды содержат значительные количества марганца. Существующий способ ограничен в своей способности обрабатывать цинковые минеральные концентраты, содержащие значительное количество марганца, т.к. марганец выщелачивается в щелок от выщелачивания вместе с цинком и не может быть эффективно удален. Марганец создает проблемы в стадии электролитического извлечения цинка осаждением на аноде в виде MnO2.
В патенте Австралии 669906 заявители настоящего изобретения разработали многостадийный способ выщелачивания с последующим электролизом для извлечения меди. И наоборот, в патенте США 4292147 описан способ извлечения цинка с использованием хлоридного выщелачивания с последующим электролизом.
Заявители настоящего изобретения наблюдали также, что в случае раствора марганец не осаждается на аноде во время электролитического извлечения металла из раствора, особенно растворов, полученных выщелачиванием руд цинка и/или свинца. Это делает поправку на удаление марганца из раствора другими способами.
Кроме того, в гидрометаллургических способах, в которых имеется высокая концентрация галогенидов в растворе (например, от 200 до 300 граммов на литр NaCl и от 10 до 50 граммов на литр NaBr), желательно удалить вредные примеси перед электровыделением различных металлов, таких как цинк или медь в указанном способе. Многие примеси могут быть удалены из растворов электролитов этих способов постепенным регулированием рН и осаждением (например, вплоть до около рН 6), однако как серебро, так и ртуть так легко не удаляются.
В патенте США 4124379 описано удаление серебра из электролита хлорида меди(I), при помощи которого к электролиту для восстановления ионов меди(II) в ионы меди(I) добавляют металлическую медь с последующим контактированием с амальгамой, которая обменивает металл на серебро. Амальгаму получают из металлической ртути с одним металлом из меди, цинка или железа, предпочтительно медной дроби, покрытой или ассоциированной с металлической ртутью. Амальгама требует отдельного получения, требующего физическую ассоциацию ртути с медью, а все это делает способ затруднительным и сложным, в результате чего повышается стоимость способа. Кроме того, амальгама должна затем быть введена в процесс и контактирована с содержащим серебро электролитом, что повышает сложность и стоимость проведения способа.
Сущность изобретения
В первом аспекте настоящее изобретение относится к способу извлечения металлического цинка из цинкового минерала, включающему стадии:
- выщелачивание цинкового минерала в одну стадию с использованием раствора, включающего галогенидные соединения, образованные из двух или более разных галогенидов, для выщелачивания цинка в раствор;
- электролиз содержащего цинк раствора с получением металлического цинка и генерацией галогенидного соединения и
- возвращение электролизованного раствора, включающего галогенидное соединение, в стадию выщелачивания.
Авторами настоящего изобретения неожиданно было обнаружено, что галогенидное соединение, образованное из двух или более разных галогенидов, имеет достаточно высокий окисляющий потенциал, так что цинк (и другие металлы, такие как свинец) можно непосредственно выщелочить в раствор в одну стадию без необходимости многостадийной операции выщелачивания (например, как описано автором изобретения в патенте Австралии 669906).
Галогенидное соединение обычно образуется анодно (т.е. у анода) в стадии электролиза. Обычно галогенидное соединение образуется при более низком потенциале окисления, чем потенциал для образования многих нерастворимых форм примесей в растворе. Например, галогенидное соединение в типичном случае образуется при более низком потенциале окисления, чем потенциал для диоксида марганца. Это позволяет сохранять примеси в растворе и затем удалять из раствора, либо в настоящей линии, либо в отдельной стадии удаления.
Двумя разными галогенидами или большим числом разных галогенидов являются хлор и бром, и, предпочтительно, галогенидным соединением является растворимый галогенидный комплекс, образованный у анода, такой как 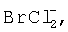 хотя может быть также образован или затем использован газообразный BrCl. Было указано, что такие соединения эффективно окисляют цинковый минерал (и другие минералы), так что требуется только одностадийный способ выщелачивания цинка.
хотя может быть также образован или затем использован газообразный BrCl. Было указано, что такие соединения эффективно окисляют цинковый минерал (и другие минералы), так что требуется только одностадийный способ выщелачивания цинка.
Выщелачивание минерала, предпочтительно, облегчают катализатором, который обычно катализирует окисление минерала галогенидным соединением. В этом отношении катализатор, предпочтительно, является металлическим катализатором, таким как медь, которая может присутствовать в цинковой руде или которую вводят в процесс выщелачивания (например, в виде частиц меди в первой стадии выщелачивания).
Способ, предпочтительно, дополнительно включает одну или несколько последующих стадий для обеспечения выщелачивания цинка в одной стадии и удаления примесей в последующей стадии(ях). Для этого, предпочтительно, по меньшей мере, две последующие стадии сочетают со стадией выщелачивания, так что способ включает первую стадию выщелачивания цинка, вторую стадию аэрации и третью стадию осаждения сульфата.
Воздух, предпочтительно, вводят во второй стадии для окисления и осаждения любого присутствующего железа в цинковом минерале. Когда в минерале присутствует сера, предпочтительно, добавляют известняк в третьей стадии для осаждения сульфата, образованного в результате окисления серы в первой стадии выщелачивания, в виде сульфата кальция.
Щелок от процесса выщелачивания, предпочтительно, имеет эти твердые осадки, выделенные из него, и перед электролизом любой металл из золота и металлов платиновой группы (PGM's), присутствующего в нем, предпочтительно, удаляют пропусканием щелока над активированным углем (обычно применяют колонку с углем) для адсорбции золота и PGM's на угле.
Перед электролизом щелок, предпочтительно, затем пропускают через серию процессов цементации, в которых цинковую пыль (обычно с использованием части цинка, образованного в процессе электролиза) добавляют к щелоку для цементации любого из металлов меди, серебра, свинца и других примесей, присутствующих в щелоке (в результате присутствия их в минерале).
Предпочтительно, перед электролизом, и, если необходимо, щелок затем пропускают на стадию дальнейшего удаления железа (и остаточных металлов), в которой для окисления и осаждения железа в виде оксида железа(III) добавляют известь и галогенидное соединение из стадии электролиза. В этой же самой стадии, предпочтительно, известь и галогенидное соединение будут окислять и осаждать, по меньшей мере, часть марганца, присутствующего в виде диоксида марганца.
Часть электролизованного раствора (обычно отработанный католит), предпочтительно, удаляют и обрабатывают для удаления из него марганца. Эта часть, предпочтительно, является потоком, выходящим из катодного отделения электролитической ячейки для процесса электролиза, причем выходящий поток имеет добавленный в него известняк и галогенидное соединение из анодного отделения процесса электролиза для осаждения диоксида марганца.
В стадии удаления марганца рН и Eh раствора, предпочтительно, регулируют таким образом, чтобы происходило предпочтительное образование осадка диоксида марганца по сравнению с образованием осадка цинка.
рН регулируют, предпочтительно, инкрементальным добавлением известняка для повышения рН раствора до уровня, при котором Eh может быть повышен галогенидным соединением до уровня, при котором более благоприятным является образование MnO2, или до более высокого уровня. Количество добавленного известняка, предпочтительно, составляет меньше, чем стехиометрическое количество, требуемое для образования MnO2, так что осаждается меньше цинка.
Перед возвращением электролизованного щелока в процесс выщелачивания, если необходимо, часть католита (обычно католит, из которого был удален марганец), предпочтительно, пропускают в стадию удаления магния, в которую добавляют гашеную известь для удаления сначала любого цинка (который возвращают в процесс выщелачивания) и затем удаления магния в виде осадка оксида магния.
Следовательно, во втором аспекте настоящее изобретение относится к способу удаления марганца из раствора галогенида металла, который подвергают электролизу для получения одного или нескольких металлов, включающему стадии:
- в электролизе катодное извлечение одного или нескольких металлов, в то же время анодное образование галогенидного соединения из двух или более разных галогенидов при потенциале окисления ниже, чем потенциал окисления для образования диоксида марганца;
- удаление части раствора и обработка его для удаления из него марганца и
- возвращение обработанной части к раствору галогенида металла.
Образованием галогенидного соединения при потенциале окисления ниже, чем потенциал для образования диоксида марганца, марганец может быть сохранен в растворе и это затем позволяет удалять его из раствора, обычно в отдельной стадии отделения.
Раствор галогенида металла представляет собой, предпочтительно, щелок, полученный в результате процесса выщелачивания, в котором минеральный концентрат выщелачивают в содержащем галогенид растворе для выщелачивания одного или нескольких металлов в раствор, наиболее предпочтительно щелок галогенида цинка по первому аспекту.
Щелок, предпочтительно, направляют на стадию электролиза в качестве электролита и после электролиза возвращают в процесс выщелачивания для дальнейшего выщелачивания минерального концентрата. В этом отношении способ удаления марганца настоящего изобретения проводят как часть процесса выщелачивания минерала и электролитического извлечения в замкнутом контуре.
Часть раствора, которую удаляют и обрабатывают для удаления из него марганца, предпочтительно, представляет собой поток, выходящий из процесса выщелачивания минерала и электролитического извлечения металла в закрытом контуре, этот поток возвращают в указанный процесс после удаления марганца.
Выщелачивание минерала, предпочтительно, облегчают образованием у анода галогенидного соединения, которое, предпочтительно, возвращают с электролитом в процесс выщелачивания.
Предпочтительно, двумя или более разными галогенидами являются хлор и бром и предпочтительным галогенидным соединением является растворимый галогенидный комплекс, образованный у анода, такой как 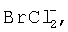 хотя можно также использовать газообразный BrCl.
хотя можно также использовать газообразный BrCl.
Выщелачивание минерала, предпочтительно, облегчают катализатором, который обычно катализирует окисление минерала галогенидным соединением. Для этой цели катализатором, предпочтительно, является металлический катализатор, такой как медь, который присутствует в процессе выщелачивания или его вводят в него.
Минерал, предпочтительно, включает цинк и/или свинец, являющиеся металлами, образуемыми в стадии электролиза.
Марганец в этой части раствора выделяют из него, предпочтительно, инкрементальным добавлением щелочного реагента, предпочтительно реагента, который вызывает осаждение марганца в виде MnO2. Осадок MnO2 может быть затем отделен от части раствора до возвращения его в раствор галогенида металла. Часть раствора, предпочтительно, является частью католита из стадии электролиза, обычно отработанного католитом.
Щелочным реагентом, предпочтительно, является карбонат кальция. Когда металл, который нужно выделить, также имеет тенденцию осаждаться при добавлении щелочного реагента, такого как карбонат кальция (например, цинк), щелочной реагент, предпочтительно, добавляют в количестве, меньшем, чем стехиометрическое количество для образования MnO2. Для повышения окислительного потенциала части раствора до уровня, который благоприятствует образованию MnO2, добавляют также реагент с высоким окислительно-восстановительным потенциалом. Предпочтительным для этого реагентом с высоким окислительно-восстановительным потенциалом является галогенидное соединение (или его газообразная форма), образованное у анода в стадии электролиза. В альтернативном случае, реагентом с высоким окислительно-восстановительным потенциалом может быть гипохлоритная или гипобромитная соль (такая как гипохлорит кальция), которую добавляют к части раствора вместе со щелочным реагентом.
На основании этого, в третьем аспекте настоящего изобретения предложен способ удаления марганца из раствора галогенида металла, из которого может быть получен, по меньшей мере, один металл, включающий стадии:
- регулирование рН и Eh раствора способом, который благоприятствует образованию осадка диоксида марганца по сравнению с образованием осадка, по меньшей мере, одного металла и
- удаление осадка диоксида марганца из раствора.
Значение рН, предпочтительно, регулируют инкрементальным добавлением щелочного реагента для повышения рН раствора до уровня, при котором Eh может быть повышен до уровня, который благоприятствует образованию MnO2, или выше такого уровня. Количество добавляемого щелочного реагента, предпочтительно, меньше, чем стехиометрическое количество, требуемое для образования MnO2, так чтобы произошло меньшее осаждение, по меньшей мере, одного металла.
Значение рН, предпочтительно, повышают добавлением карбоната кальция, a Eh, предпочтительно, повышают добавлением реагента с высоким окислительно-восстановительным потенциалом согласно первому аспекту.
По меньшей мере одним металлом, предпочтительно, является цинк и/или свинец.
Раствором в третьем аспекте, предпочтительно, является выходящий поток из второго аспекта. Раствором третьего аспекта, предпочтительно, является также щелок из процесса выщелачивания первого аспекта.
В четвертом аспекте настоящего изобретения предложен способ удаления растворенного серебра и/или ртути из раствора галогенида металла, где металл способен образовывать цемент с серебром и/или ртутью, причем способ включает стадии:
(a) снижения Eh раствора восстановителем до уровня, который вызывает осаждение металла;
(b) добавления ионного соединения к раствору, который взаимодействует с осажденным металлом способом, который вызывает образование цемента серебра и/или ртути с осажденным металлом, и
(c) удаления цемента.
Образование осадка металла и добавление ионного соединения приводит к цементации серебра и/или ртути, что является специфическим для настоящего изобретения, без необходимости образования и затем введения отдельной амальгамы.
Способ четвертого аспекта обычно обеспечивает комбинационное удаление серебра и ртути и имеет конкретное применение при обработке растворов хлоридов, полученных из минеральных руд, содержащих как серебро, так и ртуть (которые часто в природе встречаются вместе во многих рудах).
Наиболее предпочтительное применение способа относится к растворам хлоридов цинка и меди (таким как растворы, полученные способом выщелачивания цинковой или медной руды). В этом отношении металлом является цинк и/или медь и галогенидом является хлор, и способ, предпочтительно, осуществляют, когда медь находится в ее форме меди(I). По меньшей мере, в предпочтительных формах способа серебро и ртуть желательно удаляют с осаждением только минимального количества меди в виде этого металла.
В дальнейшем величины Eh представлены со ссылкой на стандартный потенциал электрода Ag/AgCl. Eh раствора, предпочтительно, снижают до величины, ниже 0 мВ. Eh может быть снижен вплоть до приблизительно -200 мВ, но обычно его снижают до около 150 мВ. Типичный электролит способа хлорида меди(I) имеет Eh около +150 мВ, и, таким образом, когда Eh раствора снижают до -150 мВ, доступными становятся дополнительные 300 мВ движущей силы для осаждения серебра.
Eh, предпочтительно, снижают добавлением к раствору восстановителя, выбранного из одного или нескольких восстановителей: металлического алюминия, металлического цинка, металлического железа или гидрида, борогидрида или дитионита металла. Наиболее предпочтительным восстановителем является металлический алюминий, так как он является эффективным по стоимости, легко доступен и вызывает образование более легко фильтруемого цемента.
В качестве восстановителя может также быть использован дитионит натрия для снижения Eh, причем конечное снижение Eh, необязательно, достигают борогидридом натрия (т.е. в конце стадии снижения Eh). Посредством использования немедного восстановителя на удаление любой ртути, присутствующей в серебре, не влияет сплавление с большими количествами меди.
Добавленным ионным соединением, предпочтительно, является ионная ртуть в любом или обоих валентных состояниях одновалентной ртути и двухвалентной ртути (Hg(I) или Hg(II)). Другое ионное соединение включает ионное золото и т.д., которое является менее рентабельным. Использование ионного соединения, такого как ионная ртуть, является предпочтительным по сравнению с использованием металлической ртути из-за проблем, указанных выше в патенте США 4124379.
Цементированную ртуть обычно удаляют из раствора пропусканием инертного газа через раствор, так чтобы, по меньшей мере, некоторое количество ртути удалялось из него с газом. Например, в раствор можно барботировать инертный газ, обычно используют такой инертный газ, как азот (т.е. по причине его доступности и низкой стоимости).
После удаления из раствора инертный газ обычно промывают для удаления из него ртути перед рециркуляцией его в раствор для дальнейшего использования. В этом случае инертный газ можно промыть раствором двухвалентной меди (т.е. содержащим ион двухвалентной меди) для удаления из него выделенной ртути. Для промывки ртути из азота могут быть использованы другие окислители, такие как хлорид ртути(II). Можно также использовать диоксид углерода.
Кроме того, удаление металлической ртути из раствора может быть повышено нагреванием раствора для дополнительного испарения металлической ртути. Когда в способе удаления используют инертный газ, повышенное количество испаренной металлической ртути, таким образом, улавливается в газе.
В альтернативном случае, металлическая ртуть может быть удалена из раствора пропусканием раствора над активированным углем, так чтобы металлическая ртуть адсорбировалась на угле. В случае такой альтернативы ртуть можно затем удалить из активированного угля пропусканием второго раствора над активированным углем, причем второй раствор имеет значение Eh, которое является достаточным для превращения адсорбированной ртути в ионную ртуть, чтобы тем самым растворить ее во втором растворе.
Данный альтернативный способ является пригодным для легкого осуществления в линии и, таким образом, легко приспособлен для коммерциализации; например, можно использовать колонку, содержащую активированный уголь, и через колонку непрерывным способом можно подавать насосом электролит с пониженным Eh (например, приблизительно при -150 мВ). После того, как предельное количество ртути было адсорбировано на угле, может быть использовано автоматическое переключение для перекачки через колонку второго раствора. Растворенная ртуть может быть затем легко извлечена из второго раствора.
Типичное применение способа четвертого аспекта наблюдается в гидрометаллургических способах извлечения с растворами хлорида цинка и/или меди(I). Типичной величиной Eh в гидрометаллургических способах с использованием таких растворов и до удаления серебра и/или ртути является приблизительно +150 мВ.
Краткое описание графического материала
Несмотря на любые другие варианты, которые могут находиться в пределах объема настоящего изобретения, теперь будут описаны предпочтительные варианты изобретения посредством примера и со ссылкой также на прилагаемый графический материал, в котором:
на фиг.1 показана схематично технологическая диаграмма, иллюстрирующая способ выщелачивания и электролитического извлечения цинка в замкнутом цикле, включающий стадию удаления марганца;
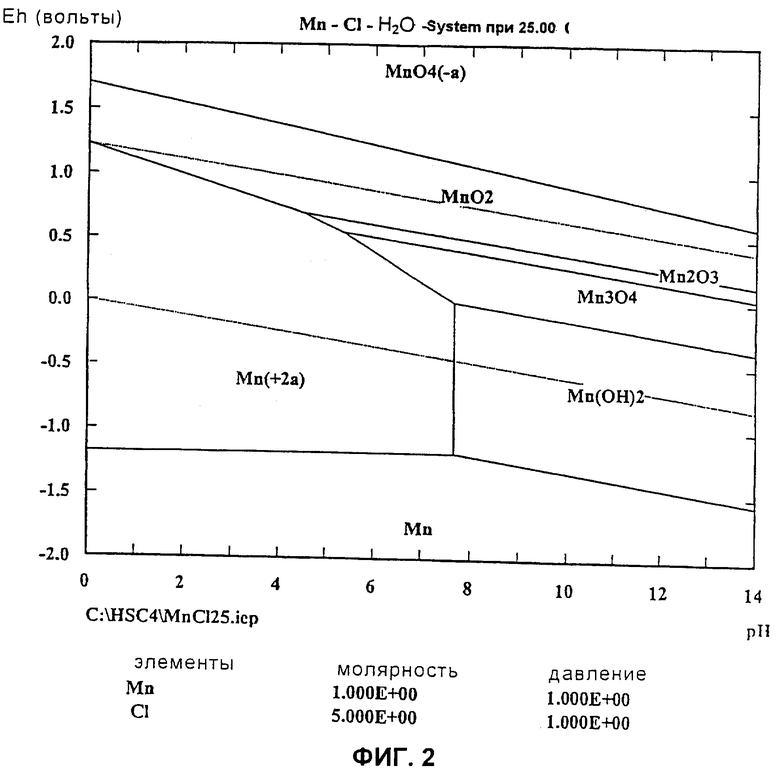
на фиг.2 показана диаграмма Pourbaix для системы Mn-Cl-H2O при 25°С;
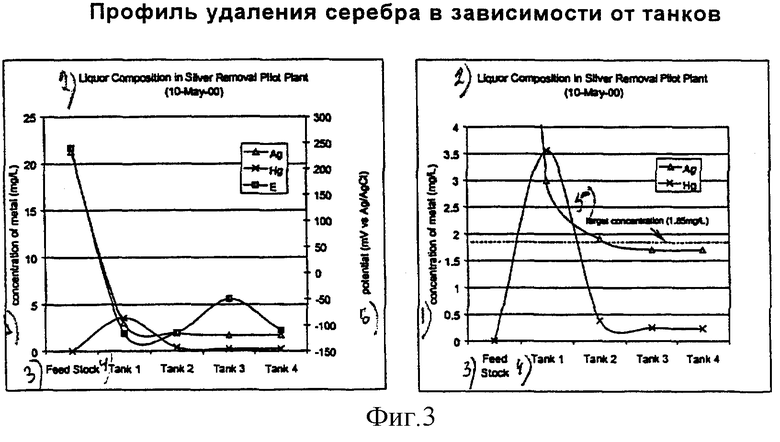
фиг.3 представляет собой график зависимости удаления серебра и ртути от развития процесса и
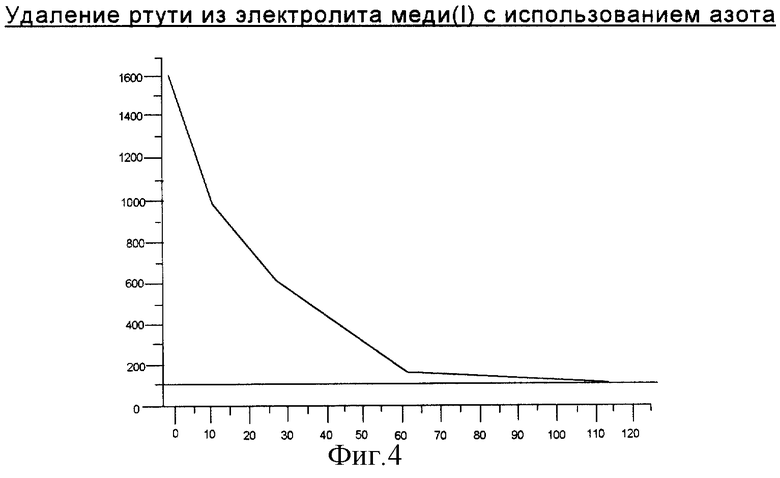
фиг.4 представляет собой график зависимости удаления ртути в зависимости от времени из электролита меди(I) с использованием барботирования азотом.
Способы проведения извлечения цинка по изобретению
Предпочтительный способ извлечения цинка по настоящему изобретению схематически показан на фиг.1, и описание данного способа теперь будет сделано со ссылкой на фиг.1.
Способ предназначен для получения металлического цинка высокой чистоты из концентратов комплексных смешанных сульфидов цинка/свинца, полученных из руд цинк/свинец. Свинец и серебро получали в виде цементных побочных продуктов, тогда как золото и металлы платиновой группы (PGM's), когда они присутствовали, получали в виде слитка.
Концентраты, содержащие значительные уровни железа, легко обрабатывали, причем все выщелачиваемое железо переходило в остаток щелока в виде гематита, тогда как сульфидная сера превращалась в элементную серу. Высокие уровни примесей, таких как марганец и мышьяк, также легко приводили в соответствие, причем мышьяк переходил в остаток щелока в виде стабильного в окружающей среде арсената железа, а марганец осаждался в отдельном остатке в виде диоксида марганца (описано ниже).
Предпочтительный способ был основан на электролитическом осаждении у катода цинка высокой чистоты из очищенного электролита хлорид натрия - бромид натрия. Во время стадии электрохимического извлечения галогенидное соединение было генерировано в растворе у анода. Такое соединение было смешанным галогенидным соединением, таким как растворимый 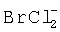 (в дальнейшем "Halex"). Это соединение проявляло высокие характеристики выщелачивания, когда его рециркулировали для обработки поступающего концентратного сырья.
(в дальнейшем "Halex"). Это соединение проявляло высокие характеристики выщелачивания, когда его рециркулировали для обработки поступающего концентратного сырья.
Предпочтительный способ включает три основные стадии выщелачивания, очистки и электрохимического выделения, как показано на фиг.1. Процесс выщелачивания включал одну стадию выщелачивания (один реактор) и был объединен с рядом последующих стадий (реакторов). Концентрат цинка и окислитель (галогенидное соединение) направляли на стадию выщелачивания. Очистка состояла из стадий цементации и щелочного осаждения. При электрохимическом выделении использовали ряд электролизеров с диафрагмой с вариантом непрерывного удаления продукта в дендритной форме или получения общепринятого катода с электролитическим покрытием цинком.
Электролиз Zn (электролитическое осаждение)
Электролитическое осаждение было совокупной частью предпочтительного способа. Металлический цинк осаждали электролизом из очищенного электролита, который имел в своем составе 100 г/л цинка, 50 г/л хлорид натрия (обычная соль, NaCl), 50 г/л хлорида кальция (CaCl2) и 110 г/л бромида натрия (NaBr). Все другие компоненты, в том числе "равновесные" уровни многих других элементов (марганца, магния и т.д.), рассматривали как примеси.
Электролиз включал пропускание электрического тока при 500 А/м2 вобласти электрода с образованием очень чистого цинка на отрицательно заряженном катоде. Исходный концентрат электролита цинка, в свою очередь, обеднялся от концентрации 100 до 50 г/л, которая была концентрацией устойчивого состояния ячейки.
Окислитель (выщелачивающий)
Отработанный католит непрерывно проникал через мембрану нетканой ткани М, расположенную в электролитической ячейке ЕС (фиг.1). Католит проникал к положительно заряженному электроду (аноду).
Хлорид (Cl-) и бромид (Br-), предпочтительно, присутствовали в растворе, и, следовательно, происходило предпочтительное образование галогенидного соединения 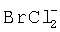 (Halex). Однако могли быть образованы другие галогенидные соединения. Это галогенидное соединение рассматривалось как молекула хлора, удерживаемая в растворе бромид-ионом, и было отмечено, что это соединение является очень сильным выщелачивающим агентом при окислительном потенциале (Eh) 1000 мВ (против Ag/AgCl). Образовавшийся, содержащий Halex раствор (электролит) из отделения анода (анолит) используют для выщелачивания концентрата сульфида цинка.
(Halex). Однако могли быть образованы другие галогенидные соединения. Это галогенидное соединение рассматривалось как молекула хлора, удерживаемая в растворе бромид-ионом, и было отмечено, что это соединение является очень сильным выщелачивающим агентом при окислительном потенциале (Eh) 1000 мВ (против Ag/AgCl). Образовавшийся, содержащий Halex раствор (электролит) из отделения анода (анолит) используют для выщелачивания концентрата сульфида цинка.
Стадия выщелачивания
Концентрат цинка и окислитель Halex из процесса электролиза направляли в щелок первой стадии (первый, непрерывно перемешиваемый реактор-резервуар (CSTR) на фиг.1). Операции на CSTR проводили при атмосферном давлении и температуре раствора (электролита) 85°С. Реакцию выщелачивания (окисления) сначала проводили без барботирования воздухом (аэрации (или введения воздуха)) до тех пор, пока весь окислитель Halex 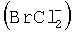 не был израсходован. В первом CSTR имело место значительное растворение железа и окисление сульфида.
не был израсходован. В первом CSTR имело место значительное растворение железа и окисление сульфида.
Второй и третий CSTR's вводили в процесс для дальнейшей аэрации с целью отвода железа в виде осадка оксида железа(III). Любой присутствующий мышьяк окисляли в первом CSTR и затем осаждали в виде стабильного в окружающей среде арсената железа.
Рецикловый цемент меди (т.е. цемент из последующей стадии цементации Cu и Ag) добавляли к первому CSTR для повышения как повторного поглощения кислорода, так и экстракции металла. Медь помогала катализировать окисление концентрата цинка галогенидным соединением.
Когда выщелачивание завершалось, в третий CSTR добавляли известняк для отвода (осаждения) любого растворенного железа, который оставался, и любого присутствующего сульфата. Известняк уравновешивал также генерацию серной кислоты в результате окисления серы в первом CSTR. Необязательно применяли четвертый CSTR для повышения времени пребывания (реакции) и предоставления возможности для максимального осаждения железа и сульфата.
Стадия очистки
Остаток выщелачивания отделяют от обогащенного цинком "богатого" раствора фильтрованием и промывают перед отведением до обвала у первого места разделения твердое вещество-жидкость (S/L).
Когда присутствовало золото или PGM's, их экстрагировали (окисляли) во время выщелачивания и извлекали подачей богатого цинком раствора через колонку, заполненную активированным углем, на котором золото и PGM's адсорбировались. Этот уголь можно затем отдельно элюировать элюэнтом для выделения золота и других PGM's.
Обогащенный цинком раствор затем далее очищали посредством ряда реакций цементирования с реагентом цинковой пылью. Это была двустадийная, CSTR-облегченная операция с медью и серебром, преимущественно удаленными в первой стадии, которую проводили при температуре 85°С. Во второй стадии добавляли избыточную цинковую пыль для удаления оставшихся примесей, таких как кадмий, свинец, никель, кобальт, таллий и т.д.
После двух дополнительных стадий разделения системы твердое вещество-жидкость теперь уже к загруженному относительно чистым цинком раствору в CSTR добавляли небольшое количество паров Halex из анолита электролитической ячейки до достижения Eh 700 мВ. Это гарантировало, что любое оставшееся железо окислилось до степени окисления трехвалентного железа (Fe3+). Последующее добавление измельченного известняка для повышения рН до 4,5 осаждало большую часть оставшихся примесей (например, Bi, Fe, In, Ge и т.д.). Эти осадки удаляли фильтрованием и либо выгружали, либо снова обрабатывали для извлечения экономически пригодных побочных продуктов, таких как индий.
Было также очевидно, что, по меньшей мере, некоторое количество марганца было способно удаляться из раствора галогенида металла в виде осадка диоксида марганца, если рН регулировали до выше, чем 3,2 на этой стадии CSTR. рН повышали выше этого уровня добавлением карбоната кальция (обычно измельченного известняка). При этом значении рН и при окислительно-восстановительном потенциале 600-800 мВ против Ag/AgCl (800-1000 мВ против SHE) марганец входил в благоприятную область стабильности MnO2 диаграммы Pourbaix. Остаток диоксида марганца затем удаляли с осажденным железом из раствора. Eh также регулировали (повышали) добавлением реагента Halex с высоким окислительно-восстановительным потенциалом. Специфические химические реакции и условия реакций для удаления марганца описаны в деталях коротко в нижеследующем тексте для последующего цикла удаления марганца (для отработанного выходящего потока католита), в котором также используют известняк и Halex для этой цели. Следует отметить, что в выходящем потоке, который нужно описать, концентрация марганца в растворе обычно выше, чем она была в настоящей стадии очистки CSTR.
Отмечено, что оставшиеся теперь любые примеси не загрязняют цинк во время получения электролизом и были удалены либо в циклах очистки марганца, либо магния. В частности, поскольку галогенидное соединение образуется у анода при потенциале окисления ниже, чем потенциал окисления для образования оксида марганца, этот металл не загрязняет электролитическим образом извлеченный цинк.
Раствор очищенного цинка затем электролизовали, как описано выше, для получения цинка высокой чистоты и генерирования выщелачивателя, галогенидного соединения, для рециркуляции на стадию выщелачивания. Цинковый продукт промывали и сушили в инертной атмосфере перед плавлением в печи. Некоторое количество цинковой пыли, образованной из цинка в печи, использовали в стадиях цементации (описаны выше).
Удаление марганца и магния
Эти циклы удаления металлов включали обработку католитным выходящим потоком, причем в цикле марганца использовали известняк и Halex, а в цикле магния использовали гашеную известь.
Отмечено, что этот способ обычно пригоден при обработке минеральных концентратов, содержащих марганец. В настоящем способе извлечения цинка марганец, выщелаченный в щелок, удаляли в равной пропорции (т.е. удаляли, по меньшей мере, со скоростью выщелачивания его в щелок), чтобы предотвратить аккумулирование его в растворе способа.
Вплоть до максимальных 20% общего раствора, протекающего через электролитическую ячейку ЕС, отводили в виде выходящего потока BS из отработанного католита. Этот поток обрабатывали парами Halex и известняком для осаждения марганца в виде диоксида марганца MnO2.
Отмечали, что давление паров Halex выше электролита зависит от температуры и сам пар, вероятно, состоит из газообразного BrCl.
Способ удаления марганца химически изображен ниже в уравнениях (1)-(3), где предполагается, что пар Halex представляет собой BrCl.
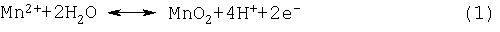
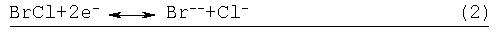

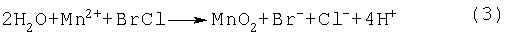

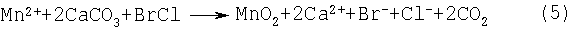
Состав электролита в отработанном католите был приблизительно следующим: 50 г/л NaCl, 110 г/л NaBr, 50 г/л CaCl2 и 50 г/л Zn2+. Однако способ удаления марганца можно также проводить на электролите способа перед электролизом. При использовании выходящего потока из отработанного католита ячейки получения электролизом цинка уровень марганца в растворе зависит от количества выщелачиваемого в раствор и количества выходящего потока, доходящего до удаления Mn.
Авторы настоящего изобретения показали, что марганец был полностью удален из выходящего потока в виде диоксида марганца добавлением к нему паров Halex. Обнаружено, что реакция электролит-пары является очень быстрой в присутствии инкрементально добавляемых небольших количеств известняка.
Осаждение марганца в виде диоксида марганца предсказывается диаграммой Pourbaix, показанной на фиг.2. Как можно видеть, марганец не осаждается при нейтральном окислительно-восстановительном потенциале до рН выше 7,5. При высоком окислительно-восстановительном потенциале 600-800 мВ против Ag/AgCl (800-1000 мВ против SHE) и рН 3,2, однако, марганец входил в область стабильности MnO2 и был способен осаждаться в виде MnO2
Во время удаления марганца осаждается также небольшое количество цинка. Однако авторы настоящего изобретения показали, что меньше цинка осаждалось при более низких уровнях водного цинка (например, 25 г/л Zn2+ вместо 50 г/л Zn2+) или когда известняк инкрементально добавляли в небольших количествах для поддержания рН около 3,2 (в противоположность осаждению марганца в присутствии стехиометрического избытка известняка).
Так, с использованием отработанного католита, содержащего 50 г/л Zn2+и 15 г/л Mn2+, при медленном добавлении известняка только 7,8% цинка в растворе осаждалось совместно с марганцем. Для 8% католитного отходящего потока это равно потере, меньшей, чем 0,7% общего получения цинка относительно осадка выходящего потока.
Примеры удачных экспериментов удаления марганца показаны ниже. Как можно видеть из них, полное удаление марганца было выполнено в первых двух экспериментах, тогда как полное удаление не было достигнуто в третьем эксперименте. Следует отметить, что промежуточные анализы цинка в растворе были только приблизительным руководящим принципом, так как цинк, осажденный из раствора, было трудно характеризовать из-за экспериментальной ошибки, связанной с этим анализом. Точные определения осаждения цинка определяли прямым анализом конечного остатка.
Результаты экспериментов 2 и 3, показанные в таблицах 2 и 3, отражают путь, которым данный способ применяли для способа выделения металлов свинец/цинк, в котором у анода образовывался Halex. Результаты показали, что для 8% потока, выходящего из отработанного католита, поддерживали концентрацию рециркулирующего марганца при 15 г/л. Совместное осаждение цинка с осаждением MnO2 составляет потерю приблизительно 0,6% общего получения цинка.
Примеры удаления марганца
Теперь будут описаны неограничивающие примеры способов удаления марганца.
Пример 1
Электролит, включающий 200 г/л NaCl, 150 г/л NaBr, 30 г/л Са2+, 25 г/л Zn2+ и 5 г/л Mn2+, получали в виде типичного выходящего потока способа извлечения свинца/цинка. 25 г/л СаСО3 добавляли к электролиту в реакционном сосуде в начале способа удаления. Са(OCl)2 добавляли непосредственно к электролиту для окисления раствора. Температуру раствора поддерживали при типичной температуре электролита способа от 60 до 65°С. Результаты показаны ниже в таблице 1.
Пример 2
Электролит, включающий 50 г/л NaCl, 110 г/л NaBr, 50 г/л CaCl2, 50 г/л Zn2+ и 15 г/л Mn2+, получали в виде типичного выходящего потока способа извлечения свинца/цинка. 85 г/л СаСО3 добавляли к электролиту в реакционном сосуде в начале способа удаления. Пары Halex генерировали снаружи и закачивали насосом в реакционный сосуд. Температуру раствора поддерживали при типичной температуре электролита способа от 60 до 65°С. Результаты показаны ниже в таблице 2.
Пример 3
Электролит, включающий 50 г/л NaCl, 110 г/л NaBr, 50 г/л CaCl2, 50 г/л Zn2+ и 15 г/л Mn2+ получали в виде типичного выходящего потока способа извлечения свинца/цинка. СаСО3 добавляли к электролиту в реакционном сосуде небольшими дозами на всем протяжении способа удаления. Пары Halex генерировали снаружи и закачивали насосом в реакционный сосуд. Температуру раствора поддерживали при типичной температуре электролита способа от 60 до 65°С. Результаты показаны ниже в таблице 3.
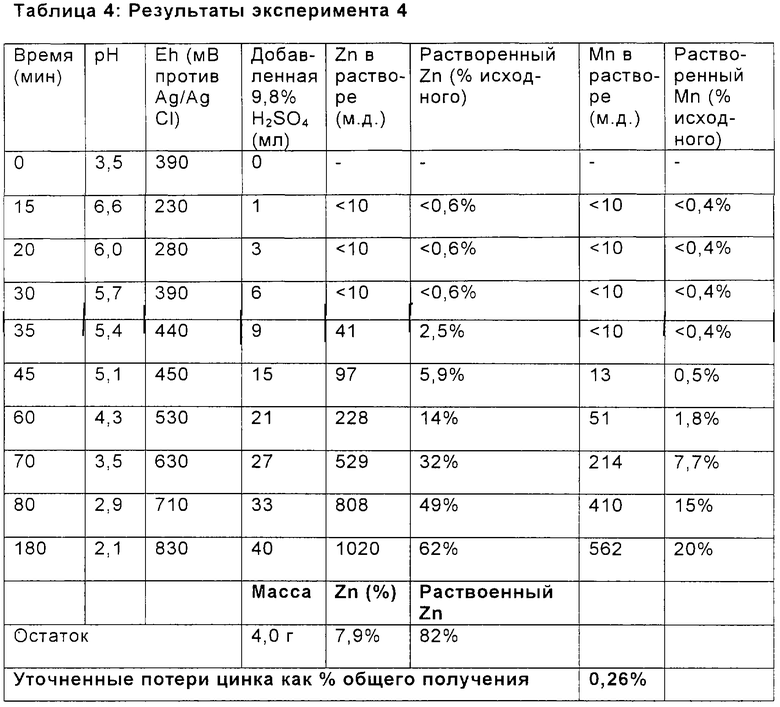
Пример 4
10,0 г осадка марганца из примера 2 добавляли к 1,0 литру деминерализованной воды в реакционном сосуде. Добавляли H2SO4. Результаты показаны ниже в таблице 4.
Пример 5
10,0 г осадка из примера 3 добавляли к 1,0 литру деминерализованной воды в реакционном сосуде. Пары Halex генерировали снаружи и закачивали насосом в реакционный сосуд. Результаты показаны ниже в таблице 5.
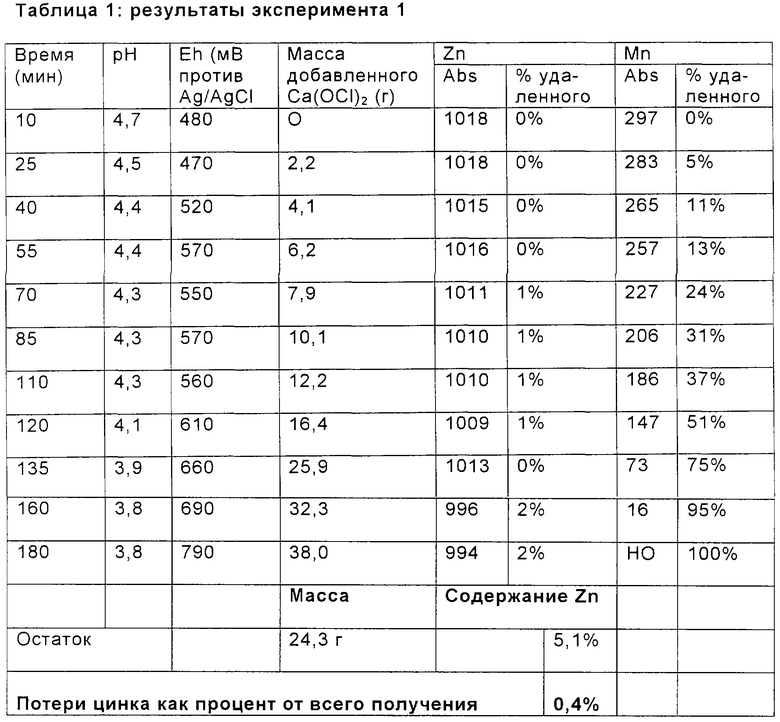
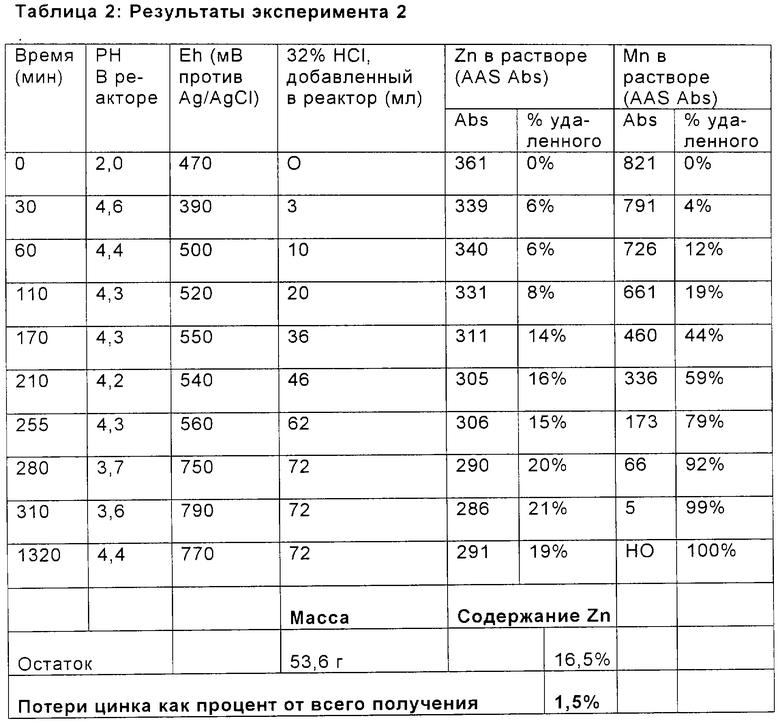
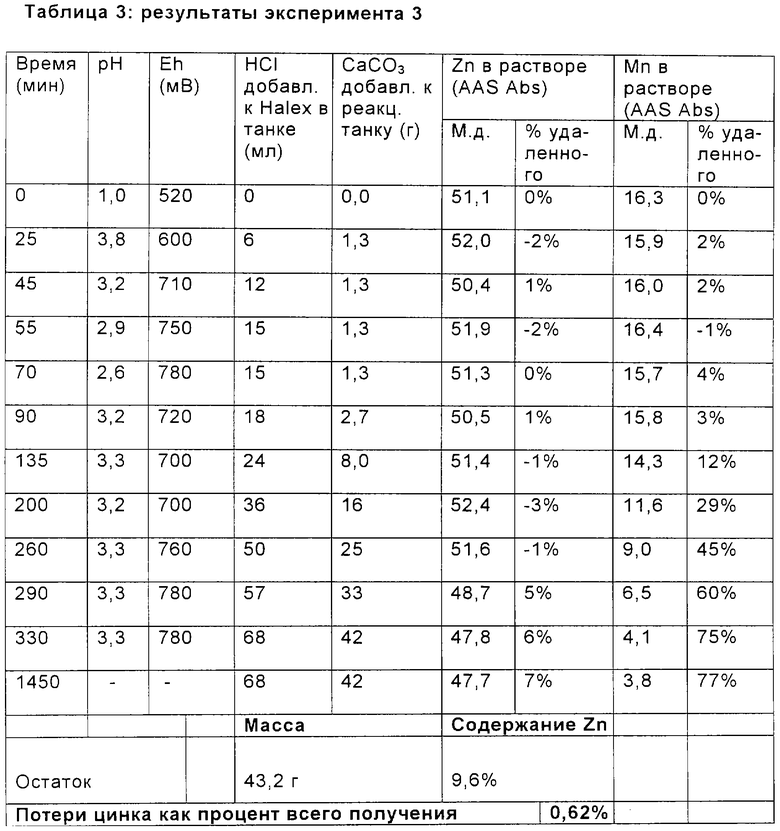
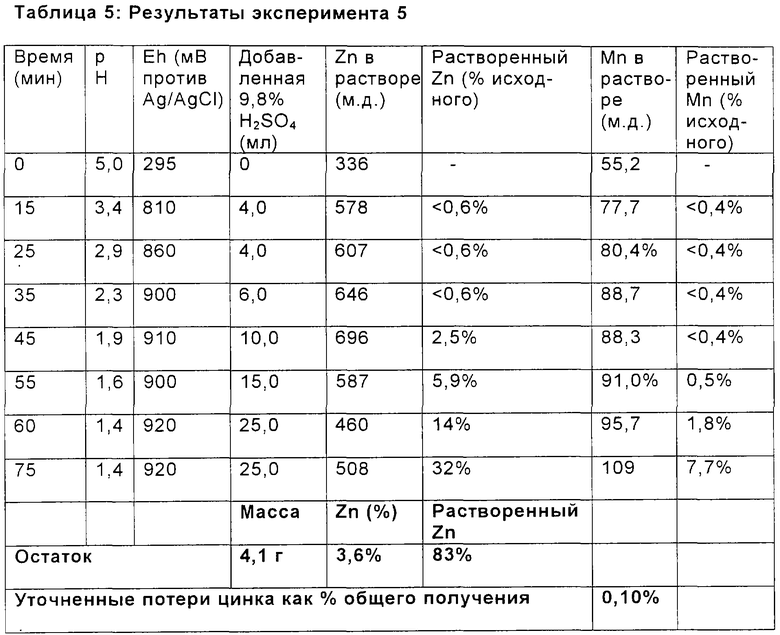
Марганец, таким образом, полностью удаляли из выходящего потока в виде диоксида марганца добавлением паров Halex. Обнаружено, что реакция электролит-пары протекает очень быстро в присутствии небольших количеств известняка.
Небольшое количество цинка было осаждено также во время удаления марганца. Однако меньше цинка осаждалось при более низких уровнях водного цинка (например, 25 г/л Zn2+ вместо 50 г/л Zn2+) или когда известняк добавляли инкрементально в небольших количествах для поддержания рН около 3,2 (в противоположность осаждению марганца в присутствии стехиометрического избытка известняка).
Таким образом, посредством использования отработанного католита, содержащего 50 г/л Zn2+ и 15 г/л Mn2+, при медленном добавлении известняка только 8,4% цинка в растворе осаждали совместно с марганцем. Для 8% католитного потока выходящие потери составляют менее чем 0,7% общего получения цинка в осадке выходящего потока.
В процессе удаления магния отработанный католит из процесса удаления марганца имел в ряде CSTR's гашеную (или каустическую) известь, добавленную в них для осаждения в первых двух CSTR's цинка. Этот цинк затем возвращали в процесс выщелачивания, обычно на стадии добавления известняка (как показано на фиг.1). Затем в двух следующих CSTR более гашеную известь добавляли для осаждения оксида магния и тем самым предотвращения введения магния в процесс. Эта стадия удаления требовалась только для периодического действия, поскольку обычно снижала уровни магния в цинковом минерале. Обработанный отработанный католит затем возвращали в процесс выщелачивания, обычно в первый CSTR выщелачивания.
Следует отметить, что экономика предпочтительного способа извлечения цинка, в котором Halex образуется у анода, является специфичной для участка. Для производителя концентрата потеря 0,6% цинка при производстве как результат удаления примесей (особенно, марганца) представляет собой значительное усовершенствование относительно потерь в плавильной печи известного уровня техники, где приблизительно 4% содержащегося цинка вычитают до вычисления подходящего содержания металла. Однако, когда по способу желательны более высокие извлечения цинка, некоторое количество цинка, осажденного из раствора с марганцем, извлекали повторным суспендированием осадка выходящего потока в воде и подкислением серной кислотой. Цинк был способен снова растворяться с селективностью приблизительно 90%. Посредством корректирования более высокой доли выходящего потока, требуемой для частичного повторного растворения марганца, потерю цинка с осадком выходящего потока снижали до 0,1% общего получения цинка.
Важным признаком предпочтительного способа было то, что все примеси, в том числе марганец, ртуть и мышьяк, либо извлекали в качестве пригодных для продажи побочных продуктов, либо стабилизировали для удаления в отходы. Другим равноважным признаком было то, что тепло обеспечивали экзотермическими реакциями выщелачивания. Это в сочетании с добавлением воздуха к щелоку выпаривало воду и тем самым поддерживало водный баланс при нейтральном значении. Как такового жидкого потока не было.
Удаление серебра и ртути
Теперь предпочтительные варианты осуществления удаления серебра и ртути будут описаны со ссылкой на щелок хлорида меди(I), но должно быть понятно, что изобретение может быть использовано с растворами хлоридов других металлов (в том числе хлорид цинка).
Отмечено, что при электролитическом получении меди типичной величиной Eh раствора иона меди(I) при контактировании с металлической медью было +150 мВ (относит. Ag/AgCl). Неожиданно было обнаружено возможное химическое снижение Eh раствора иона меди(I) до -150 мВ (Ag/AgCl) с минимальным осаждением металлической меди. Это допускает значение движущей силы выше 300 мВ для осаждения серебра. Кроме того, эффективность образования амальгамы серебро-ртуть значительно не снижалась сплавлением с Cu. Наблюдали, что некоторое количество Cu осаждается совместно с амальгамой серебро/ртуть, но отмечено, что количество Cu в амальгаме (остаток) составляет 1/20 количества в остатке способов существующего уровня техники, что, таким образом, делает извлечение серебра и ртути значительно более легким.
Обнаружено, что после удаления серебра можно удалять следы ртути из раствора ионов меди(I) барботированием через него азота. После барботирования азот промывают, например, раствором ионов меди(I) для удаления из него уловленной ртути. Азот затем рециркулируют в раствор для дальнейшего удаления ртути.
Примеры удаления серебра/ртути
Пример 6
Усовершенствованный способ удаления серебра и ртути из растворов хлоридов разработали с использованием усовершенствованного восстановителя, а именно металлического алюминия, который, как было отмечено, является дешевым и легко доступным восстановителем по сравнению с восстановителями, описанными ниже, и по сравнению с цинковой пылью или металлическим железом.
Кроме того, использование металлического алюминия вызывало образование подобного губке осадка меди в растворах хлорида меди, который после последующей цементации серебра и/или ртути было легче фильтровать, чем осадок, образованный из других восстановителей. Далее алюминий вовлекался в этот осадок, тогда как цинковая пыль не вовлекалась в него, и алюминий мог быть, таким образом, удален из раствора с цементом. Образуемое металлическим железом наружное покрытие меди и ее сердцевина не реагировали, что, таким образом, делало ее менее эффективной в качестве восстановителя.
В усовершенствованном способе удаления серебра и ртути из растворов хлоридов металлический алюминий добавляют в небольших количествах (0,05-0,3 грамма на литр электролита) к электролиту, что вызывает снижение в Eh раствора до величины от -120 до -150 мВ (против Ag/AgCl) и осаждение меди с высокой площадью поверхности. Отмечено, что эта медь является относительно грубым, подобным губке осадком. Она была очень реакционноспособной для добавленных ионов ртути и была способна образовывать амальгаму с химической композицией, в которой имеется приблизительно 7,5% серебра, медь, количество которой варьирует от 10% вплоть до 50%, балансом является количество ртути.
Амальгама, образуемая благодаря добавлению алюминия, была также более совместимой и имела более легко фильтруемый размер частиц. Применение амальгамы является усовершенствованием по сравнению со способами известного уровня техники для разделения твердых и жидких фаз.
Уровни ртути в растворе, выходящем из этой стадии, были аналогичны уровням, описанным для примера 8, и использовали такие же стадии удаления ртути (барботирование азотом или адсорбция на активированном угле), как описано ниже.
Усовершенствованный способ испытывали в стендовом масштабе перед испытанием на протяжении 48-часовой операции в пилотном масштабе при скорости потока раствора непрерывного способа 20 л/ч. Пилотное испытание проводили при помощи четырех 20-литровых танков, через которые барботировали азот, причем алюминиевую фольгу добавляли в танк 1 при скорости дозирования от 0,05 до 0,15 граммов на литр электролита (1-3 г/ч) и ионную ртуть (например, нитрат ртути(I) или ртути(II)) добавляли в танк 1 при массовом отношении 3:1 с серебряным исходным материалом (1,5 г/ч). Обработанный электролит имел концентрации: 75 г/л Cu+, 280 г/л NaCl и 28 г/л NaBr при 35°С. На фиг.3 показаны результаты средних содержаний серебра и ртути и Eh в течение 48 часов операции.
Как можно видеть на фиг.3, средняя концентрация серебра в танках 3 и 4 на всем протяжении 48 часов операции была 1,5 мг/л с минимальной концентрацией 1,2 мг/л. Наблюдаемые диапазоны концентрации ртути были такими, как показано в таблице 6.
Пример 7
В этом примере восстановителем был борогидрид натрия, но было отмечено, что могут быть использованы также другие восстановители, такие как дитионит натрия и гидриды металлов (например, гидрид натрия и кальция, необязательно в комбинации с борогидридом натрия для снижения количества используемого борогидрида). Более эффективный по стоимости способ включал применение дитионита натрия для проведения снижения Eh в массе (т.е. обычно до предельного уровня), причем конечное снижение проводят борогидридом натрия (т.е. до достижения предпочтительного более низкого уровня около -150 мВ (Ag/AgCl)).
В противоположность использованию металлического алюминия в качестве восстановителя, борогидрид натрия вызывал осаждение ультрамелкой губчатой меди и при добавлении ионной ртути образование амальгамы, которую трудно и дорого фильтровать и которая является менее стабильной. Кроме того, борогидридное соединение само было как дорогим, так и нестабильным в воде. Если борогидридное соединение не хранят при высоком значении рН, оно быстро гидролизуется, вызывая потерю дорогого реагента. Аналогично этому, мелкая амальгама, образованная после добавления ртути и борогидрида натрия, должна быть абсолютно защищена от окисления или ее быстро снова растворяют, высвобождая ионы серебра и ртути обратно в раствор. Несмотря на эти трудности, было возможно также использование борогидрида натрия в качестве восстановителя и с добавлением ионной ртути (Hg(I) или Hg(II), одновалентной или двухвалентной ртути, соответственно), причем происходило образование амальгамы меди, ртути и серебра, что приводило к удалению как ртути, так и серебра из раствора.
Удаление серебра
45 мг NaBH4 добавляли к 1,5 литрам электролита с восстановленной медью, который содержал 22 м.д. серебра и вызывал снижение Eh раствора от +120 мВ до -135 мВ (Ag/AgCl). 65 мг ртути в виде нитрата ртути(II) добавляли к электролиту и тем самым снижали уровень серебра в растворе от 22 м.д. до 4,4 м.д. за 40 минут. Другие 65 мг ртути добавляли в виде нитрата ртути(II), и на протяжении 20 минут уровень серебра снижался до 1 м.д. Осажденное твердое вещество фильтровали и сушили, и было обнаружено, что оно содержит 7,4% серебра, а содержание меди варьировало от 10% вплоть до 47%, остальную часть составляла ртуть.
Процесс повторяли с использованием дитионита натрия для достижения уровней Eh ниже, чем 0 мВ, причем конечное снижение Eh достигали небольшими количествами NaBH4.
Пример 8
Удаление ртути
Электролит меди(I) из примера 7 удаления серебра регулировали до -150 мВ добавлением к нему восстановителя, такого как NaBH4. Это смещает обычное равновесие раствора (т.е. равновесие между металлической ртутью, ионом ртути(I) и ионом ртути(II)) в сторону образования металлической ртути. В обработанный таким образом электролит в течение 1 часа барботируют газообразный азот. Отмечено, что во время этого периода содержание ртути электролита снижается от 0,29 м.д. до 0,037 м.д. Отмечено, что удаление ртути повышается нагреванием раствора во время барботирования азотом.
Во втором испытании начальную концентрацию ртути 1600 мкг/л снижали до 150 мкг/л за 60 минут и 100 мкг/л за 120 минут. Результаты показаны на фиг.4 ниже.
Пример 9
Альтернативное удаление ртути
Значение Eh электролита меди(I) из примера 2 удаления серебра, содержащего 500 мкг/л ртути, регулировали приблизительно до -150 мВ (Ag/AgCl). Данный раствор затем пропускали (например, нагнетанием насосом под давлением) через колонку, упакованную активированным углем, при скорости 4 мл/мин (в течение первых трех часов) и затем 20 мл/мин (в течение следующих 2 часов). Металлическую ртуть адсорбировали на активированном угле, снижая тем самым концентрацию ее в растворе ниже, чем 55 мкг/л. Металлическую ртуть затем отделяли от активированного угля пропусканием второго другого раствора с высоким Eh через колонку, тем самым превращая металлическую ртуть в растворенную ионную ртуть для прохождения из колонки во второй раствор. Ртуть затем выделяли из второго раствора.
Вышеописанные экспериментальные процедуры показали, что очень эффективное удаление как серебра, так и ртути можно было достичь без необходимости использования меди (согласно существующему уровню техники). Кроме того, указанные способы удаления легко выполняются. Простота способа легко позволяла увеличить масштаб его до полностью коммерческого и непрерывного осуществления.
Способ извлечения цинка по настоящему изобретению имеет следующие несомненные преимущества по сравнению со способом обжига/выщелачивания/электровыделения цинка и другими гидрометаллургическими способами известного уровня техники:
- значительно более низкие операционные и капитальные расходы;
- выделение благородных металлов в цикле выщелачивания цинка (например, при очистке нецинковых металлов из раствора, при выделении пользующихся спросом металлов меди, свинца и серебра (Cu, Ag, Pb и Fe в стадии цементации и осаждения фиг.1));
- толерантность к имеющим низкое качество и "загрязненным" концентратам;
- низкий расход энергии;
- отсутствие эмиссии жидкости;
- отсутствие образования ядовитых газов;
- мягкие условия проведения операций: низкая температура и атмосферное давление;
- отсутствие необходимости экстракции растворителем и
- отсутствие потребности в чистом кислороде в стадиях аэрации.
Хотя изобретение было описано со ссылкой на ряд предпочтительных вариантов осуществления, должно быть понятно, что изобретение может быть осуществлено во многих других формах.
Изобретение относится к способу извлечения цинка из цинковой руды с использованием выщелачивающего раствора на основе галогенида и способу удаления марганца из растворов галогенида цинка и другого металла. Извлечение металлического цинка из цинкового минерала включает стадии: выщелачивание цинкового минерала раствором, содержащим галогенидное соединение из двух или более разных галогенидов, электролиз полученного раствора для получения металлического цинка и генерирования галогенидного соединения и возвращение электролизованного раствора, содержащего галогенидное соединение, на стадию выщелачивания. Часть электролизованного раствора может быть удалена в виде выходящего потока из катодного отделения электролитической ячейки процесса электролиза и обработана для удаления марганца в виде осадка диоксида марганца добавлением в нее известняка и галогенидного соединения из анодного отделения процесса электролиза. В этом случае рН и Eh раствора можно регулировать способом, который благоприятствует образованию осадка диоксида марганца по сравнению с образованием осадка цинка. Изобретение характеризуется значительно более низкими операционными и капитальными расходами по сравнению с известными способами, выделением благородных металлов из растворов, толерантностью к имеющим низкое качество и «загрязненным» концентратам, низким расходом энергии, отсутствием эмиссии жидкости и образования ядовитых газов, а также низкой температурой и атмосферным давлением при проведении операций. 3 н. и 17 з.п. ф-лы, 6 табл., 4 ил.
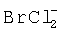 и/или газообразный BrCl.
и/или газообразный BrCl.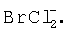
| Экономайзер | 0 |
|
SU94A1 |
| US 4071421 А, 31.01.1978 | |||
| Устройство для идентификации параметров систем управления | 1979 |
|
SU885976A1 |
| Устройство для электровыщелачивания цветных металлов | 1976 |
|
SU658179A1 |
| Способ извлечения марганца | 1982 |
|
SU1054302A1 |
Авторы
Даты
2007-05-10—Публикация
2002-09-12—Подача