Область техники, к которой относится изобретение
Настоящее изобретение относится к иммуноконъюгатам для специфической индукции цитотоксичности Т-клеток против клеток-мишеней, включающим, по меньшей мере, один вызывающий ответ Т-клеток пептид, который может быть презентирован через МНС класса I и соединен со связывающей частью молекулы клетки-мишени, а также к способам их получения и применения.
Предпосылки создания изобретения
Т-клетки, в отличие от В-клеток, распознают пептиды, производные от процессированных антигенов, которые презентированы на поверхности клетки через молекулы на поверхности аутологичных клеток главного комплекса гистосовместимости (major histocompatibility complex - МНС).
Современное представление о презентации антигена через МНС класса II (МНС II) заключается в том, что экзогенные белки получают доступ к МНС II посредством фагоцитоза и эндоцитоза, а эндогенные белки проникают в МНС II через аутофагию. Антигены процессируются в пептидные антигены (пептидные эпитопы) соответствующей длины (~10-16 аминокислот) для связывания с молекулами МНС II в фагосоме, эндосоме или аутофагосоме. Ненагруженные димеры αβ-цепи МНС II собираются в эндоплазматической сети (endoplasmic reticulum - ER) в виде нонамерного комплекса с инвариантной цепью (Ii), которая защищает от преждевременных пептидных или белковых взаимодействий в предлизосомальных компартментах. Этот комплекс перемещается в лизосомальный компартмент МНС II, где инвариантная цепь подвергается последующему протеолизу. Конечный продукт расщепления - пептид, называемый класса II-ассоциированным пептидом Ii (class II-associated Ii peptide - CLIP), занимает пептид-связывающую канавку и должен быть высвобожден до загрузки молекул МНС II высокоаффинными пептидами (МНС II рестректированные пептиды) (Wearsch и Creswell, постер доступен в сети по адресу http://www.nature.com/nri/posters/antigenprocessing).
Связывание наивных CD4 Т-клеток с загруженным пептидом МНС II на клеточной поверхности опосредует иммунизацию антигеном путем праймирования наивных CD4 Т-клеток для поляризации в эффекторные Т-клетки (Th1, Th2, Th17) или Т-клетки памяти. В другом варианте, в зависимости от окружающей среды (например, от баланса цитокинов) в микроокружении антигенпрезентирующих клеток (antigen presenting cells - АРС), связывание наивных CD4 Т-клеток с загруженным пептидом МНС II может опосредовать иммунную толерантность к антигену путем праймирования наивных CD4 Т-клеток для поляризации в регуляторные Т-клетки (Treg).
Если молекулы МНС II обычно встречаются только на антигенпрезентирующих клетках, например на макрофагах, В-клетках и дендритных клетках, то молекулы МНС-класса I (МНС I) встречаются на всех ядерных клетках.
В настоящее время считают, что механизм презентации антигена через МНС класса I (МНС I) заключается в том, что эндогенные антигены, например, вирусные белки или аутологичные белки, которые вырабатываются внутри клеток, процессируются в пептиды внутри цитозоля протеасомой и цитозольными протеазами. Такие пептиды затем транспортируются в ER через специальные насосы, называемые транспортерами, ассоциированными с антиген-презентирующим комплексом (ТАР), где их дополнительно формируют аминопептидазы ER (ER aminopeptidase - ERAP) для получения пептидов из 8-12 аминокислот.
Было установлено, что пептидные эпитопы экзогенных белков, которые интернализируются в клетки, преимущественно в специализированные антигенпрезентирующие клетки (АРС), например, дендритные клетки или макрофаги, также могут быть презентированы главным комплексом гистосовместимости (МНС I). Это связано с наличием домена транслокации, включенного в экзогенный белок, который поддерживает ретротрансляцию указанного белка из фагосомы или эндосомы и тем самым направляет белки в цитоплазму клетки (Donnelly с соавт., Proc Natl Acad Sci USA, постер доступен в сети по адресу http://www.nature.com/nri/posters/antigenprocessing).
Сборка гетеродимеров тяжелой цепи-β2-микроглобулина МНС I с короткими пептидами координируется загруженным пептидом комплексом, который состоит из дисульфид-связанного димера тапазина и ERp57, калретикулина (calreticulin - CRT) и молекул ТАР. Тапазин также поддерживает пептидное редактирование для выбора для презентации стабильных комплексов пептид-МНС I на поверхности клеток (Wearsch и Creswell, Nat. Rev. Immunol, http://www.nature.com/nri/posters/antigenprocessing). После загрузки пептида на молекулу МНС I нагруженный пептидом комплекс диссоциирует и загруженный пептидом МНС I покидает ER по секреторному пути, чтобы достичь поверхности клетки. Пептиды, которые не способны связывать молекулы МНС I в просвете ER, выводятся из ER по канал sec61 в цитозоль, где они могут подвергаться дальнейшему формированию по размеру и могут быть транслоцированы с помощью ТАР обратно в ER для связывания с молекулой МНС I (Koopmann J.O. с соавт., Immunity, 13 (1): 117-27.; Albring J. с соавт., Mol. Immunol., 40(10): 733-741).
Молекулы МНС I на поверхности клеток презентируют свои загруженные пептиды в цитотоксические CD8 Т-лимфоциты (CD8 Т-клетки, также называемые CTL). CTL запускают клетку, которая презентирует пептидные эпитопы через МНС I, чтобы осуществить запрограммированную клеточную гибель по механизму апоптоза. Следовательно, МНС I участвует в качестве посредника в клеточно-опосредованном иммунитете, который является основным средством иммунной системы, для борьбы с внутриклеточными патогенами, а также для борьбы с собственными клетками, экспрессирующими мутированные или нарушенные белки
В последние годы основные исследования были сосредоточены на использовании механизма индукции клеточно-опосредованного иммунитета, чтобы индуцировать уничтожение множества пораженных клеток (например, опухолевых клеток), на которые не влияют внутриклеточные патогены. Поскольку все ядерные клетки экспрессируют МНС I, индуцированная презентация антигенов внутриклеточных патогенов через МНС I является многообещающим подходом к индукции запрограммированной гибели клеток CTL в различных популяциях пораженных клеток, например, опухолевых клеток.
В связи с этим были разработаны подходы для доставки антигенов, производных от внутриклеточных патогенов, например, от вирусов, иммуноконъюгатами, сформированными из связывающего партнера, который связывается с клеткой-мишенью, и из пептидной фракции внутриклеточного патогена, к определенной популяции пораженных клеток, чтобы индуцировать презентацию процессированных фрагментов доставленных пептидов на поверхность пораженных клеток через МНС I. Связанные с болезнью клетки затем могут быть элиминированы CTL.
Один из подходов описан в ЕР 0659439 А1. В иммуноконъюгате, описанном в ЕР 0659439 А1, производный от вируса пептид (модифицированный пептид матрикса вируса гриппа 57-68) или производный от бактерии пептид (Plasmodium bergei пептид 249-260) соединен с антителами, связывающими клетки-мишени. Соответствующий пептид соединен с антителом путем добавления остатка N-концевого цистеина и последующего перекрестного связывания через SPDP-линкер с антителом для получения иммуноконъюгата. При интернализации соответствующий пептид, включающий добавленный N-концевой остаток цистеина, выщепляется из конъюгата, дополнительно процессируется в клетке и презентируется МНС I. Однако, величина IC50 иммуноконъюгатов очень высокая (0,5 мкМ/л).
В подходе в соответствии с ЕР 0659439 А1 описано, что основной проблемой является стимуляция МНС I, связанного с CTL-ответом против экзогенных антигенов. В большинстве случаев, когда антиген поступает экзогенно, он не направляется в цитоплазму, откуда он мог бы быть перенесен на метаболический путь МНС I.
Одна из методологий повышения величины IC50 для иммуноконъюгатов, включающих пептиды, которые могут быть презентированы через МНС I путем процессирования, предложена в ЕР 0659439 А1. В этом изобретении рекомендуют включать домен транслокации в иммуноконъюгат, чтобы провести иммуноконъюгат в цитоплазму посредством ретротранслокации. Однако в ЕР 0659439 А1 нет результатов применения данного подхода.
Поэтому по-прежнему существует потребность в улучшенных подходах к индукции уничтожения клеток-мишеней путем вызова клеточно-опосредованного иммунитета.
Краткое описание изобретения
Настоящее изобретение относится к иммуноконъюгату, содержащему, по меньшей мере, один вызывающий ответ Т-клеток пептид, презентируемый через МНС класса I, который соединен с частью молекулы, связывающейся с клеткой-мишенью через расщепляемую связь. В иммуноконъюгате расщепляемая связь устроена таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид, который непосредственно презентируется через молекулу МНС класса I, высвобождается из иммуноконъюгата.
Один из вариантов осуществления настоящего изобретения относится к иммуноконъюгату, в котором вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом.
Один из вариантов осуществления настоящего изобретения относится к иммуноконъюгату, в котором вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом, включающим, по меньшей мере, один остаток цистеина.
Один из вариантов осуществления настоящего изобретения относится к иммуноконъюгату, в котором расщепляемая связь расщепляется в компартменте эндосомы клетки-мишени.
Один из вариантов осуществления настоящего изобретения относится к иммуноконъюгату, в котором иммуноконъюгат не включает домен транслокации.
Один из вариантов осуществления настоящего изобретения относится к иммуноконъюгату, причем менее чем за 12 ч после интернализации иммуноконъюгата в клетке-мишени вызывающий ответ Т-клеток пептид презентируется на поверхности клетки-мишени через молекулу МНС класса I.
Другим объектом настоящего изобретения является фармацевтическая композиция, включающая иммуноконъюгат по настоящему изобретению в комбинации с фармацевтически приемлемым носителем.
Еще одним объектом настоящего изобретения является применение иммуноконъюгата по настоящему изобретению для специфической индукции цитотоксичности Т-клеток против клеток-мишеней.
Другим объектом настоящего изобретения является способ получения иммуноконъюгата по настоящему изобретению, включающий стадии:
а) получения рекомбинантной части молекулы, связывающей клетки-мишени,
б) получения вызывающего ответ Т-клеток пептида, и
в) соединения, по меньшей мере, одного вызывающего ответ Т-клеток пептида с указанной частью молекулы, связывающей клетки-мишени, через расщепляемую связь.
Один из вариантов осуществления настоящего изобретения относится к способу получения иммуноконъюгата, в котором немодифицированный вызывающий ответ Т-клеток пептид соединен с частью молекулы, связывающей клетку-мишень.
Другим объектом настоящего изобретения является иммуноконъюгат по настоящему изобретению для применения в качестве лекарственного средства.
Еще одним объектом настоящего изобретения является иммуноконъюгат по настоящему изобретению, включающий часть молекулы, связывающую раковые клетки, предназначенный для лечения рака.
Другим объектом настоящего изобретения является иммуноконъюгат по настоящему изобретению для применения в лечении инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии.
Другим объектом настоящего изобретения является способ лечения больного пациента, нуждающемуся в таком лечении, путем введения иммуноконъюгата по настоящему изобретению.
В соответствии с настоящим изобретением вызывающий ответ Т-клеток пептид, выщепленный из иммуноконъюгата, может быть непосредственно презентирован молекулами МНС класса I без дополнительного процессирования или изменения в клетках-мишенях. Вызывающий ответ Т-клеток пептид выщепляется из иммуноконъюгата в компартменте эндосомы клетки-мишени при интернализации иммуноконъюгата, и пептид непосредственно (т.е. без дальнейшего процессирования или формирования) нагружается на молекулы МНС класса I в компартменте эндосомы и транспортируется к поверхности клетки-мишени для презентации через МНС класса I. Неожиданно было установлено, что достигают существенно меньших значений показателя IC50 по сравнению с другими подходами, известными в данной области техники.
Описание фигур
Фиг. 1. Ослабленная активация Т-клеток в модифицированных пептидах CMV по данным измерения IFNγ-ELISPOT с использованием различных линий опухолевых клеток и культуральных сред. А) клетки MDA-MB231 в среде RPMI+, Б) клетки MDA-MB231 в среде AIM-V, В) клетки НСТ-116 в среде RPMI+, Г) клетки НСТ-116 в среде AIM-V, Д) клетки Т2 в среде RPMI+. Исследование проводят, используя концентрации пептидов 13,245 мкМ или 1,3245 мкМ согласно указанному.
Фиг. 2. Предполагаемый механизм действия иммуноконъюгата по настоящему изобретению. А: Связывание иммуноконъюгата с клетками-мишенями. Б: Интернализация иммуноконъюгата в компартмент эндосомы. В: Высвобождение вызывающего ответ Т-клеток пептида из иммуноконъюгата в компартмент эндосомы. Г: Нагрузка молекул МНС I высвободившимся пептидом в компартментах эндосом. Д: Движение нагруженных пептидом молекул МНС I к поверхности клеток-мишеней. Е: Распознавание нагруженных пептидом молекул МНС I на поверхности клеток-мишеней пептид-специфичными CD8 Т-клетками, индуцирующими гибель клеток-мишеней.
Фиг. 3. Связывание иммуноконъюгатов, включающих анти-CDCP1 антитело, соединенное с пептидом EBV и/или FLU, с CDCP1-экспрессирующими клетками MDA-MB 231.
Фиг. 4. Связывание иммуноконъюгатов, включающих анти-СD19 антитело, соединенное с пептидом EBV и/или FLU, с CD19-экспрессирующими клетками RL.
Фиг. 5. Результаты IFN-γ ELISPOT при использовании иммуноконъюгатов по настоящему изобретению для активации пептид-специфических Т-клеток. Представленные концентрации относятся к концентрациям пептида. A) CDCP-1-экспрессирующие клетки НСТ-116, обработанные иммуноконъюгатами, включающими моноклональное анти-CDCP-1 антитело и HLA-A2 ограниченный пептид EBV. Б) CD19-экспрессирующие HLA-А2-положительные RL и HLA-A2-отрицательные клетки Ramos, обработанные иммуноконъюгатами, включающими моноклональное анти-CD19 антитело и HLA-A2 ограниченный пептид EBV. В) Различные CDCP-1-экспрессирующие опухолевые клетки, обработанные иммуноконъюгатами, включающими моноклональное анти-CDCP-1 антитело и HLA-A2 ограниченный пептид EBV.
Фиг. 6. Уничтожение опухолевых клеток по результатам метода xCELLigence и по высвобождению LDH. (А) Уничтожение опухолевых клеток HLA-А2-положительных клеток MDA-MB231, опосредованное иммуноконъюгатом, включающим анти-CDCP1 антитело, соединенное с HLA-A2 ограниченным пептидом EBV. (Б) Специфическое уничтожение клеток А-375, опосредованное иммуноконъюгатом, включающим анти-CDCP1 антитело, соединенного с HLA-A2 ограниченным пептидом EBV с неконцевым остатком цистеина. (В) Специфическое уничтожение HLA-А2-положительных MDA-МВ231 клеток, опосредованное иммуноконъюгатом, включающим анти-CDCP1 антитело, соединенное с HLA-A2 ограниченным пептидом EBV с неконцевым остатком цистеина. Представленные концентрации относятся к концентрациям пептида.
Фиг. 7. Уничтожение HLA-A1-положительных опухолевых клеток, опосредованное иммуноконъюгатом, включающим HLA-A1 ограниченный пептид FLU. А-В). Результаты, полученные методом xCELLigence через 6, 10 и 18 ч. Г-Е) Результаты, полученные методом на основе высвобождения LDH. А и Г) Соотношение эффекторных клеток к клеткам-мишеням (А-375) (Е:Т) 1:1 и 1:2, Б и Д) клетки НСТ-116, В и Е) клетки РС3.
Фиг. 8. Противоопухолевая активность иммуноконъюгатов по настоящему изобретению, содержащих моноклональное анти-CDCP1 антитело, в экспериментальной модели подкожного введения MDA-MB231 с внутривенным введением МКПК человека. Схема тестирования (фиг. 8А) и результаты (фиг. 8Б).
Фиг. 9. Противоопухолевая активность иммуноконъюгатов по настоящему изобретению, содержащих моноклональное анти-CDCP1, в комбинации с анти-PD1-лечением в разработанной модели подкожного введения MDA-MB231 с внутривенным введением МКПК человека. Схема тестирования (фиг. 9А) и результаты ингибирования роста опухоли (фиг. 9Б) и повышения Т-клеток (фиг. 9В).
Подробное описание изобретения
Определения
Понятие «иммуноконъюгат» в контексте настоящего изобретения относится к части молекулы, связывающей клетку-мишень (например, к антителу, специфически связывающемуся с клеткой-мишенью, или к лиганду, связывающемуся с рецептором на клетке-мишени), соединенной с гетерологичной функциональной молекулой. Функциональной молекулой, по существу присутствующей в иммуноконъюгатах по настоящему изобретению, является вызывающий ответ Т-клеток пептид. Кроме того, могут быть дополнительные функциональные молекулы, например, цитотоксические агенты.
Понятие «часть молекулы, связывающая клетку-мишень» в настоящем изобретении относится к части молекулы, которая специфически связывается с клеткой-мишенью. Это понятие относится к антителам, а также к другим природным (например, рецепторам, лигандам) или синтетическим (например, DARPins - designed ankyrin repeat proteins) молекулам, способным специфически связываться с клеткой-мишенью. Понятие «специфическое связывание с клеткой-мишенью» в настоящем изобретении означает, что указанная часть молекулы предпочтительно связывается с определенной клеткой-мишенью в сложной смеси.
Связывающее сродство (аффинность) части молекулы, связывающейся с клеткой-мишенью, обозначают с помощью ka (константа скорости ассоциации белка из комплекса белок/клетка-мишень), kD (константа диссоциации) и KD (kD/ka). В одном из вариантов осуществления настоящего изобретения, в котором часть молекулы, связывающая клетку-мишень, является антителом, специфически связывающимся с клеткой-мишенью, аффинность составляет (KD) 10-8 М/л или менее, в еще одном варианте осуществления настоящего изобретения - от 10-8 М до 10-13 М/л.
Понятие «антитело» применяют в настоящем изобретении в самом широком смысле, и оно охватывает различные структуры антител, включая, но ими не ограничиваясь, моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и фрагменты антител, при условии, что они обладают требуемой антиген-связывающей активностью.
В настоящем изобретении понятие «лиганд» применяют в отношении молекулы, предпочтительно белка, который образует комплекс с биомолекулой на клетке-мишени для осуществления биологической цели. В одном из вариантов осуществления настоящего изобретения лиганд является селективным лигандом, который проявляет тенденцию связываться с ограниченным типом рецепторов.
В настоящем изобретении понятие «пептид» означает короткую цепь из мономеров аминокислот, связанных пептидными связями. Пептиды, которые связываются с МНС класса I, обычно содержат от 8 до 12 аминокислот в длину. Понятие «пептид, вызывающий ответ Т-клеток, который способен к презентации через МНС класса I» в контексте настоящего изобретения относится к пептидам, которые могут быть презентированы через молекулы МНС класса I, но которые не могут быть презентированы через МНС II, и которые инициируют ответ CD8 Т-клеток. Для упрощения это понятие в настоящем изобретении формулируют просто как «вызывающий ответ Т-клеток пептид».
В настоящем изобретении вызывающие ответ Т-клеток пептиды по настоящему изобретению обычно являются производными от чужого источника (то есть не являются производными организма человека). Понятие «является производным» в этом контексте означает, что вызывающий ответ Т-клеток пептид идентичен природному эпитопу Т-клеток от патогенного, чужого, источника (т.е. разделяет одну и ту же аминокислотную последовательность). Иначе говоря, аминокислотная последовательность вызывающего ответ Т-клеток пептида идентична части аминокислотной последовательности белкового антигена от патогенного, чужого, источника. Хотя патогенный источник вызывающего ответ Т-клеток пептида может иметь вирусное или бактериальное происхождение, обычно вызывающие ответ Т-клеток пептиды, которые могут презентироваться МНС I, являются производными от внутриклеточных или внеклеточных патогенов. К внутриклеточным патогенам относятся вирусы, внутриклеточные бактерии или паразиты. К внутриклеточным патогенам относятся паразиты и бактерии. Несмотря на то, вызывающие ответ Т-клеток пептиды, используемые в настоящем изобретении, имеют ту же аминокислотную последовательность, что и соответствующий природный эпитоп Т-клеток, вызывающие ответ Т-клеток пептиды иммуноконъюгата согласно настоящему изобретению обычно имеют синтетическое происхождение.
Пептиды, полученные из внутриклеточных патогенов, которые применяют в данной области для индукции цитотоксичности Т-клеток, направленных против клеток-мишеней, иногда модифицируют аминокислотными замещениями или добавлениями для улучшения их физиологических свойств, например, растворимости. В настоящем изобретения, однако, применяют только встречающиеся в природе вызывающие ответ Т-клеток пептиды (т.е. пептиды, разделяющие аминокислотную последовательность патогенного пептида дикого типа без включения дополнительных модификаций аминокислотной последовательности).
В настоящем изобретении понятие «встречающийся в природе (природный)» означает, что вызывающий ответ Т-клеток пептид, который может быть презентирован через МНС класса I, который соединен с частью молекулы, связывающей клетку-мишень, состоит из аминокислотной последовательности соответствующего чужого («не своего») патогенного эпитопа Т-клеток, представляемого через МНС класса I. Иначе говоря, вызывающий ответ Т-клеток пептид состоит из аминокислотной последовательности, которая идентична аминокислотной последовательности, вырабатываемой путем расщепления соответствующего природного «не своего» патогена в клетке-мишени. Следовательно, «встречающийся в природе вызывающий ответ Т-клеток пептид» или «вызывающий ответ Т-клеток пептид, который способен к презентации через МНС-класса I» в понятиях настоящего изобретения может быть синтетическим, однако его аминокислотная последовательность не включает каких-либо модификаций аминокислот, в частности, не включает никаких добавок, делеций или замещений аминокислот по сравнению с пептидом, вырабатываемым путем расщепления соответствующего природного чужого патогена. Можно перефразировать и сказать, что аминокислотная последовательность природного вызывающего ответ Т-клеток пептида, соединенного с частью молекулы, связывающейся с клеткой-мишенью, идентична (в одном из предпочтительных вариантов осуществления настоящего изобретения имеет в длину от 8 до 12 аминокислот) части аминокислотной последовательности белкового антигена чужого патогена.
Утверждение, что вызывающий ответ Т-клеток пептид «естественным образом содержит» определенный аминокислотный остаток, означает, что определенный аминокислотный остаток находится в том же положении в соответствующем природном вызывающим ответ Т-клеток пептиде. Следовательно, вызывающий ответ Т-клеток пептид, который естественным образом содержит остаток цистеина, означает пептид, являющийся производным от чужого патогена, причем частично аминокислотная последовательность белкового антигена чужого патогена, которая соответствует аминокислотной последовательности указанного вызывающего ответ Т-клеток пептида, содержит остаток цистеина в том же положении.
Когда отмечают, что вызывающий ответ Т-клеток пептид не содержит «модификации аминокислотной последовательности» относительно патогенного эпитопа Т-клеток дикого типа, подразумевают, что аминокислотная последовательность пептида идентична аминокислотной последовательности соответствующего естественным образом производного эпитопа Т-клеток чужого патогена (т.е. эпитоп Т-клеток, продуцируемый расщеплением соответствующего естественного чужого патогена). В частности, аминокислотная последовательность пептида не включает вставок, делеций или замещений аминокислотных остатков при сравнении с природным пептидом.
Используемое в настоящем изобретении понятие «аминокислота» означает органическую молекулу, имеющую аминогруппу, расположенную в α-положении по отношению к карбоксильной группе. К примерам аминокислот относятся: аргинин, глицин, орнитин, лизин, гистидин, глутаминовая кислота, аспарагиновая кислота, изолейцин, лейцин, аланин, фенилаланин, тирозин, триптофан, метионин, серии, пролин. Аминокислоты необязательно каждый раз используют в L-форме. Аминокислоты могут быть сгруппированы на основании общих свойств боковых цепей:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные: Cys, Ser, Thr, Asn, Gln;
(3) кислые: Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, которые влияют на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
Таблица. Аминокислоты со специфическими свойствами
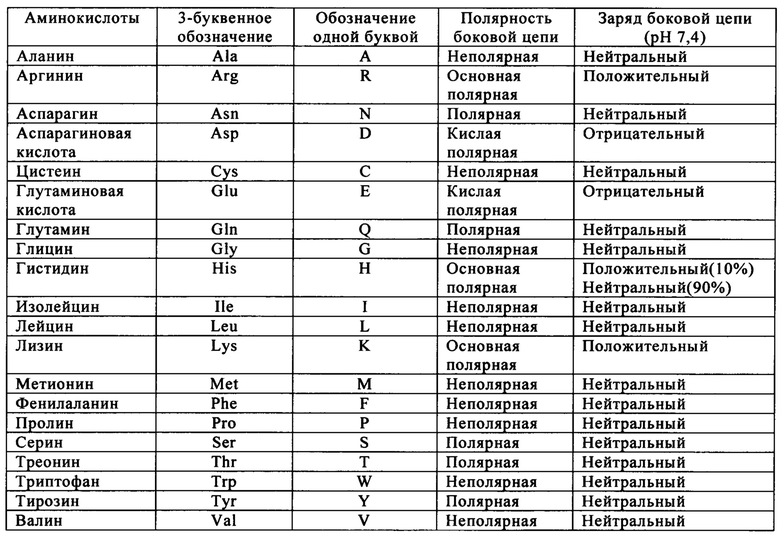
Понятие «эпитоп» означает часть белкового антигена, который распознается иммунной системой, например, антителами, В-клетками или Т-клетками. «Эпитоп Т-клеток» презентирован на поверхности клетки, где он связан с молекулами МНС. Эпитопы Т-клеток, презентируемые МНС I, могут быть связаны Т-клеточным рецептором цитотоксических CD8 Т-лимфоцитов (CD8 Т-клеток или CTL). Т-клеточные эпитопы, презентируемые МНС I, обычно представляют пептиды длиной от 8 до 12 аминокислот. Следовательно, «вызывающий ответ Т-клеток пептид, который презентируется через МНС класса I» по настоящему изобретению означает пептид, полученный из патогена (в одном из вариантов осуществления настоящего изобретения пептид состоит из 8-12 аминокислотных остатков), который способен связываться с комплексом МНС I (но не с МНС II) без потребности в процессировании (например, путем расщепления одного или нескольких аминокислотных остатков) в клетке-мишени.
В настоящем изобретении понятие «расщепляемая связь» означает связь внутри иммуноконъюгата, расположенную между частью молекулы, связывающей клетку-мишень, и вызывающим ответ Т-клеток пептидом, что позволяет выщеплять вызывающий ответ Т-клеток пептид для непосредственной презентации молекулой МНС класса I. Расщепляемая связь расположена в прямом контакте с вызывающим ответ Т-клеток пептидом. Выщепление вызывающего ответ Т-клеток пептида из иммуноконъюгата приводит к высвобождению вызывающего ответ Т-клеток пептида из его исходной аминокислотной последовательности, причем без каких-либо дополнительных аминокислотных остатков.
В зависимости от типа расщепляемой связи вызывающий ответ Т-клеток пептид высвобождается из иммуноконъюгата при расщеплении либо «без следа», либо «со следами». Под понятием «со следами» в контексте настоящего изобретения подразумевают, что высвобождаемый вызывающий ответ Т-клеток пептид включает следы линкера (т.е. следы в форме части химической молекулы, не состоящей из аминокислот (аминокислоты)), при условии, что указанные следы не мешают связыванию с МНС класса I. Следует уточнить, что в настоящем изобретении понятие «высвобождение со следами» не включает высвобождения вызывающего ответ Т-клеток пептида, включающего дополнительный аминокислотный остаток (остатки). Под понятием «без следа» в контексте настоящего изобретения подразумевают, что высвобождаемый вызывающий ответ Т-клеток пептид не содержит каких-либо следов линкера.
Понятие «зависящее от рН расщепление» означает, что расщепление расщепляемой связи индуцируется изменением рН. В одном из вариантов осуществления настоящего изобретения зависящее от рН расщепление индуцируется величиной рН в компартменте эндосом клеток-мишеней. В одном из вариантов осуществления настоящего изобретения зависящее от рН расщепление индуцируется величиной рН рН 5,5-6,5.
В контексте настоящего изобретения понятие «ферментативное расщепление» означает протеолитическое расщепление иммуноконъюгата, которое обычно происходит за счет гидролиза пептидной связи. Ферментативное расщепление вызывают протеазы, например, фурин. Создание расщепляемой связи в иммуноконъюгате, которая расщепляется путем ферментативного расщепления, может быть достигнуто, например, путем связывания вызывающего ответ Т-клеток пептида с частью молекулы, связывающей клетки-мишени через пептидный линкер.
Связывание вызывающего ответ Т-клеток пептида с частью молекулы, связывающей клетки-мишени через пептидный линкер, может быть осуществлено за счет дисульфидной связи, сложноэфирной связи, химического линкера, пептидного линкера или за счет нековалентного связывания (например, биотин/стрептавидин, биотин/теофиллин).
Понятие «ковалентная связь» или «ковалентное связывание» вызывающего ответ Т-клеток пептида с частью молекулы, связывающей клетки-мишени, означает связывание химической связью, при которой происходит распределение электронов между атомом вызывающего ответ Т-клеток пептида и атомом части молекулы, связывающей клетки-мишени.
Под понятием «нековалентная связь» или «нековалентное связывание» вызывающего ответ Т-клеток пептида с частью молекулы, связывающей клетки-мишени, подразумевают связывание, которое не связано с распределением электронов. К примерам нековалентного связывания включают иммунологические связывания или связывание через биотин/авидин, биотин/стрептавидин и др. В одном из вариантов осуществления настоящего изобретения иммунологическое связывание означает соединение, осуществляемое через антитело, включенное в иммуноконъюгат, в котором антитело специфически связывается с органической молекулой, которая связывается с вызывающим ответ Т-клеток пептидом. Чтобы высвободить вызывающий ответ Т-клеток пептид после интернализации, в таком варианте осуществления настоящего изобретения вызывающий ответ Т-клеток пептид соединяют с указанной органической молекулой через расщепляемую связь. Органическая молекула предпочтительно представляет собой небольшую молекулу с молекулярной массой до 900 Да. К примерам таких органических молекул относятся биотин и теофиллин.
В контексте настоящего изобретения понятие «пептидный линкер» или «линкерный пептид» означает пептид с аминокислотной последовательностью, предпочтительно искусственно синтезированный. В настоящем изобретении пептидный линкер либо включает функциональный домен с сайтом расщепления, в одном из вариантов осуществления настоящего изобретения сайт является сайтом расщепления протеазой, или пептидный линкер формирует сайт расщепления, в одном из вариантов осуществления настоящего изобретения сайт расщепления протеазой в случае гибридизации с вызывающим ответ Т-клеток пептидом. Аминокислотная последовательность пептидного линкера в настоящем изобретении обычно имеет от 8 до 50 аминокислотных остатков в длину. В одном из вариантов осуществления настоящего изобретения пептидный линкер по настоящему изобретению включает сайт расщепления фурином, и аминокислотная последовательность пептидного линкера включает:
- R-X-R-R, где X означает какой-либо аминокислотный остаток, или
- R-X-K-R, где X означает какой-либо аминокислотный остаток.
Понятие «домен транслокации» в рамках настоящего изобретения представляет структурный белковый домен, который отвечает за возможность мембранной транслокации и доступ в цитозоль, или функциональную часть указанного белкового домена. Примером домена транслокации является домен II из экзотоксина A Pseudomonas aeruginosa.
Понятие «фармацевтическая композиция» относится к препарату, который представлен в форме, обеспечивающей проявление биологической активности содержащегося в нем действующего ингредиента, и который не содержит дополнительных компонентов, неприемлемо токсичных для субъекта, которому могут вводить эту композицию. Фармацевтическую композицию по настоящему изобретению можно вводить различными способами, известными в данной области. Специалистам известно, что способ введения может варьировать в зависимости от требуемых результатов. Для введения иммуноконъюгата по настоящему изобретению в зависимости от способа введения может потребоваться нанесение покрытия на иммуноконъюгат или совместное введение иммуноконъюгата с материалом для предотвращения его инактивации. Например, иммуноконъюгат можно вводить субъекту в подходящем носителе, например в липосомах или в разбавителе. Фармацевтически приемлемые разбавители включают солевые и водные буферные растворы.
Понятие «фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтической композиции, отличной от активного ингредиента, который нетоксичен для субъекта. К фармацевтически приемлемым носителям относят какие-любо или все растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые агенты, изотонические агенты и агенты задержки абсорбции и другие, которые физиологически совместимы. Предпочтительно носитель применим для внутривенного, внутримышечного, подкожного, парентерального, спинального или эпидермального введения (например, путем инъекции или инфузии).
Фармацевтические композиции по настоящему изобретению также могут содержать адъюванты, например, консерванты, смачивающие агенты, эмульгаторы и диспергирующие агенты. Предотвращение наличия микроорганизмов может быть обеспечено путем описанной выше стерилизации, а также включением различных антибактериальных и противогрибковых агентов, например, парабена, хлорбутанола, фенола, сорбиновой кислоты и других. Также может быть желательно включать в композиции изотонические агенты, например, сахара, хлорид натрия и другие. Кроме того, пролонгированная абсорбция инъекционной фармацевтической формы может быть вызвана включением агентов, которые задерживают абсорбцию, например, моностеарата алюминия и желатина.
В настоящем изобретении понятия «парентеральное введение» и «вводимые парентерально» означают способы введения, отличные от введения внутрь и местного введения, обычно осуществляемые путем инъекции и включающие внутривенный, внутримышечный, внутриартериальный, интратекальный, внутрикапсулярный, внутриглазничный, внутрисердечный, внутрикожный, внутрибрюшинный, транстрахеальный, подкожный, подкутикулярный, внутрисуставный, субкапсулярный, субарахноидальный, внутриспинальный, эпидуральный и внутрисуставный способ введения инъекцией или инфузией, но ими перечень не ограничивается.
Независимо от выбранного способа введения иммуноконъюгаты по настоящему изобретению, которые могут быть использованы в соответствующей гидратированной форме, и/или фармацевтические композиции по настоящему изобретению, перерабатывают в фармацевтически приемлемые дозовые лекарственные формы с помощью обычных методов, известных специалистам в данной области.
Фактические уровни дозировки действующих ингредиентов в фармацевтических композициях по настоящему изобретению можно варьировать таким образом, чтобы получить количество действующего ингредиента, которое эффективно для достижения требуемого терапевтического ответа для конкретного пациента, в случае определенной композиции и определенного способа введения без токсичности для пациента. Выбранный уровень дозировки зависит от множества фармакокинетических факторов, включая действие применяемых конкретных композиций по настоящему изобретению, способа введения, времени введения, скорости экскреции конкретного используемого соединения, продолжительности лечения, других лекарственных средств, соединений и/или материалов, используемых в комбинации с определенными используемыми композициями, возраста, пола, массы тела, состояния больного, общего состояния здоровья и предыдущей истории болезни пациента, подвергаемого лечению, и подобных факторов, известных в медицине.
Композиция должна быть стерильной и текучей в такой степени, чтобы ее можно было ввести шприцом. Помимо воды предпочтительно носителем является изотонический буферный солевой раствор.
Должную текучесть можно поддерживать, например, с помощью покрытия, например, из лецитина, путем поддержания требуемого размера частиц в случае дисперсии и с использованием поверхностно-активных веществ. Во многих случаях предпочтительно включать в состав композиции изотонические агенты, например сахара, полиспирты, например маннит или сорбит, и хлорид натрия.
В настоящем изобретении понятие «цитотоксический агент» относится к соединению, которое ингибирует или препятствует клеточной функции и/или вызывает гибель или разрушение клеток. К цитотоксическим агентам относят, но ими перечень не ограничивают, радиоактивные изотопы (например, At211, I131, I125, Y90, Re186, Re188, Sm153, Bi212, P32, Pb212 и радиоактивные изотопы Lu), химиотерапевтические агенты или лекарственные средства (например, метотрексат, адриамицин, алкалоиды винка (винкристин, винбластин, этопозид), доксорубицин, мелфалан, митомицин С, хлорамбуцил, даунорубицин или другие интеркалирующие агенты), ингибирующие рост агенты, ферменты и их фрагменты, например нуклеолитические ферменты, антибиотики, токсины, например низкомолекулярные токсины или ферментативно активные токсины бактериального, грибного, растительного или животного происхождения, включая фрагменты и/или их варианты, а также описанные ниже различные противоопухолевые или противораковые агенты.
В контексте настоящего изобретения понятие «рак» относят к пролиферативным заболеваниям, например, к лимфомам, лимфоцитарным лейкозам, раку легкого, немелкоклеточному раку легкого (non small cell lung - NSCL), бронхоалвиолярному раку легких, раку костей, раку поджелудочной железы, раку кожи, раку головы или шеи, кожной или интраокулярной меланоме, раку матки, раку яичников, раку прямой кишки, раку анальной области, раку желудка, раку толстой кишки, раку молочной железы, раку матки, карциноме фаллопиевых труб, карциноме эндометрия, карциноме шейки матки, карциноме влагалища, карциноме вульвы, болезни Ходжкина, раку пищевода, раку тонкой кишки, раку эндокринной системы, раку щитовидной железы, раку щитовидной железы, раку надпочечника железа, саркоме мягких тканей, раку мочеиспускательного канала, раку полового члена, раку предстательной железы, раку мочевого пузыря, раку почки или мочеточника, карциноме почек, карциноме почечной лоханки, мезотелиоме, гепатоцеллюлярному раку, раку желчного пузыря, новообразованиям центральной нервной системы (ЦНС), опухолям позвоночника, глиоме ствола головного мозга, мультиформным глиобластомам, астроцитомам, шванномам, эпендимомам, медуллобластомам, менингиомам, плоскоклеточным карциномам, аденоме гипофиза и саркоме Юинга, включая устойчивые версии каких-либо перечисленных выше форм рака, или комбинации одного или нескольких из указанных выше форм рака.
Понятие «половина максимальной ингибирующей концентрации» («half maximal inhibitory concentration - IC50») означает концентрацию конкретного соединения или молекулы, необходимую для получения 50% ингибирования биологического процесса in vitro. Величины IC50 могут быть конвертированы логарифмически (-log IC50) для более высоких значений, показывающих экспоненциально большую эффективность. Величина IC50 не является абсолютным значением и зависит от условий эксперимента, например, от используемых концентраций. Величина IC50 может быть преобразована в абсолютную константу ингибирования (absolute inhibition constant - Ki), используя уравнение Ченга-Прусоффа (Biochem. Pharmacol. 22, 1973, 3099).
Понятие «рекомбинантный белок» является белком, который вырабатывается рекомбинантно сконструированными клетками-хозяевами. Такой белок необязательно выделяют или очищают.
В случае если часть молекулы, связывающей клетки-мишени, является белком, белок, связывающий клетку-мишень, предпочтительно вырабатывается методами рекомбинации. Методы рекомбинантного получения белков широко известны в данной области и включают экспрессию белка в прокариотических и эукариотических клетках с последующим выделением белка и обычно очисткой до фармацевтически приемлемой чистоты. Для экспрессии белков в клетке-хозяине нуклеиновые кислоты, кодирующие белок или его части, инсертируют в векторы экспрессии стандартными методами. Экспрессию осуществляют в соответствующих прокариотических или эукариотических клетках-хозяевах, например в клетках СНО, NS0, SP2/0, HEK293, COS, PER.C6, в клетках дрожжей или в клетках Е. coli, и выделяют белок из клеток (из супернатанта или клеток после лизиса). Общие методы рекомбинантного получения антител хорошо известны в данной области и описаны, например, в обзорах Makrides, Protein Expr. Purif. 17, 1999, 183-202; Geisse с соавт., Protein Expr. Purif. 8, 1996, 271-282; Kaufman, Mol. Biotechnol. 16, 2000, 151-161; Werner, Drug Res. 48, 1998, 870-880.
Подробное описание вариантов осуществления настоящего изобретения
Конъюгаты, содержащие специфический для Т-клеток патогенный пептид и белок, специфически связывающийся с рецептором на поверхности клетки-мишени, известны из ЕР 069497 А1. Однако эффективность презентации пептида МНС класса I на поверхности клеток и активация Т-клеток низки при использовании подхода, описанного в ЕР 069497 А1. В настоящем изобретении отмечают, не обосновывая какой-либо теорией, что этот эффект возникает из-за того, что конъюгат, содержащий описанный в ЕР 0694977 А1 пептид, требует дальнейшего процессирования в клетке-мишени. Это ограничивается тем обстоятельством, что в большинстве случаев экзогенно вырабатываемый антиген не направляется в цитоплазму, где он может быть процессирован протеосомами, далее транспортирован к метаболическому пути МНС класса I и презентирован на поверхности клетки. Другой, предположительно дополнительной причиной, может быть то обстоятельство, что дефектным являются механизм процессирования антигена или процесс презентации, особенно в опухолевых клетках (Ферроне, Advances in Cancer Research, 93, 2005, 189-234).
В настоящем изобретении предусматривают подход к улучшению презентации МНС класса I патогенных пептидов, специфических в отношении Т-клеток. По настоящему изобретению вызывающий ответ Т-клеток пептид, высвобождаемый из иммуноконъюгата в компартменте эндосом после интернализации иммуноконъюгата, непосредственно применим для презентации через связывание с МНС класса I комплексом (без необходимости дальнейшего процессирования или формирования в клетке-мишени). Вызывающий ответ Т-клеток пептид, связанный с молекулами МНС класса I в компартменте эндосом, переходит на поверхность клетки-мишени в контексте МНС класса I по метаболическому пути рециркуляции эндосом (Donaldson, Nat Rev Mol Cell Biol. 10(9), 2009, 597-608), не требует транспортировки к механизму процессирования антигена в цитозоле и дальнейшего процессирования внутри клетки. Таким образом, вызывающий ответ Т-клеток пептид и часть молекулы, связывающая клетки-мишени, соединены друг с другом через расщепляемую связь так, чтобы высвободить (после расщепления) вызывающий ответ Т-клеток пептид, состоящий из его первоначальной аминокислотной последовательности. Иначе говоря, если вызывающий ответ Т-клеток пептид выщепляется из иммуноконъюгата, он не содержит каких-либо дополнительных аминокислотных остатков и не утрачивает каких-либо аминокислотных остатков по сравнению с природной аминокислотной последовательностью вызывающего ответ Т-клеток пептида (т.е. высвобождаемый вызывающий ответ Т-клеток пептид имеет такую же длину, что и соответствующий природный вызывающий ответ Т-клеток пептид). В связи с этим иммуноконъюгаты по настоящему изобретению более применимы в качестве кандидатов для опосредования активации CD8 Т-клеток и индукции гибели клеток в клетках-мишенях. С иммуноконъюгатами по настоящему изобретению лизис клеток-мишеней индуцируется (а) значительно меньшим количеством необходимого иммуноконъюгата и (б) быстрее, особенно по сравнению с конструкциями, от которых пептид отщепляется, которые требуют дополнительного процессирования в клетке-мишени.
Настоящее изобретение относится к иммуноконъюгату, содержащему, по меньшей мере, один вызывающий ответ Т-клеток пептид, который презентируется через МНС класса I, соединенный с часть молекулы, связывающая клетки-мишени, через расщепляемую связь, причем расщепляемая часть составлена таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид, который (непосредственно) способен презентироваться через молекулу МНС класса I, высвобождается из иммуноконъюгата. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид высвобождается в компартмент клетки-мишени. В другом варианте осуществления настоящего изобретения высвобождаемый вызывающий ответ Т-клеток пептид способен презентироваться через МНС класса I без дополнительного процессирования в клетке-мишени.
Настоящее изобретение также относится к иммуноконъюгату, в котором аминокислотная последовательность высвобождаемого вызывающего ответ Т-клеток пептида идентична аминокислотной последовательности природного вызывающего ответ Т-клеток пептида.
В одном из вариантов осуществления настоящего изобретения аминокислотная последовательность высвобождаемого вызывающего ответ Т-клеток пептида идентична аминокислотной последовательности вызывающего ответ Т-клеток пептида, связанного с частью молекулы, связывающей клетку-мишень.
Настоящее изобретение также относится к иммуноконъюгату, содержащему, по меньшей мере, один вызывающий ответ Т-клеток пептид, который может быть презентирован через МНС класса I, связанный с частью молекулы, связывающей клетку-мишень, через расщепляемую связь, причем расщепляемая связь устроена таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид высвобождается из иммуноконъюгата, и высвобождаемый вызывающий ответ Т-клеток пептид состоит из такого же количества аминокислот, что и вызывающий ответ Т-клеток пептид, связанный с белком, связывающим клетку-мишень, причем вызывающий ответ Т-клеток пептид пригоден для презентации через МНС класса I комплекс.
Настоящее изобретение также относится к иммуноконъюгату, содержащему, по меньшей мере, один вызывающий ответ Т-клеток пептид, состоящий из 8-12 аминокислотных остатков, который способен к презентации через МНС класса I, соединенный с частью молекулы, связывающей клетку-мишень, через расщепляемую связь, причем расщепляемая связь устроена таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид высвобождается из иммуноконъюгата, и высвобождаемый вызывающий ответ Т-клеток пептид состоит из такого же количества аминокислот, что и вызывающий ответ Т-клеток пептид, связанный с частью молекулы, связывающей клетку-мишень,
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид состоит из 8-12 аминокислот.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом, включающим, по меньшей мере, один остаток цистеина. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид включает N- или С-концевой остаток цистеина. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом, включающим N-или С-концевой остаток цистеина.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид включает остаток цистеина с N-конца (положение 1 с N-конца в направлении к С-концу) его аминокислотной последовательности. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид естественным образом включает остаток цистеина с N-конца (положение 1 с N-конца в направлении к С-концу) его аминокислотной последовательности.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид включает остаток лейцина в положении 2 от N-конца в направлении к С-концу его аминокислотной последовательности. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид естественным образом включает остаток лейцина в положении 2 с N-конца в направлении к С-концу его аминокислотной последовательности. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид состоит из 8-12 аминокислотных остатков и естественным образом включает остаток лейцина в положении 2 с N-конца в направлении к С-концу его аминокислотной последовательности.
В одном из вариантов осуществления настоящего изобретения иммуноконъюгат включает до пяти вызывающих ответ Т-клеток пептидов. В одном из вариантов осуществления настоящего изобретения иммуноконъюгат включает до десяти вызывающих ответ Т-клеток пептидов.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным «не своего» патогена, который распознается иммунными клетками организма хозяина клеток-мишеней. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным внутриклеточного или внеклеточного патогена. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным внутриклеточного патогена. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным вирусного внутриклеточного патогена.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид выбран из последовательностей с SEQ ID NO: 2 по SEQ ID NO: 5.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным вируса Эпштейна-Барра. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным вируса Эпштейна-Барра и выбран из последовательностей с SEQ ID NO: 2 по SEQ ID NO: 4.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным герпесвируса человека 5. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным герпесвируса человека 5 и представляет последовательность SEQ ID NO: 5.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным вируса гриппа А. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид является производным вируса гриппа А и представляет последовательность SEQ ID NO: 3.
В одном из вариантов осуществления настоящего изобретения аминокислотная последовательность вызывающего ответ Т-клеток пептида, соединенная с частью молекулы, связывающей клетку-мишень, идентична, предпочтительно, аминокислотной последовательности из 8-12 аминокислот в длину, частично последовательности аминокислотной последовательности белкового антигена чужого патогена (в одном из вариантов осуществления настоящего изобретения внутриклеточного патогена).
Вызывающий ответ Т-клеток пептид связан с частью молекулы, связывающей клетку-мишень, через расщепляемую связь. В одном из вариантов осуществления настоящего изобретения расщепляемая связь расщепляется химически, в зависимости от рН или ферментативным расщеплением.
В одном из вариантов осуществления настоящего изобретения расщепляемая связь расщепляется после интернализации иммуноконъюгата в клетке-мишени.
В одном из вариантов осуществления настоящего изобретения расщепляемая связь расщепляется в компартменте эндосомы клетки-мишени. В одном из вариантов осуществления настоящего изобретения расщепляемая связь расщепляется после интернализации иммуноконъюгата в клетке-мишени в компартменте эндосомы клетки-мишени.
В одном из вариантов осуществления настоящего изобретения расщепляемая связь допускает бесследное высвобождение вызывающего ответ Т-клеток пептида из иммуноконъюгата.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид ковалентно связан с частью молекулы, связывающей клетку-мишень. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид ковалентно связан с частью молекулы, связывающей клетку-мишень, через дисульфидную связь, эфирную связь, пептидную связь или через линкерную часть молекулы.
В одном из вариантов осуществления настоящего изобретения расщепляемая связь выбрана из дисульфидной связи и эфирной связи. В одном из вариантов осуществления настоящего изобретения расщепляемая связь является дисульфидной связью. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина, и расщепляемой связью является дисульфидная связь. В одном из вариантов осуществления настоящего изобретения частью молекулы, связывающей клетку-мишень, является белок, и дисульфидная связь сформирована между остатком цистеина вызывающего ответ Т-клеток пептида и остатком цистеина белка, связывающего клетку-мишень. В другом предпочтительном варианте осуществления настоящего изобретения пептидный линкер содержится между частью молекулы, связывающей клетку-мишень, и вызывающим ответ Т-клеток пептидом. В этом случае дисульфидная связь формируется между остатком цистеина вызывающего ответ Т-клеток пептида и остатком цистеина пептидного линкера.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид и часть молекулы, связывающая клетки-мишени, соединены через расщепляемую линкерную часть молекулы.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид и часть молекулы, связывающая клетки-мишени, соединены через пептидный линкер или через химический линкер.
В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид и часть молекулы, связывающая клетки-мишени, соединены через пептидный линкер. В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид и связывающая клетки-мишени часть молекулы соединены через пептидный линкер с аминокислотной последовательностью из 8-50 аминокислотных остатков в длину.
В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает сайт расщепления протеазой. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает сайт расщепления протеазой, способный к расщеплению в эндосомальном или липосомальном компартменте клетки-мишени. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает сайт расщепления фурином.
В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы, включающая сайт расщепления протеазой, является пептидным линкером. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы, включающая сайт расщепления протеазой, является пептидным линкером, включающим указанный сайт расщепления протеазой. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы, включающая сайт расщепления протеазой, является пептидным линкером, включающим указанный сайт расщепления фурином.
В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает сайт расщепления, зависящий от рН. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает рН-зависимый сайт расщепления, расщепляемый в компартменте эндосом клетки-мишени. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы включает рН-зависимый сайт расщепления, расщепляемый при рН 5,5-6,5.
В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы, включающая рН-зависимый сайт расщепления, является химическим линкером. В одном из вариантов осуществления настоящего изобретения расщепляемая линкерная часть молекулы, включающая рН-зависимый сайт расщепления, выбрана из гидразона, оксима, амида малеиновой кислоты и кетала, представленных ниже:


В одном из вариантов осуществления настоящего изобретения вызывающий ответ Т-клеток пептид нековалентно связан с частью молекулы, соединенной с клеткой-мишенью. В одном из вариантов осуществления настоящего изобретения нековалентное соединение осуществляется иммунологическим связыванием.
В одном из предпочтительных вариантов осуществления настоящего изобретения иммунологическое связывание осуществляется антителом, специфически связывающимся с органической молекулой, которая включена в иммуноконъюгат. Связывание с вызывающим ответ Т-клеток пептидом, затем происходит между антителом и указанной органической молекулой, соединенной с вызывающим ответ Т-клеток пептидом. Для достижения высвобождения вызывающего ответ Т-клеток пептида без следа, вызывающий ответ Т-клеток пептид соединяют через расщепляемую связь с указанной органической молекулой. Таким образом, в одном из вариантов осуществления настоящего изобретения иммуноконъюгат включает:
- часть молекулы, соединенную с клеткой-мишенью, в форме мультиспецифичного, предпочтительно биспецифичного, объекта (в одном из вариантов осуществления настоящего изобретения рекомбинантный гибридный белок), включающего часть молекулы, соединенную с клеткой-мишенью, и вторую часть молекулы (в одном из вариантов осуществления настоящего изобретения это антитело), специфически связывающуюся с органической молекулой, предпочтительно с биотином или теофиллином, и
- вызывающий ответ Т-клеток пептид, который может специфически связываться вторым белком через расщепляемую связь.
В одном из вариантов осуществления настоящего изобретения органической молекулой является малая молекула с молекулярной массой до 900 Да. В одном из предпочтительных вариантов осуществления настоящего изобретения органической молекулой является биотин или теофиллин. В другом предпочтительном варианте осуществления настоящего изобретения органической молекулой является теофиллин.
В другом варианте осуществления настоящего изобретения нековалентное связывание осуществляется высоко аффинным связыванием, в одном из вариантов осуществления настоящего изобретения связыванием биотин-авидин. В другом варианте осуществления настоящего изобретения нековалентное связывание осуществляется высоко аффинным связыванием между пептидными метками, распознаваемыми второй связывающей частью молекулы (например, фрагментом Fab), резентированным в части молекулы, связывающей клетки-мишени, причем расщепляемая связь презентирована между вызывающим ответ Т-клеток пептидом и пептидной меткой. Таким образом, в одном из вариантов осуществления настоящего изобретения иммуноконъюгат включает:
- часть молекулы, соединенную с клеткой-мишенью, в форме мультиспецифичного, предпочтительно биспецифичного, объекта (в одном из вариантов осуществления настоящего изобретения рекомбинантный гибридный белок), включающего часть молекулы, связывающуюся с клеткой-мишенью, и вторую часть молекулы (в одном из вариантов осуществления настоящего изобретения это антитело), специфически связывающуюся с пептидной меткой, предпочтительно FLAG или V5, и
- вызывающий ответ Т-клеток пептид, который соединен с пептидной меткой, которая может быть специфически связана вторым белком через расщепляемую связь.
Иммуноконъюгат по настоящему изобретению содержит часть молекулы, связывающуюся с клеткой-мишенью, чтобы направить вызывающий ответ Т-клеток пептид в клетку-мишень.
В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, способна интернализироваться в клетке-мишени.
В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, связывается с антигеном на поверхности клетки-мишени.
В одном из вариантов осуществления настоящего изобретения клеткой-мишенью является опухолевая клетка. В другом варианте осуществления настоящего изобретения, в котором клеткой-мишенью является опухолевая клетка, часть молекулы, связывающаяся с клеткой-мишенью, способна специфически связываться с экспрессированным на поверхности опухоль-специфичным антигеном (tumor specific antigen - TSA), который презентирован только на опухолевых клетках, но не на других клетках), или с экспрессированным на поверхности опухоль-ассоциированным антигеном (tumor associated antigen - ТАА), который презентирован только на опухолевых клетках и в меньшей степени на некоторых других клетках).
В одном из вариантов осуществления настоящего изобретения клетки-мишени являются клетками, ассоциированными с тяжестью заболевания в случае инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии.
В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является белком. В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является рекомбинантным белком. В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является белком, специфически связывающимся с клеткой-мишенью, или лигандом, связывающимся с рецепторами на клетке-мишени. В другом варианте осуществления настоящего изобретения белок, связывающийся с клеткой-мишенью, выбран из антител, цитокинов и факторов роста. В одном из предпочтительных вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является антителом.
В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, специфически связывается с CD19 или CDCP-1. В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, связывается с CD19. В одном из вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, связывается с CDCP-1.
В одном из предпочтительных вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является антителом, которое специфически связывается с CD19 или CDCP-1. В одном из предпочтительных вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является антителом, которое специфически связывается с CD19. В одном из предпочтительных вариантов осуществления настоящего изобретения часть молекулы, связывающаяся с клеткой-мишенью, является антителом, которое специфически связывается с CDCP-1.
В одном из вариантов осуществления настоящего изобретения иммунокунъюгат способен интернализироваться в клетках-мишенях.
В соответствии с настоящим изобретением вызывающий ответ Т-клеток пептид способен непосредственно презентироваться МНС класса I и не требует дополнительного процессинга внутри клеток-мишеней. Таким образом, в одном из вариантов осуществления настоящего изобретения иммуноконъюгат не включает домена транслокации.
В соответствии с настоящим изобретением предусматривают иммуноконъюгат, который позволяет высвобождать вызывающий ответ Т-клеток пептид, который способен непосредственно презентироваться через МНС класса I. Поскольку высвобождаемый вызывающий ответ Т-клеток пептид не требует доставки на антиген-процессирующий механизм в цитозоле, вызывающие ответ Т-клеток пептиды презентируются на поверхности целевых клеток за короткий период времени. Поэтому в одном из вариантов осуществления настоящего изобретения менее чем через 12 ч после интернализации иммуноконъюгата в клетках-мишенях вызывающий ответ Т-клеток пептид презентируется на поверхности клеток-мишеней через молекулу МНС класса I. В другом варианте осуществления настоящего изобретения менее чем через 6 ч после интернализации иммуноконъюгата в клетках-мишенях вызывающий ответ Т-клеток пептид презентируется на поверхности клеток-мишеней через молекулу МНС класса I. В другом варианте осуществления настоящего изобретения иммуноконъюгат способен опосредовать цитотоксичность Т-клеток в отношении клеток-мишеней менее чем за 6 ч после интернализации иммуноконъюгата в клетке-мишени.
Настоящее изобретение также относится к фармацевтической композиции, включающий иммуноконъюгат по настоящему изобретению. В одном из вариантов осуществления настоящего изобретения фармацевтическая композиция, включающая иммуноконъюгат по настоящему изобретению в комбинации с фармацевтически приемлемым носителем.
Другой объект настоящего изобретения представляет применение вызывающего ответ Т-клеток пептида, который может быть презентирован через МНС класса I в качестве дополнительно описанного и определенного выше для выработки иммуноконъюгата по настоящему изобретению.
Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для специфически индуцируемой цитотоксичности Т-клеток против клеток-мишеней. В одном из вариантов осуществления настоящего изобретения иммуноконъюгат применяют для специфически индуцируемого опосредованного клетками иммунитета через CD8 Т-клетки против клеток-мишеней. В одном из вариантов осуществления настоящего изобретения иммуноконъюгат интернализуется в клетку-мишень и вызывающийся ответ Т-клеток пептид высвобождается из иммуноконъюгата в компартменте эндосом клетки-мишени. В одном из вариантов осуществления настоящего изобретения менее чем через 12 ч после интернализации иммуноконъюгата в клетке-мишени пептид, вызывающий ответ Т-клеток, презентируется на поверхности клетки-мишени через молекулу МНС класса I. В другом варианте осуществления настоящего изобретения не менее чем через 6 ч после интернализации иммуноконъюгата на поверхности клетки-мишени пептид, вызывающий ответ Т-клеток, презентируется на поверхности клетки-мишени через молекулу МНС класса I.
В другом варианте осуществления настоящего изобретения иммуноконъюгат применяют для опосредования цитотоксичности Т-клеток против клетки-мишени менее чем за 6 ч после интернализации иммуноконъюгата в клетке-мишени.
Другой объект настоящего изобретения представляет способ получения иммуноконъюгата по настоящему изобретению, включающий стадии:
а) получения рекомбинантной части молекулы, связывающей клетку-мишень,
б) получения вызывающего ответ Т-клеток пептида, и
в) соединения, по меньшей мере, одного указанного вызывающего ответ Т-клеток пептида с указанной частью молекулы, связывающей клетку-мишень, через расщепляемую связь.
В одном из вариантов осуществления настоящее изобретение связано со способом получения иммуноконъюгата, в котором немодифицированный вызывающий ответ Т-клеток пептид соединен с частью молекулы, связывающей клетку-мишень. Иначе говоря, в одном из вариантов осуществления настоящее изобретение связано со способом получения иммуноконъюгата, в котором предусматривают вызывающий ответ Т-клеток пептид без модификаций аминокислотной последовательности, соединенный с частью молекулы, связывающей клетку-мишень.
Другой объект настоящего изобретения представляет способ получения иммуноконъюгата по настоящему изобретению для специфической индукции клеточно-опосредованного иммунитета посредством CD8 Т-клеток против клеток-мишеней, включающий стадии:
а) получения рекомбинантной части молекулы, связывающей клетку-мишень,
б) получения вызывающего ответ Т-клеток пептида, и
в) соединения, по меньшей мере, одного указанного вызывающего ответ Т-клеток пептида с указанной частью молекулы, связывающей клетку-мишень.
Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для получения фармацевтической композиции. Другой объект настоящего изобретения представляет способ для получения фармацевтической композиции, включающий иммуноконъюгат по настоящему изобретению, в том числе иммуноконъюгат по настоящему изобретению в комбинации, по меньшей мере, с одним фармацевтически приемлемым носителем.
Другой объект настоящего изобретения представляет иммуноконъюгат по настоящему изобретению для применения в качестве лекарственного средства. Другой объект настоящего изобретения представляет иммуноконъюгат по настоящему изобретению, включающий связывающую раковые клетки часть молекулы для лечения рака.
Другой объект настоящего изобретения представляет иммуноконъюгат по настоящему изобретению для применения в лечения инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии.
Другой объект настоящего изобретения представляет иммуноконъюгат по настоящему изобретению для применения в специфически индуцируемом клеточно-опосредованном иммунитете через CD8 Т клетки против клеток-мишеней.
Другой объект настоящего изобретения представляет фармацевтическую композицию по настоящему изобретению для применения в качестве лекарственного средства. Другой объект настоящего изобретения представляет фармацевтическую композицию по настоящему изобретению, в которой иммуноконъюгат, включенный в фармацевтическую композицию, содержит часть молекулы, связывающую раковую клетку, для лечения рака. Другой объект настоящего изобретения представляет фармацевтическую композицию по настоящему изобретению для лечения инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии. Другой объект настоящего изобретения представляет фармацевтическую композицию по настоящему изобретению для применения в специфически индуцированном клеточно-опосредованном иммунитете через CD8 Т-клетки против клеток-мишеней.
Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для получения лекарственного средства. Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для получения лекарственного средства для лечения рака.
Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для получения лекарственного средства для лечения инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии. Другой объект настоящего изобретения представляет применение иммуноконъюгата по настоящему изобретению для получения лекарственного средства для специфической индукции опосредованного клетками иммунитета через CD8 Т-клетки против клеток-мишеней.
Другой объект настоящего изобретения представляет способ лечения больного пациента путем введения иммуноконъюгата по настоящему изобретению пациенту, нуждающемуся в таком лечении. Другой объект настоящего изобретения представляет способ лечения пациента больного раком путем введения иммуноконъюгата по настоящему изобретению, включающему часть молекулы, связывающую раковые клетки, пациенту, нуждающемуся в таком лечении. Другой объект настоящего изобретения представляет способ лечения пациента с инфекционным заболеванием, аутоиммунным заболеванием, диабетом или аллергией путем введения иммуноконъюгата по настоящему изобретению пациенту, нуждающемуся в таком лечении.
Другой объект настоящего изобретения представляет способ лечения больного путем введения фармацевтической композиции по настоящему изобретению пациенту, нуждающемуся в таком лечении. Другой объект настоящего изобретения представляет способ лечения пациента больного раком путем введения фармацевтической композиции по настоящему изобретению пациенту, нуждающемуся в таком лечении. Другой объект настоящего изобретения представляет способ лечения пациента с инфекционным заболеванием, аутоиммунным заболеванием, диабетом или аллергией путем введения иммуноконъюгата по настоящему изобретению пациенту, нуждающемуся в таком лечении.
Конкретные варианты осуществления настоящего изобретения
Ниже перечислены варианты осуществления настоящего изобретения.
1. Иммуноконъюгат, содержащий, по меньшей мере, один вызывающий ответ Т-клеток пептид, который может быть презентирован через МНС-класса I, соединенный с частью молекулы, связывающей клетку-мишень, через расщепляемую связь, в котором расщепляемая связь сконструирована таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид, который непосредственно презентируется через молекулу МНС класса I, высвобождается из иммуноконъюгата.
2. Иммуноконъюгат по варианту осуществления настоящего изобретения 1, в котором аминокислотная последовательность высвободившегося вызывающего ответ Т-клеток пептида идентична аминокислотной последовательности природного вызывающего ответ Т-клеток пептида.
3. Иммуноконъюгат по варианту осуществления настоящего изобретения 2, в котором высвободившийся вызывающий ответ Т-клеток пептид такой же длины, что и природный вызывающий ответ Т-клеток пептид.
4. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в котором вызывающий ответ Т-клеток пептид является природным вызывающим ответ Т-клеток пептидом.
5. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в котором вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина.
6. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в котором вызывающий ответ Т-клеток пептид включает N- или С-концевой остаток цистеина.
7. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в котором вызывающий ответ Т-клеток пептид включает лейцин в положении 2 (отсчет в направлении от N-конца с С-концу).
8. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, включающий до пяти вызывающих ответ Т-клеток пептидов.
9. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид состоит из 8-12 аминокислот.
10. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид является производным вируса Эпштейна-Барра, герпесвируса 5 человека или вируса гриппа А.
11. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид является производным вируса Эпштейна-Барра.
12. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид является производным вируса герпесвируса 5 человека.
13. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид является производным вируса гриппа А.
14. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид выбран из последовательностей с SEQ ID NO: 2 по SEQ ID NO: 5.
15. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых расщепляемой связью является связь, расщепляемая химически, в зависимости от рН или ферментативно.
16. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых расщепляемой связью является связь, расщепляемая после интернализации иммуноконъюгата в клетке-мишени.
17. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых расщепляемой связью является связь, расщепляемая в компартменте эндосом клетки-мишени.
18. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид ковалентно связан с частью молекулы, связывающей клетку-мишень.
19. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых расщепляемая связь выбрана из дисульфидной связи или из сложноэфирной связи.
20. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых расщепляемая связь является дисульфидной связью.
21. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина и расщепляемая связь является дисульфидной связью.
22. Иммуноконъюгат по вариантам осуществления настоящего изобретения 1-18, в которых вызывающий ответ Т-клеток пептид и часть молекулы, связывающая клетку-мишень, соединены через расщепляемую линкерную часть молекулы.
23. Иммуноконъюгат по варианту осуществления настоящего изобретения 22, в котором расщепляемая линкерная часть молекулы включает сайт расщепления протеазой.
24. Иммуноконъюгат по варианту осуществления настоящего изобретения 23, в котором расщепляемая линкерная часть молекулы включает сайт расщепления фурином.
25. Иммуноконъюгат по варианту осуществления настоящего изобретения 22, в котором расщепляемая линкерная часть молекулы включает рН-зависимый сайт расщепления.
26. Иммуноконъюгат по варианту осуществления настоящего изобретения 25, в котором рН-зависимый сайт расщепления способен расщепляться при рН 5,5-6,5.
27. Иммуноконъюгат по вариантам осуществления настоящего изобретения 22-26, в которых расщепляемой линкерной частью молекулы является химический линкер.
28. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, способна интернализироваться в клетке-мишени.
29. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, связывается с антигеном на поверхности клетки-мишени.
30. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых клетка-мишень является опухолевой клеткой.
31. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, является белком.
32. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, является антителом, специфически связывающимся с клеткой-мишенью, или лигандом, связывающимся с его рецептором на клетке-мишени.
33. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, специфически связывается с CD19 или CDCP-1.
34. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, специфически связывается с CD19.
35. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, специфически связывается с CDCP-1.
36. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, является антителом, специфически связывающимся с CD19 или CDCP-1.
37. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, является антителом, специфически связывающимся с CD19.
38. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых часть молекулы, связывающая клетку-мишень, является антителом, специфически связывающимся с CDCP-1.
39. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, способный интернализироваться в клетке-мишени.
40. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых иммуноконъюгат не включает домена транслокации.
41. Иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в которых менее чем за 12 ч после интернализации иммуноконъюгата в клетке-мишени вызывающий ответ Т-клеток пептид презентируют на поверхности клетки-мишени через молекулу МНС класса I.
42. Фармацевтическая композиция, включающая иммуноконъюгат по какому-либо из предшествующих вариантов осуществления настоящего изобретения, в комбинации с фармацевтически приемлемым носителем.
43. Применение вызывающего ответ Т-клеток пептида, презентируемого через МНС класса I для выработки иммуноконъюгата по вариантам осуществления настоящего изобретения 1-41.
44. Применение иммуноконъюгата по вариантам осуществления настоящего изобретения 1-41 для специфической индукции цитотоксичности Т-клеток против клеток-мишеней.
45. Применение по варианту осуществления настоящего изобретения 44, в котором иммуноконъюгат интернализуется в клетке-мишени, и вызывающий ответ Т-клеток пептид высвобождается из иммуноконъюгата в компартменте эндосом клетки-мишени.
46. Применение по вариантам осуществления настоящего изобретения 44 или 45, в которых не менее чем через 12 ч после интернализации иммуноконъюгата в клетке-мишени презентируется вызывающий ответ Т-клеток пептид на поверхности клетки-мишени через молекулу МНС класса I.
47. Способ выработки иммуноконъюгата по какому-либо из вариантов осуществления настоящего изобретения 1-41, включающий стадии:
- получения рекомбинантной части молекулы, связывающей клетку-мишень,
- получения вызывающего ответ Т-клеток пептида,
- соединения, по меньшей мере, одного из указанных вызывающих ответ Т-клеток пептида с указанной частью молекулы, связывающей клетку-мишень, через расщепляемую связь.
48. Способ по варианту осуществления настоящего изобретения 47, в котором немодифицированный вызывающий ответ Т-клеток пептид, соединен с частью молекулы, связывающей клетку-мишень.
49. Иммуноконъюгат по вариантам осуществления настоящего изобретения 1-41 для применения в качестве лекарственного средства.
50. Иммуноконъюгат по вариантам осуществления настоящего изобретения 1-41, включающий часть молекулы, связывающую раковую клетку, для лечения рака.
51. Иммуноконъюгат по какому-либо из вариантов осуществления настоящего изобретения 1-41 для лечения инфекционных заболеваний, аутоиммунных заболеваний, диабета или аллергии.
52. Способ лечения пациента, нуждающегося в таком лечении, путем введения иммуноконъюгата по какому-либо из вариантов осуществления настоящего изобретения 1-41.
53. Способ лечения пациента, больного раком и нуждающемуся в таком лечении, путем введения иммуноконъюгата по какому-либо из вариантов его осуществления 1-41, содержащего связывающую раковые клетки часть молекулы.
Описание аминокислотных последовательностей

Примеры
Приводимые ниже примеры предназначены для лучшего понимания и не ограничивают области охвата настоящего изобретения, истинный объем которого изложен в формуле изобретения. Очевидно, что в приводимых ниже примерах могут быть произведены изменения без отклонения от сущности настоящего изобретения.
Пример 1. Влияние С- или N-концевой модификации пептида CMV на связывание с МНС класса I (HLA-A2) и CMV-специфическую активацию Т-клеток
Чтобы оценить роль модификаций С- или N-концевой аминокислоты, произведенных в вызывающем ответ Т-клеток пептиде, производят следующие модификации в природном пептиде CMV с аминокислотной последовательностью NLVPMVATV (SEQ ID NO: 1):
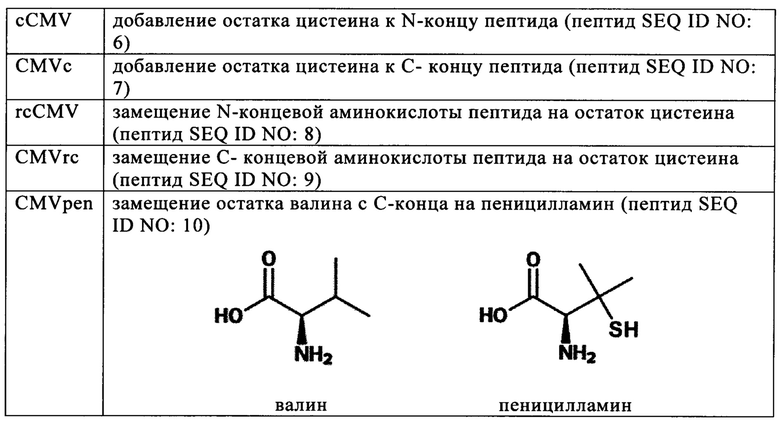
Пептиды синтезируют с использованием стандартной Fmoc-химии. Все используемые аминокислоты являются L-изомерами.
Пример 1А. Получение специфичных по CMV-пептиду Т-клеток из периферической крови здоровых доноров
Исследуют частоту встречаемости специфичных по CMV-пептиду CD8 Т-клеток в свежевыделенных МКПК здоровых доноров или в культурах Т-клеток методом FACS с помощью окрашивания пентамером.
Вкратце, аликвоты культур Т-клеток, содержащие 3-5×105 клеток, или свежевыделенные МКПК от HLA-А2-соответствующих здоровых доноров промывают буфером BD FACS и инкубируют со 100 мкл буфера BD FACS, содержащего 5 мкл human TruStain FcX (фирма BioLegend, номер в каталоге 422302), в течение 15 мин при комнатной температуре. Затем добавляют 90 мкл буфера BD FACS, содержащего 10 мкл конъюгированного с биотином активного продукта CMV-Pentamer (фирма ProImmune, F008-4, 1:10) и инкубируют в течение 1 часа при 4°C.
После промывки буфером BD FACS клетки окрашивают в 100 мкл буфера BD FACS с FITC-меченым анти-CD8a mAb (клон LT8, фирма ProImmune), а также конъюгатом стрептавидин-АРС при 4°C в течение 20 мин. После трехкратных промываний буфером BD FACS и центрифугирования клетки ресуспендируют в 200 мкл буфера BD FACS, содержащего 1 мкг/мл DAPI, сигналы MFI окрашенных клеток исследуют в проточном цитофлуориметре BD Biosciences FACSCanto II. Клетки от доноров HLA-A1 используют для оценки неспецифического связывания тетрамеров.
Свежевыделенные МКПК применяют для стимуляции в день выделения с CMV-производным пептидом NLVPMVATV (SEQ ID NO: 1) следующим образом:
В 96-луночный планшет вносят клетки в количестве 2×105 на лунку в 200 мкл среды RPMI+ с 1 мкМ пептида и инкубируют трое суток. На третьи сутки планшет центрифугируют в режиме 300 g в течение 2 мин, после чего из лунок удаляют по 160 мкл супернатанта, который заменяют свежей средой RPMI+, содержащей 1 мкМ пептида и 100 ЕД/мл IL-2. На 8 и 10 сутки среду опять заменяют так же, как это описано на 3 сутки. Культивируемые клетки разделяют на 14 сутки без стимуляции пептидом. На 16 сутки культуру клеток повторно стимулируют без аутологичных МКПК (облученных 11 Гру) и обрабатывают CMV-пептидом следующим образом: в лунки 6-луночного планшета вносят 12×106 Т-клеток в 200 мкл среды RPMI+, содержащей 1 мкМ пептида, плюс 8,7×106 облученных МКПК. На 19, 21 и 25 сутки культуры расщепляют опять и стимулируют согласно описанному выше на 30 сутки. На 35, 37 и 41 сутки культуры расщепляют еще раз и на 44 сутки ресуспендируют в соответствии с протоколом. Культуру исследуют на содержание CMV-пептид специфических клеток и применяют на 51 сутки в методе анализа LDH цитотоксичности на 54 сутки в методе ELISPOT для определения специфичности против Т-клеток, нагруженных индикаторным CMV-пептидом.
Пример 1Б. Оценка активации CMV-пептид специфичных Т-клеток после обработки опухолевых клеток свободными пептидами CMV методом IFNγ-ELISPOT.
HLA-A2 ограниченную активацию CMV-пептид специфических Т-клеток оценивают методом IFNγ-ELISPOT на разных линиях опухолевых клеток, экспрессирующих различные уровни соответствующих молекул МНС I на поверхности клеток:
- MDA-MB 231: высокий уровень HLA-A2
- НСТ-116: низкий уровень HLA-A2
- Т2: линии ТАР-недостаточных клеток, которые не экспрессируют ненагруженные молекулы МНС класса I на поверхности клеток
Вкратце, 10000 опухолевых клеток соответственно обрабатывают разными концентрациями свободных модифицированных пептидов CMV (cCMV, CMVc, rcCMV, CMVrc, CMVpen) или природного немодифицированного пептида CMV (в концентрациях 13,245 мкМ или 1,3245 мкМ) в присутствии 500 CMV-специфичных CD8 Т-клеток, полученных в примере 1А. В качестве контролей опухолевые клетки и Т-клетки инкубируют в отсутствии свободного пептида и, в качестве дополнительного контроля, Т-клетки инкубируют отдельно в тех же условиях.
Эксперименты проводят либо с использованием среды RPMI+ с сывороткой или среды AIM-V без сыворотки.
Анализ методом IFNγ-ELISPOT проводят следующим образом:
В первые сутки планшеты промывают стерильным ФСБ. Затем в лунки добавляют по 50 мкл среды RPMI+ и планшеты инкубируют в течение 20-30 мин. После этого пептиды добавляют 50 мкл RPMI+ в соответствующие лунки. Соответствующие опухолевые клетки собирают с использованием аккутазы. Добавляют по 10000 опухолевых клеток в 100 мкл RPMI+ в соответствующие лунки. После инкубации в течение 20 мин планшеты инкубируют в темноте в течение примерно 6 ч. Т-клетки фильтруют через сито с порами 40 мкм и промывают однократно RPMI+ (центрифугируют в режиме 300 g в течение 2 мин). Добавляют 50 мкл среды RPMI+, содержащих 500 пептид-специфических CD8 Т-клеток. Планшеты инкубируют в течение ночи.
На второй день планшет освобождают и промывают ФСБ. Моноклональное антитело против IFN-γ человека (Mabtech 7-B6-ALP) разводят 1:200 в отфильтрованном ФСБ/0,5% ФСТ. По 100 мкл разведенного антитела вносят в лунки и инкубируют в течение 2 ч. Затем планшеты промывают ФСБ. Раствор субстрата (BCIP/NBT-plus) фильтруют через фильтр с порами 0,45 мкм. По 100 мкл раствора субстрата добавляют в лунки и выдерживают до появления отдельных пятен. После остановки процесса промыванием в водопроводной воде пластины высушивают в темноте.
Планшеты исследуют с помощью системы ELISPOT Reader (фирма Cellular Technology Ltd.) для метода иммуноферментных пятен, используя программное обеспечение «ImmunoSpot 5.0 professional DC».
Состав среды RPMI+:
500 мл среды RPMI 1640 (фирма Life Technologies)
8% сыворотка человека (инактивированная нагреванием и отфильтрованная)
1% L-глутамин
1% NEAA
1% натрий пируват
0,2% ПенициллинСтрептомицин
0,1% β-меркаптоэтанол
Результаты представлены на фиг. 1.
Установлено, что N-концевая модификация CMV-пептида приводит к утрате активации Т-клеток. С-концевая модификация ослабляет активацию Т-клеток. Кроме того, модификация боковой цепи аминокислоты, естественным образом присутствующей в аминокислотной последовательности CMV-пептида, приводит к потере активации Т-клеток. Следовательно, можно сделать вывод, что модификации в природном вызывающем ответ Т-клеток пептиде могут влиять (то есть ослаблять) на нагрузку на молекулы МНС класса I и, соответственно, на активацию Т-клеток.
Тем не менее, при использовании природных вызывающих ответ Т-клеток пептидов можно гарантировать оптимальное связывание и загрузку МНС класса I.
Пример 2. Предполагаемый способ действия иммуноконъюгатов по настоящему изобретению
На фиг. 2 показывают предполагаемый способ действия иммуноконъюгатов по настоящему изобретению. Например, антитело показывают в качестве части молекулы, связывающей клетки-мишени, однако другие части молекулы также могут быть применимы.
В устойчивом состоянии поверхность клетки-мишени (например, поверхность опухолевой клетки) содержит антиген-мишень, с которой специфически связывается часть молекулы, связывающая клетки-мишени. Кроме того, молекулы МНС класса I, презентирующие собственные пептиды, экспрессируются на поверхности клетки.
Без теоретического обоснования, связывание иммуноконъюгата с целевым антигеном (А) приводит к интернализации комплекса целевого антиген-иммуноконъюгата (Б) и к последующему высвобождению вызывающего ответ Т-клеток пептида из иммуноконъюгата в компартменте ранних эндосом (В). Важно отметить, что высвобождаемый пептид состоит из аминокислотной последовательности, идентичной соответствующему природному пептиду, и не содержит каких-либо модификаций аминокислот, в частности, каких-либо модификаций С- или N-концевой аминокислоты.
Собственные пептиды, презентированные на молекулах МНС класса I, пассивно заменяются на чужой пептид (т.е. вызывающий ответ Т-клеток пептид отщепляется от иммуноконъюгата) в компартменте эндосом (Г). Нагруженные пептидом молекулы МНС класса I поступают на поверхность клетки по траффику эндосом (Д), что приводит к презентации вызывающего ответ Т-клеток пептида на поверхности клетки-мишени в контексте МНС класса I.
Пептид-специфичные CD8 Т-клетки распознают и связываются с нагруженными пептидом молекулами МНС класса I на клетках-мишенях (Е), приводя к специфической индукции цитотоксичности Т-клеток против клеток-мишеней.
Пример 3. Конъюгирование моноклонального анти-CDCP1 антитела, по меньшей мере, с одним вызывающим ответ Т-клеток пептидом, способным к презентации через МНС класса I.
Для получения иммуноконъюгата по настоящему изобретению, моноклональное антитело (mAb), специфически связывающееся с CUB-домен-содержащим белком 1 (CDCP1, также обозначаемым CD318, описанным в ЕР 1396501 А1), соединяют с одним из следующих пептидов, производных от патогенов:
- пептидом вируса Эпштейна-Барра (EBV) 426-434 (SEQ ID NO: 2, CLGGLLTMV), или
- пептидом вируса гриппа A NP (FLU) 44-52 (SEQ ID NO: 3, CTELKLSDY).
Пептиды синтезируют, используя стандартную Fmoc-химию. Все используемые аминокислоты являются L-изомерами.
Пример 3А. Получение иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело и пептид EBV и/или FLU, в которых пептиды соединены с антителом через расщепляемую связь S-S.
Для получения вариантов иммуноконъюгатов по настоящему изобретению, в которых иммуноконъюгат включает дисульфидную связь для высвобождения пептида при интернализации в клетке-мишени, пептиды соединяют с антителом следующим образом:
αCDCP1-mAb сначала модифицируют в 0,1 М калий-фосфатном буфере при рН 7,2 при наличии 10 эквивалентов N-сукцинимидил-3-(2-пиридилдитио)-пропионата (SPDP, фирма Pierce). Через 2 ч протекания реакции модифицированное антитело очищают гель-фильтрацией в 0,1 М калий-фосфатном буфере, содержащем 10 мМ EDTA, при рН 7,0.
Для получения иммуноконъюгатов, включающих либо пептид EBV, либо пептид FLU, к модифицированному антителу добавляют 10 эквивалентов соответствующего пептида и осуществляют реакцию на протяжении ночи. Иммуноконъюгаты по настоящему изобретению очищают гель-фильтрацией.
Для получения иммуноконъюгатов, включающих и пептид EBV, и пептид FLU, к модифицированному антителу добавляют по 5 эквивалентов каждого из пептидов, EBV и FLU, и осуществляют реакцию на протяжении ночи. Иммуноконъюгаты по настоящему изобретению очищают гель-фильтрацией.
В настоящем изобретении получают следующие иммуноконъюгаты по настоящему изобретению:
- <CDCP1-SS-pEBV> иммуноконъюгат, включающий анти-CDCP1 моноклональное антитело, соединенное с пептидом EBV 426-434 дисульфидной связью
- <CDCP1-SS-pFLU> иммуноконъюгат, включающий анти-CDCP1 моноклональное антитело, соединенное с пептидом FLU 44-52 дисульфидной связью
- <CDCP1-SS-pEBV/FLU> иммуноконъюгат, включающий анти-CDCP1 моноклональное антитело, соединенное с пептидом EBV 426-434 и пептидом FLU 44-52 соответствующими дисульфидными связями
Пример 3Б (сравнение). Получение иммуноконъюгатов, включающих анти-CDCP1 моноклональное антитело и пептид EBV или пептид FLU, где пептиды соединены с антителом через нерасщепляемую тиоэфирную связь.
Для сравнительного исследования пептиды конъюгируют с антителом без возможности расщепления через тиоэфирную связь:
Сначала αCDCP1-mAb сначала модифицируют в 0,1 М калий-фосфатном буфере при рН 7,2 при наличии 10 эквивалентов сложного эфира N-эпсилон-малемидокапроил-оксисукцинимида (SPDP, фирма Pierce). Через 2 ч протекания реакции модифицированное антитело очищают гель-фильтрацией в 0,1 М калий-фосфатном буфере, содержащем 10 мМ EDTA, при рН 7,0.
Затем 10 эквивалентов соответствующего пептида добавляют к модифицированному антителу и осуществляют реакцию на протяжении ночи. Иммуноконъюгаты очищают гель-фильтрацией.
Получаемые иммуноконъюгаты, используемые для сравнения, обозначают следующим образом:
- <CDCP1-S-pEBV> иммуноконъюгат, включающий анти-CDCP1 Mab, соединенное с пептидом EBV 425-433 тиоэфирной связью
- <CDCP1-S-pFLU> иммуноконъюгат, включающий анти-CDCP1 Mab, соединенное с пептидом FLU 44-52 тиоэфирной связью
Пример 3В. Анализ методом масс-спектрометрии (MS) и оценка стабильности иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело, соединенное с пептидом EBV и/или FLU.
Оценку интенсивности нанесенной метки на иммуноконъюгаты, полученные в примерах 3А и 3Б, исследуют методом LC-ESI масс-спектрометрии.
Подготовка препаратов: IgG или меченый-IgG дегликозилируют перед измерением N-гликозилазой F. IgG или меченый IgG в другом варианте снижают с помощью ТСЕР после гликозилирования для измерения по отдельности легкой цепи и тяжелой цепи.
Исследования проводят с помощью системы LC-ESI-MS (фирма Waters) HPLC System с обратнофазовой колонкой в градиенте вода : ацетонитрил измерением и детекцией методом ESI-TOF-MS. Анализ данных MS осуществляют с применением программного обеспечения MassLynx Software (фирма Waters).
Анализ показал, что в среднем 0,8 пептидов соединяется с каждой молекулой антитела (данные не показаны).
Чтобы проверить стабильность иммуноконъюгатов, оценивают стабильность в исходном растворе и в среде культуры клеток. Исходные растворы иммуноконъюгатов фильтруют с помощью спиновых колонок (отсечение по молекулярной массе 50 кДа) и анализируют с помощью жидкостной хроматографии с масс-спектрометрией (LC-MS). Свободный пептид не выявляют. Клеточную культуральную среду, которую очищают иммуноконъюгатами, анализируют методом LC-MS. Свободный пептид не выявляют. В качестве положительного контроля в среду для культуры клеток вносят свободный пептид.
Пример 3Г. Изучение связывания с клетками иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело, соединенное с пептидом EBV и/или FLU, с CDCP1-экспрессирующими клетками MDA-MB 231.
Для оценки связывания иммуноконъюгатов с соответствующими антигенами, оценивают связывание иммуноконъюгатов из примеров 3А и 3Б с CDCP1-экспрессирующими клетками MDA-MB 231 в анализе на основе FACS.
Вкратце, клетки MDA-MB 231 отсоединяют путем обработки аккутазой, освобождают от среды для отсоединения клеток центрифугированием и суспендируют в среде для клеток MDA-MB 231 в концентрации 4×106 клеток/мл. Аликвоты по 50 мкл инкубируют с серийными разведениями (20 мкг/мл - 0,02 мкг/мл иммуноконъюгата в буфере BD FACS) иммуноконъюгата или неконъюгированных анти-CDCP1 антител (исходных анти-CDCP1 антител) в течение 30 мин при 4°C. После промывки буфером BD FACS клетки окрашивают FITC-меченым anti-human IgG H+L (фирма Invitrogen, номер в каталоге А11013; 10 мкг/мл в буфере BD FACS) в течение 30 мин при 4°C. После промывки и центрифугирования исследуют сигналы MFI окрашенных клеток с помощью жидкостного цитометра BD Biosciences FACSCanto (фиг. 3).
Результаты исследования связывания клеток методом на основе FACS, представленные на фиг. 3, показывают, что все иммуноконъюгаты связываются с CDCP1-экспрессирующими опухолевыми клетками MDA-MB 231 сопоставимым образом.
Пример 3Д. Изучение методом поверхностного плазмонного резонанса связывания иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело, соединенное с пептидом EBV и/или FLU, с внеклеточным доменом (extracellular domain - ECD) CDCP1.
Биохимическое связывание иммуноконъюгатов из примеров 3А и 3Б с human CDCP1-ECD человека исследуют методом поверхностного плазмонного резонанса, используя прибор BIACORE Т100 (фирма GE Healthcare).
Около 2000 резонансных единиц (resonance unit - RU) системы захвата (10 мкг/мл goat anti-human IgG Fc Fragment specific; фирма Jackson Immuno Research) соединены с чипом CM4 (фирма GE Healthcare, BR-1005-34) при рН 5,0 с использованием амина фирмы GE Healthcare. Подвижным буфером для иммобилизации является буфер HBS-N, рН 7,4 (10 мМ HEPES, 150 мМ NaCl, рН 7,4, фирма GE Healthcare, BR-1006-70). Для последующего кинетического анализа и буфера для разведения используют буфер HBS-P рН 7,4 (10 мМ HEPES, 150 мМ NaCl, 0,05% поверхностно-активное вещество Р20, рН 7,4, фирма GE Healthcare, номер в каталоге BR-1006-71).
Проточную кювету устанавливают на 25°C - образец устанавливают на 12°C - и дважды заполняют подвижным буфером. Иммуноконъюгаты, а также для сравнения исходное анти-CDCP1 моноклональное антитело (RO5464169-000-0004), захватывают впрыскиванием 1 мкг/мл раствора в течение 60 сек при скорости тока 10 мкл/мин.
Ассоциацию измеряют путем инъекции CDCP1-ECD человека в различных концентрациях в растворе в течение 180 сек при скорости потока 30 мкл/мин, начиная с концентрации 1350 нМ с последующим разбавлением 1:1,5 и далее в разведении 1:3. Фазу диссоциации подвергают мониторингу до 300 сек и запускают путем переключения с раствора образца на подвижный буфер. Поверхность регенерируют промывкой в виде двух последовательных инъекций раствора глицина с рН 1,7 в течение 60 сек при скорости потока 10 мкл/мин. Разницу показателей индекса преломления корректируют путем вычитания ответа, полученного с поверхности от goat anti human IgG Fc. Инъекции без действующего начала также вычитают (= двойной контроль). Для расчета KD и других кинетических параметров применяют модель Лэнгмюра 1:1.
Результаты представлены в табл. 1.
Таблица 1. Связывание иммуноконъюгатов с CDCP1 по оценке Biacore®

Результаты исследования с применением Biacore, представленные в табл. 1, показывают, что все иммуноконъюгаты связываются с CDCP1-ECD сопоставимо с исходным анти-CDCP1 контрольным антителом.
Пример 3Е. Изучение интернализации иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело, соединенное с пептидом EBV и/или FLU, в CDCP1-экспрессирующих опухолевых клетках человека (MDA-MB 231).
Для оценки способности к интернализации полученных иммуноконъюгатов по сравнению с исходным анти-CDCP1 mAb осуществляют исследование на основе FACS с CDCP1-экспрессирующими клетками опухоли человека линии MDA-MB 231.
Вкратце, клетки MDA-MB 231 отсоединяют обработкой аккутазой, отделяют от отсоединяющей среды путем центрифугирования и суспендируют в среде для культуры клеток MDA-MB 231 (RPMI/2 мМ глутамин/10% ФСТ) в концентрации 3×106 клеток/мл. Аликвоты по 50 мкл клеток инкубируют с иммуноконъюгатами или исходными антителами (5 мкг/мл в среде для культуры клеток MDA-MB 231) в течение 30 мин при 4°C. После двухкратного промывания холодной средой для культуры клеток MDA-MB 231 (RPMI/2 мМ глутамина/10% ФСТ) клетки инкубируют в 100 мкл среды при 4°C или 37°C в течение 30, 60, 120, 240 мин и в течение ночи [23 ч].
По истечении указанных периодов времени клетки промывают, центрифугируют и окрашивают меченым Alexa488 антителом против IgG Н+L человека (фирма Invitrogen, номер в каталоге А11013; 10 мкг/мл в буфере BD FACS) в течение 30 мин при 4°C. После двукратного промывания и центрифугирования клетки выдерживают в 100 мкл буфера BD Cell-Fix, и сигналы окрашенных MFI клеток анализируют проточным цитометром BD Biosciences FACSCanto.
Интернализацию не выявляют при инкубировании при 4°C. Результаты исследования интернализации при 37°C показаны в табл. 2.
Таблица 2. Интернализация иммуноконъюгатов, включающих моноклональное анти-CDCP1 антитело, соединенное с EBV и/или FLU пептидом в CDCP1-экспрессирующих опухолевых клетках человека (MDA-MB 231) при 37°C.

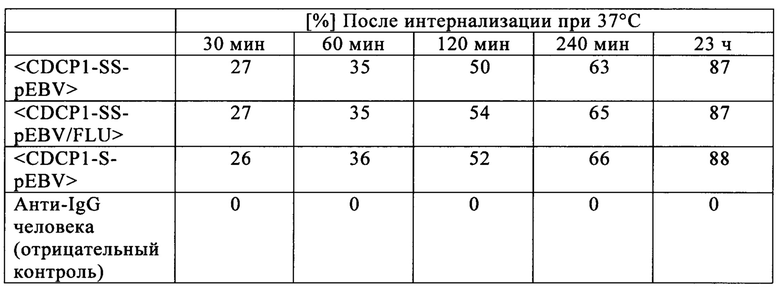
Результаты исследования интернализации на основе FACS показывают, что все исследованные иммуноконъюгаты, интернализованные в CDCP1-экспрессирующих MDA-MB 231 опухолевых клетках, сопоставимы с исходным анти-CDCP1 контрольным антителом (RO5464169-000-0004).
Пример 4. Конъюгация моноклонального анти-CD19 антитела, по меньшей мере, с одним вызывающим ответ Т-клеток пептидом, который способен к презентации через МНС класс I.
Пример 4А. Получение иммуноконъюгатов, включающих моноклональное анти-CD19 антитело и пептид EBV и/или FLU, в которых пептиды соединены с антителом через расщепляемую связь S-S.
Моноклональное антитело, специфически связывающееся с CD19 (в домашнем препарате, очищенном от супернатанта гибридомы), соединяют с одним из пептидов, используемых в примере 3А.
Для получения вариантов иммуноконъюгатов по настоящему изобретению, в которых иммуноконъюгат включает дисульфидную связь для высвобождения пептида при интернализации в клетках-мишенях, пептиды конъюгированы с антителом через дисульфидную связь согласно описанию в примере 3А.
Получаемые по настоящему изобретению иммуноконъюгаты обозначают следующим образом:
- <CD19-SS-pEBV> иммуноконъюгат, включающий анти-CD19 MAb, соединенное с пептидом EBV 426-434 дисульфидной связью
- <CD19-SS-pFLU> иммуноконъюгат, включающий анти-CD19 MAb, соединенное с пептидом FLU 44-52 дисульфидной связью
- <CD19-SS-pEBV/FLU> иммуноконъюгат, включающий анти-CD19 MAb, соединенное с пептидом EBV 426-434 и пептидом FLU 44-52 дисульфидной связью.
Пример 4Б. Исследование связывания клеток иммуноконъюгатами, включающими моноклональное анти-CD19 антитело, связанное с пептидом EBV и/или FLU с CD19-экспрессирующими клетками RL неходжскинской лимфомы.
Чтобы оценить связывание иммуноконъюгатов с их соответствующими антигенами, связывание иммуноконъюгатов из примера 4А с CD19-экспрессирующими клетками RL оценивают в анализе связывания на основе FACS.
Вкратце, клетки RL культивируют in vitro в среде RPMI/2 мМ глютамин/10% ФСТ (низкое содержание IgG). Аликвоты по 50 мкл суспензии клеток RL (4×106 клеток/мл) инкубируют с иммуноконъюгатами (2 мкг/мл в буфере BD FACS) в течение 30 мин при 4°C. После промывки буфером BD FACS клетки окрашивают меченым Alexa488 anti-mouse IgA Н+L (фирма Invitrogen 65Е1-1, 10 мкг/мл в буфере BD FACS) в течение 30 мин при 4°C. После промывки и центрифугирования сигналы MFI окрашенных клеток анализируют в проточном цитометре BD Biosciences FACSCanto. Результаты представлены на фиг. 4.
Результаты исследований связывания клеток на основе FACS, представленные на фиг. 4, показывают, что все иммуноконъюгаты связываются с CD19-экспрессирующими клетками RL сопоставимым образом.
Пример 4В. Исследование интернализации иммуноконъюгатов, включающих моноклональное анти-CD19 антитело, соединенное с пептидом EBV и/или FLU, в CD19-экспрессирующих клетках RL неходжскинской лимфомы (клетках RL) и в клетках лимфомы Беркитта человека (клетках Ramos).
Для оценки способности к интернализации получаемых иммуноконъюгатов в сравнении с исходным анти-CD19 mAb выполняют анализ интернализации на основе FACS с CD19-экспрессирующими линиями клеток RL и Ramos.
Вкратце, клетки RL и Ramos культивируют in vitro в среде RPMI/2 мМ глутамин/10% ФСТ (низкое содержание IgG).
Аликвоты по 50 мкл клеток RL и Ramos (4×106 клеток/мл) инкубируют с иммуноконъюгатами или параллельно с анти-CD19 mAb (5 мкг/мл в среде для культивирования клеток RL) в течение 30 мин при 4°C. После двух промываний холодной средой для клеток RL клетки инкубируют в 100 мкл среды при 4°C или 37°C в течение 30, 60, 120, 240 и 360 мин и в течение ночи [23 ч].
Через указанные временные интервалы клетки промывают, центрифугируют и окрашивают Alexa488-меченым anti-human IgG H+L (фирма JacksonImmuno 715-116-150 Lot 90812; 2,5 мкг/мл в буфере BD FACS) в течение 30 мин при 4°C. После двух промывок и центрифугирования клетки выдерживают в 100 мкл буфера BD Cell-Fix, после чего сигналы окрашенных MFI клеток анализируют с помощью проточного цитометра BD Biosciences FACSCanto.
Интернализацию не обнаруживают при инкубировании при 4°C. Результаты изучения интернализации при инкубировании при 37°C представлены в табл. 3.
Таблица 3. Интернализация иммуноконъюгатов, включающих моноклональное анти-CD19 антитело, соединенное с пептидом EBV и/или FLU в CD19-экспрессирующих опухолевых клетках человека (RL) при 37°C
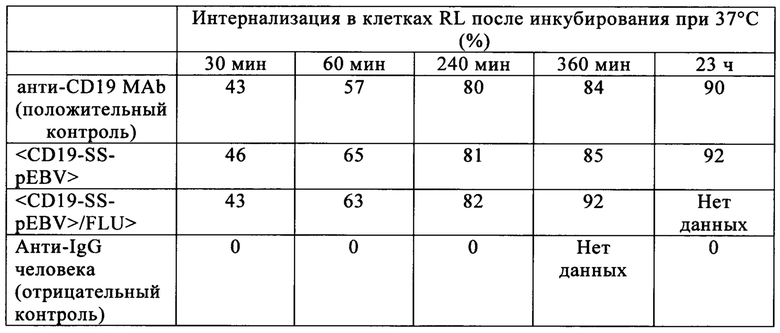
Результаты исследования интернализации на основе метода FACS показывают, что интернализация тестируемых иммуноконъюгатов в CD19-экспрессирующих клетках RL сопоставима с исходным анти-CD19-контрольным антителом.
Пример 5. Активирование CD8 Т-клеток после обработки опухолевых клеток иммуноконъюгатами, включающими моноклональное анти-CDCP1 антитело и пептиды EBV, и иммуноконъюгатами, включающими моноклональное анти-CD19 антитело и пептиды EBV.
Пример 5А. Получение специфичных по пептиду EBV Т-клеток из периферической крови здоровых доноров.
Частоту встречаемости специфичных по пептиду EBV CD8 Т-клеток в свежевыделенных МКПК здоровых доноров или в культурах Т-клеток исследуют методом FACS при окрашивании пентамером.
Вкратце, аликвоты с 4-5×105 Т-клетками культуры клеток или свежевыделенных МКПК от здоровых доноров, или свежевыделенных МКПК от HLA-А2-совместимых здоровых доноров промывают буфером BD FACS и инкубируют со 100 мкл буфера BD FACS, включающего 5 мкл human TruStain FcX (фирма BioLegend, номер в каталоге 422302) в течение 15 мин при комнатной температуре. После этого 90 мкл буфера BD FACS, включающего 10 мкл биотина, конъюгированного с EBV-Pentamer (фирма ProImmune, номер в каталоге F042-84A-E), добавляют и инкубируют в течение 1 ч при 4°C.
После промывания буфером BD FACS клетки окрашивают в 100 мкл буфера BD FACS с FITC-меченым анти-CD8a mAb (клон LT8, фирма ProImmune), а также конъюгатом стрептавидин-АРС при 4°C в течение 20 мин. После трех промываний буфером BD FACS и центрифугирования клетки ресуспендируют в 200 мкл буфера BD FACS, и сигналы MFI окрашенных клеток исследуют с помощью проточного цитометра BD Biosciences FACSCanto II. Клетки от HLA-А1 доноров применяют для оценки неспецифического связывания тетрамеров.
Специфичные по EBV-пептиду Т-клетки получают по протоколу, описанному в примере 1 для пептида, производного от CMV, отличающегося тем, что в данном эксперименте пептид EBV с последовательностью SEQ ID NO: 2 применяют для стимуляции.
Пример 5Б. Оценка активации специфичных в отношении пептида EBV Т-клеток после обработки опухолевых клеток НСТ-116 иммуноконъюгатами, включающими моноклональное анти-CDCP1 антитело и пептиды EBV, и иммуноконъюгатами, включающими моноклональное анти-CDCP1 антитело и пептиды EBV, методом IFNγ-ELISPOT.
Активацию специфичных в отношении пептида EBV Т-клеток оценивают методом IFNγ-ELISPOT, используя опухолевые клетки НСТ-116, обработанные иммуноконъюгатами (IC) из примеров 3А, 3Б (IC, включающими анти-CDCP1 и EBV пептиды) и 4А (IC, включающими анти-CD19 и EBV пептиды) в присутствии CD8 Т-клеток, полученных в примере 5А. Для сравнительного анализа эксперименты одновременно выполняют со свободным пептидом (pEBV, положительный контроль) и с контрольным иммуноконъюгатом, образованным анти-Dig антителом, соединенным с пептидом EBV согласно описанию в примере 3А (обозначение <DIG-SS-pEBV>, отрицательный контроль).
Метод IFNγ-ELISPOT осуществляют по общему протоколу, описанному в примере 1Б.
Результаты представлены на фиг. 5А.
Результаты IFNγ-ELISPOT показывают, что из исследованных иммуноконъюгатов только те, которые включают моноклональное анти-CDCP1 антитело и пептиды EBV, соединенные расщепляемой связью (<CDCP1-SS-EBV>), существенно активируют CD8 Т-клетки при интернализации в опухолевых клетках, причем иммуноконъюгаты, включающие моноклональное анти-CDCP1 антитело и пептиды EBV, соединенные через нерасщепляемую связь (<CDCP1-S-EBV>), не могут активировать специфичные в отношении CD8 Т-клетки. Иммуноконъюгаты, включающие антитела, которые не связываются с клетками-мишенями (<DIG-SS-EBV> и <CD19-SS-EBV>), не активируют Т-клетки. Кроме того, иммуноконъюгаты по настоящему изобретению способны активировать CD8 Т-клетки в малых количествах, даже менее 1 нМ/л.
Пример 5В. Оценка активации специфичных в отношении пептида EBV Т-клеток после обработки клеток RL и Ramos иммуноконъюгатами, включающими моноклональное анти-CD19 антитело и пептиды EBV, методом IFNγ-ELISPOT.
Для того чтобы продемонстрировать, что уничтожение опухолевых клеток ограничено клетками-мишенями, экспрессирующими HLA-подтип, оценивают способность презентировать соответствующий вызывающий ответ Т-клеток пептид, активацию EBV-специфичных Т-клеток с помощью IFNγ-ELISPOT с использованием клеток RL, которые экспрессируют HLA-A2, и клеток Ramos, которые не экспрессируют HLA-A2, обработанные иммуноконъюгатами (IC) из примера 4А (IC, содержащий анти-CD19 и НЕА-А2-ограниченный пептид EBV) в присутствии CD8 Т-клеток, полученных в примере 5А. Для сравнительного анализа экспериментов проводят одновременно проводят исследование со свободным пептидом (pEBV, положительный контроль).
Метод IFNγ-ELISPOT осуществляют по общему протоколу, описанному в примере 1Б.
Представленные на фиг. 5А результаты показывают, что уничтожение опухолевых клеток наблюдают только в клетках RL, но не в клетках Ramos.
Пример 6. Получение иммуноконъюгата, включающего моноклональное анти-CDCP1-антитело, связанное с EBV-пептидом через расщепляемую дисульфидную связь, где пептид EBV естественным образом содержит неконцевой остаток цистеина, и оценка активации Т-клеток CD8 с помощью IFNγ-ELISPOT.
Хотя в примерах 3 и 4 представлены иммуноконъюгаты, в которых вызывающие ответ Т-клеток пептиды по концам связаны с соответствующими антителами с образованием иммуноконъюгата, в настоящем примере расщепляемая дисульфидная связь образована между остатком неконцевого цистеина в пептиде и антителом. Для этого предусмотрен пептид EBV аминокислотной последовательности GLCTLVAML (SEQ ID NO: 4), соединенный с анти-CDCP1 антителом согласно описанному в примере 3А.
Активацию специфичных по пептидам Т-клеток оценивают с помощью IFNγ-ELISPOT на разных линиях опухолевых клеток, экспрессирующих различные уровни МНС I:
- MDA-MB 231, высокий уровень HLA-A2, и
- A375, низкий уровень HLA-A2.
Вкратце, 10000 опухолевых клеток соответственно обрабатывают разными концентрациями иммуноконъюгата в присутствии 500 пептид-специфичных CD8 Т-клеток, получаемых в соответствии с описанием в примере 5Б, но с использованием пептида EBV GLCTLVAML. В качестве контролей опухолевые клетки и Т-клетки инкубируют в отсутствии иммуноконъюгата, и, в качестве дополнительного контроля, Т-клетки инкубируют отдельно в таких же условиях.
Полученные иммуноконъюгаты по настоящему изобретению в настоящем изобретении обозначают следующим образом:
- <CDCP1-SS-pEBV(GLC)> иммуноконъюгат, включающий анти-CDCP1 Mab, соединенное с пептидом EBV GLCTLVAML дисульфидной связью.
Результаты IFNγ-ELISPOT показаны на фиг. 5В. Пептид-специфичную активацию Т-клеток наблюдают для обеих исследованных линий опухолевых клеток для иммуноконъюгата по настоящему изобретению доза-зависимым образом.
Пример 7. Опосредованная CD8 Т-клетками индуцированная гибель опухолевых клеток MDA-MB231, обработанных иммуноконъюгатами по настоящему изобретению, включающими моноклональное анти-CDCP1 антитело и пептиды EBV, по оценке высвобождения LDH и методом xCELLigence.
Активацию специфичными в отношении пептида Т-клеток и гибель опухолевых клеток оценивают по высвобождению LDH и методом xCELLigence, используя опухолевые клетки MDA-MB231, обработанные разными концентрациями иммуноконъюгатов (immunoconjugates - IC) из примеров 3А, 3Б (IC, включающий анти-CDCP1 и пептиды EBV) в присутствии CD8 Т-клеток, полученных в примере 5А, в соотношении эффекторных клеток к клеткам-мишеням 3:1. Для сравнительного анализа эксперименты одновременно выполняют со свободным пептидом (pEBV, положительный контроль).
Оценку уничтожения опухолевых клеток, нагруженных вирусным пептидом в результате обработки иммуноконъюгатами, проводят посредством динамического мониторинга пролиферации и жизнеспособности клеток в системе xCELLigence с использованием следующего общего метода: по 50 мкл среды для опухолевых клеток вносят в лунки и проводят начальное фоновое измерение (стадия 1) на приборе RTCA (фирма Roche Applied Sciences). Вещества, суспендированные в 50 мкл среды для опухолевых клеток, добавляют в Е-планшет. Опухолевые клетки собирают с использованием аккутазы и соответствующее число клеток суспендируют в 50 мкл среды для опухолевых клеток и вносят среду в Е-планшет.
Следующие количества клеток применяют для разных линий опухолевых клеток: А-375: 10000 клеток; НСТ-116: 20000 клеток; РС-3: 10000 клеток; MDA-МВ231: 10000 клеток.
Через 10 мин при комнатной температуре планшеты помещают в прибор RTCA и осуществляют стадию 2 (интервал 10 мин, 200 интервалов). Затем планшеты инкубируют в течение примерно 24 ч.
На следующие сутки Т-клетки промывают в среде AIM-V и суспендируют в среде AIM-V. Т-клетки добавляют в планшеты до общего объема 200 мкл. Пластины помещают в прибор RTCA для выполнения стадии 3 (интервал 5 мин, 300 интервалов). Планшеты инкубируют в течение ночи.
Образцы используют для последующего анализа высвобождения LDH.
Для оценки высвобождения LDH клетки лизируют, добавляя 1% Triton X-100. Супернатант переносят в 96-луночный планшет с V-образными лунками и удаляют остатки клеток центрифугированием, после чего супернатант без остатков клеток переносят в плоскодонный 96-луночный планшет. Высвобождение LDH исследуют, применяя метод анализа цитотоксичности LDH (фирма Roche, номер в каталоге 11644793001) по инструкциям производителя. Вкратце, катализатор и раствор красителя перемешивают, по 100 мкл получаемой реакционной смеси вносят в каждую лунку и инкубируют при комнатной температуре в темноте. Измеряют поглощение при 492 нм (контроль: 620 нм), используя ридер Tecan ELISA, в течение t=15-45 мин (обычно 30 мин).
Показанные на фиг. 6А результаты свидетельствуют, что применение иммуноконъюгатов по настоящему изобретению приводит к интенсивному уничтожению опухолевых клеток в пикомолярных концентрациях.
Пример 8. Опосредование, индуцированное CD8 Т-клетками, гибели опухолевых клеток MDA-MB231 и А-375, обработанных иммуноконъюгатами по настоящему изобретению, содержащими моноклональное анти-CDCP1 и пептид EBV, который, естественным образом содержит неконцевой остаток цистеина, по оценке высвобождения LDH и методом xCELLigence.
Активацию EBV-пептид-специфичных Т-клеток и уничтожение опухолевых клеток оценивают путем анализа высвобождающегося LDH и методом xCELLigence, используя опухолевые клетки MDA-MB231 и А-375, обработанные разными концентрациями иммуноконъюгата (immunoconjugate - IC) из примера 6 (IC включает анти-CDCP1 и пептид EBV, который естественным образом включает неконцевой остаток цистеина) в присутствии специфических по пептиду клеток CD8 Т-клетках, полученных в соответствии с примером 5А, но используя для стимуляции пептид EBV GLCTLVAML, при соотношении эффекторных клеток к клеткам-мишеням 3:1. Для сравнительных анализов эксперименты одновременно выполняют со свободным пептидом (pEBV) в двух разных концентрациях пептида.
Анализ xCELLigence и оценку высвобождения LDH осуществляют согласно описанному в примере 7.
Результаты, представленные на фиг. 6Б (для клеток А-375) и 6В (для клеток MDA-MB231) вместе с данными по анализу xCELLigence, измеряют через 13,5 ч.
Результаты показывают, что только иммуноконъюгат по настоящему изобретению способен опосредовать специфическое уничтожение исследуемых опухолевых клеток посредством Т-клеток со специфическим пептидом. Напротив, не наблюдают уничтожения опухолевых клеток при использовании эквимолярной концентрации свободного пептида EBV.
Пример 9. Опосредование, индуцированное CD8 Т-клетками, гибели опухолевых клеток, обработанных иммуноконъюгатами по настоящему изобретению, содержащими моноклональное анти-CDCP1 и пептиды FLU, по оценке высвобождения LDH и методом xCELLigence.
Уничтожение опухолевых клеток иммуноконъюгатами по настоящему изобретению оценивают, используя HLA-A1 ограниченные FLU-пептид-содержащие иммуноконъюгаты (CDCP1-SS-pFLU, согласно описанию в примере 3А) для лечения разных линий опухолевых клеток (А-375, РС-3, НСТ-116) в присутствии FLU-специфичных CD8 Т-клеток. Пептид-специфическую активацию Т-клеток и уничтожение опухолевых клеток оценивают по анализу высвобождения LDH и методом xCELLigence согласно описанному в примере 7.
Исследуемые линии клеток обладают следующими свойствами в отношении HLA-подтипа и экспрессии мишени (CDCP-1):
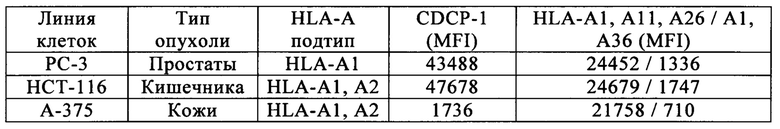
Результаты анализа xCELLigence показаны на фиг. 7А-В. Результаты анализа, основанного на высвобождении LDH, показаны на фиг. 7Г-Е.
Эффективное уничтожение опухолевых клеток при обработке опухолевых клеток иммуноконъюгатом наблюдают во всех тестируемых линиях опухолевых клеток. По сравнению с использованием свободного пептида иммуноконъюгат опосредует активацию Т-клеток более эффективно, чем свободный пептид в более высокой 100-кратной концентрации.
Уничтожение опухолевых клеток, опосредуемое иммуноконъюгатом, можно наблюдать уже через 6 ч после обработки иммуноконъюгатом, что указывает на то, что пептид не требует транспортировки к антиген-процессирующему механизму в цитозоль для презентации через МНС класса I. Кроме того, наблюдают повышенное уничтожение количества опухолевых клеток с течением времени, хотя, наоборот, уничтожение опухолевых клеток, опосредованное свободным пептидом, обычно снижается по мере продления времени инкубирования. Подобные эффекты наблюдают в разных линиях опухолевых клеток, что указывает на то, что эффект не зависит от уровня экспрессии МНС класса I в клетке-мишени. Результаты анализа xCelligence подтверждают результаты, полученные по анализу высвобождения LDH.
Пример 10. Доказательство in vivo концепции I
Противоопухолевая активность иммуноконъюгатов по настоящему изобретению, включающих моноклональное анти-CDCP1 антитело и пептид EBV, в модели подкожного трансплантата MDA-MB231 с внутривенным введением МПКП человека (включая EBV-специфические CD8 Т-клетки).
Мышам NOG трансплантируют опухолевые клетки (5×106 Mio MDA-МВ231) путем подкожной инъекции в 0 сутки. Применяют стимуляцию МКПК человека (~10% CLG-пептид EBV-специфические CD8 Т-клетки) дважды - в 0 сутки и 20 сутки, путем внутривенного введения 6×106 (подробнее см. фиг. 8А). Схема обработки антителами/иммуноконъюгатами следующая:
<CDCP1>-IgG4-SS-CLG пептид (получение согласно примеру 3, с константной цепью IgG4): 5 мг/кг (сутки: 0, 3, 6, 9, 13, 16, 20, 23, 27, 30)
Контрольное антитело: <CDCP1>-IgG4 (константная цепь IgG4): 5 мг/кг (на 0, 3, 6, 9, 13, 16, 20, 23, 27 и 30 сутки).
Схема тестирования и результаты показаны на фиг. 8А и Б. Результаты показывают in vivo эффективность иммуноконъюгатов по настоящему изобретению, включающих моноклональное анти-CDCP1 антитело, в модели подкожного трансплантата MDA-MB231 с адаптивным переносом CLG-специфических МКПК человека (huPBMC).
Пример 11. Доказательство in vivo концепции II.
Противоопухолевая активность иммуноконъюгатов по настоящему изобретению, включающих моноклональное анти-CDCP1 антитело и пептид EBV, в комбинации с обработкой анти-PD1 в разработанной модели подкожного трансплантата MDA-MB231 с внутривенным введением МПКП человека (включающих EBV-специфические CD8 Т-клетки).
Мышам NOG трансплантируют опухолевые клетки человека (5×106 Mio MDA-MB231) путем подкожной инъекции в 0 сутки. Применяют стимуляцию МКПК человека (~10% CLG-пептид EBV-специфические CD8 Т-клетки) дважды - в 0 сутки и 20 сутки, путем внутривенного введения 10×106 клеток (подробнее см. фиг. 8А). Схема обработки исследуемой группы исследуемым конъюгатом <CDCP1>-IgG1-PGLala-SS-CLG пептид (получение согласно описанному в примере 3, с константной цепью IgG1 с мутациями L234A, L235A и P329G (по индексу Kabat EU) в части Fc) и контрольной группы с контрольным антителом <CDCP1>-IgG1 PGLALA, плюс добавление анти-PD1-антитела для обеих групп:

Схема тестирования и результаты показывают на фиг. 9А и Б. Результаты показывают комбинированный эффект иммуноконъюгатов по настоящему изобретению, включающих моноклональное анти-CDCP1 антитело, плюс анти-PD-1 терапии в модели ксенотрансплантата MDA-MB231 с адаптивным переносом EBV CLG-специфических МКПК человека. Показано сильное увеличение CLG-специфических Т-клеток в опухолях после лечения АТРР в комбинации с анти-PD-1 антителом.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> F. Hoffmann-La Roche AG
<120> IMMUNOCONJUGATES FOR SPECIFIC INDUCTION OF T CELL CYTOTOXICITY
AGAINST A TARGET CELL
<130> P32622-WO
<150> EP15155598
<151> 2015-02-18
<150> EP15199306
<151> 2015-12-10
<160> 10
<170> PatentIn version 3.5
<210> 1
<211> 9
<212> PRT
<213> Human herpesvirus 5
<220>
<221> misc_feature
<223> Human herpesvirus 5 (CMV) peptide pp65 495-503
<400> 1
Asn Leu Val Pro Met Val Ala Thr Val
1 5
<210> 2
<211> 9
<212> PRT
<213> Epstein-Barr virus
<220>
<221> misc_feature
<223> Epstein-Barr virus (EBV) peptide LMP-2 426-434
<400> 2
Cys Leu Gly Gly Leu Leu Thr Met Val
1 5
<210> 3
<211> 9
<212> PRT
<213> Influenza A virus
<220>
<221> misc_feature
<223> Influenza A (FLU) peptide NP 44-52
<400> 3
Cys Thr Glu Leu Lys Leu Ser Asp Tyr
1 5
<210> 4
<211> 9
<212> PRT
<213> Epstein-Barr virus
<220>
<221> misc_feature
<223> Epstein-Barr virus (EBV) peptide BLMF-1 280-288
<400> 4
Gly Leu Cys Thr Leu Val Ala Met Leu
1 5
<210> 5
<211> 9
<212> PRT
<213> Human herpesvirus 5
<220>
<221> misc_feature
<223> Human herpesvirus 5 (CMV) peptide 309-317
<400> 5
Cys Arg Val Leu Cys Cys Tyr Val Leu
1 5
<210> 6
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> modified Human herpesvirus 5 (CMV) peptide pp65 495-503
(cCMV peptide)
<400> 6
Cys Asn Leu Val Pro Met Val Ala Thr Val
1 5 10
<210> 7
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> modified Human herpesvirus 5 (CMV) peptide pp65 495-503 (CMVc
peptide)
<400> 7
Asn Leu Val Pro Met Val Ala Thr Val Cys
1 5 10
<210> 8
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> modified Human herpesvirus 5 (CMV) peptide pp65 495-503 (rcCMV
peptide)
<400> 8
Cys Leu Val Pro Met Val Ala Thr Val
1 5
<210> 9
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> modified Human herpesvirus 5 (CMV) peptide pp65 495-503 (CMVrc
peptide)
<400> 9
Asn Leu Val Pro Met Val Ala Thr Cys
1 5
<210> 10
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> modified Human herpesvirus 5 (CMV) peptide pp65 495-503 (CMVpen
peptide)
<220>
<221> misc_feature
<223> Xaa is penicillamine
<220>
<221> misc_feature
<222> (9)..(9)
<223> Xaa can be any naturally occurring amino acid
<400> 10
Asn Leu Val Pro Met Val Ala Thr Xaa
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИГЕН-СВЯЗЫВАЮЩИЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОДУКТА ДЛЯ АДРЕСНОЙ ДОСТАВКИ ПРИ ЛЕЧЕНИИ РАКА | 2012 |
|
RU2650771C1 |
| НОВЫЕ ПРОНИКАЮЩИЕ В КЛЕТКУ ПЕПТИДЫ | 2013 |
|
RU2670488C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К CDCP1 | 2010 |
|
RU2571207C2 |
| СПОСОБЫ ЭКСПАНДИРОВАНИЯ АНТИГЕНСПЕЦИФИЧЕСКИХ CAR-T-КЛЕТОК, КОМПОЗИЦИИ И ПРИМЕНЕНИЯ, СВЯЗАННЫЕ С НИМИ | 2019 |
|
RU2800920C2 |
| ПРЕДСКАЗАНИЕ ИММУНОГЕННОСТИ Т-КЛЕТОЧНЫХ ЭПИТОПОВ | 2014 |
|
RU2724370C2 |
| КОМПОЗИЦИИ И СПОСОБЫ WT1-СПЕЦИФИЧНОЙ ИММУНОТЕРАПИИ | 1999 |
|
RU2237674C2 |
| АНТИ-TIM3 АНТИТЕЛА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2723708C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ДВА АНТИТЕЛА, СКОНСТРУИРОВАННЫХ ТАК, ЧТОБЫ ОНИ ОБЛАДАЛИ ПОНИЖЕННОЙ И ПОВЫШЕННОЙ ЭФФЕКТОРНОЙ ФУНКЦИЕЙ | 2013 |
|
RU2650788C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОДУКТА ДЛЯ АДРЕСНОЙ ДОСТАВКИ ПРИ ЛЕЧЕНИИ РАКА | 2012 |
|
RU2659094C2 |
| АНТИТЕЛА К HER3 И ИХ ПРИМЕНЕНИЯ | 2010 |
|
RU2560583C2 |
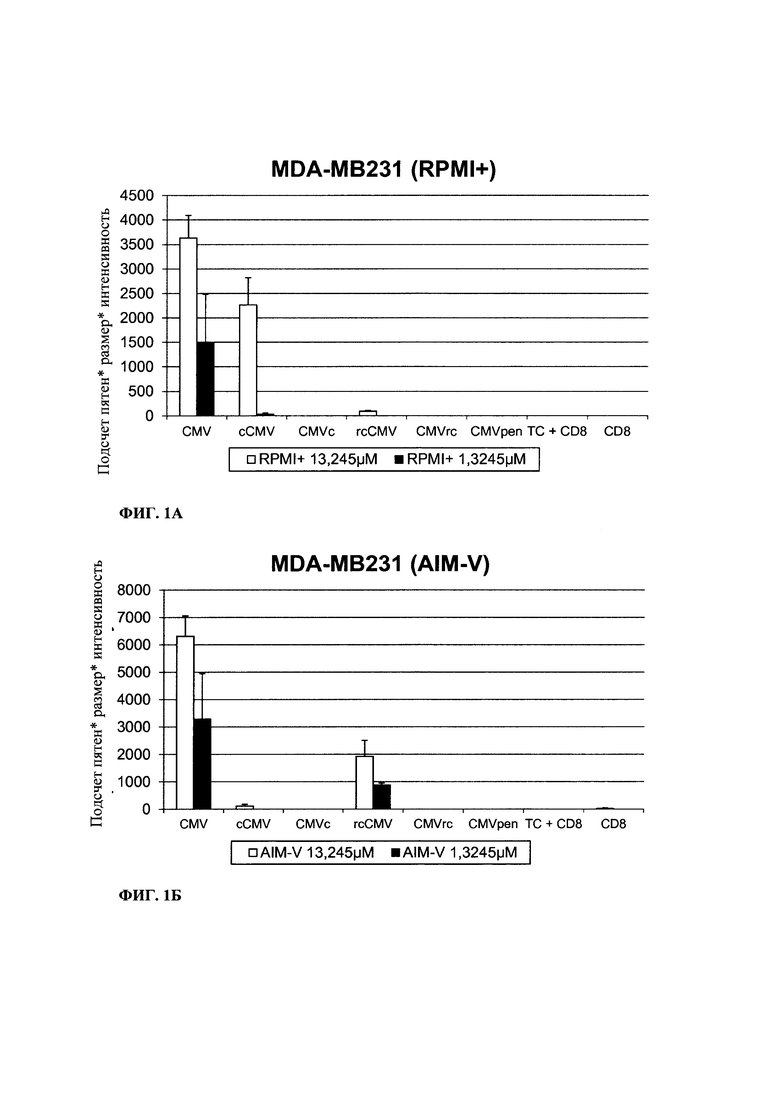
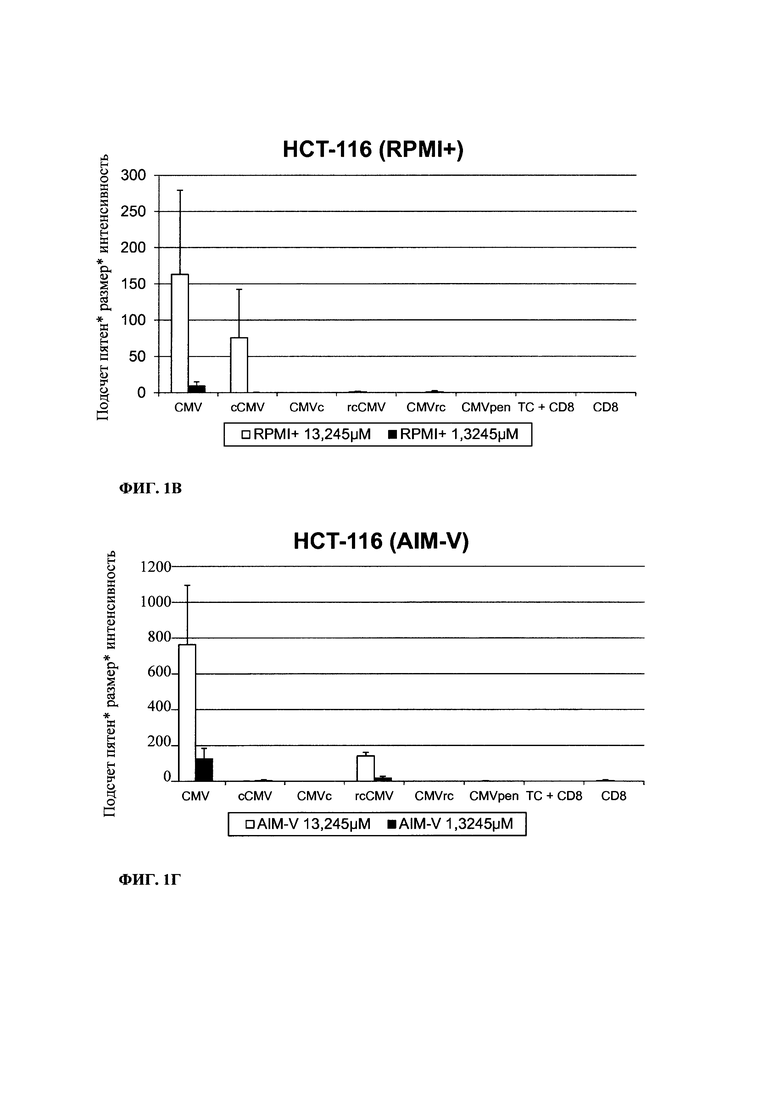
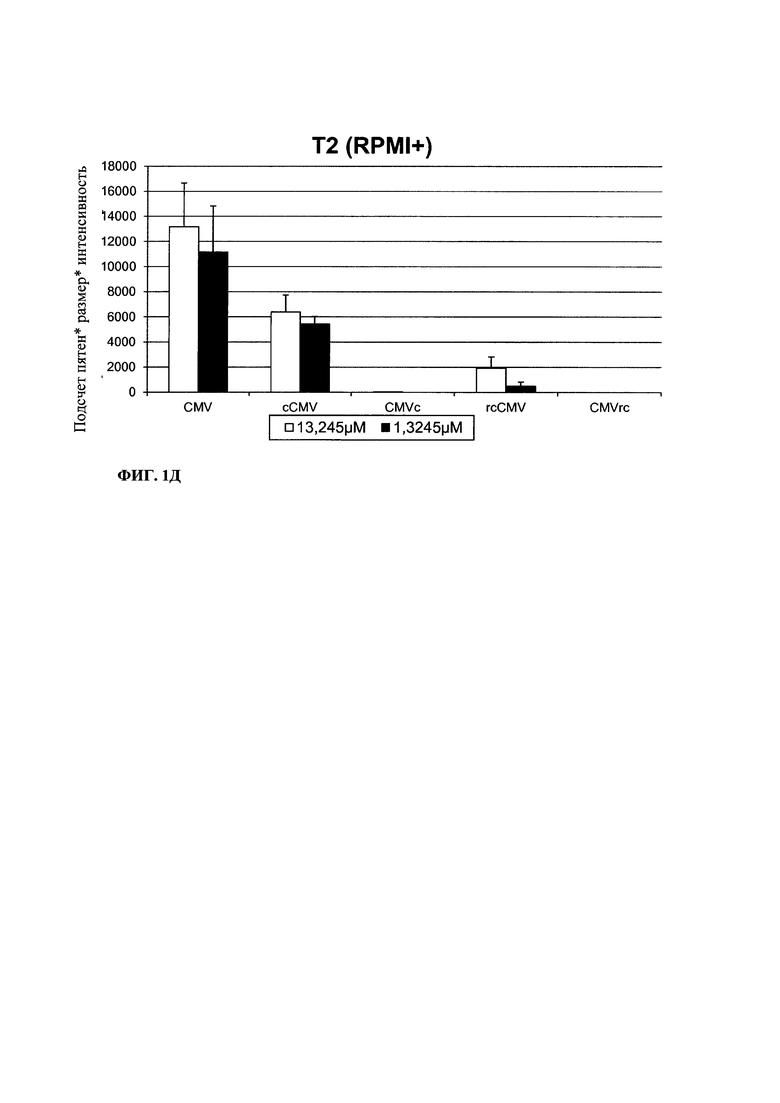
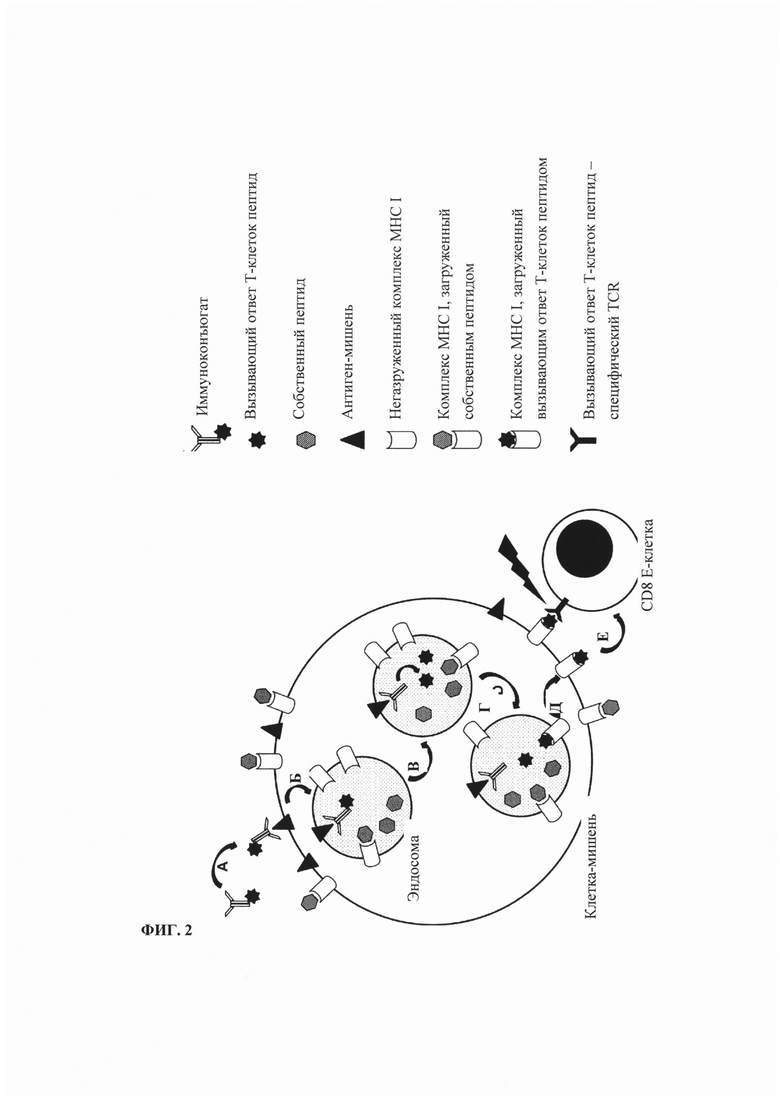
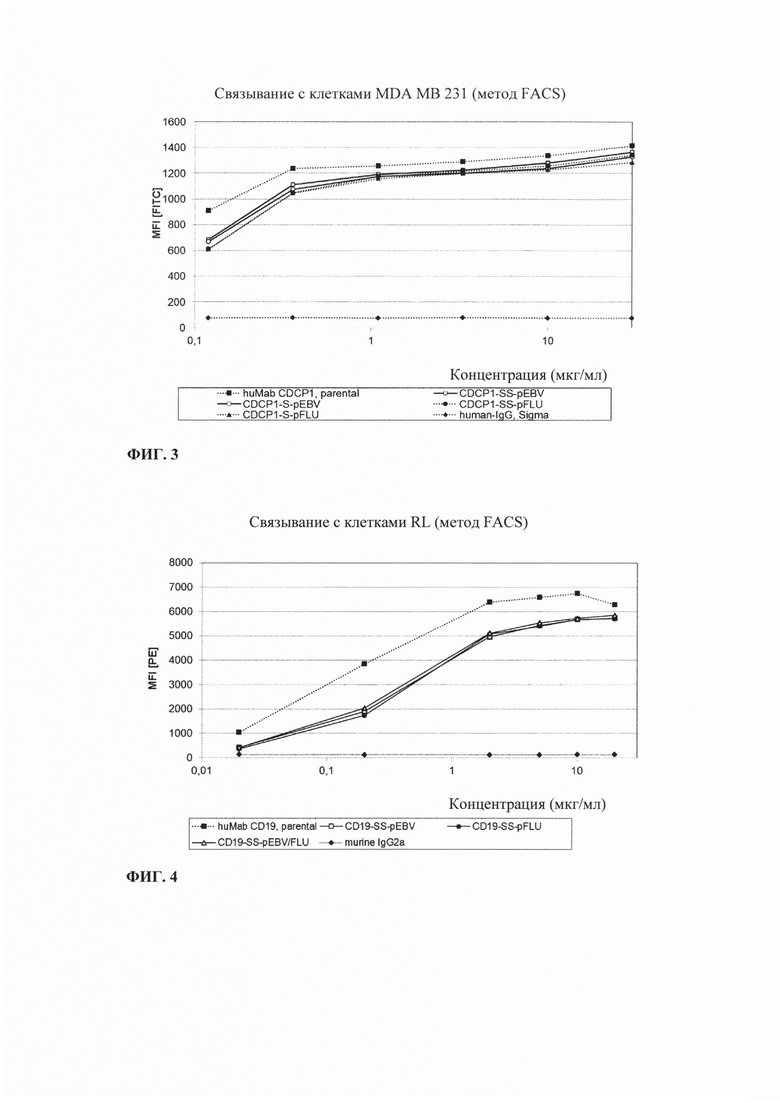
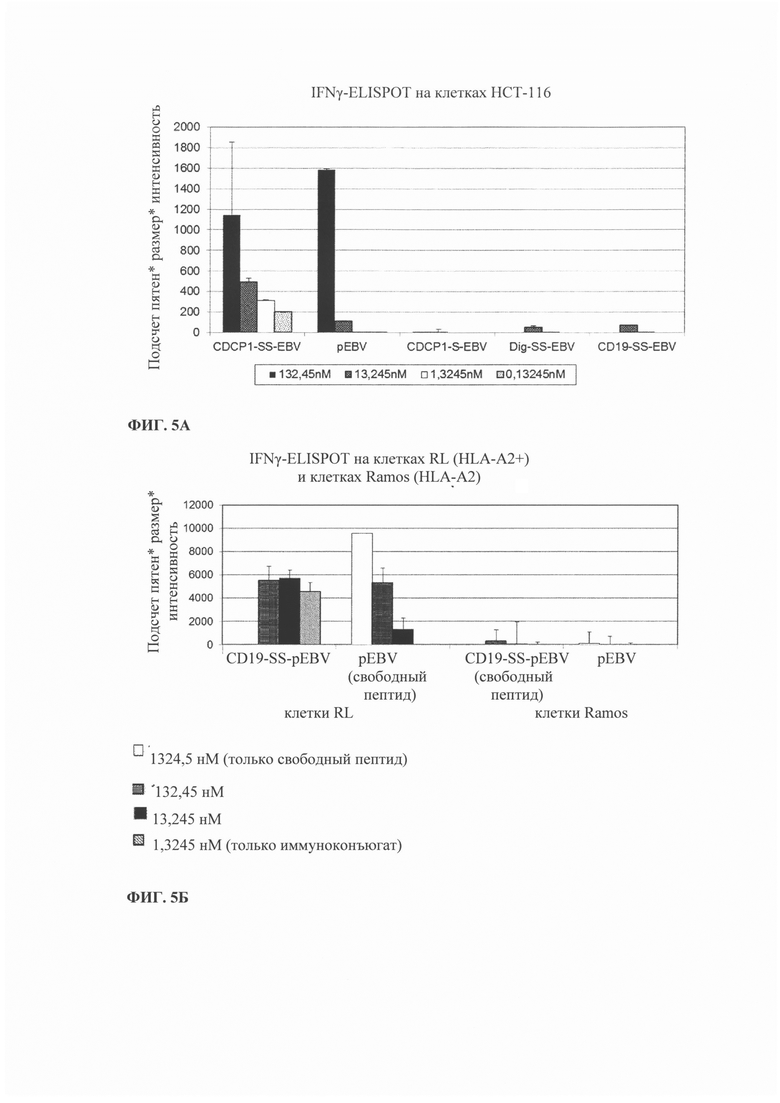
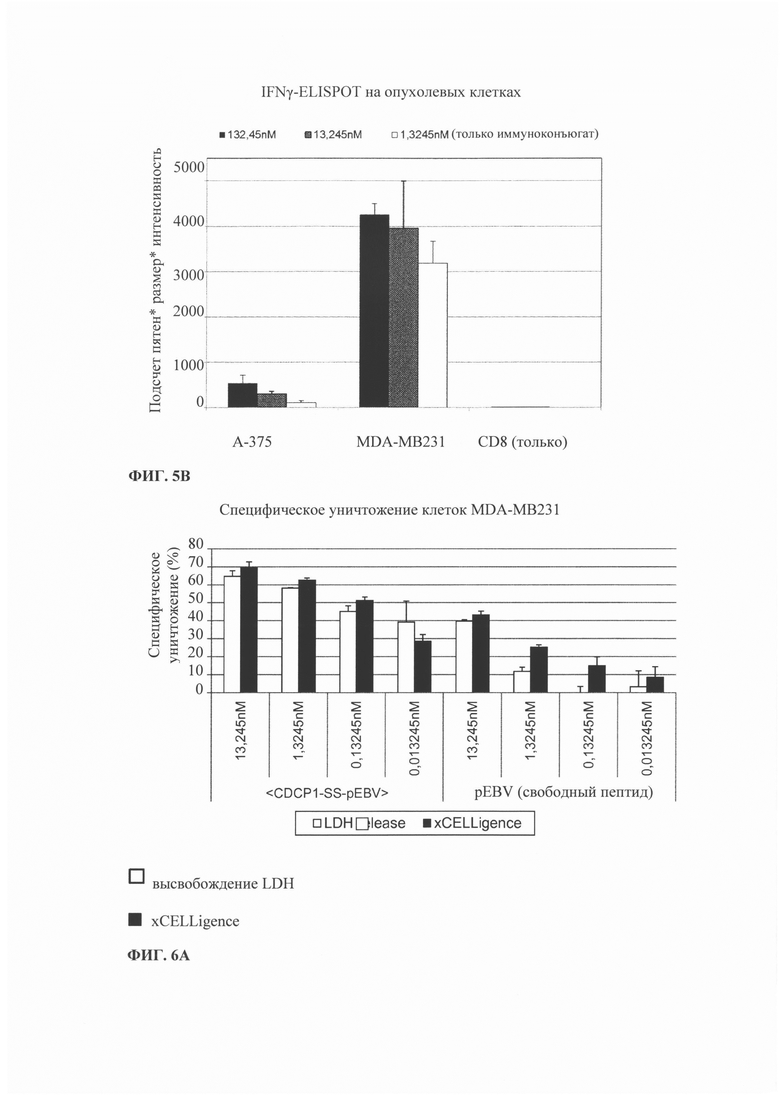
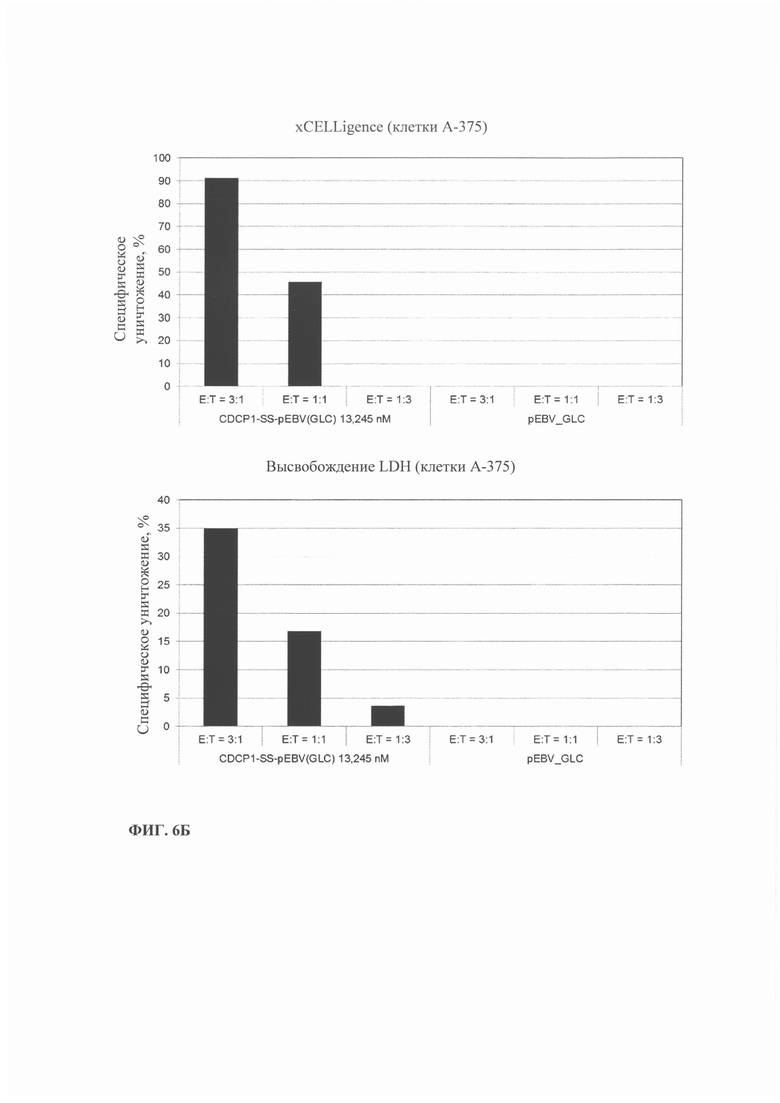

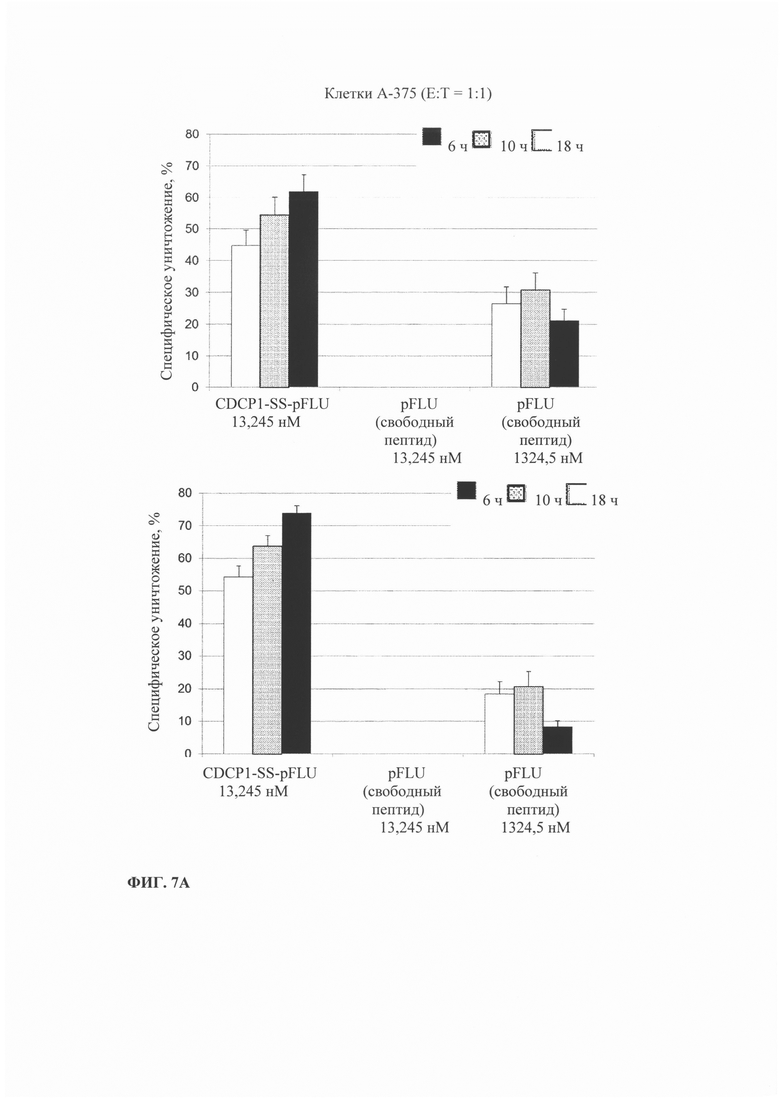
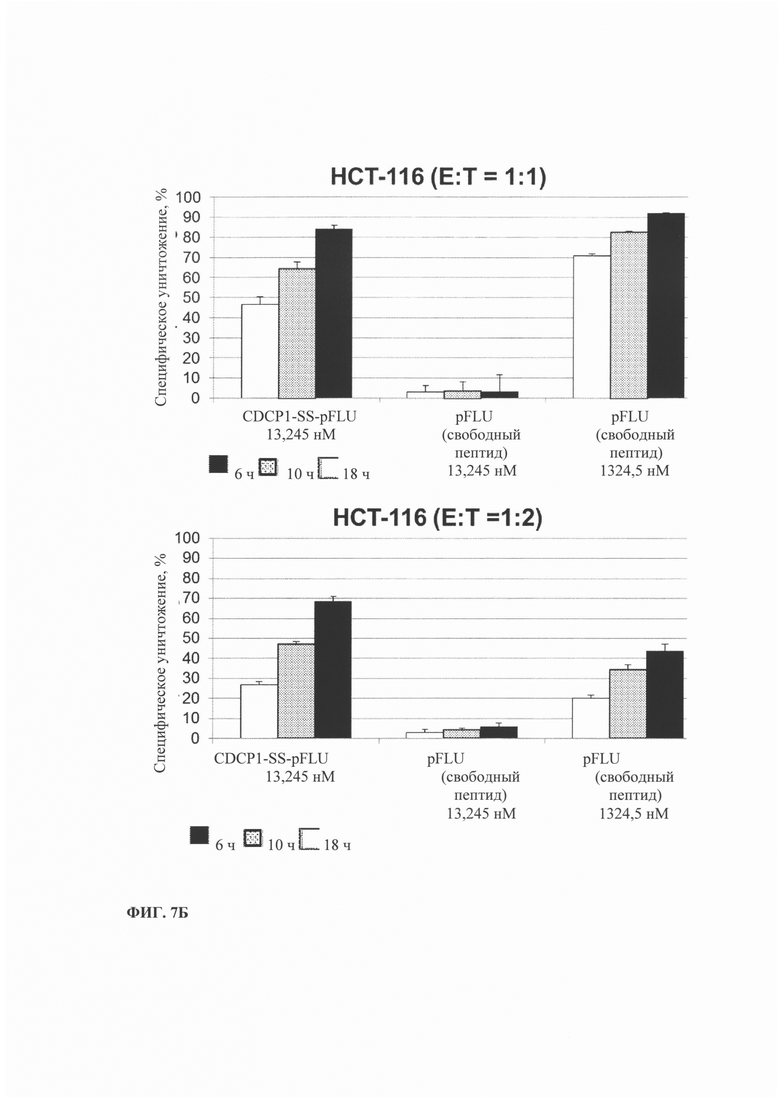
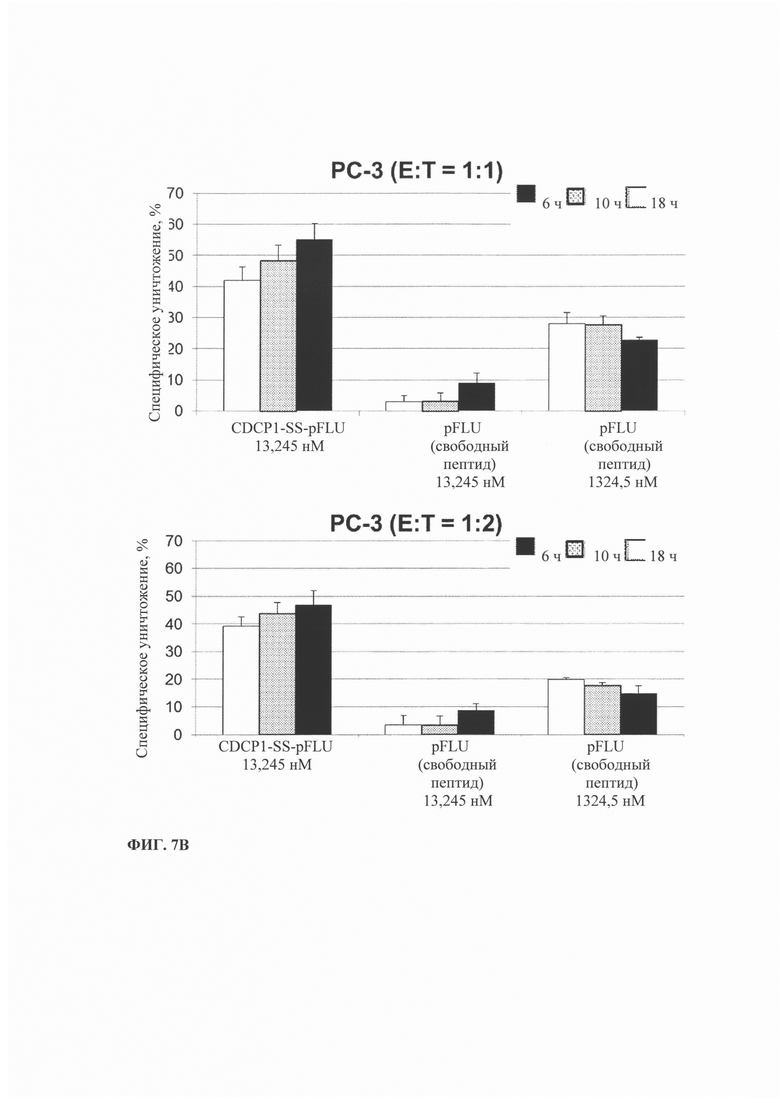
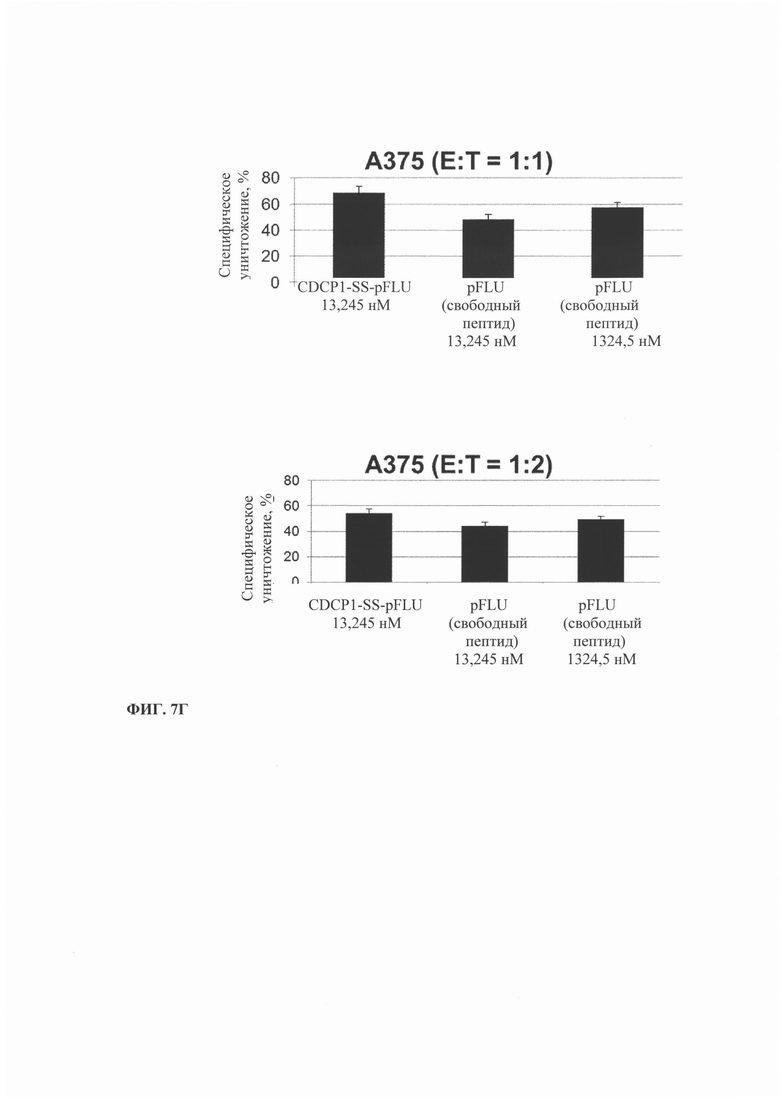
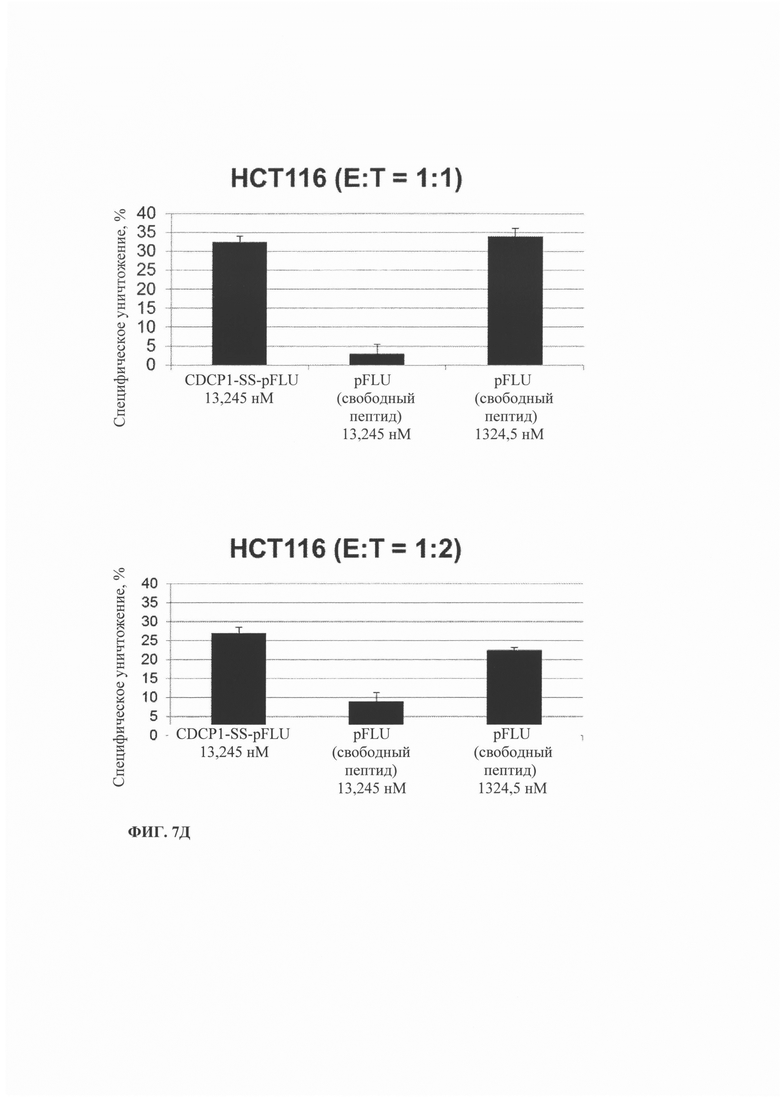
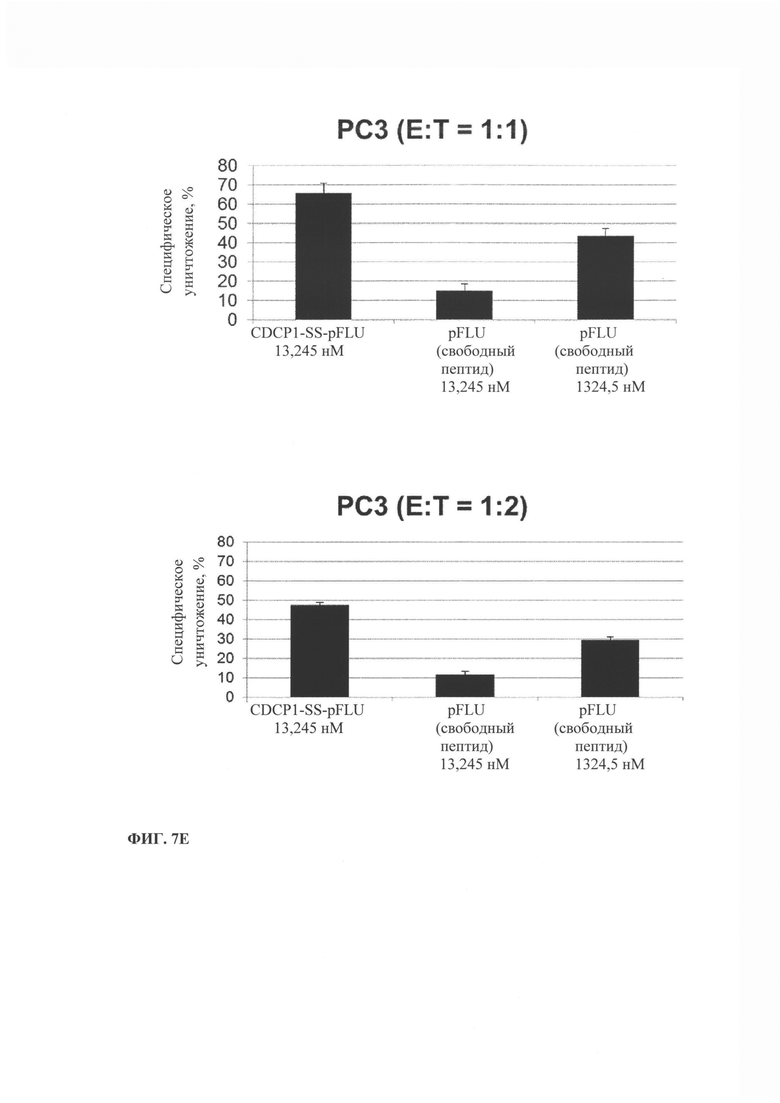

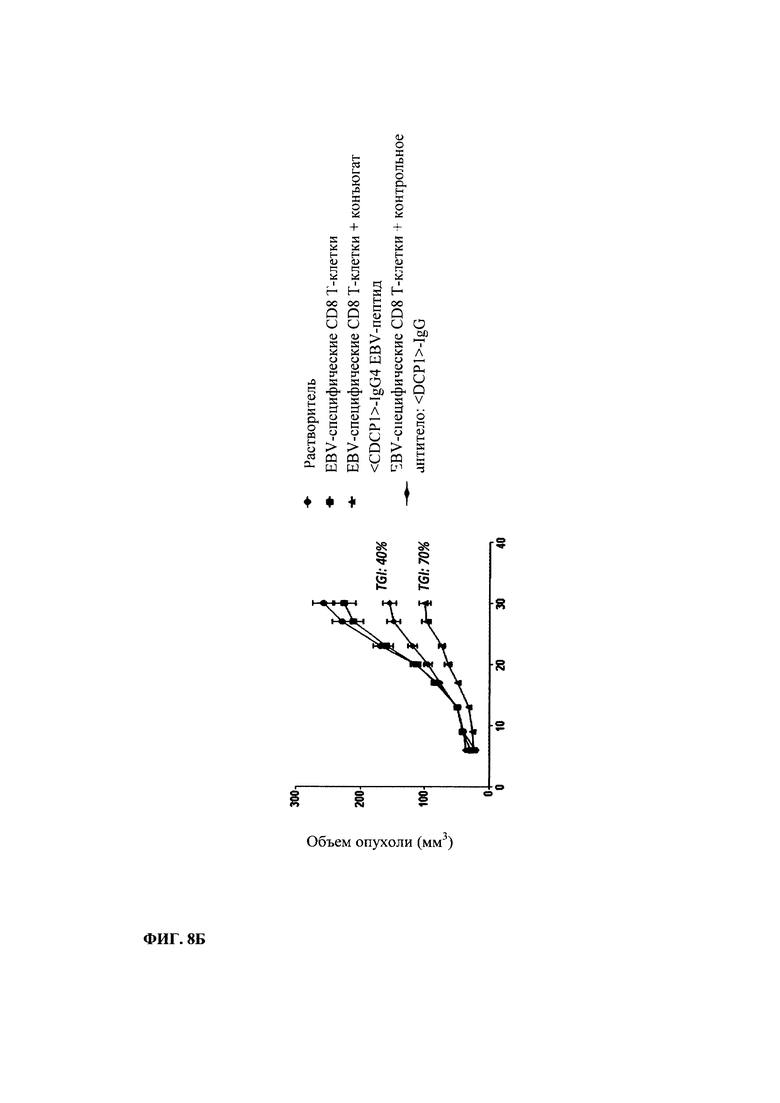

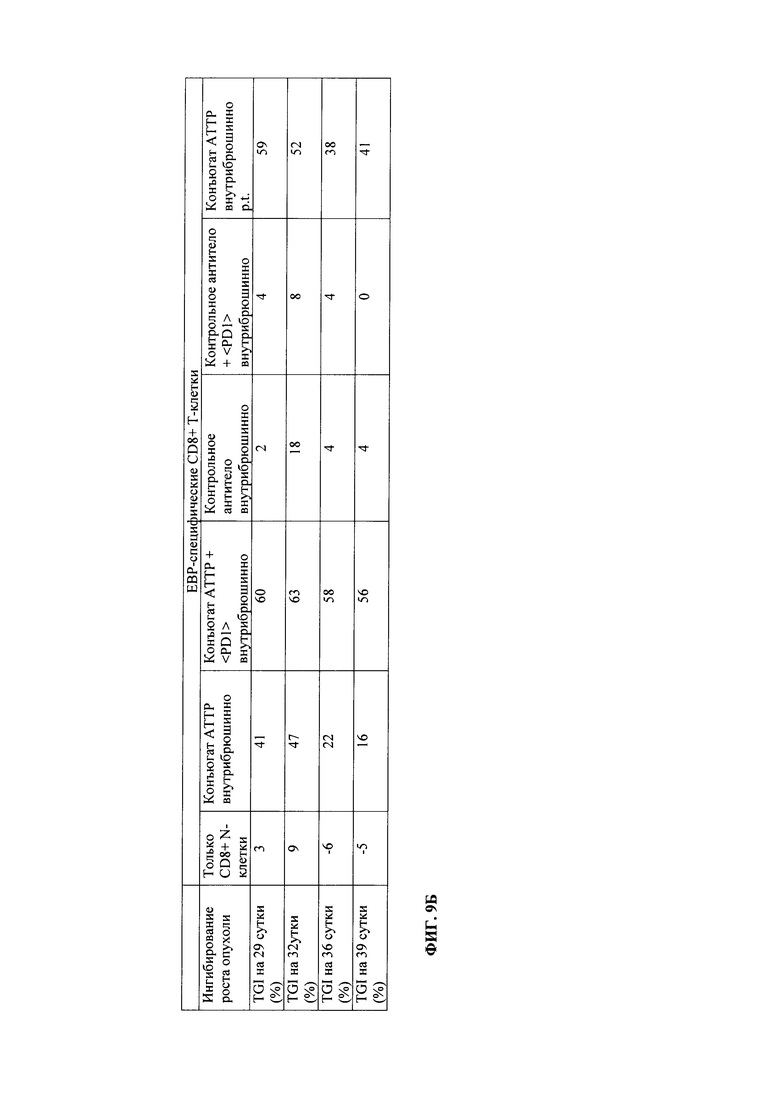

Изобретение относится к области биотехнологии. Предложен иммуноконъюгат для специфической индукции цитотоксичности Т-клеток против клеток-мишеней. Иммуноконъюгат включает, по меньшей мере, один природный вызывающий ответ Т-клеток пептид, который способен к презентации через МНС класса I, соединенный с антителом, связывающим клетку-мишень, через расщепляемую связь. Указанный вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина и ковалентно соединен с антителом через дисульфидную связь. Также раскрыты способы получения иммуноконъюгата и применения его для лечения опухоли. 7 н. и 5 з.п. ф-лы, 25 ил., 4 табл., 11 пр.
1. Иммуноконъюгат для специфической индукции цитотоксичности, включающий, по меньшей мере, один природный вызывающий ответ Т-клеток пептид, который способен к презентации через МНС класса I, соединенный с антителом, связывающим клетку-мишень, через расщепляемую связь, причем расщепляемая связь устроена таким образом, что при расщеплении указанный вызывающий ответ Т-клеток пептид, который непосредственно способен к презентации через молекулу МНС класса I, высвобождается из иммуноконъюгата, отличающийся тем, что природный вызывающий ответ Т-клеток пептид включает, по меньшей мере, один остаток цистеина, и тем, что немодифицированный вызывающий ответ Т-клеток пептид ковалентно соединен с антителом, связывающим клетку-мишень, через дисульфидную связь.
2. Иммуноконъюгат по п. 1, в котором клетка-мишень является опухолевой клеткой.
3. Иммуноконъюгат по любому из предшествующих пунктов, способный к интернализации в клетке-мишени.
4. Иммуноконъюгат по любому из предшествующих пунктов, в которых иммуноконъюгат не включает домена транслокации.
5. Иммуноконъюгат по любому из предшествующих пунктов, в которых менее чем за 12 ч после интернализации иммуноконъюгата в клетку-мишень вызывающий ответ Т-клеток пептид презентируется на поверхности клетки-мишени через молекулу МНС класса I.
6. Фармацевтическая композиция для лечения опухоли, включающая иммуноконъюгат по любому из предшествующих пунктов в эффективном количестве в комбинации с фармацевтически приемлемым носителем.
7. Применение вызывающего ответ Т-клеток пептида, способного к презентации через МНС класса I, для получения иммуноконъюгата по любому из пп. 1-5.
8. Применение иммуноконъюгата по любому из пп. 1-5 для специфической индукции цитотоксичности Т-клеток против клеток-мишеней.
9. Способ получения иммуноконъюгата по любому из пп. 1-5, включающий стадии:
а) получения рекомбинантного антитела, связывающего клетки-мишени,
б) получения вызывающего ответ Т-клеток пептида,
в) соединения, по меньшей мере, одного из указанных вызывающих ответ Т-клеток пептидов с указанным антителом, связывающим клетку-мишень, через расщепляемую связь.
10. Способ по п. 9, в котором немодифицированный вызывающий ответ Т-клеток пептид соединен с антителом, связывающим клетку-мишень.
11. Применение иммуноконъюгата по пп. 1-5 в качестве лекарственного средства для лечения опухоли.
12. Способ лечения опухоли путем введения иммуноконъюгата по пп. 1-5 пациенту, нуждающемуся в таком лечении.
| WO 2014096015 A1, 26.06.2014 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| WO 2005066203 A2, 21.07.2005 | |||
| TRUSCOTT S.M | |||
| et al | |||
| Disulfide Bond Engineering to Trap Peptides in the MHC Class I Binding Groove, J | |||
| Immunol., 2007, 178:6280-6289 | |||
| ИММУНОКОНЬЮГАТ, СПОСОБ ПОЛУЧЕНИЯ ИММУНОКОНЬЮГАТА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2129018C1 |
| РОЙТ А., БРОСТОФФФ ДЖ., МЕЙЛ Д | |||
| Иммунология | |||
| Пер | |||
| с англ | |||
| - М.: Мир, 2000 | |||
| Телефонная трансляция с катодными лампами | 1920 |
|
SU592A1 |
Авторы
Даты
2021-04-06—Публикация
2016-02-17—Подача