Изобретение относится к области молекулярной генетики и медицинской биотехнологии и может быть использовано в медицине при создании технологий дифференциальной диагностики аутоиммунного сахарного диабета, синдрома мышечной скованности и других заболеваний.
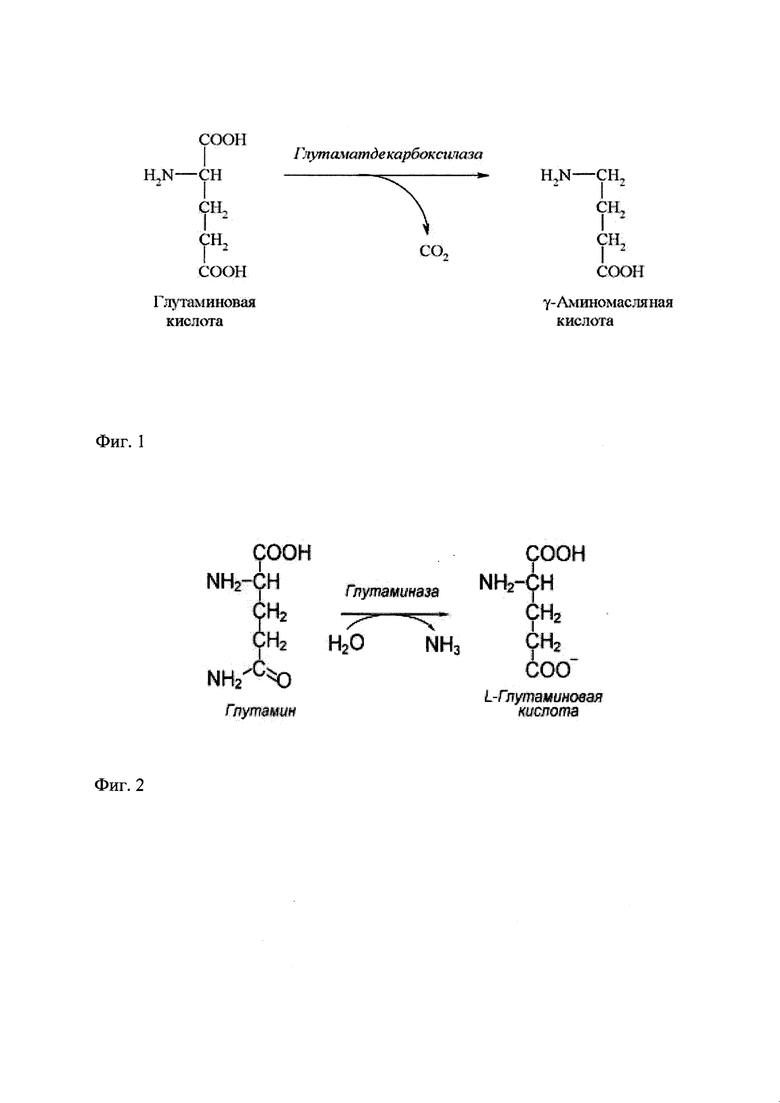
Глутаматдекарбоксилазa (GAD, GAD65, GAD67) - это фермент, катализирующий преобразование глутаминовой кислоты в гамма-аминомасляную кислоту (ГАМК) посредством реакции декарбоксилирования, как показано на фиг. 1.
В организме млекопитающих глутаматдекарбоксилазa существует в виде двух изоформ - GAD67 и GAD65, кодируемых двумя генами - GAD1 и GAD2. Числа 67 и 65 указывают на молекулярную массу изоформ - 67 кДа и 65 кДа соответственно. Оба гена экспрессируются в клетках мозга и в поджелудочной железе, причем GAD65 обнаруживается в основном в синаптических терминалях, а GAD67 - в синаптических терминалях, в теле нейрона и в аксонах (Kaufman D.L., Houser C.R., Tobin A.J. Two forms of the gamma-aminobutyric acid synthetic enzyme glutamate decarboxylase have distinct intraneuronal distributions and cofactor interactions. - J. Neurochem. 1991; 56:720-723). Появление аутоантител к GAD65 предшествует развитию инсулин-зависимого сахарного диабета (Baekkeskov S., Aanstoot H.J., Christgau S., Reetz A., Solimena M, Cascalho M, Folli F, Richter-Olesen H, De Camilli P., Identification of the 64K autoantigen in insulin-dependent diabetes as the GABA-synthesizing enzyme glutamic acid decarboxylase. Nature. 1990, 347(6289):151-6).
Также антитела к GAD часто обнаруживаются у пациентов с синдромом мышечной скованности (Lohmann T., Hawa M., Leslie R.D., Lane R., Picard J., Londei M. “Immune reactivity to glutamic acid decarboxylase 65 in stiffman syndrome and type 1 diabetes mellitus”. Lancet, July 2000, 356 (9223): 31-5. DOI:10.1016/S0140-6736(00)02431-4). По сути, в этих случаях аутоантитела к GAD65 являются маркерами соответствующего аутоиммунного заболевания. У здоровых людей аутоантитела к GAD65 отсутствуют. Обнаружение аутоантител к GAD65 в крови больных является важным шагом в дифференциальной диагностике аутоиммунного сахарного диабета, синдрома мышечной скованности и других заболеваний.
Для лабораторного измерения концентрации аутоантител к GAD65 в биологических жидкостях человека нужен антиген, представляющий собой GAD65, имеющий ту же аминокислотную последовательность и, предпочтительно, ту же конформацию, что GAD65, присутствующий в человеческих клетках.
Тематика культивирования белка глутаматдекарбоксилазы или использования культур, экспрессирующих ген глутаматдекарбоксилазы, уже становилась предметом исследований. Известен способ добавления витамина B6 для улучшения выхода глутаматдекарбоксилазы в культуре клеток E. coli ((Pat. No CN 104531652) Method for adding vitamin B6 to improve yield of glutamate decarboxylase, and application thereof). Однако этот способ не подходит для работы с глутаматдекарбоксилазой в эукариотических клетках. Культивирование глутаматдекарбоксилазы предпочтительно осуществляют в эукариотических культурах клеток, т.к. данный белок в природе существует в клетках млекопитающих.
Задачей настоящего изобретения явилась разработка способа получения такого антигена в лабораторных условиях. Для решения этой задачи нами создана тест-система, состоящая из клеточной культуры HEK293, полученной из клетки надпочечника абортированного эмбриона человека, экспрессирующей ген белка GAD65. Предполагается, что с синтезированным таким образом антигеном будут взаимодействовать аутоантитела, присутствующие в крови пациентов. Для этого сконструирована плазмида, содержащая под эукариотическим промотором ген человеческого белка GAD65. После трансфекции клеточной культуры HEK293 полученной плазмидой достигнута стабильная экспрессия гена и синтез белка GAD65 в трансфицированных клетках HEK293. Такая клеточная культура может использоваться для обнаружения аутоантител к GAD65 в сыворотках больных при помощи стандартного иммуноцитохимического анализа, (Bosman FT. Monoclonal antibodies in immunocytochemistry. Acta Histochem Suppl. 1988;35:27-32). Под больными здесь подразумеваются люди, которым достоверно диагностирован диабет первого типа, возникший из-за появления аутоантител к GAD65. Кровь больных получена с их согласия, и после центрифугирования плазма отделена от форменных элементов, а затем заморожена при -20°С для дальнейшего анализа.
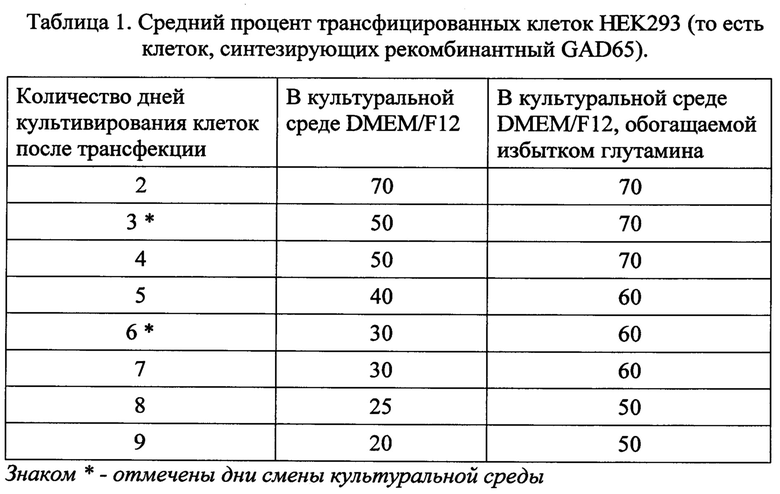
Однако в ходе работы с клеточной культурой HEK293 было выявлено, что скорость деления клеток HEK293, синтезирующих рекомбинантный белок глутаматдекарбоксилазу (GAD65) (далее по тексту HEK293-GAD) снижена по сравнению с клетками, не синтезирующими указанный белок (табл. 1). Этот эффект обусловлен тем, что синтезируемая в трансфицированных клетках глутаматдекарбоксилаза преобразует поступающую из культуральной среды глутаминовую кислоту в гамма-аминомасляную кислоту, в результате чего трансфицированные клетки испытывают дефицит глутаминовой кислоты, что снижает скорость синтеза белков, необходимых для деления клетки.
В результате любой трансфекции получается смесь из трансфицированных и не трансфицированных клеток. При дальнейшей культивации все клетки делятся или погибают. Поскольку нетрансфицированные клетки делятся быстрее, то со временем они практически вытесняют из культуры трансфицированные клетки (табл. 1).
Это затрудняет использование культивируемых клеток для обнаружения аутоантител к GAD65 в сыворотках пациентов при помощи имунноцитохимического исследования. Этот же фактор, кроме того, является препятствием для создания клеточной линии, стабильно синтезирующей рекомбинантную глутаматдекарбоксилазу GAD65.
Техническая задача настоящего изобретения состоит в разработке способа трансфекции и культивирования клеток-продуцентов, обеспечивающих стабильный синтез глутаматдекарбоксилазы GAD65.
Предлагаемое техническое решение
Стандартные среды для культивирования клеток животных (например, среда Игла, Игла МЕМ, 199, DMEM, DMEM/F12) содержат, помимо других компонентов, глутамин (0,3-0,6 мг/мл) и глутаминовую кислоту (от 0,007). При хранении среды глутамин постепенно превращается в глутаминовую кислоту. В организмах животных этот процесс катализируется глутаминазой (фиг. 2).
В живых организмах глутаминовая кислота присутствует в составе белков, ряда низкомолекулярных веществ и в свободном виде. Она играет важную роль в азотистом обмене. Глутаминовая кислота относится к группе заменимых аминокислот и играет важную роль в организме, ее содержание в организме составляет до 25% от всех аминокислот.
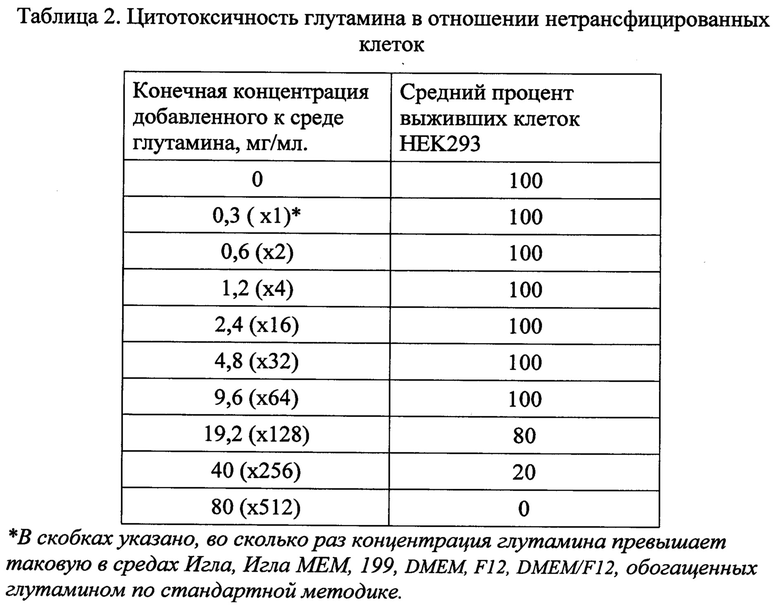
Использование трансфицированных клеток для обнаружения аутоантител к GAD65 в сыворотках пациентов при помощи иммуноцитохимического исследования предполагает гиперэкспрессию GAD65 в этих клетках. То есть полезные в диагностике трансфицированные клетки должны синтезировать намного больше GAD65, чем его синтезируется в природных условиях. Если не будет гиперэкспресии, то чувствительность таких тест-систем будет слишком низкой. Вполне ожидаемо, что большое количество синтезированного GAD65 метаболизирует значимое количество глутаминовой кислоты, тем самым обедняя клетку данной аминокислотой.
Нами установлено, что регулярное дополнительное обогащение глутамином среды, в которой культивируются HEK293-GAD клетки, решает указанную выше техническую задачу (табл. 1). Кроме того, установлено, что обогащение глутамином среды, в которой осуществляется трансфекция клеток плазмидой, содержащей ген GAD65, значительно повышает эффективность трансфекции (табл. 3). При этом для достижения указанных эффектов конечная концентрация глутамина в культуральной среде должна значительно превышать концентрацию глутаминовой кислоты в стандартных культуральных средах, таких как Игла, Игла МЕМ, 199, DMEM, F12, DMEM/F12 и других.

Пример 1. Детекция GAD65 с помощью Вестерн-блот-анализа.
Клетки HEK293 культивировали при +37°С в CO2-инкубаторе (5% CO2, влажность 100) в среде DMEM/F12, содержащей эмбриональную телячью сыворотку (FBS) (10%), антибиотики (5000 ЕД/мл пенициллина G, и 50 мкг/мл стрептомицина), амфотерицин В (25 мкг/мл) и глутамин (до 9,6 мг/мл). При образовании клетками монослоя, его дезинтегрировали с помощью раствора Версена и клетки дважды отмывали PBS. К 107 клеток добавляли по 500 мкл буферных растворов I и II для экстракции белков (буфер I: 50 мМ Трис-HCl, pH 7.4, 250 мМ сахарозы, 25 мМ NaCl, 0.1 мг/мл ингибитора трипсина из сои, 2 мМ ЭДТА, 0.1% NP-40; буфер II: 50 мМ Трис-HCl, pH 8.0, 1% Тритон X-100, 150 мМ NaCl). Клетки в буфере пипетировали, ресуспендировали с помощью вортекса, инкубировали на льду в течение 30 мин и центрифугировали при 13000 g в течение 10 мин при 4°С. В надосадочной жидкости, содержащей солюбилизированные мембранные белки, определяли концентрацию белка. Белки супернатанта разделяли электрофоретически (50 мкг общего белка на дорожку) в полиакриламидном геле в денатурирующих условиях, а затем переносили (полусухой электроперенос) на нитроцеллюлозную мембрану (Anderson et al., 1982) для последующего Вестерн-блот-анализа. Свободные от белков участки мембраны блокировали с помощью 3%-ного раствора обезжиренного молока, приготовленного на PBS (Fluka, Швейцария), в течение 30 мин, затем мембрану инкубировали с сыворотками, содержащими антитела к GAD65 (разведение от 1:10 до 1:100) в течение 1 часа, затем промывали и инкубировали с антителами к антителам человека, конъюгированными с пероксидазой хрена в течение 1 ч (разведение 1:5000). В качестве положительного контроля наносили 1 мкг рекомбинантного GAD65. В качестве хромогенного субстрата использовали 4-хлор-1-нафтол, либо осуществляли визуализацию хемилюминесцентным методом с использованием реагентов ECL (GE Healthcare, Великобритания).
Пример 2. Конструирование плазмиды pGAD65-RFP, кодирующей химерный белок.
Кодирующую последовательность гена (кДНК) GAD65 вставляли в плазмиду pRFP (Novagen, США), имеющую MCS перед RFP. Для амплификации нужного фрагмента GAD65 применяли ПЦР с использованием двух специально сконструированных праймеров.
Прямой праймер характеризуется последовательностью SEQ ID No 1, а именно 5'-ctgAAGCTTcaATGGGGCCCTGGGGCTGGA, его расчетная температура отжига (Ta) - 60°С; полужирным шрифтом выделена часть олигонуклеотида, комплементарная GAD65; подчеркнут сайт узнавания для эндонуклеазы рестрикции Hind III.
Обратный праймер характеризуется последовательностью SEQ ID No 2, а именно 5'-ctgGTCGACCGCCACGTCATCCTCCAGACT, его расчетная температура отжига (Ta) - 58°С, полужирным шрифтом выделена часть олигонуклеотида, комплементарная 3'-концу кодирующей части GAD65; подчеркнут сайт узнавания для эндонуклеазы рестрикции Sal I. Для вычисления температур плавления и отжига праймеров использовали программу Oligos v.7.1.
ПЦР проводили в 30 мкл реакционной смеси. Плазмиду pEGFP-N3 и полученный продукт ПЦР обрабатывали эндонуклеазами рестрикции Hind III и Sal I (Fermentas, Литва), и затем очищали. Выделение ДНК из агарозного геля осуществляли с помощью набора фирмы Promega (WizardSV Gel and PCR Clean-Up System, США) согласно инструкции производителя. Лигирование осуществляли при помощи T4 ДНК-лигазы (Fermentas, Литва). Компетентные клетки Escherichia coli штамм DH5(alpha) были трансформированы ДНК, полученной после лигирования, и перенесены на селективную среду, содержащую 100 мкг/мл канамицина. Плазмидную ДНК из выросших клонов выделяли с помощью щелочного лизиса с последующей обработкой РНК-азой, депротеинизацией при экстракции ДНК смесью фенола и хлороформа и осаждением ДНК спиртом. Качество плазмидной ДНК оценивали с помощью электрофореза в 0.8%-ном агарозном геле. Для выявления плазмид со вставкой кДНК GAD65 осуществляли секвенирование на секвенаторе 3500 genetic analyzer (Applied Biosystems, США). Для дальнейшей работы использовали клоны, в плазмидной ДНК которых присутствовала вставка и отсутствовали мутации в кодирующей области GAD65.
Пример 3. Трансфекция клеток плазмидной ДНК.
Клетки HEK293 культивировали при +37°С в CO2-инкубаторе (5% CO2, влажность 100) в среде DMEM/F12, содержащей эмбриональную телячью сыворотку (FBS) (10%), антибиотики (5000 ЕД/мл пенициллина G, и 50 мкг/мл стрептомицина), амфотерицин В (25 мкг/мл) и глутамин (300 мкг/мл). За день до трансфекции клетки переносили в лунки планшетов с покровными стеклами на дне. Число вносимых в лунку клеток подбирали таким образом, чтобы на следующий день они занимали 20-30% поверхности стекла. Клеточную линию HEK293 трансфицировали кольцевыми формами исходной pEGFP-N3 и pLDLR-EGFP, очищенными из агарозного геля. Трансфекцию осуществляли по стандартному методу (Chen C., Okayama H 1987. High-efficiency transformation of mammalian cells by plasmid DNA. Mol Cell Biol. 7: 2745-2752), используя 100 нг плазмидной ДНК на 1 лунку 96-луночного планшета. Через 24 ч после трансфекции культуральную среду заменяли средой DMEM/F12, содержащей антибиотики и антимикотики, а также 10% FBS и глутамин в концентрации от 4,8 мг/мл. до 9,6 мг/мл. После инкубации в течение от 1 до 9 суток клетки аккуратно промывали PBS и фиксировали 4%-ным параформальдегидом в PBS в течение 10 мин. Препараты отмывали РВS не менее 1 ч, инкубировали 1 ч при комнатной температуре в блокирующем растворе TNB (0.1 M Трис-HCl, pH 7.5, 0.15 M NaCl, 0.5% блокирующего реагента (Perkin Elmer, FP1020, США)), затем 1 ч с антителами против GAD65 при 37°C во влажной камере. Препараты промывали 3 раза в растворе PBS в течение 5 мин. Затем инкубировали 1 час с флуоресцентно-меченными вторичными антителами при 37°C. После промывания препаратов в PBS (3 раза по 5 мин) монтировали покровные стекла на предметные с помощью полимеризующейся смолы для флуоресцентной микроскопии (DAKO, США).
Предложенный способ культивирования клеток-продуцентов GAD65 в среде с повышенным содержанием глутамина обеспечил стабильный синтез глутаматдекарбоксилазы в лабораторных условиях с одновременным повышением эффективности трансфекции.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ФГБНУ "ИЭМ" FSBSI “IEM”
<120> Способ трансфекции и культивирования клеток,
синтезирующих рекомбинантный белок глутаматдекарбоксилазу
<140>
<141>
<160> 2
<210> 1
<211> 30
<212> Нуклеотидная последовательность
<213> Искусственная последовательность
<220>
<223> Нуклеотидная последовательность прямого праймера для амплификации гена
GAD65
<400> 1
ctgaagcttc aatggggccc tggggctgga
<210> 2
<211> 30
<212> Нуклеотидная последовательность
<213> Искусственная последовательность
<220>
<223> Нуклеотидная последовательность обратного праймера для амплификации гена
GAD65
<400> 2
ctggtcgacc gccacgtcat cctccagact
<---
Изобретение относится к области молекулярной генетики и медицинской биотехнологии и может быть использовано в медицине при создании технологий дифференциальной диагностики аутоиммунного сахарного диабета, синдрома мышечной скованности и других заболеваний. Разработан способ трансфекции и культивирования клеток, синтезирующих рекомбинантный белок глутаматдекарбоксилазу GAD65, основанный на трансфекции клеточной культуры HEK293 специально сконструированной плазмидой, содержащей под эукариотическим промотором ген человеческого белка GAD65. Стабильная экспрессия гена и синтез белка GAD65 в трансфицированных клетках HEK293 достигнута за счет регулярного дополнительного обогащения глутамином культуральной среды. Предложенный способ культивирования клеток-продуцентов GAD65 в среде с повышенным содержанием глутамина позволяет обеспечивать стабильный синтез глутаматдекарбоксилазы в лабораторных условиях с одновременным повышением эффективности трансфекции. 2 ил., 3 табл, 3 пр.
Способ трансфекции и культивирования клеток, синтезирующих рекомбинантную глутаматдекарбоксилазу GAD65, включающий создание плазмиды, содержащей эукариотический промотор и нуклеотидную последовательность, кодирующую белок глутаматдекарбоксилазу GAD65, трансфекцию культуры клеток животного полученной плазмидой и культивирование их на питательной среде, отличающийся тем, что культивирование клеток, трансфицированных плазмидой, содержащей ген белка GAD65, осуществляется в течение не менее 3 дней в питательной среде с повышенным содержанием глутамина в концентрации от 2,4 мг/мл до 9,6 мг/мл.
| CN 104531652 A, 22.04.2015 | |||
| СПОСОБЫ И ПРЕПАРАТЫ ДЛЯ ТРАНСФЕКЦИИ КЛЕТОК | 2012 |
|
RU2624139C2 |
| BOSMAN FT | |||
| Monoclonal antibodies in immunocytochemistry, Acta Histochem Suppl | |||
| Механическая топочная решетка с наклонными частью подвижными, частью неподвижными колосниковыми элементами | 1917 |
|
SU1988A1 |
Авторы
Даты
2021-04-08—Публикация
2019-07-30—Подача