Изобретение относится к химико-фармацевтической промышленности и может быть использовано в центрах контроля качества лекарственных средств и контрольно-аналитических лабораториях при проведении количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной (Syringa vulgaris L.).
Действующая система контроля качества лекарственных препаратов требует постоянного усовершенствования подходов к стандартизации биологически активных соединений (БАС) с использованием современных методов анализа и актуальных данных об их физико-химических, спектральных и фармакологических свойствах, позволяющих объективно и селективно определять содержание целевых веществ [4].
Сирень обыкновенная (Syringa vulgaris L.) является одним из видов растений, не включенных в Государственную Фармакопею Российской Федерации XIV издания, но в качестве лекарственного растительного сырья (ЛРС) зарегистрирована кора (ВФС 42-2106-92) [1, 2]. Препараты на основе коры сирени обладают широким спектром фармакологической активности: иммуномодулирующим, адаптогенным, анксиолитическим и антидепессивным действием [3].
Особый интерес, наряду с фармакопейным сырьем - корой, представляют цветки данного растения. Цветки сирени обыкновенной (Syringa vulgaris L.) являются перспективным источником БАС, обладающим иммуностимулирующим, анксиолитическим и антидепрессивным действием. Однако проблема стандартизации данного вида сырья остается нерешенной.
На данный момент нет известных способов количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной методом прямой спектрофотометрии [2].
Таким образом, целью изобретения является разработка способа количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной, обладающего высокой специфичностью, точностью и воспроизводимостью.
Техническим результатом является создание способа количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной в пересчете на хлорогеновую кислоту.
Технический результат достигается тем, что предварительно получают водно-спиртовое извлечение из растительного сырья путем экстракции 1 г точной навески измельченного до размера частиц 1 мм растительного сырья 60% этиловым спиртом, в пересчете на вещество фенилпропаноидной природы, методом прямой спектрофотометрии в отношении «сырье-экстрагент» - 1:100, определение фенилпропаноидов проводят при длине волны 330 нм в пересчете на хлорогеновую кислоту и абсолютно сухое сырье рассчитывают по формуле:

где:
x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %;
D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора Государственного стандартного образца хлорогеновой кислоты;
m - масса сырья, г;
mo - масса Государственного стандартного образца хлорогеновой кислоты, г;
W - потеря в массе при высушивании, %;
в случае отсутствия стандартного образца хлорогеновой кислоты для расчета целесообразно использовать теоретическое значение его удельного показателя поглощения, равное 497:

где:
x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %;
D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
497 - удельный показатель поглощения ( ) Государственного стандартного образца хлорогеновой кислоты при длине волны 330 нм;
) Государственного стандартного образца хлорогеновой кислоты при длине волны 330 нм;
W - потеря в массе при высушивании, %.
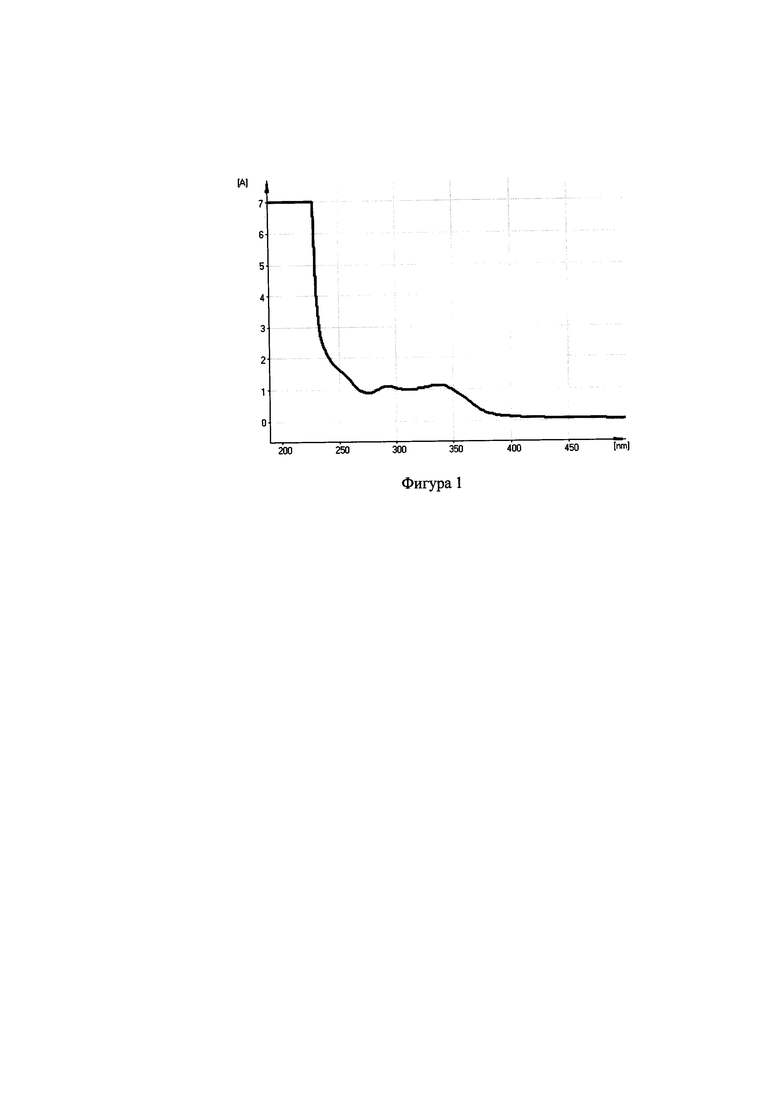
При изучении спектральных характеристик было выявлено, что именно хлорогеновая кислота определяет характер кривой поглощения водно-спиртового извлечения из цветков сирени обыкновенной. Определено, что в УФ-спектре водно-спиртового извлечения сирени обыкновенной наблюдается максимум поглощения фенилпропаноидов (Фиг. 1 в Приложении 1), как и в случае хлорогеновой кислоты (Фиг. 2 в Приложении 2), где кривая 1 на фиг. 1 и фиг. 2 демонстрирует исходный раствор водно-спиртового извлечения из цветков сирени обыкновенной или исходный раствор хлорогеновой кислоты соответственно.
Изучение УФ-спектров фиг. 2 (где кривая 1 - раствор хлорогеновой кислоты) показало, что раствор ГСО хлорогеновой кислоты имеет максимум поглощения при длине волны 330 нм. В УФ-спектре водно-спиртового извлечения из цветков сирени обыкновенной в прямом варианте на фиг. 1 (Приложение 1) так же обнаруживается при длине волны 330 нм максимум поглощения, который соответствует максимуму поглощения спиртового раствора хлорогеновой кислоты.
Данный факт позволяет проводить спектрофотометрическое определение суммы фенилпропаноидов в цветках сирени обыкновенной при аналитической длине волны 330 нм.
Также нами было изучено влияние экстрагента на процесс экстракции. В таблице 1 (Приложение 3) представлена зависимость выхода фенилпропаноидов цветков сирени обыкновенной от концентрации экстрагента. В результате эксперимента в качестве оптимального экстрагента нами был выбран 60% этиловый спирт, так как выход действующих веществ из сырья при его использовании максимален.
Далее нами был изучен вопрос относительно продолжительности экстракции на кипящей водяной бане, в таблице 2 (Приложение 4) представлена зависимость выхода фенилпропаноидов цветков сирени обыкновенной от времени экстракции на кипящей водяной бане, при этом было выбрано время экстракции 45 минут, при котором наблюдался максимальный выход веществ.
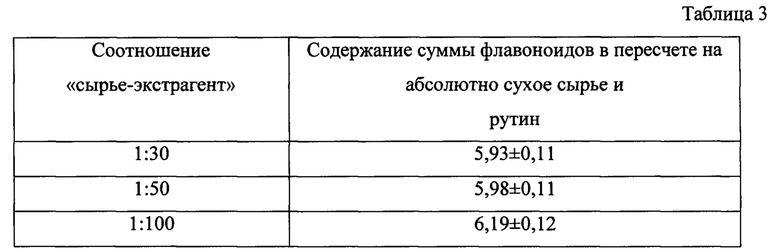
В таблице 3 (Приложение 5) представлена зависимость выхода фенилпропаноидов цветков сирени обыкновенной от соотношения «сырье-экстрагент». Из таблицы 3 видно, что максимальный выход действующих веществ наблюдается при соотношении «сырье-экстрагент» 1:100, по этой причине данное соотношение было выбрано нами в качестве оптимального.
Финальной стадией стало изучение влияния степени измельчения сырья на выход фенилпропаноидов из цветков сирени обыкновенной. Из таблицы 4 (Приложение 6) следует, что максимальный выход веществ наблюдался при экстракции частиц, проходящих сквозь сито диаметром 1 мм.
Учитывая, что увеличение числа операций на стадии пробоподготовки ведет к возрастанию ошибки, выбор сделан в пользу одностадийного процесса экстракции с подтверждением требуемой точности количественного определения.
Таким образом, было определено, что оптимальными параметрами экстракции являются: однократное извлечение 60% этиловым спиртом на кипящей водяной бане в течение 45 минут в соотношении «сырье-экстрагент» - 1:100, степень измельчения сырья 1 мм.
Принимая по внимание тот факт, что специфической для цветков сирени обыкновенной является хлорогеновая кислота, а максимумы поглощения раствора хлорогеновой кислоты и водно-спиртового извлечения цветков сирени обыкновенной находятся в области 330 нм, целесообразным является определение содержания суммы фенилпропаноидов в пересчете на хлорогеновую кислоту при длине волны 330 нм.
Способ реализуется следующим образом.
Аналитическую пробу воздушно-сухого сырья сирени обыкновенной измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. Около 1 г точной навески измельченного сырья помещают в колбу со шлифом вместимостью 250 мл, прибавляют 100 мл 60% этилового спирта. Колбу закрывают пробкой и взвешивают на тарирных весах с точностью до ±0,01. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 45 минут. Затем колбу охлаждают в течение 30 мин, закрывают той же пробкой, снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение фильтруют через фильтр с красной полосой (извлечения из травы).
Испытуемый раствор для анализа суммы фенилпропаноидов готовят следующим образом: 1 мл полученного извлечения помещают в мерную колбу вместимостью 50 мл и доводят объем раствора до метки 96% этиловым спиртом (испытуемый раствор).
Для расчета содержания суммы фенилпропаноидов готовят раствор стандартного образца хлорогеновой кислоты, измеряют оптическую плотность раствора при аналитической длине волны 330 нм и определенное значение оптической плотности используют в формуле расчета.
Приготовление раствора стандартного образца хлорогеновой кислоты.
Около 0,020 г (точная навеска) хлорогеновой кислоты помещают в мерную колбу вместимостью 100 мл, растворяют в 70 мл 70% этилового спирта при нагревании на водяной бане. После охлаждения содержимого колбы до комнатной температуры доводят объем раствора 70% этиловым спиртом до метки (раствор А хлорогеновой кислоты). После чего 1 мл раствора А хлорогеновой кислоты помещают в мерную колбу на 25 мл, доводят объем раствора до метки спиртом этиловым 96% (испытуемый раствор Б хлорогеновой кислоты).
Измерение оптической плотности проводят при длине волны 330 нм через 40 минут после приготовления всех растворов.
Содержание суммы фенилпропаноидов (х, %) в пересчете на хлорогеновую кислоту и абсолютно сухое сырье вычисляют по формуле:

где:
D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора Государственного стандартного образца хлорогеновой кислоты;
m - масса сырья, г;
mo - масса Государственного стандартного образца хлорогеновой кислоты, г;
W - потеря в массе при высушивании в процентах.
В случае отсутствия стандартного образца хлорогеновой кислоты для расчета целесообразно использовать теоретическое значение его удельного показателя поглощения, равное 497:

где:
D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
497 - удельный показатель поглощения ( ) Государственного стандартного образца хлорогеновой кислоты при 330 нм;
) Государственного стандартного образца хлорогеновой кислоты при 330 нм;
W - потеря в массе при высушивании в процентах.
Предлагаемый способ поясняется следующими примерами.
Пример 1
Аналитическую пробу сырья сирени обыкновенной (заготовлено в Ботаническом саду Самарского университета, 2016 г.) измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. 0,9950 г измельченного сырья помещают в колбу со шлифом вместимостью 250 мл, прибавляют 100 мл 60% этилового спирта. Колбу закрывают пробкой и взвешивают на тарирных весах с точностью до ±0,01. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане (умеренное кипение) в течение 45 минут. Затем колбу охлаждают в течение 30 мин, закрывают той же пробкой, снова взвешивают и восполняют недостающий экстрагент до первоначальной массы. Извлечение фильтруют через бумажный фильтр (красная полоса).
Испытуемый раствор для анализа суммы фенилпропаноидов готовят следующим образом: 1 мл полученного извлечения помещают в мерную колбу вместимостью 50 мл и доводят объем раствора до метки спиртом этиловым 96% (испытуемый раствор).
Для расчета содержания суммы фенилпропаноидов готовят раствор стандартного образца хлорогеновой кислоты и измеряют оптическую плотность раствора при длине волны 330 нм и определенное значение оптической плотности используют в формуле расчета.
Приготовление раствора стандартного образца хлорогеновой кислоты.
0,020 г хлорогеновой кислоты помещают в мерную колбу вместимостью 100 мл, растворяют в 70 мл 70% этилового спирта при нагревании на водяной бане. После охлаждения содержимого колбы до комнатной температуры доводят объем раствора 70% этиловым спиртом до метки (раствор А хлорогеновой кислоты). После чего 1 мл раствора А хлорогеновой кислоты помещают в мерную колбу на 25 мл, затем доводят объем раствора до метки спиртом этиловым 96%.
Измерение оптической плотности проводят при длине волны 330 нм через 40 минут после приготовления всех растворов.
Содержание суммы фенилпропаноидов (х, %) в пересчете на хлорогеновую кислоту и абсолютно сухое сырье вычисляют по формуле:

где:
0,5511 - оптическая плотность испытуемого раствора;
0,3829 - оптическая плотность раствора стандартного образца хлорогеновой кислоты;
0,9950 - масса сырья, г;
0,0202 - масса стандартного образца хлорогеновой кислоты, г;
9,8 - потеря в массе при высушивании в процентах.
Х=6,48%.
Содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту равно 6,48%.
Пример 2
При необходимости определения суммы фенилпропаноидов в цветках сирени обыкновенной в отсутствии стандартного образца хлорогеновой кислоты, необходимо провести все действия из примера 1 до приготовления раствора стандартного образца хлорогеновой кислоты.
После измерения оптической плотности извлечения из цветков сирени обыкновенной при длине волны 330 нм, содержание суммы фенилпропаноидов (х, %) в пересчете на хлорогеновую кислоту и абсолютно сухое сырье вычисляют по формуле, используя теоретическое значение удельного показателя поглощения рутина, равное 497:

где:
0,5511 - оптическая плотность испытуемого раствора;
0,9950 - масса сырья, г;
497 - удельный показатель поглощения (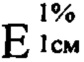 ) стандартного образца хлорогеновой кислоты при 330 нм;
) стандартного образца хлорогеновой кислоты при 330 нм;
9,8 - потеря в массе при высушивании в процентах.
Х=6,18%.
Содержание суммы фенилпопаноидов в пересчете на хлорогеновую кислоту равно 6,18%, что сопоставимо со значением, полученном в примере 1.
Все результаты были статистически обработаны. Ошибка единичного количественного определения составила ±1,85%.
Таким образом, предлагаемый способ количественного определения суммы фенилпропаноидов в пересчете на хлорогеновую кислоту в цветках сирени обыкновенной с использованием прямой спектрофотометрии разработан впервые для данного вида сырья и обладает следующими преимуществами:
1. Разработанный метод является специфичным и селективным, а также позволяет проводить экстракцию сырья однократно 60% этиловым спиртом, позволяющим исчерпывающе извлекать целевые вещества (фенилпропаноиды).
2. Пересчет суммы фенилпропаноидов идет на специфическое для цветков сирени обыкновенной фенилпропаноидное вещество - хлорогеновую кислоту, определяющее характер кривой поглощения в УФ - спектре испытуемого раствора (длина волны 330 нм).
3. Ошибка единичного определения предлагаемого способа составляет ±1,85%, что свидетельствует об объективности разработанного способа.
4. Разработанный способ позволяет исключить пробоподготовку, заключающуюся в обработке экстракта токсическими растворителями.
Этот способ можно применять в центрах контроля качества лекарственных средств, на фармацевтических предприятиях и контрольно-аналитических лабораториях при проведении количественного анализа цветков сирени обыкновенной (Syringa vulgaris L.)
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. ВФС 42-2106-92 «Кора сирени обыкновенной».
2. Государственная фармакопея Российской Федерации. XIV издание. М., 2018 г. Режим доступа: http://femb.ru/femb/pharmacopea.php. (дата обращения: 27.11.2019).
3. Климова И.Ю. Аналитические и технические исследования по разработке новых препаратов на основе коры сирени обыкновенной./ И.Ю. Климова - Самара, 2005. -159 с.
4. Куркин В.А. К вопросу о стандартизации лекарственного сырья содержащего флавоноиды и фенилпропаноиды / В.А. Куркин, О.В. Маевская, В.Б. Браславский и др.// Применение хроматографии в пищевой, микробиологической и медицинской промышленности: Материалы Всесоюзной конференции. Геленджик, 1990. - С. 85-
5. Куркин В.А. Фармакогнозия: Учебник для студентов фармац. вузов - Изд. 4-е, перераб. и доп./ В.А. Куркин. - Самара: ООО «Офорт», ФГБОУ ВО СамГМУ Минздрава России, 2019. - 1278 с.
6. Куркин В.А., Запесочная Г.Г., Гриненко Н.А. Золотарев Б.М. Фенольные соединения коры Syringa vulgaris // Химия природных соединений. - 1989. - №4. -С. 581-582.
ПРИЛОЖЕНИЕ 3

ПРИЛОЖЕНИЕ 4

ПРИЛОЖЕНИЕ 5
ПРИЛОЖЕНИЕ 6

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ЛИСТЬЯХ СИРЕНИ ОБЫКНОВЕННОЙ | 2020 |
|
RU2752316C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЕНИЛПРОПАНОИДОВ В МОРИНГИ МАСЛИЧНОЙ ЛИСТЬЯХ | 2021 |
|
RU2763264C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГИДРОКСИКОРИЧНЫХ КИСЛОТ В ПОБЕГАХ БОЯРЫШНИКА КРУПНОКОЛЮЧКОВОГО | 2023 |
|
RU2812737C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЕНИЛПРОПАНОИДОВ В КОРНЕВИЩАХ И КОРНЯХ ЭЛЕУТЕРОКОККА КОЛЮЧЕГО | 2022 |
|
RU2797411C1 |
| Способ количественного определения сирингина в коре сирени обыкновенной | 2021 |
|
RU2782620C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2012 |
|
RU2496510C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ В ЖЕЛЧЕГОННОМ СБОРЕ № 3 | 2014 |
|
RU2554780C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РОЗМАРИНОВОЙ КИСЛОТЫ В ЛИСТЬЯХ МЯТЫ ПЕРЕЧНОЙ | 2024 |
|
RU2833834C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ ФЛАВОНОИДОВ В ТРАВЕ ТЫСЯЧЕЛИСТНИКА ОБЫКНОВЕННОГО | 2022 |
|
RU2806035C1 |
| Способ получения средства, обладающего желчегонной, противовоспалительной и антиоксидантной активностью | 2017 |
|
RU2665968C1 |

Изобретение относится к химико-фармацевтической промышленности, а именно к способу количественного определения суммы фенилпопаноидов в цветках сирени обыкновенной (Syringa vulgaris L.). Способ количественного определения фенилпропаноидов, заключающийся в предварительном получении водно-спиртового извлечения из растительного сырья путем экстракции 1 г точной навески измельченного до размера частиц 1 мм растительного сырья 60% этиловым спиртом в течение 45 минут, в пересчете на вещество фенилпропаноидной природы, методом прямой спектрофотометрии в отношении «сырье-экстрагент» - 1:100, определение фенилпропаноидов проводят при длине волны 330 нм в пересчете на хлорогеновую кислоту, содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, и абсолютно сухое сырье рассчитывают по формуле:
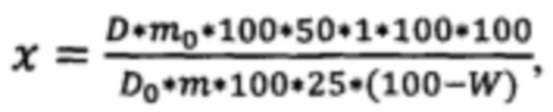
где x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %; D - оптическая плотность испытуемого раствора; Do - оптическая плотность раствора Государственного стандартного образца хлорогеновой кислоты; m - масса сырья, г; mo - масса Государственного стандартного образца хлорогеновой кислоты, г; W - потеря в массе при высушивании, %; в случае отсутствия стандартного образца хлорогеновой кислоты целесообразно использовать теоретическое значение его удельного показателя поглощения, равное 497:

где x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %; D - оптическая плотность испытуемого раствора; m - масса сырья, г; 497 - удельный показатель поглощения (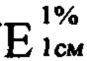 ) Государственного стандартного образца рутина при 330 нм; W - потеря в массе при высушивании, %. Вышеописанный способ количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной является специфичным и точным. 4 табл., 2 пр., 2 ил.
) Государственного стандартного образца рутина при 330 нм; W - потеря в массе при высушивании, %. Вышеописанный способ количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной является специфичным и точным. 4 табл., 2 пр., 2 ил.
Способ количественного определения суммы фенилпропаноидов в цветках сирени обыкновенной, заключающийся в предварительном получении водно-спиртового извлечения из цветков сирени обыкновенной путем однократной экстракции в течение 45 минут 60% этиловым спиртом воздушно-сухого сырья точной навеской массой 1 г, измельченного до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм, при соотношении «сырье-экстрагент» 1:100; количественное определение суммы фенилпропаноидов в цветках сирени обыкновенной проводят при длине волны 330 нм в пересчете на хлорогеновую кислоту и содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, и абсолютно сухое сырье рассчитывают по формуле:

где:
x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %;
D - оптическая плотность испытуемого раствора;
Do - оптическая плотность раствора Государственного стандартного образца хлорогеновой кислоты;
m - масса сырья, г;
m0 - масса Государственного стандартного образца хлорогеновой кислоты, г;
W - потеря в массе при высушивании, %;
в случае отсутствия стандартного образца хлорогеновой кислоты целесообразно использовать теоретическое значение его удельного показателя поглощения, равное 497:
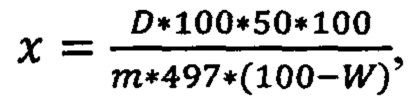
где:
x - содержание суммы фенилпропаноидов в пересчете на хлорогеновую кислоту, %;
D - оптическая плотность испытуемого раствора;
m - масса сырья, г;
497 - удельный показатель поглощения (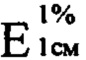 ) Государственного стандартного образца хлорогеновой кислоты при 330 нм;
) Государственного стандартного образца хлорогеновой кислоты при 330 нм;
W - потеря в массе при высушивании, %.
| КУРДЮКОВ Е.Е., Фармакогностическое исследование семян льна и листьев стевии как компонентов растительного сбора "СТЕЛИНОЛ", Пенза 2019, [найдено онлайн], [дата обращения 08.02.2021], найдено из Интернета: https://www.samsmu.ru/files/referats/2019/kurdyukov/dissertation.pdf, подтверждено |
Авторы
Даты
2021-05-05—Публикация
2020-10-14—Подача