Изобретение относится к области биоразлагаемых и биосовместимых полимерных материалов, обладающих гидрофобно-гидрофильными свойствами, и может быть использовано в медицине и косметологии.
Наиболее перспективными природными биодеградируемыми полимерами являются полиэфиры алкановых кислот, так называемые полигидроксиалканоаты (ПГА) - термопластичные линейные полиэфиры микробиологического происхождения. Однако гидрофобный характер поверхности ПГА препятствует их широкому использованию в биологии и медицине, поскольку смачиваемость материала является ключевым фактором для пролиферации клеток и регенерации тканей.
Наиболее распространенным и широко изученным представителем ПГА является поли(3-гидроксибутират) (ПГБ), который обладает целым рядом ценных свойств: термопластичностью, биоразлагаемостью, нетоксичностью по отношению к живым системам, биосовместимостью с тканями организма и др.
Одним из путей придания ПГБ гидрофильности является создание на его поверхности слоя привитого поли-2-гидроксиэтилметакрилата (ПГЭМА) путем радикальной полимеризации 2-гидроксиэтилметакрилата (ГЭМА). ПГЭМА давно и широко применяется в медицине в силу своей гидрофильности, нетоксичности и биосовместимости ("Hydrogels in Medicine and Pharmacy: Fundamentals", Ed. N.A. Peppas, CRS Press, 2019, v. 1, 193 p.). Существенное ограничение при использовании ПГЭМА связано с отсутствием у него способности к биодеградации.
При инициировании полимеризации ГЭМА на поверхности ПГБ γ-облучением (Н. Mitomo,  Y. Watanabe, F. Yoshii, K. MakuuchiJ. Saito // J. Macromol. Sci. A, 1995, 3, 429-42) степень прививки зависела от величины дозы облучения, и при увеличении степени прививки повышалась смачиваемость сополимера, но биодеградируемость привитого сополимера резко снижалась по сравнению с исходным ПГБ.
Y. Watanabe, F. Yoshii, K. MakuuchiJ. Saito // J. Macromol. Sci. A, 1995, 3, 429-42) степень прививки зависела от величины дозы облучения, и при увеличении степени прививки повышалась смачиваемость сополимера, но биодеградируемость привитого сополимера резко снижалась по сравнению с исходным ПГБ.
При осуществлении прививочной полимеризации ГЭМА на пленках полигидроксибутират-со-гидроксивалерата в присутствии химического инициатора -перекиси бензоила (Н-К. Lao, Е. Renard, I. Linossier, V. Langlois, // Biomacromolecules, 2007, 8 (2), 416-23) при высокой степени прививки (>30%) смачиваемость привитого сополимера была заметно улучшена, однако биодеградируемость привитого сополимера была сильно снижена.
// Biomacromolecules, 2007, 8 (2), 416-23) при высокой степени прививки (>30%) смачиваемость привитого сополимера была заметно улучшена, однако биодеградируемость привитого сополимера была сильно снижена.
В работе Н-K. Lao, Е. Renard, I. Linossier, V. Langlois,  // J. Appl. Polym. Sci., 2010, 116 (1), 288-97 была исследована фотохимическая прививка ГЭМА на пленки полигидроксибутират-согидроксивалерата под действием УФ-облучения в присутствии фотоинициатора: бензофенона или Н2О2. Степень прививки варьировалась в широком диапазоне, что повышало гидрофильность сополимера, но снижало способность к биодеградации - сохранить полную биоразлагаемость ПГА у привитого сополимера удавалось только при содержании в нем привитого ПГЭМА менее 10%.
// J. Appl. Polym. Sci., 2010, 116 (1), 288-97 была исследована фотохимическая прививка ГЭМА на пленки полигидроксибутират-согидроксивалерата под действием УФ-облучения в присутствии фотоинициатора: бензофенона или Н2О2. Степень прививки варьировалась в широком диапазоне, что повышало гидрофильность сополимера, но снижало способность к биодеградации - сохранить полную биоразлагаемость ПГА у привитого сополимера удавалось только при содержании в нем привитого ПГЭМА менее 10%.
Известен способ присоединения к ПГБ природных гидрофильных полимеров, содержащих гидроксильные (целлюлоза) или аминогруппы (хитозан), за счет потенциальной активности карбоксильных терминальных групп ПГБ в реакциях переэтерификации или амидирования (М. Yalpani, R.H. Marchessault, F.G. Morin, C.J. Monasterios // Macromolecules, 1991, 24, 6046-49). Взаимодействие осуществляли перемешиванием растворов ПГБ с ацетатом целлюлозы или хитозаном в течение 4-5 дней, достигнутая степень присоединения была очень мала - 0.02-0.03.
Задачей изобретения является создание биодеградируемого материала с гидрофобно-гидрофильными свойствами на основе ПГБ, который может быть использован в медицине и косметологии.
Решение поставленной задачи достигается предлагаемым микроволокнистым биодеградируемым материалом с гидрофобно-гидрофильными свойствами на основе микроволокнистого поли-3-гидроксибутирата (ПГБ), полученным обработкой ПГБ 2-гидроксиэтилметакрилатом (ГЭМА) при соотношении ПГБ : ГЭМА, равном 1:0,6-2,2 в присутствии ионно-координационного катализатора полимеризации VO(DMSO)5(ClO4)2 при температуре 75-85°С, сохраняющим способность волокон ПГБ к полному биоразложению и характеризующимся сорбционной емкостью к водяному пару не менее 3%.
Диаметр волокон предлагаемого микроволокнистого биодеградируемого материала не превышает 16 мкм.
Взаимодействие поли-3-гидроксибутирата с 2-гидроксиэтилметакрилатом осуществляют под давлением 15-17 г/см2.
В настоящее время все шире разрабатываются и применяются в медицине микроволокнистые полимерные биоматериалы, которые получают методом электроформования (электроспиннига) (Филатов Ю.Н. Электроформование волокнистых материалов (ЭФВ-процесс). М.: Нефть и Газ, 1997,297 с.; Н. Pant, P. Pokharel, М.K. Joshi, et al., Chemical Engineering Journal, 2015, V. 270, P. 336-342; P. Boodagh, D. Guo, N. Nagiah, W. Tan, Journal of Biomaterials Science, Polymer Edition, 2015, V. 27, N. 11, P. 1086-1099). Это связано с тем, что микроволокнистые материалы характеризуются более высокой скоростью биодеградации благодаря большей удельной площади поверхности и, следовательно, повышенной доступностью для атаки микроорганизмов. Подобные закономерности описаны для нетканых материалов на основе полилактида (Jie Ren. Biodegradable Poly (Lactic Acid): Synthesis, Modification, Processing and Applications. - Springer Science & Business Media, Apr 5, 2011 - Technology & Engineering, pp. 208-253). Кроме того, величина удельной поверхности волокнистых материалов, наряду со степенью гидрофильности волокон, имеет определяющее значение для сорбционной емкости материала.
Использование для получения предлагаемого гидрофобно-гидрофильного материала природного микроволокнистого биополимера ПГБ придает ему важное качество - возможность интенсивного биоразложения. Диаметр исходных ПГБ волокон колеблется в диапазоне 8-14 мкм.
Катализатор VO(DMSO)5(ClO4)2 (I) был синтезирован нами по методу, описанному в работе: J. Selbin, L.H. Holmes // J. Inorg. and Nucl. Chem., 1962, 24 (9), 1111-1119. Предварительно был исследован механизм реакции полимеризация ГЭМА, катализированной ионным комплексом (I) (Холуйская С.Н., Метлин А.Ю., Самойленко А.А. // Химическая технология. 2016, т. 17, №5, с. 209-215; С.Н. Холуйская, А.А. Гриднев // Химическая физика. 2019, т.38, №4, с. 62-68). Было установлено, что комплекс оксованадия (I) проявляет высокую каталитическую активность в реакции полимеризации ГЭМА в аэробных и анаэробных условиях, отличается высокой селективностью по мономеру. Образующийся ПГЭМА имеет карбоцепную структуру.
Представлялось интересным провести полимеризацию гидрофильного ГЭМА с использованием катализатора VO(DMSO)5(ClO4)2 (I) на поверхности гидрофобного ПГБ с целью получения нового материала, сохраняющего основные свойства природного биополимера, но с модифицированной гидрофильной поверхностью.
Было исследовано влияние условий реакции взаимодействия ПГБ с мономером ГЭМА в присутствии катализатора полимеризации на свойства получаемого материала, что позволило найти оптимальные параметры.
Было установлено, что при уменьшении количества ГЭМА в реакционной смеси ниже заявленного предела уменьшается гидрофильность материала, а при увеличении -наблюдается образование ПГЭМА не только на поверхности волокон ПГБ, но и между волокнами, что приводит к ухудшению биоразлагаемости материала.
Оптимальной температурой полимеризации ГЭМА в присутствии комплекса VO(DMSO)5(ClO4)2 (I) является 75-85°С. Снижение температуры замедляет процесс, а повышение приводит к увеличению низкомолекулярной фракции ПГЭМА (золь-фракции).
Для усиления контакта поверхности волокон ПГБ с ГЭМА взаимодействие осуществляют под небольшим давлением.
Для получения ультратонких волокон ПГБ методом электроформования использовали ПГБ серии 16F, получаемый микробиологическим синтезом компанией "BIOMER®" (Германия). Была использована технология формования волокон из раствора полимера, что позволило получать микроволокна ПГБ средним диаметром 8-14 мкм и повысить удельную поверхность полимера. Использовали раствор ПГБ в хлороформе с добавкой муравьиной кислоты до удельной электропроводности раствора полимера 9-10 мкСм/см. Напряжение электрического поля при электроформовании волокон составляло 12-15 кВ.
Мономер ГЭМА («ФГУП НИИ химии и технологии полимеров им. В.А. Каргина» г. Дзержинск) очищали от примесей дистилляцией в вакууме, отделяя фракцию с температурой кипения 67°С при давлении 3,5 мм рт.ст.
Приводим примеры получения предлагаемого материала.
Пример 1.
1 г нетканого волокнистого материала из волокон ПГБ средним диаметром 8-14 мкм пропитывали 0,6 г ГЭМА, содержащим катализатор VO(DMSO)5(ClO4)2 в концентрации 4,0 мМ, помещали под груз, создающий постоянное давление 15 г/см2, нагревали на воздухе до температуры 75°С и выдерживали 2 ч. Характеристики образца исследовали после предварительного отмывания от растворимой золь-фракции ПГЭМА и остаточного мономера. Для этого выдерживали образец в дистиллированной воде до постоянного веса, затем высушивали в вакууме также до постоянного веса.
Пример 2.
1 г нетканого волокнистого материала из волокон ПГБ средним диаметром 8-14 мкм пропитывали 1,2 г ГЭМА, содержащим катализатор VO(DMSO)5(ClO4)- в концентрации 4,0 мМ, помещали под груз, создающий постоянное давление 17 г/см2, нагревали на воздухе до температуры 85°С и выдерживали 2 ч. Дальнейшую обработку образца проводили аналогично примеру 1.
Пример 3.
1 г нетканого волокнистого материала из волокон ПГБ средним диаметром 8-14 мкм пропитывали 2,2 г ГЭМА, содержащим катализатор VO(DMSO)5(ClO4)2 в концентрации 4,0 мМ, помещали под груз, создающий постоянное давление 17 г/см2, нагревали на воздухе до температуры 80°С и выдерживали 2 ч. Дальнейшую обработку образца проводили аналогично примеру 1.
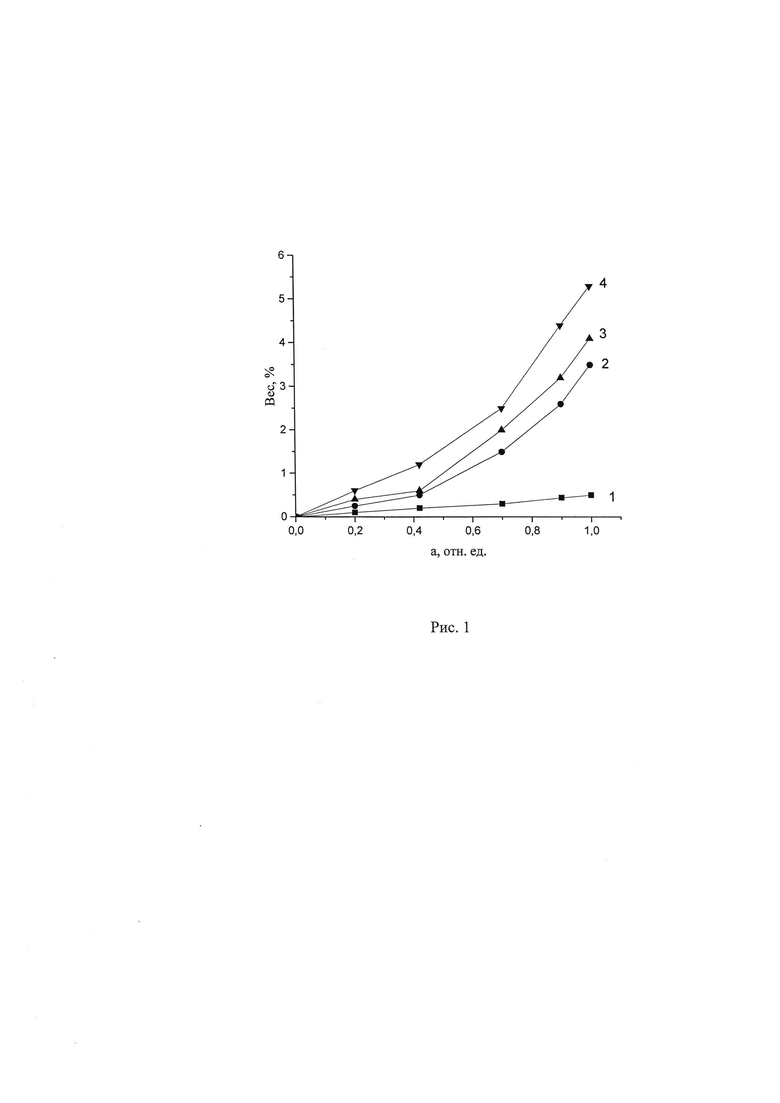
Сорбцию паров воды полученными образцами заявляемого материала (далее обозначен ПГБ-ПГЭМА) и исходным ПГБ для сравнительной оценки их гидрофильности определяли на весах Мак-Бена с кварцевой спиралью по высокочувствительному методу изотермической гравиметрии, описанному в работе: А.Я. Малкин, А.Е. Чалых // Диффузия и вязкость полимеров. Методы измерения. М.: Химия. 1979. 301 с., в интервалах давления паров воды 0-9; 9-14,5; 14,5-18,5 мм рт.ст. Методом интервальной сорбции построены изотермы сорбции паров воды в следующих координатах: активность паров воды (а) - весовой % воды в образце. Активность паров воды определяется как отношение а=Pi/Рнас., где Pi - давление паров воды в колонне с образцом, Рнас. - давление насыщенных паров воды. На рис. 1 приведены полученные изотермы сорбции при температуре 23°С.
Анализ изотерм показывает, что заявляемый материал, полученный при разном массовом соотношении ПГБ : ГЭМА (изотерма 2 - соотношение 1:0,6; изотерма 3 - соотношение 1:1,2; изотерма 4 - соотношение 1:2,2) и исходный ПГБ (изотерма 1) сильно различаются по сорбционной емкости и, соответственно по степени гидрофильности - увеличение у предлагаемого материала в 5-10 раз.
Исследование степени биоразложения предлагаемого материала проводили по ГОСТ 32427 (метод В - определение выделения диоксида углерода). Биодеградацию осуществляли под действием почвенных микроорганизмов по выделению диоксида углерода (метод Штурма). ПГБ является полностью биодеградируемым полимером - в компосте ПГБ разлагается на воду и углекислый газ за 7-10 недель (в зависимости от температуры).
Для получения инокулята (исходная культура почвенных бактерий) готовили почвенный грунт согласно ГОСТ 9.060-75, затем 860 г полученной почвы смешивали с 2 л бидистиллированной воды, процеживали через сито с размером ячеек 0,5 мм, далее жидкую часть сепарировали на лабораторной центрифуге в течение 5 минут при скорости вращения 1500 об/мин, после чего отбирали жидкую фракцию (суспензию) и трижды отфильтровывали через фильтровальную бумагу. Получившийся почвенный концентрат разбавляли бидистилированной водой до объема 9 л и разливали в круглодонные колбы по 500 мл. Колбы с инокулятом без образцов барботировали очищенным от углекислого газа воздухом в течение 3 суток. Жизнеспособность бактерий в инокуляте анализировали с помощью оптического микроскопа Micromed Polar 3 ToupCam 5.1 MP (КНР) при увеличении 400×. Исследование образцов заявляемого материала и исходного ПГБ на биоразложение проводили в течение 60 дней. Анализ накопления углекислого газа проводился с интервалом 2-4 суток. В качестве абсорбента использовался 0,0125 М раствор Ва(ОН)2. Количество выделившегося углекислого газа оценивалось титрованием 0,05 М раствором HCl при помощи комплекта для автоматического титрования «Титрион» (ООО "Эконикс-Эксперт", Россия).
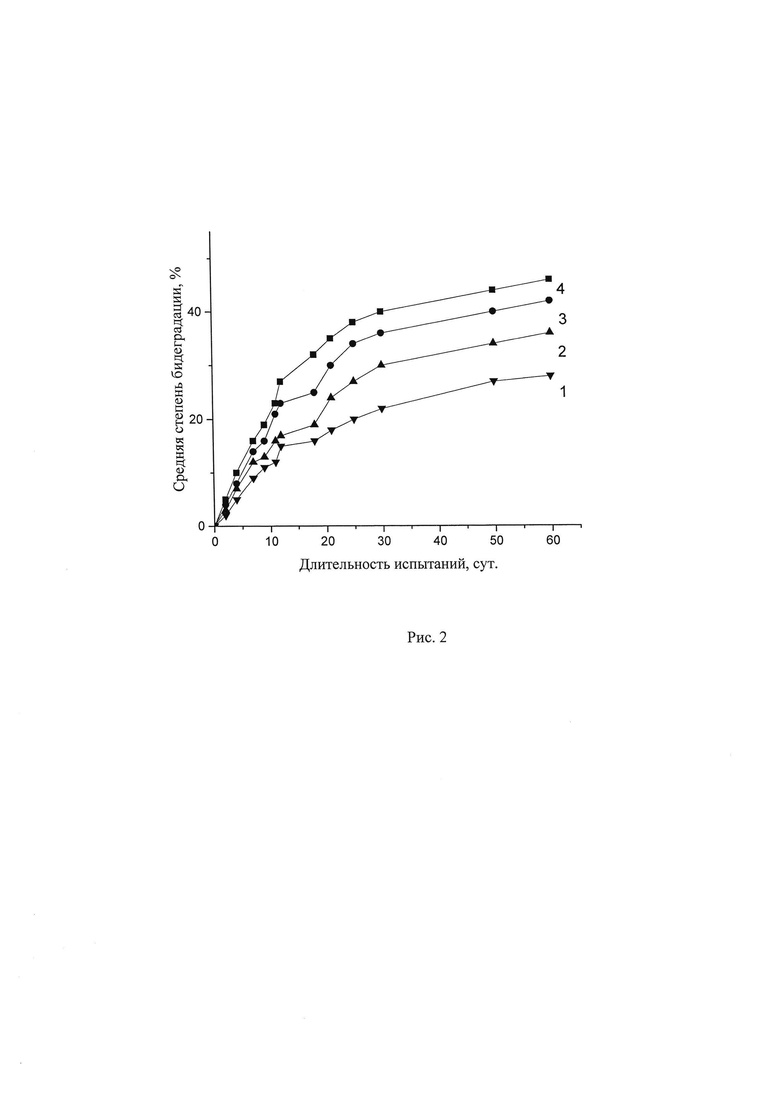
На рис. 2 приведены полученные кинетические данные биодеградации образцов предлагаемого материала и исходного ПГБ под действием почвенных микроорганизмов по выделению диоксида углерода: кривая 4 - ПГБ; кривые 1, 2, 3 - материал ПГБ-ПГЭМА, полученный при различном массовом соотношении ПГБ : ГЭМА (кривая 3 - соотношение 1: 0,6; кривая 2 - соотношение 1:1,2; кривая 1 - соотношение 1:2,2). Как видно из рис. 2, при низком содержании ПГЭМА в предлагаемом материале кривая биоразложения очень близка к данным для исходного ПГБ, увеличение содержания ПГЭМА замедляет процесс биоразложения, но он продолжается до полного разложения волокон ПГБ. Здесь можно отметить важность того, что заявляемый материал, как и исходный ПГБ, имеют микроволокнистую структуру, что обеспечивает высокую скорость биодеградации.
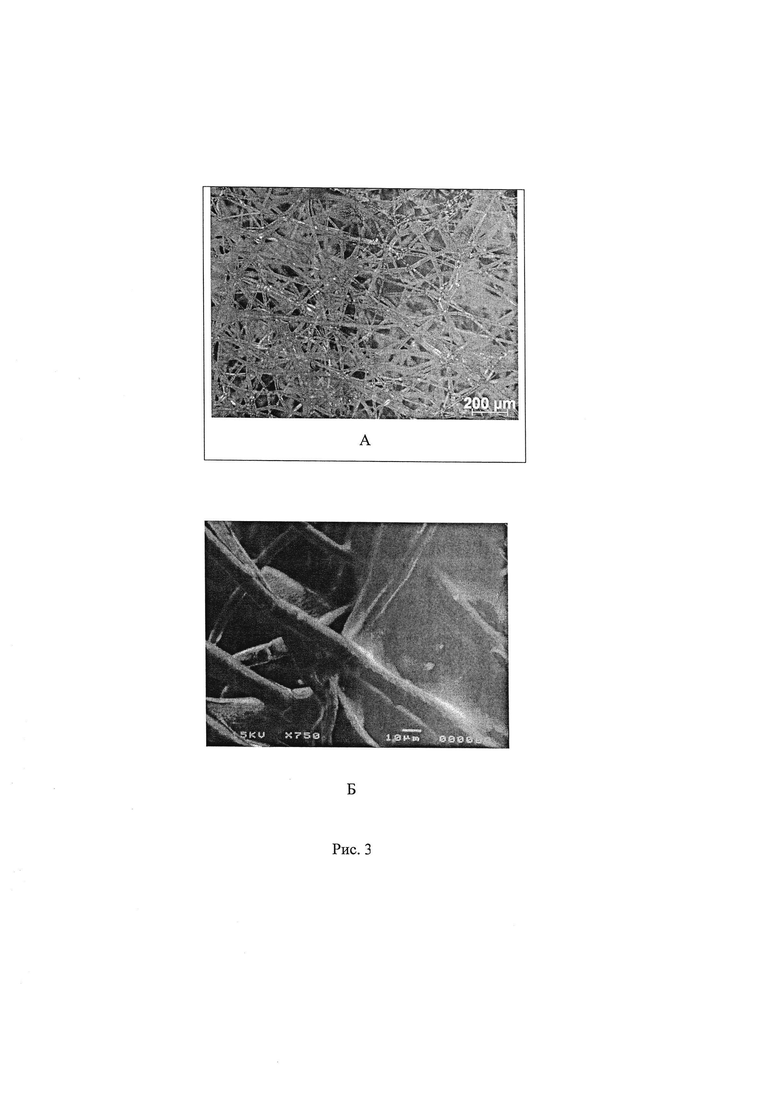
Структуру и морфологию полученного микроволокнистого материала исследовали методами оптической (в отраженном свете) и сканирующей электронной микроскопии (СЭМ). Использовали поляризационный микроскоп Микромед Полар-3 (Россия) и сканирующий электронный микроскоп JEOL JSM-T330A (Япония) при ускоряющем напряжении 10-15 кВ (предварительно на образцы напыляли тонкий слой золота (~10 нм) на установке вакуумного напыления JEOL JFC-1500).
На рис. 3 представлены микрофотографии образца ПГБ-ПГЭМА, полученного по примеру 3 (соотношение ПГБ : ГЭМА = 1:2,2): А - оптическая микроскопия, Б - сканирующая электронная микроскопия. Четко видимая фактура микроволокнистого материала позволяет сделать вывод о достаточно равномерном покрытии ПГЭМА поверхности исходных ПГБ волокон. По данным микроскопического анализа средняя толщина слоя ПГЭМА на волокнах ПГБ варьируется в диапазоне 0,5-1 мкм. Наблюдаются также пленочные структуры (спайки) из ПГЭМА в межволоконном пространстве, скрепляющие отдельные волокна. Диаметр волокон полученного образца ПГБ-ПГЭМА колеблется в диапазоне 9-16 мкм.
Для оценки степени адгезии слоя ПГЭМА к поверхности волокон ПГБ полученные образцы материала ПГБ-ПГЭМА выдерживали 1 час в дистиллированной воде при комнатной температуре с последующей сушкой и изучением морфологии методом СЭМ - морфологических изменений по сравнению с необработанными образцами не обнаружено, что свидетельствует о высокой адгезии слоя ПГЭМА к поверхности волокон ПГБ.
Хороший адгезионный контакт между ПГБ и ПГЭМА обеспечивают полярные функциональные группы, присутствующие в основной цепи обоих полимеров и формирующие межмолекулярные физические связи между ними. Кроме того, не исключается химическое взаимодействие ГЭМА и ПГЭМА с ПГБ, который, как уже упоминалось выше, содержит реакционноспособные концевые карбоксильные группы.
Проверка гипотезы о химической модификации ПГБ в результате взаимодействия с ГЭМА и ПГЭМА осуществлялась методом спектроскопии ЯМР. Образец ПГБ-ПГЭМА, полученный по примеру 3, обработали последовательно двумя дейтерированными растворителями: метанолом CD3OD для извлечения низкомолекулярных продуктов и хлороформом CDCl3, чтобы выявить признаки трансформации ПГБ, который растворим в хлороформе. В 1Н спектре раствора CD3OD помимо сигналов остаточного мономера ГЭМА с характерными сдвигами обнаружены сигналы протонов гидроксильных групп (-ОН) с химическим сдвигом δ=3,03 ppm и метиленовых протонов (-СН2) с δ=3,61 ppm, относящихся к этиленгликолю. Контрольный эксперимент с добавкой этиленгликоля показал возрастание интенсивности указанных сигналов. Аналогично наблюдалось увеличение сигнала протонов воды по сравнению с водой исходного CD3OD.
Комплекс VO(DMSO)5(ClO4)2 (I), используемый для полимеризации ГЭМА, является сильной кислотой Льюиса и способен эффективно катализировать как реакцию переэтерификации ГЭМА с участием концевых карбоксильных групп ПГБ по схеме 1, так и реакцию этерификации карбоксильных терминальных групп ПГБ с участием гидроксильных групп ГЭМА или ПГЭМА по схеме 2:
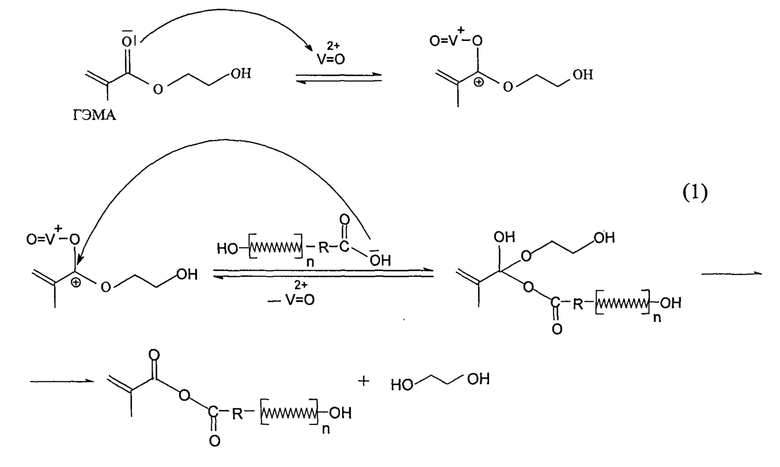
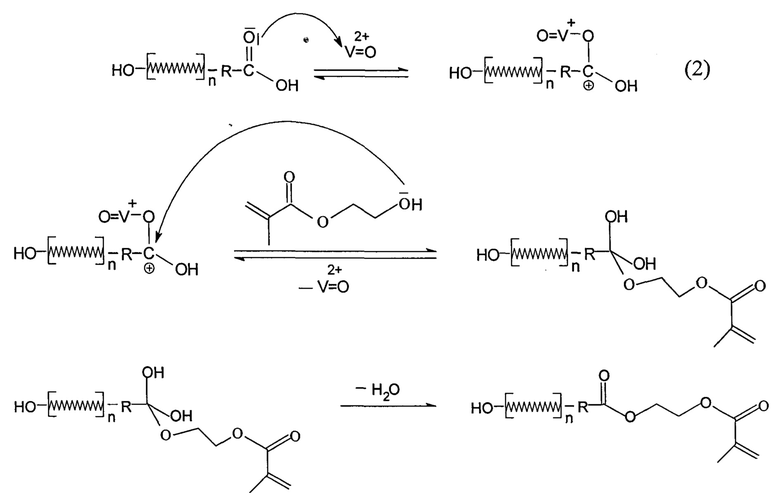
Таким образом, разработан биодеградируемый материал на основе ПГБ с гидрофобно-гидрофильными свойствами; способ его получения отличается простотой и обеспечивает материалу требуемые свойства. Предлагаемый материал обладает гидрофильностью, в несколько раз превышающей гидрофильность исходного ПГБ, и одновременно он сохраняет высокую способность к биоразложению.
| название | год | авторы | номер документа |
|---|---|---|---|
| Биодеградируемый сорбирующий материал для сбора нефти и нефтепродуктов и способ его получения | 2019 |
|
RU2714079C1 |
| БИОРАЗЛАГАЕМЫЕ ФЛЕКСОГРАФИЧЕСКИЕ ЧЕРНИЛА И СПОСОБ ИХ ПРИГОТОВЛЕНИЯ | 2003 |
|
RU2398806C2 |
| Материал "Вторая кожа" | 2022 |
|
RU2836691C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕЛЯ, КОМПОЗИЦИЯ ВОДНОГО ГЕЛЯ И СПОСОБ ИЗМЕНЕНИЯ ЕГО ФИЗИЧЕСКИХ ХАРАКТЕРИСТИК | 2002 |
|
RU2300541C2 |
| Способ улучшения эксплуатационных свойств нетканого волокнистого материала | 2021 |
|
RU2760862C1 |
| Биоразлагаемый композиционный нетканый материал на основе полилактида и его применение для выращивания растений | 2019 |
|
RU2734883C1 |
| Способ повышения регенерационного потенциала имплантируемого материала для восстановительной хирургии (варианты) | 2019 |
|
RU2721880C1 |
| ТЕРМИЧЕСКИ ИНДУЦИРОВАННАЯ ПРИВИВКА НЕТКАНЫХ МАТЕРИАЛОВ ДЛЯ ВЫСОКОЭФФЕКТИВНОГО ИОНООБМЕННОГО РАЗДЕЛЕНИЯ | 2017 |
|
RU2715660C1 |
| СЕЛЕКТИВНОЕ ОТДЕЛЕНИЕ НИТРОЗОСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2012 |
|
RU2622410C2 |
| СМЕСИ ПОЛИМОЛОЧНОЙ КИСЛОТЫ И РАСТВОРИМОГО В ВОДЕ ПОЛИМЕРА | 2012 |
|
RU2561103C2 |
Изобретение относится к области биоразлагаемых и биосовместимых полимерных материалов, обладающих гидрофобно-гидрофильными свойствами, и может быть использовано в медицине и косметологии. Микроволокнистый биодеградируемый материал с гидрофобно-гидрофильными свойствами на основе микроволокнистого поли-3-гидроксибутирата (ПГБ), полученный взаимодействием ПГБ с 2-гидроксиэтилметакрилатом (ГЭМА) при массовом соотношении ПГБ : ГЭМА, равном 1:0.6-2.2, в присутствии ионно-координационного катализатора полимеризации VO(DMSO)5(ClO4)2 при температуре 75-85°С, сохраняет способность волокон ПГБ к полному биоразложению и характеризуется сорбционной емкостью к водяному пару не менее 3%. Диаметр волокон материала не превышает 16 мкм. Материал обладает гидрофильностью, в несколько раз превышающей гидрофильность исходного ПГБ, и одновременно он сохраняет высокую способность к биоразложению. Способ получения материала отличается простотой и обеспечивает требуемые свойства. 2 з.п. ф-лы, 3 ил., 3 пр.
1. Микроволокнистый биодеградируемый материал с гидрофобно-гидрофильными свойствами на основе микроволокнистого поли-3-гидроксибутирата (ПГБ), полученный взаимодействием ПГБ с 2-гидроксиэтилметакрилатом (ГЭМА) при массовом соотношении ПГБ : ГЭМА, равном 1:0.6-2.2, в присутствии ионно-координационного катализатора полимеризации VO(DMSO)5(ClO4)2 при температуре 75-85°С, сохраняющий способность волокон ПГБ к полному биоразложению и характеризующийся сорбционной емкостью к водяному пару не менее 3%.
2. Микроволокнистый биодеградируемый материал по п. 1, отличающийся тем, что диаметр волокон не превышает 16 мкм.
3. Микроволокнистый биодеградируемый материал по п. 1, отличающийся тем, что взаимодействие поли-3-гидроксибутирата с 2-гидроксиэтилметакрилатом осуществляют под давлением 15-17 г/см2.
| "Hydrogels in Medicine and Pharmacy: Fundamentals", Ed | |||
| N.A | |||
| Peppas, CRS Press, 2019, v | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| H-K.Lao, E | |||
| Renard, I linossier, V | |||
| Langlois, K | |||
| Vallee-Rehel// J | |||
| Appl | |||
| Polym | |||
| Sci., 2010, 116 (1), 288-97 | |||
| M | |||
| Yalpani, Marchessault, F.G.Morin, C.J | |||
| Monasterios//Macromolecules, 1991, 24, 6046-49 | |||
| Ультраволокнистый биополимерный материал с бактерицидным эффектом | 2017 |
|
RU2681319C1 |
| RU 20566863 С1, | |||
Авторы
Даты
2021-06-04—Публикация
2020-11-23—Подача