Изобретение для коррекции гипогонадизма, возникающего при остром повреждении спинного мозга на животных, относится к области экспериментальной медицины, а именно к андрологии, урологии, эндокринологии, неврологии и нейрохирургии. Этот способ лечения в дальнейшем может быть использован в терапии гипогонадизма, возникающего при остром повреждении спинного мозга различного генеза, с целью коррекции нарушенной продукции тестостерона и уменьшения степени атрофии семенников.
Заболевания, последствием которых становится острое повреждение спинного мозга, в том числе спинальный инсульт, приводят к значительным нарушениям функции мужской половой системы: развивается атрофия семенников, нарушается сперматогенез, снижается продукция тестостерона, развивается гипогонадизм (Fortune R.D. Changes in gene expression and metabolism in the testes of the rat following spinal cord injury // J. Neurotrauma. 2006. DOI: 10/1089/neu.2016.4641).
Разработка способов увеличения концентрации тестостерона, уменьшения атрофии семенников и, следовательно, улучшения процесса сперматогенеза, является перспективным направлением современной медицинской науки, так как сохранение мужской фертильности необходимо для планирования семьи и формирования здорового населения. Решение проблемы мужского бесплодия является одним из нереализованных резервов повышения рождаемости, что имеет большое социально-экономическое значение для современной России с ее крайне неблагоприятными демографическими показателями (G.R. Dohle, Т. Diemer, A. Giwercman, А. Jungwirth, Z. Кора, С. Krausz, Мужское бесплодие. Европейская ассоциация урологов 2011 г http://www.volgmed.ru/uploads/files/2013-3/17470-muzhskoj_besplodie_2011.pdf).
Первичный гипогонадизм корректируется пожизненным приемом гормон-заместительной терапии. На сегодняшний день на рынке представлен довольно широкий выбор препаратов тестостерона, а именно андриол, метилтестостерон, эфиры тестостерона для парентеральной терапии (тестостерона пропионат, Омнадрен-250, Сустанон-250) и трансдермальный препарат Андрогель.
Метилтестостерон является алкилированным соединением тестостерона, в настоящее время широко не применяется в связи с гепатотоксичностью и необходимостью многократного приема.
Андриол - препарат тестостерона ундеканоата, применяемым перорально. Недостатками препарата являются его относительно слабое андрогенное действие и необходимость многократного приема.
Препараты эфиров тестостерона для парентеральной терапии (Сустанон-250 и Омнадрен-250) наиболее распространены, так как их состав (комбинация различных эфиров тестостерона с разными периодами полураспада) позволяет добиться быстрого и продолжительного андроген-заместительного эффекта.
Недостатком этих препаратов является непостоянная концентрация тестостерона в крови: от супрафизиологических пиков в первые дни до снижения уровня гормона ниже нормы через некоторое время.
Андрогель - это гель, содержащий тестостерон, который наносится непосредственно на кожу ежедневно.
Среди побочных эффектов андроген-заместительной терапии следует отметить гепатотоксичность, иммуносупрессию, повышение артериального давления и уровня холестерина, нарушение работы сердца, образование угрей вследствие стимуляции кожных сальных желез, увеличение массы тела и возникновение гинекомастии (в результате ароматизации тестостерона в эстрогены).
Передозировка андрогенов может также вызывать задержку натрия и воды, что приводит к отекам. Все препараты тестостерона подавляют сперматогенез, что ведет к тяжелым нарушениям репродуктивной функции и бесплодию (Роживанов Р.В. (2014) Синдром гипогонадизма у мужчин DOI: 10.14341/ОМЕТ2014230-34).
Ближайшим аналогом предлагаемого способа коррекции является использование препаратов, действующими веществами которых являются лютеинизирующий (ЛГ) и фолликулостимулирующий гормоны (ФСГ), а также хорионический гонадотропин, который может взаимодействовать с рецепторами лютеинизирующего и фолликулостимулирующего гормонов.
Гонадтропин хорионический - гликопротеин, гормон плаценты, который включает в себя две субъединицы α и β. Хорионический гонадотропин взаимодействует со специфическими рецепторами, активирует систему аденилатциклазы и воспроизводит эффекты лютеинизирующего гормона. У мужчин стимулирует работу клеток Лейдига, увеличивает образование и выработку тестостерона, стимулирует сперматогенез, развитие вторичных половых признаков и опускание яичек в мошонку.
Препараты имеют ряд серьезных побочных эффектов: увеличение яичек в паховом канале, преждевременное половое созревание, атрофия семенных канальцев, дегенерация половых желез; увеличение молочных желез, образование антител (при продолжительном использовании); ангионевротический отек, диспноэ, головная боль, беспокойство, раздражительность, утомляемость, депрессия, слабость, угревая сыпь (https://www.rlsnet.ru/mnn_index_id_2387.htm).
Все перечисленные аналоги, в том числе ближайший, косвенно защищают способы их использования и имеют недостатки традиционной гормон-заместительной терапии.
Задачи:
1. Обеспечить коррекцию гипогонадизма, а именно дефицита тестостерона и атрофии семенников, на животных при моделировании острого повреждения спинного мозга
2. Исключить побочные эффекты традиционной гормон-заместительной терапии
Сущность способа коррекции гипогонадизма является однократное ежедневное внутривенное введение 0,5% водного раствора D-аспарагина в курсовой дозе 21,7 мг/кг с 3 по 5 сутки от развития заболевания, приведшего к острому повреждению спинного мозга.
D-аспарагин представляюет собой белый кристаллический порошок без запаха, хорошо растворимый в воде, химическое название - правовращающий изомер моноамида аспарагиновой кислоты.
Препарат получают путем растворения 0,5 г сухого порошка D-аспарагина в 99,5 г высокоочищенной воды.
Технический результат: способ позволяет нормализовать уровень тестостерона и уменьшить степень выраженности атрофии семенников, возникающей при повреждении спинного мозга. D-аспарагиновая кислота опосредованно через вторичные мессенджеры (цГМФ в гипофизе и цАМФ в семенниках) стимулирует высвобождение соматотропина, лютеинизирующего гормона и тестостерона (Торо Е. The role and molecular mechanism of D-aspartic acid in the release and synthesis of LH and testosterone in humans and rats // Reproductive Biology and Endocrinology. 2009. 7:120. DOI: 10.1186/1477-7827-7-120). Лютеинезирующий гормон в свою очередь стимулирует работу клеток Лейдига, которые синтезируют тестостерон, так же сама D-аспарагиновая кислота повышает уровень тестостерона, действуя на клетки Лейдига, что в перспективе создает условия для восстановления половой функции и сперматогенеза. Показано, что применение D-аспарагина препятствует развитию глиозной трансформации после острого повреждения спинного мозга у крыс, что в перспективе может оказаться полезным при лечении данной категории пациентов (Chitanava Т. The Influence of D-Asparagine on the Glial Cicatrix Formation in Experimental Spinal Stroke. American Journal of Clinical and Experimental Medicine. Vol. 5. №3. 2017. pp. 93-96. doi: 10.11648/j.ajcem.20170503.15).
Эксперименты проведены на 60 белых нелинейных самцах крыс средней массой 350±75 гр. Характеристика групп животных: группа №1 (интактные) - из 20 крыс, которых использовали в качестве контроля; группа №2 (сравнения) - из 20 крыс которым воспроизводили фокальный фототромбоз грудного отдела спинного мозга с последующим забором крови на 17 сутки; группа №3 (опытная) - из 20 животных, которым выполняли моделирование спинального инсульта с последующим введением D-аспарагина на 3-й сутки в течение 3 дней, с последующим забором крови и семенников на 17 сутки. D-аспарагин у крыс из группы №3 применяли внутривенно в виде 0,5% раствора, приготовленного на воде для инъекций.
Моделирование спинального инсульта проводили по модифицированной методике М. Von Euler, путем фототромбоза сосудов грудного отдела спинного мозга лазером с длиной волны 514 нм. Для операции применяли золетил-ксилазиновый наркоз. В качестве фотосенсибилизатора использован эритрозин, для ингибирования фибринолиза применяли транексамовую кислоту (Von Euler М. Morphological characterization of the evolving rat spinal cord injury after photochemically induced ischemia // Acta Neuropathol. - 1997 Sep; 94(3). - P. 232-239).
В плазме крови исследуемых животных определяли уровень общего тестостерона методом иммуноферментного анализа (ИФА) с помощью набора «Ray Biotech, Inc.» (Германия). ИФА проводили на фотометре вертикального сканирования «ANTHOS 2010» (Австрия) с помощью программного обеспечения «Auswerte-Softwere anthos labtec», версия 2.3.0.7.
После извлечения семенники помещали в цинк-формалиновый фиксатор с сульфатом цинка (Kierman J.A. Histological and histochemical methods. Theory and practice. - London: Scion Publishing Ltd. - 2008. - 606 p.). Выполняли проводку полученных образцов через изопропанол-минеральное масло, с последующей их заливкой в парафин. Парафиновые блоки нарезали на срезы толщиной 10 мкм на микротоме МПС-2 (СССР). Окрашивание микропрепаратов проводили гематоксилином и эозином. Для фотографии микропрепаратов использовали микроскоп Микмед-5 (Россия) и окулярную камеру Levenhuk-230 (США). Для анализа фотографий микропрепаратов применяли программу ImageJ (инструменты откалиброваны с помощью объект микрометра), с ее помощью определяли численность клеток по слоям сперматогенного эпителия (на 3 мкм2), толщину сперматогенного эпителия (в мкм) и площадь семенных канальцев (в мкм2).
Статистическую обработку полученных данных проводили с использованием программного обеспечения «Statistica 10 version» фирмы «Stat Soft Inc.». Полученные результаты исследуемых групп после статистической обработки выражали в виде медианы (Me) с использованием 25 и 75 процентилей (р25 и р75). Для проверки гипотезы о гауссовом распределении показателей в исследуемых группах использовали критерий Шапиро-Уилка. В связи с тем, что распределение значений исследуемых показателей в группах отличалось от нормального, их сравнение проводилось по непараметрическому критерию Манна-Уитни (U test), с установлением уровня значимости *p≤0,05.
При исследовании плазмы крови крыс из группы №1 (интактные) концентрация общего тестостерона составила 3,31 нг/мл. В плазме крови животных из группы №2 (без D-аспарагина) на 17 сутки после моделирования спинального инсульта уровень общего тестостерона составил 0,154 нг/мл., что статистически достоверно (p≤0,05) в 21,5 раз ниже контроля. В плазме крови животных из группы №3 получавших 0,5% водный раствор D-аспарагина с 3 по 5 сутки эксперимента в виде внутривенных инъекций, на 17 сутки после моделирования спинального инсульта уровень общего тестостерона составил 0,627 нг/мл., что статистически достоверно (p≤0,05) в 5,3 раза ниже контроля. Таким образом, в плазме крови самцов крыс группы №3, которые получали D-аспарагин с 3 по 5 сутки от начала экспериментального инсульта, к 17 суткам концентрация общего тестостерона составила 0,627 нг/мл, что статистически достоверно (p≤0,05) в 4 раза выше, чем в группе №2 (без D-аспарагина).
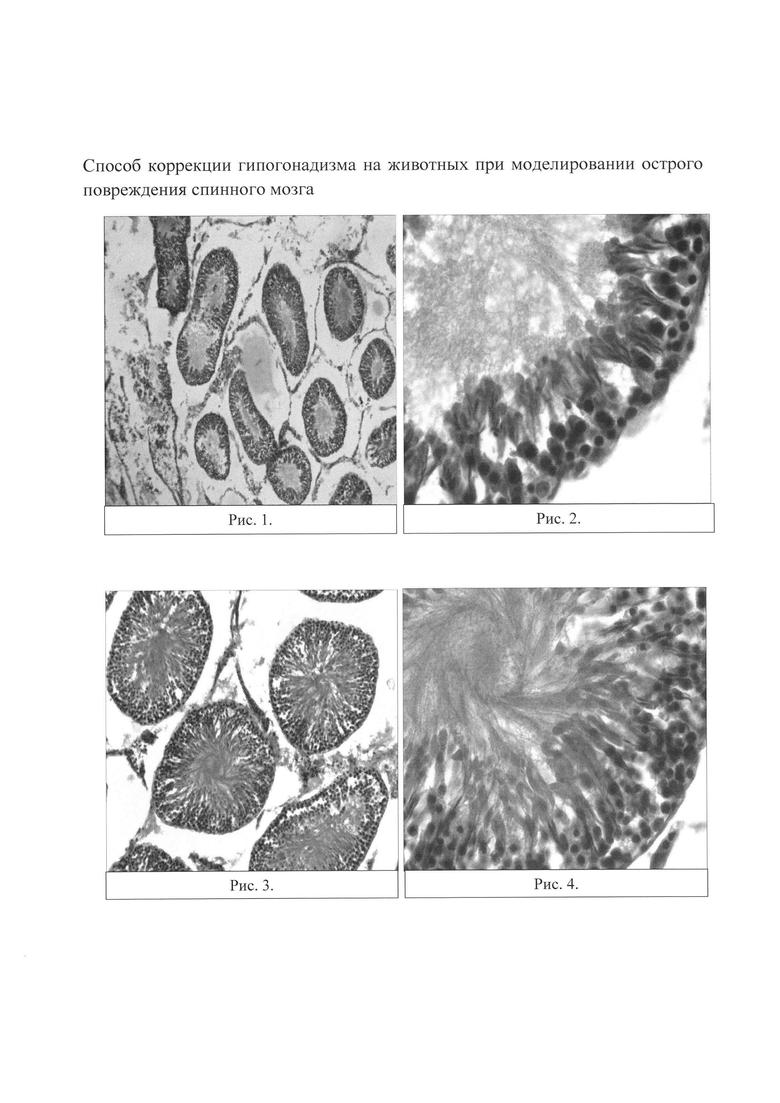
На микропрепаратах семенников, полученных от крыс из группы №2 (без применения D-аспарагина) видна выраженная атрофия семенных канальцев, диффузный асперматогенез, разрушение стенки семенных канальцев, выраженная атрофия сперматогенного эпителия (см. фото 1 при увеличении Х4, фото 2, при увеличении Х40).
На микропрепаратах семенников, полученных от крыс из группы №3 (с применением D-аспарагина) в сравнении с микропрепаратами из группы №2 (без применения D-аспарагина), прослеживается наличие единичных семенных канальцев с признаками легкой атрофии, отмечаются признаки умеренного нарушения сперматогенеза, стенки семенных канальцев грубых дефектов не имеют, видны единичные семенные канальцы с признаками атрофии сперматогенного эпителия (см. рисунок 3, при увеличении X10, 4, при увеличении Х40).
Пример 1. Нелинейный самец крысы, массой 265 гр. был прооперирован. Выполнено моделирование фототромбоза сосудов грудного отдела спинного мозга лазером с длиной волны 514 нм. Для операции применяли золетил-ксилазиновый наркоз. С 3 по 5 день после операции, вводили 0,5% раствор D-аспарагина внутривенно в вены хвоста. Эвтаназия была проведена на 17 сутки, после чего производили забор крови, для определения в плазме крови исследуемых животных уровня общего тестостерона методом иммуноферментного анализа (ИФА) с помощью набора «Ray Biotech, Inc.» (Германия). ИФА проводили на фотометре вертикального сканирования «ANTHOS 2010» (Австрия) с помощью программного обеспечения «Auswerte-Softwere anthos labtec», версия 2.3.0.7. Также проводили забор семенников для гистологического анализа. Затем, выполнили проводку образца через изопропанол-минеральное масло, окрасили полученный микропрепарат, сфотографировали с помощью камеры Levenhuk-230 (США) и провели статистическую обработку полученных результатов с помощью программы «Statistica 10 version». В результате проведенного иммуноферментного анализа концентрация общего тестостерона в плазме крови составила 0,627 нг/мл. Результаты эксперимента подтверждены фото 3-4, где на фото 3 видны семенные канальцы без атрофии, отсутствуют признаки асперматогенеза, стенки семенных канальцев не имеют выраженных дефектов, под увеличением в X10 (окраска гематоксилином эозином). На фото 4 не наблюдается признаков выраженной атрофии сперматогенного эпителия, под увеличением Х40 (окраска гематоксилином эозином). Также у самца крысы не было выявлено побочных эффектов гормон-заместительной терапии (угревой сыпи, гинекомастии, увеличения массы тела, слабости и утомляемости).
Таким образом, применение 0,5% водного раствора D-аспарагина в виде внутривенных инъекций в курсовой дозе 21,7 мг/кг в период с 3 по 5 сутки от начала экспериментального спинального инсульта у крыс приводит к 4-х кратному нарастанию концентрации общего тестостерона к 17 суткам от начала эксперимента, а также сопровождается значительно меньшей выраженностью процессов атрофии семенных канальцев, разрушения их стенок, нарушений сперматогенеза и атрофии сперматогенного эпителия, в сравнении с крысами не получавших D-аспарагин.
| название | год | авторы | номер документа |
|---|---|---|---|
| Препарат для предотвращения образования глиальных рубцов | 2017 |
|
RU2651756C1 |
| Гидрогель для коррекции посттрепанационного дефекта черепа | 2017 |
|
RU2666595C1 |
| Гидрогель для замещения дефектов биологических тканей | 2017 |
|
RU2643922C1 |
| СПОСОБ СТИМУЛЯЦИИ СПЕРМАТОГЕННОЙ И АНДРОГЕНПРОДУЦИРУЮЩЕЙ ФУНКЦИИ МУЖСКИХ ПОЛОВЫХ ЖЕЛЕЗ | 1991 |
|
RU2040258C1 |
| Средство для профилактики образования патологических кожных рубцов | 2018 |
|
RU2691647C1 |
| Способ профилактики пролиферативной витриоретинопатии, развивающейся при отслойке сетчатки в эксперименте на крысах | 2018 |
|
RU2689324C1 |
| Композиция для профилактики и лечения воспалительных заболеваний полости рта | 2019 |
|
RU2716501C1 |
| Способ моделирования гипогонадизма, вызванного метаболическими нарушениями | 2016 |
|
RU2611936C1 |
| ФИКСАТОР ПРОБ ДЛЯ ЦИТОЛОГИЧЕСКИХ ИССЛЕДОВАНИЙ | 2016 |
|
RU2630983C1 |
| Способ лечения подросткового гипогонадотропного гипогонадизма в эксперименте | 2020 |
|
RU2750713C1 |
Изобретение относится к экспериментальной медицине и может быть использовано для коррекции гипогонадизма у животных при моделировании острого повреждения спинного мозга. Для этого животному внутривенно однократно ежедневно вводят в курсовой дозе 21,7 мг/кг водный раствор 0,5%-ного препарата D-аспарагина с 3 по 5 сутки от начала моделирования острого повреждения спинного мозга. Изобретение позволяет увеличить концентрацию тестостерона и уменьшить степень атрофии семенников. 4 ил., 1 пр.
Способ коррекции гипогонадизма у животных при моделировании острого повреждения спинного мозга, включающий использование медикаментов, отличающийся тем, что животному внутривенно однократно ежедневно вводят в курсовой дозе 21,7 мг/кг водный раствор 0,5%-ного препарата D-аспарагина с 3 по 5 сутки от начала моделирования острого повреждения спинного мозга.
| CHITANAVA T | |||
| et al | |||
| The Influence of D-Asparagine on the Glial Cicatrix Formation in Experimental Spinal Stroke | |||
| American Journal of Clinical and Experimental Medicine | |||
| Vol | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| СПОСОБ СТИМУЛЯЦИИ СПЕРМАТОГЕННОЙ И АНДРОГЕНПРОДУЦИРУЮЩЕЙ ФУНКЦИИ МУЖСКИХ ПОЛОВЫХ ЖЕЛЕЗ | 1991 |
|
RU2040258C1 |
| US 8202908 B1,19.06.2012 | |||
| D'Aniello A | |||
| et al | |||
| Involvement of D-aspartic acid in the synthesis of testosterone in rat testes //Life sciences | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| - Т | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| - N | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - С | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Topo E | |||
| et al | |||
| The role and molecular mechanism of D-aspartic acid in the release and synthesis of LH and testosterone in humans and rats //Reproductive Biology and Endocrinology | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| - Т | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| - N | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - С | |||
| Кровля из глиняных обожженных плит с арматурой из проволочной сетки | 1921 |
|
SU120A1 |
Авторы
Даты
2019-05-24—Публикация
2017-11-10—Подача