Изобретение относится к биотехнологии и фармакологии и представляет собой конъюгаты рекомбинантного человеческого гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) с алендроновой кислотой, представителем бифосфонатов, имеющие повышенное сродство к клеткам-мишеням костного мозга.
Природный человеческий гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) является важнейшим регуляторным фактором, обеспечивающим рост, созревание и функциональную активность многих клеток крови, в том числе гранулоцитов и макрофагов.
Лекарственные препараты на основе GM-CSF используют в качестве стимуляторов кроветворения у больных нейтропенией, онкологических больных, при пересадках костного мозга, органов и тканей. Однако их клиническое применение затруднено токсичностью препарата [Steward W.P., Scarffel J.H., Austin R., Bonnem E., Thatcher N., Morgenstern G., Crowther D. Recombinant human granulocyte macrophage colony stimulating factor (rhGM-CSF) given as daily short infusions-a phase I dose-toxicity study // Br.J. Cancer. 1989. V. 59. P. 142-145]. Можно предположить, что создание адресного средства доставки GM-CSF в костный мозг позволит снизить эффективную дозу препарата и повысить эффективность терапии.
Использование таргетных средств доставки иммунорегуляторных лигандов, таких как белки-цитокины, актуально и хорошо описано в литературе [Lee J.H., Nan A. Combination drug delivery approaches in metastatic breast cancer // Journal of drug delivery. 2012. Vol.2012:915375; Кособокова E.H., Косоруков B.C. Получение гибридных белков на основе антител и цитокинов с целью изучения возможности таргетной доставки противоопухолевых препаратов // Сборник трудов конференции «XXVIII зимняя молодежная научная школа «Перспективные направления физико-химической биологии и биотехнологии», Москва 08-11 февраля 2016, С. 14.]. Описаны методы ковалентного присоединения молекул цитокинов к различным носителям (монометоксиполиэтиленгликоль, полиглюкин, поливинилпирролидон, дивиниловый эфир) [Kamada Н., Tsutsumi Y., Yamamoto Y., Kihira Т., Kaneda Y., Yu Mu, Kodaira H., Tsunoda Shin-ichi, Nakagawa S. Antitumor Activity of Tumor Necrosis Factor-a Conjugated with Polyvinylpyrrolidone on Solid Tumors in Mice // Cancer Research. 2000. Vol. 60. Issue 22. P. 6416-6420; Шмелёв В.А. Интерферон-гамма, фактор некроза опухолей, тимозин-альфа1-противоинфекционные и противоопухолевые цитокины и препараты. М.: Медпрактика, 2008.].
В литературных источниках встречаются примеры получения конъюгатов гранулоцитарного колониестимулирующего фактора (Г-КСФ) с полиэтиленгликолем (ПЭГ). Показано, что ПЭГилирование Г-КСФ приводило к улучшению его фармакокинетики: увеличению времени полувыведения, уменьшению клиренса и диапазона колебаний концентрации в крови, снижению иммуногенности и токсичности, повышению активности in vivo, увеличению стабильности [Патент РФ №2446173 опубл. 27.03.2012 г. ]. В указанном патенте представлен функционально активный, высокоочищенный стабильный конъюгат гранулоцитарного колониестимулирующего фактора (Г-КСФ) с полиэтиленгликолем с пролонгированным биологическим действием пригодным для медицинского применения, на основе которого получено иммунобиологическое средство. В данном патенте описано получение конъюгатов ПЭГ-Г-КСФ с использованием активированного монометоксиполиэтиленгликоля (мПЭГ) с молекулярной массой 4500-30000 Да, в частности мПЭГ-сукцинимидил бутаноата, мПЭГ-сукцинимидил пропионата, мПЭГ-сукцинимидил а-метилбутаноата. Полученные конъюгаты ПЭГ-Г-КСФ обладали пролонгированным действием, их удельная специфическая активность составляла от 11 до 60% от активности немодифицированного Г-КСФ.
В качестве векторной молекулы может быть использован бифосфонат алендроновая кислота (ALN), одним из свойств которой является повышенное сродство к костному матриксу и массированное накопление в нем [Farrell KB, Karpeisky A, Thamm DH, Zinnen S. Bisphosphonate conjugation for bone specific drug targeting // Bone Reports. 2018. Vol.9. PP. 47-607; Большакова С.Ф., Бычков Ю.М. Современные подходы в лечении метастазов в кости рака молочной железы: от бисфосфонатов к таргетной терапии // Вестник Российского научного центра рентгенрадиологии Минздрава России. 2016. Т. 16, С. 1-28; Даниленко Е.Д., Белкина А.О. Использование бисфосфонатов в качестве средств доставки лекарственных препаратов // Биофармацевтический журнал. 2014. Т. 6 (6). С. 44-53.]. Описано получение конъюгатов фактора некроза опухоли альфа (ФНО-альфа) с алендроновой кислотой, приводящее к повышению сродства цитокина к костной ткани при сохранении его биологической активности [Патент РФ №2631486 Способ получения противоопухолевого средства против метастазов костей в виде конъюгата белка-цитокина и аминобисфосфоната / Даниленко Е.Д., Закабунин А.И., Волосникова Е.А., Левагина Г.М., Гамалей С.Г., Титов Г.Г., опубл. 22.09.2017 г.].
Данных, описывающих получение конъюгатов GM-CSF и бифосфонатов, в научной и патентной литературе не найдено.
В качестве прототипа настоящего изобретения выбран конъюгат ФНО-альфа с алендроновой кислотой, описанный в [Патент РФ №2631486 Способ получения противоопухолевого средства против метастазов костей в виде конъюгата белка-цитокина и аминобисфосфоната / Даниленко Е.Д., Закабунин А.И., Волосникова Е.А., Левагина Г.М., Гамалей С.Г., Титов Г.Г., опубл. 22.09.2017 г. ], который наиболее близок по технологии получения таргетного средства и его составу. В качестве аминобисфосфоната средство содержит алендроновую кислоту, а алендроновая кислота и фактор некроза опухоли альфа человека связаны между собой через спейсерный участок (Y) в виде моноаддукта, имеющего высокое сродство к гидрокси л апатиту. В патенте описана схема получения конъюгатов ФНО-альфа с ALN, показана их биологическая активность и способность к накоплению в костном матриксе.
Техническим результатом заявляемого изобретения является создание гемостимулирующего таргетного средства на основе конъюгата GM-CSF и алендроновой кислоты со свойствами векторной молекулы, направленной к клеткам-мишеням костного мозга.
Указанный технический результат достигается тем, что согласно изобретения, таргетное колониестимулирующее средство представляет собой конъюгат белка гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) с алендроновой кислотой, связанных между собой по карбоксигруппе белка в виде моноаддукта, имеющего высокое сродство к гидроксилапатиту, полученного реакцией в присутствии водорастворимого сшивающего агента 1-этил-3-[3-диметиламинопропил] карбодиимида (EDC) и имеющего следующую структуру:
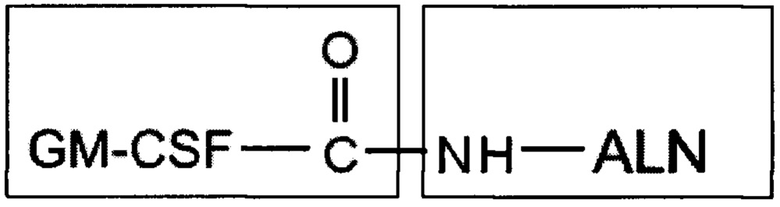
где: ALN - алендроновая кислота;
GM-CSF - гранулоцитарно-макрофагальный колониестимулирующий фактор.
Причем, конъюгат GM-CSF с алендроновой кислотой получен при стехиометрическом соотношении на 1 моль GM-CSF- 1 моль алендроновой кислоты, сохраняет высокую специфическую активность, близкую к нативному белку, и имеет повышенное сродство к аналогу основного минерального компонента костной ткани - гидроксилапатиту (НАР).
Выбор алендроната среди аминобисфосфосфонатов связан с его высокой активностью и умеренно выраженными побочными эффектами. Алендроновая кислота (4-амино-1-гидроксибутилиден)-дифосфоновая кислота) - бифосфонат, в котором заместитель R1 представляет собой гидроксильную группу, а боковой радикал R2 содержит первичную аминогруппу (-CH2CH2CH2NH2), представленную на фиг. 1. Алендроновая кислота имеет формулу (C4H12NNaO7P2) и М.м. 325.1.
Первичная аминогруппа в структуре ALN облегчает проведение реакции ковалентного связывания с молекулой GM-CSF. Присоединение ALN через ее аминогруппу к GM-CSF производится через карбоксильную группу белка с использованием в качестве водорастворимого сшивающего агента 1-этил-3-[3-диметиламинопропил] карбодиимида (EDC).
Из приведенных данных (табл. 1) видно, что полученный конъюгат GM-CSF и ALN обладает более высоким сродством к гидроксилапатиту по сравнению с GM-CSF. Биологическая активность после модификации белка остается на высоком уровне.
Действие конъюгатов GM-CSF с ALN, полученных в стехиометрическом отношении 1:1 в реакциях с использованием водорастворимого карбодиимида EDC, предполагается следующим образом.
После введения в организм конъюгата GM-CSF с ALN GM-CSF может накапливаться в костной ткани в высоких концентрациях и взаимодействовать непосредственно с клетками-мишенями костного мозга.
Полученные конъюгаты характеризовали по чистоте продукта, определенной методом гель-электрофореза в денатурирующих условиях; сохранению специфической биологической активности in vitro по уровню стимуляции пролиферации цитокин-зависимых клеток эритролейкоза человека TF-1; по эффективности связывания с НАР - аналогом основного минерального компонента костей (по увеличению ионной силы раствора, необходимой для элюции конъюгата в сравнении с интактным GM-CSF); способности к накоплению в костной ткани и костном мозге мышей; уровню специфической гемостимулирующей активности, определенной на модели цитостатической миелосупрессии у мышей.
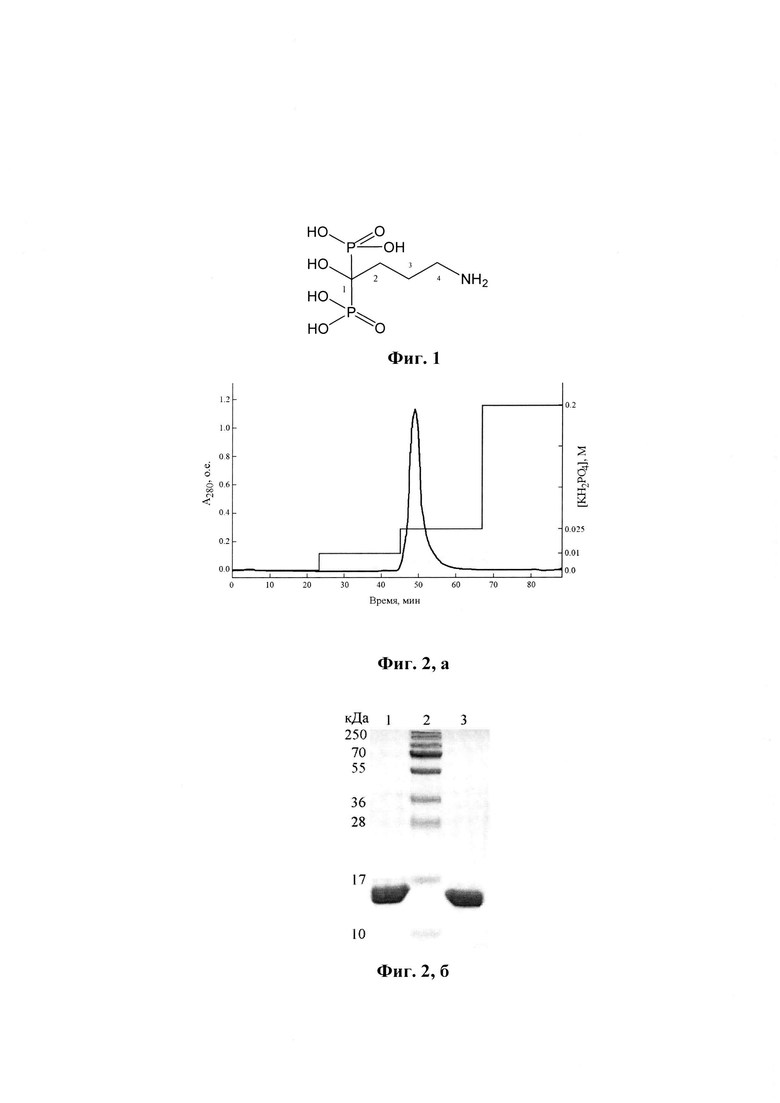
Изобретение поясняется следующими графическими материалами. На фиг. 1. изображена структура алендроновой кислоты. На фиг. 2, а представлен профиль элюции конъюгата GM-CSF с ALN на колонке с НАР. На фиг. 2, б - электрофореграмма образца конъюгата в 15% полиакриламидном геле (ПААГ) в восстанавливающих условиях, окрашивание Кумасси R-250. На фиг. 3, а приведена кривая десорбции с НАР свободного GM-CSF; на фиг. 3, б - кривая десорбции с НАР GM-CSF в составе конъюгата, полученного с помощью EDC. На фиг. 4 приведены данные по количеству лейкоцитов (А), сегментоядерных нейтрофилов (Б) в периферической крови, кариоцитов (В) в костном мозге мышей линии СВА на фоне введения циклофосфана (ЦФ), препарата GM-CSF и его коньюгата с ALN. На фиг. 5 представлена динамика изменения содержания GM-CSF в бедренных костях (а), костном мозге (б) и сыворотке крови (в) мышей после однократного внутривенного введения конъюгата GM-CSF с ALN и свободного GM-CSF.
Сущность изобретения поясняется, но не ограничивается, следующими примерами 1-6.
Пример 1. Конъюгат GM-CSF с алендроновой кислотой получают в результате химической реакции по карбоксигруппе белка в присутствии водорастворимого 1-этил-3-[3-диметиламинопропил] карбодиимида (EDC), схема реакции приведена ниже.
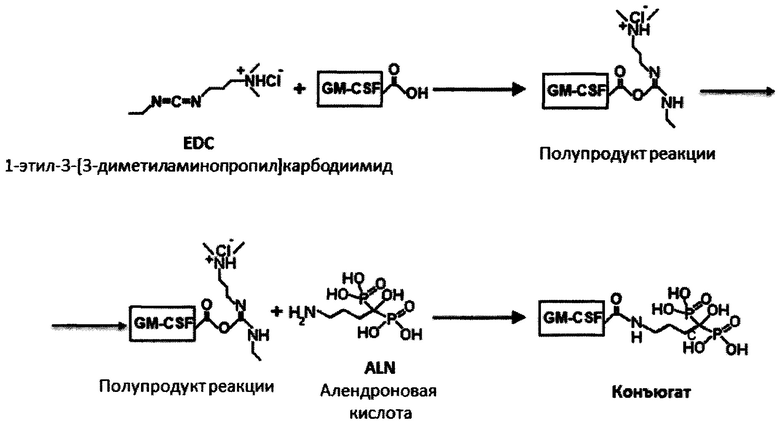
Конечный продукт представляет собой конъюгат гранулоцитарно-макрофагального колониестимулирующего фактора с алендроновой кислотой при соотношении на 1 моль GM-CSF - 1 моль алендроновой кислоты.
Эквимолярные количества GM-CSF и ALN при проведении реакции конъюгации были использованы для минимизации конформационных изменений, которые могут пагубно влиять на связывание GM-CSF с рецепторами и его биологическую активность.
Пример 2. В качестве твердой фазы для конъюгирования был использован гидроксиапатит (НАР) в связи с высокой степенью сродства к этому сорбенту как GM-CSF, так и ALN.
При проведении синтеза колонку с НАР уравновешивали 2 мМ калий-фосфатным буфером, рН 7.0. Раствор GM-CSF наносили на колонку со скоростью потока 0.5 мл/мин. После нанесения колонку промывали 2 мМ калий-фосфатным буфером, рН 7.0, в объеме, соответствующем 1/3 объема колонки, и перекрывали выход раствора из колонки на 2 часа для сорбции GM-CSF на НАР. Сорбент промывали 2 мМ калий-фосфатным буфером, рН 7.0, в объеме, соответствующем 1 объему колонки, затем на колонку наносили раствор сшивающего агента (1-этил-3-[3-диметиламинопропил] карбодиимида EDC) с последующей промывкой тем же буфером в объеме, соответствующем 1/3 объема колонки (0,5 мл/мин). Выход раствора из колонки перекрывали на 2 часа для проведения реакции конъюгирования, после чего на колонку наносили раствор ALN с последующей промывкой 2 мМ калий-фосфатным буфером в объеме, соответствующем 1 объему колонки. Длительность реакции на этой стадии составляла 2 часа. Элюцию конъюгата проводили 0,2 М калий-фосфатным буфером (фиг. 2, а, б). На фиг. 2, а приведен профиль элюции конъюгата GM-CSF с ALN, на колонке с НАР (а), на оси ординат: оптическое поглощение раствора при 280 нм, о.е. (левая ось), молярность элюирующего буфера, М (справа); на оси абсцисс - время элюции, мин. На фиг. 2, б представлена электрофореграмма образца конъюгата после электрофореза в 15% ПААГ в восстанавливающих условиях, окрашивание Кумасси R-250. Конъюгат GM-CSF с ALN, 20 мкг/лунка (1); белковый маркер 10-250 кДа (2); контроль, GM-CSF, 20 мкг/лунка (3).
Полученный раствор конъюгата стерильно разливали и замораживали при минус 20°С.
Молекулярный вес полученного конъюгата определяли электрофорезом в 15% ПААГ в восстанавливающих условиях, окрашивание Кумасси R-250 (фиг. 2, б).
По результатам электрофореза, молекулярная масса конъюгата составляет 15,4 кДа и идентична молекулярной массе нативного белка GM-CSF.
Пример 3. Биологическую активность GM-CSF в конъюгатах оценивали in vitro по уровню стимуляции пролиферации цитокин-зависимых клеток эритролейкоза человека TF-1. Данный тест основан на способности клеток линии TF-1 пролиферировать в присутствии GM-CSF. Пролиферативную активность определяли микрометодом на 96-луночных культуральных планшетах с использованием реагента (2,3-бис-(2-метокси-4-нитро-5-сульфо-фенил)-2Н-тетразолий-5-карбоксанилид) (ХТТ). Метод основан на способности митохондриальных дегидрогеназ конвертировать водорастворимый ХТТ в формазан, который кристаллизуется внутри клетки. Перевод формазана в раствор с помощью феназин-метасульфата (PMS) и последующая фотометрия позволяют точно соотнести изменение оптической плотности раствора с изменением количества жизнеспособных клеток.
Для калибровки активности GM-CSF в исследуемых образцах использовали очищенный и охарактеризованный препарат рекомбинантного GM-CSF, полученный в клетках E. coli [Топоркова Л.Б., Орловская И.А., Сенников С.В., Сахно Л.В., Козлова Ю.Н., Лебедев Л.Р., Гилева И.П. Изучение in vitro биологических свойств рекомбинантного гранулоцитарно-макрофагального колониестимулирующего фактора // Иммунология. 2009. №4. С. 203-205.]. Для проведения эксперимента в среде RPMI (Invitrogen) с добавлением 10% эмбриональной телячьей сыворотки готовили 2-кратные разведения исследуемого и контрольного препаратов в диапазоне 8 нг/мл - 0,25 нг/мл. В качестве контроля использовали среду RPMI (Invitrogen) с добавлением 10% эмбриональной телячьей сыворотки (HyClone). В лунки 96-ти луночного планшета вносили 50 мкл вышеуказанных разведений образцов и добавляли 50 мкл суспензии клеток TF-1 в среде RPMI с 10% эмбриональной телячьей сывороткой по 104 клеток/лунка. Планшеты помещали в термостат при температуре 37°С, 5% CO2, влажности 85% и инкубировали 72 часа. После инкубации в каждую тестируемую лунку добавляли 50 мкл реагента ХТТ (Sigma) и PMS (Fluka), который получали добавлением к рабочему раствору с содержанием ХТТ 1 мг/мл раствора PMS 1,25 мМ из расчета: на каждый мл ХТТ - 20 мкл PMS. Планшет инкубировали еще 4 часа и определяли оптическую плотность ОП490/620 на планшетном спектрофотометре SpectraCount (Packard). Каждую точку делали в пяти повторностях, определяли среднее значение и дисперсию для различных концентраций GM-CSF, строили гистограмму зависимости ОП от разведений и концентрации. Стимуляцию пролиферации TF-1 клеток рассчитывали в процентах по отношению к контролю; за 100%) принимали количество живых клеток в отрицательном контроле. Для оценки биологической активности препаратов рассчитывали 50% эффективную дозу (ED50, нг/мл), равную концентрации GM-CSF, при которой стимуляция пролиферации в 2 раза превышает пролиферацию контрольной культуры клеток. Все расчеты проводили с использованием программного обеспечения Lab View.
Определение биологической активности конъюгата GM-CSF и ALN показало, что белок в составе конъюгата с ALN сохранял способность к стимуляции пролиферации клеток эритролейкоза человека TF-1: ЕД50 как конъюгата, так и исходного GM-CSF составляла 0,28 нг/мл.
Пример 4. Изучение накопления конъюгатов GM-CSF и ALN на модели костного матрикса в условиях in vitro проводили методом хроматографии на НАР, как описано в [Скоупс P. // Методы очистки белков. М.: Мир, 1985.]. Десорбцию проводили линейным градиентом соли 0.01- 0.2 М калий фосфатный буфер, рН 7.0.
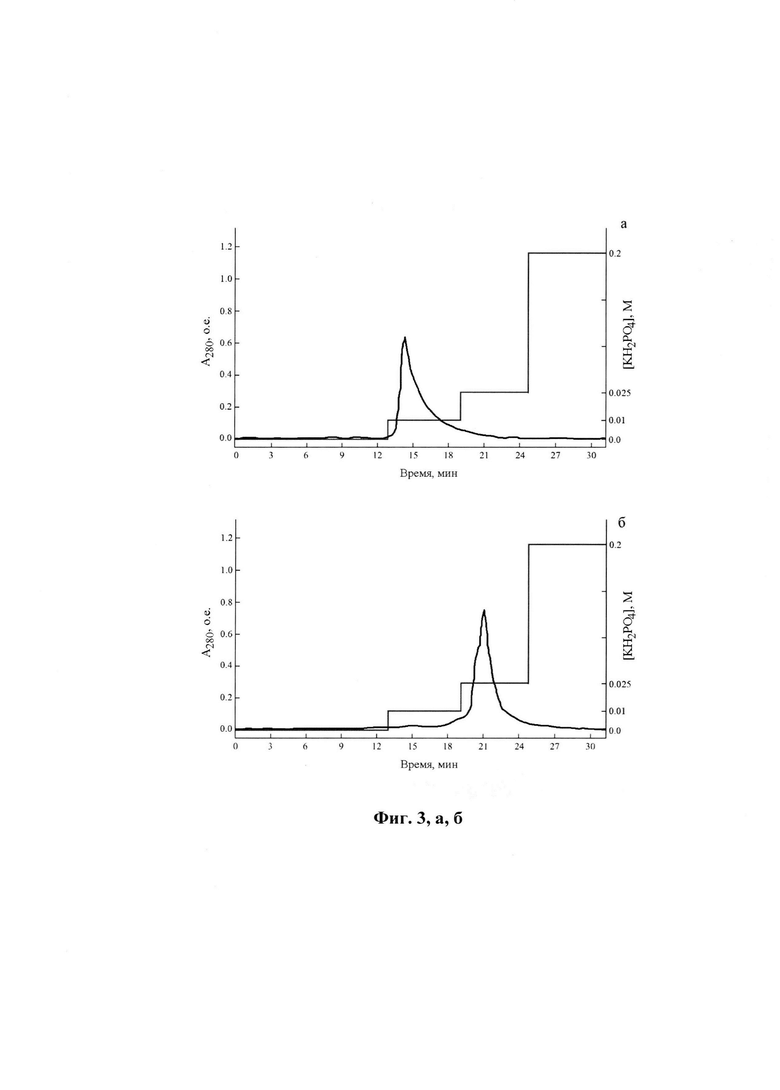
Связывание полученных конъюгатов - не менее 1 мг/мл смолы, конъюгат элюируется 0.025 М калий-фосфатом и не содержит интактного GM-CSF (фиг. 3, а, б). На фиг. 3, а - приведена кривая десорбции с НАР свободного GM-CSF. На фиг. 3, б представлена кривая десорбции с НАР GM-CSF в составе конъюгата, полученного с помощью EDC. На оси ординат: оптическое поглощение раствора при 280 нм, о.е. (левая ось), молярность элюирующего буфера, М (справа); на оси абсцисс - время элюции, мин. Как видно на фиг. 3, для десорбции белка в составе конъюгата требуется буфер с концентрацией фосфата калия в 2,5 раза более высокой, чем для исходного GM-CSF (0.025 и 0.01 М, соответственно), что свидетельствует о повышенном сродстве конъюгата к гидроксиапатиту в сравнении с исходным белком.
Пример 5. Исследование накопления конъюгата GM-CSF в костной ткани и костном мозге мышей проводили на самках аутбредных мышей CD-1 (ICR). Препараты вводили однократно внутривенно в дозе 90 мкг/кг. Животные опытной группы получали инъекции конъюгата GM-CSF с ALN, мышам группы сравнения вводили препарат GM-CSF. Контрольными животными служили интактные мыши. Спустя 3 мин, 1, 4 и 24 ч после введения препаратов у животных забирали на анализ образцы крови и бедренной кости. В сыворотке крови, гомогенатах кости и костного мозга определяли содержание GM-CSF иммуноферментным методом с применением наборов реагентов для определения ГМ-КСФ человека в сыворотке, плазме крови, супернатантах культур клеток и гомогенатов органов «Human Granulocyte-Macrophage Colony Stimulating Factor (GM-CSF) ELISA Kit», «CUSABIO», КНР.
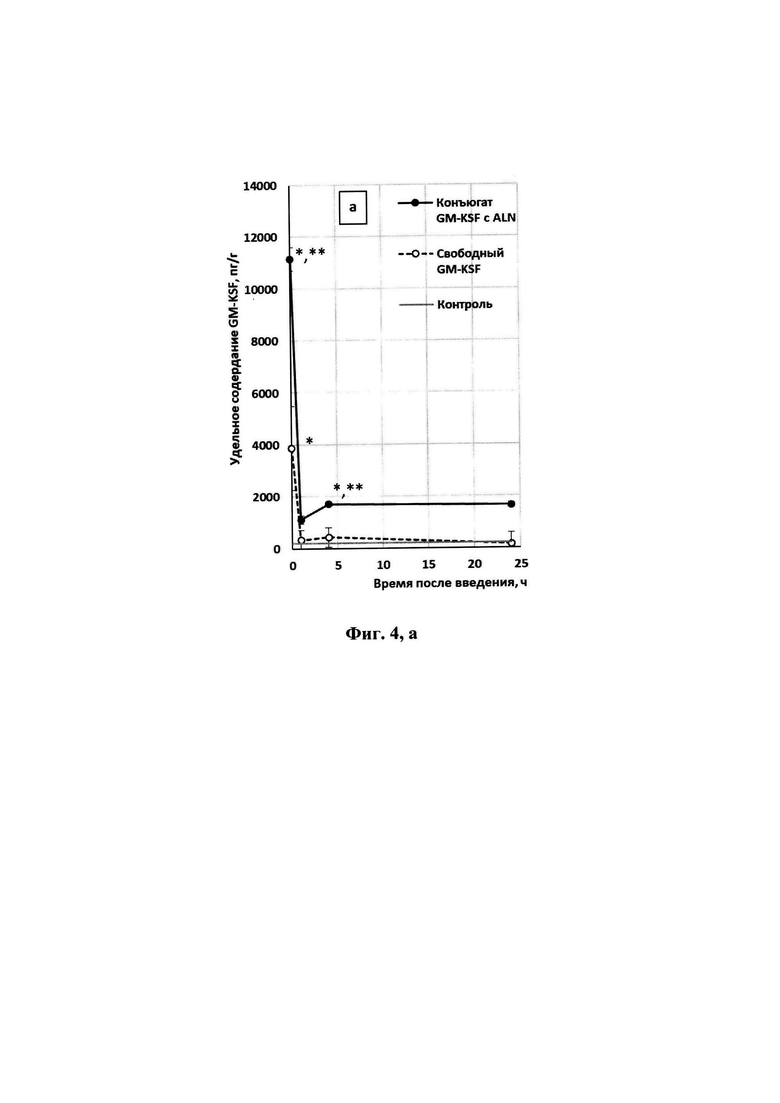
Динамика изменения концентрации GM-CSF в крови, костной ткани и костном мозге мышей после однократного внутривенного введения конъюгата GM-CSF или GM-CSF представлена на фиг. 4.
Наибольший уровень GM-CSF в гомогенатах бедренных костей мышей наблюдался через 3 мин после введения препаратов (фиг. 4а). Содержание белка в костной ткани животных, которым вводили препарат сравнения, через 1 ч после введения снижалось до уровня контроля (интактные мыши). Концентрация белка в костях мышей, получавших конъюгат GM-CSF, на протяжении всего срока наблюдения была выше, чем в группе сравнения и контроле (в 2,9 раза через 3 мин; в 12 раз через 3-24 ч).
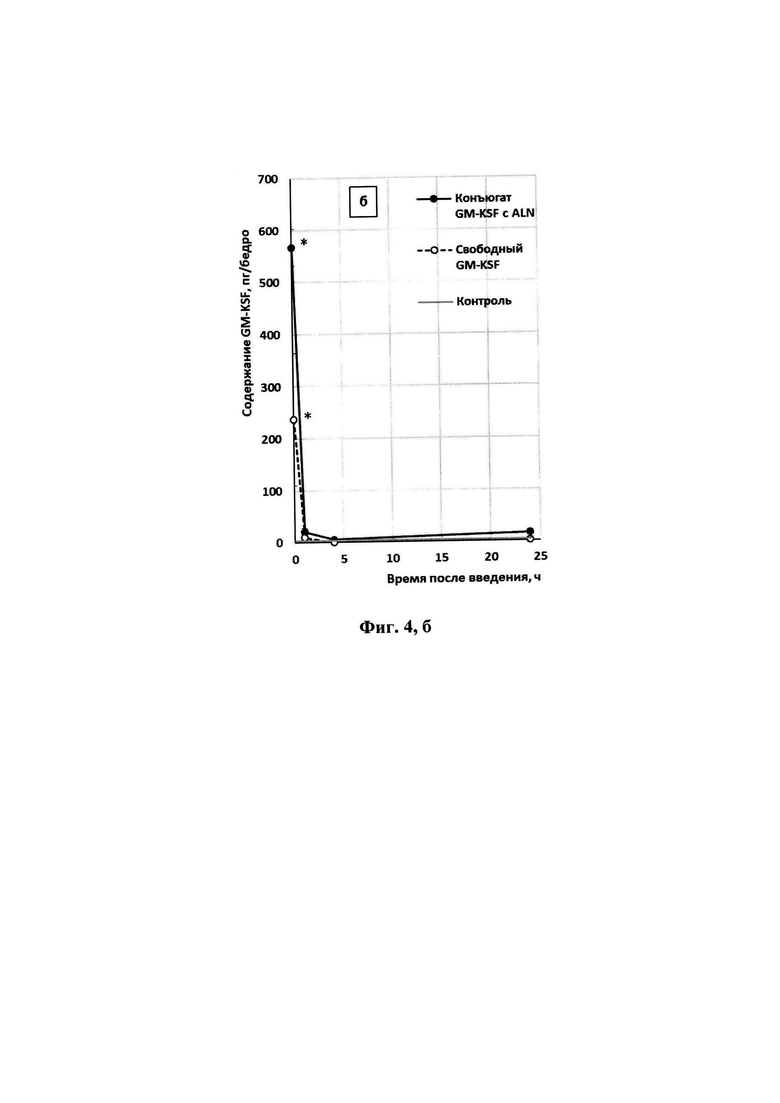
Максимальные значения концентрации GM-CSF в костном мозге мышей, так же, как в гомогенатах бедренных костей, регистрировали через 3 минуты после введения препаратов (фиг. 4б). Содержание белка после введения конъюгата GM-CSF в этот срок в 2,4 раза превышало показатель группы сравнения и в 161 раз - контрольные значения. В последующие сроки уровень белка в опытной группе и группе сравнения не отличался от контрольного.
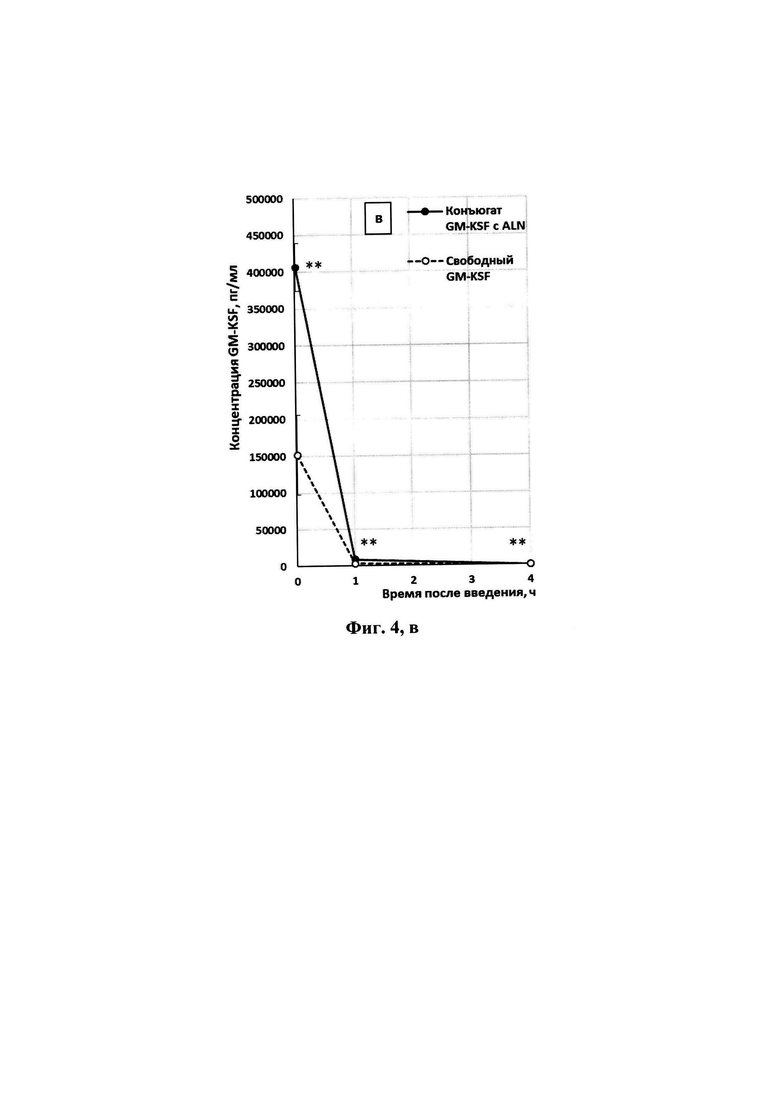
Максимальные значения GM-CSF крови, зарегистрированные через 3 мин после введения препаратов, составляли 19,2% от введенной дозы в группе мышей, получавших конъюгат GM-CSF, и 7,2% - у мышей после введения GM-CSF (фиг. 4в). На протяжении 4 часов наблюдения концентрация белка в крови мышей опытной группы статистически значимо превышала показатель группы сравнения (в 2,7 раза через 3 мин и 1 ч, в 2 раза - через 4 ч). Через 24 часа после введения уровень показателя в сыворотке крови животных, получивших инъекцию конъюгата GM-CSF, в 3,9 раза превышал его значение в группе сравнения. Значения показателя контрольных животных ни в один из сроков наблюдения не отличались от нуля.
Полученные данные свидетельствуют о том, что конъюгат GM-CSF с ALN обладает повышенной способностью к проникновению в костный мозг и костную ткань, а также более длительно циркулирует в крови мышей, по сравнению с исходным GM-CSF. На фиг. 4 приведена динамика изменения содержания GM-CSF в бедренных костях (а), костном мозге (б) и сыворотке крови (в) мышей после однократного внутривенного введения конъюгата GM-CSF с ALN и GM-CSF. (*) - отличия статистически значимы, по сравнению с контролем; (**) - отличия статистически значимы, по сравнению с препаратом GM-CSF (р<0,0170 при сравнении показателя в тканях; р<0,05 при сравнении в сыворотке крови).
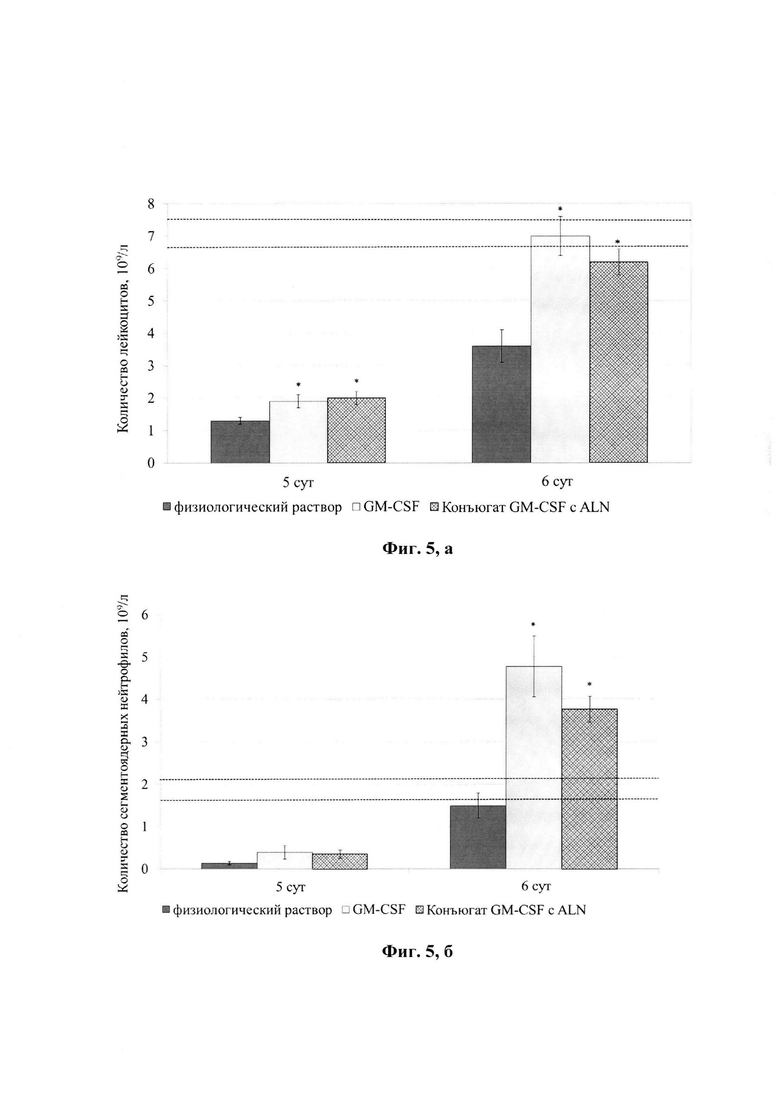
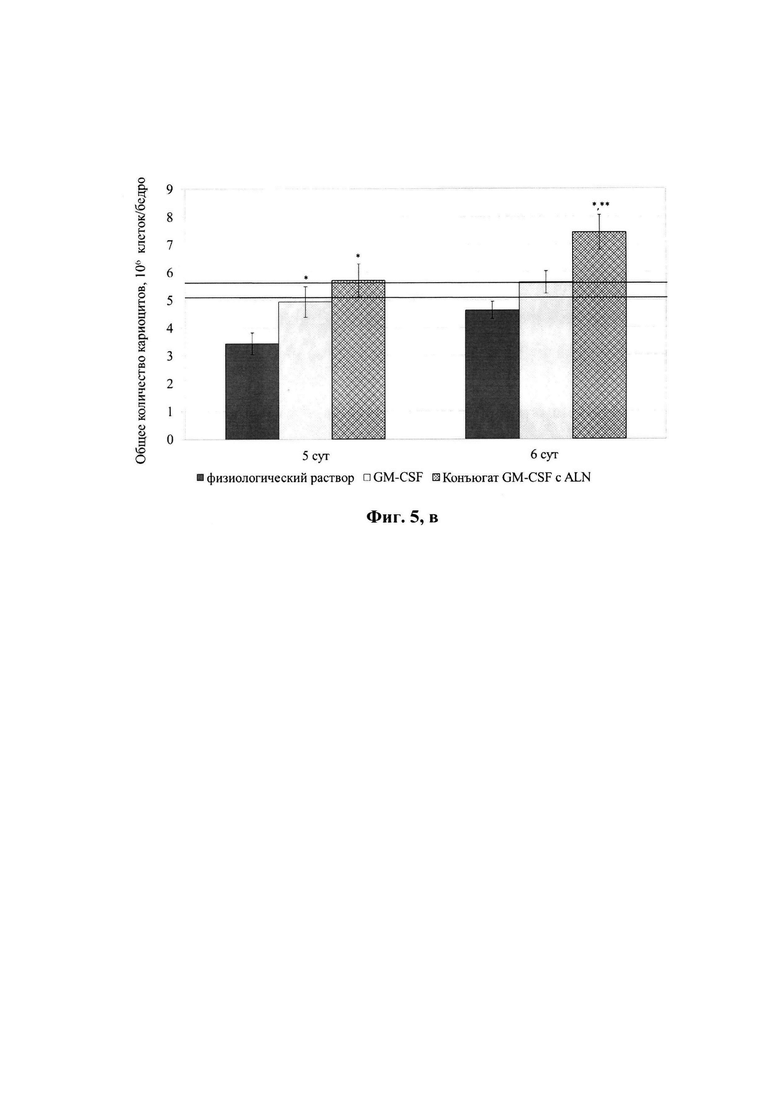
Пример 6. На модели цитостатической миелосупрессии у мышей проведена оценка гемостимулирующей активности конъюгатов GM-CSF с ALN и GM-CSF. Исследование проводили на здоровых мышах линии CBA/Calac с массой тела 19-23 г. Животным всех экспериментальных групп вводили раствор ЦФ однократно внутрибрюшинно в дозе 250 мг/кг. Через 24 ч после инъекции мышам опытных групп подкожно в течение 4 или 5 суток вводили GM-CSF или конъюгат GM-CSF с ALN. Доза препаратов составляла 90 мкг/кг, объем 0,2 мл на 20 г массы тела. Мыши контрольной группы получали подкожно физиологический раствор в эквивалентном объеме и по аналогичной схеме. В каждой экспериментальной группе было по 6-7 мышей. В качестве дополнительной контрольной группы использовали интактных животных (без введения препаратов и ЦФ). На 5 и 6-е сутки после введения ЦФ у животных забирали на анализ образцы периферической крови и после эвтаназии - образцы костного мозга. В крови определяли общее количество лейкоцитов, рассчитывали лейкограмму, в образцах костного мозга -общее число кариоцитов.
Полученные результаты обрабатывали с помощью пакета программ «Statgraphics, Vers.5.0» «Statistical Graphics Corp.», США. В связи с малыми объемами выборок для оценки значимости межгрупповых различий применяли непараметрические критерии - двухвыборочный U-критерий Манна-Уитни и Н-критерий множественных сравнений Краскела-Уоллиса с критическим уровнем статистической значимости (р), равным 0,05. При обнаружении статистически значимых различий в Н-тесте проводили апостериорные сравнения с помощью U-критерия, при этом скорректированный критический уровень значимости (р) для трех попарных сравнений принимали равным 0,0170 (при Р=95%) [Гржибовский A.M. Одномерный анализ повторных измерений // Экология человека. 2008. №4. С. 51-60].
Оценка гемостимулирующей активности препаратов, проведенная на мышах с цитостатической миелосупрессией, показала, что конъюгат GM-CSF, также как исходный белок, обладал способностью повышать содержание лейкоцитов, сегментоядерных нейтрофилов периферической крови и кариоцитов костного мозга по сравнению с контролем (физиологический раствор). Стимуляция продукции нейтрофилов под действием конъюгата GM-CSF с ALN наблюдалась в более ранние сроки, чем в случае GM-CSF. Увеличение общего числа клеток костного мозга после введения конъюгата было более выраженным по сравнению с исходным белком.
На фиг. 5 представлены данные по количеству лейкоцитов (А), сегментоядерных нейтрофилов (Б) в периферической крови, кариоцитов (В) в костном мозге мышей линии СВА на фоне введения ЦФ, препарата GM-CSF и его коньюгата с ALN. По оси абсцисс - сроки исследования (сутки); по оси ординат- количество клеток, 109/л (109/бедро); * - статистически значимое отличие от контрольной группы (физиологический раствор), р≤0,05; ** - статистически значимое отличие от группы мышей, которым вводили GM-CSF, р≤0,0170. Область между пунктирными прямыми - доверительный интервал показателя у интактных мышей при р≤0,05.
Приведенные выше примеры 1-6 подтверждают достижение заявляемого технического результата, а именно: получено новое лекарственное средство с повышенной тропностью к костному мозгу с гемостимулирующей активностью на основе конъюгата GM-CSF с ALN.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАЗМНОЖЕНИЯ КРОВЕТВОРНЫХ СТВОЛОВЫХ КЛЕТОК | 2002 |
|
RU2297451C2 |
| ФАРМАКОЛОГИЧЕСКАЯ КОМБИНАЦИЯ ПОЛИКАТИОННОГО НОСИТЕЛЯ ПЭГ-ПЭИ-ТАТ С ЗАКЛЮЧЕННОЙ В НЕМ ПЛАЗМИДОЙ, НЕСУЩЕЙ ТЕРАПЕВТИЧЕСКИЕ ГЕНЫ HSVtk И GM-CSF ДЛЯ ЦЕЛЕЙ ГЕНОТЕРАПИИ ОПУХОЛЕВЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2575077C2 |
| Противоопухолевое средство | 2015 |
|
RU2609871C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ ГЕМОСТИМУЛЯТОРОВ ПРИ ЦИТОСТАТИЧЕСКОЙ МИЕЛОСУПРЕССИИ | 2009 |
|
RU2421720C2 |
| ИНГИБИТОР И СТИМУЛЯТОР ПРОЛИФЕРАЦИИ СТВОЛОВОЙ КЛЕТКИ И ИХ ИСПОЛЬЗОВАНИЕ | 1997 |
|
RU2292352C9 |
| Гемостимулирующее средство | 2017 |
|
RU2647833C1 |
| Способ получения противоопухолевого средства против метастазов костей в виде конъюгата белка-цитокина и аминобисфосфоната | 2016 |
|
RU2631486C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЧЕЛОВЕЧЕСКОГО ГРАНУЛОЦИТАРНОГО КОЛОНИЕСТИМУЛИРУЮЩЕГО ФАКТОРА | 2002 |
|
RU2207373C1 |
| ЦИКЛОФИЛИН А - СТИМУЛЯТОР ГРАНУЛОЦИТОПОЭЗА, РАДИОПРОТЕКТОР И ИММУНОСТИМУЛЯТОР | 2008 |
|
RU2370277C1 |
| АЛЛОГЕННОЕ ПРОТИВООПУХОЛЕВОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО | 2004 |
|
RU2354694C2 |
Изобретение относится к биотехнологии и фармакологии и представляет собой конъюгат рекомбинантного человеческого гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) с алендроновой кислотой, представителем бифосфонатов, имеющий повышенное сродство к клеткам-мишеням костного мозга. Техническим результатом заявляемого изобретения является создание гемостимулирующего таргетного средства на основе конъюгата GM-CSF и алендроновой кислоты со свойствами векторной молекулы, направленной к клеткам-мишеням костного мозга. Таргетное колониестимулирующее средство характеризуется тем, что оно представляет собой конъюгат белка гранулоцитарно-макрофагального колониестимулирующего фактора GM-CSF с алендроновой кислотой, связанных между собой по карбоксигруппе белка в виде моноаддукта, имеющего высокое сродство к гидроксилапатиту, полученного реакцией в присутствии водорастворимого сшивающего агента 1-этил-3-[3-диметиламинопропил] карбодиимида (EDC) и имеющего следующую структуру:
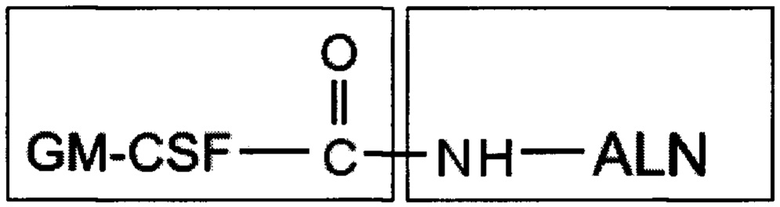
где ALN - алендроновая кислота; GM-CSF - гранулоцитарно-макрофагальный колониестимулирующий фактор. Конъюгат гранулоцитарно-макрофагального колониестимулирующего фактора с алендроновой кислотой получен при их стехиометрическом соотношении на 1 моль GM-CSF - 1 моль алендроновой кислоты. 1 з.п. ф-лы, 5 ил., 1 табл.
1. Таргетное колониестимулирующее средство, характеризующееся тем, что оно представляет собой конъюгат белка гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) с алендроновой кислотой, связанных между собой по карбоксигруппе белка в виде моноаддукта, имеющего высокое сродство к гидроксилапатиту, полученного реакцией в присутствии водорастворимого сшивающего агента 1-этил-3-[3-диметиламинопропил] карбодиимида (EDC) и имеющего следующую структуру:
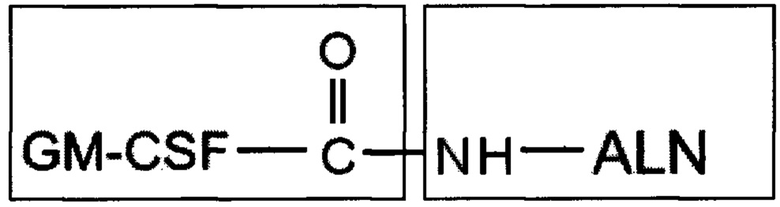
где ALN - алендроновая кислота;
GM-CSF - гранулоцитарно-макрофагальный колониестимулирующий фактор.
2. Средство по п. 1, отличающееся тем, что конъюгат гранулоцитарно-макрофагального колониестимулирующего фактора с алендроновой кислотой получен при их стехиометрическом соотношении на 1 моль GM-CSF - 1 моль алендроновой кислоты.
| Запорный кран для трубопроводов | 1930 |
|
SU20425A1 |
| Способ получения противоопухолевого средства против метастазов костей в виде конъюгата белка-цитокина и аминобисфосфоната | 2016 |
|
RU2631486C1 |
| WO 2017160855 A1, 21.09.2017 | |||
| Kristen B | |||
| Farrell et al, "Bisphosphonate conjugation for bone specific drug targeting", Bone Rep | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
Авторы
Даты
2021-06-11—Публикация
2020-07-28—Подача