ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к жидкой композиции, содержащей высокую концентрацию иммуноглобулинов с улучшенными свойствами транспортировки, введения и хранения.
УРОВЕНЬ ТЕХНИКИ
Иммуноглобулины или антитела применяются иммунной системой для идентификации и нейтрализации патогенов, таких как вирусы и бактерии. Следовательно, концентраты человеческого иммуноглобулина уже давно применяют для лечения и профилактики заболеваний, таких как инфекционные заболевания и иммунодефициты.
Препараты иммуноглобулина обычно вводят внутривенно (в.в.), подкожно (п.к.) или внутримышечно (в.м.). Если введение проводится п.к. или в.м. путем, препараты иммуноглобулина должны иметь низкий объем и поэтому высокие концентрации иммуноглобулина для удобства пациента в виде больших объемов, вводимых в подкожную или мышечную ткань, могут привести к раздражению и боли и могут увеличивать время введения.
Однако увеличение концентрации белка оказывает влияние на стабильность белка, агрегацию и вязкость композиции. Кроме аспектов конформационной стабильности, ассоциация и агрегация является важным препятствием для высоких концентраций белка из-за более высокой скорости молекулярных столкновений повышается межмолекулярная ассоциация и последующая агрегация.
Более того, в препаратах иммуноглобулина обычно происходит рост вязкости в геометрической прогрессии во время повышения концентрации иммуноглобулина, в частности, из-за тенденции к агрегации белка.
Повышение вязкости композиции ограничивает проходимость через иглу и применимость для подкожного введения через шприцы с тонкой иглой. Кроме того, высокая вязкость может вызывать проблемы во время обработки, например, во время диафильтрации или заполнения. Следовательно, желательно поддерживать вязкость лекарственных средств, вливаемых или впрыскиваемых, настолько низкой, насколько возможно.
Также желательно получить конформационно стабильные препараты иммуноглобулина, которые обладают стабильностью при длительном хранении. В общем, конформационная стабильность иммуноглобулинов очень близка к изоэлектрической точке (тИ) (Muelleretal.2013).
Растворимость белков, однако, является минимальной в тИ (Wangetal.,2008), что может стать проблемой, особенно для препаратов IgG с высокой концентрацией.
McCue и соавторы демонстрируют, что тИ в IgG человеческой плазмы составляет от pH 4,5 до 11, демонстрируя четкий максимум между pH 7 и pH 9. Группа также обнаружила увеличение олигометрических видов и нарушение свойств связывания при нейтральном pH и выше (McCueetal.1986).
С другой стороны, в кислых условиях конформационная стабильность падает из-за высокого заряда поверхности белка (Chietal.,2003). Особенно уровни pH ниже 4, в частности, могут приводить к фрагментации и агрегации IgG (Bollietal.,2010;Wangetal.,2007;Vermeeretal.,2000orSzenczietal.,2006).
Одним из способов снижения вязкости таких концентратов иммуноглобулина является изменение pH концентратов до высоких или низких значений. В WO 02/30463 A2, например, описан способ снижения вязкости концентрированной композиции иммуноглобулина с концентрацией по меньшей мере 80 г/л изменением pH композиции до низкого (4,0-5,3) или повышенного значения (6,5-12,0), буферы или соли добавляют в концентрации 50-200 мМ. В качестве альтернативы, источник предлагает повышение общей ионной силы композиции через добавление солей или буферных компонентов.
Снижение pH приводит к снижению стабильности белка и тенденции к разворачиванию, как показано в примере 1 и на фиг. 1. Во время длительного хранения последствием является повышенная фрагментация белка. С другой стороны, повышение pH до значений в интервале 6,5-9 снижает растворимость иммуноглобулинов, в то время как значения pH выше 10 вызывают конформационную нестабильность во время длительного хранения.
Для других фармацевтических композиций, а именно, композиций, содержащих моноклональные антитела, в WO 2013/063510 A1 описано применение аминокислот для снижения вязкости. Однако неизвестно, применимы ли эти открытия к высококонцентрированным иммуноглобулинам, полученным из человеческой плазмы, и, если так, какая из множества аминокислот и сочетаний аминокислот будет обладать снижающим вязкость действием.
Таким образом, объектом данного изобретения является получение композиций для стабилизации иммуноглобулинов, полученных из человеческой плазмы, в высоких концентрациях.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение, кроме прочего, основано на открытии, что при составлении высококонцентрированных композиций иммуноглобулина с сочетанием определенного слегка кислого интервала pH, в частности, от pH 5,5 до 5,9, и добавлении стабилизирующей аминокислоты, такой как глицин или пролин, а также аминокислоты, снижающей вязкость, такой как гистидин или аргинин, с определенной концентрацией аминокислоты, дает композиции, которые имеют пониженную вязкость и повышенную стабильность.
Следовательно, в данном изобретении представлена жидкая композиция, содержащая поликлональные иммуноглобулины, по меньшей мере одну аминокислоту, модулирующую вязкость, выбранную из аргинина и гистидина, и по меньшей мере одну стабилизирующую аминокислоту, выбранную из глицина и пролина, где более 90% поликлональных иммуноглобулинов имеют форму мономеров или димеров, и менее 5% имеют форму полимеров, и где концентрация иммуноглобулина в композиции выше 160 г/л и pH равен от 5,5 до 5,9.
Это сочетание дает высококонцентрированную композицию иммуноглобулина, которая имеет достаточно низкую вязкость для того, чтобы позволить качественную обработку композиции и достаточную проходимость через иглу. Более того, иммуноглобулины в композиции достаточно стабильны для долговременного хранения. Это означает, что образование фрагментов иммуноглобулина минимизировано, и иммуноглобулины имеют низкую тенденцию к образованию полимеров.
Во втором аспекте, изобретение относится к жидкой композиции по первому аспекту для применения в медицинском лечении.
Согласно третьему аспекту, изобретение относится к способу составления высококонцентрированной композиции поликлонального иммуноглобулина, включающему стадии получения высококонцентрированной композиции поликлонального иммуноглобулина, доведения pH композиции до значения в интервале от 5,5 до 5,9, и добавления по меньшей мере одной стабилизирующей аминокислоты, выбранной из глицина и пролина, и по меньшей мере одной модулирующей вязкость аминокислоты, выбранной из аргинина и гистидина.
ОПИСАНИЕ ЧЕРТЕЖЕЙ
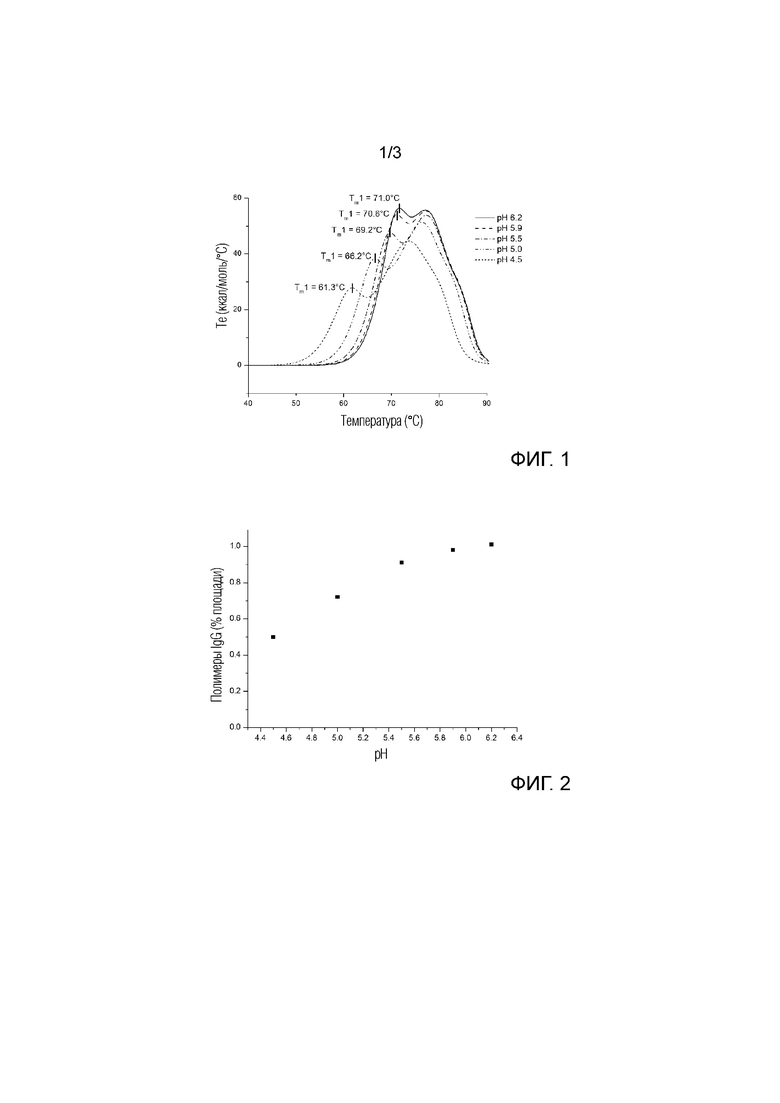
На фиг. 1 показаны кривые теплопередачи композиций, содержащих полученный из человеческой плазмы IgG. Кривые теплопередачи представляют молярную теплоемкость композиции в зависимости от температуры и определяются измерениями ДСК. Композиции содержат IgG, 20 мМ NaCl, 20 мМ ацетата натрия и отличаются pH как показано на фигуре (pH 4,5, 5,0, 5,5, 5,9, 6,2). Локальный максимум кривых представляет конформационные переходы с разворачиванием. Точные температуры первого максимума (Tm1) идентифицируют для каждой кривой. Tm1-температуры для указанных растворов IgG при различных значениях pH составляют 61,3°C для pH=4,5, 66,2°C для pH=5,0, 69,2°C для pH=5,5, 70,6 для pH=5,9 и 71,0°C при pH=6,2.
На фиг. 2 количественно показано отношение между pH препарата IgG и фракции полимеров IgG. Фракцию полимеров IgG композиции IgG (20 мМ NaCl, 20 мМ ацетата натрия) измеряют ГПХ и определяют в % по отношению к общему IgG при различных уровнях pH.
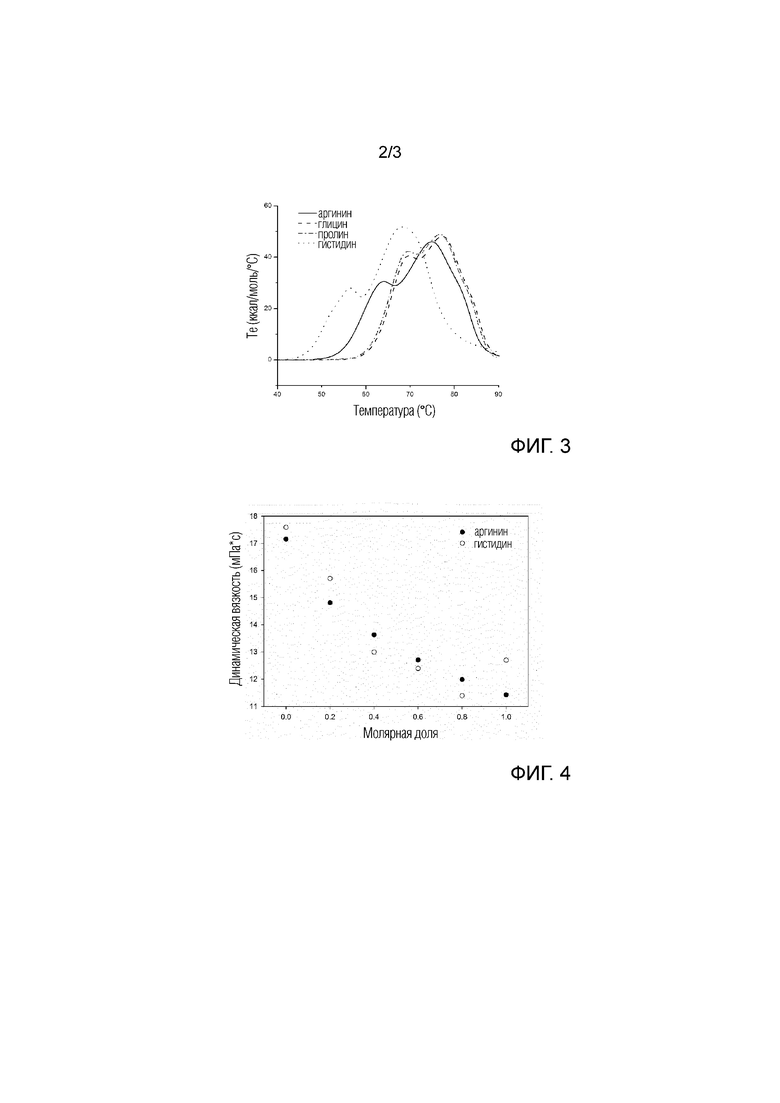
На фиг. 3 показаны кривые теплопередачи композиций, содержащих полученный из человеческой плазмы IgG. Кривые теплопередачи представляют молярную теплоемкость композиции в зависимости от температуры и определяются измерениями ДСК. Композиции содержат IgG, 20 мМ NaCl, 20 мМ ацетата натрия и имеют pH 5,7. Композиции также содержат какую либо из аргинина, глицина, пролина или гистидина, как указано на фигуре, в концентрации 230 мМ. Местный максимум кривых представляет конформационные переходы с разворачиванием.
На фиг. 4 показано влияние концентрации различных аминокислот на динамическую вязкость композиции, содержащей полученный из человеческой плазмы IgG. К композиции, содержащей 20 мМ NaCl и 20 мМ ацетата натрия с pH of 5,7, аминокислоты добавляют до конечной концентрации 250 мМ и определяют полученную динамическую вязкость (Y-оси). Полученные композиции содержат глицин и различные молярные фракции (показаны на осях X) либо гистидина, либо аргинина. При повышении концентрации аргинина или гистидина динамическая вязкость значительно снижается.
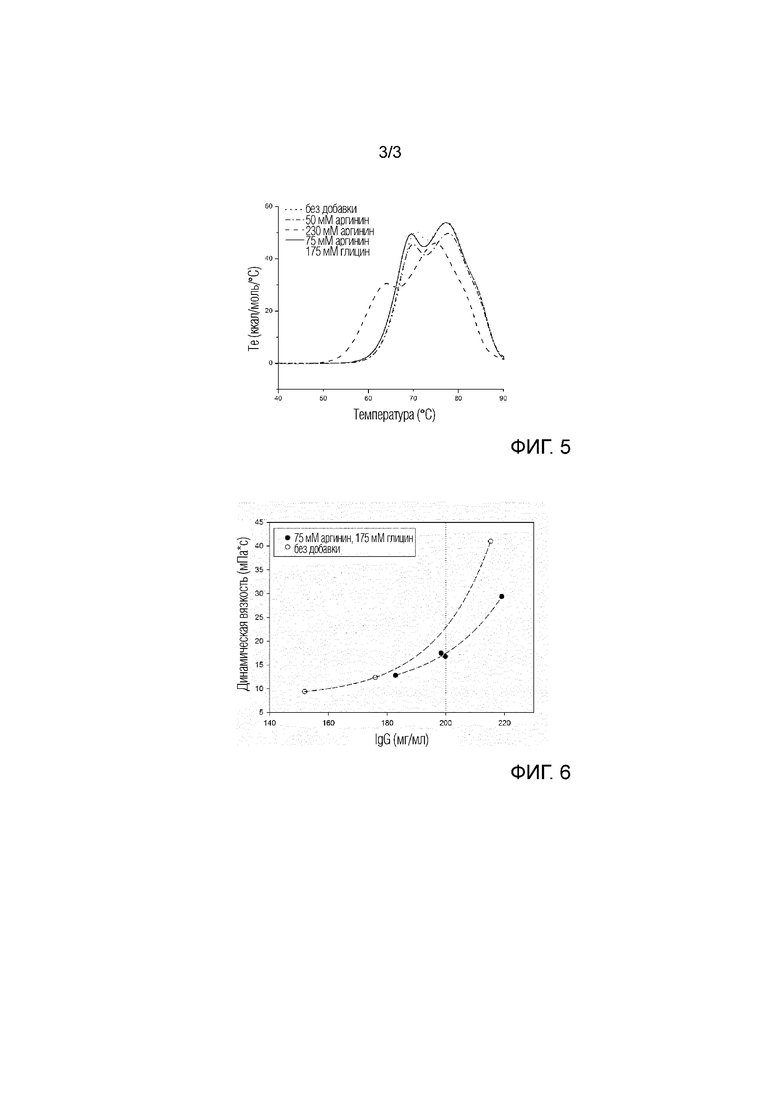
На фиг. 5 показаны кривые теплопередачи композиций, содержащих полученный из человеческой плазмы IgG. Кривые теплопередачи представляют молярную теплоемкость композиции в зависимости от температуры и определяются измерениями ДСК. Композиции содержат IgG, 20 мМ NaCl, 20 мМ ацетата натрия и имеют pH 5,7. В дополнение измеренные композиции содержат либо 50 мМ аргинина, 230 мМ аргинина, либо смесь 75 мМ аргинина и 175 мМ глицина или не содержат аминокислоту (ʺбез добавкиʺ) как указано на фигуре.
На фиг. 6 показана корреляция концентрации IgG и динамической вязкости композиций IgG с и без аминокислотных добавок. При применении сочетания аргинина и глицина, возможно снижать вязкость в высококонцентрированных растворах полученного из человеческой плазмы IgG по отношению к природной, не стабилизированной аминокислотой, композиции. Кривые представляют композиции IgG с 20 мМ NaCl, 20 мМ ацетата натрия, pH 5,7, различными концентрациями IgG. Композиции, представленные черными точками, содержат 75 мМ аргинина и 175 мМ глицина, композиции, представленные кругами, не содержат добавку (ʺбез добавкиʺ).
ПОДРОБНОЕ ОПИСАНИЕ
Согласно первому аспекту, в данном изобретении представлена жидкая композиция, содержащая поликлональные иммуноглобулины, по меньшей мере одну модулирующую вязкость аминокислоту, выбранную из аргинина и гистидина, и по меньшей мере одну стабилизирующую аминокислоту, выбранную из глицина и пролина, где более 90% поликлональных иммуноглобулинов имеют форму мономеров или димеров, и менее 5% имеют форму полимеров, и где концентрация иммуноглобулина в композиции составляет выше 160 г/л и pH составляет от 5,5 до 5,9.
Поликлональные иммуноглобулины в соответствии с данным изобретением получают из человеческой плазмы. Поликлональные иммуноглобулины в соответствии с данным изобретением могут содержать иммуноглобулин G (IgG), иммуноглобулин A (IgA), иммуноглобулин M (IgM). Поликлональные иммуноглобулины являются, в частности, концентратом человеческого IgG. Концентрат IgG в основном содержит различные примеси, такие как другие иммуноглобулины, такие как IgA или IgM, и другие белки крови, такие как альбумин.
Основным компонентом препаратов иммуноглобулина являются иммуноглобулины. Таким образом, в композиции в соответствии с данным изобретением содержание иммуноглобулинов составляет более 90%, предпочтительно, более 95% и более предпочтительно, более 98% в отношении к общему белку.
Общим белком в данном описании является общая концентрация белка, определенная в биуретовом анализе, который основан на появлении фиолетового цвета при реакции ионов меди (II) аминогрупп при щелочном pH.
Концентрат иммуноглобулина G (IgG) в соответствии с данным изобретением, например, может быть получен как описано в WO 2005/082937 A2. Следовательно, исходным материалом является Фракция I+II+III, полученная из пула плазмы согласно методике фракционирования из холодного этанола (такой как Кон, Кистлер-Ничманн или их модификации). Затем восстановленная Фракция I+II+III может быть обработана с применением каприлатного осаждения и анионообменных хроматографий. Специальные патогенные меры безопасности включают обработку растворителем/моющим средством (Р/М), последующее удаление реагента Р/М а также нанофильтрацию.
для улучшения продукта могут быть использованы дополнительные способы, направленные на снижение примесей, например, для снижения гемагглютинина через контакт с аффинными смолами на основе определенных трисахаридов, таких как описаны в WO-A2-01/27623. Такие способы получения иммуноглобулина обычно включают по меньшей мере обработку растворителем/моющим средством (Р/М) и стадию нанофильтрации для патогенной безопасности.
В данном описании термин ʺиммуноглобулинʺ относится к белкам, которые связываются со специфическими антигенами. Иммуноглобулины включают, но не ограничены ими, поликлональные, моноклональные, химерные и гуманизированные антитела, и включают следующие классы: IgA, IgG, IgM, IgD и IgE. Иммуноглобулины обычно содержат две идентичные тяжелые цепи и легкие цепи. Однако термин иммуноглобулин в данном описании также включает фрагменты, такие как иммуноглобулины с одной цепью, а также белковые димеры, полимеры или агрегаты.
Поликлональные иммуноглобулины в жидкой композиции в соответствии с данным изобретением демонстрируют низкий уровень полимеризации, подтвержденный измерением распределения по размеру молекул. Это означает, что поликлональные иммуноглобулины содержат по меньшей мере 90% мономеров и димеров в сумме и не более 5% полимеров. Более того, поликлональные иммуноглобулины демонстрируют только низкую степень фрагментирования. Это означает, что не более 5% поликлональных иммуноглобулинов являются фрагментами. Процент рассчитывают из площади под кривой для агрегатов, димеров, мономеров и фрагментов, измеренной гельпроникающей жидкостной хроматографией высокого давления. Необходимо отметить, что в данном документе нет строгого различия между агрегатами и полимерами или между агрегацией и полимеризацией, так как специалист в данной области техники знают, что подразумеваются молекулы или молекулярные кластеры, соответственно способы их образования, с большей молекулярной массой, чем масса иммуноглобулиновых димеров. Следовательно, общая сумма мономеров, димеров, полимеров и фрагментов иммуноглобулинов составляет 100%. Процент полимеров не более 5% значительно ниже порога, требуемого по фармакопее.
В предпочтительном варианте данного изобретения поликлональные иммуноглобулины содержат по меньшей мере 94% мономеров и димеров в сумме, не более 5% полимеров и не более 5% фрагментов. Это означает, так как процент всегда основан на общей сумме мономеров, димеров, полимеров и фрагментов, что сумма полимеров и фрагментов меньше 6%.
Распределение по размеру молекул в данном описании определяют гельпроникающей жидкостной хроматографией высокого давления (ГП-ЖХВД или ГПХ) с гидрофильным силикагелем, подходящим для фракционированием глобулярных белков с относительными молекулярными массами 10000-500000 и определением спектрофотометром при 280 нм. Результат показан как % площади под кривой для агрегатов, димеров, мономеров и фрагментов.
Концентрация иммуноглобулина в жидкой композиции в соответствии с данным изобретением составляет выше 160 г/л. Концентрации иммуноглобулина ниже этого значения не считаются высококонцентрированной композицией иммуноглобулина. Низкоконцентрированные композиции иммуноглобулина не имеют проблем с вязкостью, так как высококонцентрированные композиции иммуноглобулина.
В соответствии с данным изобретением, если не указано иначе, концентрацию иммуноглобулина определяют ГПХ. Иммуноглобулин определяют ГПХ на том же оборудовании, которое применяют для определения распределения по размеру молекул, для получения качественных результатов необходимо сравнить полученную площадь под кривой образца иммуноглобулина со значениями, полученными построением калибровочной кривой с калибровочным материалом с известной концентрацией иммуноглобулина. Для достаточно чистых композиций иммуноглобулина дополнительная коррекция полученного значения не требуется.
pH жидкой композиции составляет 5,5-5,9. Как указано во введении, растворимость IgG и склонность IgG к образованию полимеров и агрегатов повышается при достижении нейтральных значений pH. Однако, как показано в примере, представленном на фигуре 2, процент полимеров все еще является приемлемым. Более высокие значения pH не рекомендуются, так как они могут привести к значительно более высокой агрегации. Таким образом, максимальный pH в соответствии с данным изобретением составляет 5,9.
Кроме того, существует нижний предел pH жидкой композиции иммуноглобулина. Как показано в примере 1, термодинамическая стабильность иммуноглобулинов в композиции значительно снижается при значениях pH 4,5 и 5,0 по сравнению с более высокими значениями pH 5,5-6,2. Можно сделать вывод, что значение pH 5,2 может быть приемлемым в отношении стабильности белка и фрагментации. Однако при pH в интервале pH 5,5 и pH 5,9 возможно сохранять термодинамически стабильные условия без достижения максимального распределения тИ d.
В данном описании, если не указано иначе, вязкость композиции является динамической вязкостью. В соответствии с данным изобретением, динамическую вязкость определяют на Automated Microviscositymeter ʺAMVnʺ от Anton Paar® GmbH (Austria) при температуре +20,0°C и с углом наклона капилляров 50°. Определение проводят согласно инструкции производителя. Результатом измерения является кинематическая вязкость. Для получения динамической вязкости также определяют плотность на ареометре ʺDMA 4500Mʺ, также от Anton Paar® GmbH (Austria) при той же температуре. Продуктом кинематической вязкости и плотности является динамическая вязкость.
Дифференциальную сканирующую калориметрию (ДСК) применяют для оценки стабильности белка при тепловой денатурации. В отношении калориметрической ссылки измеряют изменение энтальпии при тепловом развертывании белка и средней точки (Tm) теплового развертывания одного или нескольких переходов. ДСК считается приемлемой методикой для прогнозной оценки агрегации белка в течение определенного желаемого времени (срока годности), особенно в случае, когда желательно ранжирование условий (составления) в отношении конформационной стабильности (Muelleretal.2013andWeissetal.2009).
Во время длительного хранения может возникнуть агрегация, полимеризация и фрагментация и, соответственно, снижение суммы фракции мономеров и димеров иммуноглобулина.
Необходимо отметить, что в данном документе нет строгого различия между агрегатами и полимерами или между агрегацией и полимеризацией, так как специалист в данной области техники знают, что подразумеваются молекулы или молекулярные кластеры, соответственно способы их образования, с большей молекулярной массой, чем масса иммуноглобулиновых димеров.
ʺСтабильность при храненииʺ в течение определенного времени в данном описании означает, что иммуноглобулины в композиции имеют распределение по размеру молекул более чем 90% мономеров и димеров в сумме, не более 5% полимеров и не более 5% фрагментов, где общая сумма мономеров, димеров, полимеров и фрагментов составляет 100% после хранения в течение определенного периода времени. Например, если определено, что композиция иммуноглобулина имеет стабильность при хранении в течение шестидесяти месяцев, это означает что по меньшей мере в течение 60 месяцев распределение по размеру молекул показывает более 90% мономеров и димеров в сумме, не более 5% полимеров и не более 5% фрагментов.
Жидкая композиция в соответствии с данным изобретением содержит два типа аминокислот. Первым типом является модулирующая вязкость аминокислота, выбранная из аргинина и гистидина. Как показано в примере 4, добавление любой из аргинина и гистидина к композиции иммуноглобулина приводит к значительному снижению вязкости композиции с высокой концентрацией иммуноглобулина. С двумя этими модулирующими вязкость аминокислотами возможно корректировать вязкость композиции до значений, которые предпочтительны для введения композиции через шприц.
Вторым типом аминокислоты в жидкой композиции в соответствии с данным изобретением является стабилизирующая аминокислота. Стабилизирующую аминокислоту выбирают из глицина и пролина. Как показано в примере 3, добавление глицина или пролина приводит к значительному повышению тепловой стабильности.
Более того, как показано в примерах 5 и 6, сочетание модулирующей вязкость аминокислоты и стабилизирующей аминокислоты оказывают оба действия. Из примера 5 очевидно, что сочетание стабилизирующей и модулирующей вязкость аминокислот приводит к той же стабилизации, как со стабилизирующей аминокислотой отдельно. Также, стабилизирующая аминокислота не оказывает отрицательного влияния на вязкость композиции при добавлении к модулирующей вязкость аминокислоте.
Согласно одному варианту, концентрация иммуноглобулина в жидкой композиции составляет от 150 до 300 г/л, предпочтительно, концентрация иммуноглобулина составляет от 160 до 260 г/л. Если концентрация иммуноглобулина превышает 300 г/л, компоненты в соответствии с данным изобретением не могут больше снижать вязкость до интервала, в котором жидкая композиция может обрабатываться или вводиться через шприц. Как показано в примерах, вплоть до концентрации 260 г/л композиции могут быть получены с разумной вязкостью и долговременной тепловой стабильностью.
pH жидкой композиции составляет от 5,5 до 5,9. Значение pH 5,9 находится в значительном удалении от изоэлектрической точки иммуноглобулинов, в частности, IgG. Следовательно, значение 5,9 вызывает меньшее образование полимеров или агрегатов по сравнению со значением 6,2. Таким образом, удержание pH ниже 5,9 вероятно дает более стабильные и менее агрегированные композиции. Как показано на фигуре 2, конечная нестабильность сильно возрастает при снижении pH от 5,5 до 5,0. Таким образом, даже если pH 5,2 может быть подходящим для жидкой композиции в соответствии с данным изобретением, минимум pH 5,5 дает большую стабильность иммуноглобулинов в жидкой композиции. Очень хорошие результаты в отношении вязкости и стабильности получают при pH 5,7. Таким образом, согласно одному варианту, pH находится в интервале от 5,6 до 5,8, в частности, pH составляет около 5,7.
Согласно одному варианту, жидкая композиция характеризуется концентрацией белка в интервале от 160 до 180 г/л, динамической вязкостью в интервале от 5 до ≤12 мПа*с. Согласно альтернативному варианту, жидкая композиция характеризуется концентрацией белка в интервале от около 180 до 220 г/л и динамической вязкостью от >12 до ≤35 мПа*с. Согласно другому альтернативному варианту, жидкая композиция характеризуется концентрацией белка в интервале от около 220 до 260 г/л и динамической вязкостью от >35 до ≤100 мПа*с.
Согласно одному варианту данного изобретения, концентрация одной или более стабилизирующей аминокислоты и одной или более модулирующей вязкость аминокислоты, т.е. общая концентрация стабилизирующей аминокислоты и модулирующей вязкость аминокислоты составляет от ста до 400 мМ. В общей концентрации ниже 100 мМ, концентрация отдельных модулирующих вязкость и стабилизирующих аминокислот будет недостаточной для получения высококонцентрированной композиции иммуноглобулина с подходящей вязкостью и долговременной стабильностью.
Согласно предпочтительному варианту, общая концентрация стабилизирующих и снижающих вязкость аминокислот составляет от 150 до 350 мМ. Как показано в примерах, особенно в примере 7, общая концентрация аминокислот в этом интервале дает стабильность при долговременном хранении композиций иммуноглобулина.
Особенно хорошие результаты получают с общей концентрацией стабилизирующих и модулирующих вязкость аминокислот, составляющей около 250 мМ. Поэтому, согласно предпочтительному варианту, общая концентрация аминокислот стабилизирующих и модулирующих вязкость аминокислот составляет от 200 до 300 мМ, более предпочтительно, в интервале от 225 до 275 мМ, наиболее предпочтительно, около 250 мМ.
Согласно одному варианту, стабилизирующей аминокислотой является глицин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно альтернативному варианту, стабилизирующей аминокислотой является пролин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно другому альтернативному варианту, стабилизирующей аминокислотой является глицин или пролин и модулирующими вязкость аминокислотами являются аргинин и гистидин, согласно другому альтернативному варианту стабилизирующими аминокислотами являются глицин и пролин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно другому варианту, стабилизирующими аминокислотами являются глицин и пролин и модулирующими вязкость аминокислотами являются аргинин и гистидин. Согласно предпочтительному варианту, стабилизирующей аминокислотой является глицин и модулирующей вязкость аминокислотой является аргинин.
Согласно одному варианту, концентрация модулирующей вязкость аминокислоты в жидкой композиции составляет от 50 до 100 мМ. Ниже 50 мМ снижающее вязкость действие модулирующих вязкость аминокислот обычно недостаточно для сохранения вязкости композиции на подходящем уровне.
Выше значения 100 мМ дестабилизирующее действие модулирующих вязкость аминокислот становится слишком сильным так, что очень высокие концентрации стабилизирующей аминокислоты будут в ней противодействовать дестабилизирующему действию и, следовательно, общая концентрация аминокислоты будет превышать 400 мМ.
Предпочтительно, концентрация модулирующих вязкость аминокислот составляет от 60 до 90 мМ. Как показано в примерах, в частности, для аргинина было найдено, что концентрация 75 мМ дает наилучшие результаты в отношении снижения вязкости и стабилизации. Таким образом, предпочтительно, концентрация модулирующих вязкость аминокислот составляет от 65 до 85 мМ, наиболее предпочтительно, в интервале от 70 до 80 мМ, и в частности, около 75 мМ. Согласно предпочтительному варианту, жидкая композиция содержит аргинин в концентрации от 70 до 80 мМ.
Согласно одному варианту, концентрация стабилизирующей аминокислоты составляет от 80 до 300 мМ. Ниже концентрации 80 мМ, полагают, что стабилизирующее действие не может противодействовать дестабилизирующему действию модулирующих вязкость аминокислот. Выше концентрации 300 мМ общая концентрация аминокислот попадает в интервал, в котором аминокислоты могут отрицательно влиять на функцию иммуноглобулинов.
Было обнаружено, что предпочтительной концентрацией для стабилизирующей аминокислоты глицина составляет 175 мМ, см. пример 7. Таким образом, согласно предпочтительному варианту, концентрация стабилизирующих аминокислот составляет от 130 до 220 мМ. Согласно более предпочтительному варианту, концентрация составляет от 160 до 190 мМ. Более предпочтительная концентрация стабилизирующей аминокислоты составляет от 170 до 180 мМ. В частности, концентрация составляет около 175 мМ. Согласно предпочтительному варианту, жидкая композиция содержит стабилизирующие аминокислоты в концентрации от 170 до 180 мМ.
Как показано в примере 7, иммуноглобулины в жидкой композиции в соответствии с данным изобретением обладают стабильность при хранении в течение длительного периода времени, как при низких температурах, в интервале от 2 до 8°C, так и при комнатной температуре, которая составляет от 15 до 27°C.
Согласно одному варианту, стабильность при хранении иммуноглобулинов в жидкой композиции составляет по меньшей мере 40 месяцев при температуре от 2 до 8°C. Предпочтительно, срок стабильности при хранении составляет по меньшей мере 60 месяцев, более предпочтительно по меньшей мере 69 месяцев при температуре от 2 до 8°C. При температуре хранения от 23 до 27°C, срок стабильности при хранении иммуноглобулинов в жидкой композиции в соответствии с данным изобретением составляет по меньшей мере 12 месяцев хранения, более предпочтительно по меньшей мере 24 месяцев хранения, и наиболее предпочтительно по меньшей мере 40 месяцев хранения.
Другие наполнители или стабилизаторы также могут присутствовать в препарате иммуноглобулина в соответствии с данным изобретением, но они не нужны для достижения заявленной стабильности. Согласно одному варианту, жидкая композиция может содержать один или более из поверхностно-активных веществ, моющих средств или сахарида. Жидкая композиция также может содержать один или более каждого из поверхностно-активных веществ, моющих средств или сахарида. Примеры подходящих сахаридов включают мальтозу, сорбит, маннозу, мелезитозу или глюкозу. Примером подходящего поверхностно-активного вещества является полисорбат. Полисорбат предпочтительно присутствует в количестве от 5 до 60 мг/л.
Согласно одному варианту, жидкая композиция содержит дополнительно соль, выбранную из ацетата натрия, хлорида натрия или дигидроцитрата натрия. Предпочтительно, жидкая композиция содержит ацетат натрия и NaCl. Ацетат натрия предпочтительно присутствует в концентрации от 10 до 50 мМ. Более предпочтительно, ацетат натрия присутствует в концентрации около 20 мМ. NaCl предпочтительно присутствует в концентрации от 10 до 50 мМ. Более предпочтительно, NaCl присутствует в концентрации около 20 мМ. Согласно одному варианту, ацетат натрия и NaCl присутствуют в концентрации около 20 мМ.
Согласно одному варианту данного изобретения, жидкая композиция практически не содержит тромбогенных факторов и имеет менее мИЕ/мл FXIa-подобной активности относительно 5% общего белкового раствора, определенного в анализе образования тромбина (АОТ) от Technoclone (Austria) с применением ссылочного стандарта NIBSC FXIa.
Согласно одному варианту, жидкая композиция в соответствии с данным изобретением имеет титры гемагглутинина, сниженные до ≤16 для анти-A и ≤8 для анти-B при определении прямой пробой Кумбса.
В соответствии с данным изобретением, прямую пробу Кумбса проводят по протоколу, определенному в Pharmacopoeia Europaea. Кратко, анти-A или анти-B антитела контактируют в данном анализе с папаином, и определяют титр, который является наивысшим разведением с наблюдаемым агглютинированием.
Предпочтительными вариантами данного изобретения являются препараты иммуноглобулина G с содержанием иммуноглобулина G 185-215 г/л, значением pH 5,5-5,9 или 5,6-5,9, и динамической вязкостью >12 и вплоть до 30 мПа*с, при составлении с 150-210 мМ глицина и 50-105 мМ аргинина. Эти предпочтительные варианты имеют стабильность при хранении по меньшей мере 12 месяцев при 23-27°C и стабильность при хранении по меньшей мере 24 месяца при хранении в холодильнике при 2-8°C, где стабильность хранимых в холодильнике препаратов иммуноглобулина G также определяют через 67 и 69 месяцев и препараты все еще находят стабильными в соответствии с указанными выше критериями.
Иммуноглобулин в соответствии с данным изобретением может применяться в лечении или профилактике множества заболеваний. Таким образом, согласно второму аспекту, данное изобретение относится к жидкой композиции, содержащей высокую концентрацию поликлональных иммуноглобулинов для применения в медицинском лечении. Медицинское лечение в соответствии с данным изобретением включает профилактику и терапию.
Другими словами, согласно второму аспекту данное изобретение относится к лечению или профилактике заболеваний введением жидкой композиции, содержащей высокую концентрацию поликлональных иммуноглобулинов, пациенту.
Жидкая композиция для применения согласно второму аспекту содержит по меньшей мере одну стабилизирующую аминокислоту и по меньшей мере одну модулирующую вязкость аминокислоту. Далее, жидкая композиция согласно второму аспекту, в частности, имеет pH в интервале 5,5-5,9. В частности, жидкой композицией согласно второму варианту является, в частности, жидкая композиция, определенная в первом аспекте.
Медицинское лечение включает лечение и профилактику заболеваний, таких как иммунодефицит, такой как врожденная агаммаглобулинемия, гипогаммаглобулинемия, вариабельный неклассифицируемый иммунодефицит, тяжелый комбинированный иммунодефицит, дефицит подклассов IgG с рецидивирующими инфекциями, миелома, хронический лимфатический лейкоз с тяжелой вторичной гипогаммаглобулинемией, болезнь Альцгеймера, легкое когнитивное ухудшение (ЛКУ), синдром приобретенного иммунодефицита (СПИД), синдром Вискотта-Алдрича и тяжелый комбинированный иммунодефицит (ТКИД), острая и хроническая геморрагическая пурпура (ГП), аллогенная трансплантация костного мозга (ТКМ), болезнь Кавасаки, синдром Гийена-Барре, хроническая воспалительная демиелинирующая полинефропатия (ХВДП), многоочаговая моторная невропатия, рассеянный склероз, миастения гравис, синдром Итона-Ламберта, ревматоидный артрит, системная красная волчанка, системная склеродерма, васкулит, гранулематоз Вегнера, синдром Съоргена, аутоиммунная нейтропения, аутоиммунная гемолитическая анемия, нейтропения, болезнь Крона, язвенный колит, целиакия, астма, синдром септического шока, синдром хронической усталости, токсический шок или рецидивирующие инфекции.
Лечение или профилактика предпочтительно включают введение пациенту эффективного количества жидкой композиции. Жидкая композиция, например, может вводиться в форме фармацевтической композиции.
Фармацевтические композиции в соответствии с данным изобретением могут быть получены и введены субъекту любыми способами, хорошо известными в области фармацевтики. См., например, Goodman & Gilman's The Pharmacological Basis of Therapeutics, Hardman et al., eds., McGraw-Hill Professional (10th ed., 2001); Remington: The Science and Practice of Pharmacy, Gennaro, ed., Lippincott Williams & Wilkins (20th ed., 2003); и Pharmaceutical Dosage Forms and Drug Delivery Systems, Ansel et al. (eds), Lippincott Williams & Wilkins (7th ed., 1999). Кроме того, фармацевтические композиции в соответствии с данным изобретением также могут быть составлены так, чтобы включать другие медицинские лекарственные средства или биологические агенты.
Фармацевтические композиции в соответствии с данным изобретением содержат жидкую композицию с эффективным количеством иммуноглобулинов, с жидкой композицией, дополнительно составленной с по меньшей мере одним фармацевтически приемлемым носителем.
Фармацевтически приемлемым носителем является любой носитель, известный или открытый в данной области техники. Типовые фармацевтически приемлемые носители включают стерильную апирогенную воду и стерильный апирогенный физиологический раствор.
Другие формы фармацевтически приемлемых носителей, которые могут применяться для данных вариантов, включают связующие агенты, разрыхлители, поверхностно-активные вещества, усилители абсорбции, агенты, удерживающие влагу, абсорбенты, смазывающие агенты, наполнители, наполнители, агенты, придающие влажность, консерванты, стабилизаторы, эмульгаторы, солюбилизирующие агенты, соли, которые контролируют осмотическое давление, разбавители, такие как буферы и наполнители, обычно применяемые в зависимости от применяемой формы композиции. Их необязательно выбирают и применяют в зависимости от стандартной лекарственной формы полученной композиции.
Жидкая композиция или фармацевтическая композиция может вводиться пациенту любым обычным путем введения, например, перорально, парентерально или ингаляцией. Парентеральное введение включает подкожную инъекцию, внутрибрюшинную инъекцию, внутримышечную инъекцию и внутрибрюшинную инъекцию, жидкие агенты, суспензии, эмульсии и агенты для капельницы. Предпочтительно внутримышечное (в.м.) и подкожное (п.к.) введение.
Согласно третьему аспекту, данное изобретение относится к способу составления высококонцентрированного препарата поликлонального иммуноглобулина, включающему получение высококонцентрированного препарата поликлонального иммуноглобулина, доведение pH композиции до значения в интервале 5,5-5,9, добавление по меньшей мере одной стабилизирующей аминокислоты, выбранной из глицина и пролина, и добавление по меньшей мере одной модулирующей вязкость аминокислоты, выбранной из аргинина и гистидина.
Продуктом такого способа составления является жидкая композиция, содержащая поликлональные иммуноглобулины, по меньшей мере одну стабилизирующую аминокислоту и одну модулирующую вязкость аминокислоту с pH в интервале 5,5-5,9. Препаратом иммуноглобулина в частности является концентрат IgG, который может быть получен как определено выше.
Согласно одному варианту способа, pH доводят до значения в интервале 5,5-5,9, более предпочтительно, в интервале 5,7-5,9, в частности, до pH около 5,8.
В одном варианте способа, буферные компоненты, такие как ацетат натрия или NaCl, добавляют к препарату иммуноглобулина до добавления аминокислот и корректировки pH.
Согласно одному варианту способа, стабилизирующую аминокислоту добавляют в высококонцентрированную композицию поликлонального иммуноглобулина до добавления в нее модулирующей вязкость аминокислоты и корректировки pH. Следовательно, на следующей стадии модулирующая вязкость аминокислота может быть добавлена до корректировки pH. Альтернативно, на следующей стадии pH корректируют до добавления модулирующей вязкость аминокислоты.
В альтернативном варианте способа pH корректируют до добавления стабилизирующей аминокислоты и модулирующей вязкость аминокислоты. Следовательно, на следующей стадии добавляют стабилизирующую аминокислоту. Альтернативно, модулирующую вязкость аминокислоту добавляют до добавления стабилизирующей аминокислоты.
Другой альтернативный вариант способа включает добавление модулирующей вязкость аминокислоты до добавления стабилизирующей аминокислот и корректировки pH. В этом случае, на следующей стадии может быть добавлена стабилизирующая аминокислота до корректировки pH. Альтернативно, pH корректируют до добавления стабилизирующей аминокислоты.
Согласно одному варианту, стабилизирующую и модулирующую вязкость аминокислоты смешивают до добавления смеси в высококонцентрированную композицию поликлонального иммуноглобулина. Таким образом, смесь аминокислот может быть добавлена для корректировки pH или, альтернативно, после корректировки pH.
В одном варианте способа концентрация иммуноглобулина в полученной жидкой композиции составляет более 160 г/л. Предпочтительно, она составляет 160-300 г/л, более предпочтительно, концентрация иммуноглобулина составляет 160-260 г/л.
Согласно предпочтительному варианту способа, аминокислоты добавляют в таких концентрациях, что общая концентрация стабилизирующей и модулирующей вязкость аминокислот в полученной жидкой композиции составляет 150-350 мМ. Предпочтительно, общая концентрация добавляемых стабилизирующих аминокислот и модулирующих вязкость аминокислот такова, что полученная жидкая композиция имеет общую концентрацию в интервале от 200 до 300 мМ, более предпочтительно, в интервале от 225 до 275 мМ, наиболее предпочтительно, около 250 мМ.
Согласно одному варианту способа, стабилизирующей аминокислотой является глицин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно альтернативному варианту способа, стабилизирующей аминокислотой является пролин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно другому альтернативному варианту способа, стабилизирующей аминокислотой является глицин или пролин и модулирующими вязкость аминокислотами являются аргинин и гистидин. Согласно другому альтернативному варианту способа, стабилизирующими аминокислотами являются глицин и пролин и модулирующей вязкость аминокислотой является аргинин или гистидин. Согласно другому варианту способа, стабилизирующими аминокислотами являются глицин и пролин и модулирующими вязкость аминокислотами являются аргинин и гистидин. Согласно предпочтительному варианту способа, стабилизирующей аминокислотой является глицин и модулирующей вязкость аминокислотой является аргинин.
Способ согласно третьему аспекту может включать добавление любых ингредиентов, перечисленных для жидкой композиции согласно первому аспекту. Следовательно, другие ингредиенты, описанные для жидкой композиции первого аспекта, в частности, наполнители, такие как моющее средство, поверхностно-активное вещество и сахара, могут быть добавлены до, после или вместе со стабилизирующей и модулирующей вязкость аминокислотами. Также, ингредиенты могут быть добавлены до или после корректировки pH. Согласно одному варианту, наполнители добавляют после добавления модулирующей вязкость и стабилизирующей аминокислот и после корректировки pH.
Способ составления согласно четвертому аспекту, в частности, дает получение жидкой композиции по первому аспекту.
В четвертом аспекте, данное изобретение относится к применению стабилизирующей аминокислоты, в частности, глицина или пролина, в сочетании с модулирующей вязкость аминокислотой, в частности, гистидином или аргинином, в композиции высококонцентрированного препарата поликлонального иммуноглобулина. Применение стабилизирующей аминокислоты и модулирующей вязкость аминокислоты дает получение жидкой композиции, содержащей поликлональные аминокислоты. В частности, применение дает получение жидкой композиции по первому аспекту. Специалист в данной области техники поймет, что применение может включать любую из стадий способа, описанных для способа по третьему аспекту.
Далее изобретение описано следующими не ограничивающими примерами.
ПРИМЕРЫ
Пример 1 - pH зависимость стабильности иммуноглобулина
Иммуноглобулин G (IgG) получают согласно способу, описанному в WO 2005/082937 A2. Следовательно, исходным материалом является восстановленная Фракция I+II+III, полученная из пула плазмы и обработанная с применением каприлатного осаждения и анионообменных хроматографий. Специальные патогенные меры безопасности включают обработку растворителем/моющим средством (Р/М), последующее удаление реагента Р/М а также нанофильтрацию.
Затем полученный раствор, содержащий IgG, концентрируют ультра-/диафильтрацией и составляют с различными буферами. Разные композиции получают со значениями pH 4,5, 5,0, 5,5, 5,9 и 6,2, соответственно, с содержанием 20 мМ NaCl и 20 мМ ацетата натрия.
Композиции измеряют дифференциальной сканирующей калориметрией (ДСК). MicroCal™ VP-Capillary DSC System применяют для построения кривой плавления, а также определения средней точки (Tm) и изменения энтальпии развертывания белка при нагревании от 25°C до 120°C со скоростью 1°C/мин. В качестве калориметрической ссылки применяют буфер, имеющий тот же pH и состоящий из тех же компонентов, как и образец белка, за исключением белка.
Результаты измерений показаны на фигуре 1. Кривая теплопередачи представляет молярную теплоемкость в зависимости от температуры, и определяется измерениями ДСК. Местные максимумы кривых представляют конформационные переходы с разворачиванием. Точные температуры первого максимума (Tm1) идентифицируют для каждой кривой. Tm1-температуры для указанных композиций иммуноглобулина составляют 61,3°C для pH=4,5, 66,2°C для pH=5,0, 69,2°C для pH=5,5, 70,6 для pH=5,9 и 71,0°C при pH=6,2.
При снижении pH сдвиг кривой теплопередачи к низким температурам можно увидеть на фигуре 1. Это означает, что измеренные белки, в частности, иммуноглобулины, в композиции плавятся при более низких температурах при снижении pH. Из этой фигуры можно определить снижение конформационной стабильности полученного из человеческой плазмы иммуноглобулина при более низких значениях pH.
В частности, при pH 4,5, значительно более низкая термодинамическая стабильность иммуноглобулина может быть установлена из представленных данных, в то время как более высокая структурная стабильность может быть найдена при значениях pH 5,5 и выше.
Пример 2 - pH зависимость агрегации иммуноглобулина
Для определения степени агрегации содержащих иммуноглобулин композиций из примера 1 проводят гельпроникающую хроматографию (ГПХ) с применением гидрофильного силикагеля, подходящего для фракционирования глобулярных белков с относительными молекулярными массами 10000-500000, и определения на спектрофотометре при 280 нм. Рассчитывают площади под кривыми ГПХ хроматограммы, относящиеся к агрегатам, димерам, мономерам и фрагментам. На фигуре 2 процент полимеров, определенный распределением по размеру молекул в композициях, представлен относительно pH.
Пример 3 - Влияние аминокислоты на стабильность иммуноглобулина
В этом эксперименте тестируют влияние различных аминокислот на стабильность иммуноглобулина с применением ДСК. Для этого композиции иммуноглобулина получают как описано в примере 1. Конечные композиции содержат 20 мМ NaCl, 20 мМ ацетата натрия и 230 мМ аминокислоты, выбранной из аргинина, глицина, пролина и гистидина, доведенных до 5,7. Как описано в примере 1, кривую теплопередачи четырех композиций иммуноглобулина определяют ДСК. Результаты изображены на фигуре 3.
Следовательно, из фигуры 3 очевидно, что добавление глицина или пролина приводит к сдвигу кривой к более высоким температурам по сравнению с кривыми композиций, содержащих гистидин или аргинин. Таким образом, глицин и пролин могут считаться стабилизирующими аминокислотами.
Пример 4 - Влияние аминокислот на вязкость композиции
На следующей стадии тестируют какие аминокислоты подходят для снижения вязкости композиции иммуноглобулина. Следовательно, композиции иммуноглобулина готовят как описано в примере 1 и составляют с 20 мМ ацетата натрия и 20 мМ NaCl при pH 5,7. Получают различные композиции аминокислот, содержащие только глицин или с увеличивающимися молярными долями аргинина или гистидина с общей концентрацией аминокислоты 250 мМ.
Динамическую вязкость этих композиций иммуноглобулина определяют на Automated Microviscometer ʺAMVnʺ от Anton Paar® GmbH (Austria) при температуре +20,0°C и углом наклона капилляров 50°.
Результаты показаны на фигуре 4. Следовательно, и аргинин и гистидин вызывают сильное снижение динамической вязкости при увеличении молярных долей указанных аминокислот.
Пример 5 - Стабильность композиции иммуноглобулина с различными аминокислотами
На следующей стадии проверяют действие сочетания аргинина и глицина на стабильность иммуноглобулинов в препарате. Композицию иммуноглобулина готовят согласно примеру 1 и составляют с 20 мМ ацетата натрия и 20 мМ NaCl при pH 5,7. К первой композиции иммуноглобулина добавляют 175 мМ глицина и 75 мМ аргинина. Для сравнения, три композиции готовят с 50 мМ аргинина, 230 мМ аргинина или без добавок. Снова кривую теплопередачи композиций иммуноглобулина измеряют ДСК. Результаты показаны на фигуре 5. Следовательно, композиция с 75 мМ аргинина и 175 мМ глицина имеет сравнимый переход кривой с композицией без добавок. Наоборот, применение низких количеств аргинина (50 мМ) или высоких количеств аргинина (230 мМ) дестабилизируют композицию. Последний результат ожидаем, так как снижение вязкости раствора часто приводит к дестабилизации белков в растворе.
Этот эксперимент показывает, что дестабилизирующее действие снижения вязкости, вызванного модулирующей вязкость аминокислотой аргинином, полностью отменяется применением достаточного количества глицина.
Пример 6 - Вязкость композиции иммуноглобулина с глицином и аргинином
Для определения того, оказывает ли стабилизирующая аминокислота глицин негативное действие на вязкость композиции иммуноглобулина, динамическую вязкость композиций иммуноглобулина с 175 мМ глицина и 75 мМ аргинина и увеличивающимися концентрациями иммуноглобулина (180 г/л, 200 г/л и 220 г/л) тестируют как описано в примере 3. Также для сравнения измеряют динамическую вязкость композиции без добавок и повышенных количеств иммуноглобулина. Результаты показаны на фигуре 6. Из диаграммы на фигуре 6 очевидно, что стабилизирующая аминокислота глицин не оказывает негативного действия на снижение вязкости.
Пример 7 - Стабильность при хранении различных композиций иммуноглобулина
Концентраты поликлонального иммуноглобулина готовят как описано в примере 1. В следующих экспериментах хранения составляют и хранят различные концентраты иммуноглобулина. До и после хранения композиции, композиции иммуноглобулина тестируют.
Эксперименты хранения для композиции иммуноглобулина 1
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 202 мМ глицина и 51 мМ аргинина до концентрации иммуноглобулина 208 г/л при pH 5,8. Динамическую вязкость определяют как 20,0 мПа*с. Образцы композиции иммуноглобулина хранят при 2-8°C или при 23-27°C в течение 12 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до и после хранения.
Результаты хранения при различных температурах показаны в таблицах 1 и 2.
Таблица 1: Результаты хранения при температуре 2-8°C
Таблица 2: Результаты хранения при температуре 23-27°C
Эксперименты хранения для композиции иммуноглобулина 2
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 173 мМ глицина и 74 мМ аргинина до концентрации иммуноглобулина 207 г/л при pH 5,8. Динамическую вязкость определяют как 19,1 мПа*с. Образцы композиции иммуноглобулина хранят при 2-8°C в течение 12 месяцев или при 23-27°C в течение 69 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения, через 12 месяцев и, для композиции 2.2, после 69 месяцев хранения.
Результаты хранения при различных температурах показаны в таблицах 3 и 4.
Таблица 3: Результаты хранения при температуре 2-8°C
Таблица 4: Результаты хранения композиции 2 при температуре 23-27°C
Эксперимент хранения для композиции иммуноглобулина 3
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 168 мМ глицина и 87 мМ аргинина до концентрации иммуноглобулина 195 г/л при pH 5,7. Динамическую вязкость определяют как 19,1 мПа*с. Образцы композиции 3 хранят при 2-8°C в течение 67 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения, через 12 месяцев, через 24 месяца и через 69 месяцев хранения.
Результаты хранения при различных температурах показаны в таблице 5.
Таблица 5: Результаты хранения композиции 3 при температуре 2-8°C
Эксперимент хранения для композиции иммуноглобулина 4
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 172 мМ глицина и 70 мМ аргинина до концентрации иммуноглобулина 200 г/л при pH 5,7. Динамическую вязкость определяют как 19,1 мПа*с. Образцы композиции 4 хранят при 2-8°C в течение 24 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения, через 12 месяцев и через 24 месяца хранения.
Результаты хранения при различных температурах показаны в таблице 6.
Таблица 6: Результаты хранения композиции 4 при температуре 2-8°C
Эксперимент хранения для композиции иммуноглобулина 5
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 172 мМ глицина и 77 мМ аргинина до концентрации иммуноглобулина 200 г/л при pH 5,7. Динамическую вязкость определяют как 19,1 мПа*с. Образцы композиции 4 хранят при 2-8°C в течение 12 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения и через 12 месяцев хранения.
Результаты хранения при различных температурах показаны в таблице 7.
Таблица 7: Результаты хранения композиции 5 при температуре 2-8°C
Эксперименты хранения для композиции иммуноглобулина 6
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 150 мМ глицина и 100 мМ аргинина до концентрации иммуноглобулина 210 г/л при pH 5,7. Динамическую вязкость определяют как 18,1 мПа*с. Образцы композиции 6 хранят при 2-8°C или 23-27°C в течение 12 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения и через 12 месяцев хранения.
Результаты хранения при различных температурах показаны в таблицах 8 и 9.
Таблица 8: Результаты хранения композиции 6 при температуре 2-8°C
Таблица 9: Результаты хранения композиции 6 при температуре 23-27°C
Эксперименты хранения для композиции иммуноглобулина 7
Концентрат иммуноглобулина составляют с 20 мМ ацетата натрия, 20 мМ NaCl, 196 мМ глицина и 51 мМ аргинина до концентрации иммуноглобулина 184 г/л при pH 5,7. Динамическую вязкость определяют как 12,2 мПа*с. Образцы композиции 7 хранят при 2-8°C или 23-27°C в течение 12 месяцев.
Фракции полимеров, димеров, мономеров, мономеров плюс димеров и фрагментов определяют из хроматограмм, полученных гельпроникающей хроматографией до хранения и через 12 месяцев хранения.
Результаты хранения при различных температурах показаны в таблицах 10 и 11.
Таблица 10: Результаты хранения композиции 7 при температуре 2-8°C
Таблица 11: Результаты хранения композиции 7 при температуре 23-27°C
ССЫЛКИ
Bolli R, Woodtli K, Bärtschi M, Höfferer L, Lerch P. L-Prolin reduces IgG dimer content and enhances the stability of intravenous immunoglobulin (IVIG) solutions; Biologicals. 2010;38(1):150-157.
Chi EY, Krishnan S, Randolph TW, Carpenter JF. Physical stability of proteins in aqueous solution: Mechanism and driving forces in nonnative protein aggregation. Pharm Res. Springer; 2003;20(9):1325-36.
McCue JP, Hein RH, Tenold R. Three generations of immunoglobulin G preparations for clinical use; Rev Infect Dis. 1986;8 Suppl 4:S374-81.
Mueller M, Loh MQT, Tee DHY, Yang Y, Jungbauer A. Liquid compositions for long-term storage of monoclonal IgGs; Appl Biochem Biotechnol. 2013;169:1431-48.
Szenczi Á, Kardos J, Medgyesi G a., Závodszky P - The effect of solvent environment on the conformation and stability of human polyclonal IgG in solution. Biologicals. 2006;34:5-14.
Trevino SR, Scholtz JM, Pace CN. Measuring and Increasing Protein Solubility; 2008;97(10):4155-66.
Wang W, Roberts CJ, editors. Aggregation of Therapeutic Proteins; John Wiley & Sons, Inc., Hoboken, New Jersey; 2013. 325-356.
Vermeer AWP, Norde W. The thermal stability of immunoglobulin: unfolding and aggregation of a multi-domain protein; Biophys J; 2000 Jan;78(1):394-404.
Wang W, Singh S, Zeng DL, King K, Nema S. Antibody structure, instability, and composition; J Pharm Sci. 2007;96(1):1-26.
Weiss I V, William F, Young TM, Roberts CJ. Principles, approaches, and challenges for predicting protein aggregation rates and shelf life; J Pharm Sci.; 2009;98(4):1246-77.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ СПОСОБ СТАБИЛИЗАЦИИ БИОФАРМАЦЕВТИЧЕСКОГО ЛЕКАРСТВЕННОГО ПРОДУКТА ПРИ ПРОИЗВОДСТВЕ | 2017 |
|
RU2744630C2 |
| ЖИДКИЕ ИММУНОГЛОБУЛИНОВЫЕ ПРЕПАРАТЫ | 1995 |
|
RU2158605C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2017 |
|
RU2775944C2 |
| РАСПЫЛЕНИЕ ИММУНОГЛОБУЛИНА | 2015 |
|
RU2729546C2 |
| СТАБИЛЬНЫЕ ПРЕПАРАТЫ СВЯЗЫВАЮЩЕГО СРЕДСТВА НА ОСНОВЕ IgG4 | 2013 |
|
RU2644214C2 |
| ЖИДКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛО ВЫСОКОЙ КОНЦЕНТРАЦИИ | 2008 |
|
RU2497544C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРОДУКТ С УВЕЛИЧЕННОЙ СТАБИЛЬНОСТЬЮ, СОДЕРЖАЩИЙ ИММУНОГЛОБУЛИНЫ | 2015 |
|
RU2748841C2 |
| ЖИДКИЕ СОСТАВЫ ДЛЯ КОНЪЮГАТА ЭРИТРОПОЭТИНА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ | 2011 |
|
RU2682720C2 |
| ЖИДКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛО ВЫСОКОЙ КОНЦЕНТРАЦИИ | 2013 |
|
RU2701181C2 |
| ЖИДКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИТЕЛО ВЫСОКОЙ КОНЦЕНТРАЦИИ | 2019 |
|
RU2795116C2 |
Настоящее изобретение относится к жидкой композиции для стабилизации иммуноглобулинов, содержащей поликлональные иммуноглобулины, модулирующую вязкость аминокислоту и стабилизирующую аминокислоту, где модулирующая вязкость аминокислота представляет собой аргинин, и стабилизирующая аминокислота представляет собой глицин, где общая концентрация стабилизирующей аминокислоты и модулирующей вязкость аминокислоты находится в интервале 100-400 мМ, и где концентрация стабилизирующей аминокислоты находится в интервале 80-300 мМ, где более 90% поликлональных иммуноглобулинов имеют форму мономеров или димеров, и менее 5% имеют форму полимеров, и где концентрация иммуноглобулина в композиции выше 160 г/л, и pH составляет 5,5-5,9. Также настоящее изобретение относится к применению жидкой композиции для стабилизации иммуноглобулинов и к способу составления жидкой композиции. Техническим результатом настоящего изобретения является получение конформационно стабильных препаратов иммуноглобулина, которые обладают стабильностью при длительном хранении, а также поддерживют вязкость лекарственных средств, вливаемых или впрыскиваемых, настолько низкой, насколько возможно. 3 н. и 11 з.п. ф-лы, 6 ил., 7 пр., 11 табл.
1. Жидкая композиция для стабилизации иммуноглобулинов, содержащая поликлональные иммуноглобулины, модулирующую вязкость аминокислоту и стабилизирующую аминокислоту,
где модулирующая вязкость аминокислота представляет собой аргинин, и стабилизирующая аминокислота представляет собой глицин,
где общая концентрация стабилизирующей аминокислоты и модулирующей вязкость аминокислоты находится в интервале 100-400 мМ, и где концентрация стабилизирующей аминокислоты находится в интервале 80-300 мМ, где более 90% поликлональных иммуноглобулинов имеют форму мономеров или димеров, и менее 5% имеют форму полимеров, и где концентрация иммуноглобулина в композиции выше 160 г/л, и pH составляет 5,5-5,9.
2. Жидкая композиция по п. 1, где концентрация иммуноглобулина составляет от выше 160 до 300 г/л, в частности 160-260 г/л.
3. Жидкая композиция по п. 1 или 2, где pH составляет 5,6-5,8.
4. Жидкая композиция по любому из пп. 1-3, отличающаяся тем, что
- концентрация иммуноглобулина в интервале от выше 160 до 180 г/л и динамическая вязкость в интервале 5-≤12 мПа*с;
- концентрация иммуноглобулина в интервале выше 180-220 г/л и динамическая вязкость >12-≤35 мПа*с; или
- концентрация иммуноглобулина в интервале выше 220-260 г/л и динамическая вязкость >35-≤100 мПа*с.
5. Жидкая композиция по любому из пп. 1-4, где общая концентрация стабилизирующей аминокислоты и модулирующей вязкость аминокислоты составляет в диапазоне 150-350 мМ, предпочтительно 200-300 мМ, в частности 225-275 мМ.
6. Жидкая композиция по любому из пп. 1-5, где концентрация стабилизирующей аминокислоты составляет 130-220 мМ, предпочтительно 150-200 мМ, предпочтительно 160-190 мМ, в частности 170-180 мМ.
7. Жидкая композиция по любому из пп. 1-6, где концентрация модулирующих вязкость аминокислот составляет 50-100 мМ, предпочтительно 60-90 мМ, предпочтительно 65-85 мМ, в частности 70-80 мМ.
8. Жидкая композиция по любому из пп. 1-7, где препарат имеет стабильность при хранении по меньшей мере 40 месяцев, предпочтительно по меньшей мере 60 месяцев при 2-8°C, более предпочтительно по меньшей мере 69 месяцев.
9. Жидкая композиция по любому из пп. 1-8, где композиция содержит ацетат натрия, предпочтительно, в интервале 10-30 мМ, более предпочтительно около 20 мМ, и/или хлорид натрия, предпочтительно в интервале 10-30 мМ, более предпочтительно около 20 мМ.
10. Жидкая композиция по любому из пп. 1-9, содержащая один или более наполнителей, выбранных из поверхностно-активного вещества, моющего средства или сахарида или их сочетания.
11. Жидкая композиция по любому из пп. 1-10, где композиция имеет титры гемагглютининов ≤16 для анти-A и ≤8 для анти-B при определении прямой пробой Кумбса.
12. Жидкая композиция по любому из пп. 1-11, где композицией является композиция иммуноглобулина G с содержанием иммуноглобулина G 185-215 г/л, значением pH 5,5-5,9 и динамической вязкостью >12 вплоть до 30 мПа*с, при составлении с 150-210 мМ глицина и 50-105 мМ аргинина.
13. Применение жидкой композиции по любому из пп. 1-12 для стабилизации иммуноглобулинов.
14. Способ составления жидкой композиции по любому из пп. 1-12, включающий стадии:
- получения композиции поликлонального иммуноглобулина с концентрацией иммуноглобулина выше 160 г/л,
- доведение pH композиции до значения в интервале 5,5-5,9.
- добавление стабилизирующей аминокислоты в форме глицина, и
- добавление модулирующей вязкость аминокислоты в форме аргинина.
| US 20130121991 A1, 16.05.2013 | |||
| US 4597966 A1, 01.07.1986 | |||
| Robert J Falconer, Stabilization of a monoclonal antibody during purification and formulation by addition of basic amino acid excipients, Journal of Chemical Technology & Biotechnology, 2011, 86, p.942-948 | |||
| ВЫСОКОКОНЦЕНТРИРОВАННЫЕ КОМПОЗИЦИИ АНТИТЕЛ И БЕЛКОВ | 2004 |
|
RU2332986C2 |
Авторы
Даты
2021-06-21—Публикация
2017-06-12—Подача