Изобретение относится к хроматографическому анализу химических соединений и может быть использовано для идентификации и выявления наркотических и психоактивных веществ, в частности, определения в трупной крови или в крови, отобранной у живого человека, этилглюкуронида - прямого метаболита/маркера алкоголя для диагностики факта употребления алкоголя и степени опьянения.
При интерпретации результатов определения этилглюкуронида (EtG) следует учитывать, что этанол элиминируется в кровь с определенной скоростью, а этилглюкуронид начинает накапливаться только через некоторое время после появления этанола в крови. В то же время, EtG определяется в биологических средах в течение нескольких часов после того, как этанол уже не определяется в крови. Поэтому результаты определения EtG используется для установления ретроспективы употребления этилового спирта, что крайне необходимо при судебно-медицинской экспертизе живых лиц и трупов, но не применимы для оперативного установления состояния опьянения.
Известен способ выявления и определения происхождения неизвестных веществ в спиртных напитках [RU 2392616, C1, G01N 30/02, 20.06.2010], при котором готовят пробу исследуемого напитка, подвергают ее ГХ/МС анализу, регистрируют масс-спектры и ассоциированные с ними хроматограммы и проводят распознавание компонентов сравнением с базой данных эталонных аналитических характеристик объекта, при этом, дополнительно готовят смесь стандартных веществ, и на ее основе готовят ряд модельных образцов путем введения стандартной смеси в интактный образец в разных концентрациях и анализируют образцы с известным введенным содержанием компонентов при температуре узла ввода 180°С, 250°С и 310°С, и при обнаружении в модельном образце неизвестное вещество квалифицируют как артефакт, образующийся при анализе, а при отсутствии его в модельных образцах готовят контрольный образец путем объединения всего ряда модельных образцов, анализируют его также при температуре узла ввода 180°С, 250°С и 310°С, регистрируют масс-спектры и ассоциированные с ними хроматограммы и при отсутствии в контрольном образце найденного неизвестного вещества его квалифицируют как маркер идентификации.
Недостатком способа является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения происхождения неизвестных веществ в суррогатных спиртсодержащих жидкостях или биологических объектах, содержащих летучие яды.
Известен также способ выявления неизвестных веществ в биологических жидкостях пациентов, принимавших наркотические или психотропные вещества [RU 241788, С2, G01N 30/02, 27.09.2010], при котором готовят пробу исследуемого образца, подвергают ее ГХ/МС анализу, регистрируют масс-спектры образца, и ассоциированные с ними хроматограммы и проводят распознавание вещества сравнением с базой данных эталонных аналитических характеристик веществ, при этом, готовят три пробы исследуемого образца биологической жидкости - первую путем экстракции с перерастворением, вторую путем кислотного гидролиза и третью путем ферментативного гидролиза, причем, первую пробу подвергают ГХ/МС анализу в режиме градиента температуры 15°С/мин и данные анализируют путем сравнения с базой данных, по которой выявляют признаки неизвестного вещества (НВ), а именно - спектры с m/z, совпадающими с базовыми ионами наркотического или психотропного вещества или метаболитов, и содержание (НВ) в пробе, вторую пробу подвергают ГХ/МС анализу в режиме градиента температуры 25°С/мин и третью пробу подвергают ГХ/МС анализу также в режиме градиента температуры 15°С/мин и при увеличении содержания НВ в последних двух пробах по сравнению с первой, подвергают ГХ/МС анализу также в режиме градиента температуры 15°С/мин базовое наркотическое или психотропное вещество на присутствие в нем НВ, и при его отсутствии в базовом веществе, проверяют присутствие НВ в интактной биологической жидкости, для чего пробу ее готовят путем кислотного гидролиза и подвергают ГХ/МС анализу в режимах градиента температуры 15°С/мин и 25°С/мин и в случае обнаружения НВ в интактной биологической жидкости его квалифицируют как эндогенное, а при отсутствии признаков аликвоту первой пробы смешивают с пробой интактной биологической жидкости, готовят пробу путем кислотного гидролиза смеси, подвергают пробу ГХ/МС анализу в режимах градиента температуры 15°С/мин и 25°С/мин, определяют содержание НВ по результатам обоих режимов анализа и сравнивают его с содержанием НВ в первой пробе и при совпадающих значениях содержания НВ в указанных трех пробах квалифицируют НВ как новый, ранее неизвестный продукт метаболизма базового наркотического или психотропного вещества.
Недостатком этого способа также является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения происхождения неизвестных веществ в биологических жидкостях пациентов.
Кроме того, известен способ идентификации наркотических и психоактивных веществ в биологических жидкостях [RU 2390771, С12, G01N 30/86, 27.05.2010], при котором готовят пробу исследуемого образца, пропускают ее через хроматографическую колонку с неподвижной жидкой фазой и регистрируют сигналы детектора в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу сравнением с эталонными аналитическими характеристиками вещества, при этом готовят две аликвоты пробы исследуемого образца - нативную и дериватизированную и каждую из них пропускают через колонку, по меньшей мере, в двух режимах кондиционирования параметров изменением градиента температуры, и, дополнительно, каждую из указанных аликвот пропускают через колонку с разделением потока при тех же режимах кондиционирования, далее регистрируют сигналы детектора на хроматограммах, выбирают на них пики со значениями асимметрии на 0,1, 0,5 и 0,6 высоты пика от основания ≤1,05, как наиболее соответствующие биномиальному распределению плотности вероятности и недеформированные влиянием фоновых компонентов, и идентифицируют определяемые вещества по отобранным пикам сопоставлением с эталонными аналитическими характеристиками определяемых веществ.
Недостатком этого технического решения является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения неизвестных веществ в организме человека на основе исследований его биологических жидкостей. Это сужает арсенал технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека или в условиях отсутствия его биологических жидкостей.
Помимо указанных выше, способ идентификации наркотических и психоактивных веществ в сложных биологических матрицах организма человека [RU 2705932, C1, G01N 30/86, 12.11.2019], согласно которому готовят образец биосубстрата человека в виде срезов волос или ногтевых пластин и осуществляют его первое предварительное масс-спектрометрическое исследование с регистрацией сигнала детектора масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу сравнением с эталонными аналитическими характеристиками вещества, при этом, после проведения первого предварительного масс-спектрометрического исследования последовательно проводят еще N последующих предварительных масс-спектрометрических исследований, перед каждым из которых образец биосубстрата промывают метанолом, при этом после проведения предварительных масс-спектрометрических исследований измельчают образец биосубстрата человека до состояния пудры до долей миллиметров и проводят заключительное масс-спектрометрическое исследование, причем если при последовательном проведении предварительных масс-спектрометрических исследований наблюдается последовательное уменьшение массы анализируемых веществ и существенное увеличение их массы при заключительном масс-спектрометрическом исследовании, то принимают решение об идентификации этих веществ в биосубстрате человека.
Особенностью этого технического решения является то, что, число (N+1) предварительных масс-спектрометрических исследований равно 6, при масс-спектрометрическом анализе используют один пластиковый флакон емкостью 50 мл, а при промывке образца биосубстрата внесение и отбор метанола из пластикового флакона используют разовые дозаторы, при предварительном масс-спектрометрическом анализе принимают во внимание принадлежность каждого пика анализируемого вещества при сравнении с эталонной аналитической характеристикой этого вещества при уменьшения его массы при последующем предварительном анализе относительно предыдущего предварительного анализа не менее 10%, о существенном увеличении массы анализируемого вещества при заключительном масс-спектрометрическом анализе судят относительно того вещества, масса которого при заключительном масс-спектрометрическом анализе превышает массу при последнем предварительном анализе не менее чем на 100%.
Недостатком этого технического решения является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения неизвестных веществ в организме человека через биосубстрат в виде срезов волос или ногтевых пластин.
Это сужает арсенал технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека, например, через образцы органов или мышечных тканей при отсутствии биологического материала другого вида.
Известен также идентификации наркотических и психоактивных веществ в биологических объектах [RU 2723907, C1, G01N 30/86, 18.06.2020], согласно которому образец биосубстрата человека в виде органа или фрагмента мышечной ткани измельчают до состояния гомогената и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, при этом, образец биосубстрата человека в виде гомогената перед хромато-спектрометрическим исследованием подвергают щелочному гидролизу и экстрагируют неполярным растворителем из щелочной среды для обеспечения оптимального соотношения сигнал/шум для целевых аналитов, затем полученный экстракт упаривают и при образовании вязкого маслянистого осадка его реэкстрагируют водным кислым раствором и далее целевые вещества извлекают из полученного водного раствора неполярным растворителем при щелочных значениях рН, а хромато-спектрометрическое исследование проводят в режиме регистрации SIM-спектров, причем, набор ионов для SIM-регистрации выбирают из условия выбора всех фрагментов масс-спектра с интенсивностью более 1%.
Недостатком наиболее близкого технического решения является его относительно узкая область применения, поскольку он предназначен для выявления и определения в организме человека через биосубстрат в виде органа или фрагмента мышечной ткани преимущественно фентанила, являющимся опиоидным анальгетикоми и мощным агонист μ-опиоидным рецептором, а также близких к нему по химическому строению и свойствам (слабополярных, устойчивых к щелочному гидролизу) 3-метилфенанила, карфентанила, ЛСД, трамадола, кетамина, промедола, диазепама и т.п.
Это сужает арсенал технических средств, которые могут быть использованы для определения в крови (в трупной крови или крови, отобранной у живого человека) этилглюкуронида - прямого метаболита/маркера алкоголя для диагностики факта употребления алкоголя и степени опьянения.
Наиболее близким по технической сущности к предложенному является способ идентификации этилглюкуронида в крови, не имеющей гнилостные изменения [Lena Kristoffersen, Veronica Н. Liane, Olav Spigset. EtG and EtS in Autopsy Blood Samples With and Without Putrefaction Using UPLC-MS-MS Solfrid Hegstadl. Published by Oxford University Press. Journal of Analytical Toxicology, 2017; 41:107-113], в соответствии с которым готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, при этом, для подготовки образца биосубстрата в кровь добавляют метанол, производят центрифугирование, отделяют органические фракции, упаривают их и добавляют воду, после чего проводят хромато-спектрометрическое исследование.
Недостатком наиболее близкого технического решения является относительно узкая область применения, обусловленная тем, что исходная кровь не должна иметь гнилостных изменений, поскольку при их наличии снижается до недопустимой точность идентификации этилглюкуронида в крови.
Это сужает арсенал технических средств, которые могут быть использованы для определения в крови (в трупной крови или крови, отобранной у живого человека) этилглюкуронида - прямого метаболита/маркера алкоголя для диагностики факта употребления алкоголя и степени опьянения.
Задачей, которая решается в изобретении, является разработка способа выявления и идентификации в организме человека этилглюкуронида с использованием в качестве объекта исследований трупной крови или крови, отобранной у живого человека, который обладает более высокой точностью идентификации.
Требуемый технический результат заключается в повышении точности идентификации этилглюкуронида в трупной крови или крови, отобранной у живого человека.
Поставленная задача решается, а требуемый технический результат достигается тем, что, в способе, согласно которому готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, согласно изобретению, для подготовки образца биосубстрата 200 мкл крови ввводят во флакон с плоским дном (пенициллиновый флакон) и высушивают при 100°С в течение 7 минут с целью денатурации белков и удаления влаги из образца, а затем его охлаждают до комнатной температуры, добавляют 250 мкл метанола, закрывают крышкой, встряхивают на вибромиксере в течение 2 мин, полученный экстракт переносят в виалу и реконструируют 100 мкл деионизированной воды, после чего 5 мкл экстракта вводят в хроматограф.
Кроме того, требуемый технический результат достигается тем, что, перед реконструированием 100 мкл деионизированной воды проводят упаривание.
На чертеже представлены:
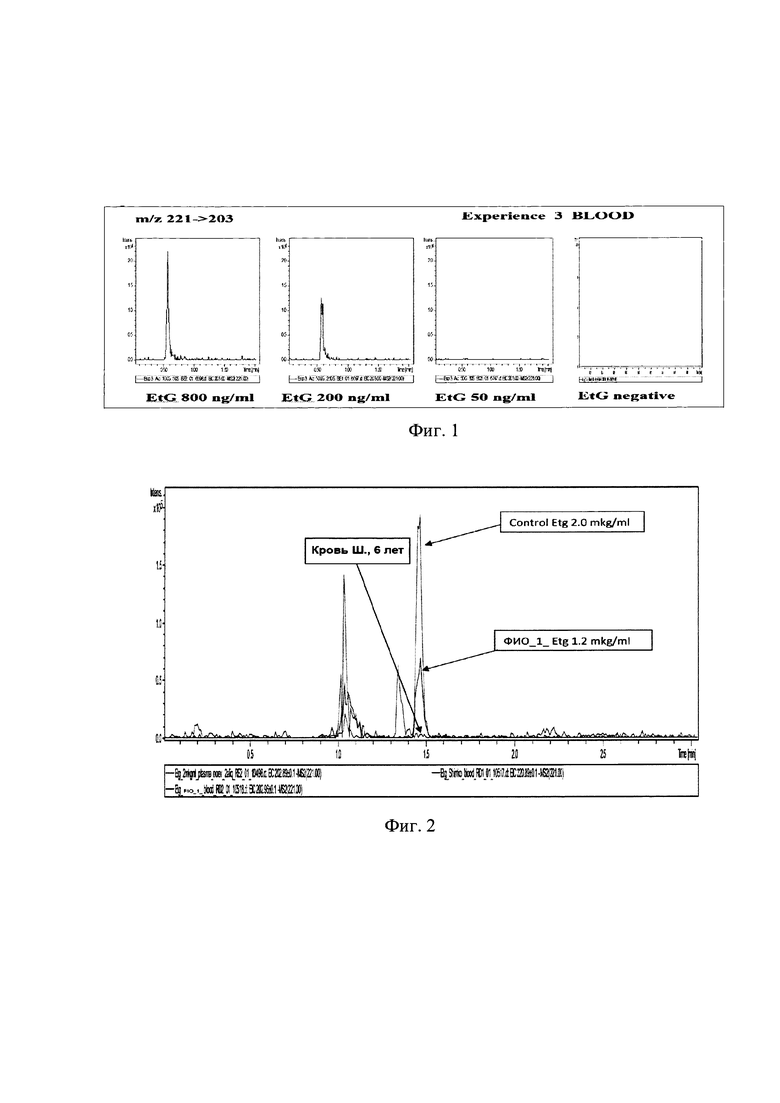
- на фиг. 1 - хроматограммы серии градуировочных измерений на приборе Toxtyper Bruker растворов этилглюкуронида, приготовленных на основе цельной крови (колонка Acclaim RSLC 120 С18, 120А 2.1×100 mm, 2.2 urn (Dionex);
- на фиг. 2 - хроматографические профили (Toxtyper Bruker, колонка Acclaim RSLC 120 С18, 120А 2.1×100 mm, 2.2 μm) по иону-прекурсору этилглюкуронида m/z 221 (М-Н) - экстракта образца крови от трупа Ш., муж. 6 лет, калибровочного образца EtG 2,0 мкг/мл и крови, положительной по этилглюкурониду (кровь от трупа ФИО_1_), содержание этанола в крови от трупа Ш., 6 лет составило 1,34%, обзорный анализ, проведенный на приборе Toxtyper Bruker, показал отсутствие этилглюкуронида в крови Ш., 6 лет;
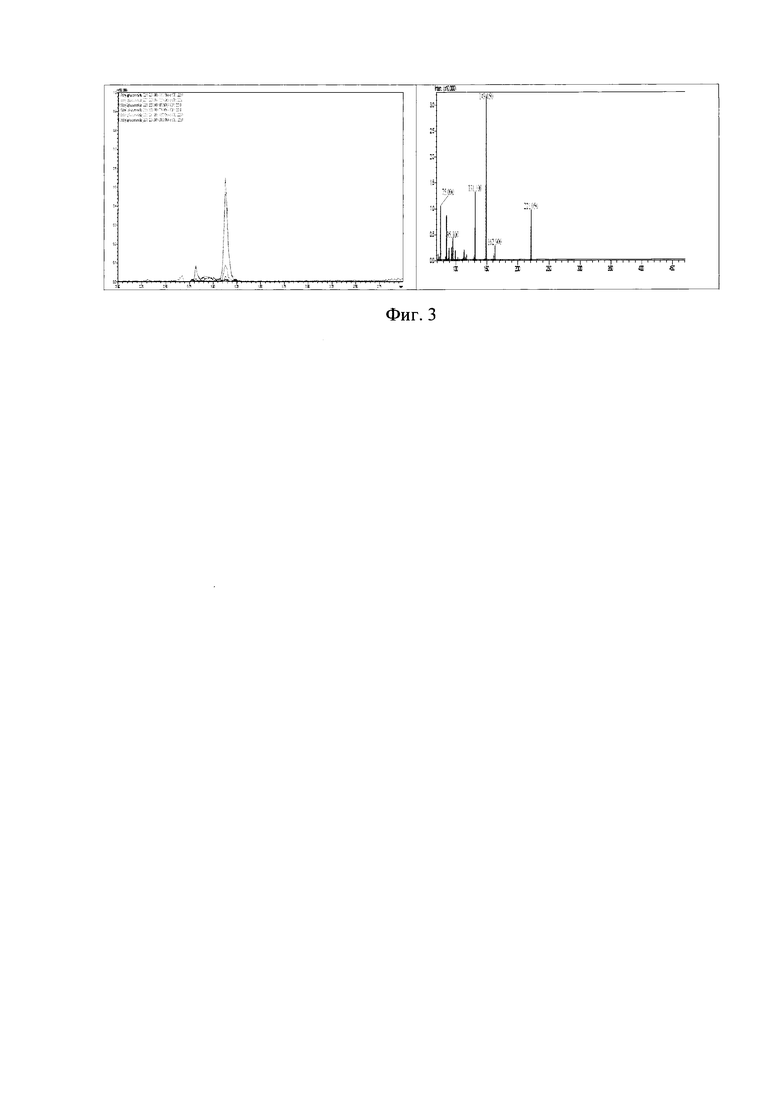
- на фиг. 3 - хроматографический профиль экстракта крови от живого человека ФИО_2_, употреблявшего этиловый алкоголь на приборе Shimadzu 8050 (хроматографическая колонка Agilent Eclipse С18, 2.1×100 mm 1.8 μm), содержание этанола 0,3 г/л, этилглюкуронида 0.7 мкг/мл, профиль по MRM: m/z 221 - 113, 221 - 129, 221 - 85, 221 - 75 и спектр, соответствующий этилглюкурониду, ион m/z 149 - фоновый, характерен для эфиров фталевой кислоты.
Способ идентификации этилглюкуронида в крови осуществляется следующим образом.
200 мкл крови вводят во флакон с плоским дном (пенициллиновый флакон) и высушивают при 100°С в течение 7 минут. При этом происходит денатурация белков и удаление влаги из образца. После охлаждения до комнатной температуры добавляют 250 мкл метанола, закрывают крышкой и встряхивают на вибромиксере 2 мин. Экстракт получается прозрачным и почти бесцветным, его переносят в виалу, упаривают и реконструируют 100 мкл деионизированной воды. 5 мкл экстракта вводят в хроматограф.
Допускается вводить в хроматограф непосредственно метанольный экстракт, при этом возможно ухудшение качества хроматографических пиков.
Далее проводят хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме проводят с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества.
Важнейшей операцией, существенно определяющая повышение точности идентификации, является высушивание при 100°С в течение 7 минут, поскольку в этом случае белковая грязь коагулирует и ее влияние на точность идентификации резко снижается.
Таким образом, в предложенном способе достигается требуемый технический результат, который заключается в повышении точности идентификации, с одновременным расширением арсенала технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека с одновременным повышением чувствительности и точности определения этилглюкуронида в крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ идентификации этилглюкуронида в сухих пятнах крови | 2020 |
|
RU2740269C1 |
| Способ идентификации наркотических и психоактивных веществ в биосубстрате человека | 2019 |
|
RU2723907C1 |
| Способ идентификации наркотических и психоактивных веществ в сложных биологических матрицах организма человека | 2019 |
|
RU2705932C1 |
| СПОСОБ ВЫЯВЛЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ПАЦИЕНТОВ, ПРИНИМАВШИХ НАРКОТИЧЕСКИЕ ИЛИ ПСИХОАКТИВНЫЕ ВЕЩЕСТВА | 2009 |
|
RU2419788C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ НАРКОТИЧЕСКИХ И ПСИХОАКТИВНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2009 |
|
RU2390771C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СПИРТОВ В БИОЛОГИЧЕСКИХ ТКАНЯХ И ВЫДЕЛЕНИЯХ ОРГАНИЗМА ЧЕЛОВЕКА | 2012 |
|
RU2516344C1 |
| СПОСОБ ВЫЯВЛЕНИЯ И ОПРЕДЕЛЕНИЯ ПРОИСХОЖДЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В СПИРТНЫХ НАПИТКАХ | 2009 |
|
RU2392616C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РОДА ВОЗБУДИТЕЛЕЙ БАКТЕРИЕМИЙ | 2011 |
|
RU2495939C2 |
| СПОСОБ КАЛИБРОВКИ СИСТЕМЫ ГАЗОВОЙ ХРОМАТОГРАФИИ - МАСС СПЕКТРОМЕТРИИ (ГХ-МС), ОСНАЩЕННОЙ СПЕЦИАЛЬНЫМ ПО, ДЛЯ ОПРЕДЕЛЕНИЯ МАРКЕРОВ МИКРООРГАНИЗМОВ В ИССЛЕДУЕМОЙ ПРОБЕ МАТЕРИАЛА БИОЛОГИЧЕСКОГО ПРОИСХОЖДЕНИЯ | 2012 |
|
RU2501011C2 |
| ПРОТЕОТИПИЧЕСКИЙ ПЕПТИД Q9Y4W6-02 И СПОСОБ МАСС-СПЕКТРОМЕТРИЧЕСКОГО АНАЛИЗА СОДЕРЖАНИЯ AFG3-ПОДОБНОГО БЕЛКА ЧЕЛОВЕКА НА ЕГО ОСНОВЕ | 2012 |
|
RU2673551C2 |
Изобретение относится к медицине, а именно к лабораторной диагностике, и может быть использовано при осуществлении пробоподготовки для идентификации этилглюкуронида в крови. Готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества. Для подготовки образца биосубстрата 200 мкл крови вводят во флакон с плоским дном и высушивают при 100°С в течение 7 минут с целью денатурации белков и удаления влаги из образца. Затем его охлаждают до комнатной температуры, добавляют 250 мкл метанола, закрывают крышкой, встряхивают на вибромиксере в течение 2 мин. Полученный экстракт переносят в виалу и добавляют 100 мкл деионизированной воды. После чего 5 мкл экстракта вводят в хроматограф. Способ обеспечивает возможность повышения точности идентификации этилглюкуронида в трупной крови или крови, отобранной у живого человека, за счет проведения хромато-спектрометрического исследования с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме, в котором важнейшей операцией, существенно определяющей повышение точности идентификации, является высушивание образца при 100°С в течение 7 минут, поскольку в этом случае белковая грязь коагулирует и ее влияние на точность идентификации резко снижается. 1 з.п. ф-лы, 3 ил.
1. Способ пробоподготовки для идентификации этилглюкуронида в крови, согласно которому готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, отличающийся тем, что для подготовки образца биосубстрата 200 мкл крови вводят во флакон с плоским дном и высушивают при 100°С в течение 7 минут с целью денатурации белков и удаления влаги из образца, а затем его охлаждают до комнатной температуры, добавляют 250 мкл метанола, закрывают крышкой, встряхивают на вибромиксере в течение 2 мин, полученный экстракт переносят в виалу и добавляют 100 мкл деионизированной воды, после чего 5 мкл экстракта вводят в хроматограф.
2. Способ по п. 1, отличающийся тем, что перед добавлением в полученный экстракт 100 мкл деионизированной воды проводят его упаривание.
| САВЧУК С.А | |||
| и др | |||
| Обнаружение и количественное определение летучих токсичных веществ и гликолей в биологических объектах методами газовой хроматографии и хромато-масс-спектрометрии | |||
| Информационное письмо | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Способ идентификации этилглюкуронида в сухих пятнах крови | 2020 |
|
RU2740269C1 |
| CN 107664664 B, 01.09.2020 | |||
| CN 111487329 A, 04.08.2020 | |||
| Способ восстановления кожного покрова при обширных глубоких ожогах | 2018 |
|
RU2671642C1 |
| US 8168402 | |||
Авторы
Даты
2021-06-28—Публикация
2020-08-12—Подача