Изобретение относится к хроматографическому анализу химических соединений и может быть использовано для идентификации и выявления наркотических и психоактивных веществ, в частности, определения в сухих пятнах крови этилглюкуронида - прямого метаболита/маркера алкоголя для диагностики факта употребления алкоголя и степени опьянения.
Известен способ выявления и определения происхождения неизвестных веществ в спиртных напитках [RU 2392616, C1, G01N 30/02, 20.06.2010], при котором готовят пробу исследуемого напитка, подвергают ее ГХ/МС анализу, регистрируют масс-спектры и ассоциированные с ними хроматограммы и проводят распознавание компонентов сравнением с базой данных эталонных аналитических характеристик объекта, при этом, дополнительно готовят смесь стандартных веществ, и на ее основе готовят ряд модельных образцов путем введения стандартной смеси в интактный образец в разных концентрациях и анализируют образцы с известным введенным содержанием компонентов при температуре узла ввода 180°С, 250°С и 310°С, и при обнаружении в модельном образце неизвестное вещество квалифицируют как артефакт, образующийся при анализе, а при отсутствии его в модельных образцах готовят контрольный образец путем объединения всего ряда модельных образцов, анализируют его также при температуре узла ввода 180°С, 250°С и 310°С, регистрируют масс-спектры и ассоциированные с ними хроматограммы и при отсутствии в контрольном образце найденного неизвестного вещества его квалифицируют как маркер идентификации.
Недостатком способа является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения происхождения неизвестных веществ в суррогатных спиртсодержащих жидкостях или биологических объектах, содержащих летучие яды.
Известен также способ выявления неизвестных веществ в биологических жидкостях пациентов, принимавших наркотические или психотропные вещества [RU 241788, С2, G01N 30/02, 27.09.2010], при котором готовят пробу исследуемого образца, подвергают ее ГХ/МС анализу, регистрируют масс-спектры образца, и ассоциированные с ними хроматограммы и проводят распознавание вещества сравнением с базой данных эталонных аналитических характеристик веществ, при этом, готовят три пробы исследуемого образца биологической жидкости -первую путем экстракции с перерастворением, вторую путем кислотного гидролиза и третью путем ферментативного гидролиза, причем, первую пробу подвергают ГХ/МС анализу в режиме градиента температуры 15°С/мин и данные анализируют путем сравнения с базой данных, по которой выявляют признаки неизвестного вещества (НВ), а именно - спектры с m/z, совпадающими с базовыми ионами наркотического или психотропного вещества или метаболитов, и содержание (НВ) в пробе, вторую пробу подвергают ГХ/МС анализу в режиме градиента температуры 25°С/мин и третью пробу подвергают ГХ/МС анализу также в режиме градиента температуры 15°С/мин и при увеличении содержания НВ в последних двух пробах по сравнению с первой, подвергают ГХ/МС анализу также в режиме градиента температуры 15°С/мин базовое наркотическое или психотропное вещество на присутствие в нем НВ, и при его отсутствии в базовом веществе, проверяют присутствие НВ в интактной биологической жидкости, для чего пробу ее готовят путем кислотного гидролиза и подвергают ГХ/МС анализу в режимах градиента температуры 15°С/мин и 25°С/мин и в случае обнаружения НВ в интактной биологической жидкости его квалифицируют как эндогенное, а при отсутствии признаков аликвоту первой пробы смешивают с пробой интактной биологической жидкости, готовят пробу путем кислотного гидролиза смеси, подвергают пробу ГХ/МС анализу в режимах градиента температуры 15°С/мин и 25°С/мин, определяют содержание НВ по результатам обоих режимов анализа и сравнивают его с содержанием НВ в первой пробе и при совпадающих значениях содержания НВ в указанных трех пробах квалифицируют НВ как новый, ранее неизвестный продукт метаболизма базового наркотического или психотропного вещества.
Недостатком этого способа также является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения происхождения неизвестных веществ в биологических жидкостях пациентов.
Кроме того, известен способ идентификации наркотических и психоактивных веществ в биологических жидкостях [RU 2390771, С12, G01N 30/86, 27.05.2010], при котором готовят пробу исследуемого образца, пропускают ее через хроматографическую колонку с неподвижной жидкой фазой и регистрируют сигналы детектора в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу сравнением с эталонными аналитическими характеристиками вещества, при этом готовят две аликвоты пробы исследуемого образца - нативную и дериватизированную и каждую из них пропускают через колонку, по меньшей мере, в двух режимах кондиционирования параметров изменением градиента температуры, и, дополнительно, каждую из указанных аликвот пропускают через колонку с разделением потока при тех же режимах кондиционирования, далее регистрируют сигналы детектора на хроматограммах, выбирают на них пики со значениями асимметрии на 0,1, 0,5 и 0,6 высоты пика от основания ≤1,05, как наиболее соответствующие биномиальному распределению плотности вероятности и недеформированные влиянием фоновых компонентов, и идентифицируют определяемые вещества по отобранным пикам сопоставлением с эталонными аналитическими характеристиками определяемых веществ.
Недостатком этого технического решения является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения неизвестных веществ в организме человека на основе исследований его биологических жидкостей. Это сужает арсенал технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека или в условиях отсутствия его биологических жидкостей.
Помимо казанных выше, способ идентификации наркотических и психоактивных веществ в сложных биологических матрицах организма человека [RU 2705932, C1, G01N 30/86, 12.11.2019], согласно которому готовят образец биосубстрата человека в виде срезов волос или ногтевых пластин и осуществляют его первое предварительное масс-спектрометрическое исследование с регистрацией сигнала детектора масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу сравнением с эталонными аналитическими характеристиками вещества, при этом, после проведения первого предварительного масс-спектрометрического исследования последовательно проводят еще N последующих предварительных масс-спектрометрических исследований, перед каждым из которых образец биосубстрата промывают метанолом, при этом после проведения предварительных масс-спектрометрических исследований измельчают образец биосубстрата человека до состояния пудры до долей миллиметров и проводят заключительное масс-спектрометрическое исследование, причем если при последовательном проведении предварительных масс-спектрометрических исследований наблюдается последовательное уменьшение массы анализируемых веществ и существенное увеличение их массы при заключительном масс-спектрометрическом исследовании, то принимают решение об идентификации этих веществ в биосубстрате человека.
Особенностью этого технического решения является то, что, число (N+1) предварительных масс-спектрометрических исследований равно 6, при масс-спектрометрическом анализе используют один пластиковый флакон емкостью 50 мл, а при промывке образца биосубстрата внесение и отбор метанола из пластикового флакона используют разовые дозаторы, при предварительном масс-спектрометрическом анализе принимают во внимание принадлежность каждого пика анализируемого вещества при сравнении с эталонной аналитической характеристикой этого вещества при уменьшения его массы при последующем предварительном анализе относительно предыдущего предварительного анализа не менее 10%, о существенном увеличении массы анализируемого вещества при заключительном масс-спектрометрическом анализе судят относительно того вещества, масса которого при заключительном масс-спектрометрическом анализе превышает массу при последнем предварительном анализе не менее чем на 100%.
Недостатком этого технического решения является его относительно узкая область применения, поскольку он предназначен, преимущественно, для выявления и определения неизвестных веществ в организме человека через биосубстрат в виде срезов волос или ногтевых пластин.
Это сужает арсенал технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека, например, через образцы органов или мышечных тканей при отсутствии биологического материала другого вида.
Наиболее близким по технической сущности к предложенному является способ идентификации наркотических и психоактивных веществ в биологических объектах [RU 2723907, C1, G01N 30/86, 18.06.2020], согласно которому образец биосубстрата человека в виде органа или фрагмента мышечной ткани измельчают до состояния гомогената и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, при этом, образец биосубстрата человека в виде гомогената перед хромато-спектрометрическим исследованием подвергают щелочному гидролизу и экстрагируют неполярным растворителем из щелочной среды для обеспечения оптимального соотношения сигнал/шум для целевых аналитов, затем полученный экстракт упаривают и при образовании вязкого маслянистого осадка его реэкстрагируют водным кислым раствором и далее целевые вещества извлекают из полученного водного раствора неполярным растворителем при щелочных значениях рН, а хромато-спектрометрическое исследование проводят в режиме регистрации SIM-спектров, причем, набор ионов для SIM-регистрации выбирают из условия выбора всех фрагментов масс-спектра с интенсивностью более 1%.
Недостатком наиболее близкого технического решения является его относительно узкая область применения, поскольку он предназначен для выявления и определения в организме человека через биосубстрат в виде органа или фрагмента мышечной ткани преимущественно фентанила, являющимся опиоидным анальгетикоми и мощным агонист μ-опиоидным рецептором, а также близких к нему по химическому строению и свойствам (слабополярных, устойчивых к щелочному гидролизу) 3-метилфенанила, карфентанила, ЛСД, трамадола, кетамина, промедола, диазепама и т.п.
Это сужает арсенал технических средств, которые могут быть использованы для определения в сухих пятнах крови этилглюкуронида - прямого метаболита/маркера алкоголя для диагностики факта употребления алкоголя и степени опьянения.
Задачей, которая решается в изобретении, является разработка способа выявления и идентификации в организме человека этилглюкуронида с использованием в качестве объекта исследований сухих пятен крови на мягких и твердых носителях с целью расширения арсенала технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ.
Требуемый технический результат заключается в расширении арсенала технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека с одновременным повышением чувствительности и точности определения этилглюкуронида в сухих пятнах крови.
Поставленная задача решается, а требуемый технический результат достигается тем, что, в способе, согласно которому готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, согласно изобретению, для подготовки образца биосубстрата для хромато-спектрометрического исследования из исходного материала в виде сухого пятна крови на мягком носителе вырезают круг с диаметром 1,5 см с последующим измельчением или с поверхности исходного материала в виде сухого пятна крови на твердом носителе соскабливают сухое пятно крови диаметром 1,5 см, и помещают образец биосубстрата в виалу или пробирку, добавляют 1,0 мл метанола, встряхивают на вибромиксере 2 минуты и переносят органический слой в сухую чистую виалу, упаривают досуха в токе воздуха при 40-60°С, к сухому остатку добавляют 100 мкл деионизованной воды, центрифугируют 5 минут при 14 000 об/мин и 5 мк полученного супернатанта вводят в хроматограф.
На чертеже представлены:
на фиг.1 - сухие пятна крови на различных носителях: (а) - вискоза; (б) - хлопок; (в) - предметы одежды; (г) - шерстяной трикотаж (слева) и джинсовая ткань (справа); (д) - резиновый автомобильный коврик;(е) - обувь из кожзаменителя; (ж) - кожа; (з) - линолеум;
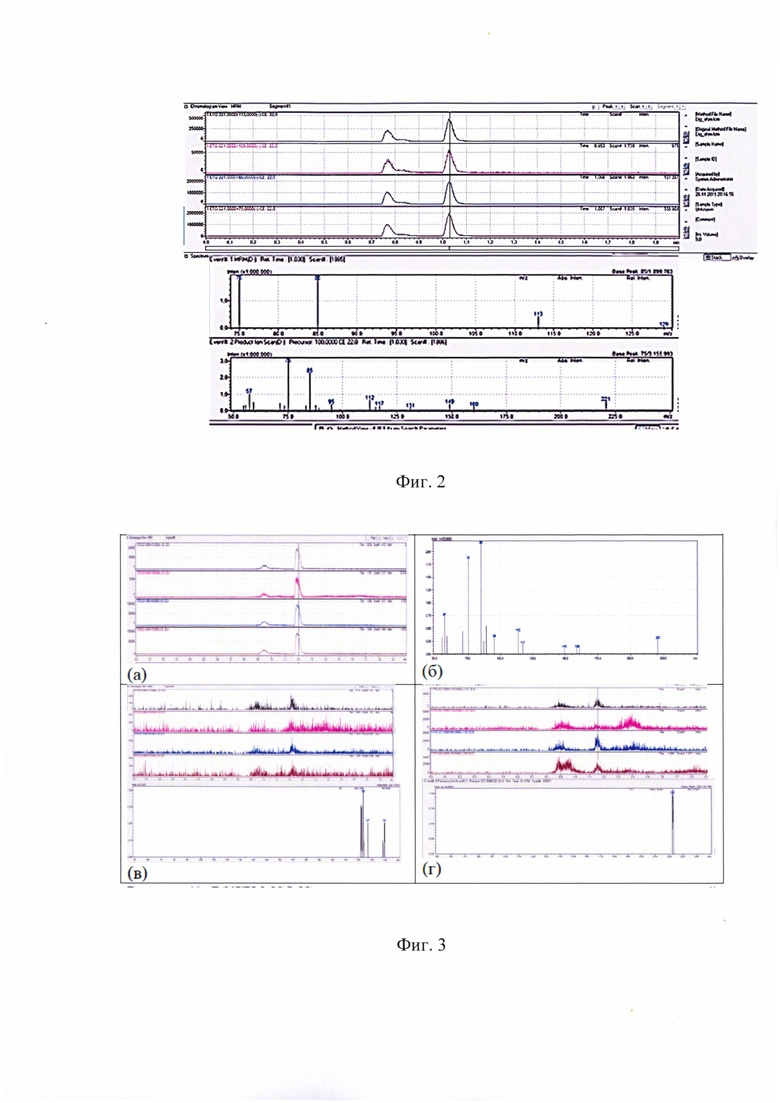
на фиг.2 - представлены хроматографические профили, полученные методом ВЭЖХ-МС/МС, хроматографические профили по MRM: m/z 221 - 113, 221 - 129, 221 - 85, 221 -75 метанольного экстракта сухого пятна из 200 мкл гнилостно измененной трупной крови, этанол 3,1 г/л, положительная по этилглюкурониду, с джинсовой ткани, после 2 дней хранения в помещении при комнатной температуре и естественной влажности, масс-спектр, соответствующий масс-спектру этилглюкуронида, ВЭЖХ-МС/МС система Shimadzu 8050, хроматографическая колонка Agilent Eclipse С18, 2.1×100 mm 1.8 μm. определении этилглюкуронида в сухих пятнах крови на предметах одежды;
на фиг.3 - ВЭЖХ-МС/МС исследование метанольных экстрактов сухих пятен трупной крови, хроматографические профили на приборе Shimadzu 8050, хроматографическая колонка Agilent Eclipse С18, 2.1×100 mm 1.8 μm, результаты определения EtG методом ВЭЖХ-МС/МС указывают на то, что этанол не был употреблен прижизненно, (а) - «положительный контроль»: метанольный экстракт сухого пятна из 200 мкл трупной крови, этанол 3,1 г/л, положительной по этилглюкуронид, джинсовая ткань после 5,5 месяцев хранения в закрытом пластиковом пакете при комнатной температуре и естественной влажности, в условиях, аналогичных условиям хранения исследуемых вещественных доказательств, ррофили по MRM: m/z 221-113, 221-129, 221-85, 221-75, (б) - «положительный контроль»: масс-спектр хроматографического пика со временем удерживания 1.2 мин, соответствующий масс-спектру этилглюкуронида, (в) - метанольный экстракт сухого пятна трупной крови С, 7 лет с хлопчатобумажной трикотажной ткани (футболка), до начала исследования вещественные доказательства были на хранении 6 месяцев в закрытом пластиковом пакете при комнатной температуре и естественной влажности, в крови ранее был выявлен этанол в концентрации 0,5 г/л, профили по MRM: m/z 221 - 113, 221 - 129, 221 - 85, 221 - 75 и масс-спектр по времени удерживания 1.2 мин, этилглюкуронид отсутствует, (б) - метанольный экстракт сухого пятна трупной крови С., 7 лет с плащевой ткани (куртка), до начала исследования вещественные доказательства были на хранении 6 месяцев в закрытом пластиковом пакете при комнатной температуре и естественной влажности, в крови ранее был выявлен этанол в концентрации 0,5 г/л, профили по MRM: m/z 221 - 113, 221 - 129, 221 - 85, 221 - 75 и масс-спектр по времени удерживания 1.2 мин, этилглюкуронид отсутствует.
Способ идентификации этилглюкуронида в сухих пятнах крови реализуется следующим образом.
В серии экспериментов, проведенных на значительной выборке материала и на различных носителях: ткань (вискоза, полиэстер, хлопок, шерсть), кожзаменитель, натуральная кожа, бумага, резина, стекло - показана возможность определения этилглюкуронида в сухих пятнах крови на объектах вещественных доказательств. Для исследования использовали четыре образца трупной крови с гнилостными изменениями, содержащие этанол в концентрациях: 3.3, 3.1, 3.1 и 1.5 г/л. Сухие пятна крови, нанесенные на шерстяной трикотаж, резиновый автомобильный коврик, обувь из кожзаменителя, натуральную кожу, линолеум, выдерживали два дня, пять дней и неделю в помещении при комнатной температуре и естественной влажности, после чего анализировали. При повторных анализах не наблюдали значимых потерь этилглюкуронида. Сухое пятно крови диаметром 1,5 см, ориентировочно соответствующее 200-300 мкл, вырезают и при необходимости измельчают (бумага, ткань, кожзаменитель, кожа) или соскабливают с твердой поверхности (стекло, резина, пластмасса). Помещают в виалу или пробирку, добавляют 1,0 мл метанола, встряхивают на вибромиксере 2 минуты. Переносят органический слой в сухую чистую виалу, упаривают досуха в токе воздуха при 40-60°С. К сухому остатку добавляют 100 мкл деионизованной воды, центрифугируют 5 минут при 14 000 об/мин, 5 мкл супернатанта вводят в хроматограф.
Допускается вводить в хроматограф непосредственно метанольный экстракт, но при этом возможно ухудшение качества хроматографических пиков.
Сухие пятна крови на сорбенте - носителе вырезают (при необходимости измельчают) и помещают во флаконы для фильтрации/центрифугирования. Диаметр пор фильтра 0.22 μm. К образцам добавляют 60 мкл водного раствора глюконовой кислоты концентрацией 200 ммоль/л. После 1 ч инкубирования при комнатной температуре в течение 10 мин при 1500g отбирают 20 мкл фильтрованного образца и добавляют к нему 5 мкл водного раствора TbCl3, центрифугируют при 10 мин при 10000g, 5 мкл надосадочной жидкости вводят в хроматограф.
Хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме проводят с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества.
Таким образом, в предложенном способе достигается требуемый технический результат, который заключается в расширении арсенала технических средств, которые могут быть использованы для идентификации наркотических и психоактивных веществ в организме человека с одновременным повышением чувствительности и точности определения этилглюкуронида в сухих пятнах крови.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ идентификации этилглюкуронида в крови | 2020 |
|
RU2750408C1 |
| Способ идентификации наркотических и психоактивных веществ в биосубстрате человека | 2019 |
|
RU2723907C1 |
| Способ идентификации наркотических и психоактивных веществ в сложных биологических матрицах организма человека | 2019 |
|
RU2705932C1 |
| СПОСОБ ВЫЯВЛЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ ПАЦИЕНТОВ, ПРИНИМАВШИХ НАРКОТИЧЕСКИЕ ИЛИ ПСИХОАКТИВНЫЕ ВЕЩЕСТВА | 2009 |
|
RU2419788C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ НАРКОТИЧЕСКИХ И ПСИХОАКТИВНЫХ ВЕЩЕСТВ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ | 2009 |
|
RU2390771C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СПИРТОВ В БИОЛОГИЧЕСКИХ ТКАНЯХ И ВЫДЕЛЕНИЯХ ОРГАНИЗМА ЧЕЛОВЕКА | 2012 |
|
RU2516344C1 |
| СПОСОБ ВЫЯВЛЕНИЯ И ОПРЕДЕЛЕНИЯ ПРОИСХОЖДЕНИЯ НЕИЗВЕСТНЫХ ВЕЩЕСТВ В СПИРТНЫХ НАПИТКАХ | 2009 |
|
RU2392616C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РОДА ВОЗБУДИТЕЛЕЙ БАКТЕРИЕМИЙ | 2011 |
|
RU2495939C2 |
| Способ одновременного количественного определения стойких хлорорганических пестицидов в шерсти животных методом газовой хромато-масс-спектрометрии | 2022 |
|
RU2806370C1 |
| Способ количественного определения ликарбазепина в плазме крови | 2017 |
|
RU2660364C1 |

Изобретение относится к медицине и касается способа идентификации этилглюкуронида в сухих пятнах крови, согласно которому готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, где для подготовки образца биосубстрата для хромато-спектрометрического исследования из исходного материала в виде сухого пятна крови на мягком носителе вырезают круг диаметром 1,5 см с последующим измельчением или с поверхности исходного материала в виде сухого пятна крови на твердом носителе соскабливают сухое пятно крови диаметром 1,5 см, и помещают образец биосубстрата в виалу или пробирку, добавляют 1,0 мл метанола, встряхивают на вибромиксере 2 минуты и переносят органический слой в сухую чистую виалу, упаривают досуха в токе воздуха при 40-60°С, к сухому остатку добавляют 100 мкл деионизованной воды, центрифугируют 5 минут при 14 000 об/мин и 5 мкл полученного супернатанта вводят в хроматограф. Изобретение обеспечивает повышение чувствительности и точности определения этилглюкуронида в сухих пятнах крови. 3 ил., 1 пр.
Способ идентификации этилглюкуронида в сухих пятнах крови, согласно которому готовят образец биосубстрата и осуществляют его хромато-спектрометрическое исследование с регистрацией сигнала масс-спектрометра в виде профиля пиков анализируемых веществ на хроматограмме с последующим определением принадлежности каждого пика анализируемому веществу и сравнением с эталонными аналитическими характеристиками искомого вещества, отличающийся тем, что для подготовки образца биосубстрата для хромато-спектрометрического исследования из исходного материала в виде сухого пятна крови на мягком носителе вырезают круг диаметром 1,5 см с последующим измельчением или с поверхности исходного материала в виде сухого пятна крови на твердом носителе соскабливают сухое пятно крови диаметром 1,5 см, и помещают образец биосубстрата в виалу или пробирку, добавляют 1,0 мл метанола, встряхивают на вибромиксере 2 минуты и переносят органический слой в сухую чистую виалу, упаривают досуха в токе воздуха при 40-60°С, к сухому остатку добавляют 100 мкл деионизованной воды, центрифугируют 5 минут при 14 000 об/мин и 5 мкл полученного супернатанта вводят в хроматограф.
| Способ идентификации наркотических и психоактивных веществ в биосубстрате человека | 2019 |
|
RU2723907C1 |
| Способ идентификации наркотических и психоактивных веществ в сложных биологических матрицах организма человека | 2019 |
|
RU2705932C1 |
| US 2006240496 A1, 26.10.2006 | |||
| US 2006019400 A1, 26.01.2006 | |||
| HEGSTAD S., et al., EtG/EtS in Serum by UHPLC-MS-MS in Suspected Sexual Assault Cases.J Anal Toxicol | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2021-01-12—Публикация
2020-08-04—Подача