Область техники
Изобретение относится к биомаркерной композиции для оценки старения кожи с использованием гиалуронана и протеогликан сшивающего белка 1 (HAPLN1), и фармацевтической композиции для профилактики и уменьшения старения кожи, косметической композиции и функциональной оздоровительной пищевой продукции.
Уровень техники
Одним из наиболее очевидных симптомов старения кожи является уменьшение внеклеточного матрикса дермы, вызывающее морщины. Внеклеточный матрикс слоя дермы включает различные белки, такие как коллаген, эластин и гликопротеин, в качестве основных компонентов. Среди указанных белков коллаген составляет более 90% и около 90% коллагена является коллагеном I типа. Около 70% уменьшения количества коллагена I типа, вызванного старением, обнаруживают во внеклеточном матриксе дермы.
Гиалуроновая кислота, которая представляет собой полисахарид, состоящий из аминосахаров и уроновой кислоты, распределена во всех тканях живого организма, и около 50% общего количества в организме распределено в коже. Гиалуроновая кислота может связывать до 1000 крат своей массы в воде и заполняет внеклеточный матрикс ткани дермы. Кроме того, гиалуроновая кислота может образовывать агрегаты различных гликопротеинов и протеогликанов для хранения или сохранения в них различных факторов роста. В соответствии с результатами клинических исследований, гиалуроновая кислота увеличивает пролиферацию фибробластов, продукцию коллагена и секрецию факторов роста, и известно, что уровень гиалуроновой кислоты с возрастом снижается более чем на 40%.
Старение кожи происходит двумя путями: внутреннее старение и внешнее старение. Внешнее старение кожи, главным образом вызывается факторами внешней окружающей среды, такими как ультрафиолетовое излучение (УФ) и курение, и внутреннее старение кожи ассоциировано с возрастом. Хотя сообщают, что в настоящее время для предотвращения внешнего старения кожи имеются различные методы, например, использование УФ–блокирующей косметики, способы профилактики внутреннего старения до настоящего времени еще не разработаны. Следовательно, требуются попытки предотвратить или уменьшить внутреннее старение кожи.
Описание вариантов осуществления изобретения
Техническая задача
Изобретение относится к биомаркерной композиции для оценки старения кожи.
Изобретение относится к набору для оценки старения кожи.
Изобретение относится к способу скрининга средства, уменьшающего старение кожи.
Изобретение относится к фармацевтической композиции для профилактики или уменьшения старения кожи.
Изобретение относится к косметической композиции для профилактики или уменьшения старения кожи или косметическую композицию для уменьшения морщин.
Изобретение относится к функциональному оздоровительному пищевому продукту для уменьшения морщин.
Решение задачи
В соответствии с одним аспектом настоящего изобретения,изобретение относится к биомаркерной композиции для оценки старения кожи, включающей средство для определения гиалуронана и белка 1, связывающего протеогликан (HAPLN1), или гена HAPLN1 в биологическом образце.
Также в соответствии с другим аспектом настоящего изобретения, изобретение относится к набору для оценки старения кожи, включающему средство для определения белка HAPLN1 или гена HAPLN1 в биологическом образце.
Также в соответствии с другим аспектом настоящего изобретения, изобретение относится к способу скрининга средства, уменьшающего старение кожи, включающему: инкубацию биологического образца с соединением; определение уровня экспрессии белка или гена HAPLN1 в биологическом образце; и сравнение уровня экспрессии с уровнем экспрессии того же белка или гена у нормального контроля, который не инкубировали с соединением.
Также, в соответствии с другим аспектом настоящего изобретения, изобретение относится к фармацевтической композиции для профилактики или уменьшения старения кожи, включающей в качестве активного ингредиента по меньшей мере одно средство, выбранное из группы, состоящей из белка HAPLN1, гена, кодирующего белок HAPLN1, и эффективного средства для обеспечения экспрессии или активации функций белка или гена HAPLN1.
Также в соответствии с другим аспектом настоящего изобретения, изобретение относится к косметической композиции для профилактики или уменьшения старения кожи или косметической композиции для уменьшения морщин, включающим в качестве активного ингредиента белок HAPLN1 или эффективное средство, усиливающее экспрессию или активацию функций белка HAPLN1.
Также, в соответствии с другим аспектом настоящего раскрытия, изобретение относится к функциональному оздоровительному пищевому продукту для уменьшения морщин, функциональному оздоровительному пищевому продукту для профилактики или уменьшения старения кожи или функциональному оздоровительному пищевому продукту для уменьшения морщин, включающим в качестве активного ингредиента белок HAPLN1 или эффективное средство для усиления экспрессии или активации функций белка HAPLN1.
Фармацевтическая композиция, косметическая композиция или функциональный оздоровительный пищевой продукт может дополнительно включать гиалуроновую кислоту.
Предпочтительные эффекты осуществления изобретения
В соответствии с настоящим описанием, экспрессия белка HAPLN1 снижена у пожилых, и его введение обладает превосходным эффектом в уменьшении и обратном развитии старения кожи, включая морщины. Следовательно, настоящее изобретение может эффективно обеспечивать биомаркерную композицию и набор для оценки старения кожи, каждый способный диагностировать старение кожи и включающий средство определения белка HAPLN1 или гена HAPLN1, способ скрининга средства, предотвращающего или уменьшающего старение кожи, способ, включающий определение уровня экспрессии белка HAPLN1 или гена HAPLN1, фармацевтическую композицию, косметическую композицию или функциональный оздоровительный пищевой продукт для профилактики или уменьшения старения кожи, и косметическую композицию или функциональный оздоровительный пищевой продукт для уменьшения морщин.
Краткое описание чертежей
На фиг. 1A и 1B показаны результаты определения продукции коллагена в гетерохронной парабиотической паре старой мыши O и молодой мыши Y.
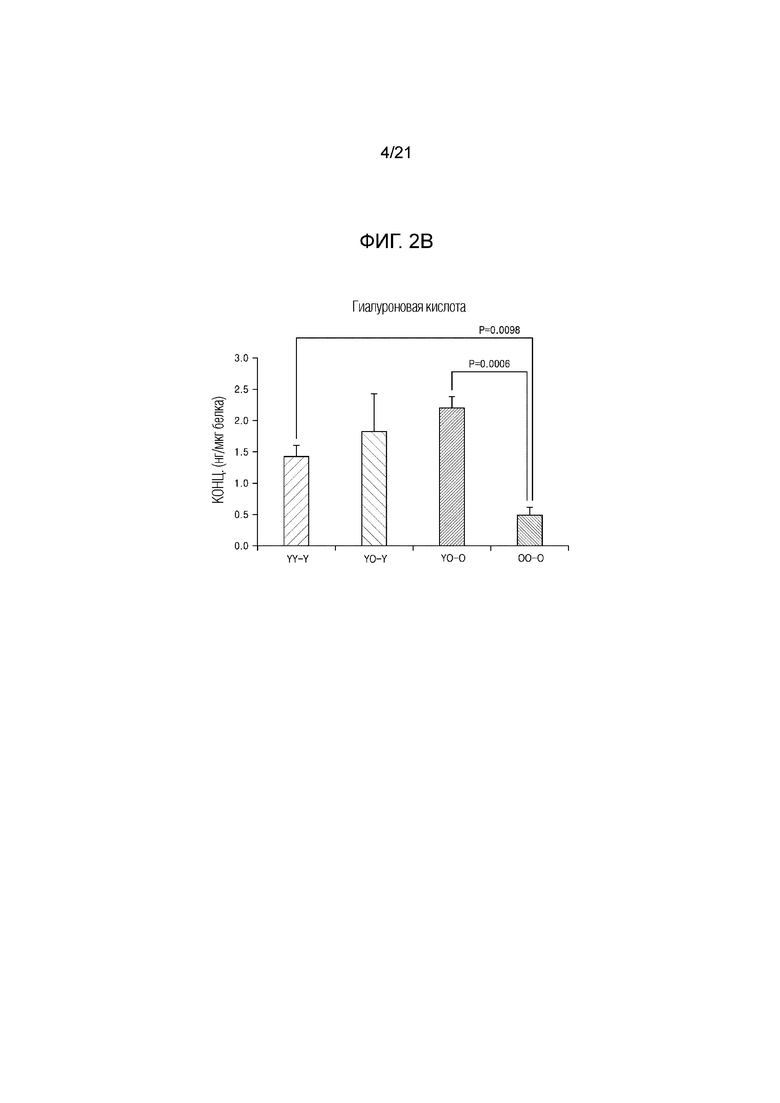
На фиг. 2A и 2B показаны результаты определения уровня гиалуроновой кислоты (HA) соответствующей старой мыши (YO–O) и молодой мыши (YO–Y) в гетерохронной парабиотической паре старой мыши O и молодой мыши Y; уровень HA молодой мыши (YY–Y) в гетерохронной парабиотической паре молодой мыши Y и молодой мыши Y; и уровень HA старой мыши (OO–O) в гетерохронной парабиотической паре старой мыши O и старой мыши O.
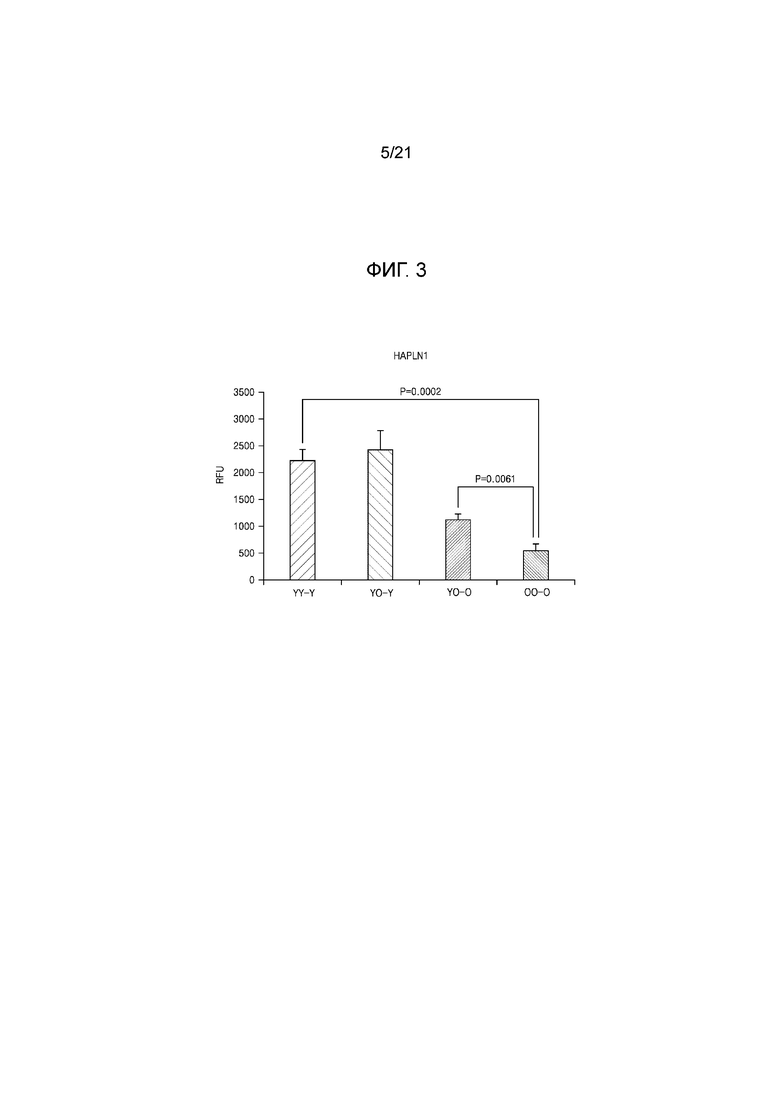
На фиг. 3 показаны результаты, подтверждающие, что внутренним фактором, связанным со старением кожи, является HAPLN1.
На фиг. 4A и 4B показаны результаты сравнения количества мРНК проколлагена и распределение проколлагена в коже старой мыши и молодой мыши.
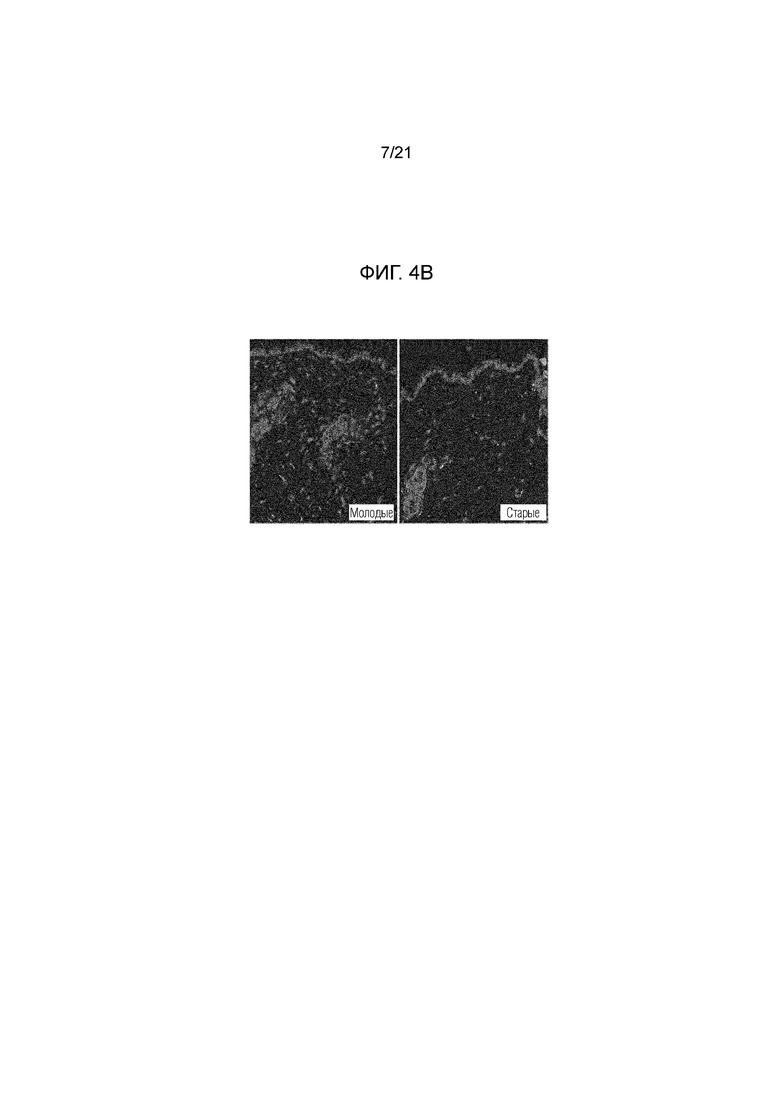
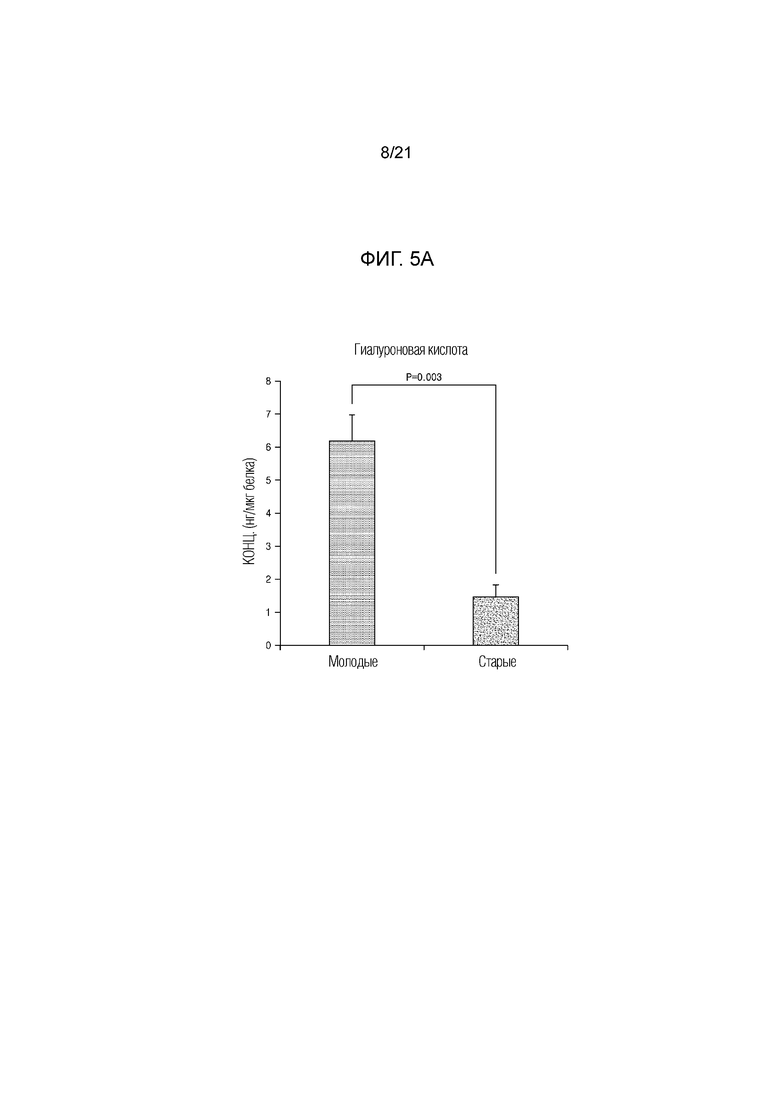
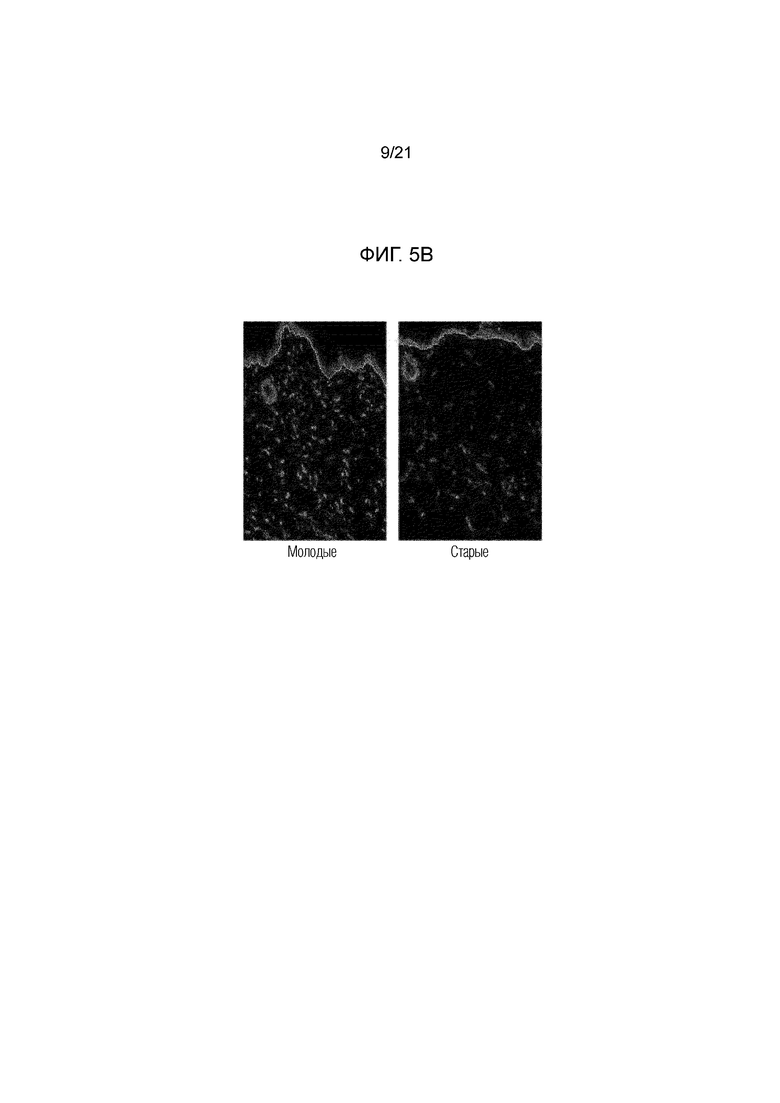
На фиг. 5A и 5B показаны результаты сравнения концентраций и распределения гиалуроновой кислоты в коже старой мыши и молодой мыши.
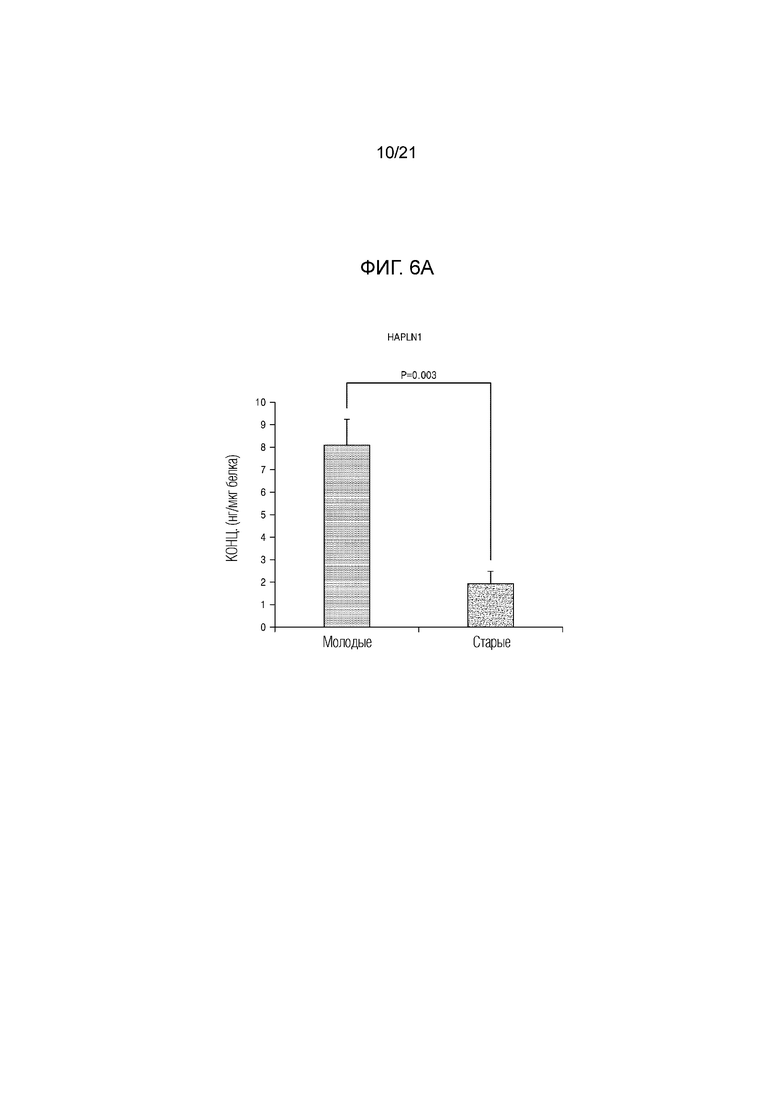
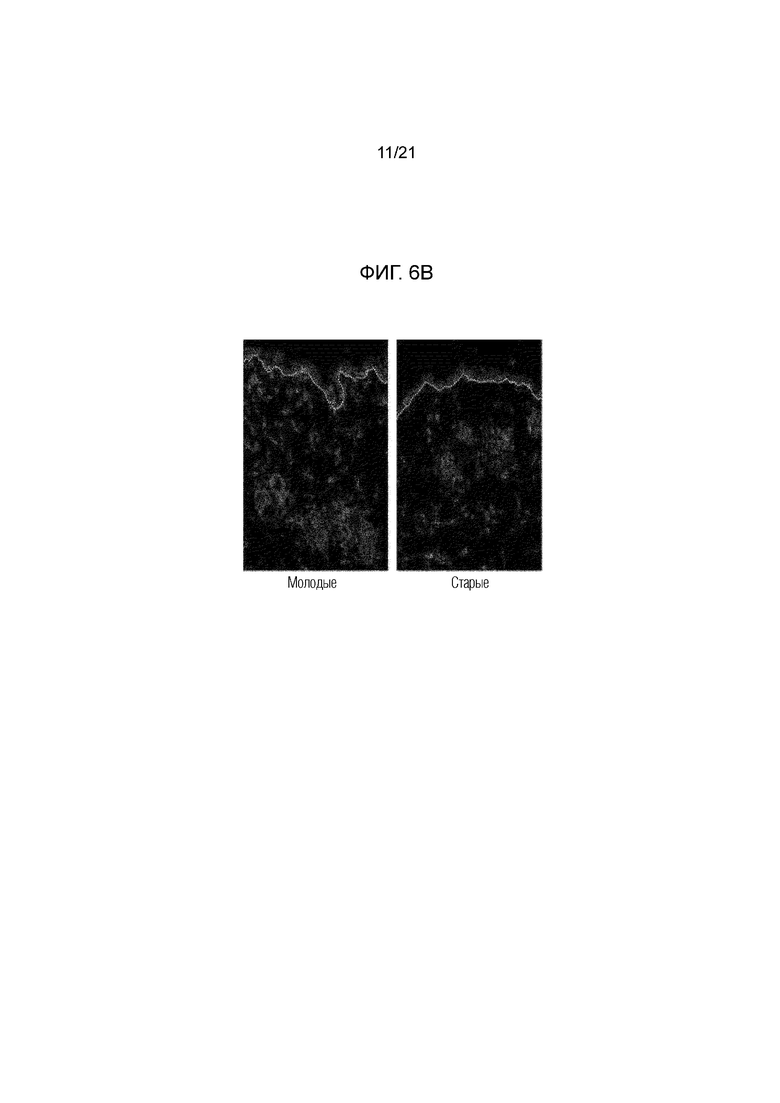
На фиг. 6A и 6B показаны результаты сравнения концентраций и распределения HAPLN1 в коже старой мыши и молодой мыши.
На фиг. 7A и 7B показаны результаты определения повышения коллагена у старой мыши при введении HAPLN1.
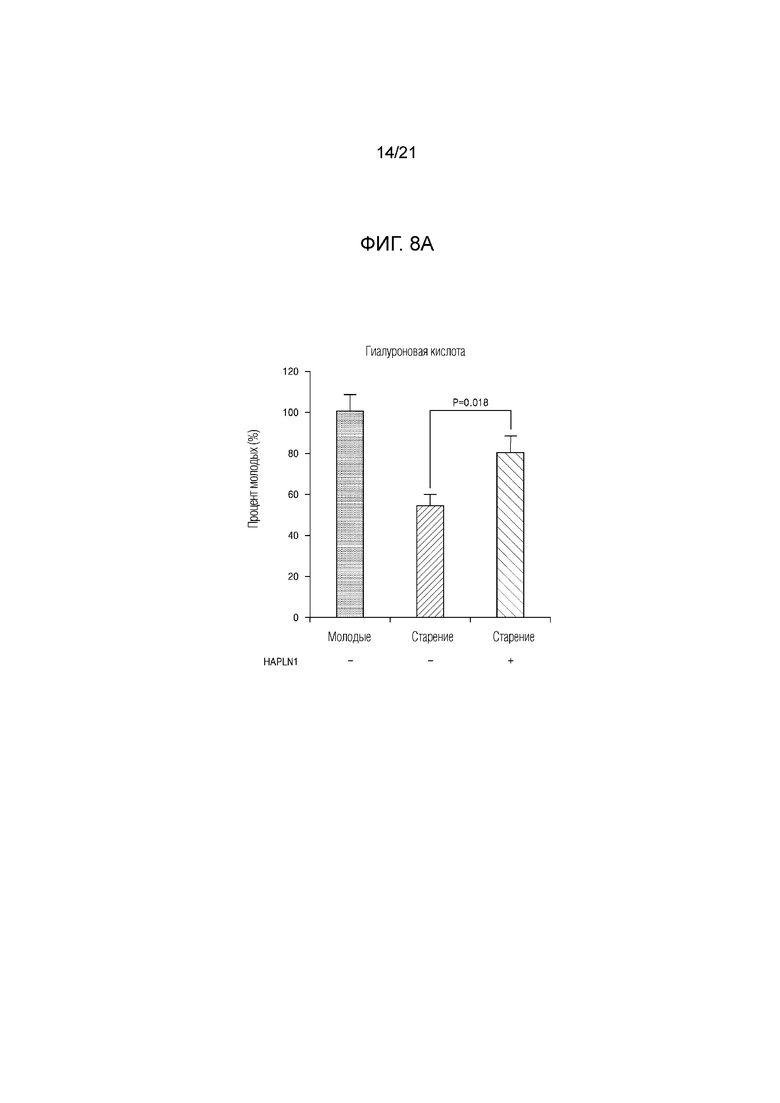
На. 8A и 8B показаны результаты определения повышения гиалуроновой кислоты у старой мыши при введении HAPLN1.
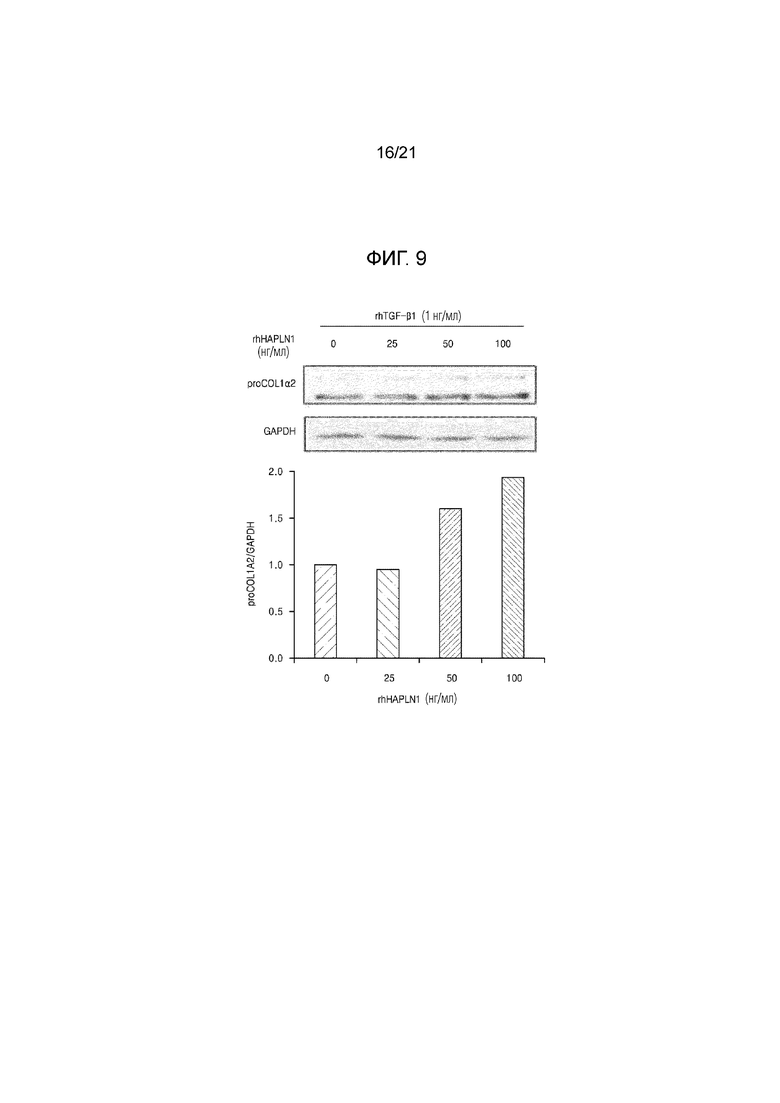
На фиг. 9 показаны результаты определения повышения TGF–β–индуцированного коллагена в клетках нормальных человеческих кожных фибробластов (NHDF) в результате лечения HAPLN1.
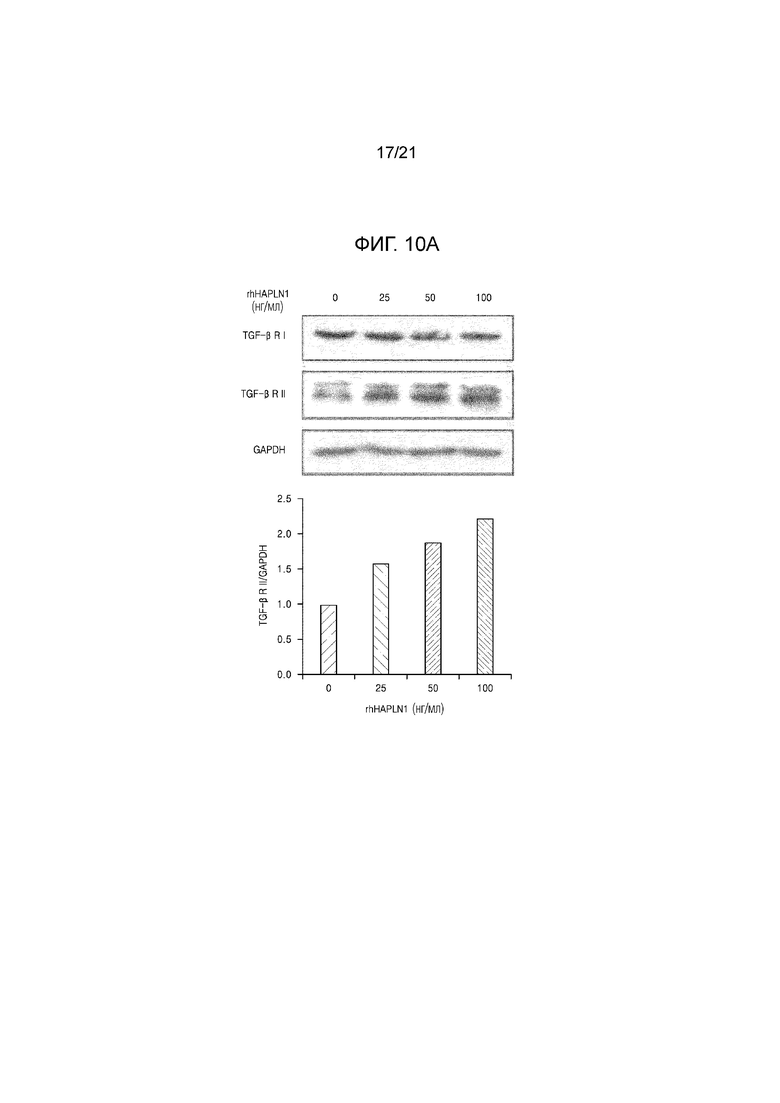
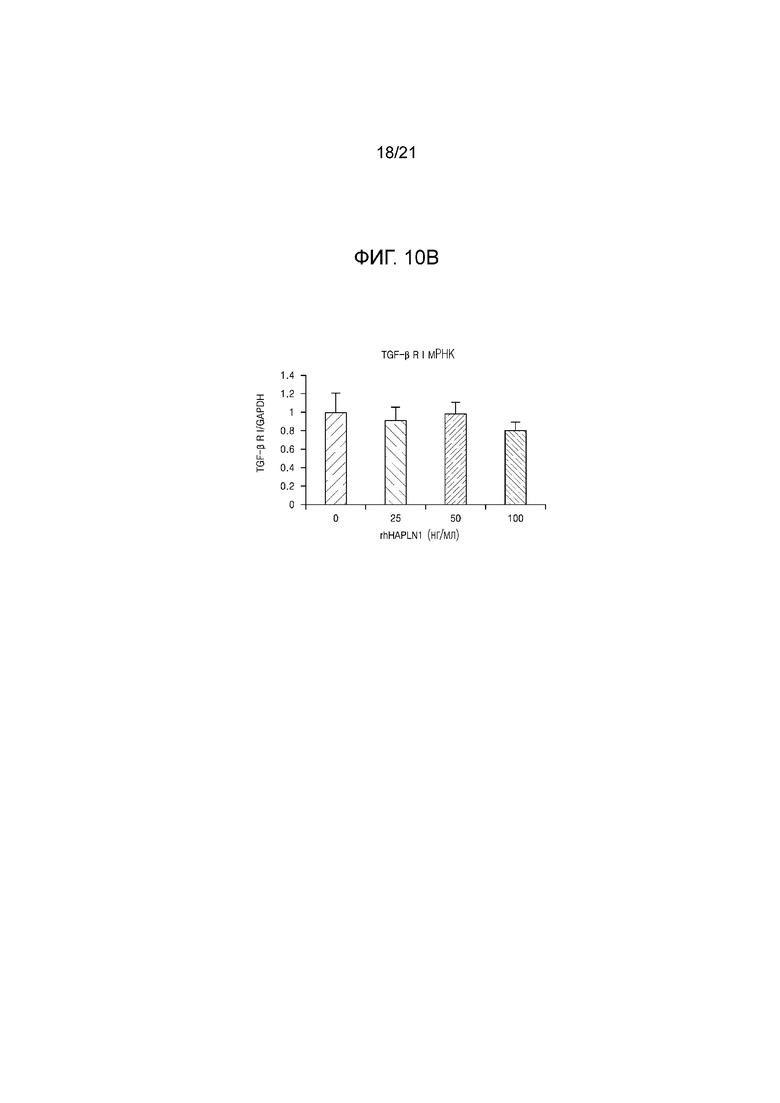
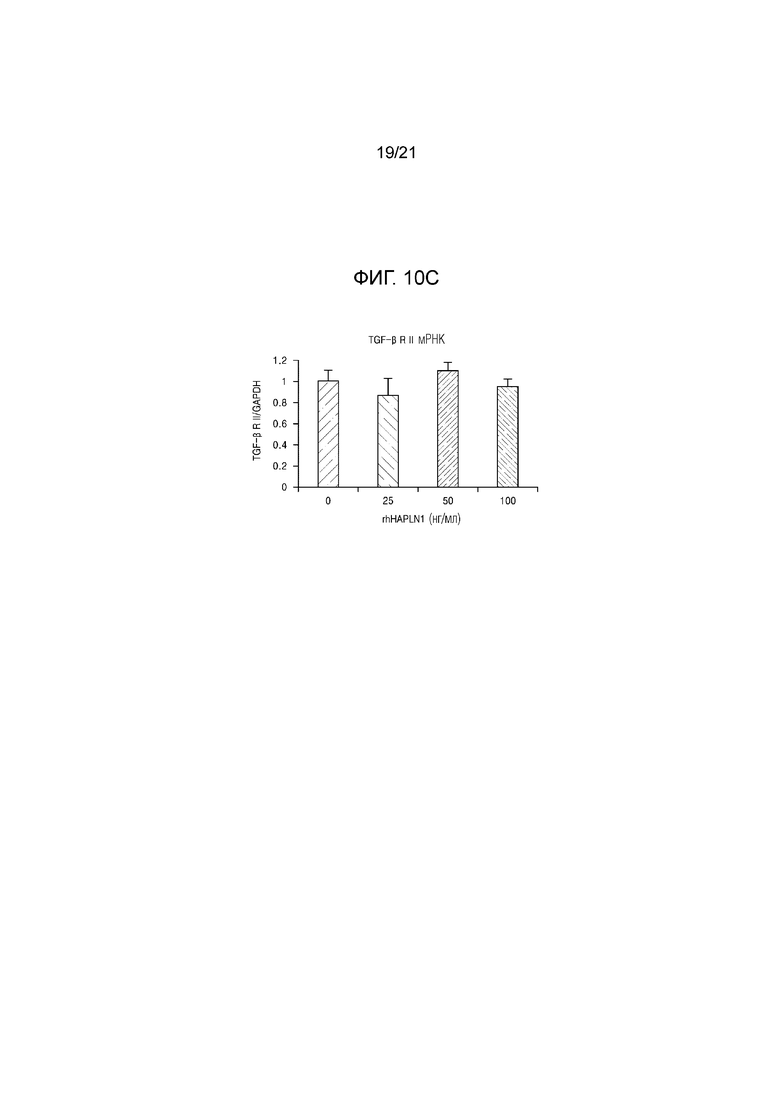
На фиг. 10A–10C показаны результаты определения повышения уровня экспрессии белка TGF–β рецептора II в сигнальном пути синтеза коллагена в клетках NHDF в результате обработки HAPLN1.
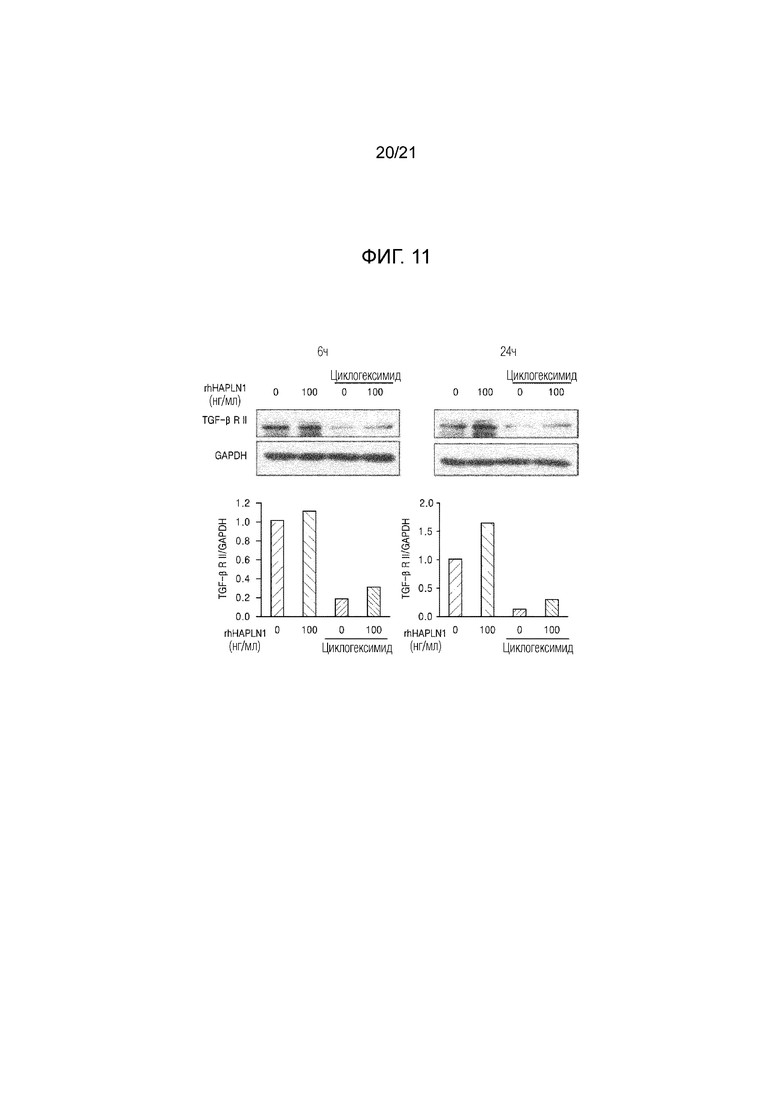
На фиг. 11 показаны результаты определения повышения стабильности рецептора II TGF–β в клетках NHDF в результате обработки HAPLN1.
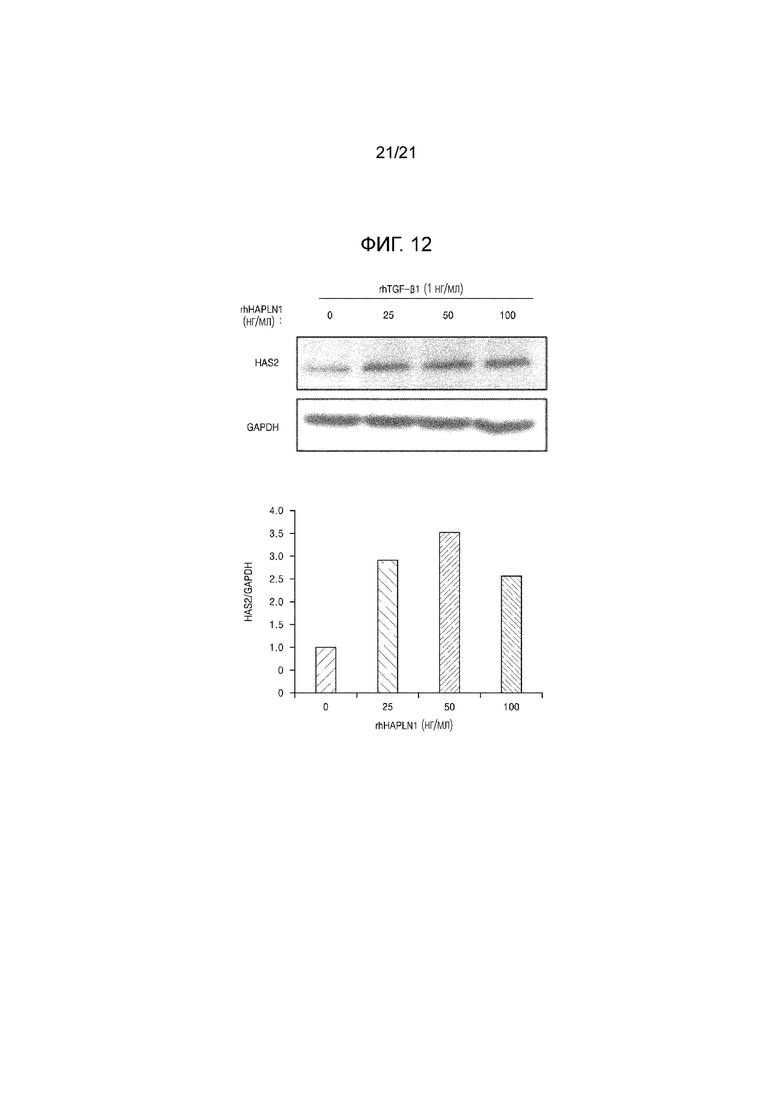
На фиг. 12 показаны результаты определения повышения уровня TGF–β–индуцированной экспрессии белка синтазы гиалуроновой кислоты 2 (HAS2) в клетках NHDF в результате обработки HAPLN1.
Наилучший вариант осуществления изобретения
Авторы настоящего изобретения обнаружили, что уровень экспрессии гиалуронана и протеогликан–связывающего белка 1 (HAPLN1) снижается у старых мышей при сравнении уровня экспрессии белка у старых мышей и молодых мышей, таким образом завершив настоящее изобретение. HAPLN1 представляет собой белок, который стабилизирует гиалуроновую кислоту посредством связывания гиалуроновой кислоты с протеогликаном, и об эффектах HAPLN1 в отношении уменьшения старения кожи к настоящему времени не сообщалось.
Настоящее изобретение относится к биомаркерной композиции для оценки старения кожи, включающей средство для определения белка HAPLN1 или гена HAPLN1 в биологическом образце.
Белком HAPLN1 может быть мышиный HAPLN1 (каталожный NCBI: NP_038528.3, Gene ID:12950) или человеческий HAPLN1 (каталожный NCBI: AAH57808.1, Gene ID: 1404), без ограничения.
Средство может включать, без ограничения, по меньшей мере один компонент, выбранный из антитела, антисмысловой РНК, аптамера и соединения.
Старение кожи может включать морщины, вызванные снижением внеклеточного матрикса дермы кожи.
Настоящее изобретение также относится к набору для оценки старения кожи, включающему средство для определения белка HAPLN1 или гена HAPLN1 в биологическом образце.
Средство может включать, без ограничения, по меньшей мере один компонент, выбранный из антитела, антисмысловой РНК, аптамера и соединения.
Антителом является поликлональное антитело или моноклональное антитело.
Поликлональное антитело может быть получено посредством введения белка, экспрессируемого геном или его фрагментом, в организм–хозяин в качестве иммуногена в соответствии с любым способом, известным в области техники. Организм хозяин может включать млекопитающее, такое как мышь, крыса, овца или кролик. Иммуноген вводят внутримышечно, интраперитонеально или подкожно и обычно вводят с добавкой для улучшения антигенности. Сыворотку можно периодически получать от организма–хозяина для получения сыворотки, имеющей повышенный титр и антигенную специфичность, и очищать из нее антитела.
Моноклональное антитело может быть получено посредством методики получения иммортализованных клеточных линий в результате сшивки, хорошо известной в области техники. Например, мышь может быть иммунизирована посредством белка, экспрессируемого геном или синтетическим пептидом, конъюгированным с альбумином бычьей сыворотки. Антиген–продуцирующие B лимфоциты, выделенные от мыши, сшивают с человеческими или мышиными клетками миеломы для получения иммортализованных гибридомных клеток. Продукцию моноклонального антитела определяют посредством анализа гибридомных клеток с использованием с использованием непрямого иммуноферментного анализа (ELISA). Позитивный клон может быть выбран и культивирован и антитело может быть выделено из него и очищено. Альтернативно, позитивный клон может быть интраперитонеально введен крысам и у них может быть получена асцитическая жидкость для получения моноклонального антитела.
В общем, моноклональное антитело может быть количественно проанализировано посредством реакции окрашивания с использованием вторичного антитела, конъюгированного с ферментом, таким как щелочная фосфатаза (AP) или пероксидаза хрена (HRP), и его субстратом, или количественно проанализировано с использованием AP или HRP, непосредственно конъюгированного с моноклональным антителом белка.
Реакция между белком и антителом может быть идентифицирована посредством экспериментов идентификации белка, таких как вестерн блоттинг, иммунопреципитация (IP), иммуноферментный анализ (ELISA), и иммуногистохимия (IHC), без ограничения ими.
Набор, включающий антитело, может обычно включать лиофилизированное антитело и буфер, стабилизатор, инактивированный белок или подобные, и антитело может быть мечено радионуклидом, флуоресцентным красителем, ферментом или подобным.
Настоящее изобретение также относится к способу скрининга средства, уменьшающего старение кожи, включающему: инкубацию биологического образца с соединением; определение уровня белка или гена HAPLN1 в биологическом образце; и сравнение уровня экспрессии с уровнем экспрессии того же белка или гена у нормального контроля, не инкубированного с соединением.
Биологический образец может включать по меньшей мере один компонент, выбранный из ткани, клеток, цельной крови, сыворотки и плазмы.
Настоящее изобретение также относится к фармацевтической композиции для профилактики или уменьшения старения кожи, включающей по меньшей мере один компонент, выбранный из группы, состоящей из белка HAPLN1, гена, кодирующего белок HAPLN1, и эффективного средства для стимуляции экспрессии или активации функций белка или гена HAPLN1, в качестве активного ингредиента.
Фармацевтическая композиция может дополнительно включать гиалуроновую кислоту (HA).
Фармацевтическая композиция может находиться в одной или более композициях, выбранных из группы, состоящей из гелей, эмульсий, инъекций, порошков, гранул, аэрозолей, паст, чрескожных абсорбентов и пластырей в соответствии с обычным способом, но не ограничиваются ими.
В соответствии с другим вариантом осуществления изобретения фармацевтическая композиция может дополнительно включать по меньшей мере одну добавку, выбранную из группы, состоящей из подходящих носителей, эксципиентов, разрыхлителей, подсластителей, оболочек, средств, вызывающих набухание, лубрикантов, глидантов, ароматизаторов, антиоксидантов, буферов, бактериостатиков, разбавителей, диспергирующих веществ, поверхностно–активных веществ и связующих, которые обычно используют в фармацевтических композициях.
В частности, носители, эксципиенты и разбавители могут включать лактозу, декстрозу, сахарозу, сорбит, маннит, ксилит, эритрит, мальтит, крахмал, гуммиарабик, альгинат, желатин, фосфат кальция, силикат кальция, целлюлозу, метилцеллюлозу, микрокристаллическую целлюлозу, поливинилпирролидон, воду, метилгидроксибензоат, пропилгидроксибензоат, тальк, стеарат магния и минеральное масло. Твердые композиции для перорального введения могут включать таблетки, пилюли, порошки, гранулы, капсулы и подобные формы, и твердые композиции могут быть получены посредством смешивания по меньшей мере одного эксципиента, такого как крахмал, карбонат кальция, сахароза, лактоза или желатин, с композицией. Лубриканты, такие как стеарат магния и тальк, также могут быть использованы в добавление к простому эксципиенту. Жидкая композиция для перорального введения может представлять собой суспензии, составы для внутреннего применения, эмульсии, сиропы или подобные композиции, и могут включать различные эксципиенты, такие как увлажнители, подсластители, ароматизаторы и консерванты, в добавление к обычным разбавителям, таким как вода и жидкий парафин. Композиции для парентерального введения могут включать стерильные водные растворы, неводные растворители, суспензии, эмульсии, лиофилизаты, суппозитории и подобные вещества. Нежидкими растворами и суспензиями могут быть пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, инъекционные сложные эфиры, такие как этилолеат, или подобные соединения. Основания для суппозиториев могут включать WITEPSOL, Macrogol, TWEEN 61, масло какао, лауриновое масло, глицерожелатин, или подобные вещества.
Дозировка белка HAPLN1 и эффективного средства может варьировать в зависимости от условий и массы тела пациента, типа и степени старения, композиции лекарственного средства, пути введения и продолжительности введения и могут быть соответственно установлены обычным специалистом в области техники.
В рамках изобретения 'пациент' может быть млекопитающим, включая человека, без ограничения.
Настоящее изобретение также относится к косметической композиции для профилактики или уменьшения старения кожи, включающей белок HAPLN1 или эффективное средство для усиления экспрессии или активации функций белка HAPLN1, в качестве активного ингредиента.
Косметическая композиция может дополнительно включать гиалуроновую кислоту.
Косметическая композиция может дополнительно включать обычные добавки, такие как стабилизаторы, растворители, витамины, пигменты и ароматизаторы в добавление к белку HAPLN1 и эффективному средству, которыми являются активными ингредиентами.
Косметическая композиция может быть получена в любой форме, обычно используемой в области техники, например, растворах, суспензиях, эмульсиях, пастах, гелях, кремах, лосьонах, порошках, маслах, порошковых основах, эмульсионных основах, восковых основах и спреев, без ограничения. Точнее, косметическая композиция может быть составлена в кремах от солнца, увлажняющих растворах, вяжущих растворах, увлажняющих растворах, увлажняющих кремах, массажных кремах, эссенциях, кремах для глаз, масках, спреях или порошках.
Когда косметическую композицию составляют в пастах, кремах или гелях, носителем может быть животное масло, растительное масло, воск, парафин, крахмал, трагакант, производные целлюлозы, полиэтиленликоль, силикон, бентонит, диоксид кремния, тальк, оксид цинка или подобные компоненты.
Когда косметическую композицию составляют в порошках или спреях, носителем может быть лактоза, тальк, диоксид кремния, гидроксид алюминия, силикат кальция или полиамидный порошок. В частности, в форме спреев косметическая композиция может дополнительно включать пропеллент, такой как хлорфторгидроуглерод, пропан/бутан или диметиловый эфир.
Когда косметическую композицию составляют в растворах или эмульсиях, носителем может быть растворитель, разбавитель или эмульгатор, например, вода, этанол, изопропанол, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3–бутилгликолевое масло, алифатический эфир глицерина, полиэтиленгликоль или сложный эфир жирной кислоты и сорбита.
Когда косметическую композицию составляют в суспензиях, носителем может быть жидкий разбавитель, такой как вода, этанол, или пропиленгликоль, суспендирующий агент, такой как этоксилированный изостеариловый спирт, сложный эфир полиоксиэтиленсорбита и сложный эфир полиоксиэтилен сорбитана, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар и трагакант.
Настоящее изобретение также относится к функциональному оздоровительному пищевому продукту для профилактики или уменьшения старения кожи или функциональному оздоровительному пищевому продукту для уменьшения морщин, включающим в качестве активного ингредиента белок HAPLN1 или эффективное средство для усиления экспрессии или активации функций белка HAPLN1.
Функциональный оздоровительный пищевой продукт может дополнительно включать гиалуроновую кислоту.
Функциональный оздоровительный пищевой продукт может быть получен в форме порошков, гранул, таблеток, капсул, сиропов или напитков, и функциональный оздоровительный пищевой продукт может быть использован в соответствии с любым способом в комбинации с любой другой пищей или пищевыми добавками в добавление к белку HAPLN1 или эффективному агенту по настоящему изобретению, используемыми в качестве активных ингредиентов. Количество активного ингредиента для смешивания с ним может быть определено в соответствии с его целями, например, профилактикой, здоровьем или лечением.
Эффективные дозы белка HAPLN1 и эффективного агента, содержащихся в функциональном оздоровительном пищевом продукте, могут быть адаптированы в соответствии с эффективной дозой фармацевтической композиции. Однако, когда для здоровья и гигиены предпочтительно пролонгированное употребление, эффективные дозы могут быть ниже вышеуказанного диапазона. Кроме того, так как не существует проблемы безопасности, активный ингредиент может быть использован в количестве выше диапазона.
Типы оздоровительных функциональных пищевых продуктов особо не ограничены и примеры оздоровительных функциональных пищевых продуктов могут включать мясо, сосиски, хлеб, шоколад, конфеты, закуски, печенья, пицца, лапша, другие макароны, жевательные резинки, молочные продукты, включая мороженое, различные виды супов, напитки, чай, напитки, алкогольные напитки и витаминные комплексы.
Вариант осуществления изобретения
Далее настоящее изобретение будет описано более подробно в соответствии со следующими примерами. Однако следующие примеры представлены только для иллюстрации настоящего изобретения, и рамки настоящего изобретения не ограничены ими. Примеры настоящего изобретения приведены для более полного объяснения настоящего изобретения обычному специалисту в данной области техники.
<Пример 1> Поиск внутреннего фактора старения кожи
Гетерохронный парабиоз представляет собой эксперимент соединения кровеносных сосудов старой мыши и молодой мыши одного вида для объединения крови. Гетерохронная парабиотическая экспериментальная модель используется для поиска и идентификации внутреннего фактора, вызывающего старение нервов, сердец и мышц живых организмов.
Следовательно, для подтверждения присутствия внутреннего фактора, связанного со старением кожи живых организмов, старую мышь C57BL/6J в возрасте 20 месяцев покупали у Korea Basic Science Institute и молодую мышь C57BL/6J в возрасте 6 недель покупали у Central Lab Animal Inc., анестезировали и кожу и мышцы брюшной стенки мышей, полученные путем надреза объединяли посредством парабиоза. В случае молодой мыши кожу надрезали с правой передней лапы до правой задней лапы на около 5 см и затем правые мышцы передней брюшной стенки надрезали на около 1 см. В случае старой мыши кожу надрезали с левой передней лапы до левой задней лапы на около 5 см и затем левые мышцы передней брюшной стенки надрезали на около 1 см. Надрезанные брюшные мышцы и кожу объединяли и сшивали для парабиоза. После этого мышей содержали в течение 3 недель и умерщвляли, плазму и ткани кожи забирали у мышей из каждой группы. Общее количество крови собирали посредством сбора крови из глазницы и инкубировали в пробирке для забора крови с этилендиаминтетрауксусной кислотой (EDTA) в течение около 30 минут и затем центрифугировали со скоростью 10000 x g для отделения плазмы. Выделенную плазму хранили при –70°C. В качестве кожной ткани, у мышей забирали кожу шеи размером 1 см х 1 см после удаления волос.
Для иммунофлуоресценции собранные ткани кожи фиксировали в 10%(об/об) формалине для получения парафинового сечения. Полученное стекло депарафинизировали и регидратировали и затем окрашивали иммунофлуоресценцией с использованием поликлонального козьего анти–мышиного проколлаген типа I α2 IgG (COL1A2) (Santa Cruz Biotechnology) и ослиного анти–козьего IgG(H+L) Alexa Fluor 594 (Life technologies) антитела.
Для ОТ–ПЦР выделенную ткань кожи культивировали в течение ночи в 0,25%(масс/об) трипсин/EDTA при 4°C, и затем оттуда удаляли слой дермы и общую мРНК экстрагировали с использованием реагента TRIzol. Из экстрагированной мРНК синтезировали кДНК с использованием набора для синтеза кДНК (Life technologies). Затем, proCOL1A1, proCOL1A2, proCOL3A1, и GAPDH оценивали количественно посредством ОТ–ПЦР (количественная полимеразная цепная реакция с обратной транскриптазой).
В результате, как показано на фиг. 1A, 1B, 2A, и 2B, было подтверждено, что продукция коллагена (фиг. 1A и 1B) и гиалуроновой кислоты (фиг. 2A и 2B) увеличивалась в ткани кожи старой мыши (YO–O) в гетерохронной парабиотической паре старой мыши O и молодой мыши Y, при сравнении с таковой старой мыши (OO–O) в изохронной парабиотической паре старой мыши O и старой мыши O.
Следовательно, было подтверждено, что существует внутренний фактор, связанный со старением кожи в живых организмах.
Кроме того, плазму выделяли у мышей из каждого эксперимента, и внутренний фактор определяли посредством протеомики SomaScan proteomics (SomaLogic, Inc.). В результате, HAPLN1 был идентифицирован как белок, связанный со старением, как показано на фиг. 3.
<Пример 2> Определение количественного снижения HAPLN1 при старении кожи
1. Снижение продукции коллагена при старении кожи
Ткань кожи шеи получали от старого самца мыши C57BL/6J в возрасте 20 месяцев и молодого самца мыши C57BL/6J в возрасте 6 месяцев в размере 1 см х 1 см, и общую мРНК экстрагировали из нее таким же образом как в примере 1. Из экстрагированной мРНК синтезировали кДНК с использованием набора для синтеза кДНК, и затем количественно оценивали количество мРНК проколлагена типа I (proCOL1A1 и proCOL1A2) и типа III (proCOL3A1) посредством ОТ–ПЦР.
В результате, как показано на фиг. 4A, уровни мРНК proCOL1A1, proCOL1A2 и proCOL3A1 у старой мыши снижались до 1/4,3, 1/4,2, and 1/5,6, соответственно, при сравнении с таковой молодой мыши.
Кроме того, парафиновые сечения получали с использованием ткани кожи шеи, полученной от старой мыши и молодой мыши, и окрашенной иммунофлуоресценцией таким же образом, как в примере 1. В результате наблюдения с использованием конфокального микроскопа было подтверждено, что распределение проколлагена типа I уменьшалось в коже старой мыши, как показано на фиг. 4B.
2. Снижение количества гиалуроновой кислоты при старении кожи
Ткань кожи шеи получали от старого самца мыши C57BL/6J в возрасте 20 месяцев и молодого самца мыши C57BL/6J в возрасте 6 месяцев в размере 1 см х 1 см таким же образом, как в примере 1 и подвергали иммуноферментному анализу (ELISA). Сначала подкожный жир удаляли из выделенной ткани кожи с использованием скребка, и ткань кожи гомогенизировали в фосфатном буферном растворе (PBS), дополненном 1X ингибитором протеаз. Гиалуроновую кислоту оценивали количественно в соответствии с инструкциями производителя с использованием набора ELISA для гиалуроновой кислоты (CUSABIO).
В результате концентрация гиалуроновой кислоты у старой мыши снизилась до около 1/4,2 таковой молодой мыши, как показано на фиг. 5A.
Срезы ткани кожи старой мыши и молодой мыши окрашивали иммунофлуоресценцией таким же образом, как в примере 1. В таком случае овечьи поликлональные антитела к гиалуроновой кислоте (Abcam) и ослиные анти–овечьи IgG H&L Alexa Fluor 488 (Abcam) использовали в качестве антитела к гиалуроновой кислоте. В результате наблюдения с использованием конфокального микроскопа, было подтверждено, что распределение гиалуроновой кислоты снижалось в коже старой мыши, как показано на фиг. 5B.
3. Снижение уровня экспрессии HAPLN1 при старении кожи
Ткань кожи шеи получали от старого самца мыши C57BL/6J в возрасте 20 месяцев и молодого самца мыши C57BL/6J в возрасте 6 месяцев и гомогенизировали в растворе PBS таким же образом, как в примере 2–2, описанном выше, и затем концентрацию HAPLN1 измеряли с использованием набора ELISA к мышиному HAPLN1 (CUSABIO).
В результате измерения концентрация HAPLN1 снижалась у старой мыши до 1/4,2 таковой молодой мыши, как показано на фиг. 6A.
Также срезы ткани кожи старой мыши и молодой мыши окрашивали иммунофлуоресценцией таким же образом, как в примере 1. В таком случае использовали козье анти–HAPLN1 поликлональное IgG (Santa Cruz Biotechnology) и ослиное анти–козье IgG(H+L) Alexa Fluor 594 (Life technologies).
В результате наблюдения с использованием конфокального микроскопа было подтверждено, что распределение HAPLN1 снижалось в коже старой мыши, как показано на фиг. 6B.
<Пример 3> Определение эффектов введения HAPLN1 в отношении уменьшения старения кожи
Рекомбинантный мышиный HAPLN1 (купленный у Cusabio Biotech Co) растворяли в PBS и вводили старому самцу мыши C57BL/6J в возрасте 20 месяцев интраперитонеальным путем в дозе 0,1 мг/кг один раз в сутки в течение 14 дней. То же количество PBS вводили старой мыши и молодой мыши (в возрасте 6 месяцев) для получения контрольных групп сравнения между ними.
1. Определение увеличения коллагена у старой мыши в результате введения HAPLN1
После завершения введения слой дермы отделяли от ткани кожи каждой экспериментальной группы и контрольных групп таким же образом, как в примере 1, и из них экстрагировали РНК для количественной оценки проколлагена типа I (proCOL1A1 и proCOL1A2) и типа III (proCOL3A1) посредством ОТ–ПЦР.
В результате, как показано на фиг. 7A, было подтверждено, что уровни мРНК proCOL1A1, proCOL1A2 и proCOL3A1 увеличивались в 2,6 раз, 2,5 раз, и 2,8 раз, соответственно в группе, которой вводили HAPLN1, при сравнении с группой, которой не вводили, показывая восстановление до уровня, сходного с таковым молодой мыши. Кроме того, срезы ткани кожи окрашивали антителом к про–коллагену типа I и оценивали с использованием конфокального микроскопа таким же образом, как в примере 2–1. В результате было подтверждено, что распределение про–коллагена типа I в группе, которой вводили HAPLN1, увеличивалось до уровня, сходного с таковым молодой мыши, как показано на фиг. 7B.
2. Определение повышения гиалуроновой кислоты у старой мыши в результате введения HAPLN1
После завершения введения ткань кожи шеи получали у каждой экспериментальной группы и контрольных групп и гомогенизировали в растворе PBS таким же образом, как в примере 2–2, и затем количественно оценивали гиалуроновую кислоту с использованием набора ELISA для гиалуроновой кислоты (CUSABIO) в соответствии с инструкциями производителя.
В результате, как показано на фиг. 8A, было подтверждено, что количество гиалуроновой кислоты увеличивалось в группе, которой вводили HAPLN1, в 1,5 раза при сравнении с группой, которой не вводили, демонстрируя восстановление до уровня, сходного с таковым молодой мыши.
Кроме того, гиалуроновую кислоту в срезах ткани кожи окрашивали иммунофлуоресценцией таким же образом, как в примере 2–2, и исследовали с использованием конфокального микроскопа. В результате, было подтверждено, что распределение гиалуроновой кислоты увеличивалось в группе, которой вводили HAPLN1, до уровня, сходного с таковым молодой мыши, при сравнении с группой, которой не вводили, как показано на фиг. 8B.
<Пример 4> Определение повышения рецептора II TGF–β1, TGF–β1–индуцированной продукции коллагена и фермента синтеза гиалуроновой кислоты (HAS2) в результате обработки HAPLN1
1. Идентификация повышения TGF–β1–индуцированной продукции коллагена в клетке NHDF в результате обработки HAPLN1
Клеточные линии нормальных человеческих кожных фибробластов (NHDF) подвергали вестерн–блоттинг анализу для определения, влияет ли HAPLN1 на TGF–β1–индуцированную продукцию proCOL1α2. TGF–β представляет собой фактор, индуцирующий продукцию коллагена. Через 30 минут после этого клеточные линии NHDF обрабатывали различными концентрациями рекомбинантного человеческого HAPLN1 (rhHAPLN1) (0, 25, 50, и 100 нг/мл), клеточные линии NHDF обрабатывали 1 нг/мл рекомбинантного человеческого TGF–β1 в течение 24 часов.
В результате было подтверждено, что TGF–β1–индуцированная продукция proCOL1α2 увеличивалась в результате обработки HAPLN1, как показано на фиг. 9.
2. Определение увеличения рецептора II TGF–β в клетках NHDF в результате обработки HAPLN1
Для определения, влияет ли HAPLN1 на передачу сигнала TGF–β, клеточные линии NHDF обрабатывали различными концентрациями рекомбинантного человеческого HAPLN1 (rhHAPLN1) (0, 25, 50, и 100 нг/мл). Через 24 часа уровень экспрессии белка рецептора TGF–β оценивали вестерн блоттингом.
В результате было подтверждено, что уровень экспрессии белка рецептора II TGF–β из двух типов рецепторов, как показано на фиг. 10A, увеличивался в зависимости от концентрации при обработке HAPLN1. В результате измерения уровня экспрессии мРНК рецепторов TGF–β посредством ОТ–ПЦР в таких же условиях было подтверждено, отсутствие различий при обработке HAPLN1, как показано на фиг. 10B и 10C.
Следовательно, для определения увеличивает ли HAPLN1 количество рецептора II TGF–β в результате регуляции стабильности вместо транскрипционной регуляции, клетки, которые были предварительно обработаны циклогексимидом в качестве ингибитора синтеза белка в концентрации 10 мкM в течение 1 часа, обрабатывали 100 нг/мл rhHAPLN1 в течение 6 часов или 24 часов, и уровень экспрессии белка рецептора II TGF–β идентифицировали вестерн блоттингом.
В результате было подтверждено, что количество рецептора II TGF–β увеличивалось в результате обработки rhHAPLN1 даже в присутствии циклофосфамида, как показано на фиг. 11. Следовательно, очевидно, что HAPLN1 увеличивает стабильность рецептора II TGF–β.
3. Определение увеличения экспрессии TGF–β1–индуцированной синтазы гиалуроновой кислоты (HAS2) в клетке NHDF в результате обработки HAPLN1
В кожных фибробластах синтаза гиалуроновой кислоты 2 HAS2 главным образом существует в виде трех типов синтаз гиалуроновой кислоты HAS1, HAS2, и HAS3. Чтобы определить влияет ли HAPLN1 на экспрессию TGF–β1–индуцированной HAS2 в клеточных линиях NHDF, через 30 минут после того, как клеточные линии NHDF обрабатывали различными концентрациями рекомбинантного человеческого HAPLN1 (rhHAPLN1) (0, 25, 50, и 100 нг/мл), клеточные линии NHDF обрабатывали 1 нг/мл рекомбинантного человеческого TGF–β1 в течение 24 часов и уровень экспрессии белка HAS2 идентифицировали вестерн блоттингом.
В результате было подтверждено, что уровень экспрессии TGF–β1–индуцированной HAS2 увеличивался в результате обработки HAPLN1, как показано на фиг. 12.
Вышеуказанное описание изобретения приведено с целью иллюстрации и специалисту в области техники понятно, что вышеописанные варианты осуществления изобретения являются иллюстративными во всех аспектах и не ограничивают изобретение. Следовательно, рамки изобретения определяются следующей формулой изобретения и ее эквивалентами, а не подробным описанием иллюстративных вариантов осуществления изобретения.







Изобретение относится к области фармацевтики, а именно к применению белка HAPLN1 или гена, кодирующего белок HAPLN1, или эффективного агента для промотирования экспрессии или активации функций белка или гена HAPLN1 для профилактики или уменьшения старения кожи. Использования изобретения обеспечивает уменьшение или профилактику старения кожи или признаков старения кожи, таких как морщины, за счет введения белка HAPLN1 или гена, кодирующего белок HAPLN1, или эффективного средства для обеспечения экспрессии или активации функций белка или гена HAPLN1. 4 з.п. ф-лы, 12 ил., 4 пр.
1. Применение белка HAPLN1 или гена, кодирующего белок HAPLN1, или эффективного агента для промотирования экспрессии или активации функций белка или гена HAPLN1 для профилактики или уменьшения старения кожи.
2. Применение по п.1, в котором старение кожи представляет собой морщины.
3. Применение по п.1, в котором старение кожи представляет собой образование морщин, вызванное уменьшением внеклеточного матрикса дермы.
4. Применение по п.1, где белок HAPLN1, ген, кодирующий белок HAPLN1, или эффективный агент вводят субъекту пероральным или парентеральным введением.
5. Применение по п.1, где белок HAPLN1, ген, кодирующий белок HAPLN1, или эффективный агент вводят с гиалуроновой кислотой.
| US 20140163118 A1, 12.06.2014 | |||
| POETSCHKE J | |||
| et al | |||
| Anti-wrinkle creams with hyaluronic acid: how effective are they? //MMW Fortschritte der Medizin | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| - Т | |||
| Система механической тяги | 1919 |
|
SU158A1 |
| - С | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| US 20160192689 A1, 07.07.2016 | |||
| УСТРОЙСТВО ДЛЯ ЛЕЧЕНИЯ ДЕРМАТОЛОГИЧЕСКИХ СОСТОЯНИЙ | 2005 |
|
RU2388504C2 |
| VEGH M | |||
| J | |||
| et al | |||
| Hippocampal extracellular matrix levels and stochasticity in synaptic protein expression | |||
Авторы
Даты
2021-06-28—Публикация
2017-03-06—Подача