Изобретение относится к фармакологии и ветеринарной медицине, в частности – гинекологии, и может быть использовано для профилактики и лечения вагинитов у коров.
Вагинит - воспаление влагалища, возникающее из-за проникновения в половые органы животного микроорганизмов Streptococcus vaginitis. В настоящее время основные выпускаемые в промышленном масштабе ветеринарные препараты для лечения вагинитов содержат в своем составе дезинфицирующие компоненты (фурацилин, йод), антисептики (марганцовокислый калий, ихтаммол, гидрохлорид хлоргексидина) или антибиотики (энрофлоксацин, тетрациклин и др.). Присутствие в составе препаратов антисептиков и антибиотиков, как правило, приводит к снижению иммунитета животных, аллергическим реакциям и другим негативным последствиям. Кроме того, широкое применение антибиотиков приводит к антибиотикорезистентности живого организма, вызывая необходимость разработки и внедрения новых лекарственных форм.
Известен препарат «Метролек» в виде пенной эмульсии для лечения и профилактики послеродовых осложнений, в том числе вагинитов, у коров (см. инструкцию по применению «Метролека» № регистрационного удостоверения ПВР-1-35.13/02987), содержащий 0.5% тилозин тартрата в качестве действующего вещества, 3.3% вспомогательных веществ (масло подсолнечное, эмульгатор Т-2, бета-каротин) и воду для инъекций.
Недостатком препарата является наличие в составе антибиотика - тилозин тартрата, что может инициировать переход заболевания в скрытую форму без клинических проявлений, а также существенно ограничивает использование молока для пищевых целей во время и в первые несколько дней после лечения.
В качестве альтернативы антибиотикам предлагается использовать препараты природного происхождения с собственной антибактериальной активностью, которые могут использоваться как самостоятельные ветпрепараты или в виде биологически активной матрицы для пролонгированной доставки лекарственных веществ.
Известно средство в форме эмульсии для профилактики и лечения гинекологических заболеваний у животных (см. патент РФ №2384323, МПК A61K 9/107, опубл. 20.03.2010), содержащее 20-60% сапропелевой композиции, 5-15% эмульгатора ОП-10 для стабилизации эмульсии и воду. Сапропель представляет собой отложения, накапливающиеся на дне пресных водоемов, обогащенные биологически активными минеральными веществами (кальций, фосфор, сера, железо) и микроэлементами (йод, кобальт, медь, марганец, бром).
Недостатком средства следует считать высокое содержание сапропеля в композиции, необходимое для достижения терапевтического эффекта. В небольших количествах сапропель обладает слабым антибактериальным и кератолитическим действием. Препарат не удобен в применении, поскольку, согласно изобретению, средство является концентратом и для получения требуемой лечебной концентрации для каждого конкретного случая необходимо его предварительное разведение.
Перспективным для создания биологически активных лекарственных препаратов может рассматриваться природный аминополисахарид хитозан. Хитозан в разных морфологических формах проявляет широкий спектр биологической активности, а материалы на его основе обладают ускоренным ранозаживляющим и высоким противовоспалительным действием (см. патент РФ №2617501, МПК С08J 3/075, опубл. 25.04.2017).
Известен биопрепарат «Биометрин» для профилактики и лечения эндометритов у коров, содержащий в своем составе 0.5-1.5% раствор хитозана в 2% уксусной кислоте, раствор культур Bacillus subtilis СН 201 и Bacillus licheniformis СН 200 с титром спор 108-1011 в соотношении 1:1 и вспомогательные вещества: лактозу, СаСО3, молочную сыворотку или свекольный сок (см. патент РФ №2687041, МПК C12N 1/20, опубл. 06.05.2019).
Недостатком представленного препарата следует считать использование уксусной кислоты для растворения хитозана, что может вызвать раздражение слизистой оболочки. Согласно изобретению, свежеприготовленный водно-кислый раствор хитозана подвергается автоклавированию при температуре 121°С, что может приводить к деструкции и снижению фармакологической активности хитозана. При этом также наблюдается значительное снижение динамической вязкости исходного раствора хитозана. Кроме того, применение данного биопрепарата ограниченно профилактикой и лечением только послеродовых эндометритов у коров. Лечение вагинитов у коров в изобретение не ставилось.
Наиболее близким техническим решением к заявляемому изобретению является внутриматочное средство для лечения и профилактики вульвовагинитов у коров в виде свечей (см. патент РФ № 2375067, МПК A61K 35/12, опубл. 10.12.2009). Свечи содержат в своем составе натуральный фармакопейный препарат «Виватон», препарат антисептик-стимулятор Дорогова 2-я фракция, состоящий из не менее 10% биологически активных веществ, эмульгатор ланолин, а также формообразующую основу в виде масла какао, при следующем соотношении компонентов на одну свечу, г: 1.0:1.0:0.5:8.0 соответственно. «Виватон» представляет собой комплекс из экстрактов и настоев лекарственных растений и содержит 207 компонентов, такие как: органические кислоты и аминокислоты, в том числе незаменимые (лауриновая, пролин, лимонная, масляная, щавелевая, аскорбиновая, глютаминовая, фолиевая, янтарная, линоленовая, яблочная и др.), комплекс витаминов (В1, В2, Е, С, В6, А, Р), холин, провитамины, фитонциды, гликозиды, сапонины, флавоноиды, каротиноиды, хатинин, лецитин, катехины, сахароза, терпеноиды, дубильные вещества, эфирные масла, макро- и микроэлементы и другие компоненты природного происхождения (регистрационное удостоверение № 98/183/8 от 4.06.98 г., ТУ 112-84-803-3615-001-13). Антисептик-стимулятор Дорогова 2-я фракция - препарат, полученный из продуктов животноводства (мяса, костей и пр.) методом сухой возгонки при повышенных температурах (регистрационное удостоверение № ПВР-3-1.1/00937 от 23.08.13 г.). Препарат состоит из низших карбоновых кислот, их аммонийных солей, амидов и холиновых эфиров, разнообразных производных аммиака и солей аммония, холина, метилмеркаптана, соединений с активной сульфгидрильной группой и воды.
Недостатком является многокомпонентность и трудоёмкость процесса изготовления исходных ингредиентов препарата, высокое содержание эмульгатора в готовом продукте, а также дозировка в применении свечей - 2 шт./2 раза в сутки в течение 3-5 дней, что является экономически затратным при использовании в больших хозяйствах с высоким поголовьем скота.
Технической проблемой изобретения является создание высокоэффективного биологически активного средства для лечения и профилактики вагинита у крупного рогатого скота, не содержащее в своем составе антибиотиков и антисептиков.
Техническим результатом является получение средства на основе гидрохлорида хитозана, выполненного в форме инъецируемой композиции или свечного суппозитория. Под инъецируемой композицией следует понимать композицию, которая при температуре менее 4-15°С представляет собой жидкость, а при температурах, близких к физиологическим (~35-37°С), претерпевает фазовый переход в формоустойчивый гидрогель.
Указанный технический результат достигается тем, что средство для профилактики и лечения вагинита у коров, содержащее активную и вспомогательную части, согласно изобретению, содержит в качестве активной части гидрохлорид хитозана, а в качестве вспомогательной части - гелеобразующую основу, при следующем соотношении компонентов, мас.%:
В качестве гелеобразующей основы средство может содержать триблок сополимер этиленоксида и пропиленоксида при следующем соотношении компонентов, мас. %:
Активная часть средства может дополнительно содержать аскорбиновую или борную кислоту при следующем соотношении компонентов, мас. %:
В случае наличия в активной части средства аскорбиновой или борной кислоты средство может содержать в качестве гелеобразующей основы триблок сополимер этиленоксида и пропиленоксида при следующем соотношении компонентов, мас. %:
Средство может содержать в активной части только аскорбиновую кислоту, а в качестве гелеобразующей основы смесь желатины с глицерином при следующем соотношении компонентов, мас. %:
В случае наличия в активной части только аскорбиновой кислоты средство может содержать в качестве гелеобразующей основы смесь триблок сополимера этиленоксида и пропиленоксида с желатиной при следующем соотношении компонентов, мас. %:
В случае наличия в активной части только аскорбиновой кислоты средство может содержать в качестве гелеобразующей основы смесь триблок сополимера этиленоксида и пропиленоксида с желатиной и тетраглицеролатом кремния при следующем соотношении компонентов, мас. %:
В случае наличия в активной части только аскорбиновой кислоты средство может содержать в качестве гелеобразующей основы смесь кондитерского жира и пчелиного воска, и дополнительно содержать неионное поверхностно-активное вещество ТВИН-80 при следующем соотношении компонентов, мас. %:
Используют гидрохлорид хитозана с молекулярной массой (ММ) 30-70 кДа и степенью дезацетилирования ≥75-80 мол.%.
D-аскорбиновая кислота - антиоксидант, в составе ветпрепаратов при интравагинальном применении снижает рН, ингибируя рост бактерий, а также способствует восстановлению и поддержанию нормальных показателей рН и флоры.
Борная кислота - одноосновная кислота, обладающая фунгистатической и бактериостатической активностью. Используется при лечении грибковых заболеваний.
Pluronic F - 127 (Pl F - 127) - триблок сополимер этиленоксида и пропиленоксида с молекулярной массой 12.6 кДа. Является нетоксичным неионногенным поверхностно-активным веществом. Разрешен к использованию в фармацевтике в качестве основы для гидрогелей (European Pharmacopoeia 5-th Edition, Order Code P2164030).
Тетраглицеролат кремния (Si(OGly)4) - раствор глицеролата кремния в глицерине (GlyOH) при мольном соотношении Si(OGly)4 : GlyOH = 1:3. Биологически активное вещество, проявляет транскутанную и антибактериальную активности. В водной среде гидролизуется с протеканием золь-гель реакции и формированием полисилоксановой пространственной сетки ≡Si-О-Si≡ связей, центрами нуклеации которых выступают свободные гидроксигруппы. Золь-гель гидрогели на основе тетраглицеролата кремния рекомендованы для практического использования в качестве самостоятельных лекарственных средств или основ фармацевтических композиций.
Глицерин (Gly(ОН)3) в составе водно-глицериновой среды является растворителем для тетраглицеролата кремния и пластификатором для хитозана. Разрешен к применению в медицине.
Желатина - частично гидролизованный белок коллаген. Используется как гелеобразующий компонент для получения лекарственных препаратов в виде гелей и свечей.
Пчелиный воск - продукт жизнедеятельности пчёл с большим спектром лечебных свойств и применений. В качестве загущающий добавки входит в состав гелей и свечей.
Кондитерский жир - очищенный животный жир. Используется в фармацевтике в качестве мазевой и суппозиторной основы.
ТВИН-80 - неионное поверхностно-активное вещество природного происхождения, применяется для стабилизации эмульсий, в том числе фармакологического назначения.
Вязкоупругие свойства оценивают по величине модуля упругости (G') и потерь (G") в осцилляционном режиме на ротационном вискозиметре Rheotest RN4.1 (Германия) с системой измерения «конус-цилиндр» при постоянной амплитуде 0.01 мНм в диапазоне частот (ω) 0.5-10 Гц при 4, 25 и 37°С и времени термостатирования 30 мин.
Время фазового перехода «жидкость-гидрогель» оценивают визуально при 37°С по времени потери текучести системы методом переворачивания колбы. За время гелеобразования принимают время, по истечении которого система переходит в гелеобразное состояние и не проявляет течения в течение 10-15 сек.
Антибактериальную активность исследуют методом диффузии в агар на культуре штаммов грамотрицательных (S. typhimurium 55) и грамположительных микроорганизмов (В. cereus 8833, S. aureus 6538). На чашки Петри со стерильным агаром наносят по 100 мкл суточной бульонной культуры микроорганизма, распределяют по поверхности стерильным шпателем и помещают в термостат при 37°С на 40 мин. Затем на поверхность чашек наносят 50 мкл испытуемых препаратов и термостатируют в течение 24 часов. Оценку результата проводят по наличию или отсутствию зоны задержки роста микроорганизмов.
Терапевтическую и профилактическую эффективность полученных средств проверяют на половозрелых коровах после отела с серозно-катаральным вагинитом. В качестве традиционной терапии сравнения используют препарат «Внутриматочные палочки с ихтиолом» (ЗАО НПП «Агрофарм»). Коровы, находящиеся в эксперименте, не подвергаются обработке другими лекарственными препаратами. Перед лечением наружные половые органы животных обмывают 0.1% водным раствором перманганата калия. Препараты вводят после утренней дойки животных интравагинально. Контроль лечения проводят 2 раза в день путем осмотра с помощью влагалищного зеркала. Динамику выздоровления оценивают по следующим клиническим признакам: уменьшение эксудативных выделений, прозрачность и консистенция экссудата.
Изобретение иллюстрируется фотографиями, на которых представлены:
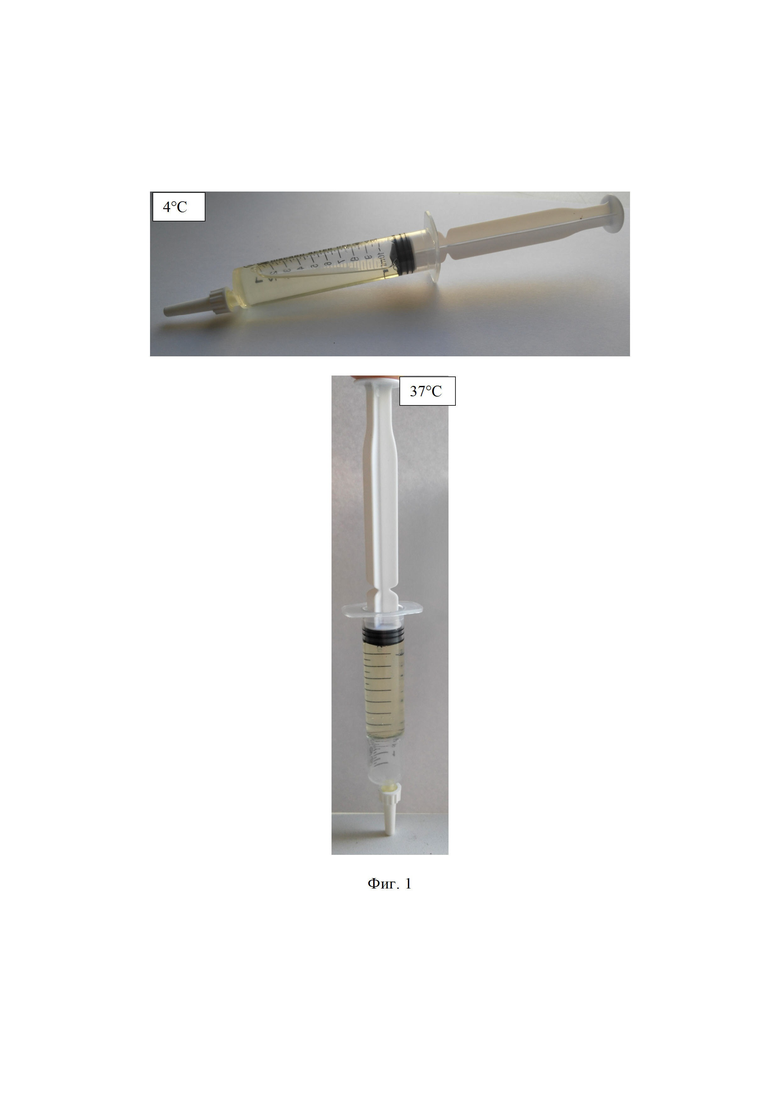
на фиг. 1 - фото инъецируемого гидрогеля на основе гидрохлорида хитозана и Pluronic F-127 при 4 и 37°С (пример №2);
на фиг. 2 - фото свечного суппозитория на основе гидрохлорида хитозана, аскорбиновой кислоты, Pluronic F-127 и желатины (пример №10);
на фиг. 3 - фото свечного суппозитория на основе гидрохлорида хитозана, аскорбиновой кислоты, Pluronic F-127, глицеролата кремния в глицерине и желатины (пример №11).
Изобретение иллюстрируется таблицами, в которых представлено:
в таблице 1 - компонентный и массовый состав, реологические параметры и время гелеобразования композиций для получения инъецируемых гидрогелей на основе гидрохлорида хитозана (примеры №1-9);
в таблице 2 - компонентный и массовый состав композиций для получения свечных суппозиториев на основе гидрохлорида хитозана (примеры №10-13);
в таблице 3 - антибактериальная активность композиций на основе гидрохлорида хитозана (пример №14);
в таблице 4 - эффективность лечения коров с послеродовым серозно-катаральном вагинитом с использованием композиций на основе гидрохлорида хитозана (примеры №15, 16).
в таблице 5 - эффективность профилактики серозно-катарального послеродового вагинита у коров с использованием композиций на основе гидрохлорида хитозана (примеры №17, 18).
Способ получения средства заключается в следующем. Готовят водный раствор гидрохлорида хитозана концентрации 1.0-3.0 мас. % в дистиллированной воде или в водном растворе органической кислоты концентрации 1.0-3.0 мас. % при мольном соотношении гидрохлорид хитозана : кислота = 1:1. Процесс растворения компонентов проводят по стандартной методике при комнатной температуре. Полученный раствор вводят в фармацевтически пригодную гелевую основу, предпочтительно состоящую (но не ограничивающуюся) из раствора Pl F-127 и/или желатины или смеси Pl F-127 и желатины с глицериновым раствором глицеролата кремния или водно-глицеринового раствора желатины или смеси кондитерского жира и пчелиного воска, механически гомогенизируют в смесителе согласно рецептуре. Полученную композицию разливают в шприцы для получения инъецируемых гидрогелей или специальные формы для получения свечного суппозитория.
Способ приготовления инъецируемого гидрогеля осуществляется следующим образом. В качестве гелеобразующей основы используют Pl F-127. Для этого готовят раствор полимера в дистиллированной воде при 4°С в течение 24 часов. В полученный раствор вводят водный или водно-кислотный раствор гидрохлорида хитозана при соотношении компонентов в готовом средстве гидрохлорид хитозана : Pl F-127 = 0.3-2.1 : 7.5-18.0, перемешивают на механической мешалке при температуре 20±2°С в течение 5-10 мин, разливают в инъекционные шприцы заданного объема (1-20 мл) и хранят при температуре не выше 4-15°С. Оптимальными для формирования инъецируемого гидрогеля считают условия, при которых фазовый переход «жидкость-гидрогель» реализуется при Т≥25-37°С, при этом значение G>Gʺ, а время гелеобразования (t) составляет не более 5 мин.
Способ формования свечных суппозиториев осуществляется следующим образом. В качестве гелеобразующей основы используют: 6-13% водный раствор желатины или смесь 6% водного раствора желатины и глицерина в соотношении 1:2 или смесь 13% водного раствора желатины и 25% водного раствора Pl F-127 или их смесь с глицериновым раствором глицеролата кремния или смесь кондитерского жира и пчелиного воска в соотношении 5:1. При необходимости в систему дополнительно вводят эмульгатор. Все используемые гелеобразные основы предварительно расплавляют на водяной бане при 60-80°С в течение 1-2 час, вводят водный или водно-кислотный раствор гидрохлорида хитозана при соотношении компонентов гидрохлорид хитозана : гелеобразующая основа = 0.3-3.0 : 14.5-77.0, перемешивают, разливают в форму для изготовления свечей и охлаждают до 4-15°С в течение 24 часов. Готовый суппозиторий в виде свечного стержня помещают в герметичную упаковку и хранят в темном месте при температуре не выше 15°С.
Группа примеров №1-6. Получение инъецируемых гидрогелей на основе гидрохлорида хитозана (таблица 1).
Пример №1. Готовят 1 мас.% водный раствор гидрохлорида хитозана с ММ = 30 кДа и 25 мас. % водный раствор Pluronic F-127. Растворы гидрохлорида хитозана и гелеобразующей основы смешивают в объемном соотношении 30:70, перемешивают на механической мешалке при 20°С в течение 5-10 мин, расфасовывают в инъекционные шприцы объемом 10 мл и хранят при 4°С. Состав и содержание компонентов, мас.%:
гидрохлорид хитозана - 0.3;
гелеобразующая основа (Pluronic F-127) - 17.5;
вода - остальное.
Значения модулей упругости (G') и потерь (Gʺ) составляют: 4°С – 0.7 и 0.7 кПа; 25°С – 1.0 и 1.0 кПа; 37°С – 5.0 и 5.0 кПа, соответственно. Гелеобразования композиции при температуре 30°С и выше не происходит.
Пример №2. Все стадии аналогичны примеру №1. Отличие состоит в том, что используют гидрохлорид хитозана с ММ = 70 кДа, его 5 мас.% водный раствор и 15 мас.% раствор Pluronic F-127, которые смешивают в объемном соотношении 10:90. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.5;
гелеобразующая основа (Pluronic F-127) – 13.5;
вода – остальное.
Значения модулей упругости (G') и потерь (Gʺ) составляют: 4°С – 0.2 и 0.3 кПа; 25°С – 0.2 и 0.6 кПа; 37°С – 1.5 и 0.2 кПа, соответственно. Время гелеобразования (t) при температуре 37°С составляет 3 мин.
Пример №3. Все стадии аналогичны примеру №2. Отличие состоит в том, что используют 7 мас.% водный раствор гидрохлорида хитозана и 20 мас. % раствор Pluronic F-127. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.7;
гелеобразующая основа (Pluronic F-127) – 18.0;
вода – остальное.
Значения G' и Gʺ: 4°С – 0.1 и 0.1 кПа; 25°С – 0.9 и 0.5 кПа; 37°С – 1.6 и 0.5 кПа, соответственно; t = 3 мин.
Пример №4. Все стадии аналогичны примеру №1. Отличие состоит в том, что используют гидрохлорид хитозана с ММ = 38 кДа, его 3 мас. % водный раствор и 25 мас. % водный раствор раствор Pluronic F-127. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.9;
гелеобразующая основа (Pluronic F-127) – 17.5;
вода – остальное.
Значения G' и Gʺ: 4°С – 1.0 и 1.0 кПа; 25°С – 3.5 и 3.2 кПа; 37°С – 32.0 и 28.0 кПа, соответственно; t = 3 мин.
Пример №5. Все стадии способа получения гидрогеля аналогичны примеру №4. Отличие заключается в том, что в состав гидрогеля дополнительно вводят D-аскорбиновую кислоту при мольном соотношении гидрохлорид хитозана : D-аскорбиновая кислота – 1:1. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.9;
D-аскорбиновая кислота – 0.9;
гелеобразующая основа (Pluronic F-127) – 17.5;
вода – остальное.
Значения G' и Gʺ: 4°С – 1.0 и 1.0 кПа; 25°С – 12.4 и 12.8 кПа; 37°С – 15.3 и 13.0 кПа, соответственно; t = 3 мин.
Пример №6.
Все стадии способа получения гидрогеля аналогичны примеру №5. Отличие в том, что используют борную кислоту. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.9;
борная кислота – 0.9;
гелеобразующая основа (Pluronic F-127) – 17.5;
вода – остальное.
Значения G' и Gʺ: 4°С – 3.0 и 3.0 кПа; 25°С – 10.0 и 20.0 кПа; 37°С – 78.0 и 25.0 кПа, соответственно; t = 3 мин.
Пример №7. Все стадии способа получения гидрогеля аналогичны примеру №1. Отличие состоит в том, что используют 3 мас. % водный раствор гидрохлорида хитозана, растворы гидрохлорида хитозана и Pluronic F-127 смешивают в объемном соотношении 50:50. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 1.5;
гелеобразующая основа (Pluronic F-127) – 12.5;
вода – остальное.
Значения G' и Gʺ: 4°С – 5.0 и 5.0 кПа; 25°С – 20.0 и 18.0 кПа; 37°С – 25.0 и 24.0 кПа, соответственно; t = 5 мин.
Пример №8. Все стадии способа получения гидрогеля аналогичны примеру №3. Отличие состоит в том, что используют 8 мас. % водный раствор гидрохлорида хитозана, растворы гидрохлорида хитозана и Pluronic F-127 смешивают в объемном соотношении 20:80. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 1.6;
гелеобразующая основа (Pluronic F-127) – 16.0;
вода – остальное.
Значения G' и Gʺ: 4°С – 0.1 и 0.1 кПа; 25°С – 0.4 и 0.3 кПа; 37°С – 1.3 и 0.5 кПа, соответственно; t = 5 мин.
Пример №9. Все стадии способа получения гидрогеля аналогичны примеру №4. Отличие состоит в том, растворы гидрохлорида хитозана и Pluronic F-127 смешивают в объемном соотношении 70:30. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 2.1;
гелеобразующая основа (Pluronic F-127) – 7.5;
вода – остальное.
Значения G' и Gʺ: 4°С – 3.0 и 3.0 кПа; 25°С – 16.0 и 17.0 кПа; 37°С – 20.0 и 20.0 кПа, соответственно. Гелеобразования при температуре 30°С и выше не происходит.
Таким образом, на основании примеров №1-9 можно заключить, что оптимальным для формирования инъецируемого гидрогеля является соотношение гидрохлорид хитозана : Pl F-127 = 0.5-1.6 : 12.5-18.0. В данном диапазоне соотношений компонентов композиция при 4 и 25°С представляет собой жидкость, а при физиологической температуре 37°С – формоустойчивый гидрогель.
Группа примеров №10-13. Получения свечных суппозиториев на основе гидрохлорида хитозана (таблица 2).
Пример №10. Способ получения суппозитория аналогичен примеру №5. Отличие в том, что в композицию дополнительно вводят нагретый до 60°С 13% раствор желатины в соотношении компонентов раствор гидрохлорида хитозана в D-аскорбиновой кислоте : раствор Pluronic F-127 : раствор желатины = 0.3 : 0.7 : 2.0, смешение компонентов проводят при 60°С, полученную композицию разливают в форму для изготовления свечей и охлаждают до 4-15°С в течение 24 часов. Готовый суппозиторий в виде свечного стержня помещают в герметичную упаковку и хранят в темном месте при температуре не выше 15°С. Состав и содержание компонентов, мас.%:
гидрохлорид хитозана – 0.3;
D-аскорбиновая кислота – 0.3;
гелеобразующая основа (Pluronic F-127 + желатина) – 14.5;
вода – остальное.
Пример №11.
Все стадии получения свечного суппозитория аналогичны примеру №10. Отличие в том, что в композицию дополнительно вводят глицериновый раствор глицеролата кремния в соотношении компонентов раствор гидрохлорида хитозана в D-аскорбиновой кислоте : раствор Pluronic F-127 : раствор желатины : раствор глицеролата кремния = 0.3 : 0.7 : 1 : 2. Состав и содержание компонентов, мас.%:
гидрохлорид хитозана – 0.3;
D-аскорбиновая кислота – 0.3;
гелеобразующая основа (Pluronic F-127 + желатина + глицериновый раствор глицеролата кремния) – 29.0;
вода – остальное.
Пример №12. Стадии получения свечного суппозитория аналогичны примеру №10. Отличие в том, что в качестве гелеобразующей основы используют нагретый до 70°С 6% водно-глицериновый раствор желатины, гидрохлорид хитозана и D-аскорбиновую кислоту вводят в гелеобразующую основу в виде смеси сухих порошков, смешение компонентов проводят при температуре 70°С. Состав и содержание компонентов, мас.%:
гидрохлорид хитозана – 3;
D-аскорбиновая кислота – 3;
гелеобразующая основа (глицерин + желатина) – 40.0;
вода – остальное.
Пример №13.
Все стадии получения свечного суппозитория аналогичны примеру №10. Отличие заключается в том, что в качестве гелеобразующей основы используют нагретую до 80°С смесь кондитерского жира и пчелиного воска (5:1), компоненты смешивают в соотношении раствор гидрохлорида хитозана в D-аскорбиновой кислоте : смесь кондитерского жира и пчелиного воска = 1.0 : 4.0, дополнительно вводят эмульгатор ТВИН-80, смешение компонентов проводят при температуре 80°С. Состав и содержание компонентов, мас. %:
гидрохлорид хитозана – 0.6;
D-аскорбиновая кислота – 0.6;
гелеобразующая основа (кондитерский жир + пчелиный воск) – 77.0;
эмульгатор ТВИН-80 – 3;
вода – остальное.
Экспериментально установлено, что при использовании в свечном суппозитории соотношения компонентов гидрохлорид хитозана : гелеобразующая основа = 0.3-3.0:14.5-77.0, заявленных в примерах №10-13, достигается результат изобретения.
Пример №14. Оценка антибактериальной активности композиций на основе гидрохлорида хитозана (таблица 3).
В стерильные чашки Петри со стерильным агаром вносят вносят по 100 мкл суточной бульонной культуры микроорганизмов B. cereus 8833 или S. aureus 6538 или S. typhimurium и термостатируют при 37°С в течение 40 мин. Затем на поверхность чашек наносят по 50 мкл инъецируемых гидрогелей, полученных по примерам №4-6, и термостатируют в течение 24 часов. Антибактериальную активность оценивают по наличию или отсутствию зоны задержки роста микроорганизмов.
Как видно из данных таблицы 3, все испытуемые средства проявляют антибактериальную активность в отношении всех тестируемых культур. Наибольшая антибактериальная активность наблюдается в случае грампозитивных микроорганизмов (B. cereus 8833, S. aureus 6538), а также грамнегативных микроорганизмов (S. typhimurium) для композиции, полученной по примеру №6.
Примеры №15-18. Лечение и профилактика серозно-катарального вагинита с использованием композиций на основе гидрохлорида хитозана (таблица 4, 5).
Пример №15.
Определение терапевтического эффекта композиций на основе гидрохлорида хитозана проведено на коровах черно-перстой породы в возрасте 3-4 лет, болеющих серозно-катаральным вагинитом. Исследование проведено в колхозе «Заря» Тамалинского района Пензенской области. Опытной группе животных (5 коров) применяли инъецируемый гидрогель по примеру №5 в дозировке 1 шприц на 10 мл один раз в сутки в течение 3-х дней. Животным контрольной группы (5 коров) применяли традиционный препарат «Внутриматочные палочки с ихтиолом» (производства ЗАО НПП «Агрофарм») согласно инструкции.
Положительная динамика у животных, лечение которых проводили с использованием инъецируемого гидрогеля, отмечалась на 2 сутки лечения и достигала 40% выздоровевших животных. В контроле на 2 сутки лечения наблюдалось лишь 20% выздоровевших животных. Полное выздоровление животных опытной группы наблюдалось на 3 сутки лечения, контрольной группы – на 5 сутки.
Пример №16. Все стадии лечения коров с серозно-катаральным вагинитом (опытная группа и контроль) аналогичны примеру №15. Отличие в том, что лечение животных опытной группы осуществляли с применением свечных суппозиториев по примеру №12.
Положительная динамика у животных, лечение которых проводили с использованием свечного суппозитория, отмечалась уже на первые сутки лечения и достигала 20% выздоровевших. На вторые сутки лечения количество выздоровевших животных составило 60%. Полное выздоровление (100% выздоровевших животных) наблюдалось на 3 сутки лечения.
Пример №17. Все стадии профилактической терапии коров, направленной на предупреждение появления серозно-катарального вагинита, аналогичны примеру №15. Отличие в том, что терапию проводят на коровах на 2-3 день после отела (после закрытия шейки матки), еще не проявляющих признаки серозно-катарального вагинита, с однократным применением препарата.
В опытной группе в течение 5 суток наблюдения животных, заболевших острым серозно-катаральном вагинитом, не выявлено. В контроле на 2 сутки наблюдалось 60% заболевших животных. В течение следующих 3 суток наблюдения процент заболевших животных контрольной группы не изменился. В дальнейшем контрольной группе животных применяли медикаментозное лечение с использованием антимикробных средств («Нитокс 200», «Дитрим») до полного выздоровления.
Пример №18. Все стадии профилактической терапии коров аналогичны примеру №17. Отличие в том, что терапию проводили с применением свечных суппозиториев, полученных по примеру №12. В опытной группе на 3 сутки наблюдений отмечалось 20% заболевших животных. В течение следующих 3 суток наблюдения процент заболевших животных контрольной группы не изменился. В дальнейшем животных опытной группы лечили аналогично примеру №16 до полного выздоровления.
Из примеров №15, 16 и таблицы 4 видно, что в группах животных, лечение которых осуществлялась с применением композиции на основе хитозана в виде инъецируемого гидрогеля или свечного суппозитория, эффективность выздоровления существенно выше по сравнению со стандартным терапевтическим лечением.
Из примеров №17, 18 и таблицы 5 видно, что в группах животных, профилактическая терапия которых осуществлялась с применением композиции на основе гидрохлорида хитозана в виде инъецируемого гидрогеля или свечного суппозитория, наблюдается более высокий профилактический эффект по сравнению со стандартной терапией.
Кроме того, лечение и профилактика серозно-катарального вагинита коров с применением разработанных средств на основе гидрохлорида хитозана не накладывает ограничение на использование молока и мяса животных в пищевых целях как во время, так и в первые несколько суток после лечения.
Таблица 1
Компонентный и массовый состав, реологические параметры и время гелеобразования композиций для получения инъецируемых гидрогелей на основе хитозана
хитозана
Таблица 2
Компонентный и массовый состав композиций для получения свечных суппозиториев на основе хитозана
ММ = 38 кДа
кислота
Таблица 3
Антибактериальная активность композиций на основе хитозана
тест-культуры
+ – умеренная антибактериальная активность;
++ – высокая антибактериальная активность.
Таблица 4
Эффективность лечения коров с послеродовым серозно-катаральном вагинитом с использованием композиций на основе хитозана
Таблица 5
Эффективность профилактики серозно-катарального послеродового вагинита у коров с использованием композиций на основе хитозана
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОДЕГРАДИРУЕМАЯ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКАЯ ГИДРОГЕЛЕВАЯ ПЛАСТИНА И СПОСОБ ЕЁ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2020 |
|
RU2732241C1 |
| ГИДРОГЕЛЬ НА ОСНОВЕ КОМПЛЕКСНОЙ СОЛИ ХИТОЗАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2617501C1 |
| ГИДРОГЕЛЕВЫЙ МАТЕРИАЛ НА ОСНОВЕ СОЛИ ХИТОЗАНСОДЕРЖАЩЕГО ВЕЩЕСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2707973C1 |
| Композиция для получения гидрогеля | 2017 |
|
RU2657826C1 |
| ГИДРОГЕЛЕВЫЙ МАТЕРИАЛ НА ОСНОВЕ СОЛИ ХИТОЗАНСОДЕРЖАЩЕГО ВЕЩЕСТВА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2695223C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ N,N'-БИС[2-(1Н-ИМИДАЗОЛ-4-ИЛ)ЭТИЛ]МАЛОНАМИДА | 2022 |
|
RU2818073C2 |
| ПОЛИМЕРНЫЕ КОМПОЗИТЫ, ПОЛУЧЕННЫЕ ПО СПОСОБУ ЗОЛЬ-ГЕЛЬ, И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2761212C2 |
| ЖИДКИЙ ГИДРОГЕЛЕВЫЙ ПЛАСТЫРЬ И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2022 |
|
RU2799938C1 |
| ПРОФИЛАКТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ВЕЩЕСТВ ФЕНОЛЬНОЙ ПРИРОДЫ В ЛИПОСОМНОЙ ФОРМЕ | 2008 |
|
RU2372929C1 |
| ХИТОЗАНСОДЕРЖАЩИЙ ГИДРОГЕЛЬ И СПОСОБ КОСМЕТИЧЕСКОГО УХОДА ЗА КОЖЕЙ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2017 |
|
RU2667130C1 |

Изобретение относится к области фармацевтики и ветеринарной медицины, а именно к средству для профилактики и лечения вагинита у коров. Средство содержит в качестве активной части гидрохлорид хитозана с определенной молекулярной массой и аскорбиновую или борную кислоту, а в качестве вспомогательной части − гелеобразующую основу, выбранную из триблок сополимера этиленоксида и пропиленоксида, или смеси желатины с глицерином, или триблок сополимера этиленоксида и пропиленоксида с желатиной, или триблок сополимера этиленоксида и пропиленоксида с желатиной и тетраглицеролатом кремния, или кондитерского жира с пчелиным воском и неионного поверхностно-активного вещества ТВИН-80, а также воду при определенном соотношении компонентов. Изобретение обеспечивает получение высокоэффективного биологически активного средства на основе гидрохлорида хитозана для лечения и профилактики вагинита у крупного рогатого скота, не содержащего в своем составе антибиотиков и антисептиков, выполненного в форме инъецируемой композиции или свечного суппозитория, причем инъецируемая композиция при температуре менее 4-15° представляет собой жидкость, а при температурах, близких к физиологическим, претерпевает фазовый переход в формоустойчивый гидрогель. 5 табл., 18 пр., 3 ил.
Средство для профилактики и лечения вагинита у коров, содержащее активную и вспомогательную части, отличающееся тем, что оно содержит в качестве активной части гидрохлорид хитозана с молекулярной массой 30-70 кДа и аскорбиновую или борную кислоту, а в качестве вспомогательной части − гелеобразующую основу, выбранную из триблок сополимера этиленоксида и пропиленоксида, или смеси желатины с глицерином, или триблок сополимера этиленоксида и пропиленоксида с желатиной, или триблок сополимера этиленоксида и пропиленоксида с желатиной и тетраглицеролатом кремния, или кондитерского жира с пчелиным воском и неионного поверхностно-активного вещества ТВИН-80 при следующем соотношении компонентов, мас.%:
| ВНУТРИМАТОЧНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВУЛЬВОВАГИНИТОВ У КОРОВ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2008 |
|
RU2375067C1 |
| ГИДРОГЕЛЬ НА ОСНОВЕ КОМПЛЕКСНОЙ СОЛИ ХИТОЗАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2617501C1 |
| ГЕЛЕОБРАЗНАЯ КОМПОЗИЦИЯ ШИРОКОГО СПЕКТРА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ | 2013 |
|
RU2535141C1 |
| Композиция для получения гидрогеля | 2017 |
|
RU2657826C1 |
| DOMINGUEZ-DELGADO C | |||
| L | |||
| et al | |||
| Способ получения морфия из опия | 1922 |
|
SU127A1 |
| Токарный резец | 1924 |
|
SU2016A1 |
| - P | |||
| Рельсовая педаль | 1922 |
|
SU1513A1 |
| МАЛИНКИНА О | |||
| Н | |||
| и др | |||
Авторы
Даты
2021-07-19—Публикация
2020-07-02—Подача