Настоящее изобретение относится к биотехнологии в частности к выделенному из растения штамму Bacillus subtilis П19, производящему антимикробное вещество пептидной природы (бактериоцин), способу его получения и заключения в липосомы.
Предшествующий уровень техники
Бесконтрольное применение антибиотиков привело к глобальной проблеме множественной лекарственной устойчивости среди микроорганизмов, создавая трудности при лечении инфицированных больных. Одним из подходов к решению данной проблемы является применение натуральных пробиотиков, и противомикробных веществ, лишенных деструктивного влияния на кишечный микробном, особенно свойственного традиционным антибиотикам.
Наиболее доступным и экономически оправданным источником антимикробных веществ натурального происхождения являются микроорганизмы. На сегодня известны многие тысячи таких соединений и наиболее перспективные из них теперь могут быть синтезированы химически [Nguyen, 2018]. Чтобы определить, какие из антимикробных веществ могут принести практическую пользу, а какие нет, необходимо их предварительно изучить. К числу наиболее интересных с потенциалом терапевтического применения, как считают большинство исследователей, относятся противомикробные пептиды [Cotter et al. 2005]. Исследование противомикробных пептидов включает их скрининг на предмет спектра антимикробной, антигрибковой, противовирусной, иммуномодулирующей, иммуносупрессирующей, противовоспалительной и противоопухолевой активностей.
Противомикробные пептиды это четыре разнородных класса веществ, отличающиеся молекулярной массой, химическим строением, устойчивостью и спектром бактериоцидного действия [Drider et. al., 2006; Klaenhammer, 2008; Abriouel et. al., 2011; Cochranea et. al., 2016; Olishevska et. al., 2019].. Наиболее изученными являются низкомолекулярные пептиды или лантибиотики [Parisot et. al., 2008; Spies et. al., 2015]. Лантибиотики обладают летальным действием на патогенные грамположительные бактерии (например, бациллы группы В. cereus-thuringiensis) и некоторые плесневые грибки (например, Aspergillus flavus), вызывающие пищевые отравления. Этот класс пептидов наиболее часто находит применение в качестве биоконсервантов для защиты скоропортящихся пищевых продуктов от микробной контаминации, для подавления патогенных бактерий и предотвращения инфекций у людей и животных. Наряду с лантибиотиками непатогенные виды Bacillus способны продуцировать и полезные вторичные метаболиты. Например, это сурфактин и микосубтилизин, представляющие собой амфифильные липопептиды, которые способны снижать поверхностное натяжение среды обитания, разрушая тем самым клеточные мембраны организмов. Эти свойства делают их очень сильными противовирусными и антимикробными соединениями.
У представителей рода Bacillus выделены и описаны такие лантибиотики как субтилин, субтилозин А, эрицин, мерцацидин, субтиломицин, субланцин, эпидермин [Parisot J., et al., 2008; Сидорова T.M. и др., 2018]. Технология их выделения базируется, в основном на методах мембранной фильтрации, экстракции в системе органических растворителей и хроматографии [Патент РФ №2553547]. У каждого из них имеются преимущества и недостатки. Так, преимуществом мембранных методов выделения целевого вещества является сокращение времени проведения процессов, а главными недостатками - сложности в подборе мембран с требуемым отсечением по молекулярному весу, вариабельность свойств, существенные физические потери и падение активности продукта. Методы экстракции в органических растворителях дают возможность выделять вещество из значительного объема ферментата, но при этом экстрактивные субстанции часто могут быть токсичными как для оператора, окружающей среды, так и конечного потребителя препарата прочно встраиваясь в его структуру.
Известен способ получения субтилозина, основанный на обработке н-бутанолом бесклеточного ферментата Bacillus subtilis [Babasaki, K. et al., 1985; Huang Т., et al., 2009]. Супернатант культуральной жидкости (500 мл) экстрагируют добавлением четверти объема н-бутанола (125 мл) и встряхиванием в течение 1 ч, а полученную смесь оставляют на ночь в делительной воронке. Образуемый органический слой концентрируют с образованием желтого остатка, который ресуспендируют в метаноле (5 мл). Грубый субтилозин очищают методом высокоэффективной жидкостной хроматографии с использованием колонки Waters Bondapak С18. Смыв с колонки начинают с 20% до 80% и заканчивают 20% ацетонитрилом (CH3CN) в течение 40 мин. Чистый продукт лиофилизируют, получая 3 мг субтилозина на 1 л среды культивирования.
Наиболее близким к предлагаемому изобретению является метод концентрирования бактериоцина на поверхности клеток молочнокислых бактерий при кислых значениях рН с последующей их экстракцией [Yang R., et al., 1992]. К недостаткам этого способа можно отнести сильное варьирование выхода и чистоты целевых продуктов, применение NaCl и, в связи с этим, использование малопроизводительного метода диализа солевого раствора бактериоцина.
Техническим результатом является получение летально действующего на патогенные бактерии грамположительной природы - В. anthracis, В. cereus, L. monocytogenes и некоторые штаммы Staphylococcus aureus за счет выработки им низкомолекулярного антимикробного пептида (АМП).
Технический результат достигается тем, что предложен штамм Bacillus subtilis П19, который вырабатывает низкомолекулярный антимикробный пептид, обладающий активностью против патогенных микроорганизмов грамположительной природы, а также способ получения низкомолекулярного антимикробного пептида из культуральной жидкости штамма Bacillus subtilis П19 путем концентрирования на клетках штамма-продуцента, с дальнейшим его сбором с клеточной поверхности, очисткой и стабилизацией, причем способ осуществляется закислением культуральной жидкости до рН 2,5 с последующим выделением, ресуспендированием осадка клеточной массы в воде (1:10/объемы) с восстановлением концентрированной взвеси клеточной массы до нейтральных значений рН (7,0±0,2), обработкой концентрата смесью 96° этанола и ацетонитрила в соотношении объемов (1,0:0,9:0,1 / соответственно), дальнейшим осаждением, сбором супернатанта, его упариванием и растворением получаемого преципитата в воде, молекулярная масса АМП составляет 3,4 кДа.
Технический результат также достигается тем, что предложен инкапсулированный в липосомы препарат, содержащий низкомолекулярный пептид АМП 0,5-1,0 мг, липиды 4,2-4,8 мг, поливинилпирролидон 3,8 мг, соли фосфатов и натрий 5,0-5,5 мг.
Отличием и преимуществом предлагаемого изобретения является прием концентрирования бактериоцина на клетках штамма-продуцента из рода Bacillus с последующей его экстракцией этанолом и ацетонитрилом (9:1), что существенно (в разы) сокращает временные и материальные затраты на его выделение из культуральной жидкости.
Штамм Bacillus subtilis П19 нами выделен из растительного сырья страстоцвета (Passiflora edulis). Штамм Bacillus subtilis П19, обладающий антагонистическим действием на некоторые представители патогенных микроорганизмов, в частности, на листерии, бациллы и кокки, депонирован в «ГКПМ - Оболенск» под № В-8711.
Описание графических материалов
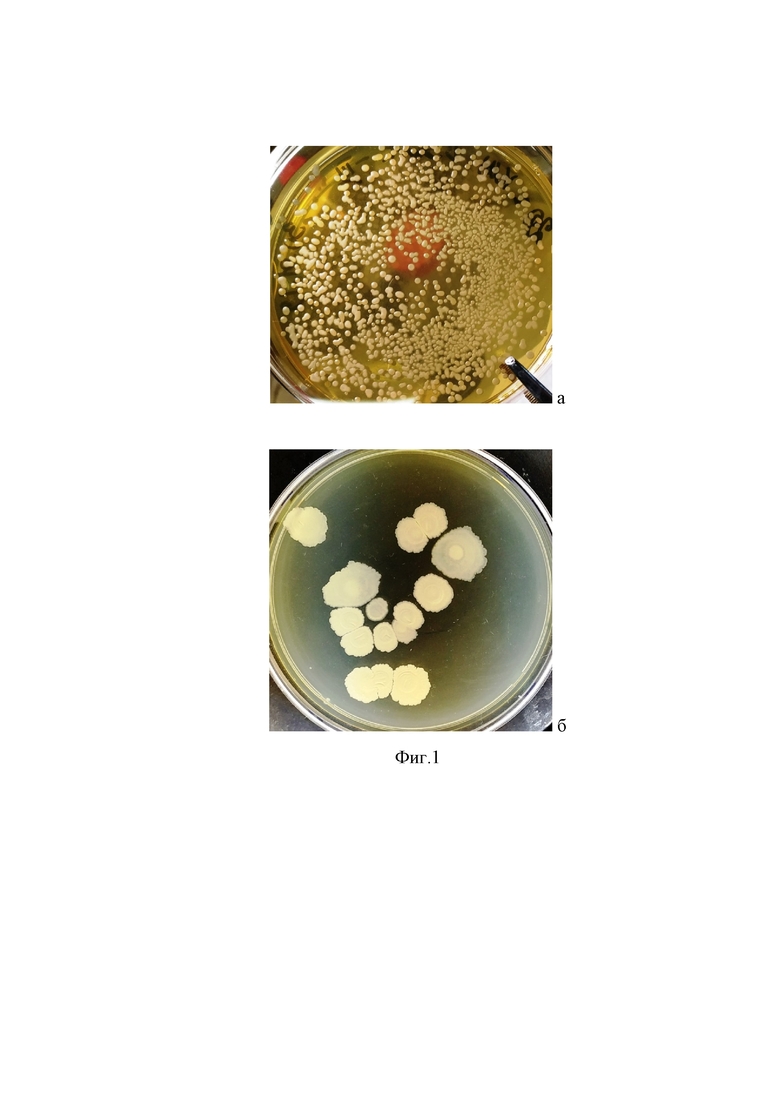
На фиг. 1 представлены суточные колонии штамм В. subtilis П19, выращенные при 36°С при высокой (около 500 КОЕ/мл, а) и низкой (15 КОЕ/мл, б) концентрации клеток в посевах на ГРМ-агаре.
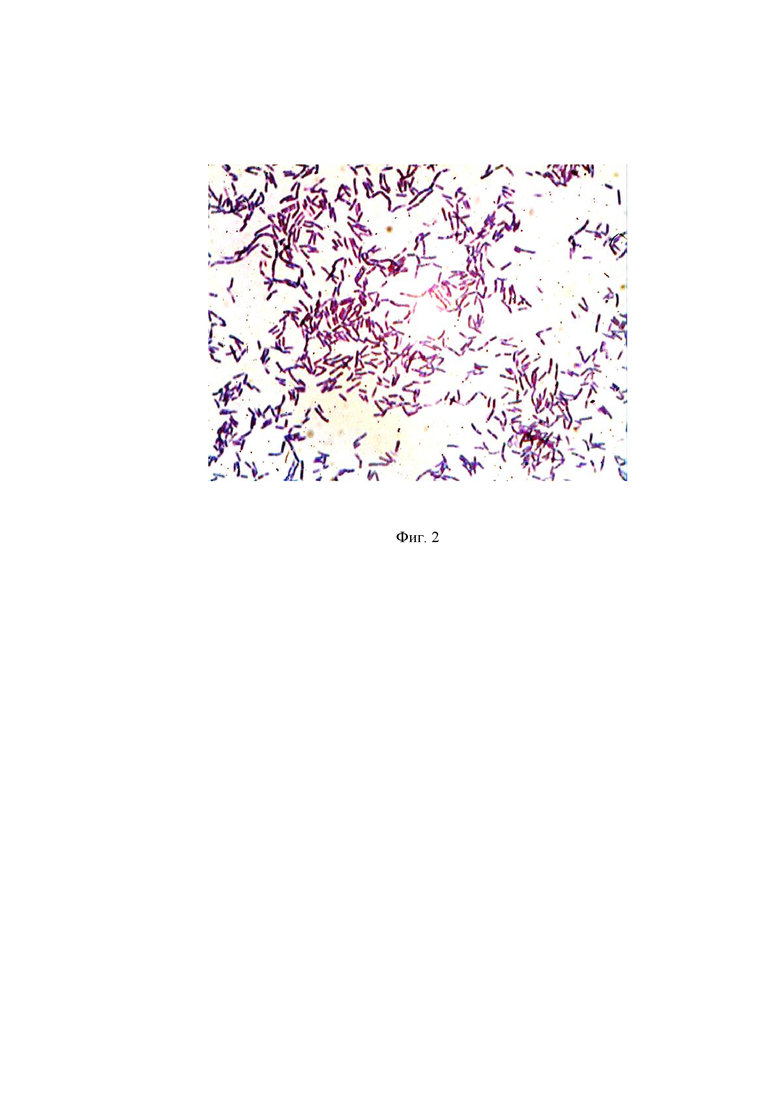
На фиг. 2 суточные колонии штамм В. subtilis П19 выращенные при 36°С в ГРМ-бульоне
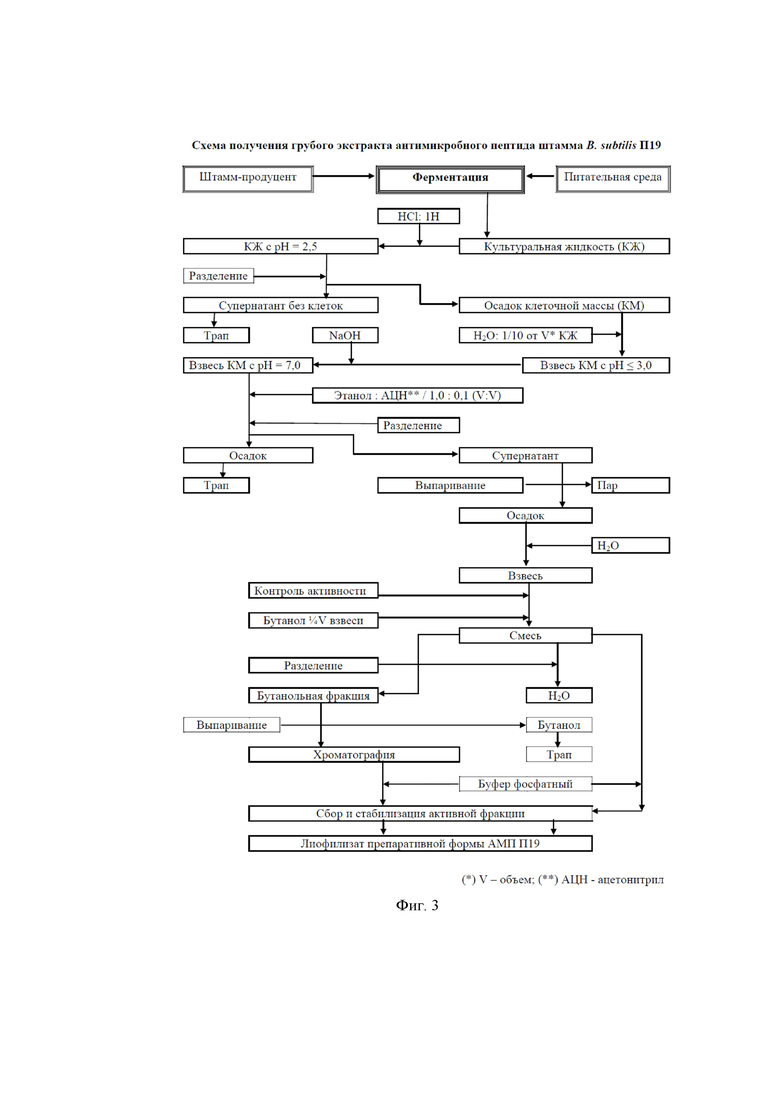
На фиг. 3 приведена схема получения грубой фракции бактериоцина.
На фиг. 4. чашки с индикаторый штаммом с результатами определения титра антимикробной активности пробы полученного экстракта клеточной поверхности (ЭКП) до и после обработки бутанолом.
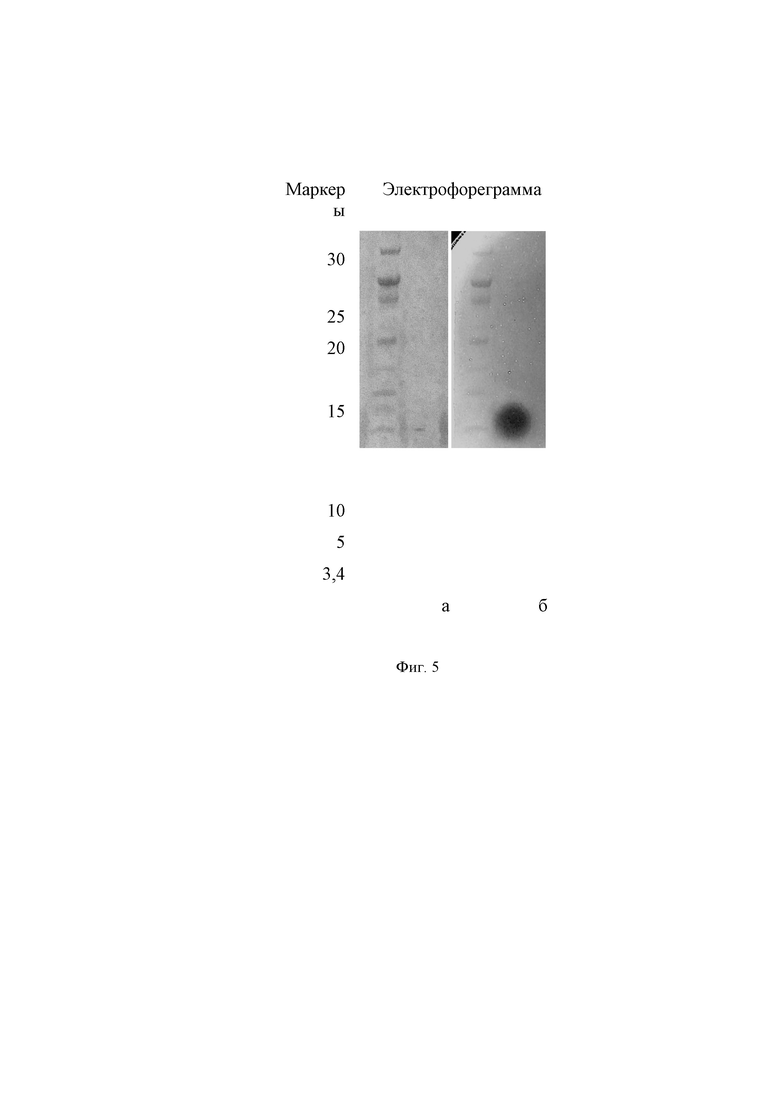
На фиг. 5 гель-электрофорез пептида в системе Tris-tricine SDS-PAGE (18%) с последующим биотестированием гелевой пластины индикаторным штаммом, позволяющим определить наличие и молекулярную массу активной фракции. Использовали пептидные маркеры PageRuler™ Low Range, кДа; а - ПААГ с BS после окраски Coomassie brilliant blue G250.
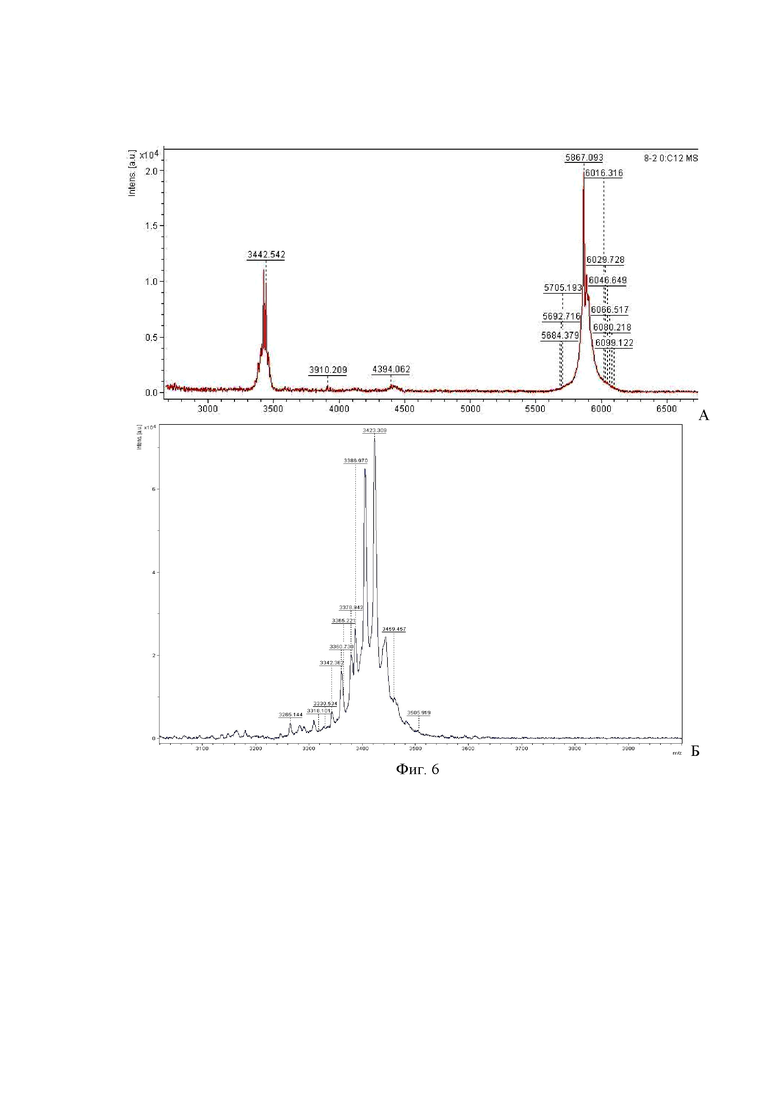
На фиг. 6 приведены данные масс-спектроскопии методом MALDI-TOFF в процессе выделения бактериоцина после экстракции этанолом (А) и после дополнительной обработки полученного раствора бутанолом (Б), демонстрирующие наличие пика в 3,4 кДа, который соответствует субтилозину.
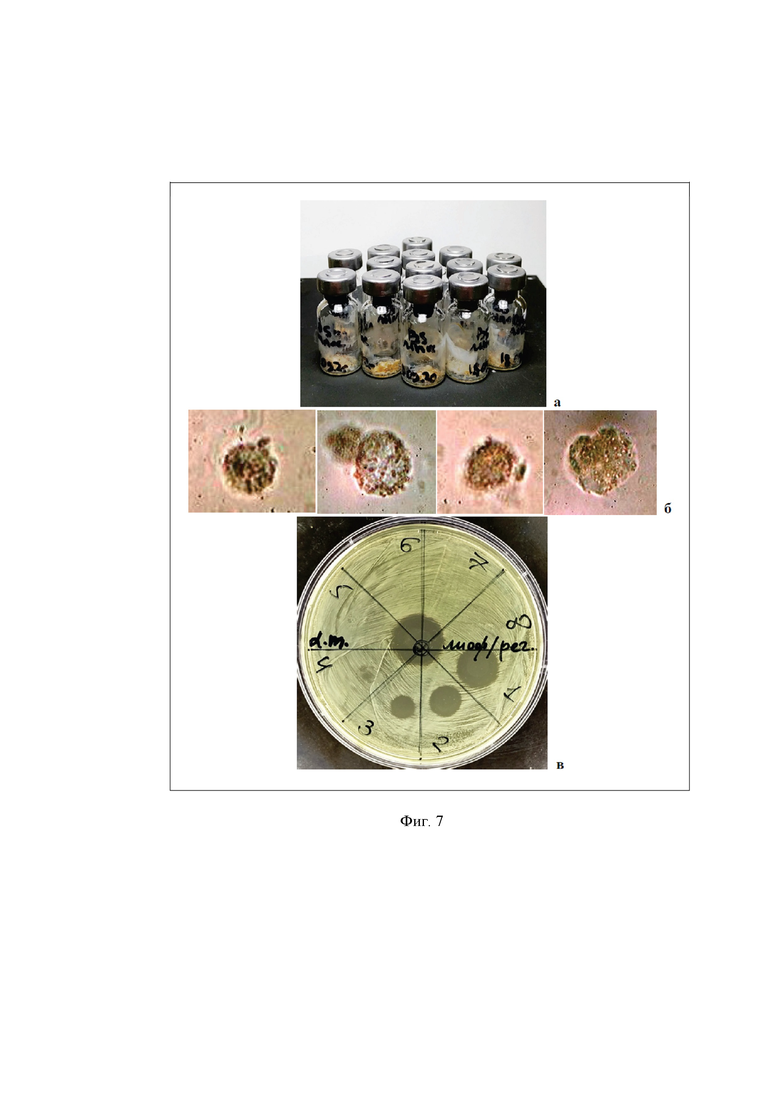
На фиг. 7 представлены флаконы, содержащие лиофилизированный препарат АМП на основе штамма В. subtilis П19, заключенный в липосомы (а), размером 10-50 мкм, вид липосом под микроскопом (1600х) после регидратации содержимого флакона (б), а также результаты определения титра активности липосомированного препарата, который равен 1600 АЕ/мл в отношении L. monocytogenes 766 (в).
Получение и свойства штамма продуцента АМП
Изоляты микроорганизмов были выделены из растительного сырья - страстоцвета (Passiflora edulis), обычно используемого для приготовления иммуномодуляторной пищевой добавки «Пассифлора». Изначально получили 9 антагонистически активных изолятов бациллярной природы, обозначенные как П13…П21. Наиболее активный из них далее был назван как П19. После идентификации штамма на основе культурально-морфологических, биохимических признаков он был отнесен к виду subtilis из рода Bacillus. На основании MALDI Biotyper штамм определен с высокой долей вероятности (2,32-2,357) как Bacillus subtilis. Видовая принадлежность штамма была также подтверждена методом генотипирования по 16S РНК.
Штамм В. subtilis П19, хорошо растет на агаризованных питательных средах промышленного изготовления, включая ГРМ-агар («Питательные среды», Оболенск), крахмальный агар («HiMedia», India). Оптимум роста составляет 36±1°С. Рекомендованная продолжительность глубинного выращивания в колбах при 120-150 об/мин составляет 18 ч. Суточные колонии штамма выпуклой округлой формы, светло-бежевые (фиг. 1а) и они легко снимаются с поверхности агара при помощи бактериологической петли. Одиночные колонии быстро разрастаются на питательном агаре, достигая 10-12 мм в диаметре (фиг. 1б). При этом они не высыхают, оставаясь на вид увлажненными. Клетки штамма предпочитают расти в аэробных условиях с интенсивной продукцией каталазы.
Клетки палочковидные, грамположительные, имеют размер 2-4×0,4-0,6 мкм, после деления, остаются соединенными в короткие цепи (фиг. 2). В клетках просматриваются проспоры, которые не раздувают клетки и располагаются в ее центре. Клетки подвижные с перитрихиальным расположением жгутиков. Споры овальные, не превышающие размер клетки, расположены преимущественно центрально.
Культура ферментирует глюкозу, сахарозу, маннит и мальтозу. Дает положительную реакцию Фогес-Проскауэра, гидролизует крахмал, желатину, не гидролизует мочевину, утилизирует цитрат натрия с глюкозой, не использует пропионат и малонат натрия, не расщепляет тирозин. Вырабатывает каталазу, протеазы, амилазу. Не образует лецитиназу, уреазу и липазу. Редуцирует нитраты, не образует газ на среде с нитратами в анаэробных условиях. Не образует индол и сероводород. В процессе аэробного культивирования клетки выделяют в окружающую среду соединения, ингибирующие рост некоторых штаммов грамположительных микроорганизмов - Listeria, Micrococcus, Staphylococcus, Streptococcus и Enterococcus. Штамм устойчив в полимиксину, лизоциму, чувствителен к пенициллину, стрептомицину, эритромицину, тетрациклину и новобиоцину.
Согласно санитарно-эпидемиологическому правилу СП 1.3.2322-08 «Безопасность работы с микроорганизмами III-IV групп патогенности (опасности) и возбудителями паразитарных болезней» (приложение №1) Bacillus subtilis не относится к патогенным для человека микроорганизмам. Вирулентность для лабораторных животных: в тесте на белых мышах и цыплятах не установлена.
Штамм может храниться без потери свойств при температуре 5-10°С на ГРМ-агаре не менее 6 месяцев с обязательным пересевом не реже 1 раза в 2 месяца, в замороженном виде при (-10)°С не менее 12 месяцев. Для длительного хранения штамма предпочтительна лиофилизация. Для регидратации культуры используется 0,9% физиологический раствор.
Выращивание штамма- продуцента, выделение АМП из культуральной жидкости и тестирование активности
Часть суточной колонии штамма В. subtilis П19, выращенной при 36°С на ГРМ-агаре, при помощи бактериологической петли переносят в 750 мл качалочную колбу Эрленмейера со 100 мл питательного бульона в составе (г/л): ферментативный гидролизат казеина - 7,0…10,0; дрожжевой экстракт - 5,0; сахароза - 11,0; магния сульфат - 1,0. Колб/у(ы) с инокулятом помещают в ячейку платформы термостатируемой качалки, устанавливают температуру на 36°С, задают качение в 135 оборотов/мин и время культивирования 20 ч. По завершению культивирования отбирают пробы культуральной жидкости (далее КЖ) на определение биологической чистоты (однородности), показателей кислотности (рН), концентрации живых клеток и антимикробной активности. Если показатели рН находятся в пределах 6,5-7,5 ед., в мазках при микроскопии отсутствуют посторонние микроорганизмы, а при добавлении 6% перекиси водорода к ферментату (1:1) происходит интенсивное выделение водорода в виде пенообразования, что соответствует наличию высокой каталазной активности, то КЖ берут в дальнейшую работу.
Для выделения антимикробного пептида последовательно проводят следующие процедуры (фиг. 3). Первое. КЖ с помощью концентрированной соляной кислоты (HCl, 38%) закисляют до рН 2,5 с последующим разделением смеси в поле центробежных сил (4000 об/мин, 30 мин) на центрифуге с охлаждением. Второе. Супернатант отбрасывают, а осадок клеточной массы (КМ) ресуспендируют в воде (1:10/объемы) с последующим восстановлением у концентрированной взвеси (КВ) КМ нейтральных значений рН (7,0±0,2) с помощью 0,25 М раствора едкого натра (NaOH). Третье. КВ обрабатывают смесью 96° этанола (С2Н5ОН -Эт) и ацетонитрила (CH3CN - Ацн) в соотношении объемов (1,0:0,9:0,1 / КВ: Эт: Ацн) путем перемешивания в течение 20 мин при комнатной температуре с дальнейшим осаждением на центрифуге (4000 об/мин, 10 мин) и сбором супернатанта. Четвертое. Супернатант водно-спиртового экстракта клеточной поверхности упаривают на роторном вакуумном испарителе при температуре 50-55°С, а преципитат растворяют в воде (10-15 мл), получая смесь пептидов (фиг. 5а). Пятое. Для выделения из смеси только пептида с молекулярной массой 3,4 кДа водный раствор смыва/экстракта клеточной поверхности (СКП/ЭКП) обрабатывают бутанолом (1:0,25/объемы) путем смешивания с последующим отстаиванием на холоде в течение ночи, сбором бутанольной фракции и упариванием в сушильной шкафу при температуре 70°С; преципитат растворяют в 3-5 мл воды, переливают во флакон.
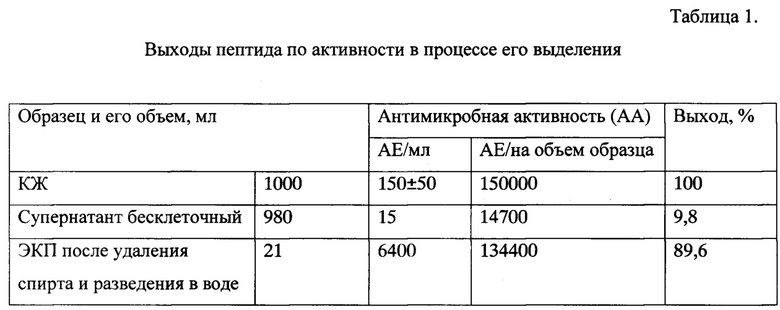
Далее определяют титр активности против листерий образцов АМП до и после бутанольной экстракции (фиг. 4), молекулярную массу методами электрофореза в системе Tris-tricine SDS-PAG (18%) с пептидными маркерами PageRuler™LowRange и масс-спектроскопии по MALDI-TOFF (фиг. 5 и 6). Обработка ЭКП бутанолом позволяет выделить из смеси пептидов (фиг. 5а) активный против грамположительных бактерий пептид (фиг. 5б), который по молекулярной массе в 3,4 кДа соответствует субтилозину - бактериоцину из группы лантибиотиков. Изучение баланса образцов АМП по активности указывает на то, что выход целевого вещества в виде водного раствора до обработки бутанолом составляет 89,6% (табл. 1).
Получение липосомальной формы АМП П19
Для приготовления липосомальной суспензии используют метод гидратации липидной пленки. Для этого в ламинарном боксе готовят смесь липидов в стерильном стеклянном стаканчике емкостью 20-50 мл, последовательно внося мл раствора POPE (50 мг липида), 0,9 мл раствора холестерола (90 мг), 1 мл раствора лецитина (100 мг) и 0,6 мл раствора СтПЭГ400 (60 мг), и на выходе получая 300 мг липидов в 7,5 мл легколетучего органического растворителя. В круглодонную колбу от ротационного испарителя, выдавливают липосомальную суспензию через фильтр, обеспечивая стерилизацию липидов. Колбу подсоединяют колбу к приемному патрубку ротационного испарителя, включают вращение, затем вакуум, избегая вскипания жидкости в колбе. При полном высыхании на стенках колбы образуется полупрозрачная пленка липидов. По окончании сушки выключают вакуумный насос, вращение и в установку напускают воздух через стерилизующий фильтр, колбу снимают и закрывают пробкой.
Загрузка АМП в липосомы. Раствор АМП смешивают со стерильным фосфатно-солевым буфером (ФСБ) в соотношении от 1:10 до 10:1 в зависимости от желаемой активности препарата. Полученные 15-25 мл раствора переносят в круглодонную колбу с липидной пленкой. Колбу переносят в термостатируемую качалку, устанавливая режим: температура +42°С, скорость 150 об/мин. Полное смывание липидов раствором АМП занимает от 1 до 2 часов. В процессе образуется грубая суспензия липидных везикул с включенными в них АМП (фиг. 7б)..
Полученные липосомы с АМП с подтвержденным тестом на активность (титр не менее 800 АЕ/мл, фиг. 7в) разливают по 1 мл в стеклянные флаконы, которые могут храниться в холодильнике в течение 6 месяцев. При необходимости они могут быть лиофилизированы (фиг. 7а), что дает возможность их транспортировки не опасаясь потери активности.
Пример 1. Для выбора компонентного состава среды при глубинном культивировании штамма В. subtilis П19 готовят 4 варианта питательного бульона (табл. 2).
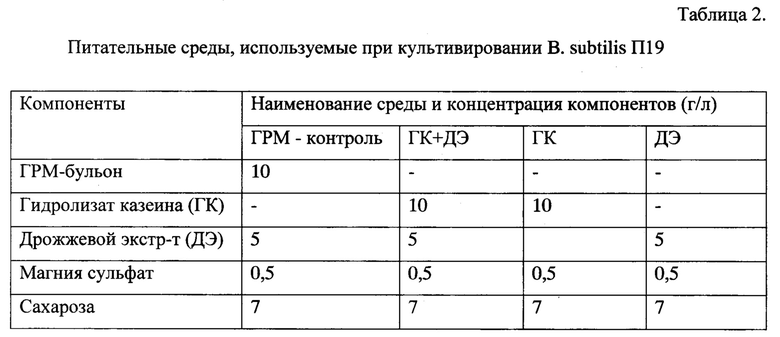
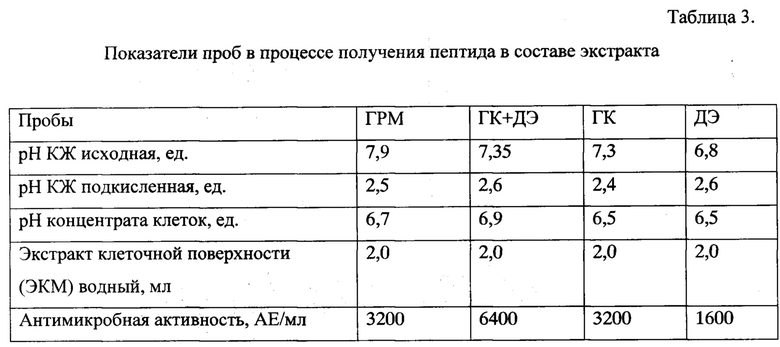
Засев 4 качал очных колб на 750 мл со 100 мл стерильного бульона указанного состава (табл. 2) проводят петлей с одной свежей колонии штамма В. subtilis П19. Посевы культивируют на качалке при 36°С, 135 об/мин в течение 21 ч. После съема колб определяют рН в КЖ и с помощью 1Н HCl снижают рН до 2,5 ед. Пробы закисленной КЖ разделяют центрифугированием (4000 об/мин, 35 мин) со сбором осадка клеточной массы (КМ) продуцента для дальнейшей работы. Осадки КМ ресуспендируют водой до 10 мл и поднимают рН до 6-7 ед. с помощью 0,1 М NaOH. Взвеси КМ обрабатывают смесью этанола с ацетонитрилом (9:1) и осаждают центрифугированием (4000 об/мин, 10 мин). Осадки отбрасывают, а супернатанты высушивают (+70°С). Получаемые преципитаты регидратируют добавлением по 2 мл воды и переливают во флаконы для проверки противимикробной активности. Алгоритм получения и показатели образцов, включая и значения их активностей против индикаторного штамма L. monocytogenes 766, приведены в табл. 3. Питательный бульон на основе гидролизата казеина (ГК), судя по представленным данным, обеспечивает получение АМП с наибольшей противимикробной активностью.
Пример 2. Для получения целевого вещества из смеси пептидов (фиг. 6А) наработку штамма-продуцента В. subtilis П19 проводят в питательном бульоне на основе гидролизата казеина со всеми последующими стадиями выделения АМП как в примере №1 (табл. 3). Для этого 2 мл водной взвеси в стеклянном флаконе на 20 мл, имеющую активность 6400 АЕ/мл против L. monocytogenes 766, разводят до 10 мл и гомогенизируют в течение 5 мин с помощью вортекса - вибрационного прибора для пробирок. Во флакон вносят 2,5 мл н-бутанола и полученную смесь тщательно (не менее 20 мин) гомогенизируют на вортексе -вибрационном приборе для пробирок. Полученную смесь центрифугируют (4000 об/мин) при субнулевой температуре в течение 30 мин. Образуемый органический слой собирают пипеткой и высушивают в стеклянной чашке при 70°С с образованием желтого остатка, который ресуспендируют в 2 мл диметилсульфоксида ((СН3)2SO - ДМСО) с водой (1:1). Полученный раствор дополнительно очищают методом высокоэффективной жидкостной хроматографии с использованием колонки Waters Bondapak С18 (WAT015814; 10 м, 125 Å, 25 на 100 мм). Элюирование начинают с 20% ацетонитрила (Ацн) в течение 5 мин, затем увеличивают до 50% Ацн в течение 20 мин и в конце снижают до 20% Ацн в течение 5 мин.
Получаемый на выходе продукт представляет собой по данным MALDI-TOFF (фиг. 6Б) пептид с молекулярной массой 4,3 кДа, как у субтилозина A [Babasaki, K. et al., 1985; Huang Т., et al., 2009].
Пример 3. Для определения активности и устойчивости АМП В. subtilis П19 его нарабатывают в процессе глубинного культивирования в колбе на 2 л с 500 мл питательного бульона в составе (г/л): гидролизат казеина - 7; дрожжевой экстракт - 5; магния сульфат - 0,5; сахароза - 10. Засев проводят предварительно 30 мл выращенной 18 ч КЖ с использованием питательного бульона на основе гидролизата казеина. Режимы культивирования: температура - 36°С; перемешивание - 120 об/мин; время - 20 ч.
После окончания выращивания штамма в КЖ с помощью 1Н HCl снижают рН до 2,5 ед. и затем проводят ее центрифугирование (4000 об/мин, 35 мин) со сбором осадка клеточной массы (КМ) для дальнейшей работы. Осадок КМ ресуспендируют водой до 20 мл и поднимают рН до 6-7 ед. с помощью 0,1 М NaOH. Взвесь КМ обрабатывают смесью этанола с ацетонитрилом (9:1) и осаждают центрифугированием (4000 об/мин, 10 мин). Собирают и высушивают супернатант (+70°С), а преципитат регидратируют добавлением 10 мл воды и переливают во флакон для проверки противимикробной активности. Из флакона отбирают 5 мл и переливают во вторую емкость для выделения пептида с помощью н-бутанола, как описано в примере 2.
Полученные пробы АМП в виде сырого экстракта (смыва) клеточной поверхности (ЭКП) до и после обработки н-бутанолом исследуют на противомикробную активность, устойчивость к протеазам и нагреву.
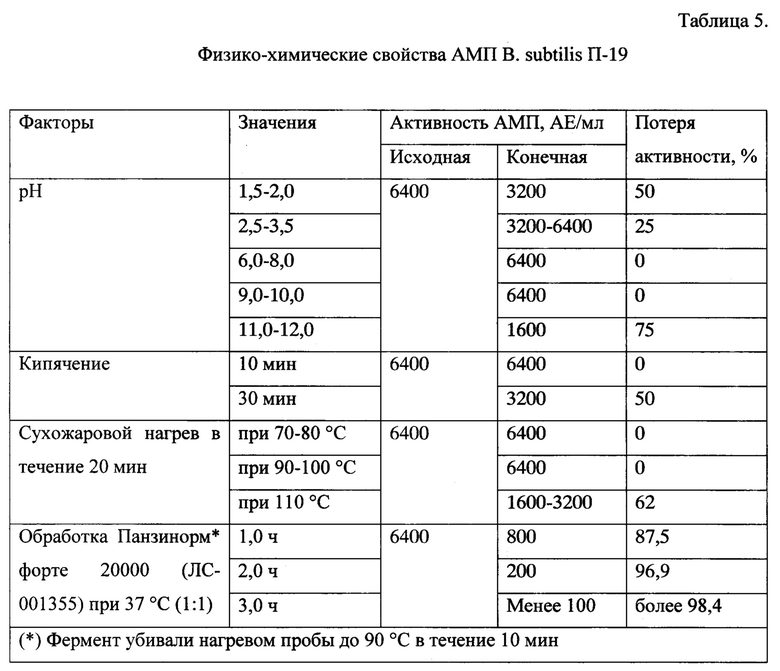
Результаты тестирования ЭКП П19 приведены в табл. 4 и 5. Из данных табл.4 следует, что пробы ЭКП активны в отношении всех штаммов исследованных бактерий родов Bacillus, Listeria, Micrococcus luteus и некоторых штаммов Staphylococcus aureus. В то же время АМП из В. subtilis П-19 на грамотрицательные микроорганизмы не действует.
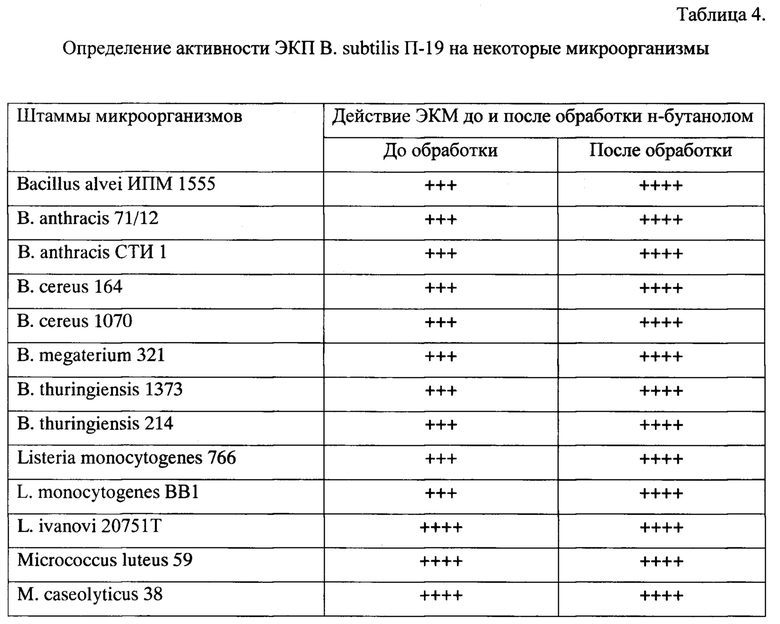

Из данных табл. 5 видно, что АМП В. subtilis П-19 выдерживает кипячение (10 мин), сухожаровой нагрев (+105°С, 20 мин), но разрушается в условиях имитирующих физиолого-биохимические параметры процесса пищеварения человека и животных [Дармов И.В. и др., 2011; Marques M.R., et al., 2011].
Пример 4. Для наработки АМП с целью использования в качестве антилистериозного средства культивирование штамма и выделение АМП в виде ЭКП проводят, как описано в примере 3. Всю последующую работу проводят с 10 мл ЭКМ, полученного с помощью этанольной обработки клеточной массы продуцента. При этом пробу ЭКМ для получения стойкой взвеси АМП дополнительно озвучивают на ультразвуковом дезинтеграторе Bandelin SonoPulse GM3400 и проводят определение титра активности против индикаторного штамма листерий, что важно для расчета количественного состава рецептурной формы препарата.
Для приготовления липосомальной суспензии используют метод гидратации липидной пленки. Для этого в ламинарном боксе ЛБ-2К готовят смесь липидов в стерильном стеклянном стаканчике на 50 мл, последовательно внося 2,5 мл раствора POPE (50 мг липида), 0,9 мл раствора холестерола (90 мг), 1 мл раствора лецитина (100 мг) и 0,6 мл раствора СтПЭГ400 (60 мг), получая 300 мг липидов в 5 мл легколетучего органического растворителя (смесь этанола и трихлорметана). В круглодонную колбу от ротационного испарителя выдавливают через бактериальный фильтр (0,2 мкм) липосомальную суспензию, тем самым обеспечивая ее холодную стерилизацию. Колбу подсоединяют к приемному патрубку ротационного испарителя, включают вращение, затем вакуум, избегая вскипания жидкости. При полном высыхании на стенках колбы образуется полупрозрачная пленка липидов. Для загрузки АМП в липосомы раствор АМП смешивают со стерильным ФСБ в соотношении, обеспечивающего активность в препарате не менее 1600 АЕ/мл. Полученные 15-25 мл раствора переносят в круглодонную колбу с липидной пленкой и запускают качалку на скорости 150 об/мин при температуре +42°С, смывая липиды. Полное смывание липидов раствором АМП занимает от 1 до 2 часов. В процессе образуется грубая суспензия липидных везикул с включениями АМП (фиг. 7б). Грубую суспензию обрабатывают ультразвуком на установке Bandelin SonoPulse GM3400 в режиме 900 Вт 3×10 с, получая тонкую устойчивую дисперсию липосом с АМП. Включение АМП в липосомы контролируют с помощью спектрофотометра Shimadzu UV-1601 (Япония).
Перед лиофилизацией к липосомированному АМП добавляют равный объем полимерного стабилизатора-криопротектора в составе: 0,75…1,0% поливинилпирролидон молекулярной массой 25…500 кД в фосфатно-солевом буферном растворе и полученную смесь разливают по 1 мл в стеклянные флаконы емкостью 3 мл. Флаконы замораживают при (-50…-70°С не менее 5 ч и переносят в камеру лиофилизатора Virtis BT-4k (США). После перекрытия доступа воздуха в камеру сразу же включают вакуумный насос.Лиофилизацию проводят в течение 20 ч, включающую на завершающем этапе процесса досушивание в течение не менее 3 ч. Сброс вакуума проводят напуском аргона в камеру лиофилизатора. Высушенные флаконы закрывают резиновыми пробками и герметизируют обжиманием алюминиевыми колпачками при помощи кримпера (рис. 7а). Контроль активности лиофилизированного липосомального препарата проводят путем регидратации содержимого, и нанесением последовательных разведений препарата по 10 мкл на ГРМ-агар со свежезасеянным газоном индикаторного штамма (фиг. 7в). Титр активности препарата не должен быть менее 1600 АЕ/мл.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ Bacillus lentus - ПРОДУЦЕНТ БАКТЕРИОЦИНОПОДОБНОЙ СУБСТАНЦИИ АНТИМИКРОБНОГО ДЕЙСТВИЯ И СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОЦИНОПОДОБНОЙ СУБСТАНЦИИ | 2013 |
|
RU2530552C1 |
| ПЕПТИД LanA1, ВЫДЕЛЕННЫЙ ИЗ БАКТЕРИИ Bacillus licheniformis VK21, ОБЛАДАЮЩИЙ АНТИМИКРОБНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2408732C1 |
| ПЕПТИДЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ АКТИВНОСТЬ | 2005 |
|
RU2302425C2 |
| ПЕПТИД НИКОМИЦИН ИЗ МОРСКОГО КОЛЬЧАТОГО ЧЕРВЯ NICOMACHE MINOR, ОБЛАДАЮЩИЙ АНТИМИКРОБНЫМ И ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ. | 2019 |
|
RU2721273C1 |
| ПЕПТИД LanA2, ВЫДЕЛЕННЫЙ ИЗ БАКТЕРИИ BACILLUS LICHENIFORMIS VK21, ОБЛАДАЮЩИЙ АНТИМИКРОБНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2408604C1 |
| ПЛАЗМИДНЫЙ ВЕКТОР pE-Trx-Aur, ШТАММ ESCHERICHIA COLI ДЛЯ ЭКСПРЕССИИ АНТИМИКРОБНОГО ПЕПТИДА АУРЕЛИНА И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОГО ПЕПТИДА | 2009 |
|
RU2412999C1 |
| Способ получения фунгистатических липопептидов | 2023 |
|
RU2825156C1 |
| ШТАММ ENTERОCOCCUS MUNDTII, ПРОДУЦИРУЮЩИЙ СУБСТАНЦИЮ ПЕПТИДНОЙ ПРИРОДЫ С АНТИЛИСТЕРИОЗНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532227C1 |
| Способ получения антимикробного пептида цекропина Р1 из экстракта трансгенных растений каланхоэ перистого | 2016 |
|
RU2632116C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИМИКРОБНОГО ПЕПТИДА АРЕНИЦИНА | 2006 |
|
RU2316595C1 |

Группа изобретений относится к биотехнологии. Предложен штамм Bacillus subtilis П19, синтезирующий антимикробный пептид (АМП) с активностью на патогенные бактерии - Bacillus anthracis, B. cereus, Listeria monocytogenes и некоторые штаммы Staphylococcus aureus. Штамм, депонированный в «ГКПМ – Оболенск» под номером В-8711, и способ получения низкомолекулярного антимикробного пептида, предусматривающий культивирование штамма Bacillus subtilis П19 на питательной среде при 360°С в течение 20 ч, отбор культуральной жидкости, закисление культуральной жидкости концентрированной соляной кислотой до рН 2,5, отделение осадка центрифугированием с охлаждением, рессуспендирование осадка в воде в соотношении 1:10, восстановление рН до 7,0±0,2 0,25 М раствором едкого натра, обработка полученной клеточной взвеси смесью этанола и ацетонитрила (CH3CN) в соотношении объемов 1,0:0,9:0,1 путем перемешивания в течение 20 мин при комнатной температуре с дальнейшим центрифугированием с получением преципитата, полученный преципитат растворяют в воде с получением смеси пептидов с последующим выделением пептида молекулярной массой 3,4 кДа путем смешивания смеси пептидов с бутанолом в соотношении 1:0,25 с последующим сбором бутанольной фракции, упариванием в сушильном шкафу при температуре 70°С с последующим растворением полученного преципитата в воде. Группа изобретений позволяет повысить выход целевого продукта. 2 н.п. ф-лы, 7 ил., 5 табл., 4 пр.
1. Штамм Bacillus subtilis П19 - продуцент низкомолекулярного антимикробного пептида, обладающий активностью против патогенных микроорганизмов грамположительной природы, депонированный в «ГКПМ – Оболенск» под № В-8711.
2. Способ получения низкомолекулярного антимикробного пептида (АМП) из культуральной жидкости штамма Bacillus subtilis П19 по п.1 путем концентрирования на клетках продуцента с дальнейшим его сбором с клеточной поверхности, очисткой и стабилизацией, отличающийся тем, что способ осуществляется закислением культуральной жидкости 38 % соляной кислотой до рН 2,5 с последующим разделением смеси 30 мин на центрифуге 4000 об/мин с охлаждением , затем осадок клеточной массы ресуспендируют в воде 1:10, с последующим восстановлением у концентрированной взвеси нейтральных значений рН с помощью 0,25 М раствора едкого натра до 7±0,2, добавляют к клеточной взвеси 96° этанола (С2Н5ОН) и ацетонитрила (CH3CN) в соотношении объемов 1,0:0,9:0,1 и перемешивают в течение 20 мин при комнатной температуре с дальнейшим осаждением на центрифуге (4000 об/мин, 10 мин), супернатант водно-спиртового экстракта собирают и упаривают, а преципитат растворяют в 10-15 мл воды, смесь пептидов смешивают с бутанолом 1:0,25, с последующим сбором бутанольной фракции и упариванием в сушильном шкафу при температуре 70°С, полученный преципитат АМП, молекулярная масса которого составляет 3,4 кДа, растворяют в 3-5 мл воды и собирают во флакон.
| ЗИМИНА М.И., ПРОСЕКОВ А.Ю | |||
| и др | |||
| Определение оптимальных условий культивирования для синтеза бактериоцинов штаммами Bacillus endopheticus и Bacillus licheniformis и изучение их стабильности | |||
| Техника и технология пищевых производств, 2016, Т | |||
| Механический грохот | 1922 |
|
SU41A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| ШТАММ ENTEROCOCCUS FAECIUM LVP1073, ПРОДУЦЕНТ БАКТЕРИОЦИНА ПРОТИВ БАКТЕРИАЛЬНЫХ ПАТОГЕНОВ, БАКТЕРИОЦИН E1073 ПРОТИВ БАКТЕРИАЛЬНЫХ ПАТОГЕНОВ, ШТАММ LACTOBACILLUS PLANTARUM 1 LVP7 - ИНДУКТОР СИНТЕЗА БАКТЕРИОЦИНА E1073, СИГНАЛЬНЫЙ ПЕПТИД СП1073 - РЕГУЛЯТОР СИНТЕЗА БАКТЕРИОЦИНА E1073, СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИОЦИНА E1073 | 2009 |
|
RU2409661C2 |
| СПОСОБ ПРОИЗВОДСТВА ФЕРМЕНТИРОВАННОГО ПИЩЕВОГО ПРОДУКТА, ШТАММ PEDIOCOCCUS ACIDILACTICI DSM 10313 - ПРОДУЦЕНТ БАКТЕРИОЦИНА, ЕГО ПРИМЕНЕНИЕ И СОДЕРЖАЩИЙ ЕГО ПИЩЕВОЙ ПРОДУКТ | 2005 |
|
RU2336705C2 |
| БИСЕНОВА Г.Н | |||
| и др | |||
| Изучение | |||
Авторы
Даты
2021-10-26—Публикация
2020-10-19—Подача