Область техники
Настоящее изобретение относится к способу амплификации нуклеиновой кислоты и устройству для осуществления такого способа.
Предпосылки изобретения
Полимеразная цепная реакция (ПЦР) была первым, широко используемым in vitro способом амплификации ДНК. Хотя данная методика имеет чрезвычайно широкие возможности, для осуществления амплификации требуется применение термоциклического устройства, чтобы подвергать реакционную смесь периодическим изменениям температуры. Соответственно ПЦР не особенно подходит для применения вне лабораторных условий, например, в рамках устройства для диагностики «у постели больного» (ʺPoCʺ).
Отчасти, чтобы преодолеть этот недостаток, были изобретены многочисленные различные методики изотермической амплификации, в которых исключена необходимость термоциклирования. Такие методики включают, например: технологию опосредованной сигналом амплификации РНК (ʺSMARTʺ; WO 99/037805); амплификацию, основанную на последовательности нуклеиновых кислот (ʺNASBAʺ, Compton 1991 Nature 350, 91-92); амплификацию по типу катящегося кольца (ʺRCAʺ, например, см. Lizardi et al., 1998 Nature Genetics 19, 225-232); петлевую изотермическую амплификацию (ʺLAMPʺ, см. Notomi et al., 2000 Nucl. Acids Res. 28, (12) e63); рекомбиназную полимеразную амплификацию (ʺRPAʺ, см. Piepenberg et al., 2006 PLoS Biology 4 (7) e204); амплификацию с замещением нитей (ʺSDAʺ); геликаза-зависимую амплификацию (ʺHDAʺ, Vincent et al., 2004 EMBO Rep. 5, 795-800): транскрипционно-опосредованную амплификацию (ʺTMAʺ), однопраймерную изотермическую амплификацию (ʺSPIAʺ, см. Kurn et al., 2005 Clinical Chemistry 51, 1973-81); самоподдерживающуюся репликацию последовательностей (ʺ3SRʺ) и реакцию амплификации с использованием фермента никующей эндонуклеазы (ʺNEARʺ).
SDA представляет собой методику (раскрытую Walker et al., 1992 Nucl. Acids Res. 20, 1691-1696), которая предусматривает применение пары коротких ʺбамперныхʺ праймеров, расположенных в направлении против хода транскрипции от пары праймеров, содержащих участок, комплементарный мишени, и сайт распознавания и разрезания для эндонуклеазы в 5'-направлении от участка, комплементарного мишени. ʺБамперныеʺ праймеры помогают инициировать реакцию SDA за счет образования комплементарной однонитевой мишени для амплификации с использованием праймеров. Праймеры гибридизируются с соответствующими комплементарными однонитевыми молекулами-мишенями. 3'-конец нитей-мишеней элонгируется с применением реакционной смеси, включающей ДНК-полимеразу и по меньшей мере один модифицированный нуклеозидтрифосфат, с применением праймера в качестве матрицы (и, аналогично, 3'-концы праймеров элонгируются с применением мишени в качестве матрицы).
Элонгация нитей-мишеней приводит к образованию двухнитевого сайта распознавания для эндонуклеазы. Однако, поскольку мишень элонгируется с применением модифицированного трифосфата, то эндонуклеаза не расщепляет обе нити, а создает однонитевой разрыв в праймере. 3'-концы в местах разрывов затем элонгируются с помощью ДНК-полимеразы (как правило, фрагмента Кленова ДНК-полимеразы I, который не обладает экзонуклеазной активностью). По мере того, как содержащие разрыв праймеры элонгируются, они вытесняют изначально образованный продукт элонгации. Вытесненный продукт затем может свободно гибридизироваться с противоположным праймером, поскольку он фактически повторяет последовательность мишени для противоположного праймера. Вследствие этого достигается экспоненциальная амплификация обеих нитей последовательности-мишени.
Стадия амплификации процесса SDA является фактически изотермической - как правило, осуществляется при 37°C - оптимальной температуре для эндонуклеазы и полимеразы. Однако перед наступлением стадии амплификации необходимо, чтобы двухнитевая мишень полностью диссоциировала на составляющие ее одиночные нити, чтобы обеспечить возможность гибридизации пары праймеров со своими комплементарными нитями-мишенями.
Такая диссоциация или ʺплавлениеʺ в норме выполняется за счет нагревания двухнитевой мишени до высокой температуры - обычно приблизительно 90°C - чтобы разрушить водородные связи между двумя нитями мишени. Затем реакционную смесь охлаждают, чтобы обеспечить возможность добавления ферментов, которые необходимы для реакции амплификации. Вследствие высокой температуры, применяемой для образования однонитевых мишеней, методика SDA не является идеально подходящей в рамках PoC.
В US 6191267 раскрыто клонирование и экспрессия никующей эндонуклеазы N.BstNBI и ее применение в SDA вместо рестрикционных эндонуклеаз и модифицированных трифосфатов.
Другой методикой амплификации, которая аналогична SDA, является реакция амплификации с использованием никующей эндонуклеазы (или ʺNEARʺ).
В случае 'NEAR' (например, как раскрыто в US2009/0017453 и EP 2181196) прямые и обратные праймеры (обозначаемые в US 2009/0017453 и EP 2181196 как ʺматрицыʺ) гибридизируются с соответствующими нитями двухнитевой мишени и элонгируются. Дополнительные копии прямого и обратного праймеров (присутствующие в избытке) гибридизируются с продуктом элонгации противоположного праймера и сами элонгируются, создавая ʺамплификационный дуплексʺ. Каждый амплификационный дуплекс, образованным таким образом, содержит сайт образования разрыва в направлении 5'-конца каждой нити, в котором образуется разрыв под действием никующей эндонуклеазы, что обеспечивает возможность синтеза дополнительных продуктов элонгации. Ранее синтезированные продукты элонгации тем временем могут гибридизироваться с дополнительными копиями комплементарных праймеров, вызывая элонгацию праймеров и, тем самым, создавая дополнительные копии ʺамплификационного дуплексаʺ. Вследствие этого может достигаться экспоненциальная амплификация.
NEAR отличается от SDA, в частности тем, что не требует ʺбамперныхʺ праймеров и начальной стадии термической диссоциации. Начальное событие гибридизации праймера/мишени, необходимое для запуска процесса амплификации, происходит в то время, когда мишень все еще является практически двухнитевой: считается, что начальная гибридизация праймера/мишени использует локализованную диссоциацию нитей мишени - явлением, известным как ʺдыханиеʺ (см., Alexandrov et al., 2012 Nucl. Acids Res., и обзор в Von Hippel et al., 2013 Biopolymers 99 (12), 923-954). Дыхание представляет собой локализованное и временное ослабление спаривания оснований между нитями ДНК. Температура плавления (Tm) начального гетеродуплекса праймер/мишень, как правило, намного ниже, чем температура реакционной смеси, поэтому обнаруживается тенденция диссоциация праймера, однако временная гибридизация длится достаточно долго, чтобы полимераза элонгировала праймер, что повышает Tm гетеродуплекса и стабилизирует его.
Стадия амплификации в NEAR осуществляется изотермически, при постоянной температуре. Действительно, общепринятым является осуществление как начальной гибридизации мишень/праймер, так и последующих раундов амплификации при одной и той же постоянной температуре, обычно в диапазоне 54-56°C.
Исключение необходимости в термоциклировании означает, что в рамках P°C изотермические методики потенциально являются более подходящими, чем ПЦР. Кроме того, можно достигать синтеза значительных количеств продукта амплификации, даже если он начинается с очень малого числа копий молекул-мишеней (например, всего лишь 10 двухнитевых молекул-мишеней).
В WO 2011/030145 (Enigma Diagnostics Limited) раскрыта ʺизотермическаяʺ реакция амплификации нуклеиновой кислоты в условиях колебания температуры, при которых реакция изначально осуществляется при заранее определенной температуре, допускается отклонение температуры вверх или вниз от заранее определенной температуры, и затем температуру заставляют вернуться к заранее определенной температуре по меньшей мере один раз во время реакции амплификации. Чаще допускается ʺколебаниеʺ температуры на незначительную величину (приблизительно 5°C) вверх и вниз от заранее определенной температуры.
Настоящее изобретение направлено, среди прочего, на улучшенную методику амплификации нуклеиновой кислоты, характеризующуюся одним или несколькими преимуществами над существующими методиками, которые включают, например, снижение времени реакции, и/или повышение продуктивности, и/или снижение образования неспецифических продуктов амплификации.
Краткое описание изобретения
В первом аспекте настоящего изобретения предусмотрен способ осуществления неизотермической реакции амплификации нуклеиновой кислоты, причем способ предусматривает стадии:
(a) смешивания последовательности-мишени с одним или несколькими комплементарными однонитевыми праймерами в условиях, которые способствуют событию гибридизации, при котором праймеры гибридизируются с мишенью, при этом событие гибридизации напрямую или опосредованно приводит к образованию дуплексной структуры, содержащей два сайта образования разрыва, расположенных на противоположных концах дуплекса или возле них; и осуществления процесса амплификации за счет;
(b) создания разрыва в каждом из указанных сайтов образования разрыва в нитях дуплекса;
(c) применения полимеразы для элонгации содержащих разрыв нитей таким образом, чтобы образовывалась вновь синтезированная нуклеиновая кислота, при этом элонгация с помощью полимеразы восстанавливает указанные сайты образования разрыва;
(d) повторения, при необходимости, стадий (b) и (c) таким образом, чтобы привести к получению множественных копий вновь синтезированной нуклеиновой кислоты;
при этом он отличается тем, что температура, при которой осуществляют способ, является неизотермической, и ее подвергают снижению на по меньшей мере 2°C, предпочтительно на по меньшей мере 5°C, во время стадий (b) - (d) процесса амплификации.
Во втором аспекте настоящего изобретения предусмотрено устройство для осуществления способа по первому аспекту настоящего изобретения, при этом устройство содержит средства регуляции температуры и программируемые средства контроля, причем программируемые средства контроля программируют таким образом, чтобы управлять средствами регуляции температуры для осуществления снижения температуры на по меньшей мере 2°C, предпочтительно на по меньшей мере 5°C, во время процесса амплификации реакционной смеси, применяемой для осуществления способа по первому аспекту.
Процесс амплификации из способа по настоящему изобретению можно применять в общеизвестных и стандартных методиках амплификации, в том числе SDA и NEAR.
Таким образом, например, процесс амплификации может быть основан на процессе амплификации, используемом в амплификации с замещением нитей, или основан на процессе, применяемом в NEAR или фактически любом другом процессе амплификации нуклеиновой кислоты, который обусловлен созданием однонитевого разрыва и последующей элонгацией, начиная от 3'-конца содержащей разрыв нити. Соответственно идеи из предшествующего уровня техники, связанные со стадиями амплификации SDA или NEAR, в целом будут равным образом применимы к процессу амплификации из способа по настоящему изобретению (отличному от идей из предшествующего уровня техники, связанных с поддержанием постоянной температуры во время амплификации).
Предпочтительно стадия (a) предусматривает смешивание образца, содержащего двухнитевую мишень, с двумя однонитевыми праймерами, причем один из указанных праймеров является комплементарным первой нити мишени, а второй из указанных праймеров является комплементарным второй нити мишени, вследствие чего два праймера гибридизируются с мишенью, а свободные 3'-концы указанных праймеров обращены друг к другу.
Для удобства два праймера могут быть описаны как 'прямой' и 'обратный' праймеры.
Желательно, как прямой, так и обратный праймеры будут содержать последовательность сайт распознавания для никующей эндонуклеазы. Как правило, разрыв, создаваемый никующей эндонуклеазой, будет находиться в непосредственной близости от сайта распознавания для никующей эндонуклеазы и, как правило, в направлении 3' от него.
В предпочтительном варианте осуществления прямой праймер будет содержать на своем 3'-конце или возле него участок, который является комплементарным 3'-концу антисмысловой нити мишени и может гибридизироваться с ним, в то время как обратный праймер содержит на своем 3'-конце или возле него участок, который является комплементарным 3'-концу смысловой нити мишени или может гибридизироваться с ним.
Вследствие этого сайт распознавания для никующей эндонуклеазы вводится на противоположные концы последовательности-мишени, и амплификация последовательности-мишени (вместе с любой промежуточной последовательностью праймеров в направлении по ходу транскрипции от сайта разрыва) выполняется путем осуществления множественных циклов элонгации под действием полимеразы прямых и обратных праймеров таким образом, чтобы образовывался двухнитевой сайт разрыва, и за счет создания разрыва в сайтах разрыва под действием никующей эндонуклеазы обеспечивается возможность дальнейшей элонгации содержащих разрыв праймеров под действием полимеразы и т. д., фактически как раскрыто, например, в US 2009/0017453, содержание которой включено в данный документ посредством ссылки.
Подробное описание изобретения
Настоящее изобретение относится, среди прочего, к способу амплификации выбранной нуклеиновой кислоты-мишени.
Мишень может быть однонитевой, двухнитевой или представлять собой смесь из них обеих. Мишень может предусматривать РНК, ДНК или смесь из них обеих. В частности, мишень может включать один или несколько модифицированных нуклеозидтрифосфатов (т. е. нуклеозидтрифосфат в норме не находящийся во встречающихся в природе нуклеиновых кислотах), хотя это не является обязательным и в действительности не является предпочтительным.
Мишень может быть выбрана из следующего неисчерпывающего перечня: геномная нуклеиновая кислота (этот термин охватывает геномную нуклеиновую кислоту любого животного, растения, гриба, бактерии или вируса), плазмидная ДНК, митохондриальная ДНК, кДНК, мРНК, рРНК, тРНК или синтетический олигонуклеотид или другая молекула нуклеиновой кислоты.
В частности, способ может дополнительно предусматривать начальную стадию обратной транскрипции. Например, РНК (например, вирусную геномную РНК, или клеточную мРНК, или РНК из какого-то другого источника) можно применять для синтеза ДНК или кДНК с применением обратной транскриптазы с помощью способов, хорошо известных специалистам в данной области. Затем ДНК можно применять в качестве последовательности-мишени в способе по настоящему изобретению. Исходная РНК, как правило, будет разрушаться под действием рибонуклеазной активности обратной транскриптазы, однако, после того, как обратная транскрипция была завершена, при необходимости можно добавлять дополнительную РНКазу H. Молекулы РНК часто присутствуют в образцах при большем числе копий, чем соответствующие (например, геномные) последовательности ДНК, поэтому для эффективного повышения числа копий последовательности ДНК может быть удобно получать ДНК-транскрипты из молекулы РНК.
ʺПоследовательность-мишеньʺ представляет собой последовательность из оснований в нуклеиновой кислоте-мишени, и может обозначать смысловую и/или антисмысловую нить двухнитевой мишени, и, если из контекста явно не следует иное, также охватывает последовательность из таких же оснований после воспроизведения или репликации в амплифицированных копиях, продуктах элонгации или продуктах амплификации начальной нуклеиновой кислоты-мишени.
Последовательность-мишень может присутствовать в образце любого типа, например, биологическом образце или образе среды (воде, воздухе и т. д.). Биологический образец может представлять собой, например, образец продукта питания или клинический образец. Клинические образцы могут включать следующее: мочу, слюну, кровь, сыворотку крови, плазму крови, слизь, мокроту, слезную жидкость или кал.
Образец может подвергаться или может не подвергаться обработке перед приведением в контакт с праймерами. Такая обработка может включать одно или несколько из фильтрации, концентрирования, частичной очистки, ультразвуковой обработки, лизиса и т. п. Такие процессы хорошо известны специалистам в данной области.
Способ по настоящему изобретению предусматривает применение сайта разрыва и средств для создания разрыва в сайте разрыва. ʺРазрывʺ представляет собой расщепление фосфодиэфирного остова только одной нити у полностью или по меньшей мере частично двухнитевой молекулы нуклеиновой кислоты. Сайт разрыва представляет собой место в молекуле, где выполняется разрыв.
В предпочтительных вариантах осуществления ʺсайт распознавания для никующей эндонуклеазыʺ будет присутствовать в сайте разрыва, в его пределах или возле него. (В данном контексте ʺвозлеʺ означает, что самое близкое основание сайта распознавания для никующей эндонуклеазы находится в пределах 10 оснований от сайта разрыва, предпочтительно в пределах 5 оснований от сайта разрыва).
Сайт распознавания для никующей эндонуклеазы может содержать по меньшей мере одну нить сайта распознавания для рестрикционной нуклеазы, а сайт разрыва может содержать по меньшей мере одну нить последовательности оснований нуклеиновой кислоты, которая, если она присутствует в виде двухнитевой молекулы, разрезается рестрикционной эндонуклеазой. Как правило, рестрикционная эндонуклеаза будет разрезать обе нити двухнитевой молекулы нуклеиновой кислоты. В настоящем изобретении двухнитевой разрыв может быть исключен за счет включения одного или нескольких модифицированных оснований в сайт разрыва или возле него, при этом модифицированные основания делают нить нуклеиновой кислоты невосприимчивой к расщеплению под действием рестрикционной эндонуклеазы. Вследствие этого рестрикционную эндонуклеазу, которая обычно разрезает обе нити двухнитевой молекулы нуклеиновой кислоты, можно применять для введения однонитевого разрыва в двухнитевую молекулу. Модифицированные основания и тому подобное, что подходит для достижения этого, хорошо известны специалистам в данной области, и они включают, например, все модифицированные по альфа-фосфату нуклеозидтрифосфаты и бор-модифицированные по альфа-фосфату нуклеозидтрифосфаты, в частности, 2'-дезоксиаденозин-5'-O-(тиотрифосфат), 5-метилдезоксицитидин-5'-трифосфат, 2'-дезоксиуридин-5'-трифосфат, 7-деаза-2'-дезоксигуанозин-5'-трифосфат, 2'-дезоксигуанозин-5'-O-(1-боранотрифосфат) и другие. Трифосфаты, включающие модифицированное основание, могут присутствовать в реакционной смеси, применяемой для осуществления процесса амплификации, вследствие чего модифицированные основания включаются в соответствующие положения во время последующих циклов амплификации для предотвращения образования сайта, расщепляемого эндонуклеазой.
Однако в предпочтительном варианте осуществления разрыв выполняется в сайте разрыва с помощью никующей эндонуклеазы. Они представляют собой ферменты, которые при обычных обстоятельствах создают только однонитевой разрыв в двухнитевой молекуле нуклеиновой кислоты. У никующей эндонуклеазы имеется сайт распознавания для никующей эндонуклеазы, и сайт разрыва может находиться в сайте распознавания для никующей эндонуклеазы или может находиться в направлении либо 5', либо 3' от сайта распознавания. Многие никующие эндонуклеазы известны специалистам в данной области и коммерчески доступны. Неисчерпывающий перечень примеров никующих эндонуклеаз включает Nb.Bsml, Nb.Bts, Nt.Alwl, Nt.BbvC, Nt.BstNBI и Nt.Bpu101. Последний фермент коммерчески доступен от ThermoFisher Scientific; другие доступны, например, от New England Biolabs.
В предпочтительных вариантах осуществления никующую эндонуклеазу вводят в реакционную смесь в начале осуществления способа (например, не позднее одной минуты после приведения образца в контакт с праймерами и ДНК-полимеразой). Однако в некоторых случаях желательным может быть включение никующей эндонуклеазы в реакционную смесь с более длительной отсрочкой (например, чтобы обеспечить возможность снижения температуры ближе к оптимальной температуре для никующей эндонуклеазы).
Способ по настоящему изобретению предусматривает применение ДНК-полимеразы. Предпочтительно способ по настоящему изобретению предусматривает применение по меньшей мере одной термофильной ДНК-полимеразы (т. е. оптимальная температура для которой составляет свыше 60°C). Предпочтительно ДНК-полимераза представляет собой полимеразу, замещающую нить. Предпочтительно ДНК-полимераза характеризуется отсутствием экзонуклеазной активности. Предпочтительно ДНК-полимераза представляет собой полимеразу, замещающую нить, с отсутствием экзонуклеазной активности и также предпочтительно термофильную.
Примеры предпочтительных ДНК-полимераз включают полимеразу Bst, ДНК-полимеразу Vent®, полимеразу 9°N, полимеразу Manta 1.0 (Qiagen), полимеразу BstX (Qiagen) и большой фрагмент ДНК-полимеразы Bsm (ThermoFisher Scientific).
В некоторых вариантах осуществления способ по настоящему изобретению может для удобства предусматривать стадию предамплификации или обогащения. Это стадия, на которой последовательность-мишень приводят в контакт с прямыми и обратными праймерами и ДНК-полимеразой, но не с никующей эндонуклеазой. Она продолжается, как правило, приблизительно 2-5 минут и приводит к начальной (линейной) амплификации последовательности-мишени приблизительно в 1000 раз, что может быть особенно пригодным, если последовательность-мишень присутствует в образце при низком числе копий.
В некоторых вариантах осуществления стадию предамплификации или обогащения осуществляют с применением мезофильной ДНК-полимеразы, такой как фрагмент Кленова ДНК-полимеразы без экзонуклеазной активности или психрофильной ДНК-полимеразы без экзонуклеазной активности из Cenarchaeum symbiosum, при температуре ниже 50°C, а затем смесь нагревают выше 50°C, чтобы денатурировать или инактивировать термолабильную ДНК-полимеразу, и затем термофильную ДНК-полимеразу добавляют для последующей амплификации.
Как правило, способ по настоящему изобретению предусматривает стадию выявления, на которой выявляют и необязательно количественно оценивают один или несколько прямых или непрямых продуктов процесса амплификации, что указывает на присутствие и/или количество последовательности-мишени в образце. Известно огромное множество подходящих методик для выявления и/или количественной оценки, включая гель-электрофорез, масс-спектрометрию, иммунохроматографический анализ, включение меченых нуклеотидов, интеркалирующие красители, молекулярные маяки и другие зонды, в частности, специфично гибридизирующиеся олигонуклеотиды или другие молекулы, содержащие нуклеиновые кислоты.
Продукт или продукты, которые выявляют на стадии выявления, могут обозначаться в данном документе как ʺвыявляемая мишеньʺ. Применительно к стадии выявления 'мишень' не обязательно является одинаковой с 'мишенью' в процессе амплификации, и, в действительности, эти две молекулы обычно будут отличаться по меньшей мере в некоторой степени, хотя они могут иметь некоторую общую последовательность (как правило, 10-20 оснований), когда мишень выявления содержит молекулу нуклеиновой кислоты или олигонуклеотид.
В способах выявления нуклеиновых кислот может использоваться применение красителей, которые обеспечивают возможность специфического выявления двухнитевой ДНК. Хорошо известны интеркалирующие красители, которые проявляют усиленную флуоресценцию после связывания с ДНК или РНК. Красители могут представлять собой, например, ДНК- или РНК-интеркалирующие флуорофоры и, среди прочего, могут включать следующие: акридиновый оранжевый, этидия бромид, Pico Green, пропидия йодид, SYBR I, SYBR II, SYBR Gold, TOTO-3 (димер тиазолового оранжевого), Oli Green и YOYO (димер оксазолового желтого).
В способах выявления нуклеиновых кислот можно также использовать применение меченых нуклеотидов, вводимых прямо в последовательность-мишень для выявления или в зонды, содержащие последовательности, комплементарные или практически комплементарные мишени для выявления, представляющей интерес. Подходящие метки могут быть радиоактивными и/или флуоресцентными, и их можно анализировать с помощью любого из способов, традиционно используемых в данной области. Меченые нуклеотиды, которые могут быть выявлены, во всех остальных отношениях функционируют как нативные нуклеотиды (например, распознаются природными ферментами и могут выступать в качестве субстратов для них), следует отличать от модифицированных нуклеотидов, которые не функционируют как нативные нуклеотиды.
Присутствие и/или количество нуклеиновых кислот-мишеней и последовательностей нуклеиновых кислот-мишеней можно выявлять и контролировать с помощью молекулярных маяков. Молекулярные маяки представляют собой олигонуклеотиды в форме шпильки, содержащие флуорофор на одном конце и гасящий краситель (ʺгасительʺ) на противоположном конце. Петля шпильки содержит последовательность зонда, которая комплементарна или практически комплементарна последовательности-мишени для выявления, а ствол образуется за счет гибридизации самокомплементарных или в значительной степени самокомплементарных последовательностей, расположенных по обе стороны от последовательности зонда.
Флуорофор и гаситель связаны на противоположных сторонах маяка. При условиях, которые не допускают гибридизации молекулярного маяка с его мишенью, или в случае, когда молекулярный маяк находится в свободном состоянии в растворе, флуорофор и гаситель расположены вблизи друг другу, что предотвращает флуоресценцию. Когда молекулярный маяк сталкивается с молекулой-мишенью для выявления, происходит гибридизация; при этом петлевая структура переходит в стабильную, более жесткую конформацию, что вызывает разделение флуорофора и гасителя, обеспечивая возможность возникновения флуоресценции (Tyagi et al. 1996, Nature Biotechnology 14: 303-308). Вследствие специфичности зонда появление флуоресценции происходит практически исключительно вследствие присутствия предусмотренного амплифицированного продукта/мишени для выявления.
Молекулярные маяки являются высокоспецифичными и позволяют различать последовательности нуклеиновой кислоты, отличающиеся одним основанием (например, однонуклеотидные полиморфизмы). Молекулярные маяки можно синтезировать с различными окрашенными флуорофорами и различными последовательности, комплементарными мишени для выявления, что обеспечивает условия для одновременного выявления и/или количественной оценки нескольких различных мишеней для выявления в одной и той же реакции, обеспечивая возможность ʺмультиплексированияʺ одного анализа P°C для выявления множества различных патогенов или биохимических маркеров. В случае количественной оценки процессов амплификации молекулярные маяки могут специфически связываться с амплифицированной мишенью для выявления, и поскольку негибридизированные молекулярные маяки не флуоресцируют, отсутствует необходимость в выделении гибридов зонд-мишень для количественной оценки количества амплифицированного продукта. Полученный сигнал пропорционален количеству амплифицированного продукта. Это можно выполнять в реальном времени. Как и в случае других форматов в реальном времени, специфические условия реакции должны быть оптимизированы для каждого набора праймер/зонд, чтобы гарантировать точность и прецизионность.
Образование или присутствие нуклеиновых кислот-мишеней и последовательностей нуклеиновых кислот-мишеней для выявления можно также выявлять и отслеживать с помощью резонансного переноса энергии флуоресценции (FRET). FRET представляет собой механизм переноса энергии между двумя флуорофорами: молекулой-донором и молекулой-акцептором. Вкратце, флуорофорная молекула-донор возбуждается при специфической длине волны возбуждения. Следующее за этим излучение от молекулы-донора, когда она возвращается к своему исходному состоянию, может переносить энергию возбуждения на молекулу-акцептор (посредством диполь-дипольного взаимодействия дальнего действия). FRET является применимым инструментом для количественной оценки молекулярной динамики, например, при взаимодействиях ДНК-ДНК, как наблюдается в случае молекулярных маяков. Для отслеживания образования специфического продукта зонд можно метить молекулой-донором на одном конце и молекулой-акцептором на другом. Гибридизация зонда-мишени для выявления изменяет расстояние или ориентацию донора и акцептора и наблюдается изменение свойств FRET. (Joseph R. Lakowicz. ʺPrinciples of Fluorescent Spectroscopyʺ, Plenum Publishing Corporation, 2nd edition (July 1, 1999)).
Образование или присутствие нуклеиновых кислот-мишеней для выявления можно также выявлять или отслеживать с помощью устройств для иммунохроматографического анализа. Устройства для иммунохроматографического анализа хорошо известны. Эти устройства обычно включают твердофазный проницаемый для жидкости проточный канал, через который жидкость течет под действием капиллярных сил. Примеры включают без ограничения анализы с тест-полосками и планшеты для тонкослойной хроматографии с различными соответствующими покрытиями. В проточном канале или на нем иммобилизованы различные связывающие реагенты для образца, связывающие партнеры или конъюгаты, включающие связывающих партнеров для образца, и системы для выработки сигнала. Выявление аналитов может достигаться несколькими различными путями, включая ферментативное выявление, выявление с помощью наночастиц, колориметрическое выявление и флуоресцентное выявление. Ферментативное выявление может включать меченые ферментом зонды, которые гибридизируются с комплементарными или практически комплементарными нуклеиновыми кислотами-мишенями для выявления на поверхности устройства для иммунохроматографического анализа. Образующийся комплекс можно обрабатывать соответствующими маркерами для возникновения доступного для считывания сигнала. Выявление с помощью наночастиц включает технологию на основе гранул, в которой можно применять наночастицы из коллоидного золота, латекса и парамагнитные наночастицы. В одном примере гранулы могут быть конъюгированы с антителом к биотину. Последовательности-мишени можно биотинилировать напрямую, или последовательности-мишени могут гибридизироваться со биотинилированными зондами, специфическими в отношении последовательности. Золото и латекс приводят к образованию колориметрических сигналов, заметных невооруженным глазом, а парамагнитные частицы приводят к образованию невидимого сигнала при возбуждении в магнитном поле, и они могут быть расшифрованы специализированным ридером.
Также известны способы выявления с помощью иммунохроматографических анализов на основе флуоресценции, например, способы с олигонуклеотидными зондами с двойной меткой флуоресцеином и биотином, или применение квантовых точек.
Нуклеиновые кислоты также могут захватываться на устройствах для иммунохроматографического анализа. Средства захвата могут предусматривать антителозависимые и антителонезависимые способы. При антителонезависимом захвате обычно применяются нековалентные взаимодействия между двумя связывающими партнерами, например, высокая аффинность и необратимое связывание между биотинилированным зондом и молекулой захвата на основе стрептавидина. Зонды для захвата можно иммобилизовать прямо на мембранах для иммунохроматографического анализа.
Весь способ по настоящему изобретению или по меньшей мере часть способа, представляющая собой процесс амплификации, можно осуществлять в реакционном сосуде (таком как стандартная лабораторная пластиковая пробирка для реактивов, например, от Eppendorf®) или можно осуществлять в твердой подложке и/или на ней. Твердая подложка может быть пористой или непористой. В конкретном варианте осуществления твердая подложка может предусматривать пористый мембранный материал (такой как нитроцеллюлоза или подобное). Более конкретно, твердая подложка может представлять собой или составлять часть пористого устройства для иммунохроматографического анализа, описываемого выше. Альтернативно твердая подложка может представлять собой или составлять часть микрофлюидного анализа, в котором для транспорта жидкости вдоль аналитического устройства применяются одна или несколько твердых капиллярных трубок, полученных с помощью тонкого бура.
В предпочтительном варианте осуществления весь способ по настоящему изобретению или по меньшей мере его часть можно выполнять с помощью устройства для анализа «у постели больного» (PoC). Как правило, устройство P°C имеет следующие характеристики: является дешевым для изготовления, утилизируется после однократного применения, обычно обеспечено всем необходимым, при этом для осуществления или расшифровки анализа не требуется никакое другое устройство или оборудование и, желательно, для применения не требуется клинических знаний или обучения.
Примеры праймеров, подходящих для применения в настоящем изобретении, раскрыты в данном документе. Другие примеры, которые могут быть пригодными для применения в способе по настоящему изобретению, раскрыты, среди прочего, в US 2009/0017453 и EP 2181196, содержание обоих из которых включено в данный документ посредством ссылки. Специалист в данной области легко сможет сконструировать другие праймеры, подходящие для амплификации других последовательностей-мишеней без проведения дополнительных экспериментов.
Как объясняется в других разделах данного документа, праймеры для применения в настоящем изобретении предпочтительно будут содержать не только участок, комплементарный мишени, но также и сайт связывания никующей эндонуклеазы и сайт образования разрыва, а также стабилизирующий участок. Предпочтительные праймеры могут содержать самокомплементарную последовательность, которая может формировать структуру «петля на стебле» у праймерной молекулы.
Праймеры для применения в способе по настоящему изобретению могут содержать модифицированные нуклеотиды (т. е. нуклеотиды, не обнаруженные в молекулах нуклеиновых кислот, встречающихся в природе). Такие модифицированные нуклеотиды могут для удобства присутствовать в участке праймера, комплементарном мишени, и/или в любом другом месте праймера. Предпочтительные примеры модифицированных нуклеотидов представляют собой 2'-модифицированные нуклеотиды, в частности, 2'-O-метил-модифицированные нуклеотиды, хотя многие другие модифицированные нуклеотиды известны специалистам в данной области.
Температурный профиль
Хотя способ по настоящему изобретению и является изотермическим, для него не требуется термоциклирование. В результате этого в способе по настоящему изобретению не требуется применение относительно сложного устройства для термоциклирования, применяемого в ПЦР, и соответственно он в большей степени пригоден для применения в рамках PoC.
ʺТермоциклированиеʺ или циклическое изменение температуры, в частности, означает, что температура реакционной смеси поддерживается при определенной температуре (допустим, t1) в течение определенного промежутка времени (как правило, по меньшей мере 30 секунд). Затем температуру корректируют (либо поднимают вверх, либо опускают вниз) перед возвращением к ранее поддерживаемой температуре.
Как правило, для реакций неизотермической амплификации нуклеиновой кислоты, таких как ПЦР, требуется осуществления множественных стадий нагревания на цикл (т. е. по меньшей мере две или более) и множественных циклов нагревания на реакцию.
Снижение температуры в способе по настоящему изобретению является запланированным и контролируемым в том смысле, что величина снижения температуры больше предварительно определенного минимального уровня и меньше предварительно определенного максимального уровня. Кроме того, скорость снижения температуры предпочтительно находится в предварительно определенном диапазоне.
Начальная стадия (a) в способе по настоящему изобретению включает приведение последовательности-мишени в контакт с праймером, имеющим по меньшей мере участок, который является комплементарным последовательности-мишени, в условиях, которые обеспечивают гибридизацию праймера с мишенью, по меньшей мере временно. Это может быть описано как фаза ʺинициацииʺ.
Данная стадия, как правило, выполняется при температуре в диапазоне 50-65°C, предпочтительно в диапазоне 52-62°C, более предпочтительно в диапазоне 54-62°C, наиболее предпочтительно в диапазоне 58-62°C. Реакционная смесь, содержащая мишень и праймер, может поддерживаться при данной температуре в течение подходящего периода времени. Оптимальная температура и оптимальный период времени, в течение которого реакционная смесь поддерживается при данной температуре, могут определяться специалистом в данном области, принимая во внимание преимущества настоящего изобретения, и на них могут влиять такие параметры, как длина последовательности-мишени, длина праймеров - и, в частности, длина участка праймера, который является комплементарным мишени, содержание G:C в гибриде мишень:праймер, pH и концентрации солей реакционной смеси. Типичное время поддержания начальной температуры может находиться в диапазоне от 5 секунд до 5 минут, предпочтительно от 10 секунд до 3 минут. Типичные условия для осуществления события начальной гибридизации на стадии (a) будут известны специалистам в данной области, и они описаны в прилагаемых примерах.
Температурный диапазон 58-62°C является предпочтительным для фазы инициации. Считается, что она является достаточно высокой для сведения к минимуму образования димеров праймеров (и, тем самым, снижения количества неспецифической амплификации) и повышения вероятности образования потенциальных ʺсайтов инициацииʺ в дуплексе-мишени, и в то же время достаточно низкой, чтобы обеспечить возможность гибридизации с мишенью по меньшей мере некоторые из праймерных молекул.
Последующее снижение температуры помогает стабилизировать гибридизацию сравнительно коротких праймеров и продуктов элонгации, а не гибридизацию праймеров с исходной молекулой-мишенью. Дополнительно предполагается, что дополнительное охлаждение реакционной смеси облегчает гибридизацию зонда для выявления с мишенью для детекции.
Во время процесса амплификации, предусмотренного на стадиях (b) -(d) способа, температуру реакционной смеси снижают. Это можно выполнять регулируемым образом, например, с помощью средств регуляции температуры, со снижением температуры реакционной смеси в соответствии с заранее определенным температурным профилем. Снижение температуры может начинаться немедленно после фазы инициации (стадия a). Предпочтительно объем реакционной смеси является небольшим, вследствие чего теплоемкость реакционной смеси (и реакционного сосуда или субстрата, в котором или на котором реакция осуществляется) снижена.
Для удобства объем реакционной смеси составляет меньше 100 мкл, предпочтительно меньше 50 мкл, более предпочтительно меньше 25 мкл и наиболее предпочтительно меньше 20 мкл. Вследствие этого температуру реакционной смеси можно точнее и быстрее регулировать с помощью средств регуляции температуры. В подходящих вариантах осуществления средства регуляции температуры могут быть очень простыми (например, вентилятор) или можно обходиться полностью без них, при этом достаточное охлаждение достигается главным образом или целиком за счет пассивных средств (например, за счет излучения тепла от реакционной смеси). Как правило, объем реакционной смеси может находиться в диапазоне 1-50 мкл, предпочтительно 1-20 мкл и более предпочтительно 1 10 мкл.
Объем реакционной смеси может составлять меньше 10 мкл. В частности, в способе по настоящему изобретению может использоваться подход по типу ʺцифровой ПЦРʺ (см., обзор Morley 2014 Biomolecular Detection and Quantification 1, 1-2), при котором образец разбавляют и разделяют на множество (обычно несколько сотен, несколько тысяч или даже миллион) аликвот, которые обрабатываются параллельно: некоторые из аликвот будут содержать последовательность-мишень, а некоторые - нет: если последовательность-мишень не присутствует, то сигнал не генерируется. Долю отрицательных аликвот можно применять для вычисления числа и/или концентрации последовательности-мишени в исходном образце. В таких вариантах осуществления объем реакционной смеси в каждой аликвоте может быть очень небольшим, однако, как правило, минимальный объем будет составлять 2500 нл, предпочтительно 50 мкл.
Температуру можно снижать в виде любого необходимого профиля. Например, температуру можно снижать в соответствии с практически линейным профилем (т. е. при фактически постоянной скорости снижения температуры) или можно снижать любым нелинейным способом, включая кривую или поэтапный способ, или в виде любой комбинации линейных и нелинейных профилей (например, один или несколько периодов постоянной скорости снижения температуры, при этом скорость может быть нулевой или относительно низкой, в чередовании с периодами относительно высоких скоростей снижения температуры).
Температурный профиль реакции в соответствии с настоящим изобретением является таким, что температуре реакции не позволяют вернуться к температуре, при которой осуществляется фаза ʺинициацииʺ. Таким образом, в способе по настоящему изобретению отсутствует колебание около заранее определенной температуры и отсутствует ʺвозвратʺ к предварительно определенной температуре, в отличие, например, от раскрытия WO 2011/030145.
Температура реакционной смеси в начале процесса амплификации, как правило, будет такой же, как на стадии (a), например, предпочтительно в диапазоне 54-62°C и наиболее предпочтительно 58-62°C. Во время процесса амплификации температура падает на по меньшей мере 2°C, предпочтительно на по меньшей мере 3, 4 или 5°C, более предпочтительно на по меньшей мере 8, 9 или 10°C и наиболее предпочтительно на по меньшей мере 13, 14 или 15°C, хотя будет понятно, что предпочтительная величина понижения температуры в абсолютных значениях может по меньшей мере частично зависеть от выбранной начальной температуры в начале процесса амплификации, при этом более низкая начальная температура (например, в диапазоне 45-55°C) может обуславливать меньшее падение температуры и/или меньшую скорость падения температуры. Как правило, максимальная величина снижения температуры во время процесса амплификации составляет приблизительно 20°C, хотя будет понятно, что максимальное снижение температуры может быть меньше (например, 16, 17, 18 или 19°C) или больше (например, 25 или 30°C) этого.
В предпочтительных вариантах осуществления величина снижения температуры реакционной смеси во время процесса амплификации может находиться в диапазоне 5-40°C, предпочтительно в диапазоне 8-35°C, более предпочтительно в диапазоне 8-30°C или даже 8-25°C, и наиболее предпочтительно в диапазоне 8-20°C. Типичная начальная температура реакционной смеси в начале процесса амплификации находится в диапазоне 50-62°C, предпочтительно 54-62°C, более предпочтительно в диапазоне 56-60°C и наиболее предпочтительно в диапазоне 58-60°C.
В предпочтительных вариантах осуществления снижение температуры во время процесса амплификации (стадии (b) -(d) способа по настоящему изобретению) включает снижение, охватывающее диапазон от 54 до 50°C, от 56 до 50 или от 58 до 50, более предпочтительно от 58 до 45, от 58 до 40 или даже от 60 до 40°C. Следует понимать, что снижение температуры во время процесса амплификации может быть большим, чем указанные диапазоны, определенные выше. Т. е. максимальная температура может превышать верхнюю температуру указанного диапазона и/или минимальная температура может быть ниже нижней температуры указанного диапазона.
Конечную температуру реакции амплификации предпочтительно выбирают для совместимости с выбранным способом выявления. Например, если способ выявления предусматривает применение ферментативной метки, то может быть желательно приспособить конечную температуру реакции амплификации таким образом, чтобы она была совместима с ферментом и, например, находилась в пределах+5°C от оптимальной температуры фермента. Альтернативно, если способ выявления предусматривает применение гибридизирующего зонда для выявления, такого как молекулярный маяк или т. п., будет предпочтительным приспособить конечную температуру реакции амплификации с возможность выбора таким образом, чтобы она была совместима с Tm дуплекса зонд для выявления/мишень для выявления.
Например, для удобства конечная температура может быть ниже Tm дуплекса зонд для выявления/мишень для выявления, предпочтительно ниже на по меньшей мере 2°C, чтобы облегчить гибридизацию зонда с мишенью для выявления.
Типичная средняя скорость снижения температуры во время процесса амплификации находится в диапазоне от -0,10 до -6,0°C мин-1, предпочтительно в диапазоне от -0,20 до -3,5°C мин-1, более предпочтительно в диапазоне от -0,30 до -3,5°C мин-1 и наиболее предпочтительно в диапазоне от -0,40 до -3,5°C мин-1. Как будет очевидно из вышеизложенного, фактическая скорость снижения температуры в любой момент во время процесса амплификации может отклоняться от предпочтительной средней скорости, в зависимости от природы градиента снижения температуры.
В некоторых вариантах осуществления градиент снижения температуры является практически линейным в течение по меньшей мере 3 минут, более предпочтительно в течение по меньшей мере 4 минут и наиболее предпочтительно в течение большей части периода процесса амплификации. Как правило, градиент снижения температуры является практически линейным в течение периода в диапазоне 3-12 минут, предпочтительно в диапазоне 4-10 минут, более предпочтительно в диапазоне 4-8 минут. Для целей настоящего изобретения ʺпрактически линейныйʺ означает, что для любого полинома второго порядка, описывающего градиент температуры, величина коэффициента X составляет менее 5% от значения коэффициента Y.
Для достижения необходимого снижения температуры во время процесса амплификации может предусматриваться большое число различных методик. Они могут включать одно или несколько из следующего: (a) прекращение подведения тепла к реакционной смеси и/или удаление реакционной смеси из нагретой и/или изолированной среды и оставление реакционной смеси для охлаждения фактически за счет пассивной потери тепла до температуры окружающей среды; (b) применение в отношении реакционной смеси активного охлаждения. Активное охлаждение может предусматривать воздействие на реакционную смесь охлажденной средой, например, помещение реакционной смеси в теплообменный (проводящий, излучающий или конвекционный) контакт с охлажденной средой, в частности жидкостью. Оно может предусматривать, например, приведение реакционной смеси в контакт с охлажденной водяной баней, применение вентилятора для продувания холодного воздуха или другого газа над реакционной смесью или через нее, приведение реакционной смеси в контакт с совместимым с реакционной смесью охладителем, который может представлять собой газ, жидкость или твердое вещество, или применение охладительного устройства типа Пельтье. Например, совместимый с реакционной смесью охладитель может представлять собой совместимый с реакционной смесью буфер в замороженной или охлажденной жидкой форме. Добавление холодного буфера может приводить к разбавлению реакционной смеси, поэтому, если внедряется данный подход, то может быть предпочтительным применение малых объемов (например, менее 1-2 мкл) охладителя при температуре намного ниже (т. е. более чем на 20°C ниже) температуры реакционной смеси.
Любые стадии с активным охлаждением можно применять во время процесса амплификации с перерывами таким образом, чтобы достичь необходимого уровня снижения температуры и/или необходимого профиля снижения температуры. В частности, активное охлаждение во время процесса амплификации можно осуществлять через два или более разделенных во времени интервала, и оно может необязательно сочетаться с пассивным охлаждением, одновременным или попеременным.
В целом, предпочтительным является достижение необходимой величины и скорости снижения температуры практически за счет исключительно пассивных средств, поскольку это упрощает способ и любое устройство или набор, требуемые для осуществления способа. Чтобы достичь необходимой величины и скорости охлаждения за счет практически исключительно пассивных средств, желательно, чтобы объем реакционной смеси был небольшим с целью снижения его теплоемкости, как отмечено ранее.
Предпочтительным признаком способа по настоящему изобретению является то, что в процессе амплификации можно использовать первую полимеразу, характеризующуюся оптимальной температурой, и вторую полимеразу, характеризующуюся оптимальной температурой, где оптимальная температура второй полимеразы ниже, чем оптимальная температура первой полимеразы. Соответственно первая полимера может быть особенно активной в начале процесса амплификации, поскольку температура реакционной смеси может составлять оптимальную температуру первой полимеразы или приближаться к ней.
Таким образом, например, первая полимераза предпочтительно может быть ʺтермофильнымʺ ферментом (т. е. характеризующимся оптимальной температурой выше 60°C).
В отличие от этого, вторая полимераза характеризуется более низкой оптимальной температурой, чем первая полимераза. По мере продолжения процесса амплификации температура реакционной смеси падает и приближается ближе к оптимальной температуре второй полимеразы. Таким образом, вторая полимераза становится все более активной, что по меньшей мере частично компенсирует скорость снижения реакции, причем такое снижение обусловлено (i) общим термодинамическим замедлением реакции вследствие более низкой температуры и тем, что (ii) температура реакционной смеси возможно падает ниже оптимальной температуры первой полимеразы, что приводит к сниженному катализу.
Предпочтительно оптимальная температура второй полимеразы находится в диапазоне 30-55°C, более предпочтительно в диапазоне 30-45°C.
В конкретном варианте осуществления вторая полимераза может представлять собой фрагмент Кленова ДНК-полимеразы I или полимеразу Bsu.
Можно допустить, что может применяться даже третья или последующая полимераза, предпочтительно с еще более низкой третьей оптимальной температурой.
Вторая полимераза предпочтительно находится в реакционной смеси с начала процесса амплификации, однако, при необходимости, вторую полимеразу можно добавлять с отсрочкой, обеспечивая возможность снижения температуры реакционной смеси от высокой начальной температуры. Это может быть предпочтительным, например, если вторая полимераза является особенно термолабильной и, по-видимому, практически денатурирует, когда присутствует при сравнительно высоких температурах, в норме используемых в начале процесса амплификации.
В порядке, полностью аналогичном вышеизложенному, в процессе амплификации можно использовать первый и второй никующие эндонуклеазы, с более высокой и более низкой оптимальными температурами соответственно. Первую и вторую никующие эндонуклеазы можно применять в сочетании с одной полимеразой или множественными полимеразами, в зависимости от ситуации.
Как указывалось выше, применение второй никующей эндонуклеазы с более низкой оптимальной температурой может по меньшей мере частично компенсировать сниженные скорости реакции, ожидаемые по мере падения температуры во время процесса амплификации.
Таким образом, в некоторых вариантах осуществления температура реакционной смеси в самом начале может быть ниже оптимальной температуры первой полимеразы и/или первой никующей эндонуклеазы или может быть снижена во время протекания процесса амплификации и будет стремиться достичь или может даже достичь оптимальной температуры второй полимеразы и/или второй никующей эндонуклеазы.
Для удобства в некоторых вариантах осуществления способ по настоящему изобретению может предусматривать стадию приведения реакционной смеси в контакт с деструктивным ферментом, которые разрушает нуклеиновую кислоту. Желательно, чтобы эта стадия не осуществлялась до тех пор, пока пользователь не получит необходимый результат реакции амплификации (например, выявление патогена). Следовательно, деструктивный фермент, как правило, добавляют к реакционной смеси после того, как процесс амплификации достиг необходимой конечной точки. Предпочтительно, деструктивный фермент является термолабильным, чтобы в случае его непреднамеренного введения в реакционную смесь или приведения в контакт с ней до того, как процесс амплификации достиг необходимой конечной точки, температура была достаточной, чтобы практически денатурировать или иным образом инактивировать фермент. Подходящие примеры включают урацил-ДНК-гликозилазу трески (ʺUDGʺ), доступную от ArcticZymes® и антарктическую термолабильную UDG (доступную от New England BioLabs). Эти ферменты быстро и необратимо инактивируются при воздействии температуры 55°C или 50°C соответственно, и термин ʺтермолабильныйʺ в отношении деструктивного фермента следует толковать соответствующим образом. Альтернативно можно применять термочувствительный деструктивный фермент (т. е. фермент, который по меньшей мере частично активен при температуре ниже 50°C, однако обратимо, практически неактивен при температуре выше 55°C).
Теперь настоящее изобретение будет дополнительно описано с помощью иллюстративных примеров и со ссылкой на следующие прилагаемые графические материалы.
Фигуры 1A-1C представляют собой схематические изображения типичного варианта осуществления праймера, применимого при осуществлении способа по настоящему изобретению.
Фигуры 2A и 2B представляют собой схематические изображения фазы инициации и экспоненциальной фазы амплификации нуклеиновой кислоты соответственно при реакции амплификации нуклеиновой кислоты, подходящей для осуществления способа по настоящему изобретению.
Фигуры 3-11 представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) и температуры (°C) в зависимости от времени (минуты).
Фигуры 12A-12C представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) в зависимости от времени для отдельных повторностей реакций амплификации.
Фигура 13 представляет собой диаграмму рассеивания, в которой сравнивается время, необходимое для достижения амплификации, начиная с 10 копий последовательности-мишени, в условиях ʺSTARʺ в соответствии с настоящим изобретением или при изотермических условиях.
Фигуры 14A и 14B представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) и температуры (°C) в зависимости от времени при применении условий изотермической амплификации (63 ˚C или 49°C соответственно);
Фигуры 15A, 15B и 15C представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) и температуры (°C) в зависимости от времени (минуты) для отдельных повторностей (10 копий или 100 копий; штрихпунктирные или сплошные линии соответственно) в случае реакций амплификации в соответствии с настоящим изобретением при различных температурных профилях.
Фигуры 16A и 16B представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) и температуры в зависимости от времени (минуты) в случае реакций амплификации в соответствии с настоящим изобретением при разных температурных профилях.
Фигуры 17A и 17B представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) и температуры (°C) в зависимости от времени (минуты) в случае реакций амплификации в соответствии с настоящим изобретением, осуществляемых с применением праймеров, содержащих 6 (фиг. 17A) или 7 (фиг. 17B) O-метилированных оснований.
Фигура 18 представляет собой график (с вычитанием фонового уровня) флуоресценции (условные единицы) в зависимости от времени (минуты) в случае реакций амплификации, осуществляемых в соответствии с настоящим изобретением, с применением ДНК-мишени, полученной с помощью обратной транскрипции 23S РНК Listeria monocytogenes.
Примеры
Пример 1. Протоколы для тестирования снижения температуры
Влияние снижения температуры на реакцию амплификации тестировали путем сравнения амплификаций с применением снижений температуры с течением времени и стандартных изотермический условий. Амплификация со снижением температуры называется в данном документе ʺSTARʺ (реакция амплификации при выбранной температуре). Эти сравнения проводили с применением протокола, описываемого ниже, если не указано иное.
Ферменты, олигонуклеотиды и мишень
Chlamydia trachomatis (Ct) применяли в качестве начальной мишени для разработки механизма STAR. Геномную ДНК Chlamydia trachomatis серовар J (ATCC VR-886) получали из Американской коллекции типовых культур (Манассас, Вирджиния). Область открытой рамки считывания 6 криптической плазмиды амплифицировали с помощью праймеров STARctF61a (SEQ ID NO:1, 5'-CGACTCCATATGGAGTCGATTTCCCCGAATTA-3') и STARctR61c (SEQ ID NO: 2, 5'-GGACTCCACACGGAGTCTTTTTCCTTGTTTAC-3'). Полученную ДНК-матрицу выявляли с применением молекулярного маяка STARctMB1 (SEQ ID NO:3, 5'-FAM/ccattCCTTGTTTACTCGTATTTTTAGGaatgg/BHQ1-3'), как описано в EP № 0728218. ДНК-полимеразу Manta 1.0 приобретали в Enzymatics (Беверли, Массачусетс). Никующую эндонуклеазу Nt.BstNBI приобретали у New England BioLabs (Ипсвич, Массачусетс), как описано в патенте США № 6191267.
Олигонуклеотиды и молекулярные маяки синтезировали в Integrated DNA Technologies (Коралвиль, Айова) и Bio-Synthesis (Льюисвиль, Техас). Общие признаки праймеров, применяемых в реакциях STAR, были следующими.
Наборы праймеров конструировали со стабилизирующей областью, расположенной в направлении 5' от сайта разрыва, и мишень-специфической связывающей областью, расположенной в направлении 3' от сайта разрыва (фигура 1A). Праймеры конструировали таким образом, что структура типа «петля на стебле» могла формироваться на 5'-конце олигонуклеотида за счет создания самокомплементарной структуры, которая формирует по меньшей мере часть стебля. Tm этой структуры выбирали так, чтобы в зависимости от температуры реакции в данный момент времени управлять либо линейной, либо экспоненциальной амплификацией. Стебель дополнительно охватывал по меньшей мере часть последовательности распознавания для никующей эндонуклеазы. Последовательность распознавания для никующей эндонуклеазы в праймерах является частью двухнитевой стеблевой структуры, однако по меньшей мере один нуклеотид является однонитевым для предотвращения образования разрыва. При необходимости, последовательность, которая является комплементарной последовательности-мишени, может содержать вторичную структуру или может не содержать вторичной структуры. Кроме того, эта последовательность может содержать модифицированные нуклеотиды, такие как 2'-модификации или фосфотиоатные связи.
Обращаясь к фигуре 1A, ʺпраймерная областьʺ представляет собой последовательность, которая является комплементарной последовательности мишени и отжигается с ней. ʺОбласть NEBʺ представляет собой область связывания никующей эндонуклеазы, т. е. область распознавания для никующей эндонуклеазы, которая в данном случае образует разрыв в сайте праймера, расположенном через четыре нуклеотида в направлении по ходу транскрипции от конца области NEB. ʺПетля амплификацииʺ обеспечивает стабилизацию и гибридизацию праймера в случае процесса амплификации, и она образует петлю с самой собой путем самокомплементарности во время фазы инициации для снижения фоновой неспецифической амплификации. На фигурах 1B и 1C представлены слегка отличающиеся варианты осуществления праймеров, применимых в способе по настоящему изобретению. Структура праймера является фактически идентичной варианту осуществления, представленному на фигуре 1A, однако измененные праймеры включают модифицированные основания в ʺпраймерной областиʺ. В частности, на 3'-конце праймерной области находится фрагмент из следующих друг за другом 2'-O-метилированных оснований. На фигуре 1B длина данного фрагмента составляет 7 оснований, а на фигуре 1C длина фрагмента составляет 6 оснований. Праймеры такого типа, как представлены на фигурах 1B и 1C, применяли в примере 8 ниже.
Краткий обзор олигонуклеотидов и механизма амплификации, встречающихся в реакции, предусматривает: (1) молекулу нуклеиновой кислоты-мишени; (2) две или более молекулы праймерных олигонуклеотидов, содержащих некоторое число олигонуклеотидов, которые комплементарны молекуле нуклеиновой кислоты-мишени, и (3) сайт в пределах праймера, в котором может образовываться разрыв под действием никующей эндонуклеазы. Способ предусматривает приведение молекулы нуклеиновой кислоты-мишени в контакт с полимеразой, двумя или более праймерными олигонуклеотидами, каждый из которых специфически связывается с комплементарной последовательностью на нуклеотидной молекуле-мишени, и никующей эндонуклеазой; и в неизотермических условиях получение выявляемого ампликона, который содержит по меньшей мере часть праймерного олигонуклеотида, который связывается с последовательностью-мишенью. Может быть понятно, что реакция STAR в целом проходит две отдельные фазы: инициации и экспоненциальной амплификации. Фаза инициации представляет собой начальное образование экспоненциального матричного дуплекса, за счет которого может происходить экспоненциальная амплификация. Эти две фазы схематически проиллюстрированы на фигурах 2A и 2B. На этих фигурах треугольным символом обозначена никующая эндонуклеаза, а шестиугольным символом обозначена ДНК-полимераза. За начальным контактом праймера с нуклеиновой кислотой-мишенью следует элонгация и образование прямой матрицы инициации. Затем праймер для противоположной нити связывается с вновь образованной прямой матрицей инициации, с элонгацией в направлении сайта разрыва матрицы инициации и через него. Может быть понятно, что в данный начальный процесс вовлечена полимераза для элонгации, и он очень предрасположен к образованию димеров праймеров и ложной амплификации усеченных или фоновых продуктов. После начала образования разрыва на одной из нитей полимераза будет проникать в сайт разрыва и элонгировать нить в направлении противоположного праймера и через сайт разрыва.
После того как цикл образования разрыва с последующей элонгацией под действием полимеразы произошел на обеих прямой нити инициации и на обратной нити инициации, образуется дуплекс, известный как экспоненциальный дуплекс. Начинается вторая фаза реакции; при этом данный экспоненциальный процесс амплификации сам себя подпитывает, поскольку каждая новая матрица, образованная за счет разрыва и элонгации, теперь представляет собой мишень для другого праймера.
Теперь понятно, что для быстрого образования матрицы на второй фазе требуется активная никующая эндонуклеаза. Ранее было известно, что такая репликаций с замещением нити с разрывом устраняла необходимость в термоциклировании, таким образом, реакция могла осуществляться и всегда осуществлялась при постоянной температуре. Новое настоящее изобретение обеспечивает возможность создания уникальных и отличных способов амплификации со значительно более высокой производительностью, чем существующие способы, включая высокий выход продукта с высокой специфичностью за короткий период времени.
Условия амплификации
Основная смесь для реакции амплификации при выбранной температуре (STAR) содержит два праймера, полимеразу и никующую эндонуклеазу (упомянутые выше). Реакции осуществляли в конечном объеме 20 мкл, включающем 0,41 мкM прямого праймера, 0,2 мкМ обратного праймера, 0,18 мкМ молекулярного маяка, 10 мкл мастер-микса STAR и 5 мкл образца ДНК. Мастер-микс STAR содержит следующие реагенты; 15 мM MgSO4, 90 мM Tris-HCl (pH 8,5), по 300 мкМ каждого dNTP, 15 мM (NH4)2SO4, 15 мM Na2SO4, 1 мM DTT, 0,01% Triton X-100, 7 ЕД никующей эндонуклеазы, 48 ЕД полимеразы. Температура реакции была изотермической или варьировала, исходя из величины снижения температуры. Если в самом начале амплификации температура в каждой реакции составляет 60°C и снижается на определенную величину каждые 15 секунд или 1 минуту, то, например, скорость минус 0,5°C (т. е. снижение температуры на 0,5°C каждые 15 секунд) в течение 10 минут приведет к снижению температуры от 60°C до 40°C в ходе реакции. Амплификацию и выявление продукта STAR осуществляли с помощью устройства Agilent Mx3005 P QPCR (Agilent). В следующей таблице перечислены тестируемые температурные профили, за исключением отмеченных случаев.
Таблица 1
Инкубация перед реакцией позволяет реагентам достичь температуры, подходящей для тестирования влияния снижения температур на кинетику реакции амплификации, производительность фермента и флуоресценцию сигнала. Такой порядок проведения реакций исключает переменные, связанные с повышением температуры, и обеспечивает возможность прямого сравнения существующих методик изотермической амплификации и нового способа STAR.
Процедура амплификации
Точные стадии осуществления реакции амплификации были следующими: 1) подготовка мастер-микса; 2) подготовка праймеров с мишенью или без мишени; 3) внесение смеси праймеров в ряды A-G 96-луночного планшета в зависимости от числа реакций, подлежащих выполнению на планшет; 4) внесение мастер-микса в ряд H того же 96-луночного планшета; 5) герметизация планшета и выполнение инкубации перед реакцией в течение 2 минут; 6) перенос мастер-микса из ряда H в каждый ряд со смесью праймеров, пауза в 15 секунд между переносами; 7) герметизация и начало выполнения предварительно выбранного температурного профиля, а также сбор данных.
В ходе реакции амплифицированный продукт измеряли каждые 15 секунд с применением молекулярного маяка, как описано выше. Флуоресценцию молекулярного маяка в реакционной смеси отслеживали для измерения количества специфического продукта, образующегося во время реакции. Специфический продукт, образующийся во время реакции, связывается с молекулярным маяком, отделяя флуорофор от гасителя, что приводит к генерированию флуоресценции. Из показателей флуоресценции вычитали фоновый уровень, исходя из среднего значения первых 3 считываний каждой реакционной лунки перед началом амплификации. Дополнительные характеристики определяли на основании роста показателя от исходного порогового уровня (TL). TL выбирали вблизи исходного уровня фоновой вычитаемой флуоресценции, однако выше диапазона случайных флуктуаций. Снижение температуры вызывает снижение исходной флуоресценции молекулярного маяка вследствие повышения прочности стебля, что вызывает постоянное линейное снижение исходного уровня, поскольку гаситель и флуорофор взаимодействую с большей силой. TL, составляющий 2000, был выбран для всех реакций. Для сравнения точное число определяли, исходя из времени, при котором амплификация достигала TL, обозначаемое как значение AT. Применение значения AT обеспечивало возможность сравнения значений одного планшета с другим.
Пример 2. Результаты при применении немодифицированных праймеров
Чтобы продемонстрировать улучшение, которое обеспечивает STAR по сравнению с существующими изотермическими технологиями, выполняли амплификации с применением 18 повторностей в случае применения мишени и 6 повторностей в случае отсутствия мишени. Реакции STAR показывают поразительное улучшение в скорости, чувствительности и общей флуоресценции по сравнению с изотермическими условиями. В частности, диапазон от -0,8°C в минуту до -3,2°C в минуту был заметно лучшим, чем все изотермические условия (фигуры 3-11). Удивительным и неожиданным было то, что при таком значительном понижении температуры все еще получали превосходные результаты. Не ограничивая настоящую заявку какой-либо конкретной теорией, полагают, что улучшения амплификации могли быть связаны по меньшей мере с тремя характеристиками, дополнительно обсуждаемыми ниже.
Результаты экспериментов с применением немодифицированных праймеров представлены на фигурах 3-11. На этих фигурах температурный профиль указан с помощью фоновой штриховки. Величина сигнала (флуоресценция) для отрицательных контролей ʺбез использования мишениʺ указана в виде темной кривой. Величина сигнала, генерируемого в присутствии 10 или 100 копий мишени (геномной ДНК C. trachomatis) указана в виде кривых более светлого цвета.
На фигурах 3, 4 и 5 представлены результаты для изотермических амплификаций (т. е. выполняемых не в соответствии со способом по настоящему изобретению) при 50, 56 и 60°C соответственно. Как можно заметить на фигуре 3, наблюдалось фактически отсутствие специфической амплификации при 50°C, сильная амплификация при 56°C (фигура 4), по меньшей мере для 100 копий мишени, и слабая амплификация при 60°C (фигура 5).
На фигурах 6-10 представлены результаты, полученные для неизотермических реакций амплификации (STAR) в соответствии с настоящим изобретением, в которых температура снижалась во время амплификации. Скорость снижения температуры была линейной, варьируя в диапазоне от -0,1°C за 15 секунд (т. е. -0,4°C за минуту) на фигуре 6 до -1,0°C за 15 секунд (т. е. -4,0°C за минуту) на фигуре 10. Можно заметить, что во всех случаях в реакциях со 100 копиями мишеней генерировался больший сигнал флуоресценции, чем в реакциях с 10 копиями мишеней, как и следовало ожидать. Более существенно, в реакциях производился намного больший сигнал, чем в эквивалентных изотермических амплификациях, особенно в случае реакций с 10 копиями мишени. Кроме того, выявляемый сигнал производился быстрее, чем в эквивалентных изотермических реакциях.
Аналогичные результаты получали, когда способ по настоящему изобретению осуществляли с применением нелинейного пошагового снижения температуры (как представлено на фигуре 11).
Авторы настоящего изобретения также обнаружили (данные не представлены для краткости изложения), что разброс величины сигнала между различными повторностями в реакциях STAR был значимо ниже, чем между повторами в изотермических реакциях, доказывая, что способ по настоящему изобретению давал более достоверные результаты. В следующих комментариях предложен возможный механизм, с помощью которого способ по настоящему изобретение мог обеспечивать отмеченные выше преимущества.
В большинстве реакций амплификации нуклеиновой кислоты со временем образуются димеры праймеров, конкурируя за ограниченные реагенты, и при низких концентрациях мишени димеры праймеров могут стать основным путем в реакции амплификации. Ограничение или отсрочка образования димеров праймеров, даже в незначительном количестве, обеспечивает значительные преимущества для реакции. В связи с быстрой природой реакции амплификации отсрочка образования димеров праймеров обеспечивает возможность того, что создаются благоприятные условия для предпочтительных путей амплификации (т. е. образования матриц), улучшая все аспекты амплификации. За счет инициации реакций при повышенных температурах создаются благоприятные условия для этих путей образования матриц, и они становятся даже предпочтительными. Это заметно по повышению чувствительности в способе STAR, повышению сигнала флуоресценции, более плотной группировке повторностей (т. е. лучшей воспроизводимости) и повышению скорости.
После фазы инициации реакции начинается экспоненциальная фаза. Поскольку создаются благоприятные условия для пути образования матриц по сравнению с ошибочными путями, желательным является образование как можно большего количества продукта как можно быстрее, и это облегчается за счет STAR. Одной из наиболее вероятных стадий ограничения такого образования является образование разрыва в сайтах под действием никующей эндонуклеазы. Поскольку температура реакционной смеси снижается, она приближается к наиболее благоприятной температуре для никующей эндонуклеазы, и эффективность реакции возрастает, при этом образуется максимально возможное число матриц для выявления.
По мере дальнейшего снижения температуры создаются благоприятные условия для выявления матриц с помощью молекулярных маяков и снижается фоновая флуоресценция. Температура плавления матрицы с молекулярными маяками становится значительно выше, чем температура выявления, за счет чего генерируется усиленный сигнал, поскольку меньше матриц отсоединяется от молекулярного маяка. В результате снижения температуры, кроме того, температуры плавления стебля становятся выше, чем температуры реакции. Таким образом, в отсутствие матрицы создаются благоприятные условия для закрытой фазы молекулярного маяка, что приводит к генерации меньшего фонового сигнала.
Новый способ неизотермической реакции по настоящему изобретению предусматривает значительное улучшение по сравнению с существующими изотермическими и термоциклическими условиями. За счет создания благоприятных условий для активности ферментов и оптимальной кинетики реакций способ привел к улучшению изменения AT, повышению общего количества генерируемой флуоресценции, повышению однородности амплификации и повышению чувствительности выявления.
Пример 3. Результаты при применении SYBR Green II
Поскольку молекулярные маяки только измеряют повышение общего количества специфического продукта, представляющего собой однонитевую ДНК, то продукт неспецифической амплификации не измеряется независимо от предусмотренного продукта амплификации. Для измерения образования продуктов неспецифической амплификации (например, возникающих в результате образования димеров праймеров), отдельные реакции проводили в присутствии SYBR Green II. SYBR Green II представляет собой один из наиболее чувствительных красителей, которые известны для выявления однонитевой ДНК, РНК и двухнитевой ДНК. Поскольку SYBR Green II характеризуется слабой естественной флуоресценцией, он является идеальным выбором для выявления общей амплификации в реакции или неспецифической амплификации, если амплификация выполняется в присутствии или в отсутствие мишени. Проводили прямое сравнение реакций при двух условиях, изотермических и неизотермических (STAR), как показано в таблице 2.
Таблица 2
Кроме того, сравнивали реакции с использованием 50 копий геномной ДНК и без использования мишени. SYBR Green II (Life Technologies, Карлсбад) приобретали с концентрацией 10000x, а в реакции применяли концентрацию 0,5x. Для расчета AT применяли более высокий TL, составляющий 9000, вследствие естественными свойствами интеркалирующих красителей. Для SYBR Green II характерна обратно пропорциональная зависимость между флуоресценцией и температурой. Чем ниже температура, тем выше флуоресцентный сигнал, как описано в ʺComparison of multiple DNA dyes for real-time PCR: effects of dye concentration and sequence composition on DNA amplification and melting temperatureʺ (Gudnason et al., 2007 Nucl. Acids Res. 35 (19) e 127). Результаты представлены в таблице 3 ниже.
Таблица 3
Способ STAR демонстрирует множество улучшений; во-первых, он снижает образование фонового продукта, на что указывает более длительное время до проявления амплификации с помощью SYBR Green II в случае ʺотсутствия мишениʺ, чем для сигнала мишени. Во-вторых, он характеризуется повышением амплификации продукта, что заметно по меньшему времени амплификации при присутствии мишени. В сочетании эти улучшения более чем в четыре раза увеличивают разницу между AT в сравнении с изотермическими способами.
Следует отметить, что значения AT, полученные в изотермических реакциях, характеризовались большей вариабельностью по сравнению со значениями AT, полученными в STAR. Это показывает преимущество, которое новый способ имеет при контроле процесса амплификации, и отражает непредсказуемость неспецифических путей амплификации при применении традиционных способов.
Пример 4. Результаты при применении 2'-O-метил-модифицированных праймеров
Как описано в патентах США №№ 6794142 и 6130038, известно, что применение 2'-O-метил-модифицированных праймеров снижает образование димеров праймеров во время амплификации. В US 2005-0059003 описано применение 2'-O-метил-модификаций, находящихся на 3'-конце праймеров для SDA, из это следует, что ДНК-полимераза I Bst и ее производные могут эффективно использовать 2'-модифицированные рибонуклеотиды в качестве праймеров для синтеза ДНК. Мишень-специфические области праймеров, содержащие один или несколько 2'-модифицированных нуклеотидов (например, 2'-O-метил, 2'-метоксиэтокси, 2'-фтор, 2'-аллил, 2'-O-[2(метиламино)-2-оксоэтил], 2'-гидроксил (РНК), 4'-тио, 4'-CH3-O-2'-мостик, 4'-(CH3)-3-O-2'-мостик, 2'-LNA и 2'-O- (N-метилкарбамат-2'-Suc-OH)), должны улучшать изотермические реакции. Если 2'-модифицированные нуклеотиды полностью исключали образование димеров праймеров, то было бы удивительно, что способ STAR может дополнительно улучшать амплификацию. Проводили прямое сравнение реакций при двух условиях, изотермических и неизотермических (STAR), как показано ниже.
Таблица 4
Результаты амплификации с применением 2'-модифицированных нуклеотидов на 3'-конце праймеров представлены в таблице 5 ниже. Реакции проводили как минимум в шести повторностях в случае реакций с отсутствием мишени и в двенадцати повторностях в случае реакций с использованием мишени.
Таблица 5
Данные показывают, что применение по меньшей мере одного праймера, включающего 2'-O-метильные нуклеотиды, отсрочивает образования димеров праймеров, улучшая реакцию, хотя и замедляя ее. Кроме того, применение способа STAR не только улучшало применение амплификации с 2'-O-метил-модификациями праймеров, в некоторой степени восстанавливая потерю скорости, но также в три раза увеличивало разницу между амплификацией с мишенью и отсутствием мишени. Это указывает на то, что хотя 2'-O-метил-модификации действительно снижают образование неспецифических ошибочных продуктов амплификации, в действительности они не устраняют ее. Данные дополнительно указывают на то, что в способе STAR более эффективно используются улучшения, обусловленные 2'-O-метил-модификациями, чем в существующих методиках, раскрытых ранее.
Не ограничивая настоящее изобретение какой-либо конкретной теорией, потенциальные улучшения, полученные за счет применения одного или нескольких 2'-модифицированных нуклеотидов в праймерной области, предположительно в большой степени обусловлены улучшениями в фазе инициации амплификации.
Во время начальной элонгации праймерной области на мишени включение одного или нескольких 2'-модифицированных нуклеотидов в праймерную область STAR приводит к тому, что эти нуклеотиды являются неподходящими, чтобы выступать в качестве матрицы для элонгации под действием полимеразы в неспецифических комплексах, образованных за счет взаимодействий праймеров, что снижает фоновый сигнал. Вполне возможно, что полимераза останавливается в то время, когда нуклеотид попадает в карман связывания. При непродуктивных реакциях (т. е. нецелевом связывании или образовании димеров праймеров) эффект остановки является достаточным для сведения к минимуму аберрантной элонгации, поскольку связывание матрицы происходит почти при ее температуре плавления. Следовательно, 2'-модификации способны ограничить нежелательные пути амплификации, поскольку реакция приостановлена. Однако во время благоприятных амплификаций 2'-модификации снижают температуры плавления, таким образом отрицательно влияя на амплификацию, замедляя время амплификации. STAR способна использовать преимущества 2'-модификаций, при этом сводя к минимуму отрицательные последствия при амплификации мишени.
Такая остановка полимеразы дополнительно объясняет, почему STAR в сочетании с 2'-O-метил-модификациями усиливают друг друга. Начальное повышение температуры, предусмотренное в способе STAR, кроме закономерного снижения образования димеров праймеров, усиливает остановку под действием 2'-модификаций и плавление праймеров перед осуществлением ошибочной амплификации, таким образом, оба способа дополняют друг друга. Кроме того, поскольку STAR включает снижение температуры, то снижения температуры плавления, вызванные 2'-модификациями в праймерах, могут сводиться к минимуму по мере протекания реакции.
Пример 5. Результаты при применении множественных полимераз
Существующие технологии амплификации выполняются либо с использованием термоциклирования, либо при постоянной температуре. Способ по настоящему изобретению не относится ни к одной из них, а вместо этого выполняется за счет снижения температуры без проведения циклирования. Конкретным новым признаком настоящего изобретения является возможность применения ферментов с аналогичной функцией, но с отличающимся температурным оптимумом. Например, данная технология обеспечивает возможность применения множественных праймеров, разработанных для никующих эндонуклеаз, которые функционируют при различных температурных оптимумах, вместе с полимеразами, приводящими к замещению нити, с отличающимися оптимумами. Не ограничивая настоящее изобретение какой-либо конкретной теорией, данный способ открывает доступ к быстрым способам амплификации, обеспечивая возможность новых комбинаций ферментов и праймеров, не используемых в существующих технологиях. Проводили прямое сравнение описанных ниже (таблица 6) реакций при трех условиях, изотермических, неизотермических (STAR) и неизотермических (STAR) с полимеразой BSU (в дополнение к начальной полимеразе Manta 1.0), как описано ниже. Полимеразу BSU приобретали в England BioLabs (Ипсвич, Массачусетс) и использовали из расчета 0,5 ЕД на реакцию. При всех условиях эксперименты осуществляли с применением 18 повторностей с мишенью и 6 повторностями в отсутствие мишени.
Таблица 6
Реакции амплификации осуществляли с применением образцов, содержащих 10 копий геномной ДНК C. trachomatis, и результаты представлены на фигурах 12A-12C.
На фигуре 12A представлены результаты для изотермической реакции (не в соответствии с настоящим изобретением). На фигуре 12B представлены результаты для реакции STAR в присутствии только полимеразы Manta, а на фигуре 12C представлены результаты для реакции STAR в присутствии дополнительной полимеразы BSU.
Первой очевидной разницей является отсутствие выявления 10 копий геномной ДНК при использовании изотермического способа, лишь 9 из 18 повторностей превысили пороговый уровень флуоресценции (TL) и можно было сказать, что они амплифицировались. При обоих способах STAR выявление осуществили в 17 из 18 повторностей. (Следует отметить, что пропущенная повторность в каждом способе STAR была обусловлена бракованной многоканальной пипеткой).
Хотя разница между способами STAR была менее очевидной, добавление второй полимеразы с более низкой оптимальной температурой, составляющей 37°C, повышало общую флуоресценцию через 10 минут. Кроме того, вторая полимераза также уплотняла повторности, снижая вариабельность AT. Это разница была бы продемонстрирована далее, если бы на рынке была доступна коммерческая полимераза, приводящая к замещению нити, с температурным оптимумом от 45°C до 50°C. Результаты указывают на то, что способ STAR превосходит изотермические условия, и, кроме того, что данная технология обеспечивает возможность новых механизмов, комбинаций ферментов и схем амплификации с праймерами.
Пример 6. Воспроизводимость
Для валидации однородности технологии STAR проводили исследование с большим числом повторностей, в котором сравнивали STAR и опубликованные изотермические условия, описываемые в патенте США № 9562263. Амплификации, STAR в сравнении с изотермическими условиями, проводили с применением более 100 повторностей для реакций, содержащих мишень, и 16 повторностей для контрольных реакционных смесей без мишени. При обоих условиях применяли одинаковые буферы, полимеразу, никующую эндонуклеазу и мишень. Как представлено на графике рассеивания на фигуре 13, для технологии STAR показано явное уменьшение среднего времени (AT) для достижения амплификацией порогового уровня флуоресценции (TL), повышение чувствительности и снижение стандартного отклонения между повторностями. Время AT для реакций, осуществляемых в соответствии с настоящим изобретением, составляло 3,35 минуты, в то время как значение AT для реакций, осуществляемых в соответствии с традиционными изотермическими протоколами, составляло 4,88 минут, при этом разница является статистически значимой, что определено с помощью двустороннего t-критерия. Не ограничивая настоящую заявку какой-либо конкретной теорией, полагают, что значимое снижение времени амплификации обусловлено улучшенной инициацией реакции, что обеспечивает возможность более эффективной амплификации при меньшем числе копий, сводит к минимуму события образования димеров праймеров, а повышенное число специфических продуктов элонгации образует матрицы быстрее, чем в ранее раскрытых способах.
Пример 7. Реакции амплификации, осуществляемые за пределами традиционных диапазонов температуры для изотермических условий
Дополнительным преимуществом технологии STAR является способность к амплификации за пределами наиболее обычных диапазонов температур для изотермической амплификации. Как описано в патентах США №№ 5712124, 9562263 и 5399391, большинство технологий изотермической амплификации имеют узкий диапазон температур, при которых может происходить амплификация. За пределами таких типичных диапазонов температуры, традиционные изотермические методики имеют сложности в осуществлении амплификации. Чтобы продемонстрировать универсальность STAR, амплификации выполняли, как описано в таблице 7 ниже.
Таблица 7
Изотермические реакции осуществляли, как описано в патенте США № 9562263. Фигуры 14A и 14B представляют собой графики, показывающие величину сигнала флуоресценции (с вычитанием фонового уровня; условные единицы) в зависимости от времени (минуты) для реакций изотермической амплификации, осуществляемых либо при 63°C (фигура 14A), либо при 49°C (фигура 14B). На обеих фигурах в виде пунктирных кривых представлены результаты, полученные в реакциях отрицательного контроля без матрицы; в виде кривых со сплошной линией представлены результаты для тестируемых реакций, содержащих матрицу.
Из фигуры 14A становится очевидным, что если температуру реакции поддерживали при 63°C специфическая в отношении матрицы амплификация практически отсутствовала. В случае фигуры 14B, результаты, вероятно, указывают на то, что при 49°C амплификация происходит в интервале времени от приблизительно 9 минут и далее, однако в действительности это, возможно, был ложный сигнал, возникающий в результате взаимодействий молекулярных маяков с праймерами (данные не представлены).
В отличие от изотермических реакций реакции ʺSTARʺ, осуществляемые в соответствии с настоящим изобретением, могли быть инициированы при повышенных температурах и все же приводить к высокому уровню амплификации. Результаты таких реакций представлены на фигурах 15A, B и C. Они представляют собой графики флуоресценции (с вычитанием фонового уровня, условные единицы) в зависимости от времени (минуты). Однородная штриховка указывает на температуру (°C) во время протекания реакций. Пунктирные кривые представляют результаты, полученные с применением 10 копий мишени, сплошные кривые представляют результаты, полученные с применением 100 копий мишени. На фигуре 15A начальная температура составляла 62°C, а скорость снижения температуры составляла -0,8°C за 15 секунд (т. е. -3,2°C за минуту). На фигуре 15В начальная температура составляла 63°C, а скорость снижения температуры составляла -0,8°C за 15 секунд. На фигуре 15С начальная температура составляла 64°C, а скорость снижения температуры составляла -0,9°C за 15 секунд (т. е. -3,6°C за минуту). На основании этих фигур становится очевидно, что начальная температура, составляющая 62 или даже 63°C, обеспечивала высокие результаты реакций STAR, и даже некоторые амплификации с применением начальной температуры, составляющей 64°C, хотя они были явно субоптимальными.
Кроме того, эксперименты осуществляли с применением больших понижений температуры. Результаты представлены на фигурах 16A и 16B. На графиках представлены результаты для отрицательных контролей без мишени (отсутствие сигнала флуоресценции выше порогового уровня) и для реакций STAR, осуществляемых в присутствии 10 или 100 копий геномной ДНК-мишени C. trachomatis.
На фигуре 16A представлены результаты, полученные с применением начальной температуры 63°C, за которым следовало снижение температуры со скоростью -0,8°C за 15 секунд в течение 1 минуты, за которым следовало резкое снижение до 49°C, а затем постепенное снижение температуры, составляющее -0,2°C за 15 секунд (т. е. -0,8°C за минуту) на всем протяжении реакции. На графике показано, что амплификация осуществлялась в обеих реакциях с числом копий 10 и 100, хотя сигнал флуоресценции для реакций со 100 копиями мишени был примерно в два раза больше по сравнению с реакциями с 10 копиями мишени, и у них наблюдалась значительная внутригрупповая изменчивость.
На фигуре 16B представлены результаты, полученные с применением той же начальной температуры 63°C в течение 1 минуты, за которым следовало резкое снижение до 49°C. После этого температуру реакции поддерживали при 49°C на всем протяжении эксперимента. На основании графика можно заметить, что наблюдался высокий уровень специфической амплификации и намного меньшая внутригрупповая изменчивость (только реакции, осуществляемые со 100 копиями мишени или без мишени).
Способность STAR к амплификации в пределах температурного диапазона 40°C явно указывает на то, что STAR очень сильно отличается от традиционных реакций амплификации. Атипичные температуры реакции с большими диапазонами являются непривычными и, как ожидалось, не должны были быть функциональными. Не ограничивая настоящую заявку какой-либо конкретной теорией, неожиданно, что такие большие температурные диапазоны, по-видимому, менее ограничивают амплификацию в случае STAR, чем в случае традиционных способов амплификации. Вероятно, способность STAR к обеспечению более эффективной амплификации при более широком диапазоне температур обусловлена увеличением специфичности и связывания праймеров наряду со стратегическим использованием температурных оптимумов ферментов. За счет использования более высокой температуры для фазы инициации создаются благоприятные условия для амплификации истинных продуктов, и, таким образом, повышается эффективность всех последующих фаз, экспоненциальной амплификации и выявления. Данный выбор и последующее понижение температуры открывают доступ к набору инструментов для амплификации, поскольку можно воплощать новые схемы в отношении ферментов, праймеров и температур.
Пример 8. Результаты при применении праймеров с шестью и семью 2'-O-метил-модификациями
Как описано ранее, известно, что 2'-O-метил-модифицированные праймеры снижают образование димеров праймеров во время амплификации. Дополнительной иллюстрацией совместного действия этих модификаций с технологией STAR является возможность включения больших фрагментов 2'-O-метил-модификаций и все же осуществление амплификации. Как правило, 2'-O-метил-модификации останавливают полимеразу, надолго затормаживая амплификацию; при этом полагают, что шесть или более модификаций приведут к тому, что полимераза ʺвыпадетʺ из комплекса, а не просто остановит свое действие. На фигурах 17A и 17B продемонстрирована способность STAR допускать данные модификации и обеспечивать значительную амплификацию при более длинных фрагментах 2'-O-метил-модификаций, чем ранее установленные. Структура праймеров, содержащих 2'-O-метилированные основания, показана на фигурах 1B и 1C.
Фигуры 17A и 17B представляют собой графики (с вычитанием фонового уровня) флуоресценции (условные единицы) в зависимости от времени (минуты). Штриховка указывает температурный профиль (°C) в зависимости от времени в ходе реакций амплификации. На фигуре 17A представлены результаты реакций, осуществляемых с применением праймеров, содержащих 6 2'-O-метил-модифицированных оснований, а на фигуре 17B представлены результаты реакций, осуществляемых с применением 7 2'-O-метил-модифицированных оснований. В обоих случаях в реакциях отрицательного контроля без мишени не происходило образования какого-либо сигнала флуоресценции, в то время как при применении каждого из модифицированных праймеров наблюдали высокий уровень амплификации, хотя среднее значение сигнала флуоресценции было несколько выше в случае праймеров с 6 модифицированными основаниями, а внутригрупповая изменчивость была значимо ниже по сравнению с результатами для праймеров с 7 модифицированными основаниями.
Как видно на фигурах, праймеры, содержащие фрагменты из шести и семи 2'-O-метил-модификаций, приводят к надлежащей амплификации в случае STAR. Это могло быть обусловлено способностью STAR начинать амплификацию при очень благоприятных температурных диапазонах для полимераз, приводящих к замещению нити, около 65°C. Такой благоприятный диапазон может обеспечивать возможность того, что полимераза элонгирует более длинные фрагменты 2'-модификаций, обеспечивая инициацию, что отсутствует при других технологиях. Для краткости эти данные не представлены, однако также можно описать, что полноразмерные праймерные области модифицировали с помощью 2'-O-метил-модификаций, и при этом амплификация происходила, хотя и более медленно и при более слабом флуоресцентном сигнале.
Пример 9. Результаты при применении рибонуклеиновой кислоты
STAR может осуществлять амплификацию на основе любой нуклеиновой кислоты, с применением любой композиции из ДНК (кДНК и гДНК), РНК (мРНК, тРНК, рРНК, миРНК, микроРНК), аналогов РНК/ДНК, сахарных аналогов, гибридов, полиамидной нуклеиновой кислоты и других известных аналогов. Амплификацию рибосомальной РНК проводили, как описано ниже.
Ферменты, олигонуклеотиды и мишень
Listeria monocytogenes использовали в качестве мишени для разработки анализа РНК на основе STAR. Геномную ДНК Listeria monocytogenes (ATCC VR-886) приобретали в Американской коллекции типовых культур (Манассас, Вирджиния). Первоначальный скрининг осуществляли с помощью гДНК, и было обнаружено, что область 23S рибосомальной РНК амплифицировался с помощью праймеров LMONF72 (SEQ ID NO: 4, 5'-GGACTCGATATCGAGTCCAGTTACGATTTGTTG-3') и LMONR86 (SEQ ID NO: 5, 5'-gGACTCCATATGGAGTCCTACGGCTCCGCTTTT-3'). Полученную ДНК-матрицу выявляли с применением молекулярного маяка LMONMB1 (SEQ ID NO: 6, 5'-FAM/gctgcGTTCCAATTCGCCTTTTTCGCagc/BHQ1-3'), как описано в EP № 0728218. Общую РНК выделяли с применением набора RNeasy Plus mini от Qiagen (Хильден, Германия) в сочетании с быстрым механическим лизисом на Mini Bead Mill 4 (VWR). Listeria monocytogenes (ATCC BAA-2660) приобретали в Американской коллекции типовых культур (Манассас, Вирджиния), и культуру возобновляли на агаровых пластинах с сердечно-мозговым экстрактом (BHI). Для инокуляции 25 мл среды BHI использовали одиночную колонию, которую выращивали в течение 18 часов при 37°C до достижения стационарной фазы. Затем культуру подвергали обратному разведению и выращивали в течение дополнительных четырех часов перед сбором. Осадки из бактерий ресуспендировали в буфере для лизиса RLT, и гомогенизировали на Mini Bead Mill (VWR). Общую РНК очищали согласно инструкциям производителя (Qiagen). Геномную ДНК удаляли, пропуская лизаты через ДНК-связывающую колонку, предоставленную в наборе для очистки RNeasy Plus. Примеси геномной ДНК дополнительно сводили к минимуму за счет непосредственного расщепления образцов ДНКазой I на РНК-связывающей колонке RNeasy. ДНК-полимеразу Bst X приобретали у Beverly Qiagen (Беверли, Массачусетс). Omniscript, обратную транскриптазу, приобретали в Qiagen (Хильден, Германия). Никующую эндонуклеазу Nt.BstNBI приобретали у New England BioLabs (Ипсвич, Массачусетс), как описано в патенте США № 6191267. Олигонуклеотиды и молекулярные маяки синтезировали в Integrated DNA Technologies (Коралвиль, Айова).
Условия амплификации
Основная смесь для STAR содержала все, что описано в примере 1 выше, с дополнительным включением следующего элемента, 4 ЕД обратной транскриптазы (упомянутой выше), и заменой Manta 1.0 на Bst.X.
Результаты представлены на фигуре 18, которая представляет собой график флуоресценции (условные единицы) в зависимости от времени (минуты). Штриховка обозначает температурный профиль в ходе реакции. Реакции отрицательного контроля не приводили к образованию какого-либо сигнала флуоресценции, в то время как реакции с числом копий мишени 10, 100 или 1000 приводили к образованию сигнала флуоресценции выше порогового значения при снижении количества времени (примерно 3,5 минуты, 3,0 и 2,75 минуты соответственно). Результаты показали, что STAR может осуществлять эффективную амплификацию на основе обратно транскрибированной РНК-мишени.
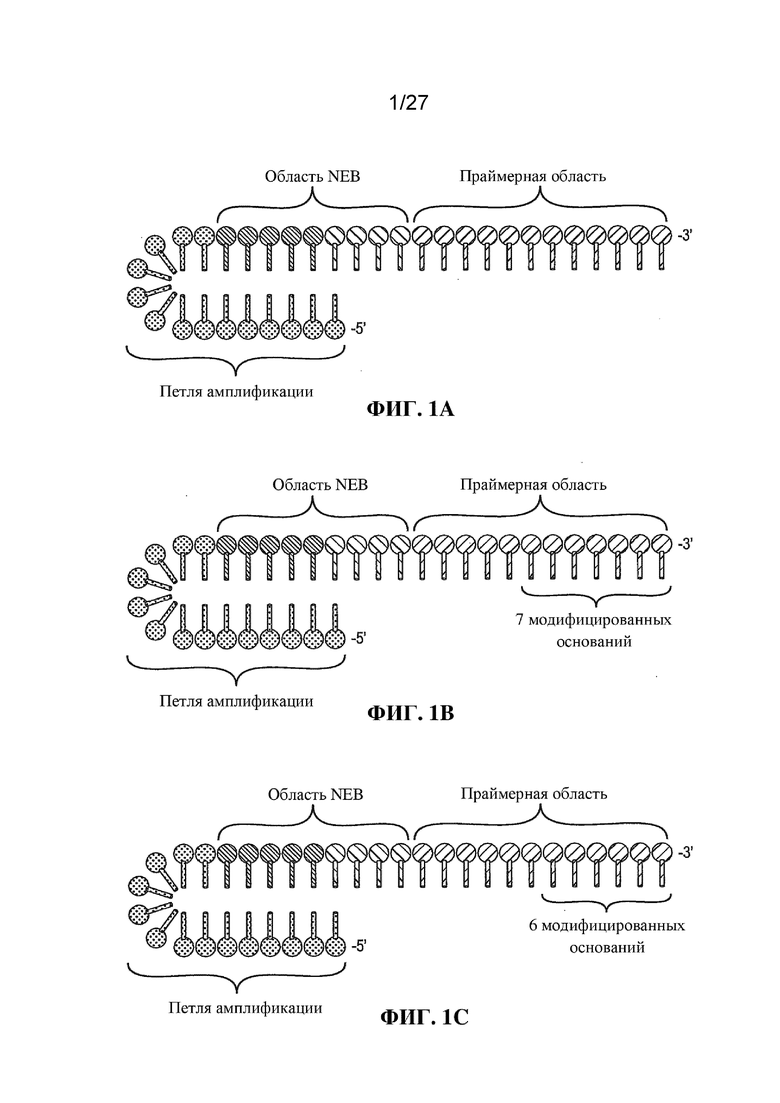
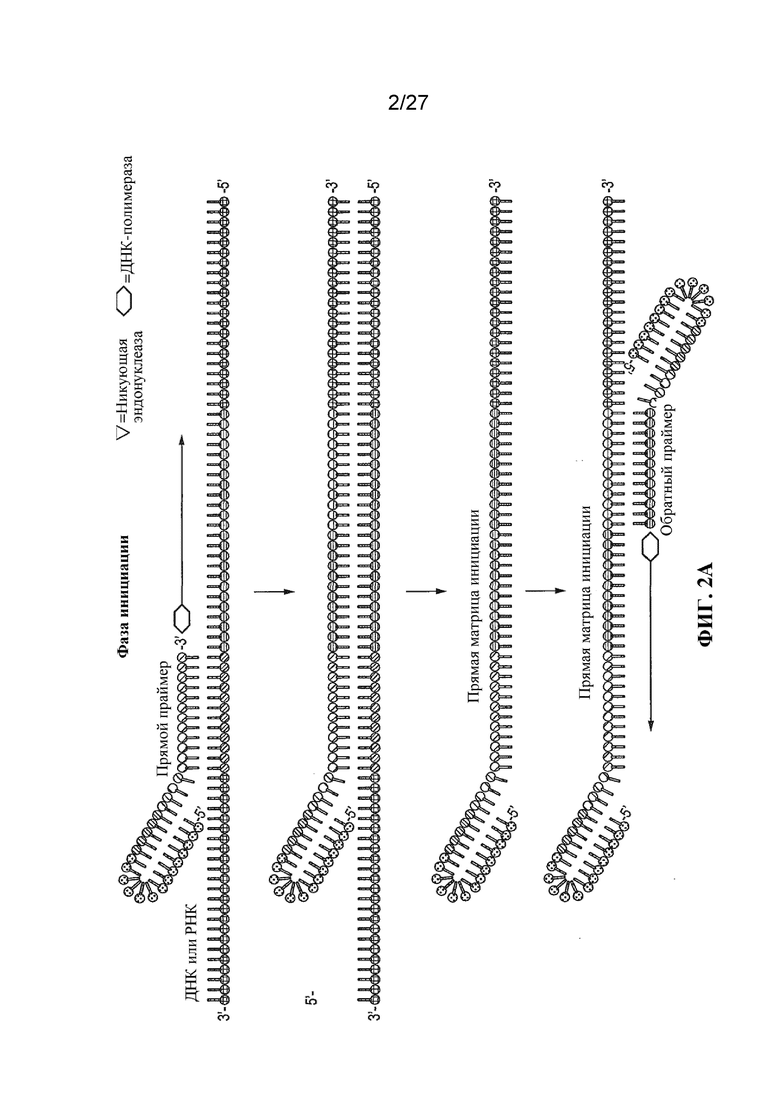
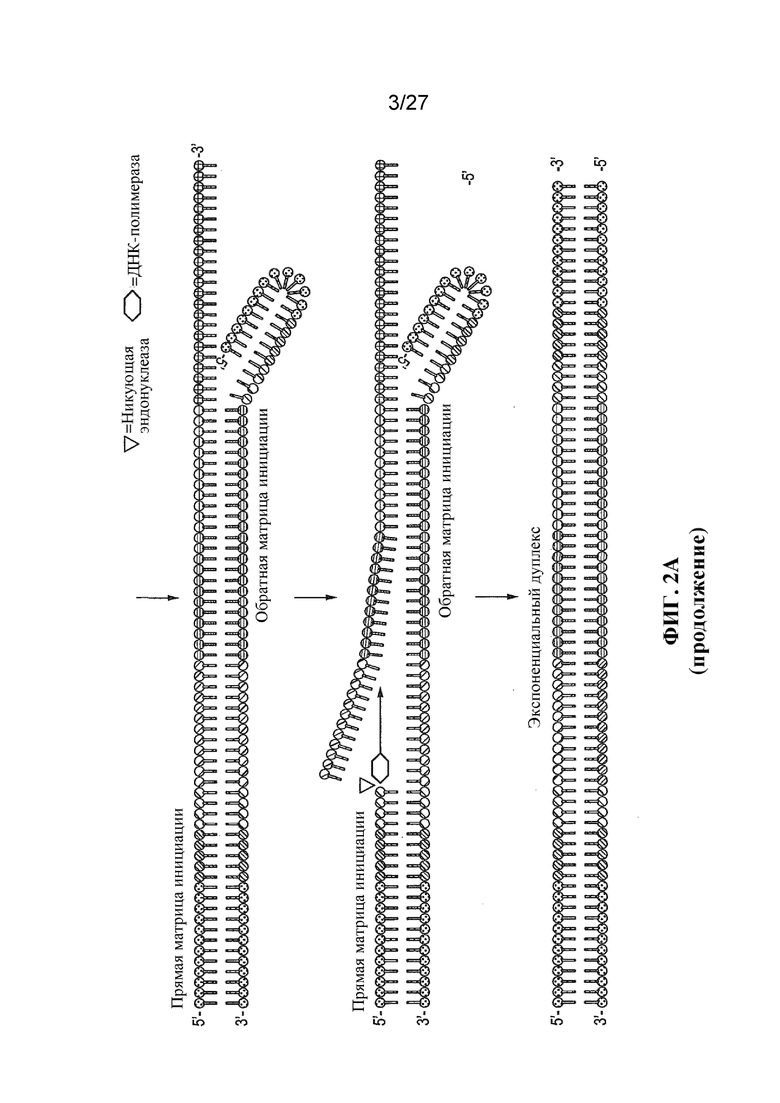
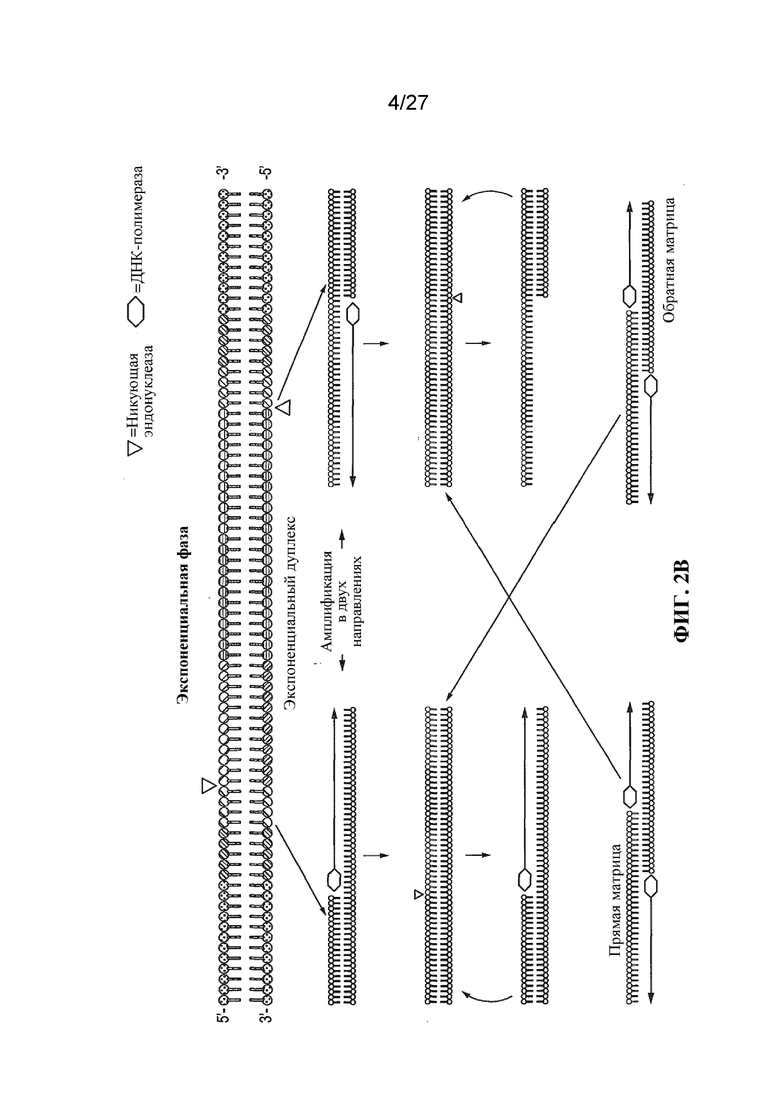


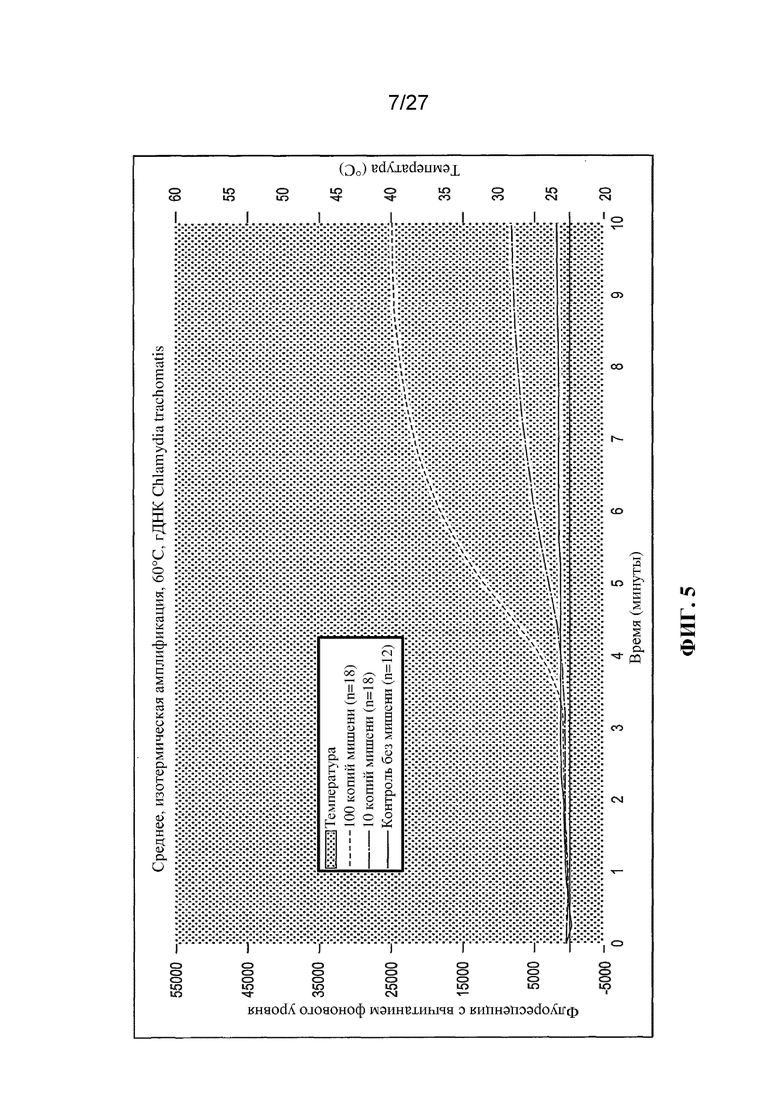
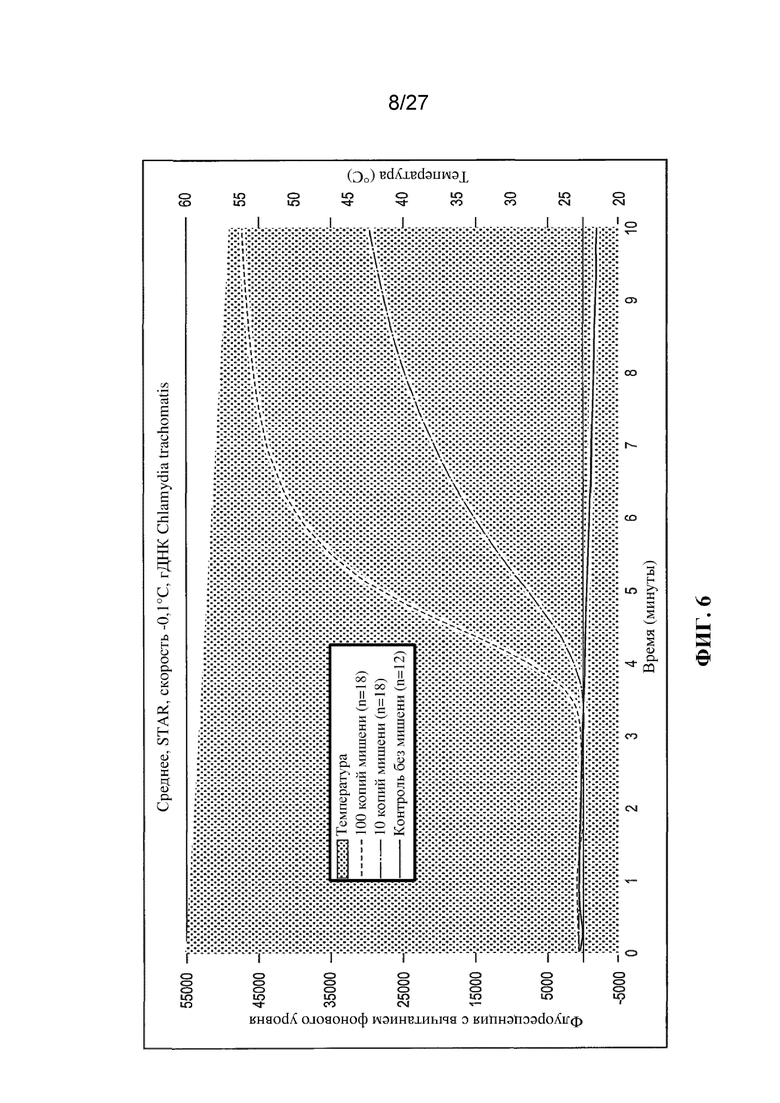
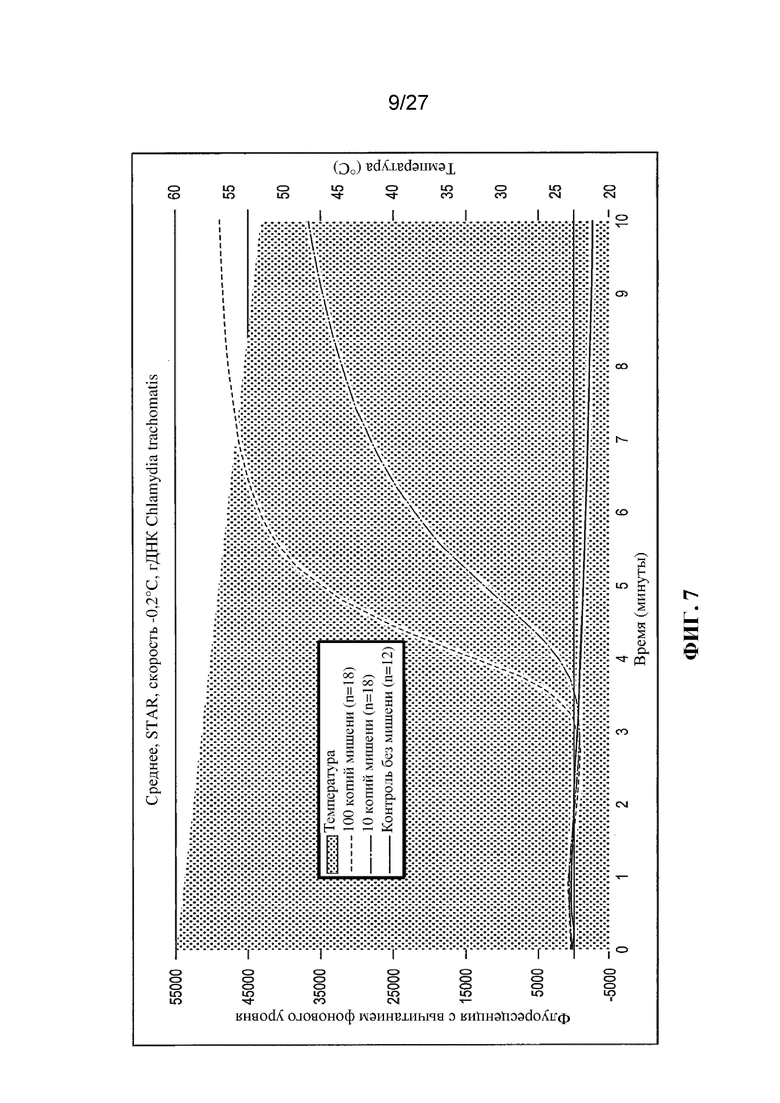
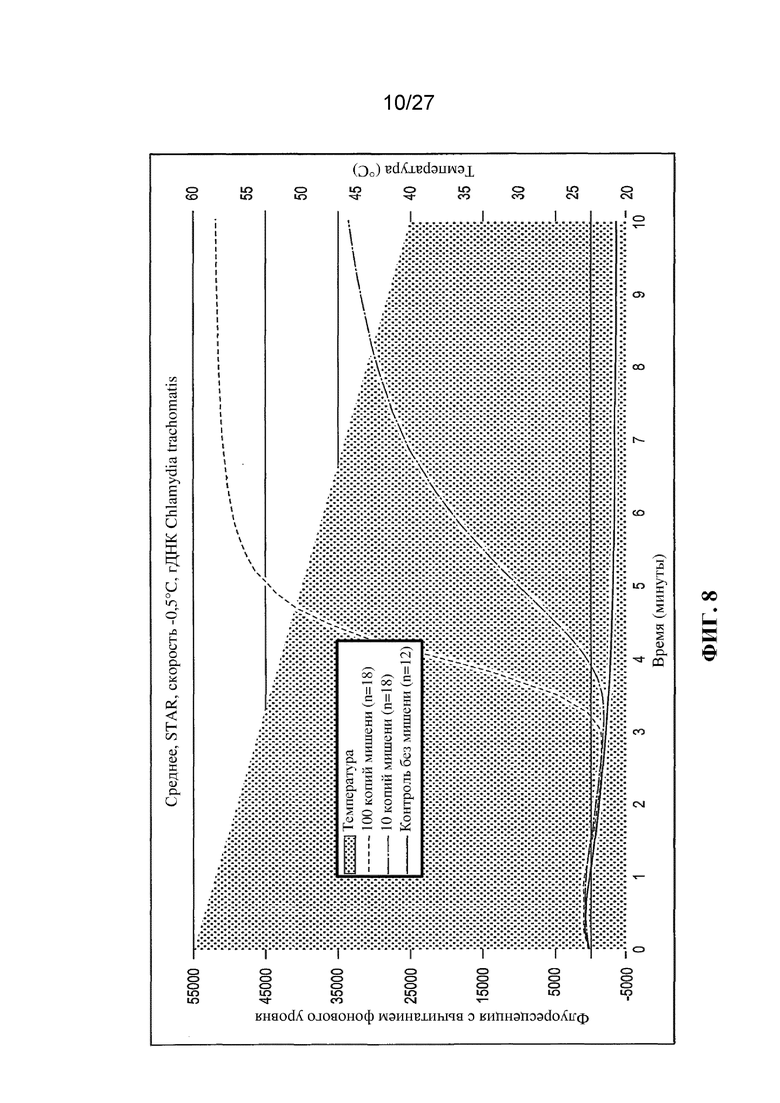
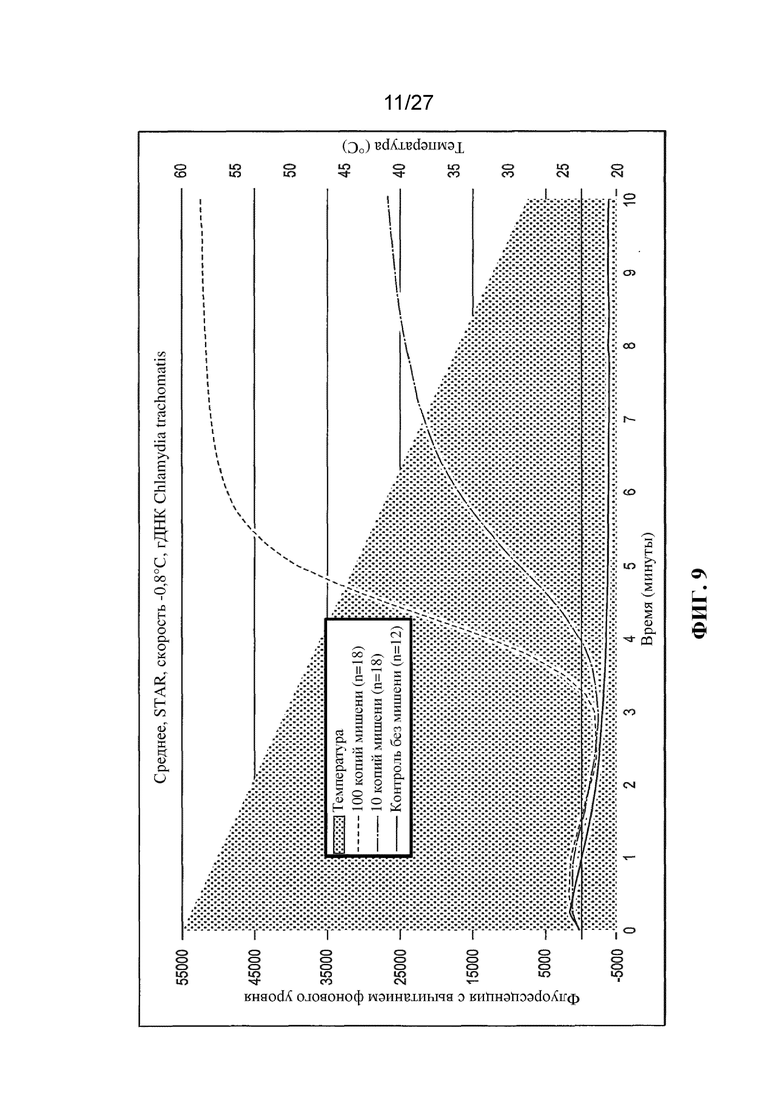
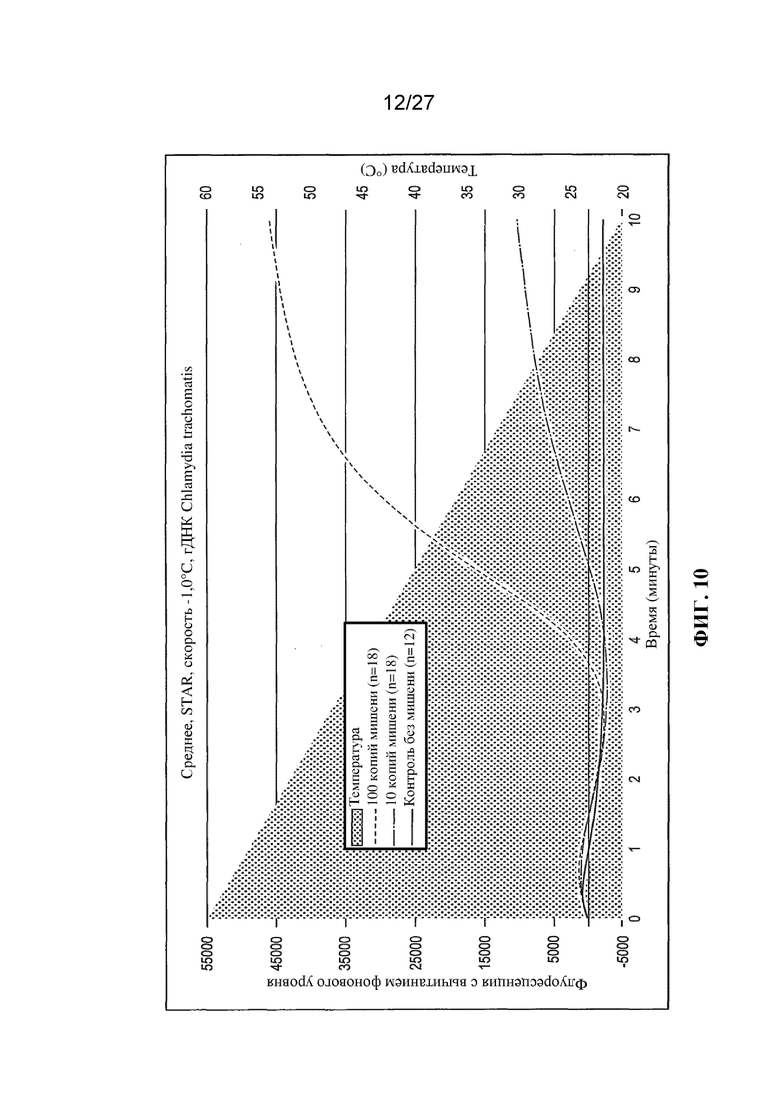
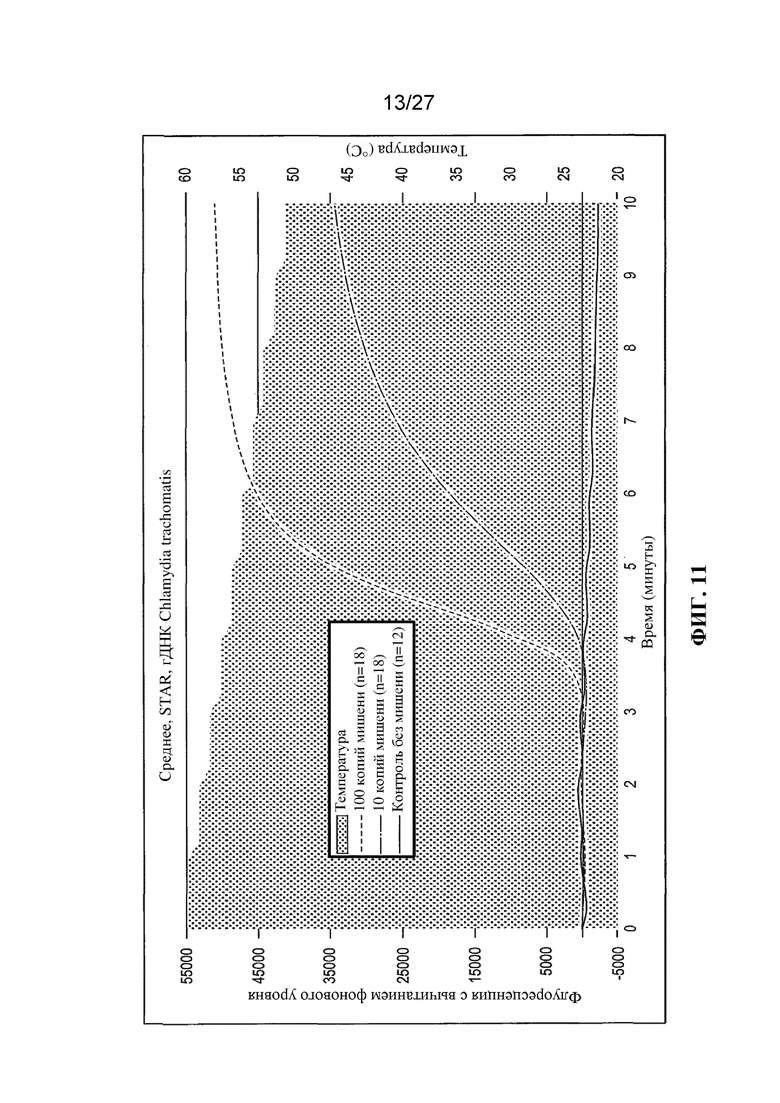
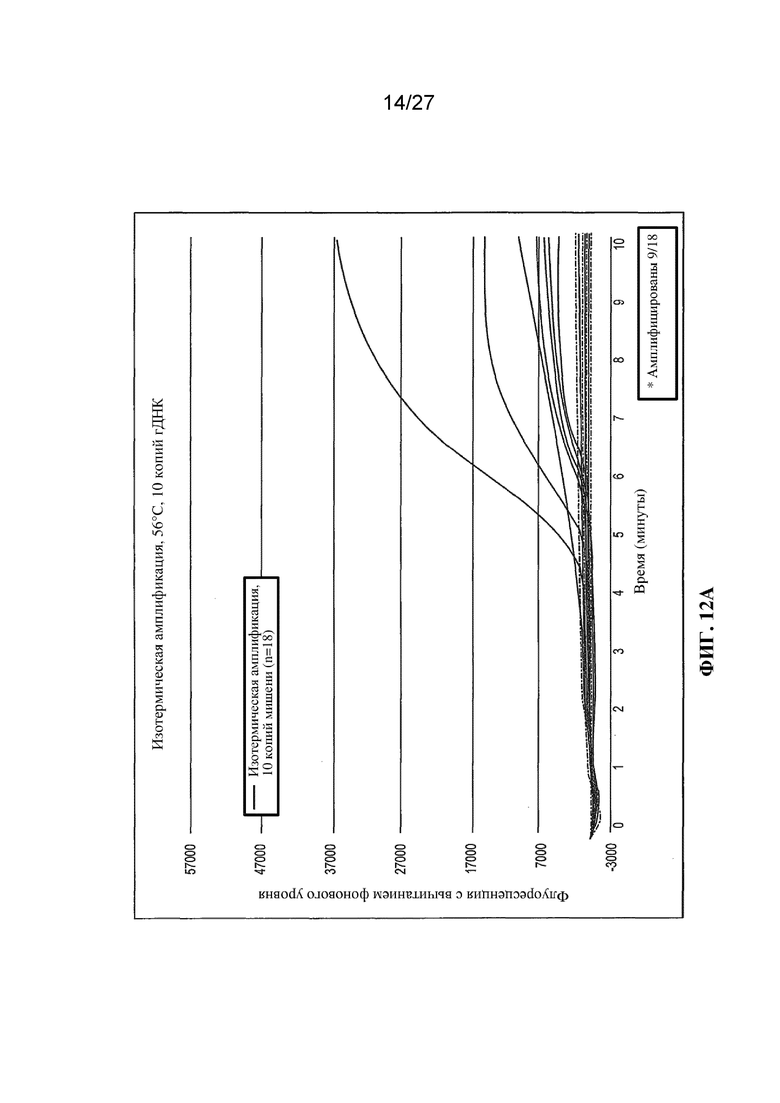
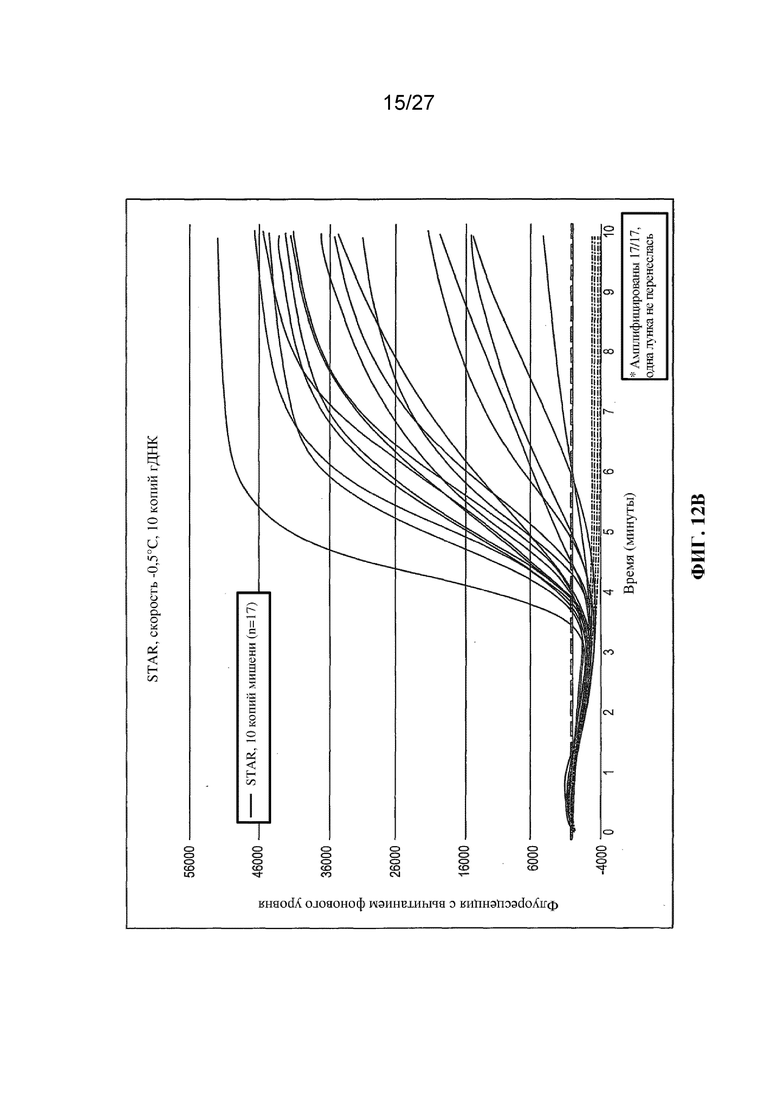
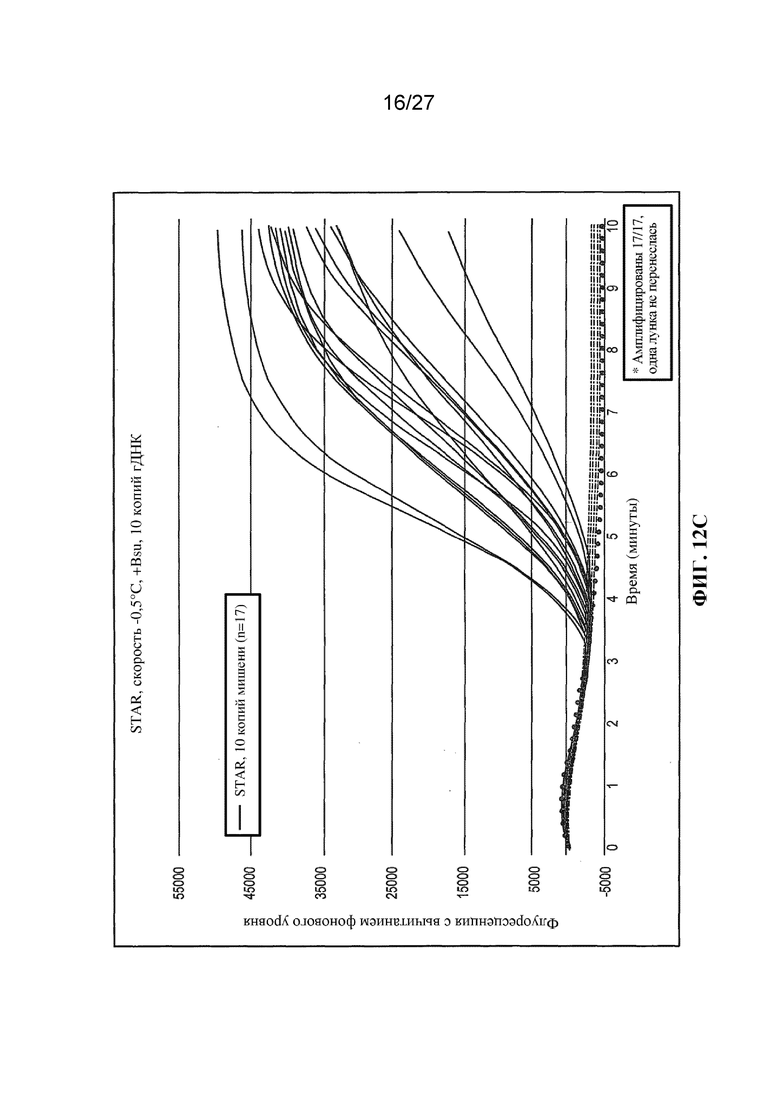
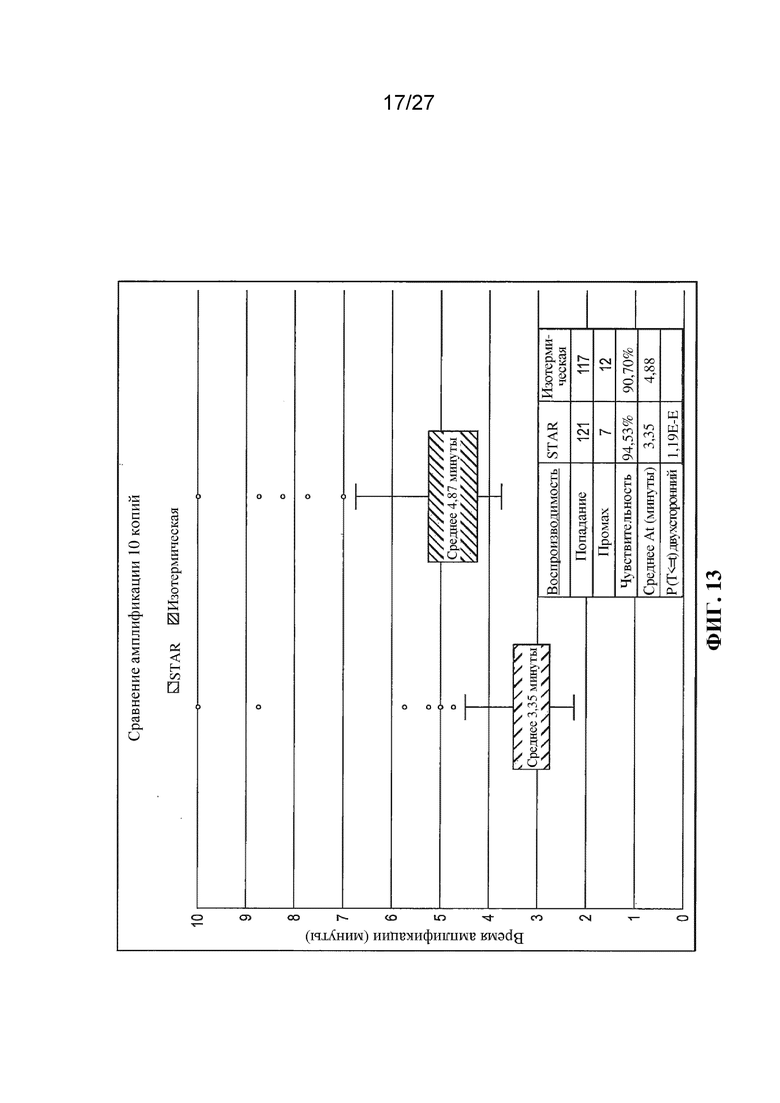
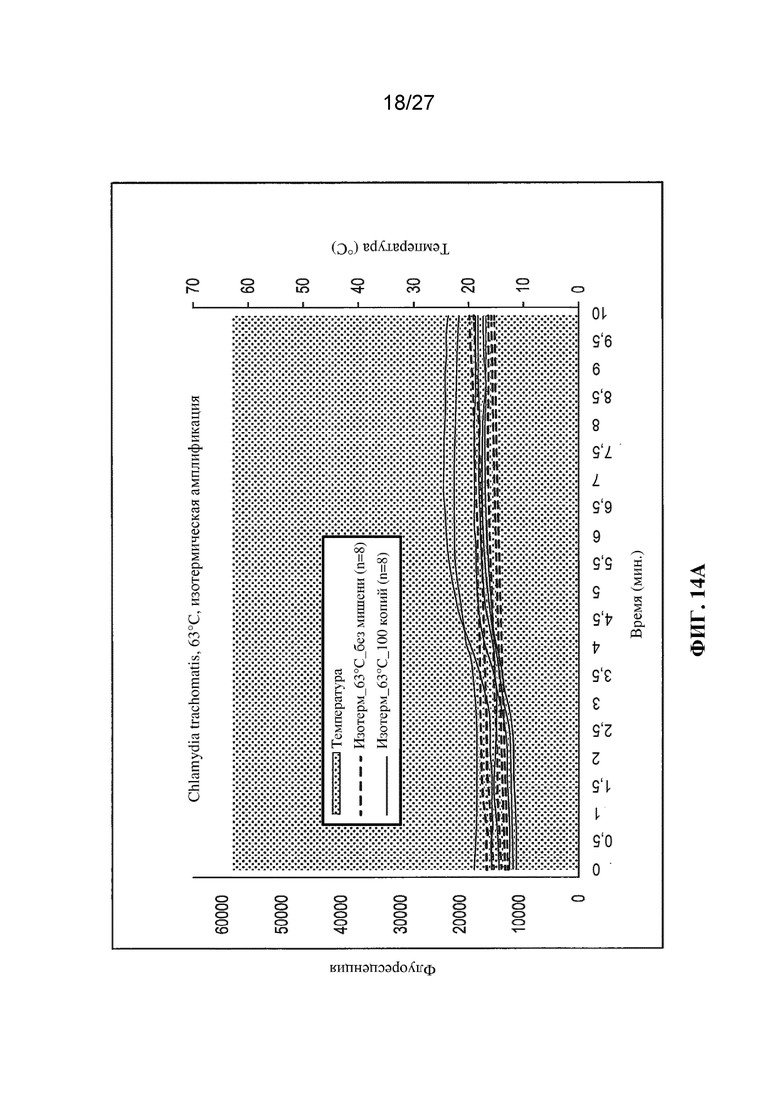
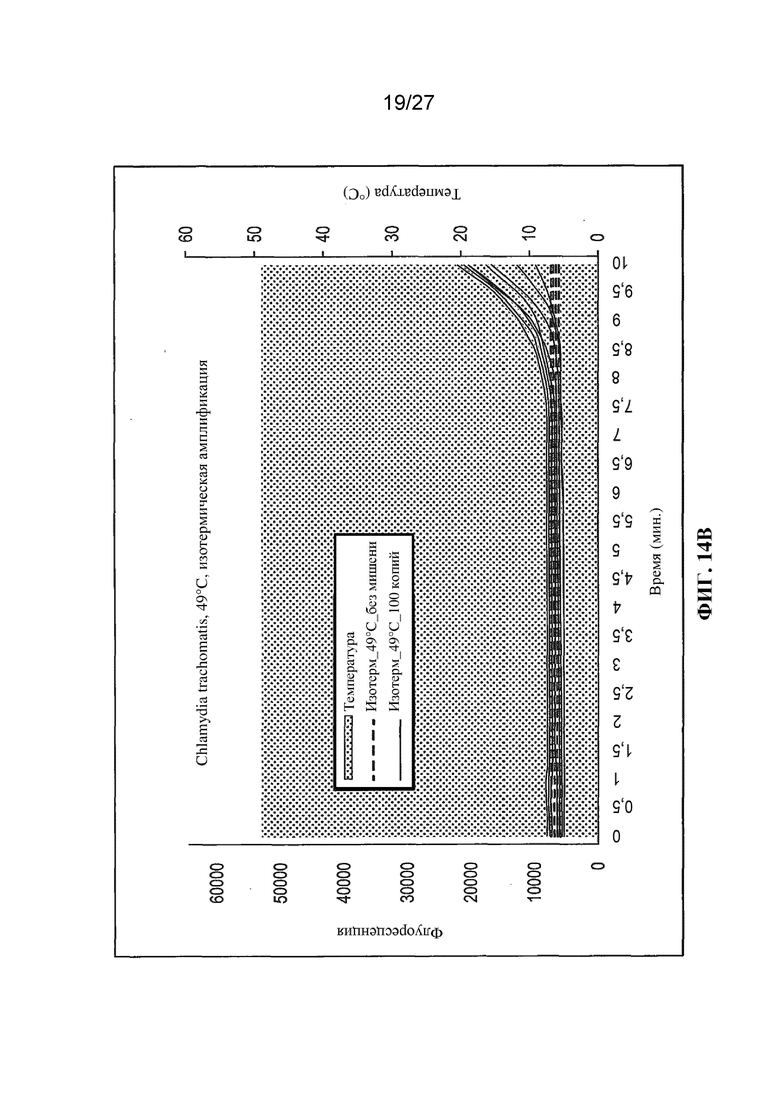
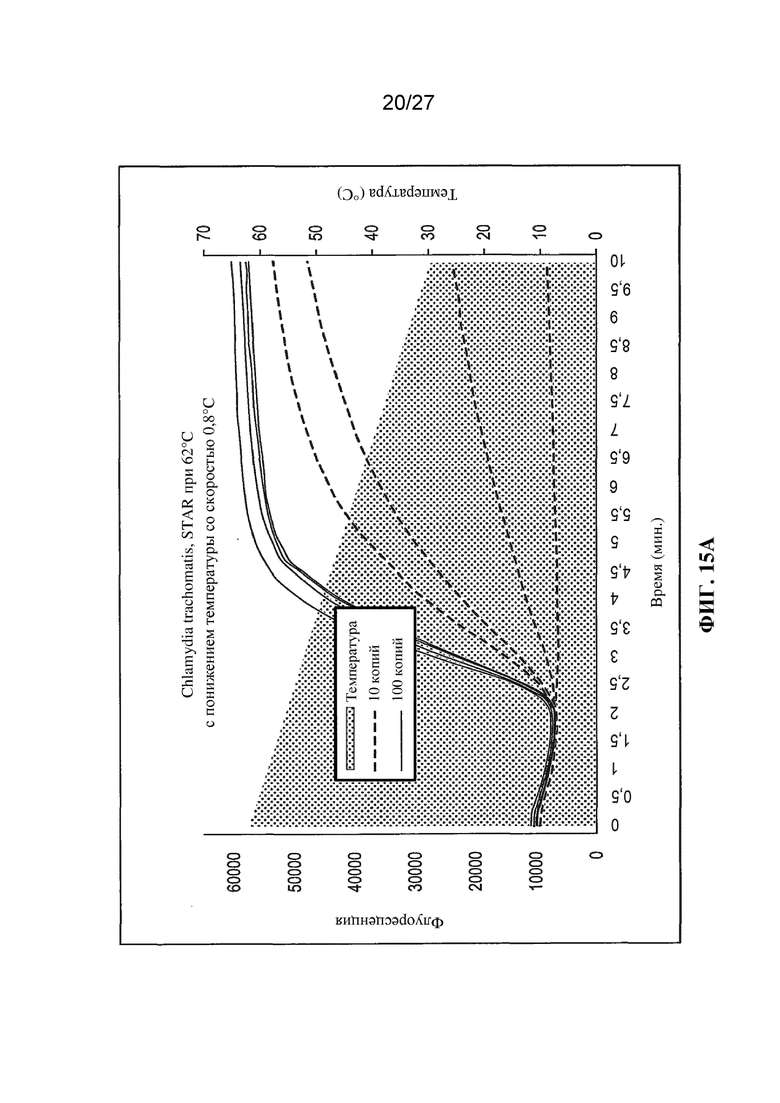
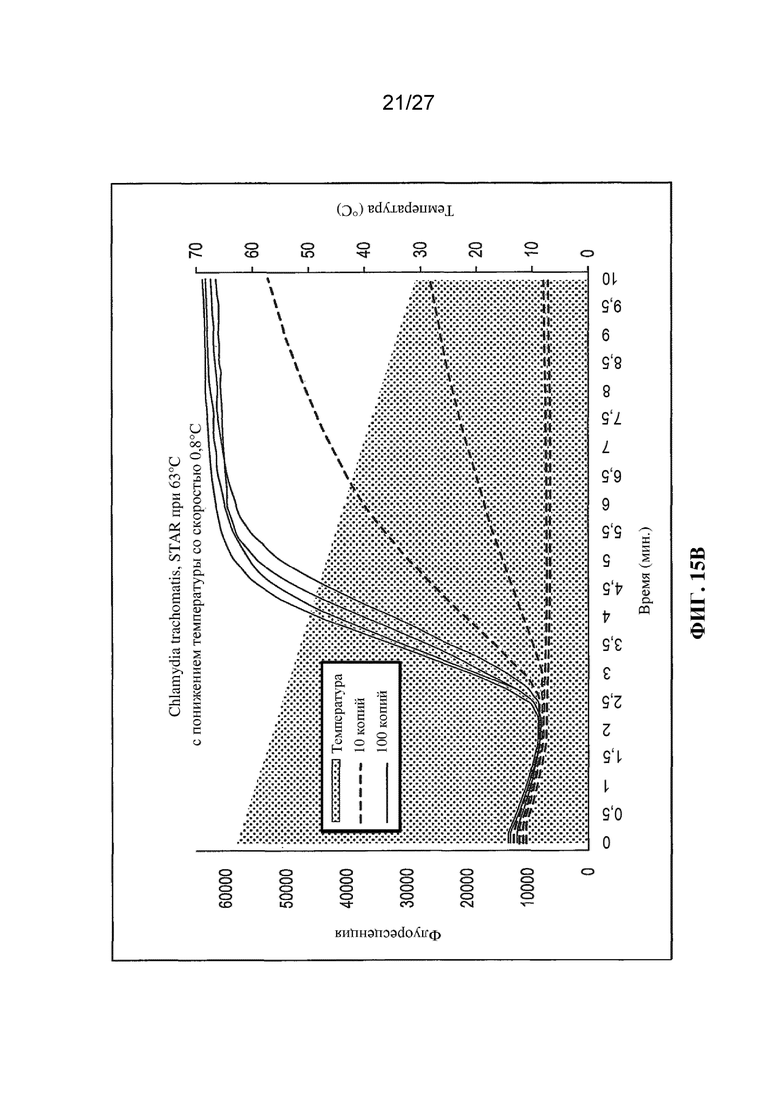
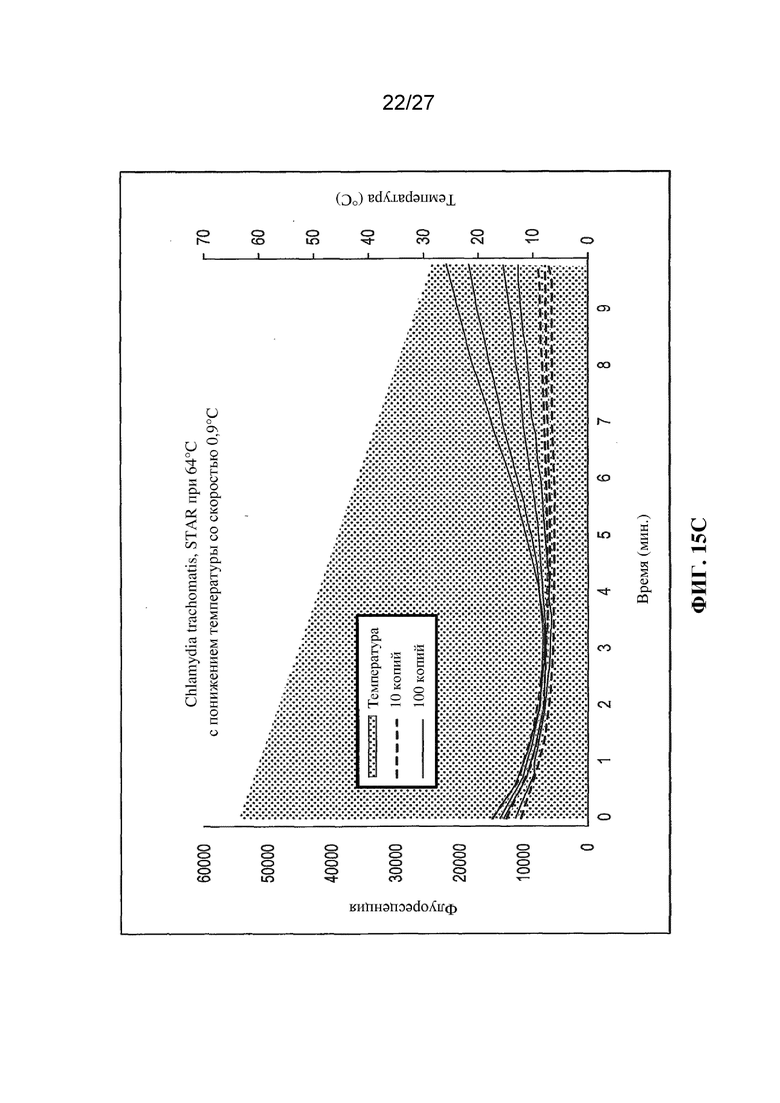
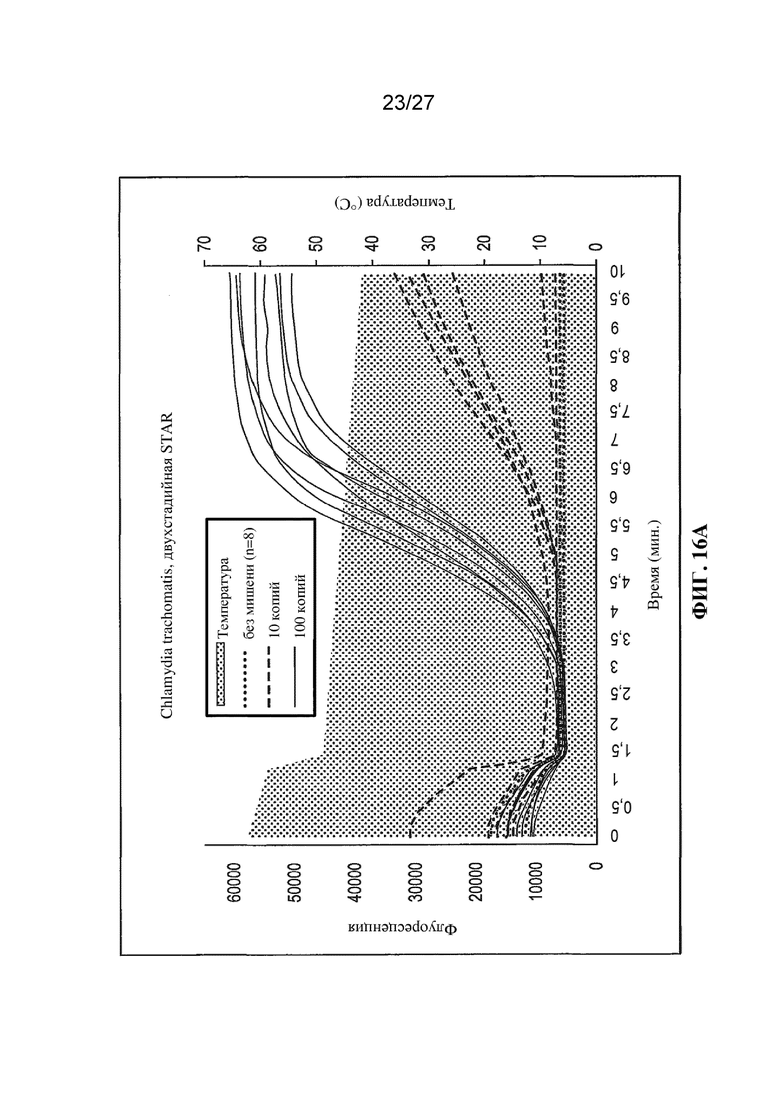
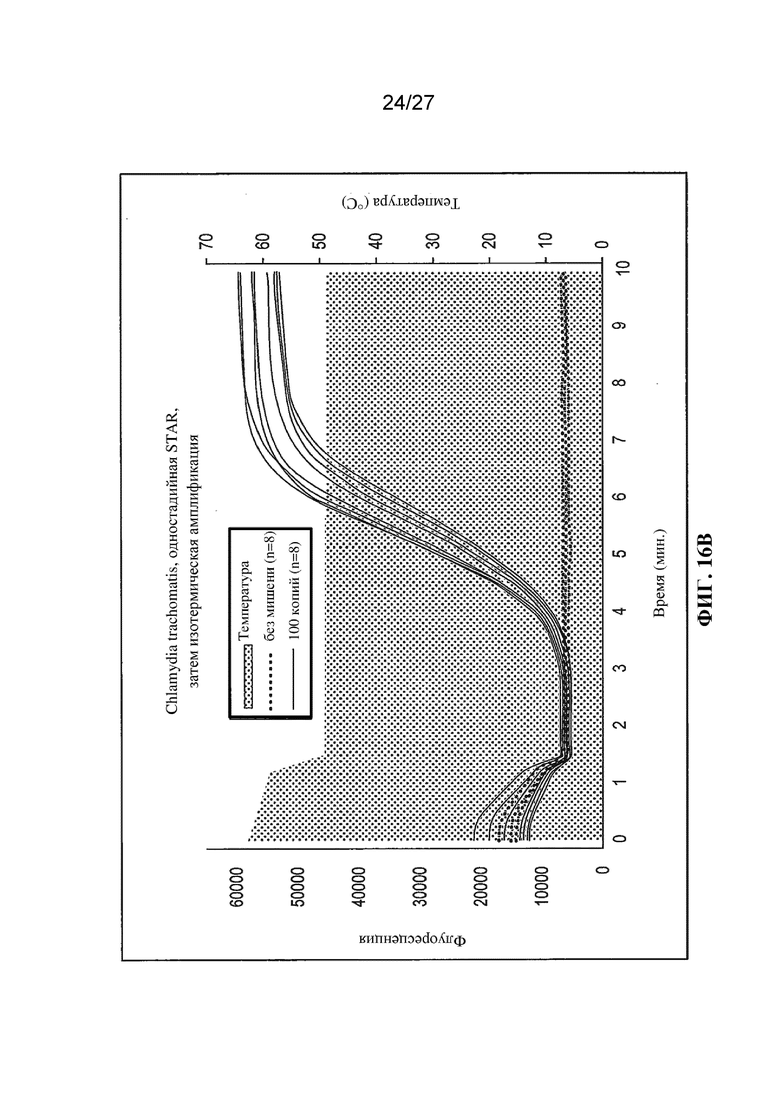
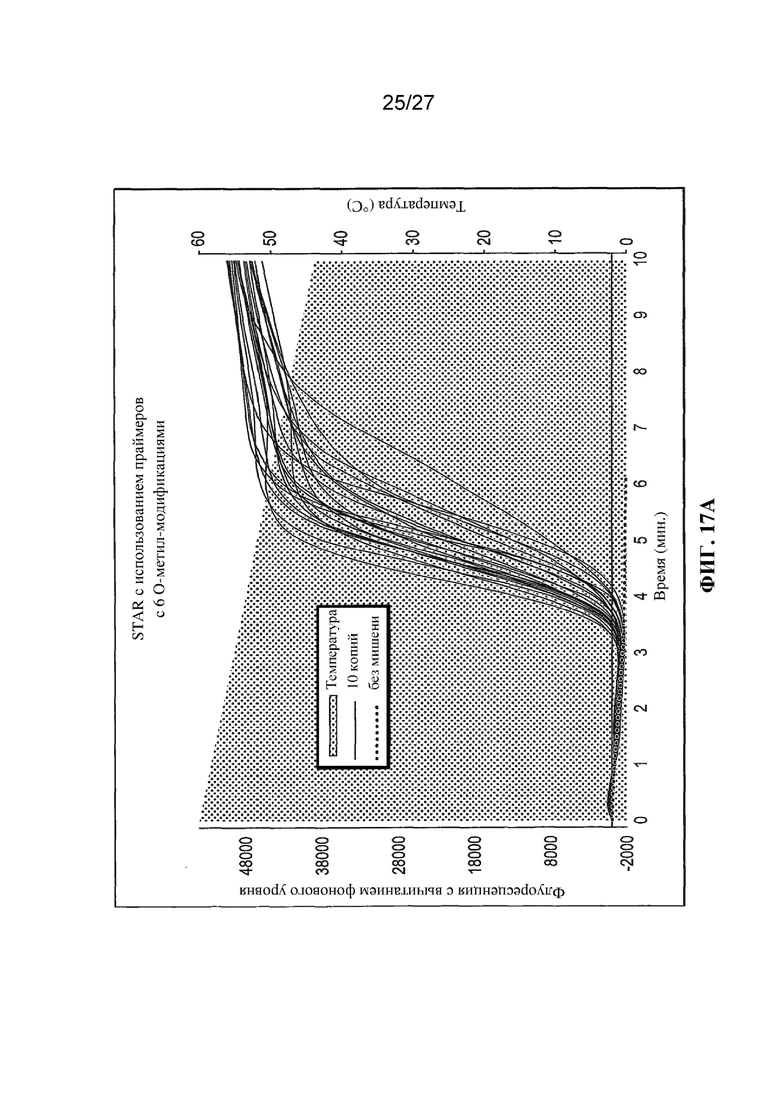
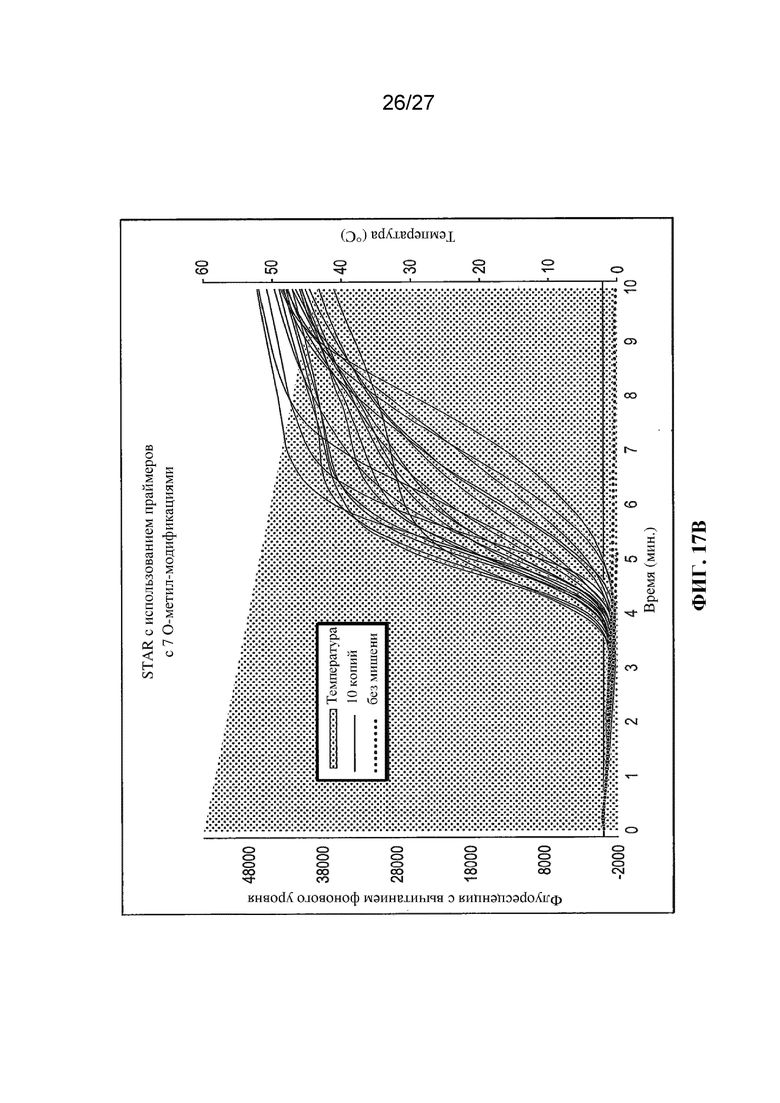
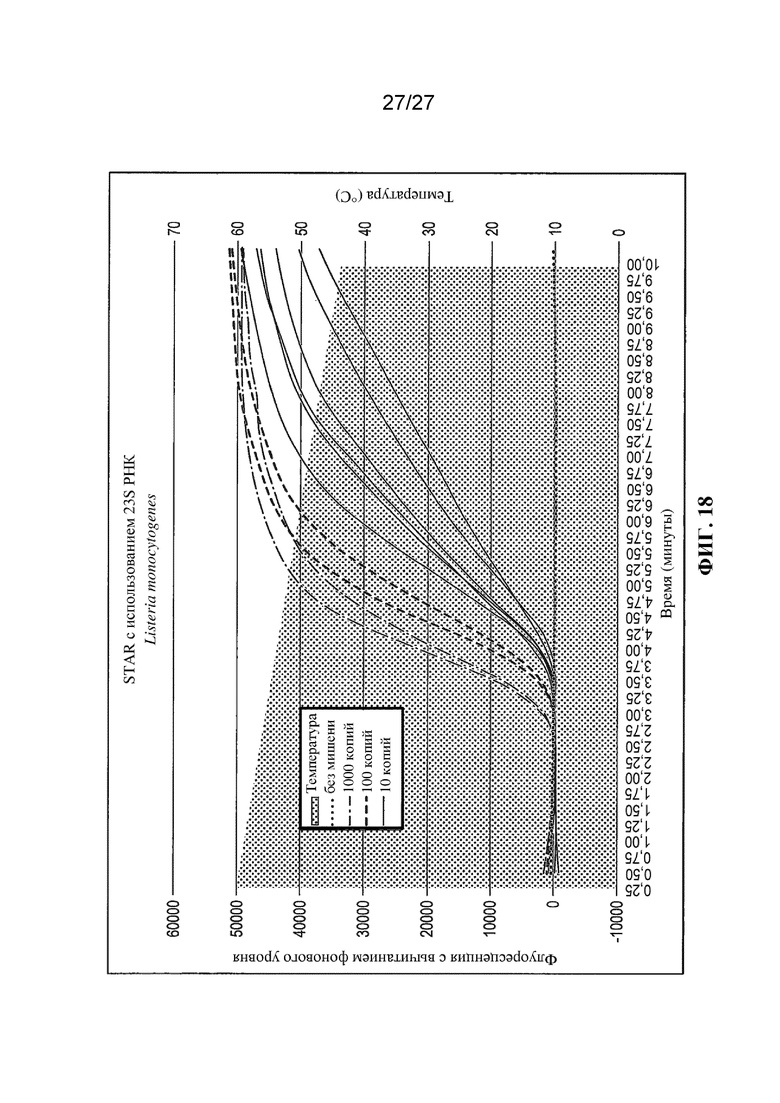
Изобретение относится к области биотехнологии. Раскрыт способ осуществления неизотермической реакции амплификации нуклеиновой кислоты. Способ включает смешивание последовательности-мишени с праймерами, их гибридизацию с образованием дуплекса, содержащего два сайта образования разрыва, расположенных на противоположных концах дуплекса или возле них, и амплификацию. В процессе амплификации происходит создание разрыва в каждом сайте образования разрыва, элонгация содержащих разрыв нитей с образованием вновь синтезированной нуклеиновой кислоты и восстановлением сайтов образования разрыва и повторение, при необходимости, этих стадий для получения множественных копий вновь синтезированной нуклеиновой кислоты. Температуру, при которой осуществляют способ, подвергают снижению в диапазоне 2-40°C во время процесса амплификации, причем не происходит возвращение к температуре, при которой осуществляют стадию гибридизации. Также предложено устройство для осуществления указанного способа. Изобретение обеспечивает повышение производительности способа амплификации. 2 н. и 28 з.п. ф-лы, 28 ил., 7 табл., 9 пр.
1. Способ осуществления неизотермической реакции амплификации нуклеиновой кислоты, причем способ предусматривает стадии:
(a) смешивания последовательности-мишени с одним или несколькими комплементарными однонитевыми праймерами в условиях, которые способствуют событию гибридизации, при котором праймеры гибридизируются с мишенью, при этом событие гибридизации напрямую или опосредованно приводит к образованию дуплексной структуры, содержащей два сайта образования разрыва, расположенных на противоположных концах дуплекса или возле них; и осуществления процесса амплификации за счет;
(b) создания разрыва в каждом из указанных сайтов образования разрыва в нитях дуплекса;
(c) применения полимеразы для элонгации содержащих разрыв нитей таким образом, чтобы образовывалась вновь синтезированная нуклеиновая кислота, при этом элонгация с помощью полимеразы восстанавливает сайты образования разрыва;
(d) повторения, при необходимости, стадий (b) и (c) таким образом, чтобы привести к получению множественных копий вновь синтезированной нуклеиновой кислоты;
при этом он отличается тем, что температура, при которой осуществляют способ, является неизотермической и ее подвергают снижению в диапазоне 2-40°C во время стадий (b)-(d) процесса амплификации,
и где температура реакции во время стадий (b)-(d) не возвращается к температуре, при которой осуществляют стадию (a).
2. Способ по п. 1, где на стадии (a) мишень содержит две комплементарные нити нуклеиновой кислоты, а праймер предусматривает прямой и обратный праймеры, каждый из которых является комплементарным соответствующей нити мишени, вследствие чего 3'-концы прямого и обратного праймеров ориентированы в направлении друг друга.
3. Способ по п. 1 или 2, где температуру подвергают контролируемому снижению, составляющему по меньшей мере 5°C, предпочтительно по меньшей мере 10°C, более предпочтительно по меньшей мере 15°C, во время реакции амплификации.
4. Способ по любому из предыдущих пунктов, где средняя скорость снижения температуры во время реакции амплификации находится в диапазоне от 0,10 до 6,0°C мин-1, предпочтительно от 0,20 до 3,5°C мин-1, более предпочтительно от 0,30 до 3,5°C мин-1 и наиболее предпочтительно от 0,40 до 3,5°C мин-1.
5. Способ по любому из предыдущих пунктов, где стадии (b)-(d) осуществляют практически немедленно после стадии (a) и где стадии (a)-(d) предпочтительно осуществляют в одном и том же реакционном сосуде или на одной и той же твердой подложке.
6. Способ по любому из предыдущих пунктов, где стадию (a) осуществляют при температуре в диапазоне 55-62°C, предпочтительно 57-61°C, более предпочтительно 58-60°C.
7. Способ по любому из предыдущих пунктов, дополнительно предусматривающий стадию выявления напрямую или опосредованно вновь синтезированной нуклеиновой кислоты.
8. Способ по п. 7, где указанная стадия выявления предусматривает применение молекулярного маяка или флуоресцентного красителя, меченого зонда для иммунохроматографического анализа или фермента, который катализирует электрохимическую реакцию.
9. Способ по любому из предыдущих пунктов, где стадия (b) предусматривает применение никующей эндонуклеазы.
10. Способ по любому из предыдущих пунктов, предусматривающий применение первой полимеразы и/или первой никующей эндонуклеазы, характеризующихся оптимальной температурой, и второй полимеразы и/или второй никующей эндонуклеазы, характеризующихся оптимальной температурой, где оптимальная температура второй полимеразы и/или второй никующей эндонуклеазы ниже, чем оптимальная температура соответствующих первой полимеразы и/или первой никующей эндонуклеазы.
11. Способ по п. 10, где вторая полимераза представляет собой полимеразу Bsu или фрагмент Кленова ДНК-полимеразы.
12. Способ по п. 10, где начальная температура реакции амплификации находится на уровне оптимальной температуры первой никующей эндонуклеазы или выше нее, и температуру снижают в ходе реакции амплификации до температуры ниже оптимальной температуры первой никующей эндонуклеазы.
13. Способ по пп. 10, 11 или 12, где температуру реакции амплификации снижают до оптимальной температуры второй полимеразы и/или второй никующей эндонуклеазы или ниже нее.
14. Способ по любому из предыдущих пунктов, дополнительно предусматривающий стадию приведения смеси, полученной с помощью осуществления способа, в контакт с термолабильным ферментом, который разрушает нуклеиновую кислоту, при этом смесь приводят в контакт с термолабильным ферментом при температуре, при которой термолабильный фермент является в значительной степени активным.
15. Способ по п. 14, где фермент представляет собой урацил-ДНК-гликозилазу (UDG) трески или антарктическую термолабильную UDG.
16. Способ по любому из предыдущих пунктов, где стадии (a) предшествует осуществление стадии обратной транскрипции, предусматривающей приведение представляющего интерес аналита РНК в контакт с обратной транскриптазой таким образом, чтобы образовывался ДНК-транскрипт представляющего интерес аналита РНК.
17. Способ по п. 16, дополнительно предусматривающий стадию образования двухнитевой ДНК из ДНК-транскрипта.
18. Способ по любому из предыдущих пунктов, дополнительно предусматривающий стадию предамплификации или обогащения.
19. Способ по любому из предыдущих пунктов, где один или несколько праймеров содержат модифицированный нуклеотид.
20. Способ по п. 19, где модифицированный нуклеотид находится в участке праймера, комплементарном мишени.
21. Способ по п. 19 или 20, где один или несколько праймеров содержат 2'-модифицированный нуклеотид.
22. Способ по любому из пп. 19-21, где один или несколько праймеров содержат 2'-O-метил-модифицированный нуклеотид.
23. Способ по п. 22, где один или несколько праймеров содержат несколько 2'-O-метил-модифицированных нуклеотидов.
24. Способ по п. 23, где один или несколько праймеров содержат до семи 2'-O-метил-модифицированных нуклеотидов.
25. Способ по любому из предыдущих пунктов, в котором температура реакции не возвращается к заранее определенной температуре.
26. Способ по любому из предыдущих пунктов, где один или несколько праймеров содержат самокомплементарный участок.
27. Способ по п. 26, где самокомплементарный участок образует шпилечную структуру.
28. Способ по п. 27, где шпилька содержит от 5 до 10 пар оснований.
29. Способ по любому из предыдущих пунктов, где величина снижения температуры во время стадий (b)-(d) находится в диапазоне 8-20°C.
30. Устройство для осуществления способа по любому из предыдущих пунктов, причем устройство содержит программируемые средства контроля и средства регуляции температуры, при этом программируемые средства контроля программируют таким образом, чтобы управлять средствами регуляции температуры для осуществления снижения температуры в диапазоне 2-40°C во время процесса амплификации реакционной смеси, применяемой для осуществления способа.
| US 2009017453 A1, 15.01.2009 | |||
| WANG DE-GUO et al | |||
| Two Methods for Increased Specificity and Sensitivity in Loop-Mediated Isothermal Amplification, Molecules, 2015, vol.20, pp.6048-6059 | |||
| WO 2011030145 A1, 17.03.2011 | |||
| JONEJA ARIC, HUANG XIAOHUA | |||
| Linear nicking endonuclease-mediated strand-displacement DNA amplification | |||
| Analytical biochemistry, |
Авторы
Даты
2021-12-01—Публикация
2017-06-30—Подача