Изобретение относится к области биотехнологии, а именно к диагностическим методам, позволяющим диагностировать развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С.
Из уровня техники известен способ определения риска развития гепатоцеллюлярной карциномы, описанный в патенте «Применение микроРНК (микрорибонуклеиновой кислоты) в качестве прогностического маркера развития гепатоцеллюлярной карциномы» [CN 103616518, 25.11.2013]. Данный способ включает в себя получение образца опухолевой ткани от пациента с раком печени, выделение и определение уровня экспрессии микроРНК-1269а и методику применения данной микроРНК в качестве прогностического маркера развития гепатоцеллюлярной карциномы.
Недостатком данного метода является, во-первых, включение в список одной молекулы микроРНК, во-вторых, использование в качестве аналита для исследования только опухолевой ткани, полученной после резекции печени, и, в-третьих, отсутствие указаний о заболевании гепатитом С в анамнезе у пациентов, среди которых планируется применение теста. Другим недостатком метода является использование в качестве показателя риска развития гепатоцеллюлярной карциномы уровня экспрессии свободных микроРНК, которые в сравнении с экзосомальными микроРНК в более значительной степени подвержены изменениям на фоне воздействия различных внешних стимулов (диета, эмоциональное возбуждение, физическая активность и проч.), что может отрицательным образом сказываться на воспроизводимости результатов теста. В свою очередь, гепатит С или цирроз печени, резвившийся вследствие инфицирования вирусом гепатита С или иной этиологии, могут изменять уровень экспрессии микроРНК и таким образом влиять на результаты исследования, что требует дополнительных указаний для интерпретации полученных результатов исследования, которые не приведены в данном методе.
Помимо этого, известен способ диагностики первичной гепатоцеллюлярной карциномы на основе панели нескольких микроРНК «Применение комбинации нескольких молекул микроРНК для диагностики первичной гепатоцеллюлярной карциномы» [CN 104293914, 5.09.2014]. Метод включает в себя забор биологического материала от пациента, выделение микроРНК и определение профиля уровней экспрессии в плазме 8 микроРНК в качестве диагностического маркера ранней стадии гепатоцеллюлярной карциномы: микроРНК-206, микроРНК-141-3р, микроРНК-433-3р, микроРНК-1228-5р, микроРНК-199а-5р, микроРНК-122-5р, микроРНК-192-5р и микроРНК-26а-5р. Основным недостатком метода является применение уровней экспрессии свободных микроРНК, воспроизводимость которых ниже воспроизводимости экзосомальных микроРНК.
Наиболее близким аналогом по отношению к предлагаемому изобретению является способ диагностики гепатоцеллюлярной карциномы при помощи анализа экзосомальной микро-РНК в плазме крови [US 20110223607 A1, 15.09.2011], включающий стадии забора биологического материала (описана периферическая венозная кровь), выделение экзосом из полученного материала, выделение из экзосом микроРНК и определение уровней экспрессии микроРНК, выбранной из группы микроРНК-16, микроРНК-195 и микроРНК-199а в образце, и диагностику гепатоцеллюлярной карциномы путем сравнения полученных значений содержания микроРНК с референсными значениями. Экзосомальные микроРНК выделяют из плазмы крови, полученной путем центрифугирования образца цельной крови (в способе предлагается использование любой биологической жидкости, фактически в описании фигурирует плазма периферической венозной крови).
Способ имеет следующие недостатки: требует проведения инвазивной процедуры забора крови с дальнейшим немедленным (в течение часа после забора) центрифугированием. Описанная в патенте технология также не указывает, как следует выделять наряду с экзосомальной фракцией микроРНК свободные молекулы микроРНК, которые служат дополнительным источником информации по развитию злокачественного процесса. Наряду с этим не указаны показатели уровней экспрессии данных микроРНК в группе пациентов с циррозом печени вследствие перенесенного гепатита С.
Техническим результатом заявленного способа является возможность диагностики гепатоцеллюлярной карциномы среди пациентов с циррозом печени вследствие перенесенного гепатита С по изменению профиля уровней экспрессии следующих микроРНК в плазме крови или слюне: микроРНК-let-7а, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246.
Результат достигается за счет того, что заявленный способ включает следующие стадии: забор материала (слюна или кровь); выделение из одного образца экзосом методом ультрацентрифугирования и экзосомальных микроРНК и свободных микроРНК; постановка реакции ПЦР в реальном времени с праймерами на отдельные типы микроРНК, ассоциированные с развитием гепатоцеллюлярной карциномы: микроРНК-let-7а, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246; расчет коэффициента, диагностирующего развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С по формуле (1) «Расчет коэффициента вероятности развития у пациента гепатоцеллюлярной карциномы»; диагностику развития гепатоцеллюлярной карциномы у пациента в соответствии с полученными числовыми значениями.
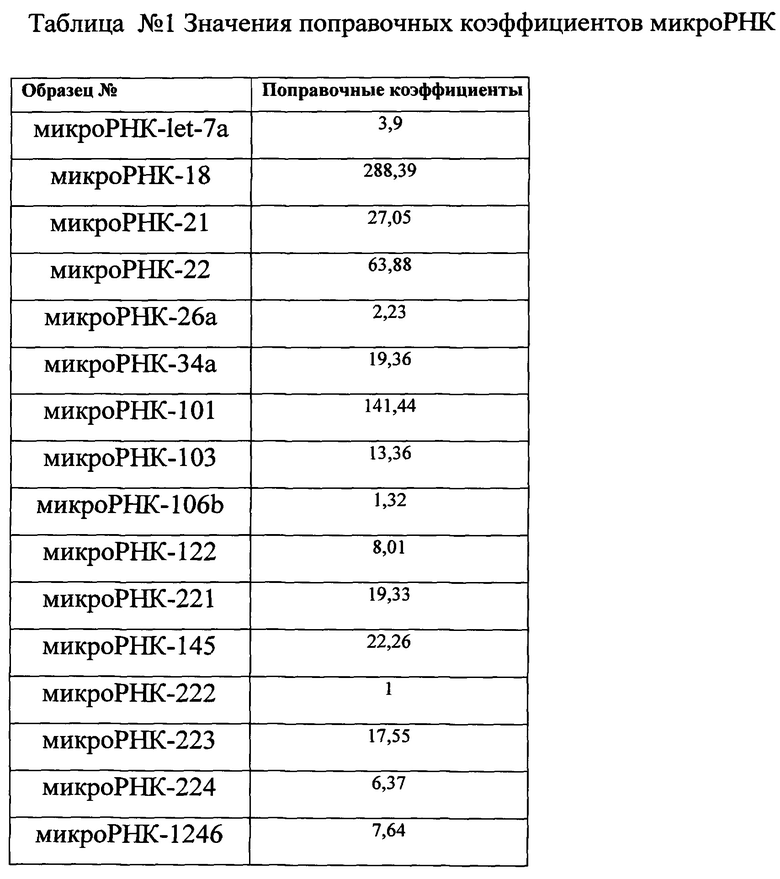
Перерасчет концентраций микроРНК, включаемый в расчет, осуществляется в соответствии с поправочными коэффициентами (см. таблицу 1)
Диагностика вероятности развития ГЦК осуществляется по цифровому показателю коэффициента R, когда R в диапазоне от 0 до 0,99 - низкий риск развития ГЦК, если показатель находится в интервале от 1 до 1,99 - средний риск развития ГЦР, если показатель выше 2 - высокая вероятность ГЦК.
Формула 1 «Расчет коэффициента вероятности развития у пациента гепатоцеллюлярной карциномы», описывающая способ расчета коэффициента, в соответствии с которым возможно диагностировать развитие гепатоцеллюлярной карциномы у пациентов с гепатитом С в анамнезе.  (1)
(1)
Табл. 1 «Значения поправочных коэффициентов микроРНК», содержащая в себе значение поправочных коэффициентов для каждой микроРНК.
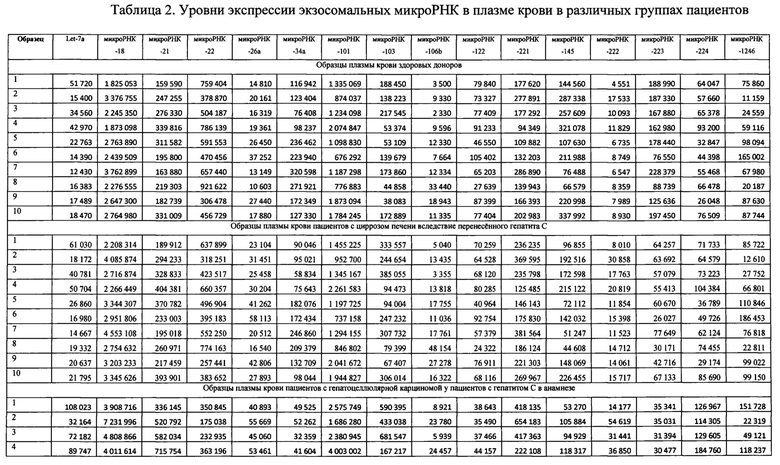
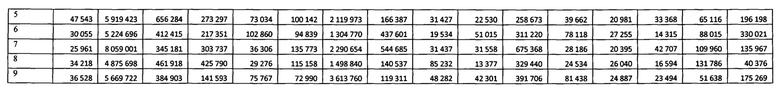
Табл. 2 «Уровни экспрессии экзосомальных микроРНК в плазме крови в различных группах пациентов», содержащая в себе значения уровней экспрессии экзосомальных микроРНК в плазме крови здоровых доноров, пациентов с циррозом печени вследствие перенесенного гепатита С и пациентов с гепатоцеллюлярной карциномой с гепатитом С в анамнезе.
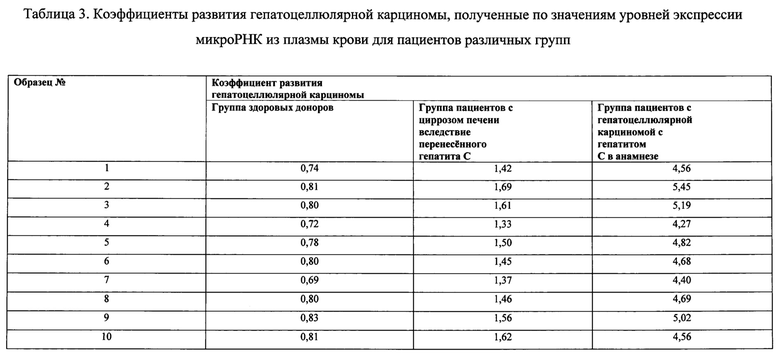
Табл. 3 «Коэффициенты развития гепатоцеллюлярной карциномы, полученные по значениям уровней экспрессии микроРНК из плазмы крови для пациентов различных групп», содержащая в себе числовые коэффициента вероятности развития гепатоцеллюлярной карциномы у здоровых доноров, пациентов с циррозом печени вследствие перенесенного гепатита С и пациентов с гепатоцеллюлярной карциномой с гепатитом С в анамнезе.
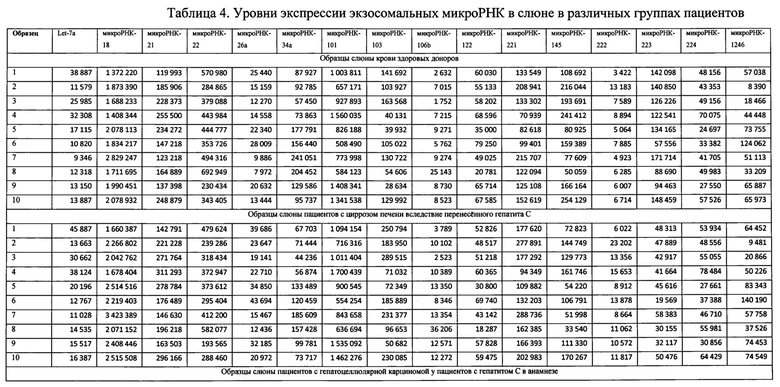
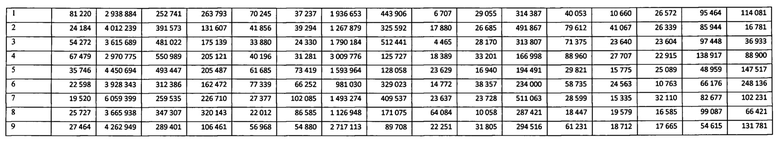
Табл. 4 «Уровни экспрессии экзосомальных микроРНК в слюне в различных группах пациентов», содержащая в себе значения уровней экспрессии экзосомальных микроРНК в плазме крови здоровых доноров, пациентов с циррозом печени вследствие перенесенного гепатита С и пациентов с гепатоцеллюлярной карциномой с гепатитом С в анамнезе.
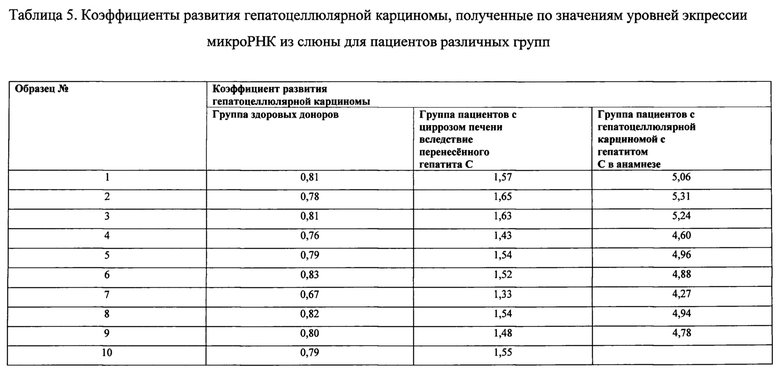
Табл. 5 «Коэффициенты развития гепатоцеллюлярной карциномы, полученные по значениям уровней экспрессии микроРНК из слюны для пациентов различных групп», содержащая в себе числовые коэффициента вероятности развития гепатоцеллюлярной карциномы у здоровых доноров, пациентов с циррозом печени вследствие перенесенного гепатита С и пациентов с гепатоцеллюлярной карциномой с гепатитом С в анамнезе.
Заявляемый способ может быть проиллюстрирован следующими примерами.
Пример 1. Определение уровней экспрессии микроРНК в плазме крови различных групп пациентов и у здоровых доноров
У 10 здоровых доноров (возраст 35-55 лет, 5 мужчин, 5 женщин) в амбулаторных условиях производят забор 2 мл крови в пробирку ЭДТА К2 (забор возможен в любую пробирку, где в качестве антикоагулянта используется ЭДТА). Кровь в течение 2 часов после забора центрифугирует в течение 10 минут на 3000 g, отбирают в чистую пробирку плазму, готовят несколько аликвот по 250 мкл и замораживают при -80°С. Аналогичным образом производят забор материала у 10 пациентов (6 мужчин, 4 женщины, возраст 35-55 лет) с циррозом печени вследствие перенесенного гепатита С и у 9 пациентов с гепатоцеллюлярной карциномой (5 мужчин, 4 женщины, возраст 45-55 лет).
Затем следует этап выделения экзосомальной фракции микроРНК, для чего необходимы следующие действия: 1) проведение центрифугирования в режиме 2000 g в течение 20 минут при комнатной температуре и отбирают супернатант; 2) проведение центрифугирования в режиме 10000 g в течение 30 минут при комнатной температуре и отбирают супернатант; 3) проведение ультрацентрифугирования на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000 g в течение 2-х часов при +4С.
Далее приступают к выделению свободных микроРНК: к надосадочной жидкости, образовавшейся на последнем (третьем) этапе выделения экзосом, добавляют 5 мкл протеиназы К, инкубируют при 56°С в течение 1 часа, далее проводят выделение миркоРНК на наборах "miRNeasy serum/plasma advanced kit" (Qiagen Q-217004) по стандартному протоколу: наносят на колонку Exiqon, после чего проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, потом на колонку наносится 20 мкл безнуклеазной воды и колонку оставляют на 10 минут при комнатной температуре, затем проводят центрифугирование при 3000 g на центрифуге eppendorf 5104 в течение 10 минут при комнатной температуре, после чего проводят реакцию обратной транскрипции при помощи набора для обратной транскрипции "miRCURY LNA RT Kit" (Qiagen-339340) по стандартному протоколу.
Для выделения фракции экзосомальных микроРНК полученный на последнем (третьем) этапе выделения экзосом осадок разводят в 100 мкл безнуклеазной воды. К полученному раствору добавляют 5 мкл протеиназы К, инкубируют при 56°С в течение 1 часа, далее проводят выделение миркоРНК на наборах "miRNeasy serum/plasma advanced kit" (Qiagen Q-217004) по стандартному протоколу: наносят на колонку Exiqon, после чего проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, потом на колонку наносится 20 мкл безнуклеазной воды и колонку оставляют на 10 минут при комнатной температуре, затем проводят центрифугирование при 3000 g на центрифуге eppendorf 5104 в течение 10 минут при комнатной температуре, после чего проводят реакцию обратной транскрипции при помощи набора для обратной транскрипции "miRCURY LNA RT Kit" (Qiagen-339340) по стандартному протоколу.
Далее с целью выявления отдельных типов микроРНК проводят полимеразную цепную реакцию с детекцией в режиме реального времени с использованием наборов "meRCURY LNA SYBR Green PCR kit" (Qiagen-339347) на приборе 7500 Applied Biosystems с праймерами на отдельные типы микроРНК, ассоциированные с развитием гепатоцеллюлярной карциномы: микроPHK-let-7a, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246.
Затем при помощи программного обеспечения, поставляемого производителем оборудования (GenEx 6.1 - qPCR Data Analysis Software, bioMCC, 29.02.2016), вычисляют количество каждой из исследуемых микроРНК, выделенной из каждой фракции, полученные данные приводятся в формате таблицы.
Затем проводят расчет поправочных коэфициентов для каждой микроРНК. Значения поправочных коэффициентов отображены в табл.№1.
Расчет коэффициента, отражающего развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С происходит по формуле 1, приведенной выше.
Значения уровней экспрессии экзосомальных микроРНК отражены в табл. №2.
Полученные коэффициенты отражены в табл. №3
Пример 2. Определение уровней экспрессии микроРНК в слюне различных групп пациентов и здоровых доноров.
У 10 здоровых доноров (возраст 35-55 лет, 5 мужчин, 5 женщин) в амбулаторных условиях производят забор слюны следующим образом: ватную палочку держат в ротовой полости в течение 45-60 с в районе выхода протоков поднижнечелюстной слюнной железы, после чего палочку вытаскивают и помещают в чистый бумажный конверт. Аналогичным образом производят забор материала у 10 пациентов (6 мужчин, 4 женщины, возраст 35-55 лет) с циррозом печени вследствие перенесенного гепатита С и у 9 пациентов с гепатоцеллюлярной карциномой (5 мужчин, 4 женщины, возраст 45-55 лет).
Затем следует этап выделения экзосомальной фракции микроРНК, для чего необходимы следующие действия: 1) ватную палочку извлекают из контейнера, помещают в физиологический раствор объем 500 мкл на 1 час; 2) проводят центрифугирование в режиме 2000 g в течение 20 минут при комнатной температуре и отбирают супернатант; 3) проводят центрифугирование в режиме 10000 g в течение 30 минут при комнатной температуре и отбирают супернатант; 4) проводят ультрацентрифугирование на центрифуге Avanti 301 (ротор JA-30.50) в режиме 100000 g в течение 2-х часов при +4С.
Далее приступают к выделению свободных микроРНК: к надосадочной жидкости, образовавшейся на последнем (четвертом) этапе выделения экзосом, добавляют 5 мкл протеиназы К, инкубируют при 56°С в течение 1 часа, далее проводят выделение миркоРНК на наборах "miRNeasy serum/plasma advanced kit" (Qiagen Q-217004) по стандартному протоколу: наносят на колонку Exiqon, после чего проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, потом на колонку наносится 20 мкл безнуклеазной воды и колонку оставляют на 10 минут при комнатной температуре, затем проводят центрифугирование при 3000 g на центрифуге eppendorf 5104 в течение 10 минут при комнатной температуре, после чего проводят реакцию обратной транскрипции при помощи набора для обратной транскрипции "miRCURY LNA RT Kit" (Qiagen-339340) по стандартному протоколу.
Для выделения фракции экзосомальных микроРНК полученный на последнем (четвертом) этапе выделения экзосом осадок разводят в 100 мкл безнуклеазной воды. К полученному раствору добавляют 5 мкл протеиназы К, инкубируют при 56°С в течение 1 часа, далее проводят выделение миркоРНК на наборах "miRNeasy serum/plasma advanced kit" (Qiagen Q-217004) по стандартному протоколу: наносят на колонку Exiqon, после чего проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, затем колонку промывают 3 раза промывочным буфером, после каждого промывания проводят центрифугирование при 2000 g на центрифуге eppendorf 5104 в течение 5 минут при комнатной температуре, потом на колонку наносится 20 мкл безнуклеазной воды и колонку оставляют на 10 минут при комнатной температуре, затем проводят центрифугирование при 3000 g на центрифуге eppendorf 5104 в течение 10 минут при комнатной температуре, после чего проводят реакцию обратной транскрипции при помощи набора для обратной транскрипции "miRCURY LNA RT Kit" (Qiagen-339340) по стандартному протоколу.
Далее с целью выявления отдельных типов микроРНК проводят полимеразную цепную реакцию с детекцией в режиме реального времени с использованием наборов "meRCURY LNA SYBR Green PCR kit" (Qiagen-339347) на приборе 7500 Applied Biosystems с праймерами на отдельные типы микроРНК, ассоциированные с развитием гепатоцеллюлярной карциномы: микроPHK-let-7a, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246.
Затем при помощи программного обеспечения, поставляемого производителем оборудования (GenEx 6.1 - qPCR Data Analysis Software, bioMCC, 29.02.2016), вычисляют количество каждой из исследуемых микроРНК, выделенной из каждой фракции, полученные данные приводятся в формате таблицы.
Расчет коэффициента, отражающего развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С происходит по формуле 1.
Значения уровней экспрессии экзосомальных микроРНК отражены в табл. №4.
Полученные коэффициенты отражены в табл. №5
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выделения свободных и экзосомальных микроРНК из слюны | 2018 |
|
RU2729423C2 |
| Способ диагностики меланомы с помощью экзосомальных микроРНК | 2020 |
|
RU2769927C2 |
| СПОСОБ ВЫДЕЛЕНИЯ МИКРОРНК ИЗ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2013 |
|
RU2548816C1 |
| Способ диагностики атерогенных нарушений у детей при помощи циркулирующих микроРНК | 2024 |
|
RU2834937C1 |
| СПОСОБ ДИАГНОСТИКИ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2003 |
|
RU2319969C2 |
| Малоинвазивный способ дифференциальной ранней диагностики гепатоцеллюлярной карциномы и жирового гепатоза | 2023 |
|
RU2822224C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2020 |
|
RU2749117C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2019 |
|
RU2723891C1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА 1 ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2016 |
|
RU2770021C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОГО РАКА | 2012 |
|
RU2498775C1 |
Изобретение относится к области биотехнологии, а именно к диагностическим методам, позволяющим диагностировать развитие злокачественной опухоли. Способ заключается в определении коэффициента, диагностирующего развитие гепатоцеллюлярной карциномы, рассчитываемого на основании изменений профиля уровней экспрессии следующих микроРНК в плазме крови или слюне: микроPHK-let-7a, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246. Способ позволяет диагностировать гепатоцеллюлярную карциному среди пациентов с циррозом печени вследствие перенесенного гепатита С. 2 н.п. ф-лы, 6 табл., 2 пр.
1. Способ диагностики гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С, включающий следующие стадии: забор периферической венозной крови; выделение из одного образца экзосом методом ультрацентрифугирования и экзосомальных микроРНК и свободных микроРНК; постановка реакции ПЦР в реальном времени с праймерами на отдельные типы микроРНК, ассоциированные с развитием гепатоцеллюлярной карциномы: микроРНК-let-7а, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246; расчет коэффициента, диагностирующего развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С, по формуле

где R - коэффициент вероятности наличия у пациента гепатоцеллюлярной карциномы,
С - значения уровня экспрессии микроРНК, в квадратных скобках указаны номера соответствующих микроРНК ([let7a] соответствует MHKpoPHK-let7a и т.д.);
и диагностика развития гепатоцеллюлярной карциномы в соответствии с полученными числовыми значениями, а именно по цифровому показателю коэффициента R: когда R в диапазоне от 0 до 0,99, низкий риск развития ГЦК, если R находится в интервале от 1 до 1,99, средний риск развития ГЦР, если R выше 2, высокая вероятность ГЦК.
2. Способ диагностики гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С, включающий следующие стадии: забор слюны; выделение из одного образца экзосом методом ультрацентрифугирования и экзосомальных микроРНК и свободных микроРНК; постановка реакции ПЦР в реальном времени с праймерами на отдельные типы микроРНК, ассоциированные с развитием гепатоцеллюлярной карциномы: микроРНК-let-7а, микроРНК-18, микроРНК-21, микроРНК-22, микроРНК-26а, микроРНК-34а, микроРНК-101, микроРНК-103, микроРНК-106b, микроРНК-122, микроРНК-221, микроРНК-145, микроРНК-222, микроРНК-223, микроРНК-224, микроРНК-1246; расчет коэффициента, диагностирующего развитие гепатоцеллюлярной карциномы у пациентов с циррозом печени вследствие перенесенного гепатита С, по формуле

где R - коэффициент вероятности наличия у пациента гепатоцеллюлярной карциномы,
С - значения уровня экспрессии микроРНК, в квадратных скобках указаны номера соответствующих микроРНК ([let7a] соответствует MHKpoPHK-let7a и т.д.);
и диагностика развития гепатоцеллюлярной карциномы в соответствии с полученными числовыми значениями, а именно по цифровому показателю коэффициента R: когда R в диапазоне от 0 до 0,99, низкий риск развития ГЦК, если R находится в интервале от 1 до 1,99, средний риск развития ГЦР, если R выше 2, высокая вероятность ГЦК.
| US 20110223607 A, 15.09.2011 | |||
| CN 104293914 A, 21.05.2015 | |||
| КАРЕВ В.Е | |||
| Клинические и иммунологические аспекты патогенеза хронической HBV и HCV инфекции, автореферат диссертации, Санкт-Петербург, 2016, весь документ. |
Авторы
Даты
2021-12-01—Публикация
2020-12-15—Подача