Предлагаемое изобретение относится к области медицины, а именно к онкологии, гастроэнтерологии и инфекционным болезням, и позволяет прогнозировать риск развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С.
Среди причин смерти онкологических больных в мире гепатоцеллюлярная карцинома (ГЦК) занимает второе место. Такой высокий показатель обусловлен поздней диагностикой заболевания, так как на ранней стадии ГЦК протекает бессимптомно и может быть выявлена уже на стадии роста опухолевого узла при проведении ультразвукового обследования печени.
Основным фактором риска развития ГЦК является инфицирование вирусами гепатитов В и С. В связи с появлением в 90-х годах вакцины против гепатита В и массовой вакцинацией населения во всех странах мире его значение как фактора риска значительно уменьшилось. Наряду с этим в оценке этиологической значимости акценты сместились в сторону гепатита С, который сегодня стал основной инфекционной причиной развития ГЦК.
Патогенез ГЦК при гепатите С предполагает в качестве первого этапа развитие цирроза печени, на фоне которого риски. возникновения ГЦК многократно увеличиваются. Так, даже после элиминации вируса в результате противовирусной терапии, у больных сохраняются риски возникновения ГЦК, которые составляют при циррозе класса А по шкале Чайлд-Пью 2,1% в год, а при классе В - 7,8% в год.
В связи с поздней обращаемостью больных за медицинской помощью и, соответственно, поздней диагностикой эффективность лечения ГЦК остается неудовлетворительной.
В этих условиях совершенствование методов раннего обнаружения ГЦК является основной задачей современного здравоохранения, позволяющей выстроить систему оказания эффективной помощи больным и снизить смертность от этого заболевания.
В соответствии с клиническими рекомендациями европейской ассоциации по изучению печени ранняя диагностика ГЦК основывается на ультразвуковом исследовании печени (УЗИ) и определении уровня альфа-фетопротеина (AFP) в крови [EASL Clinical Practice Guidelines: 2018]. УЗИ брюшной полости широко распространено в медицинских учреждениях, но его эффективность зависит от класса аппарата, опыта врача и размера опухоли. Чувствительность УЗИ достигает 90% для опухолей более 5 см в диаметре; 70% для узлов диаметром 1-2 см и только 50% при размере опухоли менее 1 см (Singal A., et al, Meta-analisis: Surveilance with ultrasound for early-stage hepatocellular carcinoma in patients with cirrhosis// Aliment Pharmacol Ther,-2009-30-37-47).
Второй диагностический компонент, AFP, представляет собой гликопротеин с молекулярной массой 70 кДа, синтезируемый эндодермальными клетками желточного мешка зародыша, а в последующем - эмбриональными гепатоцитами (Abelev G.I. Production of embryonal serum alpha-globulin by hepatomas: review of experimental and clinical data. Cancer Res. 1968; 28:1344-1350). Повышение уровня AFP в сыворотке крови наблюдается при различных онкологических заболеваниях, но в большей степени характерно для ГЦК. Анализ литературы, оценивающий AFP, как биомаркера ГЦК, показал диапазон чувствительности и специфичности на разных стадиях развития ГЦК 26-65% и 80-94%) соответственно [Zhang K., 2014; Shu Н., 2017]. В связи с низкой чувствительностью в последних версиях европейских и американских клинических рекомендаций AFP был исключен из диагностического алгоритма.
В связи с этим в последнее десятилетие во всех странах мира ведутся интенсивные поиски молекул и веществ, определение которых в биологических средах организма позволило бы на ранней стадии и с высокой степенью эффективности диагностировать ГЦК. Такие разработки ведутся в области протеомики, геномики и метаболомики. Наиболее перспективно определение белковых молекул (протеомика), так как методы индикации различных протеинов достаточно хорошо автоматизированы, имеют высокую чувствительность и воспроизводимость.
По мнению экспертов идеальный биомаркер ГЦК должен приближаться по уровню чувствительности и специфичности к 90% и быть применимым для скрининговых исследований. Кроме этого, желательно чтобы методика исследования была малоинвазивной и экономически обоснованной.
За последние время в мире для ранней диагностики ГЦК предложено несколько десятков онкомаркеров, находящихся на различных стадиях клинической апробации [Reichl Р., 2016; Sengupta S. et all., 2017; Hemken P.M. et all., 2019]. Как следует из отдельных публикаций и комплексных обзоров статей, добиться восьмидесяти процентного уровня чувствительности позволяет использование в диагностике таких специфических белков как аннексии А2 (AnnA2), гепарин-связывающий фактор роста (MDK), α-1-фукозидаза (AFU), иммунный комплекс IgM-антиген плоскоклеточного рака (SCCA-IgM). Однако, при высокой чувствительности диагностическая специфичность определения этих онкомаркеров оказалась низкой и варьирует от 50,0 до 70,5% [Reichl Р., 2016; Hodeib Н. Et all., 2017; Junna Z. et all., 2017; Liu C.H., 2018; Malov S.I., 2019]. И наоборот, высокоспецифичные (>90%) белковые маркеры: гликозилированная L-3 изоформа альфа-фетопротеина (AFP-L3), рецептор-активатор плазминогена (suPAR), дез-гамма-карбоксипротромбин (DCP) показывают низкую чувствительность от 28,0 до 76,0% [Taketa K., 1993; Chounta А., 2015; Reichl Р., 2016; Wu J. 2018; Malov S.I., 2019]. Таким образом, в настоящее время ни один онкомаркер, взятый по отдельности, не обеспечивает на ранней стадии ГЦК искомой диагностической эффективности.
По этим причинам в настоящее время основной поиск идет в направлении комбинированного применения двух, трех и даже четырех онкомаркеров с различными механизмами экспрессии в процессе канцерогенеза.
Известны комбинации, включающие AFP, AFP-L3, DCP, AnnA2, остеопонтин (OPN), диккопф-подобный протеин-1 (DKK-1), рецептор тирозинкиназы sAxl (AXL), тиоредоксин (Trx1) (см. Tsuchiya N., et al. Biomarkers for the early diagnosis of heratocellular carcinoma. World J Gastroenterol. 2015; 21(37):10573-10583. Doi:10.3748/wjg.v21.i37.10573). Это позволило повысить точность диагностики (АС) на уровне 0,8-0,87. Однако, н указанные исследования были выполнены с использованием неоднородных по этиологическому фактору клинических групп (чаще всего этиология ГЦК включала вирусный гепатит В, вирусный гепатит С и алкогольный гепатит). Кроме этого, в исследования включались пациенты, находящиеся на разных стадиях болезни. Очевидно, что присутствие в анализируемых группах больных с продвинутой стадией (III-IV стадия по классификации TNM) не позволяет оценить значение маркера именно для ранней диагностики ГЦК (I-II стадия по классификации TNM). Тем более, что при размере опухолевого узла более 2,0 см достаточно эффективны инструментальные методы диагностики (УЗИ, КТ, МРТ) и необходимость применения сывороточных онкомаркеров отпадает.
Известен способ диагностики ГЦК, основанный на определении белка глипикана-3 (GPC-3) в сыворотке крови и печени (Патент РФ №2319969, 2005), который показывает улучшенную специфичность в неинвазивной диагностике ГЦК. При высокой специфичности, данный способ позволяет диагностировать ГЦК только у половины больных. При этом в примере не приводится клиническая характеристика больных ГЦК, поэтому нет данных о стадировании больных по распространенности онкологического процесса.
В дальнейшем, с целью повышения диагностической чувствительности было предложено комбинированное использование GPC-3 с другими маркерами ГЦК: AFP, AFP-L3, DCP [Jia X., 2014; A. A. Ghweil et al., 2018; Cerban R., 2019; Shimzu Y, 2019; Liu S., 2020]. Это позволило повысить чувствительность диагностики до 76,0-90,4% на промежуточной и поздней стадии заболевания (стадия B-C-D по шкале BCLC), но оказалось недостаточно эффективным для ранней стадии (стадия А по шкале BCLC) 72,0-76,4%.
Наиболее близким является способ, в котором используется комбинация AFP и GPC-3. АФП является наиболее изученным биомаркером ГЦК. Но уровень AFP зависит от размера опухоли, что затрудняет его использование для диагностики раковых образований небольшого размера. Поэтому авторами способа в диагностический набор дополнительно включен GPC-3, обладающий высокой специфичностью. GPC-3 продуцируют только клетки гепатоцеллюлярной карциномы и его повышение в крови не зависит от распространенности опухолевого процесса и наблюдается даже при небольших размерах узла (Ghweil А.А., Khodery A.,Tag-Adeen М., El-Sayed М., Shahat K., Abdelrazek G. Role of serum Glypican-3 in the diagnosis of hepatocellular carcinoma in the upper Egypt.// Open Journal of Gastroentrrology.2018; 8, 415-423.). Однако, указанная комбинация онкомаркеров имеет существенный диагностический недостаток, проявляющийся в низкой чувствительности (72%). Другими словами, данная комбинация позволяет заподозрить развитие ГЦК среди больных с разной стадией развития болезни (в прототипе: от очень ранней до терминальной) менее чем у 2/3 пациентов. Если взять когорту больных ГЦК только с ранней стадией болезни (I-II стадия по классификации TNM) чувствительность оказывается еще ниже - 69,1%, что оказывает свое негативное влияние и на показатель диагностической точности (80%) (табл. 3).
Техническим результатом предлагаемого способа является повышение чувствительности и точности прогнозирования риска развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С.
Новым является то, что определяют совокупность показателей уровня альфа-фетопротеина, глипикана-3 и остепонтина в венозной крови, при этом предварительно рассчитывают пороговое значение для каждого онкомаркера, сопоставляют полученные показатели по каждому онкомаркеру с его пороговым значением и прогнозируют риск развития заболевания.
Новым является также и то, что при уровне трех определяемых онкомаркеров меньше или равном пороговому значению риск развития гепатоцеллюлярной карциномы отсутствует; при превышении порогового значения одного из онкомаркеров риск развития заболевания низкий; при превышении порогового значения двух онкомаркеров риск развития заболевания высокий; при превышении порогового значения трех определяемых онкомаркеров прогнозируют абсолютный риск развития гепатоцеллюлярной карциномы.
Отличием в предлагаемом способе является то, что для определения риска развития ГЦК, кроме AFP и GPC-3, используется еще один дополнительный онкомаркер - остеопонтин (OPN), что обеспечивает высокую чувствительность. Кроме этого прогноз осуществляется не суммированием показателей по каждому онкомаркеру, как в прототипе, а путем использования определенного алгоритма, что обеспечивает более высокую точность определения. При таком подходе у больных на ранней стадии ГЦК (I-II по классификации TNM) чувствительность метода составляет 89,1%), специфичность - 90,9%, диагностическая точность - 90,0%.
Достоинством предложенного способа является использование белковых онкомаркеров - альфа-фетопротеина (AFP), глипикана-3 (GPC-3) и остеопонтина (OPN), комбинация которых обладает значительно более высокой чувствительностью и диагностической точностью (АС), чем комбинация AFP+GPC-3. Уровень в крови трех предложенных онкомаркеров не коррелирует между собой, соответственно, каждый белок вносит свой самостоятельный вклад в обеспечение прогностической эффективности. Важным компонентом является включение в комбинацию онкомаркеров остеопонтина, диагностическая чувствительность которого, в отличие от AFP и GPC-3, значительно выше и поэтому он эффективен на ранней стадии канцерогенеза. Недостаточная специфичность OPN компенсируется включением высокоспецифичных для ГЦК онкомаркеров AFP и GPC-3. Тест-наборы для определения указанных онкомаркеров широко представлены на рынке лабораторных реактивов, доступны. Оборудование для их определения в соответствии с табелем оснащения имеется не только в специализированных медицинских учреждениях онкологического профиля, но и в районных больницах общего профиля. Кроме этого существенно упрощена трактовка результата: учитывается количество положительных проб из трех возможных.
Для сравнения обоих способов были обследованы 55 больных хроническим гепатитом С в стадии цирроза печени, у которых при диспансерном наблюдении в течение 1 года была выявлена гепатоцеллюлярная карцинома и 55 больных хроническим гепатитом С в стадии цирроза печени, у которых при диспансеризации в течение 1 года не обнаружено развитие гепатоцеллюлярной карциномы. Диагноз ХГС устанавливали на основании данных анамнеза, клинического обследования, определения активности печеночных трансаминаз, выявлении анти-HCV IgG и РНК HCV. Степень фиброза печени определяли с помощью аппарата FibroScan-502. Диагноз ГЦК устанавливался с учетом критериев европейской ассоциации по изучению болезней печени (EASL). Больные наблюдались и лечились в ГБУЗ «Областная клиническая инфекционная больница (г.Иркутск), «Областного клинический консультативно-диагностический центр» (г.Иркутск), «Областной онкологический диспансер» (г. Иркутск). У всех больных диагноз был верифицирован морфологически. У 10 больных (18,2%) заболевание было выявлено на I стадии болезни по классификации TNM, у 45 (81,8%) - на II стадии. Для лабораторных исследований использовались пробы крови, полученные до проведения оперативного лечения или процедуры локальной деструкции опухоли. Группу сравнения составили 55 больных ХГС в стадии цирроза печени, у которых через 6-12 месяцев после взятия крови были выполнены УЗИ печени, мультифазная контрастная компьютерная томография и/или динамическая контрастная магнитно-резонансная томография и не было обнаружено объемного образования печени и изменений сосудистой васкуляризации характерной для ГЦК. После забора крови все образцы сыворотки центрифугировали и хранили при -80 С. Информированное согласие было получено от каждого участника исследования, а проведение настоящей работы было одобрено комитетом по этике Иркутского государственного медицинского университета. Статистическую обработку материалов проводили с использованием программы Meta Disc 1.4 Software, которая находится в открытом доступе по ссылке: https://meta-disc.software.informer.com/1.4/.
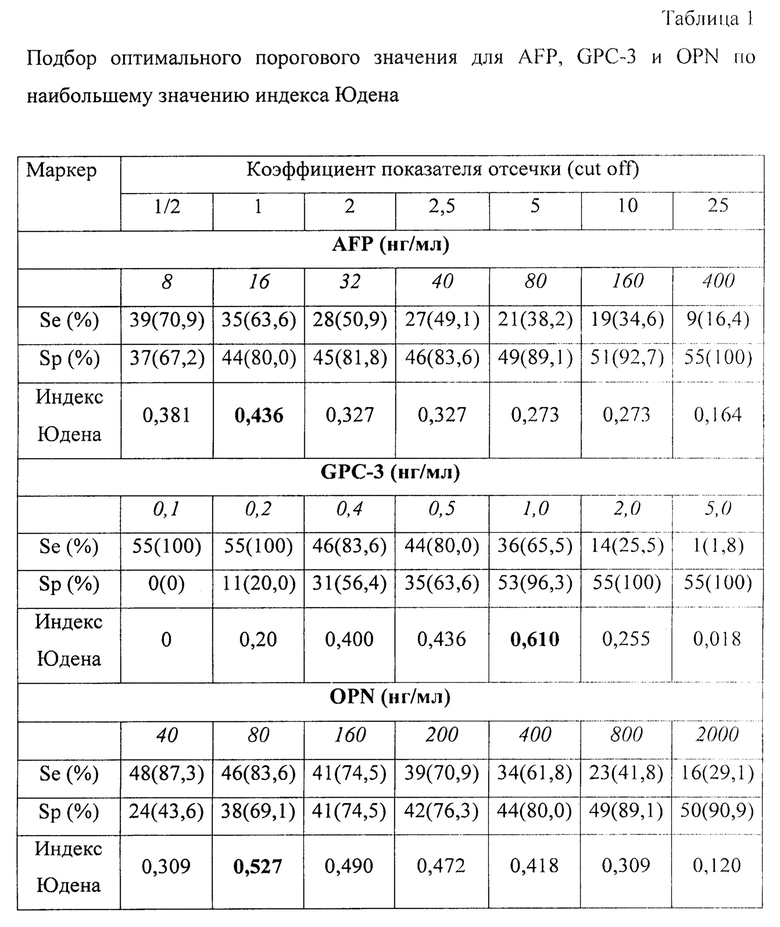
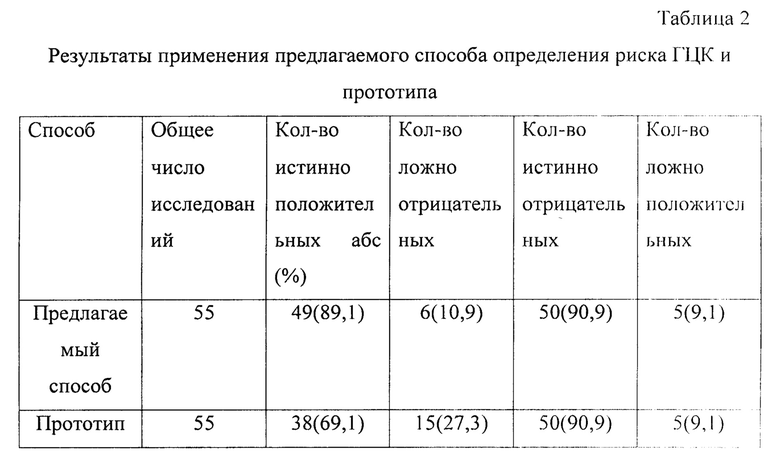
Авторы осуществляли определение порогового значения для каждого онкомаркера путем расчета наибольшего значения индекса Юдена(Приложение к заявке, таблица 1) и выявили, что пороговое значение для альфа-фетопротеина соответствует 16,0 нг/мл; для остеопонтина - 80,0 нг/мл, а для глипикана-3 - это 1,0 нг/мл. Оценивали такие показатели как диагностическая чувствительность (Se), специфичность (Sp), положительное прогностическое значение (PPV), отрицательное прогностическое значение (NPV) и отношение правдоподобия положительного результата (PLR). Для выявления достоверности различий показателей в сравниваемых группах применяли непараметрические критерии статистики (хи-квадрат (χ2)). Уровень статистической значимости был принят при р≤0,05. Результаты сравнения двух способов приведены в таблице (см. Приложение к заявке, таблица 2,3).
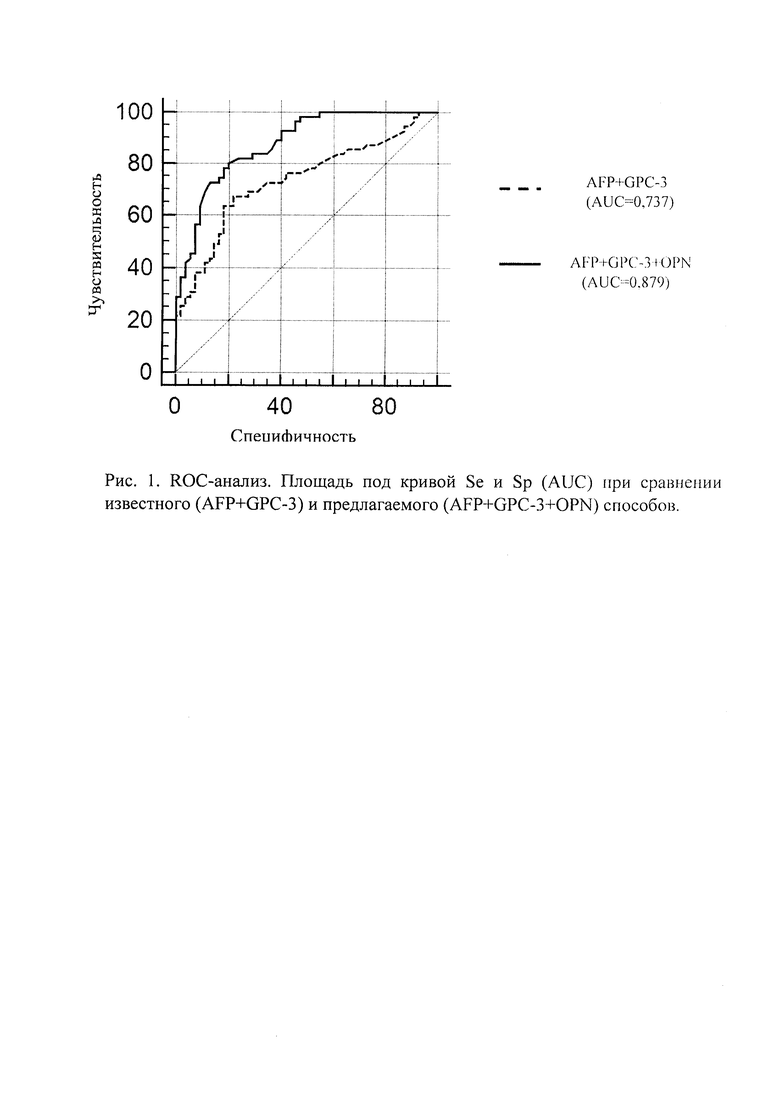
Предлагаемый способ имеет чувствительность (Se) 89,1%, специфичность (Sp) - 90,9%. Статистически достоверно чувствительность предлагаемого способа выше чувствительности известного способа (р=0,0099), что также подтверждается более высоким показателем отрицательного прогностического значения (р=0,007). Отношение правдоподобия положительного результата (PLR) предлагаемого способа выше, чем у известного способа. Это означает, что вероятность положительного теста у больных хроническим гепатитом С в 9,79 раз выше, чем у здоровых лиц, что свидетельствует о высокой точности определения риска ГЦК (Приложение, таблица 3). Проведение ROC-анализа показало, что площадь под кривой AUC (эффективность диагностики) при использовании предлагаемого способы существенно больше, чем при использовании известного метода (AUC 0,879 ДИ:0,802-0,933; р<0,001 и AUC 0,737 ДИ:0,644-0,816; р<0,001) (Приложение, рис. 1).
Сравнительный анализ предлагаемого способа и прототипа показывает, что предлагаемый способ отличается от известного тем, что определяют совокупность показателей уровня альфа-фетопротеина, глипикана-3 и остепонтина в венозной крови, при этом предварительно рассчитывают пороговое значение для каждого онкомаркера, сопоставляют полученные показатели по каждому онкомаркеру с его пороговым значением и прогнозируют риск развития заболевания по следующему алгоритму: при уровне трех определяемых онкомаркеров меньше или равным пороговому значению риск развития гепатоцеллюлярной карциномы отсутствует; при превышении порогового значения одного из онкомаркеров риск развития заболевания низкий; при превышении порогового значения двух онкомаркеров риск развития заболевания высокий; при превышении порогового значения трех определяемых онкомаркеров прогнозируют абсолютный риск развития гепатоцеллюлярной карциномы, что соответствует критерию «новизна».
Предлагаемый способ повышает чувствительность и точность определения риска развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С. Высокая чувствительность предлагаемого способа позволяет выявить максимальное количество пациентов, у которых возможен риск развития ГЦК. Способ отличается простотой выполнения и доступностью, так как для лабораторий доступны коммерческие диагностические наборы для определения указанных онкомаркеров, а оборудование для иммуноферментного анализа входит в табель оснащения медицинских учреждений, начиная с уровня центральной районной больницы.
Таким образом, данный способ может быть применен в рутинной медицинской практике и позволяет обеспечить эффективную диспансеризацию больных гепатитом С с целью оценки риска развития ГЦК. и маршрутизации больных из группы высокого риска в специализированные медицинские учреждения онкологического профиля.
Способ осуществляют следующим образом: забор венозной крови у пациента производят натощак в пробирки с антикоагулянтом (ЭДТА) для гематологического анализа в соответствии с общими правилами забора биологического материала. Для определения уровня альфа-фетопротеина используют анализатор ARCHITECT i System и набор реагентов 3Р36 ARCHITECT AFP. Чувствительность теста - 2,0 нг/мл. Для определения остеопонтина используют иммуноферментный анализатор и набор реактивов для иммуноферментного анализа "Human Osteopontin Platinum ELISA" (Affymetrix eBioscience). Чувствительность теста - 0,26 нг/мл. Для определения глипикана-3 используют иммуноферментный анализатор и набор реактивов для иммуноферментного анализа "Enzyme-linked immunosorbent assay kit for Glypican 3. SEA971Hu" (Cloud-Clone Corp). Чувстительность теста - 0,057 нг/мл. После проведения исследования проводят сравнение результата с пороговым значением. Тест для AFP считается положительным, если его значение превышает показатель 16,0 нг/мл; для OPN>80,0 нг/мл; для GPC-3>1,0 нг/мл. Окончательный прогноз риска заболевания определяют количеством положительных тестов по всем трем определениям:
ни один из трех тестов не превышает порогового значения - риск ГЦК отсутствует;
один из трех определяемых маркеров превышает пороговое значение - риск ГЦК низкий;
два из трех определяемых маркеров превышают пороговое значение - риск ГЦК высокий;
три из трех определяемых маркеров превышают пороговое значение - риск ГЦК очень высокий (вероятность диагноза ГЦК 98,2%).
Способ подтверждается следующими клиническими примерами.
Пример 1.
Пациентка Л, женского пола, родилась 12.11.1956, впервые обратилась в ОГАУЗ «Иркутский областной клинический консультативно-диагностический центр» в 2017 году с жалобами на повышенную утомляемость, тяжесть в правом подреберье. На момент обращения пациентке исполнился 61 год. Из изучения медицинской документации, представленной больной, установлены эпизоды повышения печеночных трансаминаз и ГГТП начиная с 2012 года. В анамнезе: частые ангины, тонзилэктомия в 15 лет. Переливание крови, употребление наркотиков отрицает. Сопутствующие заболевания: Гипертоническая болезнь, хронический пиелонефрит.
При обследовании в условиях диагностического центра в мае 2017 года у больной выявлена РНК вируса гепатита С методом ПЦР, I генотип, вирусная нагрузка 5,6×105 копий/мл, АЛТ 87,8 МЕ/мл ACT 97,6 МЕ/мл, ЩФ 288 Ед/л. Выявлено снижение альбумина до 34,89 г/л. Билирубин, общий белок - в пределах нормальных значений. УЗС органов брюшной полости: в печени очаговых изменений не выявлено, увеличенный парапанкреатический лимфоузел и признаки липоматоза поджелудочной железы. По результатам эластометрии печени выявлен фиброз F4 (32,0 кПа) по шкале METAVIR.
Поставлен диагноз: Хронический вирусный гепатит С, фаза репликации, 1 генотип, средняя степень виремии, низкая биохимическая активность. Фиброз печени F4.
Больной назначена противовирусная терапия комбинация препаратов омбитасвир+паритапревир+ритонавир+дасабувир в течении 12 недель. Лечение переносила удовлетворительно. Данные лабораторного и инструментального обследования к моменту окончания терапии: эритроциты 4,0*1012/л. Лейкоциты 6,5*109/л, тромбоциты 153*109/л, АЛТ 22,7 Ед/л, ACT 31,7 Ед/л, общий билирубин 20,3 мкмоль/л, альбумин 35,0 г/л, глюкоза 5,4 ммоль/л, креатинин 90,3 ммоль/л. HCV RNA - не обнаружена. УЗИ брюшной полости: печень не увеличена. КВР 150 мм. Площадь селезенки 52 см, асцита - нет, очаговых изменений в печени не выявлено. По предлагаемому способу выполнено определение уровня онкомаркеров в венозной крови. АФП - 10 нг/мл (пороговое значение 16 нг/мл), ОПН- 472 нг/мл (пороговое значение 80 нг/мл), ГПК-3,25 нг/мл (пороговое значение 1 нг/мл). Таким образом, на момент окончания терапии два из трех онкомаркеров находились на уровне превышающем пороговое значение. Прогноз заболевания высокий.
В процессе диспансерного наблюдения подтверждено отсутствие вируса в крови в ПЦР через 1 и 3 месяца после окончания противовирусной терапии.
Через 3,5 месяца после окончания противовирусной терапии во время диспансерного наблюдения на УЗИ выявлено объемное образование размером 110*92 мм в левой доле печени, неоднородное, средней эхогенности. Для уточнения диагноза выполнено МСКТ с в/в усилением. После контрастирования в сегменте S3 визуализируется гиподенсивное образование с нечеткими контурами. В артериальную фазу накапливает контраст. Размеры 0,8*0,9*1,1 см. Внутрипеченочные и внепеченочные протоки не расширены. Заключение: объемное образование левой доли печени. Гепатоцеллюлярный рак. Под контролем УЗИ выполнена тонкоигольная аспирационная биопсия образования. В мазках пунктата среди пролиферирующего печеночного эпителия обнаружены опухолевые клетки карциномы. В марте 2018 г. больной на стадии T1M0N0 выполнена левосторонняя гемигепатэктомия. Патолого-гистологическое заключение: гепатоцеллюлярная карцинома. В крае резекции опухолевых клеток нет. В лимфатических узлах метастазы не обнаружены. Выписана в удовлетворительном состоянии. По состоянию на февраль 2019 г. больная жива, состояние удовлетворительное. Таким образом, у больной Л. ГЦК развилась через 3,5 месяца после успешного курса противовирусной терапии на фоне цирроза печени. Применение предлагаемого способа позволило отнести больную к категории высокого риска, что через 3,5 месяца после прогноза было подтверждено обнаружением опухоли методами визуализации (УЗС, МСКТ) и гистологическим анализом биоптата ткани печени.
Пример 2.
Пациент Ю., мужского пола, родился 02.04.1948, обратился в ОГАУЗ «Иркутский областной клинический консультативно-диагностический центр» в 2017 году. На момент обращения пациенту исполнилось 69 лет. Обратился к гастроэнтерологу с жалобами на ноющие боли в правом подреберье, вздутие, урчание после еды, боли беспокоят в течение 3 лет, появились после холецистэктомии (из минидоступа). Вредные привычки отрицает. Объективно: рост 148 см, вес 72 кг, ИМТ 33. АД 170/90 мм.рт.ст. ЧСС 82 в мин. Язык влажный, обложен. Живот мягкий безболезненный. Печень у края реберной дуги, селезенка не пальпируется. Был поставлен диагноз: неалкогольный стеатогепатит, минимальная биохимическая активность (АЛТ 52,3 МЕ/мл, ACT 44,9 МЕ/мл). ЩФ 387 Ед/л. Рекомендовано обследование на вирусные гепатиты, назначена мамбраностабилизирующая и метаболическая терапия.
Через полгода при обследовании общий анализ крови в пределах нормы, АЛТ 45,2 МЕ/мл, ACT 42,2 МЕ/мл, ЩФ 388 Ед/л, билирубин 19,7 мкмоль/мл, HBsAg и anti-HBcor - отрицательные; anti-HCV -положительные, выявлена РНК вируса гепатита С, I генотип, вирусная нагрузка 6,0×104 копий/мл. По данным УЗС органов брюшной полости: признаки диффузного поражения без портальной гипертензии. Поставлен диагноз: Хронический гепатит С, фаза репликации, 1 генотип, средняя степень виремии, минимальная биохимическая активность. Рекомендовано противовирусное лечение по двум возможным схемам, от чего больной категорически отказался.
В сентябре 2018 года на приеме у гастроэнтеролога предъявлял жалобы на отеки на ногах к вечеру, боли в правом подреберье, изжогу, горечь во рту, тошноту. При осмотре: живот мягкий безболезненный, печень у края реберной дуги, селезенка не пальпируется. По данным УЗС: признаки диффузного поражения печени (цирроз), спленомегалия (62 см2). АЛТ 48 МЕ/мл, ACT 39,3 МЕ/мл, билирубин 17,1 мкмоль/мл, общий анализ крови в пределах нормы. Диагноз прежний. Вирусная нагрузка - 1,4×106 копий/мл. Уровень онкомаркеров в крови: АФП 35,1 нг/мл (пороговое значение 16 нг/мл), ОПН 125,1 нг/мл (пороговое значение 80 нг/мл), ГПК-31,20 нг/мл (пороговое значение 1,0 нг/мл). Таким образом, на момент настоящего обследования три из трех онкомаркеров находились на уровне, превышающем пороговое значение. В связи с отказом от противовирусной терапии рекомендовано продолжить прием гепатопротекторов и повторить УЗС через 3 месяца.
В начале 2019 г. проконсультирован гастроэнтерологом. Жалобы на сохраняющиеся отеки, общую слабость. Похудел на 6 кг за 3 месяца. Объективно: рост 148 см, вес 66 кг. Пальмарная эритема, расширена капиллярная сеть на шее. Отеки голеней и стоп. Живот мягкий болезненный в левой боковой области. Печень у края реберной дуги, селезенка не пальпируется. По результатам обследования: АЛТ 53,6 МЕ/мл, ACT 79,6 МЕ/мл, СОЭ 27 мм/час, при нормальных значениях общего белка гипоальбуминемия (37,8 г/л) и гиперглобулинемия, Количественный анализ РНК гепатита С в крови (ПНР): 7×106 копий/мл. ФГДС: варикозное расширение вен пищевода 0-1 степени, гастрит с эрозиями. УЗС: объемное образование печени в 5 сегменте 3,9×3,1×3,7 см. Площадь селезенки 78 см2.
МСКТ органов брюшной полости: в правой доле неоднородное бугристое образование размером 3,82×3,0×3,74 см, с четкими контурами, накапливает контраст в артериальную фазу. Направлен на консультацию к онкологу. Установлен диагноз ГЦК, стадия T2N0M0. Дальнейшее лечение проходил за границей.
Таким образом, наличие положительных результатов анализа АФП, ОПН и ГПК-3 позволило отнести больного Ю. к категории лиц с очень высоким риском развития ГЦК, что было подтверждено выявлением рака печени через 5 месяцев после прогноза.
Пример 3.
Пациент С, мужского пола, родился 20.08.1955, обратился в ОГАУЗ «Иркутский областной клинический консультативно-диагностический центр» в 2016 году. На момент обращения пациенту исполнился 61 год. Консультирован инфекционистом. Клинический диагноз: Хронический гепатит С, фаза репликации, 1 генотип, средняя степень виремии, минимальная биохимическая активность, индекс гистологической активности 14-15 баллов с признаками формирующегося цирроза печени, минимальная ферментативная активность. По данным УЗС: увеличение печени (вертикальный размер 16 см), жировой гепатоз I степени. ФГДС: умеренно выраженный смешанный гастрит. Дуоденит.
Рекомендована противовирусная терапия препаратами: омбитасвир + паритапревир + ритонавир + дасабувир + рибавирин в течении 12 недель.
В январе 2017 года на фоне проводимой противовирусной терапии: HCV RNA не определяется методом ПЦР, АЛТ 95 МЕ/мл, ACT 64 МЕ/мл, билирубин 21,2 мкмоль/мл, альбумин 31,03 г/л. К моменту завершения терапии (12 недель) вирус гепатита С в крови не определяется, показатели общего анализа крови в норме, АЛТ 22,6 МЕ/мл, ACT 29,0 МЕ/мл. ГГТП 88 Ед/л, общий белок и альбумин в пределах нормальных значений. Уровень онкомаркеров в крови: АФП 8,0 нг/мл (пороговое значение 16 нг/мл), ОНИ 66,2 нг/мл (пороговое значение 80 нг/мл), ГПК-3 0,3 нг/мл (пороговое значение 1,0 нг/мл). Таким образом, на момент обследования ни один из трех онкомаркеров не превысил уровня порогового значения.
Больной находился в состоянии диспансерного наблюдения в течение двух лет. Каждые полгода проходил обследование, включающее: общий анализ крови, мочи, биохимические анализы, ПЦР на HCV RNA, УЗС органов брюшной полости. Через 1 год после окончания терапии АФП 8,05 МЕ/мл, ОПН 23,1 нг/мл, ГПК-3 0,2 нг/мл. Заключение МСКТ печени: очаговых изменений в печени не обнаружено, данных за гепатоцеллюлярный рак не выявлено.
По прошествии двух лет после противовирусной терапии (февраль 2019 г.) констатировано достижение стойкого вирусологического ответа. HCV RNA не определяется. Общий анализ крови в норме. АЛТ 25 МЕ/мл, ACT 27 МЕ/мл, билирубин 17,5 мкмоль/мл, ЩФ 249 Ед/л, ГГТП 72 Ед/л, сохраняется гипоальбуминемия и гиперглобулинемия. По данным УЗС: признаки цирроза печени без портальной гипертензии. Площадь селезенки 55 см2. Очаговых образований в печени не выявлено.
Таким образом, у больного с циррозом печени, ассоциированным с гепатитом С, после успешной противовирусной терапии достигнут стойкий вирусологический ответ. Исследование онкомаркеров на момент окончания терапии и через 1 год после ее проведения не выявило положительных результатов анализа на АФП, ОПН и ГПК-3, что позволило исключить риск развития ГЦК. В процессе двухлетнего диспансерного наблюдения было подтверждено отсутствие ГЦК у данного больного.
Настоящая работа выполнена при финансовой поддержке Министерства науки и высшего образования Российской Федерации в рамках Федеральной целевой программы проведения исследований по приоритетным направлениям с участием научно-исследовательских организаций и университетов российско-французской Партнерской программы Юбера Кюрьена «Колмогоров» (контракт №14.616.21.0098; уникальный идентификационный номер проекта RFMEFI61618X0098).
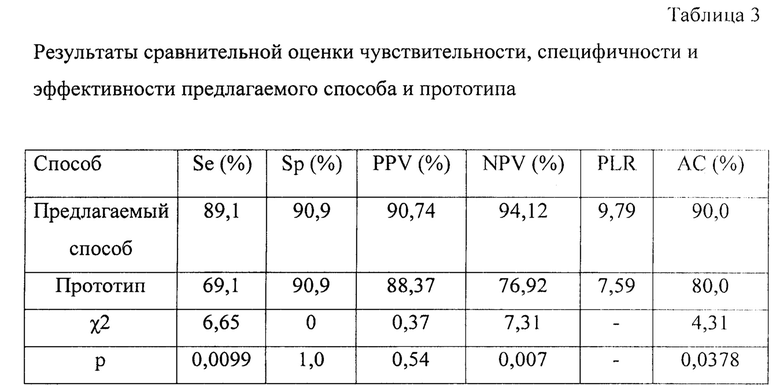
Se - чувствительность, Sp - специфичность, PPV - положительное прогностическое значение, NPV - отрицательное прогностическое значение, PLR - отношение правдоподобия положительного результата, АС диагностическая точность; р - уровень статистической значимости различий.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ У БОЛЬНЫХ ХРОНИЧЕСКИМ ГЕПАТИТОМ С | 2019 |
|
RU2723891C1 |
| Способ прогнозирования формирования цирроза печени у пациентов с хроническим гепатитом C | 2024 |
|
RU2834154C1 |
| СПОСОБ ДИАГНОСТИКИ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2003 |
|
RU2319969C2 |
| Способ прогнозирования повышенного риска декомпенсации цирроза печени или развития гепатоцеллюлярной карциномы у пациентов с циррозом печени в исходе хронического гепатита С после достижения устойчивого вирусологического ответа | 2022 |
|
RU2800251C1 |
| Способ дифференциальной диагностики новообразований печени при ультразвуковом исследовании | 2016 |
|
RU2632768C1 |
| Способ дифференциальной диагностики диффузных и очаговых заболеваний печени | 2020 |
|
RU2771257C1 |
| ХИНОНОВОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ПЕЧЕНИ | 2003 |
|
RU2292875C2 |
| Способ диагностики гепатоцеллюлярной карциномы с помощью определения коэффициента развития гепатоцеллюлярной карциномы на основании изменений уровней экспрессии микроРНК в плазме крови и слюне человека | 2020 |
|
RU2760937C1 |
| Способ дифференциальной диагностики хронического гепатита В, хронического гепатита С и аутоиммунных заболеваний печени у пациентов с тяжелым фиброзом и циррозом печени | 2024 |
|
RU2834902C1 |
| Способ идентификации биологических маркеров, обнаруживаемых в биологических материалах человека в связи с возможным наличием патологических состояний организма человека, в том числе онкологических заболеваний, осуществляемый путем мультиплексного иммуноферментного сэндвич-иммуноанализа | 2021 |
|
RU2779104C1 |
Изобретение относится к области медицины и касается способа прогнозирования риска развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С. Сущность способа заключается в том, что определяют совокупность показателей уровня альфа-фетопротеина, глипикана-3 и остепонтина в венозной крови. Предварительно рассчитывают пороговое значение для каждого онкомаркера, проводят сравнение результата с пороговыми значениями для альфа-фетопротеина 16,0 нг/мл; для остеопонтина 80,0 нг/мл; для глипикана-3 1,0 нг/мл. Прогнозируют риск развития заболевания по следующему алгоритму: при уровне трех определяемых онкомаркеров меньше или равном пороговому значению риск развития гепатоцеллюлярной карциномы отсутствует; при превышении порогового значения одного из онкомаркеров риск развития заболевания низкий; при превышении порогового значения двух онкомаркеров риск развития заболевания высокий; при превышении порогового значения трех определяемых онкомаркеров прогнозируют абсолютный риск развития гепатоцеллюлярной карциномы. Использование способа позволяет с высокой точностью прогнозировать риск развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С. 3 пр., 3 табл., 1 ил.
Способ прогнозирования риска развития гепатоцеллюлярной карциномы у больных хроническим гепатитом С путем определения онкомаркеров в крови пациента, отличающийся тем, что определяют совокупность показателей уровня альфа-фетопротеина, глипикана-3 и остепонтина в венозной крови, проводят сравнение результата с пороговыми значениями для альфа-фетопротеина 16,0 нг/мл; для остеопонтина 80,0 нг/мл; для глипикана-3 1,0 нг/мл и прогнозируют риск развития заболевания по следующему алгоритму: при уровне трех определяемых онкомаркеров меньше или равном пороговому значению риск развития гепатоцеллюлярной карциномы отсутствует; при превышении порогового значения одного из онкомаркеров риск развития заболевания низкий; при превышении порогового значения двух онкомаркеров риск развития заболевания высокий; при превышении порогового значения трех определяемых онкомаркеров прогнозируют абсолютный риск развития гепатоцеллюлярной карциномы.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВОЗНИКНОВЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОГО РАКА | 2012 |
|
RU2498775C1 |
| WO2019076830, 25.04.2019 | |||
| МАЛОВ С.И | |||
| и др | |||
| Биомаркеры в диагностике и прогнозировании рецидивирования гепатоцеллюлярной карциномы (обзор) // Современные технологии в медицине, 2019, Т.11, N2, C.183-196 | |||
| ГОРДЕЙЧУК И.Н | |||
| и др | |||
| Вопросы ранней диагностики гепатоцеллюлярной карциномы // Верхневолжский медицинский журнал., | |||
Авторы
Даты
2021-06-04—Публикация
2020-08-10—Подача