Область техники
Изобретение относится к области катализаторов реакции синтеза Фишера-Тропша, в частности, к катализатору из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, способу его приготовления и способу синтеза Фишера-Тропша.
Уровень техники
Структура первичной энергии в Китайской Народной Республике (КНР) характеризуется богатыми запасами угля и недостаточными нефти и газа, причем степень зависимости от импортируемой нефти в Китае постоянно растет вместе с быстрым экономическим развитием, темпы которого достигают 61% в 2015 году, тем самым серьезно влияя на энергетическую безопасность в Китае. Посредством синтеза Фишера-Тропша можно превращать синтез-газ, состоящий из моноксида углерода и водорода, в жидкое топливо и химические вещества, в последние годы он становится все более важным путем преобразования энергии. Технологию косвенного сжижения угля, основанная на синтезе Фишера-Тропша, можно применять для реализации чистого использования угля и частичного смягчение проблемы, состоящей в том, что Китай в значительной степени зависит от импортируемой нефти; эта технология стала одной из предпочтительных технологий замены нефти углем и чистого использования угля в Китае. Благодаря промышленным усилиям в течение многих лет, в Китае введен в эксплуатацию технический промышленный демонстрационный проект косвенного сжижения угля на основе железа с производственной мощностью 160000 тонн/год; кроме того, в экспериментальную работу запущены заводы по косвенному сжижению угля на основе железа с производственной мощностью 1 млн. тонн в год, инвестированные Shandong Yankuang Group и другими компаниями, и заводы по косвенному сжижению угля на основе железа с производственной мощностью 4 млн тонн в год, инвестированные Shenhua Ningxia Coal Industry Group Co., Ltd.
Уравнения реакций в синтезе Фишера-Тропша являются следующими: 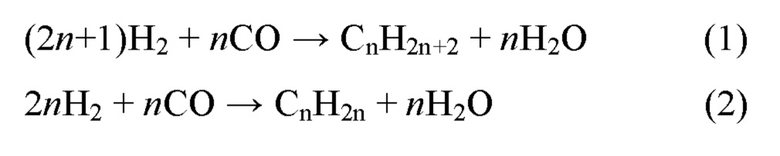
Помимо конечных продуктов - алканов и алкенов - промышленный синтез Фишера-Тропша может также производить побочные продукты - диоксид углерода (СО2) и метан (СН4). Реакция синтеза Фишера-Тропша имеет сложный механизм и многочисленные стадии, такие как диссоциация СО, гидрогенизация углерода (С), рост цепи СНх, а также реакции гидрогенизации и дегидрогенизации, которые приводят к десорбции углеводородных продуктов и удалению кислорода (О). С точки зрения практического применения, основной целью совершенствования катализатора синтеза Фишера-Тропша является повышение селективности по отношению к целевым продуктам, снижение селективности по отношению к побочным продуктам, повышение стабильности катализатора и продление срока службы катализатора.
Железо является самым дешевым переходным металлом, используемым в производстве катализаторов синтеза Фишера-Тропша. Активной фазой катализаторов Фишера-Тропша на основе железа, как правило, считают карбид железа. Традиционный катализатор на основе железа имеет высокую активность конверсии водяного газа (СО+Н2О→СO2+Н2), так что традиционный катализатор на основе железа обычно имеет высокую селективность по отношению к побочному продукту - СО2, на который обычно приходится 25%-45% конверсии сырьевого моноксида углерода. Это является одним из основных недостатков катализаторов на основе железа для реакции синтеза Фишера-Тропша.
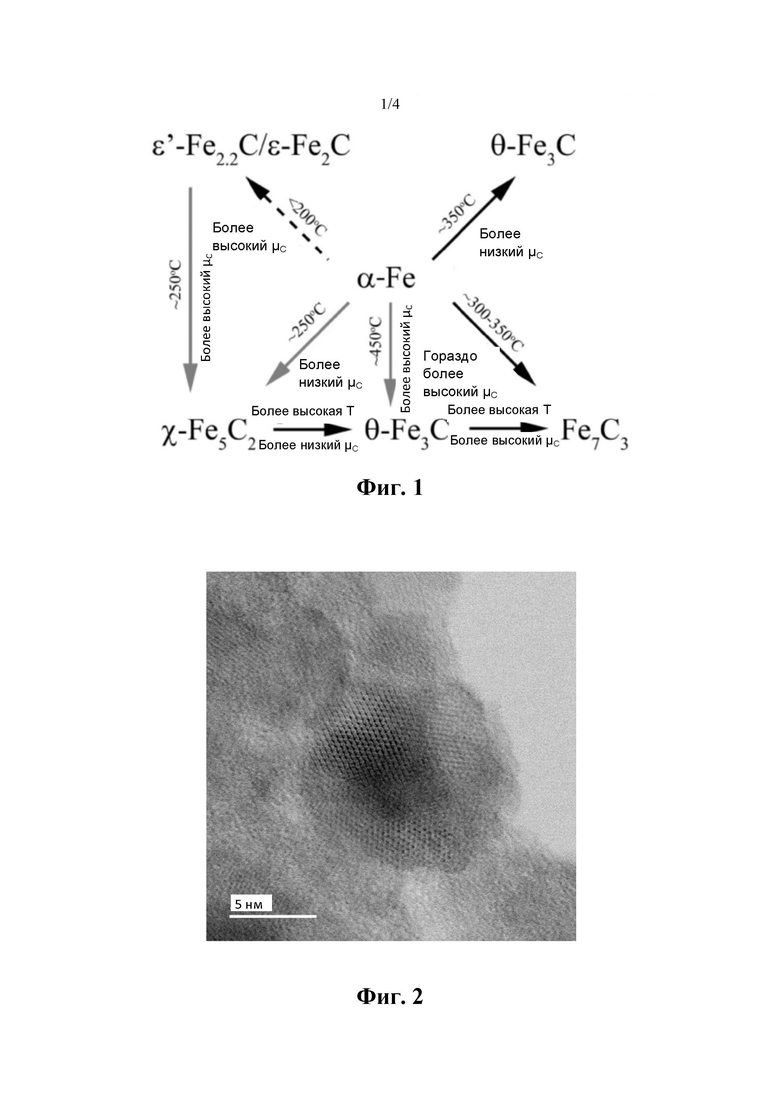
Трудно синтезировать чистую фазу карбида железа, который является активной фазой катализатора синтеза Фишера-Тропша на основе железа. Активная фаза катализатора на основе железа имеет очень сложные варианты, что вызывает значительные споры о природе активной фазы и механизме реакции синтеза Фишера-Тропша с катализатором на основе железа. Рассматривали различные карбиды в условиях реакции Фишера-Тропша, в том числе ε-Fe2С, →ε'-Fe2,2C, Fe7С3, χ-Fe5C2 и θ-Fe3C. В статье "Stability and reactivity of ε-χ-θ iron carbide catalyst phases in Fischer-Tropsch synthesis: Controlling μC", опубликованной в журнале высшего уровня Journal of the American Chemical Society (JACS) в 2010 году, содержится систематический расчет и экспериментальные данные об условиях получения различных карбидов железа, как показано на фиг. 1, возникновение фазового перехода карбидов железа (фазовый переход ε-χ-θ ) зависит от температуры и отношения Н2/СО. В частности, высокотемпературный низкий углеродный химический потенциал (μC), т.е. высокое отношение Н2/СО, в общем приводит к преимущественному образованию карбида железа θ-Fe3С; напротив, высокий /лC (низкое отношение Н2/СО) и умеренная температура (~250°С) способствуют образованию карбида железа χ-Fe5C2; ε-карбид преимущественно образуется при более низких температурах и более высоком углеродном химическом потенциале μC.
Основная точка зрения этой статьи является такой, как показано на фиг. 1, в статье принимают Fe2О3 в качестве инициирующего предшественника, проводят серию экспериментов в атмосфере реакции синтеза Фишера-Тропша, и фазовое изменение продукта определяют с помощью рентгеновской дифракции (XRD) и рентгеновской абсорбционной спектроскопии тонкой структуры с синхротронным излучением in situ (XAS). При более высоком углеродном химическом потенциале μC необходимо, чтобы ε/ε' карбид железа был получен и стабильно существовал в мягких условиях ~200°С, а когда температура близка к 250°С, ε/ε' карбид железа превращается в χ-Fe5C2, который обладает термодинамической стабильностью. В промышленном производстве с помощью синтеза Фишера-Тропша температура синтеза Фишера-Тропша на основе железа находится в пределах 235-265°С, чтобы увеличить давление насыщенных паров побочного продукта - водяного пара, получить высококачественный водяной пар и повысить экономическую выгоду. Другими словами, в этой авторитетной статье указано, что ε/ε' карбид железа является нестабильным при температуре выше 200°С, поэтому его нельзя использовать в качестве катализатора, подходящего для современного промышленного синтеза Фишера-Тропша.
В статье "Metal organic framework-mediated synthesis of highly active and stable Fischer-Tropsch catalysts", опубликованной в 2015 году в журнале Nature communication, дочернем издании журнала высшего уровня Nature, представлена попытка синтеза карбидов и успешный синтез χ-Fe5C2, представляющего собой катализатор, который может быть использован при промышленных температурах современного синтеза Фишера-Тропша, однако его селективность по отношению к СО2 достигает 46%, и это означает, что его теоретически максимальная эффективность использования СО составляет всего 54%, и эффективность производства является относительно низкой.
В CN 104399501 A раскрыт способ получения наночастиц ε-Fe2C, пригодных для низкотемпературной реакции синтеза Фишера-Тропша. Первоначальным предшественником является каркасный железный материал, а реакционная система является периодической прерываемой реакцией растворителя полиэтиленгликоля. Селективность катализатора по отношению к СО2 составляет 18,9%, а селективность по отношению к СН4 - 17,3%. Его недостатки состоят в том, что способ получения можно применять только при низкой температуре менее 200°С, и реакция не может быть проведена непрерывно. Это означает, что катализатор не подходит для непрерывного производства в современных промышленных условиях синтеза Фишера-Тропша.
В каждой из вышеупомянутых технологий имеются такие проблемы, как сложный способ получения, дорогостоящие материалы сырья, низкая стабильность катализатора и излишне высокая селективность по отношению к побочному продукту - СО2 или СН4.
Краткое описание изобретения
В настоящем изобретении, направленном на устранение технических проблем уровня техники, предложен катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, способ его приготовления и способ синтеза Фишера-Тропша.
Для достижения вышеуказанной цели, в первом аспекте изобретения предложен способ приготовления катализатора из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, включающий следующие стадии:
(1) обработка нанометрового порошка железа или нанометрового порошка соединения железа, способного обеспечить получение нанометрового порошка железа с помощью восстановления in-situ, и Н2, для очистки поверхности при температуре 250-510°С;
(2) предварительная обработка материала, полученного на стадии (1), с использованием Н2 и СО при температуре 80-180°С, где молярное отношение Н2/СО составляет 1,2-2,8: 1;
(3) приготовление карбида с использованием материала, полученного на стадии (2), Н2 и СО при температуре 180-280°С, где молярное отношение Н2/СО составляет 1,0-3,0: 1.
Во втором аспекте изобретения предложен катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, полученный способом приготовления согласно изобретению.
В третьем аспекте изобретения предложен способ синтеза Фишера-Тропша, включающий: приведение сырьевого газа для синтеза в контакт с катализатором в условиях реакции синтеза Фишера-Тропша, где катализатор представляет собой катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша согласно изобретению.
Данное изобретение обеспечивает получение следующих технических результатов:
(1) требуемые материалы сырья являются простыми и легко получаемыми, при их низкой стоимости: источником основного сырьевого материала - железа является только нанометровый порошок железа, доступный на рынке, или же обычный и коммерчески доступный нанометровый порошок оксида железа (Fe2О3), нанометровый порошок магнетита (Fe3O4), нанометровый порошок гетита, нанометровый порошок гидроксида железа и другие нанометровые порошки соединений железа, которые могут быть восстановлены в реакторе синтеза Фишера-Тропша для получения нанометрового железа; при синтезе активной фазы карбида используют только первоначальный реакционный газ (монооксид углерода и Н2) реакционной системы синтеза Фишера-Тропша, он не связан с каким-либо неорганическим или органическим реакционным сырьем, так что материалы сырья являются значительно более простыми по сравнению с уровнем техники, описанным в литературе.
(2) Технологические стадии являются простыми и удобными, и в предпочтительном воплощении процесс приготовления катализатора и процесс синтеза Фишера-Тропша проходят в одном и том же реакторе, так что не требуется какого-либо дополнительного реакционного устройства для реакции приготовления активной фазы карбида; весь процесс приготовления требует осуществления только трех стадий, а именно очистки поверхности предшественника, предварительной обработки и приготовления карбида, причем реакция приготовления и синтеза активной фазы может быть выполнена in situ в одном и том же реакторе.
(3) Способ согласно изобретению может быть использован для приготовления активной фазы - ε/ε' карбида железа со 100% чистотой, который пригоден для высокотемпературного реактора высокого давления (например, температура 235-250°С, давление 2,3-2,5 МПа и высокий углеродный химический потенциал μC отношением Н2/СО=1,5-2,0) непрерывного действия, стабильность реакции является чрезвычайно высокой, так что разрушен теоретический технический барьер в традиционной теории, изложенной в литературе, а именно: «ε/ε' карбид железа должен стабильно существовать при мягких условиях менее 200°С при более высоком углеродном химическом потенциале μC», стабильная температура может составлять до 250°С, и селективность по отношению к СО2 является крайне низкой; в условиях реакции промышленного синтеза Фишера-Тропша непрерывный реактор высокого давления можно использовать для поддержания непрерывной и стабильной реакции в течение более 400 часов, а селективность по отношению к СО2 составляет менее 8% (предпочтительно 5% или меньше); кроме того, селективность по отношению к побочному продукту CH4 поддерживается на уровне ниже 14% (предпочтительно ниже 11%), селективность по отношению к эффективному продукту достигает 78% или более (предпочтительно 84% или более), и способ приготовления очень хорошо подходит для эффективного промышленного производства масляных восковых продуктов с помощью синтеза Фишера-Тропша в современной углехимической промышленности.
Краткое описание чертежей:
на фиг. 1 показан график соотношения конверсии карбидов железа в уровне техники;
на фиг. 2 показано изображение, полученное методом трансмиссионной электронной микроскопии (ТЕМ), предшественника 1 в примере 1;
на фиг. 3 показано изображение, полученное методом трансмиссионной электронной микроскопии высокого разрешения (HRTEM) предшественника 1 в примере 1;
на фиг. 4 показана рентгеновская дифрактограмма (XRD) in situ приготовления катализатора А из ε/ε' карбида железа примера 1;
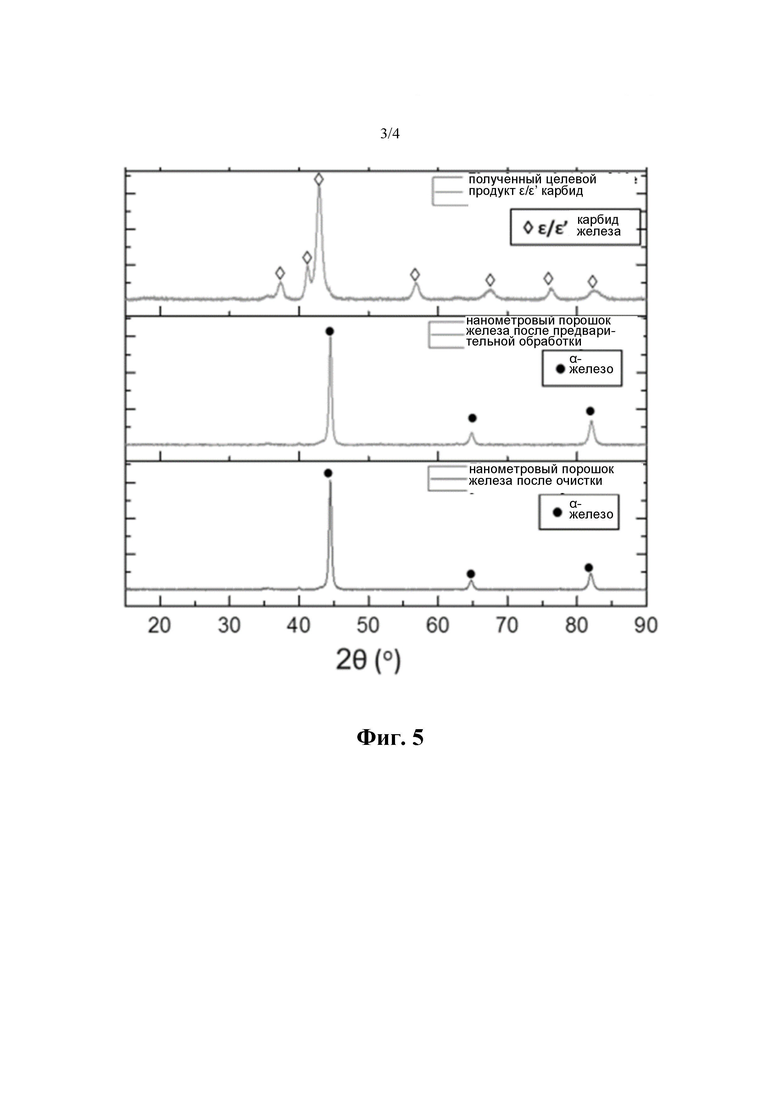
на фиг. 5 показана XRD in situ катализатора А из ε/ε' карбида железа, полученного в примере 1;
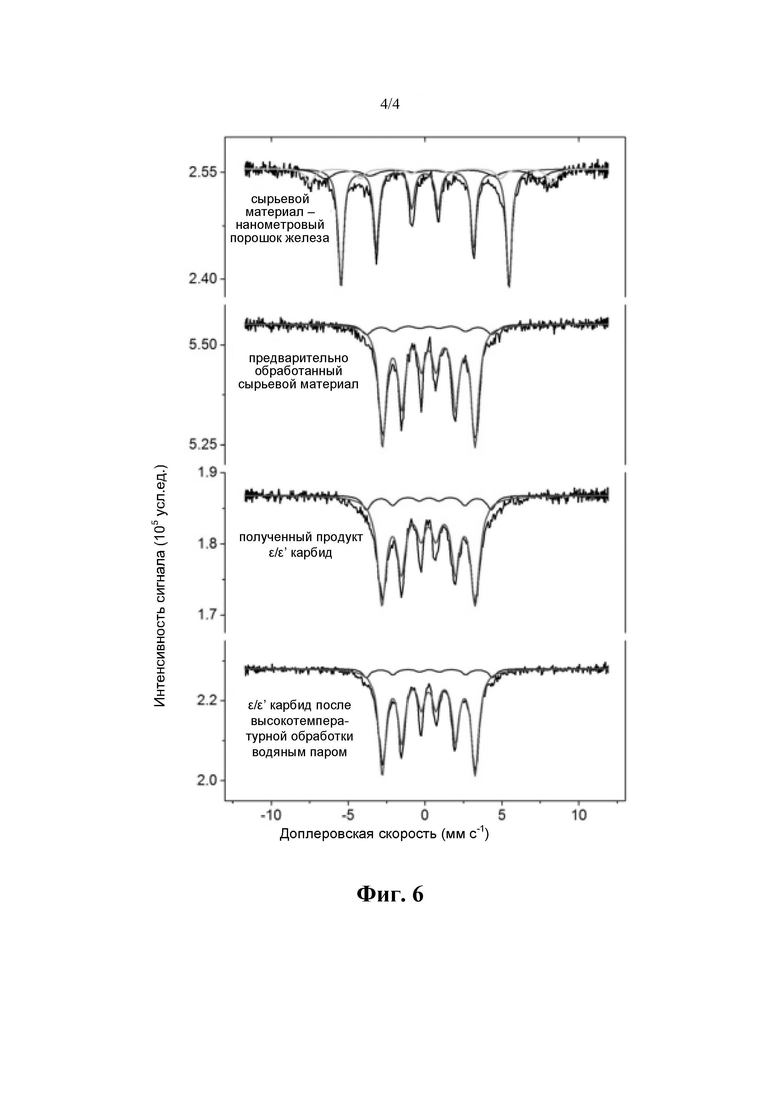
на фиг. 6 показана мессбауэровская спектрограмма in situ способа приготовления катализатора А из ε/ε' карбида железа в примере 1.
Подробное описание
Граничные значения и любая величина в диапазонах, раскрытых в настоящем описании, не ограничиваются точными диапазонами или значениями, но такие диапазоны или значения следует понимать как включающие значения, прилегающие к этим диапазонам или значениям. Что касается численных диапазонов, то значения конечных точек различных диапазонов, значения конечных точек и индивидуальное точечное значение различных диапазонов, а также отдельные точечные значения могут быть объединены друг с другом с получением одного или более новых численных диапазонов, которые следует считать специально раскрытыми здесь.
В первом аспекте изобретения предложен способ приготовления катализатора из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, включающий следующие стадии:
(1) обработка нанометрового порошка железа или нанометрового порошка соединения железа, способного обеспечить получение нанометрового порошка железа с помощью восстановления in-situ, и Н2, для очистки поверхности при температуре 250-510°С;
(2) предварительная обработка материала, полученного на стадии (1), с использованием Н2 и СО при температуре 80-180°С, где молярное отношение Н2/СО составляет 1,2-2,8: 1;
(3) приготовление карбида с использованием материала, полученного на стадии (2), Н2 и СО при температуре 180-280°С, где молярное отношение Н2/СО составляет 1,0-3,0: 1.
В способе приготовления согласно изобретению исходные материалы являются простыми и легко доступными при низкой стоимости, где нанометровый порошок железа может быть выбран обычным в данной области техники образом и может представлять собой обычный продукт, продаваемый на рынке, и средний диаметр частиц нанометрового порошка железа предпочтительно составляет 4-30 нм, более предпочтительно 10-27 нм; нанопорошок соединения железа может быть выбран обычным в данной области техники образом и может представлять собой обычный продукт, продаваемый на рынке, например, нанопорошок соединения железа может представлять собой по меньшей мере один, выбранный из группы, состоящей из нанометрового порошка оксида железа, нанометрового порошка магнетита, нанометрового порошка гетита и нанометрового порошка гидроксида железа.
Согласно изобретению, если сырьем на стадии (1) является нанометровый порошок железа, то стадия (1) может служить для обработки для очистки поверхности нанометрового порошка железа; если сырьем на стадии (1) является нанопорошок соединения железа, способный обеспечить получение нанометрового порошка железа путем восстановления in situ, то стадия (1) может одновременно служить для получения in situ нанометрового порошка железа из нанопорошка соединения железа и проведения обработки для очистки поверхности получаемого нанометрового порошка железа.
Согласно изобретению, Н2 на стадии (1) можно подавать в реакционную систему в виде потока Н2, и давление при обработке для очистки поверхности регулируют путем регулирования давления потока Н2, предпочтительно, на стадии (1) давление при обработке для очистки поверхности составляет 0,1-15 атмосферного давления, предпочтительно 0,2-2,5 атмосферного давления; время составляет 0,5-8 ч, предпочтительно 1 -7 ч.
Согласно изобретению, количество Н2 можно выбирать в зависимости от количества сырьевого материала для обработки, и предпочтительно скорость газа Н2 на стадии (1) составляет 500-20000 мл/ч/г, и более предпочтительно 2500-15000 мл/ч/ г.
Согласно изобретению, Н2 и СО на стадии (2) можно пропускать через реакционную систему в виде смешанного потока газа (Н2+СО), и в то же время давление в процессе предварительной обработки регулируют путем регулирования давления смешанного потока газов (Н2+СО); предпочтительно на стадии (2) давление в процессе предварительной обработки составляет 0,05-7 атмосферного давления, предпочтительно 0,05-2,5 атмосферного давления; время составляет 15-90 мин, предпочтительно 25-75 мин.
Согласно изобретению, скорость газов Н2 и СО на стадии (2) предпочтительно составляет 200-8000 мл/ч/г, и более предпочтительно 1000-6500 мл/ч/г.
Согласно изобретению, Н2 и СО на стадии (3) можно пропускать через реакционную систему в виде смешанного потока газов (Н2+СО), и в то же время давление в процессе приготовления карбида регулируют путем регулирования давления смешанного потока газов (Н2+СО), предпочтительно давление при приготовлении карбида на стадии (3) составляет 0,09-10 атмосферного давления, предпочтительно 0,15-3 атмосферного давления; время составляет 0,5-10 ч, предпочтительно 1,5-8 ч.
Согласно изобретению, скорость газов Н2 и СО на стадии (3) предпочтительно составляет 200-20000 мл/ч/г, и более предпочтительно 4000-15000 мл/ч/г.
Согласно изобретению, предпочтительно молярное отношение Н2/СО на стадии (2) больше, чем молярное отношение Н2/СО на стадии (3).
Если в описании не указано иное, термин «мл/ч/г» относится к объему подаваемого газа на грамм материала сырья в час.
Согласно предпочтительному воплощению настоящего изобретения, способ приготовления дополнительно включает повышение температуры системы после предварительной обработки до 180-280°С при скорости повышения температуры 0,2-5°С/мин. В предпочтительном воплощении приготовленный катализатор из чистой фазы ε/ε' карбида железа может иметь лучшую селективность по отношению к эффективному продукту в реакции синтеза Фишера-Тропша. Кроме того, предпочтительно, температуру системы после предварительной обработки повышают до 200-270°С при скорости нагревания 0,2-2,5°С /мин.
Согласно другому предпочтительному воплощению настоящего изобретения, стадии обработки для очистки поверхности, предварительной обработки и приготовления карбида осуществляют в реакторе синтеза Фишера-Тропша. В предпочтительном воплощении приготовление катализатора и синтез Фишера-Тропша проводят в одном и том же реакторе, так что сырьевые материалы Н2 и СО в процессе приготовления катализатора могут представлять собой исходные сырьевые материалы реакционной системы синтеза Фишера-Тропша, и не требуется дополнительного устройства для проведения реакции приготовления активной фазы карбида; процесс приготовления в целом может обеспечить возможность проведения реакции приготовления и синтеза активной фазы in situ в одном и том же реакторе, и технологические стадии являются более простыми и удобными.
Во втором аспекте настоящего изобретения предложен катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, полученный способом приготовления согласно изобретению. Катализатор из чистой фазы ε/ε' карбида железа представляет собой активную фазу ε/ε' карбида железа 100% чистоты.
В третьем аспекте настоящего изобретения предложен способ синтеза Фишера-Тропша, включающий: приведение сырьевого газа для синтеза в контакт с катализатором в условиях реакции синтеза Фишера-Тропша, где катализатор представляет собой катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша согласно изобретению.
Катализатор из чистой фазы ε/ε' карбида железа используют в качестве катализатора для синтеза Фишера-Тропша, и катализатор выполнен с возможностью проведения реакции синтеза Фишера-Тропша при высокой температуре и высоком давлении, например, условия реакции синтеза Фишера-Тропша включают температуру в диапазоне 235-250°С и давление в диапазоне 2,3-2,5 МПа.
Если не указано иное, в настоящем описании, давление означает абсолютное давление.
Согласно изобретению, предпочтительно, синтез Фишера-Тропша осуществляют в высокотемпературном реакторе высокого давления непрерывного действия. Катализатор из чистой фазы ε/ε' карбида железа согласно изобретению может обеспечить возможность проведения реакции синтеза Фишера-Тропша непрерывно и стабильно в течение более 400 часов в высокотемпературном реакторе высокого давления непрерывного действия.
Изобретение подробно описано ниже со ссылкой на примеры. В следующих далее примерах:
Коэффициент конверсии СО (%) = [(количество молей СО в сырье - количество молей СО в выгружаемом материале) / количество молей СО в сырье] × 100%;
Селективность по СО2% = [количество молей СО2 в выгружаемом материале / (количество молей СО в сырье - количество молей СО в выгружаемом материале)] × 100%;
Селективность по СН4% = [количество молей СН4 в выгружаемом материале / (количество молей СО в сырье × коэффициент конверсии СО % (1 - селективность по СО2%))] × 100%;
Эффективная селективность по продукту % = [1 - селективность по СО2 % - селективность по СН4%] × 100%.
Пример 1
Пример предназначен для иллюстрации катализатора из чистой фазы ε/ε' карбида железа и способа его приготовления. (Для облегчения сравнения, все сырьевые материалы были получены от одной и той же компании, но в ходе фактической эксплуатации сырьевые материалы не были ограничены этой компанией).
(1) Взвешивали 1,00 г нанометрового железного порошка (от Alfa Reagent Company, CAS No. 7439-89-6) со средним диаметром частиц 21±6 нм, и этот нанометровый порошок железа обозначен как предшественник 1.
(2) Предшественник 1 помещали в трубчатый реактор синтеза Фишера-Тропша, и подавали поток Н2 со скоростью газа 2500 мл/ч/г, при давлении 2,5 атмосферного давления и температуре 250°С для проведения реакции в течение 7 часов.
(3) Температуру в реакторе снижали до 180°С, поток Н2 заменяли газовым потоком (Н2+СО), который имеет молярное отношение Н2/СО=1,2, скорость газа 6500 мл/ч/г и общее давление 0,05 атмосферного давления, и проводили реакцию предварительной обработки в течение 75 мин;
(4) Поток газа в реакторе заменяли газовым потоком (Н2СО), который имеет молярное отношение Н2/СО=1,0, скорость газа 4000 мл/ч/г и общее давление 3 атмосферы, в то же время температуру постепенно повышали до 200°С при скорости повышения температуры 0,2°С/мин, и эту температуру поддерживали в течение 1,5 ч. Завершали приготовление катализатора из чистой фазы ε/ε' карбида железа, обозначенного как катализатор А1 из ε/ε' карбида железа.
Испытания
Предшественник 1 был исследован методами трансмиссионной электронной микроскопии (ТЕМ) и трансмиссионной электронной микроскопии высокого разрешения (HRTEM), и результаты измерений показаны на фиг. 2 и фиг. 3, соответственно.
Использовали метод XRD обнаружения in situ, то есть вышеуказанный способ приготовления катализатора проводили при мониторинге изменения кристаллической фазы материалов с помощью рентгеновского дифрактометра (XFD, поставщик Rigaku Corporation, модель D/max-2600/PC), результаты показаны на фиг. 4 и фиг. 5.
При этом процесс перехода от нанометрового порошка железа к целевому карбиду хорошо виден на фиг. 4; как видно из фиг. 5, приготовленный целевой продукт ε/ε' карбид железа подтвердил желаемую кристалличность, продукт ε/ε' карбид железа идеально соответствовал всем характеристическим пикам ε/ε' карбида железа, чистота была чрезвычайно высокой, и продукт не содержал никаких других примесей.
Применяли метод обнаружения с использованием мессбауэровского спектра in situ, а именно использовали мессбауэровский спектр (трансмиссионный спектрометр с синусоидной скоростью источника 57Fe, 57Со (Rh)) для мониторинга изменения компонентов материалов в процессе приготовления, целевой продукт - активную фазу ε/ε' карбида железа подвергают обработке посредством добавления в реакционный газ при 250°С водяного пара под давлением насыщенных паров, так что было смоделировано состояние после длительной работы в промышленных условиях. Процесс изменения от предшественника 1 к целевому карбиду и ситуация после долгосрочной работы в промышленных условиях, смоделированных путем высокотемпературной обработки водяным паром, были хорошо видны посредством мониторинга мессбауэровского спектра in situ. Результаты показаны на фиг. 6 и в таблице 1.
Фиг. 6 наглядно иллюстрирует процесс изменения от нанометрового порошка железа к целевому карбиду и процесс проведения высокотемпературной обработки водяным паром.
В таблице 1 показаны статистические результаты конкретных данных фазовой трансформации; чистота активной фазы ε/ε' карбида железа в целевом продукте, приготовленном в примере 1, составляет 100%, и чистота по-прежнему составляла 100% после длительной работы в смоделированных промышленных условиях, как представлено в таблице 1. В ней показано, что способ согласно изобретению можно применять для приготовления нанесенного катализатора из активной фазой ε/ε' карбида железа с чистотой 100%, и нанесенный катализатор из активной фазы ε/ε' карбида железа, полученный способом приготовления согласно изобретению, может стабильно существовать при высокой температуре 250°С, и кроме того, катализатор из ε/ε' карбида железа может сохранять 100% чистоту даже после коррозии водяным паром, при моделировании промышленных условий высокой температуры и высокого давления.

Пример 2
Этот пример служит иллюстрацией приготовления катализатора из чистой фазы ε/ε' карбида железа.
(1) Взвешивали 1,00 г нанометрового порошка магнетита (Fe3О4 (от Alfa Reagent Company, CAS No. 1317-61-9) со средним диаметром частиц 17±7 нм, и этот нанометровый порошок магнетита обозначен как предшественник 2.
(2) Предшественник 2 помещали в трубчатый реактор синтеза Фишера-Тропша, и подавали поток Н2 со скоростью газа 15000 мл/ч/г, при давлении 0,2 атмосферного давления и температуре 510°С для проведения реакции в течение 1 часа.
(3) Температуру в реакторе снижали до 80°С, поток Н2 заменяли газовым потоком (Н2+СО), который имеет молярное отношение Н2/СО=2,8, скорость газа 1000 мл/ч/г и общее давление 2,5 атмосферного давления, и проводили реакцию предварительной обработки в течение 25 мин.
(4) Поток газа в реакторе переключали на газовый поток (Н2+СО), который имеет молярное отношение Н2/СО=3,0, скорость газа 15000 мл/ч/г и общее давление 0,15 атмосферного давления, в то же время температуру постепенно повышали до 270°С при скорости повышения температуры 2,5°С/мин, и эту температуру поддерживали в течение 8 ч. Завершали приготовление катализатора из чистой фазы ε/ε' карбида железа, обозначенного как катализатор А2 из ε/ε' карбида железа.
Пример 3
Этот пример служит иллюстрацией приготовления катализатора из чистой фазы ε/ε' карбида железа.
(1) Взвешивали 1,00 г нанометрового порошка гетита (альфа-FeО(ОН)) (от Alfa Reagent Company, CAS No. 20344-49-4) со средним диаметром частиц 19±7 нм, и этот нанометровый порошок гетита обозначен как предшественник 3.
(2) Предшественник 3 помещали в трубчатый реактор синтеза Фишера-Тропша, и подавали поток Н2 со скоростью газа 5000 мл/ч/г, при давлении 1,3 атмосферного давления и температуре 470°С для проведения реакции в течение 5 часов.
(3) Температуру в реакторе снижали до 137°С, поток Н2 заменяли газовым потоком (Н2+СО), который имеет молярное отношение Н2/СО=2,4, скорость газа 5000 мл/ч/г и общее давление 0,1 атмосферного давления, и проводили реакцию предварительной обработки в течение 50 мин.
(4) Поток газа в реакторе заменяли газовым потоком (Н2+СО), который имеет молярное отношение Н2/СО=2,5, скорость газа 10000 мл/ч/г и общее давление 2 атмосферы, в то же время температуру постепенно повышали до 240°С при скорости повышения температуры 1°С/мин, и эту температуру поддерживали в течение 4 ч. Завершали приготовление катализатора из чистой фазы ε/ε' карбида железа, обозначенного как катализатор A3 из ε/ε' карбида железа.
Пример 4
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (2) давление потока Н2 составило 15 атмосфер. Получили катализатор А4 из ε/ε' карбида железа.
Пример 5
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (2) скорость потока газа Н2 составила 500 мл/ч/г. Получили катализатор А5 из ε/ε' карбида железа.
Пример 6
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (3) давление потока газа (Н2+СО) составило 7 атмосфер. Получили катализатор А6 из ε/ε' карбида железа.
Пример 7
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (3) скорость потока газа (Н2+СО) составила 200 мл/ч/г. Получили катализатор А7 из ε/ε' карбида железа.
Пример 8
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (4) давление потока газа (Н2+СО) составило 0,09 атмосферного давления. Получили катализатор А8 из ε/ε' карбида железа.
Пример 9
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (4) скорость потока газа (Н2+СО) составила 200 мл/ч/г. Получили катализатор А9 из ε/ε' карбида железа.
Пример 10
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (4) скорость повышения температуры составила 5°С/мин. Получили катализатор А10 из ε/ε' карбида железа.
Сравнительный пример 1
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что материал, полученный на стадии (2), непосредственно обрабатывали в соответствии со стадией (4) без выполнения стадии (3). Получили катализатор D1 из карбида железа.
Сравнительный пример 2
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (3) молярное отношение Н2/СО составляло 1,1. Получили катализатор D2 из карбида железа.
Сравнительный пример 3
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что на стадии (4) молярное отношение Н2/СО составляло 0,9. Получили катализатор D3 из карбида железа.
Сравнительный пример 4
Катализатор из чистой фазы ε/ε' карбида железа приготовили в соответствии со способом примера 1, за исключением того, что температура предварительной обработки на стадии (3) составляла 200°С, и температура приготовления карбида на стадии (4) составляла 290°С. Получили катализатор D4 из карбида железа.
Сравнительный пример 5
Этот сравнительный пример служит иллюстрацией способа приготовления катализаторов на основе карбида железа согласно уровню техники (N. Lohitharn et al. / Journal of Catalysis 255 (2008) 104-113).
(1) В соответствии с молярным отношением 100Fe/5Cu/17Si, смешивали в сырье 0,6 мол/л Fe(NO3)3 9Н2O и C1u2O6⋅Н2O, добавляли для растворения 60 мл Н2O, другой ингредиент - Si(OC2H5)4 добавляли для растворения в 40 мл пропанола. Два раствора, полученные выше, смешивали и нагревали до температуры 83±3°С.
(2) Раствор NH4OH 2,7 мол/л подогревали до 83±3°С.
(3) Раствор NH4OH, полученный на стадии (2), непрерывно добавляли в смешанный раствор, полученный на стадии (1), и смешанный раствор энергично перемешивали до тех пор, пока не получали осадок, при этом поддерживали рН=8-9 в конечной точке осаждения. Осадок подвергали старению при комнатной температуре в течение 17 часов и тщательно промывали 1,3-1,5 л деионизированной воды для удаления NH3 до достижения рН=7-8. Промытый осадок подвергали сушке при температуре 110°С в течение 18-24 часов и прокаливанию при температуре 300°С на воздухе в течение 5 часов и охлаждали до комнатной температуры в течение 2 часов.
(4) Материал с размером частиц менее 90 мкм просеивали и подвергали активации в типичных условиях активации промышленного катализатора, с использованием молярного отношения Н2/СО=1,0, при общей скорости газа 5000 мл/ч/г и температуре 260°С в течение 12 ч, с получением катализатора D5 из карбида железа.
Пример испытаний
(1) Для измерения молярного содержания фаз ε' -Fe2.2С/ ε -Fe2C в активных фазах полученных катализаторов А2-А10 и D1-D5, соответственно, использовали мессбауэровскую спектроскопию. Результаты показаны в таблице 2.
(2) В условиях, включающих молярное отношение реакционных газов Н2/СО=1,5, давление 2,5 МПа, температуру 240°С и общую скорость газа (Н2+СО) 20000 мл/ч/г,
полученные катализаторы А1-А10 и D1-D5 соответственно приводили в контакт с реакционными газами Н2 и СО для проведения реакции синтеза Фишера-Тропша. Активность катализатора и селективность катализаторов по отношению к продуктам отслеживали через 10 ч и 400 ч реакции. Результаты показаны в таблице 3.
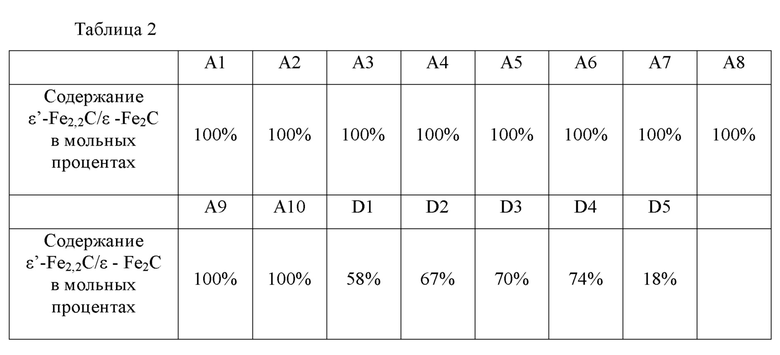
Результаты, представленные в таблице 2, показывают, что чистую фазу ε/ε' карбида железа можно получить способом приготовления согласно изобретению.
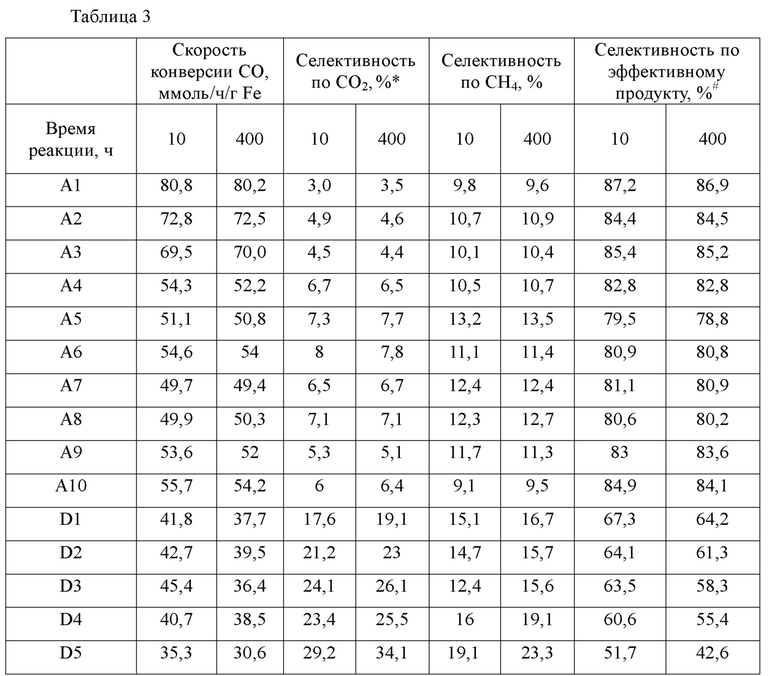
Примечание *: каждая из указанных выше селективностей основана на величине общей конверсии СО; примечание #: селективность по эффективному продукту относится к селективности по продуктам, отличающимся от побочных продуктов СО2 и СН4.
Как видно из результатов, представленных в таблице 3, катализатор из чистой фазы ε/ε' карбида железа, приготовленный способом согласно изобретению, демонстрирует в промышленных условиях сверхнизкую селективность по отношению к СО2, предпочтительно селективность по отношению к СО2 может быть ниже 5%; напротив, селективность по отношению к СО2 катализатора D5 из карбида железа, приготовленного согласно уровню техники, в тех же промышленных условиях составляет 29,2%-34,1%.
Кроме того, селективность по отношению к СН4 катализатора из чистой фазы ε/ε' карбида железа, приготовленного способом согласно изобретению, ниже 14% (предпочтительно ниже 11%), а селективность по отношению к эффективным продуктам может достигать 78% или более (предпочтительно достигать 84% или более); катализатор D5 из карбида железа, приготовленный согласно уровню техники, имеет высокую селективность по отношению к СН4, но селективность по отношению к эффективным продуктам составляет лишь 51,7%, таким образом эффективность использования СО является низкой.
Наконец, при сравнении экспериментальных данных по времени 10 часов и 400 часов результаты показывают, что катализатор из чистой фазы ε/ε' карбида железа, приготовленный способом согласно изобретению, остается стабильным и не показывает видимых изменений как в коэффициенте конверсии СО, так и в селективности по отношению к продуктам после реакции в течение 400 часов; однако различные параметры катализатора D5 из карбида железа, приготовленного согласно уровню техники, очевидно, деградируют, и это показывает, что стабильность катализатора из чистой фазы ε/ε' карбида железа, приготовленного способом согласно изобретению, значительно превосходит стабильность катализатора на основе карбида железа согласно уровню техники.
В приведенном выше описании подробно раскрыты предпочтительные воплощения изобретения, которое, однако, ими не ограничивается. Различные простые модификации могут быть произведены в отношении технических решений настоящего изобретения в рамках технического замысла изобретения, включая сочетание отдельных технических признаков любым другим подходящим образом, и такие простые изменения и их сочетания также следует считать раскрытыми в настоящем описании, каждое из которых попадает в объем охраны данного изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НАНЕСЕННЫЙ КАТАЛИЗАТОР ИЗ ε/ε’ КАРБИДА ЖЕЛЕЗА ДЛЯ РЕАКЦИИ СИНТЕЗА ФИШЕРА-ТРОПША, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И СПОСОБ СИНТЕЗА ФИШЕРА-ТРОПША | 2018 |
|
RU2760367C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА СИНТЕЗА ФИШЕРА-ТРОПША | 2013 |
|
RU2629940C2 |
| Способ получения катализатора для синтеза Фишера-Тропша | 2022 |
|
RU2788375C1 |
| КАТАЛИЗАТОР СИНТЕЗА ФИШЕРА-ТРОПША, СОДЕРЖАЩИЙ НИТРИДНЫЙ НОСИТЕЛЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ, И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2760904C2 |
| СПОСОБ АКТИВАЦИИ КАТАЛИЗАТОРА СИНТЕЗА ФИШЕРА-ТРОПША | 2008 |
|
RU2450044C2 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА ФИШЕРА-ТРОПША И СПОСОБ ПОЛУЧЕНИЯ ЭТОГО КАТАЛИЗАТОРА | 2017 |
|
RU2685437C2 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА ФИШЕРА-ТРОПША И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2325226C1 |
| КАТАЛИЗАТОР ДЛЯ СИНТЕЗА ФИШЕРА-ТРОПША И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2326732C1 |
| КАТАЛИЗАТОР НА ОСНОВЕ Fe ДЛЯ СИНТЕЗА ФИШЕРА-ТРОПША, СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2468863C1 |
| СПОСОБ РЕГЕНЕРАЦИИ КОБАЛЬТОВОГО КАТАЛИЗАТОРА СИНТЕЗА ФИШЕРА-ТРОПША | 2008 |
|
RU2456080C2 |

Изобретение относится к области катализаторов реакции синтеза Фишера-Тропша, и в нем предложен катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, способ его приготовления и способ синтеза Фишера-Тропша, при этом способ приготовления включает следующие стадии: (1) обработка нанометрового порошка железа или нанометрового порошка соединения железа, способного обеспечить получение нанометрового порошка железа с помощью восстановления in-situ и Н2, для очистки поверхности при температуре 250-510°С; (2) предварительная обработка материала, полученного на стадии (1), с использованием H2 и СО при температуре 80-180°С, где молярное отношение H2/СО составляет 1,2-2,8:1; (3) приготовление карбида с использованием материала, полученного на стадии (2), Н2 и СО при температуре 180-280°С, где молярное отношение Н2/СО составляет 1,0-3,0:1, где нанопорошок соединения железа представляет собой по меньшей мере одно вещество, выбранное из группы, состоящей из нанометрового порошка оксида железа, нанометрового порошка магнетита, нанометрового порошка гетита и нанометрового порошка гидроксида железа. Технический результат – возможность приготовления катализатора со 100 %-ной чистой фазой ε/ε' карбида железа, имеющего более низкую селективность по отношению к СО2 и СН4 и более высокую селективность по отношению к полученным продуктам. 3 н. и 12 з.п. ф-лы, 3 табл., 6 ил., 10 пр.
1. Способ приготовления катализатора из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, включающий следующие стадии:
(1) обработка нанометрового порошка железа или нанометрового порошка соединения железа, способного обеспечить получение нанометрового порошка железа с помощью восстановления in-situ и Н2, для очистки поверхности при температуре 250-510°С;
(2) предварительная обработка материала, полученного на стадии (1), с использованием H2 и СО при температуре 80-180°С, где молярное отношение H2/СО составляет 1,2-2,8:1;
(3) приготовление карбида с использованием материала, полученного на стадии (2), Н2 и СО при температуре 180-280°С, где молярное отношение Н2/СО составляет 1,0-3,0:1,
где нанопорошок соединения железа представляет собой по меньшей мере одно вещество, выбранное из группы, состоящей из нанометрового порошка оксида железа, нанометрового порошка магнетита, нанометрового порошка гетита и нанометрового порошка гидроксида железа.
2. Способ по п. 1, где средний диаметр частиц нанометрового порошка железа составляет 4-30 нм.
3. Способ по п. 2, где средний диаметр частиц нанометрового порошка железа составляет 10-27 нм.
4. Способ по п. 1, где на стадии (1) давление при обработке для очистки поверхности составляет 0,1-15 атмосферного давления; время составляет 0,5-8 ч; скорость газа Н2 на стадии (1) составляет 500-20000 мл/ч/г.
5. Способ по п. 4, где на стадии (1) давление при обработке для очистки поверхности составляет 0,2-2,5 атмосферного давления; время составляет 1-7 ч; скорость газа H2 на стадии (1) находится в диапазоне 2500-15000 мл/ч/г.
6. Способ по п. 1, где на стадии (2) давление в процессе предварительной обработки составляет 0,05-7 атмосферного давления; время составляет 15-90 мин; скорость газов H2 и СО на стадии (2) составляет 200-8000 мл/ч/г.
7. Способ по п. 6, где на стадии (2) давление в процессе предварительной обработки составляет 0,05-2,5 атмосферного давления; время составляет 25-75 мин; скорость газов H2 и СО на стадии (2) составляет 1000-6500 мл/ч/г.
8. Способ по п. 1, где на стадии (3) давление при приготовлении карбида составляет 0,09-10 атмосферного давления; время составляет 0,5-10 ч; скорость газов H2 и СО на стадии (3) составляет 200-20000 мл/ч/г.
9. Способ по п. 8, где на стадии (3) давление при приготовлении карбида составляет 0,15-3 атмосферного давления; время составляет 1,5-8 ч; скорость газов Н2 и СО на стадии (3) составляет 4000-15000 мл/ч/г.
10. Способ по п. 1, дополнительно включающий повышение температуры системы после предварительной обработки до 180-280°С при скорости нагревания 0,2-5°С/мин.
11. Способ по п. 10, где температуру системы после предварительной обработки повышают до 200-270°С при скорости нагревания 0,2-2,5°С/мин.
12. Способ по п. 1, где стадии обработки для очистки поверхности, предварительной обработки и приготовления карбида осуществляют в реакторе синтеза Фишера-Тропша.
13. Катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша, полученный способом согласно любому из пп. 1-12.
14. Способ синтеза Фишера-Тропша, включающий приведение сырьевого газа для синтеза в контакт с катализатором в условиях реакции синтеза Фишера-Тропша, где катализатор представляет собой катализатор из чистой фазы ε/ε' карбида железа для реакции синтеза Фишера-Тропша согласно п. 13, где температура находится в диапазоне 235-250°С и давление в диапазоне 2,3-2,5 МПа.
15. Способ по п. 14, где синтез Фишера-Тропша осуществляют в высокотемпературном реакторе высокого давления непрерывного действия.
| CN 105728020 A, 06.07.2016 | |||
| CN 107442147 A, 08.12.2017 | |||
| CN 104399501 A, 11.03.2015 | |||
| CN 105195189 A, 30.12.2015 | |||
| WO 2012135089 A1, 04.10.2012 | |||
| Пресс для обезвоживания картофельной мязги | 1929 |
|
SU28460A1 |
| Пусковое приспособление для компрессоров холодильных установок | 1930 |
|
SU19236A1 |
| KR 20160104546 A, 05.09.2016. | |||
Авторы
Даты
2021-12-02—Публикация
2018-06-21—Подача