Родственные заявки
Данная заявка испрашивает приоритет предварительной заявки на патент США № 62/425907 (№ дела патентного поверенного ALN-260PRO1), поданной 23 ноября 2016 г.; предварительной заявки на патент США № 62/548589 (№ дела патентного поверенного ALN-260PRO2), поданной 22 августа 2017 г.; предварительной заявки на патент США № 62/549099 (№ дела патентного поверенного ALN-273PRO1), поданной 23 августа 2017 г.; и предварительной заявки на патент США № 62/561514 (№ дела патентного поверенного ALN-260PRO3), поданной 21 сентября 2017 г. Полное содержание каждой из вышеупомянутых заявок настоящим включено в данный документ посредством ссылки.
Данная заявка относится к предварительной заявке на патент США № 61/826125, поданной 22 мая 2013 г., предварительной заявке на патент США № 61/898695, поданной 1 ноября 2013 г.; предварительной заявке на патент США № 61/979727, поданной 15 апреля 2014 г.; предварительной заявке на патент США № 61/989028, поданной 6 мая 2014 г.; заявке на патент США № 14/284745, по которой в настоящее время выдан патент США № 9574192 от 21 февраля 2017 г.; заявке на патент США № 15/399820, поданной 6 января 2017 г.; и международной заявке на патент № PCT/US2014/039109, поданной 22 мая 2014 г. Полное содержание каждой из вышеупомянутых заявок настоящим включено в данный документ посредством ссылки.
Перечень последовательностей
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим включен в данный документ посредством ссылки во всей своей полноте. Указанная ASCII-копия, созданная 16 ноября 2017 г., называется 121301-07820_SL.txt, и ее размер составляет 129236 байт.
Уровень техники
Serpina1 кодирует альфа-1-антитрипсин, который преимущественно образует комплекс с нейтрофильной эластазой, продуцируемой гепатоцитами, одноядерными моноцитами, альвеолярными макрофагами, энтероцитами и миелоидными клетками, а также ингибирует ее активность. Субъекты, имеющие вариации в одной или обеих копиях гена Serpina1, могут страдать недостаточностью альфа-1-антитрипсина и подвергаются риску развития эмфиземы легких и/или хронического заболевания печени из-за превышающей нормальную активности эластазы в легких и печени.
У пораженных заболеванием субъектов дефицит альфа-1-антитрипсина является дефицитом функционального альфа-1-антитрипсина дикого типа. В одних случаях субъект с вариацией в одной или обеих копиях гена Serpina1 несет нулевой аллель. В других случаях субъект с вариацией в одной или обеих копиях гена Serpina1 несет дефектный аллель.
Например, у субъекта с дефектным аллелем Serpina1, таким как аллель PIZ, могут продуцироваться неправильно свернутые белки, которые не могут надлежащим образом транспортироваться из участка синтеза в участок действия в организме. Такие субъекты, как правило, подвергаются риску развития заболевания легких и/или печени. Субъекты с нулевым аллелем Serpina1, таким как PINULL (Granite Falls), как правило, подвергаются риску развития только заболевания легкого.
Заболевание печени, возникающее из-за дефицита альфа-1-антитрипсина, обусловлено вариантными формами альфа-1-антитрипсина, продуцируемого в клетках печени, являющегося неправильно свернутым и, таким образом, с трудом транспортируемого из клеток. Это ведет к накоплению неправильно свернутого белка в клетках печени и может вызвать одно или несколько заболеваний или нарушений функции печени, в том числе без ограничения хроническое заболевание печени, воспаление печени, цирроз, фиброз печени и/или гепатоцеллюлярную карциному.
На данный момент имеются довольно ограниченные возможности лечения пациентов с болезнью печени, возникающей из-за недостаточности альфа-1-антитрипсина, включающие вакцинацию против гепатита, поддерживающее лечение и избегание наносящих вред средств (например, спирта и NSAID). Хотя существует замещающая альфа-1-антитрипсин терапия, подобное лечение не оказывает влияния на заболевание печени у таких субъектов, и, несмотря на то, что эффективной может быть трансплантация печени, она является трудной, дорогой и рискованной процедурой, к тому же печень является не всегда имеющимся в наличие органом.
Следовательно, в данной области техники существует потребность в эффективных методах лечения ассоциированных с Serpina1 заболеваний, таких как хроническое заболевание печени, воспаление печени, цирроз, фиброз печени и/или гепатоцеллюлярная карцинома.
Краткое описание изобретения
Как описано более подробно ниже, в данном документе раскрыты композиции, содержащие средства, например средства для RNAi, например средства на основе двухнитевой iRNA, нацеливающиеся на Serpina1. Также раскрыты способы применения композиций согласно настоящему изобретению для ингибирования экспрессии Serpina1 и для лечения ассоциированных c Serpina1 заболеваний, например, хронического заболевания печени, воспаления печени, цирроза, фиброза печени и/или гепатоцеллюлярной карциномы.
Настоящее изобретение основано, по меньшей мере частично, на обнаружении эффективных нуклеотидных или химических мотивов для средств на основе dsRNA, нацеливающихся на Serpina1, которые характеризуются преимуществом в отношении ингибирования экспрессии целевого гена, хотя и обладают сниженными эффектами сайленсинга нецелевых генов, а также на композициях, содержащих такие средства, которые подходят для терапевтического применения. Более конкретно, было обнаружено, среди прочего, что средства на основе dsRNA, нацеливающиеся на Serpina1, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и/или средство на основе dsRNA, характеризующееся температурой плавления в диапазоне от приблизительно 40°C до приблизительно 80°C, могут быть более эффективными в опосредовании РНК-интерференции, чем исходное средство на основе dsRNA, не имеющее дестабилизирующей модификации.
Соответственно, в одном аспекте настоящего изобретения предусмотрено средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию последовательности целевого гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию в пределах первых 9 положений нуклеотидов 5′-области или ее предшественника, при этом указанная смысловая нить содержит лиганд асиалогликопротеинового рецептора (ASGPR), и при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов.
В другом аспекте настоящего изобретения предусмотрено средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок, где смысловая нить содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:1, и антисмысловая нить содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:15, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию двухнитевого участка в пределах первых 9 положений нуклеотидов 5′-области или ее предшественника, при этом указанная смысловая нить содержит лиганд асиалогликопротеинового рецептора (ASGPR), и при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов.
В еще одном аспекте настоящего изобретения предусмотрено средство на основе двухнитевой (dsRNA) РНК, которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок, причем указанная антисмысловая нить содержит участок комплементарности с mRNA, кодирующей Serpina1, где участок комплементарности содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:15, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию в пределах первых 9 положений нуклеотидов 5′-области или ее предшественника, при этом указанная смысловая нить содержит лиганд асиалогликопротеинового рецептора (ASGPR), при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов.
В одном варианте осуществления средство на основе dsRNA содержит по меньшей мере четыре нуклеотида, содержащие 2'-фтор-модификацию.
В одном варианте осуществления средство на основе dsRNA соответствует следующим характеристикам: a) нарушающая термостабильность модификация находится в положении 4-8 5′-области антисмысловой нити; b) и каждая из смысловой и антисмысловой нитей независимо содержит по меньшей мере два нуклеотида, содержащих 2'-фтор-модификацию; и c) лиганд ASGPR присоединен к каждому из концов смысловой нити.
В другом варианте осуществления антисмысловая нить соответствует по меньшей мере двум из следующих характеристик: a) нарушающая термостабильность модификация находится в положении 4-8 антисмысловой нити; b) по меньшей мере два нуклеотида содержат 2'-фтор-модификацию; c) фосфотиоатные межнуклеотидные связи находятся между положениями нуклеотидов 1 и 2 (считая от 5'-конца); d) длина составляет от 18 до 35 нуклеотидов.
В одном варианте осуществления смысловая нить соответствует по меньшей мере одной из следующих характеристик:
a) лиганд ASGPR присоединен к каждому из концов смысловой нити; b) по меньшей мере два нуклеотида содержат 2'-фтор-модификацию; c) смысловая нить и антисмысловая нить образуют двухнитевой участок, охватывающий по меньшей мере 19 положений нуклеотидов, и при этом нарушающая термостабильность модификация находится в пределах указанного двухнитевого участка.
В одном варианте осуществления нарушающая термостабильность модификация выбрана из группы, состоящей из
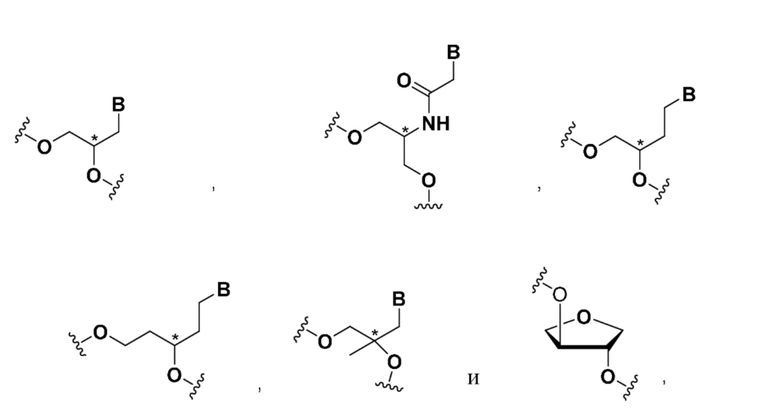
где B представляет собой нуклеотидное основание.
В одном варианте осуществления дестабилизирующая модификация находится в положении 7 антисмысловой нити.
В одном варианте осуществления лиганд ASGPR представляет собой одно или несколько производных GalNAc, присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В одном варианте осуществления лиганд ASGPR представляет собой:
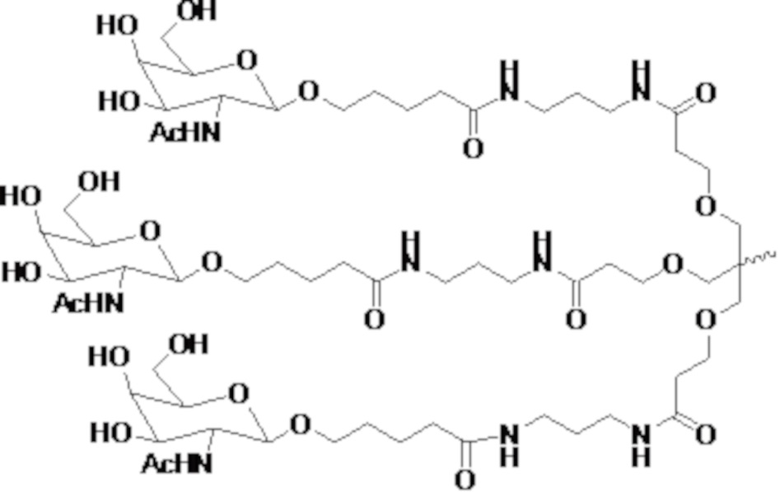 .
.
В одном варианте осуществления средство на основе dsRNA конъюгировано с лигандом, как показано на следующей схеме:
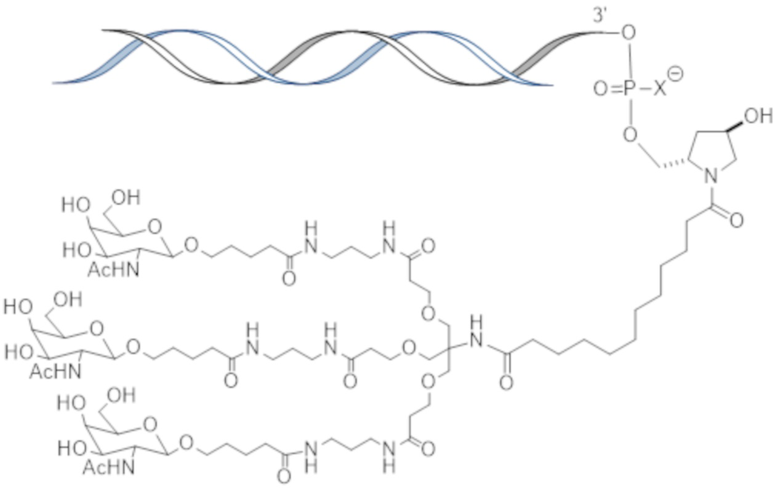 ,
,
где X представляет собой O или S.
В одном аспекте настоящего изобретения предусмотрено средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию последовательности целевого гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности для опосредования РНК-интерференции, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию в пределах первых 9 положений нуклеотидов 5′-области, при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В другом аспекте настоящего изобретения предусмотрено средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию последовательности целевого гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, где смысловая нить содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:1, и антисмысловая нить содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:15, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию в пределах первых 9 положений нуклеотидов 5′-области, при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В еще одном аспекте настоящего изобретения предусмотрено средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию последовательности целевого гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, причем указанная антисмысловая нить содержит участок комплементарности с mRNA, кодирующей Serpina1, где участок комплементарности содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности под SEQ ID NO:15, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию в пределах первых 9 положений нуклеотидов 5′-области, при этом каждая из смысловой нити и антисмысловой нити независимо имеет длину от 14 до 40 нуклеотидов, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В одном варианте осуществления средство на основе dsRNA характеризуется температурой плавления от приблизительно 55°C до приблизительно 67°C. В другом варианте осуществления средство на основе dsRNA характеризуется температурой плавления от приблизительно 60°C до приблизительно 67°C.
В одном варианте осуществления средство на основе dsRNA дополнительно содержит лиганд асиалогликопротеинового рецептора (ASGPR).
В одном варианте осуществления лиганд ASGPR представляет собой одно или несколько производных GalNAc, присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В одном варианте осуществления лиганд ASGPR представляет собой:
 .
.
В одном варианте осуществления средство на основе dsRNA конъюгировано с лигандом, как показано на следующей схеме:
 ,
,
где X представляет собой O или S.
В одном варианте осуществления средство на основе dsRNA дополнительно соответствует по меньшей мере одной из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 нуклеотидов, содержащих 2'-фтор-модификации, (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 нуклеотидов, содержащих 2'-фтор-модификацию; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре нуклеотида, содержащих 2'-фтор-модификацию; (vii) dsRNA содержит двухнитевой участок участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) тупой конец на 5'-конце антисмысловой нити.
В определенном варианте осуществления каждая нить средства на основе dsRNA может содержать 15-30 нуклеотидов, 19-30 нуклеотидов; или смысловая нить может содержать 21 нуклеотид, и антисмысловая нить может содержать 23 нуклеотида.
В одном варианте осуществления антисмысловая нить содержит участок комплементарности, содержащий по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидов 1440-1480 из SEQ ID NO:1; или нуклеотидов 1441-1479 из SEQ ID NO:1; или нуклеотидов 1442-1478 из SEQ ID NO:1; или нуклеотидов 1443-1477 из SEQ ID NO:1; или нуклеотидов 1444-1476 из SEQ ID NO:1; или нуклеотидов 1445-1475 из SEQ ID NO:1; или нуклеотидов 1446-1474 из SEQ ID NO:1; или нуклеотидов 1447-1473 из SEQ ID NO:1; или нуклеотидов 1448-1473 из SEQ ID NO:1; или нуклеотидов 1448-1472 из SEQ ID NO:1; или нуклеотидов 1448-1471 из SEQ ID NO:1; или нуклеотидов 1448-1470 из SEQ ID NO:1; или нуклеотидов 1447-1469 из SEQ ID NO:1; или нуклеотидов 1446-1478 из SEQ ID NO:1; или нуклеотидов 1449-1471 из SEQ ID NO:1; или нуклеотидов 1450-1472 из SEQ ID NO:1; или нуклеотидов 1440-1475 из SEQ ID NO:1; или нуклеотидов 1445-1480 из SEQ ID NO:1; или нуклеотидов 1445-1475 из SEQ ID NO:1.
В одном варианте осуществления участок комплементарности содержит по меньшей мере 15 смежных нуклеотидов, отличающихся не более чем 3 нуклеотидами от нуклеотидной последовательности 5' - UUUUGUUCAAUCAUUAAGAAGAC - 3' (SEQ ID NO: 419).
В одном варианте осуществления смысловая нить содержит нуклеотидную последовательность 5' - CUUCUUAAUGAUUGAACAAAA - 3' (SEQ ID NO: 417), и антисмысловая нить содержит нуклеотидную последовательность 5' - UUUUGUUCAAUCAUUAAGAAGAC - 3' (SEQ ID NO: 419).
В одном варианте осуществления смысловая нить содержит нуклеотидную последовательность
5' - csusucuuAfaUfGfAfuugaacaaaa - 3' (SEQ ID NO: 33), и антисмысловая нить содержит нуклеотидную последовательность 5' - usUfsuugu(Tgn)caaucaUfuAfagaagsasc - 3' (SEQ ID NO: 34), где a, g, c и u представляют собой 2'-O-метил-модифицированные (2'-OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′-фтор-модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S-изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA).
В одном аспекте настоящего изобретения предусмотрена молекула двухнитевой РНК (dsRNA), которая ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащая смысловую нить и антисмысловую нить, образующие двухнитевой участок, где смысловая нить содержит нуклеотидную последовательность 5' - csusucuuAfaUfGfAfuugaacaaaaL96-3' (SEQ ID NO: 35), и антисмысловая нить содержит нуклеотидную последовательность 5' - usUfsuugu(Tgn)caaucaUfuAfagaagsasc - 3' (SEQ ID NO: 34), где a, g, c и u представляют собой 2'-O-метил-модифицированные (2'-OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′-фтор-модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; (Tgn) представляет собой S-изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA); и L96 представляет собой N-[трис(GalNAc-алкил)-амидодеканоил)]-4-гидроксипролинол.
В одном аспекте настоящего изобретения предусмотрено средство на основе dsRNA, которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и dsRNA дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи, восьми или всем девяти) из следующих характеристик: (i) температура плавления (Tm) составляет от приблизительно 40°C до приблизительно 80°C; (ii) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (iii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iv) смысловая нить конъюгирована с лигандом; (v) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (vi) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vii) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (viii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (ix) тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления настоящего изобретения предусмотрено средство на основе dsRNA, которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и dsRNA дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи, восьми или всем девяти) из следующих характеристик: (i) температура плавления (Tm) составляет от приблизительно 40°C до приблизительно 80°C; (ii) антисмысловая нить содержит 6, 7, 8, 9, 10, 11 или 12 2'-OMe-модификаций; (iii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iv) смысловая нить конъюгирована с лигандом; (v) смысловая нить содержит 6, 7, 8, 9, 10, 11 или 12 2'-OMe-модификаций; (vi) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vii) dsRNA содержит по меньшей мере 1, 2, 3, 4 или 5 2'-дезокси-модификаций; (viii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (ix) тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления dsRNA характеризуется температурой плавления, находящейся в пределах нижней границы диапазона приблизительно 40°C, 45°C, 50°C, 55°C, 60°C или 65°C и верхней границы диапазона приблизительно 70°C, 75°C или 80°C. В некоторых вариантах осуществления dsRNA характеризуется температурой плавления в диапазоне от приблизительно 55°C до приблизительно 70°C. В некоторых вариантах осуществления dsRNA характеризуется температурой плавления в диапазоне от приблизительно 57°C до приблизительно 67°C. В некоторых конкретных вариантах осуществления dsRNA характеризуется температурой плавления в диапазоне от приблизительно 60°C до приблизительно 67°C. В некоторых дополнительных вариантах осуществления dsRNA характеризуется температурой плавления в диапазоне от приблизительно 62°C до приблизительно 66°C.
Также было установлено, что средства на основе dsRNA, характеризующиеся температурой плавления, составляющей по меньшей мере 60°C, являются более эффективными in vivo и in vitro. Таким образом, в некоторых вариантах осуществления dsRNA характеризуется температурой плавления, составляющей по меньшей мере 60°C.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), причем dsRNA характеризуется температурой плавления (Tm) от приблизительно 40°C до приблизительно 80°C, и dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двумя, тремя, четырьмя, пятью, шестью, семью, или всеми восемью) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5'-конца), и dsRNA характеризуется значением Tm от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и vii) тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C (например, 40°C, 50°C, 60°C, 70°C или 80°C).
В некоторых конкретных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 5, 6, 7 или 8 антисмысловой нити, считая от 5'-конца антисмысловой нити.
В некоторых конкретных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 6 антисмысловой нити, считая от 5'-конца антисмысловой нити.
В некоторых конкретных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 7 антисмысловой нити, считая от 5'-конца антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и антисмысловая нить дополнительно соответствует одной или обеим из следующих характеристик:
(i) 2, 3, 4, 5 или 6 2'-фтор-модификаций; и
(ii) 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и
смысловая нить предусматривает одну, две или три из следующих характеристик:
(i) лиганд конъюгирован со смысловой нитью;
(ii) 2, 3, 4 или 5 2'-фтор-модификаций; и
(iii) 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5′-конца, и лиганд конъюгирован со смысловой нитью, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5′-конца, причем лиганд конъюгирован со смысловой нитью, и dsRNA содержит по меньшей мере четыре 2'-фтор-модификации.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, причем указанная смысловая нить содержит лиганд, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C. В некоторых дополнительных вариантах осуществления настоящего изобретения лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 4-8, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C. В некоторых дополнительных вариантах осуществления настоящего изобретения лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом антисмысловая нить дополнительно соответствует по меньшей мере двум из следующих характеристик: (i) нарушающая термостабильность модификация дуплекса находится в положении 4-8 антисмысловой нити; (ii) по меньшей мере две 2'-фтор-модификации; (iii) фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 (считая от 5'-конца); и антисмысловая нить имеет длину, составляющую от 18 до 35 нуклеотидов. В некоторых дополнительных вариантах осуществления лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и смысловая нить обладает по меньшей мере одной из следующих характеристик: (i) лиганд присоединен к каждому из концов смысловой нити; (ii) смысловая нить содержит по меньшей мере две 2'-фтор-модификации; и (iii) смысловая нить и антисмысловая нить характеризуются достаточной комплементарностью для образования двухнитевого участка, охватывающего по меньшей мере 19 положений нуклеотидов, и при этом нарушающая термостабильность модификация дуплекса находится в пределах указанного двухнитевого участка.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
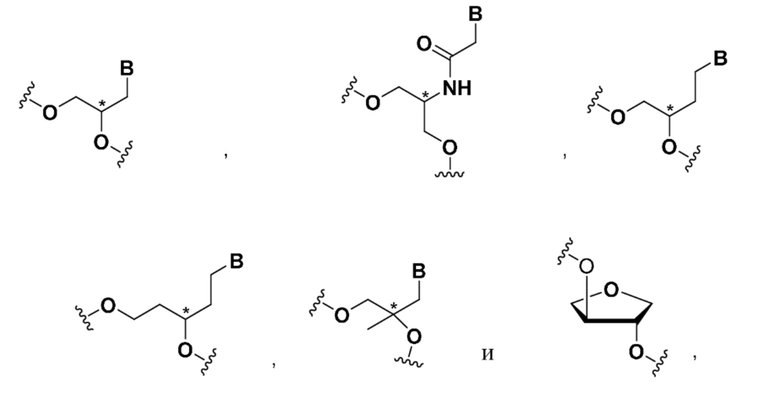
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 4-8, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, и при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
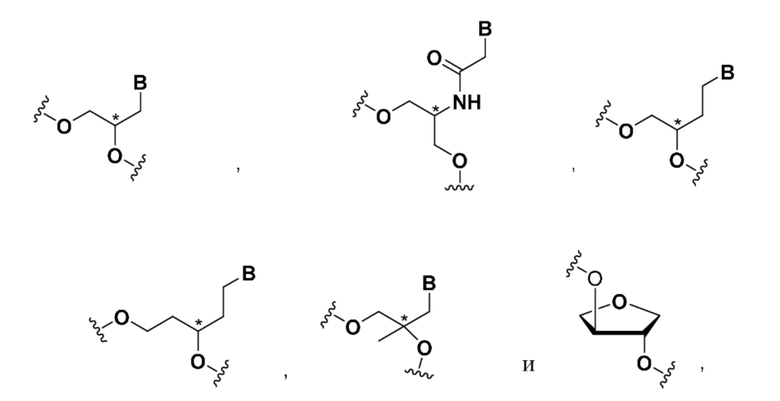
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 7, считая от 5'-конца антисмысловой нити, при этом указанная смысловая нить содержит лиганд, и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 7, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, и при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
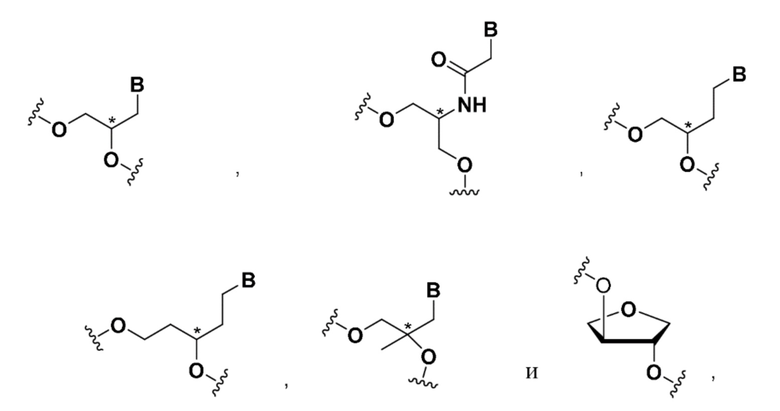
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет собой либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом лиганд предусматривает одно или несколько производных GalNAc, присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом лиганд представляет собой лиганд ASGPR со структурой:
 .
.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0, 1 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 3, 4, 5 или 6 2'-фтор-модификаций, содержит 2, 3 или 4 фосфотиоатные межнуклеотидные связи; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 3, 4, 5 или 6 2'-фтор-модификаций, содержит 2, 3 или 4 фосфотиоатные межнуклеотидные связи; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22, между положениями нуклеотидов 22 и 23, между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 18, 19, 21, 22, 23, 24 или 24 пары нуклеотидов; и (viii) dsRNA содержит тупой конец на 5'-конце смысловой нити. В некоторых конкретных вариантах осуществления смысловая нить имеет длину 19, 20, или 21, или 22 нуклеотида, и антисмысловая нить имеет длину 20, 21 или 22 нуклеотида.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22, между положениями нуклеотидов 22 и 23, между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3; при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления один конец dsRNA представляет собой тупой конец, а другой конец предусматривает «липкий» конец, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) и dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов. В некоторых вариантах осуществления «липкий» конец находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити. В некоторых конкретных вариантах осуществления «липкий» конец имеет длину 2, 3 или 4 нуклеотида.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, где один конец dsRNA представляет собой тупой конец, а другой конец предусматривает «липкий» конец, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти или всем шести) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, и необязательно «липкий» конец из 2 нуклеотидов находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити. В некоторых вариантах осуществления «липкий» конец находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению может также иметь два тупых конца на обоих концах dsRNA-дуплекса.
В некоторых вариантах осуществления dsRNA предусматривает тупой конец на обоих концах дуплекса, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, и предусматривает тупой конец на обоих концах дуплекса, где один конец dsRNA представляет собой тупой конец, а другой конец предусматривает «липкий» конец, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти или всем шести) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую нить из 21 нуклеотида (нт) и антисмысловую нить из 23 нуклеотидов (нт), где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом один конец dsRNA является тупым, в то время как другой конец предусматривает «липкий» конец из 2 нт, при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити. Предпочтительно «липкий» конец из 2 нт находится на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую и антисмысловую нити, где длина смысловой нити составляет 25-30 нуклеотидных остатков, при этом, считая от 5'-концевого нуклеотида (положение 1), в положениях 1-23 указанной смысловой нити содержится по меньшей мере 8 рибонуклеотидов; длина антисмысловой нити составляет 36-66 нуклеотидных остатков, и, считая от 3'-концевого нуклеотида, она содержит по меньшей мере 8 рибонуклеотидов в положениях, спаренных с положениями 1-23 смысловой нити, с образованием дуплекса; при этом по меньшей мере 3'-концевой нуклеотид антисмысловой нити является неспаренным со смысловой нитью, и не более 6 последовательных 3'-концевых нуклеотидов являются неспаренными со смысловой нитью, образуя тем самым 3'-однонитевой «липкий» конец из 1-6 нуклеотидов; при этом 5'-конец антисмысловой нити содержит 10-30 последовательных нуклеотидов, неспаренных со смысловой нитью, образуя тем самым 5'-однонитевой «липкий» конец из 10-30 нуклеотидов; при этом по меньшей мере 5'-концевые и 3'-концевые нуклеотиды смысловой нити образуют пары оснований с нуклеотидами антисмысловой нити, если смысловая и антисмысловая нити выровнены с обеспечением максимальной комплементарности, образуя тем самым практически дуплексный участок между смысловой и антисмысловой нитями; и антисмысловая нить в достаточной степени комплементарна целевой РНК на протяжении по меньшей мере 19 рибонуклеотидов по длине антисмысловой нити для снижения экспрессии целевого гена Serpina1 при введении указанной двухнитевой нуклеиновой кислоты в клетку млекопитающего; и при этом антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т. е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C. Например, нарушающий термостабильность нуклеотид находится между положениями, являющимися противоположными или комплементарными положениям 14-17 5'-конца смысловой нити, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-30 пар нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую и антисмысловую нити, где указанное средство на основе dsRNA содержит смысловую нить, длина которой составляет по меньшей мере 25 и не более 29 нуклеотидов, и антисмысловую нить, длина которой составляет не более 30 нуклеотидов, при этом смысловая нить содержит модифицированный нуклеотид, придающей чувствительность к ферментативному расщеплению, в положении 11 от 5'-конца, при этом 3'-конец указанной смысловой нити и 5'-конец указанной антисмысловой нити образуют тупой конец, и указанная антисмысловая нить на своем 3'-конце на 1-4 нуклеотида длиннее, чем смысловая нить, при этом длина дуплексного участка составляет по меньшей мере 25 нуклеотидов, и указанная антисмысловая нить в достаточной степени комплементарна целевой mRNA Serpina1 на протяжении по меньшей мере 19 нт по длине указанной антисмысловой нити для снижения экспрессии целевого гена при введении указанного средства на основе dsRNA в клетку млекопитающего, и при этом расщепление указанной dsRNA под действием Dicer предпочтительно приводит к siRNA, содержащей указанный 3'-конец указанной антисмысловой нити, за счет чего обеспечивается снижение экспрессии целевого гена у млекопитающего, при этом антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-29 пар нуклеотидов.
В некоторых вариантах осуществления антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) смысловая нить конъюгирована с лигандом; (iii) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (iv) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (v) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vi) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3, антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), при этом dsRNA характеризуется температурой плавления от приблизительно 40°C до приблизительно 80°C, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) смысловая нить конъюгирована с лигандом; (iii) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (iv) смысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (v) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vi) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (vii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В одном аспекте настоящего изобретения предусмотрено средство на основе dsRNA, способное к ингибированию экспрессии целевой последовательности Serpina1, например нуклеотидов 1440-1480 из SEQ ID NO:1, содержащее смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и dsRNA дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик:
(i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций;
(ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи;
(iii) смысловая нить конъюгирована с лигандом;
(iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций;
(v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи;
(vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации;
(vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и
(viii) тупой конец - на 5'-конце антисмысловой нити.
В некоторых конкретных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 7 антисмысловой нити, считая от 5'-конца антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и антисмысловая нить дополнительно предусматривает одну или несколько из следующих характеристик:
(iii) 2, 3, 4, 5 или 6 2'-фтор-модификаций; и
(iv) 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и
смысловая нить предусматривает одну, две или три из следующих характеристик:
(iv) лиганд, конъюгирован со смысловой нитью;
(v) 2, 3, 4 или 5 2'-фтор-модификаций и
(vi) 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5′-конца, и лиганд конъюгирован со смысловой нитью.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, и при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5′-конца, причем лиганд конъюгирован со смысловой нитью, и dsRNA содержит по меньшей мере четыре 2'-фтор-модификации.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд. В некоторых дополнительных вариантах осуществления настоящего изобретения лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 4-8, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, и при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации. В некоторых дополнительных вариантах осуществления настоящего изобретения лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, и при этом антисмысловая нить дополнительно предусматривает по меньшей мере две из следующих характеристик: (i) нарушающая термостабильность модификация дуплекса находится в положении 4-8 антисмысловой нити; (ii) по меньшей мере две 2'-фтор-модификации; (iii) фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 (считая от 5'-конца); и антисмысловая нить имеет длину, составляющую от 18 до 35 нуклеотидов. В некоторых дополнительных вариантах осуществления лиганд представляет собой лиганд ASGPR.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, и смысловая нить соответствует по меньшей мере одной из следующих характеристик: (i) лиганд присоединен к каждому из концов смысловой нити; (ii) смысловая нить содержит по меньшей мере две 2'-фтор-модификации; и (iii) смысловая нить и антисмысловая нить характеризуются достаточной комплементарностью для образования двухнитевого участка, охватывающего по меньшей мере 19 положений нуклеотидов, и при этом нарушающая термостабильность модификация дуплекса находится в пределах указанного двухнитевого участка.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
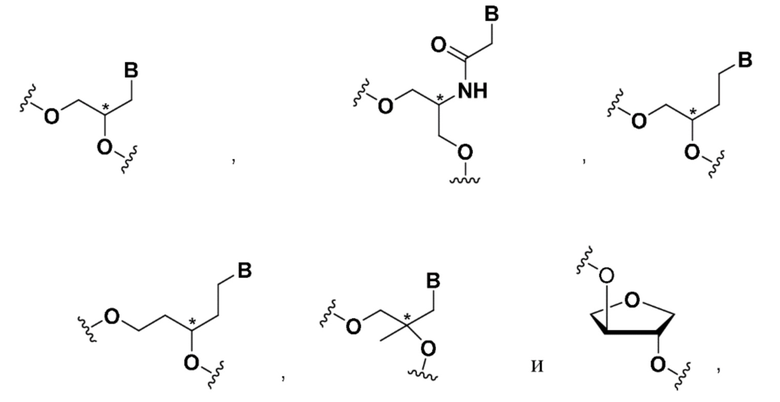
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет собой либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 4-8, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, и при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
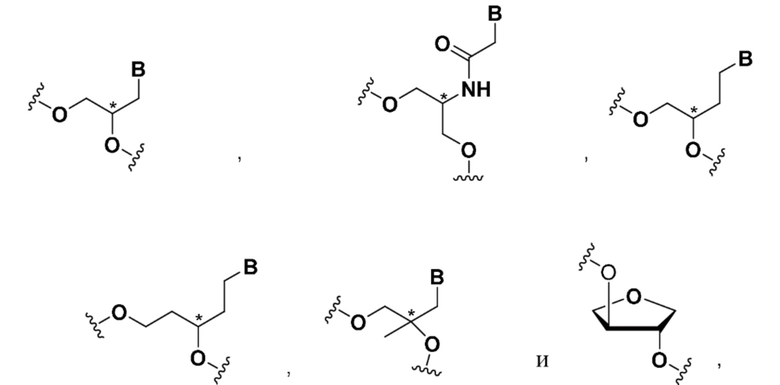
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет собой либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 7, считая от 5'-конца антисмысловой нити, и при этом указанная смысловая нить содержит лиганд.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в положении 7, считая от 5'-конца, при этом указанная смысловая нить содержит лиганд, и при этом каждая из смысловой и антисмысловой нитей содержит по меньшей мере две 2'-фтор-модификации, и при этом нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
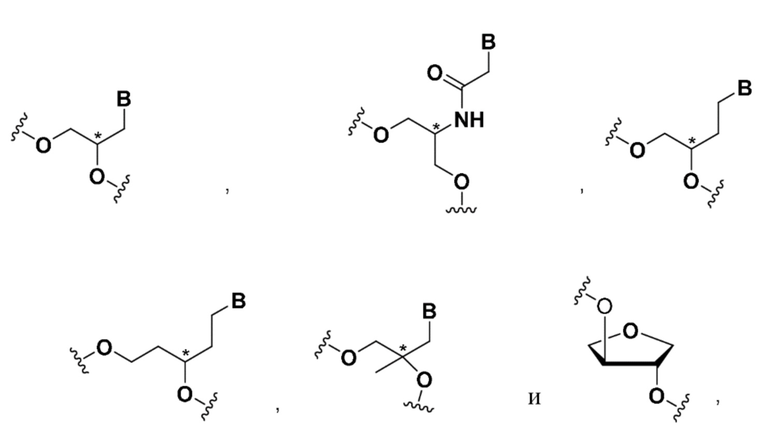
где B представляет собой модифицированное или немодифицированное нуклеотидное основание, и звездочка на каждой структуре представляет либо R, S, либо рацемическое соединение.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, где лиганд предусматривает одно или несколько производных GalNAc, присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В некоторых вариантах осуществления средство на основе dsRNA содержит смысловую нить и антисмысловую нить, причем каждая нить содержит от 14 до 40 нуклеотидов, где антисмысловая нить характеризуется достаточной комплементарностью к целевой последовательности Serpina1, например нуклеотидам 1440-1480 из SEQ ID NO:1, для опосредования РНК-интерференции, при этом dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, при этом указанная антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов, считая от 5'-конца, и при этом указанная смысловая нить содержит лиганд, где лиганд представляет собой лиганд ASGPR со структурой:
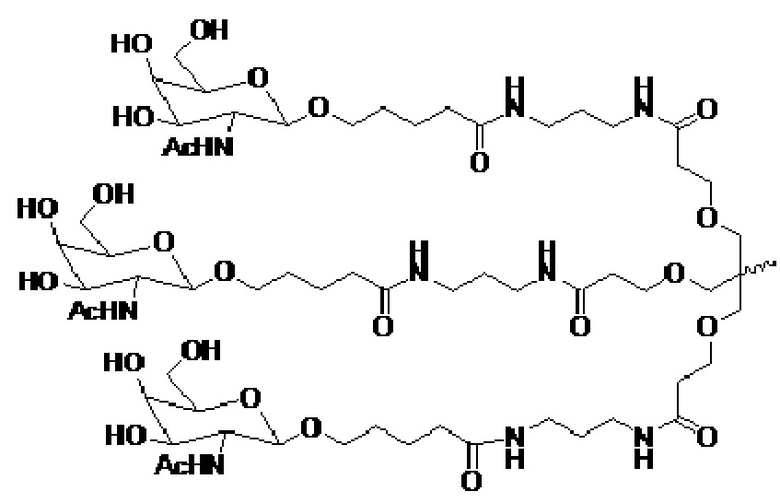 .
.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0, 1 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 3, 4, 5 или 6 2'-фтор-модификаций, содержит 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 3, 4, 5 или 6 2'-фтор-модификаций, содержит 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 3 или 4 2'-фтор-модификации и содержит 0 или 2 фосфотиоатные межнуклеотидные связи; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22, между положениями нуклеотидов 22 и 23, между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; причем антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); при этом смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум или всем трем) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов; антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, причем по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити); смысловая нить конъюгирована с лигандом, содержит 2'-фтор-модификации в положениях 7, 10 и 11 или в положениях 7, 9, 10 и 11 (считая от 5'-конца смысловой нити) и необязательно содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3; при этом антисмысловая нить содержит 2'-фтор-модификации в положениях 2, 6, 8, 9, 14 или 16, или в положениях 2, 6, 14 или 16, или в положениях 2, 14 и 16; и антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22, между положениями нуклеотидов 22 и 23, между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3; и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, две или все три) из следующих характеристик: (i) dsRNA содержит дуплексный участок с длиной, составляющей 12-25 пар нуклеотидов; (ii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити; и (iii) dsRNA имеет «липкий» конец из по меньшей мере двух нуклеотидов на 3'-конце антисмысловой нити.
В конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) длиной, составляющей 21 нуклеотид;
(ii) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера; и
(iii) 2'-F-модификациями в положениях 7, 10 и 11 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) длиной, составляющей 23 нуклеотида;
(ii) 2'-F-модификациями в положениях 2, 6-8, 9, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) длиной, составляющей 21 нуклеотид;
(ii) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера;
(iii) 2'-F-модификациями в положениях 7, 9, 10 и 11 (считая от 5'-конца); и
(iv) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) длиной, составляющей 23 нуклеотида;
(ii) 2'-F-модификациями в положениях 2, 6, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) длиной, составляющей 21 нуклеотид;
(ii) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера;
(iii) 2'-F-модификациями в положениях 7, 9, 10 и 11 (считая от 5'-конца); и
(iv) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) длиной, составляющей 23 нуклеотида;
(ii) 2'-F-модификациями в положениях 2, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 6 или 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) длиной, составляющей 21 нуклеотид;
(ii) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера;
(iii) 2'-F-модификациями в положениях 7, 9, 10 и 11 (считая от 5'-конца); и
(iv) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) длиной, составляющей 23 нуклеотида;
(ii) 2'-F-модификациями в положениях 2, 6, 8, 9, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) длиной, составляющей 21 нуклеотид;
(ii) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера;
(iii) 2'-F-модификациями в положениях 7, 9, 10 и 11 (считая от 5'-конца); и
(iv) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) длиной, составляющей 23 нуклеотида;
(ii) 2'-F-модификациями в положениях 2, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат антисмысловую нить, характеризующуюся:
(i) 2'-F-модификациями в положениях 2, 14 и 16 (считая от 5'-конца); и
(2) нарушающей термостабильность модификацией дуплекса в положении 6 или 7 (считая от 5'-конца).
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) лигандом ASGPR, где указанный лиганд ASGPR;
(ii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(i) 2'-F-модификациями в положениях 2, 14 и 16 (считая от 5'-конца);
(ii) нарушающей термостабильность модификацией дуплекса в положении 6 или 7 (считая от 5'-конца).
В другом конкретном варианте осуществления средства на основе dsRNA по настоящему изобретению содержат:
(a) смысловую нить, характеризующуюся:
(i) лигандом ASGPR, присоединенным к 3'-концу, где указанный лиганд ASGPR содержит три производных GalNAc, присоединенных посредством трехвалентного разветвленного линкера;
(ii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3 (считая от 5'-конца);
и
(b) антисмысловую нить, характеризующуюся:
(ii) 2'-F-модификациями в положениях 2, 14 и 16 (считая от 5'-конца);
(iii) фосфотиоатными межнуклеотидными связями между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23 (считая от 5'-конца); и
(iv) нарушающей термостабильность модификацией дуплекса в положении 6 или 7 (считая от 5'-конца);
где средства на основе dsRNA имеют «липкий» конец из двух нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA дополнительно содержит по меньшей мере один лиганд ASGPR. Например, лиганд ASGPR представляет собой одно или несколько производных GalNAc, присоединенных посредством двухвалентного или трехвалентного разветвленного линкера, например:
 .
.
В одном примере лиганд ASGPR присоединен к 3-концу смысловой нити.
Участок mRNA Serpina1, на который направлено воздействие любого из средств на основе dsRNA, описанных в данном документе, может представлять собой нуклеотиды 1440-1480 из SEQ ID NO:1; или нуклеотиды 1441-1479 из SEQ ID NO:1; или нуклеотиды 1442-1478 из SEQ ID NO:1; или нуклеотиды 1443-1477 из SEQ ID NO:1; или нуклеотиды 1444-1476 из SEQ ID NO:1; или нуклеотиды 1445-1475 из SEQ ID NO:1; или нуклеотиды 1446-1474 из SEQ ID NO:1; или нуклеотиды 1447-1473 из SEQ ID NO:1; или нуклеотиды 1448-1473 из SEQ ID NO:1; или нуклеотиды 1448-1472 из SEQ ID NO:1; или нуклеотиды 1448-1471 из SEQ ID NO:1; или нуклеотиды 1448-1470 из SEQ ID NO:1; или нуклеотиды 1447-1469 из SEQ ID NO:1; или нуклеотиды 1446-1478 из SEQ ID NO:1; или нуклеотиды 1449-1471 из SEQ ID NO:1; или нуклеотиды 1450-1472 из SEQ ID NO:1; или нуклеотиды 1440-1475 из SEQ ID NO:1; или нуклеотиды 1445-1480 из SEQ ID NO:1; или нуклеотиды 1445-1475 из SEQ ID NO:1.
Настоящее изобретение также предусматривает векторы, клетки и фармацевтические композиции, содержащие средства на основе dsRNA согласно настоящему изобретению.
Фармацевтические композиции по настоящему изобретению могут представлять собой незабуференный раствор, например, солевой раствор или воду; или буферный раствор, например, буферный раствор, содержащий ацетат, цитрат, проламин, карбонат, или фосфат, или любую их комбинацию, или фосфатно-солевой буферный раствор (PBS).
В одном аспекте настоящего изобретения предусмотрен способ ингибирования экспрессии Serpina1 в клетке. Способ предусматривает приведение клетки в контакт с любым из вышеупомянутых средств на основе dsRNA или фармацевтической композицией по настоящему изобретению, за счет чего обеспечивается ингибирование экспрессии гена Serpina1 в клетке.
В одном варианте осуществления клетка находится в организме субъекта, такого как субъект-человек.
В одном варианте осуществления экспрессия Serpina1 ингибируется на по меньшей мере приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 95%, приблизительно 98% или приблизительно 100%.
В одном аспекте настоящего изобретения предусмотрен способ лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание. Способ предусматривает введение субъекту терапевтически эффективного количества любого из вышеупомянутых средств на основе dsRNA или фармацевтической композиции по настоящему изобретению, за счет чего осуществляется лечение указанного субъекта.
В одном варианте осуществления субъектом является человек.
В одном варианте осуществления ассоциированное с Serpina1 заболевание представляет собой нарушение функции печени.
В одном варианте осуществления нарушение функции печени выбрано из группы, состоящей из хронического заболевания печени, воспаления печени, цирроза, фиброза печени и/или гепатоцеллюлярной карциномы.
В другом аспекте настоящего изобретения предусмотрен способ ингибирования развития гепатоцеллюлярной карциномы у субъекта с дефектным вариантом Serpina1. Способ предусматривает введение субъекту терапевтически эффективного количества любого из вышеупомянутых средств на основе dsRNA или фармацевтической композиции по настоящему изобретению, за счет чего обеспечивается ингибирование развития гепатоцеллюлярной карциномы у субъекта.
В еще одном аспекте настоящего изобретения предусмотрен способ снижения накопления неправильно свернутого Serpina1 в печени субъекта с дефектным вариантом Serpina1. Способ предусматривает введение субъекту терапевтически эффективного количества любого из вышеупомянутых средств на основе dsRNA или фармацевтической композиции по настоящему изобретению, за счет чего осуществляется снижение накопления неправильно свернутого Serpina1 в печени субъекта.
Средство на основе dsRNA можно вводить субъекту в дозе, составляющей от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг или от приблизительно 0,5 мг/кг до приблизительно 50 мг/кг, или в дозе, составляющей от приблизительно 10 мг/кг до приблизительно 30 мг/кг.
Средство на основе dsRNA можно вводить субъекту подкожно или внутривенно.
Средство на основе dsRNA можно вводить субъекту в двух или более дозах.
Настоящее изобретение далее проиллюстрировано следующим подробным описанием и графическими материалами.
Краткое описание графических материалов
На фигуре 1A схематически изображены нуклеотидные последовательности модифицированных смысловой и антисмысловой нитей AD-61444, AD-75994 и AD-75995. На фигуре 1A раскрыты SEQ ID NO: 36-37, 36, 38, 36 и 39 соответственно в том порядке, в котором они приведены в тексте.
Фигура 1B представляет собой график, показывающий влияние in vivo введения указанных средств на основе dsRNA на уровень экспрессии AAT (Serpina). Уровень экспрессии AAT показан относительно уровня экспрессии AAT в предварительно отобранной крови.
На фигуре 1C схематически изображены нуклеотидные последовательности модифицированных смысловой и антисмысловой нитей AD-61444, AD-77404 и AD-77412. На фигуре 1C раскрыты SEQ ID NO: 36-37, 36-37, 36 и 39 соответственно в том порядке, в котором они приведены в тексте.
Фигура 1D представляет собой график, показывающий влияние in vivo введения указанных средств на основе dsRNA на уровень экспрессии AAT (Serpina).
Фигура 2A представляет собой график, показывающий нецелевой эффект AD-61444 в клетках Hep3B, трансфицированных 10 нМ средства на основе dsRNA, через 16 часов после обработки.
Фигура 2B представляет собой график, показывающий нецелевой эффект AD-77412 в клетках Hep3B, трансфицированных 10 нМ средства на основе dsRNA, через 16 часов после обработки.
Фигура 3A представляет собой график, показывающий эффективность и продолжительность действия сайленсинга AAT у приматов, отличных от человека (NHP), которым вводили однократную дозу указанных средств, составляющую 0,3 мг/кг. Уровень экспрессии AAT показан относительно уровня экспрессии AAT в предварительно отобранной крови, определенного в дни -7 и -1 до введения дозы.
Фигура 3B представляет собой график, показывающий продолжительность действия сайленсинга AAT у приматов, отличных от человека, которым вводили однократную дозу указанных средств, составляющую 1 мг/кг. Уровень экспрессии AAT показан относительно уровня экспрессии AAT в предварительно отобранной крови, определенного в дни -7 и -1 до введения дозы.
Фигура 3C представляет собой график, показывающий продолжительность действия сайленсинга AAT у приматов, отличных от человека, которым вводили однократную дозу указанных средств, составляющую 3 мг/кг. Уровень экспрессии AAT показан относительно уровня экспрессии AAT в предварительно отобранной крови, определенного в дни -7 и -1 до введения дозы.
Фигура 3D представляет собой график, показывающий продолжительность действия сайленсинга AAT у приматов, отличных от человека, которым вводили однократную дозу указанных средств, составляющую 10 мг/кг. Уровень экспрессии AAT показан относительно уровня экспрессии AAT в предварительно отобранной крови, определенного в дни -7 и -1 до введения дозы.
Подробное описание изобретения
Настоящее изобретение предусматривает композиции, содержащие средства, например средства для RNAi, например средства на основе двухнитевой iRNA, нацеливающиеся на Serpina1. Также раскрыты способы применения композиций согласно настоящему изобретению для ингибирования экспрессии Serpina1 и для лечения ассоциированных c Serpina1 заболеваний, таких как нарушения функции печени, например, хронического заболевания печени, воспаления печени, цирроза, фиброза печени и/или гепатоцеллюлярной карциномы.
Настоящее изобретение основано, по меньшей мере частично, на обнаружении эффективных нуклеотидных или химических мотивов для средств на основе dsRNA, нацеливающихся на Serpina1, которые характеризуются преимуществом в отношении ингибирования экспрессии целевого гена, хотя и обладают сниженными эффектами сайленсинга нецелевых генов, а также на композициях, содержащих такие средства, которые подходят для терапевтического применения. Более конкретно, было обнаружено, среди прочего, что средства на основе dsRNA, нацеливающиеся на Serpina1, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца), и/или средство на основе dsRNA, характеризующееся температурой плавления в диапазоне от приблизительно 40°C до приблизительно 80°C, могут быть более эффективными в опосредовании РНК-интерференции, чем исходное средство на основе dsRNA, не имеющее дестабилизирующей модификации.
I. Определения
Чтобы можно было легче понимать настоящее изобретение, вначале приводятся определения некоторых терминов. Кроме того, следует отметить, что во всех случаях изложения значения или диапазона значений параметра подразумевается, что значения и диапазоны, промежуточные по отношению к изложенным значениям, также подразумеваются как часть настоящего изобретения.
Форму единственного числа используют в данном документе для обозначения одной или нескольких (т.e. по меньшей мере одного) грамматических форм предмета заявки. В качестве примера "элемент" означает один элемент или несколько элементов, например, множество элементов.
Термин "включающий" используют в данном документе для обозначения фразы "включающий без ограничения" и используют взаимозаменяемо с ней.
Термин "или" используют в данном документе для обозначения термина "и/или", если из контекста явно не следует иное, и используют взаимозаменяемо с ним.
Используемый в данном документе термин "Serpina1" относится к гену ингибитора серпин-пептидазы, клады A, представителя 1 или белку серпин-пептидазы, клады A, представителя 1. Serpina1 также известен как альфа-1-антитрипсин, α-1-антитрипсин, AAT, ингибитор протеазы 1, PI, PI1, антиэластаза и антитрипсин.
Термин Serpina1 включает Serpina1 человека, аминокислотную и нуклеотидную последовательность которого можно найти, например, в GenBank под №№ доступа GI:189163524 (SEQ ID NO:1), GI:189163525 (SEQ ID NO:2), GI:189163526 (SEQ ID NO:3), GI:189163527 (SEQ ID NO:4), GI:189163529 (SEQ ID NO:5), GI:189163531 (SEQ ID NO:6), GI:189163533 (SEQ ID NO:7), GI:189163535 (SEQ ID NO:8), GI:189163537 (SEQ ID NO:9), GI:189163539 (SEQ ID NO:10) и/или GI:189163541 (SEQ ID NO:11); Serpina1 резус, аминокислотную и нуклеотидную последовательность которого можно найти, например, в GenBank под №№ доступа GI:402766667 (SEQ ID NO:12), GI:297298519 (SEQ ID NO:13) и/или GI: 297298520 (SEQ ID NO:14); Serpina1 мыши, аминокислотную и нуклеотидную последовательность которого можно найти, например, в GenBank под № доступа GI:357588423 и/или GI:357588426; и крысы, аминокислотную и нуклеотидную последовательность которого можно найти, например, в GenBank под № доступа GI:77020249. Дополнительные примеры последовательностей mRNA Serpina1 легко доступны при обращении, например, к GenBank и OMIM.
Было идентифицировано больше 120 аллелей Serpina1, и аллель "M" считается аллелем дикого типа или "нормальным" аллелем (например, "PIM1-ALA213" (также известный как PI, M1A), "PIM1-VAL213" (также известный как PI, MIV), "PIM2", "PIM3" и "PIM4"). Дополнительные варианты можно найти, например, в базе данных A(1)ATVar (см., например, Zaimidou, S., et al. (2009) Hum Mutat. 230(3):308-13 и www.goldenhelix.org/A1ATVar).
Используемый в данном документе термин "дефектный аллель Serpina1" относится к вариантному аллелю, продуцирующему белки, которые не могут сворачиваться надлежащим образом и могут агрегироваться внутриклеточно и, таким образом, не транспортируются надлежащим образом из участка синтеза в печени до участка действия в организме.
Иллюстративные дефектные аллели Serpina1 включают "Z-аллель", "S-аллель", "PIM(Malton)-аллель" и "PIM(Procida)-аллель".
Используемые в данном документе термины "Z-аллель", "PIZ" и "Z-AAT" относятся к вариантному аллелю Serpinal, в котором аминокислота в положении 342 белка изменяется с глутамина на лизин в результате изменения соответствующего кодона с GAG на AAG. Субъект, гомозиготный по Z-аллелю, может упоминаться как "PIZZ". Мутации Z-AAT являются причиной дефектной формы Serpina1 у 95% пациентов и по оценкам присутствуют у 100000 американцев и приблизительно 3 миллионов индивидуумов по всему миру. Z-аллель достигает частот полиморфов у представителей европеоидной расы и реже встречается или отсутствует у азиатов и чернокожих. Гомозиготный по ZZ фенотип ассоциирован с высоким риском как эмфиземы, так и болезни печени. Белок Z-AAT неправильно сворачивается в эндоплазматическом ретикулуме, что приводит к полимерам "петля-лист", которые агрегируются и снижают секрецию, провоцируют реакцию на несвернутые белки, апоптоз, реакцию на перегрузку эндоплазматического ретикулума, аутофагию, митохондриальный стресс и измененную функцию гепатоцитов.
При использовании в данном документе термины "PIM(Malton)" и "M(Malton)-AAT" относятся к вариантному аллелю Serpina1, в котором удален один из соседних фенилаланиновых остатков в положении 51 или 52 зрелого белка. Делеция данной одной аминокислоты укорачивает одну нить бета-листа, B6, препятствуя нормальному процессингу и секреции в печени, что ассоциируется с включениями в гепатоцитах и нарушенной секрецией белка из печени.
При использовании в данном документе термин "PIS" относится к вариантному аллелю Serpina1, в котором глутаминовая кислота в положении 264 замещена валином. Хотя большая часть этого вариантного белка распадается внутриклеточно, наблюдается высокая частота встречаемости аллеля PIS в популяции представителей европеоидной расы, и, таким образом, часто встречаются сложные гетерозиготы с Z-аллелем или нулевым аллелем.
Используемая в данном документе "целевая последовательность" относится к непрерывной части нуклеотидной последовательности молекулы mRNA, образующейся в ходе транскрипции гена Serpina1, в том числе mRNA, которая является продуктом РНК-процессинга первичного продукта транскрипции.
Используемый в данном документе термин "нить, содержащая последовательность" обозначает олигонуклеотид, содержащий цепь из нуклеотидов, которая описывается последовательностью, обозначаемой с использованием стандартной номенклатуры нуклеотидов.
Каждый из "G", "C", "A" и "U", как правило, обозначает нуклеотид, который в качестве основания содержит гуанин, цитозин, аденин и урацил соответственно. "T" и "dT" используют в данном документе взаимозаменяемо, и они относятся к дезоксирибонуклеотиду, где нуклеотидным основанием является тимин, например, дезоксириботимину, 2'-дезокситимидину или тимидину. Однако будет понятно, что термины "рибонуклеотид", или "нуклеотид", или "дезоксирибонуклеотид" также могут относиться к модифицированному нуклеотиду, как более подробно описано ниже, или имитирующему заменяющему фрагменту. Специалисту в данной области хорошо известно, что гуанин, цитозин, аденин и урацил могут быть замещены другими фрагментами без значительного изменения свойств в отношении спаривания оснований олигонуклеотида, содержащего нуклеотид, несущий такой заменяющий фрагмент. Например, без ограничения, нуклеотид, содержащий в качестве основания инозин, может образовывать пару оснований с нуклеотидами, содержащими аденин, цитозин или урацил. Следовательно, нуклеотиды, содержащие урацил, гуанин или аденин, могут быть замещены в нуклеотидных последовательностях согласно настоящему изобретению нуклеотидами, содержащими, например, инозин. Последовательности, содержащие такие заменяющие фрагменты, являются вариантами осуществления настоящего изобретения.
"Полинуклеотиды", также называемые "олигонуклеотидами", образованы посредством ковалентного связывания соседних нуклеозидов друг с другом с получением линейного полимерного олигонуклеотида. Фосфатные группы в составе полинуклеотидной структуры обычно рассматривают как образующие межнуклеозидные связи полинуклеотида. Полинуклеотиды могут представлять собой либо РНК, либо ДНК, и их длина составляет, например, менее приблизительно 100, 200, 300 или приблизительно 400 нуклеотидов.
Термины "iRNA", "средство для RNAi", "средство на основе iRNA", "средство для РНК-интерференции", используемые в данном документе взаимозаменяемо, относятся к средству, которое содержит РНК, в том значении, в котором этот термин определен в данном документе, и которое опосредует нацеленное расщепление РНК-транскрипта посредством пути с участием РНК-индуцируемого комплекса сайленсинга (RISC). iRNA управляет специфичным в отношении последовательности распадом mRNA посредством процесса, который известен как РНК-интерференция (RNAi). iRNA модулирует, например ингибирует, экспрессию Serpina1 в клетке, например в клетке в организме субъекта, такого как субъект-млекопитающее.
Используемое в данном документе выражение "опосредовать RNAi" относится к способности осуществлять сайленсинг целевой РНК посредством специфического в отношении последовательности механизма. Не желая быть ограниченными какой-либо теорией, полагают, что при сайленсинге используется система или процесс RNAi и направляющая РНК, например средство на основе siRNA из 21-23 нуклеотидов.
В одном варианте осуществления средство для RNAi по настоящему изобретению включает однонитевую РНК, которая взаимодействует с последовательностью целевой РНК, например последовательностью целевой mRNA Serpina1, управляя расщеплением целевой РНК. Не желая ограничиваться какой-либо теорией, предполагают, что длинная двухнитевая РНК, введенная в клетки, расщепляется на siRNA под действием эндонуклеазы III типа, известной под названием Dicer (Sharp et al. (2001) Genes Dev. 15:485). Dicer, фермент, подобный рибонуклеазе III типа, обеспечивает процессинг dsRNA до коротких интерферирующих РНК длиной 19-23 пары оснований с характерными 3'-липкими концами из двух оснований (Bernstein, et al., (2001) Nature 409:363). Затем siRNA встраиваются в РНК-индуцируемый комплекс сайленсинга (RISC), в котором одна или несколько хеликаз раскручивают дуплекс siRNA, что позволяет комплементарной антисмысловой нити управлять распознаванием мишени (Nykanen, et al., (2001) Cell 107:309). После связывания с соответствующей целевой mRNA одна или несколько эндонуклеаз в RISC расщепляют мишень с индукцией сайленсинга (Elbashir, et al., (2001) Genes Dev. 15:188). Таким образом, в одном аспекте настоящее изобретение относится к однонитевой РНК (sssiRNA), образуемой внутри клетки, которая способствует образованию RISC-комплекса для осуществления сайленсинга гена-мишени, т.е. гена Serpina1. Соответственно, термин "siRNA" также используют в данном документе для обозначения RNAi, описанной выше.
В другом варианте осуществления средство для RNAi может представлять собой однонитевое средство для RNAi, которое вводят в клетку или организм для ингибирования целевой mRNA. Однонитевые средства для RNAi (ssRNAi) связываются с RISC-эндонуклеазой Argonaute 2, которая затем расщепляет целевую mRNA. Однонитевые siRNA, как правило, содержат 15-30 нуклеотидов и являются химически модифицированными. Конструирование и тестирование однонитевых средств для RNAi описано в патенте США № 8101348 и в Lima et al., (2012) Cell 150: 883-894, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки. Любые антисмысловые нуклеотидные последовательности, описанные в данном документе, можно использовать в качестве однонитевой siRNA, которая описана в данном документе или которая химически модифицирована способами, описанными в Lima et al., (2012) Cell 150:883-894.
В другом варианте осуществления "iRNA" для применения в композициях и способах по настоящему изобретению представляет собой двухнитевую РНК, и в данном документе ее называют "двухнитевым средством для RNAi", "молекулой двухнитевой РНК (dsRNA)", "средством на основе dsRNA" или "dsRNA". Термин "dsRNA" относится к комплексу молекул рибонуклеиновой кислоты, имеющему дуплексную структуру, что содержит две антипараллельные и практически комплементарные нити нуклеиновой кислоты, рассматриваемые как имеющие "смысловую" и "антисмысловую" ориентации по отношению к целевой РНК, т.е. гену Serpina1. В некоторых вариантах осуществления настоящего изобретения двухнитевая РНК (dsRNA) запускает разрушение целевой РНК, например, mRNA, через пост-транскрипционный механизм сайленсинга генов, обозначаемый в данном документе как РНК-интерференция или RNAi.
Как правило, большинство нуклеотидов каждой нити средства на основе dsRNA являются рибонуклеотидами, но, как подробно описано в данном документе, каждая нить или обе нити могут также содержать один или несколько нуклеотидов, не являющихся рибонуклеотидами, например дезоксирибонуклеотид и/или модифицированный нуклеотид. Кроме того, используемый в настоящем описании термин "средство для RNAi" может включать рибонуклеотиды с химическими модификациями; при этом средство для RNAi может включать значительные модификации нескольких нуклеотидов. Используемый в данном документе термин "модифицированный нуклеотид" относится к нуклеотиду, независимо имеющему модифицированный сахарный фрагмент, модифицированную межнуклеотидную связь и/или модифицированное нуклеотидное основание. Таким образом, термин "модифицированный нуклеотид" охватывает замены, добавления или удаления, например, функциональной группы или атома в межнуклеозидных связях, сахарных фрагментах или нуклеотидных основаниях. Модификации, подходящие для применения в средствах по настоящему изобретению, включают все типы модификаций, раскрытых в данном документе или известных из уровня техники. Любые такие модификации, как используемые в молекуле типа siRNA, охватываются термином "средство для RNAi" для целей настоящего описания и формулы изобретения.
Дуплексный участок может быть любой длины, которая обеспечивает возможность специфического расщепление необходимой целевой РНК посредством пути с участием RISC, и может иметь длину в диапазоне от приблизительно 9 до 36 пар оснований, например, иметь длину приблизительно 15-30 пар оснований, например приблизительно 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35 или 36 пар оснований, как, например, приблизительно 15-30, 15-29, 15-28, 15-27, 15-26, 15-25, 15-24, 15-23, 15-22, 15-21, 15-20, 15-19, 15-18, 15-17, 18-30, 18-29, 18-28, 18-27, 18-26, 18-25, 18-24, 18-23, 18-22, 18-21, 18-20, 19-30, 19-29, 19-28, 19-27, 19-26, 19-25, 19-24, 19-23, 19-22, 19-21, 19-20, 20-30, 20-29, 20-28, 20-27, 20-26, 20-25, 20-24,20-23, 20-22, 20-21, 21-30, 21-29, 21-28, 21-27, 21-26, 21-25, 21-24, 21-23 или 21-22 пары оснований. Также предусматривается, что диапазоны и значения длины, промежуточные относительно вышеупомянутых диапазонов и значений длины, являются частью настоящего изобретения.
Две нити, образующие дуплексную структуру, могут быть различными частями одной более крупной молекулы РНК, или они могут представлять собой отдельные молекулы РНК. В тех случаях, когда две нити являются частью одной более крупной молекулы и, следовательно, соединены непрерывающейся цепью нуклеотидов от 3'-конца одной нити до 5'-конца соответствующей другой нити, образующих дуплексную структуру, соединительная цепь РНК называется петлей типа "шпилька". Петля типа "шпилька" может содержать по меньшей мере один неспаренный нуклеотид. В некоторых вариантах осуществления петля типа "шпилька" может содержать по меньшей мере 2, по меньшей мере 3, по меньшей мере 4, по меньшей мере 5, по меньшей мере 6, по меньшей мере 7, по меньшей мере 8, по меньшей мере 9, по меньшей мере 10, по меньшей мере 20, по меньшей мере 23 или больше неспаренных нуклеотидов.
Если две практически комплементарные нити dsRNA образованы отдельными молекулами РНК, то эти молекулы не должны, но могут быть соединены ковалентно. Если две нити соединены ковалентно иным образом, нежели непрерывающейся цепью нуклеотидов от 3'-конца одной нити до 5'-конца соответствующей другой нити, образующих дуплексную структуру, то соединительная структура обозначается как "линкер". Нити РНК могут иметь одинаковое или разное число нуклеотидов. Максимальное число пар оснований представляет собой число нуклеотидов в самой короткой нити dsRNA за вычетом любых «липких» концов, которые присутствуют в дуплексе. Помимо дуплексной структуры средство для RNAi может содержать один или несколько нуклеотидных «липких» концов.
В одном варианте осуществления средство для RNAi по настоящему изобретению представляет собой dsRNA, каждая нить которой содержит 19-23 нуклеотида, которая взаимодействует с последовательностью целевой РНК, например с последовательностью целевой mRNA Serpina1, для управления расщеплением целевой РНК. Не желая ограничиваться какой-либо теорией, длинная двухнитевая РНК, введенная в клетки, расщепляется на siRNA под действием эндонуклеазы III типа, известной под названием Dicer (Sharp et al. (2001) Genes Dev. 15:485). Dicer, фермент, подобный рибонуклеазе III типа, обеспечивает процессинг dsRNA до коротких интерферирующих РНК длиной 19-23 пары оснований с характерными 3'-липкими концами из двух оснований (Bernstein, et al., (2001) Nature 409:363). Затем siRNA встраиваются в РНК-индуцируемый комплекс сайленсинга (RISC), в котором одна или несколько хеликаз раскручивают дуплекс siRNA, что позволяет комплементарной антисмысловой нити управлять распознаванием мишени (Nykanen, et al., (2001) Cell 107:309). После связывания с соответствующей целевой mRNA одна или несколько эндонуклеаз в RISC расщепляют мишень с индукцией сайленсинга (Elbashir, et al., (2001) Genes Dev. 15:188).
Используемый в данном документе термин "нуклеотидный «липкий» конец" обозначает по меньшей мере один неспаренный нуклеотид, который выступает из дуплексной структуры iRNA, например dsRNA. Например, если 3'-конец одной нити dsRNA выходит за пределы 5'-конца другой нити или наоборот, то образуется нуклеотидный «липкий» конец. dsRNA может содержать «липкий» конец по меньшей мере из одного нуклеотида; в качестве альтернативы «липкий» конец может содержать по меньшей мере два нуклеотида, по меньшей мере три нуклеотида, по меньшей мере четыре нуклеотида, по меньшей мере пять нуклеотидов или больше. Нуклеотидный «липкий» конец может содержать аналог нуклеотида/нуклеозида, в том числе дезоксинуклеотид/нуклеозид, или состоять из него. «Липкий» конец(ы) может находиться на смысловой нити, антисмысловой нити или любой их комбинации. Более того, нуклеотид(ы) «липкого» конца может присутствовать на 5'-конце, 3'-конце или на обоих концах антисмысловой или смысловой нити dsRNA.
В одном варианте осуществления антисмысловая нить dsRNA содержит «липкий» конец из 1-10 нуклеотидов, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов, на 3'-конце и/или 5'-конце. В одном варианте осуществления смысловая нить dsRNA содержит «липкий» конец из 1-10 нуклеотидов, например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов, на 3'-конце и/или 5'-конце. В другом варианте осуществления один или несколько нуклеотидов в «липком» конце заменены на нуклеозидтиофосфат.
В определенных вариантах осуществления «липкий» конец на смысловой нити, или антисмысловой нити, или обеих может содержать удлиненные отрезки длиной более 10 нуклеотидов, например, длиной 10-30 нуклеотидов, 10-25 нуклеотидов, 10-20 нуклеотидов или 10-15 нуклеотидов. В определенных вариантах осуществления удлиненный «липкий» конец присутствует на смысловой нити дуплекса. В определенных вариантах осуществления удлиненный «липкий» конец присутствует на 3'-конце смысловой нити дуплекса. В определенных вариантах осуществления удлиненный «липкий» конец присутствует на 5'-конце смысловой нити дуплекса. В определенных вариантах осуществления удлиненный «липкий» конец находится на антисмысловой нити дуплекса. В определенных вариантах осуществления удлиненный «липкий» конец присутствует на 3'-конце антисмысловой нити дуплекса. В определенных вариантах осуществления удлиненный «липкий» конец присутствует на 5'-конце антисмысловой нити дуплекса. В определенных вариантах осуществления один или несколько нуклеотидов удлиненного «липкого» конца заменены нуклеозидтиофосфатом.
Термины "тупой конец" или "с тупыми концами", используемые в данном документе в отношении dsRNA, означают, что на указанном терминальном конце dsRNA отсутствуют неспаренные нуклеотиды или аналоги нуклеотидов, т. е. отсутствует нуклеотидный «липкий» конец. Один или оба конца dsRNA могут быть тупыми. Если оба конца dsRNA являются тупыми, то говорят, что данная dsRNA "с тупыми концами". Для внесения ясности, dsRNA "с тупыми концами" представляет собой dsRNA, у которой оба конца являются тупыми, т. е. ни на одном из концов молекулы нет нуклеотидного «липкого» конца. Чаще всего такая молекула будет двунитевой по всей своей длине.
Термин "антисмысловая нить" или "направляющая нить" обозначает нить iRNA, например dsRNA, которая содержит участок, практически комплементарный целевой последовательности, например mRNA Serpina1.
Используемый в данном документе термин "участок комплементарности" относится к участку на антисмысловой нити, практически комплементарному последовательности, например целевой последовательности, например нуклеотидной последовательности Serpina1, которая определена в данном документе. Если участок комплементарности не полностью комплементарен целевой последовательности, во внутренних или концевых участках молекулы могут находиться ошибки спаривания. Как правило, наиболее допустимые ошибки спаривания находятся в концевых участках, например, в пределах 5, 4, 3 или 2 нуклеотидов 5'- и/или 3'-конца iRNA.
Термин "смысловая нить" или "сопровождающая нить", используемый в данном документе, относится к нити iRNA, которая содержит участок, практически комплементарный участку антисмысловой нити, в том значении, в котором этот термин определен в данном документе.
Используемый в данном документе термин "участок расщепления" обозначает участок, который непосредственно прилегает к сайту расщепления. Сайт расщепления представляет собой сайт в мишени, в котором происходит расщепление. В некоторых вариантах осуществления участок расщепления содержит три основания, которые находятся на любом из концов сайта расщепления и непосредственно прилегают к нему. В некоторых вариантах осуществления участок расщепления содержит два основания, которые находятся на любом из концов сайта расщепления и непосредственно прилегают к нему. В некоторых вариантах осуществления сайт расщепления, в частности, находится в сайте, связываемым нуклеотидами 10 и 11 антисмысловой нити, а участок расщепления содержит нуклеотиды 11, 12 и 13.
Используемый в данном документе термин "комплементарный", если не указано иное, при использовании для описания первой нуклеотидной последовательности по отношению ко второй нуклеотидной последовательности обозначает способность олигонуклеотида или полинуклеотида, содержащего первую нуклеотидную последовательность, гибридизироваться и образовывать дуплексную структуру в определенных условиях с олигонуклеотидом или полинуклеотидом, содержащим вторую нуклеотидную последовательность, что будет понятно специалисту в данной области. Такие условия, например, могут быть жесткими условиями, где жесткие условия могут включать: 400 мМ NaCl, 40 мМ PIPES, pH 6,4, 1 мМ EDTA, 50°C или 70°C в течение 12-16 часов с последующим отмыванием. Можно применять другие условия, такие как физиологически соответствующие условия, характерные для организма. Например, комплементарная последовательность является удовлетворительной для обеспечения выполнения соответствующей функции нуклеиновой кислоты, например RNAi. Специалист в данной области сможет определить набор условий, наиболее подходящих для тестирования комплементарности двух последовательностей в соответствии с конечным применением гибридизированных нуклеотидов.
Последовательности могут быть "полностью комплементарными" по отношению к каждой из них, когда присутствует спаривание оснований нуклеотидов первой нуклеотидной последовательности с нуклеотидами второй нуклеотидной последовательности по всей длине первой и второй нуклеотидных последовательностей. Однако, при указании первой последовательности как "фактически комплементарной" по отношению ко второй последовательности, две последовательности могут быть полностью комплементарными, или в них при гибридизации может происходить ошибочное спаривание одной или нескольких, но, как правило, не более 4, 3 или 2 пар оснований, с сохранением при этом способности гибридизоваться в условиях, наиболее соответствующих их конечному применению. Однако, если два олигонуклеотида разработаны так, чтобы после гибридизации образовывался один или несколько однонитевых выступающих концов, то такие выступающие концы не будут считаться ошибками спаривания применительно к определению комплементарности. Например, dsRNA, содержащая один олигонуклеотид длиной 21 нуклеотид и другой олигонуклеотид длиной 23 нуклеотида, где более длинный олигонуклеотид содержит последовательность из 21 нуклеотида, которая полностью комплементарна более короткому олигонуклеотиду, может при этом обозначаться как "полностью комплементарная" для целей, описанных в данном документе.
"Комплементарные" последовательности, используемые в данном документе, могут также включать пары оснований или могут быть полностью образованы из таких пар, образованных не по модели Уотсона-Крика, и/или пар оснований, образованных из неприродных и модифицированных нуклеотидов, в той мере, в которой выполняются вышеуказанные требования в отношении их способности к гибридизации. Такие пары оснований, образованные не по модели Уотсона-Крика, включают без ограничения неоднозначное или Хугстиновское спаривание оснований G:U.
Термины "комплементарный", "полностью комплементарный" и "практически комплементарный" в данном документе можно использовать по отношению к соответствию оснований между смысловой нитью и антисмысловой нитью dsRNA или между антисмысловой нитью dsRNA и целевой последовательностью, как будет понятно из контекста их применения.
Используемый в данном документе полинуклеотид, который "практически комплементарен по меньшей мере части" матричной РНК (mRNA), относится к полинуклеотиду, который практически комплементарен непрерывной части mRNA, представляющей интерес (например, mRNA, кодирующей Serpina1), в том числе 5'-UTR, открытой рамке считывания (ORF) или 3'-UTR. Например, полинуклеотид комплементарен по меньшей мере части mRNA Serpina1, если последовательность практически комплементарна непрерывающейся части mRNA, кодирующей Serpina1.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению является "в достаточной степени комплементарным" целевой РНК, например целевой mRNA, так что средство на основе dsRNA приводит к сайленсингу выработки белка, кодируемого целевой mRNA. В другом варианте осуществления средство на основе dsRNA по настоящему изобретению является "точно комплементарным" или полностью комплементарным целевой РНК, например целевая РНК и средство на основе dsRNA-дуплекса, гибридизуются, например, с образованием гибрида, получаемого исключительно за счет спаривания оснований по Уотсону-Крику в участке точной комплементарности. "Достаточная степень комплементарности" целевой РНК может распространяться на внутренний участок (например, по меньшей мере из 10 нуклеотидов), который точно комплементарен целевой РНК. Более того, согласно некоторым вариантам осуществления средство на основе dsRNA по настоящему изобретению специфично распознает различие в один нуклеотид. В данном случае средство на основе dsRNA опосредует RNAi лишь тогда, когда полная комплементарность установлена в участке (например, в пределах 7 нуклеотидов) с различием в один нуклеотид.
Термин 'BNA' относится к мостиковой нуклеиновой кислоте, и она зачастую называется затрудненной или недоступной РНК. BNA может содержать 5-, 6-членную или даже 7-членную мостиковую структуру с "фиксированным" C3'-эндовыступом сахара. Как правило, мостик встраивают на 2'-, 4'-положении рибозы с получением нуклеотида 2', 4'-BNA (например, LNA или ENA). Примеры нуклеотидов BNA включают следующие нуклеозиды:
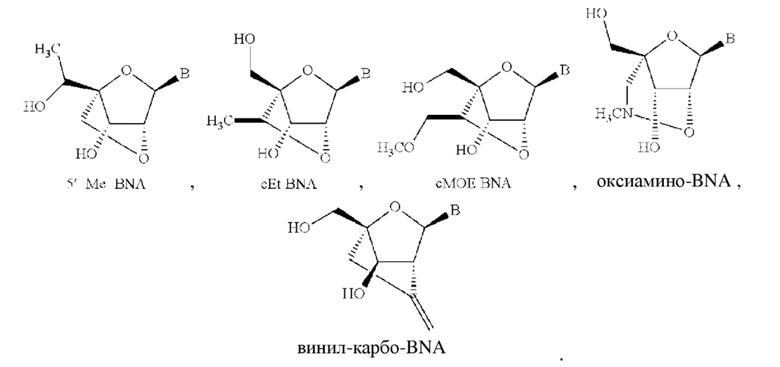
Термин 'LNA' относится к запертой нуклеиновой кислоте, и она зачастую называется затрудненной или недоступной РНК. LNA представляет собой модифицированный нуклеотид РНК. Рибозный фрагмент в нуклеотиде LNA модифицируют с помощью дополнительного мостика (например, метиленового мостика или этилeнового мостика), соединяющего 2′-гидроксил с 4′-углеродом того же рибозного сахара. К примеру, мостик может "запирать" рибозу в конформации 3′-эндо (северная):
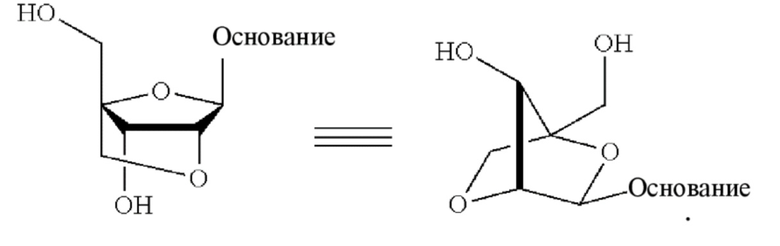
Термин 'ЕNA' относится к нуклеиновой кислоте с этиленовыми мостиками, и она зачастую называется затрудненной или недоступной РНК.
Термин "ингибирование", используемый в данном документе, применяют взаимозаменяемо со "снижением", "сайленсингом", "деактивацией", "подавлением" и другими подобными терминами, и он предусматривает любой уровень ингибирования.
Фраза "ингибирование экспрессии Serpina1", используемая в данном документе, включает ингибирование экспрессии любого гена Serpina1 (такого как, например, ген Serpina1 мыши, ген Serpina1 крысы, ген Serpina1 обезьяны или ген Serpina1 человека), а также вариантов (например, встречающихся в природе вариантов) или мутантов гена Serpina1. Таким образом, ген Serpina1 может быть геном Serpina1 дикого типа, вариантом гена Serpina1, мутантным геном Serpina1 или трансгенным геном Serpina1 в контексте клеток, группы клеток или организма, подвергнутых генетической манипуляции.
"Ингибирование экспрессии гена Serpina1" предусматривает любой уровень ингибирования гена Serpina1, например, по меньшей мере частичную супрессию экспрессии гена Serpina1, такую как ингибирование по меньшей мере на приблизительно 5%, по меньшей мере на приблизительно 10%, по меньшей мере на приблизительно 15%, по меньшей мере на приблизительно 20%, по меньшей мере на приблизительно 25%, по меньшей мере на приблизительно 30%, по меньшей мере на приблизительно 35%, по меньшей мере на приблизительно 40%, по меньшей мере на приблизительно 45%, по меньшей мере на приблизительно 50%, по меньшей мере на приблизительно 55%, по меньшей мере на приблизительно 60%, по меньшей мере на приблизительно 65%, по меньшей мере на приблизительно 70%, по меньшей мере на приблизительно 75%, по меньшей мере на приблизительно 80%, по меньшей мере на приблизительно 85%, по меньшей мере на приблизительно 90%, по меньшей мере на приблизительно 91%, по меньшей мере на приблизительно 92%, по меньшей мере на приблизительно 93%, по меньшей мере на приблизительно 94%, по меньшей мере на приблизительно 95%, по меньшей мере на приблизительно 96%, по меньшей мере на приблизительно 97%, по меньшей мере на приблизительно 98% или по меньшей мере на приблизительно 99%.
Экспрессию гена Serpina1 можно оценивать, исходя из уровня любой переменной, ассоциированной с экспрессией гена Serpina1, например, уровня mRNA Serpina1, уровня белка Serpina1 или уровней сывороточного AAT. Ингибирование можно оценивать по уменьшению абсолютного или относительного уровня одной или нескольких из этих переменных по сравнению с контрольным уровнем. Контрольный уровень может представлять собой любой тип контрольного уровня, который используют в данной области техники, например, уровень в начальный момент времени до введения дозы или уровень, определенный у сходного субъекта, клетки или образца, являющихся необработанными или обработанными контролем (таким как, например, контроль только с буфером или контроль с неактивным средством).
Фраза "приведение клетки в контакт с двухнитевым средством для RNAi", используемая в данном документе, предусматривает приведение клетки в контакт любым возможным способом. Приведение клетки в контакт с двухнитевым средством для RNAi включает приведение клетки в контакт со средством для RNAi in vitro или приведение клетки в контакт со средством для RNAi in vivo. Приведение в контакт можно осуществлять непосредственно или опосредованно. Таким образом, например, средство для RNAi может быть приведено в физический контакт с клеткой лицом, осуществляющим способ, или, в качестве альтернативы, средство для RNAi можно поместить в обстановку, которая обеспечит ему возможность впоследствии прийти в контакт с клеткой или послужит причиной этому.
Приведение клетки в контакт in vitro можно выполнять, например, путем инкубирования клетки со средством для RNAi. Приведение клетки в контакт in vivo можно выполнять, например, путем введения инъекцией средства для RNAi в ткань, в которой находится клетка, или рядом с ней или путем введения инъекцией средства для RNAi в другую область, кровоток или подкожное пространство так, что средство будет впоследствии достигать ткани, в которой находится клетка, которую необходимо привести в контакт со средством. Например, средство для RNAi может содержать лиганд, например лиганд, представляющий собой GalNAc3, который направляет средство для RNAi к месту, представляющему интерес, например к печени, и/или может быть связано с ним. Также возможны комбинации способов приведения в контакт in vitro и in vivo. По отношению к способам согласно настоящему изобретению клетку также можно приводить в контакт со средством для RNAi in vitro и в дальнейшем пересаживать субъекту.
Выражения "пациент" или "субъект", используемые в данном документе, подразумевают как включающие либо человека, либо животного, отличного от человека, предпочтительно млекопитающего, например обезьяну. Наиболее предпочтительно субъектом или пациентом является человек.
Выражение "ассоциированное с Serpina1 заболевание", используемое в данном документе, подразумевают как включающее любое заболевание, нарушение или состояние, ассоциированное с геном или белком Serpina1. Такое заболевание может быть вызвано, например, неправильным сворачиванием белка Serpina1, внутриклеточным накоплением белка Serpina1 (например, неправильно свернутого белка Serpina1), избыточным продуцированием белка Serpina1, вариантами гена Serpina1, мутациями гена Serpina1, аномальным расщеплением белка Serpina1, аномальными взаимодействиями Serpina1 с другими белками или другими эндогенными или экзогенными веществами. Ассоциированным с Serpina1 заболеванием может быть заболевание печени и/или заболевание легких.
"Заболевание печени" при использовании в данном документе предусматривает заболевание, нарушение или состояние, влияющее на печень и/или ее функцию. Нарушение функции печени может быть результатом накопления белка Serpina1 в печени и/или клетках печени. Примеры нарушений функции печени включают в себя нарушения функции печени, вызванные вирусными инфекциями, паразитарными инфекциями, генетической предрасположенностью, аутоиммунными заболеваниями, воздействием радиации, воздействием токсических для печени соединений, механическими повреждениями, различными токсинами окружающей среды, спиртом, ацетаминофеном, комбинацией спирта и ацетаминофена, ингаляционными анестетиками, ниацином, химиотерапевтическими средствами, антибиотиками, анальгетиками, противорвотными средствами, растительной добавкой кава и их комбинациями.
Например, нарушение функции печени, ассоциированное с дефицитом Serpina1, чаще может возникать у субъектов с одной или несколькими копиями некоторых аллелей (например, аллелей PIZ, PiM(Malton) и/или PIS). Не ограничиваясь какой-либо теорией, полагают, что аллели, ассоциированные с повышенным риском развития заболевания печени, связанного с альфа-1-антитрипсином, кодируют формы Serpina1, которые подвергаются неправильному сворачиванию и не секретируются надлежащим образом из гепатоцитов. Клеточные реакции на такие неправильно свернутые белки могут включать в себя реакцию на несвернутые белки (UPR), ассоциированное с эндоплазматическим ретикулумом расщепление (ERAD), апоптоз, реакцию на перегрузку эндоплазматического ретикулума, аутофагию, митохондриальный стресс и изменение функции гепатоцитов. Повреждения гепатоцитов могут приводить к таким симптомам, без ограничения, как воспаление, холестаз, фиброз, цирроз, длительная обструктивная желтуха, повышенные уровни трансаминаз, портальная гипертензия и/или гепатоцеллюлярная карцинома. Не ограничиваясь какой-либо теорией, высоко вариабельное клиническое течение данного заболевания предполагает модификаторы или "вторичные факторы" как причины развития симптомов или прогрессирования тяжести заболевания.
Например, субъекты с PIZ-аллелем могут быть более восприимчивыми к инфекциям гепатита C или алкогольной зависимости, и у них с большей вероятностью может развиться нарушение функции печени при воздействии этих факторов. Кроме того, субъекты с кистозным фиброзом (CF), несущие PIZ-аллель, подвержены большему риску развития тяжелой болезни печени с портальной гипертензией. Дефицит Serpina1 также может обуславливать развитие эмфиземы c ранним началом, некротического панникулита, бронхоэктаза и/или длительной желтухи новорожденных или способствовать этому. Некоторых пациентов с дефицитом альфа-1-антитрипсина или подвергающихся риску такового выявляют путем скрининга, если среди членов их семей есть пораженные дефицитом альфа-1-антитрипсина.
Иллюстративные нарушения функции печени включают без ограничения воспаление печени, хроническое заболевание печени, цирроз, фиброз печени, гепатоцеллюлярную карциному, некроз печени, стеатоз, холестаз и/или снижение и/или потерю функции гепатоцитов.
"Цирроз" представляет собой патологическое состояние, ассоциированное с хроническим поражением печени, которое включает обширный фиброз и регенеративные узлы в печени.
"Фиброз" представляет собой пролиферацию фибробластов и образование рубцовой ткани в печени.
Фраза "функция печени" относится к одной или нескольким из многочисленных физиологических функций, выполняемых печенью. Такие функции включают без ограничения регуляцию уровней сахара в крови, эндокринную регуляцию, ферментные системы, взаимопревращение метаболитов (например, кетоновых тел, стеролов, стероидов и аминокислот); продуцирование белков крови, таких как фибриноген, сывороточный альбумин и холинэстераза, эритропоэтическая функция, детоксификация, образование желчи и хранение витаминов. Из уровня техники известен ряд тестов для проверки функции печени, в том числе, например, измерение уровня аланинаминотрансферазы (ALT), щелочной фосфатазы, билирубина, протромбина и альбумина.
Выражение "терапевтически эффективное количество" при использовании в данном документе подразумевают как включающее количество средства для RNAi, достаточное при введении пациенту для лечения ассоциированного с Serpina1 заболевания, для эффективного лечения заболевания (например, путем ослабления, уменьшения интенсивности или поддержания существующего заболевания или одного или нескольких симптомов заболевания). "Терапевтически эффективное количество" может варьировать в зависимости от средства для RNAi, способа введения средства, заболевания и его тяжести, а также анамнеза, возраста, веса, семейного анамнеза, генетических характеристик, стадии патологических процессов, опосредованных экспрессией Serpina1, типов предшествующего или сопутствующего лечения, при наличии такового, и других индивидуальных особенностей пациента, подлежащего лечению.
Выражение "профилактически эффективное количество" при использовании в данном документе подразумевают как включающее количество средства для RNAi, достаточное при введении субъекту, у которого еще не возникли или не проявились симптомы ассоциированного с Serpina1 заболевания, но который может иметь предрасположенность к заболеванию, для предупреждения или уменьшения интенсивности заболевания или одного или нескольких симптомов заболевания. Уменьшение интенсивности заболевания включает замедление течения заболевания или снижение тяжести заболевания, развивающегося позже. "Профилактически эффективное количество" может варьироваться в зависимости от средства для RNAi, пути введения средства, степени риска развития заболевания, а также анамнеза, возраста, веса, семейного анамнеза, генетических характеристик, типов предшествующего или сопутствующего лечения, при наличии такового, и других индивидуальных особенностей пациента, подлежащего лечению.
"Терапевтически эффективное количество" или "профилактически эффективное количество" также включают количество средства для RNAi, которое вызывает некоторый требуемый локальный или системный эффект при приемлемом соотношении польза/риск, предусмотренном для любого лечения. Средства для RNAi, применяемые в способах согласно настоящему изобретению, можно вводить в количестве, достаточном для получения приемлемого соотношения польза/риск, предусмотренного для такого лечения.
Термин "образец", используемый в данном документе, предусматривает совокупность сходных жидкостей, клеток или тканей, выделенных из организма субъекта, а также жидкостей, клеток или тканей, присутствующих в организме субъекта. Примеры биологических жидкостей включают кровь, сыворотку крови и серозные жидкости, плазму, мочу, лимфу, спинномозговую жидкость, внутриглазные жидкости, слюну и т.п. Образцы ткани могут включать образцы из тканей, органов или ограниченных участков. Например, образцы могут быть получены из конкретных органов, частей органов или жидкостей или клеток этих органов. В определенных вариантах осуществления образцы можно быть получены из печени (например, всей печени, или определенных сегментов печени, или определенных типов клеток в печени, таких как, например, гепатоциты). В предпочтительных вариантах осуществления "образец, полученный от субъекта" обозначает кровь или плазму крови, взятые у субъекта. В дополнительных вариантах осуществления "образец, полученный от субъекта" означает ткань печени (или ее составляющие компоненты), полученную от субъекта.
II. iRNA по настоящему изобретению
В данном документе описаны улучшенные двухнитевые средства для RNAi, которые ингибируют экспрессию гена Serpina1 в клетке, такой как клетка субъекта, например млекопитающего, такого как человек, имеющий ассоциированное с Serpina1 заболевание, например заболевание печени, например, хроническое заболевание печени, воспаление печени, цирроз, фиброз печени и/или гепатоцеллюлярную карциному.
Соответственно, настоящее изобретение предусматривает двухнитевые средства для RNAi с химическими модификациями, способные ингибировать экспрессию целевого гена (т.е. гена Serpina1) in vivo. В определенных аспектах настоящего изобретения практически все нуклеотиды iRNA по настоящему изобретению являются модифицированными. В других вариантах осуществления настоящего изобретения все нуклеотиды в iRNA по настоящему изобретению являются модифицированными. iRNA по настоящему изобретению, в которых "практически все нуклеотиды являются модифицированными", являются в значительной степени, но не полностью модифицированными и могут содержать не более 5, 4, 3, 2 или 1 немодифицированного нуклеотида.
Средство для RNAi содержит смысловую нить и антисмысловую нить. Длина каждой нити средства для RNAi может варьироваться от 12 до 30 нуклеотидов. Например, каждая нить может составлять 14-30 нуклеотидов в длину, 17-30 нуклеотидов в длину, 19-30 нуклеотидов в длину, 25-30 нуклеотидов в длину, 27-30 нуклеотидов в длину, 17-23 нуклеотида в длину, 17-21 нуклеотид в длину, 17-19 нуклеотидов в длину, 19-25 нуклеотидов в длину, 19-23 нуклеотида в длину, 19-21 нуклеотид в длину, 21-25 нуклеотидов в длину или 21-23 нуклеотида в длину.
Смысловая нить и антисмысловая нить, как правило, образуют двухнитевой РНК-дуплекс ("dsRNA"), также обозначаемый в данном документе как "средство для RNAi". Длина дуплексного участка средства для RNAi может составлять 12-30 пар нуклеотидов. Например, длина дуплексного участка может составлять 14-30 пар нуклеотидов, 17-30 пар нуклеотидов, 27-30 пар нуклеотидов, 17-23 пары нуклеотидов, 17-21 пару нуклеотидов, 17-19 пар нуклеотидов, 19-25 пар нуклеотидов, 19-23 пары нуклеотидов, 19-21 пару нуклеотидов, 21-25 пар нуклеотидов или 21-23 пары нуклеотидов. В другом примере длина дуплексного участка выбрана из 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26 и 27 нуклеотидов.
В одном варианте осуществления средство для RNAi может содержать один или несколько участков «липких» концов и/или кэпирующих групп на 3'-конце, 5'-конце или на обоих концах одной или обеих нитей. Длина «липкого» конца может составлять 1-6 нуклеотидов, например, 2-6 нуклеотидов, 1-5 нуклеотидов, 2-5 нуклеотидов, 1-4 нуклеотида, 2-4 нуклеотида, 1-3 нуклеотида, 2-3 нуклеотида или 1-2 нуклеотида. Наличие выступающих концов может быть результатом того, что одна нить длиннее другой, или может быть результатом того, что две нити одинаковой длины расположены со сдвигом. «Липкий» конец может образовывать ошибку спаривания с целевой mRNA, или он может быть комплементарен последовательностям генов, подлежащим нацеливанию, или может иметь другую последовательность. Первая и вторая нити также могут быть соединены, например, с помощью дополнительных оснований с образованием "шпильки" или с помощью других линкеров, не содержащих основания.
В одном варианте осуществления каждый из нуклеотидов в участке «липкого» конца средства для RNAi независимо может представлять собой модифицированный или немодифицированный нуклеотид, в том числе без ограничения c 2'-модифицированным сахаром, такой как 2-F, 2'-O-метилтимидин (T), 2'-O-метоксиэтил-5-метилуридин (Teo), 2'-O-метоксиэтиладенозин (Aeo), 2'-O-метоксиэтил-5-метилцитидин (m5Ceo) и их любые комбинации. Например, последовательность «липкого» конца на обоих концах каждой нити может представлять собой TT. «Липкий» конец может образовывать ошибку спаривания с целевой mRNA, или он может быть комплементарен последовательностям генов, подлежащим нацеливанию, или может иметь другую последовательность.
5'- или 3'-выступающие концы смысловой нити, антисмысловой нити или обеих нитей средства для RNAi могут быть фосфорилированными. В некоторых вариантах осуществления «липкий» участок(и) содержит два нуклеотида с фосфотиоатной связью между двумя нуклеотидами, при этом два нуклеотида могут быть одинаковыми или различными. В одном варианте осуществления «липкий» конец присутствует на 3'-конце смысловой нити, антисмысловой нити или обеих нитей. В одном варианте осуществления этот 3'-липкий конец присутствует в антисмысловой нити. В одном варианте осуществления этот 3'-липкий конец присутствует в смысловой нити.
Средство для RNAi может содержать только один выступающий конец, который может усиливать активность интерференции у средства для RNAi без негативного воздействия на его общую стабильность. Например, однонитевой «липкий» конец может быть расположен на 3'-конце смысловой нити или в качестве альтернативы на 3'-конце антисмысловой нити. RNAi также может иметь тупой конец, расположенный на 5'-конце антисмысловой нити (или 3'-конце смысловой нити) или наоборот. Как правило, антисмысловая нить RNAi имеет нуклеотидный «липкий» конец на 3'-конце, а 5'-конец является тупым концом. Не желая ограничиваться какой-либо теорией, предполагают, что асимметричные тупой конец на 5'-конце антисмысловой нити и 3'-концевой «липкий» конец антисмысловой нити способствуют включению направляющей нити в процесс с участием RISC.
Любая из нуклеиновых кислот, представленных в настоящем изобретении, может быть синтезирована и/или модифицирована способами, хорошо известными из уровня техники, такими как описанные в "Current protocols in nucleic acid chemistry," Beaucage, S.L. et al. (Edrs.), John Wiley & Sons, Inc., New York, NY, USA, который включен в данный документ посредством ссылки. Модификации включают, например, концевые модификации, например, модификации 5'-конца (фосфорилирование, конъюгацию, инвертированные связи) или модификации 3'-конца (конъюгацию, ДНК-нуклеотиды, инвертированные связи и т.д.); модификации оснований, например, замену на стабилизирующие основания, дестабилизирующие основания или основания, которые образуют пару оснований с расширенным репертуаром партнеров, удаление оснований (нуклеотиды с удаленным азотистым основанием) или конъюгацию оснований; модификации сахаров (например, в 2'-положении или 4'-положении) или замену сахара и/или модификации остова, в том числе модификацию или замену фосфодиэфирных связей. Конкретные примеры соединений на основе iRNA, применимых в вариантах осуществления, описанных в данном документе, включают без ограничения РНК, содержащие модифицированные остовы или не встречающиеся в природе межнуклеозидные связи. РНК с модифицированными остовами включают, среди прочего, такие, которые не содержат атом фосфора в остове. Для целей данного описания и как иногда упоминается в уровне техники, модифицированные РНК, не содержащие атом фосфора в своем межнуклеозидном остове, также могут считаться олигонуклеозидами. В некоторых вариантах осуществления модифицированная iRNA будет содержать атом фосфора в своем межнуклеозидном остове.
Модифицированные остовы РНК, которые не содержат атом фосфора в своем составе, представляют собой остовы, образованные короткоцепочечными алкильными или циклоалкильными межнуклеозидными связями, смешанными гетероатомными и алкильными или циклоалкильными межнуклеозидными связями или одной или несколькими короткоцепочечными гетероатомными или гетероциклическими межнуклеозидными связями. Они включают остовы с морфолиновыми связями (частично образованные из сахарной части нуклеозида); силоксановые остовы; сульфидные, сульфоксидные и сульфоновые остовы; формацетильные и тиоформацетильные остовы; метиленформацетильные и тиоформацетильные остовы; алкенсодержащие остовы; сульфаматные остовы; метилениминовые и метиленгидразиновые остовы; сульфонатные и сульфонамидные остовы; амидные остовы и другие, содержащие смесь составляющих частей N, O, S и CH2.
Иллюстративные патенты США, в которых изложено получение вышеупомянутых олигонуклеозидов, включают без ограничения патенты США №№ 5034506; 5166315; 5185444; 5214134; 5216141; 5235033; 564562; 5264564; 5405938; 5434257; 5466677; 5470967; 5489677; 5541307; 5561225; 5596086; 5602240; 5608046; 5610289; 5618704; 5623070; 5663312; 5633360; 5677437 и 5677439, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки.
В других вариантах осуществления для применения в iRNA предусматриваются подходящие РНК-миметики, у которых как сахар, так и межнуклеозидная связь, т. е остов, нуклеотидных структурных единиц, заменены новыми группами. Структурные единицы в виде оснований сохранены для гибридизации с соответствующим целевым соединением нуклеиновой кислотой. Одно такое олигомерное соединение, РНК-миметик, который, как было показано, обладает превосходными свойствами гибридизации, обозначен как пептидная нуклеиновая кислота (PNA). В соединениях PNA сахарный остов РНК заменен на амидсодержащий остов, в частности аминоэтилглициновый остов. Нуклеотидные основания оставлены, и они связываются непосредственно или опосредованно с атомами азота азагруппы амидной части остова. Иллюстративные патенты США, в которых изложено получение соединений PNA, включают без ограничения патенты США №№ 5539082; 5714331 и 5719262, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки. Дополнительные соединения PNA, подходящие для применения в iRNA по настоящему изобретению, описаны, например, в Nielsen et al., Science, 1991, 254, 1497-1500.
Некоторые варианты осуществления, представленные в настоящем изобретении, включают РНК с фосфотиоатными остовами и олигонуклеозиды с гетероатомными остовами и, в частности, -CH2-NH-CH2-, -CH2-N(CH3)-O-CH2- [известный как метилен(метилиминовый) или MMI-остов], -CH2-O-N(CH3)-CH2-, -CH2-N(CH3)-N(CH3)-CH2- и -N(CH3)-CH2-CH2- [где нативный фосфодиэфирный остов представлен как -O-P-O-CH2-] из вышеупомянутого патента США № 5489677 и амидные остовы из вышеупомянутого патента США № 5602240. В некоторых вариантах осуществления РНК, представленные в данном документе, имеют морфолиновые структуры остова из вышеупомянутого патента США № 5034506.
Модифицированные РНК также могут содержать один или несколько замещенных сахарных фрагментов. iRNA, например dsRNA, представленные в данном документе, могут содержать в 2'-положении одно из следующего: OH; F; O-, S- или N-алкил; O-, S- или N-алкенил; O-, S- или N-алкинил или O-алкил-O-алкил, где алкил, алкенил и алкинил могут представлять собой замещенный или незамещенный C1-C10алкил или C2-C10алкенил и алкинил. Иллюстративные подходящие модификации включают O[(CH2)nO]mCH3, O(CH2).nOCH3, O(CH2)nNH2, O(CH2)nCH3, O(CH2)nONH2 и O(CH2)nON[(CH2)nCH3)]2, где n и m равняются от 1 до приблизительно 10. В других вариантах осуществления dsRNA содержат в 2'-положении одно из следующего: низший C1-C10алкил, замещенный низший алкил, алкарил, аралкил, O-алкарил или O-аралкил, SH, SCH3, OCN, Cl, Br, CN, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, гетероциклоалкил, гетероциклоалкарил, аминоалкиламино, полиалкиламино, замещенный силил, расщепляющую РНК группу, репортерную группу, интеркалятор, группу для улучшения фармакокинетических свойств iRNA или группу для улучшения фармакодинамических свойств iRNA и другие заместители с аналогичными свойствами. В некоторых вариантах осуществления модификация включает 2'-метоксиэтокси (2'-O-CH2CH2OCH3, также известный как 2'-O-(2-метоксиэтил) или 2'-MOE) (Martin et al., Helv. Chim. Acta, 1995, 78:486-504), т. e. алкокси-алкоксигруппу. Другой иллюстративной модификацией является 2'-диметиламинооксиэтокси, т. е. группа O(CH2)2ON(CH3)2, также известная как 2'-DMAOE, описанная в примерах в данном документе ниже, и 2'-диметиламиноэтоксиэтокси (также известная из уровня техники как 2'-O-диметиламиноэтоксиэтил или 2'-DMAEOE), т. е. 2'-O--CH2-O-CH2-N(CH2)2. Дополнительные иллюстративные модификации включают: 5'-Me-2'-F-модифицированные нуклеотиды, 5'-Me-2'-OMe-модифицированные нуклеотиды, 5'-Me-2'-дезоксинуклеотиды (как R-, так и S-изомеры в этих трех семействах); 2'-алкоксиалкил и 2'-NMA (N-метилацетамид).
Другие модификации включают 2'-метокси(2'-OCH3), 2'-аминопропокси(2'-OCH2CH2CH2NH2) и 2'-фтор (2'-F). Подобные модификации также могут быть осуществлены в других положениях в РНК из числа iRNA, в частности в 3'-положении сахара в 3'-концевом нуклеотиде или в dsRNA с 2'-5'-связями и в 5'-положении 5'-концевого нуклеотида. iRNA также могут содержать миметики сахаров, такие как циклобутильные фрагменты, вместо пентофуранозильного сахара. Иллюстративные патенты США, в которых изложено получение таких модифицированных сахарных структур, включают без ограничения патенты США №№ 4981957; 5118800; 5319080; 5359044; 5393878; 5446137; 5466786; 5514785; 5519134; 5567811; 5576427; 5591722; 5597909; 5610300; 5627053; 5639873; 5646265; 5658873; 5670633 и 5700920, некоторые из которых принадлежат авторам настоящей заявки. Полное содержание каждого из вышеупомянутых источников настоящим включено в данный документ посредством ссылки.
iRNA по настоящему изобретению также может содержать модификации или замены нуклеотидного основания (часто называемого в данной области техники просто "основанием"). Используемые в данном документе "немодифицированные" или "природные" нуклеотидные основания включают пуриновые основания аденин (A) и гуанин (G) и пиримидиновые основания тимин (T), цитозин (C) и урацил (U). Модифицированные нуклеотидные основания включают в себя другие синтетические и природные нуклеотидные основания, такие как 5-метилцитозин (5-Me-C), 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил- и другие алкилпроизводные аденина и гуанина, 2-пропил- и другие алкилпроизводные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галогенурацил и цитозин, 5-пропинилурацил и цитозин, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген-, 8-амино-, 8-тиол-, 8-тиоалкил-, 8-гидроксил- и другие 8-замещенные аденины и гуанины, 5-галоген-, в частности, 5-бром-, 5-трифторметил- и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 8-азагуанин и 8-азааденин, 7-дезазагуанин и 7-дезазааденин, а также 3-дезазагуанин и 3-дезазааденин. Дополнительные нуклеотидные основания включают такие, которые раскрыты в патенте США № 3687808, раскрытые в Modified Nucleosides in Biochemistry, Biotechnology and Medicine, Herdewijn, P. ed. Wiley-VCH, 2008; раскрытые в The Concise Encyclopedia Of Polymer Science And Engineering, pages 858-859, Kroschwitz, J. L, ed. John Wiley & Sons, 1990, раскрытые в Englisch et al., Angewandte Chemie, International Edition, 1991, 30:613, и раскрытые в Sanghvi, Y S., Chapter 15, dsRNA Research and Applications, pages 289-302, Crooke, S. T. and Lebleu, B., Ed., CRC Press, 1993. Некоторые из этих нуклеотидных оснований особенно применимы для повышения аффинности связывания олигомерных соединений, представленных в настоящем изобретении. Они включают 5-замещенные пиримидины, 6-азапиримидины и N-2-, N-6- и 0-6-замещенные пурины, в том числе 2-аминопропиладенин, 5-пропинилурацил и 5-пропинилцитозин. Было показано, что 5-метилцитозиновые замещения увеличивают стабильность дуплекса нуклеиновых кислот на 0,6-1,2°C (Sanghvi, Y. S., Crooke, S. T. and Lebleu, B., Eds., dsRNA Research and Applications, CRC Press, Boca Raton, 1993, pp. 276-278) и представляют собой иллюстративные замещения оснований, еще более конкретно в сочетании с 2'-O-метоксиэтиловыми модификациями сахарных фрагментов.
Иллюстративные патенты США, в которых изложено получение некоторых из вышеупомянутых модифицированных нуклеотидных оснований, а также других модифицированных нуклеотидных оснований, включают без ограничения вышеупомянутые патенты США №№ 3687808, 4845205; 513030; 5134066; 5175273; 5367066; 5432272; 5457187; 5459255; 5484908; 5502177; 5525711; 5552540; 5587469; 5594121, 5596091; 5614617; 5681941; 5750692; 6015886; 6147200; 6166197; 6222025; 6235887; 6380368; 6528640; 6639062; 6617438; 7045610; 7427672 и 7495088, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки.
iRNA по настоящему изобретению также может быть модифицирована таким образом, чтобы содержать одну или несколько запертых нуклеиновых кислот (LNA). Запертая нуклеиновая кислота представляет собой нуклеотид, содержащий модифицированный рибозный фрагмент, где рибозный фрагмент содержит дополнительный мостик, соединяющий 2'- и 4'-атомы углерода. Эта структура эффективно "запирает" рибозу в структурной конформации 3'-эндо. Было показано, что добавление запертых нуклеиновых кислот в siRNA повышает стабильность siRNA в сыворотке крови и снижает нецелевые эффекты (Elmen, J. et al., (2005) Nucleic Acids Research 33(1):439-447; Mook, OR. et al., (2007) Mol Canc Ther 6(3):833-843; Grunweller, A. et al., (2003) Nucleic Acids Research 31(12):3185-3193).
iRNA по настоящему изобретению также может быть модифицирована таким образом, чтобы содержать один или несколько бициклических сахарных фрагментов. "Бициклический сахар" представляет собой фуранозильное кольцо, модифицированное путем формирования мостика между двумя атомами. "Бициклический нуклеозид" ("BNA") представляет собой нуклеозид, имеющий сахарный фрагмент, содержащий мостик, соединяющий два атома углерода сахарного кольца, вследствие чего образуется бициклическая кольцевая система. В определенных вариантах осуществления мостик соединяет 4′-атом углерода и 2′-атом углерода в сахарном кольце. Таким образом, в некоторых вариантах осуществления средство по настоящему изобретению может содержать одну или несколько запертых нуклеиновых кислот (LNA). Запертая нуклеиновая кислота представляет собой нуклеотид, содержащий модифицированный рибозный фрагмент, где рибозный фрагмент содержит дополнительный мостик, соединяющий 2'- и 4'-атомы углерода. Другими словами, LNA представляет собой нуклеотид, содержащий бициклический сахарный фрагмент, содержащий мостик 4'-CH2-O-2'. Эта структура эффективно "запирает" рибозу в структурной конформации 3'-эндо. Было показано, что добавление запертых нуклеиновых кислот в siRNA повышает стабильность siRNA в сыворотке крови и снижает нецелевые эффекты (Elmen, J. et al., (2005) Nucleic Acids Research 33(1):439-447; Mook, OR. et al., (2007) Mol Canc Ther 6(3):833-843; Grunweller, A. et al., (2003) Nucleic Acids Research 31(12):3185-3193). Примеры бициклических нуклеозидов для применения в полинуклеотидах по настоящему изобретению включают без ограничения нуклеозиды, содержащие мостик между 4'- и 2'-атомами кольца рибозила. В определенных вариантах осуществления средства на основе антисмысловых полинуклеотидов по настоящему изобретению содержат один или несколько бициклических нуклеозидов, содержащих мостик 4'-2'. Примеры таких бициклических нуклеозидов с мостиком 4'-2' включают без ограничения 4'-(CH2)-O-2' (LNA); 4'-(CH2)-S-2'; 4'-(CH2)2-O-2' (ENA); 4'-CH(CH3)-O-2' (также называемый "конформационно затрудненный этилом" или "cEt") и 4'-CH(CH2OCH3)-O-2' (и его аналоги; см., например, патент США № 7399845); 4'-C(CH3)(CH3)-O-2' (и его аналоги; см., например, патент США № 8278283); 4'-CH2-N(OCH3)-2' (и его аналоги; см., например, патент США № 8278425); 4'-CH2-O-N(CH3)-2' (см., например, публикацию заявки на патент США № 2004/0171570); 4'-CH2-N(R)-O-2', где R представляет собой H, C1-C12-алкил или защитную группу (см., например, патент США № 7427672); 4'-CH2-C(H)(CH3)-2' (см., например., Chattopadhyaya et al., J. Org. Chem., 2009, 74, 118-134); и 4'-CH2-C(═CH2)-2' (и его аналоги; см., например., патент США № 8278426). Полное содержание каждого из вышеупомянутых источников настоящим включено в данный документ посредством ссылки.
Дополнительные иллюстративные патенты США и публикации заявок на патент США, в которых изложено получение нуклеотидов запертых нуклеиновых кислот, включают без ограничения следующие: патенты США №№ 6268490; 6525191; 6670461; 6770748; 6794499; 6998484; 7053207; 7034133;7084125; 7399845; 7427672; 7569686; 7741457; 8022193; 8030467; 8278425; 8278426; 8278283; US 2008/0039618 и US 2009/0012281, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки.
Любой из вышеупомянутых бициклических нуклеозидов можно получать с одной или несколькими стереохимическими конфигурациями сахаров, в том числе, например, α-L-рибофуранозой и β-D-рибофуранозой (см. WO 99/14226).
iRNA по настоящему изобретению также может быть модифицирована таким образом, чтобы содержать один или несколько затрудненных этилом нуклеотидов. Используемый в данном документе "затрудненный этилом нуклеотид" или "cEt" представляет собой запертую нуклеиновую кислоту, содержащую бициклический сахарный фрагмент, содержащий мостик 4'-CH(CH3)-0-2'. В одном варианте осуществления затрудненный этилом нуклеотид находится в S-конформации, обозначаемой в данном документе "S-cEt".
iRNA по настоящему изобретению может также содержать один или несколько "конформационно ограниченных нуклеотидов" ("CRN"). CRN представляют собой аналоги нуклеотидов с линкером, соединяющим C2'- и C4'-атомы углерода рибозы или C3- и C5′-атомы углерода рибозы. CRN запирает рибозное кольцо в стабильную конформацию и повышает аффинность гибридизации с mRNA. Длина линкера является достаточной, чтобы поместить атом кислорода в положение, оптимальное для стабильности и аффинности, что приводит к меньшему "сморщиванию" рибозного кольца.
Иллюстративные публикации, в которых изложено получение некоторых из вышеуказанных CRN, включают без ограничения публикацию заявки на патент США № 2013/0190383 и публикацию согласно PCT WO 2013/036868, полное содержание каждой из которых настоящим включено в данный документ посредством ссылки.
В некоторых вариантах осуществления iRNA по настоящему изобретению содержит один или несколько мономеров, которые представляют собой нуклеотиды по типу UNA (незапертых нуклеиновых кислот). UNA представляет собой незапертую ациклическую нуклеиновую кислоту, в которой какая-либо из связей в сахарном фрагменте была удалена с образованием незапертого "сахарного" остатка. В одном примере UNA также охватывает мономер, у которого были удалены связи C1'-C4' (т.е. ковалентная углерод-кислород-углеродная связь между атомами углерода C1' и C4'). В другом примере связь C2'-C3' (т.е. ковалентная углерод-углеродная связь между атомами углерода C2' и C3') в сахарном фрагменте была удалена (см. Nuc. Acids Symp. Series, 52, 133-134 (2008) и Fluiter et al., Mol. Biosyst., 2009, 10, 1039, настоящим включенные посредством ссылки).
Иллюстративные публикации США, в которых изложено получение UNA, включают без ограничения патент США № 8314227 и публикации заявок на патент США №№ 2013/0096289; 2013/0011922 и 2011/0313020, полное содержание каждого из которых настоящим включено в данный документ посредством ссылки.
Потенциально стабилизирующие модификации на концах молекул РНК могут включать N-(ацетиламинокапроил)-4-гидроксипролинол (Hyp-С6-NHAc), N-капроил-4-гидроксипролинол (Hyp-С6), N-ацетил-4-гидроксипролинол (Hyp-NHAc), тимидин-2'-0-дезокситимидин (простой эфир), N-(аминокапроил)-4-гидроксипролинол (Hyp-С6-амино), 2-докозаноилуридин-3"-фосфат, инвертированное основание dT (idT) и другие. Раскрытие этой модификации можно найти в публикации согласно PCT № WO 2011/005861.
Другие модификации iRNA по настоящему изобретению включают в себя 5'-фосфат или имитатор 5'-фосфата, например, 5'-концевой фосфат или имитатор фосфата в антисмысловой нити средства для RNAi. Подходящие миметики фосфатов раскрыты, например, в публикации заявки на патент США № 2012/0157511, полное содержание которой включено в данный документ посредством ссылки.
A. iRNA, содержащие нарушающие термостабильность модификации.
Как описано в данном документе, было обнаружено, среди прочего, что нецелевые эффекты средств на основе dsRNA, нацеливающихся на Serpina1, могут быть снижены или ингибированы путем встраивания нарушающих термостабильность нуклеотидов в некоторые положения в антисмысловой нити dsRNA. С этими нарушающими термостабильность модификациями в некоторых положениях в антисмысловой нити средства на основе dsRNA были способны сохранять активность, направленную на сайленсинг генов, сходную с исходной dsRNA, при этом характеризуясь пониженным нецелевым сайленсингом генов. Кроме того, число нецелевых генов, которые подвергаются понижающей регуляции или повышающей регуляции, также уменьшается посредством применения средств на основе dsRNA, содержащих такие нарушающие термостабильность модификации, по сравнению с исходной dsRNA.
В связи с этим, в одном аспекте настоящего изобретения предусмотрено двухнитевое средство для RNAi (dsRNA), способное к ингибированию экспрессии целевого гена Serpina1. В целом средства на основе dsRNA по настоящему изобретению демонстрируют высокий уровень целевого сайленсинга генов с понижением или минимизацией нецелевого сайленсинга генов и/или токсичности. Без ограничения средства на основе dsRNA по настоящему изобретению могут быть заменены средствами на основе dsRNA и могут применяться в методиках сайленсинга генов на основе РНК-интерференции, включающих без ограничения пути применения in vitro или in vivo.
В целом средство на основе dsRNA содержит смысловую нить (также называемую сопровождающей нитью) и антисмысловую нить (также называемую направляющей нитью). Каждая нить средства на основе dsRNA может варьировать по длине от 12 до 40 нуклеотидов. Например, длина каждой нити может составлять 14-40 нуклеотидов, 17-37 нуклеотидов, 25-37 нуклеотидов, 27-30 нуклеотидов, 17-23 нуклеотида, 17-21 нуклеотид, 17-19 нуклеотидов, 19-25 нуклеотидов, 19-23 нуклеотида, 19-21 нуклеотид, 21-25 нуклеотидов или 21-23 нуклеотида. Без ограничений смысловая и антисмысловая нити могут иметь одинаковую длину или неодинаковую длину.
В некоторых вариантах осуществления длина антисмысловой нити составляет 18-35 нуклеотидов. В некоторых вариантах осуществления длина антисмысловой нити составляет 21-25, 19-25, 19-21 или 21-23 нуклеотида. В некоторых конкретных вариантах осуществления длина антисмысловой нити составляет 23 нуклеотида. Аналогично антисмысловой нити, в некоторых вариантах осуществления длина смысловой нити может составлять 18-35 нуклеотидов. В некоторых вариантах осуществления длина смысловой нити составляет 21-25, 19-25, 19-21 или 21-23 нуклеотида. В некоторых конкретных вариантах осуществления длина антисмысловой нити составляет 21 нуклеотид.
В некоторых вариантах осуществления смысловая и антисмысловая нити независимо имеют длину 19, 20, 21, 22, 23, 24 или 25 нуклеотидов, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 18, 19, 21, 22, 23, 24 или 24 пары нуклеотидов; и (viii) dsRNA содержит тупой конец на 5'-конце смысловой нити. В некоторых конкретных вариантах осуществления смысловая нить имеет длину 19, 20, или 21, или 22 нуклеотида, и антисмысловая нить имеет длину 20, 21 или 22 нуклеотида.
Смысловая нить и антисмысловая нить, как правило, образуют дуплексную dsRNA. Длина дуплексного участка средства на основе dsRNA может составлять 12-40 пар нуклеотидов. Например, длина дуплексного участка может составлять 14-40 пар нуклеотидов, 17-30 пар нуклеотидов, 25-35 пар нуклеотидов, 27-35 пар нуклеотидов, 17-23 пары нуклеотидов, 17-21 пару нуклеотидов, 17-19 пар нуклеотидов, 19-25 пар нуклеотидов, 19-23 пары нуклеотидов, 19-21 пару нуклеотидов, 21-25 пар нуклеотидов или 21-23 пары нуклеотидов. В другом примере длина дуплексного участка выбрана из 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26 и 27 пар нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити. В некоторых конкретных вариантах осуществления длина дуплексного участка составляет 18, 19, 20, 21, 22 или 23 пары нуклеотидов. В конкретном варианте осуществления длина дуплексного участка составляет 21 пару нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит один или несколько «липких» участков и/или кэпирующих групп на 3'-конце, или 5'-конце, или обоих концах нити средства на основе dsRNA. Длина «липкого» конца может составлять 1-10 нуклеотидов, 1-6 нуклеотидов, например, 2-6 нуклеотидов, 1-5 нуклеотидов, 2-5 нуклеотидов, 1-4 нуклеотида, 2-4 нуклеотида, 1-3 нуклеотида, 2-3 нуклеотида или 1-2 нуклеотида. Наличие выступающих концов может быть результатом того, что одна нить длиннее другой, или может быть результатом того, что две нити одинаковой длины расположены со сдвигом. «Липкий» конец может образовывать ошибочное спаривание с целевой mRNA, или он может быть комплементарен последовательностям генов, подлежащим нацеливанию, или он может иметь другую последовательность. Первая и вторая нити также могут быть соединены, например, с помощью дополнительных оснований с образованием "шпильки" или с помощью других линкеров, не содержащих основания.
В некоторых вариантах осуществления каждый из нуклеотидов в участке «липкого» конца средства на основе dsRNA независимо может представлять собой модифицированный или немодифицированный нуклеотид, в том числе без ограничения с 2'-модифицированным сахаром, такой как 2-F-, 2'-O-метилтимидин (T), 2`-O-метоксиэтил-5-метилуридин (Teo), 2'-O-метоксиэтиладенозин (Aeo), 2'-O-метоксиэтил-5-метилцитидин (m5Ceo) и любые их комбинации. Например, последовательность «липкого» конца на обоих концах каждой нити может представлять собой TT. «Липкий» конец может образовывать ошибочное спаривание с целевой mRNA, или он может быть комплементарен последовательностям генов, подлежащим нацеливанию, или он может иметь другую последовательность.
5'- или 3'-выступающие концы смысловой нити, антисмысловой нити или обеих нитей средства на основе dsRNA по настоящему изобретению могут быть фосфорилированы. В некоторых вариантах осуществления участок «липкого» конца содержит два нуклеотида с фосфотиоатом между двумя нуклеотидами, при этом два нуклеотида могут быть одинаковыми или отличающимися. В некоторых вариантах осуществления «липкий» конец присутствует на 3'-конце смысловой нити, антисмысловой нити или обеих нитей. В некоторых вариантах осуществления этот 3'-липкий конец присутствует в антисмысловой нити. В некоторых вариантах осуществления этот 3'-липкий конец присутствует в смысловой нити.
Средство на основе dsRNA по настоящему изобретению может содержать только один выступающий конец, который может усиливать активность интерференции у dsRNA без воздействия на его общую стабильность. Например, однонитевой «липкий» конец расположен на 3'-конце смысловой нити или в качестве альтернативы на 3'-конце антисмысловой нити. dsRNA также может иметь тупой конец, расположенный на 5'-конце антисмысловой нити (или 3'-конце смысловой нити) или наоборот. Как правило, антисмысловая нить dsRNA имеет нуклеотидный «липкий» конец на 3'-конце, а 5'-конец является тупым концом. Не желая ограничиваться какой-либо теорией, предполагают, что асимметричные тупой конец на 5'-конце антисмысловой нити и 3'-концевой «липкий» конец антисмысловой нити способствуют включению направляющей нити в процесс с участием RISC. Например, длина одного «липкого» конца составляет по меньшей мере два, три, четыре, пять, шесть, семь, восемь, девять или десять нуклеотидов. В некоторых вариантах осуществления dsRNA имеет «липкий» конец из 2 нуклеотидов на 3'-конце антисмысловой нити и тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления один конец dsRNA представляет собой тупой конец, а другой конец предусматривает выступающий конец, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) и dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов. В некоторых вариантах осуществления «липкий» конец находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити. В некоторых конкретных вариантах осуществления «липкий» конец имеет длину 2, 3 или 4 нуклеотида.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, где один конец dsRNA представляет собой тупой конец, а другой конец предусматривает выступающий конец, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти или всем шести) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации, и необязательно «липкий» конец из 2 нуклеотидов находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити. В некоторых вариантах осуществления «липкий» конец находится на 3'-конце антисмысловой нити, а тупой конец находится на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению может также иметь два тупых конца на обоих концах dsRNA-дуплекса.
В некоторых вариантах осуществления dsRNA предусматривает тупой конец на обоих концах дуплекса, где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, и при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA содержит дуплексный участок с длиной, составляющей 19, 21, 22 или 23 пары нуклеотидных оснований, и предусматривает тупой конец на обоих концах дуплекса, где один конец dsRNA представляет собой тупой конец, а другой конец предусматривает выступающий конец, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти или всем шести) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере одну (например, одну, две, три, четыре, пять или более) нарушающую термостабильность модификацию дуплекса в пределах первых 9 положений нуклеотидов 5'-участка антисмысловой нити. В некоторых вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положениях 2-9 или предпочтительно положениях 4-8 от 5'-конца антисмысловой нити. В некоторых дополнительных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 6, 7 или 8 от 5'-конца антисмысловой нити. В еще некоторых дополнительных вариантах осуществления нарушающая термостабильность модификация дуплекса находится в положении 7 от 5'-конца антисмысловой нити. Термин "нарушающая (нарушающие) термостабильность модификация (модификации)" включает модификацию (модификации), приводящую (приводящие) в результате к dsRNA с более низкой общей температурой плавления (Tm) (предпочтительно Tm на один, два, три или четыре градуса ниже, чем Tm dsRNA, не имеющей такой (таких) модификации (модификаций).
Нарушающие термостабильность модификации могут включать без ограничения модификацию с удалением азотистого основания; ошибочное спаривание с противоположным нуклеотидом противоположной цепи; и модификацию сахара, такую как 2'-дезокси-модификация или ациклический нуклеотид, например, незапертые нуклеиновые кислоты (UNA) или гликолевая нуклеиновая кислота (GNA).
Иллюстративные модификации с удаление азотистого основания включают без ограничения следующее:
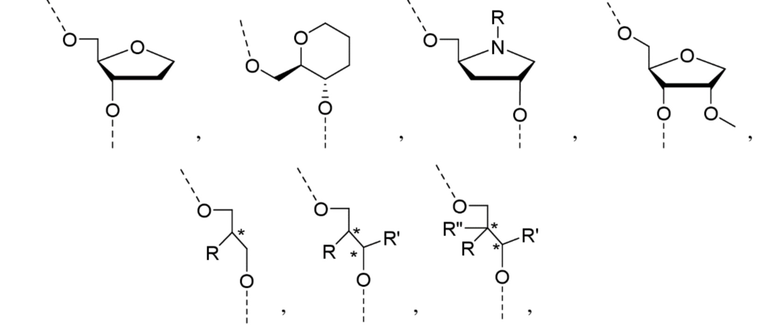
где R=H, Me, Et или OMe; R' = H, Me, Et или OMe; R" = H, Me, Et или OMe,
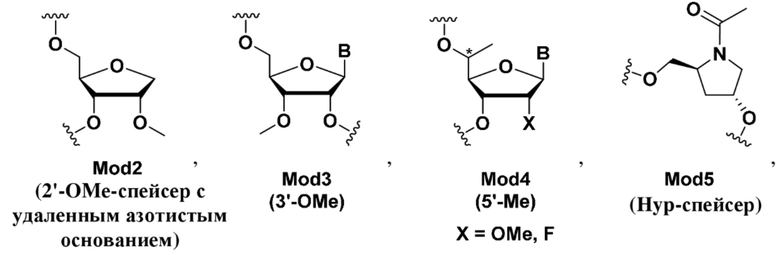
где B представляет собой модифицированное или немодифицированное нуклеотидное основание.
Иллюстративные модификации сахара включают без ограничения следующее:
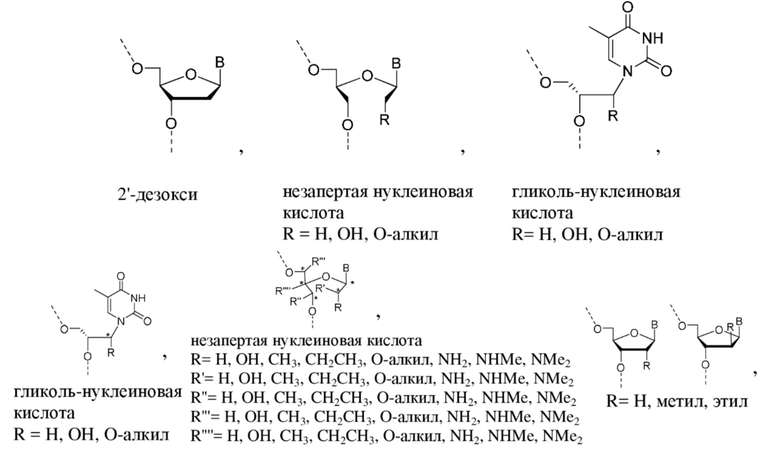
где B представляет собой модифицированное или немодифицированное нуклеотидное основание.
В некоторых вариантах осуществления нарушающая термостабильность модификация дуплекса выбрана из группы, состоящей из:
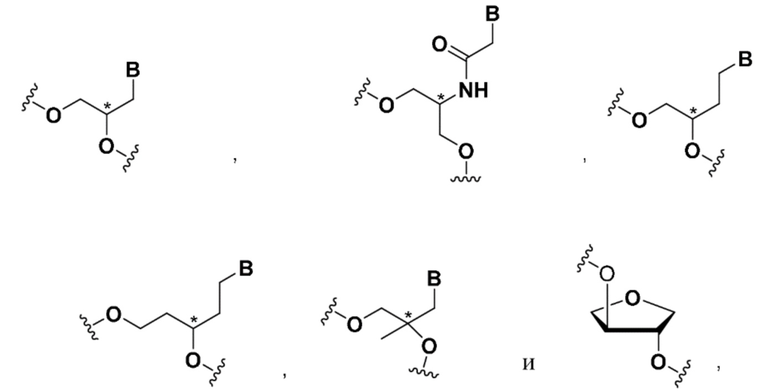
где B представляет собой модифицированное или немодифицированное нуклеотидное основание.
Термин "ациклический нуклеотид" относится к любому нуклеотиду с ациклическим рибозным сахаром, например, в котором отсутствует любая из связей между атомами углерода рибозы (например, C1'-C2', C2'-C3', C3'-C4', C4'-O4' или C1'-O4') и/или в нуклеотиде отсутствует независимо или в комбинации по меньшей мере один из атомов углерода или атом кислорода рибозы (например, C1', C2', C3', C4' или O4'). В некоторых вариантах осуществления ациклический нуклеотид представляет собой 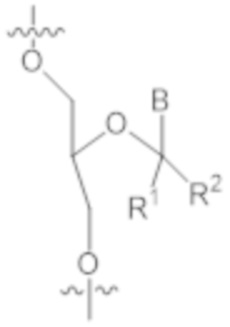 ,
, 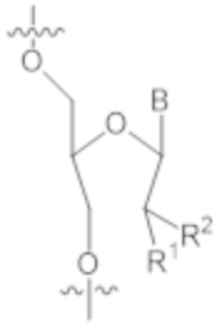 ,
, 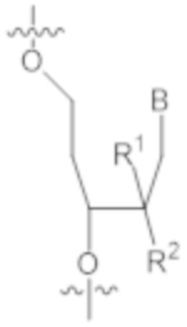 ,
, 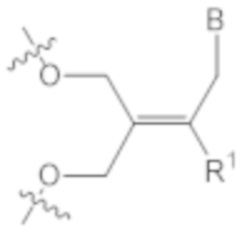 или
или 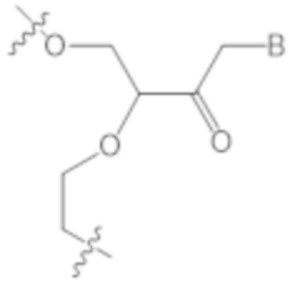 , где B представляет собой модифицированное или немодифицированное нуклеотидное основание, R1 и R2 независимо представляют собой H, галоген, OR3 или алкил; и R3 представляет собой H, алкил, циклоалкил, арил, аралкил, гетероарил или сахар. Термин "UNA" относится к незапертой ациклической нуклеиновой кислоте, в которой какая-либо из связей в сахаре была удалена с образованием незапертого "сахарного" остатка. В одном примере UNA также охватывает мономеры, у которых удалены связи между C1'-C4' (т.е. ковалентная углерод-кислород-углеродная связь между атомами углерода C1' и C4'). В другом примере связь C2'-C3' (т.е. ковалентная углерод-углеродная связь между атомами углерода C2' и C3') в сахаре удалена (см. Mikhailov et al., Tetrahedron Letters, 26 (17): 2059 (1985); и Fluiter et al., Mol. Biosyst., 10: 1039 (2009), которые тем самым включены посредством ссылки во всей своей полноте). Ациклическое производное обеспечивает большую гибкость остова, не оказывая влияние на спаривание оснований по Уотсону-Крику. Ациклический нуклеотид может быть связан посредством связи 2'-5' или 3'-5'.
, где B представляет собой модифицированное или немодифицированное нуклеотидное основание, R1 и R2 независимо представляют собой H, галоген, OR3 или алкил; и R3 представляет собой H, алкил, циклоалкил, арил, аралкил, гетероарил или сахар. Термин "UNA" относится к незапертой ациклической нуклеиновой кислоте, в которой какая-либо из связей в сахаре была удалена с образованием незапертого "сахарного" остатка. В одном примере UNA также охватывает мономеры, у которых удалены связи между C1'-C4' (т.е. ковалентная углерод-кислород-углеродная связь между атомами углерода C1' и C4'). В другом примере связь C2'-C3' (т.е. ковалентная углерод-углеродная связь между атомами углерода C2' и C3') в сахаре удалена (см. Mikhailov et al., Tetrahedron Letters, 26 (17): 2059 (1985); и Fluiter et al., Mol. Biosyst., 10: 1039 (2009), которые тем самым включены посредством ссылки во всей своей полноте). Ациклическое производное обеспечивает большую гибкость остова, не оказывая влияние на спаривание оснований по Уотсону-Крику. Ациклический нуклеотид может быть связан посредством связи 2'-5' или 3'-5'.
Термин 'GNA' относится к гликолевой нуклеиновой кислоте, которая представляет собой полимер, подобный ДНК или РНК, но отличающийся от них составом своего "остова", поскольку его составляют повторяющиеся единицы глицерина, соединенные фосфодиэфирными связями:
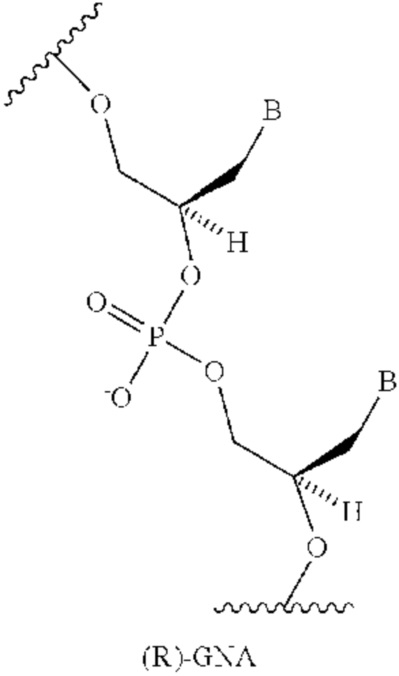 .
.
Нарушающая термостабильность модификация дуплекса может представлять собой ошибочные спаривания (т.е. некомплементарные пары оснований) между нарушающим термостабильность нуклеотидом и противоположным нуклеотидом противоположной нити dsRNA-дуплекса. Иллюстративные ошибочно спаренные пары оснований включают G:G, G:A, G:U, G:T, A:A, A:C, C:C, C:U, C:T, U:U, T:T, U:T или их комбинацию. Другие типы ошибочного спаривания оснований, известные из уровня техники, также применимы в настоящем изобретении. Может происходить ошибочное спаривание между нуклеотидами, которые представляют собой как встречающиеся в природе нуклеотиды, так и модифицированные нуклеотиды, т.е. ошибочное спаривание оснований может происходить между нуклеотидными основаниями соответствующих нуклеотидов независимо от модификаций у рибозных сахаров нуклеотидов. В определенных вариантах осуществления средство на основе dsRNA содержит по меньшей мере одно ошибочно спаренное нуклеотидное основание, то есть 2'-дезоксирибонуклеотид; например, 2'-дезоксирибонуклеотид в смысловой нити.
В некоторых вариантах осуществления нарушающая термостабильность модификация дуплекса в затравочной области антисмысловой нити включает нуклеотиды с ослабленной способностью к образованию H-связей по W-C с комплементарным основанием целевой mRNA, такие как:
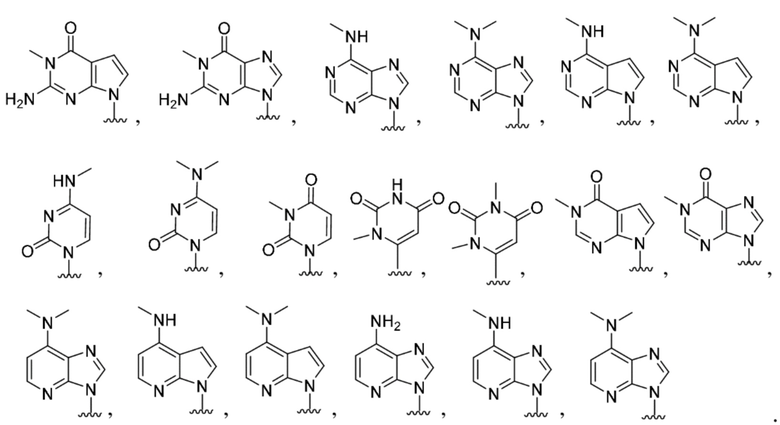
Большее число примеров нуклеотидов с удаленным азотистым основанием, модификаций в виде ациклических нуклеотидов (включая UNA и GNA) и модификаций, представляющих собой ошибочное спаривание, подробно описано в WO 2011/133876, который включен в данный документ посредством ссылки во всей своей полноте.
Нарушающие термостабильность модификации также могут включать универсальное основание со сниженной или устраненной способностью образовывать водородные связи с основаниями противоположной нити, а также фосфатные модификации.
В некоторых вариантах осуществления нарушающая термостабильность модификация дуплекса включает нуклеотиды с неканоническими основаниями, такие как без ограничения модификации нуклеотидных оснований с ослабленной или полностью устраненной способностью образовывать водородные связи с основаниями в противоположной нити. Такие модификации нуклеотидных оснований были исследованы в отношении дестабилизации центрального участка dsRNA-дуплекса, как описано в WO 2010/0011895, который включен в данный документ посредством ссылки во всей своей полноте. Иллюстративные модификации нуклеотидных оснований представляют собой:
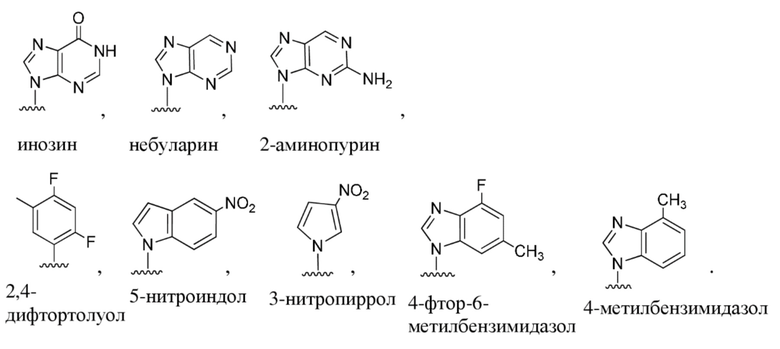
В некоторых вариантах осуществления нарушающая термостабильность модификация дуплекса в затравочной области антисмысловой нити включает один или несколько α-нуклеотидов, комплементарных основанию в целевой mRNA, таких как:
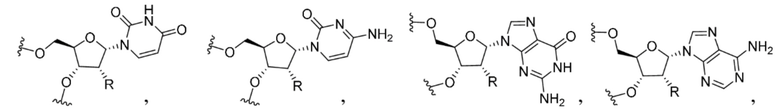
где R представляет собой H, OH, OCH3, F, NH2, NHMe, NMe2 или O-алкил.
Иллюстративные фосфатные модификации, которые, как известно, снижают термостабильность dsRNA-дуплексов по сравнению с природными фосфодиэфирными связями, представляют собой:
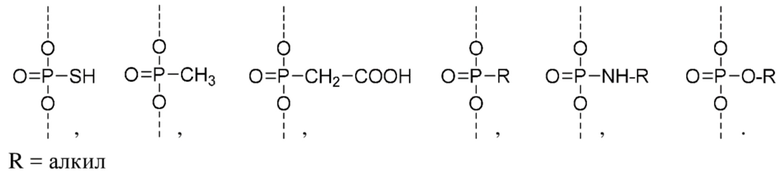
Алкил для группы R может представлять собой C1-C6алкил. Конкретные алкилы для группы R включают без ограничения метил, этил, пропил, изопропил, бутил, пентил и гексил.
В дополнение к антисмысловой нити, содержащей нарушающую термостабильность модификацию, dsRNA может также содержать одну или несколько стабилизирующих модификаций. Например, dsRNA может содержать по меньшей мере две (например, две, три, четыре, пять, шесть, семь, восемь, девять, десять или более) стабилизирующих модификаций. Без ограничений все стабилизирующие модификации могут находиться в одной нити. В некоторых вариантах осуществления как смысловая, так и антисмысловая нити содержат по меньшей мере две стабилизирующих модификации. Стабилизирующая модификация может встречаться у любого нуклеотида смысловой нити или антисмысловой нити. Например, стабилизирующая модификация может встречаться у каждого нуклеотида в смысловой нити и/или антисмысловой нити; при этом каждая стабилизирующая модификация может встречаться в виде чередующегося паттерна в смысловой нити или антисмысловой нити; или же смысловая нить или антисмысловая нить содержит обе стабилизирующие модификации в виде чередующегося паттерна. Чередующийся паттерн стабилизирующих модификаций в смысловой нити может быть таким же, как у антисмысловой нити, или отличным от него, и чередующийся паттерн стабилизирующих модификаций в смысловой нити может иметь сдвиг относительно чередующегося паттерна стабилизирующих модификаций в антисмысловой нити.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере две (например, две, три, четыре, пять, шесть, семь, восемь, девять, десять или более) стабилизирующих модификаций. Без ограничений стабилизирующая модификация в антисмысловой нити может присутствовать в любом из положений. В некоторых вариантах осуществления антисмысловая нить содержит стабилизирующие модификации в положениях 2, 6, 8, 9, 14 и 16 от 5'-конца. В некоторых других вариантах осуществления антисмысловая нить содержит стабилизирующие модификации в положениях 2, 6, 14 и 16 от 5'-конца. В еще некоторых других вариантах осуществления антисмысловая нить содержит стабилизирующие модификации в положениях 2, 14 и 16 от 5'-конца.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере одну стабилизирующую модификацию, которая расположена рядом с дестабилизирующей модификацией. Например, стабилизирующая модификация может представлять собой нуклеотид при 5'-конце или 3'-конце дестабилизирующей модификации, т.е. в положении -1 или +1 относительно положения дестабилизирующей модификации. В некоторых вариантах осуществления антисмысловая нить содержит стабилизирующую модификацию при каждом из 5'-конца и 3'-конца дестабилизирующей модификации, т. е. в положениях -1 и +1 относительно положения дестабилизирующей модификации.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере две стабилизирующие модификации при 3'-конце дестабилизирующей модификации, т.е. в положениях +1 и +2 относительно положения дестабилизирующей модификации.
В некоторых вариантах осуществления смысловая нить содержит по меньшей мере две (например, две, три, четыре, пять, шесть, семь, восемь, девять, десять или более) стабилизирующие модификации. Без ограничений стабилизирующая модификация в смысловой нити может присутствовать в любом из положений. В некоторых вариантах осуществления смысловая нить содержит стабилизирующие модификации в положениях 7, 10 и 11 от 5'-конца. В некоторых вариантах осуществления смысловая нить содержит стабилизирующие модификации в положениях 7, 9, 10 и 11 от 5'-конца. В некоторых вариантах осуществления смысловая нить содержит стабилизирующие модификации в положениях, являющихся противоположными или комплементарными положениям 11, 12 и 15 антисмысловой нити, считая от 5'-конца антисмысловой нити. В некоторых вариантах осуществления смысловая нить содержит стабилизирующие модификации в положениях, являющихся противоположными или комплементарными положениям 11, 12, 13 и 15 антисмысловой нити, считая от 5'-конца антисмысловой нити. В некоторых вариантах осуществления смысловая нить содержит блок из двух, трех или четырех стабилизирующих модификаций.
В некоторых вариантах осуществления смысловая нить не содержит стабилизирующую модификацию в положении, являющемся противоположным или комплементарным нарушающей термостабильность модификации дуплекса в антисмысловой нити.
Иллюстративные повышающие термостабильность модификации включают без ограничения 2'-фтор-модификации.
В некоторых вариантах осуществления dsRNA по настоящему изобретению содержит по меньшей мере четыре (например, четыре, пять, шесть, семь, восемь, девять, десять или более) 2'-фтор-модифицированных нуклеотида. Без ограничений все 2'-фтор-модифицированные нуклеотиды могут находиться в одной нити. В некоторых вариантах осуществления как смысловая, так и антисмысловая нити содержат по меньшей мере два 2'-фтор-модифицированных нуклеотида. 2'-Фтор-модификация может встречаться у любого нуклеотида смысловой нити или антисмысловой нити. Например, 2'-фтор-модификация может встречаться у каждого нуклеотида в смысловой нити и/или антисмысловой нити; при этом каждая 2'-фтор-модификация может встречаться в виде чередующегося паттерна в смысловой нити или антисмысловой нити; или же смысловая нить или антисмысловая нить содержит обе 2'-фтор-модификации в виде чередующегося паттерна. Чередующийся паттерн 2'-фтор-модификаций в смысловой нити может быть таким же, как у антисмысловой нити, или отличным от него, и чередующийся паттерн 2'-фтор-модификаций в смысловой нити может иметь сдвиг относительно чередующегося паттерна 2'-фтор-модификаций в антисмысловой нити.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере два (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более) 2'-фтор-модифицированных нуклеотида. Без ограничений 2'-фтор-модификация в антисмысловой нити может присутствовать в любом из положений. В некоторых вариантах осуществления антисмысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях 2, 6, 8, 9, 14 и 16 от 5'-конца. В некоторых вариантах осуществления антисмысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях 2, 6, 14 и 16 от 5'-конца. В еще некоторых других вариантах осуществления антисмысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях 2, 14 и 16 от 5'-конца.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере один 2'-фтор-модифицированный нуклеотид, который расположен рядом с дестабилизирующей модификацией. Например, 2'-фтор-модифицированным нуклеотидом может являться нуклеотид при 5'-конце или 3'-конце дестабилизирующей модификации, т.е. в положении -1 или +1 относительно положения дестабилизирующей модификации. В некоторых вариантах осуществления антисмысловая нить содержит 2'-фтор-модифицированный нуклеотид при каждом из 5'-конца и 3'-конца дестабилизирующей модификации, т.е. в положениях -1 и +1 относительно положения дестабилизирующей модификации.
В некоторых вариантах осуществления антисмысловая нить содержит по меньшей мере два 2'-фтор-модифицированных нуклеотида при 3'-конце дестабилизирующей модификации, т.е. в положениях +1 и +2 относительно положения дестабилизирующей модификации.
В некоторых вариантах осуществления смысловая нить содержит по меньшей мере два (например, два, три, четыре, пять, шесть, семь, восемь, девять, десять или более) 2'-фтор-модифицированных нуклеотида. Без ограничений 2'-фтор-модификация в смысловой нити может присутствовать в любом из положений. В некоторых вариантах осуществления антисмысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях 7, 10 и 11 от 5'-конца. В некоторых вариантах осуществления смысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях 7, 9, 10 и 11 от 5'-конца. В некоторых вариантах осуществления смысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях, являющихся противоположными или комплементарными положениям 11, 12 и 15 антисмысловой нити, считая от 5'-конца антисмысловой нити. В некоторых вариантах осуществления смысловая нить содержит 2'-фтор-модифицированные нуклеотиды в положениях, являющихся противоположными или комплементарными положениям 11, 12, 13 и 15 антисмысловой нити, считая от 5'-конца антисмысловой нити. В некоторых вариантах осуществления смысловая нить содержит блок из двух, трех или четырех 2'-фтор-модифицированных нуклеотидов.
В некоторых вариантах осуществления смысловая нить не содержит 2'-фтор-модифицированный нуклеотид в положении, являющемся противоположным или комплементарным нарушающей термостабильность модификации дуплекса в антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую нить из 21 нуклеотида (нт) и антисмысловую нить из 23 нуклеотидов (нт), где антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т. е. в положении 2-9 5'-конца антисмысловой нити), при этом один конец dsRNA является тупым, в то время как другой конец предусматривает выступающий конец из 2 нт, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит тупой конец на 5'-конце антисмысловой нити. Предпочтительно «липкий» конец из 2 нт находится на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую и антисмысловую нити, где длина смысловой нити составляет 25-30 нуклеотидных остатков, при этом, считая от 5'-концевого нуклеотида (положение 1), в положениях 1-23 указанной смысловой нити содержится по меньшей мере 8 рибонуклеотидов; длина антисмысловой нити составляет 36-66 нуклеотидных остатков и, считая от 3'-концевого нуклеотида, содержит по меньшей мере 8 рибонуклеотидов в положениях, спаренных с положениями 1-23 смысловой нити с образованием дуплекса; при этом по меньшей мере 3'-концевой нуклеотид антисмысловой нити является неспаренным со смысловой нитью, и не более 6 последовательных 3'-концевых нуклеотидов являются неспаренными со смысловой нитью, образуя тем самым 3'-однонитевой «липкий» конец из 1-6 нуклеотидов; при этом 5'-конец антисмысловой нити содержит 10-30 последовательных нуклеотидов, неспаренных со смысловой нитью, образуя тем самым 5'-однонитевой «липкий» конец из 10-30 нуклеотидов; при этом по меньшей мере 5'-концевые и 3'-концевые нуклеотиды смысловой нити образуют пары оснований с нуклеотидами антисмысловой нити, если смысловая и антисмысловая нити выровнены с обеспечением максимальной комплементарности, образуя тем самым практически дуплексный участок между смысловой и антисмысловой нитями; и антисмысловая нить в достаточной степени комплементарна целевой РНК на протяжении по меньшей мере 19 рибонуклеотидов по длине антисмысловой нити для снижения экспрессии целевого гена при введении указанной двухнитевой нуклеиновой кислоты в клетку млекопитающего; и при этом антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, где по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), например, нарушающий термостабильность нуклеотид находится между положениями, являющимися противоположными или комплементарными положениям 14-17 5'-конца смысловой нити, и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-30 пар нуклеотидов.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит смысловую и антисмысловую нити, где указанное средство на основе dsRNA содержит смысловую нить, длина которой составляет по меньшей мере 25 и не более 29 нуклеотидов, и антисмысловую нить, длина которой составляет не более 30 нуклеотидов, при этом смысловая нить содержит модифицированный нуклеотид, что придает чувствительность к ферментативному расщеплению, в положении 11 от 5'-конца, при этом 3'-конец указанной смысловой нити и 5'-конец указанной антисмысловой нити образуют тупой конец, и указанная антисмысловая нить на своем 3'-конце на 1-4 нуклеотида длиннее, чем смысловая нить, при этом длина дуплексного участка составляет по меньшей мере 25 нуклеотидов, и указанная антисмысловая нить в достаточной степени комплементарна целевой mRNA на протяжении по меньшей мере 19 нт по длине указанной антисмысловой нити для снижения экспрессии целевого гена при введении указанного средства на основе dsRNA в клетку млекопитающего, и при этом расщепление указанной dsRNA под действием Dicer предпочтительно приводит к siRNA, содержащей указанный 3'-конец указанной антисмысловой нити, вследствие чего обеспечивается снижение экспрессии целевого гена у млекопитающего, при этом антисмысловая нить содержит по меньшей мере один нарушающий термостабильность нуклеотид, при этом по меньшей мере один нарушающий термостабильность нуклеотид находится в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; и (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; и (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-29 пар нуклеотидов.
В некоторых вариантах осуществления каждый нуклеотид в смысловой нити и антисмысловой нити средства на основе dsRNA может быть модифицирован. Каждый нуклеотид может быть модифицированным с помощью одинаковой или разной модификации, которые могут включать одно или несколько изменений одного или обоих не связанных с фосфатом атомов кислорода и/или одного или нескольких связанных с фосфатом атомов кислорода; изменение компонента рибозного сахара, например, 2'-гидроксила в рибозном сахаре; полную замену фосфатного фрагмента "дефосфорилированными" линкерами; модификацию или замену встречающегося в природе основания и замену или модификацию рибозофосфатного остова.
Поскольку нуклеиновые кислоты представляют собой полимеры из субъединиц, то многие модификации встречаются в положении, которое повторяется в пределах нуклеиновой кислоты, например, модификация основания, или фосфатного фрагмента, или не образующего связь атома O фосфатного фрагмента. В некоторых случаях модификация будет встречаться во всех рассматриваемых положениях в нуклеиновой кислоте, но во многих случаях не будет. В качестве примера модификация может встречаться только в 3'- или 5'-концевом положении, может встречаться только в концевом участке, например, в положении концевого нуклеотида или в последних 2, 3, 4, 5 или 10 нуклеотидах нити. Модификация может встречаться в двухнитевом участке, в однонитевом участке или в обоих. Модификация может встречаться только в двухнитевом участке РНК или может встречаться только в однонитевом участке РНК. Например, фосфотиоатная модификация в положении не образующего связь атома O может встречаться только на одном или обоих концах, может встречаться только в концевом участке, например, в положении концевого нуклеотида или в последних 2, 3, 4, 5 или 10 нуклеотидах нити, или может встречаться в двухнитевом и однонитевом участках, в частности на концах. 5'-конец или концы могут быть фосфорилированными.
Существует возможность, например, для повышения стабильности, включения конкретных оснований в выступающие концы или включения модифицированных нуклеотидов или имитаторов нуклеотидов в однонитевые выступающие концы, например, в 5'- или 3'-выступающий конец или в оба. Например, может быть желательно включить пуриновые нуклеотиды в выступающие концы. В некоторых вариантах осуществления все или некоторые основания в 3'- или 5'-липком конце могут быть модифицированы, например, с помощью модификации, описанной в данном документе. Модификации могут включать, например, применение модификаций в 2'-положении рибозного сахара с модификациями, известными из уровня техники, например, применение дезоксирибонуклеотидов, 2'-дезокси-2'-фтор-(2'-F)- или 2'-O-метил-модифицированного вместо рибозного сахара нуклеотидного основания, а также модификации в фосфатной группе, например фосфотиоатные модификации. Выступающие концы необязательно должны быть гомологичными с целевой последовательностью.
В некоторых вариантах осуществления каждый остаток смысловой нити и антисмысловой нити независимо модифицирован с помощью LNA, HNA, CeNA, 2'-метоксиэтила, 2'-O-метила, 2'-O-аллила, 2'-C-аллила, 2'-дезокси или 2'-фтора. Нити могут содержать более одной модификации. В некоторых вариантах осуществления каждый остаток смысловой нити и антисмысловой нити независимо модифицирован с помощью 2'-O-метила или 2'-фтора. Следует понимать, что такие модификации являются дополнительными к по меньшей мере одной нарушающей термостабильность модификации дуплекса, присутствующей в антисмысловой нити.
Как правило, в смысловой нити и антисмысловой нити присутствуют по меньшей мере две различные модификации. Эти две модификации могут представлять собой 2'-дезокси, 2'-O-метил- или 2'-фтор-модификации, ациклические нуклеотиды или другие. В некоторых вариантах осуществления каждая из смысловой нити и антисмысловой нити содержит два по-разному модифицированных нуклеотида, выбранных из 2'-O-метила или 2'-дезокси. В некоторых вариантах осуществления каждый остаток в смысловой нити и в антисмысловой нити независимо модифицирован с помощью 2'-O-метилнуклеотида, 2'-дезоксинуклеотида, 2´-дезоксифторнуклеотида, 2'-O-N-метилацетамидо-(2'-O-NMA)-нуклеотида, 2'-O-диметиламиноэтоксиэтил-(2'-O-DMAEOE)-нуклеотида, 2'-O-аминопропил-(2'-O-AP)-нуклеотида или 2'-ара-F-нуклеотида. Опять же, следует понимать, что такие модификации являются дополнительными к по меньшей мере одной нарушающей термостабильность модификации дуплекса, присутствующей в антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит модификации в виде чередующегося паттерна, в частности в участках B1, B2, B3, B1', B2', B3', B4'. Термин "чередующийся мотив" или "чередующийся паттерн", используемый в данном документе, относится к мотиву с одной или несколькими модификациями, при этом каждая модификация встречается в чередующихся нуклеотидах одной нити. Чередующийся нуклеотид может обозначать каждый второй нуклеотид или каждый третий нуклеотид или аналогичный паттерн. Например, если каждый из A, B и C представляет собой один тип модификации в нуклеотиде, то чередующийся мотив может представлять собой "ABABABABABAB…", "AABBAABBAABB…", "AABAABAABAAB…", "AAABAAABAAAB…", "AAABBBAAABBB…" или "ABCABCABCABC…" и т. д.
Тип модификаций, содержащихся в чередующемся мотиве, может быть одинаковым или разным. Например, если каждый из A, B, C, D представляет собой один тип модификации в нуклеотиде, то чередующийся паттерн, т.е. модификации каждого второго нуклеотида, может быть одинаковым, но для каждой из смысловой нити или антисмысловой нити может существовать нескольких возможных вариантов модификаций в пределах чередующегося мотива, как, например, "ABABAB…", "ACACAC…", "BDBDBD…" или "CDCDCD…" и т. д.
В некоторых вариантах осуществления для средства на основе dsRNA по настоящему изобретению предусмотрено, что паттерн модификаций для чередующегося мотива на смысловой нити сдвинут относительно паттерна модификаций для чередующегося мотива на антисмысловой нити. Сдвиг может быть таким, что модифицированная группа нуклеотидов смысловой нити соответствует группе нуклеотидов антисмысловой нити, модифицированной другим способом, и наоборот. Например, при спаривании смысловой нити с антисмысловой нитью в dsRNA-дуплексе чередующийся мотив в смысловой нити может начинаться с "ABABAB" от 5'- к 3'-концу нити, а чередующийся мотив в антисмысловой нити может начинаться с "BABABA" от 3'- к 5'-концу нити в пределах дуплексного участка. В качестве другого примера чередующийся мотив в смысловой нити может начинаться с "AABBAABB" от 5'- к 3'-концу нити, а чередующийся мотив в антисмысловой нити может начинаться с "BBAABBAA" от 3'- к 5'-концу нити в пределах дуплексного участка, так что между смысловой нитью и антисмысловой нитью существует полный или частичный сдвиг паттернов модификаций.
Средство на основе dsRNA по настоящему изобретению может дополнительно содержать по меньшей мере одну фосфотиоатную или метилфосфонатную межнуклеотидную связь. Фосфотиоатная или метилфосфонатная модификация межнуклеотидной связи может встречаться на любом нуклеотиде смысловой нити, или антисмысловой нити, или обеих нитей в любом положении нити. Например, модификация межнуклеотидной связи может встречаться у каждого нуклеотида в смысловой нити и/или антисмысловой нити; при этом каждая модификация межнуклеотидной связи может встречаться в виде чередующегося паттерна в смысловой нити или антисмысловой нити; или смысловая нить или антисмысловая нить содержат обе модификации межнуклеотидной связи в виде чередующегося паттерна. Чередующийся паттерн модификаций межнуклеотидной связи в смысловой нити может быть таким же, как у антисмысловой нити, или отличным от него, и чередующийся паттерн модификаций межнуклеотидной связи в смысловой нити может иметь сдвиг относительно чередующегося паттерна модификаций межнуклеотидной связи в антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA содержит фосфотиоатную или метилфосфонатную модификацию межнуклеотидной связи в участке «липкого» конца. Например, участок «липкого» конца содержит два нуклеотида с фосфотиоатной или метилфосфонатной межнуклеотидной связью между этими двумя нуклеотидами. Модификации межнуклеотидной связи также могут быть выполнены для присоединения нуклеотидов «липкого» конца к концевым спаренным нуклеотидам в пределах дуплексного участка. Например, по меньшей мере 2, 3, 4 или все нуклеотиды «липкого» конца могут быть связаны посредством фосфотиоатной или метилфосфонатной межнуклеотидной связи и необязательно могут присутствовать дополнительные фосфотиоатные или метилфосфонатные межнуклеотидные связи, соединяющие нуклеотид «липкого» конца со спаренным нуклеотидом, который следует за нуклеотидом «липкого» конца. Например, между тремя концевыми нуклеотидами могут присутствовать по меньшей мере две фосфотиоатные межнуклеотидные связи, при этом два из трех нуклеотидов представляют собой нуклеотиды «липкого» конца, а третий представляет собой спаренный нуклеотид, следующий за нуклеотидом «липкого» конца. Предпочтительно эти три концевые нуклеотида могут находиться на 3'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая нить средства на основе dsRNA содержит 1-10 блоков из двух - десяти фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная смысловая нить спарена с антисмысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из двух фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 или 18 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA, содержит два блока из трех фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из четырех фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13 или 14 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA, содержит два блока из пяти фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из шести фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из семи фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5, 6, 7 или 8 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из восьми фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3, 4, 5 или 6 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления антисмысловая нить средства на основе dsRNA содержит два блока из девяти фосфотиоатных или метилфосфонатных межнуклеотидных связей, разделенных 1, 2, 3 или 4 фосфатными межнуклеотидными связями, где одна из фосфотиоатных или метилфосфонатных межнуклеотидных связей размещена в любом положении в олигонуклеотидной последовательности, и указанная антисмысловая нить спарена со смысловой нитью, содержащей любую комбинацию фосфотиоатных, метилфосфонатных и фосфатных межнуклеотидных связей, или с антисмысловой нитью, содержащей или фосфотиоатную, или метилфосфонатную, или фосфатную связь.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну или несколько фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в пределах 1-10 концевых положений смысловой и/или антисмысловой нити. Например, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов могут быть связаны посредством фосфотиоатной или метилфосфонатной межнуклеотидной связи на одном конце или обоих концах смысловой и/или антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну или несколько фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в пределах 1-10 остатков внутреннего участка дуплекса каждой из смысловой и/или антисмысловой нити. Например, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9 или 10 нуклеотидов могут быть соединены посредством фосфотиоатной или метилфосфонатной межнуклеотидной связи в положении 8-16 дуплексного участка, считая от 5'-конца смысловой нити; при этом средство на основе dsRNA необязательно может дополнительно содержать одну или несколько фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в пределах 1-10 концевых положений.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит от одной до пяти фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в пределах положений 1-5 и от одной до пяти фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), и от одной до пяти фосфотиоатных или метилфосфонатных модификаций межнуклеотидной связи в положениях 1 и 2 и от одной до пяти в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 1-5 и одну фосфотиоатную или метилфосфонатную модификацию межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), и одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные или метилфосфонатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), а также одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), и одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), и одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 1-5 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), и две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 1-5 и одну в пределах положений 18-23 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 1-5 (считая от 5'-конца) смысловой нити, а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 (считая от 5'-конца) смысловой нити, а также одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и одну в пределах положений 18-23 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в пределах положений 1-5 и одну фосфотиоатную модификацию межнуклеотидной связи в пределах положений 18-23 смысловой нити (считая от 5'-конца), а также одну фосфотиоатную модификацию межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в пределах положений 18-23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 20 и 21 смысловой нити (считая от 5'-конца), а также одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну в положении 21 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну фосфотиоатную модификацию межнуклеотидной связи в положении 21 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 20 и 21 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 21 и 22 смысловой нити (считая от 5'-конца), а также одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну фосфотиоатную модификацию межнуклеотидной связи в положении 21 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну фосфотиоатную модификацию межнуклеотидной связи в положении 21 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 21 и 22 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 22 и 23 смысловой нити (считая от 5'-конца), а также одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну фосфотиоатную модификацию межнуклеотидной связи в положении 21 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению дополнительно содержит одну фосфотиоатную модификацию межнуклеотидной связи в положении 1 и одну фосфотиоатную модификацию межнуклеотидной связи в положении 21 смысловой нити (считая от 5'-конца), а также две фосфотиоатные модификации межнуклеотидной связи в положениях 1 и 2 и две фосфотиоатные модификации межнуклеотидной связи в положениях 23 и 23 антисмысловой нити (считая от 5'-конца).
В некоторых вариантах осуществления антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) смысловая нить конъюгирована с лигандом; (iii) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (iv) смысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (v) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vi) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести, семи или всем восьми) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) антисмысловая нить содержит 1, 2, 3 или 4 фосфотиоатные межнуклеотидные связи; (iii) смысловая нить конъюгирована с лигандом; (iv) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (v) смысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (vi) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vii) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (viii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления смысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2 и между положениями нуклеотидов 2 и 3, антисмысловая нить содержит фосфотиоатные межнуклеотидные связи между положениями нуклеотидов 1 и 2, между положениями нуклеотидов 2 и 3, между положениями нуклеотидов 21 и 22 и между положениями нуклеотидов 22 и 23, при этом антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса, находящуюся в затравочной области антисмысловой нити (т.е. в положении 2-9 5'-конца антисмысловой нити), и при этом dsRNA необязательно дополнительно соответствует по меньшей мере одной (например, одной, двум, трем, четырем, пяти, шести или всем семи) из следующих характеристик: (i) антисмысловая нить содержит 2, 3, 4, 5 или 6 2'-фтор-модификаций; (ii) смысловая нить конъюгирована с лигандом; (iii) смысловая нить содержит 2, 3, 4 или 5 2'-фтор-модификаций; (iv) смысловая нить содержит 3 или 4 фосфотиоатные межнуклеотидные связи; (v) dsRNA содержит по меньшей мере четыре 2'-фтор-модификации; (vi) dsRNA содержит дуплексный участок с длиной, составляющей 12-40 пар нуклеотидов; и (vii) dsRNA предусматривает тупой конец на 5'-конце антисмысловой нити.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению содержит ошибку(и) спаривания с мишенью в пределах дуплекса или их комбинации. Ошибка спаривания может встречаться в участке «липкого» конца или в дуплексном участке. Пары оснований можно ранжировать на основании их способности содействовать диссоциации или плавлению (например, по свободной энергии ассоциации или диссоциации определенного спаривания, при этом наиболее простым подходом является изучение пар на основе индивидуальных пар, однако также можно использовать анализ ближайшего соседа или подобный). С точки зрения содействия диссоциации: A:U более предпочтительна, чем G:C; G:U более предпочтительна, чем G:C; а I:C более предпочтительна, чем G:C (I=инозин). Ошибки спаривания, например, неканонические или отличные от канонических типы спаривания (описанные в других частях в данном документе), предпочтительнее канонических типов спаривания (A:T, A:U, G:C); а типы спаривания, которые включают универсальное основание, предпочтительнее канонических типов спаривания.
В некоторых вариантах осуществления для средства на основе dsRNA по настоящему изобретению предусмотрено, что по меньшей мере одна из первых 1, 2, 3, 4 или 5 пар оснований от 5'-конца в пределах дуплексных участков антисмысловой нити может быть независимо выбрана из группы, состоящей из: A:U, G:U, I:C и пар с ошибками спаривания, например, неканонических, или отличных от канонических типов спаривания, или типов спаривания, которые включают универсальное основание, чтобы содействовать диссоциации антисмысловой нити на 5'-конце дуплекса.
В некоторых вариантах осуществления нуклеотид в положении 1 от 5'-конца в пределах дуплексного участка антисмысловой нити выбран из группы, состоящей из A, dA, dU, U и dT. В качестве альтернативы по меньшей мере одна из первых 1, 2 или 3 пар оснований от 5'-конца в пределах дуплексного участка антисмысловой нити представляет собой пару оснований AU. Например, первая пара оснований от 5'-конца в пределах дуплексного участка антисмысловой нити представляет собой пару оснований AU.
Также было установлено, что введение 4'-модифицированного и/или 5'-модифицированного нуклеотида в 3'-конец фосфодиэфирной (PO), фосфотиоатной (PS) и/или фосфодитиоатной (PS2) связи динуклеотида в любом положении однонитевого или двухнитевого олигонуклеотида может оказывать стерический эффект на межнуклеотидную связь и, следовательно, защищать ее от действия нуклеаз и придавать устойчивость к ним.
В некоторых вариантах осуществления 5'-модифицированный нуклеозид вводят в 3'-конец динуклеотида в любом положении однонитевой или двухнитевой siRNA. Например, 5'-алкилированный нуклеозид может быть введен в 3'-конец динуклеотида в любом положении однонитевой или двухнитевой siRNA. Алкильная группа в положении 5' рибозного сахара может быть рацемическим или хирально чистым R- или S-изомером. Иллюстративный 5'-алкилированный нуклеозид представляет собой 5'-метилнуклеозид. 5'-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером.
В некоторых вариантах осуществления 4'-модифицированный нуклеозид вводят в 3'-конец динуклеотида в любом положении однонитевой или двухнитевой siRNA. Например, 4'-алкилированный нуклеозид может быть введен в 3'-конец динуклеотида в любом положении однонитевой или двухнитевой siRNA. Алкильная группа в положении 4' рибозного сахара может быть рацемическим или хирально чистым R- или S-изомером. Иллюстративный 4'-алкилированный нуклеозид представляет собой 4'-метилнуклеозид. 4'-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером. В качестве альтернативы 4'-O-алкилированный нуклеозид может быть введен в 3'-конец динуклеотида в любом положении однонитевой или двухнитевой siRNA. 4'-O-алкил рибозного сахара может быть рацемическим или хирально чистым R- или S-изомером. Иллюстративный 4'-O-алкилированный нуклеозид представляет собой 4'-O-метилнуклеозид. 4'-O-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером.
В некоторых вариантах осуществления 5'-алкилированный нуклеозид вводят в любое положение на смысловой нити или антисмысловой нити dsRNA, и такая модификация сохраняет или увеличивает эффективность dsRNA. 5'-Алкил может быть либо рацемическим, либо хирально чистым R- или S-изомером. Иллюстративный 5'-алкилированный нуклеозид представляет собой 5'-метилнуклеозид. 5'-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером.
В некоторых вариантах осуществления 4'-алкилированный нуклеозид вводят в любое положение на смысловой нити или антисмысловой нити dsRNA, и такая модификация сохраняет или увеличивает эффективность dsRNA. 4'-Алкил может быть либо рацемическим, либо хирально чистым R- или S-изомером. Иллюстративный 4'-алкилированный нуклеозид представляет собой 4'-метилнуклеозид. 4'-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером.
В некоторых вариантах осуществления 4'-O-алкилированный нуклеозид вводят в любое положение на смысловой нити или антисмысловой нити dsRNA, и такая модификация сохраняет или увеличивает эффективность dsRNA. 5'-Алкил может быть либо рацемическим, либо хирально чистым R- или S-изомером. Иллюстративный 4'-O-алкилированный нуклеозид представляет собой 4'-O-метилнуклеозид. 4'-O-метил может быть либо рацемическим, либо хирально чистым R- или S-изомером.
В некоторых вариантах осуществления средство на основе dsRNA по настоящему изобретению может содержать 2'-5'-связи (с 2'-H, 2'-OH и 2'-OMe, а также с P=O или P=S). Например, модификации 2'-5'-связей можно использовать для содействия устойчивости к нуклеазам или для ингибирования связывания смысловой и антисмысловой нитей, или их можно использовать на 5'-конце смысловой нити для предупреждения активации смысловой нити под действием RISC.
В другом варианте осуществления средство на основе dsRNA по настоящему изобретению может содержать L-сахара (например, L-рибозу, L-арабинозу с 2'-H, 2'-OH и 2'-OMe). Например, модификации L-сахаров можно использовать для содействия устойчивости к нуклеазам или для ингибирования связывания смысловой и антисмысловой нитей, или их можно использовать на 5'-конце смысловой нити для предупреждения активации смысловой нити под действием RISC.
В различных публикациях описаны мультимерные siRNA, причем всех их можно применять в случае dsRNA по настоящему изобретению. Такие публикации включают WO2007/091269, патент США № 7858769, WO2010/141511, WO2007/117686, WO2009/014887 и WO2011/031520, которые тем самым включены посредством ссылки во всей своей полноте.
Как рассмотрено более подробно ниже, в случае средства на основе dsRNA, содержащего один или нескольких углеводных фрагментов, конъюгированных со средством на основе dsRNA, может улучшаться одно или несколько свойств средства на основе dsRNA. Во многих случаях углеводный фрагмент будет присоединен к модифицированной субъединице средства на основе dsRNA. Например, рибозный сахар одной или нескольких рибонуклеотидных субъединиц средства на основе dsRNA можно заменять на другой фрагмент, например, отличный от углевода (предпочтительно циклический) носитель, к которому присоединен углеводный лиганд. Рибонуклеотидную субъединицу, в которой рибозный сахар субъединицы был заменен таким образом, обозначают в данном документе как субъединицу с модификацией путем замены рибозы (RRMS). Циклический носитель может представлять собой карбоциклическую кольцевую системой, т.е. все атомы в кольце являются атомами углерода, или гетероциклическую кольцевую систему, т.е. один или несколько атомов в кольце могут быть гетероатомом, например, азотом, кислородом, серой. Циклический носитель может представлять собой моноциклическую кольцевую систему или может содержать два или более колец, например, конденсированных колец. Циклический носитель может представлять собой полностью насыщенную кольцевую систему или может содержать одну или несколько двойных связей.
Лиганд может быть присоединен к полинуклеотиду посредством носителя. Носители включают (i) по меньшей мере одну "точку присоединения к остову", предпочтительно две "точки присоединения к остову" и (ii) по меньшей мере одну "связывающую точку присоединения". "Точка присоединения к остову", используемая в данном документе, обозначает функциональную группу, например, гидроксильную группу, или, как правило, связь, доступную и подходящую для встраивания носителя в остов, например, фосфатный или модифицированный фосфатный, например, серосодержащий, остов рибонуклеиновой кислоты. "Связывающая точка присоединения" (TAP) в некоторых вариантах осуществления обозначает входящий в состав кольца атом циклического носителя, например, атом углерода или гетероатом (отличный от атома, который обеспечивает точку присоединения к остову), с которым связывается выбранный фрагмент. Фрагмент может быть, например, углеводом, например, моносахаридом, дисахаридом, трисахаридом, тетрасахаридом, олигосахаридом и полисахаридом. Необязательно выбранный фрагмент присоединен к циклическому носителю посредством промежуточного связывающего фрагмента. Таким образом, циклический носитель зачастую будет включать функциональную группу, например, аминогруппу, или, как правило, обеспечивать связь, подходящую для введения другого химического структурного элемента, например, лиганда, в состав кольца или связывания его с кольцом.
В одном варианте осуществления средство на основе dsRNA по настоящему изобретению конъюгируют с лигандом через носитель, где носитель может представлять собой циклическую группу или ациклическую группу; предпочтительно циклическая группа выбрана из пирролидинила, пиразолинила, пиразолидинила, имидазолинила, имидазолидинила, пиперидинила, пиперазинила, [1,3]-диоксолана, оксазолидинила, изоксазолидинила, морфолинила, тиазолидинила, изотиазолидинила, хиноксалинила, пиридазинонила, тетрагидрофурила и декалина; предпочтительно ациклическая группа выбрана из остова, представляющего собой серинол, или остова, представляющего собой диэтаноламин.
Средство, представляющие собой двухнитевую РНК (dsRNA), по настоящему изобретению необязательно может быть конъюгировано с одним или несколькими лигандами. Лиганд может быть присоединен к смысловой нити, антисмысловой нити или к обеим нитям на 3'-конце, 5'-конце или на обоих концах. Например, лиганд может быть конъюгирован со смысловой нитью, в частности с 3'-концом смысловой нити.
В некоторых вариантах осуществления средства на основе dsRNA по настоящему изобретению являются 5'-фосфорилированными или включают фосфорильный аналог на 5'-конце. 5'-Фосфатные модификации включают модификации, которые совместимы с RISC-опосредованным сайленсингом генов. Подходящие модификации включают: 5'-монофосфат ((HO)2(O)P-O-5'); 5'-дифосфат ((HO)2(O)P-O-P(HO)(O)-O-5'); 5'-трифосфат ((HO)2(O)P-O-(HO)(O)P-O-P(HO)(O)-O-5'); 5'-гуанозиновый кэп (7-метилированный или неметилированный) (7m-G-O-5'-(HO)(O)P-O-(HO)(O)P-O-P(HO)(O)-O-5'); 5'-аденозиновый кэп (Appp) и любую модифицированную или немодифицированную кэп-структуру нуклеотида (N-O-5'-(HO)(O)P-O-(HO)(O)P-O-P(HO)(O)-O-5'); 5'-монотиофосфат (фосфотиоат; (HO)2(S)P-O-5'); 5'-монодитиофосфат (фосфородитиоат; (HO)(HS)(S)P-O-5'), 5'-фосфоротиолат ((HO)2(O)P-S-5'); любую дополнительную комбинацию кислород/сера-замещенных монофосфата, дифосфата и трифосфатов (например, 5'-альфа-тиотрифосфат, 5'-гамма-тиотрифосфат и т.д.), 5'-фосфорамидаты ((HO)2(O)P-NH-5', (HO)(NH2)(O)P-O-5'), 5'-алкилфосфонаты (R=алкил=метил, этил, изопропил, пропил и т. д, например, RP(OH)(O)-O-5'-, 5'-алкенилфосфонаты (т.е. винил, замещенный винил), (OH)2(O)P-5'-CH2-), 5'-алкилэфирфосфонаты (R=алкиловый эфир=метоксиметил (MeOCH2-), этоксиметил и т.д., например RP(OH)(O)-O-5'-). В одном примере модификацию можно поместить в антисмысловую нить средства на основе dsRNA.
III. iRNA, конъюгированные с лигандами
Другая модификация РНК из числа iRNA по настоящему изобретению предусматривает химическое связывание iRNA с одним или несколькими лигандами, фрагментами или конъюгатами, которые повышают активность, распределение в клетках или поглощение iRNA клетками, например в клетке. Такие фрагменты включают без ограничения липидные фрагменты, такие как холестериновый фрагмент (Letsinger et al., Proc. Natl. Acid. Sci. USA, 1989, 86: 6553-6556). В других вариантах осуществления лиганд представляет собой холевую кислоту (Manoharan et al., Biorg. Med. Chem. Let., 1994, 4:1053-1060), простой тиоэфир, например, берил-S-тритилтиол (Manoharan et al., Ann. N.Y. Acad. Sci., 1992, 660:306-309; Manoharan et al., Biorg. Med. Chem. Let., 1993, 3:2765-2770), тиохолестерин (Oberhauser et al., Nucl. Acids Res., 1992, 20:533-538), алифатическую цепь, например, додекандиоловые или ундециловые остатки (Saison-Behmoaras et al., EMBO J, 1991, 10:1111-1118; Kabanov et al., FEBS Lett., 1990, 259:327-330; Svinarchuk et al., Biochimie, 1993, 75:49-54), фосфолипид, например, ди-гексадецил-рац-глицерин или 1,2-ди-O-гексадецил-рац-глицеро-3-фосфонат триэтиламмония (Manoharan et al., Tetrahedron Lett., 1995, 36:3651-3654; Shea et al., Nucl. Acids Res., 1990, 18:3777-3783), полиамин или полиэтиленгликолевую цепь (Manoharan et al., Nucleosides & Nucleotides, 1995, 14:969-973), или адамантануксусную кислоту (Manoharan et al., Tetrahedron Lett., 1995, 36:3651-3654), пальмитиловый фрагмент (Mishra et al., Biochim. Biophys. Acta, 1995, 1264:229-237) или октадециламинный или гексиламинокарбонилоксихолестериновый фрагмент (Crooke et al., J. Pharmacol. Exp. Ther., 1996, 277:923-937).
В определенных вариантах осуществления лиганд изменяет распределение, нацеливание или время существования средства на основе iRNA, в которое он встроен. В предпочтительных вариантах осуществления лиганд обеспечивает повышенную аффинность в отношении выбранной мишени, например, молекулы, клетки или типа клеток, компартмента, например, клеточного компартмента или части органа, ткани, органа или участка тела, как, например, по сравнению с молекулами, у которых отсутствует такой лиганд. Предпочтительные лиганды не принимают участие в спаривании дуплекса в дуплексной нуклеиновой кислоте.
Лиганды могут включать вещество, встречающееся в природе, такое как белок (например, сывороточный альбумин человека (HSA), липопротеин низкой плотности (LDL) или глобулин); углевод (например, декстран, пуллулан, хитин, хитозан, инулин, циклодекстрин, N-ацетилглюкозамин, N-ацетилгалактозамин или гиалуроновую кислоту) или липид. Лиганд также может представлять собой рекомбинантную или синтетическую молекулу, такую как синтетический полимер, например, синтетическая полиаминокислота. Примеры полиаминокислот включают полиаминокислоту, представляющую собой полилизин (PLL), поли-L-аспарагиновую кислоту, поли-L-глутаминовую кислоту, сополимер стирола и ангидрида малеиновой кислоты, сополимер L-лактида и гликолида, сополимер простого дивинилового эфира и малеинового ангидрида, N-(2-гидроксипропил)метакриламидный сополимер (HMPA), полиэтиленгликоль (PEG), поливиниловый спирт (PVA), полиуретан, поли(2-этилакриловую кислоту), N-изопропилакриламидные полимеры или полифосфазин. Примеры полиаминов включают полиэтиленимин, полилизин (PLL), спермин, спермидин, полиамин, полиамин-псевдопептид, полиамин-пептидомиметик, полиамин-дендример, аргинин, амидин, протамин, катионный липид, катионный порфирин, четвертичную соль полиамина или альфа-спиральный пептид.
Лиганды также могут включать нацеливающие группы, например, средство, нацеливающее на клетку или ткань, например, лектин, гликопротеин, липид или белок, например, антитело, которое связывается с определенным типом клеток, таким как клетка почки. Нацеливающая группа может представлять собой тиреотропин, меланотропин, лектин, гликопротеин, поверхностно-активный белок A, углевод муцин, поливалентную лактозу, поливалентную галактозу, N-ацетилгалактозамин, N-ацетилглюкозамин, поливалентную маннозу, поливалентную фукозу, гликозилированные полиаминокислоты, поливалентную галактозу, трансферрин, бисфосфонат, полиглутамат, полиаспартат, липид, холестерин, стероид, желчную кислоту, фолат, витамин B12, витамин А, биотин или RGD-пептид или миметик RGD-пептида.
В одном варианте осуществления лиганд представляет собой лиганд асиалогликопротеинового рецептора. Используемые в данном документе "лиганд асиалогликопротеинового рецептора" или "лиганд ASGPR" представляют собой лиганд, такой как углеводный лиганд (рассмотренный ниже), который нацеливает средство на основе dsRNA по настоящему изобретению на гепатоциты. В определенных вариантах осуществления лиганд представляет собой одну или несколько галактоз, например, N-ацетил-галактозамин (GalNAc) или одно или несколько производных GalNAc.
Другие примеры лигандов включают красители, интеркалирующие средства (например, акридины), сшивающие средства (например, псорален, митомицин C), порфирины (TPPC4, тексафирин, сапфирин), полициклические ароматические углеводороды (например, феназин, дигидрофеназин), искусственные эндонуклеазы (например, EDTA), липофильные молекулы, например, холестерин, холевую кислоту, адамантануксусную кислоту, 1-пиренмасляную кислоту, дигидротестостерон, 1,3-бис-O(гексадецил)глицерин, геранилоксигексильную группу, гексадецил-глицерин, борнеол, ментол, 1,3-пропандиол, гептадецильную группу, пальмитиновую кислоту, миристиновую кислоту, O3-(олеоил)литохолевую кислоту, O3-(олеоил)холеновую кислоту, диметокситритил или феноксазин и пептидные конъюгаты (например, пептид antennapedia, Tat-пептид), алкилирующие средства, фосфат, амино, меркапто, PEG (например, PEG-40K), MPEG, [MPEG]2, полиамино, алкил, замещенный алкил, меченные радиоизотопом маркеры, ферменты, гаптены (например, биотин), усилители транспорта/всасывания (например, аспирин, витамин E, фолиевую кислоту), синтетические рибонуклеазы (например, имидазол, бисимидазол, гистамин, имидазольные кластеры, конъюгаты акридин-имидазол, комплексы Eu3+ тетраазамакроциклов), динитрофенил, HRP или AP.
Лигандами могут быть белки, например, гликопротеины, или пептиды, например, молекулы со специфической аффинностью в отношении колиганда, или антитела, например, антитело, которое связывается с определенным типом клеток, таким как клетка печени. Лиганды также могут включать гормоны и рецепторы гормонов. Они также могут включать молекулы, отличные от пептидов, такие как липиды, лектины, углеводы, витамины, кофакторы, поливалентная лактоза, поливалентная галактоза, N-ацетилгалактозамин, N-ацетилглюкозамин, поливалентная манноза или поливалентная фукоза. Например, лигандом может быть липополисахарид, активатор MAP-киназы p38 или активатор NF-κB.
Лигандом может быть вещество, например лекарственное средство, которое может увеличивать проникновение средства на основе iRNA в клетку, например путем разрушения цитоскелета клетки, например путем разрушения микротрубочек, микрофиламентов или промежуточных филаментов клетки. Лекарственным средством может быть, например, таксон, винкристин, винбластин, цитохалазин, нокодазол, яплакинолид, латрункулин A, фаллоидин, свинхолид A, инданоцин или миосервин.
В некоторых вариантах осуществления лиганд, присоединенный к iRNA, как описано в данном документе, действует как фармакокинетический модулятор (PK-модулятор). PK-модуляторы включают липофилы, желчные кислоты, стероиды, аналоги фосфолипидов, пептиды, белок-связывающие средства, PEG, витамины и т.д. Иллюстративные PK-модуляторы включают без ограничения холестерин, жирные кислоты, холевую кислоту, литохолевую кислоту, диалкилглицериды, диацилглицерид, фосфолипиды, сфинголипиды, напроксен, ибупрофен, витамин E, биотин. Как также известно, олигонуклеотиды, которые содержат некоторое количество фосфотиоатных связей, связываются с сывороточным белком, следовательно, короткие олигонуклеотиды, например, олигонуклеотиды из приблизительно 5 оснований, 10 оснований, 15 оснований или 20 оснований, содержащие множественные фосфотиоатные связи в остове, также пригодны в настоящем изобретении в качестве лигандов (например, в качестве PK-модулирующих лигандов). В дополнение, аптамеры, которые связываются с компонентами сыворотки крови (например, сывороточными белками), также пригодны для применения в качестве PK-модулирующих лигандов в вариантах осуществления, описанных в данном документе.
Конъюгированные с лигандами iRNA по настоящему изобретению можно синтезировать с применением олигонуклеотида, который несет боковую реакционноспособную функциональную группу, такого как полученный в результате присоединения связывающей молекулы к олигонуклеотиду (описано ниже). Этот реакционноспособный олигонуклеотид может напрямую вступать в реакцию с коммерчески доступными лигандами, лигандами, которые синтезированы как несущие любую из разнообразных защитных групп, или лигандами, которые имеют связывающий фрагмент, присоединенный к ним.
Олигонуклеотиды, применяемые в конъюгатах по настоящему изобретению, можно получать с помощью удобной и стандартной методики хорошо известного твердофазного синтеза. Оборудование для такого синтеза реализуется несколькими фирмами-производителями, включая, например, Applied Biosystems® (Фостер Сити, Калифорния). В качестве дополнения или альтернативы можно применять любые другие способы такого синтеза, известные из уровня техники. Также известно применение аналогичных методик для получения других олигонуклеотидов, таких как фосфотиоаты и алкилированные производные.
В конъюгированные с лигандом iRNA и специфические в отношении последовательности связанные нуклеозиды, несущие молекулу-лиганд, по настоящему изобретению, олигонуклеотиды и олигонуклеозиды могут быть собраны на подходящем синтезаторе ДНК с применением стандартных предшественников нуклеотидов или нуклеозидов, или предшественников конъюгатов нуклеотидов или нуклеозидов, которые уже несут связывающий фрагмент, предшественников конъюгатов лиганд-нуклеотид или -нуклеозид, которые уже несут молекулу-лиганд, или отличных от нуклеозида структурных блоков, несущих лиганд.
При применении предшественников конъюгатов нуклеотидов, которые уже несут связывающий фрагмент, синтез специфичных в отношении последовательности связанных нуклеозидов, как правило, завершают, а затем осуществляют реакцию молекулы лиганда со связывающим фрагментом с образованием олигонуклеотида, конъюгированного с лигандом. В некоторых вариантах осуществления олигонуклеотиды или связанные нуклеозиды по настоящему изобретению синтезируют с помощью автоматического синтезатора с применением фосфорамидитов, полученных из конъюгатов лиганд-нуклеозид, в дополнение к стандартным фосфорамидитам и нестандартным фосфорамидитам, которые коммерчески доступны и обычно применяются в олигонуклеотидном синтезе.
A. Липидные конъюгаты
В определенных вариантах осуществления лиганд или конъюгат представляет собой липидную молекулу или молекулу на основе липида. Такая липидная молекула или молекула на основе липида предпочтительно связывается с сывороточным белком, например, сывороточным альбумином человека (HSA). Связывающийся с HSA лиганд делает возможным распределение конъюгата в целевой ткани, например, в отличной от ткани почек целевой ткани организма. Например, целевой тканью может быть печень, в том числе паренхиматозные клетки печени. Также в качестве лигандов можно применять другие молекулы, которые могут связываться с HSA. Например, можно применять напроксен или аспирин. Липидный лиганд или лиганд на основе липида может (a) повышать устойчивость конъюгата к разрушению, (b) улучшать нацеливание или транспорт в целевую клетку или клеточную мембрану или (c) может применяться для корректировки связывания с сывороточным белком например HSA.
Лиганд на основе липида можно применять для ингибирования, например, для контроля связывания конъюгата с целевой тканью. Например, липидный лиганд или лиганд на основе липида, который более сильно связывается с HSA, с меньшей вероятностью будет нацеливаться на почки и, следовательно, с меньшей вероятностью будет выводиться из организма. Липидный лиганд или лиганд на основе липида, который менее прочно связывается с HSA, можно применять для нацеливания конъюгата на почки.
В определенных вариантах осуществления лиганд на основе липида связывается с HSA. Предпочтительно он связывает HSA с аффинностью, достаточной для того чтобы конъюгат предпочтительно распределялся в ткань, отличную от ткани почек. Однако предпочтительно, чтобы аффинность не была настолько сильной, чтобы связывание HSA-лиганд было необратимым.
В других вариантах осуществления лиганд на основе липида слабо связывается с HSA или вообще не связывается с ним, так что конъюгат предпочтительно будет распределяться в почки. Другие фрагменты, которые нацеливаются на клетки почки, также можно использовать в дополнение к лиганду на основе липида или вместо него.
В другом аспекте лигандом является фрагмент, например, витамин, который поглощается целевой клеткой, например, пролиферирующей клеткой. Такие лиганды особенно применимы для лечения нарушений, характеризующихся нежелательной пролиферацией клеток, например, злокачественного или доброкачественного типа, например, раковых клеток. Иллюстративные витамины включают витамины A, E и K. Другие иллюстративные витамины включают витамины группы B, например, фолиевую кислоту, B12, рибофлавин, биотин, пиридоксаль, или другие витамины, или нутриенты, поглощаемые целевыми клетками, например, клетками печени. Также включены HAS и липопротеин низкой плотности (LDL).
B. Средства, обеспечивающие проникновение в клетку
В другом аспекте лигандом является средство, обеспечивающее проникновение в клетку, предпочтительно спиральное средство, обеспечивающее проникновение в клетку. Предпочтительно средство является амфипатическим. Иллюстративным средством является пептид, такой как tat или antennopedia. Если средство представляет собой пептид, то он может быть модифицированным, в том числе содержать пептидилмиметик, инвертомеры, отличные от пептидных или псевдопептидные связи, а также в нем могут использоваться D-аминокислоты. Спиральное средство предпочтительно представляет собой альфа-спиральное средство, которое предпочтительно имеет липофильную и липофобную фазы.
Лигандом может быть пептид или пептидомиметик. Пептидомиметик (также обозначаемый в данном документе как олигопептидомиметик) представляет собой молекулу, способную к укладке в определенную трехмерную структуру, аналогичную природному пептиду. Присоединение пептида и пептидомиметиков к средствам на основе iRNA может воздействовать на фармакокинетическое распределение iRNA, например, путем повышения степени распознавания и абсорбции клеткой. Длина пептидного фрагмента или фрагмента-пептидомиметика может составлять приблизительно 5-50 аминокислот, например, приблизительно 5, 10, 15, 20, 25, 30, 35, 40, 45 или 50 аминокислот.
Пептидом или пептидомиметиком, например, может быть пептид, обеспечивающий проникновение в клетку, катионный пептид, амфипатический пептид или гидрофобный пептид (например, состоящий преимущественно из Tyr, Trp или Phe). Пептидный фрагмент может представлять собой пептид-дендример, конформационно затрудненный пептид или перекрестно сшитый пептид. В другом альтернативном варианте пептидный фрагмент может включать гидрофобную последовательность, обеспечивающую перенос через мембрану (MTS). Иллюстративный содержащий гидрофобную MTS пептид представляет собой RFGF с аминокислотной последовательностью AAVALLPAVLLALLAP (SEQ ID NO:29). RFGF-аналог (например, аминокислотная последовательность AALLPVLLAAP (SEQ ID NO:30)), содержащий гидрофобную MTS, также может быть нацеливающим фрагментом. Пептидный фрагмент может представлять собой "доставляющий" пептид, который может переносить большие полярные молекулы, в том числе пептиды, олигонуклеотиды и белки, через клеточные мембраны. Например, последовательности белка Tat HIV (GRKKRRQRRRPPQ; SEQ ID NO:31) и белка Antennapedia Drosophila (RQIKIWFQNRRMKWKK; SEQ ID NO:32), как было обнаружено, способны функционировать как доставляющие пептиды. Пептид или пептидомиметик могут быть закодированы в случайной последовательности ДНК, как, например, пептид, идентифицированный из библиотеки фагового дисплея или комбинаторной библиотеки "одна гранула-одно соединение" (OBOC) (Lam et al., Nature, 354:82-84, 1991). Примерами пептида или пептидомиметика, связанного со средством на основе dsRNA посредством введенной мономерной структурной единицы в рамках нацеливания на клетку, является пептид, состоящий из аргинина-глицина-аспарагиновой кислоты (RGD), или RGD-миметик. Длина пептидного фрагмента может варьироваться от приблизительно 5 аминокислот до приблизительно 40 аминокислот. Пептидные фрагменты могут иметь структурную модификацию, как, например, для повышения стабильности или управления конформационными свойствами. Можно использовать любую из структурных модификаций, описанных ниже.
RGD-пептид для применения в композициях и способах по настоящему изобретению может быть линейным или циклическим, и может быть модифицированным, например, гликозилированным или метилированным, для облегчения нацеливания на конкретную ткань(и). Пептиды и пептидомиметики, содержащие RGD, могут включать D-аминокислоты, а также синтетические RGD-миметики. В дополнение к RGD можно применять другие фрагменты, которые нацеливают лиганд интегрин. Предпочтительные конъюгаты с таким лигандом нацеливаются на PECAM-1 или VEGF.
“Пептид, обеспечивающий проникновение в клетку” способен проникать в клетку, например, микробную клетку, такую как клетка бактерии или гриба, или в клетку млекопитающего, такую как клетка человека. Пептидом, проникающим в микробную клетку, например, может быть α-спиральный линейный пептид (например, LL-37 или Ceropin P1), содержащий дисульфидную связь пептид (например, α-дефенсин, β-дефенсин или бактенецин) или пептид, содержащий только одну или две преобладающие аминокислоты (например, PR-39 или индолицидин). Пептид, обеспечивающий проникновение в клетку, также может включать сигнал ядерной локализации (NLS). Например, пептид, обеспечивающий проникновение в клетку, может представлять собой двухкомпонентный амфипатический пептид, такой как MPG, который получен из домена слитого пептида gp41 HIV-1 и NLS из большого T-антигена SV40 (Simeoni et al., Nucl. Acids Res. 31:2717-2724, 2003).
C. Углеводные конъюгаты
В некоторых вариантах осуществления композиций и способов по настоящему изобретению iRNA дополнительно содержит углевод. iRNA, конъюгированная с углеводом, предпочтительна для in vivo доставки нуклеиновых кислот, а также композиций, подходящих для in vivo терапевтического применения, как описано в данном документе. Используемый в данном документе "углевод" обозначает соединение, которое либо представляет собой углевод per se, образованный из одной или нескольких моносахаридных структурных единиц, имеющих по меньшей мере 6 атомов углерода (которые могут образовывать линейную, разветвленную или циклическую структуру) с атомом кислорода, азота или серы, связанным с каждым атомом углерода; либо соединение, частью которого является углеводный фрагмент, образованный из одной или нескольких моносахаридных структурных единиц, каждая из которых имеет по меньшей мере шесть атомов углерода (которые могут образовывать линейную, разветвленную или циклическую структуру) с атомом кислорода, азота или серы, связанным с каждым атомом углерода. Типичные углеводы включают сахара (моно-, ди-, три- и олигосахариды, содержащие приблизительно 4, 5, 6, 7, 8 или 9 моносахаридных структурных единиц) и полисахариды, такие как крахмалы, гликоген, целлюлоза и полисахаридные камеди. Конкретные моносахариды включают сахара C5 и выше (например, C5, C6, C7 или C8); ди- и трисахариды включают сахара с двумя или тремя моносахаридными структурными единицами (например, C5, C6, C7 или C8).
В определенных вариантах осуществления углеводный конъюгат для применения в композициях и способах по настоящему изобретению представляет собой моносахарид.
В одном варианте осуществления углеводный конъюгат для применения в композициях и способах по настоящему изобретению выбран из группы, состоящей из:
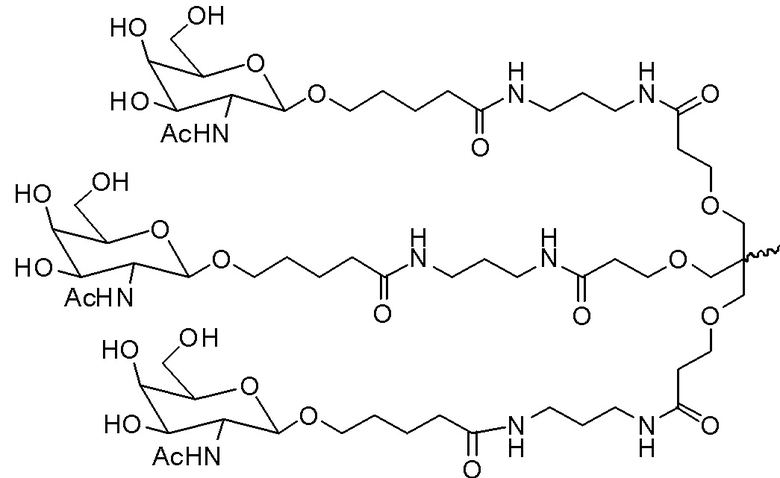 формула II,
формула II,
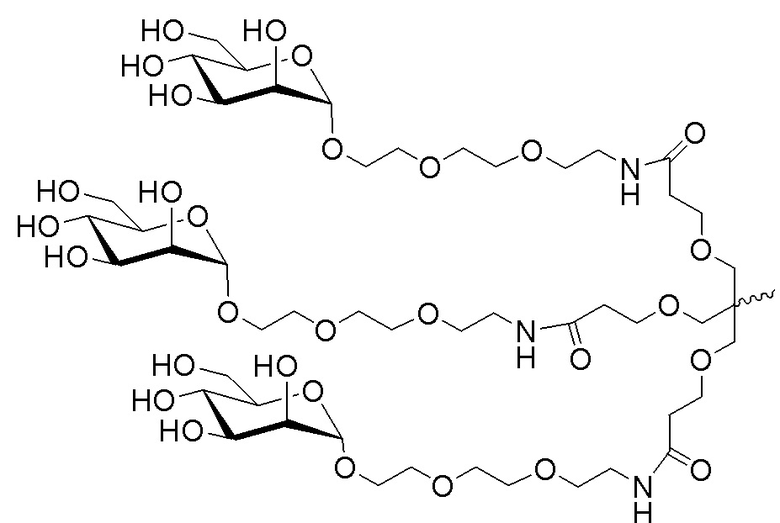 формула III,
формула III,
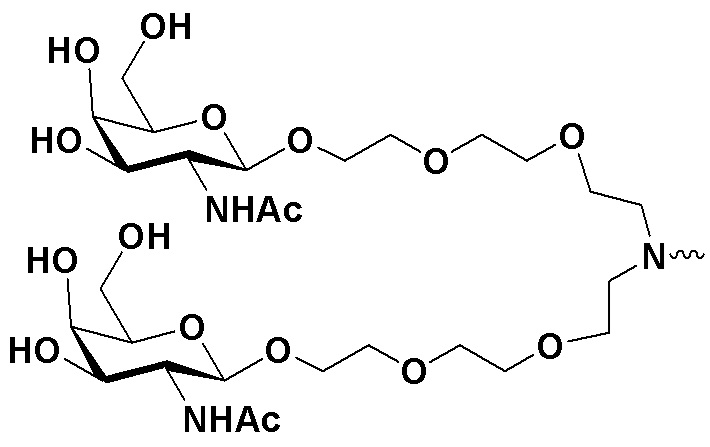 формула IV,
формула IV,
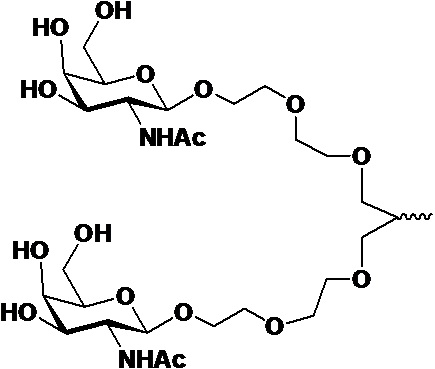 формула V,
формула V,
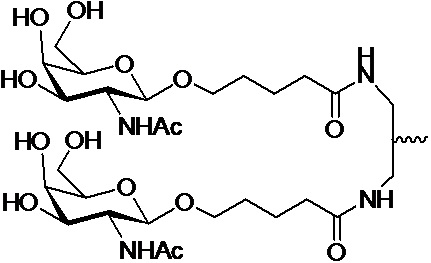 формула VI,
формула VI,
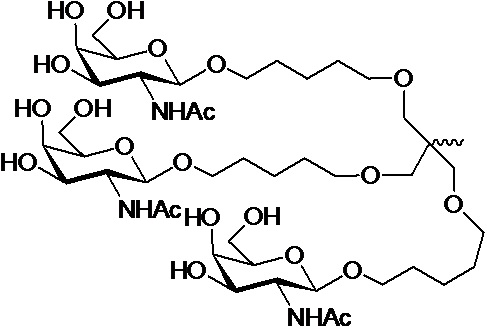 формула VII,
формула VII,
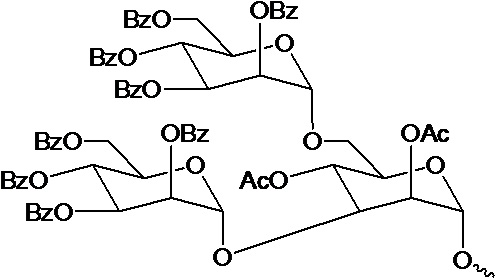 формула VIII,
формула VIII,
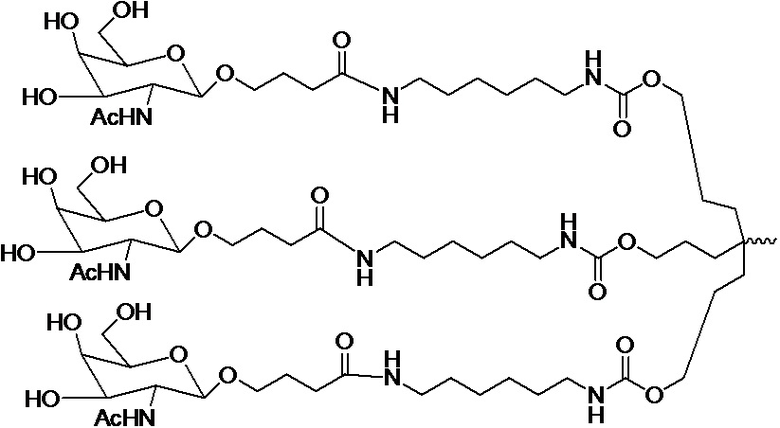 формула IX,
формула IX,
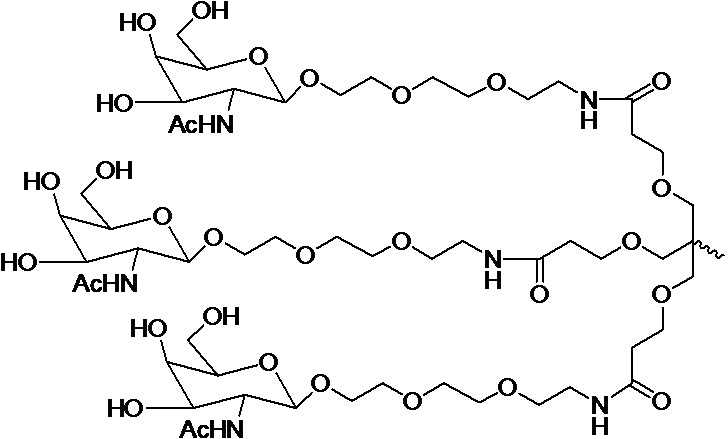 формула X,
формула X,
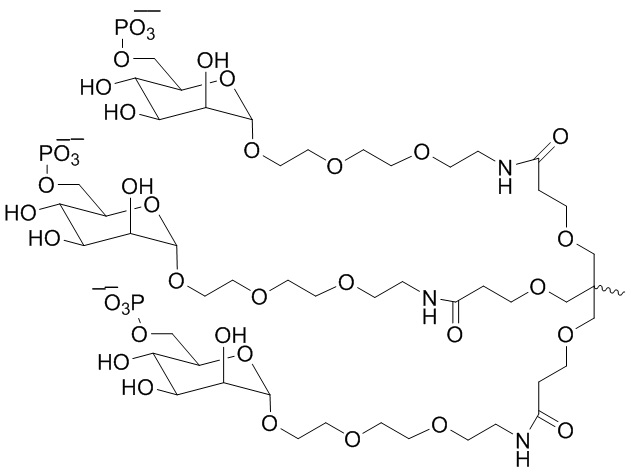 формула XI,
формула XI,
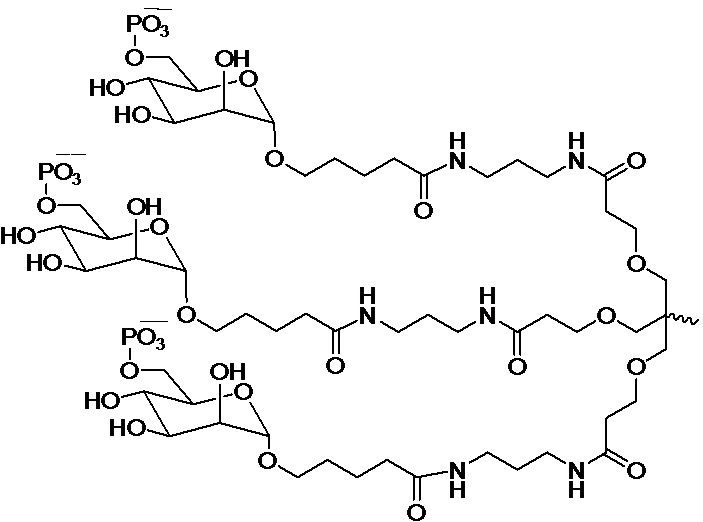 формула XII,
формула XII,
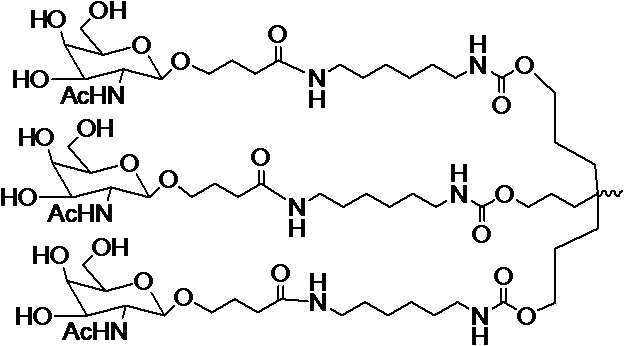 формула XIII,
формула XIII,
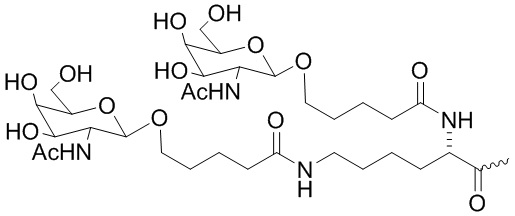 формула XIV,
формула XIV,
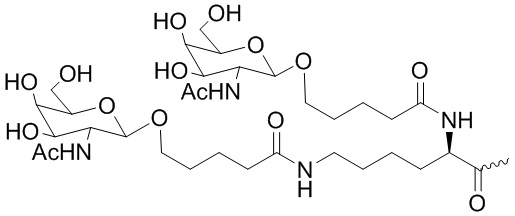 формула XV,
формула XV,
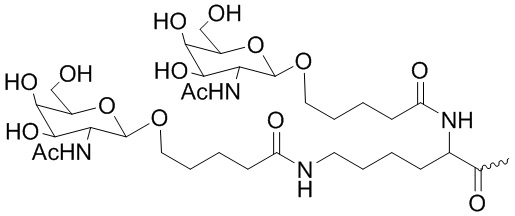 формула XVI,
формула XVI,
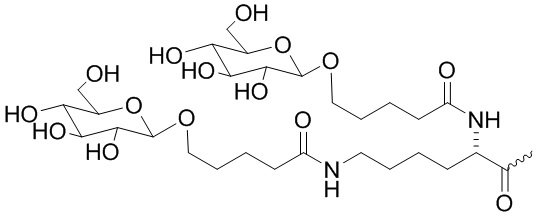 формула XVII,
формула XVII,
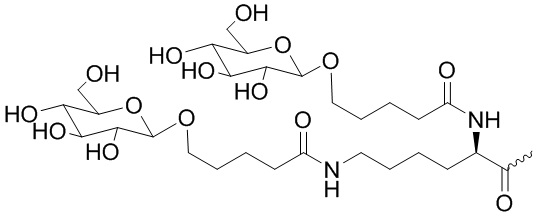 формула XVIII,
формула XVIII,
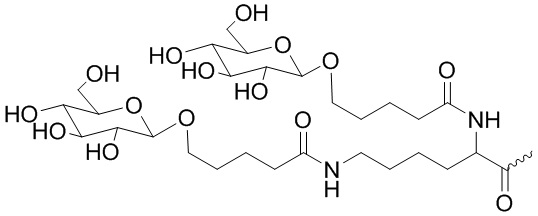 формула XIX,
формула XIX,
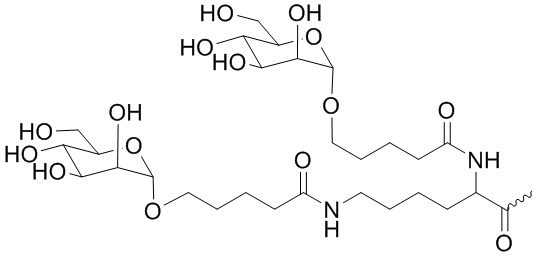 формула XX,
формула XX,
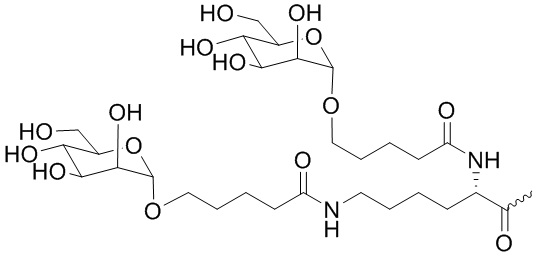 формула XXI,
формула XXI,
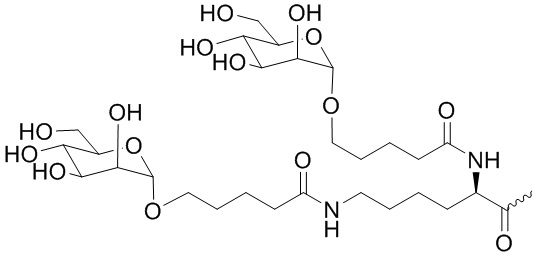 формула XXII,
формула XXII,
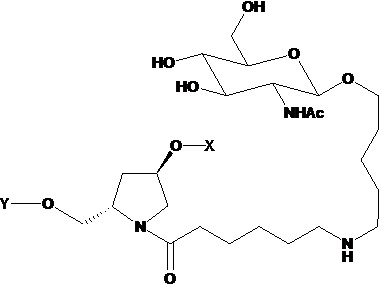 формула XXIII;
формула XXIII;
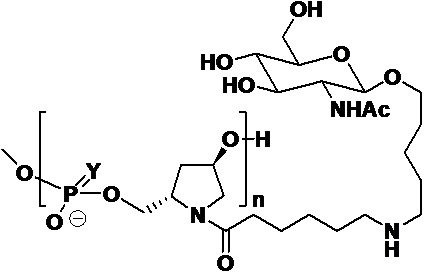 , где Y представляет собой O или S и n равняется 3-6 (формула XXIV);
, где Y представляет собой O или S и n равняется 3-6 (формула XXIV);
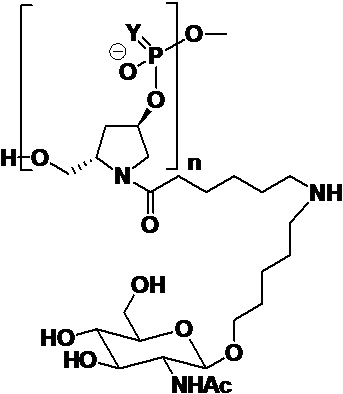 , где Y представляет собой O или S и n равняется 3-6 (формула XXV);
, где Y представляет собой O или S и n равняется 3-6 (формула XXV);
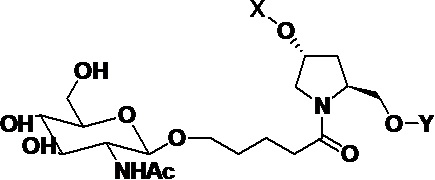 формула XXVI;
формула XXVI;
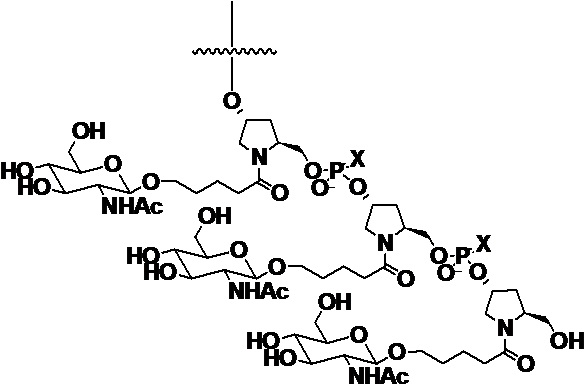 , где X представляет собой O или S (формула XXVII);
, где X представляет собой O или S (формула XXVII);
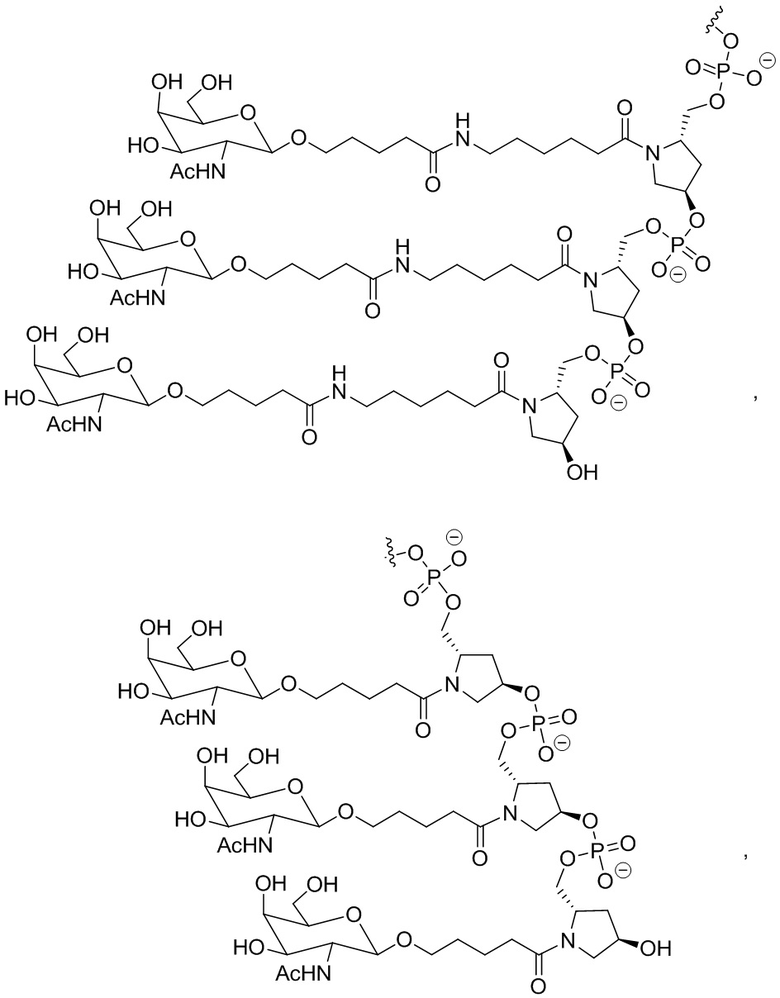 формула XXVII; формула XXIX;
формула XXVII; формула XXIX;
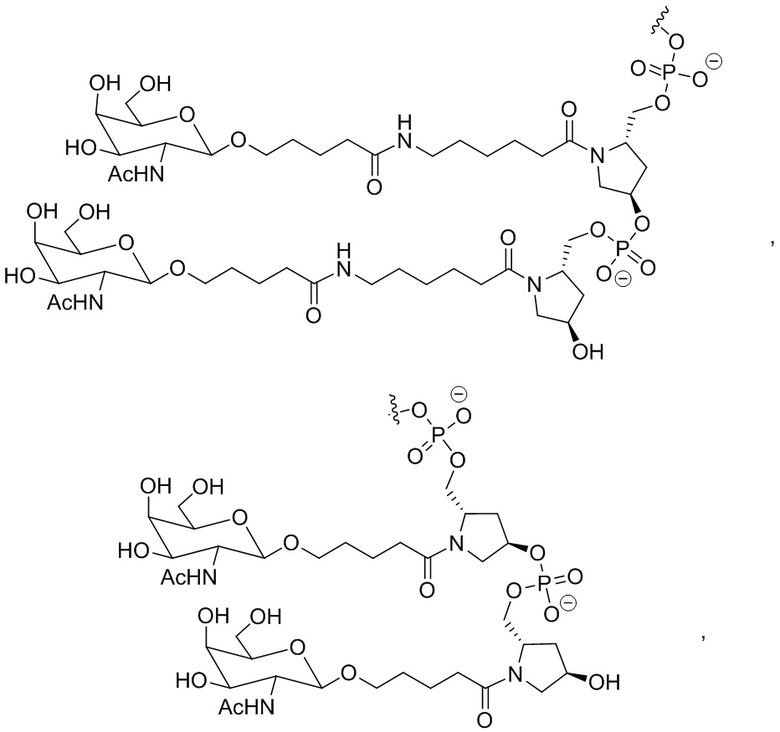 формула XXX;
формула XXX;
формула XXXI;
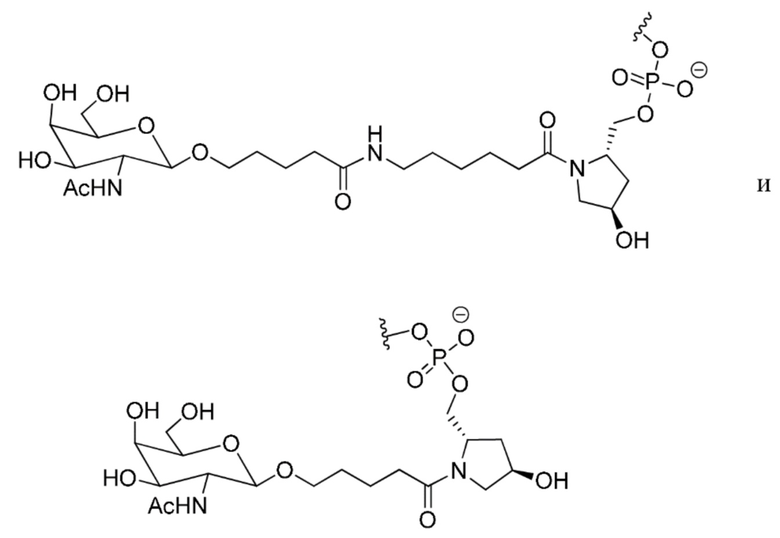 формула XXXII;
формула XXXII;
формула XXXIII;
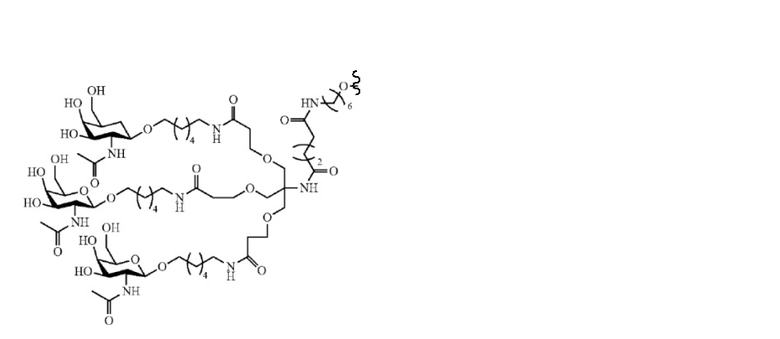 формула XXXIV.
формула XXXIV.
В другом варианте осуществления углеводный конъюгат для применения в композициях и способах по настоящему изобретению представляет собой моносахарид. В одном варианте осуществления моносахарид представляет собой N-ацетилгалактозамин, такой как
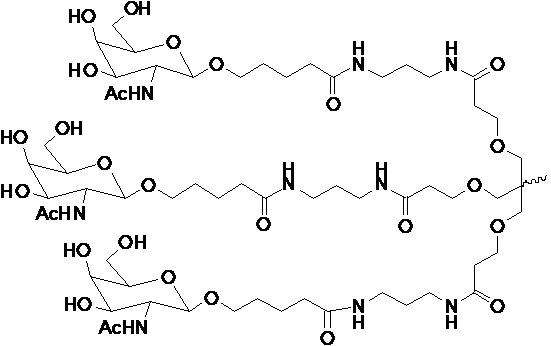 формула II.
формула II.
Другой иллюстративный углеводный конъюгат для применения в вариантах осуществления, описанных в данном документе, включает без ограничения
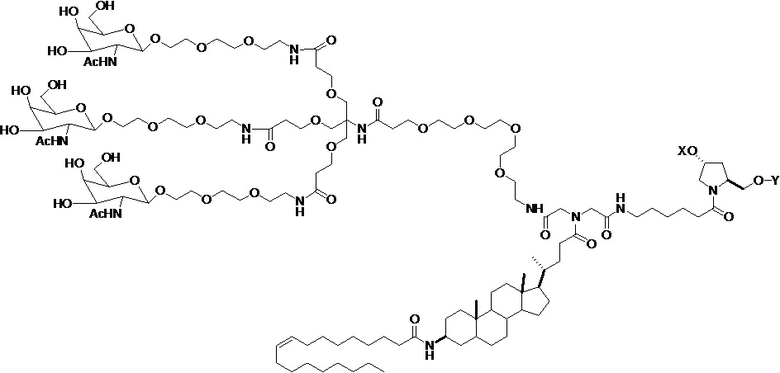
(формула XXXVI),
где один из Х или Y представляет собой олигонуклеотид, при этом другой представляет собой водород.
В определенных вариантах осуществления настоящего изобретения GalNAc или производное GalNAc присоединены к средству на основе iRNA по настоящему изобретению посредством одновалентного линкера. В некоторых вариантах осуществления GalNAc или производное GalNAc присоединены к средству на основе iRNA по настоящему изобретению посредством двухвалентного линкера. В еще нескольких других вариантах осуществления настоящего изобретения GalNAc или производное GalNAc присоединены к средству на основе iRNA по настоящему изобретению посредством трехвалентного линкера.
В одном варианте осуществления двухнитевые средства для RNAi по настоящему изобретению содержат один GalNAc или производное GalNAc, присоединенные к средству на основе iRNA, например, 5'-концу смысловой нити средства на основе dsRNA или 5'-концу одной или обеих смысловых нитей двухнитевого нацеливающегося средства для RNAi, как описано в данном документе. В другом варианте осуществления двухнитевые средства для RNAi по настоящему изобретению содержат несколько (например, 2, 3, 4, 5 или 6) GalNAc или производных GalNAc, каждый из которых независимо присоединен к нескольким нуклеотидам двухнитевого средства для RNAi посредством нескольких одновалентных линкеров.
В некоторых вариантах осуществления, например, если две нити средства на основе iRNA по настоящему изобретению являются частью одной более крупной молекулы и соединены непрерывающейся цепью нуклеотидов между 3'-концом одной нити и 5'-концом соответствующей другой нити, образующей петлю типа "шпилька", содержащую несколько неспаренных нуклеотидов, то каждый неспаренный нуклеотид в пределах петли типа "шпилька" может независимо содержать GalNAc или производное GalNAc, присоединенные посредством одновалентного линкера.
В некоторых вариантах осуществления углеводный конъюгат дополнительно содержит один или несколько дополнительных лигандов, описанных выше, таких как, без ограничения, PK-модулятор или пептид, обеспечивающий проникновение в клетку.
Дополнительные углеводные конъюгаты и линкеры, подходящие для применения в настоящем изобретении, включают описанные в публикациях согласно PCT №№ WO 2014/179620 и WO 2014/179627, полное содержание каждой из которых включено в данный документ посредством ссылки.
D. Линкеры
В некоторых вариантах осуществления конъюгат или лиганд, описанные в данном документе, могут быть присоединены к олигонуклеотиду iRNA с помощью различных линкеров, которые могут быть расщепляемыми или нерасщепляемыми.
Термин "линкер" или "линкерная группа" означает органический фрагмент, который соединяет две части соединения, например, ковалентно связывает две части соединения. Линкеры, как правило, предусматривают прямую связь или атом, такой как атом кислорода или серы, структурную единицу, такую как NR8, C(O), C(O)NH, SO, SO2, SO2NH, или цепь из атомов, такую как без ограничения замещенный или незамещенный алкил, замещенный или незамещенный алкенил, замещенный или незамещенный алкинил, арилалкил, арилалкенил, арилалкинил, гетероарилалкил, гетероарилалкенил, гетероарилалкинил, гетероциклилалкил, гетероциклилалкенил, гетероциклилалкинил, арил, гетероарил, гетероциклил, циклоалкил, циклоалкенил, алкиларилалкил, алкиларилалкенил, алкиларилалкинил, алкениларилалкил, алкениларилалкенил, алкениларилалкинил, алкиниларилалкил, алкиниларилалкенил, алкиниларилалкинил, алкилгетероарилалкил, алкилгетероарилалкенил, алкилгетероарилалкинил, алкенилгетероарилалкил, алкенилгетероарилалкенил, алкенилгетероарилалкинил, алкинилгетероарилалкил, алкинилгетероарилалкенил, алкинилгетероарилалкинил, алкилгетероциклилалкил, алкилгетероциклилалкенил, алкилгетероциклилалкинил, алкенилгетероциклилалкил, алкенилгетероциклилалкенил, алкенилгетероциклилалкинил, алкинилгетероциклилалкил, алкинилгетероциклилалкенил, алкинилгетероциклилалкинил, алкиларил, алкениларил, алкиниларил, алкилгетероарил, алкенилгетероарил, алкинилгетероарил, в котором один или несколько метиленов могут прерываться или заканчиваться O, S, S(O), SO2, N(R8), C(O), замещенным или незамещенным арилом, замещенным или незамещенным гетероарилом, замещенным или незамещенным гетероциклилом; где R8 представляет собой водород, ацил, алифатический или замещенный алифатический компонент. В одном варианте осуществления линкер состоит из приблизительно 1-24 атома, 2-24, 3-24, 4-24, 5-24, 6-24, 6-18, 7-18, 8-18, 7-17, 8-17, 6-16, 7-17 или 8-16 атомов.
Расщепляемая линкерная группа представляет собой группу, которая достаточно стабильна вне клетки, но которая после попадания в целевую клетку расщепляется с высвобождением двух частей, которые линкер удерживает вместе. В предпочтительном варианте осуществления расщепляемая линкерная группа расщепляется в приблизительно 10 раз, 20 раз, 30 раз, 40 раз, 50 раз, 60 раз, 70 раз, 80 раз, 90 раз или больше или по меньшей мере в 100 раз быстрее в целевой клетке или при первом эталонном условии (которое можно выбрать, например, чтобы оно имитировало или моделировало внутриклеточные условия), чем в крови субъекта или при втором эталонном условии (которое можно выбрать, например, чтобы оно имитировало или моделировало условия, свойственные крови или сыворотке крови).
Расщепляемые линкерные группы чувствительны к факторам расщепления, например, pH, окислительно-восстановительному потенциалу или присутствию разрушающих молекул. Как правило, средства расщепления преобладают или встречаются на более высоких уровнях или обладают большей активностью внутри клеток, чем в сыворотке крови или крови. Примеры таких разрушающих средств включают окислительно-восстановительные средства, которые выбирают для конкретных субстратов или которые не обладают субстратной специфичностью, в том числе, например, окислительные или восстановительные ферменты или восстановительные средства, такие как меркаптаны, присутствующие в клетках, которые могут разрушать расщепляемую с помощью окислительно-восстановительных реакций линкерную группу путем восстановления; эстеразы; эндосомы или средства, которые могут создавать кислую среду, например, такие, которые приводят к pH, составляющему пять или менее; ферменты, которые могут гидролизовать или разрушать расщепляемую кислотой линкерную группу, действуя в качестве универсальной кислоты, пептидазы (которые могут обладать субстратной специфичностью) и фосфатазы.
Расщепляемая линкерная группа, такая как дисульфидная связь, может быть чувствительной к pH. pH сыворотки крови человека составляет 7,4, в то время как средний pH внутри клетки немного ниже и находится в диапазоне приблизительно 7,1-7,3. Эндосомы характеризуются более кислым рН в диапазоне 5,5-6,0, а лизосомы характеризуются еще более кислым pH, составляющим приблизительно 5,0. Некоторые линкеры будут иметь расщепляемую связывающую группу, которая расщепляется в условиях предпочтительного рН, вследствие чего катионный липид высвобождается из лиганда внутри клетки или в требуемом компартменте клетки.
Линкер может включать расщепляемую линкерную группу, которая расщепляется под действием конкретного фермента. Тип расщепляемой линкерной группы, включенной в линкер, может зависеть от клетки, подлежащей нацеливанию. Например, лиганд, нацеливающий на печень, может быть связан с катионным липидом через линкер, который включает сложноэфирную группу. Клетки печени характеризуются высоким содержанием эстераз и, следовательно, линкер будет расщепляться более эффективно в клетках печени, а не в типах клеток, для которых не характерно высокое содержание эстераз. Другие типы клеток с высоким содержанием эстераз включают клетки легкого, коркового вещества почки и яичка.
Линкеры, которые содержат пептидные связи, можно применять при нацеливании на типы клеток с высоким содержанием пептидаз, такие как клетки печени и синовиоциты.
Как правило, пригодность кандидатной расщепляемой линкерной группы можно оценить путем тестирования способности разрушающего средства (или условия) расщеплять эту кандидатную линкерную группу. Кроме того, желательно также тестировать кандидатную расщепляемую линкерную группу в отношении способности противостоять расщеплению в крови или при приведении в контакт с другой нецелевой тканью. Таким образом, можно определять относительную чувствительность к расщеплению при первом и втором условиях, где первое выбирают, чтобы демонстрировать расщепление в целевой клетке, а второе выбирают, чтобы демонстрировать расщепление в других тканях или биологических жидкостях, например, крови или сыворотке крови. Измерения можно проводить в бесклеточных системах, в клетках, в культуре клеток, в культуре органов или тканей или на животных в целом. Может быть полезно провести первичные оценки в бесклеточных условиях или условиях культуры и подтвердить путем дальнейших оценок на животных в целом. В предпочтительных вариантах осуществления применимые кандидатные соединения расщепляются по меньшей мере в приблизительно 2, 4, 10, 20, 30, 40, 50, 60, 70, 80, 90 или 100 раз быстрее в клетке (или в условиях in vitro, выбранных для имитации внутриклеточных условий) по сравнению с кровью или сывороткой крови (или в условиях in vitro, выбранных для имитации внеклеточных условий).
i. Линкерные группы, расщепляемые с помощью окислительно-восстановительных реакций
В определенных вариантах осуществления расщепляемая линкерная группа представляет собой расщепляемую с помощью окислительно-восстановительных реакций линкерную группу, которая расщепляется при восстановлении или окислении. Примером расщепляемой при восстановлении линкерной группы является дисульфидная линкерная группа (-S-S-). Для определения того, подходит ли кандидатная расщепляемая линкерная группа в качестве "расщепляемой при восстановлении линкерной группой" или, например, подходит ли для применения с конкретным фрагментом iRNA и конкретным нацеливающим средством, можно обратиться к способам, описанным в данном документе. Например, кандидатное соединение можно оценивать путем инкубации с дитиотреитолом (DTT) или другим восстанавливающим средством с применением реагентов, известных из уровня техники, которые имитируют скорость расщепления, которая наблюдалась бы в клетке, например, целевой клетке. Кандидатные соединения также можно оценивать в условиях, которые выбирают для имитации условий крови или сыворотки крови. В одном варианте осуществления расщепление кандидатных соединений в крови составляет не более приблизительно 10%. В других вариантах осуществления применимые кандидатные соединения разрушаются по меньшей мере в приблизительно 2, 4, 10, 20, 30, 40, 50, 60, 70, 80, 90 или в приблизительно 100 раз быстрее в клетке (или в in vitro условиях, выбранных для имитации внутриклеточных условий) по сравнению с кровью (или in vitro условиями, выбранными для имитации внеклеточных условий). Скорость расщепления кандидатных соединений можно определить с применением стандартных анализов ферментативной кинетики в условиях, выбранных для имитации внутриклеточной среды, и сравнить с условиями, выбранными для имитации внеклеточной среды.
ii. Фосфатные расщепляемые линкерные группы
В других вариантах осуществления расщепляемый линкер предусматривает фосфатную расщепляемую линкерную группу. Фосфатная расщепляемая линкерная группа расщепляется под действием средств, которые разрушают или гидролизуют фосфатную группу. Примером средства, которое расщепляет фосфатные группы в клетках, являются ферменты, такие как фосфатазы клетки. Примерами фосфатных линкерных групп являются -O-P(O)(ORk)-O-, -O-P(S)(ORk)-O-, -O-P(S)(SRk)-O-, -S-P(O)(ORk)-O-, -O-P(O)(ORk)-S-, -S-P(O)(ORk)-S-, -O-P(S)(ORk)-S-, -S-P(S)(ORk)-O-, -O-P(O)(Rk)-O-, -O-P(S)(Rk)-O-, -S-P(O)(Rk)-O-, -S-P(S)(Rk)-O-, -S-P(O)(Rk)-S-, -O-P(S)(Rk)-S-. Предпочтительными вариантами осуществления являются -O-P(O)(OH)-O-, -O-P(S)(OH)-O-, -O-P(S)(SH)-O-, -S-P(O)(OH)-O-, -O-P(O)(OH)-S-, -S-P(O)(OH)-S-, -O-P(S)(OH)-S-, -S-P(S)(OH)-O-, -O-P(O)(H)-O-, -O-P(S)(H)-O-, -S-P(O)(H)-O, -S-P(S)(H)-O-, -S-P(O)(H)-S- и -O-P(S)(H)-S-. Предпочтительный вариант осуществления представляет собой -O-P(O)(OH)-O-. Эти кандидатные соединения можно оценивать с помощью способов, аналогичных описанным выше.
iii. Расщепляемые кислотой линкерные группы
В других вариантах осуществления расщепляемый линкер предусматривает расщепляемую кислотой линкерную группу. Расщепляемая кислотой линкерная группа представляет собой линкерную группу, которая расщепляется в кислых условиях. В предпочтительных вариантах осуществления расщепляемые кислотой линкерные группы расщепляются в кислой среде при значении pH приблизительно 6,5 или ниже (например, приблизительно 6,0, 5,5, 5,0 или ниже) или с помощью средств, таких как ферменты, которые могут выступать в роли универсальной кислоты. В клетке специфические органеллы, характеризующиеся низким pH, такие как эндосомы и лизосомы, могут обеспечить расщепляющую среду для расщепляемых кислотами линкерных групп. Примеры расщепляемых кислотами линкерных групп включают без ограничения гидразоны, сложные эфиры и сложные эфиры аминокислот. Расщепляемые кислотами группы могут характеризоваться общей формулой -C=NN-, C(O)O или -OC(O). Предпочтительным вариантом осуществления является случай, когда атом углерода, присоединенный к кислороду сложноэфирной группы (в алкоксигруппе), входит в состав арильной группы, замещенной алкильной группы или четвертичной алкильной группы, такой как диметилпентил или трет-бутил. Эти кандидатные соединения можно оценивать с помощью способов, аналогичных описанным выше.
iv. Сложноэфирные линкерные группы
В других вариантах осуществления расщепляемый линкер предусматривает сложноэфирную расщепляемую линкерную группу. Сложноэфирная расщепляемая линкерная группа расщепляется в клетках под действием ферментов, таких как эстеразы и амидазы. Примеры сложноэфирных расщепляемых линкерных групп включают без ограничения сложноэфирные производные алкиленовых, алкениленовых и алкиниленовых групп. Сложноэфирные расщепляемые линкерные группы характеризуются общей формулой -C(O)O- или -OC(O)-. Эти кандидатные соединения можно оценивать с помощью способов, аналогичных описанным выше.
v. Пептидные расщепляемые группы
В еще нескольких других вариантах осуществления расщепляемый линкер содержит пептидную расщепляемую линкерную группу. Пептидная расщепляемая линкерная группа расщепляется в клетках под действием ферментов, таких как пептидазы и протеазы. Пептидные расщепляемые линкерные группы представляют собой пептидные связи, образуемые между аминокислотами при получении олигопептидов (например, дипептидов, трипептидов и т.д.) и полипептидов. Пептидные расщепляемые группы не включают амидную группу (-C(O)NH-). Амидная группа может быть образована между любыми алкиленами, алкениленами или алкиниленами. Пептидная связь представляет собой специальный тип амидной связи, образуемый между аминокислотами при образовании пептидов и белков. Пептидная расщепляемая группа, как правило, ограничивается пептидной связью (т. е. амидной связью), образуемой между аминокислотами при образованием пептидов и белков, и не включает амидную функциональную группу в целом. Пептидные расщепляемые линкерные группы характеризуются общей формулой - NHCHRAC(O)NHCHRBC(O)-, где RA и RB представляют собой R-группы двух соседних аминокислот. Эти кандидатные соединения можно оценивать с помощью способов, аналогичных описанным выше.
В некоторых вариантах осуществления iRNA по настоящему изобретению конъюгирована с углеводом посредством линкера. Неограничивающие примеры углеводных конъюгатов iRNA с линкерами в композициях и способах по настоящему изобретению включают без ограничения
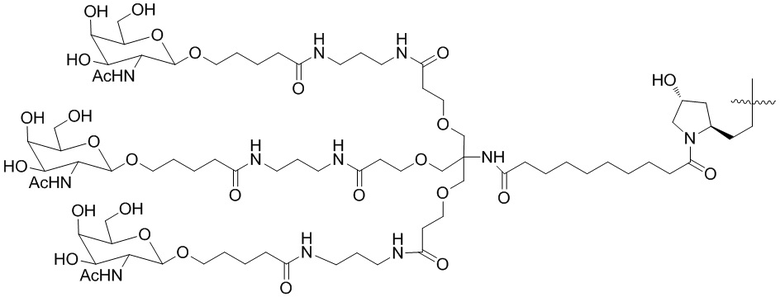 (формула XXXVII),
(формула XXXVII),
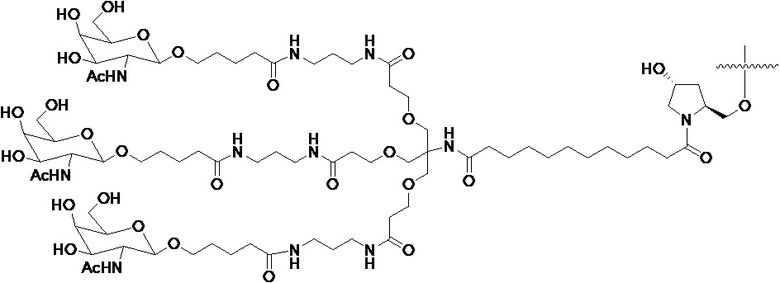 (формула XXXVIII),
(формула XXXVIII),
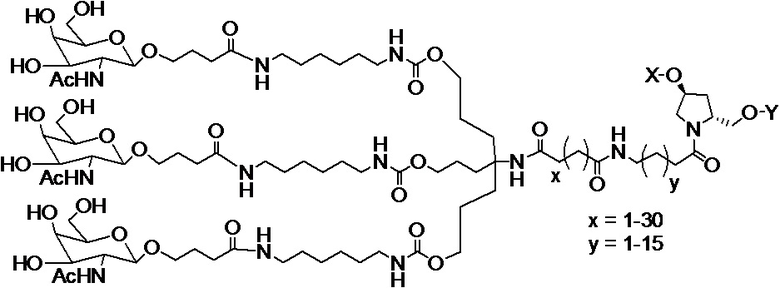 (формула XXXIX),
(формула XXXIX),
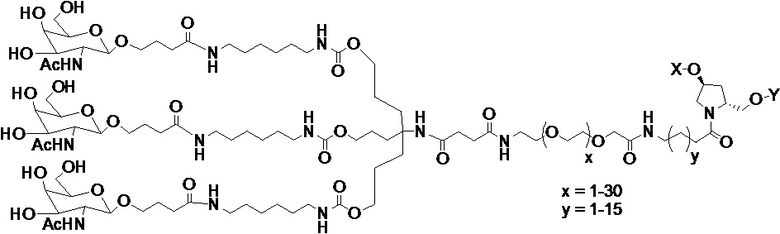
(формула XL),
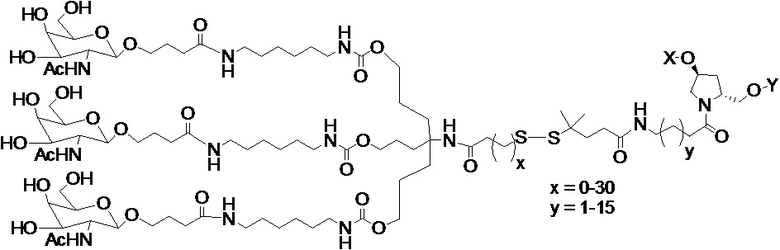
(формула XLI),
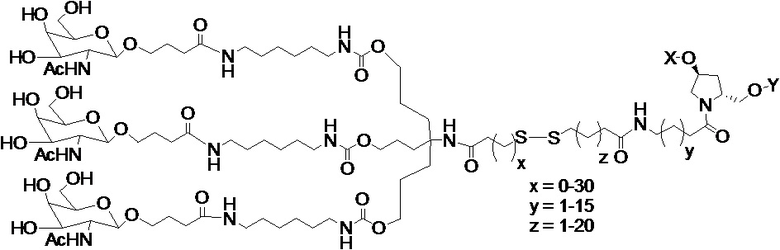
(формула XLII),
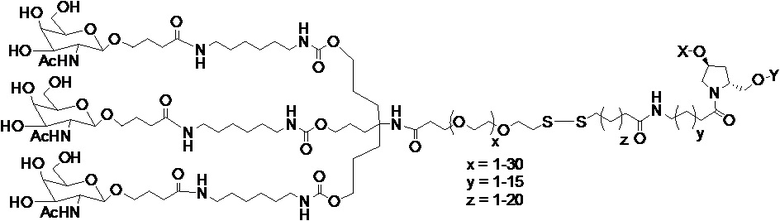
(формула XLIII) и
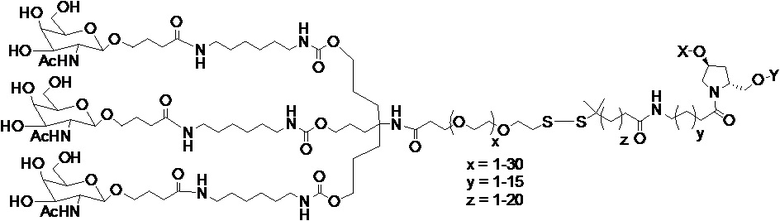
(формула XLIV), где один из X или Y представляет собой олигонуклеотид, а другой представляет собой водород.
В определенных вариантах осуществления композиций и способов по настоящему изобретению лиганд представляет собой одно или несколько производных "GalNAc" (N-ацетилгалактозамина), присоединенных посредством двухвалентного или трехвалентного разветвленного линкера.
В одном варианте осуществления dsRNA по настоящему изобретению конъюгирована с двухвалентным или трехвалентным разветвленным линкером, выбранным из группы структур, показанных в любой из формул (XLV) - (XLVI):
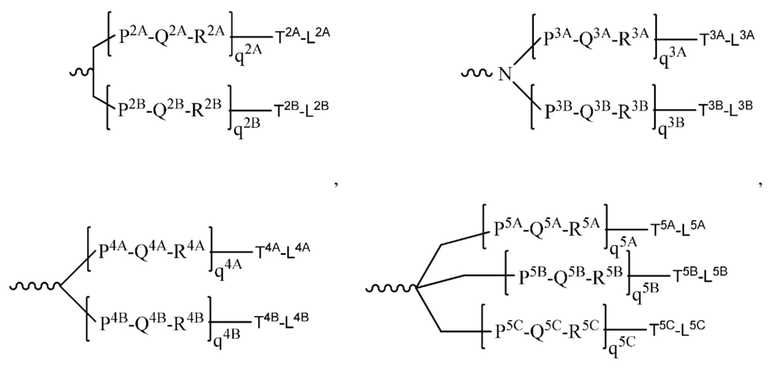
где:
q2A, q2B, q3A, q3B, q4A, q4B, q5A, q5B и q5C независимо в каждом случае равняются 0-20, и где повторяющиеся структурные единицы могут быть одинаковыми или различными;
каждый из P2A, P2B, P3A, P3B, P4A, P4B, P5A, P5B, P5C, T2A, T2B, T3A, T3B, T4A, T4B, T4A, T5B, T5C независимо в каждом случае отсутствует, представляет собой CO, NH, O, S, OC(O), NHC(O), CH2, CH2NH или CH2O;
Q2A, Q2B, Q3A, Q3B, Q4A, Q4B, Q5A, Q5B, Q5C независимо в каждом случае отсутствуют, представляют собой алкилен, замещенный алкилен, где один или несколько метиленов могут прерываться или оканчиваться одним или несколькими из O, S, S(O), SO2, N(RN), C(R')=C(R''), C≡C или C(O);
каждый из R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R5C независимо в каждом случае отсутствует, представляет собой NH, O, S, CH2, C(O)O, C(O)NH, NHCH(Ra)C(O), -C(O)-CH(Ra)-NH-, CO, CH=N-O, 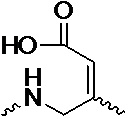 ,
, 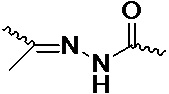 ,
, 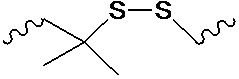 ,
, 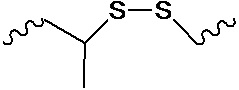 ,
, 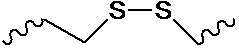 или гетероциклил;
или гетероциклил;
L2A, L2B, L3A, L3B, L4A, L4B, L5A, L5B и L5C представляют собой лиганд; т. е. каждый из них независимо в каждом случае представляет собой моносахарид (такой как GalNAc), дисахарид, трисахарид, тетрасахарид, олигосахарид или полисахарид; и Ra представляет собой H или боковую цепь аминокислоты. Трехвалентные линкеры, конъюгирующие производные GalNAc, особенно пригодны для применения со средствами для RNAi для ингибирования экспрессии гена-мишени, такие как характеризующиеся формулой (XLIX):
формула XLIX
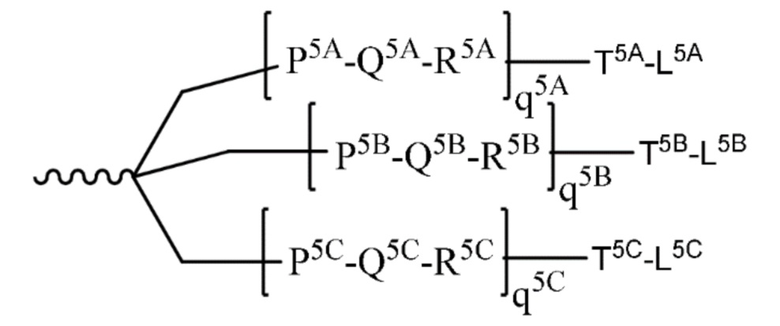 ,
,
где L5A, L5B и L5C представляют собой моносахарид, такой как производное GalNAc.
Примеры подходящих двухвалентных и трехвалентных разветвленных линкерных групп, конъюгирующих производные GalNac, включают без ограничения структуры, указанные выше как формулы II, VII, XI, X и XIII.
Иллюстративные патенты США, в которых изложено получение конъюгатов РНК, включают без ограничения патенты США №№ 4828979; 4948882; 5218105; 5525465; 5541313; 5545730; 5552538; 5578717, 5580731; 5591584; 5109124; 5118802; 5138045; 5414077; 5486603; 5512439; 5578718; 5608046; 4587044; 4605735; 4667025; 4762779; 4789737; 4824941; 4835263; 4876335; 4904582; 4958013; 5082830; 5112963; 5214136; 5082830; 5112963; 5214136; 5245022; 5254469; 5258506; 5262536; 5272250; 5292873; 5317098; 5371241, 5391723; 5416203, 5451463; 5510475; 5512667; 5514785; 5565552; 5567810; 5574142; 5585481; 5587371; 5595726; 5597696; 5599923; 5599928;5688941; 6294664; 6320017; 6576752; 6783931; 6900297; 7037646 и 8106022, полное содержание каждого из которых включено в данный документ посредством ссылки.
Не является необходимым, чтобы все положения в данном соединении были модифицированы единоообразно, и, фактически, более чем одна из вышеупомянутых модификаций может быть включена в одно соединение или даже в один нуклеозид в пределах iRNA. Настоящее изобретение также включает соединения на основе iRNA, которые представляют собой химерные соединения.
"Химерные" соединения на основе iRNA или "химеры" в контексте настоящего изобретения представляют собой соединения на основе iRNA, предпочтительно средства на основе dsRNA, которые содержат два или более химически отличающихся участка, каждый из которых состоит по меньшей мере из одной мономерной структурной единицы, т. е. нуклеотида в случае соединения на основе dsRNA. Такие iRNA, как правило, содержат по меньшей мере один участок, где РНК модифицирована таким образом, чтобы обеспечить iRNA повышенную устойчивость к разрушению нуклеазами, повышенное поглощение клеткой или повышенную аффинность связывания в отношении целевой нуклеиновой кислоты. Дополнительный участок iRNA может служить в качестве субстрата для ферментов, способных расщеплять гибриды РНК:ДНК или РНК:РНК. В качестве примера, РНКаза Н представляет собой клеточную эндонуклеазу, которая расщепляет нить РНК в дуплексе РНК:ДНК. Активация РНКазы Н, следовательно, приводит к расщеплению РНК-мишени, вследствие чего значительно повышается эффективность ингибирования экспрессии гена с помощью iRNA. Следовательно, зачастую, если применять химерные dsRNA, сравнимые результаты можно получить с более короткими iRNA по сравнению с фосфотиоатными дезокси-dsRNA, гибридизирующимися с тем же целевым участком. Расщепление РНК-мишени традиционно можно обнаруживать c помощью гель-электрофореза и при необходимости с помощью ассоциированных методик гибридизации нуклеиновых кислот, известных из уровня техники.
В некоторых случаях РНК из числа iRNA может быть модифицирована группой, не являющейся лигандом. Целый ряд молекул, не являющихся лигандами, были конъюгированы с iRNA для усиления активности, распределения в клетках или поглощения iRNA клеткой, и процедуры для выполнения таких типов конъюгации доступны в научной литературе. Такие фрагменты, не являющиеся лигандами, включали липидные фрагменты, такие как холестерин (Kubo, T. et al., Biochem. Biophys. Res. Comm., 2007, 365(1):54-61; Letsinger et al., Proc. Natl. Acad. Sci. USA, 1989, 86:6553), холевая кислота (Manoharan et al., Bioorg. Med. Chem. Lett., 1994, 4:1053), простой тиоэфир, например, гексил-S-тритилтиол (Manoharan et al., Ann. N.Y. Acad. Sci., 1992, 660:306; Manoharan et al., Bioorg. Med. Chem. Let., 1993, 3:2765), тиохолестерин (Oberhauser et al., Nucl. Acids Res., 1992, 20:533), алифатическая цепь, например, остатки додекандиола или ундецила (Saison-Behmoaras et al., EMBO J, 1991, 10:111; Kabanov et al., FEBS Lett., 1990, 259:327; Svinarchuk et al., Biochimie, 1993, 75:49), фосфолипид, например, ди-гексадецил-рац-глицерин или 1,2-ди-О-гексадецил-рац-глицеро-3-H-фосфонат триэтиламмония (Manoharan et al., Tetrahedron Lett., 1995, 36:3651; Shea et al., Nucl. Acids Res., 1990, 18:3777), полиамин или полиэтиленгликолевая цепь (Manoharan et al., Nucleosides & Nucleotides, 1995, 14:969) или адамантануксусная кислота (Manoharan et al., Tetrahedron Lett., 1995, 36:3651), пальмитиловый фрагмент (Mishra et al., Biochim. Biophys. Acta, 1995, 1264:229) или октадециламиновый или гексиламинокарбонилоксихолестериновый фрагмент (Crooke et al., J. Pharmacol. Exp. Ther., 1996, 277:923). Иллюстративные патенты США, в которых изложено получение таких конъюгатов РНК, были приведены выше. Типичные протоколы конъюгации предусматривают синтез РНК, несущих линкер с аминогруппой в одном или нескольких положениях последовательности. Затем аминогруппа вступает в реакцию с молекулой, подлежащей конъюгации, с применением соответствующего конденсирующего или активирующего реагентов. Реакцию конъюгации можно выполнять либо с РНК, все еще связанной с твердой подложкой, либо после отщепления РНК, в фазе раствора. Очистка РНК-конъюгата с помощью HPLC, как правило, обеспечивает получение чистого конъюгата.
IV. Доставка iRNA по настоящему изобретению
Доставку iRNA по настоящему изобретению в клетку, например в клетку в организме субъекта, такого как субъект-человек, можно осуществлять рядом различных путей. Например, доставку можно осуществлять путем приведения клетки в контакт с iRNA по настоящему изобретению либо in vitro, либо in vivo. In vivo доставку также можно осуществлять напрямую путем введения субъекту композиции, содержащей iRNA, например dsRNA. В качестве альтернативы in vivo доставку можно осуществлять опосредованно путем введения одного или нескольких векторов, которые кодируют iRNA и управляют ее экспрессией. Такие альтернативные случаи дополнительно обсуждаются ниже.
В целом, любой способ доставки молекулы нуклеиновой кислоты (in vitro или in vivo) может быть адаптирован для применения с iRNA по настоящему изобретению (см., например, Akhtar S. and Julian RL. (1992) Trends Cell. Biol. 2(5):139-144 и WO94/02595, которые включены в данный документ посредством ссылки в полном объеме). Что касается in vivo доставки, факторы, которые учитывают в контексте доставки молекулы iRNA, включают, например, биологическую стабильность доставляемой молекулы, предотвращение неспецифических эффектов и накопление доставляемой молекулы в целевой ткани. Неспецифические эффекты iRNA могут быть сведены к минимуму путем локального введения, например путем прямой инъекции или вживления в ткань, или местного применения препарата. Локальное введение в участок, подлежащий лечению, максимально увеличивает локальную концентрацию средства, ограничивает воздействие средства на системные ткани, которые в ином случае могут быть повреждены средством или которые могут разрушить средство, и позволяет вводить более низкую общую дозу молекулы iRNA. С помощью нескольких исследований было показано эффективное обусловленное нокдауном падение уровней продуктов генов при локальном введении средства на основе dsRNA. Например, было показано, что внутриглазная доставка dsRNA к VEGF как путем интравитреальной инъекции яванским макакам (Tolentino, MJ, et al (2004) Retina 24:132-138), так и путем субретинальных инъекций мышам (Reich, SJ., et al (2003) Mol. Vis. 9:210-216) предупреждает неоваскуляризацию в экспериментальной модели возрастной макулярной дистрофии. Кроме того, прямая внутриопухолевая инъекция dsRNA мышам снижает объем опухолей (Pille, J., et al (2005) Mol. Ther.11:267-274) и может увеличивать время жизни мышей, несущих опухоль (Kim, WJ., et al (2006) Mol. Ther. 14:343-350; Li, S., et al (2007) Mol. Ther. 15:515-523). Было показано, что РНК-интерференция была также успешной при локальной доставке в ЦНС путем прямой инъекции (Dorn, G., et al. (2004) Nucleic Acids 32:e49; Tan, PH., et al (2005) Gene Ther. 12:59-66; Makimura, H., et al (2002) BMC Neurosci. 3:18; Shishkina, GT., et al (2004) Neuroscience 129:521-528; Thakker, ER., et al (2004) Proc. Natl. Acad. Sci. U.S.A. 101:17270-17275; Akaneya,Y., et al (2005) J. Neurophysiol. 93:594-602) и в легкие путем интраназального введения (Howard, KA., et al (2006) Mol. Ther. 14:476-484; Zhang, X., et al (2004) J. Biol. Chem. 279:10677-10684; Bitko, V., et al (2005) Nat. Med. 11:50-55). В случае системного введения iRNA для предупреждения инфекции РНК может быть модифицирована или, в качестве альтернативы, доставлена с помощью системы доставки лекарственного средства; при этом оба способа предотвращают быстрое разрушение dsRNA под действием эндо- и экзонуклеаз in vivo. Модификация РНК или фармацевтический носитель также могут обеспечивать нацеливание iRNA на целевую ткань, и с их помощью можно избежать нежелательных нецелевых эффектов. Молекулы iRNA можно модифицировать с помощью химической конъюгации с липофильными группами, такими как холестерин, для увеличения поглощения клеткой и предотвращения разрушения. Например, iRNA, направленную против ApoB, которая конъюгирована с липофильным фрагментом, представляющим собой холестерин, вводили системно мышам и это приводило к нокдауну mRNA apoB как в печени, так и в тонкой кишке (Soutschek, J., et al. (2004) Nature 432:173-178). Как было показано, конъюгация iRNA с аптамером ингибирует рост опухоли и опосредует регресс опухоли на мышиной модели рака предстательной железы (McNamara, JO, et al. (2006) Nat. Biotechnol. 24:1005-1015). В альтернативном варианте осуществления iRNA можно доставлять с помощью систем доставки лекарственных средств, таких как наночастица, дендример, полимер, липосомы или катионная система доставки. Положительно заряженные катионные системы доставки способствуют связыванию молекулы iRNA (отрицательно заряженной), а также усиливают взаимодействия на отрицательно заряженной клеточной мембране с обеспечением эффективного поглощения iRNA клеткой. Катионные липиды, дендримеры или полимеры можно либо связывать с iRNA, либо индуцировать для образования везикулы или мицеллы (см., например, Kim SH, et al. (2008) Journal of Controlled Release 129(2):107-116), которые заключают в себе iRNA. Образование везикул или мицелл дополнительно предотвращает разрушение iRNA при системном введении. Способы получения и введения комплексов катионный липид-iRNA находятся в пределах квалификации специалиста в данной области (см., например, Sorensen, DR, et al. (2003) J. Mol. Biol 327:761-766; Verma, UN, et al. (2003) Clin. Cancer Res. 9:1291-1300; Arnold, AS et al. (2007) J. Hypertens. 25:197-205, которые включены в данный документ посредством ссылки во всей своей полноте). Некоторые неограничивающие примеры систем доставки лекарственных средств, применимых для системной доставки iRNA, включают DOTAP (Sorensen, DR., et al. (2003), выше; Verma, UN, et al. (2003), выше), олигофектамин, "твердые частицы с нуклеиновой кислотой-липидом" (Zimmermann, TS, et al. (2006) Nature 441:111-114), кардиолипин (Chien, PY, et al. (2005) Cancer Gene Ther. 12:321-328; Pal, A, et al. (2005) Int J. Oncol. 26:1087-1091), полиэтиленимин (Bonnet ME, et al. (2008) Pharm. Res. Aug 16, электронная публикация до выхода из печати; Aigner, A. (2006) J. Biomed. Biotechnol. 71659), пептиды Arg-Gly-Asp (RGD) (Liu, S. (2006) Mol. Pharm. 3:472-487) и полиамидоамины (Tomalia, DA, et al (2007) Biochem. Soc. Trans. 35:61-67; Yoo, H., et al. (1999) Pharm. Res. 16:1799-1804). В некоторых вариантах осуществления iRNA образует комплекс с циклодекстрином для системного введения. Способы введения и фармацевтические композиции на основе iRNA и циклодекстринов можно найти в патенте США № 7427605, который включен в данный документ посредством ссылки во всей своей полноте.
A. Вектор, кодирующий iRNA по настоящему изобретению
iRNA, нацеливающаяся на ген Serpina1, может экспрессироваться за счет единиц транскрипции, вставленных в ДНК- или РНК-векторы (см., например, Couture, A, et al., TIG. (1996), 12:5-10; Skillern, A, et al., публикацию международной заявки согласно PCT № WO 00/22113, Conrad, публикацию международной заявки согласно PCT № WO 00/22114 и Conrad, патент США № 6054299). Экспрессия может быть временной (порядка нескольких часов - недель) или длительной (недели - месяцы или дольше) в зависимости от конкретной применяемой конструкции и целевой ткани или типа клеток. Такие трансгены можно вводить в виде линейной конструкции, кольцевой плазмиды или вирусного вектора, который может представлять собой интегрирующий или неинтегрирующий вектор. Трансген также можно конструировать с возможностью его наследования в виде экстрахромосомной плазмиды (Gassmann, et al., Proc. Natl. Acad. Sci. USA (1995) 92:1292).
Отдельные нить или нити iRNA могут транскрибироваться с промотора в векторе экспрессии. Если следует экспрессировать две отдельные нити для получения, например, dsRNA, в целевую клетку можно совместно вводить два отдельных вектора экспрессии (например, путем трансфекции или инфицирования). В качестве альтернативы каждая отдельная нить dsRNA может транскрибироваться за счет промоторов, оба из которых расположены в одной и той же плазмиде экспрессии. В одном варианте осуществления dsRNA экспрессируется в виде полинуклеотидов с инвертированным повтором, соединенных линкерной полинуклеотидной последовательностью так, что dsRNA имеет структуру типа "стебель-петля".
Векторы экспрессии iRNA, как правило, представляют собой ДНК-плазмиды или вирусные векторы. Чтобы получать рекомбинантные конструкции для экспрессии iRNA, как описано в данном документе, можно применять векторы экспрессии, совместимые с эукариотическими клетками, предпочтительно совместимые с клетками позвоночных. Векторы для экспрессии в эукариотических клеток хорошо известны из уровня техники и доступны из ряда коммерческих источников. Как правило, предусматривается, что такие векторы содержат подходящие сайты рестрикции для вставки требуемого сегмента нуклеиновой кислоты. Доставка векторов, экспрессирующих iRNA, может быть системной, как, например, путем внутривенного или внутримышечного введения, путем введения в целевые клетки, эксплантированные из пациента, с последующим обратным введением пациенту или с помощью любого другого способа, который обеспечивает возможность введения в требуемую целевую клетку.
Системы на основе вирусных векторов, которые можно использовать со способами и композициями, описанными в данном документе, включают без ограничения (a) аденовирусные векторы; (b) ретровирусные векторы, в том числе без ограничения лентивирусные векторы, вирус мышиного лейкоза Молони и т.д; (c) векторы на основе аденоассоциированного вируса; (d) векторы на основе вируса простого герпеса; (e) векторы на основе SV40; (f) векторы на основе вируса полиомы; (g) векторы на основе вируса папилломы; (h) векторы на основе пикорнавируса; (i) векторы на основе поксвируса, такого как ортопокс, например, векторы на основе вируса осповакцины, или авипоксвирус, например, поксвируса канареек или вируса оспы кур; и (j) хелпер-зависимый или "слабый" аденовирус. Также преимущественными могут быть вирусы, дефектные по репликации. Различные векторы будут встраиваться в геном клеток или не будут встраиваться в геном клеток. При необходимости конструкции могут включать последовательности вирусов для трансфекции. В качестве альтернативы конструкция может быть встроена в векторы, способные к эписомальной репликации, например, векторы на основе EPV и EBV. Для обеспечения экспрессии iRNA в целевых клетках в конструкции для рекомбинантной экспрессии iRNA, как правило, будут предусматриваться регуляторные элементы, например, промоторы, энхансеры и т. д. Другие аспекты, учитываемые в отношении векторов и конструкций, известны из уровня техники.
V. Фармацевтические композиции по настоящему изобретению
Настоящее изобретение также включает фармацевтические композиции и составы, которые включают iRNA по настоящему изобретению. В одном варианте осуществления в данном документе предусмотрены фармацевтические композиции, содержащие iRNA, как описано в данном документе, и фармацевтически приемлемый носитель. Фармацевтические композиции, содержащие iRNA, являются применимыми для лечения заболевания или нарушения, ассоциированного с экспрессией или активностью гена Serpina1, например ассоциированного с дефектной формой Serpina1 нарушения, например обусловленного дефектной формой Serpina1 нарушения функции печени. Такие фармацевтические композиции составляют в зависимости от способа доставки. Одним примером являются композиции, которые составлены для системного введения посредством доставки парентеральным путем, например путем внутривенной (IV) доставки. Другим примером являются композиции, которые составлены для непосредственной доставки в паренхиму головного мозга, например, путем инфузии в головной мозг, такой как непрерывная инфузия с помощью насоса.
Фармацевтические композиции, содержащие средства для RNAi согласно настоящему изобретению, могут быть, например, растворами с буфером или без него или композициями, содержащими фармацевтически приемлемые носители. Такие композиции включают, например, водные или кристаллические композиции, липосомные составы, мицеллярные составы, эмульсии и векторы для генной терапии.
В способах согласно настоящему изобретению средство для RNAi можно вводить в растворе. Свободное средство для RNAi можно вводить в небуферном растворе, например в солевом растворе или в воде. В качестве альтернативы свободную siRNA также можно вводить в подходящем буферном растворе. Буферный раствор может содержать ацетат, цитрат, проламин, карбонат или фосфат или любую их комбинацию. В предпочтительном варианте осуществления буферным раствором является фосфатно-солевой буферный раствор (PBS). Показатель pH и осмолярность буферного раствора, содержащего средство для RNAi, можно корректировать, с тем чтобы он подходил для введения субъекту.
В некоторых вариантах осуществления буферный раствор дополнительно содержит средство для регулирования осмолярности раствора, так что осмолярность поддерживается на необходимом уровне, например при физиологических значениях для плазмы крови человека. Растворенные вещества, которые можно добавлять к буферному раствору для регулирования осмолярности, включают без ограничения белки, пептиды, аминокислоты, не поддающиеся метаболизму полимеры, витамины, ионы, сахара, метаболиты, органические кислоты, липиды или соли. В некоторых вариантах осуществления средство для регулирования осмолярности раствора представляет собой соль. В определенных вариантах осуществления средство для регулирования осмолярности раствора представляет собой хлорид натрия или хлорид калия.
Фармацевтические композиции по настоящему изобретению можно вводить в дозах, достаточных для ингибирования экспрессии гена Serpina1. Как правило, подходящая доза iRNA по настоящему изобретению будет находиться в диапазоне от приблизительно 0,001 до приблизительно 200,0 миллиграмм на килограмм веса тела реципиента в день, как правило, в диапазоне от приблизительно 1 до 50 мг на килограмм веса тела в день. Например, dsRNA можно вводить в количестве, составляющем приблизительно 0,01 мг/кг, приблизительно 0,05 мг/кг, приблизительно 0,5 мг/кг, приблизительно 1 мг/кг, приблизительно 1,5 мг/кг, приблизительно 2 мг/кг, приблизительно 3 мг/кг, приблизительно 10 мг/кг, приблизительно 20 мг/кг, приблизительно 30 мг/кг, приблизительно 40 мг/кг или приблизительно 50 мг/кг на однократную дозу.
Фармацевтическую композицию можно вводить один раз в день или iRNA можно вводить в виде двух, трех или более частей дозы через определенные интервалы времени на протяжении дня, или даже при помощи непрерывной инфузии, или доставки посредством состава с контролируемым высвобождением. В таком случае количество iRNA, содержащееся в каждой части дозы, должно быть соответственно меньше, чтобы обеспечить общую суточную дозу. Единица дозирования также может быть составлена для доставки в течение нескольких дней, например, при помощи традиционного состава с замедленным высвобождением, который обеспечивает замедленное высвобождение iRNA в течение периода, составляющего несколько дней. Составы с замедленным высвобождением хорошо известны в данной области и особенно применимы для доставки средств в определенный участок, например, их можно применять со средствами по настоящему изобретению. В данном варианте осуществления единица дозирования содержит соответствующее количество суточной дозы.
В других вариантах осуществления однократная доза фармацевтических композиций может быть длительного действия, так что последующие дозы вводят с интервалами не более 3, 4 или 5 дней или с интервалами не более 1, 2, 3 или 4 недель. В некоторых вариантах осуществления настоящего изобретения однократную дозу фармацевтических композиций по настоящему изобретению вводят один раз в неделю. В других вариантах осуществления настоящего изобретения однократную дозу фармацевтических композиций по настоящему изобретению вводят два раза в месяц.
Специалисту в данной области будет понятно, что определенные факторы могут влиять на дозировку и временные рамки, необходимые для эффективного лечения субъекта, в том числе без ограничения тяжесть заболевания или нарушения, виды предшествующего лечения, общее состояние здоровья и/или возраст субъекта и другие имеющиеся заболевания. Кроме того, лечение субъекта с помощью терапевтически эффективного количества композиции может включать один период лечения или серию периодов лечения. Расчеты эффективных дозировок и in vivo периодов полужизни для индивидуальных iRNA, охваченных настоящим изобретением, можно проводить с применением традиционных методологий или на основе in vivo тестирования с применением соответствующей животной модели, как описано в другом месте данного документа.
Достижения в области генетики мышей обеспечили ряд мышиных моделей для изучения различных заболеваний человека, как например, нарушение функции печени, на которое будет оказывать благоприятное воздействие снижение экспрессии Serpina1. Такие модели можно применять для проведения тестирования iRNA in vivo, а также для определения терапевтически эффективной дозы. Подходящие мышиные модели известны в данной области и включают, например, мышь, содержащую трансген, экспрессирующий Serpina1 человека.
Фармацевтические композиции по настоящему изобретению можно вводить различными путями в зависимости от того, требуется ли локальное или системное лечение, и от области, подлежащей обработке. Введение может быть местным (например, с помощью трансдермального пластыря), легочным, например, путем ингаляции или инсуффляции порошков или аэрозолей, в том числе с помощью ингалятора; интратрахеальным, интраназальным, эпидермальным и трансдермальным, пероральным или парентеральным. Парентеральное введение включает внутривенную, внутриартериальную, подкожную, внутрибрюшинную или внутримышечную инъекцию или инфузию; субдермальное, например, посредством имплантированного устройства; или интракраниальное, например, интрапаренхиматозное, интратекальное или интравентрикулярное введение. iRNA можно доставлять таким образом, чтобы происходило нацеливание на конкретную ткань, такую как печень (например, гепатоциты печени).
Фармацевтические композиции и составы для местного введения могут включать трансдермальные пластыри, мази, лосьоны, кремы, гели, капли, суппозитории, распыляемые растворы, жидкости и порошки. Могут быть необходимы или желательны традиционные фармацевтические носители, водные, порошкообразные или масляные основы, загустители и т. п. Также могут быть применимы презервативы, перчатки с покрытием и т. п. Подходящие составы для местного введения включают составы, в которых iRNA, представленные в настоящем изобретении, находятся в смеси со средством для местной доставки, таким как липиды, липосомы, жирные кислоты, сложные эфиры жирных кислот, стероиды, хелатирующие средства и поверхностно-активные вещества. Подходящие липиды и липосомы включают нейтральные (например, диолеоилфосфатидилэтаноламин DOPE, димиристоилфосфатидилхолин DMPC, дистеароилфосфатидилхолин), отрицательно заряженные (например, димиристоилфосфатидилглицерин DMPG) и катионные (например, диолеоилтетраметиламинопропил DOTAP и диолеоилфосфатидилэтаноламин DOTMA). iRNA, представленные в настоящем изобретении, могут быть инкапсулированы в липосомах или могут образовывать комплексы с ними, в частности, с катионными липосомами. В качестве альтернативы iRNA могут образовывать комплексы с липидами, в частности с катионными липидами. Подходящие жирные кислоты и сложные эфиры включают без ограничения арахидоновую кислоту, олеиновую кислоту, эйкозановую кислоту, лауриновую кислоту, каприловую кислоту, каприновую кислоту, миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, линолевую кислоту, линоленовую кислоту, дикапрат, трикапрат, моноолеин, дилаурин, глицерил-1-монокапрат, 1-додецилазациклогептан-2-он, ацилкарнитин, ацилхолин или сложные C1-20алкильные эфиры (например, изопропилмиристат (IPM)), моноглицерид, диглицерид или их фармацевтически приемлемую соль. Составы для местного введения подробно описаны в патенте США № 6747014, который включен в данный документ посредством ссылки.
A. Составы на основе iRNA, содержащие мембранные молекулярные ансамбли
iRNA для применения в композициях и способах по настоящему изобретению могут быть составлены для доставки в мембранном молекулярном ансамбле, например, в липосоме или мицелле. Используемый в данном документе термин "липосома" относится к везикуле, состоящей из амфифильных липидов, расположенных в виде по меньшей мере одного бислоя, например, одного бислоя или множества бислоев. Липосомы включают однослойные и многослойные везикулы, которые имеют мембрану, образованную из липофильного материала, и водную внутреннюю среду. Водная часть содержит композицию на основе iRNA. Липофильный материал отделяет водную внутреннюю среду от водной внешней среды, которая, как правило, не включает композицию на основе iRNA, хотя в некоторых примерах может включать. Липосомы применимы для переноса и доставки активных ингредиентов к участку их действия. Благодаря тому, что мембрана липосомы структурно подобна биологическим мембранам, в случае введения липосом в ткань бислой липосомы сливается с бислоем клеточных мембран. По мере того как происходит слияние липосомы и клетки внутреннее водное содержимое, которое включает iRNA, доставляется в клетку, где iRNA может специфически связываться с целевой РНК и может опосредовать RNAi. В некоторых случаях липосомы также являются специфически нацеленными, например, для направления iRNA в конкретные типы клеток.
Липосому, содержащую средство для RNAi, можно получить с помощью ряда способов. В одном примере липидный компонент липосомы растворяют в детергенте для образования таким образом мицелл из липидного компонента. Например, липидный компонент может представлять собой амфипатический катионный липид или липидный конъюгат. Детергент может характеризоваться высокой критической концентрацией мицеллообразования и может быть неионогенным. Иллюстративные детергенты включают холат, CHAPS, октилглюкозид, дезоксихолат и лауроилсаркозин. Препарат средства для RNAi затем добавляют к мицеллам, которые включают липидный компонент. Катионные группы липида взаимодействуют со средством для RNAi и конденсируются вокруг средства для RNAi с образованием липосомы. После конденсации детергент удаляют, например, с помощью диализа, с получением липосомного препарата средства для RNAi.
При необходимости соединение-носитель, которое содействует конденсации, можно добавлять в ходе реакции конденсации, например, путем контролируемого добавления. Например, соединение-носитель может быть полимером, отличным от нуклеиновой кислоты (например, спермином или спермидином). Также можно корректировать pH для содействия конденсации.
Способы получения стабильных средств для доставки полинуклеотидов, которые включают комплекс полинуклеотида/катионного липида в качестве структурных компонентов средств для доставки, дополнительно описаны, например, в WO 96/37194, полное содержание которой включено в данный документ посредством ссылки. Образование липосом может также включать один или несколько аспектов иллюстративных способов, описанных в Felgner, P. L. et al., Proc. Natl. Acad. Sci., USA 8:7413-7417, 1987; в патенте США № 4897355; патенте США № 5171678; Bangham, et al. M. Mol. Biol. 23:238, 1965; Olson, et al. Biochim. Biophys. Acta 557:9, 1979; Szoka, et al. Proc. Natl. Acad. Sci. 75: 4194, 1978; Mayhew, et al. Biochim. Biophys. Acta 775: 169, 1984; Kim, et al. Biochim. Biophys. Acta 728:339, 1983; и Fukunaga, et al. Endocrinol. 115:757, 1984. Широко применяемые методики получения липидных агрегатов с размером, соответствующим для использования в качестве средств для доставки, включают обработку ультразвуком и замораживание-оттаивание с экструзией (см., например, Mayer, et al. Biochim. Biophys. Acta 858:161, 1986). Микрофлюидизацию можно использовать в тех случаях, когда требуются стабильно малые (от 50 до 200 нм) и относительно однородные агрегаты (Mayhew, et al. Biochim. Biophys. Acta 775:169, 1984). Такие способы легко адаптировать для упаковки препаратов на основе средства для RNAi в липосомы.
Липосомы делятся на два больших класса. Катионные липосомы представляют собой положительно заряженные липосомы, которые взаимодействуют с отрицательно заряженными молекулами нуклеиновых кислот с образованием стабильного комплекса. Положительно заряженный комплекс нуклеиновой кислоты/липосомы связывается с отрицательно заряженной клеточной поверхностью и интернализируется в эндосому. Вследствие того что внутри эндосомы кислый pH, липосомы разрываются, высвобождая их содержимое в цитоплазму клетки (Wang et al., Biochem. Biophys. Res. Commun., 1987, 147, 980-985).
Липосомы, которые являются чувствительными к pH или отрицательно заряженными, захватывают нуклеиновые кислоты вместо образования комплекса с ними. Поскольку и нуклеиновая кислота, и липид имеют одинаковый заряд, то вместо образования комплекса происходит отталкивание. Тем не менее, некоторая часть нуклеиновых кислот захватывается водной внутренней средой этих липосом. Чувствительные к pH липосомы использовали для доставки нуклеиновых кислот, кодирующих ген тимидинкиназы, в монослои клеток в культуре. Экспрессию экзогенного гена выявляли в целевых клетках (Zhou et al., Journal of Controlled Release, 1992, 19, 269-274).
Один из основных типов липосомных композиций включает фосфолипиды, отличные от фосфатидилхолина природного происхождения. Композиции для нейтральных липосом, например, могут быть образованы из димиристоилфосфатидилхолина (DMPC) или дипальмитоилфосфатидилхолина (DPPC). Композиции для анионных липосом, как правило, образованы из димиристоилфосфатидилглицерина, тогда как анионные фузогенные липосомы образованы преимущественно из диолеоилфосфатидилэтаноламина (DOPE). Другой тип липосомных композиций образован из фосфатидилхолина (PC), такого как, например, PC соевых бобов и PC яиц. Другой тип образован из смесей фосфолипида, и/или фосфатидилхолина, и/или холестерина.
Примеры других способов введения липосом в клетки in vitro и in vivo включают патент США № 5283185; патент США № 5171678; WO 94/00569; WO 93/24640; WO 91/16024; Felgner, J. Biol. Chem. 269:2550, 1994; Nabel, Proc. Natl. Acad. Sci. 90:11307, 1993; Nabel, Human Gene Ther. 3:649, 1992; Gershon, Biochem. 32:7143, 1993; и Strauss EMBO J. 11:417, 1992.
Также исследовали неионогенные липосомные системы для определения их пригодности в доставке лекарственных средств в кожу, в частности системы, содержащие неионогенное поверхностно-активное вещество и холестерин. Неионогенные липосомные составы, содержащие Novasome™ I (глицерилдилаурат/холестерин/полиоксиэтилен-10-стеариловый эфир) и Novasome™ II (глицерилдистеарат/холестерин/полиоксиэтилен-10-стеариловый эфир), использовали для доставки циклоспорина-A в слой дермы кожи мышей. Результаты показали, что такие неионогенные липосомные системы были эффективны в обеспечении отложения циклоспорина A в различных слоях кожи (Hu et al. S.T.P.Pharma. Sci., 1994, 4(6) 466).
Липосомы также включают "пространственно стабилизированные" липосомы, причем термин, используемый в данном документе, относится к липосомам, содержащим один или несколько специализированных липидов, которые при включении в липосомы приводят к продлению времени пребывания в кровотоке по сравнению с липосомами, у которых отсутствуют такие специализированные липиды. Примерами пространственно стабилизированных липосом являются липосомы, в которых часть образующей везикулу липидной составляющей липосомы (A) содержит один или несколько гликолипидов, таких как моносиалоганглиозид GM1, или (B) получена из одного или нескольких гидрофильных полимеров, таких как полиэтиленгликолевый (PEG) фрагмент. Не желая ограничиваться какой-либо конкретной теорией, в данной области предполагают, что по меньшей мере для пространственно стабилизированных липосом, содержащих ганглиозиды, сфингомиелин или PEG-производные липиды, увеличенное время полужизни в кровотоке этих пространственно стабилизированных липосом является следствием сниженной степени захвата клетками ретикулоэндотелиальной системы (RES) (Allen et al., FEBS Letters, 1987, 223, 42; Wu et al., Cancer Research, 1993, 53, 3765).
В данной области известны различные липосомы, содержащие один или несколько гликолипидов. Papahadjopoulos et al. (Ann. N.Y. Acad. Sci., 1987, 507, 64) описали способность моносиалоганглиозида GM1, сульфата галактоцереброзида и фосфатидилинозитола увеличивать время полужизни липосом в крови. Эти результаты были интерпретированы Gabizon et al. (Proc. Natl. Acad. Sci. U.S.A., 1988, 85, 6949). В патенте США № 4837028 и патентном документе WO 88/04924, оба из которых принадлежат Allen et al., раскрыты липосомы, содержащие (1) сфингомиелин и (2) ганглиозид GM1 или сульфатный сложный эфир галактоцереброзида. В патенте США № 5543152 (Webb et al.) раскрыты липосомы, содержащие сфингомиелин. Липосомы, содержащие 1,2-sn-димиристоилфосфатидилхолин, раскрыты в WO 97/13499 (Lim et al.).
В одном варианте осуществления применяют катионные липосомы. Преимущество катионных липосом заключается в том, что они способны сливаться с клеточной мембраной. Некатионные липосомы, хотя и не могут сливаться настолько эффективно с плазматической мембраной, поглощаются макрофагами in vivo, и их можно использовать для доставки средств для RNAi к макрофагам.
Дополнительные преимущества липосом включают следующие: липосомы, полученные из природных фосфолипидов, биосовместимы и биоразрушаемы; липосомы могут включать широкий диапазон водо- и жирорастворимых лекарственных средств; липосомы могут защищать инкапсулированные в их внутренних отделениях средства для RNAi от метаболизма и разрушения (Rosoff в "Pharmaceutical Dosage Forms," Lieberman, Rieger and Banker (Eds.), 1988, volume 1, p. 245). Важными факторами, которые необходимо учитывать при получении липосомных составов, являются поверхностный заряд липида, размер везикулы и водный объем липосом.
Положительно заряженный синтетический катионный липид, хлорид N-[1-(2,3-диолеилокси)пропил]-N,N,N-триметиламмония (DOTMA), можно использовать для образования малых липосом, которые самопроизвольно взаимодействуют с нуклеиновой кислотой с образованием комплексов липид-нуклеиновая кислота, которые способны сливаться с отрицательно заряженными липидами клеточных мембран клеток культуры тканей, что приводит к доставке средства для RNAi (см., например, Felgner, P. L. et al., Proc. Natl. Acad. Sci., USA 8:7413-7417, 1987; и патент США № 4897355 касательно описания DOTMA и его применения с ДНК).
Аналог DOTMA, 1,2-бис(олеоилокси)-3-(триметиламмоний)пропан (DOTAP), можно применять в комбинации с фосфолипидом с образованием везикул, образующих комплекс с ДНК. Lipofectin™ (Bethesda Research Laboratories, Гейтерсберг, Мэриленд) представляет собой эффективное средство для доставки высокоанионных нуклеиновых кислот в живые клетки культуры тканей, что содержит положительно заряженные DOTMA-липосомы, которые самопроизвольно взаимодействуют с отрицательно заряженными полинуклеотидами с образованием комплексов. Суммарный заряд полученных комплексов является также положительным в тех случаях, когда используют липосомы с достаточным положительным зарядом. Положительно заряженные комплексы, полученные таким способом, самопроизвольно присоединяются к отрицательно заряженным клеточным поверхностям, сливаются с плазматической мембраной и эффективно доставляют функциональные нуклеиновые кислоты, например, в клетки культуры тканей. Другой коммерчески доступный катионный липид, 1,2-бис(олеоилокси)-3,3-(триметиламмоний)пропан ("DOTAP") (Boehringer Mannheim, Индианаполис, Индиана), отличается от DOTMA тем, что олеоиловые фрагменты связаны сложноэфирными, а не простыми эфирными связями.
Другие описанные соединения на основе катионного липида включают такие соединения, которые были конъюгированы с рядом фрагментов, в том числе, например, карбоксиспермин, который был конъюгирован с одним из двух типов липидов и включает такие соединения, как 5-карбоксиспермилглициндиоктаолеоиламид ("DOGS") (Transfectam™, Promega, Мэдисон, Висконсин) и дипальмитоилфосфатидилэтаноламина 5-карбоксиспермил-амид ("DPPES") (см., например, патент США № 5171678).
Другой конъюгат на основе катионного липида предусматривает получение производных липида с помощью холестерина ("DC-Chol"), которые были составлены в виде липосом в комбинации с DOPE (см., Gao, X. and Huang, L., Biochim. Biophys. Res. Commun. 179:280, 1991). Как сообщалось, липополилизин, полученный путем конъюгации полилизина с DOPE, является эффективным для трансфекции в присутствии сыворотки крови (Zhou, X. et al., Biochim. Biophys. Acta 1065:8, 1991). Есть сведения, что в случае определенных клеточных линий такие липосомы, содержащие конъюгированные катионные липиды, характеризуются более низкой токсичностью и обеспечивают более эффективную трансфекцию, чем DOTMA-содержащие композиции. Другие коммерчески доступные продукты на основе катионных липидов включают DMRIE и DMRIE-HP (Vical, Ла-Хойя, Калифорния) и Lipofectamine (DOSPA) (Life Technology, Inc., Гейтерсберг, Мэриленд). Другие катионные липиды, подходящие для доставки олигонуклеотидов, описаны в WO 98/39359 и WO 96/37194.
Липосомные составы особенно подходят для местного введения, при этом липосомы обладают некоторыми преимуществами по сравнению с другими составами. Такие преимущества включают уменьшение побочных действий, связанных с высокой системной абсорбции введенного лекарственного средства, повышенное накопление введенного лекарственного средства в необходимой мишени и возможность введения средства для RNAi в кожу. В некоторых вариантах осуществления липосомы используют для доставки средства для RNAi к эпидермальным клеткам, а также для усиления проникновения средства для RNAi в дермальные ткани, например в кожу. Например, липосомы можно вводить местно. Документально оформлена местная доставка лекарственных средств, составленных в виде липосом, в кожу (см., например, Weiner et al., et al., Journal of Drug Targeting, 1992, vol. 2,405-410 и du Plessis et al., Antiviral Research, 18, 1992, 259-265; Mannino, R. J. and Fould-Fogerite, S., Biotechniques 6:682-690, 1988; Itani, T. et al. Gene 56:267-276. 1987; Nicolau, C. et al. Meth. Enz. 149:157-176, 1987; Straubinger, R. M. and Papahadjopoulos, D. Meth. Enz. 101:512-527, 1983; Wang, C. Y. and Huang, L., Proc. Natl. Acad. Sci. USA 84:7851-7855, 1987).
Также исследовали неионогенные липосомные системы для определения их пригодности в доставке лекарственных средств в кожу, в частности системы, содержащие неионогенное поверхностно-активное вещество и холестерин. Для доставки лекарственного средства в дерму кожи мышей использовали неионогенные липосомные составы, содержащие Novasome I (глицерилдилаурат/холестерин/полиоксиэтилен-10-стеариловый эфир) и Novasome II (глицерилдистеарат/холестерин/полиоксиэтилен-10-стеариловый эфир). Такие составы со средством для RNAi пригодны для лечения дерматологического нарушения.
Липосомы, которые включают siRNA, могут быть получены сильно деформируемыми. Такая способность к деформации может позволить липосомам проникать через пору, которая меньше среднего радиуса липосомы. Например, типом деформируемых липосом являются трансферосомы. Трансферосомы можно получать путем добавления поверхностных пограничных активаторов, обычно поверхностно-активных веществ, в стандартную липосомную композицию. Трансферосомы, которые включают средство для RNAi, можно доставлять, например, подкожно путем инъекции для доставки средства для RNAi к кератиноцитам в коже. Для того, чтобы пройти сквозь неповрежденную кожу млекопитающего, липидные везикулы должны проникнуть через ряд мелких пор, каждая из которых имеет диаметр менее 50 нм, под воздействием подходящего трансдермального градиента. Кроме того, благодаря свойствам липидов, такие трансферосомы могут быть самооптимизирующимися (приспосабливаемыми к форме пор, например, в коже), самовосстанавливающимися, причем зачастую могут достигать своих мишеней без разделения на фрагменты, и часто могут быть самозагружающимися.
Другие составы, пригодные в настоящем изобретении, описаны в предварительных заявках США с порядковыми №№ 61/018616, поданной 2 января 2008 г.; 61/018611, поданной 2 января 2008 г.; 61/039748, поданной 26 марта 2008 г.; 61/047087, поданной 22 апреля 2008 г., и 61/051528, поданной 8 мая 2008 г. В заявке согласно PCT с № PCT/US2007/080331, поданной 3 октября 2007 г., также описаны составы, пригодные в настоящем изобретении.
Трансферосомы представляют собой еще один тип липосом и являются сильно деформируемыми липидными агрегатами, которые являются перспективными кандидатами как средства для доставки лекарственных средств Трансферосомы могут быть описаны как липидные капельки, которые являются настолько сильно деформируемыми, что они легко могут проникать через поры, меньшие, чем капельки. Трансферосомы являются приспосабливаемыми к окружающей среде, в которой их используют, например, они являются самооптимизирующимися (приспосабливаемыми к форме пор кожи), самовосстанавливающимися, зачастую достигают своих мишеней без разделения на фрагменты и часто могут быть самозагружающимися. Для получения трансферосом можно добавлять поверхностные пограничные активаторы, обычно поверхностно-активные вещества, в стандартную липосомную композицию. Трансферосомы применяли для доставки сывороточного альбумина в кожу. Как было показано, опосредованная трансферосомами доставка сывороточного альбумина была такой же эффективной, как подкожная инъекция раствора, содержащего сывороточный альбумин.
Поверхностно-активные вещества находят широкое применение в составах, таких как эмульсии (в том числе микроэмульсии) и липосомы. Наиболее распространенным способом классифицирования и ранжирования свойств многих различных типов поверхностно-активных веществ, как природных, так и синтетических, является применение гидрофильно-липофильного баланса (HLB). Природа гидрофильной группы (также известной как "головка") предоставляет наиболее эффективные средства для распределения по категориям различных поверхностно-активных веществ, применяемых в составах (Rieger, в Pharmaceutical Dosage Forms, Marcel Dekker, Inc., New York, N.Y., 1988, p. 285).
Если молекула поверхностно-активного вещества не ионизирована, то ее классифицируют как неионогенное поверхностно-активное вещество. Неионогенные поверхностно-активные вещества находят широкое применение в фармацевтических и косметических продуктах, и их применяют в широком диапазоне значений pH. В целом их значения HLB находятся в диапазоне от 2 до приблизительно 18 в зависимости от их структуры. Неионогенные поверхностно-активные вещества включают неионогенные сложные эфиры, такие как сложные эфиры этиленгликоля, сложные эфиры пропиленгликоля, сложные глицериловые эфиры, сложные полиглицериловые эфиры, сложные эфиры сорбитана, сложные эфиры сахарозы и этоксилированные сложные эфиры. Также в данный класс включены неионогенные алканоламиды и простые эфиры, как например, этоксилаты жирных спиртов, пропоксилированные спирты и этоксилированные/пропоксилированные блок-сополимеры. Полиоксиэтиленовые поверхностно-активные вещества являются наиболее распространенными представителями класса неионогенных поверхностно-активных веществ.
Если молекула поверхностно-активного вещества несет отрицательный заряд при растворении или диспергировании в воде, то поверхностно-активное вещество классифицируют как анионное. Анионные поверхностно-активные вещества включают карбоксилаты, как например, омыляющие вещества, ациллактилаты, ациламиды аминокислот, сложные эфиры серной кислоты, такие как алкилсульфаты и этоксилированные алкилсульфаты, сульфонаты, такие как алкилбензолсульфонаты, ацилизетионаты, ацилтаураты и сульфосукцинаты, и фосфаты. Наиболее важными представителями класса анионных поверхностно-активных веществ являются алкилсульфаты и омыляющие вещества.
Если молекула поверхностно-активного вещества несет положительный заряд при растворении или диспергировании в воде, то поверхностно-активное вещество классифицируют как катионное. Катионные поверхностно-активные вещества включают соли четвертичного аммония и этоксилированные амины. Соли четвертичного аммония являются наиболее используемыми представителями данного класса.
Если молекула поверхностно-активного вещества обладает способностью нести и положительный, и отрицательный заряд, то поверхностно-активное вещество классифицируют как амфотерное. Амфотерные поверхностно-активные вещества включают производные акриловой кислоты, замещенные алкиламиды, N-алкилбетаины и фосфатиды.
Было рассмотрено применение поверхностно-активных веществ в готовых лекарственных формах, составах и в эмульсиях (Rieger, в Pharmaceutical Dosage Forms, Marcel Dekker, Inc., New York, N.Y., 1988, p. 285).
Для применения в способах по настоящему изобретению iRNA может также предусматриваться в виде мицеллярных составов. "Мицеллы" в данном документе определены как конкретный тип молекулярной сборки, в которой амфипатические молекулы расположены в виде сферической структуры, так что все гидрофобные части молекул направлены вовнутрь, оставляя гидрофильные части в контакте с окружающей водной фазой. Противоположное расположение имеет место, если окружающая среда гидрофобная.
Смешанный мицеллярный состав, подходящий для доставки через трансдермальные мембраны, может быть получен путем смешивания водного раствора композиции на основе siRNA, C8-C22алкилсульфата щелочного металла и мицеллообразующих соединений. Иллюстративные мицеллообразующие соединения включают лецитин, гиалуроновую кислоту, фармацевтически приемлемые соли гиалуроновой кислоты, гликолевую кислоту, молочную кислоту, экстракт ромашки, экстракт огурца, олеиновую кислоту, линолевую кислоту, линоленовую кислоту, моноолеин, моноолеаты, монолаураты, масло бурачника, масло первоцвета вечернего, ментол, тригидроксиоксохоланил-глицин и его фармацевтически приемлемые соли, глицерин, полиглицерин, лизин, полилизин, триолеин, простые эфиры полиоксиэтилена и их аналоги, простые полидоканол-алкильные эфиры и их аналоги, хенодезоксихолат, дезоксихолат и их смеси. Мицеллообразующие соединения можно добавлять одновременно или после добавления алкилсульфата щелочного металла. Смешанные мицеллы будут образовываться практически при любом типе смешивания ингредиентов, но для получения мицелл с меньшим размером требуется интенсивное перемешивание.
В одном способе получают первую мицеллярную композицию, которая содержит композицию на основе siRNA и по меньшей мере алкилсульфат щелочного металла. Первую мицеллярную композицию затем смешивают по меньшей мере с тремя мицеллообразующими соединениями с образованием смешанной мицеллярной композиции. В другом способе мицеллярную композицию получают путем смешивания композиции на основе siRNA, алкилсульфата щелочного металла и по меньшей мере одного из мицеллообразующих соединений с последующим добавлением оставшихся мицеллообразующих соединений при интенсивном перемешивании.
Фенол и/или м-крезол можно добавлять к смешанной мицеллярной композиции для стабилизации состава и защиты от роста бактерий. В качестве альтернативы фенол и/или м-крезол можно добавлять с мицеллообразующими ингредиентами. Изотоническое средство, такое как глицерин, также можно добавлять после образования смешанной мицеллярной композиции.
Для доставки мицеллярного состава в виде распыляемого раствора состав можно поместить в аэрозольный распылитель и распылитель зарядить газом-вытеснителем. Газ-вытеснитель, который пребывает под давлением, находится в жидкой форме в распылителе. Соотношения ингредиентов корректируют так, что водная фаза и фаза газа-вытеснителя становятся единым целым, т.е. присутствует одна фаза. Если присутствуют две фазы, то необходимо встряхнуть распылитель перед распылением порции содержимого, например, через дозирующий клапан. Распыляемая доза фармацевтического средства вытесняется из дозирующего клапана в виде мелкодисперсного распыляемого раствора.
Газы-вытеснители могут включать водородсодержащие хлорфторуглероды, водородсодержащие фторуглероды, простой диметиловый эфир и простой диэтиловый эфир. В определенных вариантах осуществления можно применять HFA 134a (1,1,1,2-тетрафторэтан).
Конкретные концентрации основных ингредиентов могут быть определены путем проведения относительно простых экспериментов. Для абсорбции через ротовую полость часто требуется увеличить, например по меньшей мере удвоить или утроить, дозу, предназначенную для инъекции или введения через желудочно-кишечный тракт.
B. Липидные частицы
iRNA, например dsRNA, по настоящему изобретению могут быть полностью инкапсулированы в липидном составе, например, в LNP или другой частице на основе нуклеиновой кислоты-липида.
Используемый в данном документе термин "LNP" относится к стабильной частице на основе нуклеиновой кислоты-липида. LNP содержат катионный липид, некатионный липид и липид, который предупреждает агрегацию частиц (например, конъюгат PEG-липид). LNP в высшей степени пригодны для системных применений, поскольку они характеризуются длительным временем пребывания в кровотоке после внутривенной (i.v.) инъекции и накапливаются в дистальных участках (например, участках, физически отделенных от участка введения). LNP включают "pSPLP", которая включает инкапсулированный комплекс конденсирующее средство-нуклеиновая кислота, приведенный в PCT публикации № WO 00/03683. Частицы по настоящему изобретению обычно имеют средний диаметр, составляющий от приблизительно 50 нм до приблизительно 150 нм, чаще от приблизительно 60 нм до приблизительно 130 нм, чаще от приблизительно 70 нм до приблизительно 110 нм, наиболее часто от приблизительно 70 нм до приблизительно 90 нм, и они являются практически нетоксичными. Кроме того, если нуклеиновые кислоты присутствуют в частицах на основе нуклеиновой кислоты-липида по настоящему изобретению, то в водном растворе они устойчивы к разрушению нуклеазой. Частицы на основе нуклеиновой кислоты-липида и способ их получения раскрыты, например, в патентах США №№ 5976567; 5981501; 6534484; 6586410; 6815432; публикации США № 2010/0324120 и публикации согласно PCT № WO 96/40964.
В одном варианте осуществления соотношение липида и лекарственного средства (соотношение масса/масса) (например, соотношение липида и dsRNA) будет находиться в диапазоне от приблизительно 1:1 до приблизительно 50:1, от приблизительно 1:1 до приблизительно 25:1, от приблизительно 3:1 до приблизительно 15:1, от приблизительно 4:1 до приблизительно 10:1, от приблизительно 5:1 до приблизительно 9:1 или от приблизительно 6:1 до приблизительно 9:1. Диапазоны, промежуточные по отношению к перечисленным выше диапазонам, также рассматриваются как часть настоящего изобретения.
Катионный липид может представлять собой, например, хлорид N,N-диолеил-N,N-диметиламмония (DODAC), бромид N,N-дистеарил-N,N-диметиламмония (DDAB), хлорид N-(I-(2,3-диолеоилокси)пропил)-N,N,N-триметиламмония (DOTAP), хлорид N-(I-(2,3-диолеилокси)пропил)-N,N,N-триметиламмония (DOTMA), N,N-диметил-2,3-диолеилокси)пропиламин (DODMA), 1,2-дилинолеилокси-N,N-диметиламинопропан (DLinDMA), 1,2-дилиноленилокси-N,N-диметиламинопропан (DLenDMA), 1,2-дилинолеилкарбамоилокси-3-диметиламинопропан (DLin-C-DAP), 1,2-дилинолеилокси-3-(диметиламино)ацетоксипропан (DLin-DAC), 1,2-дилинолеилокси-3-морфолинопропан (DLin-MA), 1,2-дилинолеоил-3-диметиламинопропан (DLinDAP), 1,2-дилинолеилтио-3-диметиламинопропан (DLin-S-DMA), 1-линолеоил-2-линолеилокси-3-диметиламинопропан (DLin-2-DMAP), хлористую соль 1,2-дилинолеилокси-3-триметиламинопропана (DLin-TMA.Cl), хлористую соль 1,2-дилинолеоил-3-триметиламинопропана (DLin-TAP.Cl), 1,2-дилинолеилокси-3-(N-метилпиперазино)пропан (DLin-MPZ) или 3-(N,N-дилинолеиламино)-1,2-пропандиол (DLinAP), 3-(N,N-диолеиламино)-1,2-пропандиол (DOAP), 1,2-дилинолеилоксо-3-(2-N,N-диметиламино)этоксипропан (DLin-EG-DMA), l,2-дилиноленилокси-N,N-диметиламинопропан (DLinDMA), 2,2-дилинолеил-4-диметиламинометил-[1,3]-диоксолан (DLin-K-DMA) или его аналоги, (3aR,5s,6aS)-N,N-диметил-2,2-ди((9Z,12Z)-октадека-9,12-диенил)тетрагидро-3aH-циклопента[d][1,3]диоксол-5-амин (ALN100), (6Z,9Z,28Z,31Z)-гептатриаконта-6,9,28,31-тетраен-19-ил-4-(диметиламино)бутаноат (MC3), 1,1'-(2-(4-(2-((2-(бис(2-гидроксидодецил)амино)этил)(2-гидроксидодецил)амино)этил)пиперазин-1-ил)этилазанедиил)дидодекан-2-ол (Tech G1) или их смесь. Катионный липид может содержать от приблизительно 20 мол. % до приблизительно 50 мол. % или приблизительно 40 мол. % от общего содержания липидов, присутствующих в частице.
В другом варианте осуществления можно использовать соединение 2,2-дилинолеил-4-диметиламиноэтил-[1,3]-диоксолан для получения наночастиц на основе липида-siRNA. Синтез 2,2-дилинолеил-4-диметиламиноэтил-[1,3]-диоксолана описан в предварительной заявке на патент США номер 61/107998, поданной 23 октября 2008 г., которая включена в данный документ посредством ссылки.
В одном варианте осуществления частица на основе липида-siRNA включает 40% 2,2-дилинолеил-4-диметиламиноэтил-[1,3]-диоксолана: 10% DSPC: 40% холестерина: 10% PEG-C-DOMG (мольный процент), причем размер частиц составляет 63,0 ± 20 нм, и соотношение siRNA/липид составляет 0,027.
Ионизируемый/некатионный липид может представлять собой анионный липид или нейтральный липид, в том числе без ограничения дистеароилфосфатидилхолин (DSPC), диолеоилфосфатидилхолин (DOPC), дипальмитоилфосфатидилхолин (DPPC), диолеоилфосфатидилглицерин (DOPG), дипальмитоилфосфатидилглицерин (DPPG), диолеоил-фосфатидилэтаноламин (DOPE), пальмитоилолеоилфосфатидилхолин (POPC), пальмитоилолеоилфосфатидилэтаноламин (POPE), диолеоил-фосфатидилэтаноламин-4-(N-малеимидометил)-циклогексан-1-карбоксилат (DOPE-mal), дипальмитоилфосфатидилэтаноламин (DPPE), димиристоилфосфоэтаноламин (DMPE), дистеароил-фосфатидил-этаноламин (DSPE), 16-O-монометил-PE, 16-O-диметил-PE, 18-1-транс-PE, 1-стеароил-2-олеоил-фосфатидилэтаноламин (SOPE), холестерин или их смесь. Cодержание некатионного липида может составлять от приблизительно 5 мол. % до приблизительно 90 мол. %, приблизительно 10 мол. % или приблизительно 58 мол. %, если холестерин включен, от общего содержания липидов, присутствующих в частице.
Конъюгированный липид, который препятствует агрегации частиц, может представлять собой, например, конъюгат полиэтиленгликоль (PEG)-липид, в том числе без ограничения PEG-диацилглицерин (DAG), PEG-диалкилоксипропил (DAA), PEG-фосфолипид, PEG-церамид (Cer) или их смесь. Конъюгат PEG-DAA может представлять собой, например, PEG-дилаурилоксипропил (Ci2), PEG-димиристилоксипропил (Ci4), PEG-дипальмитилоксипропил (Ci6) или PEG-дистеарилоксипропил (Ci8). Содержание конъюгированного липида, который предупреждает агрегацию частиц, может составлять от 0 мол. % до приблизительно 20 мол. % или приблизительно 2 мол. % от общего содержания липидов, присутствующих в частице.
В некоторых вариантах осуществления частица на основе нуклеиновой кислоты-липида дополнительно включает холестерин в количестве, составляющем, например, от приблизительно 10 мол. % до приблизительно 60 мол. % или приблизительно 48 мол. % от общего содержания липидов, присутствующих в частице.
В одном варианте осуществления липидоид ND98⋅4HCl (MW 1487) (см. заявку на патент США № 12/056230, поданную 26 марта 2008 г., которая включена в данный документ посредством ссылки), холестерин (Sigma-Aldrich) и PEG-церамид C16 (Avanti Polar Lipids) можно использовать для получения наночастиц на основе липида-dsRNA (т е. частиц LNP01). Маточные растворы каждого в этаноле могут быть получены следующим образом: ND98, 133 мг/мл; холестерин, 25 мг/мл, PEG-церамид C16, 100 мг/мл. Маточные растворы ND98, холестерина и PEG-церамида C16 можно затем объединять, например, при молярном соотношении 42:48:10. Объединенный липидный раствор можно смешивать с водным раствором dsRNA (например, в ацетате натрия, pH 5) так, чтобы конечная концентрация этанола составляла приблизительно 35-45%, а конечная концентрация ацетата натрия составляла приблизительно 100-300 мМ. Наночастицы на основе липида-dsRNA обычно образуются самопроизвольно при смешивании. В зависимости от необходимого распределения частиц по размеру полученную смесь наночастиц можно продавливать через поликарбонатную мембрану (например, с отсечением по размеру в 100 нм) с использованием, например, экструдера с термоцилиндром, как например Lipex Extruder (Northern Lipids, Inc). В некоторых случаях стадию экструзии можно пропустить. Удаление этанола и одновременная замена буфера могут быть осуществлены, например, с помощью диализа или тангенциальной поточной фильтрации. Буфер можно заменить, например, фосфатно-солевым буферным раствором (PBS) со значением pH, составляющим приблизительно 7, например, pH, составляющим приблизительно 6,9, pH, составляющим приблизительно 7,0, pH, составляющим приблизительно 7,1, pH, составляющим приблизительно 7,2, pH, составляющим приблизительно 7,3, или pH, составляющим приблизительно 7,4.
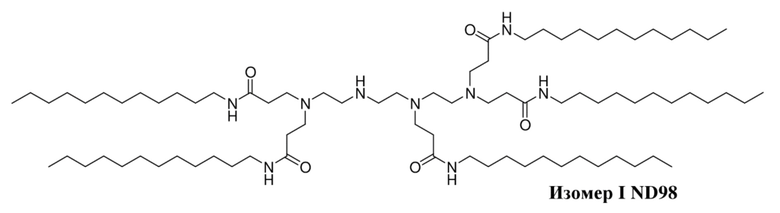
Формула 1
Составы LNP01 описаны, например, в публикации международной заявки № WO 2008/042973, которая включена в данный документ посредством ссылки.
Дополнительные иллюстративные составы на основе липида-dsRNA описаны в таблице A.
Таблица А
Соотношение липид:siRNA
(57,1/7,1/34,4/1,4)
Липид:siRNA ~ 7:1
57,1/7,1/34,4/1,4
Липид:siRNA ~ 7:1
57,5/7,5/31,5/3,5
Липид:siRNA ~ 6:1
57,5/7,5/31,5/3,5
Липид:siRNA ~ 11:1
60/7,5/31/1,5
Липид:siRNA ~ 6:1
60/7,5/31/1,5
Липид:siRNA ~ 11:1
50/10/38,5/1,5
Липид:siRNA 10:1
50/10/38,5/1,5
Липид:siRNA 10:1
50/10/38,5/1,5
Липид:siRNA 10:1
50/10/38,5/1,5
Липид:siRNA 10:1
50/10/38,5/1,5
Липид:siRNA: 33:1
40/15/40/5
Липид:siRNA: 11:1
50/10/35/4,5/0,5
Липид:siRNA: 11:1
50/10/38,5/1,5
Липид:siRNA: 7:1
50/10/38,5/1,5
Липид:siRNA: 10:1
50/10/38,5/1,5
Липид:siRNA: 12:1
50/10/35/5
Липид:siRNA: 8:1
50/10/38,5/1,5
Липид:siRNA: 10:1
50/10/38,5/1,5
Липид:siRNA: 7:1
50/10/38,5/1,5
Липид:siRNA: 10:1
DSPC: дистеароилфосфатидилхолин;
DPPC: дипальмитоилфосфатидилхолин;
PEG-DMG: PEG-дидимиристоилглицерин (C14-PEG или PEG-C14) (PEG со средн. мол. массой 2000);
PEG-DSG: PEG-дистирилглицерин (C18-PEG или PEG-C18) (PEG со средн. мол. массой 2000);
PEG-cDMA: PEG-карбамоил-1,2-димиристоилоксипропиламин (PEG со средн. мол. массой 2000).
Составы, содержащие LNP (1,2-дилиноленилокси-N,N-диметиламинопропан (DLinDMA)), описаны в публикации международной заявки № WO2009/127060, поданной 15 апреля 2009 г., которая включена в данный документ посредством ссылки.
Составы, содержащие XTC, описаны, например, в предварительной заявке США с порядковым № 61/148366, поданной 29 января 2009 г.; предварительной заявке США с порядковым № 61/156851, поданной 2 марта 2009 г.; предварительной заявке США с порядковым № , поданной 10 июня 2009 г.; предварительной заявке США с порядковым № 61/228373, поданной 24 июля 2009 г.; предварительной заявке США с порядковым № 61/239686, поданной 3 сентября 2009 г., и международной заявке № PCT/US2010/022614, поданной 29 января 2010 г., которые включены в данный документ посредством ссылки.
Составы, содержащие MC3, описаны, например, в публикации США № 2010/0324120, поданной 10 июня 2010 г., полное содержание которой включено в данный документ посредством ссылки.
Составы, содержащие ALNY-100, описаны, например, в международной заявке на патент с номером PCT/US09/63933, поданной 10 ноября 2009 г., которая включена в данный документ посредством ссылки.
Составы, содержащие C12-200, описаны в предварительной заявке США с порядковым № 61/175770, поданной 5 мая 2009 г., и международной заявке № PCT/US10/33777, поданной 5 мая 2010 г., которые включены в данный документ посредством ссылки.
Синтез ионизируемых/катионных липидов
Любое из соединений, например, катионные липиды и т.п., используемые в частицах на основе нуклеиновой кислоты-липида согласно настоящему изобретению, можно получить при помощи известных методик органического синтеза, включая способы, описанные более подробно в примерах. Все заместители являются такими, как определено ниже, если не указано иное.
"Алкил" означает углеводород с прямой цепью или разветвленный, нециклический или циклический, насыщенный алифатический углеводород, содержащий от 1 до 24 атомов углерода. Типичные насыщенные алкилы с прямой цепью включают метил, этил, н-пропил, н-бутил, н-пентил, н-гексил и т.п.; тогда как насыщенные разветвленные алкилы включают изопропил, втор-бутил, изобутил, трет-бутил, изопентил и т.п. Типичные насыщенные циклические алкилы включают циклопропил, циклобутил, циклопентил, циклогексил и т.п.; тогда как ненасыщенные циклические алкилы включают циклопентенил и циклогексенил и т.п.
"Алкенил" означает алкил, который определен выше, содержащий по меньшей мере одну двойную связь между соседними атомами углерода. Алкенилы включают как цис-, так и транс-изомеры. Типичные алкенилы с прямой цепью и разветвленные алкенилы включают этиленил, пропиленил, 1-бутенил, 2-бутенил, изобутиленил, 1-пентенил, 2-пентенил, 3-метил-1-бутенил, 2-метил-2-бутенил, 2,3-диметил-2-бутенил и т. п.
"Алкинил" означает любой алкил или алкенил, которые определены выше, дополнительно содержащие по меньшей мере одну тройную связь между соседними атомами углерода. Типичные алкинилы с прямой цепью и разветвленные алкинилы включают ацетиленил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-метил-1-бутинил и т.п.
"Ацил" означает любой алкил, алкенил или алкинил, у которых атом углерода в точке присоединения замещен оксогруппой, которая определена ниже. Например, -C(=O)алкил, -C(=O)алкенил и -C(=O)алкинил представляют собой ацильные группы.
"Гетероцикл" означает 5-7-членное моноциклическое или 7-10-членное бициклическое, гетероциклическое кольцо, которое является либо насыщенным, ненасыщенным, либо ароматическим и которое содержит 1 или 2 гетероатома, независимо выбранных из азота, кислорода и серы, и где гетероатомы азота и серы необязательно могут быть окислены, и гетероатом азота необязательно может быть необязательно кватернизирован, в том числе бициклические кольца, в которых любой из вышеперечисленных гетероциклов слит с бензольным кольцом. Гетероцикл может быть присоединен через любой гетероатом или атом углерода. Гетероциклы включают гетероарилы, которые определены ниже. Гетероциклы включают морфолинил, пирролидинонил, пирролидинил, пиперидинил, пиперизинил, гидантоинил, валеролактамил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, тетрагидропиридинил, тетрагидропиримидинил, тетрагидротиофенил, тетрагидротиопиранил, тетрагидропиримидинил, тетрагидротиофенил, тетрагидротиопиранил и т.п.
Термины "необязательно замещенный алкил", "необязательно замещенный алкенил", "необязательно замещенный алкинил", "необязательно замещенный ацил" и "необязательно замещенный гетероцикл" означают, что при замещении по меньшей мере один атом водорода заменяется заместителем. В случае оксо-заместителя (=O) заменяются два атома водорода. В связи с этим заместители включают оксо, галоген, гетероцикл, -CN, -ORx, -NRxRy, -NRxC(=O)Ry, -NRxSO2Ry, -C(=O)Rx, -C(=O)ORx, -C(=O)NRxRy, -SOnRx и -SOnNRxRy, где n равняется 0, 1 или 2, Rx и Ry являются одинаковыми или различными и независимо представляют собой водород, алкил или гетероцикл, при этом каждый из указанных заместителей алкила и гетероцикла дополнительно может быть замещен одним или несколькими из оксо, галогена, -OH, -CN, алкила, -ORx, гетероцикла, -NRxRy, -NRxC(=O)Ry, -NRxSO2Ry, -C(=O)Rx, -C(=O)ORx, -C(=O)NRxRy, -SOnRx и -SOnNRxRy.
"Галоген" означает фтор, хлор, бром и йод.
В некоторых вариантах осуществления в способах согласно настоящему изобретению может потребоваться использование защитных групп. Методика с использованием защитных групп хорошо известна специалистам в данной области (см., например, Protective Groups in Organic Synthesis, Green, T.W. et al., Wiley-Interscience, New York City, 1999). Вкратце, защитные группы в контексте настоящего изобретения представляют собой любую группу, которая снижает или устраняет нежелательную химическую активность функциональной группы. Защитную группу можно добавлять к функциональной группе для блокирования ее химической активности во время определенных реакций и затем удалять с открытием исходной функциональной группы. В некоторых вариантах осуществления применяют "защитную группу для спиртовой группы". "Защитная группа для спиртовой группы" представляет собой любую группу, которая уменьшает или устраняет нежелательную химическую активность спиртовой функциональной группы. Защитные группы можно добавлять и удалять при помощи методик, хорошо известных из уровня техники.
Композиции и составы для перорального введения включают порошки или гранулы, микрочастицы, наночастицы, суспензии или растворы в воде или неводных средах, капсулы, желатиновые капсулы, пакетики-саше, таблетки или минитаблетки. Могут потребоваться загустители, ароматизирующие вещества, разбавители, эмульгаторы, диспергирующие средства или связующие вещества. В некоторых вариантах осуществления составы для перорального введения являются такими, в которых dsRNA, представленные в настоящем изобретении, вводят в сочетании с одним или несколькими веществами, способствующими проникновению, поверхностно-активными вещества и хелаторами. Подходящие поверхностно-активные вещества включают жирные кислоты и/или их сложные эфиры или соли, желчные кислоты и/или их соли. Подходящие желчные кислоты/соли желчных кислот включают хенодезоксихолевую кислоту (CDCA) и урсодезоксихенодезоксихолевую кислоту (UDCA), холевую кислоту, дегидрохолевую кислоту, дезоксихолевую кислоту, глюкохолевую кислоту, гликохолевую кислоту, гликодезоксихолевую кислоту, таурохолевую кислоту, тауродезоксихолевую кислоту, тауро-24,25-дигидро-фузидат натрия и гликодигидрофузидат натрия. Подходящие жирные кислоты включают арахидоновую кислоту, ундекановую кислоту, олеиновую кислоту, лауриновую кислоту, каприловую кислоту, каприновую кислоту, миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, линолевую кислоту, линоленовую кислоту, дикапрат, трикапрат, моноолеин, дилаурин, глицерил-1-монокапрат, 1-додецилазациклогептан-2-он, ацилкарнитин, ацилхолин или моноглицерид, диглицерид или их фармацевтически приемлемую соль (например, натриевую). В некоторых вариантах осуществления используют комбинации веществ, способствующих проникновению, например, жирные кислоты/соли жирных кислот в комбинации с желчными кислотами/солями желчных кислот. Одной иллюстративной комбинацией является натриевая соль лауриновой кислоты, каприновая кислота и UDCA. Дополнительные вещества, способствующие проникновению, включают простой полиоксиэтилен-9-лауриловый эфир, простой полиоксиэтилен-20-цетиловый эфир. Представленные в настоящем изобретении dsRNA могут доставляться перорально, в форме гранул, в том числе высушенных распылением частиц, или в составе комплексов для образования микро- или наночастиц. Комплексообразующие средства для dsRNA включают полиаминокислоты; полиимины; полиакрилаты; полиалкилакрилаты, полиоксетаны, полиалкилцианоакрилаты; катионизированные виды желатина, альбумины, виды крахмала, акрилаты, полиэтиленгликоли (PEG) и виды крахмала; полиалкилцианоакрилаты; DEAE-производные полиимины, поллуланы, виды целлюлозы и виды крахмала. Подходящие комплексообразующие средства включают хитозан, N-триметилхитозан, поли-L-лизин, полигистидин, полиорнитин, полиспермины, протамин, поливинилпиридин, политиодиэтиламинометилэтилен (PTDAE), полиаминостирол (например, п-амино), поли(метилцианоакрилат), поли(этилцианоакрилат), поли(бутилцианоакрилат), поли(изобутилцианоакрилат), поли(изогексилцианоакрилат), DEAE-метакрилат, DEAE-гексилакрилат, DEAE-акриламид, DEAE-альбумин и DEAE-декстран, полиметилакрилат, полигексилакрилат, поли(D,L-молочную кислоту), сополимер DL-молочной и гликолевой кислот (PLGA), альгинат и полиэтиленгликоль (PEG). Составы на основе dsRNA для перорального введения и их получение подробно описаны в патенте США № 6887906, в публикации заявки на патент США № 20030027780 и патенте США № 6747014, каждый из которых включен в данный документ посредством ссылки.
Композиции и составы для парентерального, интрапаренхиматозного (в головной мозг), интратекального, интравентрикулярного или внутрипеченочного введения могут включать стерильные водные растворы, которые также могут содержать буферы, разбавители и другие подходящие добавки, такие как без ограничения вещества, способствующие проникновению, соединения-носители и другие фармацевтически приемлемые носители или наполнители.
Фармацевтические композиции по настоящему изобретению включают без ограничения растворы, эмульсии и содержащие липосомы составы. Такие композиции могут быть получены из различных компонентов, которые включают без ограничения предварительно полученные жидкости, самоэмульгирующиеся твердые вещества и самоэмульгирующиеся полутвердые вещества. При лечении заболеваний печени, таких как гепатокарцинома, особенно предпочтительными являются составы, которые нацеливаются на печень.
Фармацевтические составы по настоящему изобретению, которые в целях удобства могут находиться в виде единичной лекарственной формы, можно получать согласно традиционным методикам, хорошо известным в фармацевтической промышленности. Такие методики включают стадию объединения активных ингредиентов с фармацевтическим носителем(ями) или наполнителем(ями). Обычно составы получают путем равномерного и тщательного объединения активных ингредиентов с жидкими носителями или тонкоизмельченными твердыми носителями или обоими, а затем при необходимости придания продукту формы.
Композиции по настоящему изобретению могут быть составлены в виде любой из множества возможных лекарственных форм, таких как без ограничения таблетки, капсулы, желатиновые капсулы, жидкие сиропы, мягкие гели, суппозитории и клизмы. Композиции по настоящему изобретению также могут быть составлены в виде суспензий в водных, неводных или смешанных средах. Водные суспензии дополнительно могут содержать вещества, которые повышают вязкость суспензии, в том числе, например, натрийкарбоксиметилцеллюлозу, сорбит и/или декстран. Суспензия также может содержать стабилизаторы.
C. Дополнительные составы
i. Эмульсии
Композиции по настоящему изобретению могут быть получены и составлены в виде эмульсий. Эмульсии, как правило, представляют собой гетерогенные системы из одной жидкости, диспергированной в другой в форме капелек, диаметр которых обычно превышает 0,1 мкм (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Idson в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 199; Rosoff в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., Volume 1, p. 245; Block в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 2, p. 335; Higuchi et al. в Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa., 1985, p. 301). Эмульсии зачастую представляют собой двухфазные системы, содержащие две несмешивающиеся жидкие фазы, тщательно перемешанные и диспергированные одна в другой. Как правило, эмульсии могут быть эмульсиями по типу либо "вода в масле" (w/o), либо "масло в воде" (o/w). Когда водная фаза измельчена и диспергированной в виде мельчайших капелек в общем объеме масляной фазы, тогда полученную композицию называют эмульсией по типу "вода в масле" (w/o). В качестве альтернативы, когда масляная фаза измельчена и диспергирована в виде мельчайших капелек в общем объеме водной фазы, тогда полученную композицию называют эмульсией по типу "масло в воде" (o/w). Эмульсии могут содержать дополнительные компоненты помимо диспергированных фаз и активного лекарственного средства, которое может присутствовать либо в виде раствора в водной фазе, масляной фазе, либо само по себе в качестве отдельной фазы. Фармацевтические наполнители, такие как эмульгаторы, стабилизаторы, красители и антиоксиданты, также могут присутствовать в эмульсиях при необходимости. Фармацевтические эмульсии также могут представлять собой множественные эмульсии, которые состоят из более чем двух фаз, как, например, в случае эмульсий по типу "масло-в-воде-в-масле" (o/w/o) и "вода-в-масле-в-воде" (w/o/w). Такие сложные составы часто обеспечивают определенные преимущества, которые не обеспечивают простые двухкомпонентные эмульсии. Множественные эмульсии, в которых отдельные масляные капельки эмульсии по типу o/w заключают маленькие водные капельки, составляют эмульсию по типу w/o/w. Аналогично этому система масляных капелек, заключенная в каплях воды, стабилизированных в масляной диспергирующей фазе, дает эмульсию по типу o/w/o.
Эмульсии характеризуются малой термодинамической стабильностью либо ее отсутствием. Зачастую диспергированная или дисперсная фаза эмульсии хорошо диспергирована в дисперсионной или диспергирующей фазе и поддерживается в такой форме с помощью эмульгаторов или за счет вязкости состава. Любая из фаз эмульсии может быть полутвердой или твердой, как и в случае подобных эмульсии мазевых основ и кремов. Другие способы стабилизации эмульсий охватывают применение эмульгаторов, которые могут быть включены в любую фазу эмульсии. Эмульгаторы в целом могут быть разделены на четыре категории: синтетические поверхностно-активные вещества, встречающиеся в природе эмульгаторы, абсорбционные основы и тонкодисперные твердые вещества (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Idson, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 199).
Синтетические поверхностно-активные вещества, также известные как сурфактанты, нашли широкое применение в составлении эмульсий, и они были рассмотрены в литературе (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Rieger, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 285; Idson, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), Marcel Dekker, Inc., New York, N.Y., 1988, volume 1, p. 199). Поверхностно-активные вещества обычно являются амфифильными и содержат гидрофильную и гидрофобную части. Соотношение гидрофильной и гидрофобной природы поверхностно-активного вещества было названо гидрофильно-липофильным балансом (HLB), и оно представляет собой ценный инструмент для распределения на категории и выбора поверхностно-активных веществ при получении составов. Поверхностно-активные вещества могут быть разделены на различные классы, исходя из природы гидрофильной группы: неионогенные, анионные, катионные и амфотерные (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY Rieger, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 285).
Встречающиеся в природе эмульгаторы, применяемые в эмульсионных составах, включают ланолин, пчелиный воск, фосфатиды, лецитин и гуммиарабик. Абсорбционные основы, такие как безводный ланолин и гидрофильный вазелин, обладают гидрофильными свойствами, так что они могут впитывать воду с образованием эмульсий по типу w/o, сохраняя при этом свою полутвердую консистенцию. Тонкоизмельченные твердые вещества также применялись в качестве подходящих эмульгаторов, в особенности в комбинации с поверхностно-активными веществами и в вязких препаратах. Они включают полярные неорганические твердые вещества, такие как гидроксиды тяжелых металлов, ненабухающие глины, такие как бентонит, аттапульгит, гекторит, каолин, монтмориллонит, коллоидный силикат алюминия и коллоидный алюмосиликат магния, пигменты и неполярные твердые вещества, такие как углерод или тристеарат глицерина.
В эмульсионные составы также включают множество неэмульгирующих материалов, и они обуславливают определенные свойства эмульсий. Они включают жиры, масла, воски, жирные кислоты, жирные спирты, сложные эфиры жирных кислот, увлажнители, гидрофильные коллоиды, консерванты и антиоксиданты (Block, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 335; Idson, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 199).
Гидрофильные коллоиды или гидроколлоиды включают встречающиеся в природе смолы и синтетические полимеры, такие как полисахариды (например, гуммиарабик, агар, альгиновую кислоту, каррагенан, гуаровую камедь, камедь карайи и трагакант), производные целлюлозы (например, карбоксиметилцеллюлозу и карбоксипропилцеллюлозу) и синтетические полимеры (например, карбомеры, простые эфиры целлюлозы и карбоксивиниловые полимеры). Они диспергируются или набухают в воде с образованием коллоидных растворов, которые стабилизируют эмульсии путем образования прочных межфазных пленок вокруг капелек диспергированной фазы и путем повышения вязкости дисперсионной фазы.
Поскольку эмульсии зачастую содержат целый ряд ингредиентов, таких как углеводы, белки, стеролы и фосфатиды, которые благоприятны для поддержания роста микроорганизмов, то такие составы часто включают консерванты. Общеупотребительные консерванты, включаемые в эмульсионные составы, включают метилпарабен, пропилпарабен, соли четвертичного аммония, хлорид бензалкония, сложные эфиры п-гидроксибензойной кислоты и борную кислоту. Для предупреждения ухудшения качества состава в эмульсионные составы также обычно добавляют антиоксиданты. Применяемые антиоксиданты могут представлять собой акцепторы свободных радикалов, такие как токоферолы, алкилгаллаты, бутилированный гидроксианизол, бутилированный гидрокситолуол, или восстановители, такие как аскорбиновая кислота и метабисульфит натрия, и синергисты антиоксидантов, такие как лимонная кислота, винная кислота и лецитин.
Применение эмульсионных составов посредством дерматологического, перорального и парентерального путей введения и способы их получения были рассмотрены в литературе (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Idson, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 199). Эмульсионные составы для пероральной доставки применялись очень широко из-за удобства составления, а также с точки зрения эффективности абсорбции и биодоступности (см., например, Ansel's Pharmaceutical Dosage Forms и Drug Delivery Systems, Allen, LV., Popovich NG., и Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Rosoff в Pharmaceutical Dosage Forms, Lieberman, Rieger и Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 245; Idson в Pharmaceutical Dosage Forms, Lieberman, Rieger и Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 199). Слабительные средства на основе минеральных масел, жирорастворимые витамины и питательные препараты с высоким содержанием жиров входят в число материалов, которые обычно вводятся перорально в виде эмульсий по типу o/w.
ii. Микроэмульсии
В одном варианте осуществления настоящего изобретения композиции на основе iRNA и нуклеиновых кислот составлены в виде микроэмульсий. Можно дать определение микроэмульсии как системе из воды, масла и амфифильного вещества, которая представляет собой единый оптически изотропный и термодинамически стабильный жидкий раствор (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Rosoff, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 245). Обычно микроэмульсии представляют собой системы, которые получают вначале путем диспергирования масла в водном растворе поверхностно-активного вещества, а затем добавления достаточного количества четвертого компонента, как правило, спирта со средней длиной цепи для образования прозрачной системы. Таким образом, микроэмульсии также были описаны как термодинамически стабильные, изотропно прозрачные дисперсии двух несмешиваемых жидкостей, которые стабилизируются пленками из межфазными пленками из поверхностно-активных молекул (Leung and Shah, в Controlled Release of Drugs: Polymers and Aggregate Systems, Rosoff, M., Ed., 1989, VCH Publishers, New York, pages 185-215). Микроэмульсии обычно получают путем объединения от трех до пяти компонентов, которые включают масло, воду, поверхностно-активное вещество, вторичное поверхностно-активное вещество и электролит. Является ли микроэмульсия эмульсией по типу "вода в масле" (w/o) или по типу "масло в воде" (o/w), зависит от свойств используемого масла и поверхностно-активного вещества и от структуры и геометрической упаковки полярных головок и углеводородных хвостов молекул поверхностно-активного вещества (Schott, в Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa., 1985, p. 271).
Активно изучался феноменологический подход с использованием фазовых диаграмм, и с его помощью специалистами в данной области были получены обширные данные о том, как составлять микроэмульсии (см., например, Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, Allen, LV., Popovich NG., and Ansel HC., 2004, Lippincott Williams & Wilkins (8th ed.), New York, NY; Rosoff, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 245; Block, в Pharmaceutical Dosage Forms, Lieberman, Rieger and Banker (Eds.), 1988, Marcel Dekker, Inc., New York, N.Y., volume 1, p. 335). Преимущество микроэмульсий по сравнению с традиционными эмульсиями состоит в солюбилизации не растворимых в воде лекарственных средств в составе из термодинамически стабильных капелек, которые образуются самопроизвольно.
Поверхностно-активные вещества, используемые в получении микроэмульсий, включают без ограничения ионогенные поверхностно-активные вещества, неионогенные поверхностно-активные вещества, Brij 96, простые полиоксиэтиленолеиловые эфиры, сложные эфиры жирных кислот и полиглицерина, тетраглицерина монолаурат (ML310), тетраглицерина моноолеат (MO310), гексаглицерина моноолеат (PO310), гексаглицерина пентаолеат (PO500), декаглицерина монокапрат (MCA750), декаглицерина моноолеат (MO750), декаглицерина секвиолеат (SO750), декаглицерина декаолеат (DAO750) отдельно или в комбинации с вторичными поверхностно-активными веществами. Вторичное поверхностно-активное вещество, обычно являющееся спиртом с короткой цепью, таким как этанол, 1-пропанол и 1-бутанол, служит для увеличения межфазной текучести путем внедрения в пленку из поверхностно-активного вещества и соответственно создания неупорядоченной пленки из-за пустого пространства, образующегося между молекулами поверхностно-активного вещества. При этом микроэмульсии могут быть получены без применения вторичных поверхностно-активных веществ, и из уровня техники известны самоэмульгирующиеся микроэмульсионные системы без спирта. Водной фазой, как правило, без ограничения может быть вода, водный раствор лекарственного средства, глицерин, PEG300, PEG400, полиглицерины, пропиленгликоли и производные этиленгликоля. Масляная фаза может включать без ограничения такие материалы, как Captex 300, Captex 355, Capmul MCM, сложные эфиры жирных кислот, среднецепочечные (C8-C12)моно-, ди- и триглицериды, сложные полиоксиэтилированные эфиры жирных кислот и глицерина, жирные спирты, полигликолизированные глицериды, насыщенные полигликолизированные C8-C10-глицериды, растительные масла и силиконовое масло.
Микроэмульсии представляют особый интерес с точки зрения солюбилизации лекарственного средства и повышенной абсорбции лекарственных средств. Липидные микроэмульсии (как по типу o/w, так и по типу w/o) были предложены для увеличения пероральной биодоступности лекарственных средств, включая пептиды (см., например, патенты США №№ 6191105; 7063860; 7070802; 7157099; Constantinides et al., Pharmaceutical Research, 1994, 11, 1385-1390; Ritschel, Meth. Find. Exp. Clin. Pharmacol., 1993, 13, 205). Микроэмульсии обеспечивают преимущества в виде улучшенной солюбилизации лекарственного средства, защиты лекарственного средства от ферментативного гидролиза, возможного повышения абсорбции лекарственного средства за счет индуцированных поверхностно-активным веществом изменений текучести и проницаемости мембран, удобства получения, удобства перорального введения по сравнению с твердыми лекарственными формами, улучшенной клинической эффективности и сниженной токсичности (см., например, патенты США №№ 6191105; 7063860; 7070802; 7157099; Constantinides et al., Pharmaceutical Research, 1994, 11, 1385; Ho et al., J. Pharm. Sci., 1996, 85, 138-143). Зачастую микроэмульсии могут формироваться самопроизвольно, когда их компоненты объединяют при температуре окружающей среды. Это может иметь особенное преимущество, когда составляют термолабильные лекарственные средства, пептиды или iRNA. Микроэмульсии также были эффективными в трансдермальной доставке активных компонентов при применениях как в косметологии, так и в фармации. Предполагается, что композиции и составы микроэмульсий по настоящему изобретению будут способствовать повышенной системной абсорбции iRNA и нуклеиновых кислот из желудочно-кишечного тракта, а также улучшать локальное поглощение iRNA и нуклеиновых кислот клетками.
Микроэмульсии по настоящему изобретению также могут содержать дополнительные компоненты и добавки, такие как сорбитанмоностеарат (Grill 3), Labrasol и вещества, способствующие проникновению, для улучшения свойств состава и для повышения абсорбции iRNA и нуклеиновых кислот по настоящему изобретению. Вещества, способствующие проникновению, применяемые в микроэмульсиях по настоящему изобретению, можно классифицировать как принадлежащие к одной из пяти основных категорий: поверхностно-активные вещества, жирные кислоты, соли желчных кислот, хелатирующие средства и нехелатирующие вещества, не являющиеся поверхностно-активными (Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, p. 92). Каждый из этих классов обсуждается выше.
iii. Микрочастицы
Средство для RNAi по настоящему изобретению может быть включено в частицу, например микрочастицу. Микрочастицы можно получать при помощи высушивания распылением, но также можно получать другими способами, в том числе лиофилизацией, выпариванием, сушкой в псевдоожиженном слое, сушкой в вакууме или при помощи комбинации этих методик.
iv. Вещества, способствующие проникновению
В одном варианте осуществления настоящего изобретения разнообразные вещества, способствующие проникновению, используют для осуществления эффективной доставки нуклеиновых кислот, в частности iRNA, в кожу животных. Большинство лекарственных средств присутствуют в растворе как в ионизированной, так и в неионизированной формах. Однако обычно только жирорастворимые или липофильные лекарственные средства легко проходят через клеточные мембраны. Было установлено, что даже нелипофильные лекарственные средства могут проходить через клеточные мембраны, если мембрана, через которую необходимо пройти, обработана веществом, способствующим проникновению. В дополнение к содействию диффузии нелипофильных лекарственных средств через клеточные мембраны вещества, способствующие проникновению, также повышают проницаемость для липофильных лекарственных средств.
Вещества, способствующие проникновению, можно классифицировать как принадлежащие к одной из пяти основных категорий, т.е. поверхностно-активные вещества, жирные кислоты, соли желчных кислот, хелатирующие средства и нехелатирующие вещества, не являющиеся поверхностно-активными (см., например, Malmsten, M. Surfactants and polymers in drug delivery, Informa Health Care, New York, NY, 2002; Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, p. 92). Каждый из вышеуказанных классов веществ, способствующих проникновению, описан более подробно ниже.
Поверхностно-активные вещества (или "сурфактанты") являются химическими частицами, которые при растворении в водном растворе снижают поверхностное натяжение раствора или межфазное натяжение между водным раствором и другой жидкостью, в результате чего повышается абсорбция iRNA через слизистую оболочку. В дополнение к солям желчных кислот и жирным кислотам, эти вещества, способствующие проникновению, включают, например, лаурилсульфат натрия, полиоксиэтилен-9-лауриловый эфир и полиоксиэтилен-20-цетиловый эфир (см., например, Malmsten, M. Surfactants and polymers in drug delivery, Informa Health Care, New York, NY, 2002; Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, p.92) и перфторированные эмульсии, такие как FC-43. Takahashi et al., J. Pharm. Pharmacol., 1988, 40, 252).
Разнообразные жирные кислоты и их производные, которые выступают в роли веществ, способствующих проникновению, включают, например, олеиновую кислоту, лауриновую кислоту, каприновую кислоту (н-декановую кислоту), миристиновую кислоту, пальмитиновую кислоту, стеариновую кислоту, линолевую кислоту, линоленовую кислоту, дикапрат, трикапрат, моноолеин (1-моноолеоил-рац-глицерин), дилаурин, каприловую кислоту, арахидоновую кислоту, глицерил-1-монокапрат, 1-додецилазациклогептан-2-он, ацилкарнитины, ацилхолины, их сложные C1-20алкиловые эфиры (например, метиловый, изопропиловый и трет-бутиловый) и их моно- и диглицериды (т.е. олеат, лаурат, капрат, миристат, пальмитат, стеарат, линолеат и т.д.) (см., например, Touitou, E., et al. Enhancement in Drug Delivery, CRC Press, Danvers, MA, 2006; Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, p.92; Muranishi, Critical Reviews in Therapeutic Drug Carrier Systems, 1990, 7, 1-33; El Hariri et al., J. Pharm. Pharmacol., 1992, 44, 651-654).
Физиологическая роль желчи включает облегчение диспергирования и абсорбции липидов и жирорастворимых витаминов (см., например, Malmsten, M. Surfactants and polymers in drug delivery, Informa Health Care, New York, NY, 2002; Brunton, Chapter 38 в Goodman & Gilman's The Pharmacological Basis of Therapeutics, 9th Ed., Hardman et al. Eds., McGraw-Hill, New York, 1996, pp. 934-935). Различные природные соли желчных кислот и их синтетические производные выступают в роли веществ, способствующие проникновению. Таким образом, термин "соли желчных кислот" включает любые из встречающихся в природе компонентов желчи, а также любые из их синтетических производных. Подходящие соли желчных кислот включают, например, холевую кислоту (или ее фармацевтически приемлемую натриевую соль, холат натрия), дегидрохолевую кислоту (дегидрохолат натрия), дезоксихолевую кислоту (дезоксихолат натрия), глюкохолевую кислоту (глюкохолат натрия), гликохолевую кислоту (гликохолат натрия), гликодезоксихолевую кислоту (гликодезоксихолат натрия), таурохолевую кислоту (таурохолат натрия), тауродезоксихолевую кислоту (тауродезоксихолат натрия), хенодезоксихолевую кислоту (хенодезоксихолат натрия), урсодезоксихолевую кислоту (UDCA), тауро-24,25-дигидрофузидат натрия (STDHF), гликодигидрофузидат натрия и полиоксиэтилен-9-лауриловый эфир (POE) (см., например, Malmsten, M. Surfactants and polymers in drug delivery, Informa Health Care, New York, NY, 2002; Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, page 92; Swinyard, Chapter 39 в Remington's Pharmaceutical Sciences, 18th Ed., Gennaro, ed., Mack Publishing Co., Easton, Pa., 1990, pages 782-783; Muranishi, Critical Reviews in Therapeutic Drug Carrier Systems, 1990, 7, 1-33; Yamamoto et al., J. Pharm. Exp. Ther., 1992, 263, 25; Yamashita et al., J. Pharm. Sci., 1990, 79, 579-583).
Можно дать определение хелатирующим средствам, используемым вместе с настоящим изобретением, как соединениям, которые удаляют ионы металла из раствора путем образования комплексов с ними, в результате чего повышается абсорбция iRNA через слизистую оболочку. Что касается их применения в качестве веществ, способствующих проникновению, в настоящем изобретении, хелатирующие средства обладают дополнительным преимуществом в том, что они также служат ингибиторами ДНКаз, поскольку большинство охарактеризованных ДНК-нуклеаз требуют двухвалентный ион металла для катализа и, таким образом, ингибируются хелатирующими средствами (Jarrett, J. Chromatogr., 1993, 618, 315-339). Подходящие хелатирующие средства включают без ограничения этилендиаминтетраацетат динатрия (EDTA), лимонную кислоту, салицилаты (например, салицилат, 5-метоксисалицилат и гомовалинат натрия), N-ацилпроизводные коллагена, лаурет-9- и N-аминоацильные производные бета-дикетонов (енамины) (см., например, Katdare, A. et al., Excipient development for pharmaceutical, biotechnology, and drug delivery, CRC Press, Danvers, MA, 2006; Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, page 92; Muranishi, Critical Reviews in Therapeutic Drug Carrier Systems, 1990, 7, 1-33; Buur et al., J. Control Rel., 1990, 14, 43-51).
Можно дать определение применяемым в данном документе нехелатирующим соединениям, способствующим проникновению, которые не являются поверхностно-активными, как соединениям, которые демонстрируют незначительную активность в качестве хелатирующих средств или в качестве поверхностно-активных веществ, но которые, тем не менее, усиливают абсорбцию iRNA через слизистую оболочку пищеварительного тракта (см., например, Muranishi, Critical Reviews in Therapeutic Drug Carrier Systems, 1990, 7, 1-33). Этот класс веществ, способствующих проникновению, включает, например, ненасыщенные циклические соединения мочевины, производные 1-алкил- и 1-алкенилазациклоалканона (Lee et al., Critical Reviews in Therapeutic Drug Carrier Systems, 1991, page 92) и нестероидные противовоспалительные средства, такие как диклофенак натрия, индометацин и фенилбутазон (Yamashita et al., J. Pharm. Pharmacol., 1987, 39, 621-626).
Средства, которые повышают поглощение iRNA на клеточном уровне, также можно добавлять к фармацевтическим и другим композициям по настоящему изобретению. Например, катионные липиды, такие как липофектин (Junichi et al., патент США № 5705188), катионные производные глицерина и поликатионные молекулы, такие как полилизин (Lollo et al., заявка согласно PCT WO 97/30731), так же, как известно, повышают поглощение dsRNA клетками. Примеры коммерчески доступных реагентов для трансфекции включают, среди прочего, например, Lipofectamine™ (Invitrogen; Карлсбад, Калифорния), Lipofectamine 2000™ (Invitrogen; Карлсбад, Калифорния), 293fectin™ (Invitrogen; Карлсбад, Калифорния), Cellfectin™ (Invitrogen; Карлсбад, Калифорния), DMRIE-C™ (Invitrogen; Карлсбад, Калифорния), FreeStyle™ MAX (Invitrogen; Карлсбад, Калифорния), Lipofectamine™ 2000 CD (Invitrogen; Карлсбад, Калифорния), Lipofectamine™ (Invitrogen; Карлсбад, Калифорния), RNAiMAX (Invitrogen; Карлсбад, Калифорния), Oligofectamine™ (Invitrogen; Карлсбад, Калифорния), Optifect™ (Invitrogen; Карлсбад, Калифорния), реагент для трансфекции X-tremeGENE Q2 (Roche; Грензахерштрассе, Швейцария), реагент для липосомальной трансфекции DOTAP (Грензахерштрассе, Швейцария), реагент для липосомальной трансфекции DOSPER (Грензахерштрассе, Швейцария) или Fugene (Грензахерштрассе, Швейцария), реагент Transfectam® (Promega; Мэдисон, Висконсин), реагент для трансфекции TransFast™ (Promega; Мэдисон, Висконсин), реагент Tfx™-20 (Promega; Мэдисон, Висконсин), реагент Tfx™-50 (Promega; Мэдисон, Висконсин), DreamFect™ (OZ Biosciences; Марсель, Франция), EcoTransfect (OZ Biosciences; Марсель, Франция), реагент для трансфекции TransPassª D1 (New England Biolabs; Ипсвич, Массачусетс, США), LyoVec™/LipoGen™ (Invitrogen; Сан-Диего, Калифорния, США), реагент для трансфекции PerFectin (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции NeuroPORTER (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции GenePORTER (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции GenePORTER 2 (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции Cytofectin (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции BaculoPORTER (Genlantis; Сан-Диего, Калифорния, США), реагент для трансфекции TroganPORTER™ (Genlantis; Сан-Диего, Калифорния, США), RiboFect (Bioline; Тонтон, Массачусетс, США), PlasFect (Bioline; Тонтон, Массачусетс, США), UniFECTOR (B-Bridge International; Маунтин-Вью, Калифорния, США), SureFECTOR (B-Bridge International; Маунтин-Вью, Калифорния, США) или HiFect™ (B-Bridge International, Маунтин-Вью, Калифорния, США).
Для повышения проникновения введенных нуклеиновых кислот можно использовать другие средства, в том числе гликоли, такие как этиленгликоль и пропиленгликоль, пирролы, такие как 2-пиррол, азоны и терпены, такие как лимонен и ментон.
v. Носители
В состав некоторых композиций по настоящему изобретению также входят соединения-носители. Используемые в данном документе "соединение-носитель" или "носитель" может обозначать нуклеиновую кислоту или ее аналог, которые являются инертными (т.е. не обладают биологической активностью per se), но распознаются в качестве нуклеиновой кислоты in vivo процессами, которые снижают биодоступность нуклеиновой кислоты, обладающей биологической активностью, например путем разрушения биологически активной нуклеиновой кислоты или путем содействия ее удалению из кровотока. Совместное введение нуклеиновой кислоты и соединения-носителя, обычно с избытком последнего вещества, может приводить к существенному сокращению количества нуклеиновой кислоты, извлекаемой в печени, почках или других внесосудистых депо, предположительно вследствие конкуренции между соединением-носителем и нуклеиновой кислотой за общий рецептор. Например, извлечение частично фосфотиоатной dsRNA в ткани печени может быть снижено при ее совместном введении с полиинозиновой кислотой, сульфатом декстрана, полицитидиновой кислотой или 4-ацетамидо-4'-изотиоцианостильбен-2,2'-дисульфоновой кислотой (Miyao et al., DsRNA Res. Dev., 1995, 5, 115-121; Takakura et al., DsRNA & Nucl. Acid Drug Dev., 1996, 6, 177-183).
vi. Наполнители
В отличие от соединения-носителя "фармацевтический носитель" или "наполнитель" представляет собой фармацевтически приемлемый растворитель, суспендирующее средство или любую другую фармакологически инертную среду для доставки одной или нескольких нуклеиновых кислот в организм животного. Наполнитель может быть жидким или твердым веществом, и его выбирают с учетом предполагаемого способа введения так, чтобы обеспечить необходимый общий объем, консистенцию и т.д. при объединении с нуклеиновой кислотой и другими компонентами данной фармацевтической композиции. Типичные фармацевтические носители включают без ограничения связывающие средства (например, прежелатинизированный маисовый крахмал, поливинилпирролидон или гидроксипропилметилцеллюлозу и т.д.); заполнители (например, лактозу и другие сахара, микрокристаллическую целлюлозу, пектин, желатин, сульфат кальция, этилцеллюлозу, полиакрилаты или гидрофосфат кальция и т.д.); смазывающие вещества (например, стеараты магния, тальк, кремнезем, коллоидный диоксид кремния, стеариновую кислоту, стеараты металлов, гидрогенизированные растительные масла, кукурузный крахмал, полиэтиленгликоли, бензоат натрия, ацетат натрия и т.д.); разрыхлители (например, крахмал, крахмалгликолят натрия и т.д.) и смачивающие средства (например, лаурилсульфат натрия и т.д).
Фармацевтически приемлемые органические или неорганические наполнители, подходящие для введения, отличного от парентерального, которые не взаимодействуют неблагоприятным образом с нуклеиновыми кислотами, также можно применять для составления композиций по настоящему изобретению. Подходящие фармацевтически приемлемые носители включают без ограничения воду, растворы солей, спирты, полиэтиленгликоли, желатин, лактозу, амилозу, стеарат магния, тальк, кремниевую кислоту, вязкий парафин, гидроксиметилцеллюлозу, поливинилпирролидон и т.п.
Составы для местного введения нуклеиновых кислот могут включать стерильные и нестерильные водные растворы, неводные растворы в обычных растворителях, в таких как спирты, или растворы нуклеиновых кислот в жидких или твердых масляных основах. Растворы также могут содержать буферы, разбавители и другие подходящие добавки. Можно применять фармацевтически приемлемые органические или неорганические наполнители, подходящие для введения, отличного от парентерального, которые не взаимодействуют неблагоприятным образом с нуклеиновыми кислотами.
Подходящие фармацевтически приемлемые наполнители включают без ограничения воду, растворы солей, спирт, полиэтиленгликоли, желатин, лактозу, амилозу, стеарат магния, тальк, кремниевую кислоту, вязкий парафин, гидроксиметилцеллюлозу, поливинилпирролидон и т.п.
vii. Другие компоненты
Композиции по настоящему изобретению могут дополнительно содержать другие вспомогательные компоненты, традиционно встречающиеся в фармацевтических композициях, при уровнях применения, установленных в данной области. Так, например, композиции могут содержать дополнительные совместимые фармацевтически активные материалы, такие как, например противозудные средства, вяжущие средства, местные анестетики или противовоспалительные средства, или могут содержать дополнительные материалы, применимые для физического составления композиций по настоящему изобретению в виде различных лекарственных форм, такие как красители, ароматизирующие вещества, консерванты, антиоксиданты, замутнители, загустители и стабилизаторы. Однако такие материалы при добавлении не должны в значительной степени препятствовать проявлению биологической активности компонентов композиций по настоящему изобретению. Составы можно подвергать стерилизации и, при необходимости, смешиванию со вспомогательными средствами, например, смазывающими веществами, консервантами, стабилизаторами, смачивающими средствами, эмульгаторами, солями для оказания влияния на осмотическое давление, буферами, красящими веществами, ароматизаторами и/или отдушками и т.п., которые не взаимодействуют неблагоприятным образом с нуклеиновой кислотой(ами) состава.
Водные суспензии могут содержать вещества, которые повышают вязкость суспензии, в том числе, например, карбоксиметилцеллюлозу натрия, сорбит и/или декстран. Суспензия также может содержать стабилизаторы.
В некоторых вариантах осуществления фармацевтические композиции, представленные в настоящем изобретении, включают (a) одно или несколько соединений на основе iRNA и (b) одно или несколько средств, которые действуют по механизму, отличному от RNAi, и которые применимы в лечении нарушения свертываемости крови. Примеры таких средств включают без ограничения противовоспалительное средство, средства против стеатоза, противовирусное средство и/или средство против фиброза. Кроме того, другие вещества, обычно используемые для защиты печени, такие как силимарин, также можно применять в сочетании с iRNA, описанными в данном документе. Другие средства, применимые для лечения заболеваний печени, включают телбивудин, энтекавир и ингибиторы протеазы, такие как телапревир и другие, раскрытые, например, в публикациях заявок на патенты США №№ 2005/0148548, 2004/0167116 и 2003/0144217 от Tung et al., а также в публикации заявки на патент США № 2004/0127488 от Hale et al.
Токсичность и терапевтическая эффективность таких соединений могут быть определены с помощью стандартных фармацевтических процедур на культурах клеток или экспериментальных животных, например, для определения LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной у 50% популяции). Соотношение доз, обуславливающих токсический и терапевтический эффекты, представляет собой терапевтический индекс и его можно выразить как соотношение LD50/ED50. Предпочтительными являются соединения, которые характеризуются высоким терапевтическим индексом.
Данные, полученные в анализах на культурах клеток и в исследованиях на животных, можно применять при составлении диапазона доз для применения у людей. В настоящем изобретении дозировка композиций, представленных в данном документе, как правило, находится в пределах диапазонах циркулирующих концентраций, который включает ED50 с малой токсичностью или без таковой. Дозировка может варьироваться в этом диапазоне в зависимости от используемых лекарственной формы и пути введения. Для любого соединения, применяемого в способах, представленных в настоящем изобретении, терапевтически эффективную дозу можно первоначально установить по результатам анализов на культурах клеток. Для животных моделей дозу можно составлять таким образом, чтобы достичь диапазона циркулирующей концентрации в плазме крови соединения или при необходимости полипептидного продукта целевой последовательности (например, достижения сниженной концентрации полипептида), включающего IC50 (т.е. концентрацию исследуемого соединения, при которой достигается полумаксимальное ингибирование симптомов), определенную на культуре клеток. Такую информацию можно применять для более точного определения доз, применимых у людей. Уровни в плазме крови можно измерять, например, с помощью высокоэффективной жидкостной хроматографии.
В дополнение к обсуждаемому выше введению iRNA, представленных в настоящем изобретении, их можно вводить в комбинации с другими известными средствами, эффективными в лечении патологических процессов, опосредованных экспрессией Serpina1. В любом случае врач, осуществляющие применение, может корректировать количество и временные рамки введения iRNA, исходя из результатов, наблюдаемых при применении стандартных показателей эффективности, известных из уровня техники или описанных в данном документе.
VI. Способы ингибирования экспрессии Serpina1
Настоящим изобретением предусматриваются способы ингибирования экспрессии Serpina1 в клетке. Способы включают приведение клетки в контакт со средством для RNAi, например двухнитевым средством для RNAi, в количестве, эффективном для ингибирования экспрессии Serpina1 в клетке, за счет чего обеспечивается ингибирование экспрессии Serpina1 в клетке.
Приведение клетки в контакт с двухнитевым средством для RNAi можно выполнять in vitro или in vivo. Приведение клетки в контакт со средством для RNAi in vivo включает приведение клетки или группы клеток в организме субъекта, например субъекта-человека, в контакт со средством для RNAi. Также возможны комбинации способов приведения в контакт in vitro и in vivo. Приведение в контакт может быть непосредственным или опосредованным, как обсуждалось выше. Более того, приведение клетки в контакт можно выполнять посредством нацеливающего лиганда, в том числе любого лиганда, описанного в данном документе или известного из уровня техники. В предпочтительных вариантах осуществления нацеливающий лиганд представляет собой углеводный фрагмент, например, лиганд GalNAc3, или любой другой лиганд, который направляет средство для RNAi к сайту, представляющему интерес, например, печени субъекта.
Используемый в данном документе термин "ингибирование" используют взаимозаменяемо с "снижением", "сайленсингом", "понижающей регуляцией" и другими подобными терминами, и он включает любой уровень ингибирования.
Подразумевается, что фраза "ингибирование экспрессии Serpina1" относится к ингибированию экспрессии любого гена Serpina1 (такого как, например, ген Serpina1 мыши, ген Serpina1 крысы, ген Serpina1 обезьяны или ген Serpina1 человека), а также вариантов или мутантов гена Serpina1. Таким образом, ген Serpina1 может быть геном Serpina1 дикого типа, мутантным геном Serpina1 или трансгенным геном Serpina1 в контексте клетки, группы клеток или организма, подвергнутых генетической манипуляции.
"Ингибирование экспрессии гена Serpina1" включает любой уровень ингибирования гена Serpina1, например, по меньшей мере частичную супрессию экспрессии гена Serpina1. Экспрессию гена Serpina1 можно оценивать на основании уровня или изменения уровня любой переменной, ассоциированной с экспрессией гена Serpina1, например, уровня mRNA Serpina1, уровня белка Serpina1 или уровней липидов. Данный уровень можно оценивать в отдельной клетке или в группе клеток, в том числе, например, в образце, полученном от субъекта.
Ингибирование можно оценивать по снижению абсолютного или относительного уровня одной или нескольких переменных, которые ассоциированы с экспрессией Serpina1, по сравнению с контрольным уровнем. Контрольный уровень может представлять собой любой тип контрольного уровня, который используют в данной области техники, например, уровень в начальный момент времени до введения дозы или уровень, определенный у сходного субъекта, клетки или образца, являющихся необработанными или обработанными контролем (таким как, например, контроль только с буфером или контроль с неактивным средством).
В некоторых вариантах осуществления способов по настоящему изобретению экспрессия гена Serpina1 ингибируется по меньшей мере на приблизительно 5%, по меньшей мере на приблизительно 10%, по меньшей мере на приблизительно 15%, по меньшей мере на приблизительно 20%, по меньшей мере на приблизительно 25%, по меньшей мере на приблизительно 30%, по меньшей мере на приблизительно 35%, по меньшей мере на приблизительно 40%, по меньшей мере на приблизительно 45%, по меньшей мере на приблизительно 50%, по меньшей мере на приблизительно 55%, по меньшей мере на приблизительно 60%, по меньшей мере на приблизительно 65%, по меньшей мере на приблизительно 70%, по меньшей мере на приблизительно 75%, по меньшей мере на приблизительно 80%, по меньшей мере на приблизительно 85%, по меньшей мере на приблизительно 90%, по меньшей мере на приблизительно 91%, по меньшей мере на приблизительно 92%, по меньшей мере на приблизительно 93%, по меньшей мере на приблизительно 94%, по меньшей мере на приблизительно 95%, по меньшей мере на приблизительно 96%, по меньшей мере на приблизительно 97%, по меньшей мере на приблизительно 98% или по меньшей мере на приблизительно 99%.
Доказательством ингибирования экспрессии гена Serpina1 может служить снижение количества mRNA, экспрессируемой первой клеткой или группой клеток (такие клетки могут присутствовать, например, в образце, полученном от субъекта), в которых транскрибируется ген Serpina1 и которую или которые подвергали обработке (например, путем приведения клетки или клеток в контакт со средством для RNAi по настоящему изобретению или путем введения средства для RNAi по настоящему изобретению субъекту, в организме которого клетки находятся или находились), за счет чего ингибируется экспрессия гена Serpina1, по сравнению со второй клеткой или группой клеток, практически идентичных первой клетке или группе клеток, но которую или которые не подвергали обработке (контрольная клетка(и)). В предпочтительных вариантах осуществления ингибирование оценивают путем выражения уровня mRNA в обработанных клетках как процентной доли от уровня mRNA в контрольных клетках с помощью следующей формулы:
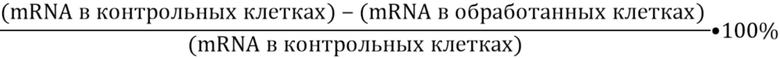
В качестве альтернативы ингибирование экспрессии гена Serpina1 можно оценивать по снижению параметра, который функционально связан с экспрессией гена Serpina1, например экспрессией белка Serpina1, такого как ALT, щелочная фосфатаза, билирубин, протромбин и альбумин. Сайленсинг гена Serpina1 можно определять в любой клетке, которая экспрессирует Serpina1 либо конститутивно, либо за счет генной инженерии, и с помощью любого анализа, известного из уровня техники. Печень является главным местом экспрессии Serpina1. Другие важные места экспрессии включают легкие и кишечник.
Доказательством ингибирования экспрессии белка Serpina1 может служить снижение уровня белка Serpina1, который экспрессируется клеткой или группой клеток (например, уровня белка, экспрессируемого в образце, полученном от субъекта). Как объяснялось выше в отношении оценки подавления экспрессии mRNA, ингибирование уровней экспрессии белка в обработанной клетке или группе клеток можно аналогично выражать как процентную долю уровня белка в контрольной клетке или группе клеток.
Контрольная клетка или группа клеток, которые можно использовать для оценки ингибирования экспрессии гена Serpina1, включают клетку или группу клеток, которые еще не были приведены в контакт со средством для RNAi по настоящему изобретению. Например, контрольная клетка или группа клеток могут быть получены от отдельного субъекта (например, субъекта-человека или субъекта-животного) перед лечением субъекта средством для RNAi.
Уровень mRNA Serpina1, которая экспрессируется клеткой или группой клеток, можно определять с помощью любого способа оценки экспрессии mRNA, известного из уровня техники. В одном варианте осуществления уровень экспрессии Serpina1 в образце определяют путем выявления транскрибированного полинуклеотида или его части, например mRNA гена Serpina1. РНК можно извлекать из клеток с помощью методик извлечения РНК, в том числе, например, извлечения с помощью кислого фенола/гуанидинизотиоцианата (RNAzol B; Biogenesis), наборов для получения РНК RNeasy (Qiagen) или PAXgene (PreAnalytix, Швейцария). Типичные форматы анализов, в которых используется гибридизация рибонуклеиновых кислот, включают ядерные "run-on" анализы, RT-PCR, анализы с защитой от РНКаз (Melton et al., Nuc. Acids Res. 12:7035), нозерн-блоттинг, гибридизацию in situ и анализы с использованием микрочипов.
В одном варианте осуществления уровень экспрессии Serpina1 определяют с использованием зонда для нуклеиновой кислоты. Используемый в данном документе термин "зонд" относится к любой молекуле, которая способна селективно связываться со специфическим Serpina1. Зонды могут быть синтезированы специалистом в данной области или получены из соответствующих биологических препаратов. Зонды можно специально разрабатывать так, чтобы они содержали метку. Примеры молекул, которые можно использовать в качестве зондов, включают без ограничения РНК, ДНК, белки, антитела и органические молекулы.
Выделенную mRNA можно использовать в анализах на основе гибридизации или амплификации, которые включают без ограничения Саузерн-блоттинг или нозерн-блот-анализы, анализы на основе полимеразной цепной реакции (PCR) и анализы с применением матриц с зондами. Один из способов определения уровней mRNA предусматривает приведение выделенной mRNA в контакт с молекулой нуклеиновой кислоты (зондом), которая может гибридизоваться с mRNA Serpina1. В одном варианте осуществления mRNA иммобилизуют на твердой поверхности и приводят в контакт с зондом, например, путем прогона выделенной мРНК в агарозном геле и переноса мРНК из геля на мембрану, например, нитроцеллюлозную. В альтернативном варианте осуществления зонд(ы) иммобилизуют на твердой поверхности и mRNA приводят в контакт с зондом(ами), например на матрице GeneChip от Affymetrix. Специалист в данной области может легко адаптировать известные способы обнаружения mRNA для применения в определении уровня mRNA Serpina1.
Альтернативный способ определения уровня экспрессии Serpina1 в образце предусматривает способ амплификации и/или обратной транскрипции нуклеиновой кислоты (с получением cDNA), например, из mRNA в образце, например с помощью RT-PCR (экспериментальный вариант осуществления изложен в Mullis, 1987, патенте США № 4683202), лигазной цепной реакции (Barany (1991) Proc. Natl. Acad. Sci. USA 88:189-193), самоподдерживающейся репликации последовательности (Guatelli et al. (1990) Proc. Natl. Acad. Sci. USA 87:1874-1878), системы транскрипционной амплификации (Kwoh et al. (1989) Proc. Natl. Acad. Sci. USA 86:1173-1177), репликазы Q-бета (Lizardi et al. (1988) Bio/Technology 6:1197), репликации по типу "катящегося кольца" (Lizardi et al., патент США № 5854033), или любой другой способ амплификации нуклеиновой кислоты с последующим обнаружением амплифицированных молекул с помощью методик, хорошо известных специалистам в данной области. Такие схемы выявления особенно применимы для выявления молекул нуклеиновой кислоты, если такие молекулы присутствуют в очень малых количествах. В конкретных аспектах настоящего изобретения уровень экспрессии Serpina1 определяют с помощью количественной флуорогенной RT-PCR (т.е. системы TaqMan™).
Уровни экспрессии mRNA Serpina1 можно контролировать с помощью мембранного блота (как, например, используемого в гибридизационном анализе, таком как нозерн-, саузерн-, дот-блот-анализ и т. п.) или микролунок, опытных пробирок, гелей, гранул или волокон (или любой твердой подложки, содержащей связанные нуклеиновые кислоты). См. патенты США №№ 5770722, 5874219, 5744305, 5677195 и 5445934, которые включены в данный документ посредством ссылки. Определение уровня экспрессии Serpina1 также может предусматривать использование зондов для нуклеиновой кислоты в растворе.
В предпочтительных вариантах осуществления уровень экспрессии mRNA оценивают с применением анализов с разветвленной ДНК (bDNA) или ПЦР в режиме реального времени (qPCR). Применение таких способов описано и проиллюстрировано в примерах, представленных в данном документе.
Уровень экспрессии белка Serpina1 можно определить с помощью любого способа измерения уровней белка, известного из уровня техники. Такие способы включают, например, электрофорез, капиллярный электрофорез, высокоэффективную жидкостную хроматографию (HPLC), тонкослойную хроматографию (TLC), гипердиффузионную хроматографию, реакции преципитации в жидкости или геле, абсорбционную спектроскопию, колориметрические анализы, спектрофотометрические анализы, проточную цитометрию, иммунодиффузию (одиночную или двойную), иммуноэлектрофорез, вестерн-блоттинг, радиоиммунологический анализ (RIA), твердофазные иммуноферментные анализы (ELISA), иммунофлуоресцентные анализы, электрохемилюминисцентные анализы и т.п.
Термин "образец", используемый в данном документе, обозначает группу аналогичных жидкостей, клеток или тканей, выделенных из организма субъекта, а также жидкостей, клеток или тканей, присутствующих в организме субъекта. Примеры биологических жидкостей включают кровь, сыворотку крови и серозные жидкости, плазму крови, лимфу, мочу, спинномозговую жидкость, слюну, внутриглазные жидкости и т.п. Образцы ткани могут включать образцы из тканей, органов или ограниченных участков. Например, образцы могут быть получены из конкретных органов, частей органов или жидкостей или клеток этих органов. В определенных вариантах осуществления образцы можно быть получены из печени (например, всей печени, или определенных сегментов печени, или определенных типов клеток в печени, таких как, например, гепатоциты). В предпочтительных вариантах осуществления "образец, полученный от субъекта" обозначает кровь или плазму крови, взятые у субъекта. В дополнительных вариантах осуществления "образец, полученный от субъекта" обозначает ткань печени, полученную от субъекта.
В некоторых вариантах осуществления способов по настоящему изобретению средство для RNAi вводят субъекту так, что средство для RNAi доставляется в специфический сайт в организме субъекта. Ингибирование экспрессии Serpina1 можно оценивать с помощью измерений уровня или изменения уровня mRNA Serpina1 или белка Serpina1 в образце, полученном из жидкости или ткани из специфического сайта в организме субъекта. В предпочтительных вариантах осуществления сайтом является печень. Сайт также может представлять собой группу или подгруппу клеток из любого из указанных выше сайтов. Сайт также может включать клетки, которые экспрессируют конкретный тип рецептора.
VII. Способы лечения или предупреждения ассоциированного с Serpina1 заболевания
Настоящее изобретение также предусматривает способы лечения или предупреждения заболеваний и состояний, на которые можно воздействовать путем подавления экспрессии гена Serpina1. Например, композиции, описанные в данном документе, можно использовать для лечения ассоциированных с Serpina1 заболеваний, таких как заболевания печени, например, хроническое заболевание печени, воспаление печени, цирроз, фиброз печени и/или гепатоцеллюлярная карцинома, и других патологических состояний, которые могут быть ассоциированы с этими нарушениями, таких как воспаление легких, эмфизема и COPD.
В настоящем изобретении также предусматриваются способы ингибирования развития гепатоцеллюлярной карциномы у субъекта, например субъекта с дефектным вариантом Serpina1. Способы предусматривают введение терапевтически эффективного количества композиции в соответствии с настоящим изобретением субъекту, за счет чего обеспечивается ингибирование развития гепатоцеллюлярной карциномы у субъекта.
Способы и пути применения композиций по настоящему изобретению для снижения накопления неправильно свернутого Serpina1 в печени субъекта, например субъекта с дефектным вариантом Serpina1, также предусмотрены настоящим изобретением. Способы предусматривают введение терапевтически эффективного количества композиции в соответствии с настоящим изобретением субъекту, со снижением таким образом накопления неправильно свернутого Serpina1 в печени субъекта.
Используемый в данном документе "субъект" включает человека или отличное от человека животное, предпочтительно позвоночное и более предпочтительно млекопитающее. Субъект может включать трансгенный организм. Наиболее предпочтительно субъектом является человек, как например человек, страдающий ассоциированным с Serpina1 заболеванием или предрасположенный к его развитию. В одном варианте осуществления субъект, страдающий ассоциированным с Serpina1 заболеванием или предрасположенный к его развитию, имеет один или несколько дефектных аллелей Serpina1, например, аллель PIZ, PIS или PIM(Malton).
В дополнительных вариантах осуществления настоящего изобретения средство на основе iRNA в соответствии с настоящим изобретением вводят в комбинации с дополнительным терапевтическим средством. Средство на основе iRNA и дополнительное терапевтическое средство можно вводить в комбинации в одной и той же композиции, например парентерально, или дополнительное терапевтическое средство можно вводить как часть отдельной композиции или другим способом, описанным в данном документе.
Примеры дополнительных терапевтических средств, подходящих для применения в способах в соответствии с настоящим изобретением, включают средства, известные для лечения нарушений функции печени, таких как цирроз печени. Например, средство на основе iRNA, описанное в настоящем изобретении, можно применять, например, вместе с урсодезоксихолевой кислотой (UDCA), иммунодепрессивными средствами, метотрексатом, кортикостероидами, циклоспорином, колхицином, средствами для лечения зуда, такими как антигистаминные средства, холестирамином, колестиполом, рифампином, дронабинолом (маринолом), а также плазмаферезом, профилактическими антибиотиками, ультрафиолетовым излучением, цинковыми добавками и вакцинацией против гепатита A, гриппа и пневмококков.
В некоторых вариантах осуществления способов по настоящему изобретению экспрессия Serpina1 снижается на длительный период времени, например, по меньшей мере на одну неделю, две недели, три недели или четыре недели, или дольше. Например, в некоторых случаях экспрессия гена Serpina1 подавляется по меньшей мере на приблизительно 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50% или 55% при введении средства на основе iRNA, описанного в данном документе. В некоторых вариантах осуществления ген Serpina1 подавляется по меньшей мере на приблизительно 60%, 70% или 80% при введении средства на основе iRNA. В некоторых вариантах осуществления ген Serpina1 подавляется по меньшей мере на приблизительно 85%, 90% или 95% при введении средства на основе iRNA.
Средства на основе iRNA согласно настоящему изобретению можно вводить субъекту при помощи любого способа введения, известного из уровня техники, в том числе без ограничения подкожного, внутривенного, внутримышечного, внутриглазного, внутрибронхиального, внутриплеврального, внутрибрюшинного, внутриартериального, лимфатического, спинномозгового и любых их комбинаций. В предпочтительных вариантах осуществления средства на основе iRNA вводят подкожно.
В некоторых вариантах осуществления введение осуществляют посредством инъекции депо-препарата. В случае инъекции депо-препарата средства на основе iRNA могут высвобождаться систематическим образом в течение длительного периода времени. Поэтому, при помощи инъекции депо-препарата можно снизить частоту введения доз, необходимых для получения требуемого эффекта, например требуемого ингибирования Serpina1, или терапевтического или профилактического эффекта. Инъекция депо-препарата может также обеспечивать более устойчивые концентрации в сыворотке крови. Инъекции депо-препарата могут включать подкожные инъекции или внутримышечные инъекции. В предпочтительных вариантах осуществления инъекция депо-препарата представляет собой подкожную инъекцию.
В некоторых вариантах осуществления введение осуществляют посредством насоса. Насос может представлять собой внешний насос или насос, имплантируемый хирургическим путем. В определенных вариантах осуществления насос представляет собой подкожно имплантированный осмотический насос. В других вариантах осуществления насос представляет собой инфузионный насос. Инфузионный насос можно применять для внутривенных, подкожных, артериальных или эпидуральных инфузий. В предпочтительных вариантах осуществления инфузионный насос представляет собой насос для подкожных инфузий. В других вариантах осуществления насос представляет собой имплантированный хирургическим путем насос, который доставляет средство для RNAi в печень.
Другие способы введения включают эпидуральное, внутримозговое, интрацеребровентрикулярное, назальное введение, внутриартериальное, внутрисердечное, внутрикостную инфузию, подоболочечное, и интравитреальное, и легочное. Способ введения можно выбрать, исходя из того, требуется ли местное или системное лечение, и исходя из области, подлежащей лечению. Путь и место введения можно выбирать для усиления нацеливания.
Способы по настоящему изобретению предусматривают введение средства на основе iRNA в дозе, достаточной для подавления/снижения уровней mRNA Serpina1 в течение по меньшей мере 5, более предпочтительно 7, 10, 14, 21, 25, 30 или 40 дней; и необязательно введение второй однократной дозы средства на основе iRNA, где вторую однократную дозу вводят по меньшей мере через 5, более предпочтительно через 7, 10, 14, 21, 25, 30 или 40 дней после введения первой однократной дозы, за счет чего обеспечивается ингибирование экспрессии гена Serpina1 у субъекта.
В одном варианте осуществления дозы средства на основе iRNA согласно настоящему изобретению вводят не более одного раза каждые четыре недели, не более одного раза каждые три недели, не более одного раза каждые две недели или не более одного раза каждую неделю. В другом варианте осуществления введения могут продолжаться в течение одного, двух, трех или шести месяцев, или одного года, или дольше.
Как правило, средство на основе iRNA не активизирует иммунную систему, например оно не повышает уровни цитокинов, как, например, уровни TNF-альфа или IFN-альфа. Например, при измерении с помощью анализа, к примеру анализа PBMC in vitro, такого как описан в данном документе, повышение уровней TNF-альфа или IFN-альфа составляет менее 30%, 20% или 10% от уровня в контрольных клетках, обработанных контрольным средством на основе iRNA, таким как средство на основе iRNA, которое не нацелено на Serpina1.
Например, субъекту можно вводить терапевтическое количество средства на основе iRNA, как, например, 0,5 мг/кг, 1,0 мг/кг, 1,5 мг/кг, 2,0 мг/кг или 2,5 мг/кг dsRNA. Средство на основе iRNA можно вводить путем внутривенной инфузии в течение некоторого периода времени, как, например, в течение периода длительностью 5 минут, 10 минут, 15 минут, 20 минут или 25 минут. Введение повторяют, например, регулярно, как, например, раз в две недели (т.е. каждые две недели) в течение одного месяца, двух месяцев, трех месяцев, четырех месяцев или дольше.
По завершении начальной схемы лечения лекарственные препараты можно вводить с меньшей частотой. Например, после введения раз в две недели в течение трех месяцев введение можно повторять один раз в месяц, причем в течение шести месяцев, или года, или дольше. Введение средства на основе iRNA может снижать уровни Serpina1, например, в клетке, ткани, крови, моче, органе (например, печени) или другой части организма пациента по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 50%, по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80% или по меньшей мере на 90% или более.
Перед введением полной дозы средства на основе iRNA пациентам можно вводить меньшую дозу и наблюдать их на предмет нежелательных явлений, как, например, аллергической реакции, или повышенных уровней липидов или кровяного давления. В другом примере пациента можно контролировать в отношении нежелательных иммуностимулирующих эффектов, такие как повышенные уровни цитокинов (например, TNF-альфа или INF-альфа). Иллюстративная меньшая доза представляет собой дозу, которая приводит в результате к частоте инфузионной реакции, меньшей или равной 5%.
Эффективность лечения или предупреждения заболевания можно оценивать, например, путем измерения прогрессирования заболевания, ремиссии заболевания, тяжести симптомов, уменьшения боли, оценки качества жизни, дозы лекарственного препарата, необходимой для поддержания эффекта лечения, уровня маркера заболевания или любого другого измеряемого параметра, соответствующего указанному заболеванию, лечение которого осуществляют или предупреждение которого предусматривают. Контроль эффективности лечения или предупреждения путем измерения любого из таких параметров или любой комбинации параметров находится в компетенции специалиста в данной области. Например, эффективность лечения фиброза печени или уменьшения симптомов фиброза печени можно оценивать, например, путем периодического контроля маркеров фиброза печени: a-2-макроглобулина(a-MA), трансферрина, аполипопротеина Al, гиалуроновой кислоты (HA), ламинина, N-концевого пептида проколлагена III(PIIINP), 7S коллагена IV (7S-IV), общего билирубина, неконъюгированного билирубина, аланинаминотрансферазы (ALT), аспартатаминотрансферазы (AST), AST/ALT, g-глутамилтранспептидазы (GGT), щелочной фосфатазы (ALP), альбумина, альбумина/глобулина, азота мочевины крови (BUN), креатинина (Cr), триглицерида, холестерина, липопротеина высокой плотности и липопротеина низкой плотности, а также пункционной биопсии печени. Можно измерять маркеры фиброза печени и/или можно осуществлять пункционную биопсию печени до лечения (исходные данные) и впоследствии (последующие данные) при осуществлении режима лечения.
Путем сравнения более поздних данных с исходными данными врач получает указание того, является ли лечение эффективным. Контроль эффективности лечения или предупреждения путем измерения любого из таких параметров или любой комбинации параметров находится в компетенции специалиста в данной области. Применительно к введению средства на основе iRNA, нацеленного на Serpina1, или фармацевтической композиции, содержащей его, "эффективный в отношении" заболевания, ассоциированного с Serpina1, такого как заболевание печени, например состояние, связанное с фиброзом печени, означает, что введение средства на основе iRNA в соответствии с настоящим изобретением клинически соответствующим образом приводит в результате к благоприятному эффекту по меньшей мере у статистически значимой части пациентов, например ослаблению симптомов, излечению, уменьшению нагрузки, обусловленной заболеванием, уменьшению массы опухоли или количества клеток, продлению жизни, улучшению качества жизни или другому эффекту, который, как правило, определяется как положительный врачами, знакомыми с лечением заболеваний печени.
В способах по настоящему изобретению можно применять средство на основе iRNA, описанное в данном документе, для лечения индивидуумов, у которых имеются признаки, симптомы и/или маркеры заболевания, ассоциированного с Serpina1, или у которых было диагностировано, или подвергающихся риску этого заболевания, а именно заболевания печени, например, воспаления печени, цирроза, фиброза печени и/или гепатоцеллюлярной карциномы. Специалист в данной области техники может легко отследить признаки, симптомы и/или маркеры этих нарушений у субъектов, получающих лечение с использованием средства на основе iRNA, описанного в данном документе, и анализировать уменьшение уровней этих признаков, симптомов и/или маркеров по меньшей мере на 10% и предпочтительно до клинического уровня, отражающего низкий риск заболевания печени.
Лечебный или превентивный эффект является очевидным, когда наблюдается статистически значимое улучшение одного или нескольких параметров патологического состояния, или когда отсутствует ухудшение или развитие симптомов в тех случаях, когда они, наоборот, прогнозировались. В качестве примера признаком эффективного лечения может служить благоприятное изменение измеряемого параметра заболевания (такого как функция печени, описанная выше) по меньшей мере на 10% и предпочтительно по меньшей мере на 20%, 30%, 40%, 50% или более.
Об эффективности данного средства на основе iRNA согласно настоящему изобретению или состава с таким средством на основе iRNA можно также судить при помощи экспериментальной животной модели для данного заболевания, которая известна из уровня техники. При использовании экспериментальной животной модели эффективность лечения доказана в том случае, когда наблюдают статистически значимое снижение маркера или ослабление симптома.
Эффект лечения или предупредительный эффект также очевидны, если наблюдается ослабление или облегчение одного или нескольких симптомов. Например, лечение или предупреждение являются эффективными в случае ослабления или облегчения одного или нескольких симптомов из слабости, утомляемости, потери веса, тошноты, рвоты, вздутия живота, отека конечностей, чрезмерного зуда и желтизны глаз и/или кожи.
Для определенных показателей эффективность можно измерять по увеличению сывороточных уровней белка Serpina1. В качестве примера признаком эффективного лечения может служить увеличение сывороточных уровней надлежащим образом свернутого Serpina1 по меньшей мере на 10%, по меньшей мере на 20%, по меньшей мере на 50%, по меньшей мере на 100%, по меньшей мере на 200% или более.
В качестве альтернативы эффективность можно измерять по уменьшению тяжести заболевания, определяемому специалистом в области техники, связанной с диагностикой, исходя из принятой в клинической практике шкалы оценивания тяжести заболевания, причем одним из примеров является оценка тяжести заболевания по шкале Чайльда-Пью (в некоторых случаях классификация Чайльда-Туркотта-Пью). В этом примере прогноз в отношении хронического заболевания печени, главным образом цирроза, определяется суммарным баллом пяти клинических количественных показателей - билирубина, сывороточного альбумина, INR, асцита и печеночной энцефалопатии. Каждому маркеру присваивается значение от 1 до 3, а суммарное значение используется для получения балла, соответствующего категории A (5-6 баллов), B (7-9 баллов) или C (10-15 баллов), что может коррелировать с уровнями выживаемости в течение одного и двух лет. Способы определения и анализа с использованием баллов по шкале Чайльда-Пью хорошо известны из уровня техники (Farnsworth et al., Am J Surgery 2004 188:580-583; Child and Turcotte. Surgery and portal hypertension. В: The liver and portal hypertension. Под редакцией CG Child. Philadelphia: Saunders 1964:50- 64; Pugh et al., Br J Surg 1973;60:648-52). В этом примере эффективность можно измерять с использованием перемещения пациента, например, из "B" в "A." Любое положительное изменение, приводящее, например, к уменьшению тяжести заболевания, как измерено с использованием соответствующей шкалы, свидетельствует об адекватном лечении с использованием iRNA или состава на основе iRNA, как описано в данном документе.
Согласно одному варианту осуществления средство для RNAi вводят в дозе от приблизительно 0,25 мг/кг до приблизительно 50 мг/кг, например, от приблизительно 0,25 мг/кг до приблизительно 0,5 мг/кг, от приблизительно 0,25 мг/кг до приблизительно 1 мг/кг, от приблизительно 0,25 мг/кг до приблизительно 5 мг/кг, от приблизительно 0,25 мг/кг до приблизительно 10 мг/кг, от приблизительно 1 мг/кг до приблизительно 10 мг/кг, от приблизительно 5 мг/кг до приблизительно 15 мг/кг, от приблизительно 10 мг/кг до приблизительно 20 мг/кг, от приблизительно 15 мг/кг до приблизительно 25 мг/кг, от приблизительно 20 мг/кг до приблизительно 30 мг/кг, от приблизительно 25 мг/кг до приблизительно 35 мг/кг или от приблизительно 40 мг/кг до приблизительно 50 мг/кг.
Доза средства для RNAi, которую вводят субъекту, может быть подобрана с уравновешиванием риска и пользы определенной дозы, например, для достижения необходимого уровня супрессии гена Serpina1 (который определяют, например, исходя из супрессии mRNA Serpina1, экспрессии белка Serpina1) или необходимого терапевтического или профилактического эффекта, вместе с тем одновременно избегая нежелательных побочных эффектов.
В некоторых вариантах осуществления средство для RNAi вводят в двух или более дозах. При необходимости облегчить проведение повторяющихся или частых инфузий может быть целесообразной имплантация устройства для доставки, например, насоса, полупостоянного стента (например, внутривенного, внутрибрюшинного, интрацистернального или интракапсулярного) или емкости. В некоторых вариантах осуществления число или количество последовательных доз зависит от достижения необходимого эффекта, например супрессии гена Serpina1, или достижения терапевтического или профилактического эффекта, например уменьшения интенсивности симптома заболевания печени. В некоторых вариантах осуществления средство для RNAi вводят в соответствии со схемой. Например, средство для RNAi можно вводить один раз в неделю, два раза в неделю, три раза в неделю, четыре раза в неделю или пять раз в неделю. В некоторых вариантах осуществления схема предусматривает введения с равными интервалами, например, ежечасно, каждые четыре часа, каждые шесть часов, каждые восемь часов, каждые двенадцать часов, ежедневно, каждые 2 дня, каждые 3 дня, каждые 4 дня, каждые 5 дней, еженедельно, раз в две недели или раз в месяц. В других вариантах осуществления схема предусматривает введения с небольшим интервалом с последующим более длительным периодом времени, в течение которого средство не вводят. В некоторых вариантах осуществления средство для RNAi вводят при режиме дозирования, который включает "фазу насыщения" из введений с небольшими интервалами, за которой может следовать "фаза поддержания", в которой средство для RNAi вводят с более длительными интервалами.
Любую из этих схем необязательно можно повторять с обеспечением одного или нескольких повторов. Число повторов может зависеть от достижения необходимого эффекта, например супрессии гена Serpina1, и/или достижения терапевтического или профилактического эффекта, например уменьшения интенсивности симптома ассоциированного с Serpina1 заболевания, например заболевания печени.
В другом аспекте настоящего изобретения представлен способ инструктирования конечного пользователя, например лица, осуществляющего уход или лечение, или субъекта, в отношении того, как вводить средство на основе iRNA, описанное в данном документе. Способ предусматривает необязательное обеспечение конечного пользователя одной или несколькими дозами средства на основе iRNA и инструктирование конечного пользователя в отношении введения средства на основе iRNA согласно схеме, описанной в данном документе, вследствие чего обеспечивается инструктирование конечного пользователя.
Наследственная предрасположенность играет роль в развитии заболеваний, ассоциированных с целевым геном, например заболевания печени. Таким образом, пациента, нуждающегося в лечении с помощью siRNA, можно идентифицировать путем сбора семейного анамнеза или, например, скрининга в отношении одного или нескольких генетических маркеров или вариантов. Следовательно, в одном аспекте настоящее изобретение относится к способу лечения пациента посредством выбора пациента, исходя из того, что у пациента имеется одна или несколько дефектных форм Serpina1 или дефектный вариант гена Serpina1, например, аллель PIZ, PIS или PIM(Malton). Способ предусматривает введение пациенту средства на основе iRNA в терапевтически эффективном количестве.
Медицинский работник, такой как врач, медицинская сестра, или член семьи могут собрать семейный анамнез перед назначением или введением средства на основе iRNA по настоящему изобретению. Кроме того, можно выполнить тест по определению генотипа или фенотипа. Например, можно выполнить ДНК-тест с образцом от пациента, например образцом крови, для идентификации генотипа и/или фенотипа по Serpina1 перед введением пациенту dsRNA к Serpina1.
VIII. Наборы
В настоящем изобретении также предусмотрены наборы для применения любого из средств на основе iRNA и/или осуществления любого из способов по настоящему изобретению. Такие наборы включают одно или несколько средств для RNAi и инструкции по применению, например инструкции по ингибированию экспрессии Serpina1 в клетке путем приведения клетки в контакт со средством(-и) для RNAi в количестве, эффективном для ингибирования экспрессии Serpina1. Наборы могут необязательно дополнительно содержать средства для приведения клетки в контакт со средством для RNAi (например, устройство для инъекции) или средства для определения степени ингибирования Serpina1 (например, средства для определения степени ингибирования mRNA Serpina1). Такие средства для определения степени ингибирования Serpina1 могут включать средства для получения образца от субъекта, как, например, образца плазмы крови. Наборы по настоящему изобретению необязательно могут дополнительно содержать средства для введения средства(средств) для RNAi субъекту или средства для определения терапевтически эффективного или профилактически эффективного количества.
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют такое значение, которое обычно понятно специалисту в области техники, к которой относится настоящее изобретение. Хотя способы и материалы, аналогичные или эквивалентные описанным в данном документе, можно применять при практическом осуществлении или тестировании iRNA и способов, описанных в настоящем изобретении, подходящие способы и материалы описаны ниже. Все публикации, заявки на выдачу патентов, патенты и другие литературные источники, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. В случае конфликта, настоящее описание, включая определения, будет иметь преимущественную силу. Кроме того, материалы, способы и примеры являются только иллюстративными и не подразумеваются как ограничивающие.
ПРИМЕРЫ
Пример 1. Снижение нецелевых эффектов и токсичности in vivo
РНК-интерференция или "RNAi" представляет собой термин, который изначально ввел в обращение Fire с сотрудниками для описания наблюдения, что двухнитевая РНК (dsRNA) для RNAi может блокировать экспрессию гена (Fire et al. (1998) Nature 391, 806-811; Elbashir et al. (2001) Genes Dev. 15, 188-200). Короткая dsRNA управляет ген-специфичным посттранскрипционным сайленсингом у многих организмов, в том числе у позвоночных, и обеспечила новый инструмент для изучения функции генов. RNAi опосредуется РНК-индуцируемым комплексом сайленсинга (RISC), специфичной к последовательности многокомпонентной нуклеазой, которая разрушает матричные РНК, гомологичные инициатору сайленсинга. Известно, что RISC содержит короткие РНК (длиной примерно 22 нуклеотида), происходящие из инициатора в виде двухнитевой РНК, однако белковые компоненты этого активного комплекса остаются неизвестными.
Одним из нецелевых эффектов siRNA является miRNA-подобный эффект - белок Argonaute, центральный эффектор при РНК-интерференции, воздействует на siRNA, которую вводят искусственно в качестве miRNA (microRNA) с целью индукции РНК-интерференции (Lam et al. (2015) Molecular Therapy Nucleic Acids (2015) 4, e252). Главным образом miRNA распознает целевой ген посредством спаривания оснований между затравочной областью (положения 2-7 на 5'-конце) и целевой mRNA для супрессии гена. Нецелевые эффекты, обусловленные siRNA, происходят из комплементарности оснований затравочных областей RISC-загруженной антисмысловой нити siRNA и одной или нескольких mRNA. В нескольких исследованиях были описаны miRNA-подобные нецелевые эффекты siRNA, к тому же они оказывают влияние на экспрессию многочисленных генов, в зависимости от последовательностей затравочных областей, и являются достаточно серьезными, чтобы обуславливать до 30% положительных отборов при фенотипическом скрининге на основе siRNA. Кроме того, в случае miRNA также заявлено, что они обеспечивают сайленсинг целевых генов посредством компенсаторных спариваний в своих 3'-концевых областях (компенсаторное 3'-спаривание), если взаимодействия между затравочной областью и мишенями становятся слабыми, что подразумевает, что miRNA-подобные нецелевые эффекты, вероятно, опосредованы таким механизмом.
Как описано ниже, было обнаружено, что средства на основе dsRNA, где антисмысловая нить содержит по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5′-конца) и/или средство на основе dsRNA характеризуется температурой плавления в диапазоне от приблизительно 40°C до приблизительно 80°C, могут быть более эффективными в опосредовании РНК-интерференции, чем исходное средство на основе dsRNA, не имеющее дестабилизирующей модификации. Такие средства являются преимущественными для подавления экспрессии целевых генов, при этом характеризуются пониженными нецелевыми эффектами в отношении сайленсинга генов, как и композиции для RNAi, подходящие для терапевтического применения.
Материалы и способы
В примерах использовали следующие материалы и способы.
Конструирование siRNA
Отбирали лучшие разрабатываемые кандидатные средства на основе dsRNA, нацеливающиеся на ингибитор сериновой пептидазы, клады A, представителя 1 (Serpina1) (AAT) для оценивания в экспериментах, описанных в данном документе. Средства на основе dsRNA, нацеливающиеся на Serpina1, характеризующиеся модифицированной нуклеотидной последовательностью исходного лучшего разрабатываемого кандидата, и характеризующиеся антисмысловой нитью, содержащей по меньшей мере одну нарушающую термостабильность модификацию дуплекса в пределах затравочной области (т.е. в положении 2-9 5'-конца антисмысловой нити, считая от 5'-конца), и/или характеризующиеся температурой плавления в диапазоне от приблизительно 40°C до приблизительно 80°C, конструировали, синтезировали и оценивали, как описано ниже.
В частности, как описано в предварительной заявке на патент США № 61/826125, поданной 22 мая 2013 г., предварительной заявке на патент США № 61/898695, поданной 1 ноября 2013 г.; предварительной заявке на патент США № 61/979727, поданной 15 апреля 2014 г.; предварительной заявке на патент США № 61/989028, поданной 6 мая 2014 г.; заявке на патент США № 14/284745, по которой в настоящее время выдан патент США № 9574192 от 21 февраля 2017 г.; заявке на патент США № 15/399820, поданной 6 января 2017 г., и международной заявке на патент № PCT/US2014/039109, поданной 22 мая 2014 г., было установлено и показано, что AD-61444 эффективно и продолжительно ингибирует AAT in vitro и in vivo. Немодифицированная нуклеотидная последовательность смысловой нити AD-61444 представляет собой 5' - CUUCUUAAUGAUUGAACAAAA - 3' (SEQ ID NO: 417), и немодифицированная нуклеотидная последовательность AD-61444 представляет собой 5' - UUUUGUUCAAUCAUUAAGAAGAC - 3' (SEQ ID NO: 419). Модифицированная нуклеотидная последовательность смысловой нити AD-61444 представляет собой 5' - csusucuuaauGfAfuugaacaaaaL96-3' (SEQ ID NO: 418), и модифицированная нуклеотидная последовательность антисмысловой нити AD-61444 представляет собой 5' - usUfsuUfgUfuCfaAfucaUfuAfaGfaAfgsasc - 3' (SEQ ID NO: 420).
Таблица B. Таблица 1. Сокращения нуклеотидных мономеров, используемые в представлении последовательностей нуклеиновой кислоты.
Следует понимать, что эти мономеры, если они присутствуют в олигонуклеотиде, взаимно связаны между собой 5'-3'-фосфодиэфирными связями.
Hyp-(GalNAc-алкил)3
Синтез и очистка
Все олигонуклеотиды получали на синтезаторе MerMade 192 в масштабе 1 мкмоль с применением универсальной или специально созданной подложек. Все фосфорамидиты использовали в концентрации 100 мM в 100% ацетонитриле или смеси 9:1 ацетонитрил:DMF согласно стандартному протоколу для 2-цианоэтилфосфорамидитов, за исключением того, что время связывания продлевали до 400 секунд. Окисления незадолго до этого образованных связей достигали с применением раствора 50 мM I2 в смеси 9:1 ацетонитрил:вода для образования фосфатных связей и 100 мM DDTT в смеси 9:1 пиридин:ацетонитрил для образования фосфотиоатных связей. После синтеза с удалением диметокситритильной защитной группы колонки инкубировали с 150 мкл 40% водного метиламина в течение 45 минут и раствор переносили посредством вакуумного дренажа в 96-луночный планшет. После повторения инкубации и дренажа с использованием свежей порции водного метиламина планшет, содержащий раствор неочищенных олигонуклеотидов, герметично закрывали и встряхивали при комнатной температуре в течение дополнительных 60 минут до полного удаления всех защитных групп неочищенных олигонуклеотидов, завершали посредством добавления в каждую лунку по 1,2 мл смеси 9:1 ацетонитрил:EtOH с последующей инкубацией при -20°C в течение ночи. Затем планшет центрифугировали при 3000 об/мин в течение 45 минут, из каждой лунки удаляли супернатант и осадки ресуспендировали в 950 мкл 20 мM водного NaOAc. Каждый неочищенный раствор в конечном итоге обессоливали посредством колонки для обессоливания GE Hi-Trap (Sephadex G25 Superfine) с использованием воды для элюирования конечных олигонуклеотидных продуктов. Все показатели идентичности и чистоты подтверждали с применением ESI-MS и IEX HPLC соответственно.
Температурно-зависимая УФ-спектроскопия
Исследования плавления проводили при концентрации дуплекса (состоящего из модифицированной антисмысловой нити, спаренной с комплементарной немодифицированной смысловой нитью РНК), составляющей 1 мкМ в 0,33-кратном PBS (3,3 мМ Na/K фосфатный буфер, pH 7,4, с 46 мМ NaCl и 0,9 мМ KCl) в кварцевых кюветах с толщиной слоя 1 см на спектрофотометре Beckman DU800, оснащенном программатором температуры. Каждая кювета содержала 200 мкл раствора образца, покрытого 125 мкл легкого минерального масла. Кривые плавления регистрировали при 260 нм со скоростью нагревания 1°C/мин. от 15 до 90°C. Значения температуры плавления (Tm) рассчитывали по первым производным усредненных кривых нагревания, и полученные значения являлись результатом по меньшей мере двух независимых измерений.
Репортерный анализ in vitro
Клетки COS-7 культивировали при 37°C, 5% CO2 в модифицированной по способу Дульбекко среде Игла (DMEM), дополненной 10% фетальной бычьей сывороткой (FBS). Клетки котрансфицировали в 96-луночных планшетах (15000 клеток/лунка) 10 нг репортерных плазмид с люциферазой и siRNA в 10-кратных разведениях от 50 фМ до 50 нМ с применением 2 мкг/мл Lipofectamine 2000 (Thermo Fisher Scientific) в соответствии с инструкциями изготовителя. Клетки собирали через 48 ч. после трансфекции для проведения анализа с использованием двойной люциферазы (Promega) в соответствии с инструкциями изготовителя. Нацеленная репортерная плазмида содержала один идеально комплементарный антисмысловой нити сайт в 3'-нетранслируемой области (3'-UTR) гена люциферазы Renilla. Репортерная плазмида без нацеливания содержала четыре тандемных комплементарных затравочному участку сайта, разделенных 21-28 нуклеотидами, в 3'-UTR гена люциферазы Renilla. Обе плазмиды совместно экспрессировали люциферазу светлячка в качестве контроля трансфекции.
Анализ экспрессии генов
Криоконсервированные гепатоциты крысы и человека (Bioreclamation) культивировали при 37°C, 5% CO2 в среде InVitroGRO CP со смесью антибиотиков Torpedo. Клетки трансфицировали в 96-луночных планшетах (20000 клеток/лунка) 10 нМ siRNA с применением 2 мкг/мл Lipofectamine RNAiMAX (Thermo Fisher Scientific) в соответствии с инструкциями изготовителя. Клетки собирали через 24 ч после трансфекции для проведения экстракции РНК с помощью набора miRNeasy (Qiagen) в соответствии с инструкциями изготовителя. Библиотеки cDNA получали с использованием набора TruSeq Stranded Total RNA Library Prep (Illumina) и секвенировали на NextSeq 500 (Illumina).
Исследования in vivo на мышах и крысах
Все исследования проводили с применением протоколов в соответствии с местными нормами, нормами штата и федеральными нормами, применимыми и одобренными Институциональными комитетами по уходу за животными и их использованию (IACUC) в Alnylam Pharmaceuticals.
В исследованиях фармакодинамики на мышах самкам мышей C57BL/6 (Charles River Laboratories) вводили однократную дозу контроля в виде среды-носителя (0,9% хлорид натрия, солевой раствор) или 0,5 или 1 мг/кг siRNA подкожно в верхнюю часть спины. В день 8 печени собирали, промывали в холодном солевом растворе, незамедлительно подвергали быстрому замораживанию в жидком азоте и хранили при -80C для анализа mRNA и siRNA.
В исследованиях токсичности на крысах самцам крыс Sprague Dawley (Charles River Laboratories) вводили еженедельно три повторные дозы (qw x 3) контроля в виде среды-носителя (0,9% хлорид натрия, солевой раствор) или 30 мг/кг siRNA подкожно в верхнюю часть спины. В день 16 собирали сыворотку для оценки клинический патологии и собирали печени для гистопатологической оценки и для анализа mRNA и siRNA.
Количественное определение mRNA и siRNA
РНК экстрагировали с помощью набора miRNeasy (Qiagen) в соответствии с инструкциями изготовителя, превращали в cDNA с помощью набора для обратной транскрипции High-Capacity cDNA Reverse Transcription Kit (Thermo Fisher Scientific) в соответствии с инструкциями изготовителя и оценивали уровни mRNA с помощью количественной полимеразной цепной реакции (qPCR) с применением ген-специфичных зондов Taqman (Thermo Fisher Scientific) на Roche Light Cycler 480 II с использованием LightCycler 480 Probes Master (Roche).
Для количественной оценки воздействия siRNA осажденные клетки ресуспендировали в фосфатно-солевом буферном растворе (PBS), содержащем 0,25% Triton X-100, нагревали при 95°C в течение 10 мин, центрифугировали при 14000 об/мин при 4°C в течение 10 мин. и на супернатантах проводили обратную транскрипцию с применением набора для обратной транскрипции TaqMan MicroRNA Reverse Transcription Kit (Thermo Fisher Scientific) в соответствии с инструкциями изготовителя. Проводили qPCR на Roche Light Cycler 480 II с использованием LightCycler 480 Probes Master (Roche) в соответствии с инструкциями изготовителя.
Результаты
1. Исследования in vitro
Результаты репортерного анализа in vitro обобщены в таблице 1. Как показывают данные в таблице 1, модификация с помощью гликоль-нуклеиновой кислоты (GNA) в положении 7 антисмысловой нити сохраняет целевую активность, в то же время понижая нецелевую активность in vitro.
Таблица 1. Данные репортерных анализов in vitro в отношении модификации с помощью GNA в положении 7 антисмысловых нитей
(нM)
(нM)
Клетки COS-7 котрансфицировали репортерными плазмидами с люциферазой вместе с siRNA и через 48 ч. проводили люциферазный анализ.
2. Анализ экспрессии генов
Результатов анализа экспрессии генов in vitro обобщены в таблице 2. Как видно из таблицы 2, модификация с помощью GNA в положении 7 антисмысловой нити уменьшила нецелевую активность in vitro.
Таблица 2. Анализ экспрессии генов
Гепатоциты человека (AAT) трансфицировали siRNA и собирали РНК через 24 ч. для секвенирования РНК.
3. Исследования in vivo на мышах
Результаты исследований in vivo обобщены в таблице 3. Как можно увидеть, модификация с помощью GNA в положении 7 антисмысловой нити сохраняет эффективность in vivo (таблица 3).
Таблица 3. Данные в отношении фармакодинамики у мышей
Мышам вводили однократную дозу нацеленных на AAT siRNA в количестве 1 мг/кг и в день 8 оценивали нокдаун mRNA печени.
Пример 2. Анализ in vivo и in vitro средств на основе dsRNA, нацеленных на Serpina1
Для дополнительной оценки in vivo эффекта встраивания нуклеотида GNA в AD-61444 осуществляли дополнительное модифицирование AD-61444 нуклеотидом GNA в положении 6 (AD-75994) или 7 (AD-75995) антисмысловой нити (фигура 1A), и мышам, трансгенным по AAT человека, подкожно вводили однократную дозу средства в количестве 1 мг/кг. Перед введением доз и во временные точки, указанные на фигуре 1B, получали сыворотку крови для количественного определения циркулирующего AAT. Уровни белка AAT определяли с помощью сэндвич-ELISA и данные нормализовали относительно исходного значения уровней белка AAT.
Как показано на фигуре 1B, встраивание нуклеотида GNA либо в положение 6, либо 7 антисмысловой нити AD-61444 приводило в результате к потере активности по сравнению с исходной молекулой.
Соответственно, общее число 2'-фтор-модифицированных нуклеотидов в AD-61444 понижали, получая в результате AD-77407, и нуклеотид GNA встраивали в положение 7 антисмысловой нити AD-77407, получая в результате AD-77412 (фигура 1C). Мышам, трансгенным по AAT человека, подкожно вводили однократную дозу средства в количестве 1 мг/кг. Перед введением доз и во временные точки, указанные на фигуре 1D, получали сыворотку крови для количественного определения циркулирующего AAT. Уровни белка AAT определяли с помощью сэндвич-ELISA и данные нормализовали относительно исходного значения уровней белка AAT.
На фигуре 1D продемонстрировано, что снижение содержания 2'-фтор-модификаций в AD-61444 (т.е. AD-77407) приводило в результате к заметному улучшению активности у мышей. Более того, встраивание нуклеотида GNA в данном контексте (AD-77412) приводило в результате к суммарному улучшению относительно исходной молекулы AD-61444.
Для определения влияния понижения содержания 2'-фтор-модификаций в AD-61444 и встраивания нуклеотида GNA в положении 7 антисмысловой нити на нецелевые эффекты клетки Hep3b трансфицировали 10 нМ AD-61444 или AD-77412 с применением Lipofectamine RNAiMax. Через 16 часов клетки лизировали и осуществляли подготовку к транскрипционному анализу. Как показано на фигурах 2A и 2B, полученные данные представляли в виде графика, причем транскрипты, экспрессия которых статистически значимо отличалась от клеток с имитацией обработки, показаны черными кругами, а транскрипты, экспрессия которых статистически значимо не отличалась от клеток с имитацией обработки, показаны серыми кругами. Транскрипт AAT указан и выделен с помощью окружности.
Данные, показанные на фигурах 2A и 2B, демонстрируют, что обработка клеток AD-61444 приводила в результате к пониженной регуляции пятидесяти двух транскриптов, в том числе AAT. Для сравнения GNA-содержащий дуплекс AD-77412 приводил в результате к пониженной регуляции только трех транскриптов, в том числе AAT. Таким образом, встраивание нуклеотида GNA существенно понижало число наблюдаемых нецелевых случаев пониженной регуляции, обусловленной AD-61444 in vitro.
Влияние AD-77412 также оценивали у отличных от человека приматов. Яванским макакам подкожно вводили однократную дозу в количестве 0,3 мг/кг, 1,0 мг/кг, 3 мг/кг или 10 мг/кг либо AD-61444, либо AD-77412. Перед введением доз и во временные точки, указанные на фигурах 3A-3D, получали сыворотку крови для количественного определения циркулирующего AAT. Уровни белка AAT определяли с помощью сэндвич-ELISA и данные нормализовали относительно исходного значения уровней белка AAT.
Как показано на фигурах 3A-3D, AD-61444 и AD-77412 во всех дозах осуществляли эффективный сайленсинг экспрессии AAT при сходных максимальных уровнях сайленсинга.
Подводя итог, данные анализы демонстрируют, что встраивание нуклеотида GNA в затравочную область антисмысловой нити исходной молекулы AD-61444 не приводит к потере активности по сравнению с исходной молекулой и в значительной степени понижает нецелевые эффекты.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ALNYLAM PHARMACEUTICALS, INC.
<120> КОМПОЗИЦИИ НА ОСНОВЕ iRNA SERPINA1 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 121301-07820
<140>
<141>
<150> 62/561,514
<151> 2017-09-21
<150> 62/549,099
<151> 2017-08-23
<150> 62/548,589
<151> 2017-08-22
<150> 62/425,907
<151> 2016-11-23
<160> 420
<170> PatentIn версия 3.5
<210> 1
<211> 3220
<212> ДНК
<213> Homo sapiens
<400> 1
acaatgactc ctttcggtaa gtgcagtgga agctgtacac tgcccaggca aagcgtccgg 60
gcagcgtagg cgggcgactc agatcccagc cagtggactt agcccctgtt tgctcctccg 120
ataactgggg tgaccttggt taatattcac cagcagcctc ccccgttgcc cctctggatc 180
cactgcttaa atacggacga ggacagggcc ctgtctcctc agcttcaggc accaccactg 240
acctgggaca gtgaatcgac aatgccgtct tctgtctcgt ggggcatcct cctgctggca 300
ggcctgtgct gcctggtccc tgtctccctg gctgaggatc cccagggaga tgctgcccag 360
aagacagata catcccacca tgatcaggat cacccaacct tcaacaagat cacccccaac 420
ctggctgagt tcgccttcag cctataccgc cagctggcac accagtccaa cagcaccaat 480
atcttcttct ccccagtgag catcgctaca gcctttgcaa tgctctccct ggggaccaag 540
gctgacactc acgatgaaat cctggagggc ctgaatttca acctcacgga gattccggag 600
gctcagatcc atgaaggctt ccaggaactc ctccgtaccc tcaaccagcc agacagccag 660
ctccagctga ccaccggcaa tggcctgttc ctcagcgagg gcctgaagct agtggataag 720
tttttggagg atgttaaaaa gttgtaccac tcagaagcct tcactgtcaa cttcggggac 780
accgaagagg ccaagaaaca gatcaacgat tacgtggaga agggtactca agggaaaatt 840
gtggatttgg tcaaggagct tgacagagac acagtttttg ctctggtgaa ttacatcttc 900
tttaaaggca aatgggagag accctttgaa gtcaaggaca ccgaggaaga ggacttccac 960
gtggaccagg tgaccaccgt gaaggtgcct atgatgaagc gtttaggcat gtttaacatc 1020
cagcactgta agaagctgtc cagctgggtg ctgctgatga aatacctggg caatgccacc 1080
gccatcttct tcctgcctga tgaggggaaa ctacagcacc tggaaaatga actcacccac 1140
gatatcatca ccaagttcct ggaaaatgaa gacagaaggt ctgccagctt acatttaccc 1200
aaactgtcca ttactggaac ctatgatctg aagagcgtcc tgggtcaact gggcatcact 1260
aaggtcttca gcaatggggc tgacctctcc ggggtcacag aggaggcacc cctgaagctc 1320
tccaaggccg tgcataaggc tgtgctgacc atcgacgaga aagggactga agctgctggg 1380
gccatgtttt tagaggccat acccatgtct atcccccccg aggtcaagtt caacaaaccc 1440
tttgtcttct taatgattga acaaaatacc aagtctcccc tcttcatggg aaaagtggtg 1500
aatcccaccc aaaaataact gcctctcgct cctcaacccc tcccctccat ccctggcccc 1560
ctccctggat gacattaaag aagggttgag ctggtccctg cctgcatgtg actgtaaatc 1620
cctcccatgt tttctctgag tctccctttg cctgctgagg ctgtatgtgg gctccaggta 1680
acagtgctgt cttcgggccc cctgaactgt gttcatggag catctggctg ggtaggcaca 1740
tgctgggctt gaatccaggg gggactgaat cctcagctta cggacctggg cccatctgtt 1800
tctggagggc tccagtcttc cttgtcctgt cttggagtcc ccaagaagga atcacagggg 1860
aggaaccaga taccagccat gaccccaggc tccaccaagc atcttcatgt ccccctgctc 1920
atcccccact cccccccacc cagagttgct catcctgcca gggctggctg tgcccacccc 1980
aaggctgccc tcctgggggc cccagaactg cctgatcgtg ccgtggccca gttttgtggc 2040
atctgcagca acacaagaga gaggacaatg tcctcctctt gacccgctgt cacctaacca 2100
gactcgggcc ctgcacctct caggcacttc tggaaaatga ctgaggcaga ttcttcctga 2160
agcccattct ccatggggca acaaggacac ctattctgtc cttgtccttc catcgctgcc 2220
ccagaaagcc tcacatatct ccgtttagaa tcaggtccct tctccccaga tgaagaggag 2280
ggtctctgct ttgttttctc tatctcctcc tcagacttga ccaggcccag caggccccag 2340
aagaccatta ccctatatcc cttctcctcc ctagtcacat ggccataggc ctgctgatgg 2400
ctcaggaagg ccattgcaag gactcctcag ctatgggaga ggaagcacat cacccattga 2460
cccccgcaac ccctcccttt cctcctctga gtcccgactg gggccacatg cagcctgact 2520
tctttgtgcc tgttgctgtc cctgcagtct tcagagggcc accgcagctc cagtgccacg 2580
gcaggaggct gttcctgaat agcccctgtg gtaagggcca ggagagtcct tccatcctcc 2640
aaggccctgc taaaggacac agcagccagg aagtcccctg ggcccctagc tgaaggacag 2700
cctgctccct ccgtctctac caggaatggc cttgtcctat ggaaggcact gccccatccc 2760
aaactaatct aggaatcact gtctaaccac tcactgtcat gaatgtgtac ttaaaggatg 2820
aggttgagtc ataccaaata gtgatttcga tagttcaaaa tggtgaaatt agcaattcta 2880
catgattcag tctaatcaat ggataccgac tgtttcccac acaagtctcc tgttctctta 2940
agcttactca ctgacagcct ttcactctcc acaaatacat taaagatatg gccatcacca 3000
agccccctag gatgacacca gacctgagag tctgaagacc tggatccaag ttctgacttt 3060
tccccctgac agctgtgtga ccttcgtgaa gtcgccaaac ctctctgagc cccagtcatt 3120
gctagtaaga cctgcctttg agttggtatg atgttcaagt tagataacaa aatgtttata 3180
cccattagaa cagagaataa atagaactac atttcttgca 3220
<210> 2
<211> 3199
<212> ДНК
<213> Homo sapiens
<400> 2
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaaggaca 240
atgccgtctt ctgtctcgtg gggcatcctc ctgctggcag gcctgtgctg cctggtccct 300
gtctccctgg ctgaggatcc ccagggagat gctgcccaga agacagatac atcccaccat 360
gatcaggatc acccaacctt caacaagatc acccccaacc tggctgagtt cgccttcagc 420
ctataccgcc agctggcaca ccagtccaac agcaccaata tcttcttctc cccagtgagc 480
atcgctacag cctttgcaat gctctccctg gggaccaagg ctgacactca cgatgaaatc 540
ctggagggcc tgaatttcaa cctcacggag attccggagg ctcagatcca tgaaggcttc 600
caggaactcc tccgtaccct caaccagcca gacagccagc tccagctgac caccggcaat 660
ggcctgttcc tcagcgaggg cctgaagcta gtggataagt ttttggagga tgttaaaaag 720
ttgtaccact cagaagcctt cactgtcaac ttcggggaca ccgaagaggc caagaaacag 780
atcaacgatt acgtggagaa gggtactcaa gggaaaattg tggatttggt caaggagctt 840
gacagagaca cagtttttgc tctggtgaat tacatcttct ttaaaggcaa atgggagaga 900
ccctttgaag tcaaggacac cgaggaagag gacttccacg tggaccaggt gaccaccgtg 960
aaggtgccta tgatgaagcg tttaggcatg tttaacatcc agcactgtaa gaagctgtcc 1020
agctgggtgc tgctgatgaa atacctgggc aatgccaccg ccatcttctt cctgcctgat 1080
gaggggaaac tacagcacct ggaaaatgaa ctcacccacg atatcatcac caagttcctg 1140
gaaaatgaag acagaaggtc tgccagctta catttaccca aactgtccat tactggaacc 1200
tatgatctga agagcgtcct gggtcaactg ggcatcacta aggtcttcag caatggggct 1260
gacctctccg gggtcacaga ggaggcaccc ctgaagctct ccaaggccgt gcataaggct 1320
gtgctgacca tcgacgagaa agggactgaa gctgctgggg ccatgttttt agaggccata 1380
cccatgtcta tcccccccga ggtcaagttc aacaaaccct ttgtcttctt aatgattgaa 1440
caaaatacca agtctcccct cttcatggga aaagtggtga atcccaccca aaaataactg 1500
cctctcgctc ctcaacccct cccctccatc cctggccccc tccctggatg acattaaaga 1560
agggttgagc tggtccctgc ctgcatgtga ctgtaaatcc ctcccatgtt ttctctgagt 1620
ctccctttgc ctgctgaggc tgtatgtggg ctccaggtaa cagtgctgtc ttcgggcccc 1680
ctgaactgtg ttcatggagc atctggctgg gtaggcacat gctgggcttg aatccagggg 1740
ggactgaatc ctcagcttac ggacctgggc ccatctgttt ctggagggct ccagtcttcc 1800
ttgtcctgtc ttggagtccc caagaaggaa tcacagggga ggaaccagat accagccatg 1860
accccaggct ccaccaagca tcttcatgtc cccctgctca tcccccactc ccccccaccc 1920
agagttgctc atcctgccag ggctggctgt gcccacccca aggctgccct cctgggggcc 1980
ccagaactgc ctgatcgtgc cgtggcccag ttttgtggca tctgcagcaa cacaagagag 2040
aggacaatgt cctcctcttg acccgctgtc acctaaccag actcgggccc tgcacctctc 2100
aggcacttct ggaaaatgac tgaggcagat tcttcctgaa gcccattctc catggggcaa 2160
caaggacacc tattctgtcc ttgtccttcc atcgctgccc cagaaagcct cacatatctc 2220
cgtttagaat caggtccctt ctccccagat gaagaggagg gtctctgctt tgttttctct 2280
atctcctcct cagacttgac caggcccagc aggccccaga agaccattac cctatatccc 2340
ttctcctccc tagtcacatg gccataggcc tgctgatggc tcaggaaggc cattgcaagg 2400
actcctcagc tatgggagag gaagcacatc acccattgac ccccgcaacc cctccctttc 2460
ctcctctgag tcccgactgg ggccacatgc agcctgactt ctttgtgcct gttgctgtcc 2520
ctgcagtctt cagagggcca ccgcagctcc agtgccacgg caggaggctg ttcctgaata 2580
gcccctgtgg taagggccag gagagtcctt ccatcctcca aggccctgct aaaggacaca 2640
gcagccagga agtcccctgg gcccctagct gaaggacagc ctgctccctc cgtctctacc 2700
aggaatggcc ttgtcctatg gaaggcactg ccccatccca aactaatcta ggaatcactg 2760
tctaaccact cactgtcatg aatgtgtact taaaggatga ggttgagtca taccaaatag 2820
tgatttcgat agttcaaaat ggtgaaatta gcaattctac atgattcagt ctaatcaatg 2880
gataccgact gtttcccaca caagtctcct gttctcttaa gcttactcac tgacagcctt 2940
tcactctcca caaatacatt aaagatatgg ccatcaccaa gccccctagg atgacaccag 3000
acctgagagt ctgaagacct ggatccaagt tctgactttt ccccctgaca gctgtgtgac 3060
cttcgtgaag tcgccaaacc tctctgagcc ccagtcattg ctagtaagac ctgcctttga 3120
gttggtatga tgttcaagtt agataacaaa atgtttatac ccattagaac agagaataaa 3180
tagaactaca tttcttgca 3199
<210> 3
<211> 3513
<212> ДНК
<213> Homo sapiens
<400> 3
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagggcg 240
gcagtaagtc ttcagcatca ggcattttgg ggtgactcag taaatggtag atcttgctac 300
cagtggaaca gccactaagg attctgcagt gagagcagag ggccagctaa gtggtactct 360
cccagagact gtctgactca cgccaccccc tccaccttgg acacaggacg ctgtggtttc 420
tgagccaggt acaatgactc ctttcgcagc ctcccccgtt gcccctctgg atccactgct 480
taaatacgga cgaggacagg gccctgtctc ctcagcttca ggcaccacca ctgacctggg 540
acagtgaatc gacaatgccg tcttctgtct cgtggggcat cctcctgctg gcaggcctgt 600
gctgcctggt ccctgtctcc ctggctgagg atccccaggg agatgctgcc cagaagacag 660
atacatccca ccatgatcag gatcacccaa ccttcaacaa gatcaccccc aacctggctg 720
agttcgcctt cagcctatac cgccagctgg cacaccagtc caacagcacc aatatcttct 780
tctccccagt gagcatcgct acagcctttg caatgctctc cctggggacc aaggctgaca 840
ctcacgatga aatcctggag ggcctgaatt tcaacctcac ggagattccg gaggctcaga 900
tccatgaagg cttccaggaa ctcctccgta ccctcaacca gccagacagc cagctccagc 960
tgaccaccgg caatggcctg ttcctcagcg agggcctgaa gctagtggat aagtttttgg 1020
aggatgttaa aaagttgtac cactcagaag ccttcactgt caacttcggg gacaccgaag 1080
aggccaagaa acagatcaac gattacgtgg agaagggtac tcaagggaaa attgtggatt 1140
tggtcaagga gcttgacaga gacacagttt ttgctctggt gaattacatc ttctttaaag 1200
gcaaatggga gagacccttt gaagtcaagg acaccgagga agaggacttc cacgtggacc 1260
aggtgaccac cgtgaaggtg cctatgatga agcgtttagg catgtttaac atccagcact 1320
gtaagaagct gtccagctgg gtgctgctga tgaaatacct gggcaatgcc accgccatct 1380
tcttcctgcc tgatgagggg aaactacagc acctggaaaa tgaactcacc cacgatatca 1440
tcaccaagtt cctggaaaat gaagacagaa ggtctgccag cttacattta cccaaactgt 1500
ccattactgg aacctatgat ctgaagagcg tcctgggtca actgggcatc actaaggtct 1560
tcagcaatgg ggctgacctc tccggggtca cagaggaggc acccctgaag ctctccaagg 1620
ccgtgcataa ggctgtgctg accatcgacg agaaagggac tgaagctgct ggggccatgt 1680
ttttagaggc catacccatg tctatccccc ccgaggtcaa gttcaacaaa ccctttgtct 1740
tcttaatgat tgaacaaaat accaagtctc ccctcttcat gggaaaagtg gtgaatccca 1800
cccaaaaata actgcctctc gctcctcaac ccctcccctc catccctggc cccctccctg 1860
gatgacatta aagaagggtt gagctggtcc ctgcctgcat gtgactgtaa atccctccca 1920
tgttttctct gagtctccct ttgcctgctg aggctgtatg tgggctccag gtaacagtgc 1980
tgtcttcggg ccccctgaac tgtgttcatg gagcatctgg ctgggtaggc acatgctggg 2040
cttgaatcca ggggggactg aatcctcagc ttacggacct gggcccatct gtttctggag 2100
ggctccagtc ttccttgtcc tgtcttggag tccccaagaa ggaatcacag gggaggaacc 2160
agataccagc catgacccca ggctccacca agcatcttca tgtccccctg ctcatccccc 2220
actccccccc acccagagtt gctcatcctg ccagggctgg ctgtgcccac cccaaggctg 2280
ccctcctggg ggccccagaa ctgcctgatc gtgccgtggc ccagttttgt ggcatctgca 2340
gcaacacaag agagaggaca atgtcctcct cttgacccgc tgtcacctaa ccagactcgg 2400
gccctgcacc tctcaggcac ttctggaaaa tgactgaggc agattcttcc tgaagcccat 2460
tctccatggg gcaacaagga cacctattct gtccttgtcc ttccatcgct gccccagaaa 2520
gcctcacata tctccgttta gaatcaggtc ccttctcccc agatgaagag gagggtctct 2580
gctttgtttt ctctatctcc tcctcagact tgaccaggcc cagcaggccc cagaagacca 2640
ttaccctata tcccttctcc tccctagtca catggccata ggcctgctga tggctcagga 2700
aggccattgc aaggactcct cagctatggg agaggaagca catcacccat tgacccccgc 2760
aacccctccc tttcctcctc tgagtcccga ctggggccac atgcagcctg acttctttgt 2820
gcctgttgct gtccctgcag tcttcagagg gccaccgcag ctccagtgcc acggcaggag 2880
gctgttcctg aatagcccct gtggtaaggg ccaggagagt ccttccatcc tccaaggccc 2940
tgctaaagga cacagcagcc aggaagtccc ctgggcccct agctgaagga cagcctgctc 3000
cctccgtctc taccaggaat ggccttgtcc tatggaaggc actgccccat cccaaactaa 3060
tctaggaatc actgtctaac cactcactgt catgaatgtg tacttaaagg atgaggttga 3120
gtcataccaa atagtgattt cgatagttca aaatggtgaa attagcaatt ctacatgatt 3180
cagtctaatc aatggatacc gactgtttcc cacacaagtc tcctgttctc ttaagcttac 3240
tcactgacag cctttcactc tccacaaata cattaaagat atggccatca ccaagccccc 3300
taggatgaca ccagacctga gagtctgaag acctggatcc aagttctgac ttttccccct 3360
gacagctgtg tgaccttcgt gaagtcgcca aacctctctg agccccagtc attgctagta 3420
agacctgcct ttgagttggt atgatgttca agttagataa caaaatgttt atacccatta 3480
gaacagagaa taaatagaac tacatttctt gca 3513
<210> 4
<211> 3236
<212> ДНК
<213> Homo sapiens
<400> 4
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaaggtgg 240
gacattgctg ctgctgctca ctcagttcca caggacaatg ccgtcttctg tctcgtgggg 300
catcctcctg ctggcaggcc tgtgctgcct ggtccctgtc tccctggctg aggatcccca 360
gggagatgct gcccagaaga cagatacatc ccaccatgat caggatcacc caaccttcaa 420
caagatcacc cccaacctgg ctgagttcgc cttcagccta taccgccagc tggcacacca 480
gtccaacagc accaatatct tcttctcccc agtgagcatc gctacagcct ttgcaatgct 540
ctccctgggg accaaggctg acactcacga tgaaatcctg gagggcctga atttcaacct 600
cacggagatt ccggaggctc agatccatga aggcttccag gaactcctcc gtaccctcaa 660
ccagccagac agccagctcc agctgaccac cggcaatggc ctgttcctca gcgagggcct 720
gaagctagtg gataagtttt tggaggatgt taaaaagttg taccactcag aagccttcac 780
tgtcaacttc ggggacaccg aagaggccaa gaaacagatc aacgattacg tggagaaggg 840
tactcaaggg aaaattgtgg atttggtcaa ggagcttgac agagacacag tttttgctct 900
ggtgaattac atcttcttta aaggcaaatg ggagagaccc tttgaagtca aggacaccga 960
ggaagaggac ttccacgtgg accaggtgac caccgtgaag gtgcctatga tgaagcgttt 1020
aggcatgttt aacatccagc actgtaagaa gctgtccagc tgggtgctgc tgatgaaata 1080
cctgggcaat gccaccgcca tcttcttcct gcctgatgag gggaaactac agcacctgga 1140
aaatgaactc acccacgata tcatcaccaa gttcctggaa aatgaagaca gaaggtctgc 1200
cagcttacat ttacccaaac tgtccattac tggaacctat gatctgaaga gcgtcctggg 1260
tcaactgggc atcactaagg tcttcagcaa tggggctgac ctctccgggg tcacagagga 1320
ggcacccctg aagctctcca aggccgtgca taaggctgtg ctgaccatcg acgagaaagg 1380
gactgaagct gctggggcca tgtttttaga ggccataccc atgtctatcc cccccgaggt 1440
caagttcaac aaaccctttg tcttcttaat gattgaacaa aataccaagt ctcccctctt 1500
catgggaaaa gtggtgaatc ccacccaaaa ataactgcct ctcgctcctc aacccctccc 1560
ctccatccct ggccccctcc ctggatgaca ttaaagaagg gttgagctgg tccctgcctg 1620
catgtgactg taaatccctc ccatgttttc tctgagtctc cctttgcctg ctgaggctgt 1680
atgtgggctc caggtaacag tgctgtcttc gggccccctg aactgtgttc atggagcatc 1740
tggctgggta ggcacatgct gggcttgaat ccagggggga ctgaatcctc agcttacgga 1800
cctgggccca tctgtttctg gagggctcca gtcttccttg tcctgtcttg gagtccccaa 1860
gaaggaatca caggggagga accagatacc agccatgacc ccaggctcca ccaagcatct 1920
tcatgtcccc ctgctcatcc cccactcccc cccacccaga gttgctcatc ctgccagggc 1980
tggctgtgcc caccccaagg ctgccctcct gggggcccca gaactgcctg atcgtgccgt 2040
ggcccagttt tgtggcatct gcagcaacac aagagagagg acaatgtcct cctcttgacc 2100
cgctgtcacc taaccagact cgggccctgc acctctcagg cacttctgga aaatgactga 2160
ggcagattct tcctgaagcc cattctccat ggggcaacaa ggacacctat tctgtccttg 2220
tccttccatc gctgccccag aaagcctcac atatctccgt ttagaatcag gtcccttctc 2280
cccagatgaa gaggagggtc tctgctttgt tttctctatc tcctcctcag acttgaccag 2340
gcccagcagg ccccagaaga ccattaccct atatcccttc tcctccctag tcacatggcc 2400
ataggcctgc tgatggctca ggaaggccat tgcaaggact cctcagctat gggagaggaa 2460
gcacatcacc cattgacccc cgcaacccct ccctttcctc ctctgagtcc cgactggggc 2520
cacatgcagc ctgacttctt tgtgcctgtt gctgtccctg cagtcttcag agggccaccg 2580
cagctccagt gccacggcag gaggctgttc ctgaatagcc cctgtggtaa gggccaggag 2640
agtccttcca tcctccaagg ccctgctaaa ggacacagca gccaggaagt cccctgggcc 2700
cctagctgaa ggacagcctg ctccctccgt ctctaccagg aatggccttg tcctatggaa 2760
ggcactgccc catcccaaac taatctagga atcactgtct aaccactcac tgtcatgaat 2820
gtgtacttaa aggatgaggt tgagtcatac caaatagtga tttcgatagt tcaaaatggt 2880
gaaattagca attctacatg attcagtcta atcaatggat accgactgtt tcccacacaa 2940
gtctcctgtt ctcttaagct tactcactga cagcctttca ctctccacaa atacattaaa 3000
gatatggcca tcaccaagcc ccctaggatg acaccagacc tgagagtctg aagacctgga 3060
tccaagttct gacttttccc cctgacagct gtgtgacctt cgtgaagtcg ccaaacctct 3120
ctgagcccca gtcattgcta gtaagacctg cctttgagtt ggtatgatgt tcaagttaga 3180
taacaaaatg tttataccca ttagaacaga gaataaatag aactacattt cttgca 3236
<210> 5
<211> 3532
<212> ДНК
<213> Homo sapiens
<400> 5
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaaggtgg 240
gacattgctg ctgctgctca ctcagttcca cagggcggca gtaagtcttc agcatcaggc 300
attttggggt gactcagtaa atggtagatc ttgctaccag tggaacagcc actaaggatt 360
ctgcagtgag agcagagggc cagctaagtg gtactctccc agagactgtc tgactcacgc 420
caccccctcc accttggaca caggacgctg tggtttctga gccagcagcc tcccccgttg 480
cccctctgga tccactgctt aaatacggac gaggacaggg ccctgtctcc tcagcttcag 540
gcaccaccac tgacctggga cagtgaatcg acaatgccgt cttctgtctc gtggggcatc 600
ctcctgctgg caggcctgtg ctgcctggtc cctgtctccc tggctgagga tccccaggga 660
gatgctgccc agaagacaga tacatcccac catgatcagg atcacccaac cttcaacaag 720
atcaccccca acctggctga gttcgccttc agcctatacc gccagctggc acaccagtcc 780
aacagcacca atatcttctt ctccccagtg agcatcgcta cagcctttgc aatgctctcc 840
ctggggacca aggctgacac tcacgatgaa atcctggagg gcctgaattt caacctcacg 900
gagattccgg aggctcagat ccatgaaggc ttccaggaac tcctccgtac cctcaaccag 960
ccagacagcc agctccagct gaccaccggc aatggcctgt tcctcagcga gggcctgaag 1020
ctagtggata agtttttgga ggatgttaaa aagttgtacc actcagaagc cttcactgtc 1080
aacttcgggg acaccgaaga ggccaagaaa cagatcaacg attacgtgga gaagggtact 1140
caagggaaaa ttgtggattt ggtcaaggag cttgacagag acacagtttt tgctctggtg 1200
aattacatct tctttaaagg caaatgggag agaccctttg aagtcaagga caccgaggaa 1260
gaggacttcc acgtggacca ggtgaccacc gtgaaggtgc ctatgatgaa gcgtttaggc 1320
atgtttaaca tccagcactg taagaagctg tccagctggg tgctgctgat gaaatacctg 1380
ggcaatgcca ccgccatctt cttcctgcct gatgagggga aactacagca cctggaaaat 1440
gaactcaccc acgatatcat caccaagttc ctggaaaatg aagacagaag gtctgccagc 1500
ttacatttac ccaaactgtc cattactgga acctatgatc tgaagagcgt cctgggtcaa 1560
ctgggcatca ctaaggtctt cagcaatggg gctgacctct ccggggtcac agaggaggca 1620
cccctgaagc tctccaaggc cgtgcataag gctgtgctga ccatcgacga gaaagggact 1680
gaagctgctg gggccatgtt tttagaggcc atacccatgt ctatcccccc cgaggtcaag 1740
ttcaacaaac cctttgtctt cttaatgatt gaacaaaata ccaagtctcc cctcttcatg 1800
ggaaaagtgg tgaatcccac ccaaaaataa ctgcctctcg ctcctcaacc cctcccctcc 1860
atccctggcc ccctccctgg atgacattaa agaagggttg agctggtccc tgcctgcatg 1920
tgactgtaaa tccctcccat gttttctctg agtctccctt tgcctgctga ggctgtatgt 1980
gggctccagg taacagtgct gtcttcgggc cccctgaact gtgttcatgg agcatctggc 2040
tgggtaggca catgctgggc ttgaatccag gggggactga atcctcagct tacggacctg 2100
ggcccatctg tttctggagg gctccagtct tccttgtcct gtcttggagt ccccaagaag 2160
gaatcacagg ggaggaacca gataccagcc atgaccccag gctccaccaa gcatcttcat 2220
gtccccctgc tcatccccca ctccccccca cccagagttg ctcatcctgc cagggctggc 2280
tgtgcccacc ccaaggctgc cctcctgggg gccccagaac tgcctgatcg tgccgtggcc 2340
cagttttgtg gcatctgcag caacacaaga gagaggacaa tgtcctcctc ttgacccgct 2400
gtcacctaac cagactcggg ccctgcacct ctcaggcact tctggaaaat gactgaggca 2460
gattcttcct gaagcccatt ctccatgggg caacaaggac acctattctg tccttgtcct 2520
tccatcgctg ccccagaaag cctcacatat ctccgtttag aatcaggtcc cttctcccca 2580
gatgaagagg agggtctctg ctttgttttc tctatctcct cctcagactt gaccaggccc 2640
agcaggcccc agaagaccat taccctatat cccttctcct ccctagtcac atggccatag 2700
gcctgctgat ggctcaggaa ggccattgca aggactcctc agctatggga gaggaagcac 2760
atcacccatt gacccccgca acccctccct ttcctcctct gagtcccgac tggggccaca 2820
tgcagcctga cttctttgtg cctgttgctg tccctgcagt cttcagaggg ccaccgcagc 2880
tccagtgcca cggcaggagg ctgttcctga atagcccctg tggtaagggc caggagagtc 2940
cttccatcct ccaaggccct gctaaaggac acagcagcca ggaagtcccc tgggccccta 3000
gctgaaggac agcctgctcc ctccgtctct accaggaatg gccttgtcct atggaaggca 3060
ctgccccatc ccaaactaat ctaggaatca ctgtctaacc actcactgtc atgaatgtgt 3120
acttaaagga tgaggttgag tcataccaaa tagtgatttc gatagttcaa aatggtgaaa 3180
ttagcaattc tacatgattc agtctaatca atggataccg actgtttccc acacaagtct 3240
cctgttctct taagcttact cactgacagc ctttcactct ccacaaatac attaaagata 3300
tggccatcac caagccccct aggatgacac cagacctgag agtctgaaga cctggatcca 3360
agttctgact tttccccctg acagctgtgt gaccttcgtg aagtcgccaa acctctctga 3420
gccccagtca ttgctagtaa gacctgcctt tgagttggta tgatgttcaa gttagataac 3480
aaaatgttta tacccattag aacagagaat aaatagaact acatttcttg ca 3532
<210> 6
<211> 3340
<212> ДНК
<213> Homo sapiens
<400> 6
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaaggtgg 240
gacattgctg ctgctgctca ctcagttcca cagcagcctc ccccgttgcc cctctggatc 300
cactgcttaa atacggacga ggacagggcc ctgtctcctc agcttcaggc accaccactg 360
acctgggaca gtgaatcgac aatgccgtct tctgtctcgt ggggcatcct cctgctggca 420
ggcctgtgct gcctggtccc tgtctccctg gctgaggatc cccagggaga tgctgcccag 480
aagacagata catcccacca tgatcaggat cacccaacct tcaacaagat cacccccaac 540
ctggctgagt tcgccttcag cctataccgc cagctggcac accagtccaa cagcaccaat 600
atcttcttct ccccagtgag catcgctaca gcctttgcaa tgctctccct ggggaccaag 660
gctgacactc acgatgaaat cctggagggc ctgaatttca acctcacgga gattccggag 720
gctcagatcc atgaaggctt ccaggaactc ctccgtaccc tcaaccagcc agacagccag 780
ctccagctga ccaccggcaa tggcctgttc ctcagcgagg gcctgaagct agtggataag 840
tttttggagg atgttaaaaa gttgtaccac tcagaagcct tcactgtcaa cttcggggac 900
accgaagagg ccaagaaaca gatcaacgat tacgtggaga agggtactca agggaaaatt 960
gtggatttgg tcaaggagct tgacagagac acagtttttg ctctggtgaa ttacatcttc 1020
tttaaaggca aatgggagag accctttgaa gtcaaggaca ccgaggaaga ggacttccac 1080
gtggaccagg tgaccaccgt gaaggtgcct atgatgaagc gtttaggcat gtttaacatc 1140
cagcactgta agaagctgtc cagctgggtg ctgctgatga aatacctggg caatgccacc 1200
gccatcttct tcctgcctga tgaggggaaa ctacagcacc tggaaaatga actcacccac 1260
gatatcatca ccaagttcct ggaaaatgaa gacagaaggt ctgccagctt acatttaccc 1320
aaactgtcca ttactggaac ctatgatctg aagagcgtcc tgggtcaact gggcatcact 1380
aaggtcttca gcaatggggc tgacctctcc ggggtcacag aggaggcacc cctgaagctc 1440
tccaaggccg tgcataaggc tgtgctgacc atcgacgaga aagggactga agctgctggg 1500
gccatgtttt tagaggccat acccatgtct atcccccccg aggtcaagtt caacaaaccc 1560
tttgtcttct taatgattga acaaaatacc aagtctcccc tcttcatggg aaaagtggtg 1620
aatcccaccc aaaaataact gcctctcgct cctcaacccc tcccctccat ccctggcccc 1680
ctccctggat gacattaaag aagggttgag ctggtccctg cctgcatgtg actgtaaatc 1740
cctcccatgt tttctctgag tctccctttg cctgctgagg ctgtatgtgg gctccaggta 1800
acagtgctgt cttcgggccc cctgaactgt gttcatggag catctggctg ggtaggcaca 1860
tgctgggctt gaatccaggg gggactgaat cctcagctta cggacctggg cccatctgtt 1920
tctggagggc tccagtcttc cttgtcctgt cttggagtcc ccaagaagga atcacagggg 1980
aggaaccaga taccagccat gaccccaggc tccaccaagc atcttcatgt ccccctgctc 2040
atcccccact cccccccacc cagagttgct catcctgcca gggctggctg tgcccacccc 2100
aaggctgccc tcctgggggc cccagaactg cctgatcgtg ccgtggccca gttttgtggc 2160
atctgcagca acacaagaga gaggacaatg tcctcctctt gacccgctgt cacctaacca 2220
gactcgggcc ctgcacctct caggcacttc tggaaaatga ctgaggcaga ttcttcctga 2280
agcccattct ccatggggca acaaggacac ctattctgtc cttgtccttc catcgctgcc 2340
ccagaaagcc tcacatatct ccgtttagaa tcaggtccct tctccccaga tgaagaggag 2400
ggtctctgct ttgttttctc tatctcctcc tcagacttga ccaggcccag caggccccag 2460
aagaccatta ccctatatcc cttctcctcc ctagtcacat ggccataggc ctgctgatgg 2520
ctcaggaagg ccattgcaag gactcctcag ctatgggaga ggaagcacat cacccattga 2580
cccccgcaac ccctcccttt cctcctctga gtcccgactg gggccacatg cagcctgact 2640
tctttgtgcc tgttgctgtc cctgcagtct tcagagggcc accgcagctc cagtgccacg 2700
gcaggaggct gttcctgaat agcccctgtg gtaagggcca ggagagtcct tccatcctcc 2760
aaggccctgc taaaggacac agcagccagg aagtcccctg ggcccctagc tgaaggacag 2820
cctgctccct ccgtctctac caggaatggc cttgtcctat ggaaggcact gccccatccc 2880
aaactaatct aggaatcact gtctaaccac tcactgtcat gaatgtgtac ttaaaggatg 2940
aggttgagtc ataccaaata gtgatttcga tagttcaaaa tggtgaaatt agcaattcta 3000
catgattcag tctaatcaat ggataccgac tgtttcccac acaagtctcc tgttctctta 3060
agcttactca ctgacagcct ttcactctcc acaaatacat taaagatatg gccatcacca 3120
agccccctag gatgacacca gacctgagag tctgaagacc tggatccaag ttctgacttt 3180
tccccctgac agctgtgtga ccttcgtgaa gtcgccaaac ctctctgagc cccagtcatt 3240
gctagtaaga cctgcctttg agttggtatg atgttcaagt tagataacaa aatgtttata 3300
cccattagaa cagagaataa atagaactac atttcttgca 3340
<210> 7
<211> 3495
<212> ДНК
<213> Homo sapiens
<400> 7
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagggcg 240
gcagtaagtc ttcagcatca ggcattttgg ggtgactcag taaatggtag atcttgctac 300
cagtggaaca gccactaagg attctgcagt gagagcagag ggccagctaa gtggtactct 360
cccagagact gtctgactca cgccaccccc tccaccttgg acacaggacg ctgtggtttc 420
tgagccagca gcctcccccg ttgcccctct ggatccactg cttaaatacg gacgaggaca 480
gggccctgtc tcctcagctt caggcaccac cactgacctg ggacagtgaa tcgacaatgc 540
cgtcttctgt ctcgtggggc atcctcctgc tggcaggcct gtgctgcctg gtccctgtct 600
ccctggctga ggatccccag ggagatgctg cccagaagac agatacatcc caccatgatc 660
aggatcaccc aaccttcaac aagatcaccc ccaacctggc tgagttcgcc ttcagcctat 720
accgccagct ggcacaccag tccaacagca ccaatatctt cttctcccca gtgagcatcg 780
ctacagcctt tgcaatgctc tccctgggga ccaaggctga cactcacgat gaaatcctgg 840
agggcctgaa tttcaacctc acggagattc cggaggctca gatccatgaa ggcttccagg 900
aactcctccg taccctcaac cagccagaca gccagctcca gctgaccacc ggcaatggcc 960
tgttcctcag cgagggcctg aagctagtgg ataagttttt ggaggatgtt aaaaagttgt 1020
accactcaga agccttcact gtcaacttcg gggacaccga agaggccaag aaacagatca 1080
acgattacgt ggagaagggt actcaaggga aaattgtgga tttggtcaag gagcttgaca 1140
gagacacagt ttttgctctg gtgaattaca tcttctttaa aggcaaatgg gagagaccct 1200
ttgaagtcaa ggacaccgag gaagaggact tccacgtgga ccaggtgacc accgtgaagg 1260
tgcctatgat gaagcgttta ggcatgttta acatccagca ctgtaagaag ctgtccagct 1320
gggtgctgct gatgaaatac ctgggcaatg ccaccgccat cttcttcctg cctgatgagg 1380
ggaaactaca gcacctggaa aatgaactca cccacgatat catcaccaag ttcctggaaa 1440
atgaagacag aaggtctgcc agcttacatt tacccaaact gtccattact ggaacctatg 1500
atctgaagag cgtcctgggt caactgggca tcactaaggt cttcagcaat ggggctgacc 1560
tctccggggt cacagaggag gcacccctga agctctccaa ggccgtgcat aaggctgtgc 1620
tgaccatcga cgagaaaggg actgaagctg ctggggccat gtttttagag gccataccca 1680
tgtctatccc ccccgaggtc aagttcaaca aaccctttgt cttcttaatg attgaacaaa 1740
ataccaagtc tcccctcttc atgggaaaag tggtgaatcc cacccaaaaa taactgcctc 1800
tcgctcctca acccctcccc tccatccctg gccccctccc tggatgacat taaagaaggg 1860
ttgagctggt ccctgcctgc atgtgactgt aaatccctcc catgttttct ctgagtctcc 1920
ctttgcctgc tgaggctgta tgtgggctcc aggtaacagt gctgtcttcg ggccccctga 1980
actgtgttca tggagcatct ggctgggtag gcacatgctg ggcttgaatc caggggggac 2040
tgaatcctca gcttacggac ctgggcccat ctgtttctgg agggctccag tcttccttgt 2100
cctgtcttgg agtccccaag aaggaatcac aggggaggaa ccagatacca gccatgaccc 2160
caggctccac caagcatctt catgtccccc tgctcatccc ccactccccc ccacccagag 2220
ttgctcatcc tgccagggct ggctgtgccc accccaaggc tgccctcctg ggggccccag 2280
aactgcctga tcgtgccgtg gcccagtttt gtggcatctg cagcaacaca agagagagga 2340
caatgtcctc ctcttgaccc gctgtcacct aaccagactc gggccctgca cctctcaggc 2400
acttctggaa aatgactgag gcagattctt cctgaagccc attctccatg gggcaacaag 2460
gacacctatt ctgtccttgt ccttccatcg ctgccccaga aagcctcaca tatctccgtt 2520
tagaatcagg tcccttctcc ccagatgaag aggagggtct ctgctttgtt ttctctatct 2580
cctcctcaga cttgaccagg cccagcaggc cccagaagac cattacccta tatcccttct 2640
cctccctagt cacatggcca taggcctgct gatggctcag gaaggccatt gcaaggactc 2700
ctcagctatg ggagaggaag cacatcaccc attgaccccc gcaacccctc cctttcctcc 2760
tctgagtccc gactggggcc acatgcagcc tgacttcttt gtgcctgttg ctgtccctgc 2820
agtcttcaga gggccaccgc agctccagtg ccacggcagg aggctgttcc tgaatagccc 2880
ctgtggtaag ggccaggaga gtccttccat cctccaaggc cctgctaaag gacacagcag 2940
ccaggaagtc ccctgggccc ctagctgaag gacagcctgc tccctccgtc tctaccagga 3000
atggccttgt cctatggaag gcactgcccc atcccaaact aatctaggaa tcactgtcta 3060
accactcact gtcatgaatg tgtacttaaa ggatgaggtt gagtcatacc aaatagtgat 3120
ttcgatagtt caaaatggtg aaattagcaa ttctacatga ttcagtctaa tcaatggata 3180
ccgactgttt cccacacaag tctcctgttc tcttaagctt actcactgac agcctttcac 3240
tctccacaaa tacattaaag atatggccat caccaagccc cctaggatga caccagacct 3300
gagagtctga agacctggat ccaagttctg acttttcccc ctgacagctg tgtgaccttc 3360
gtgaagtcgc caaacctctc tgagccccag tcattgctag taagacctgc ctttgagttg 3420
gtatgatgtt caagttagat aacaaaatgt ttatacccat tagaacagag aataaataga 3480
actacatttc ttgca 3495
<210> 8
<211> 3492
<212> ДНК
<213> Homo sapiens
<400> 8
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagggcg 240
gcagtaagtc ttcagcatca ggcattttgg ggtgactcag taaatggtag atcttgctac 300
cagtggaaca gccactaagg attctgcagt gagagcagag ggccagctaa gtggtactct 360
cccagagact gtctgactca cgccaccccc tccaccttgg acacaggacg ctgtggtttc 420
tgagccagcc tcccccgttg cccctctgga tccactgctt aaatacggac gaggacaggg 480
ccctgtctcc tcagcttcag gcaccaccac tgacctggga cagtgaatcg acaatgccgt 540
cttctgtctc gtggggcatc ctcctgctgg caggcctgtg ctgcctggtc cctgtctccc 600
tggctgagga tccccaggga gatgctgccc agaagacaga tacatcccac catgatcagg 660
atcacccaac cttcaacaag atcaccccca acctggctga gttcgccttc agcctatacc 720
gccagctggc acaccagtcc aacagcacca atatcttctt ctccccagtg agcatcgcta 780
cagcctttgc aatgctctcc ctggggacca aggctgacac tcacgatgaa atcctggagg 840
gcctgaattt caacctcacg gagattccgg aggctcagat ccatgaaggc ttccaggaac 900
tcctccgtac cctcaaccag ccagacagcc agctccagct gaccaccggc aatggcctgt 960
tcctcagcga gggcctgaag ctagtggata agtttttgga ggatgttaaa aagttgtacc 1020
actcagaagc cttcactgtc aacttcgggg acaccgaaga ggccaagaaa cagatcaacg 1080
attacgtgga gaagggtact caagggaaaa ttgtggattt ggtcaaggag cttgacagag 1140
acacagtttt tgctctggtg aattacatct tctttaaagg caaatgggag agaccctttg 1200
aagtcaagga caccgaggaa gaggacttcc acgtggacca ggtgaccacc gtgaaggtgc 1260
ctatgatgaa gcgtttaggc atgtttaaca tccagcactg taagaagctg tccagctggg 1320
tgctgctgat gaaatacctg ggcaatgcca ccgccatctt cttcctgcct gatgagggga 1380
aactacagca cctggaaaat gaactcaccc acgatatcat caccaagttc ctggaaaatg 1440
aagacagaag gtctgccagc ttacatttac ccaaactgtc cattactgga acctatgatc 1500
tgaagagcgt cctgggtcaa ctgggcatca ctaaggtctt cagcaatggg gctgacctct 1560
ccggggtcac agaggaggca cccctgaagc tctccaaggc cgtgcataag gctgtgctga 1620
ccatcgacga gaaagggact gaagctgctg gggccatgtt tttagaggcc atacccatgt 1680
ctatcccccc cgaggtcaag ttcaacaaac cctttgtctt cttaatgatt gaacaaaata 1740
ccaagtctcc cctcttcatg ggaaaagtgg tgaatcccac ccaaaaataa ctgcctctcg 1800
ctcctcaacc cctcccctcc atccctggcc ccctccctgg atgacattaa agaagggttg 1860
agctggtccc tgcctgcatg tgactgtaaa tccctcccat gttttctctg agtctccctt 1920
tgcctgctga ggctgtatgt gggctccagg taacagtgct gtcttcgggc cccctgaact 1980
gtgttcatgg agcatctggc tgggtaggca catgctgggc ttgaatccag gggggactga 2040
atcctcagct tacggacctg ggcccatctg tttctggagg gctccagtct tccttgtcct 2100
gtcttggagt ccccaagaag gaatcacagg ggaggaacca gataccagcc atgaccccag 2160
gctccaccaa gcatcttcat gtccccctgc tcatccccca ctccccccca cccagagttg 2220
ctcatcctgc cagggctggc tgtgcccacc ccaaggctgc cctcctgggg gccccagaac 2280
tgcctgatcg tgccgtggcc cagttttgtg gcatctgcag caacacaaga gagaggacaa 2340
tgtcctcctc ttgacccgct gtcacctaac cagactcggg ccctgcacct ctcaggcact 2400
tctggaaaat gactgaggca gattcttcct gaagcccatt ctccatgggg caacaaggac 2460
acctattctg tccttgtcct tccatcgctg ccccagaaag cctcacatat ctccgtttag 2520
aatcaggtcc cttctcccca gatgaagagg agggtctctg ctttgttttc tctatctcct 2580
cctcagactt gaccaggccc agcaggcccc agaagaccat taccctatat cccttctcct 2640
ccctagtcac atggccatag gcctgctgat ggctcaggaa ggccattgca aggactcctc 2700
agctatggga gaggaagcac atcacccatt gacccccgca acccctccct ttcctcctct 2760
gagtcccgac tggggccaca tgcagcctga cttctttgtg cctgttgctg tccctgcagt 2820
cttcagaggg ccaccgcagc tccagtgcca cggcaggagg ctgttcctga atagcccctg 2880
tggtaagggc caggagagtc cttccatcct ccaaggccct gctaaaggac acagcagcca 2940
ggaagtcccc tgggccccta gctgaaggac agcctgctcc ctccgtctct accaggaatg 3000
gccttgtcct atggaaggca ctgccccatc ccaaactaat ctaggaatca ctgtctaacc 3060
actcactgtc atgaatgtgt acttaaagga tgaggttgag tcataccaaa tagtgatttc 3120
gatagttcaa aatggtgaaa ttagcaattc tacatgattc agtctaatca atggataccg 3180
actgtttccc acacaagtct cctgttctct taagcttact cactgacagc ctttcactct 3240
ccacaaatac attaaagata tggccatcac caagccccct aggatgacac cagacctgag 3300
agtctgaaga cctggatcca agttctgact tttccccctg acagctgtgt gaccttcgtg 3360
aagtcgccaa acctctctga gccccagtca ttgctagtaa gacctgcctt tgagttggta 3420
tgatgttcaa gttagataac aaaatgttta tacccattag aacagagaat aaatagaact 3480
acatttcttg ca 3492
<210> 9
<211> 3510
<212> ДНК
<213> Homo sapiens
<400> 9
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagggcg 240
gcagtaagtc ttcagcatca ggcattttgg ggtgactcag taaatggtag atcttgctac 300
cagtggaaca gccactaagg attctgcagt gagagcagag ggccagctaa gtggtactct 360
cccagagact gtctgactca cgccaccccc tccaccttgg acacaggacg ctgtggtttc 420
tgagccaggt acaatgactc ctttcgcctc ccccgttgcc cctctggatc cactgcttaa 480
atacggacga ggacagggcc ctgtctcctc agcttcaggc accaccactg acctgggaca 540
gtgaatcgac aatgccgtct tctgtctcgt ggggcatcct cctgctggca ggcctgtgct 600
gcctggtccc tgtctccctg gctgaggatc cccagggaga tgctgcccag aagacagata 660
catcccacca tgatcaggat cacccaacct tcaacaagat cacccccaac ctggctgagt 720
tcgccttcag cctataccgc cagctggcac accagtccaa cagcaccaat atcttcttct 780
ccccagtgag catcgctaca gcctttgcaa tgctctccct ggggaccaag gctgacactc 840
acgatgaaat cctggagggc ctgaatttca acctcacgga gattccggag gctcagatcc 900
atgaaggctt ccaggaactc ctccgtaccc tcaaccagcc agacagccag ctccagctga 960
ccaccggcaa tggcctgttc ctcagcgagg gcctgaagct agtggataag tttttggagg 1020
atgttaaaaa gttgtaccac tcagaagcct tcactgtcaa cttcggggac accgaagagg 1080
ccaagaaaca gatcaacgat tacgtggaga agggtactca agggaaaatt gtggatttgg 1140
tcaaggagct tgacagagac acagtttttg ctctggtgaa ttacatcttc tttaaaggca 1200
aatgggagag accctttgaa gtcaaggaca ccgaggaaga ggacttccac gtggaccagg 1260
tgaccaccgt gaaggtgcct atgatgaagc gtttaggcat gtttaacatc cagcactgta 1320
agaagctgtc cagctgggtg ctgctgatga aatacctggg caatgccacc gccatcttct 1380
tcctgcctga tgaggggaaa ctacagcacc tggaaaatga actcacccac gatatcatca 1440
ccaagttcct ggaaaatgaa gacagaaggt ctgccagctt acatttaccc aaactgtcca 1500
ttactggaac ctatgatctg aagagcgtcc tgggtcaact gggcatcact aaggtcttca 1560
gcaatggggc tgacctctcc ggggtcacag aggaggcacc cctgaagctc tccaaggccg 1620
tgcataaggc tgtgctgacc atcgacgaga aagggactga agctgctggg gccatgtttt 1680
tagaggccat acccatgtct atcccccccg aggtcaagtt caacaaaccc tttgtcttct 1740
taatgattga acaaaatacc aagtctcccc tcttcatggg aaaagtggtg aatcccaccc 1800
aaaaataact gcctctcgct cctcaacccc tcccctccat ccctggcccc ctccctggat 1860
gacattaaag aagggttgag ctggtccctg cctgcatgtg actgtaaatc cctcccatgt 1920
tttctctgag tctccctttg cctgctgagg ctgtatgtgg gctccaggta acagtgctgt 1980
cttcgggccc cctgaactgt gttcatggag catctggctg ggtaggcaca tgctgggctt 2040
gaatccaggg gggactgaat cctcagctta cggacctggg cccatctgtt tctggagggc 2100
tccagtcttc cttgtcctgt cttggagtcc ccaagaagga atcacagggg aggaaccaga 2160
taccagccat gaccccaggc tccaccaagc atcttcatgt ccccctgctc atcccccact 2220
cccccccacc cagagttgct catcctgcca gggctggctg tgcccacccc aaggctgccc 2280
tcctgggggc cccagaactg cctgatcgtg ccgtggccca gttttgtggc atctgcagca 2340
acacaagaga gaggacaatg tcctcctctt gacccgctgt cacctaacca gactcgggcc 2400
ctgcacctct caggcacttc tggaaaatga ctgaggcaga ttcttcctga agcccattct 2460
ccatggggca acaaggacac ctattctgtc cttgtccttc catcgctgcc ccagaaagcc 2520
tcacatatct ccgtttagaa tcaggtccct tctccccaga tgaagaggag ggtctctgct 2580
ttgttttctc tatctcctcc tcagacttga ccaggcccag caggccccag aagaccatta 2640
ccctatatcc cttctcctcc ctagtcacat ggccataggc ctgctgatgg ctcaggaagg 2700
ccattgcaag gactcctcag ctatgggaga ggaagcacat cacccattga cccccgcaac 2760
ccctcccttt cctcctctga gtcccgactg gggccacatg cagcctgact tctttgtgcc 2820
tgttgctgtc cctgcagtct tcagagggcc accgcagctc cagtgccacg gcaggaggct 2880
gttcctgaat agcccctgtg gtaagggcca ggagagtcct tccatcctcc aaggccctgc 2940
taaaggacac agcagccagg aagtcccctg ggcccctagc tgaaggacag cctgctccct 3000
ccgtctctac caggaatggc cttgtcctat ggaaggcact gccccatccc aaactaatct 3060
aggaatcact gtctaaccac tcactgtcat gaatgtgtac ttaaaggatg aggttgagtc 3120
ataccaaata gtgatttcga tagttcaaaa tggtgaaatt agcaattcta catgattcag 3180
tctaatcaat ggataccgac tgtttcccac acaagtctcc tgttctctta agcttactca 3240
ctgacagcct ttcactctcc acaaatacat taaagatatg gccatcacca agccccctag 3300
gatgacacca gacctgagag tctgaagacc tggatccaag ttctgacttt tccccctgac 3360
agctgtgtga ccttcgtgaa gtcgccaaac ctctctgagc cccagtcatt gctagtaaga 3420
cctgcctttg agttggtatg atgttcaagt tagataacaa aatgtttata cccattagaa 3480
cagagaataa atagaactac atttcttgca 3510
<210> 10
<211> 3303
<212> ДНК
<213> Homo sapiens
<400> 10
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagcagc 240
ctcccccgtt gcccctctgg atccactgct taaatacgga cgaggacagg gccctgtctc 300
ctcagcttca ggcaccacca ctgacctggg acagtgaatc gacaatgccg tcttctgtct 360
cgtggggcat cctcctgctg gcaggcctgt gctgcctggt ccctgtctcc ctggctgagg 420
atccccaggg agatgctgcc cagaagacag atacatccca ccatgatcag gatcacccaa 480
ccttcaacaa gatcaccccc aacctggctg agttcgcctt cagcctatac cgccagctgg 540
cacaccagtc caacagcacc aatatcttct tctccccagt gagcatcgct acagcctttg 600
caatgctctc cctggggacc aaggctgaca ctcacgatga aatcctggag ggcctgaatt 660
tcaacctcac ggagattccg gaggctcaga tccatgaagg cttccaggaa ctcctccgta 720
ccctcaacca gccagacagc cagctccagc tgaccaccgg caatggcctg ttcctcagcg 780
agggcctgaa gctagtggat aagtttttgg aggatgttaa aaagttgtac cactcagaag 840
ccttcactgt caacttcggg gacaccgaag aggccaagaa acagatcaac gattacgtgg 900
agaagggtac tcaagggaaa attgtggatt tggtcaagga gcttgacaga gacacagttt 960
ttgctctggt gaattacatc ttctttaaag gcaaatggga gagacccttt gaagtcaagg 1020
acaccgagga agaggacttc cacgtggacc aggtgaccac cgtgaaggtg cctatgatga 1080
agcgtttagg catgtttaac atccagcact gtaagaagct gtccagctgg gtgctgctga 1140
tgaaatacct gggcaatgcc accgccatct tcttcctgcc tgatgagggg aaactacagc 1200
acctggaaaa tgaactcacc cacgatatca tcaccaagtt cctggaaaat gaagacagaa 1260
ggtctgccag cttacattta cccaaactgt ccattactgg aacctatgat ctgaagagcg 1320
tcctgggtca actgggcatc actaaggtct tcagcaatgg ggctgacctc tccggggtca 1380
cagaggaggc acccctgaag ctctccaagg ccgtgcataa ggctgtgctg accatcgacg 1440
agaaagggac tgaagctgct ggggccatgt ttttagaggc catacccatg tctatccccc 1500
ccgaggtcaa gttcaacaaa ccctttgtct tcttaatgat tgaacaaaat accaagtctc 1560
ccctcttcat gggaaaagtg gtgaatccca cccaaaaata actgcctctc gctcctcaac 1620
ccctcccctc catccctggc cccctccctg gatgacatta aagaagggtt gagctggtcc 1680
ctgcctgcat gtgactgtaa atccctccca tgttttctct gagtctccct ttgcctgctg 1740
aggctgtatg tgggctccag gtaacagtgc tgtcttcggg ccccctgaac tgtgttcatg 1800
gagcatctgg ctgggtaggc acatgctggg cttgaatcca ggggggactg aatcctcagc 1860
ttacggacct gggcccatct gtttctggag ggctccagtc ttccttgtcc tgtcttggag 1920
tccccaagaa ggaatcacag gggaggaacc agataccagc catgacccca ggctccacca 1980
agcatcttca tgtccccctg ctcatccccc actccccccc acccagagtt gctcatcctg 2040
ccagggctgg ctgtgcccac cccaaggctg ccctcctggg ggccccagaa ctgcctgatc 2100
gtgccgtggc ccagttttgt ggcatctgca gcaacacaag agagaggaca atgtcctcct 2160
cttgacccgc tgtcacctaa ccagactcgg gccctgcacc tctcaggcac ttctggaaaa 2220
tgactgaggc agattcttcc tgaagcccat tctccatggg gcaacaagga cacctattct 2280
gtccttgtcc ttccatcgct gccccagaaa gcctcacata tctccgttta gaatcaggtc 2340
ccttctcccc agatgaagag gagggtctct gctttgtttt ctctatctcc tcctcagact 2400
tgaccaggcc cagcaggccc cagaagacca ttaccctata tcccttctcc tccctagtca 2460
catggccata ggcctgctga tggctcagga aggccattgc aaggactcct cagctatggg 2520
agaggaagca catcacccat tgacccccgc aacccctccc tttcctcctc tgagtcccga 2580
ctggggccac atgcagcctg acttctttgt gcctgttgct gtccctgcag tcttcagagg 2640
gccaccgcag ctccagtgcc acggcaggag gctgttcctg aatagcccct gtggtaaggg 2700
ccaggagagt ccttccatcc tccaaggccc tgctaaagga cacagcagcc aggaagtccc 2760
ctgggcccct agctgaagga cagcctgctc cctccgtctc taccaggaat ggccttgtcc 2820
tatggaaggc actgccccat cccaaactaa tctaggaatc actgtctaac cactcactgt 2880
catgaatgtg tacttaaagg atgaggttga gtcataccaa atagtgattt cgatagttca 2940
aaatggtgaa attagcaatt ctacatgatt cagtctaatc aatggatacc gactgtttcc 3000
cacacaagtc tcctgttctc ttaagcttac tcactgacag cctttcactc tccacaaata 3060
cattaaagat atggccatca ccaagccccc taggatgaca ccagacctga gagtctgaag 3120
acctggatcc aagttctgac ttttccccct gacagctgtg tgaccttcgt gaagtcgcca 3180
aacctctctg agccccagtc attgctagta agacctgcct ttgagttggt atgatgttca 3240
agttagataa caaaatgttt atacccatta gaacagagaa taaatagaac tacatttctt 3300
gca 3303
<210> 11
<211> 3300
<212> ДНК
<213> Homo sapiens
<400> 11
tgggcaggaa ctgggcactg tgcccagggc atgcactgcc tccacgcagc aaccctcaga 60
gtcctgagct gaaccaagaa ggaggagggg gtcgggcctc cgaggaaggc ctagccgctg 120
ctgctgccag gaattccagg ttggaggggc ggcaacctcc tgccagcctt caggccactc 180
tcctgtgcct gccagaagag acagagcttg aggagagctt gaggagagca ggaaagcctc 240
ccccgttgcc cctctggatc cactgcttaa atacggacga ggacagggcc ctgtctcctc 300
agcttcaggc accaccactg acctgggaca gtgaatcgac aatgccgtct tctgtctcgt 360
ggggcatcct cctgctggca ggcctgtgct gcctggtccc tgtctccctg gctgaggatc 420
cccagggaga tgctgcccag aagacagata catcccacca tgatcaggat cacccaacct 480
tcaacaagat cacccccaac ctggctgagt tcgccttcag cctataccgc cagctggcac 540
accagtccaa cagcaccaat atcttcttct ccccagtgag catcgctaca gcctttgcaa 600
tgctctccct ggggaccaag gctgacactc acgatgaaat cctggagggc ctgaatttca 660
acctcacgga gattccggag gctcagatcc atgaaggctt ccaggaactc ctccgtaccc 720
tcaaccagcc agacagccag ctccagctga ccaccggcaa tggcctgttc ctcagcgagg 780
gcctgaagct agtggataag tttttggagg atgttaaaaa gttgtaccac tcagaagcct 840
tcactgtcaa cttcggggac accgaagagg ccaagaaaca gatcaacgat tacgtggaga 900
agggtactca agggaaaatt gtggatttgg tcaaggagct tgacagagac acagtttttg 960
ctctggtgaa ttacatcttc tttaaaggca aatgggagag accctttgaa gtcaaggaca 1020
ccgaggaaga ggacttccac gtggaccagg tgaccaccgt gaaggtgcct atgatgaagc 1080
gtttaggcat gtttaacatc cagcactgta agaagctgtc cagctgggtg ctgctgatga 1140
aatacctggg caatgccacc gccatcttct tcctgcctga tgaggggaaa ctacagcacc 1200
tggaaaatga actcacccac gatatcatca ccaagttcct ggaaaatgaa gacagaaggt 1260
ctgccagctt acatttaccc aaactgtcca ttactggaac ctatgatctg aagagcgtcc 1320
tgggtcaact gggcatcact aaggtcttca gcaatggggc tgacctctcc ggggtcacag 1380
aggaggcacc cctgaagctc tccaaggccg tgcataaggc tgtgctgacc atcgacgaga 1440
aagggactga agctgctggg gccatgtttt tagaggccat acccatgtct atcccccccg 1500
aggtcaagtt caacaaaccc tttgtcttct taatgattga acaaaatacc aagtctcccc 1560
tcttcatggg aaaagtggtg aatcccaccc aaaaataact gcctctcgct cctcaacccc 1620
tcccctccat ccctggcccc ctccctggat gacattaaag aagggttgag ctggtccctg 1680
cctgcatgtg actgtaaatc cctcccatgt tttctctgag tctccctttg cctgctgagg 1740
ctgtatgtgg gctccaggta acagtgctgt cttcgggccc cctgaactgt gttcatggag 1800
catctggctg ggtaggcaca tgctgggctt gaatccaggg gggactgaat cctcagctta 1860
cggacctggg cccatctgtt tctggagggc tccagtcttc cttgtcctgt cttggagtcc 1920
ccaagaagga atcacagggg aggaaccaga taccagccat gaccccaggc tccaccaagc 1980
atcttcatgt ccccctgctc atcccccact cccccccacc cagagttgct catcctgcca 2040
gggctggctg tgcccacccc aaggctgccc tcctgggggc cccagaactg cctgatcgtg 2100
ccgtggccca gttttgtggc atctgcagca acacaagaga gaggacaatg tcctcctctt 2160
gacccgctgt cacctaacca gactcgggcc ctgcacctct caggcacttc tggaaaatga 2220
ctgaggcaga ttcttcctga agcccattct ccatggggca acaaggacac ctattctgtc 2280
cttgtccttc catcgctgcc ccagaaagcc tcacatatct ccgtttagaa tcaggtccct 2340
tctccccaga tgaagaggag ggtctctgct ttgttttctc tatctcctcc tcagacttga 2400
ccaggcccag caggccccag aagaccatta ccctatatcc cttctcctcc ctagtcacat 2460
ggccataggc ctgctgatgg ctcaggaagg ccattgcaag gactcctcag ctatgggaga 2520
ggaagcacat cacccattga cccccgcaac ccctcccttt cctcctctga gtcccgactg 2580
gggccacatg cagcctgact tctttgtgcc tgttgctgtc cctgcagtct tcagagggcc 2640
accgcagctc cagtgccacg gcaggaggct gttcctgaat agcccctgtg gtaagggcca 2700
ggagagtcct tccatcctcc aaggccctgc taaaggacac agcagccagg aagtcccctg 2760
ggcccctagc tgaaggacag cctgctccct ccgtctctac caggaatggc cttgtcctat 2820
ggaaggcact gccccatccc aaactaatct aggaatcact gtctaaccac tcactgtcat 2880
gaatgtgtac ttaaaggatg aggttgagtc ataccaaata gtgatttcga tagttcaaaa 2940
tggtgaaatt agcaattcta catgattcag tctaatcaat ggataccgac tgtttcccac 3000
acaagtctcc tgttctctta agcttactca ctgacagcct ttcactctcc acaaatacat 3060
taaagatatg gccatcacca agccccctag gatgacacca gacctgagag tctgaagacc 3120
tggatccaag ttctgacttt tccccctgac agctgtgtga ccttcgtgaa gtcgccaaac 3180
ctctctgagc cccagtcatt gctagtaaga cctgcctttg agttggtatg atgttcaagt 3240
tagataacaa aatgtttata cccattagaa cagagaataa atagaactac atttcttgca 3300
<210> 12
<211> 1321
<212> ДНК
<213> Macaca mulatta
<400> 12
caggacaatg ccatcttctg tctcatgggg cgtcctcctg ctggcaggcc tgtgctgcct 60
gctccccggc tctctggctg aggatcccca gggagatgct gcccagaaga cggatacatc 120
ccaccatgat caggaccacc caaccctcaa caagatcacc cccagcctgg ctgagttcgg 180
cttcagccta taccgccagc tggcacacca gtccaacagc accaatatct tcttctcccc 240
agtgagcatc gctacagcct ttgcaatgct ctccctgggg accaaggctg acactcacag 300
tgaaatcctg gagggcctga atttcaacgt cacggagatt ccggaggctc aggtccatga 360
aggcttccag gaactcctcc ataccctcaa caagccagac agccagctcc agctgaccac 420
cggcaacggc ctgttcctca acaagagcct gaaggtagtg gataagtttt tggaggatgt 480
caaaaaactg taccactcag aagccttctc tgtcaacttt gaggacaccg aagaggccaa 540
gaaacagatc aacaattacg tggagaagga aactcaaggg aaaattgtgg atttggtcaa 600
ggagcttgac agagacacag tttttgctct ggtgaattac atcttcttta aaggcaaatg 660
ggagagaccc tttgacgttg aggccaccaa ggaagaggac ttccacgtgg accaggcgac 720
caccgtgaag gtgcccatga tgaggcgttt aggcatgttt aacatctacc actgtgagaa 780
gctgtccagc tgggtgctgc tgatgaaata cctgggcaat gccaccgcca tcttcttcct 840
gcctgatgag gggaaactgc agcacctgga aaatgaactc acccatgata tcatcaccaa 900
gttcctggaa aatgaaaaca gcaggtctgc caacttacat ttacccagac tggccattac 960
tggaacctat gatctgaaga cagtcctggg ccacctgggt atcactaagg tcttcagcaa 1020
tggggctgac ctctcgggga tcacggagga ggcacccctg aagctctcca aggccgtgca 1080
taaggctgtg ctgaccatcg atgagaaagg gactgaagct gctggggcca tgtttttaga 1140
ggccataccc atgtctattc cccccgaggt caagttcaac aaaccctttg tcttcttaat 1200
gattgaacaa aataccaagt ctcccctctt catgggaaaa gtggtgaatc ccacccagaa 1260
ataactgcct gtcactcctc agcccctccc ctccatccct ggccccctcc ctgaatgaca 1320
t 1321
<210> 13
<211> 2064
<212> ДНК
<213> Macaca mulatta
<400> 13
gcccagtctt gtgtctgcct ggcaatgggc aaggcccctt cctgcccaag ctccccgccc 60
ctccccaacc tattgcctcc gccacccgcc acccgaggcc aacttcctgg gtgggcagga 120
actgggccct gtgcccaggg cgtgcactgc ctccacgcag caaccctcag agtactgagc 180
tgagcaaagg aggaggaggg gatcagcact ctgaggaagg cctagccact gctgctgcca 240
ggaattccag ggcggcatca gtcttcagca tcaggcattt cggggtgaat tagtaaatgg 300
tagatcttgc taccagtgga acagccgcta aggattctgc agtgagagca gagggccagc 360
aaagtggtac tctcccagcg actggctgac tcacgccacc ccctccacct tggacgcagg 420
acactgtggt ttctgagcca ggtacaatga ctccttttgg tacgtgcagt ggaggctgta 480
tgctgctcag gcagagcgtc cggacagcgt gggcgggcga ctcagcgccc agcctgtgaa 540
cttagtccct gtttgctcct ccggtaactg gggtgatctt ggttaatatt caccagcagc 600
ctcccccgtt gcccctctgc acccactgct taaatacgga caaggacagg gctctgtctc 660
ctcagcctca ggcaccacca ctgacctggg acggtgaatc gacaatgcca tcttctgtct 720
catggggcgt cctcctgctg gcaggcctgt gctgcctgct ccccggctct ctggctgagg 780
atccccaggg agatgctgcc cagaagacgg atacatccca ccatgatcag gaccacccaa 840
ccctcaacaa gatcaccccc agcctggctg agttcggctt cagcctatac cgccagctgg 900
cacaccagtc caacagcacc aatatcttct tctccccagt gagcatcgct acagcctttg 960
caatgctctc cctggggacc aaggctgaca ctcacagtga aatcctggag ggcctgaatt 1020
tcaacgtcac ggagattccg gaggctcagg tccatgaagg cttccaggaa ctcctccata 1080
ccctcaacaa gccagacagc cagctccagc tgaccaccgg caacggcctg ttcctcaaca 1140
agagcctgaa ggtagtggat aagtttttgg aggatgtcaa aaaactgtac cactcagaag 1200
ccttctctgt caactttgag gacaccgaag aggccaagaa acagatcaac aattacgtgg 1260
agaaggaaac tcaagggaaa attgtggatt tggtcaagga gcttgacaga gacacagttt 1320
ttgctctggt gaattacatc ttctttaaag gcaaatggga gagacccttt gacgttgagg 1380
ccaccaagga agaggacttc cacgtggacc aggcgaccac cgtgaaggtg cccatgatga 1440
ggcgtttagg catgtttaac atctaccact gtgagaagct gtccagctgg gtgctgctga 1500
tgaaatacct gggcaatgcc accgccatct tcttcctgcc tgatgagggg aaactgcagc 1560
acctggaaaa tgaactcacc catgatatca tcaccaagtt cctggaaaat gaaaacagca 1620
ggtctgccaa cttacattta cccagactgg ccattactgg aacctatgat ctgaagacag 1680
tcctgggcca cctgggtatc actaaggtct tcagcaatgg ggctgacctc tcggggatca 1740
cggaggaggc acccctgaag ctctccaagg ccgtgcataa ggctgtgctg accatcgatg 1800
agaaagggac tgaagctgct ggggccatgt ttttagaggc catacccatg tctattcccc 1860
ccgaggtcaa gttcaacaaa ccctttgtct tcttaatgat tgaacaaaat accaagtctc 1920
ccctcttcat gggaaaagtg gtgaatccca cccagaaata actgcctgtc actcctcagc 1980
ccctcccctc catccctggc cccctccctg aatgacatta aagaagggtt gagctggtcc 2040
ctgcctgcgt gtgtgactgc aaac 2064
<210> 14
<211> 1608
<212> ДНК
<213> Macaca mulatta
<400> 14
tcttgtgtct gcctggcaat gggcaaggcc ccttcctgcc caagctcccc gcccctcccc 60
aacctattgc ctccgccacc cgccacccga ggccaacttc ctgggtgggc aggaactggg 120
ccctgtgccc agggcgtgca ctgcctccac gcagcaaccc tcagagtact gagctgagca 180
aaggaggagg aggggatcag cactctgagg aaggcctagc cactgctgct gccaggaatt 240
ccaggacaat gccatcttct gtctcatggg gcgtcctcct gctggcaggc ctgtgctgcc 300
tgctccccgg ctctctggct gaggatcccc agggagatgc tgcccagaag acggatacat 360
cccaccatga tcaggaccac ccaaccctca acaagatcac ccccagcctg gctgagttcg 420
gcttcagcct ataccgccag ctggcacacc agtccaacag caccaatatc ttcttctccc 480
cagtgagcat cgctacagcc tttgcaatgc tctccctggg gaccaaggct gacactcaca 540
gtgaaatcct ggagggcctg aatttcaacg tcacggagat tccggaggct caggtccatg 600
aaggcttcca ggaactcctc cataccctca acaagccaga cagccagctc cagctgacca 660
ccggcaacgg cctgttcctc aacaagagcc tgaaggtagt ggataagttt ttggaggatg 720
tcaaaaaact gtaccactca gaagccttct ctgtcaactt tgaggacacc gaagaggcca 780
agaaacagat caacaattac gtggagaagg aaactcaagg gaaaattgtg gatttggtca 840
aggagcttga cagagacaca gtttttgctc tggtgaatta catcttcttt aaaggcaaat 900
gggagagacc ctttgacgtt gaggccacca aggaagagga cttccacgtg gaccaggcga 960
ccaccgtgaa ggtgcccatg atgaggcgtt taggcatgtt taacatctac cactgtgaga 1020
agctgtccag ctgggtgctg ctgatgaaat acctgggcaa tgccaccgcc atcttcttcc 1080
tgcctgatga ggggaaactg cagcacctgg aaaatgaact cacccatgat atcatcacca 1140
agttcctgga aaatgaaaac agcaggtctg ccaacttaca tttacccaga ctggccatta 1200
ctggaaccta tgatctgaag acagtcctgg gccacctggg tatcactaag gtcttcagca 1260
atggggctga cctctcgggg atcacggagg aggcacccct gaagctctcc aaggccgtgc 1320
ataaggctgt gctgaccatc gatgagaaag ggactgaagc tgctggggcc atgtttttag 1380
aggccatacc catgtctatt ccccccgagg tcaagttcaa caaacccttt gtcttcttaa 1440
tgattgaaca aaataccaag tctcccctct tcatgggaaa agtggtgaat cccacccaga 1500
aataactgcc tgtcactcct cagcccctcc cctccatccc tggccccctc cctgaatgac 1560
attaaagaag ggttgagctg gtccctgcct gcgtgtgtga ctgcaaac 1608
<210> 15
<211> 3220
<212> ДНК
<213> Homo sapiens
<400> 15
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgctg gtgaatatta accaaggtca ccccagttat cggaggagca aacaggggct 3120
aagtccactg gctgggatct gagtcgcccg cctacgctgc ccggacgctt tgcctgggca 3180
gtgtacagct tccactgcac ttaccgaaag gagtcattgt 3220
<210> 16
<211> 3199
<212> ДНК
<213> Homo sapiens
<400> 16
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcctttcct gctctcctca agctctcctc aagctctgtc 3000
tcttctggca ggcacaggag agtggcctga aggctggcag gaggttgccg cccctccaac 3060
ctggaattcc tggcagcagc agcggctagg ccttcctcgg aggcccgacc ccctcctcct 3120
tcttggttca gctcaggact ctgagggttg ctgcgtggag gcagtgcatg ccctgggcac 3180
agtgcccagt tcctgccca 3199
<210> 17
<211> 3513
<212> ДНК
<213> Homo sapiens
<400> 17
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgcga aaggagtcat tgtacctggc tcagaaacca cagcgtcctg tgtccaaggt 3120
ggagggggtg gcgtgagtca gacagtctct gggagagtac cacttagctg gccctctgct 3180
ctcactgcag aatccttagt ggctgttcca ctggtagcaa gatctaccat ttactgagtc 3240
accccaaaat gcctgatgct gaagacttac tgccgccctt tcctgctctc ctcaagctct 3300
cctcaagctc tgtctcttct ggcaggcaca ggagagtggc ctgaaggctg gcaggaggtt 3360
gccgcccctc caacctggaa ttcctggcag cagcagcggc taggccttcc tcggaggccc 3420
gaccccctcc tccttcttgg ttcagctcag gactctgagg gttgctgcgt ggaggcagtg 3480
catgccctgg gcacagtgcc cagttcctgc cca 3513
<210> 18
<211> 3236
<212> ДНК
<213> Homo sapiens
<400> 18
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcctgtgga actgagtgag cagcagcagc aatgtcccac 3000
ctttcctgct ctcctcaagc tctcctcaag ctctgtctct tctggcaggc acaggagagt 3060
ggcctgaagg ctggcaggag gttgccgccc ctccaacctg gaattcctgg cagcagcagc 3120
ggctaggcct tcctcggagg cccgaccccc tcctccttct tggttcagct caggactctg 3180
agggttgctg cgtggaggca gtgcatgccc tgggcacagt gcccagttcc tgccca 3236
<210> 19
<211> 3532
<212> ДНК
<213> Homo sapiens
<400> 19
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgctg gctcagaaac cacagcgtcc tgtgtccaag gtggaggggg tggcgtgagt 3120
cagacagtct ctgggagagt accacttagc tggccctctg ctctcactgc agaatcctta 3180
gtggctgttc cactggtagc aagatctacc atttactgag tcaccccaaa atgcctgatg 3240
ctgaagactt actgccgccc tgtggaactg agtgagcagc agcagcaatg tcccaccttt 3300
cctgctctcc tcaagctctc ctcaagctct gtctcttctg gcaggcacag gagagtggcc 3360
tgaaggctgg caggaggttg ccgcccctcc aacctggaat tcctggcagc agcagcggct 3420
aggccttcct cggaggcccg accccctcct ccttcttggt tcagctcagg actctgaggg 3480
ttgctgcgtg gaggcagtgc atgccctggg cacagtgccc agttcctgcc ca 3532
<210> 20
<211> 3340
<212> ДНК
<213> Homo sapiens
<400> 20
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgctg tggaactgag tgagcagcag cagcaatgtc ccacctttcc tgctctcctc 3120
aagctctcct caagctctgt ctcttctggc aggcacagga gagtggcctg aaggctggca 3180
ggaggttgcc gcccctccaa cctggaattc ctggcagcag cagcggctag gccttcctcg 3240
gaggcccgac cccctcctcc ttcttggttc agctcaggac tctgagggtt gctgcgtgga 3300
ggcagtgcat gccctgggca cagtgcccag ttcctgccca 3340
<210> 21
<211> 3495
<212> ДНК
<213> Homo sapiens
<400> 21
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgctg gctcagaaac cacagcgtcc tgtgtccaag gtggaggggg tggcgtgagt 3120
cagacagtct ctgggagagt accacttagc tggccctctg ctctcactgc agaatcctta 3180
gtggctgttc cactggtagc aagatctacc atttactgag tcaccccaaa atgcctgatg 3240
ctgaagactt actgccgccc tttcctgctc tcctcaagct ctcctcaagc tctgtctctt 3300
ctggcaggca caggagagtg gcctgaaggc tggcaggagg ttgccgcccc tccaacctgg 3360
aattcctggc agcagcagcg gctaggcctt cctcggaggc ccgaccccct cctccttctt 3420
ggttcagctc aggactctga gggttgctgc gtggaggcag tgcatgccct gggcacagtg 3480
cccagttcct gccca 3495
<210> 22
<211> 3492
<212> ДНК
<213> Homo sapiens
<400> 22
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctggct cagaaaccac agcgtcctgt gtccaaggtg gagggggtgg cgtgagtcag 3120
acagtctctg ggagagtacc acttagctgg ccctctgctc tcactgcaga atccttagtg 3180
gctgttccac tggtagcaag atctaccatt tactgagtca ccccaaaatg cctgatgctg 3240
aagacttact gccgcccttt cctgctctcc tcaagctctc ctcaagctct gtctcttctg 3300
gcaggcacag gagagtggcc tgaaggctgg caggaggttg ccgcccctcc aacctggaat 3360
tcctggcagc agcagcggct aggccttcct cggaggcccg accccctcct ccttcttggt 3420
tcagctcagg actctgaggg ttgctgcgtg gaggcagtgc atgccctggg cacagtgccc 3480
agttcctgcc ca 3492
<210> 23
<211> 3510
<212> ДНК
<213> Homo sapiens
<400> 23
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggcgaaag gagtcattgt acctggctca gaaaccacag cgtcctgtgt ccaaggtgga 3120
gggggtggcg tgagtcagac agtctctggg agagtaccac ttagctggcc ctctgctctc 3180
actgcagaat ccttagtggc tgttccactg gtagcaagat ctaccattta ctgagtcacc 3240
ccaaaatgcc tgatgctgaa gacttactgc cgccctttcc tgctctcctc aagctctcct 3300
caagctctgt ctcttctggc aggcacagga gagtggcctg aaggctggca ggaggttgcc 3360
gcccctccaa cctggaattc ctggcagcag cagcggctag gccttcctcg gaggcccgac 3420
cccctcctcc ttcttggttc agctcaggac tctgagggtt gctgcgtgga ggcagtgcat 3480
gccctgggca cagtgcccag ttcctgccca 3510
<210> 24
<211> 3303
<212> ДНК
<213> Homo sapiens
<400> 24
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctgctt tcctgctctc ctcaagctct cctcaagctc tgtctcttct ggcaggcaca 3120
ggagagtggc ctgaaggctg gcaggaggtt gccgcccctc caacctggaa ttcctggcag 3180
cagcagcggc taggccttcc tcggaggccc gaccccctcc tccttcttgg ttcagctcag 3240
gactctgagg gttgctgcgt ggaggcagtg catgccctgg gcacagtgcc cagttcctgc 3300
cca 3303
<210> 25
<211> 3300
<212> ДНК
<213> Homo sapiens
<400> 25
tgcaagaaat gtagttctat ttattctctg ttctaatggg tataaacatt ttgttatcta 60
acttgaacat cataccaact caaaggcagg tcttactagc aatgactggg gctcagagag 120
gtttggcgac ttcacgaagg tcacacagct gtcaggggga aaagtcagaa cttggatcca 180
ggtcttcaga ctctcaggtc tggtgtcatc ctagggggct tggtgatggc catatcttta 240
atgtatttgt ggagagtgaa aggctgtcag tgagtaagct taagagaaca ggagacttgt 300
gtgggaaaca gtcggtatcc attgattaga ctgaatcatg tagaattgct aatttcacca 360
ttttgaacta tcgaaatcac tatttggtat gactcaacct catcctttaa gtacacattc 420
atgacagtga gtggttagac agtgattcct agattagttt gggatggggc agtgccttcc 480
ataggacaag gccattcctg gtagagacgg agggagcagg ctgtccttca gctaggggcc 540
caggggactt cctggctgct gtgtccttta gcagggcctt ggaggatgga aggactctcc 600
tggcccttac cacaggggct attcaggaac agcctcctgc cgtggcactg gagctgcggt 660
ggccctctga agactgcagg gacagcaaca ggcacaaaga agtcaggctg catgtggccc 720
cagtcgggac tcagaggagg aaagggaggg gttgcggggg tcaatgggtg atgtgcttcc 780
tctcccatag ctgaggagtc cttgcaatgg ccttcctgag ccatcagcag gcctatggcc 840
atgtgactag ggaggagaag ggatataggg taatggtctt ctggggcctg ctgggcctgg 900
tcaagtctga ggaggagata gagaaaacaa agcagagacc ctcctcttca tctggggaga 960
agggacctga ttctaaacgg agatatgtga ggctttctgg ggcagcgatg gaaggacaag 1020
gacagaatag gtgtccttgt tgccccatgg agaatgggct tcaggaagaa tctgcctcag 1080
tcattttcca gaagtgcctg agaggtgcag ggcccgagtc tggttaggtg acagcgggtc 1140
aagaggagga cattgtcctc tctcttgtgt tgctgcagat gccacaaaac tgggccacgg 1200
cacgatcagg cagttctggg gcccccagga gggcagcctt ggggtgggca cagccagccc 1260
tggcaggatg agcaactctg ggtggggggg agtgggggat gagcaggggg acatgaagat 1320
gcttggtgga gcctggggtc atggctggta tctggttcct cccctgtgat tccttcttgg 1380
ggactccaag acaggacaag gaagactgga gccctccaga aacagatggg cccaggtccg 1440
taagctgagg attcagtccc ccctggattc aagcccagca tgtgcctacc cagccagatg 1500
ctccatgaac acagttcagg gggcccgaag acagcactgt tacctggagc ccacatacag 1560
cctcagcagg caaagggaga ctcagagaaa acatgggagg gatttacagt cacatgcagg 1620
cagggaccag ctcaaccctt ctttaatgtc atccagggag ggggccaggg atggagggga 1680
ggggttgagg agcgagaggc agttattttt gggtgggatt caccactttt cccatgaaga 1740
ggggagactt ggtattttgt tcaatcatta agaagacaaa gggtttgttg aacttgacct 1800
cgggggggat agacatgggt atggcctcta aaaacatggc cccagcagct tcagtccctt 1860
tctcgtcgat ggtcagcaca gccttatgca cggccttgga gagcttcagg ggtgcctcct 1920
ctgtgacccc ggagaggtca gccccattgc tgaagacctt agtgatgccc agttgaccca 1980
ggacgctctt cagatcatag gttccagtaa tggacagttt gggtaaatgt aagctggcag 2040
accttctgtc ttcattttcc aggaacttgg tgatgatatc gtgggtgagt tcattttcca 2100
ggtgctgtag tttcccctca tcaggcagga agaagatggc ggtggcattg cccaggtatt 2160
tcatcagcag cacccagctg gacagcttct tacagtgctg gatgttaaac atgcctaaac 2220
gcttcatcat aggcaccttc acggtggtca cctggtccac gtggaagtcc tcttcctcgg 2280
tgtccttgac ttcaaagggt ctctcccatt tgcctttaaa gaagatgtaa ttcaccagag 2340
caaaaactgt gtctctgtca agctccttga ccaaatccac aattttccct tgagtaccct 2400
tctccacgta atcgttgatc tgtttcttgg cctcttcggt gtccccgaag ttgacagtga 2460
aggcttctga gtggtacaac tttttaacat cctccaaaaa cttatccact agcttcaggc 2520
cctcgctgag gaacaggcca ttgccggtgg tcagctggag ctggctgtct ggctggttga 2580
gggtacggag gagttcctgg aagccttcat ggatctgagc ctccggaatc tccgtgaggt 2640
tgaaattcag gccctccagg atttcatcgt gagtgtcagc cttggtcccc agggagagca 2700
ttgcaaaggc tgtagcgatg ctcactgggg agaagaagat attggtgctg ttggactggt 2760
gtgccagctg gcggtatagg ctgaaggcga actcagccag gttgggggtg atcttgttga 2820
aggttgggtg atcctgatca tggtgggatg tatctgtctt ctgggcagca tctccctggg 2880
gatcctcagc cagggagaca gggaccaggc agcacaggcc tgccagcagg aggatgcccc 2940
acgagacaga agacggcatt gtcgattcac tgtcccaggt cagtggtggt gcctgaagct 3000
gaggagacag ggccctgtcc tcgtccgtat ttaagcagtg gatccagagg ggcaacgggg 3060
gaggctttcc tgctctcctc aagctctcct caagctctgt ctcttctggc aggcacagga 3120
gagtggcctg aaggctggca ggaggttgcc gcccctccaa cctggaattc ctggcagcag 3180
cagcggctag gccttcctcg gaggcccgac cccctcctcc ttcttggttc agctcaggac 3240
tctgagggtt gctgcgtgga ggcagtgcat gccctgggca cagtgcccag ttcctgccca 3300
<210> 26
<211> 1321
<212> ДНК
<213> Macaca mulatta
<400> 26
atgtcattca gggagggggc cagggatgga ggggaggggc tgaggagtga caggcagtta 60
tttctgggtg ggattcacca cttttcccat gaagagggga gacttggtat tttgttcaat 120
cattaagaag acaaagggtt tgttgaactt gacctcgggg ggaatagaca tgggtatggc 180
ctctaaaaac atggccccag cagcttcagt ccctttctca tcgatggtca gcacagcctt 240
atgcacggcc ttggagagct tcaggggtgc ctcctccgtg atccccgaga ggtcagcccc 300
attgctgaag accttagtga tacccaggtg gcccaggact gtcttcagat cataggttcc 360
agtaatggcc agtctgggta aatgtaagtt ggcagacctg ctgttttcat tttccaggaa 420
cttggtgatg atatcatggg tgagttcatt ttccaggtgc tgcagtttcc cctcatcagg 480
caggaagaag atggcggtgg cattgcccag gtatttcatc agcagcaccc agctggacag 540
cttctcacag tggtagatgt taaacatgcc taaacgcctc atcatgggca ccttcacggt 600
ggtcgcctgg tccacgtgga agtcctcttc cttggtggcc tcaacgtcaa agggtctctc 660
ccatttgcct ttaaagaaga tgtaattcac cagagcaaaa actgtgtctc tgtcaagctc 720
cttgaccaaa tccacaattt tcccttgagt ttccttctcc acgtaattgt tgatctgttt 780
cttggcctct tcggtgtcct caaagttgac agagaaggct tctgagtggt acagtttttt 840
gacatcctcc aaaaacttat ccactacctt caggctcttg ttgaggaaca ggccgttgcc 900
ggtggtcagc tggagctggc tgtctggctt gttgagggta tggaggagtt cctggaagcc 960
ttcatggacc tgagcctccg gaatctccgt gacgttgaaa ttcaggccct ccaggatttc 1020
actgtgagtg tcagccttgg tccccaggga gagcattgca aaggctgtag cgatgctcac 1080
tggggagaag aagatattgg tgctgttgga ctggtgtgcc agctggcggt ataggctgaa 1140
gccgaactca gccaggctgg gggtgatctt gttgagggtt gggtggtcct gatcatggtg 1200
ggatgtatcc gtcttctggg cagcatctcc ctggggatcc tcagccagag agccggggag 1260
caggcagcac aggcctgcca gcaggaggac gccccatgag acagaagatg gcattgtcct 1320
g 1321
<210> 27
<211> 2064
<212> ДНК
<213> Macaca mulatta
<400> 27
gtttgcagtc acacacgcag gcagggacca gctcaaccct tctttaatgt cattcaggga 60
gggggccagg gatggagggg aggggctgag gagtgacagg cagttatttc tgggtgggat 120
tcaccacttt tcccatgaag aggggagact tggtattttg ttcaatcatt aagaagacaa 180
agggtttgtt gaacttgacc tcggggggaa tagacatggg tatggcctct aaaaacatgg 240
ccccagcagc ttcagtccct ttctcatcga tggtcagcac agccttatgc acggccttgg 300
agagcttcag gggtgcctcc tccgtgatcc ccgagaggtc agccccattg ctgaagacct 360
tagtgatacc caggtggccc aggactgtct tcagatcata ggttccagta atggccagtc 420
tgggtaaatg taagttggca gacctgctgt tttcattttc caggaacttg gtgatgatat 480
catgggtgag ttcattttcc aggtgctgca gtttcccctc atcaggcagg aagaagatgg 540
cggtggcatt gcccaggtat ttcatcagca gcacccagct ggacagcttc tcacagtggt 600
agatgttaaa catgcctaaa cgcctcatca tgggcacctt cacggtggtc gcctggtcca 660
cgtggaagtc ctcttccttg gtggcctcaa cgtcaaaggg tctctcccat ttgcctttaa 720
agaagatgta attcaccaga gcaaaaactg tgtctctgtc aagctccttg accaaatcca 780
caattttccc ttgagtttcc ttctccacgt aattgttgat ctgtttcttg gcctcttcgg 840
tgtcctcaaa gttgacagag aaggcttctg agtggtacag ttttttgaca tcctccaaaa 900
acttatccac taccttcagg ctcttgttga ggaacaggcc gttgccggtg gtcagctgga 960
gctggctgtc tggcttgttg agggtatgga ggagttcctg gaagccttca tggacctgag 1020
cctccggaat ctccgtgacg ttgaaattca ggccctccag gatttcactg tgagtgtcag 1080
ccttggtccc cagggagagc attgcaaagg ctgtagcgat gctcactggg gagaagaaga 1140
tattggtgct gttggactgg tgtgccagct ggcggtatag gctgaagccg aactcagcca 1200
ggctgggggt gatcttgttg agggttgggt ggtcctgatc atggtgggat gtatccgtct 1260
tctgggcagc atctccctgg ggatcctcag ccagagagcc ggggagcagg cagcacaggc 1320
ctgccagcag gaggacgccc catgagacag aagatggcat tgtcgattca ccgtcccagg 1380
tcagtggtgg tgcctgaggc tgaggagaca gagccctgtc cttgtccgta tttaagcagt 1440
gggtgcagag gggcaacggg ggaggctgct ggtgaatatt aaccaagatc accccagtta 1500
ccggaggagc aaacagggac taagttcaca ggctgggcgc tgagtcgccc gcccacgctg 1560
tccggacgct ctgcctgagc agcatacagc ctccactgca cgtaccaaaa ggagtcattg 1620
tacctggctc agaaaccaca gtgtcctgcg tccaaggtgg agggggtggc gtgagtcagc 1680
cagtcgctgg gagagtacca ctttgctggc cctctgctct cactgcagaa tccttagcgg 1740
ctgttccact ggtagcaaga tctaccattt actaattcac cccgaaatgc ctgatgctga 1800
agactgatgc cgccctggaa ttcctggcag cagcagtggc taggccttcc tcagagtgct 1860
gatcccctcc tcctcctttg ctcagctcag tactctgagg gttgctgcgt ggaggcagtg 1920
cacgccctgg gcacagggcc cagttcctgc ccacccagga agttggcctc gggtggcggg 1980
tggcggaggc aataggttgg ggaggggcgg ggagcttggg caggaagggg ccttgcccat 2040
tgccaggcag acacaagact gggc 2064
<210> 28
<211> 1608
<212> ДНК
<213> Macaca mulatta
<400> 28
gtttgcagtc acacacgcag gcagggacca gctcaaccct tctttaatgt cattcaggga 60
gggggccagg gatggagggg aggggctgag gagtgacagg cagttatttc tgggtgggat 120
tcaccacttt tcccatgaag aggggagact tggtattttg ttcaatcatt aagaagacaa 180
agggtttgtt gaacttgacc tcggggggaa tagacatggg tatggcctct aaaaacatgg 240
ccccagcagc ttcagtccct ttctcatcga tggtcagcac agccttatgc acggccttgg 300
agagcttcag gggtgcctcc tccgtgatcc ccgagaggtc agccccattg ctgaagacct 360
tagtgatacc caggtggccc aggactgtct tcagatcata ggttccagta atggccagtc 420
tgggtaaatg taagttggca gacctgctgt tttcattttc caggaacttg gtgatgatat 480
catgggtgag ttcattttcc aggtgctgca gtttcccctc atcaggcagg aagaagatgg 540
cggtggcatt gcccaggtat ttcatcagca gcacccagct ggacagcttc tcacagtggt 600
agatgttaaa catgcctaaa cgcctcatca tgggcacctt cacggtggtc gcctggtcca 660
cgtggaagtc ctcttccttg gtggcctcaa cgtcaaaggg tctctcccat ttgcctttaa 720
agaagatgta attcaccaga gcaaaaactg tgtctctgtc aagctccttg accaaatcca 780
caattttccc ttgagtttcc ttctccacgt aattgttgat ctgtttcttg gcctcttcgg 840
tgtcctcaaa gttgacagag aaggcttctg agtggtacag ttttttgaca tcctccaaaa 900
acttatccac taccttcagg ctcttgttga ggaacaggcc gttgccggtg gtcagctgga 960
gctggctgtc tggcttgttg agggtatgga ggagttcctg gaagccttca tggacctgag 1020
cctccggaat ctccgtgacg ttgaaattca ggccctccag gatttcactg tgagtgtcag 1080
ccttggtccc cagggagagc attgcaaagg ctgtagcgat gctcactggg gagaagaaga 1140
tattggtgct gttggactgg tgtgccagct ggcggtatag gctgaagccg aactcagcca 1200
ggctgggggt gatcttgttg agggttgggt ggtcctgatc atggtgggat gtatccgtct 1260
tctgggcagc atctccctgg ggatcctcag ccagagagcc ggggagcagg cagcacaggc 1320
ctgccagcag gaggacgccc catgagacag aagatggcat tgtcctggaa ttcctggcag 1380
cagcagtggc taggccttcc tcagagtgct gatcccctcc tcctcctttg ctcagctcag 1440
tactctgagg gttgctgcgt ggaggcagtg cacgccctgg gcacagggcc cagttcctgc 1500
ccacccagga agttggcctc gggtggcggg tggcggaggc aataggttgg ggaggggcgg 1560
ggagcttggg caggaagggg ccttgcccat tgccaggcag acacaaga 1608
<210> 29
<211> 16
<212> БЕЛОК
<213> Неустановленное
<220>
<223> Описание неизвестного: RFGF-пептид
<400> 29
Ala Ala Val Ala Leu Leu Pro Ala Val Leu Leu Ala Leu Leu Ala Pro
1 5 10 15
<210> 30
<211> 11
<212> БЕЛОК
<213> Неустановленное
<220>
<223> Описание неизвестного: Аналогичный RFGF пептид
<400> 30
Ala Ala Leu Leu Pro Val Leu Leu Ala Ala Pro
1 5 10
<210> 31
<211> 13
<212> БЕЛОК
<213> Вирус иммунодефицита человека
<400> 31
Gly Arg Lys Lys Arg Arg Gln Arg Arg Arg Pro Pro Gln
1 5 10
<210> 32
<211> 16
<212> БЕЛОК
<213> Drosophila sp.
<400> 32
Arg Gln Ile Lys Ile Trp Phe Gln Asn Arg Arg Met Lys Trp Lys Lys
1 5 10 15
<210> 33
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 33
cuucuuaaug auugaacaaa a 21
<210> 34
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<220>
<223> Описание объединенной молекулы ДНК/РНК: Синтетический олигонуклеотид
<400> 34
uuuugutcaa ucauuaagaa gac 23
<210> 35
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 35
cuucuuaaug auugaacaaa a 21
<210> 36
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 36
cuucuuaaug auugaacaaa a 21
<210> 37
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 37
uuuuguucaa ucauuaagaa gac 23
<210> 38
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<220>
<223> Описание объединенной молекулы ДНК/РНК: Синтетический олигонуклеотид
<400> 38
uuuugtucaa ucauuaagaa gac 23
<210> 39
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<220>
<223> Описание объединенной молекулы ДНК/РНК: Синтетический олигонуклеотид
<400> 39
uuuugutcaa ucauuaagaa gac 23
<210> 40
<400> 40
000
<210> 41
<400> 41
000
<210> 42
<400> 42
000
<210> 43
<400> 43
000
<210> 44
<400> 44
000
<210> 45
<400> 45
000
<210> 46
<400> 46
000
<210> 47
<400> 47
000
<210> 48
<400> 48
000
<210> 49
<400> 49
000
<210> 50
<400> 50
000
<210> 51
<400> 51
000
<210> 52
<400> 52
000
<210> 53
<400> 53
000
<210> 54
<400> 54
000
<210> 55
<400> 55
000
<210> 56
<400> 56
000
<210> 57
<400> 57
000
<210> 58
<400> 58
000
<210> 59
<400> 59
000
<210> 60
<400> 60
000
<210> 61
<400> 61
000
<210> 62
<400> 62
000
<210> 63
<400> 63
000
<210> 64
<400> 64
000
<210> 65
<400> 65
000
<210> 66
<400> 66
000
<210> 67
<400> 67
000
<210> 68
<400> 68
000
<210> 69
<400> 69
000
<210> 70
<400> 70
000
<210> 71
<400> 71
000
<210> 72
<400> 72
000
<210> 73
<400> 73
000
<210> 74
<400> 74
000
<210> 75
<400> 75
000
<210> 76
<400> 76
000
<210> 77
<400> 77
000
<210> 78
<400> 78
000
<210> 79
<400> 79
000
<210> 80
<400> 80
000
<210> 81
<400> 81
000
<210> 82
<400> 82
000
<210> 83
<400> 83
000
<210> 84
<400> 84
000
<210> 85
<400> 85
000
<210> 86
<400> 86
000
<210> 87
<400> 87
000
<210> 88
<400> 88
000
<210> 89
<400> 89
000
<210> 90
<400> 90
000
<210> 91
<400> 91
000
<210> 92
<400> 92
000
<210> 93
<400> 93
000
<210> 94
<400> 94
000
<210> 95
<400> 95
000
<210> 96
<400> 96
000
<210> 97
<400> 97
000
<210> 98
<400> 98
000
<210> 99
<400> 99
000
<210> 100
<400> 100
000
<210> 101
<400> 101
000
<210> 102
<400> 102
000
<210> 103
<400> 103
000
<210> 104
<400> 104
000
<210> 105
<400> 105
000
<210> 106
<400> 106
000
<210> 107
<400> 107
000
<210> 108
<400> 108
000
<210> 109
<400> 109
000
<210> 110
<400> 110
000
<210> 111
<400> 111
000
<210> 112
<400> 112
000
<210> 113
<400> 113
000
<210> 114
<400> 114
000
<210> 115
<400> 115
000
<210> 116
<400> 116
000
<210> 117
<400> 117
000
<210> 118
<400> 118
000
<210> 119
<400> 119
000
<210> 120
<400> 120
000
<210> 121
<400> 121
000
<210> 122
<400> 122
000
<210> 123
<400> 123
000
<210> 124
<400> 124
000
<210> 125
<400> 125
000
<210> 126
<400> 126
000
<210> 127
<400> 127
000
<210> 128
<400> 128
000
<210> 129
<400> 129
000
<210> 130
<400> 130
000
<210> 131
<400> 131
000
<210> 132
<400> 132
000
<210> 133
<400> 133
000
<210> 134
<400> 134
000
<210> 135
<400> 135
000
<210> 136
<400> 136
000
<210> 137
<400> 137
000
<210> 138
<400> 138
000
<210> 139
<400> 139
000
<210> 140
<400> 140
000
<210> 141
<400> 141
000
<210> 142
<400> 142
000
<210> 143
<400> 143
000
<210> 144
<400> 144
000
<210> 145
<400> 145
000
<210> 146
<400> 146
000
<210> 147
<400> 147
000
<210> 148
<400> 148
000
<210> 149
<400> 149
000
<210> 150
<400> 150
000
<210> 151
<400> 151
000
<210> 152
<400> 152
000
<210> 153
<400> 153
000
<210> 154
<400> 154
000
<210> 155
<400> 155
000
<210> 156
<400> 156
000
<210> 157
<400> 157
000
<210> 158
<400> 158
000
<210> 159
<400> 159
000
<210> 160
<400> 160
000
<210> 161
<400> 161
000
<210> 162
<400> 162
000
<210> 163
<400> 163
000
<210> 164
<400> 164
000
<210> 165
<400> 165
000
<210> 166
<400> 166
000
<210> 167
<400> 167
000
<210> 168
<400> 168
000
<210> 169
<400> 169
000
<210> 170
<400> 170
000
<210> 171
<400> 171
000
<210> 172
<400> 172
000
<210> 173
<400> 173
000
<210> 174
<400> 174
000
<210> 175
<400> 175
000
<210> 176
<400> 176
000
<210> 177
<400> 177
000
<210> 178
<400> 178
000
<210> 179
<400> 179
000
<210> 180
<400> 180
000
<210> 181
<400> 181
000
<210> 182
<400> 182
000
<210> 183
<400> 183
000
<210> 184
<400> 184
000
<210> 185
<400> 185
000
<210> 186
<400> 186
000
<210> 187
<400> 187
000
<210> 188
<400> 188
000
<210> 189
<400> 189
000
<210> 190
<400> 190
000
<210> 191
<400> 191
000
<210> 192
<400> 192
000
<210> 193
<400> 193
000
<210> 194
<400> 194
000
<210> 195
<400> 195
000
<210> 196
<400> 196
000
<210> 197
<400> 197
000
<210> 198
<400> 198
000
<210> 199
<400> 199
000
<210> 200
<400> 200
000
<210> 201
<400> 201
000
<210> 202
<400> 202
000
<210> 203
<400> 203
000
<210> 204
<400> 204
000
<210> 205
<400> 205
000
<210> 206
<400> 206
000
<210> 207
<400> 207
000
<210> 208
<400> 208
000
<210> 209
<400> 209
000
<210> 210
<400> 210
000
<210> 211
<400> 211
000
<210> 212
<400> 212
000
<210> 213
<400> 213
000
<210> 214
<400> 214
000
<210> 215
<400> 215
000
<210> 216
<400> 216
000
<210> 217
<400> 217
000
<210> 218
<400> 218
000
<210> 219
<400> 219
000
<210> 220
<400> 220
000
<210> 221
<400> 221
000
<210> 222
<400> 222
000
<210> 223
<400> 223
000
<210> 224
<400> 224
000
<210> 225
<400> 225
000
<210> 226
<400> 226
000
<210> 227
<400> 227
000
<210> 228
<400> 228
000
<210> 229
<400> 229
000
<210> 230
<400> 230
000
<210> 231
<400> 231
000
<210> 232
<400> 232
000
<210> 233
<400> 233
000
<210> 234
<400> 234
000
<210> 235
<400> 235
000
<210> 236
<400> 236
000
<210> 237
<400> 237
000
<210> 238
<400> 238
000
<210> 239
<400> 239
000
<210> 240
<400> 240
000
<210> 241
<400> 241
000
<210> 242
<400> 242
000
<210> 243
<400> 243
000
<210> 244
<400> 244
000
<210> 245
<400> 245
000
<210> 246
<400> 246
000
<210> 247
<400> 247
000
<210> 248
<400> 248
000
<210> 249
<400> 249
000
<210> 250
<400> 250
000
<210> 251
<400> 251
000
<210> 252
<400> 252
000
<210> 253
<400> 253
000
<210> 254
<400> 254
000
<210> 255
<400> 255
000
<210> 256
<400> 256
000
<210> 257
<400> 257
000
<210> 258
<400> 258
000
<210> 259
<400> 259
000
<210> 260
<400> 260
000
<210> 261
<400> 261
000
<210> 262
<400> 262
000
<210> 263
<400> 263
000
<210> 264
<400> 264
000
<210> 265
<400> 265
000
<210> 266
<400> 266
000
<210> 267
<400> 267
000
<210> 268
<400> 268
000
<210> 269
<400> 269
000
<210> 270
<400> 270
000
<210> 271
<400> 271
000
<210> 272
<400> 272
000
<210> 273
<400> 273
000
<210> 274
<400> 274
000
<210> 275
<400> 275
000
<210> 276
<400> 276
000
<210> 277
<400> 277
000
<210> 278
<400> 278
000
<210> 279
<400> 279
000
<210> 280
<400> 280
000
<210> 281
<400> 281
000
<210> 282
<400> 282
000
<210> 283
<400> 283
000
<210> 284
<400> 284
000
<210> 285
<400> 285
000
<210> 286
<400> 286
000
<210> 287
<400> 287
000
<210> 288
<400> 288
000
<210> 289
<400> 289
000
<210> 290
<400> 290
000
<210> 291
<400> 291
000
<210> 292
<400> 292
000
<210> 293
<400> 293
000
<210> 294
<400> 294
000
<210> 295
<400> 295
000
<210> 296
<400> 296
000
<210> 297
<400> 297
000
<210> 298
<400> 298
000
<210> 299
<400> 299
000
<210> 300
<400> 300
000
<210> 301
<400> 301
000
<210> 302
<400> 302
000
<210> 303
<400> 303
000
<210> 304
<400> 304
000
<210> 305
<400> 305
000
<210> 306
<400> 306
000
<210> 307
<400> 307
000
<210> 308
<400> 308
000
<210> 309
<400> 309
000
<210> 310
<400> 310
000
<210> 311
<400> 311
000
<210> 312
<400> 312
000
<210> 313
<400> 313
000
<210> 314
<400> 314
000
<210> 315
<400> 315
000
<210> 316
<400> 316
000
<210> 317
<400> 317
000
<210> 318
<400> 318
000
<210> 319
<400> 319
000
<210> 320
<400> 320
000
<210> 321
<400> 321
000
<210> 322
<400> 322
000
<210> 323
<400> 323
000
<210> 324
<400> 324
000
<210> 325
<400> 325
000
<210> 326
<400> 326
000
<210> 327
<400> 327
000
<210> 328
<400> 328
000
<210> 329
<400> 329
000
<210> 330
<400> 330
000
<210> 331
<400> 331
000
<210> 332
<400> 332
000
<210> 333
<400> 333
000
<210> 334
<400> 334
000
<210> 335
<400> 335
000
<210> 336
<400> 336
000
<210> 337
<400> 337
000
<210> 338
<400> 338
000
<210> 339
<400> 339
000
<210> 340
<400> 340
000
<210> 341
<400> 341
000
<210> 342
<400> 342
000
<210> 343
<400> 343
000
<210> 344
<400> 344
000
<210> 345
<400> 345
000
<210> 346
<400> 346
000
<210> 347
<400> 347
000
<210> 348
<400> 348
000
<210> 349
<400> 349
000
<210> 350
<400> 350
000
<210> 351
<400> 351
000
<210> 352
<400> 352
000
<210> 353
<400> 353
000
<210> 354
<400> 354
000
<210> 355
<400> 355
000
<210> 356
<400> 356
000
<210> 357
<400> 357
000
<210> 358
<400> 358
000
<210> 359
<400> 359
000
<210> 360
<400> 360
000
<210> 361
<400> 361
000
<210> 362
<400> 362
000
<210> 363
<400> 363
000
<210> 364
<400> 364
000
<210> 365
<400> 365
000
<210> 366
<400> 366
000
<210> 367
<400> 367
000
<210> 368
<400> 368
000
<210> 369
<400> 369
000
<210> 370
<400> 370
000
<210> 371
<400> 371
000
<210> 372
<400> 372
000
<210> 373
<400> 373
000
<210> 374
<400> 374
000
<210> 375
<400> 375
000
<210> 376
<400> 376
000
<210> 377
<400> 377
000
<210> 378
<400> 378
000
<210> 379
<400> 379
000
<210> 380
<400> 380
000
<210> 381
<400> 381
000
<210> 382
<400> 382
000
<210> 383
<400> 383
000
<210> 384
<400> 384
000
<210> 385
<400> 385
000
<210> 386
<400> 386
000
<210> 387
<400> 387
000
<210> 388
<400> 388
000
<210> 389
<400> 389
000
<210> 390
<400> 390
000
<210> 391
<400> 391
000
<210> 392
<400> 392
000
<210> 393
<400> 393
000
<210> 394
<400> 394
000
<210> 395
<400> 395
000
<210> 396
<400> 396
000
<210> 397
<400> 397
000
<210> 398
<400> 398
000
<210> 399
<400> 399
000
<210> 400
<400> 400
000
<210> 401
<400> 401
000
<210> 402
<400> 402
000
<210> 403
<400> 403
000
<210> 404
<400> 404
000
<210> 405
<400> 405
000
<210> 406
<400> 406
000
<210> 407
<400> 407
000
<210> 408
<400> 408
000
<210> 409
<400> 409
000
<210> 410
<400> 410
000
<210> 411
<400> 411
000
<210> 412
<400> 412
000
<210> 413
<400> 413
000
<210> 414
<400> 414
000
<210> 415
<400> 415
000
<210> 416
<400> 416
000
<210> 417
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 417
cuucuuaaug auugaacaaa a 21
<210> 418
<211> 21
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 418
cuucuuaaug auugaacaaa a 21
<210> 419
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 419
uuuuguucaa ucauuaagaa gac 23
<210> 420
<211> 23
<212> РНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 420
uuuuguucaa ucauuaagaa gac 23
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ АССОЦИИРОВАННОГО С SERPINC1 РАССТРОЙСТВА | 2016 |
|
RU2754188C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИИ ГЕПАТИТА В | 2018 |
|
RU2780021C2 |
| МОДУЛЯЦИЯ RSV, PIV И ДРУГИХ РЕСПИРАТОРНЫХ ВИРУСОВ С ПОМОЩЬЮ RNAI И ЕЕ ПРИМЕНЕНИЕ | 2005 |
|
RU2409666C2 |
| IРНК СРЕДСТВО ДЛЯ СНИЖЕНИЯ УРОВНЕЙ ВИРУСНОГО БЕЛКА, МРНК ИЛИ ТИТРА РЕСПИРАТОРНОГО СИНЦИТИАЛЬНОГО ВИРУСА В КЛЕТКЕ ДЫХАТЕЛЬНЫХ ПУТЕЙ | 2005 |
|
RU2494745C2 |
| ПРЕПАРАТЫ, ОСУЩЕСТВЛЯЮЩИЕ РНК-ИНТЕРФЕРЕНЦИЮ, ДЛЯ МОДУЛЯЦИИ ГЕНА GST-PI | 2015 |
|
RU2719185C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ ГЕНА TMPRSS6 | 2012 |
|
RU2702501C2 |
| ЛИПОСОМЫ С РЕТИНОИДОМ ДЛЯ УСИЛЕНИЯ МОДУЛЯЦИИ ЭКСПРЕССИИ HSP47 | 2012 |
|
RU2628694C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЯВЛЕНИЯ КРОВОТЕЧЕНИЯ У БОЛЬНОГО ГЕМОФИЛИЕЙ | 2018 |
|
RU2801263C2 |
| НУКЛЕИНОВЫЕ КИСЛОТЫ ДЛЯ ИНГИБИРОВАНИЯ ЭКСПРЕССИИ LPA В КЛЕТКЕ | 2018 |
|
RU2822093C1 |
| КОНТРОЛЬ ЖЕСТКОКРЫЛЫХ ВРЕДИТЕЛЕЙ С ПРИМЕНЕНИЕМ МОЛЕКУЛ РНК | 2017 |
|
RU2801251C2 |
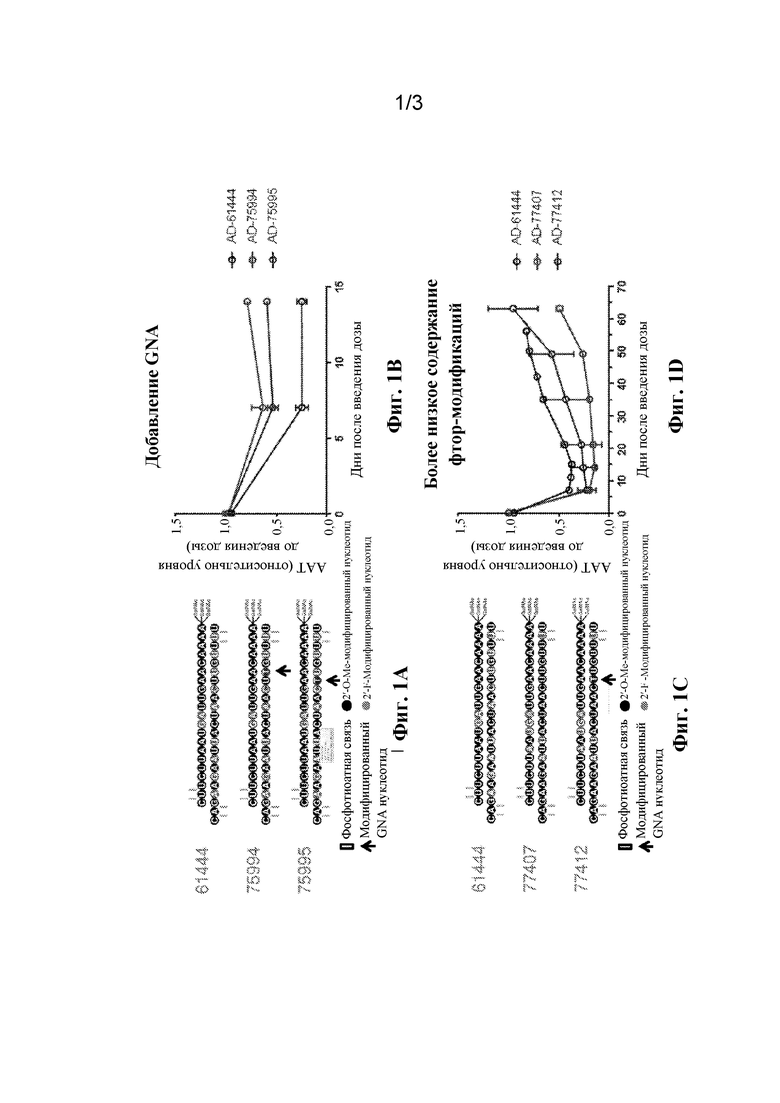
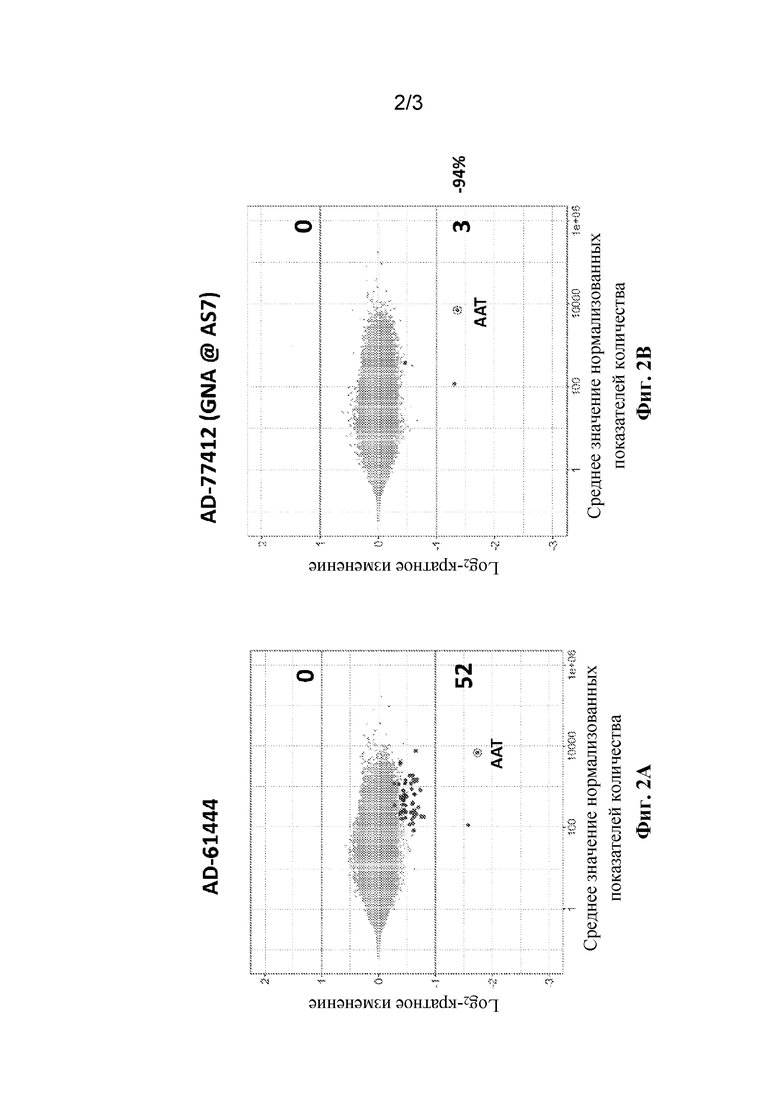
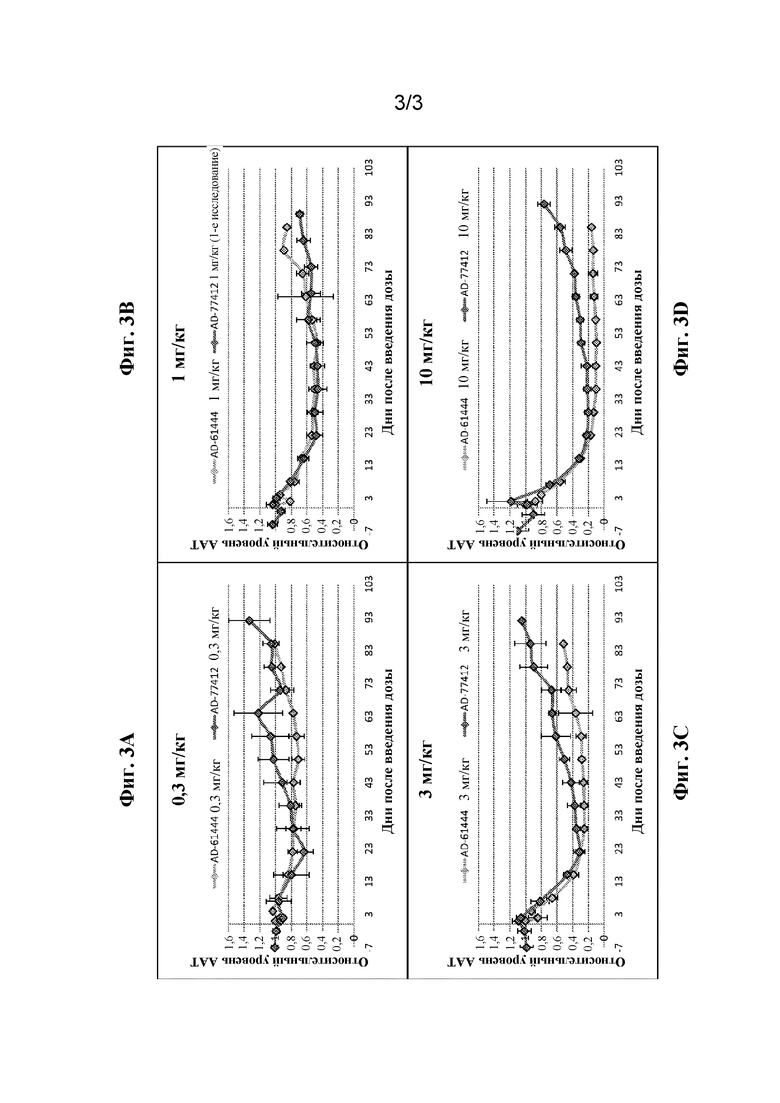
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена Serpina1 (варианты), фармацевтическую композицию (варианты), выделенную человеческую клетку, способ ингибирования экспрессии Serpina1 в клетке in vitro, применение средства на основе dsRNA или фармацевтической композиции в производстве лекарственного средства для лечения субъекта, применение средства на основе dsRNA или фармацевтической композиции в производстве лекарственного средства для ингибирования развития гепатоцеллюлярной карциномы у субъекта с дефектным вариантом Serpina1, применение средства на основе dsRNA или фармацевтической композиции в производстве лекарственного средства для снижения накопления неправильно свернутого Serpina1 в печени субъекта с дефектным вариантом Serpina1, применение фармацевтической композиции, содержащей средство на основе dsRNA, которое ингибирует экспрессию гена Serpina1, в производстве лекарственного средства для лечения субъекта. Изобретение расширяет арсенал средств для ингибирования экспрессии гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1) 13 н. и 37 з.п. ф-лы, 3 ил., 5 табл., 2 пр.
1. Средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить содержит нуклеотидную последовательность 5' – csusucuuAfaUfGfAfuugaacaaaaL96 –3' (SEQ ID NO: 35), и антисмысловая нить содержит нуклеотидную последовательность 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA); и L96 представляет собой N–[трис(GalNAc–алкил)–амидодеканоил)]–4–гидроксипролинол.
2. Средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить состоит из нуклеотидной последовательности 5' – csusucuuAfaUfGfAfuugaacaaaaL96 – 3' (SEQ ID NO: 35), и антисмысловая нить состоит из нуклеотидной последовательности 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA); и L96 представляет собой N–[трис(GalNAc–алкил)–амидодеканоил)]–4–гидроксипролинол.
3. Средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить содержит нуклеотидную последовательность 5' – csusucuuAfaUfGfAfuugaacaaaa – 3' (SEQ ID NO: 33), и антисмысловая нить содержит нуклеотидную последовательность 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA), и
где 3’-конец указанной смысловой цепи конъюгирован с лигандом, как показано на следующей схеме:
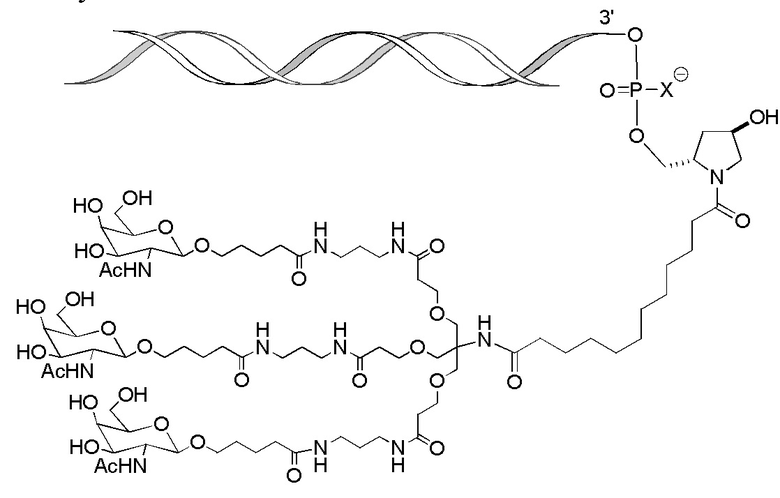 ,
,
где X представляет собой O или S.
4. Средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), содержащее смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить состоит из нуклеотидной последовательности 5' – csusucuuAfaUfGfAfuugaacaaaa – 3' (SEQ ID NO: 33), и антисмысловая нить состоит из нуклеотидной последовательности 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA), и
где 3’-конец указанной смысловой цепи конъюгирован с лигандом, как показано на следующей схеме:
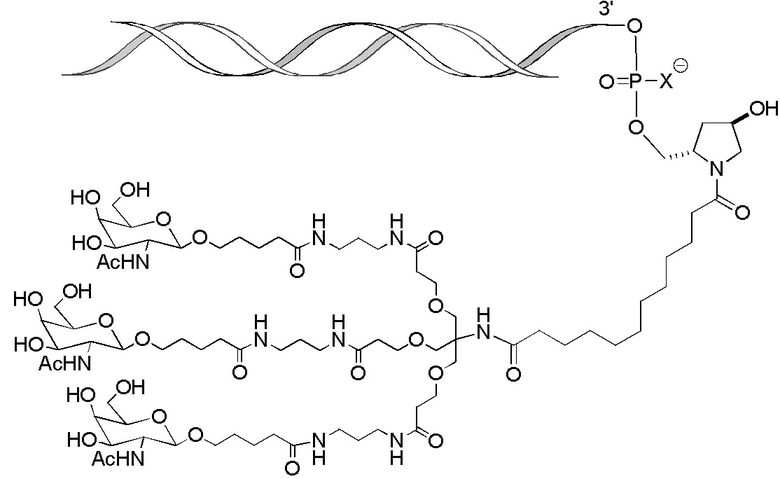 ,
,
где X представляет собой O или S.
5. Фармацевтическая композиция для лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание, содержащая эффективное количество средства на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1),
где указанное средство на основе dsRNA содержит смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить содержит нуклеотидную последовательность 5' – csusucuuAfaUfGfAfuugaacaaaa – 3' (SEQ ID NO: 33), и антисмысловая нить содержит нуклеотидную последовательность 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA), и
где 3’-конец указанной смысловой цепи конъюгирован с лигандом, как показано на следующей схеме:
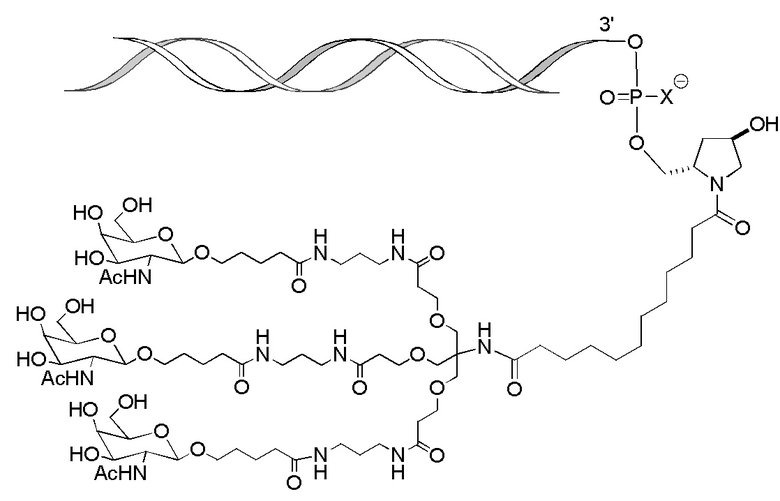 ,
,
где X представляет собой O или S.
6. Фармацевтическая композиция для лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание, содержащая эффективное количество средства на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1),
где указанное средство на основе dsRNA содержит смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить состоит из нуклеотидной последовательности 5' – csusucuuAfaUfGfAfuugaacaaaa – 3' (SEQ ID NO: 33), и антисмысловая нить состоит из нуклеотидной последовательности 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA), и
где 3’-конец указанной смысловой цепи конъюгирован с лигандом, как показано на следующей схеме:
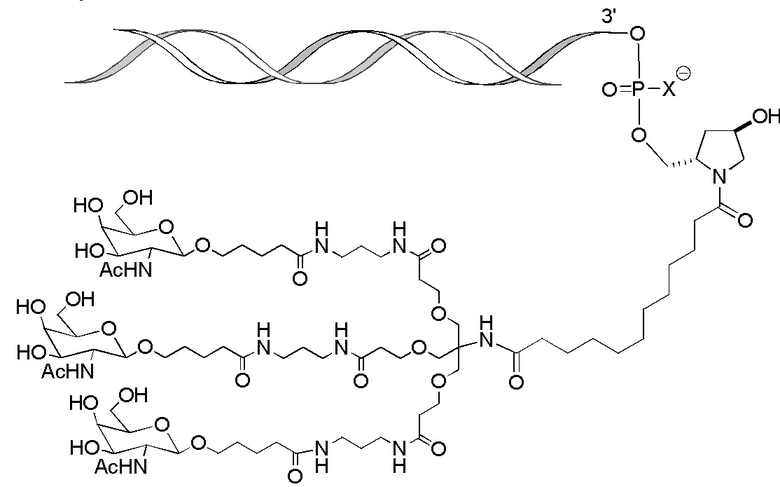 ,
,
где X представляет собой O или S.
7. Выделенная человеческая клетка, экспрессирующая средство на основе dsRNA по любому из пп. 1–4, где экспрессия указанного средства на основе dsRNA в указанной клетке ингибирует экспрессию Serpina1.
8. Фармацевтическая композиция для лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание, содержащая эффективное количество средства на основе dsRNA по любому из пп. 1–4.
9. Фармацевтическая композиция по пп. 5, 6 или 8, где указанное средство на основе dsRNA присутствует в незабуференном растворе.
10. Фармацевтическая композиция по п. 9, где указанный незабуференный раствор представляет собой солевой раствор или воду.
11. Фармацевтическая композиция по пп. 5, 6 или 8, где указанное средство на основе dsRNA присутствует в буферным растворе.
12. Фармацевтическая композиция по п. 11, где указанный буферный раствор содержит ацетат, цитрат, проламин, карбонат или фосфат или любую их комбинацию.
13. Фармацевтическая композиция по п. 11, где указанный буферный раствор представляет собой фосфатно–солевой буферный раствор (PBS).
14. Способ ингибирования экспрессии Serpina1 в клетке in vitro, где способ включает приведение клетки в контакт со средством на основе dsRNA по любому из пп. 1–4 или фармацевтической композицией по любому из пп. 5, 6 и 8-13, за счет чего обеспечивается ингибирование экспрессии гена Serpina1 в клетке.
15. Способ по п. 14, где экспрессия Serpina1 ингибируется на по меньшей мере приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 95%, приблизительно 98% или приблизительно 100%.
16. Применение средства на основе dsRNA по любому из пп. 1–4 или фармацевтической композиции по любому из пп. 5, 6 и 8-13 в производстве лекарственного средства для лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание.
17. Применение по п. 16, где субъектом является человек.
18. Применение по п. 16, где ассоциированное с Serpina1 заболевание представляет собой нарушение функции печени.
19. Применение по п. 18, где нарушение функции печени выбрано из группы, состоящей из хронического заболевания печени, воспаления печени, цирроза, фиброза печени и/или гепатоцеллюлярной карциномы.
20. Применение по п. 16, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг или от приблизительно 0,5 мг/кг до приблизительно 50 мг/кг.
21. Применение по п. 20, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 10 мг/кг до приблизительно 30 мг/кг.
22. Применение по п. 16, где двухнитевое средство для RNAi вводят подкожно.
23. Применение по п. 16, где двухнитевое средство для RNAi вводят внутривенно.
24. Применение по п. 16, где указанное средство для RNAi вводят в двух или более дозах.
25. Применение средства на основе dsRNA по любому из пп. 1–4 или фармацевтической композиции по любому из пп. 5, 6 и 8-13 в производстве лекарственного средства для ингибирования развития гепатоцеллюлярной карциномы у субъекта с дефектным вариантом Serpina1.
26. Применение по п. 25, где субъектом является примат или грызун.
27. Применение по п. 25, где субъектом является человек.
28. Применение по п. 25, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг или от приблизительно 0,5 мг/кг до приблизительно 50 мг/кг.
29. Способ по п. 28, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 10 мг/кг до приблизительно 30 мг/кг.
30. Применение по п. 25, где указанное средство для RNAi вводят в двух или более дозах.
31. Применение по п. 25, где двухнитевое средство для RNAi вводят подкожно.
32. Применение по п. 25, где двухнитевое средство для RNAi вводят внутривенно.
33. Применение средства на основе dsRNA по любому из пп. 1–4 или фармацевтической композиции по любому из пп. 5, 6 и 8-13 в производстве лекарственного средства для снижения накопления неправильно свернутого Serpina1 в печени субъекта с дефектным вариантом Serpina1.
34. Применение по п. 33, где субъектом является примат или грызун.
35. Применение по п. 33, где субъектом является человек.
36. Применение по п. 33, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг или от приблизительно 0,5 мг/кг до приблизительно 50 мг/кг.
37. Применение по п. 36, где двухнитевое средство для RNAi вводят в дозе, составляющей от приблизительно 10 мг/кг до приблизительно 30 мг/кг.
38. Применение по п. 33, где указанное средство для RNAi вводят в двух или более дозах.
39. Применение по п. 33, где двухнитевое средство для RNAi вводят подкожно.
40. Применение по п. 33, где двухнитевое средство для RNAi вводят внутривенно.
41. Применение фармацевтической композиции, содержащей средство на основе двухнитевой РНК (dsRNA), которое ингибирует экспрессию гена ингибитора сериновой пептидазы, клады A, представителя 1 (Serpina1), в производстве лекарственного средства для лечения субъекта, у которого имеется ассоциированное с Serpina1 заболевание,
где указанное средство на основе dsRNA содержит смысловую нить и антисмысловую нить, образующие двухнитевой участок,
где смысловая нить содержит нуклеотидную последовательность 5' – csusucuuAfaUfGfAfuugaacaaaa – 3' (SEQ ID NO: 33), и антисмысловая нить содержит нуклеотидную последовательность 5' – usUfsuugu(Tgn)caaucaUfuAfagaagsasc – 3' (SEQ ID NO: 34),
при этом a, g, c и u представляют собой 2′–O–метил–модифицированные (2′–OMe) A, G, C и U соответственно; Af, Gf, Cf и Uf представляют собой 2′–фтор–модифицированные A, G, C и U соответственно; s представляет собой фосфотиоатную связь; и (Tgn) представляет собой S–изомер нуклеиновой кислоты с тимидингликолевыми остатками (GNA), и
где 3’-конец указанной смысловой цепи конъюгирован с лигандом, как показано на следующей схеме:
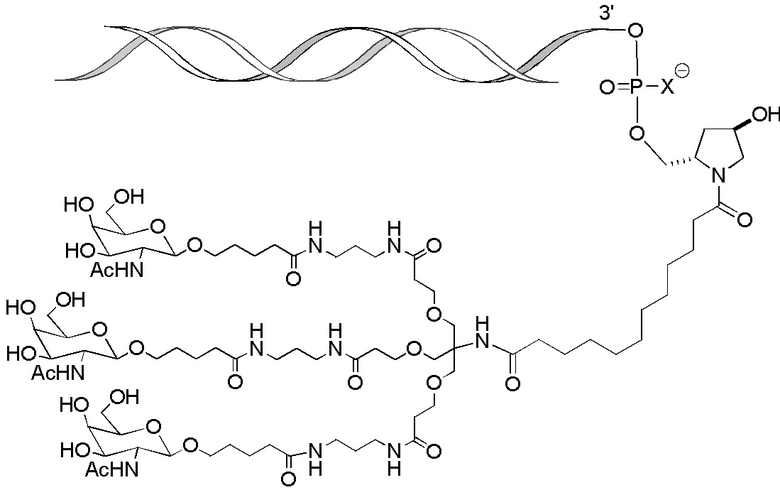 ,
,
где X представляет собой O или S.
42. Применение по п. 41, где субъектом является человек.
43. Применение по п. 41, где ассоциированное с Serpina1 заболевание представляет собой нарушение функции печени.
44. Применение по п. 43, где нарушение функции печени выбрано из группы, состоящей из хронического заболевания печени, воспаления печени, цирроза, фиброза печени и гепатоцеллюлярной карциномы.
45. Применение по п. 41, где указанное лекарственное средство пригодно для введения в дозе, составляющей от приблизительно 0,01 мг/кг до приблизительно 10 мг/кг или от приблизительно 0,5 мг/кг до приблизительно 50 мг/кг.
46. Применение по п. 45, где указанное лекарственное средство пригодно для введения в дозе, составляющей от приблизительно 10 мг/кг до приблизительно 30 мг/кг.
47. Применение по п. 41, где указанное лекарственное средство пригодно для введения в двух или более дозах.
48. Применение по п. 41, где указанное лекарственное средство пригодно для подкожного введения.
49. Применение по п. 41, где указанное лекарственное средство пригодно для внутривенного введения.
50. Применение по п. 41, где указанный субъект имеет один или более аллелей Serpina1.
| WO 2014190137 A1 27.11.2014 | |||
| Westerlind U | |||
| et al | |||
| "Ligands of the asialoglycoprotein receptor for targeted gene delivery, part 1: Synthesis of and binding studies with biotinylated cluster glycosides containing N-acetylgalactosamine." Glycoconjugate Journal, 2004, 21(5), 227-241 | |||
| WO 2016028649 A1 25.02.2016 | |||
| Нуклеиновые кислоты: от А до Я./ Б |
Авторы
Даты
2021-12-13—Публикация
2017-11-21—Подача