В данном документе представлена комбинация палбоциклиба и 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты, фармацевтическая композиция, содержащая такую комбинацию, и варианты терапевтического применения такой комбинации и фармацевтической композиции, в частности для лечения рака.
Эстрогеновый рецептор б (ESR1) экспрессируется в большинстве разновидностей опухолей молочной железы, позволяя им отвечать на митогенные действия эстрогенов.
6-(2,4-Дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновая кислота, далее в данном документе обозначенная как "соединение (1)", представляет собой селективный супрессор разрушения эстрогеновых рецепторов (SERD), который обладает свойствами полного антагониста эстрогеновых рецепторов и ускоряет протеасомное разрушение эстрогенового рецептора. Данное соединение раскрыто в заявке на патент PCT/EP2017/053282, опубликованной как WO 2017/140669.
Палбоциклиб, также известный как 6-ацетил-8-циклопентил-5-метил-2-[5-(1-пиперазинил)пиридин-2-иламино]пиридо[2,3-d]пиримидин-7(8H)-он, представляет собой ингибитор циклин-зависимой киназы (CDK) 4 и 6. Палбоциклиб представлен на рынке под торговым названием Ibrance® и предназначен для лечения гормон-рецептор(HR)-положительного, отрицательного по рецептору эпидермального фактора роста человека 2-го типа (HER2) местнораспространенного или метастатического рака молочной железы в комбинации с ингибитором ароматазы или в комбинации с фулвестрантом у женщин, которые раньше получали гормональную терапию. У женщин в период пре- или перименопаузы гормональную терапию необходимо объединять с агонистом гормона, высвобождающего лютеинизирующий гормон (LHRH).
Всегда существует необходимость в поиске новых противоопухолевых средств лечения. В таких обстоятельствах было показано, что комбинация соединения (1) с палбоциклибом хорошо переносится, демонстрирует высокую противоопухолевую эффективность и вызывает регрессию опухоли с синергетическим эффектом по сравнению с каждым активным ингредиентом в отдельности.
В данном документе представлена комбинация, содержащая соединение (1) и палбоциклиб.
В комбинации, представленной в данном документе, соединение (1) может существовать не только в форме цвиттер-иона (т. е. в целом нейтральной молекулы с кислотной группой и основной группой), но также в форме солей присоединения кислот или оснований. Такие соли присоединения можно применять в указанной выше комбинации. Следовательно, в данном документе представлена комбинация, содержащая соединение (1) или его фармацевтически приемлемую соль и палбоциклиб.
В одном варианте осуществления комбинация соединения (1) или его фармацевтически приемлемой соли с палбоциклибом демонстрирует терапевтическую синергию. Комбинация демонстрирует терапевтическую синергию, если ее терапевтический эффект выше по сравнению с кумулятивным эффектом любого активного средства из комбинации, применяемого отдельно.
В другом варианте осуществления соединение (1) или его фармацевтически приемлемую соль и палбоциклиб вводят посредством перорального пути.
В данном документе также представлена комбинация соединения (1) или его фармацевтически приемлемой соли и палбоциклиба для ее применения в качестве лекарственного препарата.
В данном документе также представлена фармацевтическая композиция, содержащая соединение (1) или его фармацевтически приемлемую соль и палбоциклиб, а также по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
Вспомогательные вещества выбраны из обычных вспомогательных веществ, которые известны специалистам в данной области техники. Более конкретно вспомогательные вещества выбраны из веществ, пригодных для перорального введения в любой форме (жидкий раствор, дисперсия или суспензия, таблетки, капсулы или т. п.).
В другом варианте осуществления соединение (1) или его фармацевтически приемлемую соль и палбоциклиб можно вводить одновременно, по отдельности или раздельно в течение некоторого периода времени (последовательное введение). Следовательно, комбинация, представленная в данном документе, конкретно не ограничена комбинацией, которую получают путем физического соединения составляющих в одной фармацевтической композиции, но также комбинациями, которые обеспечивают отдельное введение, которое может быть одновременным или разделенным (или "распределенным") во времени.
В данном документе также представлен фармацевтический набор, который содержит:
(i) первую фармацевтическую композицию, содержащую соединение (1) или его фармацевтически приемлемую соль и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество;
(ii) вторую фармацевтическую композицию, содержащую палбоциклиб и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество;
при этом обе фармацевтические композиции (i) и (ii) находятся в отдельных камерах и предназначены для независимого друг от друга введения, при этом каждое введение в отношении другого является одновременным, раздельным или распределенным (последовательным) во времени.
В комбинациях, фармацевтических композициях и фармацевтическом наборе, описанных выше, соединение (1) или его фармацевтически приемлемая соль и палбоциклиб преимущественно присутствуют в эффективных дозах, адаптированных с учетом патологии, подлежащей лечению, и состояния пациента, которому их вводят. В частности, в случае палбоциклиба рекомендуемая начальная доза при лечении рака для взрослых пациентов составляет 125 мг один раз в сутки в течение 21 дня с последующими 7 днями без лечения, наряду с прерыванием введения доз и/или снижениями доз на основе индивидуальной безопасности и переносимости.
В данном документе также представлена комбинация, содержащая соединение (1) или его фармацевтически приемлемую соль и палбоциклиб, а также фармацевтическая композиция и набор, описанные выше, предназначенные для применения в лечении рака.
В данном документе также представлено соединение (1) или его фармацевтически приемлемая соль, предназначенные для применения в лечении рака путем совместного введения с палбоциклибом.
В данном документе также представлен палбоциклиб, предназначенный для применения в лечении рака, осуществляемого путем совместного введения с соединением (1) или его фармацевтически приемлемой солью.
В другом варианте осуществления рак представляет собой гормонозависимый рак.
В другом варианте осуществления рак представляет собой рак, зависимый от эстрогеновых рецепторов, в частности, рак представляет собой рак, зависимый от эстрогеновых рецепторов б.
В другом варианте осуществления рак является резистентным к антигормональному лечению.
В другом варианте осуществления рак представляет собой рак с эстрогеновыми рецепторами дикого типа.
В другом варианте осуществления рак представляет собой рак с нарушенной регуляцией функции эстрогеновых рецепторов, связанной без ограничений по меньшей мере с одним эпигенетическим и генетическим изменением эстрогеновых рецепторов, таким как мутация, амплификация, вариант сплайсинга.
В другом варианте осуществления рак представляет собой рак с мутированными эстрогеновыми рецепторами.
В другом варианте осуществления мутации эстрогеновых рецепторов могут включать без ограничения новые или известные мутации, такие как Leu536Arg, Tyr537Ser, Tyr537Asn или Asp538Gly.
В другом варианте осуществления рак представляет собой эстрогенчувствительный рак.
В другом варианте осуществления рак представляет собой рак молочной железы, более конкретно эстрогеновый рецептор-положительный рак молочной железы (ERб-положительный рак молочной железы) или его метастаз, такой как метастаз в головной мозг.
В данном документе также представлен способ лечения патологических состояний, указанных выше, в частности рака молочной железы, включающий введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения (1) или его фармацевтически приемлемой соли и терапевтически эффективного количества палбоциклиба.
В данном документе также представлен способ лечения патологических состояний, указанных выше, в частности рака молочной железы, включающий введение субъекту, нуждающемуся в этом, фармацевтической композиции, описанной выше.
В данном документе также представлен способ лечения патологических состояний, указанных выше, в частности рака молочной железы, включающий введение субъекту, нуждающемуся в этом, комбинации, описанной выше.
В данном документе также представлен способ лечения патологических состояний, указанных выше, в частности рака молочной железы, включающий совместное введение субъекту, нуждающемуся в этом, соединения (1) или его фармацевтически приемлемой соли и палбоциклиба.
В данном документе также представлен способ лечения патологических состояний, указанных выше, в частности рака молочной железы, включающий совместное введение субъекту, нуждающемуся в этом, палбоциклиба и соединения (1) или его фармацевтически приемлемой соли.
В одном варианте осуществления способов, описанных выше, субъект представляет собой человека.
В данном документе также представлена комбинация, содержащая соединение (1) или его фармацевтически приемлемую соль и палбоциклиб, предназначенная для изготовления лекарственного препарата, пригодного в лечении патологических состояний, указанных выше, в частности рака молочной железы.
В данном документе также представлено применение соединения (1) или его фармацевтически приемлемой соли в изготовлении лекарственного препарата, пригодного в лечении патологических состояний, указанных выше, в частности рака молочной железы, осуществляемое путем совместного введения с палбоциклибом.
В данном документе также представлено применение палбоциклиба в изготовлении лекарственного препарата, пригодного в лечении патологических состояний, указанных выше, в частности рака молочной железы, осуществляемое путем совместного введения с соединением (1) или его фармацевтически приемлемой солью.
В данном документе также представлены изделие, упаковка или единица введения, содержащие:
- упаковочный материал;
- определенные выше комбинацию, фармацевтическую композицию или фармацевтический набор и
- этикетку или листок-вкладыш, содержащиеся в указанном упаковочном материале, указывающие на то, что указанные комбинация, фармацевтическая композиция или фармацевтический набор вводятся пациенту с целью лечения рака.
В примерах, представленных ниже, продемонстрированы синтез соединения (1) и фармакологические результаты, полученные для соединения (1), палбоциклиба и их комбинации в отношении ксенотрансплантата линии раковых клеток молочной железы у мышей.
1. Синтез 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты
Экспериментальный протокол синтеза 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты (соединение (1)), описанный в заявке на патент WO 2017/140669, воспроизведен ниже, наряду с его аналитическими данными. Схема синтеза для синтеза соединения (1) представлена на фигуре 1.
Получение спектров 1H ЯМР осуществляли на спектрометре Bruker Avance DRX-400 со значениями химического сдвига (д в ppm) в растворителе, представляющем собой диметилсульфоксид-d6 (d6-DMSO), приведенными при 2,5 ppm при температуре 303 K. Значения константы взаимодействия (J) приведены в герцах.
Данные жидкостной хроматографии/масс-спектры (LC/MS) получали на приборе UPLC Acquity Waters с детектором светорассеяния Sedere и масс-спектрометром SQD Waters с использованием УФ-детектора DAD 210<l<400 нм и колонки Acquity UPLC CSH C18 1,7 мкм, размер 2,1Ч30 мм, подвижная фаза H2O+0,1% HCO2H/CH3CN+0,1% HCO2H.
Применяли следующие сокращения и эмпирические формулы.
AcOEt этилацетат
AlCl3 трихлорид алюминия
Cs2CO3 карбонат цезия
DCM дихлорметан
DMF N, N-диметилформамид
DMSO диметилсульфоксид
HCl хлороводород
K2CO3 карбонат калия
LC/MS жидкостная хроматография/масс-спектрометрия
MeOH метанол
MgSO4 сульфат магния
NaHCO3 бикарбонат натрия
NaOH гидроксид натрия
Pd(dppf)Cl2 1,1′бис(дифенилфосфино)ферроцен] дихлорпалладий(II)
Ph3P или P(Ph)3 трифенилфосфин
Ph3P=O трифенилфосфиноксид
°C градусы Цельсия
мл миллилитр(миллилитры)
ммоль миллимоль(миллимоли)
мкмоль микромоль(микромоли)
мкМ микромолярный
нМ наномолярный
ppm части на миллион
Промежуточное соединение (c). Трет-бутил-(3S)-3-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидин-1-карбоксилат
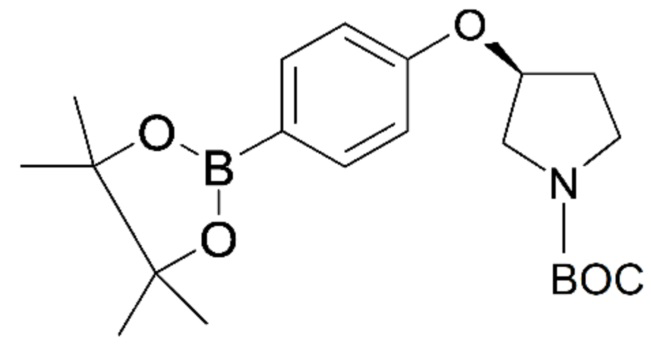
К раствору коммерчески доступного 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенола (a) (82,7 г, 364,51 ммоль) в THF (2 л) добавляли в атмосфере аргона (R)-1-N-Boc-3-гидроксипирролидин (b) (84,43 г, 437,41 ммоль) с последующим добавлением N, N,N',N'-тетраметилазодикарбоксамида (99,1 г, 546,77 ммоль). Прозрачная реакционная смесь становилась оранжевой, и добавляли трифенилфосфин (143,41 г, 546,77 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 24 часов, при этом образовывался осадок из трифенилфосфиноксида (Ph3P=O). Реакционную смесь выливали в воду (1,5 л) и экстрагировали этилацетатом (AcOEt) (3Ч1,5 л). Собранные органические фазы высушивали над сульфатом магния (MgSO4), фильтровали и концентрировали при пониженном давлении. Остаток поглощали в диизопропиловом эфире (1,5 л) и образованное твердое вещество (Ph3P=O) фильтровали. Растворитель концентрировали при пониженном давлении и остаток очищали с помощью колоночной хроматографии с элюированием смесью гептана с AcOEt (90/10; об./об.) с получением 145 г (100%) трет-бутил-(3S)-3-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидин-1-карбоксилата (c) в виде бесцветного масла.
1H ЯМР (400 МГц, DMSO-d6, д ppm): 1,27 (s : 12H); 1,39 (s : 9H); 2,05 (m : 1H); 2,14 (m : 1H); 3,37 (3H); 3,55 (m : 1H); 5,05 (s : 1H); 6,94 (d, J=8,4 Гц : 2H); 7,61 (d, J=8,4 Гц : 2H)
Промежуточное соединение (d). (3S)-3-[4-(4,4,5,5-Тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидина гидрохлорид
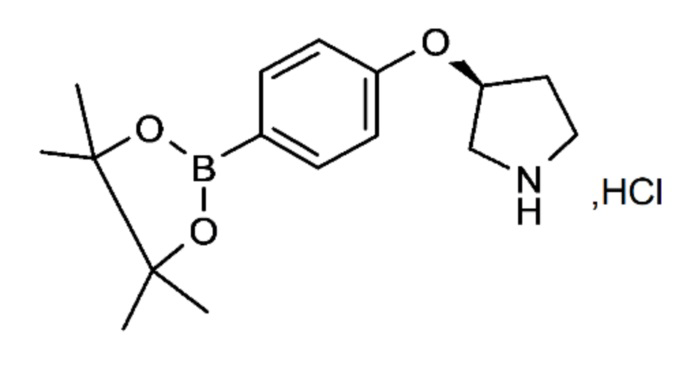
К раствору (S)-трет-бутил-3-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси)пирролидин-1-карбоксилата (c) (80 г, 195,23 ммоль) в MeOH (450 мл) медленно добавляли 4 н. HCl в диоксане (250 мл).
Через 1,5 часа реакционную смесь концентрировали при пониженном давлении и остаток поглощали в Et2O с перемешиванием с получением твердого вещества, которое затем фильтровали и высушивали под вакуумом с получением 61,8 г (95%) (3S)-3-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидина гидрохлорида (d) в виде белого порошка.
1H ЯМР (400 МГц, DMSO-d6, д ppm): 1,28 (s : 12H); 2,10 (m : 1H); 2,21 (m : 1H); 3,31 (3H); 3,48 (m : 1H); 5,19 (m : 1H); 6,97 (d, J=8,4 Гц : 2H); 7,63 (d, J=8,4 Гц : 2H); 9,48 (s : 1H); 9,71 (s : 1H).
LC/MS (масса/заряд, MH+): 290
Промежуточное соединение (e). (3S)-1-(3-Фторпропил)-3-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидин
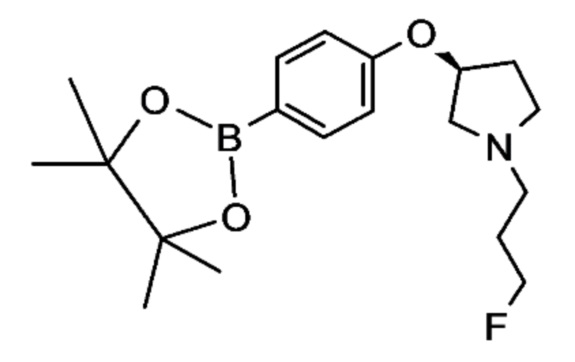
К суспензии (S)-3-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси)пирролидина гидрохлорида (d) (20 г, 61,42 ммоль) в ацетонитриле (100 мл) добавляли K2CO3 (21,22 г, 153,54 ммоль) и 1-йод-3-фторпропан (12,15 г, 61,42 ммоль) в атмосфере аргона. Реакционную смесь перемешивали при 40°C в течение 24 часов. После охлаждения до комнатной температуры реакционную смесь фильтровали и промывали ацетонитрилом. Фильтрат концентрировали при пониженном давлении и остаток поглощали в DCM и образованное твердое вещество фильтровали и промывали с помощью DCM. Фильтрат концентрировали с получением 21,5 г (100%) (3S)-1-(3-фторпропил)-3-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидина (e) в виде желтой пены.
1H ЯМР (400 МГц, DMSO-d6, д ppm): 1,27 (s : 12H); 1,77 (m : 2H); 1,84 (m : 1H); 2,27 (m : 1H); 2,41 (m : 1H); 2,49 (2H); 2,62 (dd, J=2,6 и 10,4Гц : 1H); 2,69 (m : 1H); 2,83 (dd, J=6,2 и 10,4Гц : 1H); 4,47 (td, J=6,2 и 47Гц : 2H) ; 4,99 (m : 1H); 6,77 (d , J=8,4 Гц : 2H); 7,58 (d, J=8,4 Гц : 2H).
LC/MS (масса/заряд, MH+): 350
Промежуточное соединение (B). 5-Оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-ил-2,2-диметилпропаноат
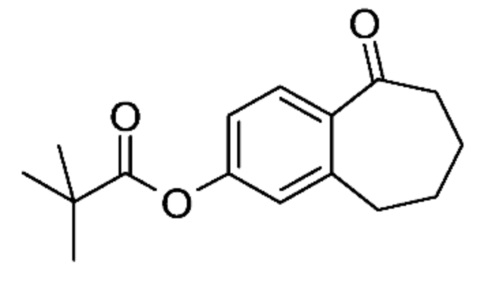
К раствору 2-гидрокси-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-5-она (A) (1,52 г, 8,63 ммоль) в ацетоне (60 мл) добавляли K2CO3 (1,19 г, 8,63 ммоль) и пивалоилхлорид (1,06 мл, 8,63 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 16 часов, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом гептана в AcOEt (от 100/0 до 85/15, об./об.) с получением 1,55 г (69%) 5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-ил-2,2-диметилпропаноата (B) в виде бесцветного масла.
1H ЯМР (400 МГц, DMSO-d6, д ppm): 7,65 (d, 1H); 7,10-7,04 (m, 2H); 2,95 (t, 2H); 2,68 (t, 2H); 1,85-1,65 (m, 4H).
LC/MS (масса/заряд, MH+): 261
Промежуточное соединение (C). 9-(Трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноат
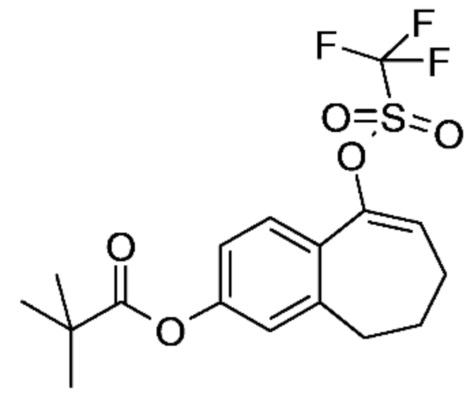
К раствору 5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-ил-2,2-диметилпропаноата (B) (15 г, 57,62 ммоль) в DCM (500 мл) добавляли по каплям в атмосфере аргона пиридин (7,28 мл, 86,43 ммоль) и ангидрид трифторметансульфоновой кислоты (19,58 мл, 115,24 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 2 часов и добавляли лед (200 г). Фазы разделяли, водную фазу промывали с помощью DCM и собранные органические фазы высушивали над MgSO4, фильтровали и выпаривали при пониженном давлении с получением 22 г (97%) 9-(трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноата (C) в виде белого твердого вещества.
LC/MS (масса/заряд, MH-): 391
Промежуточное соединение (D). 9-(4-{[(3S)-1-(3-Фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноат
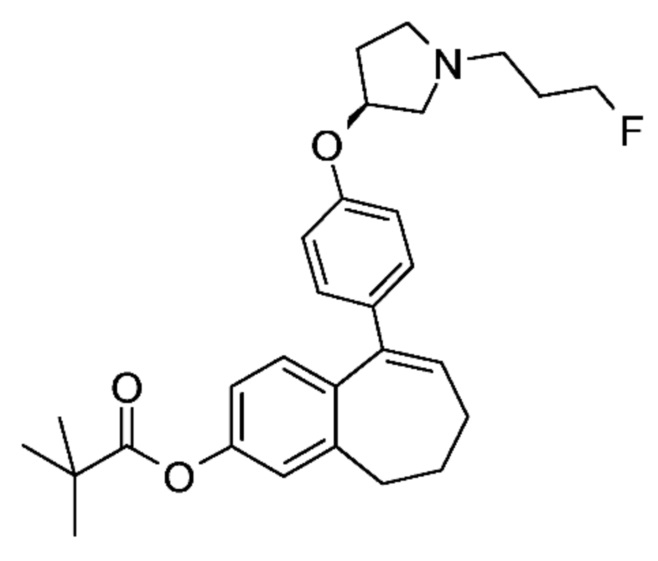
К раствору 9-(трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноата (C) (22 г, 56,07 ммоль) и (3S)-1-(3-фторпропил)-3-[4-(тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидина (e) (20,56 г, 58,87 ммоль) в диоксане (420 мл) и воде (120 мл) добавляли в атмосфере аргона Pd(dppf)Cl2 (2,75 г, 3,36 ммоль) и Cs2CO3 (36,57 г, 112,13 ммоль). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре и разделяли между водой и DCM. Водную фазу промывали с помощью DCM и собранные органические фазы высушивали над MgSO4, фильтровали и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии с элюированием градиентом MeOH в DCM (от 0 до 5%; об./об.) с получением 31 г (100%) 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноата (D).
LC/MS (масса/заряд, MH+): 466
Промежуточное соединение (E). 9-(4-{[(3S)-1-(3-Фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ол
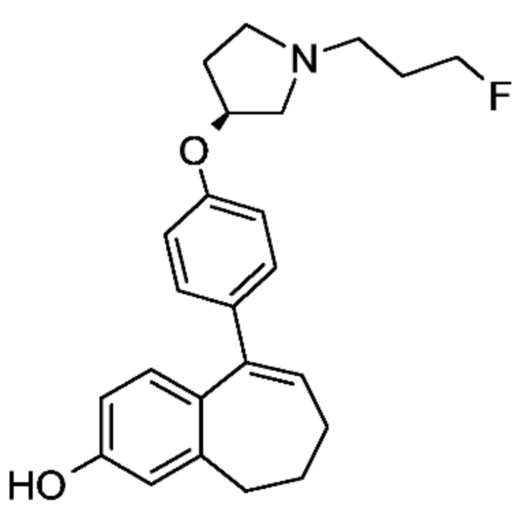
К раствору 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-2,2-диметилпропаноата (D) (24,8 г, 53,26 ммоль) в MeOH (300 мл) в атмосфере аргона добавляли 5 M NaOH (23 мл, 115,00 ммоль). Реакционную смесь перемешивали в течение 2 часов при комнатной температуре. Затем pH доводили до 7 путем добавления 6 н. водного раствора HCl. MeOH концентрировали при пониженном давлении, затем добавляли DCM. Органическую фазу высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом DCM/MeOH от 100/0 до 95/05 с получением 18,8 г (93%) 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ола (E) в виде бежевого твердого вещества.
LC/MS (масса/заряд, MH+): 382
Промежуточное соединение (F). 9-(4-{[(3S)-1-(3-Фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-трифторметансульфонат
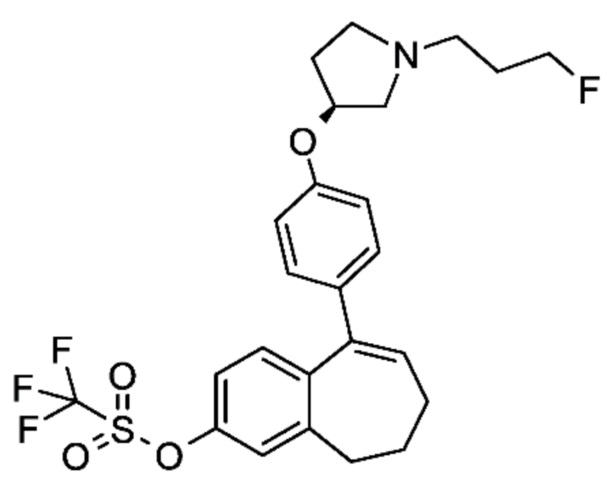
К раствору 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ола (E) (20,6 г, 54,00 ммоль) в DCM (200 мл) и пиридине (6,55 мл, 81,00 ммоль), охлажденному до 5°C (ледяная баня), добавляли по каплям ангидрид трифторметансульфоновой кислоты (18,93 мл, 108,00 ммоль) в атмосфере аргона и температуру реакции поддерживали <15°C. Ледяную баню удаляли и коричневую суспензию перемешивали при комнатной температуре в течение 2 часов. Добавляли лед (200 г) и DCM (200 мл) и фазы разделяли. Органическую фазу высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом DCM/MeOH от 100/0 до 95/05 с получением 24,7 г (89,1%) 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-трифторметансульфоната (F) в виде коричневого масла.
LC/MS (масса/заряд, MH+): 514
Промежуточное соединение (G). Метил-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилат
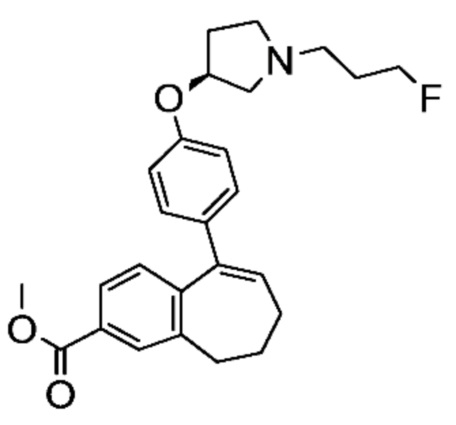
К раствору 9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-ил-трифторметансульфоната (F) (10,1 г, 19,67 ммоль) в DMF (66 мл) и MeOH (33 мл) добавляли Pd(dppf)Cl2 (909 мг, 1,18 ммоль) и диизопропилэтиламин (7,21 мл). Черную суспензию карбонилировали в автоклаве при 70°C в атмосфере CO при 5 бар в течение 5 часов. Реакционную смесь фильтровали, затем фильтрат частично концентрировали при пониженном давлении. Остаток разделяли между AcOEt и водой. Органическую фазу промывали водой (2Ч100 мл), высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом DCM/MeOH от 100/0 до 95/05 с получением 7,13 г (86%) метил-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата (G) в виде коричневой смолы.
LC/MS (масса/заряд, MH+): 424
Промежуточное соединение (A1). 5-Оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-илтрифторметансульфонат
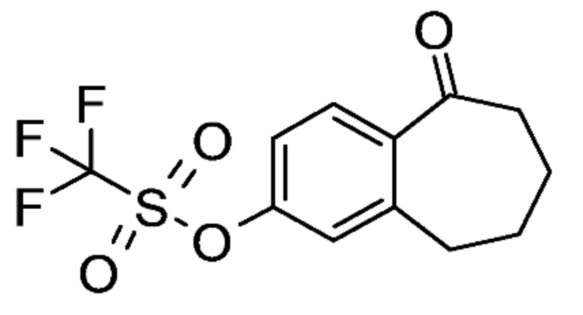
К раствору коммерчески доступного 2-гидрокси-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-5-она (A) (18,5 г, 105 ммоль) в DCM (185 мл) и лутидина (13,35 мл, 113,505 ммоль), охлажденному при 5°C в атмосфере аргона, добавляли по каплям ангидрид трифторметансульфоновой кислоты (20,22 мл, 123,29 ммоль), при этом поддерживая температуру от 10 до 20°C. Реакционную смесь перемешивали в течение 1 часа при 5°C, затем при комнатной температуре в течение 1 часа.
Затем добавляли лед (200 г) и взвесь разделяли между водой и DCM. Органическую фазу промывали водным раствором NaHCO3, высушивали над MgSO4, отфильтровывали и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом гептана/AcOEt от 100 до 90/10 с получением 28,2 г (87%) 5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-ил-трифторметансульфоната (A1) в виде оранжевого масла.
LC/MS (масса/заряд, MH+): 309
Промежуточное соединение (B1). Метил-5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-карбоксилат
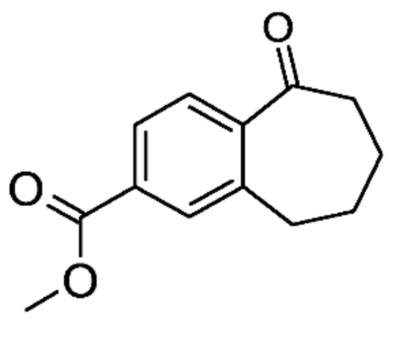
К раствору 5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-илтрифторметансульфоната (A1) (5,03 г, 16,32 ммоль) в DMF (24 мл) и MeOH (12 мл) добавляли Pd(dppf)Cl2 (754 мг, 0,98 ммоль) и диизопропилэтиламин (6 мл). Черную суспензию карбонилировали в автоклаве при 70°C в атмосфере CO при 5 бар в течение 2,5 часов. Реакционную смесь фильтровали, затем фильтрат частично концентрировали при пониженном давлении и остаток разделяли между AcOEt и водой. Органическую фазу промывали водой (2Ч75 мл) и 0,5 н. водным раствором HCl, высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом гептана/AcOEt от 100/0 до 90/10 с получением 3,4 г (95%) метил-5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-карбоксилата (B1) в виде бесцветного масла.
LC/MS (масса/заряд, MH+): 219
Промежуточное соединение (C1). Метил-9-(трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилат
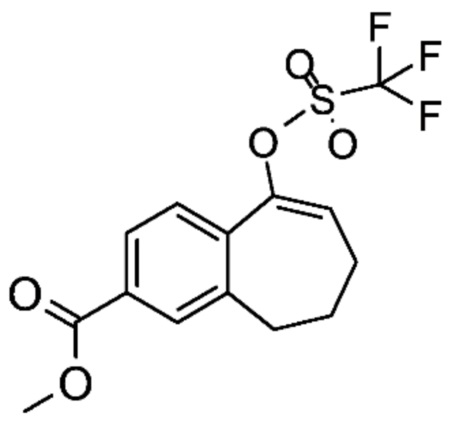
К раствору метил-5-оксо-6,7,8,9-тетрагидро-5H-бензо[7]аннулен-2-карбоксилата (B1) (18,19 г, 83,34 ммоль) в DCM (500 мл) и безводном пиридине (11 мл, 130,56 ммоль), охлажденному до 5°C в атмосфере аргона, добавляли по каплям ангидрид трифторметансульфоновой кислоты (30 мл, 176,54 ммоль). Реакционную смесь, густую суспензию, перемешивали при комнатной температуре в течение 24 часов, затем добавляли лед и разделяли между водой и DCM. Органическую фазу высушивали над MgSO4, отфильтровывали и концентрировали при пониженном давлении с получением 29 г (100%) метил-9-(трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата (C1) в виде желтой смолы.
LC/MS (масса/заряд, MH+): 351
Промежуточное соединение (G). Метил-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилат
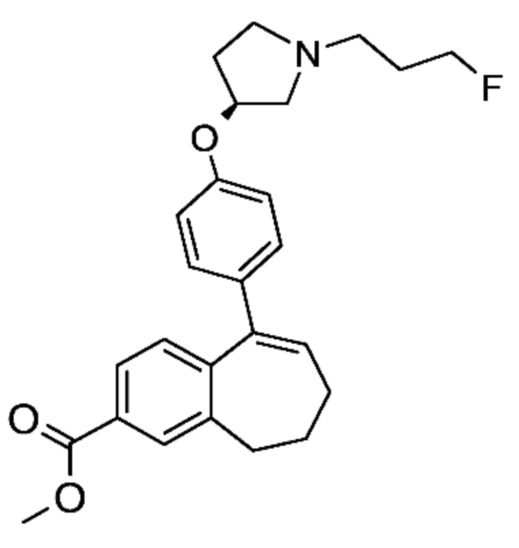
К раствору метил-9-(трифторметансульфонилокси)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата (C1) (29 г, 82,9 ммоль), (3S)-1-(3-фторпропил)-3-[4-(тетраметил-1,3,2-диоксаборолан-2-ил)фенокси]пирролидина (e) (28,9 г, 82,9 ммоль) в диоксане (225 мл) добавляли Pd(dppf)Cl2 в атмосфере аргона в комплексе с DCM (3,73 г, 4,57 ммоль) и 1,5 M водным раствором Cs2CO3 (111,12 мл, 166,68 ммоль). Реакционную смесь перемешивали при 60°C в течение 1 часа.
После охлаждения до комнатной температуры реакционную смесь выливали в смесь воды (500 мл) и AcOEt (400 мл). Органическую фазу промывали солевым раствором, высушивали над MgSO4, фильтровали на целите и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом DCM/MeOH от 100/0 до 95/05 с получением 23 г (65%) метил-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата (G) в виде коричневой смолы.
LC/MS (масса/заряд, MH+): 424
Промежуточное соединение (H). Метил-8-бром-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата гидробромид
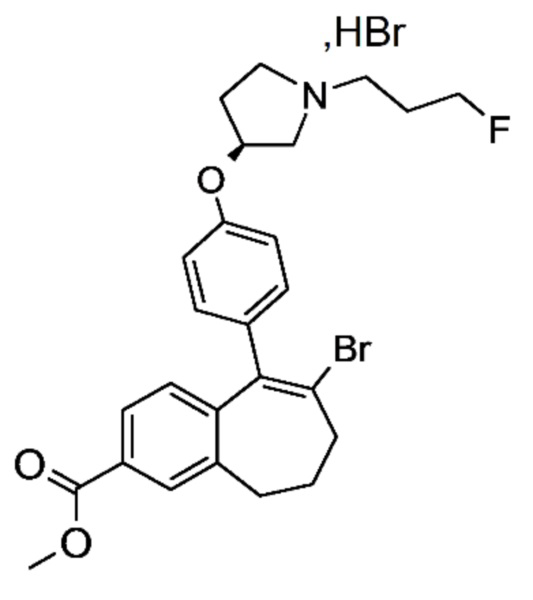
К раствору метил-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата (G) (13,93 г, 32,89 ммоль) в DCM (150 мл) добавляли в атмосфере аргона трибромид пиридиния (15,78 г, 44,41 ммоль). Реакционную смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли воду (200 мл), органическую фазу затем высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью флэш-хроматографии с элюированием градиентом DCM/MeOH от 100/0 до 95/05 с получением 16,4 г (85%) метил-8-бром-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата гидробромида (H) в виде желтой меренги.
LC/MS (масса/заряд, MH+): 502
Промежуточное соединение (I). Сложный метиловый эфир 6-(2,4-дихлорфенил)-5-{4-[1-(3-фторпропил)пирролидин-3-илокси]фенил}-8,9-дигидро-7H-бензоциклогептен-2-карбоновой кислоты
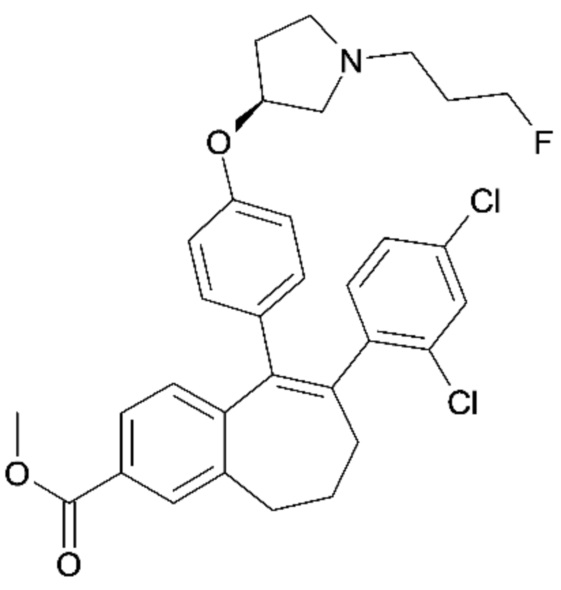
К раствору метил-8-бром-9-(4-{[(3S)-1-(3-фторпропил)пирролидин-3-ил]окси}фенил)-6,7-дигидро-5H-бензо[7]аннулен-3-карбоксилата гидробромида (H) (150 мг, 298,56 мкмоль) в диоксане (12 мл) и воде (2 мл) добавляли 2,4-дихлорфенилбороновую кислоту (62,67 мг, 328,41 мкмоль), Cs2CO3 (204,48 мг, 626,97 мкмоль) и Pd(dppf)Cl2 (14,63 мг, 17,91 мкмоль). Реакционную смесь нагревали при 90°C в течение 3 часов и разделяли между AcOEt и водой. Фазы разделяли и органическую фазу промывали солевым раствором, высушивали над MgSO4 и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии с элюированием смесью DCM, ацетонитрила и MeOH (96/2/2; об./об./об.) с получением 80 мг (47%) сложного метилового эфира 6-(2,4-дихлорфенил)-5-{4-[1-(3-фторпропил)пирролидин-3-илокси]фенил}-8,9-дигидро-7H-бензоциклогептен-2-карбоновой кислоты (I).
LC/MS (масса/заряд, MH+): 568
Соединение (1). 6-(2,4-Дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновая кислота
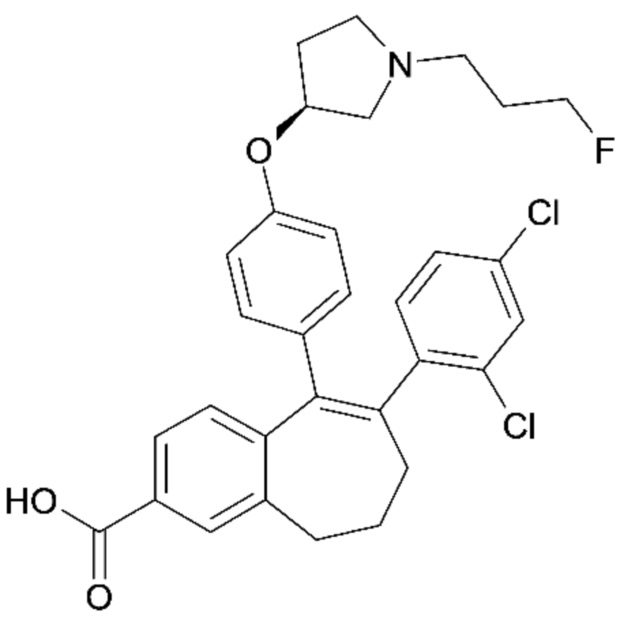
К раствору сложного метилового эфира 6-(2,4-дихлорфенил)-5-{4-[1-(3-фторпропил)пирролидин-3-илокси]фенил}-8,9-дигидро-7H-бензоциклогептен-2-карбоновой кислоты (I) (80 мг, 140,72 мкмоль) в MeOH (5 мл) добавляли раствор NaOH (562,88 мкл, 5 M), и реакционную смесь нагревали при 60°C в течение 5 часов, и растворитель удаляли при пониженном давлении. Остаток поглощали водой (10 мл) и добавляли водный раствор HCl (5 M) до pH 7. Взвесь экстрагировали с помощью DCM, высушивали над MgSO4 и концентрировали при пониженном давлении. Твердое вещество очищали с помощью колоночной хроматографии с элюированием смесью DCM, ацетонитрила и MeOH (90/5/5; об./об./об.) с получением 60 мг (77%) 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты.
1H ЯМР (400 МГц, DMSO-d6, д ppm): 1,68 (m, 1 H); 1,79 (dm, J=25,3 Гц, 2 H); 2,07 до 2,23 (m, 5 H); 2,38 (m, 1 H); 2,46 (t, J=7,2 Гц, 2 H); 2,52 (m, 1 H); 2,62 (m, 1 H); 2,55 до 2,89 (m, 3 H); 4,47 (td, J=6,2 и 47,6 Гц, 2 H); 4,72 (m, 1 H); 6,63 (d, J=8,9 Гц, 2 H); 6,71 (m, 3 H); 7,18 (d, J=8,4 Гц, 1 H); 8,26 (dd, J=2,0 и 8,4 Гц, 1 H); 7,58 (d, J=2,0 Гц, 1 H); 7,63 (d, J=8,4 Гц, 1 H); 7,79 (s, 1 H); 12,3 (m, 1 H)
LC/MS (масса/заряд, MH+): 554
2. Оценка эффективности 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты, объединенной с палбоциклибом, в отношении подкожного ксенотрансплантата линии раковых клеток молочной железы у самок мышей, лишенных шерсти
В данном исследовании исследовали противоопухолевую эффективность 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты ("соединение (1)"), объединенной с ингибитором циклин-зависимой киназы 4 (CDK4) палбоциклибом, через 30 дней обработки в отношении подкожного ксенотрансплантата линии раковых клеток молочной железы MCF7-Y537S у самок мышей, лишенных шерсти.
Обработанные группы предусматривали введение соединения (1) в дозе 5 мг/кг в отдельности, палбоциклиба в дозе 100 мг/кг в отдельности и комбинации соединения (1) и палбоциклиба в той же дозе и при той же схеме введения.
Соединение (1) вводили перорально дважды в сутки (BID) и палбоциклиб вводили перорально один раз в сутки (QD) в течение 30 дней. Противоопухолевую эффективность оценивали путем измерения объема опухоли.
2-1. Экспериментальная процедура
2-1-1. Животные, клеточная линия, соединения
Самок безтимусных мышей, лишенных шерсти, получали от Harlan (Индианаполис, Индиана, США). Животным обеспечивали возможность акклиматизации в течение по меньшей мере четырех дней до включения в исследование. Мыши имели возраст 12-13 недель и имели массу от 20,2 до 27,3 грамм в начале проведения обработок. Данных животных содержали в условиях, указанных в руководстве NIH по уходу и применению лабораторных животных согласно закону о благополучии лабораторных животных USDA.
Родительские клетки MCF7 получали от Американской коллекции типовых культур (ATCC® HTB-22™). Клеточная линия MCF7-Y537S (ESR1) представляла собой клетки MCF7, экспрессирующие вариант ER.Y537S, который был получен Sanofi Biology Discovery Group. Мутацию Y537S вводили в конструкцию ESR1 (GenBank NM_000125.3) путем сайт-направленного мутагенеза (Toy W. et al., Cancer Discovery, 2017, 7, 277-287). Конструкцией трансфицировали клетки MCF7, которые были выбраны из-за возможности их роста в отсутствие эстрадиола. MCF-Y537S представляет собой мутацию ESR1, которая придает эстроген-независимую активность ERб (эстрогеновый рецептор альфа) и способствует развитию эндокринного устойчивого заболевания (Robinson D.R. et al., Nat Genet., 2013, 45 (12), 1446-1451). Клетки выращивали в минимальной эссенциальной среде Игла (EMEM), дополненной 10% фетальной бычьей сывороткой (FBS), инсулином человека, в 5% CO2 при 37°C. Клетки собирали в 0,25% трипсин-EDTA и промывали фосфатно-солевым буферным раствором Дульбекко (DPBS) и повторно суспендировали в DPBS с 50% матригеля (№ по каталогу Becton Dickinson 356234, № партии 32277). Клетки (20 Ч 106 клеток/на мышь) подкожно (SC) имплантировали в правый бок самкам мышей, лишенных шерсти.
Когда опухоли MCF7-Y537S развились, опухоли сохраняли как исходные опухоли для имплантации фрагмента. Опухоли подвергали серийному размножению посредством подкожной трансплантации фрагмента ткани. Фрагмент опухолевых тканей подкожно имплантировали в правый бок самкам мышей, лишенных шерсти. 50 мышей распределяли в данном эксперименте.
Соединение (1) и палбоциклиб (коммерчески доступный, представленный на рынке под торговым названием Ibrance®) составляли следующим образом:
. среда-носитель A: 20% Labrasol® (полученная от Gattefosse SAS, Франция);
. среда-носитель B: 5% декстроза.
Соединение (1) подготавливали в среде-носителе A, затем добавляли Solutol HS15 (приобретенный у Sigma) до конечной концентрации 5% и обеспечивали перемешивание раствора в течение одного часа до полного растворения. После этого добавляли среду-носитель B. Конечное значение pH составляло 5,5.
Объем дозы для введения соединения (1): 10 мл/кг с помощью желудочного зонда.
Дозы: 5 мг/кг (доза соединения (1) в указанном выше объеме).
Палбоциклиб подготавливали в среде-носителе A, затем добавляли Solutol HS15 до конечной концентрации 5% и обеспечивали перемешивание раствора в течение одного часа до полного растворения. После этого добавляли среду-носитель B. Конечное значение pH составляло 5,5.
Объем дозы: 10 мл/кг с помощью желудочного зонда.
Дозы: 100 мг/кг (доза палбоциклиба в указанном выше объеме).
2-1-2. Схема исследования, конечные точки
Животных, необходимых для эксперимента (плюс дополнительные), объединяли и им имплантировали фрагменты опухолевых тканей MCF7-Y537S в день 0. В день 21 после имплантирования мышей объединяли и произвольным образом распределяли в группы обработки и контроля (10 мышей на группу), при этом значения медианного объема опухоли для каждой группы, находились в диапазоне от 202,5 до 211,5 мм3. Обработки с помощью соединения (1) и палбоциклиба начинали в день 22. Соединение (1) перорально вводили в дозе 5 мг/кг BID (с интервалом по меньшей мере 5 часов) и палбоциклиб перорально вводили в дозе 100 мг/кг QD в течение 30 дней. Массу тела животного оценивали ежедневно.
Дозы выражали в мг/кг и на основе ежедневной массы тела на животное. Обработанных средой-носителем животных применяли в качестве контролей. Мышей проверяли ежедневно и отмечали нежелательные клинические реакции. Отдельных мышей взвешивали ежедневно до конца эксперимента. Мышей умерщвляли, если наблюдали болезненность или потерю массы, составляющую ≥ 20%. Опухоли измеряли штангенциркулем два раза в неделю до умерщвления по окончании. Когда размер опухоли достигал примерно 2000 мм3 или когда возникали проблемы со здоровьем животных (изъязвление 40% площади опухоли), животных подвергали эвтаназии и записывали дату смерти. Объемы солидных опухолей оценивали на основании двух измеренных размеров опухолей и рассчитывали согласно следующему уравнению:
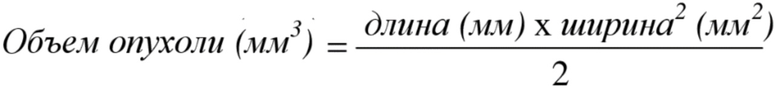
Конечные точки оценки токсичности
Доза, обеспечивающая либо потерю 15% массы тела в течение 3 дней подряд для отдельной мыши, либо потерю 20% массы тела в течение 1 дня, либо 10% или больше смертей, связанных с приемом лекарственного средства, считалась чрезмерно токсичной дозой, за исключением некоторых случаев, если потеря массы тела или смерть животного может считаться не связанной с приемом лекарственного средства. Примеры включают проблемы, связанные с обращением с животным, такие как осложнения установки желудочного зонда, связанные с моделью опухоли проблемы, такие как индуцированная опухолью кахексия, приводящая к потере массы тела, которая может наблюдаться в группах контроля или обработки средой-носителем, и чрезмерное изъязвление опухоли. Мыши, которые умерли не связанной с приемом лекарственного средства смертью или для которых наблюдалась значительная потеря массы тела, не будут считаться подвергнутыми токсичному воздействию и будут исключены из статистического анализа. Масса тела животного включала массу опухоли.
Конечные точки оценки эффективности
Первичные конечные точки оценки эффективности включают изменения объема опухоли относительно исходного уровня, кратко представленные с помощью соотношения медиан изменений объема опухоли относительно исходного уровня между группами обработки и контроля (ДT/ДC). Изменения объема опухоли для каждой группы обработки (T) и контрольной группы (C) рассчитывали для каждого животного каждый день путем вычитания объема опухоли в день первой обработки (день определения стадии) из объема опухоли в указанный день наблюдения. Медианное значение ДT рассчитывали для группы обработки, а медианное значение ДC рассчитывали для контрольной группы. Рассчитывали соотношение ДT/ДC и выражали в виде процента:
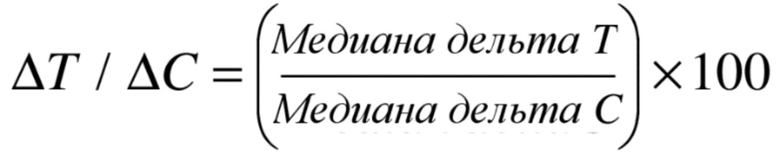
ДT/ДC ≤ 40% считается свидетельствующим о терапевтической активности, ДT/ДC=0% считается свидетельствующим об остановке роста опухоли, и ДT/ДC < 0% считается свидетельствующим о регрессии опухоли (высокая активность). ДT/ДC > 40% считается свидетельствующим об отсутствии терапевтической активности.
Процент регрессии опухоли определяли как % (процент) снижения объема опухоли в группе обработки в указанный день наблюдения по сравнению с ее объемом в начале исследования. В конкретный момент времени (t) и для каждого животного процент регрессии рассчитывали с помощью следующей формулы:
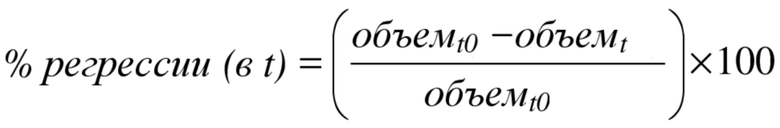
Затем рассчитывали медианный процент регрессии для группы в данный день путем определения медианы индивидуальных значений % регрессии, рассчитанных для каждого животного в группе. День расчета определяли по дню, в который рассчитывали ДT/ДC, за исключением случаев, в которых медианный процент регрессии не отражает активность в группе. В данном случае день определяли по первому дню, в который медианный процент регрессии был максимальным.
2-1-3. Статистический анализ
В отношении изменений объема опухоли относительно исходного уровня проводили двухфакторный анализ типа ANOVA с обработкой и днем в качестве факторов (с повторными измерениями). После него следовали контрастные анализы с поправкой Холма-Бонферрони на множественность для сравнения всех групп обработки с группой контроля и для сравнения комбинации с каждым отдельным средством в дозе, включенной в комбинацию, в каждый день от дня 27 до 51.
На фигурах медианы и абсолютное отклонение медианы (MAD) для каждой группы представлены для каждого дня измерения.
В таблицах медианы и нормализованные значения MAD (nMAD=1,4826*MAD) для каждой группы представлены для каждого дня измерения.
Изменения объема опухоли относительно исходного уровня рассчитывали для каждого животного и каждого дня путем вычитания объема опухоли в день первой обработки (день 21) из объема опухоли в указанный день наблюдения.
Все статистические анализы выполняли с помощью программного обеспечения SAS версии 9.2. Вероятность менее 5% (p < 0,05) считалась статистически значимой.
2-2. Результаты
Соединение (1) в дозе 5 мг/кг BID, палбоциклиб в дозе 100 мг/кг QD и комбинация соединения (1) и палбоциклиба в дозах и схеме введения в течение 30 дней хорошо переносились в данном исследовании, демонстрируя изменение средней массы тела в % на группу при максимальных значениях снижения (самое меньшее уменьшение массы тела в группе) -1,7% (день 22), -2,0% (день 22) и -6,4% (день 26) соответственно (таблица 1).
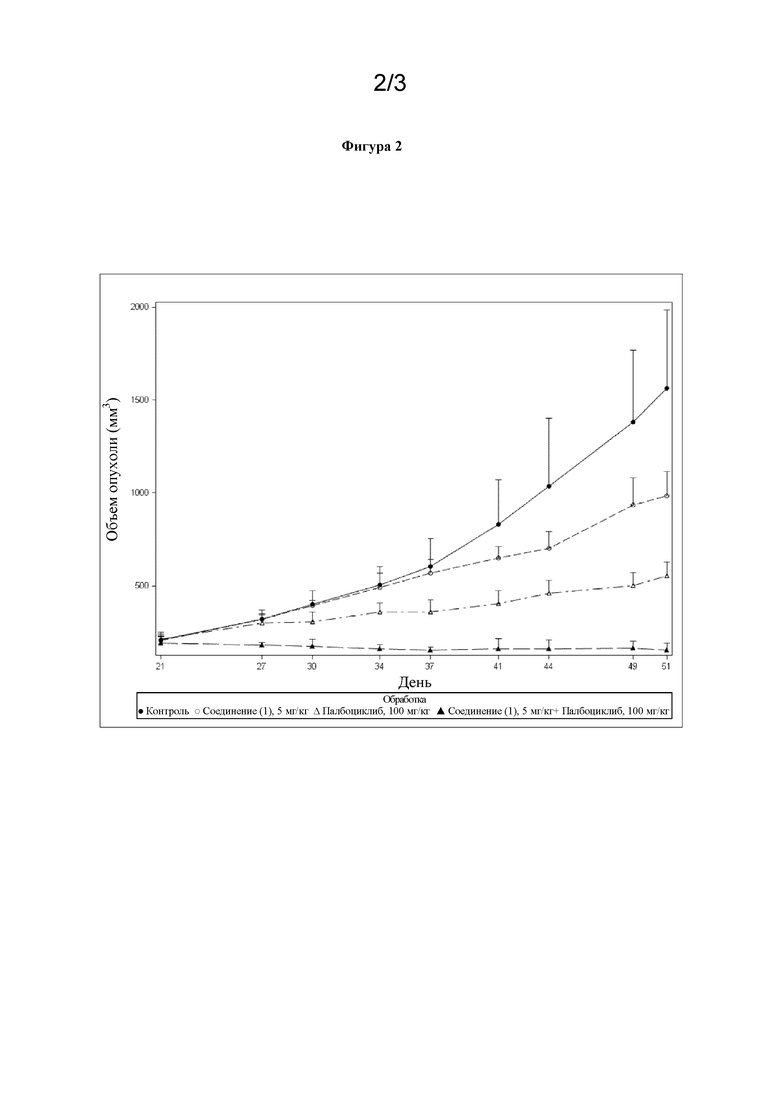
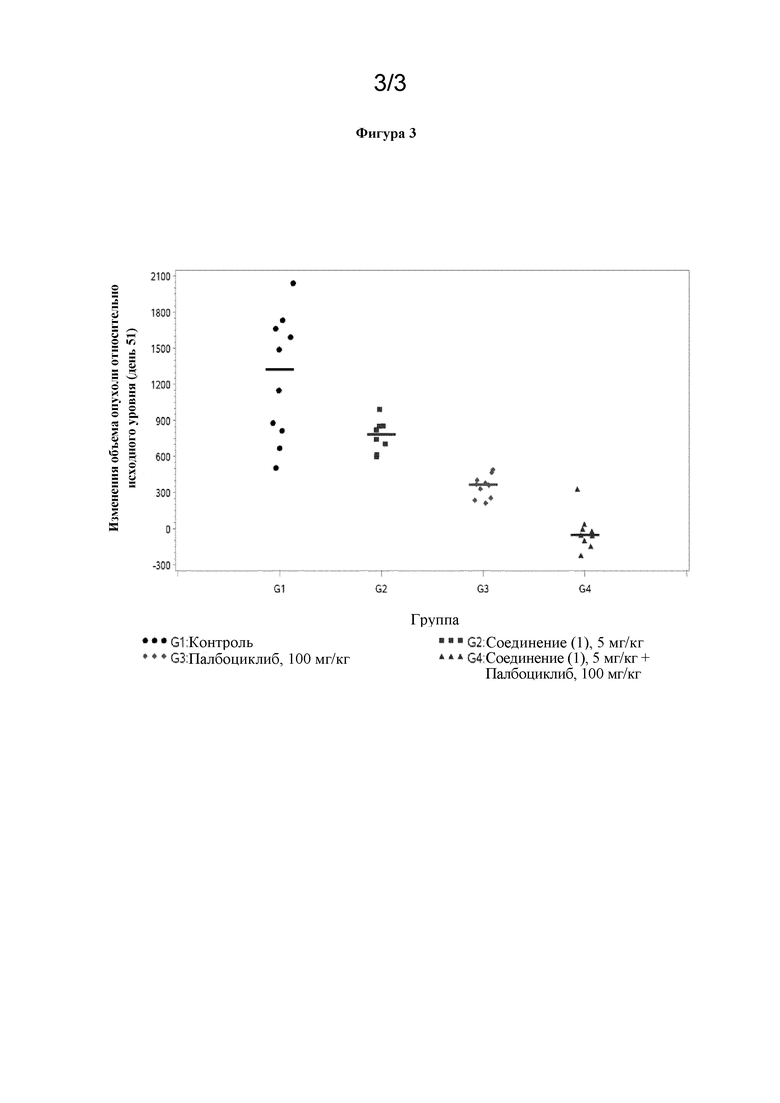
Соединение (1) в дозе 5 мг/кг BID в течение 30 дней обладало минимальным эффектом в отношении роста опухоли со значением ДT/ДC 59% (p=0,4113) в день 51. Палбоциклиб в дозе 100 мг/кг QD в течение 30 дней обладал противоопухолевой эффективностью со значением ДT/ДC 27% (p<0,0001) в день 51. При объединении соединения (1) в дозе 5 мг/кг с палбоциклибом в дозе 100 мг/кг с той же схемой введения доз в виде BID для соединения (1) и QD для палбоциклиба, обработка с помощью комбинации продемонстрировала высокую противоопухолевую эффективность со значением ДT/ДC менее 0 (p < 0,0001) и индуцировала регрессию опухоли (медиана регрессии опухоли 32%) в день 51. Статистический анализ продемонстрировал, что эффект комбинации в значительной степени отличался от эффекта либо соединения (1) в отдельности, либо палбоциклиба в отдельности в день 51 (p <0,0001). Подробные результаты показаны в таблицах 1, 2 и 3 ниже, а также на фигурах 2 и 3:
- фигура 2: противоопухолевая активность соединения (1), объединенного с палбоциклибом, в отношении подкожного ксенотрансплантата линии раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти: изменение объема опухоли. Кривые представляют собой медианы+или - MAD (абсолютное отклонение медианы) в каждый день для каждой группы;
- фигура 3: противоопухолевая активность соединения (1), объединенного с палбоциклибом, в отношении подкожного ксенотрансплантата линии раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти: изменения объема опухоли относительно исходного уровня в день 51. Точки представляют собой отдельные изменения объема опухоли относительно исходного уровня в день 51, планки соответствуют медианам.
Из данного эксперимента авторы настоящего изобретения сделали вывод, что соединение (1) в дозе 5 мг/кг два раза в сутки, объединенное с ингибитором CDK4 палбоциклибом в дозе 100 мг/кг один раз в сутки, обеспечивало значительную противоопухолевую эффективность и регрессию опухоли в модели ксенотрансплантата линии раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти, которая была лучше, чем в случае только монотерапии.
Таблица 1. Эффективность соединения (1), объединенного с палбоциклибом, в отношении подкожного ксенотрансплантата раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти.
Доза
(в мл/кг на инъекцию)
(общая доза)
в днях (всего 30 дней)
(День смерти)
день 47 #
ческая интерпре
тация
ные
ные
(10)
+
палбоциклиб
PO, QD
(10)
+
100 (3000)
N.B.: животным давали одну дозу в день начала.
NR: отсутствие регрессии (0% регрессии).
# Статистический анализ: Сравнение каждого отдельного средства и комбинации с группой контроля. Получали p-значения с применением контрастного анализа для сравнения каждой группы обработки с контролем в каждый день с применением поправки Холма-Бонферрони на множественность после двухфакторного анализа типа ANOVA с повторными измерениями изменений объема опухоли относительно исходного уровня. Вероятность менее 5% (p < 0,05) считалась статистически значимой.
*3 мышей исключали из статистического анализа, поскольку эти мыши соответствовали не связанной с приемом лекарственного средства смерти или выведению из эксперимента во время исследования.
Таблица 2. Эффективность соединения (1), объединенного с палбоциклибом, в отношении модели подкожного ксенотрансплантата линии раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти. Сравнение каждой группы с группой контроля в каждый день.
(5 мг/кг)
(100 мг/кг)
(5 мг/кг) + палбоциклиб
(100 мг/кг)
* MAD= абсолютное отклонение медианы; nMAD= нормализованные значения MAD; nMAD= 1,4826*MAD.
Для палбоциклиба в дозе 100 мг/кг эффект в отношении изменений объема опухоли относительно исходного уровня являлся значительным по сравнению с группой контроля со дня 30 по день 51.
Для комбинации соединения (1) в дозе 5 мг/кг+палбоциклиба в дозе 100 мг/кг эффект в отношении изменений объема опухоли относительно исходного уровня являлся значительным по сравнению с группой контроля со дня 27 по день 51.
n=число животных. 3 мышей исключали из статистического анализа, поскольку эти мыши соответствовали не связанной с приемом лекарственного средства смерти или выведению из эксперимента во время исследования.
Таблица 3. Эффективность соединения (1), объединенного с палбоциклибом, в отношении модели подкожного ксенотрансплантата линии раковых клеток молочной железы человека MCF7-Y537S у мышей, лишенных шерсти. Сравнение соединения (1) в дозе 5 мг/кг и палбоциклиба в дозе 100 мг/кг в виде отдельных средств с комбинацией в каждый день.
(5 мг/кг)
+
палбоциклиб
(100 мг/кг)
(100 мг/кг)
(5 мг/кг)
* MAD= абсолютное отклонение медианы; nMAD= нормализованные значения MAD; nMAD= 1,4826*MAD.
Эффект комбинации соединения (1) в дозе 5 мг/кг+палбоциклиба в дозе 100 мг/кг являлся значительно большим, чем эффект палбоциклиба в дозе 100 мг/кг в отдельности со дня 34 до день 51.
Эффект комбинации соединения (1) в дозе 5 мг/кг+палбоциклиба в дозе 100 мг/кг значительно больше, чем эффект соединения (1) в дозе 5 мг/кг в отдельности со дня 27 по день 51.
n=число животных. 3 мышей исключали из статистического анализа, поскольку эти мыши соответствовали не связанной с приемом лекарственного средства смерти или выведению из эксперимента во время исследования.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ СОЕДИНЕНИЯ ЗАМЕЩЕННОГО N-(3-ФТОРПРОПИЛ)ПИРРОЛИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2017 |
|
RU2742278C2 |
| ИНГИБИТОРЫ Axl ДЛЯ ПРИМЕНЕНИЯ В КОМБИНИРОВАННОЙ ТЕРАПИИ ДЛЯ ПРЕДОТВРАЩЕНИЯ, УСТРАНЕНИЯ ИЛИ ЛЕЧЕНИЯ МЕТАСТAЗИРУЮЩЕГО РАКА | 2010 |
|
RU2555326C2 |
| КОМБИНАЦИИ СОЕДИНЕНИЙ-ИНГИБИТОРОВ АКТ И АБИРАТЕРОНА, И СПОСОБЫ ПРИМЕНЕНИЯ | 2012 |
|
RU2631240C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2764724C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ, СОДЕРЖАЩАЯ ИНГИБИТОР ALK И ИНГИБИТОР SHP2 | 2018 |
|
RU2769132C2 |
| ЗАМЕЩЕННЫЕ ПУРИНОВЫЕ И 7-ДЕАЗАПУРИНОВЫЕ СОЕДИНЕНИЯ | 2011 |
|
RU2606514C2 |
| ДВОЙНЫЕ АНТАГОНИСТЫ РЕЦЕПТОРА НЕЙРОКИНИН-1/НЕЙРОКИНИН-3 ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ЗАВИСИМЫХ ОТ ПОЛОВЫХ ГОРМОНОВ | 2016 |
|
RU2743206C2 |
| ТРИЦИКЛИЧЕСКОЕ ТЕТРАГИДРОИЗОХИНОЛИНОВОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2021 |
|
RU2830109C1 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2017 |
|
RU2769251C2 |
| ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ МЕНИН-MLL | 2017 |
|
RU2829484C2 |

Группа изобретений относится к области медицины, а именно к комбинации для лечения рака молочной железы, содержащей 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и палбоциклиб, а также к фармацевтической композиции для лечения рака молочной железы, содержащей 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и палбоциклиб и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество, также относится к применению 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты или ее фармацевтически приемлемой соли, осуществляемому путем совместного введения с палбоциклибом для лечения рака молочной железы, и к применению палбоциклиба, осуществляемому путем совместного введения с 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислотой или ее фармацевтически приемлемой солью для лечения рака молочной железы, и также относится к фармацевтическому набору для лечения рака молочной железы, содержащему: (i) первую фармацевтическую композицию, содержащую 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество; (ii) вторую фармацевтическую композицию, содержащую палбоциклиб и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество; при этом обе фармацевтические композиции (i) и (ii) находятся в отдельных камерах и предназначены для независимого друг от друга введения, при этом каждое введение в отношении другого является одновременным, раздельным или распределенным во времени. Группа изобретений обеспечивает разработку комбинации 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3- фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты с палбоциклибом, которая хорошо переносится, демонстрирует высокую противоопухолевую эффективность и вызывает регрессию опухоли с синергетическим эффектом по сравнению с каждым активным ингредиентом в отдельности. 5 н. и 5 з.п. ф-лы, 3 табл., 2 пр., 3 ил.
1. Комбинация для лечения рака молочной железы, содержащая 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и палбоциклиб.
2. Комбинация по п. 1, демонстрирующая терапевтическую синергию.
3. Комбинация по п. 1 или 2, где оба соединения вводятся одновременно, по отдельности или раздельно в течение некоторого периода времени.
4. Фармацевтическая композиция для лечения рака молочной железы, содержащая 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и палбоциклиб и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество.
5. Фармацевтическая композиция по п. 4, где 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновая кислота или ее фармацевтически приемлемая соль и палбоциклиб вводятся одновременно, по отдельности или раздельно в течение некоторого периода времени.
6. Применение 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислоты или ее фармацевтически приемлемой соли, осуществляемого путем совместного введения с палбоциклибом для лечения рака молочной железы.
7. Применение по п. 6, где 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновая кислота или ее фармацевтически приемлемая соль вводится одновременно, по отдельности или раздельно в течение некоторого периода времени с палбоциклибом.
8. Применение палбоциклиба, осуществляемого путем совместного введения с 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислотой или ее фармацевтически приемлемой солью для лечения рака молочной железы.
9. Применение по п. 8, где палбоциклиб вводится одновременно, по отдельности или раздельно в течение некоторого периода времени с 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновой кислотой или ее фармацевтически приемлемой солью.
10. Фармацевтический набор для лечения рака молочной железы, содержащий:
(i) первую фармацевтическую композицию, содержащую 6-(2,4-дихлорфенил)-5-[4-[(3S)-1-(3-фторпропил)пирролидин-3-ил]оксифенил]-8,9-дигидро-7H-бензо[7]аннулен-2-карбоновую кислоту или ее фармацевтически приемлемую соль и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество;
(ii) вторую фармацевтическую композицию, содержащую палбоциклиб и по меньшей мере одно фармацевтически приемлемое вспомогательное вещество;
при этом обе фармацевтические композиции (i) и (ii) находятся в отдельных камерах и предназначены для независимого друг от друга введения, при этом каждое введение в отношении другого является одновременным, раздельным или распределенным во времени.
| WO 2016151063 A1, 29.09.2016 | |||
| WO 2016146591 A1, 22.09.2016 | |||
| Suzanne E Wardell et al., Efficacy of SERD/SERM Hybrid-CDK4/6 Inhibitor Combinations in Models of Endocrine Therapy-Resistant Breast Cancer / Clinical Cancer Research, 2015, Vol.21, N.22, pp.5121-5130. |
Авторы
Даты
2022-01-13—Публикация
2018-07-23—Подача