УРОВЕНЬ ТЕХНИКИ
Область техники, к которой относится изобретение:
Настоящее изобретение касается способа получения органического структурообразующего агента, используемого в синтезе цеолитов.
Описание предшествующего уровня техники:
Цеолиты представляют собой пористые кристаллические или квазикристаллические структуры, имеющие каркас, построенный из неорганических оксидов, таких как силикаты и алюминаты, организованных в регулярно повторяющуюся структуру. Эти каркасы состоят из структур пространств и каналов, которые приводят к молекулярно-пористой природе цеолита. Каждой особой структуре цеолита, признанной структурной комиссией Международной ассоциации по цеолитам (IZA), присвоен трехбуквенный код для обозначения типа каркаса, такой как CHA (хабазит), BEA (бета) и MOR (морденит).
Определенные кристаллы цеолита могут быть сформированы смешением различных оксидов в присутствии органического структурообразущего агента (SDA), например четвертичных органических солей тетраметиламмония (TMA). SDA служит своего рода матрицей, вокруг которой различные строительные блоки цеолита могут разворачиваться и объединяться, образуя кристаллическую структуру решетки. После того, как кристаллы цеолита сформируются, они могут быть отделены от маточного раствора хозяина и высушены. Затем полученные кристаллы, как правило, нагревают, чтобы термически разложить внутренние молекулы SDA, после чего остатки SDA можно экстрагировать из кристалла цеолита, оставляя тем самым только пористый оксидный каркас цеолита.
SDA часто представляют собой молекулы сложного состава, для синтеза которых требуется много времени и многостадийные процессы. Относительно высокая стоимость SDAs и тот факт, что они расходуются при синтезе цеолита, являются значительными факторами, влияющими на стоимость изготовления цеолита. Таким образом, по-прежнему существует необходимость в разработке более эффективных, экономичных путей синтеза для производства SDAs в коммерческом масштабе. Данное изобретение, среди прочего, удовлетворяет эту потребность.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Установлено, что циклический амин может быть быстро и легко превращен в функциональный SDA, например гидроксид 1,1,3,5-тетраметилпиперидин-1-ия. Например, взаимодействие циклического амина с алкилсульфатом дает новую промежуточную четвертичную аммониевую соль с алкилсульфатным противоионом. Взаимодействие этой четвертичной аммониевой/алкилсульфатной соли с гидролитическим агентом, таким как серная кислота, превращает алкилсульфатный противоион в гидросульфатный противоион, который затем может быть подвергнут взаимодействию с гидроксидным источником, с образованием гидроксидной формы SDA и неорганической сульфатной соли, последняя из которых образует осадок, который может быть легко удален из раствора. Таким образом, предлагаемый процесс, описанный здесь, является простым, но новым путем синтеза SDA. Преимущественно настоящий способ также сразу приводит к SDA в гидроксидной форме, которую легче использовать в синтезе цеолита. Кроме того, настоящее изобретение может приводить к SDA с низкими концентрациями щелочных металлов и серы.
Таким образом, предлагается способ получения структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит, включающий стадии (а) гидролиза алкилсульфатного противоиона четвертичной аммониевой соли, с получением четвертичной аммониевой соли, содержащей гидросульфатный противоион; и (b) контактирования четвертичной аммониевой соли, содержащей гидросульфатный противоион, с источником гидроксида в растворе, с образованием четвертичной аммониевой соли, содержащей гидроксидный противоион; где четвертичная аммониевая соль представляет собой структурообразущий агент (SDA) для синтеза кристаллических молекулярных сит.
В другом аспекте предлагается новая композиция, включающая, по меньшей мере, одно из нижеперечисленного: метилсульфат N,N-диметил-3,5-диметилпиперидиния; метилсульфат N,N-диэтил-2,6-диметилпиперидиния; метилсульфат N,N-диметил-9-азониабицикло[3.3.1]нонана; метилсульфат N,N-диметил-2,6-диметилпиперидиния; алкилсульфат N-этил-N-метил-2,6-диметилпиперидиния; этилсульфат N,N-диэтил-2-этилпиперидиния; метилсульфат N,N-диметил-2-этилпиперидиния; алкилсульфат N-этил-N-метил-2-этилпиперидиния; алкилсульфат N-этил-N-пропил-2,6-диметилпиперидиния и метилсульфат 2,2,4,6,6-пентаметил-2-азониабицикло[3.2.1]октана.
В другом аспекте предлагается композиция, включающая, по меньшей мере, одно из нижеперечисленного: гидросульфат N,N-диметил-3,5-диметилпиперидиния; гидросульфат N,N-диэтил-2,6-диметилпиперидиния; гидросульфат N,N-диметил-9-азониабицикло[3.3.1]нонана; гидросульфат N,N-диметил-2,6-диметилпиперидиния; гидросульфат N-этил-N-метил-2,6-диметилпиперидиния; гидросульфат N,N-диэтил-2-этилпиперидиния; гидросульфат N,N-диметил-2-этилпиперидиния; гидросульфат N-этил-N-метил-2-этилпиперидиния; гидросульфат N-этил-N-пропил-2,6-диметилпиперидиния и гидросульфат 2,2,4,6,6-пентаметил-2-азониабицикло[3.2.1]октана.
В дальнейшем аспекте предлагается способ получения структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит, включающий стадии: (a) взаимодействия предшественника четвертичного аммониевого-SDA с одним или более диалкилсульфатами в растворе, с образованием первого промежуточного раствора; (b) контактирования первого промежуточного раствора с кислотой или основанием, с образованием второго промежуточного раствора, содержащего гидросульфатный анион; и (c) контактирования второго промежуточного раствора с основанием, с образованием конечного раствора, содержащего гидроксидную форму SDA на основе аммония.
В еще одном аспекте изобретения предлагается способ получения структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит, включающий стадии: (a) взаимодействия необязательно замещенного предшественника SDA на основе пиридина с одним или более диалкилсульфатами в растворе, с образованием первого промежуточного раствора, содержащего алкилсульфат пиридиния; (b) восстановления первого промежуточного раствора алкилсульфата пиридиния, с получением второго промежуточного раствора алкилсульфата пиперидиния; (c) взаимодействия второго промежуточного раствора алкилсульфата пиперидиния с одним или более диалкилсульфатами в растворе, с образованием третьего промежуточного раствора алкилсульфата пиперидиния; (d) контактирования третьего промежуточного раствора с кислотой или основанием, с получением четвертого промежуточного раствора гидросульфата пиперидиния; и (e) контактирования четвертого промежуточного раствора с основанием, с получением конечного раствора, содержащего гидроксидную форму SDA на основе аммония.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
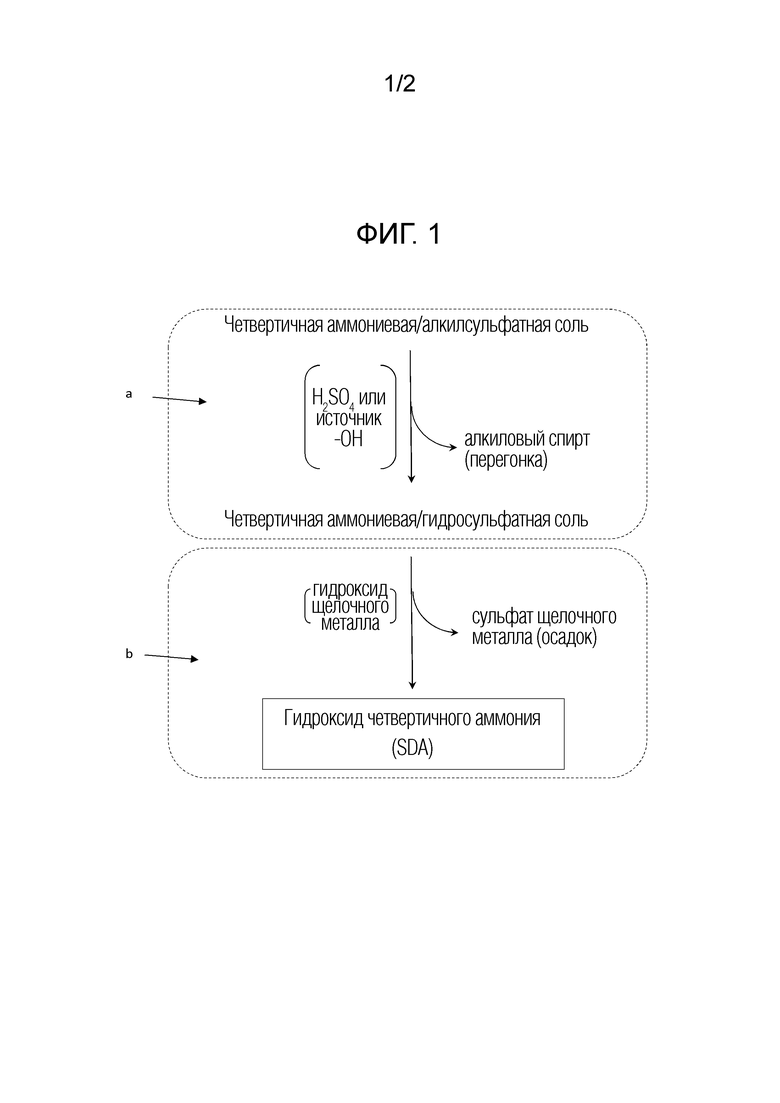
Фиг. 1 представляет собой схему, показывающую синтез SDA согласно варианту осуществления изобретения и
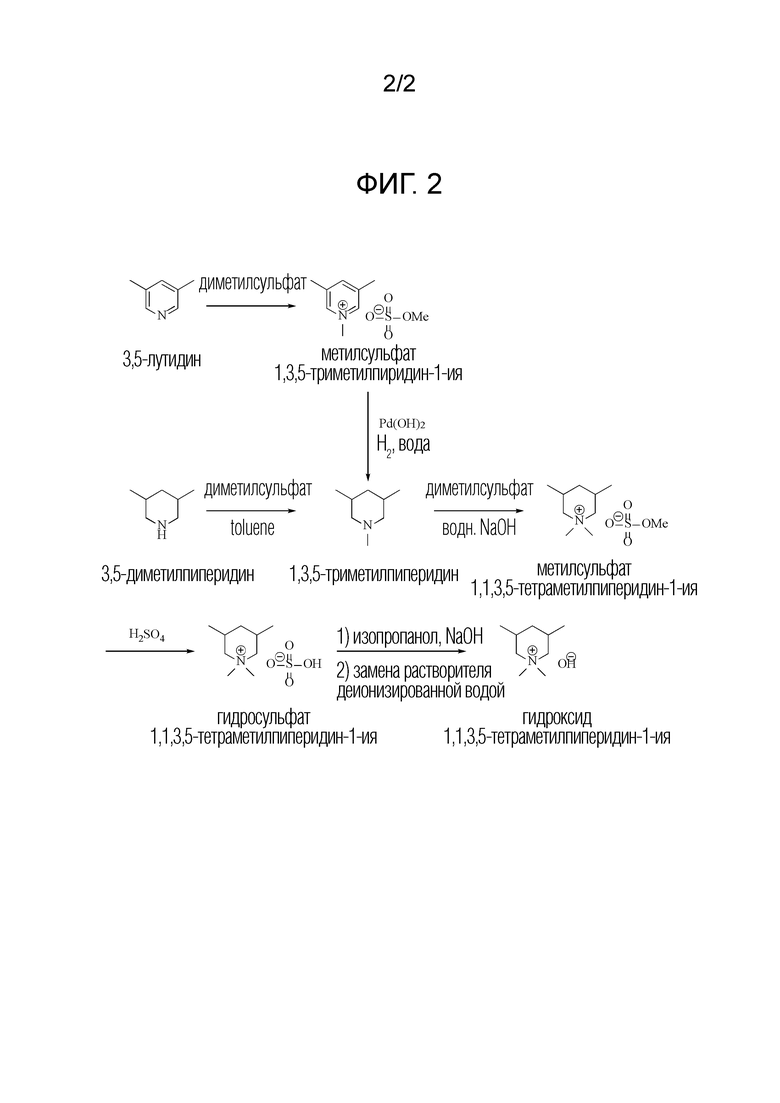
Фиг. 2 представляет собой схему, показывающую синтез гидроксида N,N-диметил-3,5-диметилпиперидиния согласно варианту осуществления изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Предложены улучшенные способы получения структурообразущих агентов (SDAs), используемых для синтеза кристаллических молекулярных сит, (напр., цеолита). В некоторых вариантах осуществления способы улучшены, отчасти, за счет быстрого образования заданного SDA в гидроксидной форме, без необходимости в процессе обмена ионами металлов (напр., с ионообменной смолой). SDAs, полученные настоящим способом, включают SDAs, полезные для синтеза цеолитов, имеющих один или более следующих каркасов: CHA, AEI, AFX, AFT, ERI и LEV, включая срастания двух или более из них. Такие SDAs включают гидроксид N,N-диметил-3,5-диметилпиперидиния и гидроксид N,N-диметил-2,6-диэтилпиперидиния.
Предложены улучшенные способы получения структурообразущих агентов (SDAs), используемых для синтеза кристаллических молекулярных сит, (напр., цеолита). В некоторых вариантах осуществления способы улучшены, отчасти, за счет быстрого образования заданного SDA в гидроксидной форме, без необходимости в процессе обмена ионами металлов (напр., с ионообменной смолой). SDAs, полученные настоящим способом, включают SDAs, полезные для синтеза цеолитов, имеющих один или более следующих каркасов: CHA, AEI, AFX, AFT, ERI и LEV, включая срастания двух или более из них. Такие SDAs включают гидроксид N,N-диметил-3,5-диметилпиперидиния и гидроксид N,N-диметил-2,6-диэтилпиперидиния.
В некоторых вариантах осуществления синтез SDA включает конверсию противоиона четвертичной аммониевой соли алкилсульфата до гидросульфата и затем до гидроксида способом, где сульфатная составляющая образует твердый осадок, который может быть легко удален из системы. Предпочтительно способ включает стадии: (a) гидролиза алкилсульфатного протитвоиона четвертичной аммониевой соли, с получением четвертичной аммониевой соли, содержащей гидросульфатный противоион; и (b) контактирования органической аммониевой соли, содержащей гидросульфатный противоион, с источником гидроксида в растворе, с образованием органической аммониевой соли, содержащей гидроксидный противоион; где гидроксидная форма органической четвертичной аммониевой соли используется в качестве структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит. Стадия (a) может быть осуществлена в присутствии кислоты, такой как серная кислота, или гидроксида. Преимущественно источник гидроксида на стадии (b) представляет собой гидроксид щелочного металла или гидроксид аммония. В некоторых вариантах осуществления способы дополнительно включают стадию экстрагирования SDA из реакционного раствора. В отдельных вариантах осуществления способы дополнительно включают образование предшественника четвертичной аммониевой соли в результате кватернизации циклического амина с использованием алкилсульфата. В некоторых вариантах осуществления способы также включают стадию алкилирования исходного материала, такого как 3,5-лутидин или 3,5-диметилпиперидин, с последующим восстановлением, с получением циклического амина, предпочтительно с использованием того же типа алкилсульфата, что использовался на стадии (a). Возвращаясь к стадии (a) способа, полезные четвертичные аммониевые соли предпочтительно включают неароматический, 5- или 6-членный, циклический ион аммония, в котором азот связан с двумя дополнительными алкилами или образует спироциклический центр второй циклической структуры. В некоторых вариантах осуществления четвертичный аммоний содержит следующую составляющую:
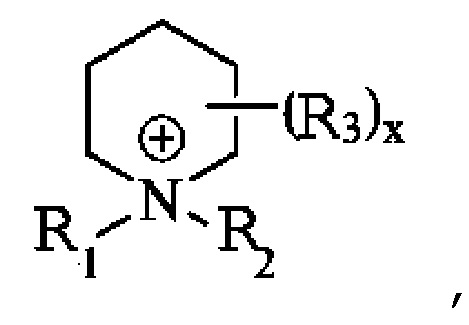
где R1 и R2 независимо означают алкил или члены циклической структуры, X означает целое число от 1 до 5 и каждый из R3 независимо означает алкильную функциональную группу. Как используется здесь, термин ʺалкилʺ охватывает линейный или разветвленный C1-C5-алкил или циклоалкильные группы.
Предпочтительные ионы аммония представляют собой 6-членные моноциклические кольца, содержащие две алкильных группы в N-положении. Примерами алкильных групп являются, в частности, метил, этил, пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 2-пентил, 2-метилбутил, 3-метилбутил, 1,2-диметилпропил, 1,1-диметилпропил и 2,2-диметилпропил. В особенности предпочтительные алкильные группы в N-положении иона аммония включают метил, этил и н-пропил. Две алкильные группы в N-положении могут быть одинаковыми, такими как диметил или диэтил, или могут быть различными, такими как этил и метил или н-пропил и этил.
Одно или более других замещений алкилами может быть выполнено в других местах циклической структуры. Например, алкильными функциональными группами могут быть замещены -2-, -3-, -4-, -5- и/или -6- положения. Число дополнительных замещений предпочтительно составляет один или два. Когда производятся два дополнительных замещения, они предпочтительно симметричны по отношению к N-атому на аммониевом кольце. Предпочтительно алкильные замещения выполняют в -2,6 - или -3,5- положениях. Две дополнительные алкильные группы могут быть одинаковыми, такими как диметил или диэтил, или могут быть различными, такими как этил-метил, н-пропил-этил. В особенности предпочтительны диметильные замещения и диэтильные замещения.
Конкретными примерами предпочтительных четвертичных аммониевых солей являются соли, содержащие ион, выбираемый из группы, состоящей из N,N-диметил-3,5-диметилпиперидиния; N,N-диэтил-2,6-диметилпиперидиния; N,N-диметил-9-азониабицикло[3.3.1]нонана; N,N-диметил-2,6-диметилпиперидиния; N-этил-N-метил-2,6-диметилпиперидиния; N,N-диэтил-2-этилпиперидиния; N,N-диметил-2-этилпиперидиния; N-этил-N-метил-2-этилпиперидиния; N-этил-N-пропил-2,6-диметилпиперидиния и 2,2,4,6,6-пентаметил-2-азониабицикло[3.2.1]октана, при этом в особенности предпочтителен N,N-диметил-3,5-диметилпиперидиний.
Предпочтительно промежуточные четвертичные аммониевые соли, полученные этим способом, также содержат алкилсульфатный противоион. В особенности предпочтительные алкилсульфатные противоионы включают метилсульфат и этилсульфат. Таким образом, настоящее изобретение охватывает такие новые соли, такие как метилсульфат 1,1,3,5-тетраметилпиперидин-1-ия. Соль предпочтительно находится в форме водного раствора.
Стадия (а) предпочтительно включает гидролиз четвертичной аммониевой/алкилсульфатной соли, с образованием четвертичной аммониевой соли, содержащей гидросульфатный противоион. Этот гидролиз может быть осуществлен, например, при контактировании четвертичной аммониевой/алкилсульфатной соли с серной кислотой или гидроксидом. Полезные гидроксиды включают гидроксиды щелочных металлов и гидроксиды аммония. Примеры гидроксидов щелочных металлов включают гидроксид лития, гидроксид натрия и гидроксид калия. В некоторых вариантах осуществления серную кислоту или источник гидроксида добавляют непосредственно к раствору четвертичной аммониевой/алкилсульфатной соли, получая реакционноспособную смесь. Как правило, реакция гидролиза продолжается приблизительно от 30 минут до нескольких часов при температуре около 25-125°C. Алкилспиртовый побочный продукт реакции гидролиза, такой как метанол, может быть удален из водного раствора азеотропной перегонкой с достижением общей конверсии алкилсульфата до гидросульфата выше 95%, и предпочтительно выше 99%. Преимущественно стадию (а) осуществляют, используя неорганический растворитель.
Стадия (b) включает контактирование раствора четвертичной аммониевой/алкилсульфатной соли с источником гидроксида, с образованием органической аммониевой соли, содержащей гидроксидный противоион. Предпочтительные источники гидроксида включают гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия и гидроксид калия. В некоторых вариантах осуществления стадия (b) приводит к SDA с незначительным содержанием или без содержания щелочного металла, несмотря на использование щелочного металла при синтезе. Предпочтительно щелочное содержание таких SDAs составляет менее 5 массовых процентов в пересчете на общую массу SDA, более предпочтительно менее 3 массовых процентов и еще предпочтительней менее 1 массового процента.
Стадия (b) может быть выполнена с использованием органического растворителя, такого как изопропиловый спирт, или неорганического растворителя. Предпочтительно щелочной гидроксид и органическую аммониевую соль/гидросульфатную соль объединяют в систему в условиях, эффективных для образования сульфата щелочного металла, который будет осаждаться из раствора. Твердый неорганический сульфат может быть удален из раствора любыми известными способами, например фильтрованием. Фильтрат содержит органическую аммониевую соль в гидроксидной форме. Таким образом, способы по настоящему изобретению могут быть использованы для получения SDA в гидроксидной форме без ионообменника, такого как ионообменная смола.
Конкретный вариант осуществления способа, включающего стадии а) и b), показан на фигуре 1.
Четвертичная аммониевая/алкилсульфатная соль стадии (a) может быть получена из азотсодержащего предшественника. Примеры полезных соединений-предшественников включают азотсодержащие, замещенные, пятичленные или шестичленные циклические соединения, такие как замещенный пиперидин или замещенный пиридин. В некоторых вариантах осуществления соединения-предшественники включают замещение (замещения) метилом, этилом и/или пропилом по одному или двум положения цикла, предпочтительно -2-, -2- и -6- или -3- и -5- положениям. Примеры таких молекул-предшественников включают 3,5-диметилпиперидин и 3,5-лутидин.
Алкилирование соединения-предшественника предпочтительно включает введение метильной, этильной или пропильной группы в -1-положение соединения. Алкилирующий агент предпочтительно представляет собой диалкилсульфат, такой как диметилсульфат, диэтилсульфат, метилэтилсульфат, дипропилсульфат, метилпропилсульфат, этилпропилсульфат и их смеси, при этом в особенности предпочтителен диметилсульфат. При необходимости алкилированное соединение-предшественник может быть дополнительно обработано, с получением соответствующего неароматического цикла. Примеры предпочтительных метилирований включают:
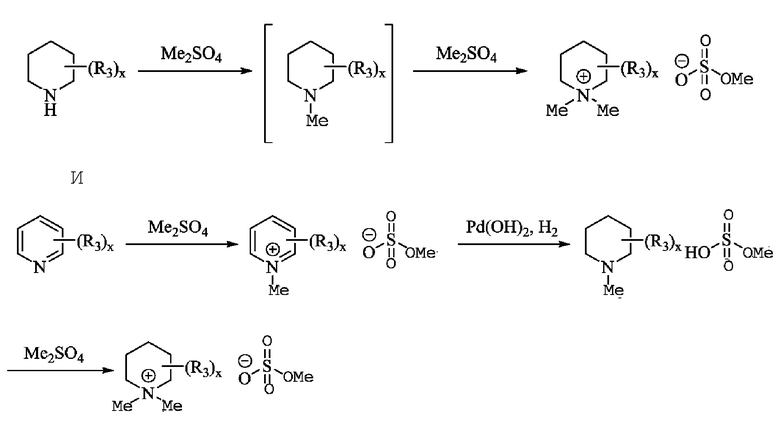
где x=целое число от 0 до 5, предпочтительно 1 или 2;
Алкилирование соединения-предшественника дает замещенный циклический амин, содержащий алкильную группу в -1-положении. Примеры замещенных циклических аминов, полезных по настоящему изобретению, включают алкил-замещенный N-метилпиперидин, алкил-замещенный N-этилпиперидин и алкил-замещенный N-пропилпиперидин. Алкильные замещения этих соединений включают метил, этил, пропил и/или бутил в -2-, -3-, -5- и/или -6-положениях. В дополнение к алкильному замещению в положении-1 эти соединения могут иметь одно, два или три дополнительных замещения. В некоторых вариантах осуществления метильные замещения выполняют по -2- и -6-положениям или по -3- и -5-положениям. В отдельных вариантах осуществления этильное замещение производят по -2-положению. Например, предпочтительные замещенные пиперидины имеют два или три алкильных замещения, такие как триметилпиперидин, триэтилпиперидин, диметилэтилпиперидин и метилэтилпиперидин, в особенности те, что имеют метильное или этильное замещение в положении-1. Другие замещения предпочтительно включают метилы, с замещением по -2 - и -6-положениям, метилы, с замещением по -3 - и -5-положениям, или этил, с замещением по 2-положению. В особенности предпочтительным замещенным пиперидином является 1,3,5-триметилпиперидин.
В некоторых вариантах осуществления, третичный циклический аминовый предшественник кватернизируют с помощью алкилсульфата, что дает четвертичную аммониевую соль. Полезные для кватернизации алкилсульфаты включают те, что раскрыты выше. В некоторых вариантах осуществления для кватернизации может использоваться тот же тип алкилсульфата, что и для алкилирования соединения-предшественника. Например, диметилсульфат может быть использован как для алкилирования соединения-предшественника, так и для кватернизации соответствующего третичного циклического амина. В других вариантах осуществления различные алкилсульфаты могут быть использованы для алкилирования соединения-предшественника и для кватернизации соответствующего третичного циклического амина.
Кватернизация предпочтительно включает алкильное или циклическое замещение в -1-положении. Предпочтительные замещения образует -1,1-диметильная, -1,1-метилэтильная или -1,1-диэтильная составляющая.
ПРИМЕРЫ
Пример 1 - Синтез метилсульфата 1,3,5-триметилпиперидиния из 3,5-лутидина
Обращаясь к фигуре 2, 3,5-лутидин (10,47 г) помещают в колбу и перемешивают при -10°C. Добавляют порциями диметилсульфат (12,89 г), поддерживая температуру смеси ниже 60°C. Затем смесь партии перемешивают при 40-50°C до завершения взаимодействия. Сразу после завершения смесь партии разбавляют водой, получая приблизительно 60 мас.% раствор метилсульфата 1,3,5-триметилпиридин-1-ия.
Этот раствор вносят в реакционный сосуд из нержавеющей стали и добавляют к смеси партии губчатый никелевый катализатор (Alfa Aesar). Затем подают водород (16 бар) (1,6 Мпа) при 25°C, и смесь партии перемешивают в течение 5 часов. После завершения катализатор фильтруют, получая метилсульфат 1,3,5-триметилпиперидиния (99%) в виде раствора в воде.
Пример 2 - Синтез гидроксида N,N-диметил-3,5-диметилпиперидиния
Вновь обращаясь к фигуре 2, в чистый и сухой реактор, снабженный рубашкой, загружают 3,5-диметилпиперидин (11 кг) и толуол (11 л). Смесь охлаждают до 0-10°C. Осторожно загружают диметилсульфат (12,2 кг), поддерживая температуру смеси партии <70°C. После завершения смесь партии охлаждают до 10-25°C и перемешивают не менее 1 ч.
Затем смесь партии дополнительно охлаждают до 5-10°C. К реакционной смеси добавляют диметилсульфат (13,5 кг), с последующим добавлением очищенной воды (11,0 кг). Добавляют раствор гидроксида натрия (10,8 кг воды; 4,6 кг гидроксида натрия) при 5-10°C, поддерживая температуру смеси партии ниже 10°C.
Сразу после завершения взаимодействия к смеси партии добавляют, за 1 час, раствор серной кислоты (4,7 кг) в очищенной воде (4,8 кг), поддерживая температуру смеси <50°C. Смесь партии нагревают до 95-100°C, и растворитель удаляют перегонкой до тех пор, пока не будет собрано приблизительно 2 объема растворителя относительно исходного материала.
После чего добавляют к смеси партии очищенную воду (2-3 л) и перегонку продолжают до удаления приблизительно 2-3 л растворителя. Эту прогонку воды повторяют дважды. Наконец смесь партии концентрируют перегонкой, пока не останется приблизительно 38-40 л. Смесь партии охлаждают приблизительно до 25°C, затем к смеси партии добавляют изопропанол (25,9 кг).
Смесь партии охлаждают до 10°C, затем к смеси партии добавляют раствор из гидроксида натрия (16,2 кг) и очищенной воды (16,2 кг), поддерживая при этом температуру <46°C. К полученной в результате суспензии загружают дополнительное количество изопропанола (5,5 кг). Смесь партии охлаждают до 0-5°C и фильтруют. Твердую фазу промывают изопропанолом (3×5,5 кг). Полученный фильтрат упаривают при ≤45°C, и оставшийся изопропанол отгоняют с водой, получая гидроксид N,N-диметил-3,5-диметилпиперидиния в виде ~50 мас.% раствора в воде (выход 97%).
Пример 3 - Синтез цеолита AEI (SAR=22)
Реакционный гель (молярного) состава: 60 частей SiO2, 1,2 частей Al2O3, 13,41 частей Na2O, 9,5 частей гидроксида N,N-диэтил-2,6-диметилпиперидиния (22,23 мас.% раствор) и 2721 частей H2O, получают следующим образом: около 130,6 грамм источника диоксида кремния (30 мас.% SiO2) загружают в автоклав из нержавеющей стали, на 1 литр, устанавливая скорость вращения мешалки на 300 об/мин. Около 341,4 г 1Н NaOH смешивают в стакане с 98,3 г матрицы. К этой смеси добавляют около 7,6 г аммониевого обменного цеолита Y. Смесь перемешивают при комнатной температуре 10-15 мин перед добавлением в автоклав коллоидного диоксида кремния. Автоклав герметически закрывают, и перемешивание продолжают, при комнатной температуре, в течение еще 10 минут, перед нагреванием до 135°С. Температуру поддерживают в течение 12 дней, после чего автоклав охлаждают до комнатной температуры, выгруженный продукт затем фильтруют, промывают деминерализованной водой и сушат при 110°C в течение ночи.
Полученный продукт проанализирован с помощью рентгеновской порошковой дифракции и найдено, что он представляет собой высококристаллический цеолит типа AEI.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИНТЕЗ ЦЕОЛИТА ТИПА AEI | 2014 |
|
RU2672744C2 |
| СИНТЕЗ ЦЕОЛИТА ТИПА AEI | 2014 |
|
RU2764725C2 |
| ПОЛУЧЕНИЕ АЛЮМОСИЛИКАТНОГО ЦЕОЛИТА AEI | 2016 |
|
RU2750048C2 |
| СИНТЕЗ ЦЕОЛИТОВ AEI и Cu-AEI | 2017 |
|
RU2743043C2 |
| СПОСОБ ПОЛУЧЕНИЯ ШАБЛОННОГО РЕАГЕНТА | 2014 |
|
RU2680406C2 |
| СПОСОБ ПОЛУЧЕНИЯ ШАБЛОННОГО РЕАГЕНТА | 2014 |
|
RU2775223C2 |
| БИМЕТАЛЛИЧЕСКИЕ МОЛЕКУЛЯРНОСИТОВЫЕ КАТАЛИЗАТОРЫ | 2016 |
|
RU2726118C2 |
| СИНТЕЗ ЦЕОЛИТА AEI | 2014 |
|
RU2744763C2 |
| Способ синтеза SSZ-39 с помощью модифицированной реакционной композиции | 2018 |
|
RU2735527C1 |
| СМОЛА С НИЗКИМ СОДЕРЖАНИЕМ НАТРИЯ | 2017 |
|
RU2752357C2 |
Предложен способ получения структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит, включающий стадии: a. гидролиза алкилсульфатного противоиона четвертичной аммониевой соли, с получением органической аммониевой соли, содержащей гидросульфатный противоион; и b. контактирования органической аммониевой соли, содержащей гидросульфатный противоион, с источником гидроксида в растворе, с образованием органической аммониевой соли, содержащей гидроксидный противоион; где четвертичная аммониевая соль включает аммониевый ион, выбираемый из N,N-диметил-3,5-диметилпиперидиния; N,N-диэтил-2,6-диметилпиперидиния; N,N-диметил-2,6-диметилпиперидиния; N-этил-N-метил-2,6-диметилпиперидиния; N,N-диэтил-2-этилпиперидиния; N,N-диметил-2-этилпиперидиния; N-этил-N-метил-2-этилпиперидиния; и N-этил-N-пропил-2,6-диметилпиперидиния, и где органическая аммониевая соль представляет собой структурообразущий агент (SDA) для синтеза кристаллических молекулярных сит. Технический результат: разработан новый улучшенный способ получения структурообразущих агентов (SDA), используемых для синтеза кристаллических молекулярных сит, (напр., цеолита), который улучшен за счет быстрого образования заданного SDA в гидроксидной форме, без необходимости в процессе обмена ионами металлов. 6 з.п. ф-лы, 3 пр., 2 ил.
1. Способ получения структурообразущего агента (SDA) для синтеза кристаллических молекулярных сит, включающий стадии:
a. гидролиза алкилсульфатного противоиона четвертичной аммониевой соли, с получением органической аммониевой соли, содержащей гидросульфатный противоион; и
b. контактирования органической аммониевой соли, содержащей гидросульфатный противоион, с источником гидроксида в растворе, с образованием органической аммониевой соли, содержащей гидроксидный противоион;
где четвертичная аммониевая соль включает аммониевый ион, выбираемый из N,N-диметил-3,5-диметилпиперидиния; N,N-диэтил-2,6-диметилпиперидиния; N,N-диметил-2,6-диметилпиперидиния; N-этил-N-метил-2,6-диметилпиперидиния; N,N-диэтил-2-этилпиперидиния; N,N-диметил-2-этилпиперидиния; N-этил-N-метил-2-этилпиперидиния; и N-этил-N-пропил-2,6-диметилпиперидиния, и где органическая аммониевая соль представляет собой структурообразущий агент (SDA) для синтеза кристаллических молекулярных сит.
2. Способ по п. 1, где стадия контактирования дополнительно включает осаждение сульфата из раствора.
3. Способ по п. 1, где стадия гидролиза включает контактирование алкилсульфатного противоиона органической аммониевой соли с серной кислотой или гидроксидом.
4. Способ по п. 1, где источник гидроксида представляет собой гидроксид щелочного металла или гидроксид аммония.
5. Способ по п. 1, где органическая аммониевая соль включает аммониевый ион, выбираемый из N,N-диметил-3,5-диметилпиперидиния или N,N-диэтил-2,6-диэтилпиперидиния.
6. Способ по п. 1, дополнительно включающий кватернизацию третичного амина с использованием диалкилсульфата, с получением органической аммониевой соли, содержащей алкилсульфатный противоион.
7. Способ по п. 6, где третичный амин представляет собой циклический третичный амин, предпочтительно выбираемый из группы, состоящей из 1,3,5-триметилпиперидина; 1-этил-2,6-диметилпиперидина; 1,2,6-триметилпиперидина; 1-метил-2-этилпиперидина; 1,2-диэтилпиперидина; 1-пропил-2,6-диметилпиперидина и предпочтительно, 1,3,5-триметилпиперидин.
| US2007254822A1, 01.11.2007 | |||
| Слиток | 1985 |
|
SU1297955A1 |
| US2007142642A1, 21.06.2007 | |||
| EA201291453A1, 30.05.2013 | |||
| US2008033209A1, 07.02.2008 | |||
| US2015065718 A1, 05.03.2015. | |||
Авторы
Даты
2022-01-18—Публикация
2016-04-20—Подача