Изобретение относится к области биотехнологии, в частности к антителам против С-концевого фрагмента антимюллерова гормона, конкретно к моноклональным мышиным антителам против С-концевого фрагмента антимюллерова гормона человека. Изобретение может быть использовано в медицине, иммунологии, биотехнологии.
Антимюллеров гормон (АМГ) является одним из наименее изученных членов суперсемейства цитокинов трансформирующего фактора роста бета. В эмбриогенезе млекопитающих этот фактор направляет развитие репродуктивной системы по мужскому типу, а в постнатальном периоде жизни — участвует в регуляции баланса половых гормонов [Гукасова Н.В., Северин С.Е. Белок MIS: структура, регуляция экспрессии и молекулярный механизм действия // Вопросы биологической, медицинской и фармацевтической химии, 2005, 4:3—9]. Большую клиническую значимость имеет определение сывороточного уровня АМГ, позволяющее судить о величине овариального резерва, характере течения беременности у женщин [La Marca A., Sighinolfi G., Radi D., Argento C., Baraldi E., Artenisio A.C., Stabile G., Volpe A. Anti-Müllerian hormone (AMH) as a predictive marker in assisted reproductive technology (ART) // Human reproduction update, 2009, 16(2):113—130; van Rooij I.A., Broekmans F.J., te Velde E.R., Fauser B.C., Bancsi L.F., de Jong F.H., Themmen A.P. Serum anti-Müllerian hormone levels: a novel measure of ovarian reserve // Human Reproduction, 2002, 17(12):3065—3071] и наличии нормально функционирующей тестикулярной ткани в организме у мужчин [MacLaughlin D.T., Donahoe P.K. Müllerian inhibiting substance/anti-Müllerian hormone: a potential therapeutic agent for human ovarian and other cancers // Future Oncology, 2010, 6(3):391—405]. Кроме того, показано, что рекомбинантный АМГ (рАМГ) обладает противоопухолевой активностью в отношении клеток, имеющих на своей поверхности специфические рецепторы АМГ II типа (MISRII), индуцируя в них апоптоз [Teixeira J., Maheswaran S., Donahoe P.K. Mullerian inhibiting substance: an instructive developmental hormone with diagnostic and possible therapeutic applications // Endocrine Reviews, 2001, 22(5):657—674].
Ген АМГ человека локализован на малом плече 19-й хромосомы и состоит из 2,75 тысяч пар нуклеотидов [Cate R.L., Mattaliano R.J., Hession C., Tizard R., Farber N.M., Cheung A., Ninfa E.G., Frey A.Z., Gash D.J., Chow E.P., Fisher R.A., Bertonis J.M., Torres G., Wallner B.P., Ramachandran K.L., Ragin R.C., Manganaro T.F., Maclaughlin D.T., Donahoe P.K. Isolation of the bovine and human genes for Müllerian inhibiting substance and expression of the human gene in animal cells // Cell, 1986, 45(5):685—698]. Он содержит 5 экзонов и 4 интрона и кодирует полипептид предшественника АМГ (так называемый про-АМГ), состоящий из 560 аминокислотных остатков, в который, помимо АМГ (25–560), входят также лидерная и сигнальная последовательности (1–24) [Rey R., Lukas-Croisier C., Lasala C., Bedecarrás P. AMH/MIS: what we know already about the gene, the protein and its regulation // Mol. Cell. Endocrinol, 2003, 211(1):21—31]. В настоящем описании при упоминании позиций аминокислот мы ссылаемся на последовательность аминокислот полноразмерного предшественника АМГ, которая представлена в базе данных UniProt [http://www.uniprot.org/uniprot/P03971]
Молекула гликопротеина АМГ имеет массу около 140 кДа и является гомодимером. Показано, что АМГ in vivo подвергается расщеплению на два главных фрагмента, которые представляют собой N- и С-концевые гомодимеры с молекулярной массой 115 и 25 кДа соответственно [Cimino I., Casoni F., Liu X., Messina A., Parkash J., Jamin S.P., Catteau-Jonard S., Collier F., Baroncini M., Dewailly D., Pigny P., Prescott M., Campbell R., Herbison A.E., Prevot V., Giacobini P. Novel role for anti-Müllerian hormone in the regulation of GnRH neuron excitability and hormone secretion // Nature communications, 2016, 7:10055]. Сайт специфического протеолиза в каждой полипептидной цепи полноразмерного гомодимера локализован между аминокислотными остатками Arg451 и Ser452 [Pepinsky R.B., Sinclair L.K., Chow E.P., Mattaliano R.J., Manganaro T.F., Donahoe P.K., Cate R.L. Proteolytic processing of mullerian inhibiting substance produces a transforming growth factor-beta-like fragment // Journal of Biological Chemistry, 1988, 263(35):18961—18964]. После такого расщепления молекула АМГ переходит в активное состояние. При этом С-концевой фрагмент АМГ (С-АМГ), действуя как индивидуальная молекула или в нековалентном комплексе с N-концевым фрагментом, связывается с рецептором АМГ II типа — MISRII — и передает активирующий сигнал внутрь клетки [di Clemente N., Jamin S.P., Lugovskoy A., Carmillo P., Ehrenfels C., Picard J. Y., Whitty A., Josso N., Pepinsky R.B., Cate R.L. Processing of anti-mullerian hormone regulates receptor activation by a mechanism distinct from TGF-β // Molecular Еndocrinology, 2010, 24(11):2193—2206].
Учитывая возможные молекулярные трансформации молекулы АМГ in vivo и in vitro, а также диагностическую важность определения сывороточного уровня АМГ для оценки репродуктивного потенциала человека, представляется важным разрабатывать новые инструменты для детекции производных АМГ, циркулирующих в крови пациентов. Кроме того, ввиду возможности использования рАМГ в качестве противоопухолевого лекарственного агента, также является весьма актуальной разработка иммунохимических средств оценки качества получаемых препаратов рАМГ.
Дифференциальная детекция производных АМГ и рАМГ in vivo и in vitro может быть достигнута путем получения панели моноклональных антител, распознающих различные фрагменты молекулы АМГ и разработки на их основе новых тест-систем. Кроме того, разнообразные моноклональные антитела могут быть использованы для синтеза иммуносорбентов, пригодных для выделения индивидуальных компонентов из сложной смеси молекулярных производных АМГ, а также для изучения их свойств.
Из заявки WO2008153433 известны моноклональные антитела М1, распознающие С-концевой домен АМГ как в форме 25 кДа димера, так и 12,5 мономера.
Из патента US 7897350 известна композиция для определения АМГ в образцах тканей млекопитающих, в частности описано моноклональное антитело F2B12H, распознающее устойчивый к протеолизу С-концевой фрагмент АМГ человека и крысы в невосстанавливающих условиях.
В статье: Mamsen L.S., Petersen T.S., Jeppesen J.V., Møllgård K., Grøndahl M.L., Larsen A., Ernst E., Oxvig C., Kumar A., Kalra B., Andersen C.Y. Proteolytic processing of anti-Müllerian hormone differs between human fetal testes and adult ovaries // MHR: Basic science of reproductive medicine, 2015, 21(7):571—582 описаны моноклональные антитела AMH-1 и AMH-29 к С-концевому фрагменту АМГ, распознающие последовательность Val491—Arg502 АМГ.
Компания R&D Systems, Inc. выпускает мышиные моноклональные антитела, полученные при иммунизации С-концевым фрагментом рекомбинантного человеческого АМГ Ala453—Arg560 (Cat# MAB1737).
Компания MyBioSource, Inc. выпускает мышиные моноклональные антитела, полученные при иммунизации С-концевым фрагментом рекомбинантного человеческого АМГ Ala453—Arg560 (Cat# MBS2001312, Cat# MBS2085832).
Компания GeneTex, Inc. выпускает мышиные моноклональные антитела 5/6 (Cat# GTX42793, Cat# GTX42794), полученные при иммунизации синтетическим пептидом, соответствующим последовательности Val527—Cys557 человеческого АМГ.
Компания Abcam выпускает мышиные моноклональные антитела MM0475-7H26 (Cat# ab90241) к С-концевому фрагменту человеческого АМГ.
Технической задачей, решаемой авторами, являлось расширение круга антител, способных распознавать различные эпитопные области С-концевого фрагмента человеческого АМГ.
Технический результат достигался созданием моноклональных антител ACMIS-1, ACMIS-3,ACMIS-4 и ACMIS-6, которые специфично и с высокой аффинностью связываются с различными эпитопными областями С-концевого фрагмента человеческого АМГ. Причём антитела ACMIS-1 и ACMIS-4 связываются с последовательностью SAGATA (Ser452—Ala457 человеческого АМГ), антитело ACMIS-6 связывается с конформационной детерминантой человеческого АМГ, а антитело ACMIS-3 распознает линейный участок как в 70кД цепи АМГ, так и в 25кД и 12,5кД С-концевого фрагмента АМГ и подавляет его связывание с рецептором MISRII.
Моноклональное антитело ACMIS-1 содержит вариабельную область тяжелой цепи по Seq ID No:3 и вариабельную область легкой цепи по Seq ID No:4, а также гипервариабельные участки вариабельной области тяжелой цепи по Seq ID No:5—7 и гипервариабельные участки вариабельной области легкой цепи по Seq ID No:8—10.
Моноклональное антитело ACMIS-3 содержит вариабельную область тяжелой цепи по Seq ID No:13 и вариабельную область легкой цепи по Seq ID No:14, а также гипервариабельные участки вариабельной области тяжелой цепи по Seq ID No:15—17 и гипервариабельные участки вариабельной области легкой цепи по Seq ID No:18—20.
Моноклональное антитело ACMIS-4 содержит вариабельную область тяжелой цепи по Seq ID No:23 и вариабельную область легкой цепи по Seq ID No:24, а также гипервариабельные участки вариабельной области тяжелой цепи по Seq ID No:25—27 и гипервариабельные участки вариабельной области легкой цепи по Seq ID No:28—30.
Моноклональное антитело ACMIS-6 содержит вариабельную область тяжелой цепи по Seq ID No:33 и вариабельную область легкой цепи по Seq ID No:34, а также гипервариабельные участки вариабельной области тяжелой цепи по Seq ID No:35—37 и гипервариабельные участки вариабельной области легкой цепи по Seq ID No:38—40.
Полученные моноклональные антитела ACMIS-1 и ACMIS-4 специфично и с высокой эффективностью связываются с N-концевым пептидом С-рАМГ SAGATA (Ser452—Ala457), но не связываются с С-рАМГ в составе 70 кДа-мономера и не ингибируют связывание С-рАМГ с MISRII. Антитело ACMIS-6 специфично и с высокой эффективностью связывается с конформационным эпитопом С-рАМГ и не связывается с денатурированным белком, и также не ингибируют связывание С-рАМГ с MISRII. Антитело ACMIS-3 связывается с димерной и мономерной формой С-рАМГ, а также и с С-концевым участком рАМГ в составе 70 кДа-мономера, кроме того это антитело способно подавлять связывание С-рАМГ с рекомбинантным MISRII.
Технология получения антител включала в себя иммунизацию животных антигеном, представляющим собой очищенный С-рАМГ, который был получен по методике, описанной в статье [Рак А.Я., Трофимов А.В., Протасов Е.А., Симбирцев А.С., Ищенко А.М. Сравнительное исследование свойств активированного рекомбинантного антимюллерова гормона человека // Российский иммунологический журнал, 2017, 11(4):755—757; патент на изобретение RU 2616273]. В качестве антигенов для отбора позитивных продуцентов моноклональных антител при постановке иммуноферментного анализа (ИФА) использовали тот же препарат С-рАМГ, что и для иммунизации.
Изобретение иллюстрируется следующими графическими материалами:
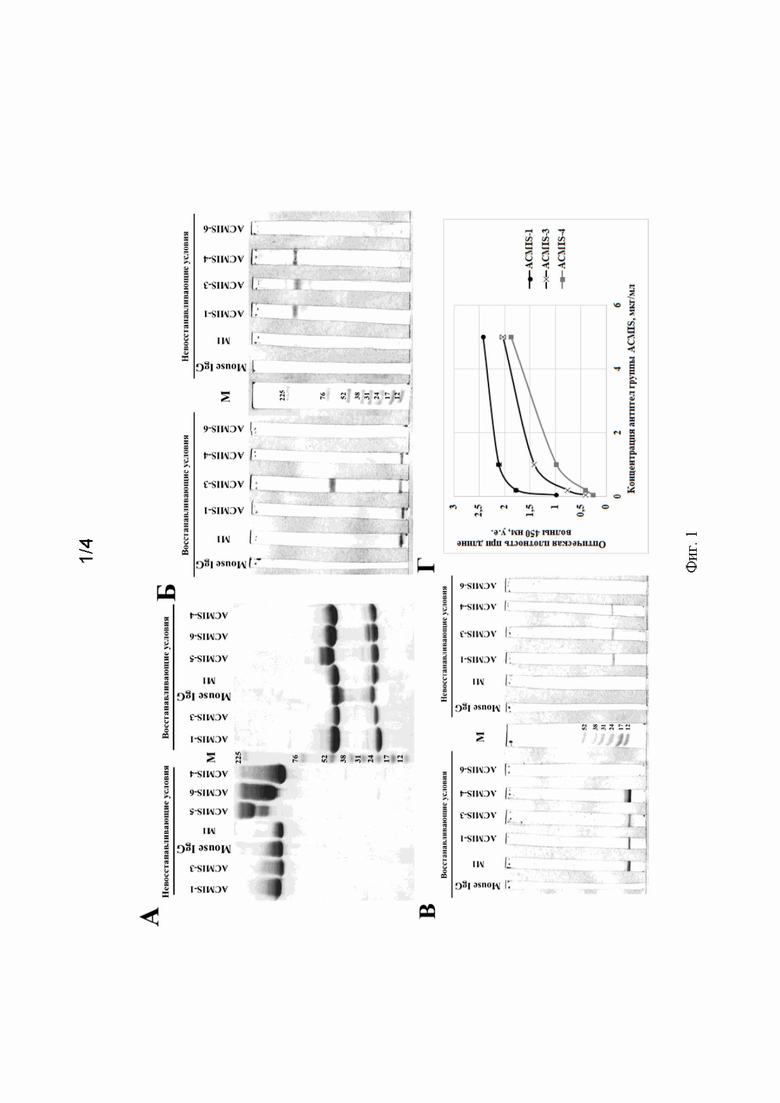
На Фиг. 1. А представлена электрофореграмма образцов препаратов полученных антител. Проба нормальных иммуноглобулинов мыши класса IgG использована в качестве позитивного контроля. М — маркеры молекулярных весов (кДа).
На Фиг. 1. Б, В представлены фотографии мембран, полученных в результате вестерн-блот анализа пробы смеси цельного и фрагментированного по одной цепи рАМГ (Б) и С-рАМГ (В). Для негативного контроля использованы нормальные иммуноглобулины мыши класса IgG. М — маркеры молекулярных весов (кДа).
На Фиг. 1. Г представлена кривая связывания антител группы ACMIS с сорбированным С-рАМГ.
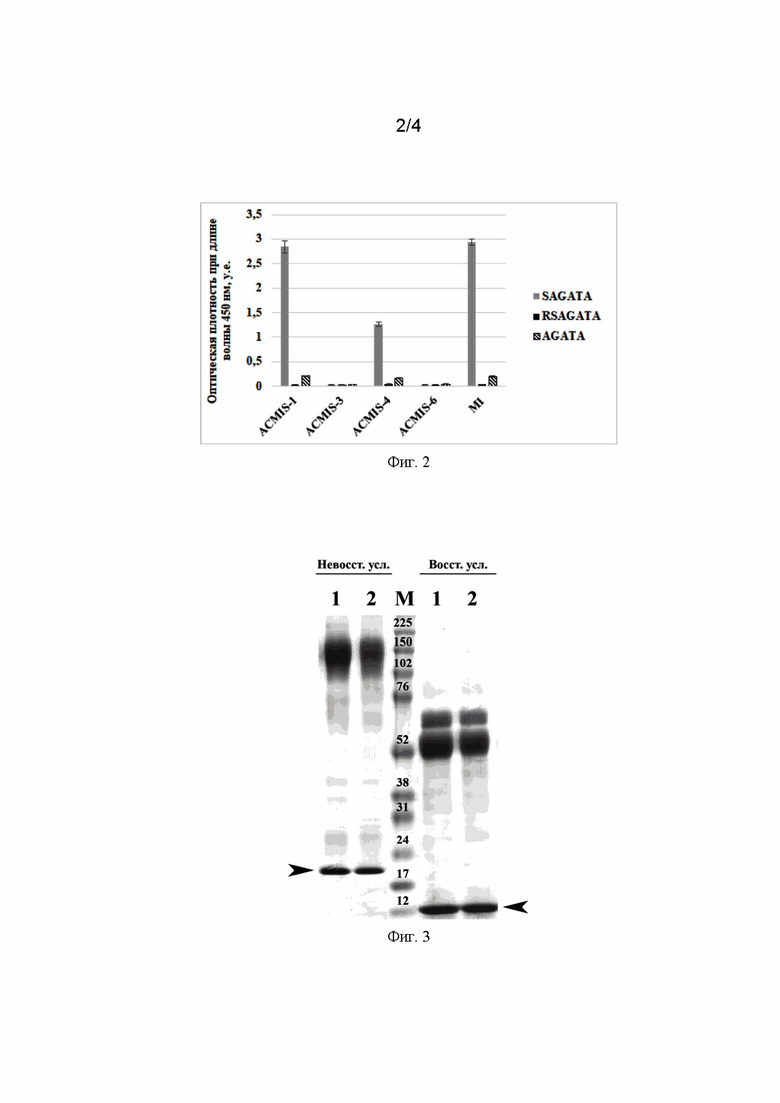
На Фиг. 2. представлен анализ специфичности полученных антител к пептидам SAGATA, RSAGATA и AGATA в прямом твердофазном ИФА.
На Фиг. 3. представлена электрофореграмма образцов двух элюатов, полученных при выделении рАМГ из культуральной жидкости с использованием иммуносорбента ACMIS-1. Стрелками указаны полосы, соответствующие гомодимерной (слева) и мономерной (справа) формам С-рАМГ. М — маркеры молекулярных весов (кДа).
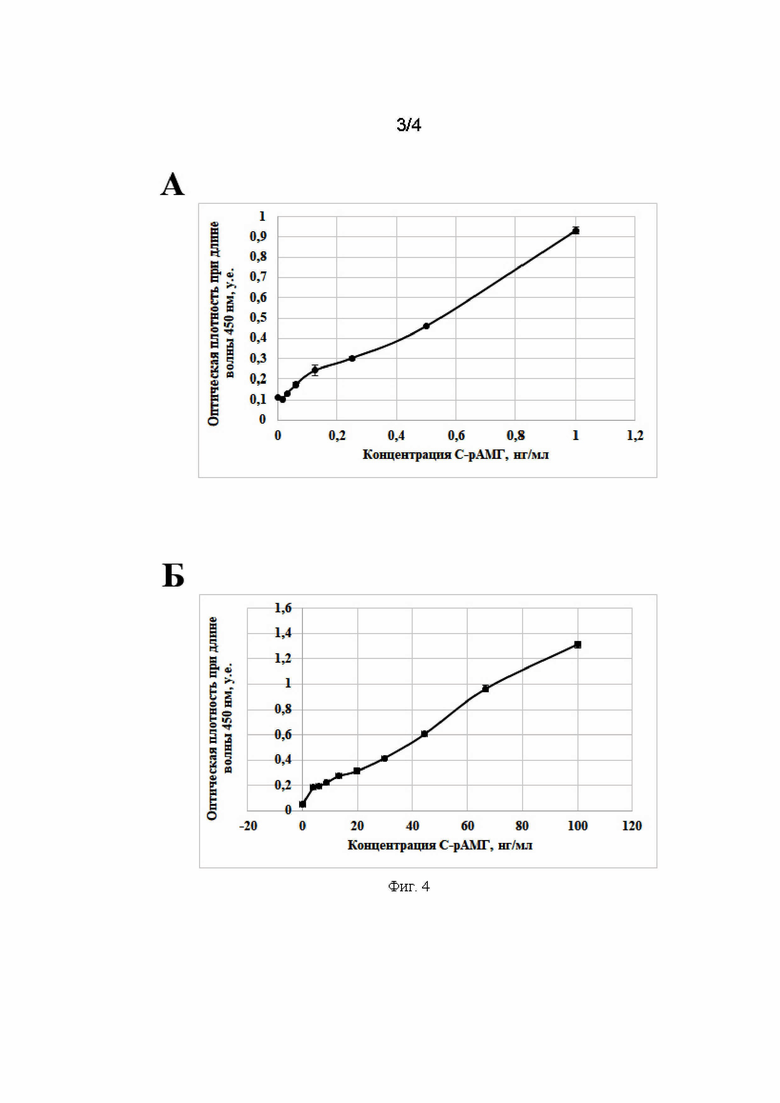
На Фиг. 4. А представлена калибровочная кривая определения концентрации препарата С-рАМГ в сэндвич-ИФА на основе антител ACMIS-3 и пероксидазного конъюгата ACMIS-4-Пх.
На Фиг. 4. Б представлена калибровочная кривая определения концентрации препарата С-рАМГ в сэндвич-ИФА на основе химерного белка MISRII+Fc и пероксидазного конъюгата ACMIS-4-Пх.
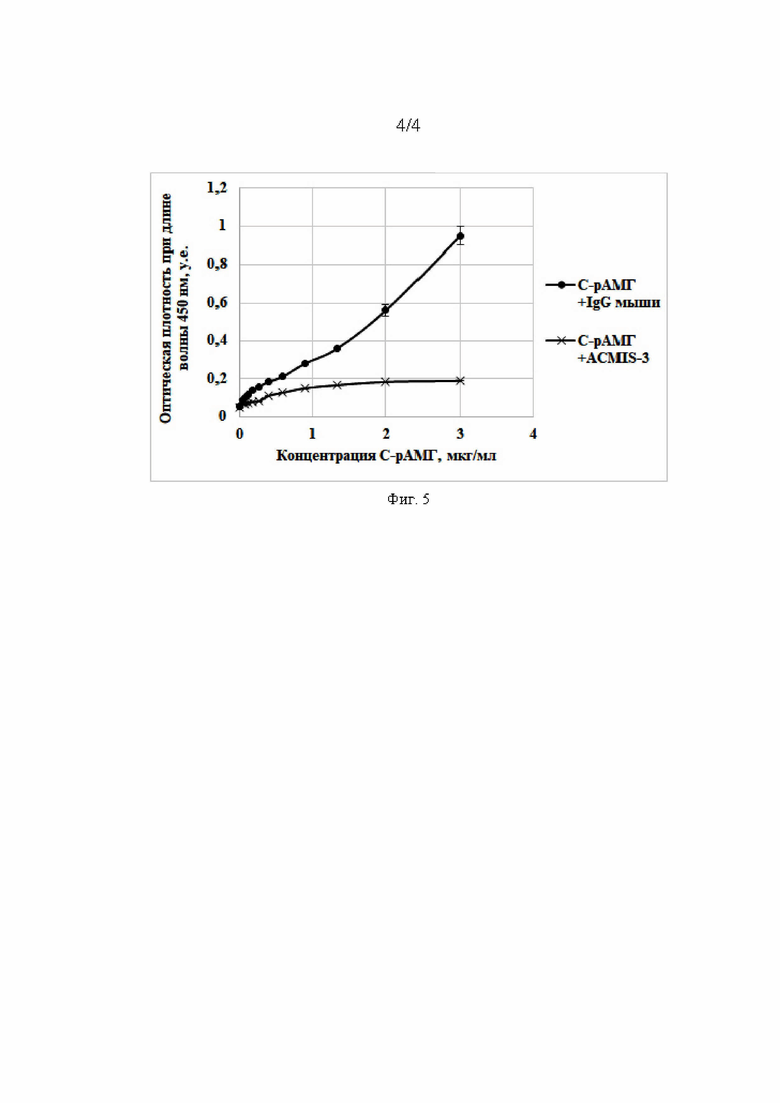
На Фиг. 5.представлена кривая связывания С-рАМГ с химерным белком MISRII+Fc в присутствии антител ACMIS-3.
Сущность и промышленная применимость изобретения поясняются следующими примерами.
Пример 1. Получение антигенов для иммунизации и скрининга гибридом, иммунизация мышей и отбор гибридом.
1.1. Получение антигенов. Для иммунизации использовали высокоочищенный препарат С-концевого фрагмента рекомбинантного человеческого АМГ (С-рАМГ), полученный по ранее разработанной методике [Рак А.Я., Трофимов А.В., Протасов Е.А., Симбирцев А.С., Ищенко А.М. Сравнительное исследование свойств активированного рекомбинантного антимюллерова гормона человека // Российский иммунологический журнал, 2017, 11(4):755—757; патент на изобретение RU 2616273]. Коротко, клетки линии СНО (ATCC, США), трансфицированные геном АМГ человека (штамм CHO-MIS#26), выращивали на бессывороточной среде CDM4CHO (HyClone, США). Для выделения С-рАМГ из культуральной жидкости вначале применяли метод иммуноаффинной хроматографии на сорбенте, приготовленном на основе цианбром-активированной сефарозы FF (GE, Швеция) и моноклональных антител 6E11 [Hudson P.L., Dougas I., Donahoe P.K., Cate R.L., Epstein J., Pepinsky R.B., MacLaughlin D.T. An immunoassay to detect human mullerian inhibiting substance in males and females during normal development. The Journal of clinical endocrinology and metabolism, 1990, 70(1):16—22] против АМГ. После нанесения культуральной жидкости на колонку, уравновешенную фосфатно-солевым буферным раствором (20 мМ, рН 7,4), ее промывали пятью объемами фосфатно-солевого буфера, содержащего 1 М NaCl, для удаления неспецифически связавшихся молекул, а затем проводили элюцию раствором 0,1 М глицина рН 2,5 при скорости потока 1 мл/мин. Далее выделение С-рАМГ из полученного элюата осуществляли методом применяли метод обращенно-фазовой хроматографии, используя хроматограф Agilent 1260, оснащенный колонкой C18 Jupiter Phenomenex размером 4,6x250 мм с диаметром пор 300Å (GE Healthcare, Швеция). Элюцию осуществляли в градиентной системе: трифторуксусная кислота-ацетонитрил 20—70% в течение 15 мин, при скорости потока 1,5 мл/мин. Детекцию пиков в ходе хроматографии проводили при длине волны 280 нм.
Препарат, содержащий цельный рАМГ и фрагментированный по одной цепи гормон, очищали методом иммуноаффинной хроматографии на сорбенте, приготовленном на основе цианбром-активированной сефарозы FF (GE, Швеция) и моноклональных антител 6E11 против АМГ. После нанесения культуральной жидкости на колонку, уравновешенную фосфатно-солевым буферным раствором (20 мМ, рН 7,4), ее промывали пятью объемами фосфатно-солевого буфера, содержащего 1 М NaCl, для удаления неспецифически связавшихся молекул, а затем проводили элюцию раствором 0,1 М глицина рН 2,5 при скорости потока 1 мл/мин. В ходе хроматографии пики детектировали при длине волны 280 нм. [Lorenzo H. K., Teixeira J., Pahlavan N., Laurich V. M., Donahoe P. K., MacLaughlin D. T. New approaches for high-yield purification of Müllerian inhibiting substance improve its bioactivity // Journal of Chromatography B, 2002, 766(1):89—98; патент на изобретение RU 2616273].
1.2. Иммунизация мышей и скрининг гибридомы. Для получения моноклональных антител использовали самцов мышей линии Balb/c. Иммунизацию животных проводили очищенным С-рАМГ, полученным по п.1.1., с интервалом в 30 дней в подошвенный апоневроз задних конечностей из расчета 50 мкг эмульгированного С-рАМГ на мышь. Гибридомы получали по методу Мильштейна-Келера, для чего лимфоциты животных, взятые на 4-е сутки после повторной иммунизации, смешивали с клетками миеломы мыши линии Sp2/0 (из расчета 50000 клеток на лунку 96-ячеечного планшета) в соотношении 2:1 в присутствии полиэтиленгликоля с молекулярной массой 1500 Да. Культивирование клеток после слияния проводили в селективной среде НАТ (Sigma, США) в планшетах с суточными перитонеальными макрофагами мыши. Первичный скрининг клонов проводили спустя 10 дней, используя прямой твердофазный ИФА. Для этого антиген (С-рАМГ) иммобилизовали в лунках планшета сорбцией из раствора с концентрацией 1,5 мкг/мл в 20 мМ боратном буфере рН 8,0 в течение 20 часов при комнатной температуре, затем добавляли культуральную жидкость, содержащую исследуемые антитела, а через 1 час вносили раствор (1:4000) вторых антител — пероксидазного конъюгата антител козы против Fc-фрагмента мышиных иммуноглобулинов класса IgG (Sigma, США).
Клетки клонов, отобранных по итогам первичного скрининга и получивших наименования ACMIS-1, ACMIS-3, ACMIS-4, и ACMIS-6, повторно клонировали для проверки стабильности секреции антител. Для этого производили отбор и рассев клеток клонов из расчета 2 клетки на лунку 96-ячеечного планшета с суточными перитонеальными макрофагами мыши. Спустя 10 дней культивирования проводили повторный скрининг клонов для подтверждения специфичности секретируемых ими антител. Затем клетки пересевали в культуральные флаконы площадью 125 см2 с перитонеальными мышиными макрофагами для наращивания с целью криоконсервации и/или введения животным. Далее для наработки антител клетки каждого клона гибридом внутрибрюшинно вводили мышам из расчета по 2 млн. клеток на мышь.
Пример 2. Исследование свойств моноклональных антител ACMIS-1, ACMIS-3, ACMIS-4 и ACMIS-6.
2.1. Очистка моноклональных антител. Выделение антител производили из асцитных жидкостей мышей, собранных спустя 10 суток после введения клеток гибридомы, с помощью метода аффинной хроматографии на белке А с использованием сорбента MabSelect (GE, США) по стандартному протоколу согласно инструкции. В качестве контрольных антител в анализах были использованы нормальные иммуноглобулины класса IgG мыши (Sigma, США).
2.2. Изучение молекулярных свойств антител. Денатурирующий электрофорез белков в полиакриламидном геле осуществляли по ранее описанной методике [Walker J.M. Gradient SDS polyacrylamide gel electrophoresis of proteins. In: Basic protein and peptide protocols. Springer: New York, 1994:35—38]. В работе использовался разделяющий гель с градиентной концентрацией акриламида 4—20% и концентрирующий гель с концентрацией акриламида 5%. Результаты электрофореза визуализировали с помощью стандартного окрашивания раствором Кумасси G-250. Изотипирование моноклональных антител проводили с использованием набора Rapid ELISA Mouse Isotyping Kit (ThermoScientific, США) по протоколу, предложенному производителем. Результаты изотипирования (таблица 1) и электрофоретический анализ очищенных антител (Фиг. 1. А) показали, что все полученные антитела являются иммуноглобулинами класса IgG, однако относятся к различным подклассам.
Таблица 1. Изотипы полученных антител.
2.3. Изучение специфичности моноклональных антител. Специфичность полученных антител анализировали с помощью вестерн-блота по стандартному протоколу [Mahmood T., Yang P.C. Westernblot: technique, theory, and troubleshooting // North American journal of medical sciences, 2012, 4(9):429]. В качестве антигена использовали как полноразмерный, так и фрагментированный по одной цепи рАМГ (Фиг. 1. Б), и препарат С-рАМГ (Фиг. 1. В). Для переноса белков использовали буферный раствор, содержащий 47,9 мМ Трис-HCl, 38,6 мМ глицина и 20% метанола, и нитроцеллюлозную мембрану с диаметром пор 0,45 мкм. Перенос проводили в течение 1 часа при силе тока 350 мА, после чего мембрану инкубировали в блокирующем растворе (2% BSA в 20 мМ фосфатном буферном растворе, рН 7,4) в течение ночи при +4°С. Затем вносили раствор первичных антител (5 мкг/мл) в блокирующем растворе, для негативного контроля использовали нормальные иммуноглобулины мыши. После часовой инкубации и двукратной отмывки мембрану также в течение часа обрабатывали раствором пероксидазного конъюгата антител козы против иммуноглобулинов класса IgG мыши (Sigma, США) с концентрацией 0,5 мкг/мл. Для проявления окрашивания использовали 0,05% раствор диаминобензидина (ДАБ) (Sigma, США) в фосфатном буфере, содержащем 1% диметилсульфоксида (Sigma, США) и 1% перекиси водорода (НеваРеактив, Россия).
Способность полученных антител к связыванию с С-рАМГ, сорбированным на микротитровальном планшете, была показана в прямом твердофазном ИФА (Фиг. 1. Г). При проведении ИФА захватывающие антитела или антиген сорбировали в лунках планшета в концентрации 1,5 мкг/мл в 20 мМ боратном буфере (рН 8,0) в течение ночи при комнатной температуре. На следующем этапе анализа после трехкратной отмывки в лунки вносили антиген или специфичные к нему антитела, инкубацию с которыми проводили в течение часа при +37°С. Затем в промытые лунки вносили раствор пероксидазного конъюгата антител, специфичных к предыдущему компоненту ИФА, в концентрации 0,5 мкг/мл, и также проводили инкубацию в течение часа при +37°С. Регистрацию иммуноферментной реакции производили при длине волны 450 нм стандартным методом с использованием тетраметилбензидина и фотометра для микропланшетов BioRad Reader Model 680 (BioRad, США).
2.4. Изучение эпитопной специфичности моноклональных антител. Для определения эпитопной специфичности полученных антител использовали полученные методом твердофазного синтеза по ранее предложенному протоколу [Coin I., Beyermann M., Bienert M. Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences // Nature protocols, 2007, 2(12):3247] биотинилированные пептиды с аминокислотными последовательностями SAGATA-(СН2)10-биотин, RSAGATA-(СН2)10-биотин и AGATA-(СН2)10-биотин. Для этого были синтезированы, а затем биотинилированы пептиды, содержащие участки аминокислотной последовательности N-концевой части С-рАМГ. Пептид SAGATA (Ser452—Ala457) точно повторяет N-концевой участок С-рАМГ, а пептиды RSAGATA (Arg451—Ala457) и AGATA (Ala453—Ala457) отличаются тем, что первый из них имеет один дополнительный аминокислотный остаток Arg (R) перед концевым остатком Ser (S), а у второго пептида этот остаток Ser (S) отсутствует. Было показано, что антитела ACMIS-1 и ACMIS-4 строго специфичны по отношению к пептиду SAGATA. Об этом свидетельствуют результаты прямого твердофазного ИФА (Фиг. 2), в котором на микротитровальном планшете в концентрации 1,5 мкг/мл был сорбирован стрептавидин, далее внесены растворы биотинилированных пептидов: SAGATA, AGATA или RSAGATA (100 нг/мл), затем — растворы исследуемых антител (10 мг/мл) и, наконец, антивидовой пероксидазный конъюгат. При этом, как видно из Фиг. 2, специфичность антител ACMIS-1 и ACMIS-4 по отношению к двум другим пептидам отсутствует. Эти данные указывают на то, что антитела ACMIS-1 и ACMIS-4 распознают эпитоп, оказывающийся доступным при специфическом протеолизе молекулы рАМГ, и могут быть использованы для выделения и детекции С-рАМГ и фрагментированного по одной цепи рАМГ. Антитела ACMIS-3 и ACMIS-6 не специфичны по отношению к пептидам SAGATA, AGATA и RSAGATA и, по-видимому, распознают другие эпитопные области в составе С-рАМГ. Это делает возможным их использование в сэндвич-ИФА для детекции С-рАМГ или фрагментированного по одной цепи гормона в качестве парных антител к ACMIS-1 и ACMIS-4.
2.5. Изучение спектра производных рАМГ, связывающихся с моноклональными антителами. Для того чтобы изучить спектр производных рАМГ, способных к связыванию с полученными антителами, на их основе были приготовлены иммуносорбенты, которые далее были использованы для выделения рАМГ из культуральной жидкости клеток-продуцентов на этапе предварительной очистки гормона. Выделение препаратов рАМГ из культуральной жидкости клеток-продуцентов осуществляли методом иммуноаффинной хроматографии. Иммуносорбенты получали путем иммобилизации полученных моноклональных антител на цианбром-активированной сефарозе FF (GE, Швеция). Колонку, уравновешенную фосфатным буфером (ФБ), после нанесения культуральной жидкости, свободной от клеток-продуцентов, промывали пятью объемами уравновешивающего буфера. Далее для удаления неспецифически связавшихся белков пропускали один объем ФБ, содержащего 1 М NaCl, после чего вновь уравновешивали колонку ФБ и проводили элюцию раствором 0,1 М глицина, рН 2,5, при скорости потока 1 мл/мин. В ходе хроматографии пики детектировали при длине волны 280 нм. На Фиг. 3 представлена электрофореграмма двух препаратов рАМГ, полученных методом аффинной хроматографии с использованием иммуносорбента ACMIS-1. Видно, что в пробах, помимо С-рАМГ, также присутствует гормон, фрагментированный по одной цепи, который может быть выделен из данных препаратов в ходе последующей очистки методом иммуноаффинной хроматографии на сорбентах, приготовленных на основе антител к N-концевому фрагменту рАМГ.
3. Использование полученных антител для определения количества АМГ в биологических жидкостях. Были разработаны две тест-системы с использованием полученных антител, одна из которых предназначена для определения концентрации С-рАМГ, а другая — для тестирования его способности к взаимодействию с MISRII.
3.1. Тест-система на основе ИФА с использованием моноклональных антител, специфичных к различным эпитопам АМГ. В тест-системе анализ включает сорбцию антител ACMIS-3 в концентрации 1,5 мкг/мл в 20 мМ боратном буфере (рН 8,0), затем внесение образцов, содержащих С-рАМГ, а затем — пероксидазного конъюгата антител ACMIS-4-Пх (0,5 мкг/мл). На Фиг. 4, А представлена калибровочная кривая, полученная с использованием разработанной тест-системы. Чувствительность этой тест-системы составила 30 пг/мл.
3.1. Тест-система на основе ИФА с использованием MISRII+Fc. Ключевым компонентом тест-системы, позволяющей тестировать способность С-рАМГ к взаимодействию с рекомбинантным рецептором MISRII, стал ранее полученный в лаборатории химерный рекомбинантный белок MISRII+Fc. Он состоит из внеклеточной части специфического рецептора АМГ — MISRII — и Fc-фрагмента иммуноглобулина IgG1 человека [Рак А.Я., Трофимов А.В., Пигарева Н.В., Симбирцев А.С., Ищенко А.М. Моноклональные антитела против рецептора антимюллерова гормона человека как новый инструмент для диагностики и терапии рака // Цитокины и воспаление, 2017, 16(3):58—61]. Анализ с применением данной тест-системы на первом этапе включает сорбцию антител И-4, специфичных к Fc фрагменту IgG человека, в концентрации 1,5 мкг/мл в 20 мМ боратном буфере (рН 8,0). И-4 являются захватывающими антителами для рецепторной химерной конструкции и обеспечивают ориентацию ее MISRII-содержащей части в направлении лиганда. На следующем этапе в лунки планшета вносится раствор химерной MISRII-содержащей конструкции (100 нг/мл) в качестве специфического акцептора для тестируемых препаратов рАМГ. После заключительной инкубации реакционной смеси детекцию связанных с рецептором препаратов рАМГ осуществляют, используя пероксидазный конъюгат антител ACMIS-4-Пх (0,5 мкг/мл). Калибровочная кривая препарата С-рАМГ с использованием данной тест-системы представлена на Фиг. 4, Б.
Пример 4. Ингибирующая активность моноклональных антител в отношении связывания АМГ со специфическим рецептором MISRII. Дальнейшее изучение свойств моноклональных антител ACMIS-3 показало, что они не только специфичны по отношению к С-рАМГ, но и
обладают способностью блокировать взаимодействие гормона с MISRII. Использование тест-системы, описанной в п. 3.1., позволило показать, что интенсивность взаимодействия С-рАМГ со специфическим рецептором снижается в присутствии антител ACMIS-3 (10 мкг/мл) (Фиг. 5.). В контрольном эксперименте для инкубации с С-рАМГ вместо антител ACMIS-3 были использованы нормальные мышиные иммуноглобулины класса IgG.
Пример 5. Синтез и секвенирование ДНК, кодирующих вариабельные части легкой и тяжелой цепей моноклональных антител
5.1. Синтез и секвенирование ДНК, кодирующих вариабельные части легкой и тяжелой цепей моноклональных антител ACMIS-1. Из клеток гибридомы ACMIS-1 выделяли РНК, на матрице которой с помощью наборов синтетических праймеров (Immunogenetics Information System http://www.imgt.org) были амплифицированы фрагменты ДНК, кодирующие вариабельные области тяжелой (VH) и легкой (VL) цепей антитела. Полученные фрагменты ДНК были клонированы в вектор рALTA (Евроген) и секвенированы с внешних праймеров (М13). Последовательности фрагментов ДНК, кодирующих VH и VL, представлены на Seq ID No: 1 и Seq ID No: 2, вычисленные аминокислотные последовательности VH и VL представлены на Seq ID No: 3 и Seq ID No: 4 . Анализ последовательностей аминокислот вариабельных областей тяжелой и легкой цепей моноклонального антитела ACMIS-1 производили по Кэботу [Kabat E.A., Wu T.T., Perry H., Gottesman K. And Foeller C. Sequences of Proteins of Immunological Interest, Fifth Edition. NIH Publication, 1991, 91:3242], что позволило выделить участки CDR, определяющие комплементарность антитела антигену.
5.2. Синтез и секвенирование ДНК, кодирующих вариабельные части легкой и тяжелой цепей моноклональных антител ACMIS-3, ACMIS-4 и ACMIS-6 проводили как описано в п. 5.1., выделяя при этом РНК из клеток соответствующего клона — продуцента моноклональных антител.
На основе данных, приведенных выше, полученные моноклональные антитела против С-рАМГ человека по специфичности можно условно разделить на три независимые группы. К первой группе относятся антитела ACMIS-1 и ACMIS-4, которые распознают N-концевой пептид С-рАМГ SAGATA (Ser452—Ala457, Фиг. 2.), но не связываются с С-рАМГ в составе 70 кДа-мономера (Фиг. 1. Б) и не ингибируют связывание С-рАМГ с MISRII. Антитело ACMIS-6 можно отнести ко второй группе, поскольку оно специфично к конформационному эпитопу С-рАМГ и не связывается с денатурированным белком (Фиг. 1, В). Свойства антитела ACMIS-3, которое условно можно отнести к третьей группе, представляют повышенный интерес с точки зрения исследования биохимии С-рАМГ. Данное антитело способно к связыванию не только с димерной и мономерной формой С-рАМГ, но также и с С-концевым участком рАМГ в составе 70 кДа-мономера (Фиг. 1, В). Еще одним уникальным свойством антитела ACMIS-3 является способность подавлять связывание С-рАМГ с рекомбинантным MISRII (Фиг. 5).
Ни одно из полученных антител не способно к распознаванию С-рАМГ в составе полноразмерной молекулы гормона. Этот факт свидетельствует о том, что все полученные антитела специфичны по отношению к неодетерминантам только протеолизированного рАМГ и его С-концевого фрагмента.
Таким образом, полученные антитела группы ACMIS против С-рАМГ человека могут быть использованы для выделения рАМГ, а также для создания диагностических систем для детекции С-АМГ в биологических жидкостях и изучения биохимии гормона.
Моноклональные антитела по настоящему изобретению могут служить основой для конструирования химерных и гуманизированных антител, пригодных для создания лекарственных препаратов.
--->
Название проекта: Моноклональное антитело к С-концевому фрагменту
антимюллерова гормона
Ведомство ИС:RU
Номер заявки 2021109276
Дата подачи: 2021-04-05
Название изобретения
Заявитель и изобретатель:
Имя заявителя: Федеральное государственное унитарное предприятие
«Государственный научно-исследовательский институт особо чистых биопрепаратов»
Федерального медико-биологического агентств
Язык: RU
Название или имя и фамилия латиницей: Federal State Unitary Enterprise “State
Research Institute of Highly Pure Biopreparations” of the Federal Medical and
Biological Agency
Последовательности
Последовательность 31 «ДНК, кодирующая вариабельную область тяжелой цепи
моноклонального антитела»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
CAGGTCCAAC TGCAGCAGCC TGGGGCTGAG CTGGTGAGGC CTGGAGCTTC AGTGAAGCTG 60
TCCTGCAAGG CTTCTGGCTA CTCCTTCACC AGCTACTGGA TGAACTGGGT GAAGCAGAGG 120
CCTGGACAAG GCCTTGAGTG GATTGGCATG ATTCATCCTT CCGATAGTGA AACTAGGTTA 180
AATCAGAAGT TCAAGGACAA GGCCACATTG ACTGTAGACA AATCCTCCAG CACAGCCTAC 240
ATGCAACTCA GCAGCCCGAC ATCTGAGGAC TCTGCGGTCT ATTACTGTGC AAGCAGGGAC 300
TACTGGGGCC AAGGCACCAC TCTCACAGTC TCCTCA 336
Последовательность 32 «ДНК, кодирующая вариабельную область легкой цепи
оноклонального антитела»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
CAAATTGTTC TCACCCAGTC TCCAGCAATC ATGTCTGCAT CTCCAGGGGA GAAGGTCACC 60
ATGACCTGCA GTGCCAGCTC AAGTGTAAGT TCCAGTTACT TGCACTGGTA CCAGCAGAAG 120
CCAGGATCCT CCCCCAACT CTGGATTTAT GGCACATCCA ACCTGGCTTC TGGAGTCCCT 180
GCTCGCTTCA GTGGCAGTGG GTCTGGGACC TCCTATTCTC TCACAATCAG CAGCATGGAG 240
GCTGAAGATG CTGCCACTTA TTACTGCCAT CAGCGGAGTA GTTATCCGTG GACGTTCGGT 300
GGAGGCACCA AGCTGGAAAT CAAA 324
Последовательность 33 «Вариабельная область тяжелой цепи моноклонального
антитела»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
QVQLQQPGAE LVRPGASVKL SCKASGYSFT SYWMNWVKQR PGQGLEWIGM IHPSDSETRL 60
NQKFDKATL TVDKSSSTAY MQLSSPTSED SAVYYCASRD YWGQGTTLTV SS 112
Последовательность 34 «Вариабельная область легкой цепи моноклонального
антитела»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
QIVLTQSPAI MSASPGEKVT MTCSASSSVS SSYLHWYQQK PGSSPKLWIY GTSNLASGVP 60
ARFSGSGSGT SYSLTISSME AEDAATYYCH QRSSYPWTFG GGTKLEIK 108
Последовательность 35 «Гипервариабельная область тяжелой цепи моноклонального
антитела (CDRH-1)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
GYSFTSYW 8
Последовательность 36 «Гипервариабельная область тяжелой цепи моноклонального
антитела (CDRH-2)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
IHPSDSET 8
Последовательность 37 «Гипервариабельная область тяжелой цепи моноклонального
антитела (CDRH-3)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
ASRDY 5
Последовательность 38 «Гипервариабельная область легкой цепи моноклонального
антитела (CDRL-1)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
SSVSSSY 7
Последовательность 39 «Гипервариабельная область легкой цепи моноклонального
антитела (CDRL-2)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
GTS 3
Последовательность 40 «Гипервариабельная область легкой цепи моноклонального
антитела (CDRL-3)»
молекулы
фрагменты ДНК
и РНК
последовательность
Характеристики
характеристики
характеристики
ORGANISM= Mus musculus
Последовательность
HQRSSYPWT 9
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Моноклональное антитело к С-концевому фрагменту антимюллерова гормона | 2021 |
|
RU2770003C1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К С-КОНЦЕВОМУ ФРАГМЕНТУ АНТИМЮЛЛЕРОВА ГОРМОНА | 2018 |
|
RU2765689C2 |
| Моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 | 2020 |
|
RU2744274C1 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К НЕКТИНУ-4 ЧЕЛОВЕКА | 2019 |
|
RU2825839C2 |
| АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ К РЕЦЕПТОРУ ПОЛИОВИРУСА (PVR) ЧЕЛОВЕКА | 2017 |
|
RU2756275C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ В ОТНОШЕНИИ НЕКТИНА-2 ЧЕЛОВЕКА | 2020 |
|
RU2820275C2 |
| Моноклональное антиидиотипическое антитело АИ-G1, обладающее антигенными свойствами морфина | 2019 |
|
RU2717989C1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К ИНТЕРЛЕЙКИНУ-31 ДЛЯ ВЕТЕРИНАРНОГО ПРИМЕНЕНИЯ | 2019 |
|
RU2795411C2 |
| Антитела против анафилатоксина C5a человека | 2019 |
|
RU2731516C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АНТИ-СЕАСАМ 1 И АНТИ-PD АНТИТЕЛА ДЛЯ ТЕРАПИИ РАКА | 2014 |
|
RU2697522C1 |
Изобретение относится к области биотехнологии. Предложено моноклональное антитело, специфически связывающееся с конформационным эпитопом С-концевого фрагмента антимюллерова гормона человека. Изобретение может быть использовано для выделения рекомбинантного антимюллерова гормона человека, а также для создания диагностических систем для детекции С-концевого фрагмента этого гормона в биологических жидкостях и изучения биохимии гормона. 2 з.п. ф-лы, 5 ил., 1 табл., 5 пр.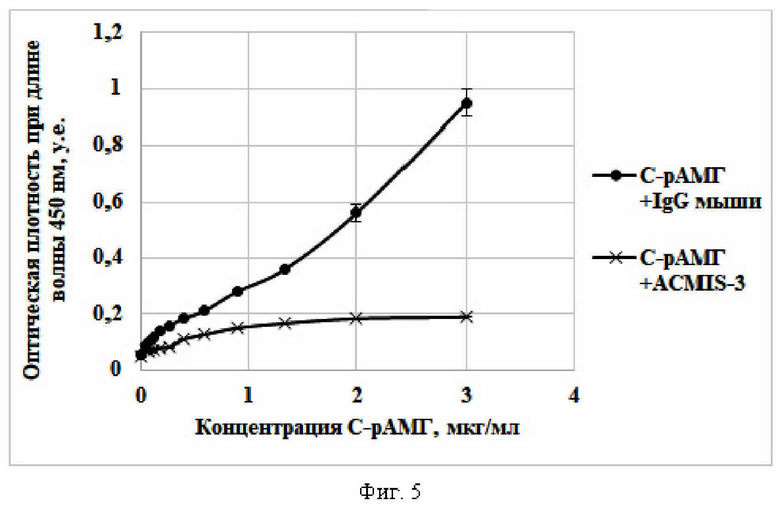
1. Моноклональное антитело, способное специфически связываться с конформационным эпитопом С-концевого фрагмента человеческого антимюллерова гормона, содержащее гипервариабельные участки CDR1, CDR2 и CDR3 тяжелой цепи с последовательностями SEQ ID NO: 35, 36 и 37, соответственно, и гипервариабельные участки CDR1, CDR2 и CDR3 легкой цепи с последовательностями SEQ ID NO: 38, 39 и 40, соответственно.
2. Моноклональное антитело по п.1, имеющее последовательность вариабельной области тяжелой цепи по SEQ ID NO: 33 и последовательность вариабельной области легкой цепи по SEQ ID NO: 34.
3. Моноклональное антитело по п.2, кодируемое ДНК, содержащей последовательности нуклеотидов по SEQ ID NO: 31 и SEQ ID NO: 32.
| WO 2006127850 A1, 30.11.2006 | |||
| WO 2008153433 A1, 18.12.2008 | |||
| Способ доклинической диагностики преждевременного истощения яичников у женщин репродуктивного возраста | 2016 |
|
RU2625723C1 |
| БОЯРСКИЙ К.Ю | |||
| и др | |||
| Роль антимюллерова гормона (амг) в норме и при различных гинекологических заболеваниях, Журнал акушерства и женских болезней, 2009, Том 58, Выпуск 3, с.75-85 | |||
| РАК А.Я | |||
| и др | |||
| Моноклональные антитела против рецептора антимюллерова гормона | |||
Авторы
Даты
2022-01-21—Публикация
2021-04-05—Подача