Группа изобретений относится к области биоорганической химии и молекулярной биологии, а именно к модифицированным направляющим РНК, и может быть использована для контролируемого редактирования генома системой CRISPR/Cas9 путем остановки системы в определенный момент времени в определенном месте путем облучения мягким ультрафиолетом.
CRISPR-системы (Clustered Regularly Interspaced Short Palindromic Repeats) - кластеризованные, регулярно распределенные короткие палиндромные повторы, разделенные уникальными последовательностями (спейсерами), которые заимствуются из чужеродных генетических фрагментов (бактериофагов) и обеспечивают противовирусную защиту бактерий. Вблизи этих повторов расположены белок-кодирующие CRISPR-ассоциированные гены (Cas). В настоящее время для редактирования генома широко используется система CRISPR/Cas9, которая состоит из белка Cas9 и двух РНК: crРНК, узнающей чужеродную ДНК по принципу комплементарности, и tracrPHK, связывающейся с crРНК и белком Cas9. Обе эти РНК могут быть объединены в одну молекулу единой направляющей РНК (sgPHK). В процессе узнавания комплекс РНК и белка Cas9 находит в двуцепочечной ДНК-мишени последовательности РАМ (Protospacer Adjacent Motif). Затем ДНК вблизи РАМ частично раскручивается, и образуется дуплекс между crРНК и ДНК-мишенью, после чего вступают в действие нуклеазные домены белка Cas9, которые разрезают обе цепи ДНК. Разрыв в ДНК далее устраняется по одному из механизмов репарации ДНК.
Известно множество примеров использования синтетических направляющих РНК в составе системы CRISPR/Cas9 для редактирования генома [1-4]. Для контролируемого включения системы геномного редактирования предложено использовать фотоблокированные РНК [5].
Недостатком этих систем является отсутствие возможности инактивации процесса редактирования генома при необходимости в определенный момент времени, например, для редактирования не всех молекул ДНК, а только их части. Такая задача, возникает, в частности, при разработке средств терапии заболеваний, вызванных увеличением числа копий (дупликацией) определенных генов.
В литературе не известны модифицированные (фоторасщепляемые) направляющие РНК, обладающие способностью инактивировать (отключать) систему редактирования генома CRISPR/Cas9.
Известна модифицированная (фоторасщепляемая) ДНК, блокирующая систему геномного редактирования CRISPR/Cas9 [6]. Данная ДНК комплементарна участку направляющей РНК, отвечающему за связывание с дцДНК (двухцепочечной ДНК) мишенью, содержит от одного до трех фоторасщепляемых линкеров. В присутствии этой ДНК происходит блокирование направляющей РНК, за счет чего достигается отсутствие активности системы геномного редактирования вплоть до облучения. В результате облучения происходит расщепление фотолинкера в составе блокирующей ДНК, высвобождение направляющей РНК и активация системы геномного редактирования CPJSPR/Cas9.
Недостатком известной фоторасщепляемой ДНК является отсутствие возможности останавливать работу этой системы в определенный момент времени и тем самым сохранять необходимую часть дцДНК в интактном виде. Данная фоторасщепляемая ДНК является дополнительным компонентом по отношению к стандартной системе редактирования генома, которая состоит из белка Cas9 и направляющей РНК (протяженной 102-звенной sgPHK или пары crPHK/tracrPHK), и требует дополнительного дизайна для каждой конкретной направляющей РНК с учетом ее нуклеотидной последовательности, и синтеза.
Наиболее близкой к заявляемой фоторасщепляемой направляющей РНК - прототипом, является фотоблокированная направляющая РНК, представляющая собой РНК, содержащую участок, отвечающий за связывание с белком Cas9 и участок связывания с ДНК-мишенью, в который встраивают фотоблокированные рибонуклеотиды, и позволяющая активировать систему геномного редактирования CPJSPR/Cas9 путем облучения светом [7].
Недостатком известной фотоблокированной направляющей РНК является то, что она не обладает способностью инактивировать (отключать) систему редактирования генома CRISPR/Cas9.
Способ получения известной фотоблокированной направляющей РНК представляет собой твердофазный фосфитамидный олигонуклеотидный синтез с использованием автоматического синтезатора LGC Bioatomation MerMade 4 DNA/RNA Synthesizer (Irving, TX, USA) по стандартному протоколу с сохранением на 5'-конце олигонуклеотида диметокситритильной группы (5'-DMTr-on протокол). В качестве носителя для синтеза используют стеклянные частицы с размером пор 1000  с присоединенным защищенным уридином. В качестве мономерных синтонов используют коммерчески доступные фосфитамиды олигорибонуклеотидов и специально синтезированные фосфитамиды нитропиперанилоксиметил(NPOM)-модифицированных по гетероциклическому основанию уридина и гуанозина (модифицированные фосфитамиды).
с присоединенным защищенным уридином. В качестве мономерных синтонов используют коммерчески доступные фосфитамиды олигорибонуклеотидов и специально синтезированные фосфитамиды нитропиперанилоксиметил(NPOM)-модифицированных по гетероциклическому основанию уридина и гуанозина (модифицированные фосфитамиды).
Каждый цикл синтеза состоит из следующих стадий:
1) детритилирование - удаление диметокситритильной защитной группы с 5'-гидроксила растущей олигонуклеотидной цепи;
2) присоединение очередного мономерного звена, которое представляет собой β-цианэтил-N,N-диизопропиламидофосфит одного из защищенных рибонуклеозидов или модифицированный фосфитамид, для чего используют 0,08 M раствор фосфитамида, а время стадии составляет 8 минут;
3) кэпирование - блокирование непрореагировавших 5'-гидроксилов, что позволяет избежать пропусков нуклеозидов в последовательности требуемого олигонуклеотида;
4) окисление, в ходе которого происходит превращение фосфиттриэфирных межнуклеозидных связей в фосфотриэфирные. После проведения необходимого числа синтетических циклов получают 5'-O-диметокситритил(ОМТг)-содержащую защищенную направляющую РНК, содержащую фотоблокированные рибонуклеотиды. Для отделения олигонуклеотида от носителя, деблокирования гетероциклических оснований и межнуклеозидных фосфатов, к полимерсвязанной РНК добавляют 1 мл смеси 40%-ного водного метиламина и аммиака (1:1 ν/ν), выдерживают в течение 20 мин при 65°С. Для удаления трет-бутилдиметилсилильных защитных групп с 2'-гидроксилов рибонуклеозидов к олигонуклеотиду добавляют 65 мкл триэтиламина и 75 мкл триэтиламинтригидрофторида (TEA-3HF) в 11 мкл диметилсульфоксида и выдерживают при 65°С в течение 2 часов.
5'-O-ОМТг-содержащую РНК очищают хроматографическим методом с использованием колонки Waters X-Bridge ВЕН С18. Финальное удаление 5'-O-DMTr-группы проводят, добавляя 400 мкл 35 мМ раствора ацетата натрия и выдерживая при 55°С в течение 2 часов. Олигорибонуклеотид осаждают из 3М раствора ацетата натрия спиртом.
Полученная этим способом модифицированная РНК содержит фотоотщепляемые по гетероциклическому основанию рибонуклеозиды в участке, отвечающем за связывание с дцДНК (двуцепочечной ДНК) мишенью. До облучения эта направляющая РНК не способна активировать систему редактирования генома CRISPR/Cas9. В результате облучения происходит отщепление фотогрупп в составе модифицированной направляющей РНК, высвобождение направляющей РНК и активация системы геномного редактирования CRISPR/Cas9.
Недостатками известного способа являются высокая трудоемкость и длительность, связанная с необходимостью предварительного получения соответствующих модифицированных мономерных синтонов для химического синтеза модифицированной РНК, а также отсутствие возможности получать модифицированную РНК, содержащую фоторасщепляемые линкеры, что позволяет инактивировать (останавливать) работу этой системы в определенный момент времени и тем самым сохранять необходимую часть дцДНК в интактном виде.
Задачей группы изобретений является получение фоторасщепляемых направляющих РНК, которые позволяли бы инактивировать (отключать) систему геномного редактирования CRISPR/Cas9 в определенный момент времени и тем самым сохранять часть дцДНК мишени интактной, что является необходимым, в частности, при разработке подходов к лечению болезней, вызванных мультиплицированием генов.
Технический результат: обеспечение адресной (специфичной) инактивации системы геномного редактирования CRISPR/Cas9 в определенный момент времени в определенном месте, а также расширение арсенала направляющих РНК, обладающих способностью инактивировать систему геномного редактирования CRISPR/Cas9.
Поставленная задача достигается предлагаемыми фоторасщепляемыми направляющими РНК, представляющими собой олигорибонуклеотид, содержащий фоторасщепляемый линкер на основе 1-(2-нитрофенил)-1,2-этандиола, встроенный между выбранными рибонуклеозидами РНК, имеющими нуклеотидную последовательность SEQ ID NO: 1 или SEQ ID NO: 2 или SEQ ID NO: 3 соответственно.
В преимущественном варианте синтезирована фоторасщепляемая направляющая РНК, имеющая нуклеотидную последовательность SEQ ID NO: 1, представляющая собой 102-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер, встроенный между 43-им и 44-ым рибонуклеозидами от 5'-конца РНК, в область ее взаимодействия с Cas9 белком, что позволяет осуществлять ее контролируемое специфичное расщепление между 43-им и 44-ым рибонуклеотидами путем облучения светом с длиной волны 365 нм.
Синтезирована также фоторасщепляемая направляющая РНК, имеющая последовательность SEQ ID NO: 2 или SEQ ID NO: 3, представляющая собой 42-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер, встроенный в область связывания с дцДНК мишенью, расположенный между 14-ым и 15-ым рибонуклеотидами от 5'-конца, что позволяет осуществлять их контролируемое расщепление между 14-ым и 15-ым рибонуклеотидами путем облучения светом с длиной волны 365 нм.
Нуклеотидные последовательности направляющих РНК выбраны на основании ранее опубликованных данных [8], положения для введения фоторасщепляемого линкера выбраны на основании анализа структуры комплекса направляющих РНК с Cas9 белком [9] и данных о влиянии модификаций направляющей РНК на эффективность расщепления дцДНК [3].
Был проведен скрининг нескольких вариантов фоторасщепляемых РНК в качестве компонентов системы CRISPR/Cas9, позволяющих инактивировать ее действие в определенный момент времени путем направленного облучения УФ-светом. В результате были выбраны направляющие РНК sgPHK_SP2_PL, crPHK GFP 1 PL и crPHK_GFP2_PL, первая из которых содержит фоторасщепляемый линкер в области взаимодействия с Cas9 белком, а вторая и третья - в области связывания с дцДНК мишенью.
Полученные модифицированные (фоторасщепляемые) направляющие РНК обладают следующими характеристиками:
- направляют расщепление дцДНК белком Cas9 в системе геномного редактирования CRISPR/Cas9 вплоть до облучения;
- разрушаются под действием облучения светом с длиной волны 365 нм;
- позволяют остановить действие системы CRISPR/Cas9 путем облучения в заданное время и в определенном месте.
Предлагаемые фоторасщепляемые направляющие РНК позволяют проводить эффективный гидролиз плазмидной ДНК белком Cas9 вплоть до облучения и останавливать процесс путем облучения реакционной смеси светом с длиной волны 365 нм.
Поставленная задача достигается также способом получения модифицированной (фоторасщепляемой) направляющей РНК, обладающей способностью инактивировать систему редактирования генома CPJSPR/Cas9.
Технический результат: сокращение трудоемкости способа и обеспечение возможности получения модифицированной направляющей РНК, обладающей способностью инактивировать систему геномного редактирования CRISPR/Cas9.
Предлагаемый способ заключается в следующем.
Синтез направляющей РНК осуществляют на автоматическом ДНК/РНК-синтезаторе ASM-800 с использованием твердофазного фосфитамидного олигонуклеотидного синтеза. В качестве твердофазного носителя для синтеза используют стекло с контролируемым размером пор (CPG, 500 А) с присоединенным через 3'-гидроксильную группу 5', 2', N-защищенным рибонуклеозидом. В качестве мономерных синтонов используют коммерчески доступные фосфитамиды рибонуклеотидов и специально синтезированный фосфитамид на основе 1-(2-нитрофенил)-1,2-этандиола (фоторасщепляемый линкер).
Каждый цикл синтеза состоит из следующих стадий: 1) детритилирование - удаление диметокситритильной защитной группы с 5'-гидроксила растущей олигонуклеотидной цепи;
2) присоединение очередного мономерного звена, которое представляет собой р-цианэтил-N,N-диизопропиламидофосфит одного из защищенных рибонуклеозидов, для чего используют 0,1 M раствор фосфитамида, а время стадии составляет 6 минут, или присоединение фоторасщепляемого линкера, который представляет собой 1-(2-циано-N,N-диизопропилфосфитамид)-2-O-4,4'-диметокситритил-1-(2-нитрофенил)-1,2-этандиол, для чего используют 0,1 M раствор фосфитамида, а время стадии составляет 25-35 минут;
3) кэпирование - блокирование непрореагировавших 5'-гидроксилов, что позволяет избежать пропусков нуклеозидов в последовательности требуемого олигонуклеотида;
4) окисление, в ходе которого происходит превращение фосфиттриэфирных межнуклеозидных связей в фосфотриэфирные.
После проведения необходимого числа синтетических циклов получают защищенную направляющую РНК, содержащую фоторасщепляемый линкер. После деблокирования ее выделяют препаративным гель-электрофорезом.
Предлагаемый способ позволяет вводить фоторасщепляемый линкер между необходимыми рибонуклеотидами направляющей РНК в область связывания с дцДНК мишенью или в область взаимодействия с Cas9 белком, что обеспечивает ее контролируемое расщепление путем облучения светом с длиной волны 365 нм.
Определяющими отличиями предлагаемого способа получения модифицированной направляющей РНК от прототипа являются:
- в ходе автоматического твердофазного фосфитамидного синтеза РНК на стадии присоединения модифицированного мономерного звена используют раствор фосфитамида на основе 1-(2-нитрофенил)-1,2-этандиола (фоторасщепляемый линкер) в абсолютном ацетонитриле с концентрацией 0,1 моль/л, при этом время этой стадии увеличивают до 25-35 минут, что позволяет вводить фоторасщепляемый линкер в состав олигорибонуклеотидов с высокой эффективностью в определенном положении;
- для кэпирования используют раствор более доступного реагента пропионового ангидрида и N-метилимидазола в тетрагидрофуране, что позволяет предотвратить появление пропусков нуклеозидов в последовательности требуемого олигонуклеотида;
- удаление 5'-концевой диметокситритильной группы осуществляют на последней стадии синтеза, перед деблокированием защитных групп с межнуклеотидных фосфатов и гетероциклических оснований, отделения от твердофазного носителя, удаления 2'-O-третбутилдиметилсилильных групп, что позволяет упростить способ и выделять РНК непосредственно после деблокирования методом препаративного гель-электрофореза. В прототипе удаление 5'-диметокситритильной группы проводят после деблокирования защитных групп с межнуклеотидных фосфатов и гетероциклических оснований, отделения от твердофазного носителя, удаления 2'-O-третбутилдиметилсилильных групп и хроматографического выделения.
Предлагаемый способ позволяет менее трудоемко получать фоторасщепляемую направляющую РНК, способную инактивировать действие системы CRISPR/Cas9 путем облучения светом с длиной волны 365 нм в заданное время и в определенном месте.
Изобретение иллюстрируется фигурами, перечень которых приведен ниже.
Фиг. 1. Нуклеотидная последовательность модифицированной направляющей РНК sgPHK_SP2_PL.
Фиг. 2. Нуклеотидная последовательность модифицированной направляющей РНК crPHKGFPlPL.
Фиг. 3. Нуклеотидная последовательность модифицированной направляющей РНК crPHK_GFP2_PL.
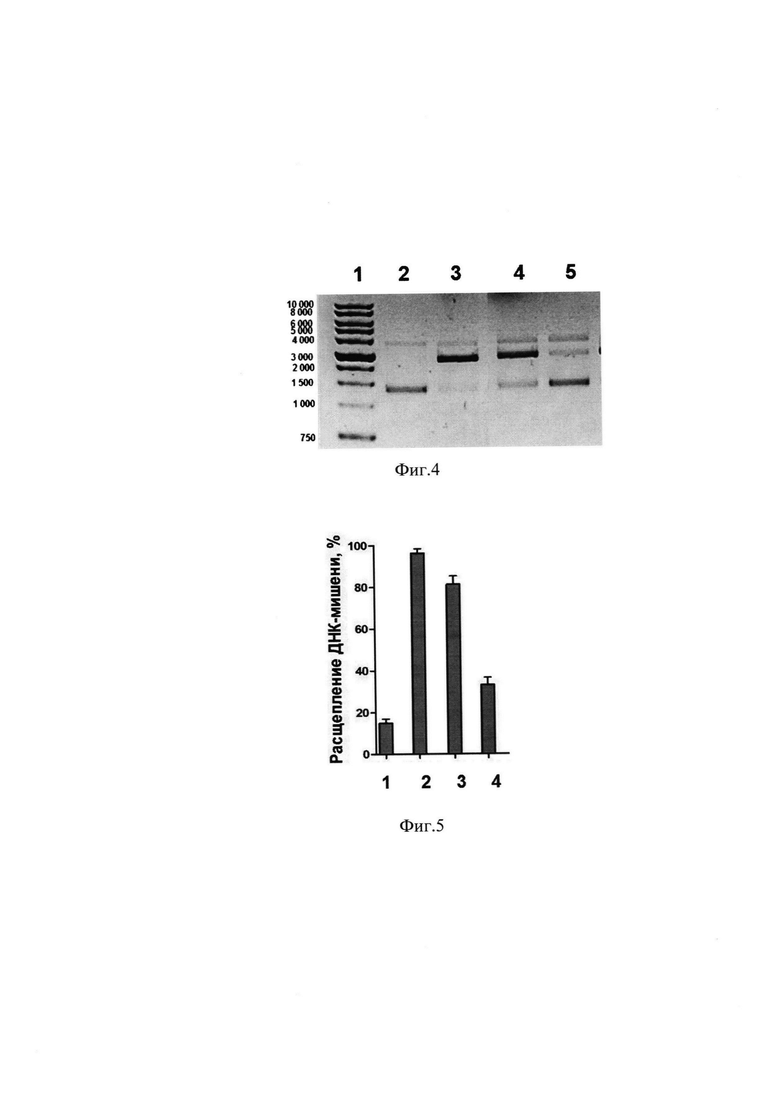
Фиг. 4. Фотография агарозного геля после разделения реакционных смесей. Дорожка 1 - маркер длины ДНК; дорожка 2 - исходная ДНК плазмида pBS2SKM; дорожка 3 - расщепление ДНК плазмиды pBS2SKM белком Cas9 в присутствии контрольной химически синтезированной 102 -звенной sgPHK; дорожка 4 - расщепление ДНК плазмиды pBS2SKM белком Cas9 в присутствии направляющей РНК sgPHK_SP2_PL; дорожка 5 - расщепление ДНК плазмиды pBS2SKM белком Cas9 в присутствии направляющей РНК sgPHK_SP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм.
Фиг. 5. Эффективность расщепления ДНК плазмиды pBS2SKM белком Cas9, где: столбец 1 - в отсутствие направляющей РНК; столбец 2 - в присутствии контрольной химически синтезированной 102 - звенной sgPHK; столбец 3 - в присутствии направляющей РНК sgPHK_SP2_PL; столбец 4 - в присутствии направляющей РНК sgPHK_SP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм.
Фиг. 6. Кинетические профили расщепления ДНК плазмиды pBS2SKM в течение 1,5 ч 15-тикратным избытком белка Cas9 в присутствии эквимолярного количества направляющей фоторасщепляемой РНК sgPHK_SP2_PL; кривая 1 - в присутствии контрольной химически синтезированной 102-звенной sgPHK; кривая 2 - в присутствии направляющей РНК sgPHK_SP2_PL; кривая 3 - в присутствии направляющей РНК sgPHK_SP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм в присутствии белка Cas9; кривая 4 - в присутствии направляющей РНК sgPHK_SP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм; кривая 5 - в присутствии направляющей РНК sgPHK_SP2_PL, при облучении в течение 5 мин светом с длиной волны 365 нм, начиная с 20 мин от начала реакции; кривая 6 - в присутствии направляющей РНК sgPHK_SP2_PL при облучении в течение 30 мин светом с длиной волны 365 нм, начиная с 20 мин от начала реакции.
Фиг. 7. Фотография агарозного геля после разделения реакционных смесей, где: дорожка 1 - маркер длины ДНК; дорожка 2 - исходная ДНК плазмида pcDNA3.1_EGFP_DP; дорожка 3 - расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии контрольной химически синтезированной 42 -звенной crРНК и tracrPHK; дорожка 4 - расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии направляющей РНК crPHKGFPIPL и tracrPHK; дорожка 5 - расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии направляющей РНК crPHK GFPI PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм, и tracrPHK; дорожка 6 - расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии контрольной химически синтезированной 42 -звенной crРНК и tracrPHK; дорожка 7 - расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии направляющей РНК crPHK_GFP2_PL и tracrPHK; дорожка 8 -расщепление ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9 в присутствии направляющей РНК crPHK_GFP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм, и tracrPHK.
Фиг. 8. Эффективность расщепления ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9, где: столбец 1 - в присутствии контрольной химически синтезированной 42 -звенной crРНК; столбец 2 - в присутствии направляющей РНК crPHK GFPI PL и tracrPHK; столбец 3 - в присутствии направляющей РНК crPHKGFPIPL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм, и tracrPHK; столбец 4 - в присутствии контрольной химически синтезированной 42 -звенной crРНК; столбец 5 - в присутствии направляющей РНК crPHK_GFP2_PL и tracrPHK; столбец 6 - в присутствии направляющей РНК crPHK_GFP2_PL, предварительно облученной в течение 30 мин светом с длиной волны 365 нм, и tracrPHK.
Изобретение иллюстрируется примерами, приведенными ниже, подтверждающими возможность осуществления изобретения и реализации заявленного назначения.
Пример 1. Получение модифицированной направляющей РНК с нуклеотидной последовательностью SEQ ID NO: 1 (sgPHK_SP2_PL) Синтез sgPHK_SP2_PL проводили на автоматическом ДНК/РНК синтезаторе ASM-800 (Биоссет, Россия) по стандартному протоколу [10] с использованием β-цианэтил-фосфитамидов 5',2', N-защищенных рибонуклеозидов и 1-(2-циано-N,N-диизопропилфосфитамид)-2-O-4,4'-диметокситритил-1 -(2-нитрофенил)-1,2-этандиола. В качестве твердофазного носителя использовали стеклянные частицы CPG (controlled pore glass) с диаметром пор 500  с присоединенным через 3'-гидроксильную группу 5',2',N-защищенным рибонуклеозидом.
с присоединенным через 3'-гидроксильную группу 5',2',N-защищенным рибонуклеозидом.
Каждый цикл синтеза состоял из следующих стадий:
5) детритилирование - удаление диметокситритильной защитной группы с 5'-гидроксила растущей олигонуклеотидной цепи путем обработки 3%-ным раствором дихлоруксусной кислоты в дихлорметане;
6) присоединение очередного мономерного звена, которое представляет собой β-цианэтил-N-диизопропиламидофосфит одного из защищенных рибонуклеозидов, для чего используют 0,1 M раствор фосфитамида в абсолютном ацетонитриле, а время стадии составляет 6 минут, или присоединение фоторасщепляемого линкера, который представляет собой 1-(2-циано-N,N-диизопропилфосфитамид)-2-O-4,4'-диметокситритил-1-(2-нитрофенил)-1,2-этандиола, для чего используют 0,1 M раствор фосфитамида в абсолютном ацетонитриле, а время стадии составляет 25-35 минут. В качестве активирующего агента на стадии присоединения использовали 5-этилтио-1Н-тетразол;
7) кэпирование - блокирование непрореагировавших 5'-гидроксилов с использованием пропионового ангидрида и N-метилимидазола, что позволяет избежать пропусков нуклеозидов в последовательности требуемого олигонуклеотида;
8) окисление раствором йода в пиридине, в ходе которого происходит превращение фосфиттриэфирных межнуклеозидных связей в фосфотриэфирные.
После проведения необходимого числа синтетических циклов и удаления 5'-концевой диметокситритильной группы получали защищенную направляющую РНК, содержащую фоторасщепляемый линкер. Для отделения олигонуклеотида от полимерного носителя, деблокирования гетероциклических оснований и межнуклеозидных фосфатов к полимерсвязанной РНК добавляли 300 мкл 40%-ного водного метиламина, выдерживали в течение 20 мин при 65°С и постоянном перемешивании, затем при -20°С в течение 15-20 мин и отделяли от полимера центрифугированием. Полимер промывали 3x100 мкл смеси этанол:ацетонитрил:вода (1:1:1). Растворы объединяли и упаривали до сухого остатка в вакуумном испарителе Speed-Vac Concentrator SVC-1 ООН. Для удаления mpem-бутилдиметилсилильных защитных групп с 2'-гидроксилов рибонуклеозидов к сухому остатку олигонуклеотида добавляли 200 мкл смеси N-метил-2-пирролидинон:триэтиламин:триэтиламинтригидрофторид (1.5: 0.75: 1.0, ν/ν/ν) и выдерживали при 65°С в течение 2.0 ч. После охлаждения раствора до комнатной температуры добавляли 300 мкл этокситриметилсилана и перемешивали в течение 10 мин. К полученной смеси добавляли 1 мл серного эфира и центрифугировали, раствор декантировали, осадок промывали серным эфиром, высушивали на воздухе. Полностью деблокированную РНК очищали препаративным электрофорезом в денатурирующем 12%-ном акриламидном геле в условиях: акриламид-.Ν,Ν'-метиленбисакриламид (30:0,5), 8 Μ мочевина, 50 мМ Трис-борат (рН 8.3), 0.1 мМ Na2EDTA, при напряжении 50 В/см. После проведения электрофореза, гель помещали на пластину для ТСХ, основную часть закрывали стеклом во избежание фоторасщепления и визуализировали края полосы РНК в УФ-свете, затем вырезали соответствующий необлученный участок геля. РНК элюировали водным раствором 0.3 M ацетата натрия (рН 5.2) в течение ночи при 25°С, элюированную РНК осаждали в виде натриевой соли добавлением 4-х кратного избытка перегнанного этилового спирта при -20°С в течение не менее 20 мин. Осадок отделяли центрифугированием в течение 10 мин при 4°С и 14500 об./мин. Супернатант отбирали, осадок олигонуклеотида промывали охлажденным до -20°С 80%-ным водным раствором этилового спирта, высушивали при 37°С.
Полученная модифицированная направляющая РНК sgPHK_SP2_PL, представляет собой 102-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер на основе 1-(2-нитрофенил)-1,2-этандиола, встроенный между 43-им и 44-ым рибонуклеозидами от 5'-конца РНК, имеет нуклеотидную последовательность SEQ ID NO: 1 (фиг. 1).
Направляющую РНК sgPHK_SP2_PL анализировали методом аналитического электрофореза в 12%-ном денатурирующем ПААГ с последующим окрашиванием геля раствором красителя "Stains-АН". В качестве контроля длины использовали ферментативно полученную не содержащую фоторасщепляемый линкер РНК той же последовательности.
Пример 2. Получение модифицированной направляющей РНК с нуклеотидной последовательностью SEQ ID NO: 2 (crPHK GFPI PL)
Синтез crPHK GFPI PL проводили на автоматическом ДНК/РНК синтезаторе ASM-800 (Биоссет, Россия) по стандартному протоколу [10], аналогично примеру 1.
После проведения необходимого числа синтетических циклов и удаления 5'-концевой диметокситритильной группы получали защищенную направляющую РНК, содержащую фоторасщепляемый линкер. Отделение олигонуклеотида от полимерного носителя, деблокирование гетероциклических оснований и межнуклеозидных фосфатов полимерсвязанной РНК и ее выделение осуществляли аналогично примеру 1.
Полученная модифицированная направляющая РНК crPHK GFPI PL представляет собой 42-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер на основе 1-(2-нитрофенил)-1,2-этандиола, встроенный между 14-ым и 15-ым рибонуклеозидами от 5'-конца РНК, имеет нуклеотидную последовательность SEQ ID NO: 2 (фиг. 2).
Направляющую РНК crPHK GFPI PL анализировали методами аналитического электрофореза в 12%-ном денатурирующем ПЛАТ с последующим окрашиванием геля раствором красителя "Stains-All" и MALDI-TOF масс-спектрометрии.
Пример 3. Получение модифицированной направляющей РНК с нуклеотидной последовательностью SEQ ID NO: 3 (crPHK_GFP2_PL)
Синтез crPHK_GFP2_PL проводили на автоматическом ДНК/РНК синтезаторе ASM-800 (Биоссет, Россия) по стандартному протоколу [10], аналогично примеру 1.
После проведения необходимого числа синтетических циклов и удаления 5'-концевой диметокситритильной группы получали защищенную направляющую РНК, содержащую фоторасщепляемый линкер. Отделение олигонуклеотида от полимерного носителя, деблокирование гетероциклических оснований и межнуклеозидных фосфатов полимерсвязанной РНК и ее выделение осуществляли аналогично примеру 1.
Полученная модифицированная направляющая РНК crPHK_GFP2_PL, представляет собой 42-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер на основе 1-(2-нитрофенил)-1,2-этандиола, встроенный между 14-ым и 15-ым рибонуклеозидами от 5'-конца РНК, имеет нуклеотидную последовательность SEQ ID NO: 3 (фиг. З).
Направляющую РНК crPHK_GFP2_PL анализировали методами аналитического электрофореза в 12%-ном денатурирующем ПААГ с последующим окрашиванием геля раствором красителя "Stains-All" и MALDI-TOF масс-спектрометрии.
Пример 4. Использование модифицированной направляющей РНК sgPHK_SP2_PL для специфичного направленного расщепления плазмидной ДНК, инактивируемого под действием облучения.
Исследовано расщепление ДНК плазмиды pBS2SKM на основе вектора pBluescript II SK(-) со вставкой протоспейсерной последовательности и РАМ (5'-TGG-3'), полученной согласно стандартному протоколу [8], нуклеазой Cas9, полученной по протоколу [11], в присутствии модифицированной направляющей РНК sgPHK_SP2_PL. Реакцию проводили при 37°С в течение 1 ч в буферном растворе (20 мМ HEPES (рН 7,5), 100 мМ КС1, 1 мМ дитиотреит, 0,5 мМ Ка2ЭДТА, 2 мМ MgCl2, 25% глицерина).
Для сборки эффекторного комплекса в буфер добавляли 1.35 мкл (1 мкМ, 1.35 пмоль) раствора направляющей РНК sgPHK_SP2_PL или sgPHK_SP2_PL, инактивированной УФ облучением в течение 30 минут (λ=365 нм), и 0.60 мкл раствора белка Cas9 (2.24 мкМ, 1.35 пмоль), находящимися в 50-кратном избытке по отношению к плазмиде pBS2SKM, и инкубировали 15 мин при 37°С. Добавляли 1 мкл раствора (50 нг/мкл, 27 фмоль) плазмиды pBS2SKM, перемешивали и инкубировали в течение часа при 37°С в условиях отсутствия прямого солнечного света или накрыв фольгой. Реакцию останавливали добавлением 2.5 мкл раствора, содержащего 250 мМ Na2 ЭДТА, 1.2% SDS, 0.01% бромфенолового синего и 30% глицерина.
Результаты ферментативной реакции анализировали в 1%-ом агарозном геле с прокрашиванием геля бромистым этидием и визуализацией с использованием системы Quantum Vilber Lourmat (Vilber Lourmat, Франция). Для получения количественных характеристик изображения переводили в цифровую форму в программном пакете Quantity One (Bio-Rad, США). Долю расщепления плазмиды рассчитывали по следующим формулам:
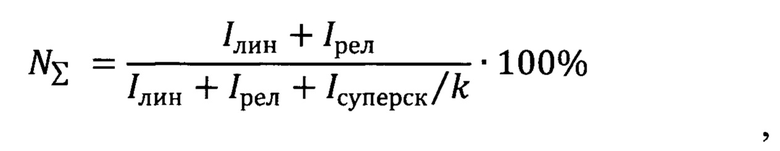
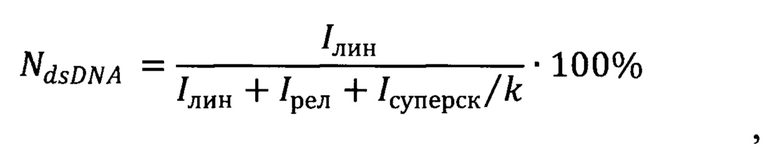

Где 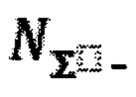 ссуммарное расщепление плазмиды,
ссуммарное расщепление плазмиды,  расщепление двух цепей ДНК плазмиды,
расщепление двух цепей ДНК плазмиды, 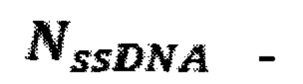 расщепление одной цепи ДНК плазмиды, - интенсивность полосы, соответствующей линейной форме плазмиды, - интенсивность полосы, соответствующей релаксированной форме плазмиды, - интенсивность полосы, соответствующей суперскрученной форме плазмиды, k=1.14 - коэффициент эффективности окрашивания суперскрученной формы ДНК относительно релаксированной формы [12].
расщепление одной цепи ДНК плазмиды, - интенсивность полосы, соответствующей линейной форме плазмиды, - интенсивность полосы, соответствующей релаксированной форме плазмиды, - интенсивность полосы, соответствующей суперскрученной форме плазмиды, k=1.14 - коэффициент эффективности окрашивания суперскрученной формы ДНК относительно релаксированной формы [12].
На фиг. 4 приведена фотография агарозного геля после разделения реакционных смесей. На фиг. 5 приведены эффективности расщепления ДНК плазмиды pBS2SKM белком Cas9.
Из фиг. 4, 5 видно, что в присутствии модифицированной (фоторасщепляемой) направляющей РНК sgPHK_SP2_PL до облучения происходит эффективное расщепление ДНК (около 80%), в то время как после облучения этой РНК эффективность расщепления значительно уменьшается (менее 40%). Полученные результаты свидетельствуют о том, что облучение светом приводит к остановке системы редактирования генома за счет разрушения фоторасщепляемой РНК.
На фиг. 6. приведены кинетические профили расщепления ДНК плазмиды pBS2SKM в течение 1,5 ч 15-ти кратным избытком белка Cas9 в присутствии эквимолярного количества модифицированной направляющей РНК sgPHK_SP2_PL. Из фиг. 6 видно, что наличие фоторасщепляемого линкера в составе направляющей РНК позволяет остановить реакцию расщепления ДНК на уровне 40% путем облучения, что позволит контролировать количество не расщепленной ДНК.
Пример 5. Использование модифицированных направляющих РНК crPHK GFPI PL и crPHK_GFP2_PL для специфичного направленного расщепления плазмидной ДНК, инактивируемой под действием облучения.
Исследовано расщепление ДНК плазмиды pcDNA3.1_EGFP_DP (6119 п. о.), нуклеазой Cas9, полученной по протоколу [12], в присутствии направляющей РНК crPHKGFPIPL или crPHK_GFP2_PL и 74-звенной tracrPHK (5'- AACAGCAUAGCAAGUUAAAAUAAGGCUAGU-CCGUAUCAACUUCAAAAAOUCOCACCCAOUCOOUOCUUUUUU). Реакцию проводили при 37°С в течение 1 ч в буферном растворе (20 мМ HEPES (рН 7,5), 100 мМ КС1, 1 мМ дитиотреит, 0,5 мМ Nа2ЭДТА, 2 мМ MgCl2, 25% глицерина).
Для сборки эффекторного комплекса в буфер добавляли по 1.35 мкл (1 мкМ, 1.35 пмоль) растворов направляющих РНК tracrPHK и crРНК (crPHKGFPIPL или crPHK_GFP2_PL) или этих же crРНК, дезактивированных УФ облучением в течение 30 минут (λ=365 нм), и 0.60 мкл раствора белка Cas9 (2.24 мкМ, 1.35 пмоль), находящимися в 50-кратном избытке по отношению к плазмиде pcDNA3.1_EGFP_DP, и инкубировали 15 мин при 37°С. Добавляли 1 мкл раствора (50 нг/мкл, 27 фмоль) плазмиды pcDNA3.1_EGFP_DP, перемешивали и инкубировали в течение часа при 37°С в условиях отсутствия прямого солнечного света или накрыв фольгой. Реакцию останавливали добавлением 2.5 мкл раствора, содержащего 250 мМ Na2 ЭДТА, 1.2% SDS, 0.01% бромфенолового синего и 30% глицерина.
Результаты ферментативной реакции анализировали в 1%-ом агарозном геле с прокрашиванием геля бромистым этидием и визуализацией с использованием системы Quantum Vilber Lourmat (Vilber Lourmat, Франция). Для получения количественных характеристик изображения переводили в цифровую форму в программном пакете Quantity One (Bio-Rad, США). Долю расщепления плазмиды рассчитывали по формулам, приведенным в примере 4.
На фиг. 7 приведена фотография агарозного геля после разделения реакционных смесей, а на фиг. 8 приведены эффективности расщепления ДНК плазмиды pcDNA3.1_EGFP_DP белком Cas9.
Из фиг. 7, 8 видно, что в присутствии модифицированных направляющих РНК (crPHK GFPI PL или crPHK_GFP2_PL) до облучения происходит эффективное расщепление ДНК (более 80%), в то время как после облучения этих РНК эффективность расщепления уменьшается, и составляет около 30% для crPHKGFPIPL и около 70% для crPHK_GFP2_PL. Полученные результаты свидетельствуют о том, что облучение светом приводит к остановке (инактивации) системы редактирования генома за счет разрушения фоторасщепляемой направляющей РНК.
Получаемые предлагаемым способом модифицированные направляющие РНК обеспечивают возможность специфично и адресно инактивировать действие системы CRISPR/Cas9 путем облучения в заданное время и в определенном месте.
Источники информации
1. US Patent for Cas9-DNA targeting unit chimeras (Patent number: 10190106, Date of Patent: Jan 29, 2019, Patent Publication Number: 20160177278, Assignee: Univesity of Massachusetts (Boston, MA), Inventors: Scot Andrew Wolfe (Winchester, MA), Mehmet Fatih Bolukbasi (Worcester, MA), Ankit Gupta (Worcester, MA), Erik J Sontheimer (Auburndale, MA), Nadia Amrani (Shrewsbury, MA), Application Number: 14/976,196).
2. US Patent Application for ARTIFICIAL SINGLE GUIDE RNA AND USE THEREOF Patent Application (Application #20190382758, Publication number: 20190382758, Publication Date: Dec 19, 2019, Applicant: BONAC CORPORATION (Kurume) Inventors: Eriko AOKI (Kurume), Tadaaki OHGI (Kurume), Takashi KJNOSHITA (Kurume), Application Number: 16/073,998).
3. Filippova J., Matveeva A., Zhuravlev E., Stepanov G. Guide RNA modification as a way to improve CRISPR/Cas9-based genome-editing systems. Biochimie. 2019 V.167. P.49-60. doi: 10.1016/j.biochi.2019.09.003.
4. US Patent for Methods and compositions for RNA-directed target DNA modification and for RNA-directed modulation of transcription (Patent number: 10421980, Date of Patent: Sep 24, 2019, Patent Publication Number: 20180312874, Assignees: The Regents of the University of California (Oakland, CA), University of Vienna (Vienna), (Braunschweig), Inventors: Jennifer A. Doudna (Berkeley, CA), Martin Jinek (Berkeley, CA), Krzysztof Chylinski (Vienna), Emmanuelle Charpentier (Braunschweig), Application Number: 16/033,002).
5. Liu Y., Zou R.S., He S., Nihongaki Y., Li X., Razavi S., Wu В., Ha T. Very fast CRISPR on demand. Science. 2020. V. 368. N.6496. P. 1265-1269. doi: 10.1126/science.aay8204.
6. Jain P.K, Ramanan V., Schepers A.G., Dalvie N.S., Panda A., Fleming H.E., Bhatia S.N. Development of Light-Activated CRISPR Using Guide RNAs with Photocleavable Protectors // Angew. Chem. Int. Ed. Engl. 2016 V.55. N.40. P. 12440-12444. doi: 10.1002/anie.2016061.
7. Zhou W., Brown W., Bardhan A., Delaney M., Ilk A.S., Rauen R.R., Kahn S.I., Tsang M., Deiters A. Spatiotemporal Control of CRISPR/Cas9 Function in Cells and Zebrafish using Light-Activated Guide RNA. Angew. Chem. Int. Ed. 2020 V.59. N.23. P.8998-9003. doi: 10.1002/anie.201914575.
8. Jinek M., Chylinski K., Fonfara I., Hauer M., Doudna J.A., Charpentier E. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science. 2012 V.337. N.6096. P.816-821. doi: 10.1126/science. 1225829.
9. US Patent Application for CAS9 CRYSTALS AND METHODS OF USE THEREOF Patent Application (Application #20160319262, Publication number: 20160319262, Publication Date: Nov 3, 2016, Inventors: Jennifer A. Doudna (Oakland, CA), Samuel H. Sternberg (Oakland, CA), Martin Jinek (Oakland, CA), Fuguo Jiang (Oakland, CA), Emine Kaya (Oakland, CA), David Taylor (Oakland, CA), Application Number: 15/108,545).
10. Bellon L. Oligoribonucleotides with 2'-O-(feri-butyldimethylsilyl) groups. Current protocols in nucleic acids chemistry. 2001. S.l. P.3.6.1-3.6.13.
11. Anders, C, Jinek, M. In vitro Enzymology of Cas9. // Methods Enzymol. 2016. Vol. 546. P. 1-20.
12. Shubsda, M. F., Goodisman, J., Dabrowiak, J. C. Quantitation of ethidium-stained closed circular DNA in agarose gels. // Biochem. Biophys. Methods. 1997. Vol. 34. N. LP. 73-79.
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение науки Институт
химической биологии и фундаментальной медицины Сибирского отделения
Российской академии наук (ИХБФМ СО РАН)
<120> Модифицированная направляющая РНК для регулируемой инактивации
системы редактирования генома CRISPR/Cas9
<160> Номер SEQ ID NO
<210> SEQ ID NO: 1
<211> 102
<212> 102-Звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер
на основе 1-(2-нитрофенил)-1,2-этандиола между 43 и 44
рибонуклеозидами от 5'-конца РНК
<213> искусственная последовательность
<400> 1
5'-GGAUAACUCAAUUUGUAAAAAAGUUUUAGAGCUAGAAAUAGCA-PL-AGUU- 47
AAAAUAAGGCUAGUCCGUUAUCAACUUGAAAAAGUGGCACCGAGUCGGUGCUUUU 102
PL – фоторасщепляемый линкер
<110> Федеральное государственное бюджетное учреждение науки Институт
химической биологии и фундаментальной медицины Сибирского отделения
Российской академии наук (ИХБФМ СО РАН)
<120> Модифицированная направляющая РНК для регулируемой инактивации
системы редактирования генома CRISPR/Cas9
<160> Номер SEQ ID NO
<210> SEQ ID NO: 2
<211> 42
<212> 42-Звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер на
основе основе 1-(2-нитрофенил)-1,2-этандиола между 14 и 15
рибонуклеозидами от 5'-конца РНК
<213> искусственная последовательность
<400> 1
5'-GGUGAACCGCAUCG-PL-AGCUGAGUUUUAGAGCUAUGCUGUUUUG 42
PL – фоторасщепляемый линкер
<110> Федеральное государственное бюджетное учреждение науки Институт
химической биологии и фундаментальной медицины Сибирского отделения
Российской академии наук (ИХБФМ СО РАН)
<120> Модифицированная направляющая РНК для регулируемой инактивации
системы редактирования генома CRISPR/Cas9
<160> Номер SEQ ID NO
<210> SEQ ID NO: 3
<211> 42
<212> 42-Звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер
на основе основе 1-(2-нитрофенил)-1,2-этандиола между 14 и 15
рибонуклеозидами от 5'-конца РНК
<213> искусственная последовательность
<400> 1
5'-CAUGCCGAGAGUGA-PL-UCCCGGGUUUUAGAGCUAUGCUGUUUUG
PL – фоторасщепляемый линкер
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА РЕДАКТИРОВАНИЯ ГЕНОМА CRISPR/CAS9 II ТИПА И ЕЕ ПРИМЕНЕНИЕ | 2022 |
|
RU2794774C1 |
| КОМПОЗИЦИИ И СПОСОБЫ С УЧАСТИЕМ НУКЛЕИНОВЫХ КИСЛОТ, НАЦЕЛЕННЫХ НА НУКЛЕИНОВЫЕ КИСЛОТЫ | 2014 |
|
RU2662932C2 |
| РНК-НАПРАВЛЯЕМАЯ ИНЖЕНЕРИЯ ГЕНОМА ЧЕЛОВЕКА | 2013 |
|
RU2699523C2 |
| Система для увеличения эффективности редактирования генома млекопитающего за счет гомологичной репарации | 2022 |
|
RU2808045C1 |
| Система привлечения белка к месту разрыва ДНК для увеличения эффективности редактирования генома млекопитающего | 2022 |
|
RU2808601C1 |
| Средство редактирования генома на основе белка LigD из бактерии Pseudomonas putida и Cas9 комплекса | 2022 |
|
RU2797049C1 |
| НОВЫЙ АКТИВАТОР ТРАНСКРИПЦИИ | 2019 |
|
RU2800921C2 |
| ЭКСПРЕССИРУЮЩИЕ CAS МЫШИНЫЕ ЭМБРИОНАЛЬНЫЕ СТВОЛОВЫЕ КЛЕТКИ И МЫШИ И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2782358C2 |
| Новая компактная нуклеаза CAS9 II типа из Anoxybacillus flavithermus | 2020 |
|
RU2749307C1 |
| РНК-проводники для подавления репликации вируса гепатита B и для элиминации вируса гепатита B из клетки-хозяина | 2017 |
|
RU2652899C1 |



Изобретение относится к области биотехнологии, в частности к модифицированной направляющей РНК для регулируемой инактивации системы редактирования генома CRISPR/Cas9, представляющей собой 42-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер, а также к способу ее получения. Изобретение эффективно для специфичной инактивации системы геномного редактирования CRISPR/Cas9 в определенный момент времени в определенном месте. 2 н. и 6 з.п. ф-лы, 8 ил., 4 пр.
1. Модифицированная направляющая РНК для регулируемой инактивации системы редактирования генома CRISPR/Cas9, представляющая собой 42-звенный олигорибонуклеотид, содержащий фоторасщепляемый линкер, встроенный между определенными рибонуклеозидами от 5'-конца РНК, имеющая нуклеотидную последовательность SEQ ID NO: 2 или SEQ ID NO: 3, соответственно, при этом фоторасщепляемый линкер встроен в область связывания с дцДНК мишенью, между 14-м и 15-м рибонуклеозидами от 5'-конца РНК.
2. Модифицированная направляющая РНК по п. 1, отличающаяся тем, что фоторасщепляемый линкер представляет собой 1-(2-нитрофенил)-1,2-этандиол.
3. Способ получения модифицированной направляющей РНК по п. 1, имеющей нуклеотидную последовательность SEQ ID NO: 2 или SEQ ID NO: 3, соответственно, для регулируемой инактивации системы редактирования генома CRISPR/Cas9, включающий проведение необходимого числа синтетических циклов на автоматическом синтезаторе на твердофазном носителе, каждый из которых состоит из стадий детритилирования, присоединения очередного мономерного звена, кэпирования и окисления межнуклеотидных фосфиттриэфирных связей в фосфотриэфирные, с использованием на стадии присоединения раствора β-цианэтил-фосфитамида 5',2',N-защищенного рибонуклеозида или модифицированного фосфитамида, с последующим удалением концевой 5'-О-диметокситритильной группы, деблокированием гетероциклических оснований и межнуклеозидных фосфатов полимерсвязанной РНК, ее отделением от носителя, удалением 2'-O-трет-бутилдиметилсилильных защитных групп и выделением целевого продукта, отличающийся тем, что стадию присоединения модифицированного фосфитамида для введения фоторасщепляемого линкера проводят в течение 25-35 минут, а в качестве последнего используют раствор 1-(2-циано-N,N-диизопропилфосфитамид)-2-O-4,4'-диметокситритил-1-(2-нитрофенил)-1,2-этандиола в абсолютном ацетонитриле с концентрацией 0,1 моль/л, на стадии кэпирования используют раствор пропионового ангидрида и N-метилимидазола в тетрагидрофуране, а удаление концевой 5'-О-диметокситритильной группы проводят перед деблокированием гетероциклических оснований и межнуклеозидных фосфатов полимерсвязанной РНК.
4. Способ по п. 3, отличающийся тем, что синтез проводят на автоматическом ДНК/РНК синтезаторе ASM-800 (Биоссет, Россия).
5. Способ по п. 3, отличающийся тем, что в качестве твердофазного носителя используют стеклянные частицы с диаметром пор 500  .
.
6. Способ по п. 3, отличающийся тем, что для отделения олигонуклеотида от твердофазного носителя используют 40%-ный водный раствор метиламина.
7. Способ по п. 3, отличающийся тем, что для удаления 2'-O-трет-бутилдиметилсилильных защитных групп используют смесь, содержащую N-метил-2-пирролидинон:триэтиламин:триэтиламинтригидрофторид в объемном соотношении 1,5:0,75:1,0.
8. Способ по п. 3, отличающийся тем, что для выделения модифицированной РНК используют электрофорез в денатурирующем 12%-ном полиакриламидном геле, содержащем акриламид и N,N'-метиленбисакриламид в молярном соотношении 30:0,5, при напряжении 50 В/см.
| WO 2015103153 A1, 09.07.2015 | |||
| WENYUAN ZHOU et al., Spatiotemporal Control of CRISPR/Cas9 Function in Cells and Zebrafish using Light-Activated Guide RNA, Angewandte Chemie International Edition, 11.03.2020, Vol | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| FILIPPOVA J et al., Guide RNA modification as a way to improve CRISPR/Cas9-based genome-editing systems, Biochimie, | |||
Авторы
Даты
2022-01-26—Публикация
2020-08-26—Подача