ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к классу замещенных цианопирролидинов с активностью ингибиторов деубиквитинирующего фермента С-концевой убиквитин-гидролазы 30, также известной как убиквитин-специфическая пептидаза 30 (USP30), их применению, способу их получения и композиции, содержащей указанные ингибиторы. Указанные ингибиторы можно применять в различных областях терапии, включая состояния, при которых имеет место дисфункция митохондрий, злокачественные новообразования и фиброз.
Все процитированные документы включены явным образом в данное описание путем ссылки.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Убиквитин представляет собой небольшой белок, состоящий из 76 аминокислот, имеющий важное значение для регуляции функции белка в клетке. Убиквитинирование и деубиквитинирование представляют собой ферментативные процессы, при которых убиквитин ковалентно связывается или отщепляется от белка-мишени деубиквитинирующими ферментами (DUB), в клетках человека существует приблизительно 100 DUB, которые подразделяют на подсемейства на основе гомологии последовательностей. Семейство USP характеризуется общими кластерами Cys и His, содержащими остатки Cys и His, играющими ключевую роль для их активности DUB. Процессы убиквитинирования и деубиквитинирования задействованы в регуляции многих клеточных функций, включая прохождение клеточного цикла, апоптоз, модификацию рецепторов клеточной поверхности, регуляцию транскрипции ДНК и репарации ДНК. Таким образом, система убиквитина задействована в патогенезе множества патологических процессов, включая воспаление, вирусную инфекцию, нарушение метаболизма, расстройства ЦНС и онкогенез.
Убиквитин является главным регулятором динамических процессов в митохондриях. Митохондрии являются динамическими органеллами, чей биогенез, события слияния и деления регулируются на посттрансляционном уровне через убиквитинирование множества ключевых факторов, таких как митофузины. У человека USP30 представляет собой белок из 517 аминокислот, который обнаруживается во внешней мембране митохондрий (Nakamura et al, 2008, Mol Biol 19:1903-11). Это единственный деубиквитинирующий фермент, несущий сигнал митохондриальной адресации, и показано, что он деубиквитинирует ряд митохондриальных белков. Показано, что USP30 препятствует паркин-опосредованной митофагии и что снижение активности USP30 может компенсировать паркин-опосредованные дефекты митофагии (Bingol et al, 2015, Nature 510:370-5; Gersch et al, 2017, Nat Struct Mol Biol 24(11): 920-930; Cunningham et al, 2015, Nat Cell Biol 17(2): 160-169). Инактивация USP30 может также увеличивать импорт белков в митохондрии, возможно через убиквитинирование белков ТОМ (Jacoupy et al, 2019, Sci Rep 9(1): 11829). Небольшая часть USP30 локализована в пероксисомах, которые образуются путем слияния митохондриальных везикул и везикул эндоплазматического ретикулума, при этом USP30 является возможным антагонистом пути Рех2/пексофагии (Riccio et al, 2019, J Cell Biol 218(3): 798-807). Е3 убиквитин лигаза March5 и деубиквитиназа USP30 ассоциируются с транслоказой и регулируют митохондриальный импорт, при этом March5 препятствует митохондриальному импорту и регулирует деградацию субстратов, a USP30 деубиквитинирует субстраты, облегчая их импорт (Phu et al, 2020, Molecular Cell 77, 1107-1123).
Дисфункцию митохондрий можно определить как пониженное содержание митохондрий (митофагия или митохондриальный биогенез), как понижение митохондриальной активности и окислительного фосфорилирования, а также как изменение образования активных форм кислорода (ROS). Таким образом, митохондриальные дисфункции играют роль в многочисленных процессах старения и патологических процессах.
Например, болезнь Паркинсона затрагивает приблизительно 10 миллионов людей во всем мире (фонд Паркинсона) и характеризуется потерей дофаминэргических нейронов в черной субстанции. Точные механизмы, лежащие в основе БП, не ясны; однако, митохондриальная дисфункция все больше признается ключевой детерминантой уязвимости дофаминергических нейронов при БП и является признаком как наследственного, так и спорадического заболевания, а также паркинсонизма, индуцированного токсинами. Паркин является одним из нескольких белков, которые задействованы при раннем начале БП. Тогда как большинство случаев БП связаны с дефектами альфа-синуклеина, 10% случаев болезни Паркинсона связаны со специфическими генетическими дефектами, одним из которых является убиквитин-Е3-лигаза паркин. Паркин и протеинкиназа PINK1 (предполагаемая киназа 1, индуцированная гомологом фосфатазы и тензина (PTEN)) совместно убиквитинируют белки митохондриальной мембраны поврежденных митохондрий, результатом чего является митофагия. Нарушение регуляции митофагии приводит к усилению окислительного стресса, что описано как характерная черта БП. Таким образом, ингибирование USP30 может быть возможной стратегией лечения БП. Например, терапевтическая компенсация у пациентов с БП с мутациями паркина, ведущими к пониженной активности, может достигаться путем ингибирования USP30.
Сообщалось, что истощение USP30 усиливает клиренс митохондрий посредством митофагии, а также усиливает паркин-индуцированную гибель клеток. Также показано, что USP30 регулирует ВАХ/BAK-зависимый апоптоз независимо от сверхэкспрессии паркина. Истощение USP30 делает злокачественные клетки более чувствительными к миметикам ВН-3, таким как АВТ-737, не требуя сверхэкспрессии паркина. Таким образом, показана анти-апоптотическая роль USP30, и, следовательно, USP30 является потенциальной мишенью противоопухолевой терапии.
Система убиквитин-протеасома привлекла интерес в качестве мишени для лечения злокачественных новообразований после одобрения ингибитора протеасом бортезомиба (Velcade®) для лечения множественной миеломы. Широкое применение бортезомиба ограничивается связанными с ним токсичностью и лекарственной устойчивостью. Однако прогнозируется, что терапевтические стратегии, направленные на специфические аспекты убиквитин-протеасомного пути, расположенные выше протеасомы, такие как DUB, будут переноситься легче (Bedford et al, 2011, Nature Rev 10:29-46).
Фиброзирующие заболевания, включая фиброз почек, печени и легких, являются ведущей причиной заболеваемости и смертности и могут негативно сказываться на всех тканях и системах органов. Фиброз считается результатом острого или хронического стресса ткани или органа, характеризуется отложением внеклеточного матрикса, снижением проходимости и нарушением функции сосудистых/дыхательных путей/канальцев/протоков, в итоге приводя к органной недостаточности. Развитию многих сопровождающихся фиброзом состояний способствуют образ жизни или факторы окружающей среды; однако, часть сопровождающихся фиброзом состояний может быть вызвана генетическими факторами или может быть идиопатической (т.е. не иметь известной причины). Некоторые фиброзирующие заболевания, такие как идиопатический легочный фиброз (ИЛФ) можно лечить неспецифическим ингибитором киназ (нинтеданиб) или лекарственными средствами, механизм действия которых еще недостаточно хорошо охарактеризован (пирфенидон). Другие виды лечения фиброза органов, такого как фиброз почек или печени, облегчают давление на сам орган (например, бета-блокаторы при циррозе, блокаторы ангиотензинового рецептора при хронических заболеваниях почек). Внимание к факторам образа жизни, таким как контролирование глюкозы и диета, также могут влиять на течение и тяжесть заболевания.
Митохондриальная дисфункция задействована в ряде фиброзирующих заболеваний, при этом окислительный стресс вследствие дисфункции является ключевым патогенным медиатором, наряду с пониженным образованием АТФ. В доклинических моделях разрушение пути митофагии (за счет мутации или нокаута паркина или PINK1) усугубляло фиброз легких и фиброз почек, что свидетельствовало об усилении окислительного стресса.
Kurita et al, 2017, Respiratory Research 18:114 описывают накопление профибротических миофибробластов как ключевой процесс при фибротическом ремоделировании при ИЛФ. Недавние исследования показали участие аутофагии/митофагии, части лизосомальных механизмов деградации, в патогенезе ИЛФ, и что митофагия задействована в дифференцировке миофибробластов, регулируя активацию рецептора фактора роста тромбоцитов (PDGFR), опосредованную митохондриальными активными формами кислорода (ROS). Результаты, полученные Kurita, позволяют предположить, что пирфенидон индуцирует PARK2-опосредованную митофагию, а также ингибирует развитие фиброза легких в условиях недостаточной митофагии, что может по меньшей мере частично объяснять антифибротические механизмы лечения ИЛФ.
Williams et al, 2015, Pharmacol Res. December; 102: 264-269, обсуждает роль PINK1-паркин-опосредованной аутофагии в защите против повреждения печени, вызванного алкоголем и ацетаминофеном, за счет удаления поврежденных митохондрий посредством митофагии. Предполагается, что фармакологическая стабилизация USP8 или инактивация USP15 и USP30 могут быть потенциальными терапевтическими мишенями для усиления паркин-индуцированной митофагии, и в свою очередь защищать от повреждения печени, вызванного лекарствами. Однако отмечается, что DUB регулируются как на транскрипционном, так и на посттрансляционном уровне, что может осложнять разработку лекарств для направленного воздействия на эти специфические ферменты и, кроме того, показано, что фосфорилированный убиквитин является устойчивым к DUB. Авторы приходят к заключению, что повышение стабилизации PINK1 или киназной активности может оказаться более эффективной мишенью, чем ингибирование DUB.
Williams et al, 2015, Biomolecules 5, 2619-2642, and Williams et al, 2015, Am J Physiol Gastrointest Liver Physiol 309: G324-G340, делают обзор механизмов, участвующих в регуляции митохондриального гомеостаза в печени и как эти механизмы могут защищать от алкоголь-индуцированного заболевания печени.
Luciani et al, 2020, Nat. Commun. 11, 970, сообщают, что дерегуляция митохондриальной сети в окончательно дифференцированных клетках вносит вклад в широкий спектр расстройств, включая метил мал о новую ацидемию (ММА). ММА является одним из самых распространенных наследственных метаболических расстройств вследствие дефицита митохондриальной метилмалонил-кофермент А-мутазы (MMUT). Дефицит MMUT вызывает метаболические и митохондриальные нарушения, которые усугубляются аномалиями PINK1/паркин-опосредованной митофагии, вызывая накопление дисфункциональных митохондрий, которые запускают эпителиальный стресс и в итоге повреждение клеток. Предполагается связь между первичным дефицитом MMUT, повреждением митохондрий, дисфункциональной митофагией и эпителиальным стрессом, и описываются возможные перспективы терапии ММА.
Kluge et al, Bioorganic & Medicinal Chemistry Letters, 2018, 28 2655-2659, сообщают, что селективные ингибиторы USP30 усиливают митофагию.
Ряд производных циано-замещенных гетероциклических соединений описаны как ингибиторы деубиквитинирующих ферментов в заявках РСТ WO 2016/046530 (US 15/513125, US 15/894025, US 16/448066), WO 2016/156816 (US 15/558632, US 16/297937, US 16/419558, US 16/419747, US 16/788446), WO 2017/009650 (US 15/738900), WO 2017/093718 (US 15/776149), WO 2017/103614 (US 15/781615), WO 2017/149313 (US 16/078518), WO 2017/109488 (US 16/060299), WO 2017/141036 (US 16/070936), WO 2017/163078 (US 16/087515), WO 2017/158381 (US 16/080229), WO 2017/158388 (US 16/080506), WO 2018/065768 (US 16/336685), WO 2018/060742 (US 16/336202), WO 2018/060689 (US 16/334836), WO 2018/060691 (US 16/336363), WO 2018/220355 (US 16/615040) и WO 2018/234755 (US 16/615709), каждая из которых включена в данное описание путем ссылки. В заявке РСТ WO 2019/171042, включенной в данное описание путем ссылки, изложено применение замещенных цианопирролидинов в качестве ингибиторов USP30 для лечения фиброзирующих заболеваний.
Falgueyret et al, 2001, J.Med.Chem. 44, 94-104, и заявка РСТ WO 01/77073 относятся к цианопирролидинам как ингибиторам катепсинов K и L с возможным применением в лечении остеопороза и других состояний, связанных с резорбцией кости. Заявка РСТ WO 2015/179190 относится к ингибиторам кислой амидазы, гидролизующей N-ацилэтаноламин с возможным применением в лечении язвенного колита и болезни Крона. Заявка РСТ WO 2013/030218 относится к соединениям хиназолин-4-она как ингибиторам убиквитин-специфических протеаз, таких как USP7, с возможным применением в лечении злокачественных новообразований, нейродегенеративных заболеваний, воспалительных расстройств и вирусных инфекций. Заявки РСТ WO 2015/017502 и WO 2016/019237 относятся к ингибиторам тирозинкиназы Брутона с возможным применением в лечении таких заболеваний, как аутоиммунные заболевания, воспалительные заболевания и злокачественные новообразования. Заявки РСТ WO 2009/026197, WO 2009/129365, WO 2009/129370 и WO 2009/129371 относятся к цианопирролидинам как ингибиторам катепсина С с возможным применением в лечении ХОБЛ. Заявка на патент США 2008/0300268 относится к полиароматическим соединениям как ингибиторам тирозинкиназного рецептора PDGFR. Заявки РСТ WO 2019/222468, WO 2019/071073, WO 2020/036940 и WO 2020/072964, а также документ Rusilowicz-Jones et al, 2020, bioRxiv 2020.04.16.044206 относятся к цианамид-содержащим соединениям как ингибиторам USP30.
Заявка РСТ WO 2015/183987 относится к фармацевтическим композициям, содержащим ингибиторы деубиквитиназы и человеческому сывороточному альбумину, в способах лечения злокачественных новообразований, фиброза, аутоиммунного заболевания или состояния и воспалительного заболевания или состояния, нейродегенеративного заболевания или состояния или инфекции. Отмечается, что деубиквитиназы, включающие UCHL5/UCH37, USP4, USP9X, USP11 и USP15, задействованы в регуляции сигнального пути TGF-бета, нарушение которого дает начало нейродегенеративным и фиброзирующим заболеваниям, аутоиммунным нарушениям и злокачественным новообразованиям.
Заявка РСТ WO 2006/067165 относится к способу лечения фиброзирующких заболеваний с применением ингибиторов индолинонкиназы. Заявка РСТ WO 2007/119214 относится к лечению ранней стадии фиброза легких с применением антагониста рецептора эндотелина. Заявка РСТ WO 2012/170290 относится к способу лечения фиброзирующих заболеваний с применением тетрагидроканнабиноловых (ТНС) кислот. Заявка РСТ WO 2018/213150 относится к сульфонамидным ингибиторам USP30 с возможным применением в лечении состояний, при которых имеют место дефекты митохондрий. Публикация Larson-Casey et al, 2016, Immunity 44, 582-596, касается митофагии, опосредованной Aktl-киназой макрофагов, устойчивости к апоптозу и фиброзу легких. В обзоре Tang et al, 2015, Kidney Diseases 1, 71-79, рассматривается потенциальная роль митофагии в патофизиологии почек.
Существует потребность в безопасных альтернативных и/или улучшенных способах и композициях для лечения или профилактики состояний, при которых имеет место дисфункция митохондрий, злокачественных новообразований и фиброза, и различных симптомов и состояний, ассоциированных с ними. Не желая ограничиваться какой-либо конкретной теорией или механизмом, полагают, что соединения по данному изобретению действуют, ингибируя фермент USP30, что в свою очередь приводит к усилению паркин-индуцированной митофагии.
Острое повреждение почек (ОПП) определяют как резкое снижение функции почек, развивающееся за 7 дней или менее, тяжесть повреждения устанавливают по повышению креатинина сыворотки (SCr) и снижению диуреза, как описано в рекомендациях Международного консорциума по улучшению глобальных результатов лечения болезней почек (KDIGO). ОПП ежегодно развивается у 13,3 миллионов людей, из которых 85% живут в развивающихся странах, и полагают, что его вклад составляет приблизительно 1,7 миллионов смертей ежегодно (Mehta et al, 2015, Lancet 385(9987): 2616-2643). ОПП более чем вероятно приводит к постоянному повреждению почек (т.е. хронической болезни почек; ХБП) и может также приводить к повреждению других органов. ОПП является важной проблемой общественного здравоохранения, особенно с учетом абсолютного числа пациентов, у которых развивается инцидентная ХБП, прогрессирующая ХБП, терминальная почечная недостаточность и сердечнососудистые явления.
ОПП и ХБП рассматриваются как континуум в едином спектре заболеваний (Chawla et al, 2017, Nat Rev Nephrol 13(4): 241-257). Пациенты, проходящие аорто-коронарное шунтирование (АКШ), имеют высокий риск повреждения почек. В медицине существует очевидная неудовлетворенная потребность в разработке медицинских продуктов для лечения и/или профилактики ОПП.
Почка является местом с высокими метаболическими потребностями, с высокой степенью митофагии, продемонстрированной in vivo (McWilliams et al, 2018, Cell Metab 27(2): 439-449 e435). Эпителиальные клетки проксимальных почечных канальцев (RPTEC), тип клеток, требующий значительного количества АТФ для осуществления обмена растворов/ионов, богаты митохондриями и представляют собой первичные эффекторные клетки почек при остром поражении почек (ОПП). Митохондриальную дисфункцию связывали с механизмами ОПП/ХБП, что в обоих случаях подтверждалось множеством данных, полученных в доклинических моделях ОПП и ХБП, а также данными, демонстрирующими аномальные фенотипы митохондрий в биопсиях пациентов (Emma et al, 2016, Nat Rev Nephrol 12(5): 267-280; Eirin et al, 2017, Handb Exp Pharmacol 240: 229-250). Кроме того, первичное митохондриальное заболевание часто манифестирует почечными симптомами, такими как фокально-сегментарный гломерулосклероз (Kawakami et al, 2015, J Am Soc Nephrol 26(5): 1040-1052) у пациентов с митохондриальной энцефаломиопатией, лактоцидозом и приступами, похожими на инсульт (MELAS)/наследуемыми по материнской линии диабетом и глухотой (MIDD), а также первичные канальцевые патологии у пациентов с дефицитом кофермента Q. Мутации митохондриальной ДНК могут вызывать наследуемую по материнской линии тубулоинтерстициальную болезнь (Connor et al, 2017, PLoS Genet 13(3): e1006620).
Что касается контролирования качества митохондрий при повреждении почек, Tang et al, 2018 (Autophagy 14(5): 880-897) продемонстрировали, что повреждение почек усиливалось после ишемического ОПП как у мышей с нокаутом PINK1, так и с нокаутом PARK2, и предположили, что PINK1/PARKIN-опосредованная митофагия играет защитную роль после ишемически-реперфузионного повреждения почек. Кроме того, паркин/PINK1 митофагия защищает от повреждения почек, индуцированного цисплатином (Wang et al, 2018, Cell Death Dis 9(11): 1113). Существующие модели ХБП для исследования митофагии ограничены, данные, подтверждающие контролирование качества митохондрий при фиброзе получали в исследованиях таких состояний с фиброзом легких, как ХОБЛ и идиопатический фиброз легких. У животных с нокаутом паркина наблюдается отягощенный фиброз легких в ответ на блеомицин (Kobayashi et al, 2016, J Immunol, 197:504-516). Аналогично, в клетках эпителия дыхательных путей у животных с нокаутом паркина наблюдается усиленный фиброз и старение в ответ на сигаретный дым (Araya et al, 2019, Autophagy 15(3): 510-526).
Существуют доклинические модели для изучения потенциальных новых терапевтических средств, позволяющие моделировать патологический фиброз (например, отложение коллагена), соответствующий состоянию человека. Доклинические модели могут быть опосредованы токсинами (например, блеомицин для фиброза легких и кожи), хирургическим вмешательством (например, модель повреждения ишемией/реперфузией и модель односторонней обструкции мочеточника для острого тубулоинтерстициального фиброза) и генетическими (например, мыши (db/db) с диабетом для диабетической нефропатии). Например, оба примера (нинтеданиб и пирфенидон), которые давали ранее для лечения ИЛФ, демонстрируют эффективность на модели фиброза легких, индуцированного блеомицином.
Соответственно, существует потребность в соединениях, которые являются ингибиторами USP30, для лечения или профилактики состояний, при которых показано ингибирование USP30. В частности, существует потребность в ингибиторах USP30, которые обладают подходящими и/или улучшенными свойствами для максимизации эффективности в отношении целевого заболевания.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Данное изобретение относится к соединениям формулы (I)
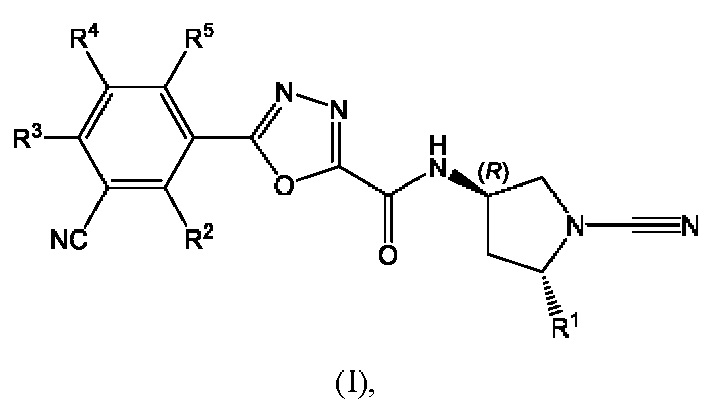
их таутомерам или фармацевтически приемлемым солям указанных соединений или таутомеров, где:
R1 выбран из (С1-С4)алкила, (С1-С4)фторалкила и CH2OCH3;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода, фтора, (С1-С4)алкокси и циклопропокси.
Данное изобретение также относится к применению соединений формулы (I), в частности, к лечению состояний, при которых имеет место дисфункция митохондрий, злокачественных новообразований и фиброза, а также к способам их получения и к фармацевтическим композициям, содержащим указанные соединения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение относится к ингибиторам, обладающим подходящими или улучшенными свойствами для максимизации эффективности в отношении целевого заболевания. Такие свойства включают, например, активность, селективность, физико-химические свойства, свойства всасывания, распределения, метаболизма и выведения (ADME), включая фармакокинетический (ФК) профиль и профиль безопасности.
Обычно желательно максимизировать активность лекарственных молекул в отношении целевого фермента в соответствующих исследованиях для снижения эффективной дозы, которую будут вводить пациентам. Аффинность соединений по изобретению в отношении USP30 можно исследовать in vitro с применением биохимического метода поляризации флуоресценции (ПФ), описанного в данном документе.
USP30 представляет собой трансмембранный белок, расположенный во внешней мембране митохондрий, представляющих собой внутриклеточные органеллы, продуцирующие энергию. Таким образом, способность продемонстрировать клеточную активность in vitro предпочтительна, и является одним из нескольких компонентов, которые могут указывать на большую способность задействовать мишень в физиологических условиях, т.е. когда соединение, являющееся ингибитором USP30, способно проникать в клетки. Описанный здесь анализ USP30 в клетках методом вестерн блот (WB) направлен на исследование активности соединений в отношении USP30 в клетках с применением для отслеживания активности USP30 сенсора, необратимо ингибирующего ферментативную активность. Аналогично исследованию клеток методом вестерн блот, можно выполнять оценку связывания с мишенью (ех vivo) в образцах ткани мозга или почки животных, получавших соединение, с применением описанного здесь анализа.
Чтобы дополнить знания о связывании мишеней информацией о фармакодинамике последующих процессов можно оценивать убиквитинирование ТОМ20 (белка внешней мембраны митохондрий).
В целом, важно, чтобы лекарство было как можно более селективным в отношении желаемого фермента-мишени; дополнительные активности являются причиной возможных побочных эффектов. Точная физиологическая роль многих DUB еще полностью не изучена, однако, независимо от того, какую роль могут или не могут играть эти DUB, твердым принципом в медицинской химии является обеспечение селективности любого лекарственного средства по сравнению с родственными по механизму действия мишенями с неизвестной физиологической функцией. Репрезентативными примерами ферментов DUB, на которых можно проводить скрининг соединений по данному изобретению, являются UCHL1, UCHL3, UCHL5, YOD1, SENP2, SENP6, TRABID, ВАР1, сезанн, MINDY2/FAM63B, OTU1, OTUD3, OTUD5, OTUD6A, OTUD6B, OTUB1/UBCH5B, OTUB2, CYLD, VCPIP, AMSH-LP, JOSD1, JOSD2, USP1/UAF1, USP2, USP4, USP5, USP6, USP7, USP8, USP9x, USP10, USP11, USP12/UAF1, USP13, USP14, USP15, USP16, USP19, USP20, USP21, USP22, USP24, USP25, USP28, USP32, USP34, USP35, USP36, USP45, USP46/UAF1, USP47 и USP48. Предпочтительно, соединения по изобретению обладают хорошей селективностью в отношении USP30 по сравнению с одним или более из этих ферментов DUB.
Помимо селективности по сравнению с другими ферментами DUB важно, чтобы лекарственное средство обладало низкой аффинностью к другим мишеням, и можно было бы выполнять фармакологическое профилирование на панелях мишеней для оценки потенциала и минимизации возможных нецелевых эффектов. Примерами мишеней, на которых можно проводить скрининг соединений по данному изобретению, являются мишени, входящие в состав панели промышленных стандартов Eurofins-Cerep SafetyScreen44, включающей 44 мишени в качестве репрезентативной выборки рецепторов GPCR, транспортеров, ионных каналов, ядерных рецепторов, а также киназ и ферментов, не являющихся киназами. Предпочтительно, соединения по изобретению обладают несущественной аффинностью в отношении мишеней из данной скрининговой панели. Дополнительными примерами мишеней, на которых можно проводить скрининг соединений по данному изобретению, являются киназы из киназной панели профилирования Thermo Fisher SelectScreen, включающей 39 мишеней в качестве репрезентативной выборки ферментов-киназ. Предпочтительно, соединения по изобретению обладают несущественной аффинностью в отношении мишеней из данной скрининговой панели. Кроме того, примерами конкретного класса ферментов, на которых можно проводить скрининг соединений по данному изобретению, являются катепсины (например, катепсины А, В, С, Н, K, L, S, V и Z). Предпочтительно, соединения по изобретению обладают хорошей селективностью в отношении USP30 по сравнению с одним или более из этих ферментов.
Также существует потребность в соединениях, которые обладают предпочтительными фармакокинетическими свойствами, благодаря которым они подходят для перорального введения. Перорально вводимое лекарственное средство должно обладать хорошей биодоступностью; это способность легко проходить через желудочно-кишечный тракт (ЖКТ) и не подвергаться интенсивному метаболизму по мере прохождения из ЖКТ в системный кровоток. Скорость метаболизма также важна для определения времени удерживания лекарственного средства в организме после поступления лекарственного средства в системный кровоток.
Таким образом, очевидно, что предпочтительные молекулы лекарственного средства должны обладать способностью легко проходить через ЖКТ и лишь медленно подвергаться метаболизму в организме. Тест на клетках Сасо-2 является общепринятой моделью для прогнозирования способности заданной молекулы проходить через ЖКТ. По большей части метаболизм молекул лекарственных средств протекает в печени, и исследования in vitro с применением цельных клеток гепатоцитов (животных или человека) являются общепринятыми способами измерения подверженности заданной молекулы к метаболизму в печени. Такие исследования нацелены на предсказание клиренса in vivo по значениям клиренса, рассчитанного для гепатоцитов.
Соединения, хорошо проникающие в Сасо-2, и стабильные в гепатоцитах согласно прогнозам, должны обладать хорошей пероральной биодоступностью (хорошим всасыванием в ЖКТ и минимальной экстракцией соединения по мере прохождения через печень) и длительным временем удерживания в организме, что является достаточным для того, чтобы лекарство было эффективным.
Растворимость соединения является важным фактором достижения желаемой концентрации лекарственного средства в системном кровотоке для предполагаемого фармакологического ответа. Низкая растворимость в воде является проблемой, с которой встречаются при разработке препаратов новых химических соединений, и для всасывания лекарственное средство должно находиться в месте всасывания в форме раствора. Кинетику растворимости соединения можно измерять с помощью турбидиметрического анализа растворимости, результаты которого можно также использовать вместе с результатами проницаемости Сасо-2 для прогнозирования дозозависимого всасывания в кишечнике человека.
Другие параметры, характеризующие профиль воздействия соединения, которые можно измерять с применением стандартных методов, включают, например, стабильность в плазме (измерение времени полужизни), значения AUC в крови, Cmax, Cmin и Tmax.
Лечение расстройств ЦНС, включая болезнь Альцгеймера, болезнь Паркинсона и другие расстройства, описанные в данном документе, требует, чтобы молекулы лекарственных средств достигали головного мозга, что требует должного прохождения через гематоэнцефалический барьер. Таким образом, существует потребность в ингибиторах USP30, которые обладают свойствами эффективного прохождения через гематоэнцефалический барьер и обеспечивают подходящее время удерживания в головном мозге, чтобы быть эффективными. Вероятность того, что соединение может пересекать гематоэнцефалический барьер, можно оценивать в in vitro анализе проницаемости с применением монослоя клеток MDR1-MDCK (клетки Мадин-Дарби почек собак, трансфицированные MDR-1, сверхэкспрессирующие эффлюксный переносчик человеческий гликопротеин-Р). Кроме того, воздействие можно также измерять непосредственно в головном мозге и плазме с использованием моделей на животных in vivo.
Также существует потребность в соединениях, которые имеют благоприятный профиль безопасности, который можно измерять различными стандартными способами in vitro и in vivo. Обратный скрининг на клеточную цитотоксичность может использоваться для оценки антипролиферативного/цитотоксического эффекта на конкретной линии клеток (например, НСТ116) путем флуориметрического определения превращения резазурина (аламаровый синий) в резофурин в ответ на митохондриальную активность.
Можно также проводить токсикологические исследования и исследования безопасности для выявления потенциальных органов-мишеней побочных эффектов и определения терапевтического индекса для выбора исходных начальных доз в клинических исследованиях. Согласно нормативным требованиям, как правило, необходимо проводить исследования по меньшей мере на двух видах лабораторных животных, один из которых относится к грызунам (крыса или мышь), а другой не относится (кролик, собака, примат, не являющийся человеком, или другие подходящие виды).
Для оценки мутагенных свойств соединений по изобретению можно использовать анализ обратных мутаций у бактерий (тест Эймса), обычно с применением штамма бактерий Salmonella typhimurium, имеющего мутацию в генах, отвечающих за биосинтез аминокислоты гистидина.
Для определения, является ли соединение генотоксичным, может применяться микроядерный тест, направленный на выявление микроядер. Микроядра могут содержать фрагменты хромосом, образованные при разрушении ДНК (кластогены) или целые хромосомы, образованные путем разрушения митотического аппарата (анеугенез).
Анализ hERG (ген специфических калиевых каналов сердца) Predictor дает ценную информацию о возможном связывании исследуемых соединений с калиевым каналом и возможным удлинением QT на электрокардиограмме. Ингибирование тока калиевых каналов hERG вызывает удлинение интервала QT, приводящее к желудочковой тахикардии, которая может стать фатальной (пируэтная тахикардия). Как правило, данные исследований могут быть получены на автоматизированной платформе локальной фиксации потенциала.
Таким образом, данное изобретение относится к ингибиторам USP30, обладающим подходящими и/или улучшенными свойствами для максимизации эффективности в отношении целевого заболевания. Такие свойства включают, например, активность, селективность, физико-химические свойства, свойства всасывания, распределения, метаболизма и выведения (ADME), включая фармакокинетический (ФК) профиль и профиль безопасности.
Обнаружили, что соединения по данному изобретению демонстрируют одно или более указанных выше свойств, которые являются важными и неожиданными. Например, все соединения по Примерам данного изобретения обладают высокой активностью в отношении USP30, по результатам биохимического анализа, описанного в данном документе. Все соединения по Примерам данного изобретения обладают существенно большей избирательностью в отношении USP30, по сравнению с другими DUB и катепсинами.
Важные и неожиданные свойства соединений по данному изобретению делают их особенно подходящими для применения в лечении и/или профилактике заболеваний, связанных с активностью UP30.
Согласно первому аспекту данного изобретения предложено соединение формулы (I):
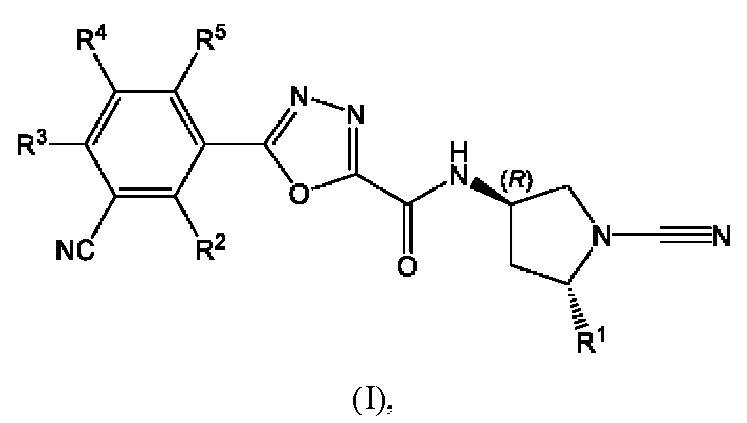
его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера, где:
R1 выбран из (С1-С4)алкила, (С1-С4)фторалкила и СН2ОСН3;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода, фтора, (С1-С4)алкокси и циклопропокси.
Соединение формулы (I) существует в виде единственного стереоизомера, абсолютная стереохимия которого показана.
Алкильные или алкокси группы могут быть линейными или разветвленными и содержать от 1 до 4 атомов углерода. Примеры алкила включают метил, этил, н-пропил, изопропил, н-бутил, изобутил и втор-бутил. Примеры алкокси включают метокси, этокси, н-пропокси, изопропокси и трет-бутокси.
Фторалкильные группы могут содержать один или более заместителей в виде атомов фтора. Примерами являются фторметил, дифторметил и трифторметил.
Если не указано иное, термин замещенный означает замещенный одной или более чем одной определенной группой. В случае, когда группы могут быть выбраны из более чем одной альтернативы, выбранные группы могут быть одинаковыми или различными. Термин «независимо» означает, что, когда из более чем одного возможного заместителя выбран более чем один заместитель, указанные заместители могут быть одинаковыми или различными.
Предпочтительные воплощения соединения формулы (I) определены ниже.
Предпочтительно, R1 выбран из метила, CH2F, CHF2, CF3 и СН2ОСН3.
Более предпочтительно, R1 выбран из метила, CH2F и СН2ОСН3.
Наиболее предпочтительно, R1 представляет собой метил.
Предпочтительно, R2 представляет собой водород.
Предпочтительно, R3 представляет собой водород.
Предпочтительно, R4 представляет собой водород.
Предпочтительно, R5 выбран из водорода, фтора, метокси и циклопропокси.
Более предпочтительно, R5 выбран из водорода и метокси.
Наиболее предпочтительно, R5 представляет собой водород.
Согласно одному из предпочтительных воплощений изобретения:
R1 представляет собой метил;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода и метокси.
Согласно другому предпочтительному воплощению изобретения:
R1 представляет собой CH2F;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода и метокси.
Согласно другому предпочтительному воплощению изобретения:
R1 представляет собой CH2OCH3;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода и метокси.
Предпочтительные соединения формулы (I) по данному изобретению выбраны из:
N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
N-((3R,5S)-1-циано-5-(фторметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
5-(5-циано-2-метоксифенил)-N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида; и
5-(5-циано-2-метоксифенил)-N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида;
их таутомера или фармацевтически приемлемой соли указанного соединения или таутомера.
Наиболее предпочтительным соединением формулы (I) по данному изобретению является:
N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид, его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера.
Фармацевтически приемлемые соли соединений формулы (I) включают соли присоединения кислоты и основные соли (включая ди-соли).
Подходящие соли присоединения кислоты образуются из кислот, образующих нетоксичные соли. Примеры включают соли ацетат, аспартат, бензоат, бесилат, бикарбонат/карбонат, бисульфат, камсилат, цитрат, эдисилат, эсилат, фумарат, глюцептат, глюконат, глюкуронат, гибензат, гидрохлорид/хлорид, гидробромид/бромид, гидроиодид/иодид, гидрофосфат, изетионат, D- и L-лактат, малат, малеат, малонат, мезилат, метилсульфат, 2-напсилат, никотинат, нитрат, оротат, пальмат, фосфат, сахарат, стеарат, сукцинат, сульфат, D- и L-тартрат и тозилат.
Подходящие основные соли образуются из оснований, образующих нетоксичные соли. Примеры включают соли алюминия, аммония, аргинина, бензатина, кальция, холина, диэтиламина, диоламина, глицина, лизина, магния, меглумина, оламина, калия, натрия, трометамина и цинка.
Подходящие соли описаны в обзоре Stahl and Wermuth, Handbook of Pharmaceutical Salts: Properties, Selection, and Use, Wiley-VCH, Weinheim, Germany (2002).
Фармацевтически приемлемую соль соединения формулы (I) можно легко получить путем смешивания растворов соединения формулы (I) с нужной кислотой или основанием, в зависимости от конкретного случая. Соль может осаждаться из раствора и может быть собрана фильтрованием или может быть выделена путем выпаривания растворителя.
Фармацевтически приемлемые сольваты в соответствии с изобретением включают гидраты и сольваты, где растворитель кристаллизации может быть изотопно замещенным, например, D2O, ацетон-d6, DMSO-d6.
Также в объем изобретения входят клатраты, комплексы включения лекарство-хозяин, где в отличие от вышеупомянутых сольватов, лекарство и хозяин находятся в нестехиометрических количествах. Такие комплексы рассмотрены в обзоре J. Pharm Sci, 64 (8), 1269-1288 by Haleblian (August 1975).
Здесь и далее все упоминания соединений формулы (I) включают упоминание их солей и сольватов, а также клатратов соединений формулы (I) и их солей.
Изобретение включает все полиморфы соединений формулы (I), как определено ранее.
Также в объем изобретения входят так называемые «пролекарства» соединений формулы (I). Таким образом, некоторые производные соединений формулы (I) которые сами по себе имеют незначительную фармакологическую активность или не имеют ее, подвергнувшись метаболизму после поступления в организм или на организм, могут давать начало соединениям формулы (I), обладающим желаемой активностью. Такие производные обозначаются «пролекарствами».
Пролекарства по изобретению могут, например, образовываться путем замещения соответствующих функциональных групп, присутствующих в соединениях формулы (I) определенными группами, известными специалистам в области техники как «про-группы», как описано, например, в документе "Design of Prodrugs" by H Bundgaard (Elsevier, 1985). Наконец, некоторые соединения формулы (I) могут сами действовать как пролекарства других соединений формулы (I).
Некоторые производные соединений формулы (I), которые содержат атом азота, могут также образовывать соответствующий N-оксид, и такие соединения также входят в объем данного изобретения.
В объем данного изобретения входят все таутомерные формы соединений формулы (I).
Стандартные методики получения/выделения отдельных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного) с применением, например, хиральной высокопроизводительной жидкостной хроматографии (HPLC). В альтернативном варианте рацемат (или рацемический предшественник) может вступить в реакцию с подходящим оптически активным соединением, например, спиртом или, в случае, когда соединение формулы (I) содержит кислотную или основную группу, основанием или кислотой, такими как 1-фенилэтиламин или винная кислота. Полученная диастереомерная смесь может быть разделена при помощи хроматографии и/или фракционной кристаллизации, и один или оба диастереоизомера конвертируются в соответствующий(е) чистый(е) энантиомер(ы) способами, хорошо известными специалистам в области техники. Хиральные соединения по изобретению (и их хиральные предшественники) могут быть получены в энантиомерно-обогащенной форме с применением хроматографии, как правило, HPLC, на асимметричной смоле с подвижной фазой, состоящей из углеводорода, обычно гептана или гексана, содержащего от 0 до 50% по объему изопропанола, обычно от 2% до 20%, и от 0 до 5% по объему алкиламина, обычно 0,1% диэтиламина. Концентрация элюата позволяет получить обогащенную смесь. Данное изобретение включает все кристаллические формы соединений формулы (I), включая их рацематы и рацемические смеси (конгломераты). Конгломераты стереоизомеров можно разделять стандартными способами, известными в области техники, см., например, "Stereochemistry of Organic Compounds" by E.L. Eliel and S.H. Wilen (Wiley, New York, 1994).
Соединения формулы (I) содержат два хиральных центра в атомах углерода пирролидинового кольца, которые замещены R1 и амидом, и указанные стереоцентры могут существовать в (R) или (S) конфигурации. Обозначение абсолютной конфигурации стереоизомеров (R) и (S) в соответствие с номенклатурой IUPAC определяется природой заместителей и применением правила последовательности. Таким образом, соединения формулы (I) могут существовать в четырех стереоизомерных формах.
Соединения формулы (I) по данному изобретению существуют в виде единственного стереоизомера. Атом углерода пирролидина заместителя амида существует в виде (R)-стереоцентра, тогда как обозначение атома углерода пирролидина группы R1 зависит от природы заместителя. Соединение формулы (I) выделено в виде единственного стереоизомера и может существовать в стереоизомерном избытке по меньшей мере 60%, предпочтительно, по меньшей мере 80%, более предпочтительно, по меньшей мере 90%, более предпочтительно, по меньшей мере 95%, например, 96%, 97%, 98%, 99% или 100%.
Дополнительные хиральные центры могут существовать в соединениях формулы (I) в самом заместителе R1. В объем данного изобретения входят все стереоизомерные формы соединений формулы (I).
Данное изобретение также охватывает все фармацевтически приемлемые изотопные варианты соединения формулы (I). Изотопный вариант определяется как вариант, в котором по меньшей мере один атом замещен атомом, имеющим такое же атомное число, но его атомная масса отличается от атомной массы, обычно встречающейся в природе.
Примеры изотопов, подходящих для включения в соединения по изобретению, включают изотопы водорода, такие как 2Н и 3Н, углерода, такие как 13С и 14С, азота, такие как 15N, кислорода, такие как 17O и 18O, фосфора, такие как 32Р, серы, такие как 35S, фтора, такие как 18F, и хлора, такие как 36CI.
Замещение соединений по изобретению изотопами, такими как дейтерий, может обеспечивать некоторые терапевтические преимущества вследствие большей метаболической стабильности, например, такие как улучшенное время полужизни in vivo или потребность в меньших дозировках, и поэтому может быть предпочтительным в некоторых обстоятельствах.
Некоторые изотопные варианты соединений формулы (I), например, такие, в которые включены радиоактивные изотопы, могут найти применение в исследованиях распределения лекарства и/или субстрата в тканях. Радиоактивные изотопы трития и 14С особенно полезны для этой задачи в виду легкости их включения и существующих способов детектирования.
Изотопные варианты соединений формулы (I) обычно могут быть получены согласно стандартным методикам, известным специалистам в области техники, или способами, аналогичными тем, которые описаны в прилагающихся Примерах с использованием соответствующих изотопных вариаций подходящих реагентов.
Соединения формулы (I) являются ингибиторами деубиквитинирующего фермента USP30.
Согласно следующему аспекту в данном изобретения предложено соединение формулы (I), описанное в данном документе, его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера для применения в качестве лекарственного средства.
Согласно следующему аспекту в данном изобретения предложен способ лечения или профилактики у млекопитающего расстройства или состояния, при котором известно или может быть показано, что ингибирование USP30 оказывает благотворное влияние, включающий введение указанному млекопитающему терапевтически эффективного количества соединения формулы (I), описанного в данном документе, его таутомера или фармацевтически приемлемой соли указанного соединения или таутомера. В одном предпочтительном воплощении всех аспектов изобретения расстройство или состояние представляет собой патологию ЦНС. В другом предпочтительном воплощении всех аспектов изобретения расстройство или состояние представляет собой периферическую патологию.
Согласно следующему аспекту в данном изобретения предложено применение соединения формулы (I), описанного в данном документе, его таутомера или фармацевтически приемлемой соли указанного соединения или таутомера в изготовлении лекарственного средства для лечения или профилактики расстройства или состояния, при котором известно или может быть показано, что ингибирование USP30 оказывает благотворное влияние. Изготовление лекарственного средства может включать, в том числе, химический синтез соединения формулы (I) или его соли или приготовление композиции или состава, содержащих соединение или соль, или упаковывание любого лекарственного средства, содержащего соединение. В одном предпочтительном воплощении всех аспектов изобретения расстройство или состояние представляет собой патологию ЦНС. В другом предпочтительном воплощении всех аспектов изобретения расстройство или состояние представляет собой периферическую патологию.
Расстройство или состояние, на которое благотворно влияет активность USP30, выбрано из состояния, при котором имеет место дисфункция митохондрий, злокачественного новообразования и фиброза.
В одном предпочтительном воплощении всех аспектов изобретения расстройство или состояние, на которое благотворно влияет активность USP30, представляет собой состояние, при котором имеет место дисфункция митохондрий. Состояние, при котором имеет место дисфункция митохондрий, может быть патологией ЦНС или периферической патологией.
Дисфункция митохондрий является следствием дефектов митохондрий, представляющих собой специализированные органеллы, присутствующие в каждой клетке организма, за исключением эритроцитов. При несостоятельности митохондрий в клетке образуется все меньше и меньше энергии и может наступить повреждение клетки или даже гибель клетки. Если этот процесс повторяется во всем организме, качество жизни субъекта, у которого это происходит, существенно падает. Митохондриальные заболевания возникают чаще всего в органах, которые потребляют много энергии, таких как головной мозг, сердце, печень, скелетные мышцы, почки и эндокринная и респираторная система.
Состояние, при котором имеет место дисфункция митохондрий, может быть выбрано из состояния, при котором имеет место дефект митофагии, состояния, при котором имеет место мутация митохондриальной ДНК, состояния, при котором имеет место окислительный стресс митохондрий, состояния, при котором имеет место нарушение мембранного потенциала митохондрий, биогенеза митохондрий, состояния, при котором имеет место дефект формы или морфологии митохондрий, и состояния, при котором имеет место лизосомная болезнь накопления.
В частности, состояние, при котором имеет место дисфункция митохондрий, может быть выбрано из нейродегенеративного заболевания; рассеянного склероза (PC); синдрома MELAS, сочетающего митохондриальную энцефалопатию, лактацидоз и инсультоподобные эпизоды; наследуемых по материнской линии диабета и глухоты (MIDD); наследственной оптической нейропатии Лебера (LHON); рака (включая, например, рак молочной железы, яичника, предстательной железы, легкого, почки, желудка, толстой кишки, яичка, головы и шеи, поджелудочной железы, головного мозга, меланому, рак кости или другие виды рака тканевых органов и рака клеток крови, такие как лимфома и лейкоз, множественная миелома, метастатическая карцинома, остеосаркома, хондросаркома, саркома Юинга, карцинома носоглотки, рак толстой и прямой кишки и немелкоклеточный рак легкого); нейропатии, атаксии, пигментной дистрофии сетчатки, наследуемого по материнской линии синдрома Лея (NARP-MILS); болезни Данона; диабета; диабетической нефропатии; метаболических нарушений; сердечной недостаточности; ишемической болезни сердца, приводящей к инфаркту миокарда; психиатрических заболеваний, например, шизофрении; множественной сульфатазной недостаточности (MSD); муколипидоза II (ML II); муколипидоза III (ML III); муколипидоза IV (ML IV); GM1-ганглиозидоза (GM1); нейронального цероидного липофусциноза (NCL1); болезни Альперса; синдрома Барта; дефектов бета-окисления; дефицита карнитина-ацилкарнитина; дефицита карнитина; синдромов дефицита креатина; дефицита кофермента Q10; дефицита комплекса I; дефицита комплекса II; дефицита комплекса III; дефицита комплекса IV; дефицита комплекса V; дефицита циклооксигеназы (СОХ); синдрома хронической прогрессирующей наружной офтальмоплегии (СРЕО); дефицита карнитин-пальмитоилтрансферазы (СРТ) I; дефицита СРТ II; глутарацидурии II типа; синдрома Кернса-Сейра; лактацидоза; дефицита ацил-СоА-дегидрогеназы жирных кислот с длинной цепью (LCHAD); болезни или синдрома Лея; франко-канадского варианта синдрома Лея (LSFC); фатальной детской кардиомиопатии (LIC); болезни Люфта; глутарацидурии II типа; дефицита ацил-СоА-дегидрогеназы жирных кислот со средней длиной цепи (MCAD); синдрома миоклонической эпилепсии с разрывом красных мышечных волокон (MERRF); митихондриальной цитопатии; синдрома рецессивной митохондриальной атаксии; синдрома истощения митохондриальной ДНК; мио-нейро-желудочно-кишечного расстройства и энцефалопатии; синдрома Пирсона; дефицита пируватдегидрогеназы; дефицита пируваткарбоксилазы; мутаций POLG (полимеразы гамма); дефицита ацил-СоА-дегидрогеназы жирных кислот со средней и короткой цепью (M/SCHAD); дефицита ацил-СоА-дегидрогеназы жирных кислот с очень длинной цепью (VLCAD); пероксисомных расстройств; метилмалоновой ацидемии и возрастного снижения когнитивной функции и мышечной силы.
Состояние, при котором имеет место дисфункция митохондрий, может представлять собой расстройство ЦНС, например, нейродегенеративное заболевание.
Нейродегенеративные заболевания включают, без ограничения, болезнь Паркинсона, болезнь Альцгеймера, боковой амиотрофический склероз (ALS), болезнь Хантингтона, ишемию, инсульт, деменцию с тельцами Леви, множественную системную атрофию (MSA), прогрессирующий надъядерный паралич (PSP), кортикобазальную дегенерацию (CBD) и лобно-височную деменцию.
В частности, соединения по изобретению могут найти применение в лечении или профилактике болезни Паркинсона, включая, без ограничения, БП, связанную с мутациями α-синуклеина, паркина, PINK1, GBA (глюкозилцерамидазы бета) и LRRK2 (богатой лейциновыми повторами киназы 2), и аутосомальную рецессивную ювенильную болезнь Паркинсона (AR-JP), при которой имеются мутации паркина.
Соединения по изобретению или их фармацевтические композиции, описанные в данном документе, можно комбинировать с одним или более дополнительными агентами при использовании в лечении или профилактике состояний, включающих дисфункцию митохондрий. Соединения можно комбинировать с одним или более дополнительными агентами, выбранными из леводопа, агониста дофаминовых рецепторов, ингибитора моноаминооксигеназы В (МАО), ингибитора катехол-О-метилтрансферазы (СОМТ), антихолинэргического средства, рилузола, амантадина, ингибитора холинэстеразы, мемантина, тетрабеназина, антипсихотического средства, диазепама, клоназепама, антидепрессанта и противосудорожного средства. Соединения можно комбинировать с агентами, которые уменьшают/удаляют патогенные агрегаты белков при нейродегенеративных заболеваниях, такими как агенты, которые уменьшают/удаляют альфа-синуклеин при болезни Паркинсона, множественной системной атрофии или деменции с тельцами Леви; агенты, которые уменьшают/удаляют белок тау при болезни Альцгеймера или прогрессирующем надъядерном параличе; агенты, которые уменьшают/удаляют TDP-43 при ALS или лобно-височной деменции.
В другом предпочтительном воплощении всех аспектов изобретения расстройство или состояние, на которое благотворно влияет активность USP30, представляет собой рак. Рак может быть связано с дисфункцией митохондрий. Предпочтительные виды рака включают, например, рак молочной железы, яичника, предстательной железы, легкого, почки, желудка, толстой кишки, яичка, головы и шеи, поджелудочной железы, головного мозга, меланому, рак кости и другие виды рака тканевых органов и рак клеток крови, такие как лимфома и лейкоз, множественную миелому, метастатическую карциному, остеосаркому, хондросаркому, саркому Юинга, карциному носоглотки, рак толстой и прямой кишки и немелкоклеточный рак легкого.
В частности, соединения по изобретению могут найти применение в лечении или профилактике рака, при котором нарушена регуляция путей апоптоза и, в частности, когда имеются мутации или пониженная или повышенная экспрессия белков семейства BCL-2.
Фиброз относится к накоплению компонентов внеклеточного матрикса, возникающему после травмы, воспаления, репарации ткани, иммунологических реакций, гиперплазии клеток и неоплазии. Фиброзирующие заболевания, которые можно лечить соединениями и композициями по данному изобретению, включают, помимо прочих, фиброз/фиброзирующие заболевания, ассоциированные с заболеваниями жизненно-важных органов, например, интерстициальное заболевание легких (ILD), цирроз печени, неалкогольную жировую дистрофию печени (NAFLD) и неалкогольный стеатогепатит (NASH) (фиброз печени), заболевание почек (фиброз почек), острое повреждение почек (ОПП), хроническую болезнь почек (ХБП), отсроченную функцию почечного трансплантата, заболевания сердца или сосудов (фиброз сердца) и глазные заболевания; фибропролиферативные расстройства, например, системную и местную склеродермию, келоидные и гипертрофический рубцы, атеросклероз, рестеноз и контрактуру Дюпюитрена; рубцевание, связанное с травмой, например, послеоперационные осложнения, фиброз, вызванный химиотерапевтическими средствами (например, фиброз, вызванный блеомицином), постлучевой фиброз, случайные повреждения и ожоги); ретроперитонеальный фиброз (болезнь Ормонда) и фиброз/рубцевание брюшины у пациентов, находящихся на перитонеальном диализе, обычно после трансплантации почки. См., например, Wynn et al, 2004, Nat Rev Immunol. August; 4(8): 583 594. Таким образом, данное изобретение относится к способам лечения или профилактики фиброза или фиброзирующих заболеваний жизненно-важных органов или связанных с жизненно-важными органами, включая, например, легкие, печень, почки, сердце, кожу, глаза, желудочно-кишечный тракт, брюшину и костный мозг, и других описанных здесь заболеваний/расстройств, а также к соединениям и композициям, применяемым в указанных способах.
Соединения можно комбинировать со средствами, которые применяют для лечения заболеваний почек, включая антидиабетические средства, средства против сердечно-сосудистых заболеваний и новые средства, мишенью которых являются связанные с заболеваниями пути, такие как окислительный стресс (включая путь nrf2/keap-1, но не ограничиваясь им) и антиапоптотические пути (включая анти-р53 средства, но не ограничиваясь ими).
Интерстициальное заболевание легких (ILD) включает нарушения, при которых воспаление легких и фиброз являются конечными общими путями патологии, например, при саркоидозе, силикозе, лекарственных реакциях, инфекциях и коллагенозах, таких как ревматоидный артрит и системный склероз (склеродермия). Фиброзирующие заболевания легких включают, например, фиброз легких, идиопатический фиброз легких (ИЛФ), обыкновенный интерстициальный пневмонит (UIP), интерстициальную легочную болезнь, криптогенный фиброзирующий альвеолит (CFA), облитерирующий бронхиолит и бронхоэктаз.
Идиопатический легочный фиброз (ИЛФ) является самым распространенным типом ILD, и причина его неизвестна.
Соединения можно комбинировать со средствами, которыми лечат ИЛФ и возможно ILD, включая нинтеданиб и пирфенидон.
Цирроз печени имеет схожие причины с ILD и включает, например, цирроз, связанный с вирусным гепатитом, шистосомозом и хроническим алкоголизмом.
Заболевание почек может быть связано с диабетом, который вызывает повреждения и рубцевания почек, приводя к прогрессирующей потере функции, а также с гипертонической болезнью. Фиброз почек может возникать на любой стадии заболевания почек, от хронической болезни почек (ХБП), такой как инцидентная ХБП и прогрессирующая ХБП, до терминальной почечной недостаточности (ТПН). Фиброз почек может развиваться в результате сердечно-сосудистого заболевания, такого как гипертензия или диабет, оба из которых оказывают огромную нагрузку на функцию почек, что провоцирует фибротический ответ. Однако фиброз почек может также быть идиопатический (без известной причины), а также некоторые наследственные митохондриальные заболевания могут манифестировать фиброзом почек и связанными симптомами.
Заболевания сердца могут приводить к рубцеванию ткани, что может нарушать способность сердца сокращаться.
Глазные болезни включают, например, макулярную дегенерацию и ретинальную и витреальную ретинопатию, которые могут нарушать зрение.
В предпочтительном воплощении данное изобретение направлено на лечение или профилактику идиопатического фиброза легких (ИЛФ).
В другом предпочтительном воплощении данное изобретение направлено на лечение или профилактику фиброза почек.
В другом предпочтительном воплощении данное изобретение направлено на лечение или профилактику острого повреждения почек (ОПП), особенно у пациентов с высоким риском. Примеры включают послеоперационное ОПП, например, при трансплантации органов, например, вследствие ишемического-реперфузионного повреждения, отсроченную функцию почечного трансплантата; в онкологии, например, как ОПП вследствие химиотерапии; контрастно-индуцированную нефропатию, как, например, прямое цитотоксическое действие на канальцы, гемодинамическая ишемия и осмотические эффекты; и острый интерстициальный нефрит, как, например, вследствие приема лекарств или инфекции. Подгруппа пациентов с наиболее высоким риском - это пациенты, которым проводят операции на сердце, например, аортокоронарное шунтирование и/или операции на клапанах. Существуют установленные постоянные факторы риска ОПП, такие как возраст 65 лет или более, инсулинозависимый диабет, ХБП (взрослые с расчетной скоростью гломерулярной фильтрации [eGFR] менее 60 мл/мин/1,73 м2 подвержены особому риску), сердечная недостаточность, заболевания печени, ОПП в анамнезе.
В другом предпочтительном воплощении данное изобретение направлено на лечение или профилактику хронической болезни почек (ХБП), в основе которой лежит ОПП, включая, например, тубулоинтерстициальный фиброз и диабетическую нефропатию.
Синдром Лея представляет собой редкое наследственное нейрометаболическое расстройство, затрагивающее центральную нервную систему. Это прогрессирующее расстройство начинается у детей в возрасте от 3 месяцев до 2 лет. В редких случаях оно возникает у подростков и взрослых. Синдром Лея может быть вызван мутациями в ядерной ДНК, кодирующей митохондриальные белки, мутациями митохондриальной ДНК (наследуемый по материнской линии синдром Лея - MILS) или дефицитом фермента под названием пируватдегидрогеназа, расположенным на коротком плече X-хромосомы (Х-сцепленный синдром Лея). Симптомы синдрома Лея обычно быстро прогрессируют. Самыми ранними признаками может быть плохое сосание и потеря удержания головки и двигательных навыков. Эти симптомы могут сопровождаться потерей аппетита, рвотой, раздражимостью, непрерывным плачем и судорогами. По мере прогрессирования расстройства симтомы могут также включать генерализованную слабость, отсутствие мышечного тонуса и эпизоды лактацидоза, которые могут привести к нарушению респираторной и почечной функции.
При наследуемом по материнской линии синдроме Лея (MILS) генетические мутации в митохондриальной ДНК (при высокой встречаемости >90%) ограничивают источники энергии, которые используют клетки в области головного мозга, играющей роль в двигательных актах. Генетические мутации в митохондриальной ДНК приводят к хроническому отсутствию энергии в этих тканях, что в свою очередь влияет на центральную нервную систему и вызывает прогрессирующую дегенерацию двигательных функций. Состояние, при котором генетические мутации в митохондриальной ДНК, вызывающие MILS, не так распространены (менее 90%), известно как нейропатия с атаксией и пигментным ретинитом (NARP). Существует также форма болезни Лея (обозначаемая Х-сцепленной болезнью Лея), которая является следствием мутаций в гене, который задействован в образовании группы других веществ, играющих важную роль в клеточном метаболизме. Существует еще один вариант синдрома Лея, обозначаемый франко-канадским вариантом, характеризующийся мутациями в гене под названием LRPPRC. Проявляется схожими с синдромом Лея неврологическими симптомами, однако при франко-канадском варианте зачастую также наблюдается стеатоз печени.
В предпочтительном воплощении данное изобретение направлено на лечение или профилактику синдрома или болезни Лея, включая, например, Х-сцепленную болезнь Лея, франко-канадский вариант синдрома Лея и/или симптомы, ассоциированные с болезнью Лея.
Соединения можно комбинировать с новыми агентами, которые можно применять в лечении митохондриальных заболеваний, включая никотинамид рибозид, но не ограничиваясь им.
Упоминание «лечения» включает средства для улучшения, облегчения симптомов, устранения причин симптомов на временной или постоянной основе. Соединения по изобретению могут найти применение в лечении заболеваний человека и других млекопитающих, описанных в данном документе.
В другом воплощении изобретение охватывает профилактику заболеваний, описанных в данном документе, и включает средства для предупреждения или замедления проявления симптомов названного расстройства или состояния. Соединения по изобретению могут найти применение для предупреждения заболеваний человека и других млекопитающих, описанных в данном документе.
Пациент, нуждающийся в лечении или предупреждении, может, например, быть человеком или другим млекопитающим, страдающим состоянием, или подверженный риску развития состояния.
Согласно следующему аспекту в данном изобретении предложена фармацевтическая композиция, содержащая соединение формулы (I), описанное в данном документе, или фармацевтически приемлемую соль указанного соединения или таутомера вместе с фармацевтически приемлемым разбавителем или носителем.
Фармацевтические композиции по изобретению содержат любое из соединений по изобретению в комбинации с любым фармацевтически приемлемым носителем, адъювантом или несущей средой. Примеры фармацевтически приемлемых носителей хорошо известны специалистам в области техники и включают, без ограничения, консерванты, наполнители, дезинтегрирующие вещества, смачивающие вещества, эмульгирующие вещества, суспендирующие вещества, подсластители, корригенты вкуса и запаха, антибактериальные вещества, противогрибковые вещества, смазывающие вещества и диспергирующие вещества, в зависимости от характера способа введения и лекарственных форм. Композиции могут быть, например, в форме таблеток, капсул, порошков, гранул, эликсиров, пастилок, суппозиториев, сиропов и жидких препаратов, включая суспензии и растворы. Термин «фармацевтическая композиция» в контексте данного изобретения означает композицию, содержащую активный агент и дополнительно содержащую один или более фармацевтически приемлемых носителей. Композиция может дополнительно содержать ингредиенты, выбранные, например, из разбавителей, адъювантов, эксципиентов, несущих сред, консервантов, наполнителей, дезинтегрирующих веществ, смачивающих веществ, эмульгирующих веществ, суспендирующих веществ, подсластителей, корригентов вкуса и запаха, антибактериальных веществ, противогрибковых веществ, смазывающих веществ и диспергирующих веществ, в зависимости от характера способа введения и лекарственных форм.
Соединения по изобретению или их фармацевтические композиции, описанные в данном документе, можно применять отдельно или в комбинации с одним или более дополнительными фармацевтическими агентами. Соединения можно комбинировать с дополнительным противоопухолевым терапевтическим агентом, например, химиотерапевтическим лекарственным средством или ингибитором или другими регуляторными белками. В одном воплощении дополнительный противоопухолевый терапевтический агент представляет собой ВН-3 миметик. В следующем воплощении ВН-3 миметик может быть выбран из одного или более из АВТ-737, АВТ-199, АВТ-263 и Obatoclax, без ограничения. В следующем воплощении дополнительный противоопухолевый агент представляет собой химиотерапевтический агент. Химиотерапевтические агенты могут быть выбраны из олапариба, митомицина С, цисплатина, карбоплатина, оксалиплатина, ионизирующего излучения (IR), камптотецина, иринотекана, топотекана, темозоломида, таксанов, 5-фторпиримидинов, гемцитабина и доксорубицина.
Для лечения или профилактики фибротических нарушений, например, соединения по изобретению или их фармацевтические композиции, описанные в данном документе, могут применяться в отдельности или в комбинации с одним или более дополнительными фармацевтическими агентами, выбранными из группы, состоящей из антихолинэргических агентов, бета-2 миметиков, стероидов, ингибиторов PDE-IV, ингибиторов МАР-киназы р38, антагонистов NK1, антагонистов LTD4, ингибиторов EGFR и антагонистов эндотелина.
В частности, соединения по изобретению или их фармацевтические композиции, описанные в данном документе, можно применять в отдельности или в комбинации с одним или более дополнительными фармацевтическими агентами, выбранными из группы, состоящей из общих иммуносупрессивных агентов, таких как кортикостероиды, иммуносупрессивных или цитотоксических агентов или антибиотиков, таких как пирфенидон или неспецифические ингибиторы киназ (например, нинтеданиб).
Фармацевтические композиции по изобретению можно вводить любым подходящим эффективным способом, таким как пероральный, парентеральный, местный, ингаляционный, интраназальный, ректальный, интравагинальный, глазной и ушной. Фармацевтические композиции, подходящие для доставки соединений по данному изобретению и способы их получения будут очевидны специалистам в области техники. Такие композиции и способы их получения можно найти, например, в документе «Remington's Pharmaceutical Sciences», 19th Edition (Mack Publishing Company, 1995).
Пероральное введение
Соединения по изобретению можно вводить перорально. Пероральное введение может включать проглатывание, чтобы соединение попадало в желудочно-кишечный тракт, или может применяться трансбуккальное или сублингвальное введение, чтобы соединение попадало в кровоток непосредственно из полости рта.
Составы, подходящие для перорального приема, включают твердые составы, такие как таблетки, капсулы, содержащие твердые частицы, жидкости или порошки, пастилки (включая наполненные жидкостью), жевательные таблетки, мульти- и наночастицы, гели, пленки (включая мукоадгезивные), капсулы яйцевидной формы, спреи и жидкие составы.
Жидкие составы включают суспензии, растворы, сиропы и эликсиры. Такие составы можно применять в качестве наполнителей в мягких или твердых капсулах, и обычно они содержат носитель, например, воду, этанол, пропиленгликоль, метилцеллюлозу или подходящее масло и один или более эмульгирующих веществ и/или суспендирующих веществ. Жидкие составы могут также быть приготовлены путем растворения твердого состава, например, из саше.
Соединения по изобретению могут также применяться в быстрорастворимой, быстрораспадающейся лекарственной форме, таких как описанные Liang and Chen в публикации Expert Opinion in Therapeutic Patents, 11 (6), 981-986 (2001).
Типичная таблетка может быть приготовлена при помощи стандартных способов, известных химикам-фармацевтам, например, путем прямого прессования, гранулирования (сухого, влажного или из расплава), отверждения из расплава или экструзии. Таблетка может иметь один или более слоев и может быть покрыта оболочкой или нет.
Примеры эксципиентов, подходящих для перорального приема, включают носители, например, целлюлозу, карбонат кальция, двухосновной фосфат кальция, маннит и цитрат натрия, связывающие вещества для гранулирования, например, поливинилпирролидон, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу и желатин, дезинтегрирующие вещества, например, натрия крахмала гликолят и силикаты, смазывающие вещества, например, стеарат магния и стеариновую кислоту, смачивающие вещества, например, додецилсульфат натрия, консерванты, антиокислители, корригенты и красители.
Твердые составы для перорального приема могут быть составлены для немедленного и/или модифицированного высвобождения. Составы с модифицированным высвобождением включают замедленное, отсроченное, прерывистое, контролируемое, двойное отсроченное, прицельное и программируемое высвобождение. Подробности о подходящих технологиях модифицированного высвобождения, таких как высокоэнергетические дисперсии, осмотические системы и частицы с покрытием, можно найти у Verma et al, Pharmaceutical Technology On-line, 25 (2), 1-14 (2001). Другие составы с модифицированным высвобождением описаны в патенте US 6106864.
Парентеральное введение
Соединения по изобретению также можно вводить непосредственно в кровоток, в мышцы или во внутренние органы. Подходящие способы парентерального введения включают внутривенное, внутриартериальное, внутрибрюшинное, интратекальное, внутрижелудочковое, внутриуретральное, внутригрудинное, внутримышечное и подкожное. Подходящие устройства для парентерального введения включают игольчатые (в том числе микроигольчатые) инжекторы, безыгольные инжекторы и инфузионные технологии.
Составы для парентерального введения обычно представляют собой водные растворы, которые могут содержать такие эксципиенты, как соли, углеводы и буферные агенты (предпочтительно, с рН от 3 до 9), но в некоторых приложениях они могут быть составлены более подходящим образом в виде стерильного неводного раствора или в высушенной форме для применения вместе с подходящей несущей средой, такой как стерильная апирогенная вода.
Получение составов для парентерального введения в стерильных условиях, например, путем лиофилизации, может легко осуществляться с применением стандартных фармацевтических технологий, хорошо известных специалистам в области техники.
Растворимость соединений формулы (I), используемых в получении растворов для парентерального применения, можно легко повышать путем подходящей обработки, например, с применением высушенных распылением высокоэнергетических дисперсий и/или с применением соответствующих технологий изготовления лекарственного препарата, таких как применение агентов, увеличивающих растворимость.
Составы для перорального применения могут быть составлены для немедленного и/или модифицированного высвобождения. Составы с модифицированным высвобождением включают замедленное, отсроченное, прерывистое, контролируемое, двойное отсроченное, прицельное и программируемое высвобождение.
Фармацевтические композиции по данному изобретению также включают композиции и способы, известные в области техники, обеспечивающие прохождение через гематоэнцефалический барьер, или можно осуществлять инъекции непосредственно в головной мозг. Подходящие области для инъекций включают кору головного мозга, мозжечок, средний мозг, ствол головного мозга, гипоталамус, спинной мозг и ткань желудочков, а также области периферической нервной системы, включая каротидный синус и мозговой слой надпочечников.
Дозировка
Размер эффективной дозы соединения будет несомненно варьировать в зависимости от природы и тяжести состояния, которое следует лечить, и способа введения. Выбор соответствующих доз находится в компетенции врача. Диапазон суточных доз составляет от приблизительно 10 мкг до приблизительно 100 мг на кг массы тела у человека и животного, не являющегося человеком, и как правило, может быть примерно от 10 мкг до 30 мг на кг массы тела на дозу. Вышеуказанную дозу можно давать от одного до трех раз в сутки.
Например, при пероральном введении может требоваться общая суточная доза от 5 мг до 1000 мг, например, от 5 до 500 мг, тогда как при внутривенном введении может требоваться от 0,01 до 30 мг/кг массы тела, например, от 0,1 до 30 мг/кг, более предпочтительно, от 0,1 до 1 мг/кг массы тела. Общую суточную дозу можно вводить однократно или разделять на несколько доз. Специалист в области техники поймет, что в ходе лечения или профилактики некоторых состояний соединения по изобретению можно принимать в виде однократной дозы или «по мере необходимости» (т.е. когда это нужно или желательно).
Способы синтеза
Соединения формулы (I) могут быть получены способами, описанными ниже в общих схемах реакции и репрезентативных примерах. При необходимости отдельные превращения в рамках схемы можно осуществлять в другом порядке. Изобретение проиллюстрировано на примерах, которые не являются исчерпывающими, в которых использовались следующие аббревиатуры и определения. Соединения характеризовали жидкостной хроматографией с масс-спектрометрией (LCMS) или 1H ЯМР, или обоими способами.
Согласно следующему аспекту в данном изобретения предложен способ получения соединения формулы (I), включающий проведение реакции между соединением формулы (IV), где Y представляет собой ОН, с амином формулы (V), где PG представляет собой защитную группу, такую как ВОС или Cbz, с получением амида формулы (III) (Схема 1). Реакцию присоединения с образованием амида можно проводить согласно стандартной методике, например, путем реакции с применением реагента для реакций присоединения, такого как DCC, HATU, HBTU, EDC или смешанного ангидрида. В альтернативном варианте кислота (IV), где Y представляет собой ОН, может превращаться в хлорангидрид (IV), где Y представляет собой Cl, с применением SOCl2, PCl3 или PCl5, который затем может вступать в реакцию с амином (V), предпочтительно в подходящем растворителе в присутствии подходящего основания. В альтернативном варианте соединение (IV), где Y образует сложный эфир, может непосредственно реагировать с амином (V), предпочтительно в подходящем растворителе.
Удалять защитную группу у соединения формулы (I) можно стандартными способами с получением амина (II), который затем может вступать в реакцию с цианогенбромидом с образованием соответствующего соединения формулы (I).
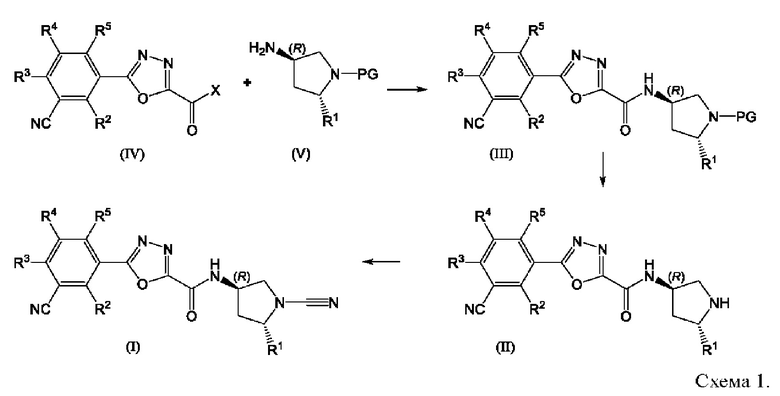
В следующем аспекте данного изобретения предложено соединение, выбранное из формул (II) и (III):
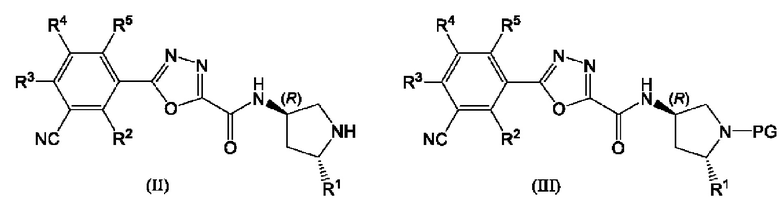
где PG представляет собой защитную группу, a R1, R2, R3, R4 и R5 являются такими, как определено для соединения формулы (I) и его предпочтительных воплощений, его таутомера или соли указанного соединения или таутомера.
Защитные группы предпочтительно выбраны из трет-бутилоксикарбонила (ВОС), бензилоксикарбонила (Cbz), пара-метоксибензилкарбонила (MeOZ), 9-флуоренилметилоксикарбонила (Fmoc), ацетила (Ас), бензоила (Bz), бензила (Bn), карбамата, р-метоксибензила (РМВ), 3,4-диметоксибензила (DMPM), пара-метоксифенила (РМР), тозила (Ts), трихлорэтоксикарбонила (Troc), 4-нитробензолсульфонила (Nosyl) и 2-нитрофенилсульфенила (Nps). Наиболее предпочтительны ВОС и Cbz.
Способы жидкостной хроматографии с масс-спектрометрией (LCMS)
Способ С

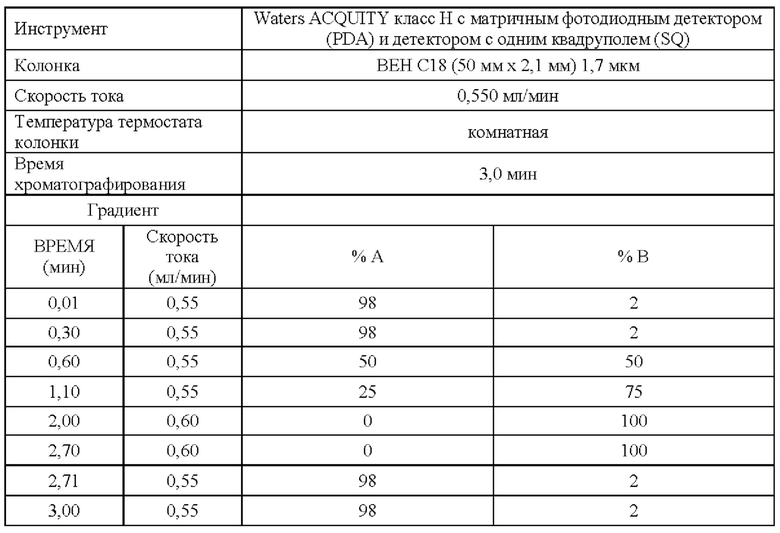
Способ Н
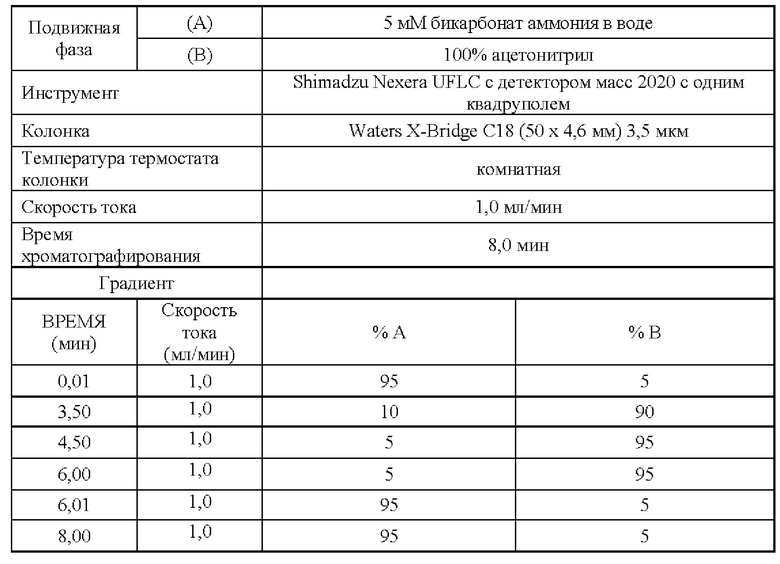
Способ H1
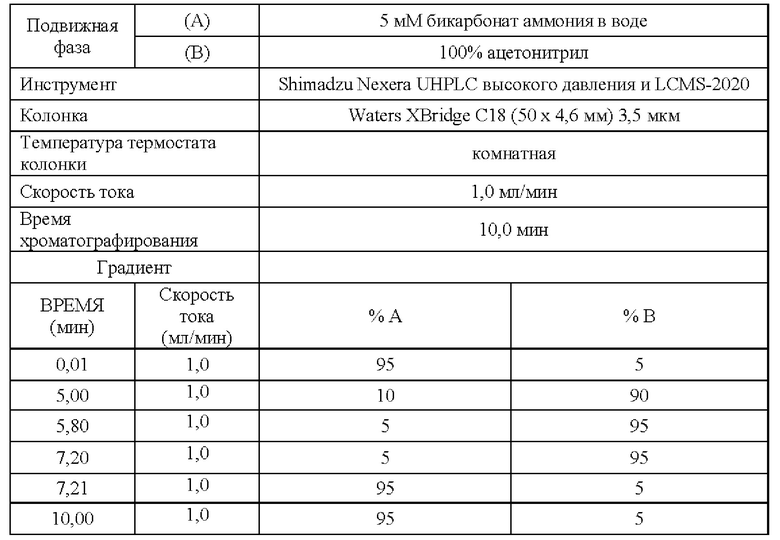
Способ J
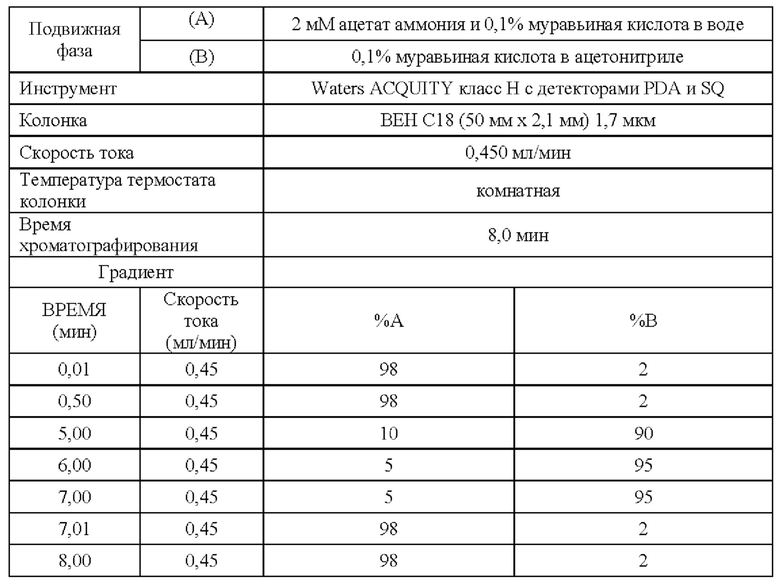
Способ Y3
Способ использовали для аналитической хиральной сверхкритической флюидной хроматографии (SFC).
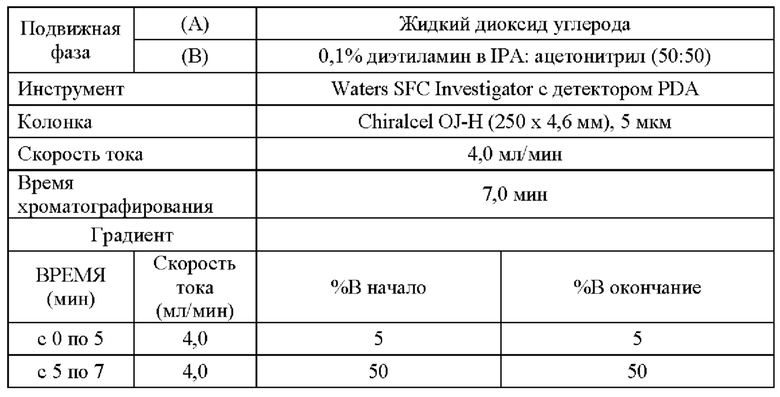
Способ Y4
Способ использовали для аналитической хиральной сверхкритической флюидной хроматографии (SFC).
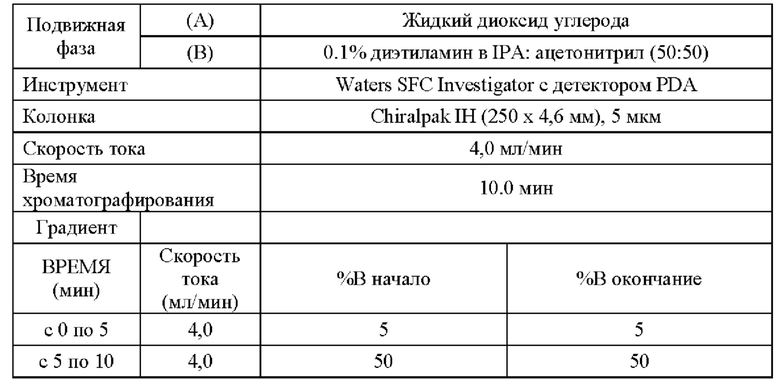
Способ Y9
Способ использовали для аналитической хиральной сверхкритической флюидной хроматографии (SFC).

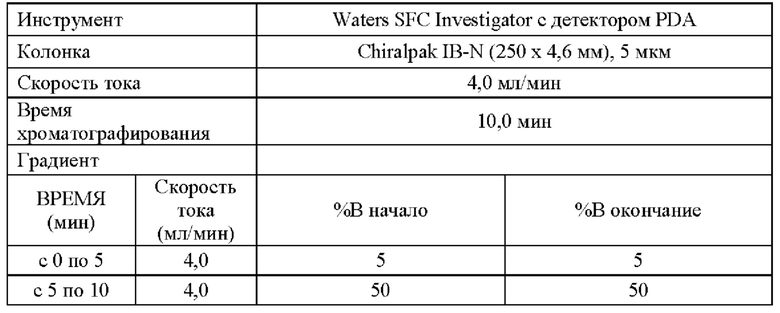
Промежуточное соединение А
Этил 5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилат
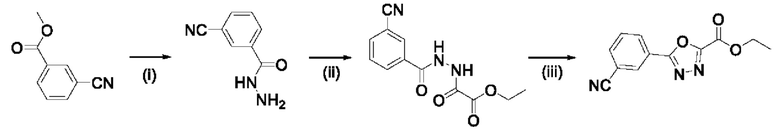
Схема: (i) гидрат гидразина, МеОН, 0°С до комнатной температуры; (ii) этилхлорооксоацетат, K2CO3, DCM, 0°С до комнатной температуры; (iii) TsCl, TEA, DCM, 0°C до комнатной температуры.
Стадия 1
3-цианобензогидразид
К перемешиваемому раствору метил 3-цианобензоата (CAS 13531-48-1, от CombiBlocks, 150,0 г, 930,5 ммоль) в МеОН (1500 мл) добавляли NH2NH2.H2O (99% водный раствор, 114,3 мл, 2326,3 ммоль) при 0°С. Смесь перемешивали в течение 16 ч при комнатной температуре, затем концентрировали под пониженным давлением, разводили водой (2000 мл) и экстрагировали DCM (3 х 800 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением с получением 3-цианобензогидразида (138 г, 857,1 ммоль, выход 92%).
LCMS: Способ С, 1,23 мин, MS: ES+ 162.2; 1H ЯМР (400 МГц, DMSO-d6) δ ppm: 10.01 (s, 1H), 8.22 (s, 1H), 8.13-8.15 (d, J=8,0 Гц, 1H), 8.00-8.02 (d, J=7,6 Гц, 1H), 7.70 (t, J=8,0 Гц, 1H), 4.60 (s, 2H).
Стадия 2
Этил-2-(2-(3-цианобензоил)гидразинил)-2-оксоацетат
К перемешиваемому раствору 3-цианобензогидразида (131 г, 813,7 ммоль) в DCM (1960 мл) добавляли K2CO3 (168,4 г, 1220,5 ммоль). Смесь перемешивали в течение 15 мин при комнатной температуре, затем охлаждали до 0°С и добавляли этилхлороацетат по каплям (203,6 мл, 1790,1 ммоль) при 0°С. Смесь перемешивали в течение 1 ч при комнатной температуре, затем разводили водой (5000 мл) и экстрагировали DCM (5 х 4000 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и концентрировали под пониженным давлением с получением этил 2-(2-(3-цианобензоил)гидразинил)-2-оксоацетата (251,9 г). Данное вещество использовали на следующей стадии без очистки.
LCMS: Способ С, 1,35 мин, MS: ES+ 262.2; 1Н ЯМР (400 МГц, DMSO-d6) δ ppm: 11.08 (s, 1H), 10.85 (s, 1H), 8.28 (s, 1H), 8.10-8.20 (m, 2H), 7.77 (t, J=8,0 Гц, 1H), 4.29-4.35 (m, 2H), 1.32 (t, 3H).
Стадия 3
Этил-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилат
К перемешиваемому раствору этил-2-(2-(3-цианобензоил)гидразинил)-2-оксоацетата (251,0 г, со стадии 2, без очистки) в DCM (4000 мл) добавляли TEA (269,8 мл, 1923,4 ммоль) при 0°С. Смесь перемешивали в течение 15 мин при 0°С, затем добавляли 4-толуолсульфонилхлорид (91,7 г, 480,8 ммоль) при 0°С. Смесь перемешивали в течение 1 ч при комнатной температуре, затем разводили водой (4000 мл) и экстрагировали DCM (2 х 5000 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной хроматографии (25% EtOAc в гексане) с получением этил-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилата (105,6 г, 434,6 ммоль, выход после двух стадий 53%).
LCMS: Способ С, 1,58 мин, MS: ES+ 244.2; 1H ЯМР (400 МГц, DMSO-d6) δ ppm: 8.51 (s, 1H), 8.38-8.40 (d, J=8,0 Гц, 1H), 8.18-8.20 (d, J=8,0 Гц, 1H), 7.87 (t, J=8,0 Гц, 1H), 4.46-4.51 (m, 2H), 1.39 (t, 3H).
Промежуточное соединение В
Этил-5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксилат
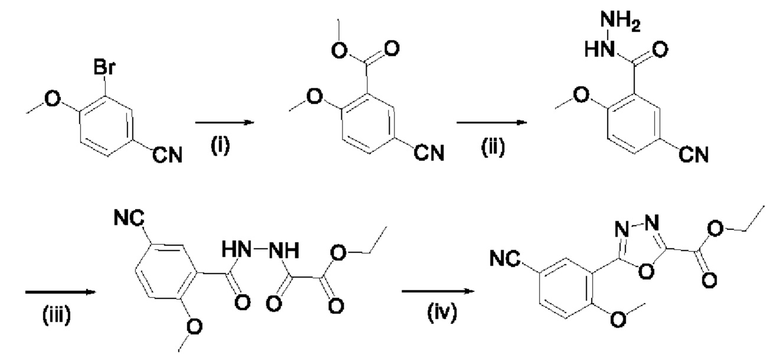
Схема: (i) газообразный СО, комплекс PdCl2(dppf)DCM, МеОН, NaOAc, 70°С; (ii) гидрат гидразина, МеОН, 0°С до комнатной температуры; (iii) этилоксалилхлорид, K2CO3, DCM, 0°С до комнатной температуры; (iv) TsCl, TEA, DCM, 0°C до комнатной температуры.
Стадия (i)
Метил-5-циано-2-метоксибензоат
К перемешиваемому раствору 3-бромо-4-метоксибензонитрила (CAS 117572-79-9, 2,0 г, 9,48 ммоль) в МеОН (20 мл), в автоклаве добавляли NaOAc (3,88 г, 47,40 ммоль) и дегазировали реакционную смесь с применением N2 в течение 20 минут. К реакционной смеси добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлоропалладий(II), комплекс с дихлорметаном (1,54 г, 1,89 ммоль) при комнатной температуре. Реакционную смесь нагревали до 70°С в течение 36 часов в атмосфере СО (газ) под давлением (20 кг/см2). Смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении. Остаток вливали в воду (50 мл) и экстрагировали EtOAc (3 х 70 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 40% EtOAc в н-гексане) с получением метил 5-циано-2-метоксибензоата (1,1 г, 5,75 ммоль, выход 60%).
1H ЯМР (400 МГц, DMSO-d6) δ ppm: 8.07 (s, 1H), 8.03 (d, J=8,8 Гц, 1H), 7.35 (d, J=8,8 Гц, 1H), 3.92 (s, 3H), 3.81 (s, 3H).
Стадия (ii)
5-циано-2-метоксибензогидразид
К перемешиваемому раствору метил-5-циано-2-метоксибензоата (1,1 г, 5,75 ммоль) в МеОН (11 мл) добавляли гидрат гидразина (0,72 мл, 14,37 ммоль) при 0°С. Смеси давали нагреться до комнатной температуры и перемешивали в течение 16 ч, затем концентрировали под пониженным давлением с получением 5-циано-2-метоксибензогидразида (1,0 г, 5,23 ммоль, выход 90%).
LCMS: Способ С, 1,24 мин, MS: ES+ 190.3.
Стадия (iii)
Этил-2-(2-(5-циано-2-метоксибензоил)гидразинеил)-2-оксоацетат
К перемешиваемому раствору метил 5-циано-2-метоксибензогидразида (1,0 г, 5,23 ммоль) в DCM (10 мл) добавляли K2CO3 (1,44 г, 10,47 ммоль) с последующим добавлением этилоксалилхлорида (1,16 мл, 10,47 ммоль) по каплям при 0°С. Смеси давали нагреться до комнатной температуры и перемешивали в течение 1 ч, затем вливали в воду (50 мл) и экстрагировали DCM (3 х 150 мл). Объединенные органические фазы высушивали над Na2SO4, фильтровали и концентрировали с получением 2-(2-(5-циано-2-метоксибензоил)гидразинеил)-2-оксоацетата (1,2 г, 4,12 ммоль, выход 78%). LCMS: Способ J, 3,08 мин, MS: ES+ 292.0.
Стадия (iv)
Этил-5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксилат
К перемешиваемому раствору этил-2-(2-(5-циано-2-метоксибензоил)гидразинеил)-2-оксоацетата (1,2 г, 4,12 ммоль) в DCM (12 мл) добавляли TEA (1,72 мл, 12,37 ммоль) и TsCl (0,78 г, 4,12 ммоль) по частям при 0°С. Смеси давали нагреться до комнатной температуры и перемешивали в течение 2 ч, затем вливали в воду (50 мл) и экстрагировали EtOAc (3 х 100 мл). Объединенные органические фазы высушивали над Na2SO4, и концентрировали под пониженным давлением, затем остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 43% EtOAc в н-гексане) с получением этил-5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксилата (0,64 г, 2,34 ммоль, выход 56%).
LCMS: Способ J, 3,94 мин, MS: ES+ 274.0.
Пример 1
N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
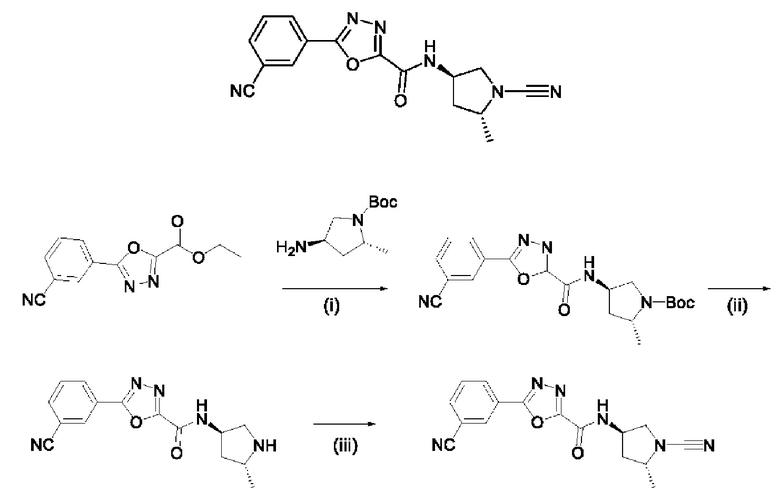
Схема: (i) TBD, THF, 0°C to rt; (ii) TFA, DCM, 0°C to rt; (iii) K2CO3, CNBr, 0°C до комнатной температуры.
Стадия (i)
трет-бутил-(2R,4R)-4-(4-(3-цианофенил)пиколинамидо)-2-метилпирролидин-1-карбоксилат
К перемешиваемому раствору этил-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилата (0,15 г, 0,617 ммоль, 1,0 экв) и трет-бутил-(2R,4R)-4-амино-2-метилпирролидин-1-карбоксилата (CAS 348165-63-9, от CombiBlocks, 0,123 г, 0,617 ммоль, 1,0 экв) в THF (4,0 мл) добавляли TBD (0,103 г, 0,741 ммоль, 1,2 экв) при 0°С. Смесь перемешивали при комнатной температуре в течение 1 ч, затем вливали в воду (100 мл) и экстрагировали EtOAc (2 х 100 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной хроматографии (60-120# силикагель, 40% EtOAc в гексане) с получением трет-бутил-(2R,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-метилпирролидин-1-карбоксилата (0,115 г, 0,289 ммоль, выход 47%).
LCMS: Способ С, 1,69 мин, MS: ES- 396.6 (М-1).
Стадия (ii)
5-(3-цианофенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соль трифторуксусной кислоты (TFA)
К перемешиваемому раствору трет-бутил-(2R,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-метилпирролидин-1-карбоксилата (0,115 г, 0,289 ммоль, 1,0 экв) в DCM (5 мл) добавляли TFA (0,35 мл, 3 объема) по каплям при 0°С. Смесь перемешивали в течение 40 мин при комнатной температуре, затем концентрировали под пониженным давлением при помощи DCM (2 х 50 мл) с получением 5-(3-цианофенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,10 г, 0,24 ммоль, выход 84%).
LCMS: Способ С, 1,28 мин, MS: ES+ 298.0.
Стадия (iii)
N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору 5-(3-цианофенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,10 г, 0,243 ммоль, 1,0 экв) в THF (5 мл) добавляли K2CO3 (0,168 г, 1,22 ммоль, 5 экв) частями при комнатной температуре. Смесь охлаждали до 0°С и добавляли цианогена бромид (0,026 мл, 0,243 ммоль, 1 экв) при 0°С. Смесь перемешивали в течение 40 ч при комнатной температуре, затем вливали в воду (80 мл) и экстрагировали EtOAc (2 х 50 мл). Органические фазы объединяли, высушивали над Na2SO4 и концентрировали под пониженным давлением. Полученный остаток очищали при помощи колоночной хроматографии (60-120# силикагель, 35% EtOAc в гексане) с получением N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида (0,07 г, 0,217 ммоль, выход 89%).
Точка плавления = от 152°С до 154°С. [α]D25=-31° (с=0,05 г/100 см3, дихлорметан).
LCMS: Способ H1 3,15 мин, MS: ES- 322.1; 1H ЯМР (400 МГц, DMSO-d6) δ ppm: 9.75-9.77 (d, J=6,8 Гц, 1H), 8.50 (s, 1H), 8.39-8.41 (d, J=8,0 Гц, 1H), 8.16 8.18 (d, J=8,0 Гц, 1H), 7.86 (t, J=8,0 Гц, 1H), 4.51-4.54 (m, 1H), 3.88-3.94 (m, 1H), 3.77-3.81 (m, 1H), 3.43-3.46 (m, 1H), 2.14-2.19 (m, 1H), 1.76-1.83 (m, 1H), 1.25-1.26 (d, J=6,4 Гц, 3H).
Пример 2
N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
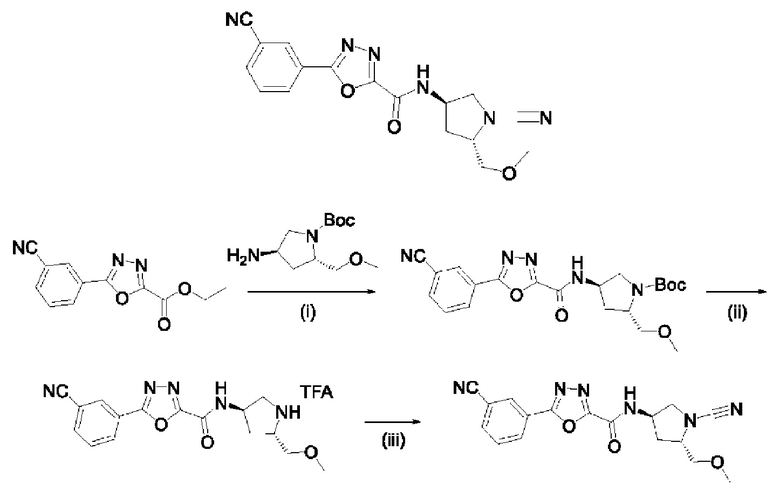
Схема: (i) TBD, THF, 0°С; (v) TFA, DCM, от 0°C до комнатной температуры; (vi) K2CO3, CNBr, 0°С.
Стадия (i)
трет-бутил (2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилат
К перемешиваемому раствору этил-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилата (0,15 г, 0,62 ммоль) и трет-бутил-(2S,4R)-4-амино-2-(метоксиметил)пирролидин-1-карбоксилата (CAS 1207853-53-9, 0,14 г, 0,62 ммоль) в THF (3,0 мл) добавляли TBD (0,13 г, 0,92 ммоль) при 0°С. Смесь перемешивали при 0°С в течение 10 мин, затем вливали в воду (50 мл) и экстрагировали EtOAc (3 х 50 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 50% EtOAc в н-гексане) с получением трет-бутил-(2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилата (0,07 г, 0,17 ммоль, выход 28%).
LCMS: Способ С, 1,62 мин, MS: ES- 426.1.
Стадия (ii)
5-(3-цианофенил)-N-((3R,5S)-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соль TFA
К перемешиваемому раствору трет-бутил-(2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилата (0,07 г, 0,16 ммоль) в DCM (3 мл) добавляли TFA (0,35 мл, 5 объемов) по каплям при 0°С. Смесь перемешивали в течение 2 ч при комнатной температуре, затем концентрировали под пониженным давлением с получением 5-(3-цианофенил)-N-((3R,5S)-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,12 г, количественный выход). LCMS: Способ С, 1,27 мин, MS: ES+ 328.0.
Стадия (iii)
N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору 5-(3-цианофенил)-N-((3R,5S)-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,11 г, 0,25 ммоль) в THF (5 мл) добавляли K2CO3 (0,1 г, 0,75 ммоль) частями при комнатной температуре. Через 10 мин добавляли цианогена бромид (0,02 г, 0,19 ммоль) при 0°С. Смесь перемешивали в течение 45 мин при 0°С, затем вливали в воду (50 мл) и экстрагировали EtOAc (3 х 40 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 70% EtOAc в н-гексане) с получением N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида (0,02 г, 0,07 ммоль, выход после двух стадий 43%).
LCMS: Способ Н, 2,47 мин, MS: ES- 351.1; 1Н ЯМР (400 МГц, DMSO-d6) δ ppm: 9.75 (d, J=6,4 Гц, 1H), 8.50 (s, 1H), 8.40 (d, J=8,0 Гц, 1H), 8.17 (d, J=7,6 Гц, 1H), 7.86 (t, J=8,0 Гц, 1H), 4.48-4.58 (m, 1H), 3.98-4.08 (m, 1H), 3.70-3.74 (m, 1H), 3.43-3.50 (m, 3H), 3.32 (s, 3H), 2.09-2.14 (m, 1H), 1.96-2.02 (m, 1H); Хиральная SFC: Способ Y4, 4,30 мин.
Пример 3
N-((3R,5S)-1-циано-5-(фторметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
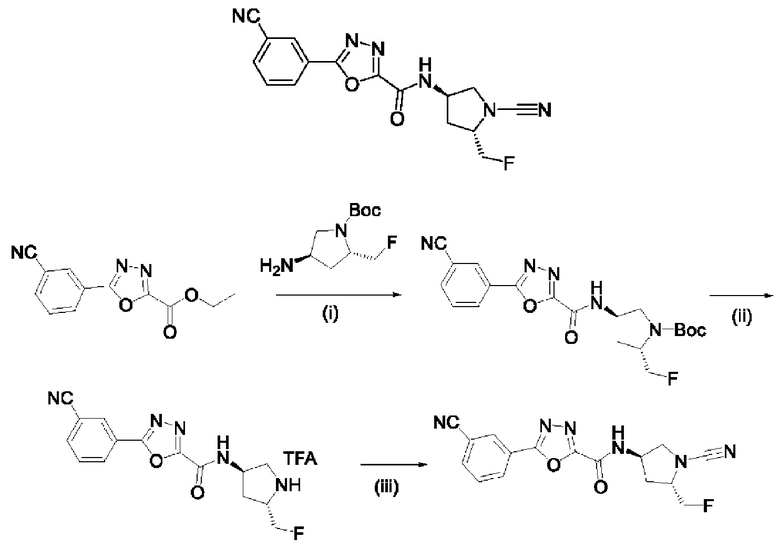
Схема: (i) TBD, THF, 0°С to rt; (v) TFA, DCM, 0°C to rt; (vi) K2CO3, CNBr, от 0°C до комнатной температуры.
Стадия (i)
трет-бутил-(2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(фторметил)пирролидин-1-карбоксилат
К перемешиваемому раствору этил-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксилата (0,15 г, 0,62 ммоль) и трет-бутил-(2S,4R)-4-амино-2-(фторметил)пирролидин-1-карбоксилата (CAS 1207853-03-9, от Angene, 0,11 г, 0,49 ммоль) в THF (5,0 мл) добавляли TBD (0,1 г, 0,74 ммоль) при 0°С. Смеси давали прогреться до комнатной температуры и перемешивали в течение 1 ч, затем вливали в воду (50 мл) и экстрагировали EtOAc (2 х 50 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 50% EtOAc в н-гексане) с получением трет-бутил-(2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(фторметил)пирролидин-1-карбоксилата (0,1 г, 0,25 ммоль, выход 40%).
LCMS: Способ С, 1,66 мин, MS: ES- 414.1.
Стадия (ii)
5-(3-цианофенил)-N-((3R,5S)-5-(фторметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид, соль TFA
К перемешиваемому раствору трет-бутил-(2S,4R)-4-(5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(фторметил)пирролидин- 1-карбоксилата (0,1 г, 0,24 ммоль) в DCM (5 мл) добавляли TFA (1,0 мл, 10 объемов) по каплям при 0°С. Смесь перемешивали в течение 1 ч при комнатной температуре, затем концентрировали под пониженным давлением с получением 5-(3-цианофенил)-N-((3R,5S)-5-(фторметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,12 г, количественный выход). LCMS: Способ С, 1,31 мин, MS: ES+ 316,2.
Стадия (iii)
N-((3R,5S)-1-циано-5-(фторметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору 5-(3-цианофенил)-N-((37?,55)-5-(фторметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,12 г, 0,28 ммоль) в THF (5 мл) добавляли K2CO3 (0,12 г, 0,84 ммоль) частями при комнатной температуре и перемешивали в течение 10 мин. Смесь охлаждали до 0°С и добавляли цианогена бромид (0,03 г, 0,28 ммоль) и смеси давали прогреться до комнатной температуры и перемешивали в течение 1 ч. Остаток вливали в воду (50 мл) и экстрагировали EtOAc (2 х 50 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 70% EtOAc в н-гексане) с получением N-((3R,5S)-1-циано-5-(фторметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида (0,03 г, 0,10 ммоль, выход после двух стадий 41%).
LCMS: Способ Н, 2,51 мин, MS: ES- 338.9; 1Н ЯМР (400 МГц, DMSO-d6) δ ppm: 9.81 (d, J=6,4 Гц, 1H), 8.51 (s, 1H), 8.40 (d, J=8,0 Гц, 1H), 8.18 (d, J=7,6 Гц, 1H), 7.87 (t, J=8,0 Гц, 1H), 4.43-4.67 (m, 3H), 4.13-4.26 (m, 1H), 3.75-3.79 (m, 1H), 3.46-3.53 (m, 1H), 2.13-2.23 (m, 1H), 2.01-2.06 (m, 1H); Хиральная SFC: Способ Y3, 3,57 мин.
Пример 4
5-(5-циано-2-метоксифенил)-N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид
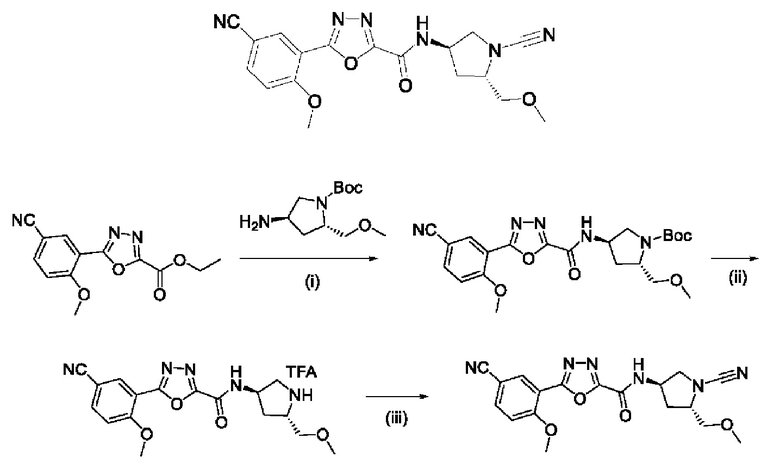
Схема: (i) TBD, THF, 0°C to rt; (v) TFA, DCM, 0°C to rt; (vi) K2CO3, CNBr, от 0°C до комнатной температуры.
Стадия (i)
трет-бутил-(2S,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилат
К перемешиваемому раствору этил-5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксилата (0,29 г, 1,06 ммоль) и трет-бутил-(2S,4R)-4-амино-2-(метоксиметил)пирролидин-1-карбоксилата (CAS 1207853-53-9, 0,24 г, 1,06 ммоль) в THF (2,9 мл) добавляли TBD (0,18 г, 1,27 ммоль) при 0°С. Смеси давали прогреться до комнатной температуры и перемешивали в течение 1 ч, затем вливали в воду (50 мл) и экстрагировали EtOAc (3 х 150 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 70% EtOAc в н-гексане) с получением трет-бутил-(2S,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилата (0,16 г, 0,35 ммоль, выход 33%).
LCMS: Способ J, 4,34 мин, MS: ES- 455,6.
Стадия (ii)
5-(5-циано-2-метоксифенил)-N-((3R,5S)-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид, соль TFA
К перемешиваемому раствору трет-бутил-(2S,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-(метоксиметил)пирролидин-1-карбоксилата (0,16 г, 0,35 ммоль) в DCM (1,6 мл) добавляли TFA (1,6 мл, 10 объемов) по каплям при 0°С. Смесь перемешивали в течение 1 ч при комнатной температуре, затем концентрировали под пониженным давлением с получением 5-(5-циано-2-метоксифенил)-N-((3R,5S)-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,15 г, количественный выход).
LCMS: Способ J, 2,92 мин, MS: ES+ 357,4.
Стадия (iii)
5-(5-циано-2-метоксифенил)-N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору 5-(5-циано-2-метоксифенил)-N-((3R,5S)-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,15 г, 0,32 ммоль) в THF (1,5 мл) добавляли K2CO3 (0,13 г, 0,95 ммоль) частями при комнатной температуре и перемешивали в течение 10 мин. Добавляли цианогена бромид (0,04 г, 0,38 ммоль) при 0°С и перемешивали смесь в течение 1 ч. Смесь вливали в воду (50 мл) и экстрагировали EtOAc (3 х 150 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали при пониженном давлении. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 90% EtOAc в н-гексане) с получением 5-(5-циано-2-метоксифенил)-N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида (0,06 г, 0,17 ммоль, выход после двух стадий 48%).
LCMS: Способ Н, 2,38 мин, MS: ES+ 383.1; 1Н ЯМР (400 МГц, DMSO-d6) δ ppm: 9.74 (d, J=6,4 Гц, 1H), 8.35 (s, 1H), 8.16 (d, J=7,2 Гц, 1H), 7.51 (d, J=8,8 Гц, 1H), 4.48-4.57 (m, 1H), 4.02 (br s, 4H), 3.69-3.73 (m, 1H), 3.43-3.51 (m, 3H), 3.33 (s, 3H), 2.10-2.17 (m, 1H), 1.96-2.02 (m, 1H); Хиральная SFC: Способ Y9, 5,42 мин.
Пример 5
5-(5-циано-2-метоксифенил)-N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид
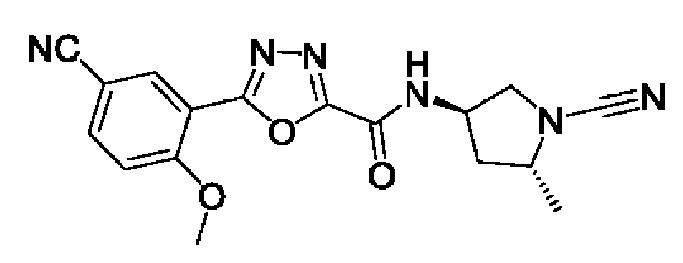
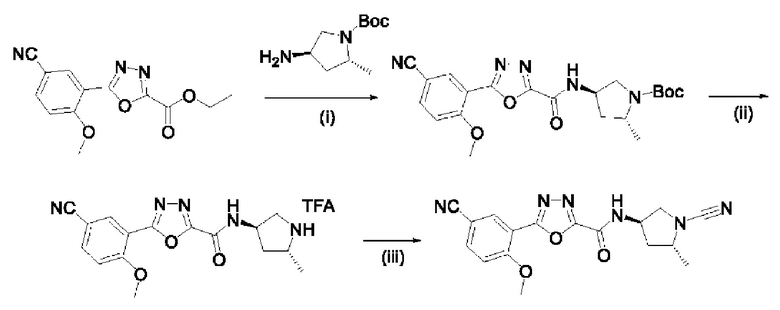
Схема: (i) TBD, THF, от 0°C до комнатной температуры; (v) TFA, DCM, от 0°C до комнатной температуры; (vi) K2CO3, CNBr, от 0°C до комнатной температуры.
Стадия (i)
трет-бутил-(2R,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-метилпирролидин-1-карбоксилат
К перемешиваемому раствору этил-5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксилата (0,31 г, 1,13 ммоль) и трет-бутил-(2R,4R)-4-амино-2-метилпирролидин-1-карбоксилата (CAS 348165-63-9, 0,23 г, 1,13 ммоль) в THF (6,0 мл) добавляли TBD (0,19 г, 1,36 ммоль) при 0°С. Смеси давали прогреться до комнатной температуры и перемешивали в течение 1 ч, затем вливали в воду (30 мл) и экстрагировали EtOAc (3 х 50 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 65% EtOAc в н-гексане) с получением трет-бутил (2R,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-метил пирролидин-1-карбоксилата (0,13 г, 0,30 ммоль, выход 27%).
LCMS: Способ J, 4,45 мин, MS: ES+ 426,2.
Стадия (ii)
5-(5-циано-2-метоксифенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору трет-бутил-(2R,4R)-4-(5-(5-циано-2-метоксифенил)-1,3,4-оксадиазол-2-карбоксамидо)-2-метилпирролидин-1-карбоксилата (0,13 г, 0,30 ммоль) в DCM (1,3 мл) добавляли TFA (1,3 мл, 10 объемов) по каплям при 0°С. Смесь перемешивали в течение 1 ч при комнатной температуре, затем концентрировали под пониженным давлением с получением 5-(5-циано-2-метоксифенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,13 г, количественный выход).
LCMS: Способ J, 2,85 мин, MS: ES+ 328.0.
Стадия (iii)
5-(5-циано-2-метоксифенил)-N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамид
К перемешиваемому раствору 5-(5-циано-2-метоксифенил)-N-((3R,5R)-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида, соли TFA (0,13 г, 0,29 ммоль) в THF (1,3 мл) добавляли K2CO3 (0,12 г, 0,88 ммоль) частями при комнатной температуре и перемешивали в течение 10 мин. Добавляли цианогена бромид (0,04 г, 0,35 ммоль) при 0°С и перемешивали смесь в течение 1 ч. Смесь вливали в воду (40 мл) и экстрагировали EtOAc (3 х 100 мл). Объединенные органические фазы высушивали над Na2SO4 и концентрировали под пониженным давлением. Остаток очищали при помощи колоночной флэш-хроматографии (силикагель, 70% EtOAc в н-гексане) с получением 5-(5-циано-2-метоксифенил)-N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида (0,01 г, 0,03 ммоль, выход после двух стадий 11%).
LCMS: Способ Н, 2,57 мин, MS: ES+ 353.2; 1H ЯМР (400 МГц, DMSO-d6) δ ppm: 9.77 (d, J=6,0 Гц, 1H), 8.35 (d, J=1,6 Гц, 1H), 8.16 (d, J=8,8 Гц, 1H), 7.51 (d, J=8,8 Гц, 1H), 4.48-4.55 (m, 1H), 4.02 (s, 3H), 3.88-3.93 (m, 1H), 3.76-3.80 (m, 1H), 3.43-3.46 (m, 1H), 2.15-2.18 (m, 1H), 1.75-1.82 (m, 1H), 1.25 (d, J=6,4 Гц, 3Н); Хиральная SFC: Способ Y4, 4,65 мин.
Биологическая активность соединений по изобретению.
Аббревиатуры
TAMRA - карбокситетраметилродамин
PBS - фосфатный солевой буфер
EDTA - этилендиаминтетрауксусная кислота
Tris - 2-амино-2-(гидроксиметил)-1,3-пропандиол
NP-40 - Nonidet Р-40, октилфеноксиполиэтоксиэтанол
BSA - бычий сывороточный альбумин
SDS-PAGE - электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия
DMSO - диметилсульфоксид
YFP - желтый флуоресцентный белок
VME - винилметиловый эфир
НА - гемагглютинин
Ahx - аминогексановая кислота.
Биохимическое исследование IC50 в отношении USP30
В 96-луночных полипропиленовых планшетах с коническим дном (Greiner #651201) готовили 21-кратные разведения (от 2100 мкМ до конечной концентрации 100 мкМ) в 50% DMSO. Типичная серия 8-кратных разведений представляла собой конечные концентрации 100, 30, 10, 3, 1, 0,3, 0,1, 0,03 мкМ. Реакции проводили в дубликатах в черных 384-луночных планшетах (уменьшенного объема, Greiner 784076), конечный объем реакционной смеси составлял 21 мкл. В планшет добавляли либо 1 мкл 50% DMSO, либо разведенного соединения. USP30 (Boston Biochem #Е582) разводили в реакционном буфере (40 мМ Tris, рН 7,5, 0.005% Tween 20, 0,5 мг/мл BSA, 5 мМ бета-меркаптоэтанол) с достижением конечной концентрации в исследовании 4 нМ, и к соединению добавляли 10 мкл разведенного USP30. Фермент инкубировали с соединением в течение 30 мин при комнатной температуре. Реакцию запускали добавлением 50 нМ меченного TAMRA пептида, связанного с убиквитином через изо-пептидную связь, в качестве субстрата для детекции поляризации флуоресценции. Измерения проводили немедленно после добавления субстрата и через 2 часа инкубации при комнатной температуре. Измерения проводили на приборе Pherastar Plus (BMG Labtech). λ возбуждения 540 нм; λ испускания 590 нм.
Активность соединений, приведенных в качестве примера, в биохимическом исследовании IC50 USP30:
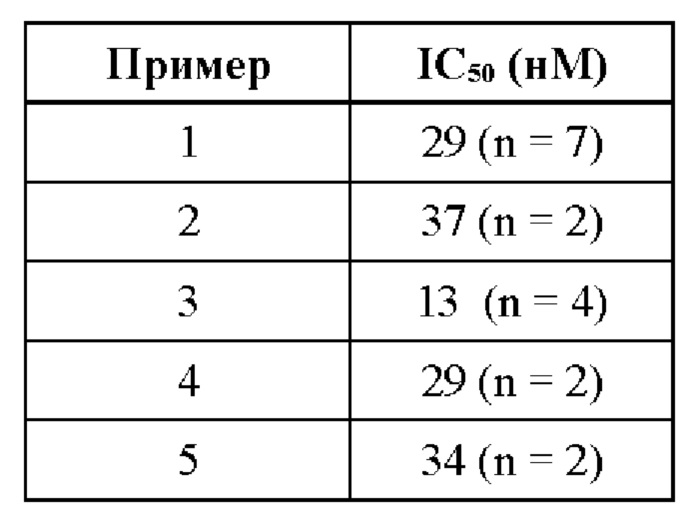
Примеры, служащие контролем
Активность соединений при биохимическом исследовании IC50 в отношении USP30:
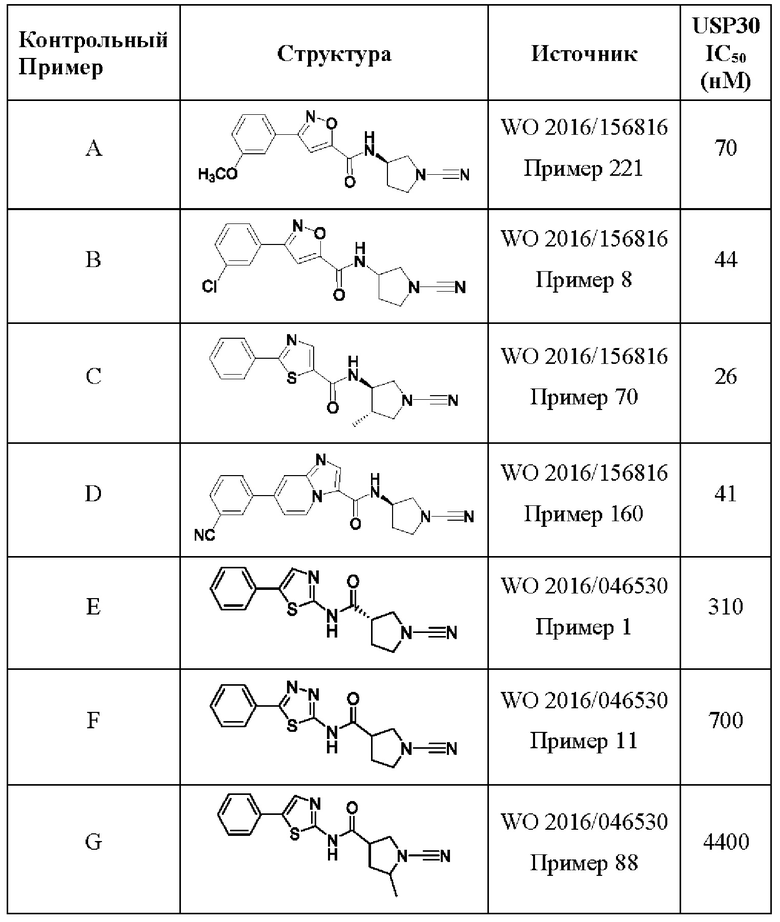
Нецелевые фармакологические свойства
Активность при биохимическом исследовании IC50 в отношении DUB:

Исследовали фармакологический профиль Примера 1 с применением панели Eurofins CEREP SafetyScreen44. При единственной концентрации 10 мкМ наблюдали менее чем 25%-ное ингибирование связывания или ферментативной активности всех мишеней, входящих в состав панели.
Вследствие низкой аффинности Примера 1 к мишеням, входящим в указанные скрининговые панели, маловероятно, что он обладает нецелевыми фармакологическими свойствами.
Фармакологическая безопасность
Оценивали влияние Примера 1 в концентрациях от 0,01 до 30 мкМ на калиевый канал hERG, стабильно экспрессируемый клетками СНО. Максимальные показатели ингибирования амплитуды тока hERG для Примера 1 составляли 7,7% и 18,8%, соответственно, при концентрации 30 мкМ, что указывало на низкую склонность влиять на интервал QT.
Генетическая токсикология
Пример 1 оценивали в тесте на обратные мутации у бактерий (тест Эймса) и в тесте на выявление микроядер in vitro. Все исследования in vitro проводили с активацией экзогенными метаболитами и без нее, с использованием концентраций, ограниченных цитотоксичностью или растворимостью. Пример 1 не вызывал мутаций при тестировании в концентрации до 100 мкг/лунку (эквивалент 5000 мкг/планшет) в тесте на обратные мутации штаммов Salmonella typhimurium ТА98, ТА100, ТА1535 и ТА97а и штамма Escherichia Coli WP2 uvrA pKM101, с метаболической активацией и без.
Индукцию повреждения хромосом оценивали с помощью теста на выявление микроядер в клетках ТК6 in vitro. Пример 1 не вызывал образования микроядер при инкубации в течение 3 часов при экзогенной метаболической активации с последующим восстановлением в течение 27 часов, а также при инкубации в течение 27 часов в отсутствие метаболической активации с последующим восстановлением в течение 27 часов.
Исследование убиквитинирования ТОМ20
Человеческие клеточные линии можно стимулировать агентами, вызывающими деполяризацию мембраны (ионофорами (например, СССР, валиномицином), ингибиторами митохондриального комплекса (олигомицином, антимицином А)) для индукции убиквитинирования ТОМ20, чему дополнительно способствует присутствие ингибиторов USP30. Затем убиквитинирование ТОМ20 оценивается методом вестерн-блоттинг с использованием клеточных лизатов, при этом детектирование аддуктов, образовавшихся при убиквитинировании ТОМ20, возможно благодаря увеличению молекулярной массы каждой молекулы на 8 кДа вследствие присоединения убиквитина, что приводит к смещению иммунореактивной полосы, соответствующей ТОМ20. Уровни убиквитинирования ТОМ20 можно оценивать количественно при помощи хемилюминесцентной денситометрии смещенных иммунореактивных полос.
Анализ связывания с эндогенной мишенью USP30
Клетки Hela, стабильно экспрессирующие YFP-Parkin, высаживали в 6-луночные планшеты. После адгезии клетки подвергали воздействию исследуемых соединений в соответствующих концентрациях или несущей средой, служившей контролем, в течение 1 часа при 37°С, 5% СО2. Лизаты цельных клеток готовили, соскабливая клетки в холодный PBS, центрифугируя и лизируя в лизирующем буфере (50 мМ Tris-base, рН 7,5, 50 мМ NaCl, 1% NP-40/Igepal СА-630, 2 мМ MgCl2, 10% глицерин, 5 мМ бета-меркаптоэтанол, таблетки cOmplete mini без EDTA (Roche), таблетки PhosStop (Roche)) в течение 10 мин. Эквивалент 20 мкг белка из просветленного лизата клеток инкубировали с зондом HA-Ahx-Ahx-Ub-VME в конечной концентрации 2,5 мкМ при комнатной температуре. Реакцию останавливали добавлением 5х SDS буфера для загрузки образцов и разделяли белки при помощи SDS PAGE и вестерн-блоттинга. USP30 определяли с применением козьего антитела к USP30 (S746D, MRC PPU Reagents and Services) и вторичного кроличьего антитела к IgG (H+L) козы, конъюгированного с пероксидазой хрена (Thermo #31480), а для визуализации использовали реагент ECL (GE #RPN2109) и визуализирующее устройство GE LAS4000. Связывание с мишенью определяли путем количественной оценки полос, соответствующих USP30 и USP30, связанному с зондом Ub-VME, и сравнивали экспрессию этой части по сравнению с контролем, который подвергали воздействию несущей среды.
Анализ связывания с мишенью USP30 ткани почки
От 50 до 100 мг ткани гомогенизировали в 3-кратном объеме лизирующего буфера (50 мМ Tris, рН 7,5, 50 мМ NaCl, 0,1% NP-40/Igepal СА-630, 0,5 мМ CHAPS, 2 мМ MgCl2, 5 мМ бета-меркаптоэтанол, таблетки cOmplete mini без EDTA (Roche), таблетки PhosStop (Roche)) с применением измельчителя Retch (ММ400). Лизат, содержащий 60 мкг белка, инкубировали с зондом HA-Ahx-Ahx-Ub-VME в конечной концентрации 6 мкМ в течение 15 мин при комнатной температуре. Реакцию останавливали добавлением 5х SDS буфера для загрузки образцов и разделяли белки при помощи SDS PAGE и вестерн-блоттинга. USP30 определяли с применением антитела козы к USP30 (S746D, MRC PPU Reagents and Services) и вторичного кроличьего антитела к IgG (H+L) козы, конъюгированного с пероксидазой хрена (Thermo #31480), а для визуализации использовали реагент ECL (GE #RPN2109) и визуализирующее устройство GE LAS4000. Связывание с мишенью определяли путем количественной оценки полос, соответствующих USP30 и USP30, связанному с зондом Ub-VME, и сравнивали экспрессию этой части по сравнению с контролем, который подвергали воздействию несущей среды.
Цитотоксичность in vitro (Cell Тох): Определяли на клетках карциномы толстой кишки человека НСТ116 с применением аламарового синего по конечной точке. Цитотоксичность соединения измеряли в течение периода времени 96 часов при непрерывном воздействии соединения.
Дополнительные исследования
log Р: коэффициент распределения неионизированной формы соединения; исследование липофильности.
log D: коэффициент распределения ионизированной и неионизированной формы соединения; исследование липофильности.
TPSA: топологическая площадь полярной поверхности.
Растворимость, турбидиметрически: Раствор исследуемого соединения в DMSO разводили в водном буфере. Поглощение измеряли турбидиметрическим методом по конечной точке при 620 нм.
FaSSIF: искусственный кишечный сок, измерение натощак при рН 6,5.
Гепатоцитарный клиренс (Cl) у мыши: клиренс в гепатоцитах мыши in vitro.
Гепатоцитарный Cl у человека: клиренс в гепатоцитах человека in vitro.
Плазменная fu,p: Свободная фракция соединения в плазме, определяемая при помощи равновесного диализа in vitro. Считается, что только одно несвязанное (свободное) соединение способно взаимодействовать с мишенью.
Мозговая fu,br: Свободная фракция соединения в гомогенате ткани головного мозга, определяемая при помощи равновесного диализа in vitro. Считается, что только одно несвязанное (свободное) соединение способно взаимодействовать с мишенью.
Clu: клиренс in vitro. Clu здесь определяют как нормированный клиренс, в свою очередь рассчитываемый по внутреннему клиренсу. Внутренний клиренс представляет собой ожидаемый клиренс вследствие метаболических реакций в печени, определяемый при инкубации соединения с препаратом гепатоцитов. Чем ниже значение в мл/мин/кг, тем более стабильно соединение.
Клиренс (Cl) in vivo: Фармакокинетическое измерение объема плазмы (или любой матрицы), из которого вещество выводится полностью за единицу времени. Чем ниже значение в мл/мин/кг, тем более стабильно соединение.
Биодоступность F, перорально: Биодоступность при пероральном применении
Исследование проницаемости монослоя клеток MDR1-MDCK (Мадин-Дарби почки собаки) (in vitro)
Связывание с мишенью в клетках, WB: Анализ связывания с эндогенной мишенью USP30 в клетках методом вестерн-блот (WB). Активность соединений в отношении USP30 исследовали в клетках, применяя для отслеживания активности USP30 сенсор, основанный на ферментативной активности, вызывающий необратимое ингибирование.
Связывание с мишенью ex vivo: Анализ связывания с мишенью USP30 в ткани почки.
Kpu,u представляет собой отношение несвязанного лекарственного средства в головном мозге к несвязанному лекарственному средству в плазме и может указывать на терапевтический потенциал в отношении периферических патологий и/или патологий ЦНС.
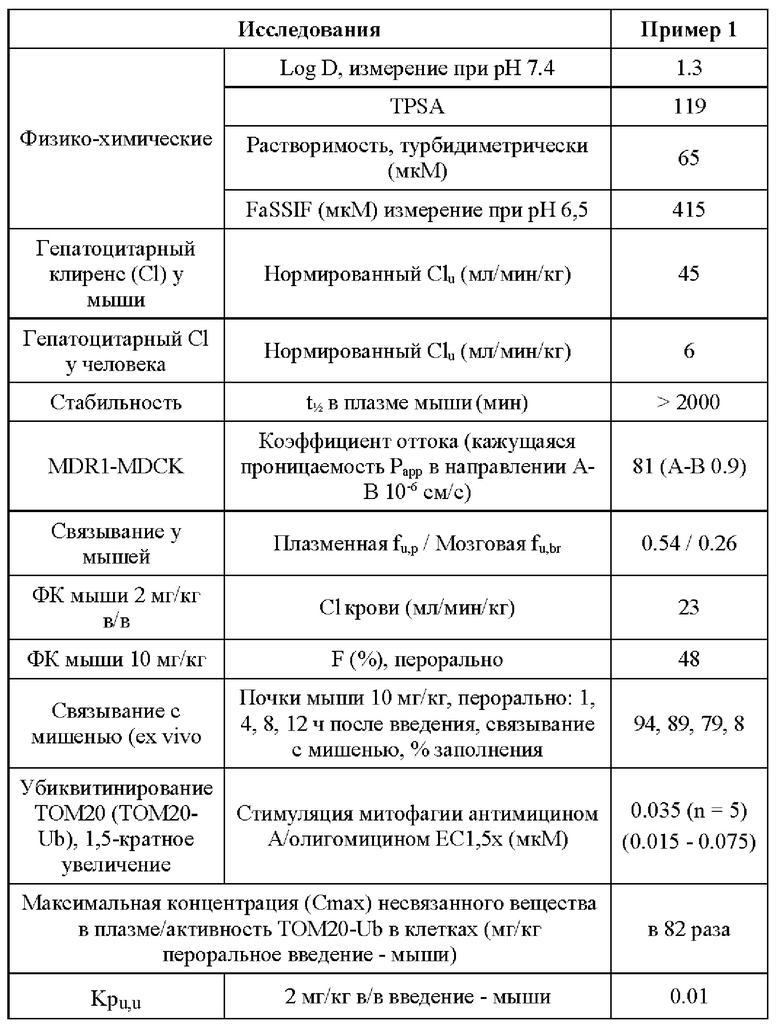
Пример 1 обладает благоприятными свойствами, демонстрирующими потенциал, превосходящий другие соединения. Например, плазматический клиренс 23 мл/мин/кг, измеренный у мышей после внутривенной инъекции, является низким, демонстрируя значительную стабильность в плазме, и соединение обладает очень хорошей биодоступностью при пероральном приеме 48%.
Высокая термодинамическая растворимость Примера 1, равная 415 мкМ по результатам измерений в искусственном кишечном соке (натощак) потенциально указывает на большее всасывание в кишечнике через портальную вену печени. Более высокая растворимость также предполагает большую вероятность того, что при увеличении дозы и неизменности всех остальных факторов, можно избежать выхода на плато системного воздействия, ограничиваемого растворимостью.
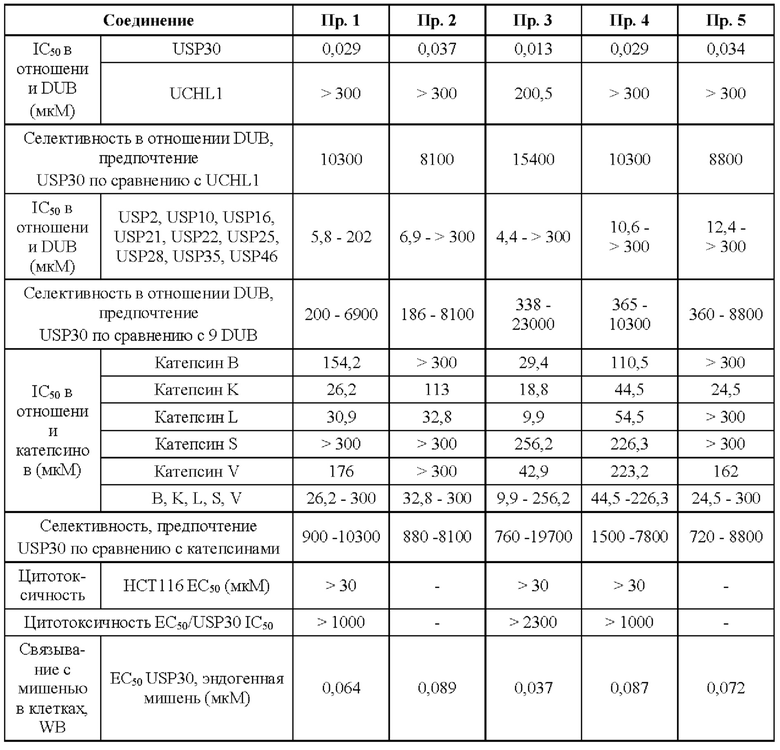
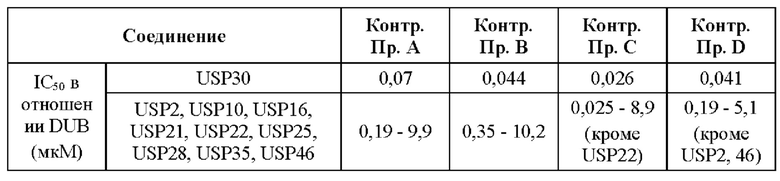
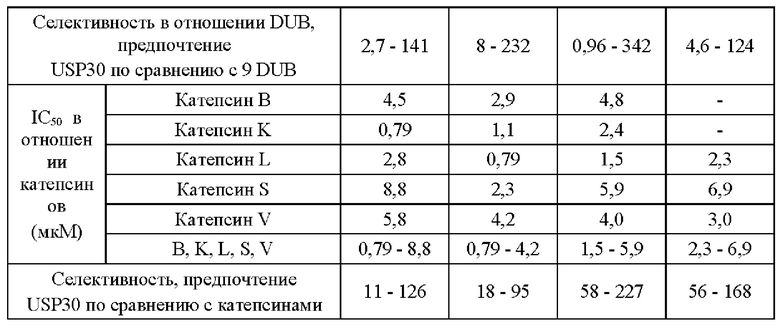
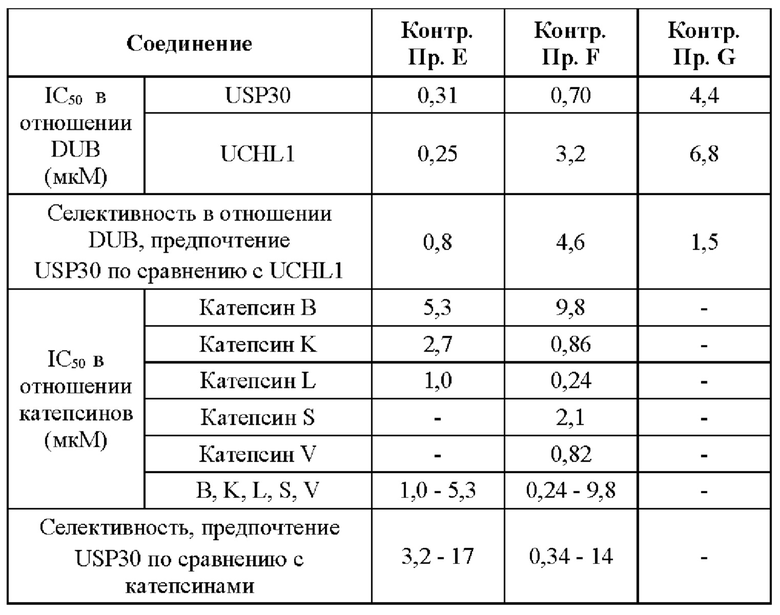
Сравнительные данные
Контрольные Примеры А, В, С, D, Е, F и G являются известными ингибиторами DUB, которые, как было обнаружено, являются активными ингибиторами USP30 и обладают некоторым структурным сходством с соединениями по данному изобретению, обладая такой структурной характеристикой, как цианамидная группа. Контрольные Примеры Е, F и G описаны в WO 2016/046530, как обладающие активностью ингибиторов UCHL1.
Активность в отношении USP30
Все Примеры с 1 по 5 в данном изобретении являются существенно более активными в отношении USP30 по сравнению с контрольными Примерами А, Е, F и G по результатам биохимического анализа. Например, Пример 1 является в 2,4, 10,7, 24 и 152 раза более активным по сравнению с контрольными Примерами А, Е, F и G, соответственно. Пример 3 является значительно более активным в отношении USP30, чем все контрольные Примеры, будучи в 5,4, 3,4, 2, 3,2, 24, 54 и 338 раз более активным по сравнению с контрольными Примерами А, В, С, D, Е, F и G, соответственно.
Селективность в отношении USP30 по сравнению с USP2. USP10. USP16. USP2L USP22. USP25. USP28. USP35 и USP46
Все Примеры с 1 по 5 являются значительно более селективными в отношении USP30 по сравнению с девятью DUB, чем контрольные Примеры А, В, С и D (USP2, USP10, USP16, USP21, USP22, USP25, USP28, USP35 и USP46; неполные данные для С и D). Примеры с 1 по 5 по меньшей мере в 186 раз более активны в отношении USP30, чем в отношении каждого из девяти DUB. Это является существенным преимуществом по сравнению с А, В, С и D, которые являются более активными в отношении одного из девяти DUB в 2,7, 8, 0,96 и 4,6 раз, соответственно (С является таким же активным).
Селективность в отношении USP30 по сравнению с UCHL1
Все из Примеров с 1 по 5 являются существенно более селективными в отношении USP3 по сравнению с UCHL1, чем контрольные Примеры Е, F и G. Примеры с 1 по 5 по меньшей мере в 8100 раз более активны в отношении USP30 по сравнению с UCHL1, тогда как Е, F и G более активны только в 0,8, 4,6 и 1,5 раза, соответственно (Е является таким же активным). Таким образом, Примеры с 1 по 5 по меньшей мере в 1700 раз более селективны в отношении USP30 по сравнению с UCHL1, чем Е, F и G.
Селективность в отношении USP30 по сравнению с катепсинами В, K, L, S и V
Все Примеры с 1 по 5 являются значительно более селективными в отношении USP30 по сравнению с катепсинами В, K, L, S и V), чем контрольные Примеры А, В, С, D и F (неполные данные для С и D). Примеры с 1 по 5 по меньшей мере в 720 раз более активные в отношении USP30, чем в отношении каждого из катепсинов. Это является существенным преимуществом по сравнению с А, В, С, D и F, которые являются более активными в отношении одного из катепсинов в 11, 18, 58, 56, 3,2 и 0,34 раз, соответственно.
Так, Пример 1 является в 27, 59, 18, 19, 333 и 3135 раз более селективным в отношении USP30 по сравнению с катепсином L, чем А, В, С, D, Е и F, соответственно.
Вышеуказанные преимущества соединений по изобретению по сравнению с известными из уровня техники контрольными Примерами, являются как существенными, так и неожиданными. И в отдельности, и особенно в комбинации эти преимущества соединений по изобретению делают их особенно подходящими для применения в лечении и/или предупреждении заболеваний, связанных с активностью UP30.
Доклинические модели in vivo
Эффективность соединений по изобретению можно исследовать in vivo в репрезентативных моделях заболеваний, с применением стандартных исследовательских процедур, опубликованных в литературе, включая, например:
(a) Модель фиброза легких, индуцированного блеомицином, которая является ведущей доклинической моделью идиопатического фиброза легких in vivo. [Kobayashi et al, 2016, J Immunol, 197(2):504-516]
(b) Индуцированная диетой модель NAFLD и гомеостаза глюкозы. [Nishida et al, 2013, Lab Invest; Feb; 93(2):230-41]
(c) Модель МРТР болезни Паркинсона, которая широко применяется для изучения нейродегенерации в дофаминергической системе головного мозга, вызванной химически индуцированной дисфункцией митохондрий. [Karuppagouner et al, 2014, Sci Rep.2014 May 2; 4:4874]
(d) Модель Ndufs4KO синдрома Лея. [Kruse et al, 2008, Cell Metab. Apr; 7(4):312-20]
(e) Модель старения у мышей: влияние на когнитивную и двигательную функцию. [Kobilo et al, 2014, Learn Mem. Jan 17; 21(2):119-26; Creed et al, 2019, Neuroscience. Jun 15; 409:169-179]
(f) Модель болезни почек посредством односторонней обструкции мочеточника (OOM). [Chevalier et al, 2009, Kidney Int 75(11): 1145-1152]
OOM приводит к повреждению почек, которое характеризуется повреждением клеток канальцев, интерстициальным воспалением и фиброзом. Это служит моделью необратимого постренального острого повреждения почек (ОПП). Эксперименты с ООМ послужили иллюстрацией молекулярных механизмов апоптоза, воспаления и фиброза, все из которых являются ключевыми процессами при повреждении почек, независимо от первичного поражения. Следовательно, модель ООМ предоставляет исследователям информацию, касающуюся не только обструкции.
Пример 1 оценивали на модели ООМ для определения способности соединения облегчать прогрессирующий тубулоинтерстициальный фиброз и хроническую болезнь почек (ХБП).
В 1 день исследования взрослые мыши C57BL/6 получали через желудочный зонд несущую среду или Пример 1 в количестве 5 мг/кг согласно схеме введения дважды в сутки. Через два часа после введения в день 1 мышам проводили операцию по лигированию левого мочеточника в двух местах. Успешность операции ООМ подтверждали позднее, наблюдая дилатацию почечной лоханки вследствие гидронефроза. Животные получали введение согласно предписанной схеме в течение 10 дней, и в этот момент времени почки забирали для гистопатологической оценки и исследования белка/РНК. Для оценки степени отложения коллагена выполняли окрашивание при помощи пикросириуса красного, а для оценки относительной экспрессии гладкомышечного α-актина (α-SMA) использовали ИГХ.
Результаты показали, что Пример 1, вводимый перорально по 5 мг/кг дважды в сутки, статистически достоверно снижал отложение коллагена, о чем свидетельствовало окрашивание лигированных почек пикросириусом красным. Окрашивание на α-SMA выявило, что пероральное введение Примера 1 дважды в сутки по 5 мг/кг также статистически достоверно снижало уровни α-SMA в почках при повреждении вследствие ООМ по сравнению с несущей средой, служившей контролем.
(g) Модель острого повреждения почек (ОПП), индуцированного ишемией.
| название | год | авторы | номер документа |
|---|---|---|---|
| Соединения 1-циано-пирролидинов в качестве ингибиторов USP30 | 2016 |
|
RU2717238C2 |
| Новые соединения | 2016 |
|
RU2734256C2 |
| ПРОИЗВОДНОЕ 7-ГИДРОКСИКУМАРИНА ДЛЯ ИНДУКЦИИ МИТОФАГИИ В КЛЕТКАХ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2022 |
|
RU2819611C1 |
| Спироконденсированные пирролидиновые производные в качестве ингибиторов деубиквитилирующих ферментов (DUB) | 2017 |
|
RU2730552C2 |
| ПРОИЗВОДНЫЕ 2-ПИРАЗИНОНА ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ИЛИ СОСТОЯНИЯ, ПРИ КОТОРЫХ ПОЛЕЗНО ИНГИБИРОВАНИЕ АКТИВНОСТИ НЕЙТРОФИЛЬНОЙ ЭЛАСТАЗЫ | 2007 |
|
RU2448098C2 |
| НОВОЕ ПРОИЗВОДНОЕ 2-АРИЛТИАЗОЛА ИЛИ ЕГО СОЛЬ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2021 |
|
RU2822057C1 |
| Бициклические конденсированные гетероарильные или арильные соединения в качестве модуляторов IRAK4 | 2016 |
|
RU2684324C1 |
| НОВЫЕ СОЕДИНЕНИЯ | 2015 |
|
RU2691389C2 |
| СОЕДИНЕНИЯ, КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ПОВЫШЕНИЯ АКТИВНОСТИ CFTR | 2015 |
|
RU2767460C2 |
| ЗАМЕЩЕННЫЕ БЕНЗОАЗЕПИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ TOLL-ПОДОБНОГО РЕЦЕПТОРА | 2010 |
|
RU2580320C2 |
Группа изобретений относится к органической химии и включает соединение формулы (I), его таутомер или фармацевтически приемлемую соль указанного соединения или таутомера, фармацевтическую композицию на его основе и промежуточные соединения формул (II) и (III). В формуле (I) R1 выбран из (С1-С4)алкила, (С1-С4)фторалкила и СН2ОСН3; каждый из R2, R3 и R4 независимо выбран из водорода и фтора; R5 выбран из водорода, фтора, (С1-С4)алкокси и циклопропокси. В формулах (II), (III) R1, R2, R3, R4 и R5 являются такими, как определено для формулы (I), PG представляет собой защитную группу, выбранную из трет-бутилоксикарбонила, бензилоксикарбонила, 9-флуоренилметилоксикарбонила или трихлорэтоксикарбонила. Технический результат - замещенные цианопирролидины формулы (I), обладающие активностью ингибиторов USP30. 3 н. и 17 з.п. ф-лы, 5 пр.
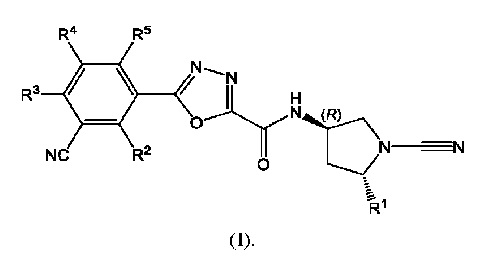
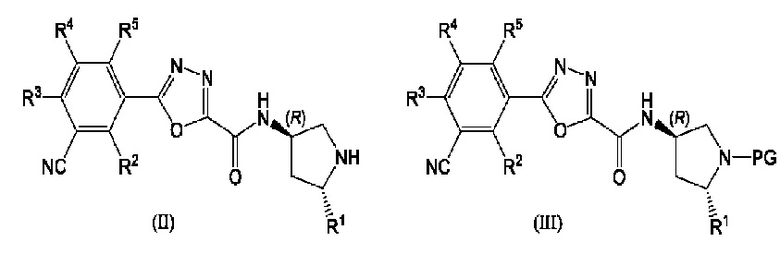
1. Соединение формулы (I)
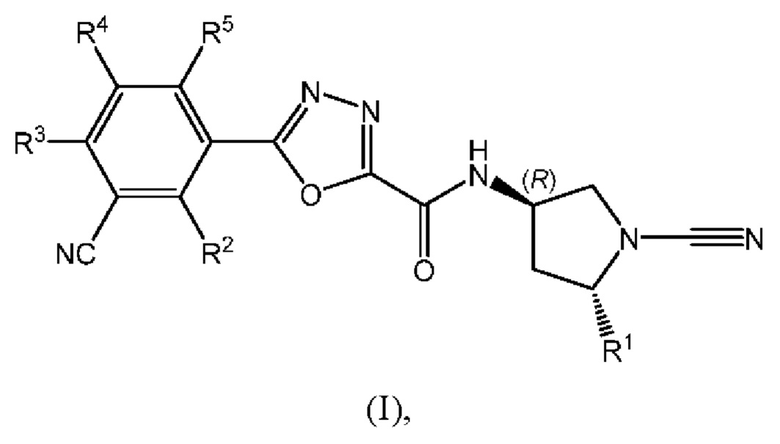
его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера, где:
R1 выбран из (С1-С4)алкила, (С1-С4)фторалкила и CH2OCH3;
каждый из R2, R3 и R4 независимо выбран из водорода и фтора; и
R5 выбран из водорода, фтора, (С1-С4)алкокси и циклопропокси.
2. Соединение по п. 1, где R1 выбран из метила, CH2F, CHF2, CF3 и СН2ОСН3.
3. Соединение по п. 2, где R1 представляет собой метил.
4. Соединение по любому из пп. 1-3, где каждый из R2, R3 и R4 представляет собой водород.
5. Соединение по любому из пп. 1-4, где R5 выбран из водорода, фтора, метокси и циклопропокси.
6. Соединение по п. 5, где R5 представляет собой водород.
7. Соединение по п. 1, выбранное из:
N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
N-((3R,5S)-1-циано-5-(фторметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-5-(3-цианофенил)-1,3,4-оксадиазол-2-карбоксамида;
5-(5-циано-2-метоксифенил)-N-((3R,5S)-1-циано-5-(метоксиметил)пирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида; и
5-(5-циано-2-метоксифенил)-N-((3R,5R)-1-циано-5-метилпирролидин-3-ил)-1,3,4-оксадиазол-2-карбоксамида;
их таутомера или фармацевтически приемлемой соли указанного соединения или таутомера.
8. Соединение по любому из пп. 1-7, его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера для применения в лечении или профилактике расстройства или состояния, связанного с активностью USP30 (С-концевая убиквитингидролаза 30).
9. Соединение по любому из пп. 1-7, его таутомер или фармацевтически приемлемая соль указанного соединения или таутомера для применения в лечении или предупреждении состояния, при котором имеет место дисфункция митохондрий, рака или фиброза, связанного с активностью USP30.
10. Соединение для применения по п. 9, где состояние, при котором имеет место дисфункция митохондрий, выбрано из расстройства ЦНС; нейродегенеративного заболевания; болезни Паркинсона; болезни Альцгеймера; бокового амиотрофического склероза; болезни Хантингтона; ишемии, инсульта; деменции с тельцами Леви; лобно-височной деменции; рассеянного склероза; синдрома митохондриальной энцефалопатии с лактацидозом и инсультоподобными эпизодами; наследуемых по материнской линии диабета и глухоты; наследственной оптической нейропатии Лебера; рака; нейропатии, атаксии, пигментной дистрофии сетчатки - наследуемого по материнской линии синдрома Лея; болезни Данона; диабета; диабетической нефропатии; метаболических расстройств; сердечной недостаточности; ишемической болезни сердца, приводящей к инфаркту миокарда; психиатрических заболеваний, шизофрении; множественной сульфатазной недостаточности; муколипидоза II; муколипидоза III; муколипидоза IV; GM1-ганглиозидоза; нейронального цероидного липофусциноза; болезни Альперса; синдрома Барта; дефектов бета-окисления; дефицита карнитина-ацилкарнитина; дефицита карнитина; синдромов дефицита креатина; дефицита кофермента Q10; дефицита комплекса I; дефицита комплекса II; дефицита комплекса III; дефицита комплекса IV; дефицита комплекса V; дефицита циклооксигеназы (СОХ); синдрома хронической прогрессирующей внешней офтальмоплегии; дефицита карнитин-пальмитоилтрансферазы (СРТ) I; дефицита СРТ II; глутарацидурии II типа; синдрома Кернса-Сейра; лактацидоза; дефицита ацил-СоА-дегидрогеназы жирных кислот с длинной цепью; болезни или синдрома Лея; франко-канадского варианта синдрома Лея; фатальной детской кардиомиопатии; болезни Люфта; глутарацидурии II типа; дефицита ацил-СоА-дегидрогеназы жирных кислот со средней длиной цепи; синдрома миоклонической эпилепсии с разрывом красных мышечных волокон; митихондриальной цитопатии; синдрома рецессивной митохондриальной атаксии; синдрома истощения митохондриальной ДНК; мио-нейро-желудочно-кишечного расстройства и энцефалопатии; синдрома Пирсона; дефицита пируват-дегидрогеназы; дефицита пируват-карбоксилазы; мутаций полимеразы гамма (POLG); дефицита 3-гидроксиацил-СоА-дегидрогеназы жирных кислот со средней и короткой цепью; дефицита ацил-СоА-дегидрогеназы жирных кислот с очень длинной цепью; пероксисомных расстройств; метилмалоновой ацидемии; и возрастного снижения когнитивной функции и мышечной силы.
11. Соединение для применения по п. 10, где нейродегенеративное заболевание выбрано из болезни Паркинсона, болезни Альцгеймера, бокового амиотрофического склероза, болезни Хантингтона, ишемии, инсульта, деменции с тельцами Леви, множественной системной атрофии, прогрессирующего надъядерного паралича, кортикобазальной дегенерации, лобно-височной деменции; и болезни Паркинсона, связанной с мутациями α-синуклеина, паркина, PINK1 (киназы 1, индуцируемой гомологом фосфатазы и тензина (PTEN)), GBA (глюкозилцерамидазы бета) и LRRK2 (богатой лейциновыми повторами киназы 2), и аутосомальной рецессивной ювенильной болезни Паркинсона, при которой имеются мутации паркина.
12. Соединение для применения по п. 10, где нейродегенеративное заболевание представляет собой синдром или болезнь Лея, Х-сцепленную болезнь Лея, франко-канадский вариант синдрома Лея и/или симптомы, ассоциированные с болезнью Лея.
13. Соединение для применения по п. 9, где рак выбран из рака молочной железы, яичника, предстательной железы, легкого, почки, желудка, толстой кишки, яичка, головы и шеи, поджелудочной железы, головного мозга, меланомы, рака кости, печени, мягкой ткани, рака тканевых органов, рака клеток крови, хронического миелолейкоза (ХМЛ), острого миелолейкоза (ОМЛ), мантийноклеточной лимфомы, нейробластомы, меланомы, саркомы мягких тканей, липосаркомы, фибробластической саркомы, лейомиосаркомы, гепатоцеллюлярной карциномы, остеосаркомы, рака пищевода, лейкоза, лимфомы, множественной миеломы, метастатической карциномы, остеосаркомы, хондросаркомы, саркомы Юинга, карциномы носоглотки, рака толстой и прямой кишки, немелкоклеточной карциномы легкого, рака, при котором нарушена регуляция путей апоптоза, и рака, при котором белки семейства BCL-2 мутированы или имеют пониженную или повышенную экспрессию.
14. Соединение для применения по п. 9, где фиброз выбран из фиброза или фиброзирующего заболевания, связанного с накоплением компонентов внеклеточного матрикса, возникающим после травмы, воспаления, репарации ткани, иммунологических реакций, гиперплазии клеток и неоплазии.
15. Соединение для применения по п. 14, где фиброз выбран из фиброза или фиброзирующего заболевания, связанного с заболеваниями жизненно важных органов, фибропролиферативных расстройств и рубцевания, связанного с травмой.
16. Соединение для применения по п. 15, где фиброз выбран из фиброза или фиброзирующего заболевания, связанного с интерстициальным заболеванием легких, циррозом печени, неалкогольной жировой дистрофией печени и неалкогольным стеатогепатитом, заболеванием почек, острым почечным повреждением, хроническим заболеванием почек, отсроченной функцией почечного трансплантата, заболеванием сердца или сосудов, глазными заболеваниями, системной и местной склеродермией, келоидными и гипертрофическими рубцами, атеросклерозом, рестенозом, контрактурой Дюпюитрена, послеоперационными осложнениями, фиброзом, вызванным химиотерапевтическими средствами, постлучевым фиброзом, случайными повреждениями и ожогами, ретроперитонеальным фиброзом и фиброзом/рубцеванием брюшины.
17. Соединение для применения по п. 16, где фиброз, связанный с интерстициальным заболеванием легких, выбран из саркоидоза, силикоза, реакций на лекарственные средства, инфекций, коллагенозов, ревматоидного артрита, системного склероза, склеродермии, фиброза легких, идиопатического фиброза легких, обычного интерстициального пневмонита, интерстициального заболевания легких, криптогенного фиброзирующего альвеолита, облитерирующего бронхиолита и бронхоэктаза.
18. Соединение для применения по п. 16, где заболевание почек представляет собой острое повреждение почек или хроническое заболевание почек.
19. Фармацевтическая композиция, обладающая активностью ингибиторов USP30, содержащая эффективное количество соединения формулы (I) по любому из пп. 1-7, его таутомера или фармацевтически приемлемой соли указанного соединения или таутомера вместе с одним или более фармацевтически приемлемыми эксципиентами.
20. Соединение, выбранное из формул (II) и (III):
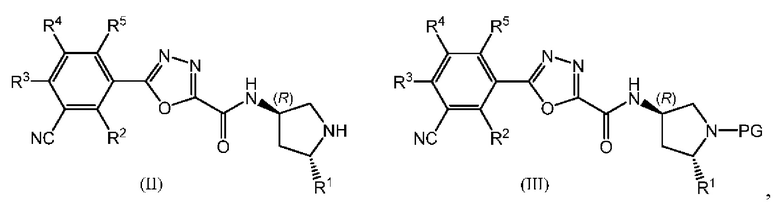
где PG представляет собой защитную группу, представляющую собой трет-бутилоксикарбонил, бензилоксикарбонил, 9-флуоренилметилоксикарбонил или трихлорэтоксикарбонил, и R1, R2, R3, R4 и R5 являются такими, как определено для соединения формулы (I) в любом из пп. 1-7, их таутомера или соли указанного соединения или таутомера.
| WO 2016156816 A1, 06.10.2016 | |||
| WO 2016046530 A1, 31.03.2016 | |||
| ЗАМЕЩЕННЫЕ ПИРРОЛИДИН-2-КАРБОКСАМИДЫ | 2011 |
|
RU2564022C2 |
| J.-P | |||
| Falgueyret et al | |||
| Novel, nonpeptidic cyanamides as potent and reversible inhibitors of human cathepsins K and L | |||
| Journal of medicinal chemistry, 2001, vol | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
Авторы
Даты
2024-07-11—Публикация
2020-09-03—Подача