ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области фармацевтических препаратов тиреоидных гормонов. В частности, изобретение относится к фармацевтическому препарату тиреоидного гормона Т4 в бесспиртовом водно-глицериновом растворе, подходящем для перорального введения и характеризующемся высокой физической, химической и микробиологической стабильностью. Настоящее изобретение также относится к применению указанного фармацевтического препарата для лечения нарушений, вызванных дефицитом гормонов щитовидной железы.
УРОВЕНЬ ТЕХНИКИ
Тиреоидный гормон тетрайодтиронин или тироксин (Т4) секретируется фолликулярными клетками щитовидной железы в ответ на гипофизарный гормон ТТГ, продукция которого, в свою очередь, регулируется гормоном гипоталамуса ТРГ. Кроме того, гипофиз секретирует гормон Т3 (трийодтиронин или лиотиронин); фактически, большая часть Т3 в организме человека появляется в результате превращения Т4 в Т3 вне щитовидной железы. Т3 в 4-5 раз активнее, чем Т4, это означает, что один мг Т3 оказывает значительно более сильное влияние на организм, чем один мг Т4.
Тиреоидные гормоны секретируются в соответствии с циркадным ритмом; максимальные уровни Т3 и Т4 достигаются ночью и в ранние утренние часы.
Т3 и Т4 необходимы для нормального роста организма детей и для созревания различных систем, в частности, скелета, и регулируют метаболическую активность у взрослых за счет влияния на функционирование всех органов и тканей. В частности, Т3 и Т4 повышают потребление кислорода в состоянии покоя, увеличивают уровень основного обмена, температуры тела и суточную потребность в энергии. Они регулируют метаболизм углеводов, стимулируя гликогенолиз и глюконеогенез, и повышают активность ферментов, участвующих в гликолизе (окислении глюкозы). Тиреоидные гормоны участвуют в липолизе и липогенезе, регулируют синтез белков, оказывая трофическое действие на мышцы, и влияют на сердечно-сосудистую систему.
Тиреоидные гормоны необходимы для функционирования сердца: они повышают сократимость миокарда (положительный инотропный эффект), повышают частоту сердечных сокращений (положительный хронотропный эффект) и повышают венозный возврат к сердцу.
В целом, тиреоидные гормоны обладают в основном анаболическим эффектом в низких дозах, тогда как в высоких дозах они оказывают катаболическое действие. В ситуациях с физиологическим дефицитом тиреоидных гормонов, как в случае с первичным и вторичным гипотиреозом, требуется лечение, основанное на тиреоидных гормонах, вводимых в исходной форме или в форме натриевых солей или гидратов. Лечение продолжается на протяжении всей жизни пациента, а дозировка (доза и частота введения) подбирается в соответствии с ответом пациента.
Подбор дозы является критическим аспектом терапии тиреоидными гормонами: недостаточная доза приводит к слабому ответу, тогда как избыточная доза может вызвать токсические симптомы гипертиреоза, такие как, тахикардия, потливость, потеря массы, возбудимость, диарея, резорбция костей вследствие активации остеокластов и проблемы со стороны сердца. Поэтому для пациентов важна возможность полагаться на надежные лекарственные формы, обеспечивающие точные дозы.
Пероральный путь удобен для введения гормонов Т4 и Т3. Несмотря на то, что гормоны Т4 и Т3 оба являются терапевтически эффективными, обычно предпочтительно вводить Т4, поскольку Т3 слишком быстро всасывается из кишечника и, это может вызвать токсическое действие тиреоидного гормона (гипертиреоз). Смеси из Т3 и Т4 также не являются предпочтительными, поскольку эти два гормона обладают разной фармакокинетикой и активностью, что осложняет определение подходящего режима дозирования для пациента.
Гормон Т4 удобно вводить в форме раствора, обеспечивающего более точное дозирование, чем твердые формы; тем не менее, введение растворов Т4 связано с рядом проблем: фактически, сообщается, что во время хранения наблюдается преждевременное частичное превращение в Т3; степень превращения сложно предсказать, поскольку на скорость превращения могут влиять различные внешние условия. Как следствие, в момент введения, в растворах Т4 могут содержаться непрогнозируемые, иногда значительные уровни Т3; это приводит к введению фактически неточной дозы гормона с риском передозировки в связи с повышенной активностью Т3; в силу значительно более высокой активности Т3 по сравнению с Т4, даже малое количество образовавшегося Т3 может значительно увеличить общую дозу введенного гормона с потенциальными последствиями для пациента, обусловленными передозировкой.
Другая сложность вытекает из низкой водной растворимости тиреоидных гормонов, которая обуславливает их частичное осуждение (преципитацию) из растворов во время хранения и/или вследствие температурных изменений; о частичном улучшении в этой области сообщается в WO 2010/086030, где тиреоидные гормоны находятся в составе водно-спиртово-глицериновых растворов, демонстрирующих хорошую стабильность; стабильность дополнительно улучшилась при упаковке раствора в емкости, сделанные из специальных полимеров. В попытке дополнительно повысить стабильность, в WO 2013072304 описаны другие упакованные растворы, характеризующиеся тем, что раствор в воде, спирте и глицерине имеет двойную упаковку (т.е., содержится в пластмассовой емкости, которая находится в саше), или одинарную упаковку в модернизированной многослойной пластмассовой емкости. Тем не менее, в этих условиях также наблюдалась значительная степень нестабильности в отношении превращения Т4 в Т3. Поэтому все еще сохраняется потребность в упакованных растворах Т4, которые остаются стабильными в течение срока хранения, в частности, в среднем/длительном периоде, т.е., 12/18 месяцев, при комнатной температуре, что обеспечивает возможность хранения препарата в течение достаточно длительного времени при нормальных внешних условиях, которые, как правило, встречаются в аптеке или больнице.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящее время неожиданно обнаружено, что нежелательное преждевременное превращение Т4 в Т3 в упакованном растворе может значительно снизиться, если Т4 будет находиться в составе водно-глицериновых, бесспиртовых растворов. Настоящее изобретение относится к высокостабильным, бесспиртовым, водно-глицериновым растворам тиреоидного гормона Т4 со сниженным количеством примеси Т3, в готовой к применению упаковке посредством емкостных систем, подходящих для поддержания общей стабильности раствора. Емкость является мультибарьерной, в них несколько слоев из разных материалов отделяют раствор от контакта с внешней средой.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В целях настоящего изобретения термин «бесспиртовый раствор» означает, что в растворе не содержатся низкомолекулярные спирты; термин «низкомолекулярный спирт» означает алканол с молекулярной массой менее 80 Дальтон: например, метанол, этанол, пропан, пропандиол, изопропанол и аналогичные спирты; термин «бесспиртовый», таким образом, не исключает присутствия глицерина в растворе (молекулярная масса которого составляет 92,1 Дальтон).
Применяемая в настоящем изобретении упаковка является мультибарьерной, т.е. упаковкой, в которой несколько слоев несколько слоев из разных материалов отделяют раствор от контакта с внешней средой; слои могут быть частью одной и той же емкости и/или могут принадлежать к разным емкостям, находящихся одна в другой, причем раствор Т4 находится в самой внутренней емкости. В частности, упаковка может быть выполненая в соответствии со следующими опциями:
(a) емкость из однокомпонентного ПЭНП-пластика, расположенная в запечатанном саше, состоящем из слоистых (laminated) пленок, выполненных из различных материалов, выбранных из следующих: полиэтилена, алюминия, полиэтилентерефталата, иономерных смол, бумаги, сополимерных смол этилена и винилового спирта, полипропилена и фторированных-хлорированных смол;
(b) емкость из многокомпонентного слоистого пластика, характеризующаяся множеством слоев пластмассовых материалов, соответствующим образом выбранных из полиэтилена, сополимерных смол этилена и винилового спирта, поливинилхлорида, поливинилиденхлорида, поливинилацетата, фторированных-хлорированных смол, иономерных смол, циклоолефиновых сополимеров, полиамида, полистирола, поликарбоната, слоистых металлов и, в частности, алюминия, связанного с пластиками.
В предпочтительном варианте пластиковая емкость, указанная в пункте (а) и (b), поддается сжатию рукой; кроме того, в предпочтительном варианте указанная емкость, указанная в пункте (а) и/или (b), име толщину от 150 до 10000 мкм, более предпочтительно от 200 до 800 мкм, например, 600 мкм ± 15%. Вышеуказанная опция (а) включает вариант, отличающийся тем, что более чем одна пластиковая емкость из ПЭНП, каждая из которых наполнена раствором Т4, находится в одном саше, содержащем все емкости. В одном предпочтительном варианте опции (а) саше состоит из слоистых пленок, выполненных из различных материалов согласно следующим комбинациям: полиэтилен, алюминий и полиэтилентерефталат; полиэтилен, алюминий и бумага, иономерные смолы, алюминий и бумага.
В стабильность раствора Т4 значительный вклад вносит сумма толщин всех пленок, составляющих саше, т.е., общей толщиной саше, состоящего из вышеупомянутых специальных слоистых пленок: она должна находиться предпочтительно в диапазоне от 40 до 100 мкм, более предпочтительно от 50 до 90 мкм; эти условия удачно сочетают эффективную защиту от разложения Т4 до Т3, позволяя в то же время избежать избыточного применения упаковочного материала; в случае необходимости в настоящем изобретении также могут применяться значения выше 90 мкм, хотя они не являются предпочтительными. Примеры вышеописанных упаковочных систем (не в связи с бесспиртовыми растворами гормона Т4) описаны в заявке на патент WO 2013/072304, включенной в данный документ посредством ссылки.
Водно-глицериновый раствор, применяемый в настоящем изобретении обычно может содержать Т4:глицерин в массовом соотношении от 0,004:1000 до 0,4:1000 (т.е., от 4 до 4000 ppm) Если лекарственная форма в виде раствора является дозированной лекарственной формой, то подходящая единица дозирования обычно содержит от 5 до 350 мкг (или предпочтительно от 5 до 250 мкг) в 1 г глицерина.
Все соотношения и количества глицерина в настоящем документе рассчитаны для глицерина в виде чистого вещества; однако на практике применяется глицерин в виде концентрированного раствора в воде, как правило, при 85% об./об.; таким образом, понятно, что содержание водного компонента настоящих растворов можно получить, по меньшей мере частично из воды, содержащейся в коммерческом глицерине; содержание воды глицерина 85% обычно достаточно для получения растворов согласно настоящему изобретению; в любом случае, добавление дополнительных количеств воды остается возможным в рамках изобретения.
Настоящие растворы Т4 содержат сниженное количество примеси Т3, где «сниженное» означает, что Т3 может присутствовать в максимальной концентрации 2,5%, предпочтительно 2,0%, более предпочтительно 1,8%. Указанные значения примеси Т3 рассчитываются в данном документе следующим образом: (Т3 мкг/мл, присутствующий в образце/Т4 мкг/мл, присутствующий в образце) * 100. Сниженное количество примеси Т3 является следствием достигаемого высокого уровня стабильности при хранении (в отношении ограниченного превращения Т4 в Т3), что находит подтверждение в экспериментальном разделе; в частности, в конце периода стабильности (25°С±2°С/60±5% ОВ), фармацевтический препарат согласно настоящему изобретению показал содержание Т4 менее 95% от исходной концентрации, а общее количество примесей - в пределах стандартных критериев допустимого.
Более того, фармацевтический препарат согласно настоящему изобретению гарантирует отсутствие микробиологического заражения со значениями ОКАМ (общее количество аэробных микроорганизмов) ≤ 100 КОЕ/г, значениями ОКДПГ (общее число дрожжевых и плесневых грибов) ≤ 10 КОЕ/г и с отсуствием Е. coli, таким образом, он пригоден для применения и не подвержен случайному загрязнению.
Высокий уровень стабильности при хранении, достигаемый с помощью настоящих водно-глицериновых растворов, полностью исключает необходимость введения стабилизаторов в состав, (например, препаратов, корректирующих рН, буферов, хелатирующих агентов и т.д.); в объединенной лекарственной форме составы настоящего изобретения имеют дополнительные преимущества, заключающиеся в исключении необязательного введения добавок пациенту и снижении соотношения сложность/стоимость готового лекарственного препарата.
Фармацевтический препарат согласно настоящему изобретению удобен в применении в лечении нарушений, ассоциированных с дефицитом тиреоидных гормонов Т3 и/или Т4. В предпочтительном варианте он вводится перорально, т.е. подходит для перорального введения. Отмечается, что, несмотря на отсутствие Т3 в настоящих растворах Т4 (или присутствие в чрезвычайно низких количествах), диапазон их применения охватывает также лечение дефицита Т3, поскольку Т4 физиологически превращается в Т3 в организме после введения.
Соответственно, следующий аспект настоящего изобретения относится к применению водно-глицеринового раствора тиреоидного гормона Т4 в описанной выше упаковке для приготовления лекарственного препарата (медикамента) для лечения нарушений, ассоциированных с дефицитом тиреоидного гормона Т3 и/или Т4; указанный лекарственный препарат предпочтительно подходит для перорального введения.
Следующий аспект настоящего изобретения относится к фармацевтическому препарату водно-глицеринового раствора тиреоидного гормона Т4 в описанной выше упаковке для применения в лечении нарушений, ассоциированных с дефицитом тиреоидного гормона Т3 и/или Т4; указанный препарат предпочтительно подходит для перорального введения.
Следующий аспект настоящего изобретения относится к способу лечения нарушений, ассоциированных с дефицитом тиреоидного гормона Т3 и/или Т4, включающего введение водно-глицеринового раствора тиреоидного гормона Т4, упакованного как описано выше, нуждающемуся в этом пациенту; указанный раствор предпочтительно подходит для перорального введения.
Таким образом, в настоящем изобретении предложены по-новому упакованные растворы Т4, которые обладают преимуществом более высокой стабильности в отношении нежелательного преждевременного превращения Т4 в Т3. Повышенная стабильность гарантирует более воспроизводимое и постоянное количество вводимого гормона, исключая любую возможную передозировку вследствие избыточного введения примесей Т3. Отсутствие применения летучих спиртов, как например, этанола, дает дополнительное преимущество, заключающееся в том, что лекарственная форма не подвержена случайному уменьшению содержания спиртов, что отражается на нежелательном изменении растворимости/стабильности гормона раствора. Кроме того, отсутствие таких спиртов в настоящих водно-глицериновых растворах не оказывает существенного влияния на общую стабильность раствора в отношении активности Т4, общих примесей и микробного заражения, что, таким образом, приводит к получению препарата, соответствующего всем критериям приемлемости для фармацевтического применения.
ЭКСПЕРИМЕНТЫ
В настоящем документе используются следующие акронимы: полиэтилен (ПЭ), полиэтилентерефталат (ПЭТ), сополимерные смолы этилена и виниловых спиртов (EVOH), поливинилхлорид (ПВХ), полив инилден хлорид (ПВдХ), поливинил ацетат (ПВА), циклоолефиновый сополимер (ЦОС), полиамиды (ПА), полистирол (ПС), поликарбонат (ПК).
ПРИМЕР 1: водно-этанола-глицериновый раствор Т4 (стандарт)
Референсная (контрольная) лекарственная форма приготовлена в соответствии с примером 1 WO 2013/072304. Соответственно, один литр водно-спиртового раствора, содержащего 100 мкг/мл Т4, приготовлен следующим образом с использованием нижеприведенного качественного/количественного состава:
1) Т4 0,105 г
2) этанол (96%) 243 г
3) глицерин (85%) 861 г
Т4 растворили в этаноле в подходящей емкости, постоянно перемешивая при комнатной температуре. После получения прозрачного раствора без видимого нерастворимого осадка, добавили глицерин и получили однородный, прозрачный, бесцветный раствор, слегка перемешивая при комнатной температуре. Раствор фильтровали (0,8 мкм), после чего он был готов для упаковки. Итоговая концентрация Т4 в растворе составила 100 мкг/мл. В соответствии с этим же способом готовили следующие растворы, имеющие итоговые концентрации 25 мкг/мл, 50 мкг/мл, 75 мкг/мл.
Упаковочная система, сделанная согласно примеру 3 документа WO 2013/072304, состояла из следующих компонентов: однодозовая емкость с номинальным объемом 1,10 мл, выполненная из однокомпонентного LDPE -пластика (толщиной 600 мкм), содержащаяся в запечатанном саше (РЕТ/А1/РЕ). Характеристики саше:
- Многослойнвя пленка с низкой проницаемостью для газа и света:
- Полиэтилентерефталат 12 мкм (значение должно рассматриваться с погрешностью ± 5-6%);
- Al (алюминий) 9 мкм, (значение должно рассматриваться с погрешностью ± 5-6%);
- Полиэтилен 50 мкм (значения должны рассматриваться с погрешностью ± 5-6%);
- Общая толщина: 71 мкм.
- Проницаемость кислорода: 0,1-0,2 см3/м2/сутки - Водопаропроницаемость: 0,1-0,2 г/м2/сутки
Проницаемость для кислорода измерялась в соответствии со стандартом Американского общества специалистов по испытаниям материалов (ASTM) D-3985. Водопроницаемость измерялась в соответствии со стандартом Американского общества специалистов по испытаниям материалов (ASTM) Е-398.
Прототипы были изготовлены в лабораторном масштабе с применением автоматической пипетки (Gilson Р-1000) для заполнения одноразовых емкостей 1,1 мл ранее описанным водно-глицерин-этаноловым раствором, после чего емкости были запечатаны с помощью настольного запаечного устройства «Pentaseal-lab». Далее их упаковали в герметически запечатанное саше вышеописанного типа.
ПРИМЕР 2: водно-глицериновый раствор Т4
Приготовили ряд растворов в соответствии с приведенным выше референсным Примером 1, заменяя вышеописанный водно-этанола-глицериновый раствор бесспиртовым водно-глицериновым раствором согласно настоящему изобретению. Соответственно, следующие возрастающие количества гормона Т4 растворяли в 1,222 г глицерина 1,85%: 25 мкг, 50 мкг, 75 мкг, 100 мкг, получая соответствующие итоговые концентрации:
25 мкг/мл, 50 мкг/мл, 75 мкг/мл, 100 мкг/мл.
Упаковочная система: однодозовая емкость с номинальным объемом 1,10 мл, выполненная из однокомпонентного LDPE-пластика (толщиной 600 мкм), содержащаяся в запечатанном саше (РЕТ/Al/РЕ). Характеристики саше: Многослойная пленка с низкой проницаемостью для газа и света: Полиэтилентерефталат 12 мкм, Al 12 мкм, полиэтилен 45 мкм, (все значения должны рассматриваться с погрешностью ± 5-6%); Общая толщина: 69 мкм.
ПРИМЕР 3 Исследования стабильности при хранении
Упакованные растворы, полученные в предыдущих примерах 1 и 2, подвергали испытаниям стабильности при хранении с целью, в частности, оценки степени превращения Т4 в Т3 во время хранения, как в нормальных, так и ускоренных условиях. При этом запечатанные саше опустили в испытательные камеры с подходящей средой, и сразу же провели исследование стабильности в условиях, утвержденных МКГ; используемый аппарат откалибровали и сразу же проверили на исправность работы. В следующих таблицах показаны сравнимые показатели препаратов, полученных в Примерах 1 и 2.
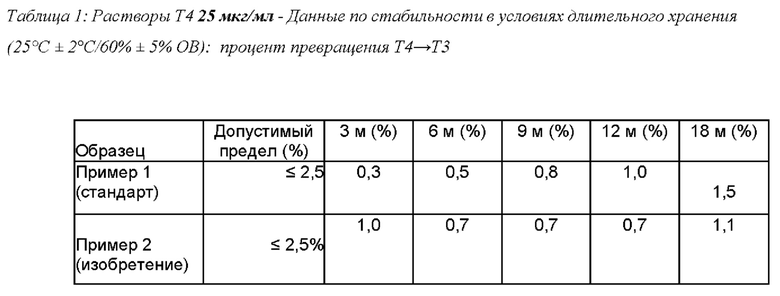

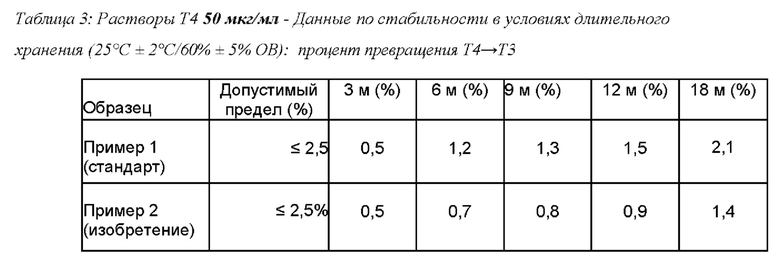
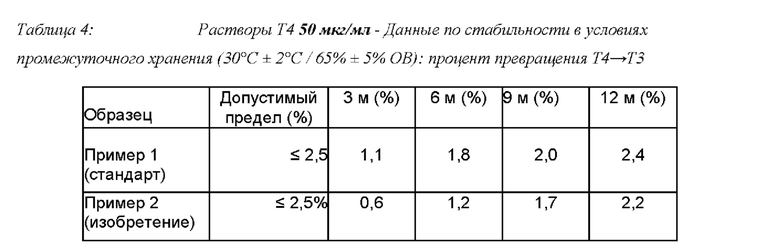

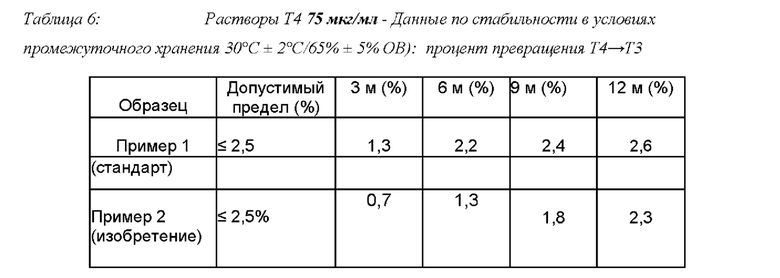
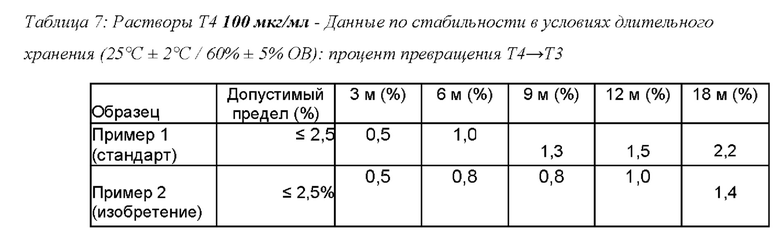

Можно отметить, что все испытанные образцы согласно изобретению практически во всех дозах, при всех сроках и условиях хранения продемонстрировали устойчивое снижение превращения Т4 в Т3. Таким образом, цели настоящего изобретения достигнуты.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОДНОДОЗОВЫЙ ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ТИРЕОИДНЫХ ГОРМОНОВ Т3 И/ИЛИ Т4 | 2012 |
|
RU2688430C2 |
| СПОСОБ ОЧИСТКИ КРОВИ ОТ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ С ПОМОЩЬЮ ИММОБИЛИЗИРОВАННОГО ГРАНУЛИРОВАННОГО МАГНИТОУПРАВЛЯЕМОГО ПРЕПАРАТА | 2007 |
|
RU2366958C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ТИРЕОТОКСИКОЗА И КОЛЛОИДНОГО ЗОБА | 2007 |
|
RU2357296C1 |
| Способ дифференциальной диагностики йоддефицитного и йодиндуцированного нарушения функции щитовидной железы у лиц, проживающих в регионах с йодным дефицитом | 2019 |
|
RU2728261C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИФФУЗНОГО ЭУТИРЕОИДНОГО ЗОБА | 2007 |
|
RU2350337C1 |
| СПОСОБ ОЧИСТКИ АНТИТЕЛ К ТИРЕОИДНЫМ ГОРМОНАМ | 1987 |
|
SU1484094A1 |
| Фармацевтическая композиция для профилактики и лечения гипотиреоза щитовидной железы | 2018 |
|
RU2708260C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ ДОБАВКИ К ПИЩЕ ДЛЯ ОПТИМИЗАЦИИ ЙОДНОГО ОБМЕНА | 2005 |
|
RU2271725C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ НАРУШЕНИЙ ФУНКЦИИ МИОКАРДА У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ НА ФОНЕ ПРОГРЕССИРУЮЩЕГО ГИПОТИРЕОЗА С АКТИВАЦИЕЙ ПЕРЕКИСНОГО МЕТАБОЛИЗМА | 2000 |
|
RU2219923C2 |
| Способ ранней диагностики первичного гипотиреоза | 2019 |
|
RU2722740C1 |
Изобретение относится к растворам тиреоидного гормона Т4. Набор для лечения заболеваний, ассоциированных с дефицитом гормона Т3 и/или Т4, включает фармацевтический препарат тиреоидного гормона Т4 в готовой к использованию упаковке, состоящий из емкости, предварительно заполненной бесспиртовым водно-глицериновым раствором гормона Т4, причем раствор не содержит агентов, корректирующих рН, причем емкость выбрана из: (а) емкости из однокомпонентного LDPE-пластика, расположенной в запечатанном саше, имеющем общую толщину от 40 до 100 мкм и состоящем из слоистых пленок, выполненных из полиэтилена, алюминия и полиэтилентерефталата; (b) емкости из многокомпонентного слоистого пластика, причем емкость содержит множество слоев пластиковых материалов, выбранных из: полиэтилена, сополимерных смол этилена и винилового спирта, поливинилхлорида, поливинилиденхлорида; поливинилацетата, фторированных-хлорированных смол, иономерных смол, циклоолефиновых сополимеров, полиамида, полистирола, поликарбоната, плакированных металлов и алюминия, связанного с пластмассовыми материалами; причем пластиковая емкость, упомянутая в (а) и/или (b), имеет толщину от 150 до 1000 мкм. Изобретение обеспечивает высокостабильные растворы тиреоидного гормона Т4 со сниженным количеством примеси Т3. 9 з.п. ф-лы, 8 табл., 3 пр.
1. Набор для лечения заболеваний, ассоциированных с дефицитом гормона Т3 и/или Т4, включающий фармацевтический препарат тиреоидного гормона Т4 в готовой к использованию упаковке, состоящий из емкости, предварительно заполненной бесспиртовым водно-глицериновым раствором гормона Т4, причем указанный раствор не содержит агентов, корректирующих рН, причем указанная емкость выбрана из:
(а) емкости из однокомпонентного LDPE-пластика, расположенной в запечатанном саше, имеющем общую толщину от 40 до 100 мкм и состоящем из слоистых пленок, выполненных из полиэтилена, алюминия и полиэтилентерефталата;
(b) емкости из многокомпонентного слоистого пластика, причем указанная емкость содержит множество слоев пластиковых материалов, выбранных из: полиэтилена, сополимерных смол этилена и винилового спирта, поливинилхлорида, поливинилиденхлорида; поливинилацетата, фторированных-хлорированных смол, иономерных смол, циклоолефиновых сополимеров, полиамида, полистирола, поликарбоната, плакированных металлов и алюминия, связанного с пластмассовыми материалами;
причем пластиковая емкость, упомянутая в (а) и/или (b), имеет толщину от 150 до 1000 мкм.
2. Набор по п. 1, характеризующийся тем, что массовое отношение Т4/глицерин в указанном водно-глицериновом растворе составляет от 4 до 400 ppm
3. Набор по пп. 1-2, характеризующийся тем, что указанный водно-глицериновый раствор содержит менее 2,5% примеси Т3.
4. Набор по пп. 1-3, характеризующийся тем, что указанный водно-глицериновый раствор содержит менее 2,0% примеси Т3.
5. Набор по пп. 1-4, характеризующийся тем, что указанный водно-глицериновый раствор содержит менее 1,8% примеси Т3.
6. Набор по пп. 1-5, характеризующийся тем, что препарат находится в однодозовой форме, содержащей от 5 до 350 мкг тиреоидного гормона Т4.
7. Набор по пп. 1-6, характеризующийся тем, что препарат находится в однодозовой форме, содержащей от 5 до 250 мкг тиреоидного гормона Т4.
8. Набор по пп. 1-7, характеризующийся тем, что указанная пластиковая емкость, упомянутая в (а) и/или (b), имеет толщину от 200 до 800 мкм.
9. Набор по пп. 1-8, характеризующийся тем, что указанное саше имеет общую толщину от 50 до 90 мкм.
10. Набор по пп. 1-9 для применения в лечении заболеваний, ассоциированных с дефицитом гормона Т3 и/или Т4.
| WO 2013072304 A1, 23.05.2013 | |||
| US 20140073695 A1, 13.03.2014 | |||
| Сутягин В.М | |||
| и др | |||
| Химия и физика полимеров: Учебное пособие | |||
| - Томск: Изд-во ТПУ, 2003 | |||
| Гидравлическая или пневматическая передача | 0 |
|
SU208A1 |
| Boulton D.W | |||
| Et Al | |||
| Stability of an extemporaneously compounded levothyroxine sodium oral liquid // Am J Health Syst Pharm | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Способ и машина для механической выделки стеклянных изделий | 1925 |
|
SU1157A1 |
Авторы
Даты
2022-02-01—Публикация
2017-10-17—Подача