ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области медицины, а конкретно - к ингибитору mTOR, фармацевтической композиции и их применению.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Опухоль - распространенное и часто встречающееся заболевание. Она представляет собой новообразование или неоплазмы, образующиеся посредством клональной атипической пролиферации и дифференциации по причине утраты нормальной регуляции роста и дифференциации клеток тканей организма из-за мутации генов при продолжительном воздействии различных внутренних и внешних онкогенных факторов. Опухоли подразделяют на доброкачественные и злокачественные, и последние дополнительно разделяются на три вида: раковые, возникающие в эпителиальных тканях, саркомы, возникающие в мезенхиме, и карциносаркомы. В отношении всех злокачественных опухолей в целом используется термин «рак».
Злокачественные опухоли - одно из основных опасных заболеваний, угрожающих здоровью человека. В настоящий момент они - причина смертности номер один в мире. Согласно новейшим статистическим данным в 2007 году около 7,9 миллионов человек в мире умерли от различных видов рака, что составило 13% от всех летальных исходов. Были диагностированы более 12 миллионов случаев заболевания раком, из которых 72% или более пациентов, заболевших раком, и летальных исходов пришлись на развивающиеся страны, и это число демонстрирует тенденцию к росту. В 2015 году число умерших от рака в мире выросло до 9 миллионов человек, и ожидается, что к 2030 году оно превысит 12 миллионов человек. В настоящее время ежегодное количество случаев заболевания раком в Китае составляет около 2,8 миллионов, а количество смертей от рака превышает 400000, занимая первое место среди различных заболеваний в Китае и демонстрируя тенденцию к возрастанию. По мере ускорения ритма социальной жизни, возрастания конкурентного давления и изменений человеческого образа жизни и окружающей среды случаи развития рака и летальных исходов растут от года к году. Он стал распространенным и часто встречаемым заболеванием в современном обществе, не только оказывая серьезное влияние на качество жизни пациентов, но также ложась тяжелым экономическим и моральным бременем на семьи пациентов и общество. Также он представляет собой важную социальную проблему, обременяющую мир. Лечение и профилактика рака всегда были одними из наиболее острых проблем в мире.
Ингибитор в виде мишени рапамицина у млекопитающих (mTOR) представляет собой атипическую серин/треонин протеинкиназу и является одним из представителей семейства протеинкиназ, связанных с фосфоинозитид-3-киназой (PI3K). mTOR существует в виде двух комплексов - mTORC1 и mTORC2 in vivo. В mTOR могут быть интегрированы множество внеклеточных сигналов, таких как питательный, энергетический и ростовой факторы, он может участвовать в таких биологических процессах, как транскрипция генов, трансляция белков, рибосомный и цитоскелетный синтезы, а также играет крайне важную роль в росте, пролиферации, апоптозе и метаболизме клеток. Исходными стимулирующими факторами для задействования сигнального пути, в основном, служат аминокислоты, различные ростовые факторы и гипоксия. mTOR существует в виде двух комплексов - mTORC1 и mTORC2 in vivo.
Путь PI3K/AKT/mTOR представлен сигнальным путем, регулирующим активность клеток у млекопитающих, и этот путь важен для выживания, роста и пролиферации клеток. Важные митогены (инсулины, гормоны, ростовые факторы и т.п.) задействуют молекулы, расположенные со стороны клеточной мембраны, вблизи цитоплазмы, за счет чего задействуется PI3K, важная молекула в пути mTOR. Активированная PI3K содействует преобразованию фосфатидилинозитол (4,5)-бисфосфата (PIP2) в фосфатидилинозитол (3,4,5)-трифосфат (PIP3), связывающий домен PH Akt, а также сопровождается фосфорилированием Akt другими киназами, что в итоге приводит к деполимеризации комплексов туберозного склероза 1 и 2 (TSC1/2) и/или фосфорилированию PRAS40 (пролин-богатый субстрат AKT 40000) для положительной регуляции mTORC1. В опухолях различных типов, включая немелкоклеточный рак легкого, рак эндометрия, рак шейки матки и т.д., часто возникают нарушения сигнального пути PI3K/AKT/mTOR.
Кроме того, другие стрессогенные факторы окружающей среды также могут регулировать сигнальный путь mTOR. Например, долговременный недостаток незаменимого кислорода при клеточном метаболизме приводит к недостатку энергии и способствует медиации ингибирования mTORC1 со стороны серин/треонинкиназы, печеночной киназы В1 (LKB1, печеночная киназа В1) или AMPK. Наличие энергии также является важным регулятором активности mTOR. В качестве «датчика энергии» mTORC1 может использоваться АМФ-активируемая протеинкиназа (AMPK). При недостатке энергии уровень АМФ в клетке повышается, связывает AMPK и активирует ее посредством киназ против хода транскрипции. После активации AMPK может фосфорилировать TSC2, повышать процесс расщепления способности продуцирования и снижать энергоемкие процессы синтеза, такие как белковый синтез.
Наиважнейшей особенностью активации mTORC1 является белковый синтез. mTORC1 непосредственно фосфорилирует гидрофобную группу Thr389 p70 рибосомальной протеинкиназы S6-1 (S6K1), за счет чего происходит фосфорилирование последующего белка за счет воздействия на PDK1. Фосфорилирование S6K1 активирует несколько субстратов по ходу транскрипции для содействия трансляции мРНК, включая eIF4B, положительный регулятор комплекса eIF4F. mTORC1 непосредственно фосфорилирует фактор инициации эукариот по ходу транскрипции, 4Е-связывающий белок 1 (4E-BP1). Фосфорилирование 4E-BP1 предотвращает его связывание с кэп-связывающим белком eIF4E, за счет чего обеспечивается возможность его участия в активации формирования комплекса eIF4F, необходимой для трансляции, зависящей от кэп-белка. Фосфорилирование S6K1 и 4E-BP1 активирует трансляцию мРНК, за счет чего повышается уровень активности различных эффекторов. mTORC1 имеет очень важное значение при трансляции мРНК. Ингибитор активного сайта mTOR может полностью ингибировать функцию mTORC1, за счет чего снижается белковый синтез в клетке. В дополнение к регулированию белкового синтеза mTORC1 также контролирует синтез липидов, необходимых для клеточных мембран. В то же время, mTORC1 также активно медиирует клеточный метаболизм и синтез АТФ.
mTORC2 состоит из mTOR, mLST8, Deptor, Rictor (рапамицин-интенсивный компаньон mTOR), стресс-активируемой протеинкиназы белка 1 млекопитающих (mSIN1) и Protor 1/2 (белка, наблюдаемого с Rictor-1/2). Посредством mSIN1 и протеинкиназы С-α (PKCα) mTORC2 может участвовать в регуляции актина и формировании цитоскелета. Высокая экспрессия mTORC2 может способствовать выживанию клетки, в то время как низкая экспрессия mTORC2 приводит к апоптозу.
Ключевой стадией на пути mTORC2 является регулировка и ингибирование преобразования PIP2 в PIP3 посредством протеинфосфатазы (PTEN, фосфатаза и гомолог тензина, делированный на хромосоме 10). mTORC1 может косвенно активировать mTORC2 за счет задействования биосинтеза рибосом и ингибирования оборота рибосом, медиированного аутофагией. Активация mTORC2 приведет к фосфорилированию серина 473 Akt (Ser473), и Akt далее индуцирует фосфорилирование SIN1-T86, рост активности mTORC2, что будет содействовать формированию положительной петли, но ингибирование комплекса TSC1/2 ослабит этот процесс.
Во многих опухолях человека mTOR активируется с нарушениями. Применение ингибиторов mTOR может эффективно ингибировать сигнальный путь PI3K/Akt/mTOR, активированного с нарушениями, в различных опухолевых клетках, таких как рак легких, рак молочной железы, рак поджелудочной железы, рак желудка, меланома, глиома, рак печени и т.д., за счет чего происходит ингибирование миграции и внедрения опухолевых клеток и эпителиально-мезенхимальной трансформации. У высокого процента больных раком имеются мутации на онкогенном пути до mTORC1, включая пути PI3K/AKT/mTOR и Ras/Raf/MEK/ERK. Мутации в двух вышеприведенных путях приводят к избыточной активации mTORC1. Кроме того, распространенные онкосупрессоры TP53 и LBK1 являются отрицательными регуляторами TSC1 и TSC2 против хода транскрипции mTORC1. Нисходящие факторы mTORC1 также вовлечены в опухолеобразование. Сверхэкспрессия генов eIF4E и S6K1 и белков присутствует во многих видах рака, среди которых наиболее критичной является фосфорилирование 4E-BP1. Клеточные линии на основе AKT и ERK зависят от фосфорилирования 4EBP. Помимо этого, ингибиторы mTOR могут изменять степень экспрессии 4EBP и eIF4E и, таким образом, оказывать сильное ингибирующее воздействие на пролиферацию этих клеток.
При раке также вовлекается сигнализация mTORC2, что в основном связано с его ролью в активации Akt. Активированная Akt содействует процессам пролиферации, таким как поглощение глюкозы и гликолиз, с одновременным ингибированием апоптоза. Фактически, опухоли, обусловленные PI3K/Akt, также зависят от активности mTORC2. У мышиных моделей рака предстательной железы отсутствует PTEN в том виде, в каком он присутствует в человеческих клетках рака предстательной железы.
Активация пути трансдукции сигналов PI3K/AKT/mTOR может привести к ингибированию апоптоза, обусловленного различными стимулами, содействовать прогрессии цикла, выживанию клеток и пролиферации, а также обеспечивать участие в ангиогенезе, встраиванию опухолей и метастазировании, равно как и играть важную роль в опухолеобразовании. AKT может регулировать множество белков, связанных с апоптозом, для ингибирования последнего. Сверхэкспрессия AKT повышает экспрессию ингибирующего фактора 1 апоптотического белка (Dap-1), который участвует в ингибировании апоптоза. AKT также может передавать сигналы выживания посредством фосфорилирования mTOR и его молекул по ходу транскрипции S6K1 и 4E-BP1, ингибировать P53-независимый апоптоз, а также содействовать выживанию клеток. В последние годы в отношении различных опухолей было установлено, что eIF-4E демонстрируют трансформацию клеток и антиапоптотическое воздействие in vitro, а сверхэкспрессия eIF-4E может защитить клетки от определенных преапоптозных эффектов.
Киназы, регулируемые внеклеточными сигналами (ERK), в которые включают ERK1 и ERK2, являются ключевым фактором передачи сигналов от поверхностных рецепторов к ядру. ERK1/2, активируемая фосфорилированием, транслоцируется из цитоплазмы в ядро, что, в свою очередь, медиирует транскрипционную активацию Elk-1, АТФ, Ap-1, c-fos и c-Jun, а также участвует в клеточной пролиферации и дифференцировке, сохранении морфологии клеток, построении цитоскелета, апоптозе и перерождении клеток в рак. ERK регулируют пролиферацию, дифференцировку и выживание клеток, а также представляют собой белки по ходу транскрипции с различными факторами роста (EGF, NGF, PDGF и т.д.). ERK и ее сигнальные пути играют свою роль в интермедиации и усилении сигналов при процессах встраивания опухолей и переноса. С одной стороны, она принимает большое количество сигналов от факторов роста, митогенов, внешних стимулов и т.д. С другой стороны, она воздействует на факторы ядерной транскрипции, такие как AP-1 и NF-kB и т.п., посредством реакции на сигнальный каскад и регулирует экспрессию генов. Избыточная активация ERK обнаруживается во многих видах рака у людей (например, рак ротовой полости, меланома, рак молочной железы и т.д.). Стандартным путем является Ras/Raf/MER/ERK.
Наибольшего внимания заслуживает то, что возникают множественные явления перекрестного взаимодействия между сигнальными путями PI3K/AKT/mTOR и ERK/MAPK, образующие сложные взаимодействия. Взаимодействие между этими двумя путями может быть представлено взаимоингибированием или взаимоактивацией. Сигнальные пути PI3K/AKT/mTOR и ERK/MAPK играют важную роль в росте, пролиферации, дифференцировке, встраивании, метастазировании и резистентности опухолевых клеток к медикаментам. Их функции и механизмы регулировки чрезвычайно сложны. Ингибирование одного из этих сигнальных путей не приводит к желаемому терапевтическому эффекту, и основной причиной этого служит усложненное перекрестное взаимодействие, возникающее между ними.
Ингибиторы в виде mTOR, такие как рапамицин и его производные, «рапалоги», в частности, могут приводить к ингибированию mTORC1, обладать концентрацией и оказывать время-зависимое ингибирующее воздействие на рост различных опухолевых клеток, а также могут повышать чувствительность опухолевых клеток к химиотерапевтическим медикаментам, обусловливать возникновение апоптоза, а также одновременно обеспечивать синергическое действие.
Карримицин, также известный как биотекспирамицин и шэнцзимицин, представляет собой новый вид антибиотика с главным компонентом, представленным 4''-изовалерил-спирамицином, получаемым клонированием гена 4''-изовалерил-трансферазы (4''-о-ацил-трансферазы) штамма-продуцента карбомицина в штамме-продуценте спирамицина посредством технологии генной модификации, направленного ацилирования спирамицина 4''-OH и добавления боковой цепи изовалерила в положение 4'', который является результатом сотрудничества института биотехнологии Китайской академии медицинских наук и заявителя.
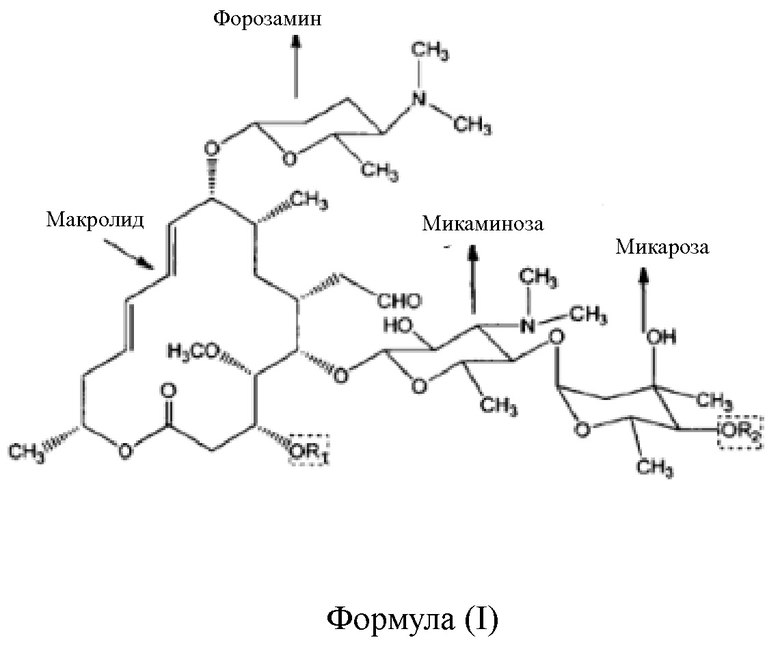
Карримицин состоит из множества производных спирамицина с общей концентрацией основных действующих ингредиентов - изовалерил-спирамицинов (I+II+III) - не менее 60%, общей концентрацией ацилированного спирамицина не менее 80%, и является фармацевтически приемлемой композицией. Центральная структура представляет собой 16-членный макролид, соединенный с молекулой форозамина, молекулой микаминозы и молекулой микарозы. Основные компоненты карримицина - изовалерил-спирамицины I, II, III - отличаются от строения спирамицина тем, что группа, объединенная с положением 4'' микарозы, представлена изовалерилом вместо гидроксила. Химическое строение карримицина представлено в формуле (1), и он содержит более десяти видов компонентов. В настоящее время стандарт композиции конечного продукта карримицина имеет следующий вид: изовалерил-спирамицин III ≥30%, общее соотношение изовалерил-спирамицина I, II, III ≥60%, общая пропорция ацилированного спирамицина ≥80%, и совокупность прочих неустановленных компонентов ≤5%.
Карримицин - 16-членный макролидный антибиотик, имеющий активные группы: карбоксильную, алкоксильную, эпокси-группу, кетонную и альдегидную, а также пару сопряженных С=С, и обладает молекулярной массой приблизительно 884-982. Благодаря схожему химическому строению карримицин и макролидные антибиотики имеют много общего: они легкорастворимы в большинстве органических растворителей, таких как сложные эфиры, ацетон, хлороформ и спирты, слаборастворимы в петролейном эфире и нерастворимы в воде; их молекулярное строение включает две диметиламино группы, имеет слабую щелочность и, таким образом, они легкорастворимы в кислых водных растворах; также они обладают «отрицательной растворимостью», при которой с повышением температуры растворимость падает. Поскольку изовалерил-спирамицин, основной компонент карримицина, обладает удлиненной углеродной цепью в положении 4'' и слабой гидрофильностью, его растворимость в воде ниже, чем у спирамицина и 4'-ацетилспирамицина.
Карримицин - белый некристаллический порошок со слабой гигроскопичностью и удельным вращением около -80,8°, с максимальной длиной волны ультрафиолетовой абсорбции, равной 231-232 нм. Сам по себе он имеет хромофорную группу со слабой флуоресценцией и выдает сильную фиолетовую реакцию при контакте с концентрированной серной или соляной кислотой с максимальным значением светопоглощения, равным 231-232 нм. Медикамент обладает хорошей липофильностью, хорошей проникаемостью в ткани, быстрой оральной абсорбцией, долгой сохраняемостью в организме и устойчивым постантибиотическим эффектом. В соответствии с отношением полезного действия и химической конформации после ацеляции положения 4'' макролидных антибиотиков улучшилась его липофильность и активность in-vivo, а также значительно улучшились противобактериальная активность in-vivo и клинические терапевтические эффекты; при этом стабильность антибиотика в организме возрастает по мере роста углеродной цепи 4''-сложного гидроксиэфира, то есть изовалерил-спирамицин > бутирил-спирамицин > пропионил-спирамицин > ацетил-спирамицин.
Предварительные фармакодинамические испытания in vivo и in vitro показывают, что препарат не только обладает хорошей противобактериальной активностью против большинства грамположительных бактерий (G+), но также оказывает определенное воздействие на грамотрицательные бактерии (G-), а его различные технические показатели явно превосходят азитромицин, эритромицин, ацетил-спирамицин и мидекамицин. Он обладает наибольшей противобактериальной активностью против микоплазмы пневмонии, а также некоторой противобактериальной активностью против бактерий, резистентных к эритромицину, против гонококка, пневмококка, золотистого стафилококка, синегнойной палочки, гемофильной палочки, бактероидов фрагилис, легионеллы, бактероидов тетайотамикрон и палочки газовой гангрены, а также обладает слабой перекрестной резистентностью к золотистому стафилококку с клинической устойчивостью к эритромицину. В основном, карримицин будет применяться в лечении инфекционных заболеваний, вызванных грамположительными бактериями, особенно инфекций верхних дыхательных путей, а также может применяться против инфекций мочевыделительной системы и т.д.
Результаты фармакокинетических исследований показывают, что действующие компоненты карримицина, в основном, представлены изовалерил-спирамицином I, II и III. Карримицин быстро распадается на спирамицин после попадания в организм, и его пероральная абсолютная биологическая доступность в среднем составляет 91,6% на основании суммарной площади фармакокинетической кривой, AUC0-t, исходных медикаментов, изовалерил-спирамицинов I, II, III, а также активных метаболитов, спирамицинов I, II и III. В литературных источниках сообщается, что пероральная абсолютная биологическая доступность спирамицина составляет 30-40% в человеческом организме [Frydman AM et al., J Antimicrob Chemother.1988, 22(suppl B):90-103 (А.М. Фридман и соавт. Журнал противомикробной химиотерапии. 1988 г., 22 (доп. В): 90-103)]. Это указывает на то, что строение изовалерил-спирамицина явно повышает биологическую доступность спирамицина, его действующего ингредиента. Выведение карримицина из организма после одной дозы медленнее, и T1/2β составляет от 23 до 27 часов.
При проведении недавнего исследования карримицина для заявителя стало неожиданностью обнаружение, что карримицин в виде единственного действующего ингредиента или в сочетании может ингибировать белки PI3K/Akt/mTOR сигнальных путей, может применяться в качестве ингибитора mTOR, оказывает терапевтический эффект при заболеваниях, связанных с сигнальным путем PI3K/Akt/mTOR и, таким образом, обеспечивает важные экономические и социальные полезные эффекты.
Ввиду этого было предложено следующее изобретение.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая задача, которую надлежит решить посредством настоящего изобретения, заключается в преодолении недостатков предыдущего уровня техники и предложении ингибитора mTOR, фармацевтической композиции и их применения. Ингибитор mTOR, предлагаемый согласно настоящему изобретению, обладает явным ингибирующим эффектом на клетки при заболеваниях, связанных с сигнальным путем mTOR, и при этом также обеспечивается теоретическое обоснование применения и клинического продвижения ингибитора mTOR при получении лекарственных препаратов для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR, а также обеспечиваются важные экономические и социальные полезные эффекты.
Для решения вышеприведенных технических задач основная идея технического решения по настоящему изобретению следующая:
первая цель настоящего изобретения состоит в получении ингибитора mTOR, включающего один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, или сочетающего в себе два или три следующих компонента карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III.
Карримицин представляет собой смесь разных действующих ингредиентов, включающих в себя три действующих ингредиента: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, а также содержит другие примеси.
Каждый из ингредиентов карримицина - изовалерил-спирамицин I, II и III - может быть использован в качестве ингибитора mTOR по отдельности. Также эти три ингредиента могут быть использованы в любом сочетании.
Кроме того, ингибитор mTOR представляет собой аллостерический или каталитический ингибитор белков в сигнальном пути PI3K/Akt/mTOR.
Также этот каталитический ингибитор является ингибитором киназ, например, AKT.
Помимо этого, ингибитор mTOR для ингибирования активации mTORC1 и mTORC2.
Также он предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
В дополнение к этому ингибитор mTOR представляет собой медикамент, подбираемый из группы, состоящей из противоопухолевого медикамента, медикамента для лечения диабета, медикамента для лечения болезни Альцгеймера и медикамента для замедления старения, причем этот медикамент оказывает воздействие через сигнальный путь mTOR.
Также он является противоопухолевым медикаментом, оказывающим воздействие через сигнальный путь mTOR, и предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Дополнительно ингибитор mTOR является медикаментом для лечения диабета, оказывающим воздействие через сигнальный путь mTOR, и он предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Также он представляет собой медикамент для лечения болезни Альцгеймера, оказывающий воздействие через сигнальный путь mTOR, и он предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Помимо этого, он представлен медикаментом для замедления старения, оказывающим влияние через сигнальный путь mTOR, и он предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Второй целью настоящего изобретения является получение фармацевтической композиции, включающей ингибитор mTOR, представленный в любом из вышеприведенных решений, и фармацевтически приемлемого носителя;
Предпочтительно, чтобы доза ингибитора mTOR находилась в диапазоне от 1 до 10000 мг/кг, более предпочтительно - от 10 до 5000 мг/кг, еще более предпочтительно - от 50 до 1000 мг/кг, а наиболее предпочтительно - от 100 до 500 мг/кг.
Согласно другому решению фармацевтическая композиция включает первый и второй действующие ингредиенты, и первый ингредиент включает ингибитор mTOR, приведенный выше, а второй - медикамент для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR;
кроме того, при получении сложного препарата дозировка первого и второго действующих ингредиентов составляет 1-99: 99-1, предпочтительно - 5-95: 95-5, более предпочтительно - 10-90: 90-10, и наиболее предпочтительно - 20-80: 80-20.
Помимо этого, фармацевтическая композиция включает фармацевтически приемлемые лекарственные формы; предпочтительно, чтобы лекарственные формы были представлены порошком, таблеткой, гранулами, капсулой, раствором, эмульсией и суспензией.
Согласно настоящему изобретению действующий ингредиент, изовалерил-спирамицин I, в ингибиторе mTOR может быть отделен и получен согласно способу из предыдущего уровня техники, например, описанному в примере 1 документа CN101785778A.
Третьей целью настоящего изобретения является получение комбинированного лекарственного препарата, включающего первый медицинский препарат, который включает ингибитор mTOR или фармацевтически приемлемую композицию, приведенную выше.
Кроме того, комбинированный лекарственный препарат дополнительно включает второй медицинский препарат.
Кроме того, второй медицинский препарат включает медикамент для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR.
Медикаменты для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR, согласно настоящему решению относятся к основным медикаментам для лечения этих заболеваний. Например, в отношении диабета второй медицинский препарат может быть представлен инсулином и его аналогами, сульфонилмочевинными стимуляторами секреции, метформинами, ингибиторами альфа-глюкозидазы, сенсибилизаторами производных тиазолидиндиона, стимуляторами секреции производных анисовой кислоты, стимуляторами рецепторов GLP-1, DPP-4, а также китайскими запатентованными лекарственными препаратами.
При комплексном лечении соотношение дозы первого и второго медицинских препаратов составляет 1-99: 99-1, предпочтительно - 5-95: 95-5, более предпочтительно - 10-90: 90-10, и наиболее предпочтительно - 20-80: 80-20.
При комплексном лечении первый и второй медицинские препараты вводятся в любом порядке. Сначала может быть использован первый или второй медицинский препарат, или же оба препарата могут быть использованы одновременно.
Четвертая цель настоящего изобретения состоит в получении противоопухолевого медикамента, включающего ингибитор mTOR, который включает один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, или сочетает в себе два или три следующих компонента карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III;
предпочтительно, чтобы ингибитор mTOR представлял собой аллостерический или каталитический ингибитор белков в сигнальном пути PI3K/Akt/mTOR;
предпочтительно, чтобы каталитический ингибитор был представлен ингибитором киназ;
предпочтительно, чтобы ингибитор mTOR активировал ингибирование как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Многие из функций клеток, тесно связанные с опухолями, такие как пролиферация, клеточный цикл, белковый синтез и миграция клеток, контролируются посредством регуляции mTOR. Было установлено, что регуляция сигнального пути mTOR у многих опухолей, таких как рак молочной железы, рак предстательной железы и рак легкого, происходит с нарушениями. В качестве ингибитора mTOR для ингибирования активности mTORC1, которая, в свою очередь, отрицательно воздействует на целевые молекулы по ходу транскрипции, регулируемые им, в том числе: p70S6K, ATG13, 4EBP1, HIF-1, PGC-1α, PPARr и т.д., применяется один из ингредиентов карримицина: изовалерил-спирамицин I, II, III. По мере снижения активности mTORC1 происходит отрицательная регуляция p70S6K, блокируется рост клеток, и ингибирование ATG13 прекращается, за счет чего обеспечиваются апоптоз клеток и аутофагия. В дополнение к терминации клеточного цикла ингибитор по настоящему изобретению также может приводить к гибели опухолевых клеток посредством апоптоза и аутофагии.
Пятая цель настоящего изобретения состоит в получении медикамента для лечения диабета, включающего ингибитор mTOR, который включает один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, или сочетает в себе два или три следующих компонента карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III;
предпочтительно, чтобы ингибитор mTOR представлял собой аллостерический или каталитический ингибитор белков в сигнальном пути PI3K/Akt/mTOR;
предпочтительно, чтобы каталитический ингибитор был представлен ингибитором киназ;
предпочтительно, чтобы ингибитор mTOR активировал ингибирование как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Кроме того, mTOR может образовывать различные функциональные комплексы (mTORC1 и mTORC2) для регуляции активности сигнального пути инсулина, воздействовать на развитие β-клетки, апоптоз и секрецию инсулина, регулировать секрецию таких гормонов, как грелин/несфатин-1, тесно связанных с метаболизмом глюкозы, а также воздействовать на поглощение глюкозы такими периферийными тканями, как скелетные мышцы, жир и т.д., для регуляции уровня сахара в крови различными способами. Механизм воздействия mTORC1 на чувствительность к инсулину сложен. С одной стороны, фактор роста может активировать mTOR через стандартный сигнальный путь PI3K-AKT, а с другой - сигнал mTOR/S6K1 может снижать чувствительность к инсулину посредством механизма отрицательной обратной связи. Ингибитор mTOR по настоящему изобретению ингибирует гиперфосфорилирование mTOR и S6K1, оборачивает вспять фосфорилирование субстрата инсулинового рецептора в состоянии резистентности к инсулину, повышает абсорбцию глюкозы адипоцитами, а также ингибирует жироотложение.
Шестая цель настоящего изобретения состоит в получении медикамента для лечения болезни Альцгеймера, включающего ингибитор mTOR, который включает один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, или сочетает в себе два или три следующих компонента карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III;
предпочтительно, чтобы ингибитор mTOR представлял собой аллостерический или каталитический ингибитор белков в сигнальном пути PI3K/Akt/mTOR;
предпочтительно, чтобы каталитический ингибитор был представлен ингибитором киназ;
предпочтительно, чтобы он был предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
В рамках нервной системы избыточная активация mTOR может привести к развитию опухолей головного мозга. Кроме того, многочисленные факты свидетельствуют о том, что при некоторых нейродегенеративных заболеваниях, таких как болезнь Альцгеймера (БА), болезнь Паркинсона, болезнь Хантингтона и т.д., в сигнальном пути mTOR имеются нарушения. Все эти заболевания объединяет общий признак - в определенных областях головного мозга теряется большое количество нейронов, что может быть связано с нарушениями в сигнальном пути mTOR. БА - нейродегенеративное заболевание с прогрессирующей деменцией в качестве основного признака, которое возникает преимущественно у пожилых людей. Наиболее типичными патологическими признаками БА являются: накопление бета-амилоидного белка (Aβ) вне нейронов с образованием сенильных бляшек, образование нейрофибриллярных клубков белками с высоким уровнем фосфорилирования в нейронах и потеря нейронов, и клинические проявления выражаются в изменении функций обучения и памяти. Поскольку патогенез БА весьма сложен, в текущем исследовании применяются два разных типа изменений (положительная/отрицательная регуляция) в сигнальном пути mTOR. Положительная регуляция сигнального пути mTOR может привести к снижению синтеза некоторых белков с нейротоксичными эффектами (например, тау-белка) и, следовательно, ингибиторы mTOR могут представлять собой эффективные медикаменты при лечении нейродегенеративных заболеваний.
Седьмая цель настоящего изобретения состоит в получении медикамента для замедления старения, включающего ингибитор mTOR, который включает один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III, или сочетает в себе два или три следующих компонента карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III;
предпочтительно, чтобы ингибитор mTOR представлял собой аллостерический или каталитический ингибитор белков в сигнальном пути PI3K/Akt/mTOR;
предпочтительно, чтобы каталитический ингибитор был представлен ингибитором киназ;
предпочтительно, чтобы он был предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
Ингибирование сигнального пути mTOR/S6K может замедлять старение, повышает митохондриальное продуцирование и улучшает активность дыхательной цепи, снижает стресс эндоплазматического ретикулума, а также способствует аутофагии для выведения поврежденных структур в клетках. Ингибирование с использованием ингибитора mTOR в сигнальном пути mTOR/S6K может значительно расширять сигнальные пути, связанные с аутофагией. После ингибирования mTORC1 повышаются аутофагия, способность к выведению продуктов жизнедеятельности и продолжительность жизни в целом. Кроме того, mTOR отвечает за аэробную дыхательную функцию митохондрий, которая содействует экспрессии генов, связанных с митохондриями, митохондриальному продуцированию, а также повышает потребление тканями кислорода за счет положительной регуляции уровней PPARr и PGC1. Ингибирование mTORC1 может активировать группы генов с защитной функцией, снижать вред, наносимый свободными кислородными радикалами за счет ограничения митохондриального дыхания, тем самым продлевая продолжительность жизни организма.
Восьмая цель настоящего изобретения состоит в предложении применения ингибитора mTOR, фармацевтической композиции или комбинированного лекарственного препарата, приведенного выше, при получении медикамента для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR.
Кроме того, карримицин, представленный изовалерил-спирамицином I, II или III, воздействует на метаболическую микросреду за счет целевого воздействия на mTOR, благодаря чему осуществляется ингибирование заболеваний, связанных с сигнальным путем mTOR.
Более того, заболевания, связанные с сигнальным путем mTOR, подбираются как минимум из одного из заболеваний, связанных со старением, заболеваний, связанных с отторжением трансплантата, хроническими воспалительными заболеваниями; заболеваний, связанных с гликогенозом, болезнью Хантингтона, злокачественными опухолями, метастатическим раком, системной красной волчанкой; заболеваний, связанных с воспалением и иммунной активацией; заболеваний, связанных с лейкопенией, анемией, тромбопенией, стентированием, почечной недостаточностью, ожирением, диабетом; заболеваний, связанных с неалкогольной жировой печенью, потерей массы тела по причине заболеваний, поликистозной болезнью почек, болезнью Паркинсона и фиброзом.
Кроме того, заболевания, связанные со старением, подбираются из группы, состоящей из саркопении, атрофии кожи, мышечной атрофии, атрофии головного мозга, атеросклероза, артериосклероза, эмфиземы, остеопороза, остеоартрита, гипертонии, эректильной дисфункции, деменции, болезни Альцгеймера, катаракты, макулодистрофии, связанной со старением, рака предстательной железы, инсульта, снижения продолжительности жизни, нарушения почечной функции и потери слуха, связанной со старением, нарушения способности к передвижению, связанного со старением, когнитивного нарушения, нарушения памяти, скованности сухожилий, дисфункции сердца, такой как гипертрофия миокарда и систолическая и диастолическая дисфункция, а также сенильности иммунной функции.
Помимо этого, фиброз включает фиброз печени, миокардиальный фиброз, сердечно-сосудистый фиброз, легочный фиброз, фиброз поджелудочной железы, почечный фиброз или фиброз селезенки.
Злокачественная опухоль подбирается из группы, состоящей из гематобластоза лимфатической системы, мозгового гемобластоза, опухоли, развившейся из мезенхимальной клетки, опухолей центральной и периферической нервных систем, меланомы, семиномы, тератомы, остеогенной саркомы, пигментной ксеродермы, кератоакантомы, фолликулярного рака щитовидной железы и саркомы Капоши;
предпочтительно, чтобы гематобластоз лимфатической системы подбирался из группы, состоящей из лейкемии, острого лимфоидного лейкоза, острого лимфобластного лейкоза, В-клеточной лимфомы, Т-клеточной лимфомы, лимфомы Ходжкина, неходжкинской лимфомы, волосатоклеточного лейкоза, мантийноклеточной лимфомы, миеломы и лимфосаркомы Беркитта; чтобы мозговой гемобластоз включал острую и хроническую миелоцитарную лейкемию, миелодиспластический синдром и промиелоцитарный лейкоз; чтобы опухоль, развившаяся из мезенхимальной клетки, включала фибросаркому и рабдомиосаркому; чтобы опухоли центральной и периферической нервных систем включали астроцитому, нейробластому, глиому и невриному.
Кроме того, злокачественная опухоль дополнительно включает рак мочевого пузыря, рак молочной железы, рак толстой кишки, мезотелиому, рак почки, рак печени, рак легкого, рак головы и шеи, рак пищевода, рак желчного пузыря, рак яичников, рак поджелудочной железы, рак желудка, лимфому, рак шейки матки, рак толстой кишки, рак щитовидной железы, рак предстательной железы, рак кожи и рак ротовой полости.
Помимо этого, клетки злокачественных опухолей, ингибируемые за счет ингибитора mTOR, включают: человеческие клетки рака молочной железы MCF-7 и MDA-MB-231, человеческие клетки рака печени HepG2, человеческие немелкоклеточные клетки рака легких A549, человеческие крупноклеточные клетки рака легких H460 и H1299, человеческие прозрачные клетки почечного эпителия аденокарциномы 786-O, человеческие клетки почечного эпителия аденокарциномы 769-P, человеческие клетки глиомы U251, человеческие клетки глиобластомы A172, клетки человеческой ткани лимфомы U937, человеческие клетки рака шейки матки HeLa, человеческие клетки рака предстательной железы PC3, человеческие клетки рака поджелудочной железы PANC-1, человеческие клетки рака пищевода TE-1, человеческие клетки аденокарциномы желудка SGC-7901, человеческие клетки рака толстой кишки HT-29 и человеческие клетки промиелоцитарного лейкоза HL-60.
Наиболее предпочтительным решением является применение ингибитора mTOR для ингибирования рака легкого, вызванного человеческими немелкоклеточными клетками рака легких A549.
Согласно настоящему изобретению дальнейшие испытания способом in vivo показали, что изовалерил-спирамицин I обладает явными ингибирующими эффектами на рост мышиных рака печени H22 и немелкоклеточных клеток рака легкого A549.
Лечение ингибиторами mTOR по настоящему изобретению можно сочетать с одним или несколькими другими способами лечения рака, включая хирургическое вмешательство, лучевую терапию (например, лучевая терапия гамма-излучением, пучком нейтронов, пучком электронов, протонная терапия, близкофокусная лучевая терапия и системная радиоизотопная терапия и т.д.), эндокринную терапию, терапию модуляторами биологического ответа (например, интерферон, интерлейкин, фактор некроза опухоли (TNF)), гипертермию, криотерапию, снятие побочных реакций на медикаменты (например, противорвотные медикаменты) и прочие химиотерапевтические медикаменты. Прочие медикаменты могут вводиться до, во время или после применения ингибитора mTOR, предлагаемого по настоящему изобретению, а также могут вводиться в одинаковых или разных лекарственных формах, разными путями введения и в разных дозировках в соответствии с ингибитором mTOR, предлагаемым в настоящем документе.
Ингибитор mTOR и фармацевтическую композицию по настоящему изобретению можно использовать совместно с другими медикаментами для снятия побочных эффектов (например, ингибином, анальгетиком, противорвотным средством, Г-КСФ, ГМ-КСФ и т.д.) и/или другими соответствующими химиотерапевтическими медикаментами. Другие медикаменты включают в себя, помимо прочего, один или несколько медикаментов из числа следующих: противораковые алкилирующие или заделанные медикаменты (например, азотистый иприт, хлорамбуцил, циклофосфамид, мелфалан и ифосфамид); антиметаболитные медикаменты (например, метотрексат); антагонисты пуринов или пиримидина (например, 6-меркаптопурин, 5-фтороурацил, цитарабин, капецитабин и гемцитабин); веретенообразные токсины (например, винбластин, винкристин, винорелбин и паклитаксел); подофиллотоксин (например, этопозид, иринотекан, топотекан); антибиотики (например, доксорубицин, блеомицин и митомицин); нитрозомочевина (например, кармустин и ломустин); неорганические ионы (например, цисплатин, карбоплатин, оксалиплатин или оксиплатин); ферменты (например, аспарагиназа); гормоны (например, тамоксифен, лейпрорелина ацетат, флутамид и мегестрол); ингибиторы протеасом (например, Velcade, прочие ингибиторы протеасом или прочие ингибиторы NF-kB, включая, к примеру, ингибиторы IkK; прочие ингибиторы киназ (например, Src, BRC/Abl, kdr, flt3, aurora-2 и гликоген-синтаза-киназа-3 («GSK-3»), киназа EGF-R (например, Iressa, Tarceva и т.д.), киназа VEGF-R, киназа PDGF-R и т.д.; антитела, растворимые рецепторы или другие рецепторы, являющиеся антагонистами рецепторов или гормонов, участвующих в развитии рака (включая EGFR, ErbB2, VEGFR, PDGFR и IGF-R), а также такие медикаменты как герцептин (или прочие антитела против Her2), авастин, эрбитукс и т.д.)).
Примеры других лечебно-профилактических препаратов включают в себя аллопуринол, алемтузумаб, гексаметиламин, амифостин, анастрозол, антитела против простатического специфического мембранного антигена (например, MLN-591, MLN591RL и MLN2704), окись мышьяка, бексаротен, блеомицин, бусульфан, капецитабин, Gliadel Wafer, целекоксиб, хлорамбуцил, цисплатин-эпинефрин гель, кладрибин, липосомальный цитарабин, липосомальный даунорубицин, даунорубицин, дауномицин, дексразоксан, доцетаксел, доксорубицин, раствор Elliott B Solution, эпирубицин, эстрамустин, этопозида фосфат, этопозид, экземестан, флударабин, 5-фторурацил, фулвестрант, гемцитабин, гемтузумаб озогамицин, гозерелина ацетат, гидроксимочевину, идарубицин, эдарубицин, деметоксидаунорубицин, ифосфамид, иматиниба мезилат, иринотекан (или прочие ингибиторы топоизомеразы, включая такие антитела, как MLN576(XR11576)), летрозол, фолиниевая кислота, левамизол-фолиниевая кислота, липосомный даунорубицин, мелфалан, L-PAM, месна, метотрексат, метоксален, митомицин С, митоксантрон, MLN518 или MLN608 (или рецепторная тирозинкиназа flt-3, PDFG-R, прочие ингибиторы c-kit), итоксантрон, паклитаксель, пегадемаза, пентостатин, порфимер натрия, ритуксимаб, тальк, тамоксифен, темозоломид, тенипозид, VM-26, топотекан, торемифен, 2С4 (или прочие антитела, препятствующие сигнализации, медиированной HER2), третиноин, ретиноевая кислота, валрубицин, винорелбин, памидронат, золедронат или бисфосфонатные соединения.
Лечение ингибитором mTOR по настоящему изобретению может проводиться с использованием одного или нескольких сочетаний цитотоксичных средств как части схемы лечения. Сочетание цитотоксичных средств подбирается из группы, состоящей из: CHOPP (циклофосфамид, доксорубицин, винкристин, преднизон и прокарбазин); CHOP (циклофосфамид, доксорубицин, винкристин и преднизон); COP (циклофосфамид, винкристин, преднизон); CAP-BOP (циклофосфамид, доксорубицин, прокарбазин, блеомицин, винкристин и преднизон); m-BACOD (метотрексат, блеомицин, доксорубицин, циклофосфамид, винкристин, дексаметазон и фолиниевая кислота); ProMACE-MOPP (преднизон, метотрексат, доксорубицин, циклофосфамид, этопозид, фолиниевая кислота, мехлоретаминоксид, винкристин, преднизон и прокарбазин); ProMACE-CytaBOM (преднизон, метотрексат, доксорубицин, циклофосфамид, этопозид, фолиниевая кислота, цитарабин, блеомицин и винкристин); MACOP-B (метотрексат, доксорубицин, циклофосфамид, винкристин, преднизон, блеомицин и фолиниевая кислота); MOPP (мехлоретаминоксид, винкристин, преднизон и прокарбазин); ABVD (доксорубицин/доксорубицин, блеомицин, винбластин и дакарбазин); MOPP (мехлоретаминоксид, винкристин, преднизон и прокарбазин) и ABV (доксорубицин/доксорубицин, блеомицин и винбластин), применяемая в качестве альтернативного варианта; MOPP (мехлоретаминоксид, винкристин, преднизон и прокарбазин) и ABVD (доксорубицин/доксорубицин, блеомицин, винбластин и дакарбазин), применяемая в качестве альтернативного варианта; ChlVPP (хлорамбуцил, винбластин, прокарбазин и преднизон); IMVP-16 (ифосфамид, метотрексат и этопозид); MIME (митогуазон, ифосфамид, метотрексат и этопозид); DHAP (дексаметазон, высокая доза цитарибина и цисплатин); ESHAP (этопозид, метилпреднизолон, высокая доза цитарабина и цисплатин); CEPP(B) (циклофосфамид, этопозид, прокарбазин, преднизон и блеомицин); CAMP (ломустин, митоксантрон, цитарабин и преднизон); CVP-1 (циклофосфамид, винкристин и преднизон); ESHOP (этопозид, метилпреднизолон, высокая доза цитарабина, винкристин и цисплатин); EPOCH (этопозид, винкристин и доксорубицин, применяемые в течение 96 часов совместно с большими дозами циклофосфамида и преднизона перорально); ICE (ифосфамид, циклофосфамид и этопозид), CEPP(B) (циклофосфамид, этопозид, прокарбазин, преднизон и блеомицин), CHOP-B (циклофосфамид, доксорубицин, винкристин, преднизон и блеомицин), CEPP-B (циклофосфамид, этопозид, прокарбазин и блеомицин) и P/DOCE (эпирубицин или доксорубицин, винкристин, циклофосфамид и преднизон).
Согласно вышеприведенному техническому решению настоящее изобретение имеет следующие положительные эффекты, превосходящие таковые на предыдущем уровне техники:
1. Ингибитор mTOR по настоящему изобретению включает один из следующих компонентов карримицина: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III или сочетает в себе два или три следующих компонента: изовалерил-спирамицин I, изовалерил-спирамицин II и изовалерил-спирамицин III. Каждый из вышеприведенных действующих ингредиентов может ингибировать активность определенных белков в сигнальном пути PI3K/Akt/mTOR как по отдельности, так и в сочетании, поэтому ингибитор mTOR по настоящему изобретению обладает явным ингибирующим эффектом на клетки при заболеваниях, связанных с сигнальным путем mTOR, и при этом также обеспечивается теоретическое обоснование его применения и клинического продвижения при получении медикаментов для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR.
2. Ингибитор mTOR по настоящему изобретению обеспечивает хорошее противоопухолевое действие, а в особенности обладает хорошими лечебными эффектами при лечении таких опухолей, как рак молочной железы, рак печени, рак легкого, лимфома, рак шейки матки, рак предстательной железы, рак толстой кишки или лейкемия и т.д., а также может ингибировать пролиферацию опухолевых клеток за счет ингибирования активности белков в сигнальном пути PI3K/Akt/mTOR. Также обеспечивается теоретическое обоснование применения и клинического продвижения ингибитора mTOR при приготовлении противоопухолевых медикаментов и, таким образом, он имеет важные экономические и социальные полезные эффекты.
В дальнейшем конкретные примеры осуществления настоящего изобретения будут подробно описываться со ссылкой на прилагаемые чертежи.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Прилагаемые чертежи являются частью настоящего изобретения для обеспечения его дополнительного понимания. Иллюстративные варианты осуществления настоящего изобретения и его описание применяются для его объяснения, но не ограничивают его каким-либо образом. Очевидно, что чертежи в следующем описании представляют собой только часть вариантов осуществления. На основании этих чертежей специалистами в данной области техники могут быть получены другие чертежи без выполнения творческой работы. Чертежи:
на фиг. 1 представлены количественные результаты уровней белков, связанных с сигнальным путем PI3K/Akt/mTOR, таких как p-PI3k/PI3K, p-AKT/AKT, p-mTOR/mTOR, p-S6K1/S6K1, p-4EBP1/4EBP1 и бета-актин, а также фосфорилированные белки согласно определению по методу вестерн-блоттинга, среди которых А1-А2 - результат относительно p-PI3k/PI3K, В1-В2 - результат относительно p-AKT/AKT, C1-C2 - результат относительно p-mTOR/mTOR, D1-D2 - результат относительно p-S6K1/S6K1, а E1-E2 - результат относительно p-4EBP1/4EBP1;
на фиг. 2 представлены уровни экспрессии белков, связанных с сигнальным путем PI3K/Akt/mTOR, таких как p-PI3k/PI3K, p-AKT/AKT, p-mTOR/mTOR, p-S6K1/S6K1, p-4EBP1/4EBP1, бета-актин и т.д., согласно определению по методу вестерн-блоттинга;
на фиг. 3 представлен результат ингибирования роста клеток A549 спустя 24 и 48 ч лечения карримицином;
на фиг. 4 представлены уровни экспрессии белков, связанных с сигнальным путем PI3K/AKT/mTOR, относительно клеток A549 спустя 24 и 48 ч лечения карримицином согласно определению по методу вестерн-блоттинга;
на фиг. 5 представлен количественный результат воздействия карримицина на уровень экспрессии белков, связанных с сигнальным путем PI3K/AKT/mTOR, относительно клеток A549 согласно определению по методу вестерн-блоттинга;
на фиг. 6 представлен результат проточной цитометрии относительно определения аутофагии клеток A549, обусловленной карримицином, где положительное соотношение окрашивания MDC увеличилось после индукции; среди прочего, на фиг. 6а представлен результат индукции клеток A549 карримицином в течение 24 ч; на фиг. 6b представлен результат индукции клеток A549 карримицином в течение 48 ч; на фиг. 7 представлены количественные результаты определения уровней экспрессии P62 и LC3 спустя 24 и 48 ч обработки клеток A549 карримицином согласно определению по методу вестерн-блоттинга;
на фиг. 8 представлен результат ингибирования роста карримицином в отношении клеток A549 после добавления ингибитора аутофагии 3-MA;
на фиг. 9 представлены результаты изменений морфологии клеток спустя 24 и 48 ч лечения карримицином согласно наблюдениям через фазово-контрастный микроскоп;
на фиг. 10 представлен результат цитометрических измерений относительно клеток A549 при обработке карримицином спустя 24 и 48 ч после окрашивания AV-PI;
на фиг. 11 представлены уровни белков прокаспазы 3, каспазы 3 и PARP клеток A549 при обработке карримицином спустя 24 и 48 ч согласно определению по методу вестерн-блоттинга;
на фиг. 12 представлены результаты определения ферментативной активности каспазы 3 в клетках A549;
на фиг. 13 представлены результаты количественного анализа уровня белка HIF-1αVEGF-A после обработки карримицином в разных концентрациях спустя 24 и 48 ч;
на фиг. 14 представлены результаты количественного анализа уровней белков Ras, Raf, p-ERK/ERK после обработки карримицином в разных концентрациях спустя 24 и 48 ч.
Следует отметить, что чертежи и текстовое описание не предполагают ограничения объема идеи изобретения каким-либо образом, и их задача заключается в объяснении идеи специалистам в этой области техники посредством ссылки на конкретные варианты осуществления.
ПОДРОБНОЕ ОПИСАНИЕ
Для обеспечения большей очевидности целей, технических решений и преимуществ примеров по настоящему изобретению далее в настоящем документе технические решения данных примеров будут описаны четко и полностью со ссылками на примеры по настоящему изобретению. Следующие примеры предназначены для объяснения настоящего изобретения, но не для ограничения его объема.
Пример 1. Таблетированный изовалерил-спирамицин I, II или III

Процесс приготовления:
Приготовление ядра таблетки: основной медикамент и вспомогательные лекарственные средства в соответствующем порядке пропускались через сито 100 меш, а затем выполнялось перемешивание рецептурного количества изовалерил-спирамицина I, II или III, рецептурного количества микрокристаллической целлюлозы и 1/2 рецептурного количества натрия крахмала гликолята до однородного состояния, после чего добавлялся водный раствор повидона K30 5% для получения мягкого материала. Для гранулирования использовалось сито 18 меш, и влажные гранулы просушивались в условиях обдува при температуре 60°С в течение 2 ч. После сушки влажных гранул для рассеивания гранул использовалось сито 18 меш, после чего добавлялась 1/2 рецептурного количества натрия крахмала гликолята и рецептурное количество стеарата магния. После равномерного перемешивания всех материалов смесь таблетировалась с помощью узкого вогнутого штампа диаметром 11 мм для получения ядра таблетки, содержащего медикамент, причем масса таблетки составляла 350 мг, а твердость - 6,5 кг.
Приготовление пленкообразующего раствора: было проведено взвешивание Opadry II (белого), в емкость для приготовления партиями было добавлено необходимое количество воды, скорость перемешивания после добавления воды была снижена до исчезновения завихрения, и для получения пленкообразующего раствора перемешивание продолжалось в течение 30 мин.
Приготовление таблеток с пленочной оболочкой: ядро таблетки размещали на установке для нанесения оболочки, устанавливались условия нанесения оболочки и производилось ее нанесение с основной частотой 20 об/мин при температуре воздуха на входе 40°С и 30°С на выходе, давлении распыла 0,02 МПа и расходом жидкого раствора 1 мл/мин. По достижении стабильного состояния оболочка непрерывно распылялась в течение 1,5 часов до тех пор, пока поверхность таблеток не становилась гладкой и не приобретала однородный цвет. Таблетка проходила контроль, если она соответствовала стандартам контроля тонкопленочного покрытия. Покрытие увеличивало массу приблизительно на 5%.
Пример 2. Таблетированный изовалерил-спирамицин I, II или III (из расчета на 10 000 таблеток)
Рецептура:
Процесс приготовления: соответствующее количество крахмала было взвешено, разбавлено до концентрации 15% и нагрето до образования пасты для получения вяжущего вещества; основной материал, изовалерил-спирамицин I, II или III, а также эксципиенты в виде крахмала, гидроксипропилцеллюлозы с низкой степенью замещения, натрия крахмала гликолята и стеарата магния были пропущены через сито 100 меш в соответствующем порядке, и затем необходимые основной материал и эксципиенты были взвешены согласно количеству, указанному в рецептуре. После полного смешивания изовалерил-спирамицина I, крахмала и гидроксипропилцеллюлозы с низкой степенью замещения до однородного состояния была использована крахмальная паста с концентрацией крахмала 15% для преобразования смеси в мягкий материал, который был гранулирован посредством сита 14 меш, и затем эти гранулы были высушены при температуре 50-60°С до получения влажности 3-5%. Для рассеивания гранул использовалось сито 14 меш, после чего для смешивания были добавлены натрия крахмала гликолят и стеарат магния, и была измерена концентрация гранул. Согласно концентрации гранул была вычислена масса таблетки, и смесь была таблетирована посредством узкого вогнутого штампа диаметром 9 мм, после чего была проведена проверка на разность массы таблеток. После прохождения проверки продукта таблетки были упакованы.
Пример 3. Капсулированный изовалерил-спирамицин I, II или III (из расчета на 10 000 гранул)
Рецептура:
Процесс приготовления: основной материал в виде изовалерил-спирамицина I, II или III и эксципиент в виде медицинского крахмала были по отдельности взвешены согласно количеству по рецептуре для данного процесса, а затем полностью перемешаны в миксере в течение 1,5-2 часов. Данные, полученные при отборе образцов и проверке концентраций, в целом должны были совпадать с теоретическими данными (масса каждой капсулы составляла приблизительно 0,105 г), и затем сертифицированные лекарственные капсулы № 3 и смешанное сырье для загрузки были помещены в приспособление для заполнения в соответствии с требованиями автоматической капсюлировочной машины, после чего заполненные капсулы подверглись испытанию на различие образцов (±10% и <0,3 г) для определения соответствия скорости растворения требованиям. Капсулы, соответствовавшие требованиям после испытания, были помещены в глянцовочную машину для глянцевания в течение 15-20 минут с добавлением вазелинового масла, после чего они были извлечены для проверки их соответствия упаковке для готовой продукции.
Пример 4. Высушенный сироп изовалерил-спирамицина I, II или III (из расчета на 10 000 пакетов)
Рецептура:
Процесс приготовления: порошок-сырец изовалерил-спирамицина I, II или III, лимонная кислота и сахароза были в соответствующем порядке измельчены до получения гранул посредством скоростной вихревой мельницы, и 85% гранул были пропущены через сито 300 меш, а 15% - через сито 180 меш. Затем мелкоизмельченный порошок был отвешен в количестве, предусмотренном рецептурой, и полностью перемешивался в течение 1-1,5 часов. Были измерены значения концентрации, рассчитана норма загрузки (теоретическая норма загрузки составила 500 мг на пакет). После этого смесь была помещена в машину для упаковки в пакеты, была установлена бумага с алюминиевой фольгой и проведено заполнение в соответствии с требованиями машины для заполнения. Допуск по расхождениям находился в пределах ±5%, и после заполнения и прохождения осмотра изготавливалась наружная упаковка.
Пример 5. Гранулированный изовалерил-спирамицин I, II или III (из расчета на 10 000 пакетов)
Рецептура:
Процесс приготовления: порошок-сырец изовалерил-спирамицина I, II или III, сахарная пудра и декстрин были пропущены через сито 120 меш, а затем отвешены в количестве, предусмотренном рецептурой, и равномерно перемешаны. Вышеприведенные смешанные материалы были преобразованы в мягкий материал с помощью повидона K30 5% в виде клейкого вещества. Затем этот мягкий материал был гранулирован с помощью колебательного гранулятора, высушен при 70°С, а гранулы были распределены и предварительно упакованы после прохождения проверки.
Пример 6. Изовалерил-спирамицин I, II или III в форме лиофилизированного порошка для инъекций
500мг порошка-сырца изовалерил-спирамицина I, II или III были перемешаны до однородного состояния с равномолярным количеством адипиновой кислоты, и эта смесь была растворена в 5 мл воды для получения светло-желтого прозрачного раствора со значением рН от 4,6 до 5,6 единиц. Далее в форме лиофилизированного пропанта в светло-желтый прозрачный раствор были добавлены 40 мг маннитола, и после быстрой заморозки при низкой температуре в течение 9 часов материал был лиофилизирован для получения рыхлого вещества светло-желтого цвета, которое перед использованием было растворено в 10 мл стерилизованной воды.
Пример 7. Изовалерил-спирамицин I и II в форме лиофилизированного порошка для инъекций
250 мг порошка-сырца изовалерил-спирамицина I и 250 мг порошка-сырца изовалерил-спирамицина II были перемешаны до однородного состояния с равномолярным количеством адипиновой кислоты, и эта смесь была растворена в 5 мл воды для получения светло-желтого прозрачного раствора со значением рН от 4,6 до 5,6 единиц. Далее в форме лиофилизированного пропанта в светло-желтый прозрачный раствор были добавлены 40 мг маннитола, и после быстрой заморозки при низкой температуре в течение 9 часов материал был лиофилизирован для получения рыхлого вещества светло-желтого цвета, которое перед использованием было растворено в 10 мл стерилизованной воды.
Пример 8. Карримицин в форме лиофилизированного порошка для инъекций
500 мг порошка-сырца карримицина были перемешаны до однородного состояния с равномолярным количеством адипиновой кислоты, и эта смесь была растворена в 5 мл воды для получения светло-желтого прозрачного раствора со значением рН от 4,6 до 5,6 единиц. Далее в форме лиофилизированного пропанта в светло-желтый прозрачный раствор были добавлены 40 мг маннитола, и после быстрой заморозки при низкой температуре в течение 9 часов материал был лиофилизирован для получения рыхлого вещества светло-желтого цвета, которое перед использованием было растворено в 10 мл стерилизованной воды.
Пример испытания 1. Биопроба на противоопухолевую активность
Цель анализа - оценка ингибирования пролиферации или цитотоксической активности клетки испытуемого образца способом in vitro.
Клеточные штаммы:
человеческие клетки рака молочной железы MCF-7 и MDA-MB-231, человеческие клетки гепатомы HepG2, человеческие немелкоклеточные клетки рака легких A549, человеческие клетки рака легких H460 и H1299, человеческие прозрачные клетки почечного эпителия аденокарциномы 786-O, человеческие клетки почечного эпителия аденокарциномы 769-P, человеческие клетки глиомы U251, человеческие клетки глиобластомы A172, клетки человеческой ткани лимфомы U937, человеческие клетки рака шейки матки HeLa, человеческие клетки рака предстательной железы PC3, человеческие клетки рака поджелудочной железы PANC-1, человеческие клетки рака пищевода TE-1, человеческие клетки рака желудочной железы SGC7901, человеческие клетки рака толстой кишки HT-29 и человеческие клетки промиелоцитарного лейкоза HL-60, приобретенные у американской коллекции типовых культур (ATCC, Манассас, Вирджиния, США).
Реагенты:
питательные среды RPMI1640, MEM, DMEM с пониженным содержанием сахара, эмбриональная телячья сыворотка, приобретенная у компании Gibco в США, а также трипсин, глютамин, пенициллин, стрептомицин, диметилсульфоксид (ДМСО), метил-тиазол-тетразолий (МТТ), приобретенные у компании Sigma в США.
Инструменты:
углекислотный инкубатор (Sanyo, Япония), анализатор иммуносорбентов с иммобилизированными ферментами (Tecan, Австрия), 96-луночный культуральный планшет (Corning, США) и инвертированный микроскоп (Motic, Китай).
Этапы процедуры следующие:
адгезивные клетки:
MCF-7, MDA-MB-231, HepG2, A549, H460, H1299, 786-O, 769-P, U251, A172, HeLa, PC3, PANC-1, TE-1, SGC7901, HT-29 были опухолевыми адгезивными клетками. Были отобраны и подкормлены трипсином адгезивные опухолевые клетки в фазе логарифмического роста, после чего они были преобразованы во взвесь отмытых клеток с концентрацией от 4 до 5×104/мл с помощью культуральной среды, содержащей 10% эмбриональной телячьей сыворотки. Взвесь отмытых клеток была посеяна на 96-луночный культуральный планшет, и каждая лунка вмещала 100 мкл, после чего при температуре 37°С и концентрации CO2 5% в течение 24 часов проводилась культивация. Группа сравнения была заменена новой культуральной средой с другой концентрацией образцов для испытания, а именно карримицином, в то время как контрольная группа была заменена культуральной средой, содержащей аналогичный объем растворителя. Также каждая группа получила 3 параллельных лунки, культивация которых проводилась при 37°С и концентрации CO2 5% в течение 48 часов. После удаления супернатанта лунки были трижды тщательно промыты фосфатно-солевым буферным раствором. Также в каждую лунку были добавлены 100 мкл свежеприготовленной культуральной среды с концентрацией МТТ 0,5 мг/мл для непрерывной инкубации в течение 4 часов при 37°С. После тщательного удаления супернатанта в каждую лунку были добавлены 150 мл ДМСО, и после смешивания материала в течение 10 минут до однородного состояния посредством микроосциллятора с помощью микропланшетного ридера было измерено значение оптической плотности при длине волны 492 нм.
Клетки во взвеси:
клетками во взвеси выступали U937 и HL-60, а в фазе логарифмического роста клетки были отобраны и преобразованы во взвесь отмытых клеток 2×105/мл с помощью культуральной среды RPMI 1640, содержащей 10% эмбриональной телячьей сыворотки. Взвесь отмытых клеток была посеяна на 96-луночный культуральный планшет, и каждая лунка вмещала 50 мкл, после чего при температуре 37°С и концентрации CO2 5% в течение 24 часов проводилась культивация на 96-луночном планшете. В группу сравнения были добавлены 50 мкл культуральной среды с разной концентрацией испытуемого образца карримицина, в то время как в контрольную группу была добавлена культуральная среда, содержащая такой же объем растворителя. Также каждая группа получила 3 параллельных лунки, культивация которых проводилась при 37°C и концентрации CO2 5% в течение 48 часов. Также в каждую лунку были добавлены 10 мкл свежеприготовленной культуральной среды с концентрацией МТТ 5 мг/мл для непрерывной инкубации в течение 4 часов при 37°С. Кристаллы были растворены в 100 мкл тройного раствора (10 г додедилсульфата натрия, 0,1 мл HCl 10 моль, 5 мл изобутанола, разбавленного 100 мл дистиллированной воды) и инкубированы при 37°С в течение 12 часов; с помощью микропланшетного ридера было измерено значение оптической плотности при длине волны 492 нм.
Оценка результата: степень ингибирования роста опухолевых клеток за счет медикаментов была рассчитана по следующей формуле:
Степень ингибирования роста опухолевой клетки (%)=[A492 (отрицательный контроль)-A492 (дозовая группа)]/A492 (отрицательный контроль)×100%
По этой формуле определялась средняя ингибирующая концентрация (IC50) образца.
Результаты: в качестве опытных образцов были использованы: человеческие клетки рака молочной железы MCF-7 и MDA-MB-231, человеческие клетки рака печени HepG2, человеческие немелкоклеточные клетки рака легких A549, человеческие крупноклеточные клетки рака легких H460 и H1299, человеческие прозрачные клетки почечного эпителия аденокарциномы 786-O, человеческие клетки почечного эпителия аденокарциномы 769-P, человеческие клетки глиомы U251, человеческие клетки глиобластомы A172, клетки человеческой ткани лимфомы U937, человеческие клетки рака шейки матки HeLa, человеческие клетки рака предстательной железы PC3, человеческие клетки рака поджелудочной железы PANC-1, человеческие клетки рака пищевода TE-1, человеческие клетки рака желудочной железы SGC-7901, человеческие клетки рака толстой кишки HT-29 и человеческие клетки промиелоцитарного лейкоза HL-60. Результаты оценки антипролиферативной активности in vitro образцов представлены в таблице 1 ниже:
Таблица 1. Ингибирование пролиферации опухолевых клеток карримицином
(мкг/мл)
(мкг/мл)
Имеющиеся результаты показывают, что образцы демонстрируют хорошую антипролиферативную активность в отношении испытуемых клеток.
Пример испытания 2. Ингибирование сигнального пути PI3k/AKT/mTOR изовалерил-спирамицином I
Клеточные штаммы:
клетки A549, приобретенные у американской коллекции типовых культур (ATCC, Манассас, Вирджиния, США). Культивация клеток выполнялась в среде DMEM, содержащей 10% эмбриональной телячьей сыворотки, 2% глютамина и пенициллин (100 ед./мл), в инкубаторе при температуре 37°С и концентрации СО2 5%. Все клетки, использованные при проведении опыта, находились в фазе логарифмического роста.
Реагенты:
рапамицин, приобретенный у компании Sigma Company (Сент-Луис, Миссури, США)
Этапы процедуры следующие:
в качестве адгезивной клетки выступила клетка A549, и в группу сравнения были отобраны клетки в фазе логарифмического роста. В группу сравнения были добавлены изовалерил-спирамицин I в разных концентрациях (0,05, 5, 17, 50 мкг/мл) и контрольный медикамент рапамицин (20 мкг/мл), была проведена ее культивация в инкубаторе при температуре 37°С и концентрации CO2 5% в течение 24 ч, после чего клетки были собраны, и был задействован метод вестерн-блоттинга.
Вестерн-блоттинг:
1. Приготовление рабочего раствора
1) Раствор полиакриламида 30%:

ддH2O была добавлена в постоянный объем 1 000 мл, помещена в коричневую склянку и хранилась при температуре 4°С.
2) Трис-буферный раствор: после полного растворения трис-основания в деионизированной воде показатель рН раствора был отрегулирован за счет HCl.
Буферный раствор из разделяющего геля: Трис-HCl 1,5 моль (pH 8,8);
Буферный раствор из концентрирующего геля: 1 Трис-HCl 1 моль (pH 6,8).
3) Натрия додецилсульфат (SDS): раствор хранения в концентрации 10%, приготовленный с помощью деионизированной воды, был оставлен для хранения при комнатной температуре для последующего применения.
4) Надсернокислый аммоний (АР): небольшое количество основного раствора в концентрации 10% (масса/объем), приготовленного с помощью деионизированной воды, было оставлено для хранения при температуре 4°С, однако через каждые две недели требуется приготовление нового, поскольку надсернокислый аммоний медленно распадается.
5) 5×трис-глициновый электрофоретический буферный раствор
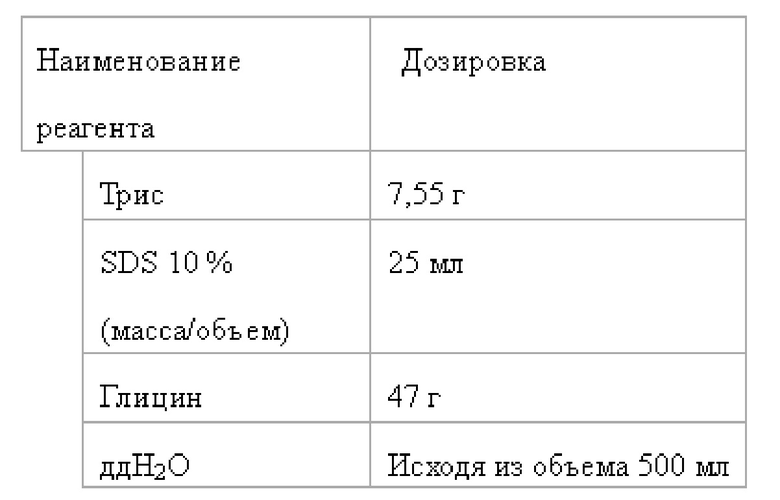
Этот раствор хранился в холодильной камере при температуре 4°С и для применения разбавлялся ддH2O в пропорции 1×буферный раствор.
6) Раствор для клеточного лизиса: ГЭПЭС - 50 ммоль (рН 7,4), 1% Triton X-100, NaF - 100 ммоль, ЭДТК - 1 ммоль, ЭГТК - 1 ммоль, ортованадат натрия - 2 ммоль, фенилметилсульфонил фторид (PMSF) - 1 ммоль, апротинин - 10 мг/мл, лейпептин - 10 мг/мл, пепсатин А - 10 мг/мл.
7)5×загрузочные буферы:
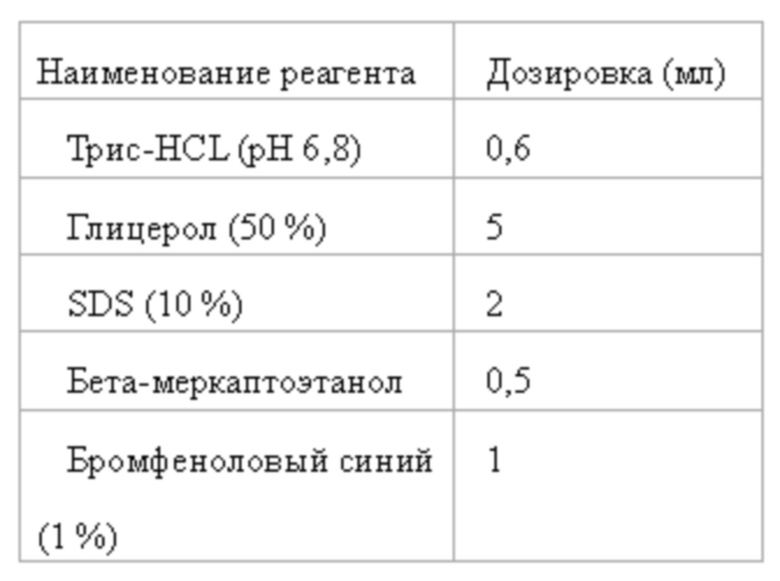
8) Буфер для блоттинга:

9)Блокирующий буфер:

2. Электрофорез белков
1) В каждую пробирку с клетками были добавлены 60-100 мкл лизата, после чего они были помещены в ванну со льдом в холодильной камере при температуре 4°С на 1 ч; раствор подвергся центрифугированию на 12 000 об/мин в течение 10-15 мин, после чего был извлечен супернатант и помещен в пробирки Эппендорф 0,5 мл; после измерения количественного содержания белков на оборудовании Bio-Rad были добавлены 5 загрузочных буферов, и раствор был помещен на кипящую водяную баню на 3-5 мин, после чего была выполнена его криоконсервация при температуре -80°С.
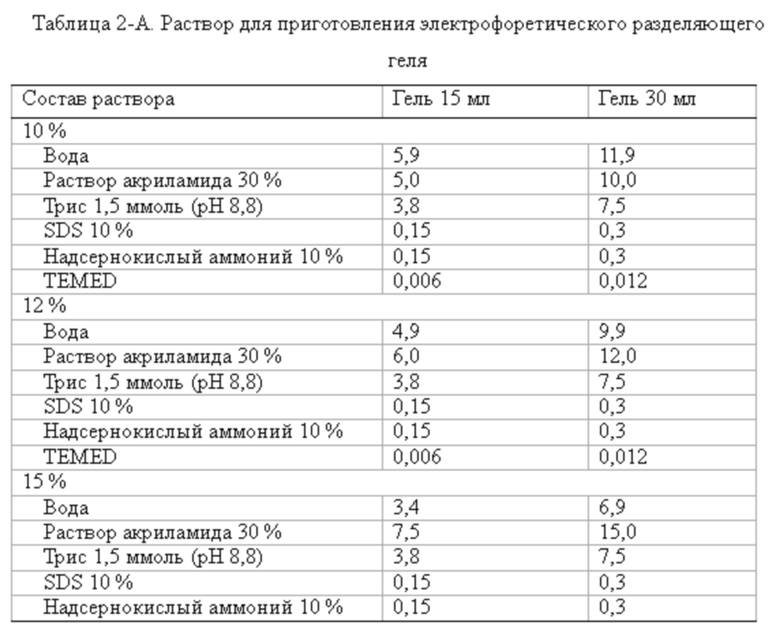
2) Был приготовлен разделяющий гель с концентрацией акриламида 15, 12 или 10% согласно таблице 2-1, после чего он последовательно смешивался с различными ингредиентами; после добавления TEMED и АР смесь была быстро взболтана и разлита по стеклам бака для электрофореза с оставлением места, необходимого для добавления концентрирующего геля.
На разделяющий гель был нанесен слой изопропилового спирта, и гель был оставлен в вертикальном положении при комнатной температуре в течение около 30 мин.
3) После полной полимеризации разделяющего геля изопропиловый спирт был удален, и гель был подвергнут десятикратной промывке деионизированной водой; вода была собрана фильтровальной бумагой, был приготовлен концентрирующий гель согласно таблице 2-2, и после добавления концентрирующего геля в бак для электрофореза был осуществлен незамедлительный ввод чистого гребенчатого образца.
4) После полной полимеризации концентрирующего геля прибор для электрофореза был заполнен 1×электрофоретическим буферным раствором, согласно заданной последовательности для начала электрофореза в пробоотборные отверстия были введены образцы, причем во время нахождения образцов в концентрирующем геле напряжение составляло 50-60 В, а затем было отрегулировано до значения 100-140 В после перехода образцов в разделяющий гель.
3. Вестерн-блоттинг
1) По завершении электрофореза полиакриламидного геля SDS гель был помещен в буфер для блоттинга и настоян для впитывания в течение 30 мин. Были вырезаны 8 листов фильтровальной бумаги 3 мм и 1 нитроцеллюлозная мембрана, соответствующая размеру геля. Нитроцеллюлозная мембрана была погружена в метанол на 1 мин, а затем - в деионизированную воду для удаления пузырьков воздуха.
2) Гель был сложен в форме «сэндвича» и помещен в передаточную камеру. В течение 3 ч к нему был подведен катод с одной стороны с силой тока 100 мА.
3) Перенесенная нитроцеллюлозная мембрана была введена в окрашивающий раствор Ponceau S на 5-10 мин и слегка встряхивалась в течение этого периода времени. При проявлении полосы белка было проведено ополаскивание деионизированной водой несколько раз, и положение молекулярной массы стандартного белка было отмечено водостойкими чернилами.
4) Мембрана была помещена в чашку Петри с блокирующим раствором, и в течение 2 ч проводилось блокирование.
5) Был долит блокирующий раствор с первым антителом в объеме 0,1 мл/см2, после чего он был оставлен на ночь при температуре 4°С (кратность разбавлений различных антител представлена в таблице 2-2)
6) Первое антитело было извлечено, мембрана трижды подвергалась ополаскиванию ФСБТ в течение 10 мин при каждом ополаскивании, а затем перенесена на раствор, содержащий NaCl 150 ммоль и трис-HCl 50 ммоль (рН 7,5), а затем проводилось встряхивание в течение 10 мин.
7) Был добавлен бесфосфатный блокирующий раствор без содержания азида натрия со вторым антителом в объеме 0,1 мл/см2, причем второе антитело, промаркированное пероксидазой из хрена, было тысячекратно разбавлено.
8) Было проведено троекратное ополаскивание раствором NaCl 150 ммоль и трис-HCl 50 ммоль/л (рН 7,5) продолжительностью 10 мин каждое. Цветное проявление проводилось в темном помещении посредством набора для иммуноанализа с меченными усиленной хемолюминесцентной меткой антителами (ECL), после чего изображения были просканированы и сохранены.

Результаты:
После воздействия изовалерил-спирамицина I на клетки А549 в течение 24 часов белок сигнального пути PI3K/Akt/mTOR и типовые уровни его фосфорилированности были исследованы по методу вестерн-блоттинга. Результаты показаны на фиг. 1 и фиг. 2.
Воздействие изовалерил-спирамицина I на экспрессию уровней белков PI3K, AKT, mTOR и субстратов mTOR - S6K1, 4EBP1, а также их активированных типов - p-PI3K, p-AKT, p-mTOR, p-S6K1, p-4EBP1 показаны на фиг. 1 и 2. Результаты показали, что изовалерил-спирамицин I может ингибировать активацию сигнального пути белками PI3K/AKT/mTOR, в особенности активацию белков PI3K, 4EBP1, mTOR, а также может ингибировать экспрессию белков Akt и S6K1 и экспрессию их активированных белков.
Кроме того, как представлено на фиг. 1 и 2, в сравнении с рапамицином ингибитор mTOR по настоящему изобретению, представленный изовалерил-спирамицином I, обладает лучшими ингибирующими эффектами на AKT, S6K1 и 4EBP1, что указывает на то, что он может оказывать сильное ингибирующее воздействие на сигнальный путь PI3K/Akt/mTOR, что обеспечивает теоретическое обоснование применения и клинического продвижения ингибитора mTOR при получении медикаментов для лечения и/или профилактики заболеваний, связанных с сигнальным путем mTOR, а также обеспечиваются важные экономические и социальные полезные эффекты.
Кроме того, заявителем также использовались карримицин, изовалерил-спирамицин II и III отдельно или в сочетании двух или трех ингредиентов - изовалерил-спирамицина I, II и III - для воздействия на клетки A549 в течение 24 часов, после чего проверялись уровни белков сигнального пути PI3K/Akt/mTOR и типы их фосфорилирования по методу вестерн-блоттинга, и результаты были аналогичны полученным в примере испытания 2, т.е., он мог ингибировать активацию белков PI3K, 4EBP1 и mTOR, экспрессию белков AKT и S6K1, а также экспрессию их активированных белков, что в настоящем документе в дальнейшем подробно приведено не будет.
Пример испытания 3. Ингибирование пролиферации немелкоклеточных клеток рака легкого A549 карримицином
(1) Для определения воздействия карримицина на выживаемость опухолевых клеток in vitro был применен МТТ-тест
Клетки А549 были посеяны на 96-луночный планшет с плотностью 4×103 клеток/мл в объеме 100 мкл на лунку и культивировались в течение 24 и 48 ч. В лунки был добавлен карримицин в разных концентрациях, 96-луночный планшет был помещен в инкубатор при температуре 37°С и с концентрацией СО2 5% для непрерывной культивации в течение разных временных промежутков. В каждую лунку для культивации в течение 2-3 ч были добавлены 100 мкл тиазолила синего тетразолий бромида, а супернатант был извлечен и утилизирован. Были добавлены 150 мкл ДМСО, а также было выполнено встряхивание в микроосцилляторе в течение 10 мин для растворения кристаллов. Значение светопоглощения (значение А) каждой лунки определялось с помощью микропланшетного ридера при длине волны 492 нм. В то же время, в качестве положительного контроля применялся рапамицин, и степень ингибирования роста при воздействии медикамента на клетки рассчитывалась по следующей формуле: степень ингибирования (%)=[A492 (контрольная группа)-A492 (группа введения карримицина)]/[A492 (контрольная группа)-A492 (группа без введения)]×100%
Результаты показали, что карримицин смог ингибировать пролиферацию клеток А549 в зависимости от концентрации с показателем IC50 24,88 и 17,84 мкг/мл в течение 24 и 48 ч соответственно.
(2) Карримицин может ингибировать сигнальный путь PI3K/AKT/mTOR
В различных типах опухолей зачастую возникают нарушения в сигнальном пути PI3K/AKT/mTOR. PI3K - внутриклеточная фосфатидилинозитол-киназа. Семейство белков PI3K задействовано в регуляции пролиферации клеток их дифференцировке, апоптозе, транспорте глюкозы и прочих клеточных функциях. AKT (протеинкиназа В) - основной эффектор по ходу транскрипции PI3K, который может активировать mTORC1 посредством непосредственного фосфорилирования mTOR или инактивации TSC2 (комплекс туберозного склероза 2). mTORC1 непосредственно фосфорилирует нисходящий фактор инициации эукариот, связывающий белок 4E-BP1, и рибосомальную протеинкиназу S6 (S6K1), за счет чего регулируется биосинтез и клеточная пролиферация.
Клетки A549 подвергались воздействию карримицина в разных концентрациях в течение 24 и 48 ч, а уровень белка mTOR, а также уровни белков против и по ходу транскрипции в клетках исследовались по методу вестерн-блоттинга. Результаты показали, что после воздействия на клетки A549 в течение 24 ч карримицин в концентрации свыше 5 мкг/мл смог снизить уровень фосфорилирования белков mTOR, а также 4E-BP1 и S6K1 по ходу транскрипции, причем он также привел к снижению уровня фосфорилирования PI3K и AKT.
После воздействия карримицином в концентрации 5, 17, 50 мкг/мл на клетки A549 в течение 48 ч уровень фосфорилирования mTOR значительно снизился, а уровень фосфорилирования белков по ходу транскрипции был значительно ингибирован. При этом карримицин в концентрации 5, 17 мкг/мл повысил уровни фосфорилирования PI3K и AKT, в то время как карримицин в концентрации 50 мкг/мл смог значительно снизить эти уровни.
Вышеприведенные результаты доказали, что карримицин ингибировал синтез клеточных белков за счет ингибирования уровня фосфорилирования mTOR и белков по ходу транскрипции, тем самым ингибировав пролиферацию клеток A549. Результаты показали, что карримицин в умеренных и низких концентрациях ингибировал mTORC1 в большей степени, и после 48 ч наблюдалась активация с отрицательной обратной связью mTORC2. Однако каррримицин в большой концентрации можно было использовать как двойной ингибитор как для mTORC1, так и для mTORC2 без возникновения активации с отрицательной обратной связью (представлено на фиг. 4 и 5).
(3) Индуцирование аутофагии в клетках A549 карримицином
Способ: для определения аутофагии использовались флуоресцентная микроскопия и проточная цитометрия
Дансилкадаверин (MDC) - флуоресцирующий пигмент и эозинофильный краситель. Обычно его применяют для определения накопления специфических маркерных окрашивающих кислотных лизосом, образующиеся при аутофагии, которые до определенной степени могут отражать уровень аутофагии.
На 6-луночный планшет были посеяны клетки A549 в фазе логарифмического роста в количестве 2×105 на лунку. После культивации в течение 24 ч культуральная среда была удалена, были введены различные медикаменты для воздействия в течение 24 и 48 ч, после чего выполнялась однократная промывка фосфатно-солевым буферным раствором, а затем добавлялась культуральная среда эквивалентного объема, содержащая MDC в концентрации 0,05 ммоль, после чего в течение 20 минут проводилась инкубация при температуре 37°С в условиях затемнения; далее проводилась однократная промывка фосфатно-солевым буферным раствором, и затем проводилась флуоресцентная микроскопия или детекция посредством проточной цитометрии.
Результаты: mTORC1 может ингибировать аутофагию за счет связывания комплекса ULK1. Таким образом, было проведено исследование уровня аутофагии клеток, обработанных карримицином в течение 24 и 48 ч. Результаты окрашивания MDC показали, что клетки в контрольной группе флуоресцировали однородным зеленым светом. При повышении концентрации карримицина в клетках проявились заметные скопления частиц с яркой зеленой флуоресценцией. Результаты проточной цитометрии показали, что степень положительного окрашивания MDC после обработки медикаментом повысилась, и результаты согласовывались по времени выдержки, равному 24 и 48 ч (фиг. 6).
LC3 - белок-метчик аутофагии. При возникновении аутофагии в клетках уровень трансформации LC3 из типа I в тип II в клетках значительно повышается. P62 - субстрат аутофагии. При возникновении аутофагии в клетках P62 медиирует связывание субстрата аутофагии и саму аутофагию, а затем инкапсулируется в лизосомах вместе с субстратом аутофагии и расщепляется. Следовательно, при возникновении аутофагии в клетках уровень экспрессии Р62 в них понижается. Анализ по методу вестерн-блоттинга показал, что добавление карримицина может снижать уровень субстрата аутофагии P62 и повышать трансформацию белка LC3, связанного с аутофагией, из типа I в тип II, с одинаковыми результатами при выдержке в течение 24 и 48 ч (фиг. 7). Вышеприведенные результаты вместе доказывают, что карримицин может индуцировать аутофагию в клетках A549.
Поскольку аутофагия обладает двойными эффектами на опухолевые клетки, она может как защищать их, так и убивать. Следовательно, был использован 3-MA, ингибитор аутофагии, для исследования роли аутофагии, индуцируемой карримицином, в гибели клетки A549. Добавление ингибитора аутофагии 3-MA привело к снижению ингибирующего эффекта карримицина на рост клеток A549 (фиг. 8), показав, что аутофагия, индуцированная карримицином, привела к ингибированию пролиферации клеток A549.
(4) Индуцирование апоптоза в клетках A549 карримицином
Способ: аннексин V - фосфолипид-связывающий белок, зависимый от Ca2+, с молекулярной массой 35 кДа, который может специфически связываться с фосфатидилсерином (ФС). Фосфатидилсерин в основном распределяется по внутренней стороне клеточной мембраны. При возникновении клеточного апоптоза клетка будет выворачивать фосфатидилсерин на поверхность клетки, т.е., на наружную часть клеточной мембраны. Зонд аннексина V, промаркированный ФИТЦ, а именно - аннексин V-ФИТЦ может специфически связывать эти вывернутые фосфатидилсерины, а апоптоз клеток может быть определен очень просто и непосредственно проточной цитометрией или посредством флуоресцентного микроскопа.
Иодид пропидия (PI) - полинуклеотидный краситель, который не может проникать через нормальные клеточные мембраны. Когда клетки находятся на средней или поздней стадии некроза или апоптоза, целостность их мембран теряется. Иодид пропидия проникает в клетку и связывается с полинуклеотидом в ядре. Для определения и отражения полной информации о состоянии клеточной мембраны могут использоваться проточная цитометрия или флуоресцентная микроскопия. Таким образом, аннексин V-ФИТЦ и PI использовались совместно для разделения клеток на разных стадиях апоптоза.
На 6-луночный планшет были посеяны клетки A549 в фазе логарифмического роста в количестве 2×105 на лунку. После культивации в течение 24 ч культуральная среда была удалена, были введены различные медикаменты для воздействия в течение 24 и 48 ч, после чего выполнялась однократная промывка фосфатно-солевым буферным раствором; был добавлен приготовленный окрашивающий раствор (250 мкл буферного раствора, 7,5 мкл аннексина V-ФИТЦ, 10 мкл иодида пропидия, смешанных до однородного состояния) для определения апоптоза, после чего в течение 15 минут проводилась инкубация при комнатной температуре в условиях затемнения, а затем проводились флуоресцентная микроскопия и детекция проточной цитометрией.
Результаты: Для подтверждения механизма воздействия карримицина на клетки A549 для исследования применялось окрашивание AV-PI, а для разделения нормальных клеток, клеток на ранней, поздней стадиях апоптоза и омертвевших клеток - поточная цитометрия. Семейство каспаз играет очень важную роль в процессе медиации клеточного апоптоза, причем каспаза 3, являясь исполнительным белком апоптоза, связана с фрагментацией ДНК, конденсацией хроматина и формированием апоптотического тела. Следовательно, была исследована активность протеаз и уровень белков каспазы 3 посредством применения метода вестерн-блоттинга.
Результаты показали, что клетки A549, обработанные карримицином в течение 24 ч, давали зеленую флуоресценцию при концентрации 17 и 50 мкг/мл, однако красная флуоресценция отсутствовала. Проточная цитометрия показала, что клетки с концентрацией 50 мкг/мл продемонстрировали наличие апоптоза на ранней стадии (фиг. 10), уровень каспазы 3 значительно не возрос, а прототип PARP не был фрагментирован (фиг. 11А). Клетки A549, обработанные карримицином в течение 48 ч, начали усыхать в цитоплазме, а при повышении концентрации также проявились апоптотические тела (фиг. 9). Результаты AV-PI продемонстрировали, что явная зеленая флуоресценция проявилась при концентрации 5 и 17 мкг/мл, а явная красная - в ядре при концентрации 50 мкг/мл. Проточная цитометрия показала, что количество клеток на ранней стадии апоптоза при концентрациях 5 и 17 мкг/мл увеличилось, а при концентрации 50 мкг/мл также в большом количестве проявились клетки на поздней стадии апоптоза (фиг. 10). Конверсия каспазы 3 из прекурсора в активированную форму возросла, PARP в качестве субстрата был фрагментирован (фиг. 11В), а активность ферментов каспазы 3 повысилась (фиг. 12), что доказывает, что в клетках происходил апоптоз.
(5) Снижение уровня белков HIF-1α карримицином
Гипоксия и другие факторы, такие как инсулиновый фактор роста, могут индуцировать экспрессию HIF-1α, в то время как сверхактивированный mTOR также может активировать экспрессию HIF-1α с уровня транскрипции при условии достаточного количества кислорода, тем самым приводя к транскрипции фактора роста сосудистого эндотелия (ФРСЭ) по ходу транскрипции и других ангиогенных генов, что оказывает эффекты содействия росту сосудистой проницаемости, распада внеклеточного матрикса, миграции клеток эндотелия сосудов, пролиферации и ангиогенезу.
Анализ методом вестерн-блоттинга показал, что уровни белков сосудистого биосинтеза HIF-1α и VEGF-A значительно снизились после обработки клеток А549 карримицином в течение 24 и 48 ч (фиг. 13), что дает основания полагать, что карримицин может ингибировать пролиферацию опухолевых клеток за счет ингибирования уровня белков фактора А549, индуцируемого гипоксией.
(6) Воздействие карримицина на путь трансдукции сигналов ERK
Сигнальный путь Ras/Raf/MEK/ERK - один из наиважнейших сигнальных путей, по которому передаются внеклеточные сигналы в ядро, и он играет ключевую роль в регуляции выживаемости, колонизации, дифференцировке, апоптозе, метаболизме и других функциях клеток.
В клетках A549, обработанных карримицином в течение 24 ч, возможен рост уровня белков Ras, Raf и уровня фосфорилирования белка ERK. В то же время в клетках A549, обработанных карримицином в течение 48 ч, может проявляться рост белков Ras и Raf. Медикаменты со средней концентрацией могут значительно повысить уровень фосфорилирования ERK, в то время как медикаменты с высокой концентрацией могут понизить его. Результаты приведены на фиг. 14.
(7) Воздействие карримицина на клеточный цикл клеток A549
Распределение клеточных циклов A549, обработанных карримицином в разных концентрациях в течение 24 и 48 ч, было определено посредством проточной цитометрии с использованием PI. Было установлено, что обработка медикаментом в течение 24 ч не оказала явного воздействия на клеточный цикл. После обработки в течение 48 ч количество клеток в фазе синтеза, обработанных медикаментом в концентрации 1,7, 5, 17 и 50 мкг/мл, по сравнению с контрольной группой возросло на 1,86, 9,39, 4,75 и 24,38% соответственно. В итоге обработка карримицином в течение 48 ч индуцирует остановку цикла синтеза клеток A549 в зависимости от концентрации.
Как можно увидеть из вышеприведенных примеров испытаний, после добавления карримицина к клеткам A549 на 24 ч уровень фосфорилирования mTOR значительно снизился, а уровни фосфорилирования фактора инициации трансляции эукариот (белка 4E-BP1) и рибосомальной протеинкиназы S6-1 (S6K1) по ходу транскрипции mTOR были значительно ингибированы. За счет снижения биосинтеза белков опухолевых клеток скорость их пролиферации была замедлена, а уровень фосфорилирования PI3K - снижен, в то время как на уровень фосфорилирования AKT значительного влияния оказано не было. После обработки клеток А549 карримицином в течение 48 ч уровень фосфорилирования белков сигнального пути mTOR все еще можно было отрицательно регулировать, но сигнальный путь PI3K/AKT был активирован способом обратной связи при средней концентрации, что привело к значительному росту уровня фосфорилирования PI3K и AKT. Однако уровни фосфорилирования белков PI3K и AKT были заново ингибированы при высокой концентрации (50 мкг/мл). Таким образом, делается уверенное допущение о том, что карримицин может выступать двойным ингибитором mTORC1 и mTORC2. В условиях низкой и средней концентраций карримицин обеспечивает сильное ингибирование mTORC1, однако существует сильная отрицательная регуляция по обратной связи через 48 ч воздействия медикамента; при высокой концентрации на mTORC2 также оказывается определенный ингибирующий эффект.
Благодаря наблюдениям клеток A549, обработанных карримицином в течение 48 ч, с помощью фазово-контрастного микроскопа были установлены конденсация хроматина и явно выраженное образование апоптотических тел. Результаты окрашивания JC-1 показали, что по мере увеличения концентрации медикамента соотношение клеток с зеленой флуоресценцией постепенно возрастало, что указывает на то, что карримицин может снижать потенциал митохондриальной мембраны клеток A549 в зависимости от концентрации. Для определения уровня белков, связанных с апоптозом, применялся метод вестерн-блоттинга. Уровень белка прокаспазы-3 понижался, а уровень расщепляющей каспасы-3 - повышался. Между тем, субстрат каспазы-3 PARP расщеплялся, указывая на то, что апоптоз клеток A549, индуцированный карримицином, активировал каскадную реакцию каспазы. Уровень Bax возрастал, а уровни Bcl-XL и Bcl-2 - снижались. Таким образом, обработка карримицином в течение 48 ч смогла ингибировать пролиферацию опухолевых клеток за счет индуцирования апоптоза клеток A549. Вышеприведенные данные показывают, что явление апоптоза не было явным после 24 часов воздействия карримицина, в то время как явно наблюдался апоптоз с зависимостью от концентрации через 48 часов, а апоптоз в ранней стадии сменялся таковым в поздней стадии.
Являясь ингибитором mTOR, карримицин значительно улучшил трансформацию LC из типа I в тип II у клеток A549, а также привел к отрицательной регуляции уровня белка субстрата аутофагии P62. Окрашивание MDC и проточная цитометрия также подтвердили рост аутофагии. После добавления ингибитора аутофагии 3-MA ингибирующий эффект карримицина на клетки A549 снизился, что доказывает, что аутофагия A549, индуцируемая карримицином, является повреждающей, т.е., карримицин ингибирует пролиферацию клеток A549 за счет повышения уровня аутофагии этих клеток, в то время как явление аутофагии явно проявляется через 24 и 48 ч. До наступления апоптоза карримицин преимущественно может ингибировать выживание клетки за счет индуцирования аутофагии. Согласно настоящему изобретению уровень фосфорилирования белков ERK значительно понизился после обработки клетки A549 карримицином в течение 24 часов, в связи с чем было сочтено, что ингибирование сигнального пути PI3K/AKT/mTOR активировало сигнальный путь Ras/Raf/MEK/ERK.
Коротко говоря, карримицин может ингибировать пролиферацию и индуцировать апоптоз человеческих немелкоклеточных клеток рака легкого A549 в зависимости от концентрации, а также может применяться в качестве двойного ингибитора как для mTORC1, так и для mTORC2. При средней и низкой концентрациях ингибируется преимущественно mTORC1, что приводит к активации отрицательной обратной связи PI3K и AKT, в то время как при высокой концентрации может ингибироваться mTORC2, а уровень фосфорилирования белков PI3K и AKT может понижаться. Этим может быть индуцирована клеточная аутофагия, и она играет свою роль в уничтожении клеток. Это может привести к остановке фазы синтеза клеток A549. Кроме того, карримицин также активирует сигнальный путь Ras/Raf/ERK, причем уровни белков Ras и Raf подвергаются положительной регуляции, а уровень фосфорилирования ERK - повышается.
Вышеприведенное описание представляет собой исключительно предпочтительные варианты осуществления настоящего изобретения, и они не предназначены для ограничения объема последнего в какой-либо форме. Несмотря на то, что настоящее изобретение было раскрыто в предпочтительных вариантах осуществления, оно не ограничивается последними. Любой специалист в настоящей области техники может вносить изменения или осуществлять модификации технического содержания настоящих вариантов в виде эквивалентных вариантов осуществления без отступления от объема технического решения по настоящему изобретению. Однако любые простые модификации, эквивалентные изменения и модификации, вносимые в вышеприведенные варианты осуществления согласно технической сущности настоящего изобретения, по-прежнему остаются в рамках объема технического решения по настоящему изобретению.


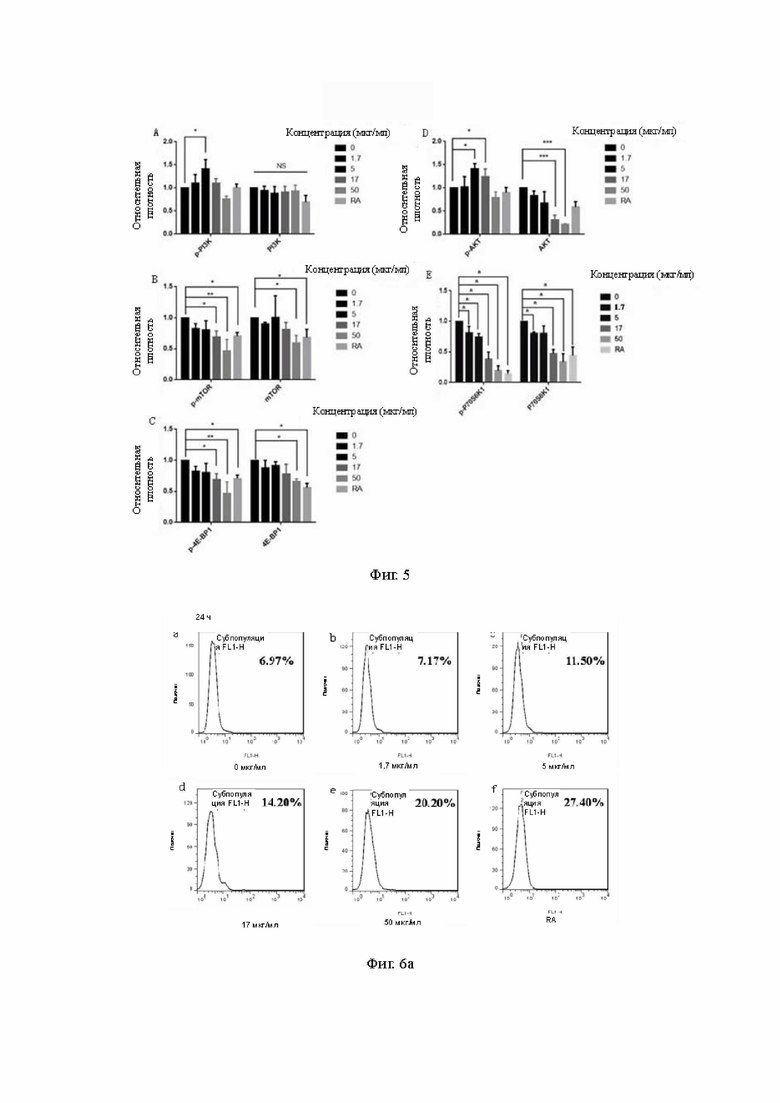


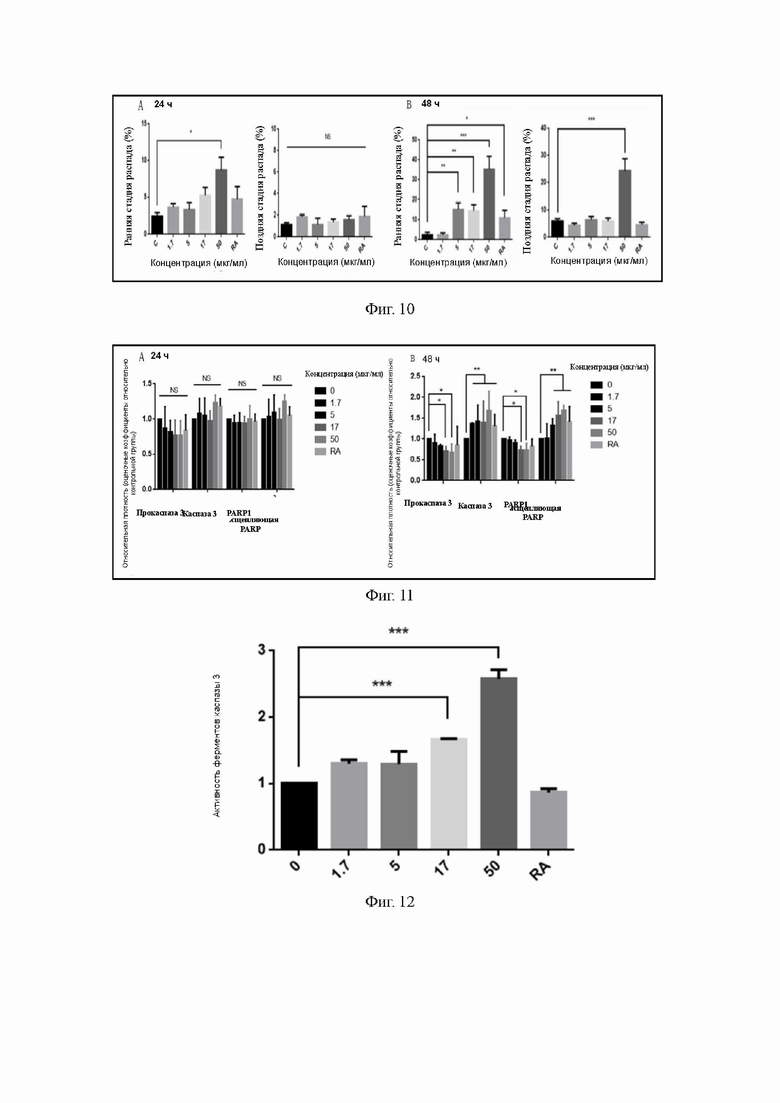

Настоящее изобретение относится к области медицины, а именно к онкологии, и раскрывает применение ингибитора mTOR в ингибировании активации белков в сигнальном пути PI3K/Akt/mTOR, отличающееся тем, что mTOR ингибитор включает карримицин или изовалерил-спирамицин I. Техническим результатом настоящего изобретения является способность карримицина ингибировать белки PI3K/Akt/mTOR сигнальных путей. 10 з.п. ф-лы, 14 ил., 2 табл., 3 пр.
1. Применение ингибитора mTOR в ингибировании активации белков в сигнальном пути PI3K/Akt/mTOR, отличающееся тем, что mTOR ингибитор включает карримицин или изовалерил-спирамицин I.
2. Применение по п. 1, отличающееся тем, что ингибитор mTOR применяется в качестве противоопухолевого медикамента, оказывая воздействие через сигнальный путь PI3K/Akt/mTOR, и предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
3. Применение по п. 3, отличающееся тем, что ингибитор mTOR применяется при лечении диабета, оказывая воздействие через сигнальный путь PI3K/Akt/mTOR, и предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
4. Применение по п. 1, отличающееся тем, что ингибитор mTOR применяется для лечения болезни Альцгеймера, оказывая воздействие через сигнальный путь PI3K/Akt/mTOR, и предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
5. Применение по п. 1, отличающееся тем, что ингибитор mTOR применяется для замедления старения, оказывая воздействие через сигнальный путь PI3K/Akt/mTOR, и предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
6. Применение по п. 1, отличающееся тем, что ингибитор mTOR предназначен для ингибирования активации mTORC1 и mTORC2.
8. Применение по п. 1, отличающееся тем, что ингибитор mTOR предназначен для ингибирования активации как минимум одного или нескольких белков PI3K, AKT, mTOR, S6K1 и 4EBP1 в сигнальном пути PI3K/Akt/mTOR.
9. Применение по любому из пп. 1-8, отличающееся тем, что доза ингибитора mTOR находится в диапазоне от 1 до 10000 мг/кг.
10. Применение по любому из пп. 1-8, отличающееся тем, что доза ингибитора mTOR находится в диапазоне от 10 до 5000 мг/кг.
11. Применение по любому из пп. 1-8, отличающееся тем, что доза ингибитора mTOR находится в диапазоне от 50 до 1000 мг/кг.
| YANG, Yali et al.: "Determination of the components of bitespiramycin by HPLC" Acta Pharmaceutica Sinica, 2009, vol | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
| ЛЕКАРСТВЕННАЯ ФОРМА ЛЕВОКАРРИМИЦИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЯ | 2011 |
|
RU2593499C2 |
| ЛЕВОВРАЩАЮЩИЕ ИЗОВАЛЕРИЛ-СПИРАМИЦИНЫ 1, II, III, ИХ ПРЕПАРАТЫ, СПОСОБ ПРИГОТОВЛЕНИЯ И УПОТРЕБЛЕНИЕ | 2011 |
|
RU2593498C2 |
| CN 1554355 A, 15.12.2004 | |||
| CN 101785778 A, 28.07.2010 | |||
| CN 101785779 A, 28.07.2010 | |||
| WO 2011110084 A1, 15.09.2011 | |||
| US 20110306571 A1, 15.12.2011 | |||
| Chi Kwan | |||
Авторы
Даты
2022-03-24—Публикация
2019-01-18—Подача