Изобретение относится к биотехнологии, в частности к способу получения комбинированной лекарственной формы гидролизного лигнина и сапонина, и может быть использовано в фармацевтической промышленности в технологии изготовления лекарств.
Тритерпеновые сапонины, выделенные из растений, составляют многочисленную группу лекарственных веществ: широко известны препараты женьшеня, аралии маньжурской, конского каштана, календулы и др. Фармакологические исследования выявили широкий спектр фармакологического действия: противоопухолевое, противовоспалительное, обезболивающее, жаропонижающее и гастропротекторное. Другими известными фармакологическими свойствами являются антинематодная, антидиабетическая, цитотоксическая и иммуностимулирующая активность, а также защита от цитотоксического повреждения [SonawaneS. М. AReviewofRecentandCurrentResearchStudiesontheBiologicalandPharmalogicalActivitiesofSapindusMukorossi I S. Μ. Sonawane, Η. Sonawane // IntemationalJoumaloflnterdisciplinaryResearchandlnnovations. - 2015. - Vol. 3, №4. - P. 85-95].
Известно, что многие соединения этого класса обладают значительной ростостимулирующей активностью. Тритерпеновые гликозиды оказывают большое влияние на проницаемость растительных клеток, что связано с их поверхностной активностью. Установлено, что их определенные концентрации ускоряют прорастание семян, рост и развитие растений, а концентрированные растворы тормозят, т.е. их действие напоминает действие ростовых гормонов [FaizalA., GeelenD. Saponinsandtheirroleinbiologicalprocessesinplants // Phytochem. Rev. 2013. Vol. 12. P. 877-893].
Молекулярная структура сапонинов может подвергаться химическим превращениям при хранении или обработке, что, в свою очередь, может изменять их фармакологические свойства. Гликозидная связь и связи между остатками углеводов могут подвергаться частичному гидролизу в условиях, близких к нейтральному значению рН, что приводит к образованию агликонов, просапогенинов, углеводных цепочек или моносахаридов.
Иммобилизация на поверхности сорбентов позволит предотвратить их разрушение с сохранением функциональных свойств. В последнее время метод клатрирования (комплексообразования) сорбентов с природными веществами приобретает особую популярность. Созданные таким путем лекарственные композиции позволяют сохранить целостность молекулярных структур лекарственных субстанций в различных средах организма, сохраняя их фармакологические свойства.
В качестве носителя-матрицы для гликозидов может быть использован лигнин. Лигнин - это органический гетероцепной кислородсодержащий полимер, у которого отсутствует единый тип связи между мономерными звеньями. В структурных единицах лигнина содержатся различные полярные группы и, в том числе, способные к ионизации (кислые) фенольные гидроксилы и в небольшом числе карбоксильные группы, вследствие чего лигнин является полярным полимером, проявляющим свойства полиэлектролита. В лигнине, благодаря наличию большого числа гидроксильных и других полярных групп, значительно развиты водородные связи (внутри- и межмолекулярные). Из-за высокой степени разветвленности макромолекулы лигнина имеют глобулярную форму и такие препараты представляют собой порошки.
Гидролизный лигнин (ГЛ) обладает высокоразвитой внутренней поверхностью и проявляет значительные сорбционные свойства, что служит предпосылкой для получения на его основе энтеросорбентов, а также использования в качестве матрицы для иммобилизации биологически активных веществ.
Известны композиционные материалы на основе лигнина и полиакрилонитрила [Патент RU 2621758, композиционный материал на основе полиакрилонитрила с лигнином, авторы - Штягина Л.М., Лысенко А. Α., Свердлова Н.И., Сазанов Ю.Н., Виноградова Л.Е., Крутов С.М.], на основе диметилгидразина [М.П. Семушина, К.Т. Боголицин, А.Ю. Кожевников, Д.С.Косяков / Сорбционные свойства технических лигнинов по отношению к 1,1-диметилгидразину // Химия в интересах устойчивого развития. - 2013. - Т. 21 - с. 551-555.], радиоактивного стронция [Никифоров А.Ф., Юрченко В.В. Сорбция радиоактивного стронция из водных растворов модифицированным гидролизным лигнином // Сорбционные и хроматографические процессы. 2010. Т. 10. Вып. 5. - С. 676-684]. Предложена композиция лигнина с поливинилпирролидоном в виде таблеток [Заявка 99107824/14 РФ, кл. А61К 35/78, заявл. 12.04.99, опубл. 20.02.2001].
Наиболее близким аналогом является композиция для приготовления влажного порошка или влажных гранул лигнина с лактулозой, используемая для профилактики и лечения заболеваний желудочно-кишечного тракта [Патент 2167669 РФ, кл. А61К 35/78, 9/14, заявл. 11.05.99, опубл. 27.05.2001]. Техническим результатом является получение новых лекарственных форм гидролизного лигнина, позволяющих избежать осложнений, вызванных приемом лигнина и лечить заболевания желудочно-кишечного тракта. Смесь веществ готовят в виде влажного порошка или влажных гранул. Композиция содержит 80% мас. гидролизного лигнина и 20% мас. 45% водного раствора лактулозы. Полученную смесь подсушивают в термостате до влажности 50% и расфасовывают в пакеты. Также вторым способом получения композиционной формы является смешивание влажного порошка лигнина (состоящего из частиц 0,25-0,55 мкм), взятого по массе в количестве 90% и 10% по мас. 45% раствора лактулозы. Смесь подсушивают до влажности 70%. Недостатком данного способа является невозможность оценить соотношение иммобилизованной на лигнине и свободной форм лактулозы, а также невысокое содержание лактулозы в составе лигнина. В основе метода получения данной композиции лежит механическое смешивание компонентов в роторном смесителе.
Прототипом настоящего изобретения является [Патент 2680600 РФ, кл. А61К 33/44, C12N 11/06, C12N 11/14, заявл. 27.12.2017, опубл. 25.02.2019] композиционный материал на основе угля обыкновенного, активированного при температуре 900-1000°С, отличающийся тем, что дополнительно содержит тритерпеновый сапонин, иммобилизованный на угле, в количестве не менее 30% от массы угля.
При этом предложен способ получения данного композиционного материала, включающий приведение сорбента в контакт с раствором иммобилизуемого вещества, сушку, где раствором иммобилизуемого вещества является водный раствор сапонина концентрацией 0,1-0,25 г/л, а сорбционный процесс проходит или в динамических условиях при пропускании раствора через сорбент из расчета 2,5-3 л/г сорбента со скоростью 0,25-0,5 мл/мин, или в статических условиях из расчета 1-2 л/г сорбента при выдерживании в течение не менее 4 часов при комнатной температуре. К недостаткам материала можно отнести низкую сорбционную емкость по сапонину.
Задачей изобретения является разработка способа получения комбинированного препарата на основе сапонин-лигнинного комплекса.
Технический результат заключается в расширении ассортимента композиционных материалов на основе гидролизного лигнина с высокой сорбционной емкостью по тритерпеновому сапонину, не менее 56% от массы сорбента.
Технический результат достигается тем, что вспособе получения композиционного материала на основе гидролизного лигнина и тритерпенового сапонина, включающем приведение сорбента в контакт с раствором иммобилизуемого вещества, сушку, согласно изобретению, сорбционный процесс проходит или в динамических условиях, при пропускании раствора тритерпенового сапонина через гидролизный лигнин из расчета 1 л/г гидролизного лигнина со скоростью 1 мл/мин, или в статических условиях, при этом диаметр сорбционной колонки 1-1,5 см, высота слоя сорбента 2,5-3,5 см, из расчета 1 л/г гидролизного лигнина; полученный композиционный материал выдерживают при перемешивании при комнатной температуре в течение 4 часов; концентрация водного раствора тритерпенового сапонина составляет 0,8-1 г/л; высушивание композиционного материала ведут на воздухе в течение 2 суток; сорбционная емкость полученного композиционного материала по сапонину составляет не менее 56% от массы сорбента.
Применение сапонина, иммобилизованного на лигнине, позволит изменить скорость высвобождения гликозида, сохранит целостность его структуры.
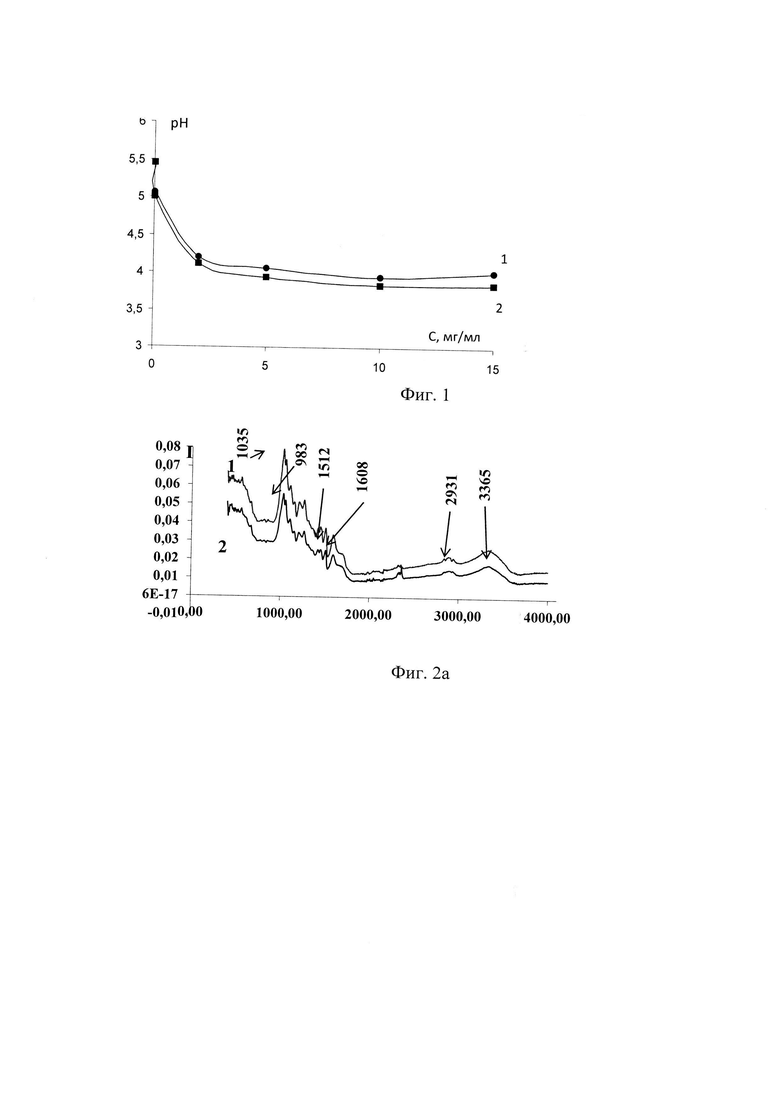
В предварительных исследованиях было установлено, что основу получаемых супрамолекулярных структур, содержащих лекарственные соединения и для сохранения базовых фармакологических эффектов, должны составлять не ковалентные взаимодействия, а водородные меж- и внутримолекулярные, а также дисперсионные связи (слабые взаимодействия). Однако в работе [Сорбция радиоактивного стронция из водных растворов модифицированным гидролизным лигнином/ Никифоров А.Ф., Юрченко В.В // Сорбционные и хроматографические процессы. 2010. Т. 10. Вып. 5] установлено, что поверхность частиц гидролизного лигнина в интервале рН 1-4 имеет положительный заряд. В интервале рН 4-11 поверхность частиц лигнина заряжена отрицательно. Следовательно, величина рН примерно равная 4 соответствует нулевому значению ξ-потенциала поверхности частиц лигнина (изоэлектрическая точка). Таким образом, при сорбции из водного раствора сапонина (рН-4,5), поверхность лигнина не имеет заряда и ионные взаимодействия с молекулой сапонина маловероятны. На фигуре 1 приведены значения рН водного раствора сапонина в контакте с лигнином (2). Аналогичный с водным раствором (1) ход кривой свидетельствует об отсутствии ионных взаимодействий в ходе сорбционного поглощения сапонина лигнином.
Примером образования комплексов на основе лигнина с помощью водородных связей является комплекс «лигнин лиственных пород - гемицеллюлоза», описанный в [Физическая химия лигнина: монография / [К.Г. Боголицын и др.; под ред. К.Г. Боголицына и В.В. Лунина; Федеральное агентство по образованию, Архангельский гос.технический ун-т. - Архангельск: Архангельский гос. технический ун-т, 2009. - 489 с.] Получаемая в работе лигноуглеводная матрица является суперпозицией взаимопроникающих сеток, образованных водородными связями. В хвойной древесине лигнин состоит в основном из единиц кониферилового типа, а гемицеллюлозы из галактозы, маннозы и ксилозы. Если сравнить полученные данные о сродстве кониферилового спирта к целлюлозному и гемицеллюлозным предшественникам, то оно гораздо выше к галактозе, маннозе и ксилозе, чем к глюкозе. В состав гемицеллюлоз входят: D-фруктоза, D-ксилоза, D-галактоза, D-манноза, L-арабиноза, L-рамноза, D-глюкоза, D-галактуроновая и 4-O-метил-D-глюкуроновая кислоты, которые присутствуют в виде боковых ответвлений.
Аналогичный моносахаридный состав присутствует и в молекуле сапонина. Поэтому можно, предположить, что связывание его с лигнином будет осуществляться за счет Η-связей между углеводными фрагментами молекулы сапонина и кислородсодержащими функциональными (сирингилпропановыми единицами) группами структуры лигнина. Высокая удельная поверхность сорбента (790 м2/г), а также наличие преимущественно макропор (500-5000 нм2) позволяет сорбировать молекулы сапонины как в свободной форме, так и в форме плотноупакованных ассоциатов различной структуры. Результатом иммобилизации является высокая сорбционная емкость по сапонину, достигающая не менее 56%.
Были сняты ИК-спектры образцов лигнина в свободной форме и в форме сапонина (фиг. 2а,б). Валентные колебания при 1608 см-1, отнесенные к карбоксильной группе, в спектре лигнина в форме сапонина смещены до 1585 см-1 за счет образования межмолекулярных Η-связей. Ароматическое бензольное кольцо, сопряженное с двойными связями карбонильных групп лигнина, поглощает в области 1512 см-1. В спектре лигнина в форме сапонина эта полоса смещена до 1504 см-1, вероятно за счет дисперсионных взаимодействия с циклической системой агликона сапонина. Образование Н-связей также подтверждается смещением полосы при 1446 см-1, характерной для поглощения кислородсодержащих групп и полосы при 1218 см-1, отнесенной к колебаниям фенольной группы до 1425 см-1 и 1215 см-1, соответственно. Наличие полосы 1035 см-1, отнесенной к скелетным колебаниям гваяцильного кольца, а также отсутствие полос поглощения сирингильного кольца, позволяют предположить, что данный лигнин является хвойным. Смещение полосы 1035 см-1 до 983 см-1 поглощения в области, отнесенные к плоскостным деформационным колебаниям С-Н групп гваяцильного кольца, может указывать на дисперсионные взаимодействия между структурой лигнина и кольцами агликона сапонина.
Образование слабых межмолекулярных взаимодействий подтверждается высокой степенью регенерации сорбента. В качестве десорбирующего вещества может использоваться вода или раствор 0,1 Μ соляной кислоты. При этом степень регенерации достигает 68 и 63% соответственно. Полученные результаты по регенерации, т.е степени высвобождения сапонина в молекулярной форме, могут использоваться при оценке биологической активности и максимального терапевтического эффекта полученных лекарственных форм.
На фиг. 1 представлена зависимость кислотности среды (рН) от концентрации водного раствора сапонина, 1- раствор сапонина, 2- раствор сапонина в контакте с лигнином.
На фиг. 2а показаны ИК-спектры 1-лигнина, 2-лигнина с сапонином С=0,05 мг/мл
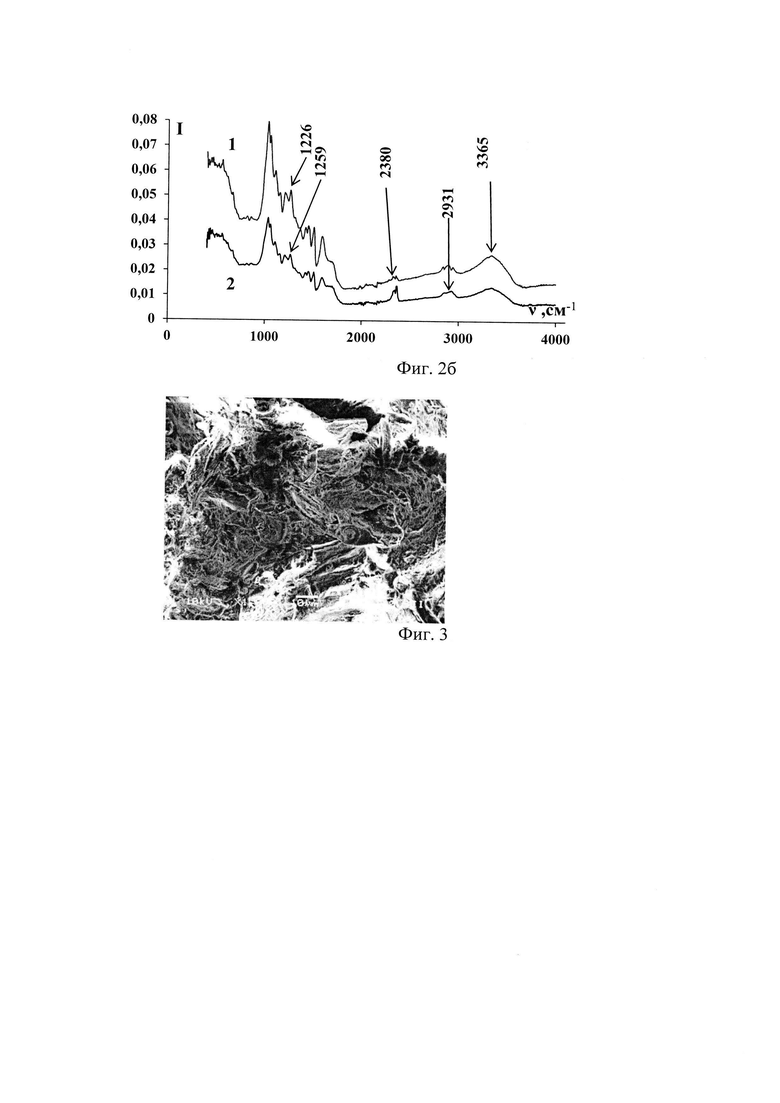
На фиг. 2б показаны ИК-спектры 1-лигнина, 2-лигнина с сапонином С=2 мг/мл
На фиг. 3 приведены РЭМ-изображения образца лигнина с сапонином.
Анализ РЭМ-изображений образца лигнина с сорбированным сапонином (фиг. 3) показал сохранение волокнистой архитектуры поверхности с темными участками, предположительно, порового пространства. Рельеф поверхности энтеросорбента неоднороден с характерными изгибами.
Получаемый модифицированный сорбент имеет высокую емкость по сапонину за счет заполнения макропор (500-5000 нм) молекулами сапонина и образованием ассоциатов в фазе сорбента. Концентрирование гликозида в порах лигнина приводит к дегидратации последнего и снижению влагосодержания с 12 до 5%. Предложенный сорбционный способ прост в исполнении, не требует предварительной подготовки сорбента. Были определены оптимальные диапазоны концентраций рабочих растворов сапонина, позволившие снизить расход вещества при сохранении максимального значения емкости сорбента.
Пример 1. Навеску воздушно-сухого лигнина массой 0,5 г переносят в стеклянную колонку с внутренним диаметром 1 см. Высота слоя сорбента составила 3,5 см. Через слой сорбента пропускают 0,5 л водного растворатритерпенового сапонина с концентрацией 0,8 г/л. Скорость пропускания поддерживают постоянной 1 мл/мин. По окончании процесса сорбент извлекают из колонки и высушивают на воздухе в течение 2 суток. Количество сорбированного сапонина составило 0,56 г/г сорбента. Степень извлечения сапонина из раствора составила 70%.
Пример 2. Навеску воздушно-сухого лигнина массой 0,5 г переносят в стеклянную колонку с внутренним диаметром 1,5 см. Высота слоя сорбента составила 2,5 см. Через слой сорбента пропускают 0,5 л водного раствора тритерпенового сапонина с концентрацией 1 г/л. Скорость пропускания поддерживают постоянной 1 мл/мин. По окончании процесса сорбент извлекают из колонки и высушивают на воздухе в течение 2 суток. Количество сорбированного сапонина составило 0,7 г/г сорбента. Степень извлечения сапонина из раствора составила 75%.
Пример 3. Навеску воздушно-сухого лигнина массой 0,8 г переносят в стеклянную колонку с внутренним диаметром 1,5 см. Высота слоя сорбента составила 3,5 см. Через слой сорбента пропускают 0,8 л водного раствора тритерпенового сапонина с концентрацией 1 г/л. Скорость пропускания поддерживают постоянной 1 мл/мин. По окончании процесса сорбент извлекают из колонки и высушивают на воздухе в течение 2 суток. Количество сорбированного сапонина составило 0,78 г/г сорбента. Степень извлечения сапонина из раствора составила 78%.
Пример 4. Навеску сорбента массой 0,2±0,0002 г в воздушно-сухом состоянии заливали в коническую колбу с притертой крышкой раствором тритерпенового сапонина объемом 200 мл с концентрацией 1,0 г/л. Содержимое колб выдерживали при перемешивании в течение 4 часов до установления равновесия в системе. Затем сорбент отфильтровывали и высушивали на воздухе в течение 2 суток. Количество сорбированного сапонина составило 0,60 г/г сорбента. Степень извлечения сапонина из раствора составила 60%.
Использование меньших концентраций сапонина для достижения тех же значений сорбционных параметров возможно при значительном снижении скорости пропускания раствора (в динамических условиях до 0,2-0,5 мл/мин) или увеличении времени контакта (в статических условиях до 6-8 часов). Увеличение концентрации сапонина делает неэффективным процесс его извлечения из раствора (количество сорбированного сапонина увеличивается незначительно).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ НА ОСНОВЕ УГЛЯ АКТИВИРОВАННОГО И ТРИТЕРПЕНОВОГО САПОНИНА | 2017 |
|
RU2680600C1 |
| Биомодифицированный материал для очистки водных сред и почвы от тяжелых металлов и радионуклидов | 2023 |
|
RU2832772C1 |
| Биомодифицированный материал для очистки почвогрунтов от тяжелых металлов, нефти и нефтепродуктов | 2022 |
|
RU2787371C1 |
| СПОСОБ РЕАБИЛИТАЦИИ ПОЧВЫ, ЗАГРЯЗНЕННОЙ РАДИОАКТИВНЫМИ НУКЛИДАМИ | 2006 |
|
RU2317603C1 |
| ЭНТЕРОСОРБЕНТ ИЗ ЛУБА БЕРЕЗОВОЙ КОРЫ | 2016 |
|
RU2611388C1 |
| Способ получения активизированного сорбента на основе гидролизного лигнина | 1980 |
|
SU891141A1 |
| СПОСОБ РЕАБИЛИТАЦИИ РАДИОАКТИВНО-ЗАГРЯЗНЁННЫХ ПОЧВ | 2023 |
|
RU2812709C1 |
| СПОСОБ СОРБЦИОННОГО ИЗВЛЕЧЕНИЯ ЦЕЗИЯ ИЗ ПРИРОДНЫХ И ТЕХНОЛОГИЧЕСКИХ ВОД | 1993 |
|
RU2065629C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО БИОКАТАЛИЗАТОРА И СПОСОБ ПОЛУЧЕНИЯ ВОДНЫХ РАСТВОРОВ АМИДОВ С ИСПОЛЬЗОВАНИЕМ ЭТОГО БИОКАТАЛИЗАТОРА | 2007 |
|
RU2352635C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ИЗ ЛИГНОЦЕЛЛЮЛОЗНОГО СЫРЬЯ | 1995 |
|
RU2089284C1 |
Изобретение относится к способу получения композиционного материала на основе гидролизного лигнина и сапонина и самому композиционному материалу, который может быть использован в фармацевтической промышленности в технологии изготовления лекарств. Способ получения композиционного материала включает приведение сорбента - гидролизного лигнина в контакт с раствором иммобилизуемого вещества - тритерпенового сапонина, выдерживание при перемешивании при комнатной температуре в течение 4 часов при концентрация водного раствора тритерпенового сапонина 0,8-1 г/л; высушивание полученного композиционного материала ведут на воздухе в течение 2 суток. Сорбционный процесс проходит или в динамических условиях при пропускании раствора тритерпенового сапонина через гидролизный лигнин из расчета 1 л/г гидролизного лигнина со скоростью 1 мл/мин, или в статических условиях, при этом диаметр сорбционной колонки 1-1,5 см, высота слоя сорбента 2,5-3,5 см, из расчета 1 л/г гидролизного лигнина. В результате получают композиционный материал, в котором тритерпеновый сапонин иммобилизован на лигнине в количестве не менее 56% от массы сорбента. Технический результат заключается в расширении ассортимента композиционных материалов на основе гидролизного лигнина с высокой сорбционной емкостью по тритерпеновому сапонину. 2 н.п. ф-лы, 3 ил, 4 пр.
1. Способ получения композиционного материала, включающий приведение сорбента в контакт с раствором иммобилизуемого вещества, сушку, отличающийся тем, что в качестве сорбента используют гидролизный лигнин, а в качестве иммобилизуемого вещества используют тритерпеновый сапонин, сорбционный процесс проходит или в динамических условиях при пропускании раствора тритерпенового сапонина через гидролизный лигнин из расчета 1 л/г гидролизного лигнина со скоростью 1 мл/мин, или в статических условиях, при этом диаметр сорбционной колонки 1-1,5 см, высота слоя сорбента 2,5-3,5 см, из расчета 1 л/г гидролизного лигнина; полученный композиционный материал выдерживают при перемешивании при комнатной температуре в течение 4 часов; концентрация водного раствора тритерпенового сапонина составляет 0,8-1 г/л; а высушивание полученного композиционного материала ведут на воздухе в течение 2 суток.
2. Композиционный материал, полученный способом по п.1, включающий тритерпеновый сапонин, который иммобилизован на сорбенте, представляющем собой гидролизный лигнин, в количестве не менее 56% от массы сорбента.
| КОМПОЗИЦИОННЫЙ МАТЕРИАЛ НА ОСНОВЕ УГЛЯ АКТИВИРОВАННОГО И ТРИТЕРПЕНОВОГО САПОНИНА | 2017 |
|
RU2680600C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРИГОТОВЛЕНИЯ ГОТОВОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ЭНТЕРОСОРБЕНТА, СПОСОБ ПРИГОТОВЛЕНИЯ ГОТОВОЙ ЛЕКАРСТВЕННОЙ ФОРМЫ ЭНТЕРОСОРБЕНТА И СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 1999 |
|
RU2167669C2 |
| СМУСЕВА С.О | |||
| и др | |||
| "Особенности модификации поверхности хитозана при поглощении ПАВ-тритерпеновых сапонинов" Химия и технология новых веществ и материалов: Тезисы докладов VІІ Всероссийской молодежной научной конференции | |||
| Сыктывкар, 2017 | |||
| Приспособление для останова мюля Dobson аnd Barlow при отработке съема | 1919 |
|
SU108A1 |
| (Коми научный центр УрО РАН), стр.95-97. | |||
Авторы
Даты
2022-04-12—Публикация
2021-04-15—Подача