Область техники, к которой относится изобретение
Изобретение относится к медицине, а именно к хирургии и может быть использовано в реконструктивной хирургии пищевода при различных патологиях.
Уровень техники
Одномоментная пластика после эзофагэктомии является приоритетной задачей оперативной гастроэнтерологии. Наиболее выгодным пластическим материалом для пластики пищевода считают желудок по причине его естественного продолжения в желудочно-кишечном тракте (ЖКТ) и надежного кровоснабжения [Wormuth J.K., Heitmiller R.F. Esophageal conduit necrosis. Thorac. Surg. Clin. 2006. Fer. 16(1). 11-22. Doi. 10.1016/j.thorsurg.2006.01.003]. Однако желудок может оказаться непригодным для эзофагопластики из-за его комбинированного с пищеводом поражения, сочетанного заболевания или его повреждения вследствие ранее перенесенных хирургических вмешательств. При отсутствии, либо непригодности желудка для эзофагопластики выполняют толсто- либо тонкокишечную пластику, которая ассоциирована с большим количеством осложнений и технически более трудоемка [Swisher SG, Hofstetter WL, Miller MJ. The supercharged microvascular jejunal interposition. Semin Thorac Cardiovasc Surg 2007; 19:56-65. Yasuda T, Shiozaki H. Esophageal reconstruction using a pedicled jejunum with microvascular augmentation. Ann Thorac Cardiovasc Surg 2011; 17:103-109]. Стоит отметить, что и эти способы реконструкции не всегда выполнимы. Причина этому ишемические расстройства трансплантата и недостаточная длина, констатируемая в ходе операции, что заставляет хирургов отказаться от первичной пластики пищевода. Существующие варианты полной или частичной реваскуляризации перемещенных висцеральных сегментов не получили широкого распространения из-за высокой частоты некрозов (до 20%), стриктур и свищей в послеоперационном периоде [Yoshimoto S., Kawabata K., Mitani H. Analysis of 59 cases with free flap thrombosis after reconstructive surgery for head and neck cancer. Auris Nasus Larynx 2010; 37: 205-211]. Именно этим определен постоянный поиск вариантов рациональной утилизации пластического материала при сочетанных или комбинированных поражениях пищевода и желудка для реализации основного принципа эзофагопластики - ее завершенности.
Аналогом предлагаемого способа эзофагопластики является формирование изоперистальтического трансплантата из большой кривизны желудка с питанием на правых желудочно-сальниковых сосудах по А.Ф. Черноусову [Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С., Хирургия пищевода: Руководство для врачей. М.: Медицина, 2000. - 352 с]. Отступив 2,5-3 см выше привратника по направлению от малой к большой кривизне в проксимальном направлении, при помощи сшивающего аппарата формируют трубку шириной 4 см, натягивая желудок за дно (фиг.1.). Механический шов дополнительно укрывают непрерывным серозно-мышечным швом. Размещают трансплантат заднемедиастинально и формируют шейное соустье двухрядными отдельными узловыми швами. Известны работы, описывающие использование оперированного желудка в качестве пластического материала для эзофагопластики после ранее сформированных гастростом или перенесенных фундопликаций [Марийко В.А, и др., Эффективность использования оперированного желудка при эзофагопластике, Вестник хирургии Т. 173 №2, 2014, С. 23-26], при условии сохраненной правой желудочно-сальниковой артерии.
Недостатком вышеуказанного способа является дефицит длины желудочного трансплантата после предшествующих резекционных вмешательств на желудке, его комбинированное с пищеводом поражение, а также сочетанная патология, требующая не только субтотальной эзофагэктомии, но и резекции желудка.
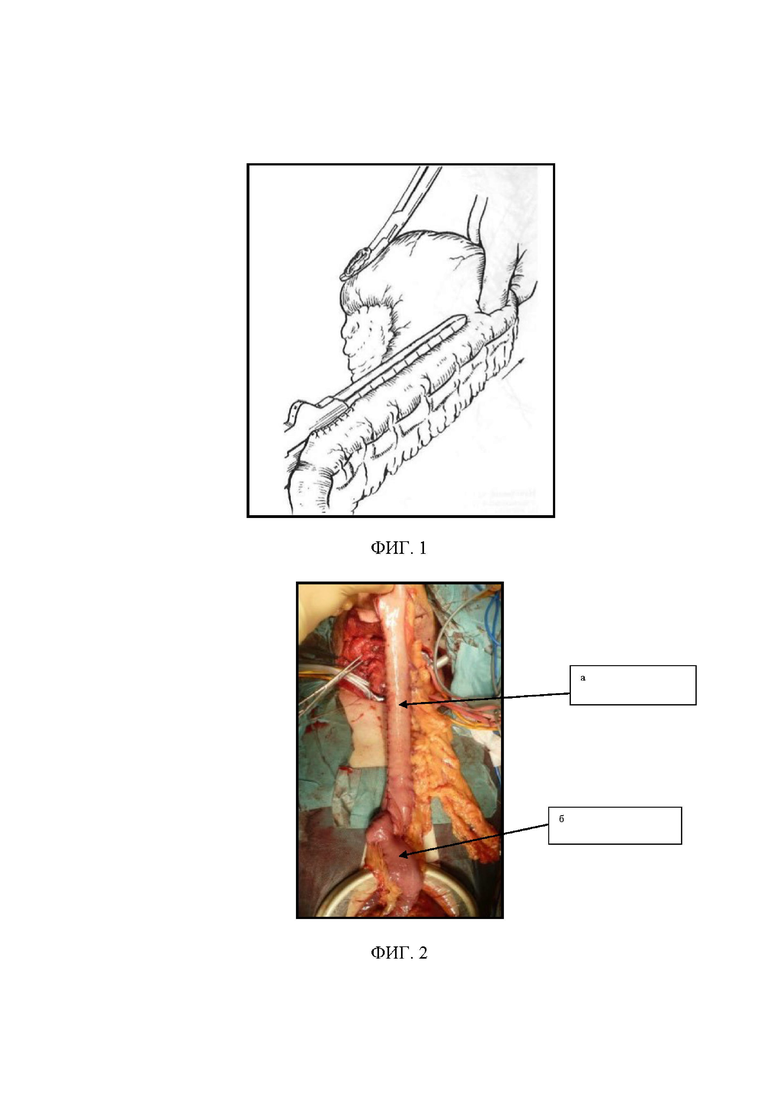
Наиболее близким к заявленному решению является способ реконструкции желудка после фаринголарингэктомии с тотальной эзофагэктомией [Watanabe M., Baba Y., Yoshida N., Ishimoto T., Sakaguchi H., Kawasuji M., Baba H. Modified gastric pull-up reconstructions following pharyngolaryngectomy with total esophagectomy. Dis Esophagus. 2014 Apr; 27(3):255-61. doi: 10.1111/dote.12086. Epub 2013 May 15. PMID: 23672461]. Согласно описанному в публикации способу, отсекают сформированный желудочный трансплантат от луковицы двенадцатиперстной кишки (ДПК) при помощи линейного степлера, после чего выполняют резекцию антрального отдела и перемещают сформированную мобильную желудочную трубку через заднее средостение на шею, с последующим формированием пищеводно-желудочного соустья однорядным непрерывным швом. Сохраняют питающую ножку трансплантата на правых желудочно-сальниковых сосудах. Данный прием позволяет придать желудочному трансплантату большую мобильность и переместить его на шею для формирования пищеводно-желудочного анастомоза в зоне наиболее благоприятного кровоснабжения, избегая натяжения тканей. Аборальный конец трансплантата соединяли с выделенной по Ру петлей тощей кишки. Для этого на расстоянии 20 см от связки Трейца пересекали тонкую кишку и анастомозировали отводящую петлю с трансплантатом «конец в бок». Приводящий отдел соединяли с Ру петлей анастомозом «бок в бок» (фиг. 2).
Недостатком вышеуказанного способа является:
1. Выключение дуоденального пассажа, что считается основной причиной развития тяжелых нарушений пищеварения в послеоперационном периоде [Ручкин Д.В., Ян Ц. Еюногастропластика как альтернативный способ реконструкции пищеварительного тракта после гастрэктомии. Хирургия. Журнал им. Н.И. Пирогова. 2015, 9, 57-62. Doi: 10.171116/hirurgia2015957-62].
2. Формирование желудочно-кишечного анастомоза «конец в бок», что в послеоперационном периоде может вызвать нарушение пассажа пищи из трансплантата в нижележащие отделы ЖКТ. Причина этому «слепой» конец отводящей петли, который под действием пищевых масс растягивается, образуя «слепой мешок», и деформирует соустье [Захаров Е.И., Захаров А.Е. Еюногастропластика при болезнях оперированного желудка. М. Медицина. - 1970. - 232 с.].
3. Однорядный шов желудочно-пищеводного соустья в 20% наблюдений осложняется несостоятельностью [Watanabe M., Baba Y., Yoshida N., Ishimoto T., Sakaguchi H., Kawasuji M., Baba H. Modified gastric pull-up reconstructions following pharyngolaryngectomy with total esophagectomy. Dis Esophagus. 2014 Apr; 27(3):255-61. doi: 10.1111/dote.12086. Epub 2013 May 15. PMID: 23672461].
Технической проблемой, решение которой обеспечивается при осуществлении изобретения, является создание способа одномоментной эзофагопластики комбинированным висцеральным трансплантатом в условиях сочетанного поражения пищевода и желудка, лишенного перечисленных выше недостатков.
Раскрытие сущности изобретения
Техническим результатом, на достижение которого направлено заявленное изобретение, является обеспечение больному полноценного питания через рот и сохранение дуоденального пассажа пищи за счет формирования комбинированного трансплантата на естественном источнике кровоснабжения из культи желудка и сегмента тощей кишки, снижение риска несостоятельности пищеводного соустья за счет формирования двухрядного анастомоза в зоне наиболее благоприятного кровоснабжения трансплантата, в условиях сочетанного поражения пищевода и желудка.
Предложенный способ позволяет использовать резецированный желудок в качестве пластического материала при осуществлении эзофагопластики путем отсечения его от ДПК с сохранением питания культи на правой желудочно-сальниковой артерии и вене. Сегмент тощей кишки на сосудистой ножке позволяет заместить возникающий диастаз между коротким желудочным кондуитом и ДПК. Изобретение также направлено на профилактику несостоятельности швов пищеводных анастомозов и послеоперационного некроза желудочного трансплантата в случае дефицита его длины. Перевод желудочного трансплантата в заднее средостение на естественном источнике кровоснабжения позволяет выполнить шейное соустье в зоне наиболее благоприятного кровоснабжения двухрядным швом, избежать его натяжения. Формирование желудочно-тонкокишечного анастомоза «конец в конец» снижает риск нарушения пассажа пищи в отдаленном периоде. Заявленное изобретение позволяет сохранить ободочную кишку в качестве висцерального резерва эзофагопластики без существенного ущерба для функции пищеварения.
Технический результат достигается за счет использования способа одномоментной эзофагопластики комбинированным висцеральным трансплантатом после субтотальной эзофагэктомии и резекции желудка при сочетанных поражениях пищевода и желудка, включающего формирование короткого желудочного трансплантата на естественном источнике кровоснабжения и перемещение его на шею, отличающегося тем, что после субтотальной эзофагэктомии формируют желудочный трансплантат в виде желудочной трубки, отсекают его от двенадцатиперстной кишки (ДПК) с сохранением питающей ножки правых желудочно-сальниковых сосудов; затем формируют тонкокишечную вставку длиной 20 см на третьей паре тощекишечных артерий (для устранения возникающего диастаза между культей ДПК и коротким желудочным трансплантатом) с последующим перемещением ее в верхний отдел брюшной полости через окно в мезоколон, не допуская перекрута сосудистой ножки по оси, после чего последовательно формируют однорядный гастроеюноанастомоз "конец в конец" и двухрядный еюнодуденоанастомоз "конец в конец"; слева на шее по медиальному краю левой кивательной мышцы выполняют разрез и мобилизуют шейный отдел пищевода с последующим выведением его через шею и пересечением на Г-образном зажиме на 3,0-5,0 см ниже глотки, сформированный желудочно-тонкокишечный трансплантат проводят через заднее средостение на шею, избыток культи шейного отдела пищевода и желудочно-тонкокишечного трансплантата отсекают и формируют двухрядный эзофагогастроанастомоз «конец в конец» отдельными узловыми швами.
Использование заявляемого способа позволит сохранить естественный пассаж пищи; избежать нарушения эвакуации пищи из трансплантата в нижележащие отделы ЖКТ; снизить риск несостоятельности пищеводного соустья, путем формирования двухрядного анастомоза в зоне наиболее благоприятного кровоснабжения трансплантата.
Краткое описание чертежей
Изобретение поясняется чертежами, рентгенограммами и интраоперационными фотографиями:
- фиг. 1 - схематично представлен этап формирования желудочной трубки по А.Ф. Черноусову;
- фиг. 2 (а - сформированная желудочная трубка, б - выключенная петля тонкой кишки по Ру) - интраоперационная фотография комбинированного желудочно-тонкокишечного трансплантата на петле по Ру по M. Watanabe;
- фиг. 3 (а - сформированная желудочная трубка, б - выключенная петля тонкой кишки по Ру) - схематично представлен окончательный вариант реконструкции по M. Watanabe;
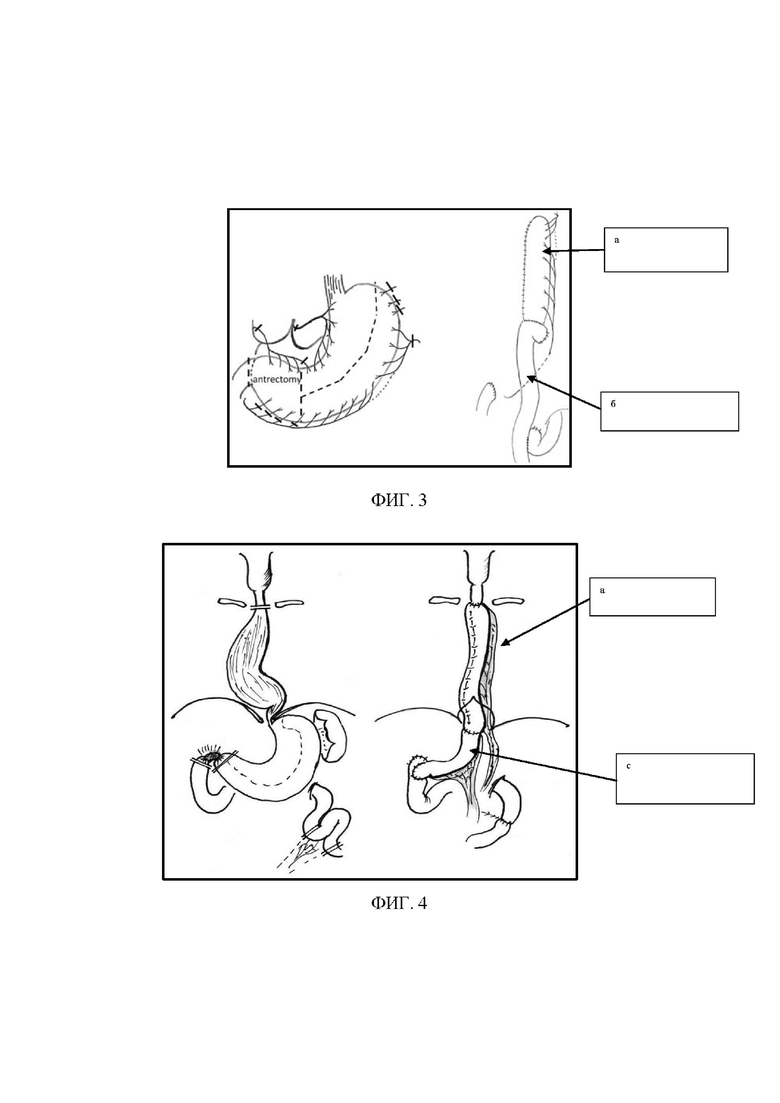
- фиг. 4 (а - сформированная желудочная трубка, с - интерпонированный сегмент тощей кишки) - схематично представлен окончательный вариант способа реконструкции с формированием желудочно-тонкокишечного трансплантата (предлагаемый способ);
- фиг. 5 (а - сформированная желудочная трубка, с - интерпонированный сегмент тощей кишки) - интраоперационная фотография сформированного трансплантата с включением в пассаж ДПК;
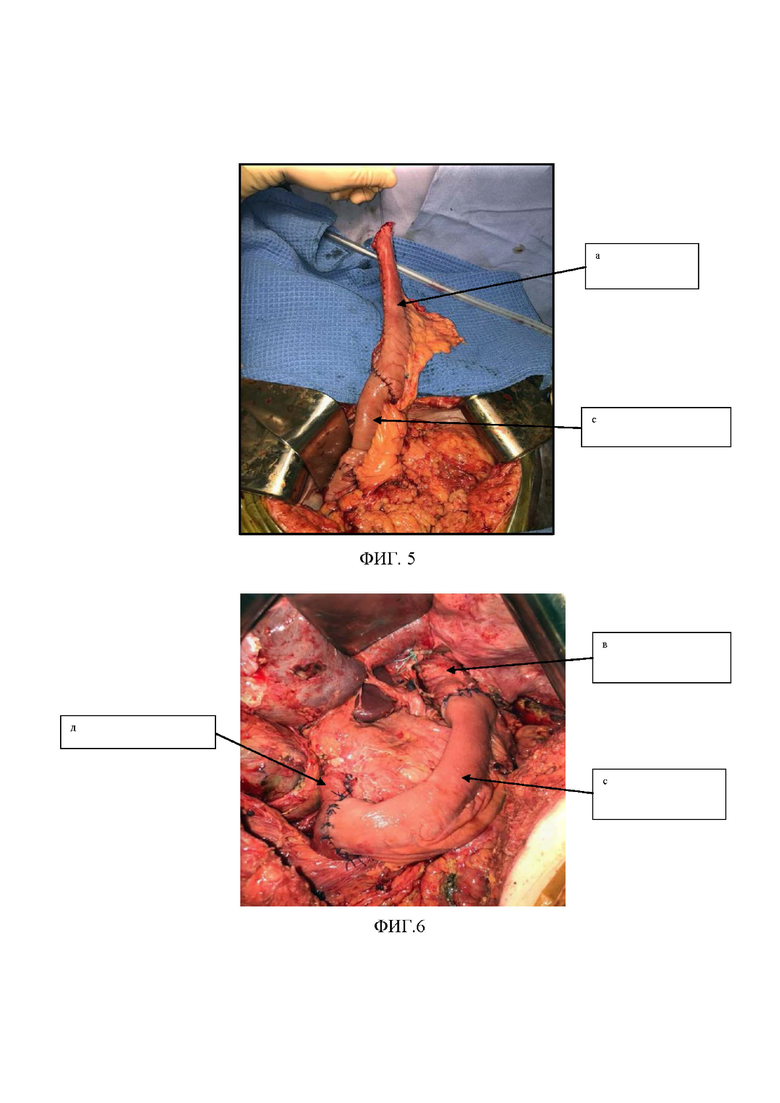
- фиг. 6 (д - двенадцатиперстная кишка, с - интерпонированный сегмент тощей кишки, в - дистальный отдел желудочной трубки) - сформированный желудочно-тонкокишечный трансплантат;
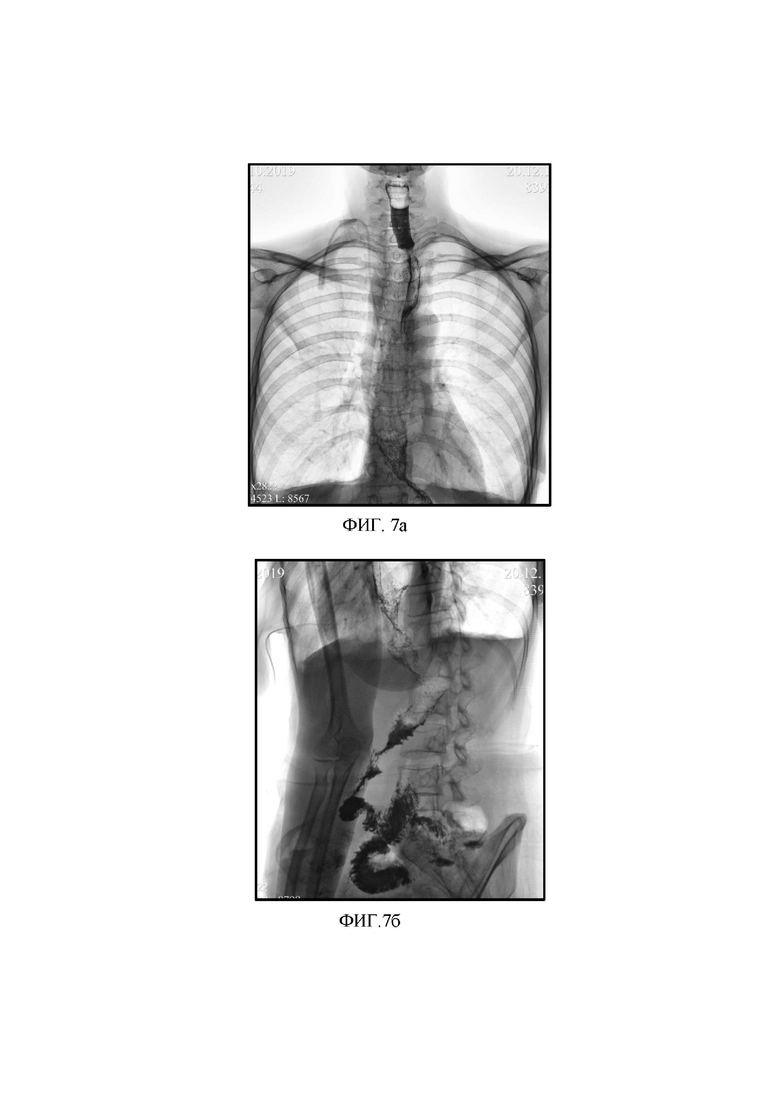
- фиг. 7 (а - прямая проекция, б - боковая) - контрольные рентгенограммы на 5 сутки после операции;
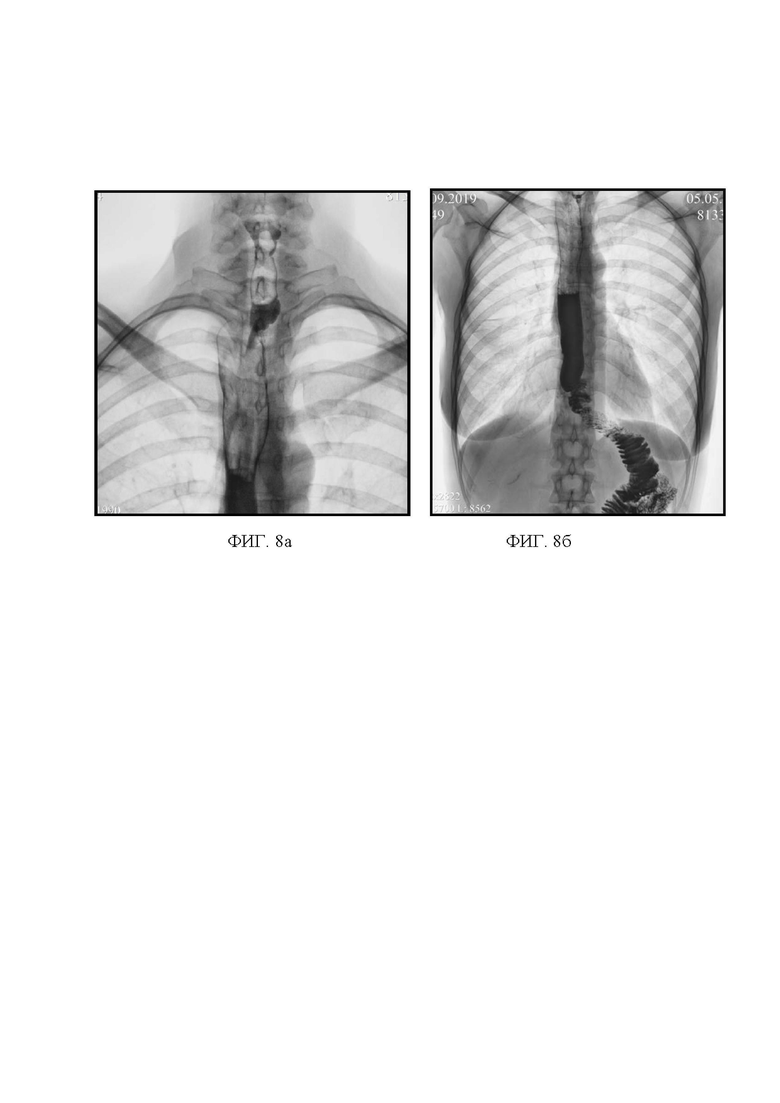
- фиг. 8 (а - прямая проекция, б - боковая) контрольные рентгенограммы через 2 года после операции.
Осуществление изобретения
Способ осуществляют следующим образом.
При выполнении комбинированной желудочно-тонкокишечной пластики пищевода после субтотальной эзофагэктомии с резекцией желудка используют следующую последовательность хирургических этапов.
Операцию выполняют через лапаротомный доступ. Для формирования шейного соустья применяют левосторонний шейный доступ. После субтотальной эзофагэктомии приступают к формированию желудочной трубки шириной примерно 4 см при помощи линейного степлера. Механический шов укрывают непрерывным серо-серозным швом, оставляя на дистальной части лигатуру на зажиме Кохера, которую связывают с лигатурой на резецированном абдоминальном сегменте пищевода. Длина желудочной трубки составляет примерно 25 см. Длина желудочной трубки 25 см не является принципиальной, но ее длины не достаточно для перемещения ее орального отдела на шею и формирования шейного соустья. Для этого желудочную трубку отсекают ниже привратника сшивающим аппаратом с сохранением питающей ножки правых желудочно-сальниковых сосудов.
Затем приступают к формированию тонкокишечной вставки. Сегмент тощей кишки выкраивают на третьей паре тощекишечных артерий. Брыжейка этого участка кишки находится в средней части брюшной полости, подвижна и имеет достаточную длину для того, чтобы проксимальный конец мобилизованного сегмента можно было без натяжения соединить с коротким желудочным трансплантатом даже при высоком его расположении в средостении. Длина используемого сегмента составляет примерно 20 см, именно такой сегмент достаточен для восполнения дефицита длины желудочного трансплантата и формирования анастомоза с проксимальным его концом и ДПК без натяжения. Более длинный сегмент может стать причиной непроходимости пищи вследствие его перегиба в отдаленном периоде.
Пригодный для пластики сегмент тощей кишки перемещают в верхний отдел брюшной полости через окно в мезоколон, не допуская перекрута сосудистой ножки по оси. Целостность тонкого кишечника восстанавливают однорядным швом «конец в конец». Последовательно формируют однорядный гастроеюноанастомоз "конец в конец" и двухрядный еюнодуденоанастомоз "конец в конец". Окно в брыжейках мезоколон ушивают.
Выполняют разрез на шее слева по медиальному краю левой кивательной мыщцы. Проводят мобилизацию шейного отдела пищевода, пищевод извлекают через шею и пересекают на Г-образном зажиме на 3,0-5,0 см ниже глотки. Данный уровень пересечения пищевода обусловлен необходимым уровнем субтотальной резекции, который определяется, соответственно, уровнем поражения пищевода. Культю пищевода оставляют на Г-образном зажиме.
Сформированный желудочно-тонкокишечный трансплантат проводят через заднее средостение на шею. Избыток культи шейного отдела пищевода и желудочного трансплантата, если таковой имеется, отсекают и формируют двухрядный эзофагогастроанастомоз «конец в конец» отдельными узловыми швами.
Заявленным способом оперировано 7 пациентов. Средний возраст составил 52,8 года, мужчин было 3 (43%), женщин 4 (57%). Все пациенты в раннем послеоперационном периоде проходили комплекс обследования. В отдаленном периоде под наблюдением находились 4 (57,1%) пациента.
Пример №1. Больная К. 45 лет поступила с жалобами на невозможность прохождения пищи по пищеводу (принимает только жидкую пищу). Из анамнеза в июне 2019 года по ошибке выпила ускусную кислоту. В одном из стационаров по месту жительства пациентке провели 2 курса бужирования стриктуры пищевода без клинического эффекта.
В ФГБУ Национальном медицинском исследовательском центре хирургии им. А.В. Вишневского МЗ РФ (далее - НМИЦ) выполнили ЭГДС, где выявили циркулярную рубцовую стриктуру средней трети пищевода, не проходимую аппаратом (диаметр аппарата 8,8 мм). При рентгеноскопии установили протяженное сужение средней и нижней трети пищевода без значимой дилатации вышележащих отделов.
08.10.2019 в НМИЦ выполнили трансхиатальную субтотальную эзофагэктомию с резекцией пилорического отдела желудка (интраоперационно выявлена рубцово-язвенная деформация привратника и антрального отдела протяженностью 3 см) с одномоментной субтотальной заднемедиастинальной эзофагопластикой комбинированным желудочно-тонкокишечным трансплантатом (фиг. 6).
При контрастной рентгеноскопии на 5-е сутки анастомозы состоятельны, проходимы (ФИГ. 7 а, б), пассаж контрастного вещества и его эвакуация из всех сегментов конструкции не нарушены. Пациентку выписали на 10-е сутки после операции в удовлетворительном состоянии и с полноценным питанием через рот.
Пример №2. Пациент, Д. 55 лет обратился в НМИЦ с жалобами на невозможность приема твердой и жидкой пищи, рвоту съеденной пищей, похудание за три месяца на 5-7 кг, общую слабость. При дообследовании выявлена ахалазия кардии IV стадии с полной дисфагией. При МСКТ визуализировали расширенный пищевод диаметром более 6 см с выраженным S-образным искривлением и удлинением; застой пищевых масс в его просвете.
31.10.17 в НМИЦ выполнили трансхиатальную субтотальную эзофагэктомию с резекцией пилорического отдела желудка пластикой пищевода комбинированным желудочно-тонкокишечным трансплантатом. При интраоперацонной ревизии выявлен рубцовый стеноз луковицы ДПК с язвой, пенетрирующей в печеночно-двенадцатиперстную связку.
Пациент выписан на 10 сутки, с полноценным питанием через рот. При контрастной рентгеноскопии через 2 года после операции, анастомозы проходимы (ФИГ. 8а, б) пассаж и эвакуация контраста по комбинированному трансплантату не нарушены.
Таким образом, всем пациентам удалось выполнить одномоментную эзофагопластику желудочной трубкой даже в случаях ее недостаточной длины. Интерпозиция сегмента тощей кишки между трансплантатом и ДПК не только позволила заместить возникший диастаз, но и сохранить дуоденальное пищеварение. В отдаленном периоде у большинства находившихся под наблюдением больных признаков нарушения эвакуации из комбинированного трансплантата не выявлено.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИНТЕРПОЗИЦИИ СЕГМЕНТА ТОЩЕЙ КИШКИ ПОСЛЕ СУБТОТАЛЬНОЙ ПРОКСИМАЛЬНОЙ РЕЗЕКЦИИ ЖЕЛУДКА | 2021 |
|
RU2774028C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С СОЗДАНИЕМ КИШЕЧНОГО РЕЗЕРВУАРА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801773C1 |
| СПОСОБ ФОРМИРОВАНИЯ АНТИРЕФЛЮКСНОГО КЛАПАНА НА ИНТЕРПОНИРОВАННОМ СЕГМЕНТЕ ТОЩЕЙ КИШКИ ПОСЛЕ ГАСТРЭКТОМИИ | 2019 |
|
RU2712042C1 |
| СПОСОБ ЕЮНОГАСТРОПЛАСТИКИ С ФОРМИРОВАНИЕМ СИММЕТРИЧНОГО ИЗОПЕРИСТАЛЬТИЧЕСКОГО РЕЗЕРВУАРА | 2019 |
|
RU2712064C1 |
| СПОСОБ РЕДУОДЕНИЗАЦИИ С ФОРМИРОВАНИЕМ АНТИРЕФЛЮКСНОГО КЛАПАНА ПРИ БОЛЕЗНЯХ ОПЕРИРОВАННОГО ЖЕЛУДКА ПОСЛЕ ГАСТРЭКТОМИИ В ПЕТЛЕВОЙ РЕКОНСТРУКЦИИ ПО БРАУНУ | 2023 |
|
RU2801772C1 |
| СПОСОБ ФАРИНГОПЛАСТИКИ В УСЛОВИЯХ ДЕФИЦИТА ПЛАСТИЧЕСКОГО МАТЕРИАЛА | 2010 |
|
RU2427339C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ ПРОФИЛАКТИКИ НЕСОСТОЯТЕЛЬНОСТИ ШВОВ ШЕЙНОГО ПИЩЕВОДНО-КИШЕЧНОГО АНАСТОМОЗА ПРИ ТОТАЛЬНОЙ ЭЗОФАГОПЛАСТИКЕ АНТИПЕРИСТАЛЬТИЧЕСКИМ ТОЛСТОКИШЕЧНЫМ ТРАНСПЛАНТАТОМ | 2008 |
|
RU2357682C1 |
| СПОСОБ ОДНОМОМЕНТНОЙ ТОТАЛЬНОЙ ЭЗОФАГОПЛАСТИКИ | 2000 |
|
RU2165737C1 |
| СПОСОБ ТОЛСТОКИШЕЧНОЙ ГАСТРОПЛАСТИКИ ПОСЛЕ ГАСТРЭКТОМИИ | 2004 |
|
RU2278619C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПРОГРЕССИРУЮЩЕЙ НУТРИТИВНОЙ НЕДОСТАТОЧНОСТИ ПОСЛЕ ГАСТРОШУНТИРОВАНИЯ ПО Ру | 2023 |
|
RU2801421C1 |
Изобретение относится к медицине, а именно к хирургии, и может быть использовано в реконструктивной хирургии пищевода после субтотальной эзофагэктомии при сочетанных поражениях пищевода и желудка. Для этого после субтотальной эзофагэктомии и резекции желудка формируют желудочный трансплантат в виде желудочной трубки, отсекая его от двенадцатиперстной кишки (ДПК) с сохранением питающей ножки правых желудочно-сальниковых сосудов. Формируют тонкокишечную вставку длиной 20 см на третьей паре тощекишечных артерий с последующим перемещением ее в верхний отдел брюшной полости через окно в мезоколон, не допуская перекрута сосудистой ножки по оси. После этого последовательно формируют однорядный гастроеюноанастомоз "конец в конец" и двухрядный еюнодуденоанастомоз "конец в конец". На шее по медиальному краю левой кивательной мыщцы выполняют разрез и мобилизуют шейный отдел пищевода с последующим выведением его на шею и пересечением. Сформированный желудочно-тонкокишечный трансплантат проводят через заднее средостение на шею, избыток культи шейного отдела пищевода и желудочно-тонкокишечного трансплантата отсекают и формируют двухрядный эзофагогастроанастомоз «конец в конец» отдельными узловыми швами. Способ обеспечивает полноценное питание через рот с сохранением дуоденального пассажа за счет формирования комбинированного трансплантата на естественном источнике кровоснабжения, а также снижение риска несостоятельности пищеводного соустья за счет формирования двухрядного анастомоза в зоне наиболее благоприятного кровоснабжения трансплантата, в условиях сочетанного поражения пищевода и желудка. 8 ил., 2 пр.
Способ эзофагопластики комбинированным висцеральным трансплантатом после субтотальной эзофагэктомии при сочетанных поражениях пищевода и желудка, включающий формирование короткого желудочного трансплантата на естественном источнике кровоснабжения и перемещение его на шею, отличающийся тем, что после субтотальной эзофагэктомии формируют желудочный трансплантат в виде желудочной трубки, отсекают его от двенадцатиперстной кишки (ДПК) с сохранением его питающей ножки на правых желудочно-сальниковых сосудах;
затем формируют тонкокишечную вставку, для чего выкраивают сегмент тощей кишки на третьей паре тощекишечных артерий с последующим перемещением его в верхний отдел брюшной полости через окно в мезоколон, не допуская перекрута сосудистой ножки по оси,
после чего последовательно формируют однорядный гастроеюноанастомоз "конец в конец" и двухрядный еюнодуденоанастомоз "конец в конец"; слева на шее по медиальному краю левой кивательной мышцы выполняют разрез и мобилизуют шейный отдел пищевода с последующим выведением его на шею и пересечением на Г-образном зажиме, отступив 3,0-5,0 см ниже глотки,
сформированный желудочно-тонкокишечный трансплантат проводят через заднее средостение на шею, избыток культи шейного отдела пищевода и желудочно-тонкокишечного трансплантата отсекают и формируют двухрядный эзофагогастроанастомоз «конец в конец» отдельными узловыми швами.
| WATANABE M | |||
| et al | |||
| Modified gastric pull-up reconstructions following pharyngolaryngectomy with total esophagectomy | |||
| Dis Esophagus | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| PMID: 23672461 | |||
| СПОСОБ ФОРМИРОВАНИЯ ПИЩЕВОДНО-ТОЛСТОКИШЕЧНОГО АНАСТОМОЗА НА ШЕЕ | 2018 |
|
RU2694214C1 |
| Способ эзофагопластики | 1990 |
|
SU1757648A1 |
| Способ улучшения кровоснабжения проксимального отдела желудочного трансплантата при эзофагопластике | 2016 |
|
RU2614213C1 |
| РУЧКИН Д.В | |||
| и др | |||
| Еюногастропластика как | |||
Авторы
Даты
2022-04-18—Публикация
2021-12-05—Подача